Изобретение относится к медицине, а именно к хирургии и комбустиологии, и может быть использовано в ходе лечения ожоговых ран для временного закрытия ран различной этиологии.
Урбанизация способствует концентрации на относительно небольших площадях значительного количества людей и мощных производственных комплексов, запасов химических и горючих материалов, энергоресурсов. При внезапном возникновении природных и антропогенных катастроф уязвимость городских жителей и численность пострадавших среди них резко повышаются.
В 1975 г. в Женеве создано Международное общество медицины катастроф. В его задачи входят: координация разработки проблем медицины катастроф в международном масштабе; научные исследования и разработка программ по проблемам медицинской помощи пострадавшим при катастрофах и их лечения в условиях массовых поражений. Наиболее часто встречаются термические ожоги (до 80-90% случаев), которые являются результатом воздействия на кожу пламени, раскаленных газов, пара, горячих жидкостей и раскаленных предметов (Герасимова Л.И. Ожоги - проблемы медицины катастроф. Военная медицина. 1990, с. 66-68). В подобных условиях зачастую складывается ситуация «один врач - множество больных», в отличие от остальной медицины, где обычной является практика «один врач - один больной».
Ожоговая рана сразу после травмы практически стерильна, но в дальнейшем ее микробное обсеменение нарастает. Денатурация дермы в результате воздействия высоких температур сопровождается мощным выбросом протеолитических ферментов, продуктов деградации ткани, что способствует размножению бактерий и приводит к углублению раны, лечение которой в этот период возможно только с помощью пересадки кожи. Тяжесть течения и длительность лечения пострадавших от термических поражений делает актуальными такие задачи, как разработка новых покрытий, ускоряющих эпителизацию аутотрансплантированных лоскутов. Пересадка кожи в сочетании с использованием предварительного покрытия является эффективным способом восстановления обожженных участков.
Покрытие раны необходимо отличать от закрытия раны. Материалы для закрытия ран являются биологически приемлемыми для раневого ложа и постепенно включаются в заживающую раневую область. В то время, как материалы для раневого покрытия основаны на включении в раневой коагулят и врастании гранулезных тканей с целью прикрепления. Материал для покрытия ран обычно не является биологически разрушаемым и, следовательно, может являться лишь временным замещением эпидермиса. Затем он должен быть заменен на кожу пациента, либо могут быть использованы методы по пересадке кожи.
В случае использования временного покрытия рана не должна быть обсеменена бактериями и должна быть достаточно неглубокой, чтобы можно было ожидать ее полного заживления в течение 3-х недель. Эпителиальные клетки из эпидермальных дериватов растут и замещают разрушенный эпидермис, и постепенно материал раневого покрытия вытесняется. Следовательно, исходной целью использования материалов для покрытия ран в случае неглубоких ожогов второй степени является сокращение микробного обсеменения раневого ложа (создание микробного барьера), обеспечивающее предотвращение инфекции, а также сокращение доступа воздуха, что тем самым ослабляет боль. Материалы для покрытия ран также используют и для глубоких повреждений III и IV степени перед окончательным закрытием раны собственной кожей больных с обширными ожоговыми повреждениями.
Оптимальный материал раневого покрытия пока не был установлен. Однако требования к современному временному покрытию следующие:
- создать нетоксичный, антисептический, непровоспалительный и неантигенный барьер для бактерий и других микробов;
- обеспечить нормальную передачу тепла, воды и кислорода;
- обеспечить непосредственное, однообразное прикрепление к раневому ложу;
- обеспечить поддержание механизмов нормального местного иммунитета и заживления раны.
В известном уровне техники: либо покрытие, выполняющее только механическую функцию закрытия раны, требующая регулярной замены (менее 7 дней), либо биологическое покрытие на основе выращенных аутологичных клеток, создание которого требует времени - более 7 дней, не говоря уже о нерешенных вопросах по применению биомедицинского клеточного продукта (ФЗ-180), имеется проблема поиска способов улучшения заживления ран и материалов для раневых покрытий. Настоящее изобретение восполняет указанную потребность в данной области техники.
Известен способ лечения ожоговых ран с использованием биологического раневого покрытия, изготовленного способом, включающим стадии отбора ткани животного, содержащей субстрат, поперечного сшивания и фиксации субстрата, минимизации активности антигенов субстрата и присоединения активного слоя к субстрату [RU 2438713 С2, опублик. 10.01.2012], Однако, ткани животного могут быть переносчиками заболеваний или инфекций, а также могут вызывать неблагоприятный иммунный ответ у донора. При использовании алло- или ксенокожи на 9-14 день происходит активная форма отторжения включая активные лимфоциты, и лоскут разрушается из-за тромбоза сосудов и ишемического некроза.
Известен способ лечения ожоговых ран с использованием биосинтетического раневого покрытия БИОКОЛ - 1, представляющего собой эластичную, пористую пленку, состоящую из смеси синтетических и натуральных, гидрофильных и гидрофобных полимеров. Лечение с помощью раневого покрытия БИОКОЛ - 1 приводит к ускорению заживления раны, однако оно не обладает выраженным антибактериальным эффектом, который необходим при лечении инфицированных ожоговых ран. Такие многокомпонентные пленки на основе синтетического материала имеют улучшенную совместимость с тканями, но обладают слабой проницаемостью для газов и ухудшают процесс регенерации клеток.
Известен способ лечения ожоговых ран на основе применения культивированных клеток. В качестве исходного материала для культивирования клеток используют штамм диплоидных клеток легкого эмбриона человека ЛЭЧ-4(81) [RU 2230500 С2, опублик. 20.06.2004]. Однако клетки легкого эмбриона человека могут вызывать неблагоприятный иммунный ответ у донора.
Известен способ лечения ожоговых ран, включающий туалет раны и наложение на ее поверхность биологической повязки, состоящей из полимерного основания, покрытого коллагеном, и живых аллогенных фибробластов человека [RU 2373944 С1, опублик. 27.11.2009]. Фибробласты - это волокнистые клетки, имеющиеся в каждом человеческом теле, представляющие собой малодифференцированные клетки человека. Недостатком этого способа является использование первичных культур аллогенных фибробластов без надлежащего обследования, что не позволяет исключить наличия вирусных и микроплазменных контаминаций культур, способных инфицировать пациента. В процессе культивирования соматические клетки человека, в том числе фибробласты, способны претерпевать спонтанную трансформацию к неограниченному росту, что определяет необходимость изучения кариотипа клеток в процессе культивирования для оценки стабильности их генома.
Известно, что у трансгенных свиней линии GAL-KO супрессирован иммунологический барьер - реакция отторжения немедленного типа (гиперактивное отторжение), в результате чего они не имеют генов 1,3-a-galactosyltransferase (a-gal), кодирующих фермент, ответственный за выработку на поверхности клеток свиньи углеводных антигенов, приводящих к гиперактивному отторжению [Wong BS, Yamada K, Okumi М, Weiner J, 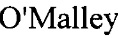 РЕ, Tseng YL, Dor FJ, Cooper DK, Saidman SL, Griesemer A, and Sachs DH, Allosensitization does not increase the risk of xenoreactivity to alpha 1,3 galactosyltransferase gene-knockout miniature swine in patients on transplantation waiting lists. Transplantation 82: 314-319, 2006]. Из уровня техники (генная инженерия) известны способы получения трансгенных свиней и возможности их использования для решения проблемы нехватки внутренних органов, тканей и клеток для пересадки человеку [Н.А. Зиновьева, и др. Использование трансгенных GAL-KO свиней в ксенотрансплантации. Проблемы и перспективы. «Сельскохозяйственная биология», 2014, №2, с. 42-49], [US 6482404 В1, опублик. 19.11.2002; US 2005120400 А1, опублик. 02.06.2005; US 2006242722 А1, опублик. 26.10.2006].
РЕ, Tseng YL, Dor FJ, Cooper DK, Saidman SL, Griesemer A, and Sachs DH, Allosensitization does not increase the risk of xenoreactivity to alpha 1,3 galactosyltransferase gene-knockout miniature swine in patients on transplantation waiting lists. Transplantation 82: 314-319, 2006]. Из уровня техники (генная инженерия) известны способы получения трансгенных свиней и возможности их использования для решения проблемы нехватки внутренних органов, тканей и клеток для пересадки человеку [Н.А. Зиновьева, и др. Использование трансгенных GAL-KO свиней в ксенотрансплантации. Проблемы и перспективы. «Сельскохозяйственная биология», 2014, №2, с. 42-49], [US 6482404 В1, опублик. 19.11.2002; US 2005120400 А1, опублик. 02.06.2005; US 2006242722 А1, опублик. 26.10.2006].
Наиболее близким изобретением является способ лечения инфицированных ожоговых ран IIIA степени, включающий хирургическую обработку раны и временное наложение раневого покрытия. На ожоговую рану IIIA степени, поверхность которой очищена от поврежденных тканей и серозно-гнойного отделяемого, наносят на 2-4 дня покрытие, представляющее собой конструкцию из кремнийорганического полимера, покрытого коллагеном типа I человека с тромбоцитарным фактором роста - PDGF-BB и пектином. Коллаген приводит к ускорению заживления раны, однако не обладает выраженным антибактериальным эффектом, который необходим при лечении инфицированных ожоговых ран. При этом коллаген типа I человека может быть переносчиком заболеваний или инфекций, а также может вызывать неблагоприятный иммунный ответ у донора. Это ограничивает использование данного способа. [RU 2455 997 С2, опублик. 20.07.2012].
Задачей изобретения является сокращение сроков заживления ожоговых ран кожи субдермального уровня при одновременной биологической безопасности используемого материала.
Поставленная задача решается тем, что в предложенном способе оперативного лечения ожоговых ран, включающем хирургическую обработку раны и временное наложение биологического раневого покрытия с последующим проведением аутотрансплантации, согласно изобретению, в качестве биологического раневого покрытия используют лоскуты кожи трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу, обеспечивающие отсутствие иммунной реакции отторжения раневого покрытия, при этом покрытие, выдержанное при температуре минус 65-70°С и стерилизованное γ- или β-излученим дозой от 12 до 18 кГр, дополнительно охлаждают при 180-190°С 6 - 8 ч и накладывают на рану на срок не более 14 дней.
Согласно изобретению в период до 14 дней с даты получения ожоговой травмы лечебные действия предлагаемого биологического покрытия, в соответствии с предложенным способом, направлены на образование здоровых грануляций, подавление микрофлоры и стимуляцию репаративных процессов. Это способствует благоприятному созданию условий для последующего проведения аутотрансплантации.
Обеспечивается бактериальное торможение за счет врожденных природных качеств кожи трансгенных свиней и при предварительной ее обработке.
Обеспечивается тесное прилипание ожогового покрытия к иссеченной ране, что является важной характеристикой, т.к. с плотно прилегающим покрытием бактерии не могут проникать в рану и, в то же время, предотвращают потерю жизненно необходимых богатых протеинами жидкостей в результате роста фибробласта. За счет отсутствия в лоскутах кожи трансгенных свиней линии GAL-KO пирогенных веществ не вызывается повышение температуры тела и других нежелательных реакций организма больного. Это касается биологически активных веществ экзогенного (бактериального и вирусного), а также эндогенного (клеточно-тканевого) происхождения.
Не происходит активной формы отторжения (HAR) покрытия за счет действия активных лимфоцитов из-за сосудистой закупорки и ишемического некроза (при аллокоже или ксенокоже) и покрытие прослужит дольше (до 14 дней). Это объясняется тем, что трансгенные свиньи линии GAL-KO не имеют генов 1,3-a-galactosyltransferase (a-gal), кодирующихфермент, ответственный за выработку на поверхности клеток свиньи углеводных антигенов, приводящих к гиперактивному отторжению.
Ускоряется заживление в процессе эпитализации в результате анатомической и физиологической совместимости кожи трансгенных свиней линии GAL-KO с человеческим организмом (гистосовместимость) при биологической безопасности используемого материала, что благоприятно влияет на метаболические процессы в ране за счет следующего:
- жидкость в достаточном количестве просачивается из раны для предотвращения образования экссудата;
- происходит хороший газообмен (газопроницаемость) раны с внешней средой, что обеспечивает высокую скорость транспорта кислорода.
При наложении временного покрытия в течение 24 часов после ожоговой травмы на срок 14 дней создаются условия реваскуляризации со стороны раны. Происходит образование новых сосудов аутокожи путем разрастания и ветвления старых сосудов с учетом отсутствия сенсибилизации (фиг. 2, 3). При этом известно, что продолжительность приживления чужеродных тканей, выдержанных при сверхнизких температурах (минус 68-70°С) [Музыка В. И., 1970; Атясов Н.И., 1985] и охлажденных при 180-190°С 6-8 ч увеличивается (до 14 дней)
Согласно изобретению, биологическое раневое покрытие (кожа трансгенной свиньи линии GAL-KO) при наложении на рану временно прилипает, но никогда не васкуляризируется по-настоящему. Глубокие ожоговые раны, с повреждением дермы заживают путем эпителизации, но это более затяжной процесс. Эпителизация начинается с первого дня образования раны, но усиливается на 4-6 день. Начинается она с края раневой поверхности, постепенно направляясь к центру. Заживление проходит в два этапа - миграция клеток эпителия и их пролиферация. Клетки базального слоя начинают интенсивно двигаться (мигрировать) и, начиная от края раны и до центра, формировать мембрану и заполнять образовавшийся дефект. Через два - три дня переместившиеся клетки базального слоя эпидермиса начинают усиленно делиться. Этот процесс идет до той поры, пока дерма полностью не восстановится. В новых клетках процесс ороговения вначале идет медленно. После завершения эпителизации молодая грануляционная ткань начинает превращаться в соединительнотканный рубец, который раневое покрытие оберегает от механического воздействия.
Наложение временного покрытия из кожи трансгенных свиней линии GAL-KO по предлагаемому способу лечения ожоговых ран способствует легкому, безболезненному ее удалению при перевязке без повреждения сформировавшегося на поверхности раны регенерировавшего слоя неоэпителия.
Таким образом, в известном уровне техники (применение медицинских изделий из материала, созданного на основе кожи трансгенных свиней) отсутствуют сведения, в которых раскрыта вся совокупность признаков относительно данного изобретения.
Совокупность известных и новых признаков позволяет получить новый технический результат - сокращение сроков заживления ожоговых ран кожи субдермального уровня при одновременной биологической безопасности используемого материала.
Изобретение поясняется графическими изображениями.
На фиг. 1 изображено кольцо для фиксации ожоговой раны животного.
На фиг. 2 представлено изображение фибробластов грануляционной ткани.
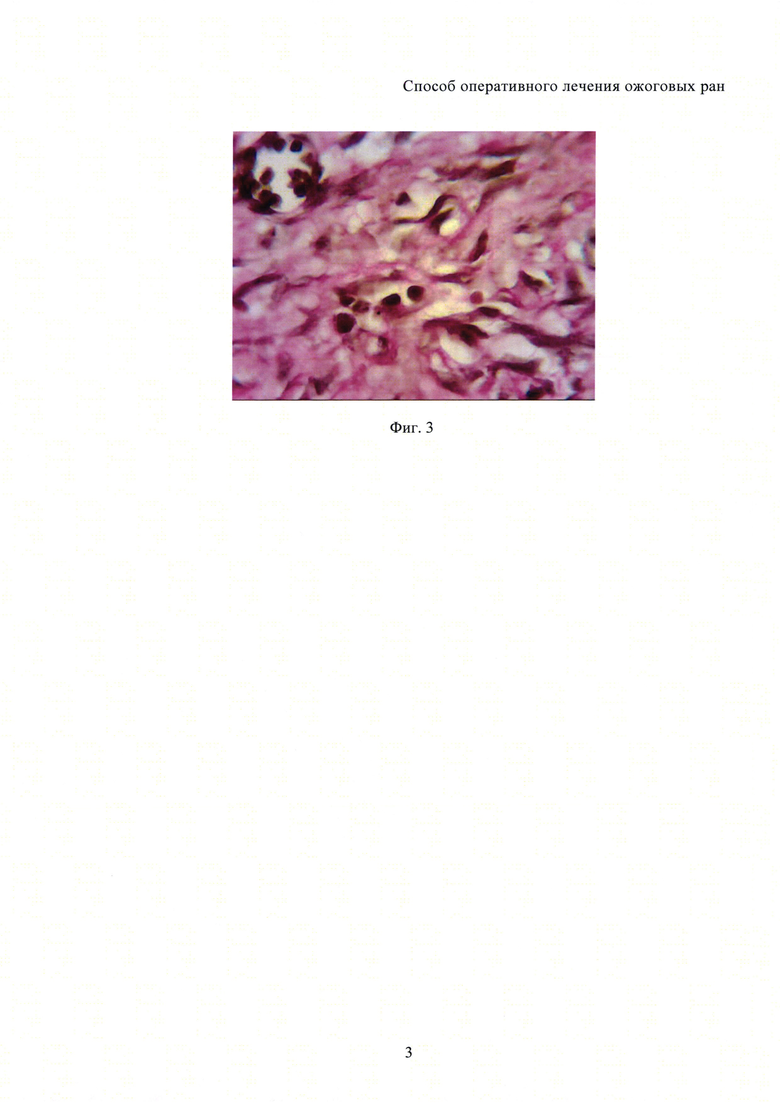
На фиг. 3 изображены коллагеновые волокна по Ван-Гизону.
Изобретение подтверждается следующим конкретным примером.
Ткани (лоскуты кожи) выделяют из трансгенных свиней, не содержащих альфа-1,3-галактозу. В качестве биологического раневого покрытия используют лоскуты кожи трансгенных свиней линии GAL-KO.
Помещают их в искусственную питательную среду для поддержания исходных естественных условий. Среда состоит из определенного соотношения аминокислот, витаминов, солей, глюкозы, гормонов, поддерживает буферную систему и осмотическое давление. Используют среду DMEM (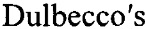 Modified
Modified 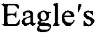 Medium), представляющую собой модификацию среды ВМЕ (Basal Medium Eagle) или среду F-12.
Medium), представляющую собой модификацию среды ВМЕ (Basal Medium Eagle) или среду F-12.
Обеспечивают герметизацию лоскутов кожи, помещают в холодильную камеру при температуре минус 68°С до использования в качестве раневого покрытия. Срок хранения не более 24 мес.
Осуществляют стерилизацию γ-излучением дозой 15 кГр.
До наложения раневое покрытие охлаждают при минус 190°С в течение 7 ч.
Подготовленное таким образом раневое покрытие доставляют в клинику в герметичном термоконтейнере.
После ожоговой травмы у больного проводят хирургическую обработку раны -очищение от поврежденных тканей и серозно-гнойного отделяемого с помощью тампонов, смоченных антисептическими растворами (например, раствором хлоргексидина).
На подготовленную таким образом раневую поверхность ожогов IIIA степени накладывали на 14 дней биологическое раневое покрытие.
В течение данного периода пациента доставляют в специализированные ожоговые центры или в общехирургические стационары. Отсутствие васкуляризации между поверхностью раны и раневым покрытием способствует легкому, безболезненному ее удалению без повреждения сформировавшегося на поверхности раны регенерировавшего слоя неоэпителия.
Изобретение подтверждается также конкретным примером при стерилизации β-излученим дозой от 15 кГр при соблюдении вышеприведенных параметров способа.
Примеры испытаний.
Для подтверждения эффективности предлагаемого способа лечения ожоговых ран IIIA степени был проведен анализ результатов использования раневого покрытия из кожи трансгенной свиньи линии GAL-KO в течение 14 дней.
Пример 1.
Для подтверждения эффективности предлагаемого оперативного способа лечения ожоговых ран IIIA степени были проведены испытания в Государственном бюджетном учреждении здравоохранения г. Москвы «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского Департамента здравоохранения г. Москвы» (ГБУЗ «НИИ СП им. Н.В. Склифосовского ДЗМ»).
Испытания проведены с использованием раневого покрытия на основе кожи трансгенных свиней линии GAL-KO для медицинских изделий, применяемых при лечении ожоговых ран.
Цель испытания: токсикологические исследования раневого покрытия при лечении ожоговых ран.
Описание материала:
Раневое покрытие представляет собой кожные лоскуты трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу, размером 4,0-4,5 на 5,0-5,5 см, толщиной до 1,0 мм, заготовленные в условиях стерильной операционной с соблюдением правил асептики и антисептики. До проведения испытаний материал хранился в течении 8 часов при сверхнизких температурах (минус 190°С) в среде содержащей 10% ДМСО.
а) Экспериментальные объекты - диплоидные фибробласты кожи человека.
Исследование токсичности in vitro проводили с диплоидными фибробластами кожи человека. Для этого материал помещали в лунки, содержавшие суспензию клеток, и отмечали время адгезии и распластывания клеток, а через трое суток - количество живых клеток. В присутствии образцов раневого покрытия на основе кожи трансгенных свиней линии GAL-KO после криохранения в клетках культуры фибробластов кожи человека не наблюдали признаков токсичности в течение всего периода наблюдения (трое суток): клетки сохранялись прозрачными, были четко очерчены, имели характерную морфологию, не содержали включений. Образцы раневого покрытия, полученного из кожи трансгенных свиней линии GAL-KO, не вызывали снижение индекса пролиферации.
б) Экспериментальные животные - мыши.
Исследование токсичности in vivo оценивали по выживаемости животных после применения раневого покрытия с учетом распространенных клинических признаков (ГОСТ РИСО 10993-11-2009). При исследовании in vivo из 24 прооперированных животных, которым трансплантировали раневое покрытие на основе кожи трансгенных свиней линии GAL-KO, выжили 23. При этом мышь погибла в результате массивной кровопотери. У выживших животных на протяжении всего исследования не отмечено конвульсий, нарушений двигательной активности, дыхания, мышечного тонуса, деятельности желудочно-кишечного тракта.
На основании оценки, проведенной in vitro, раневое покрытие на основе кожи трансгенных свиней линии GAL-KO является нетоксичным. По данным исследования in vivo каких либо токсических реакций у мышей, которым применяли раневое покрытие на основе кожи трансгенных свиней линии GAL-KO, не отмечено.
Пример 2.
Для подтверждения эффективности предлагаемого способа оперативного лечения ожоговых ран IIIA степени были проведены испытания в Государственном бюджетном учреждении здравоохранения г. Москвы «Научно-исследовательский институт скорой помощи им. Н.В. Склифосовского Департамента здравоохранения г. Москвы» (ГБУЗ «НИИ СП им. Н.В. Склифосовского ДЗМ»).
Цель испытания: исследование раневого покрытия на отсутствие иммуногенности.
Описание материала.
Раневое покрытие представляет собой кожные лоскуты трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу, размером 4,0-4,5 на 5,0-5,5 см, толщиной до 1,0 мм, заготовленные в условиях стерильной операционной с соблюдением правил асептики и антисептики. До проведения испытаний раневое покрытие, стерилизованное γ-излучением дозой 15 кГр, выдержано в течение 8 час при сверхнизкой температуре минус 190°С в среде, содержащей 10% ДМСО.
Экспериментальные животные - мыши.
Иммуногенность раневого покрытия оценивали по развитию реакции отторжения покрытия, по выраженности воспалительной реакции в ране и окружающих мягких тканях и характеру клеточной инфильтрации на основании данных гистологического исследования мышей.
В опытной группе мышей морфологическая картина соответствовала нормальному течению раневого процесса. Особо отметим, что инфильтрации клетками воспаления раневого покрытия на основе кожи трансгенных свиней линии GAL-KO не наблюдалось. На 7 сутки на материал на основе кожи трансгенных свиней линии GAL-KO морфологических признаков развития реакции отторжения у мышей не выявлено. К 14 суткам у животных опытной группы отмечалась инфильтрация тканей иммунокомпетентными клетками, что отражало развитие иммунного воспаления на чужеродную ткань. У животных опытной группы интенсивность восстановления целостности кожных покровов на 21 сутки была несколько снижена, что выражалось в незавершенности процесса эпителизации у половины животных в группе. Инфильтрация тканей свидетельствовала о продолжении реакции отторжения раневого покрытия.
Анализ результатов исследования показал, что при применении раневого покрытия на основе кожи трансгенных свиней линии GAL-KO признаки развития реакции отторжения отмечены только начиная с 14 суток послеоперационного периода.
Раневое покрытие на основе кожи трансгенных свиней линии GAL-KO является сл абоиммуногенным.
Пример 3.
Цель испытания: изучение эффективности ускорения заживления кожных ран большого объема и глубины.
Испытания проведены с использованием экспериментальной модели полнослойной плоскостной раны (Л.И. Слуцкий, 1969, A.B. Shekhteretal., 2005).
Экспериментальные животные - крысы.
Эффективность заживления оценивалась количественно по 4-х бальной системе по следующим трем признакам:
- наличие воспалительного процесса (содержание нейтрофильных лейкоцитов, отек ткани, микроциркуляторные нарушения);
- общее количество сосудов в ткани;
- зрелость грануляционной ткани (количество фибробластов, их соотношение с новообразованными коллагеновыми волоконами).
При величине балла, равной 0, оценивают отсутствие данного (каждого) признака, по величине балла 1 оценивают как очень слабую выраженность, по величине балла 2 -как умеренную, по величине балла 3 - как сильную, а по величине балла 4 - максимальную выраженность признака в образце материала.
Испытания по оценке эффективности заживления кожных ран выполнены на 80 белых лабораторных крысах с массой тела 120-140 г.
Животных наркотизировали внутримышечным введением раствора золетила (Zoletil 100, Virbac S.A., Italia) из расчета 6 мг действующего вещества на кг массы тела животного в комбинации с рометаром (Rometar, Spofa, Praha) из расчета 0,5 мл на кг массы тела. На предварительно депилированной коже спины в межлопаточной области иссекали концентрический (диаметром 8-10 мм) лоскут кожи с подкожной клетчаткой вплоть до собственной фасции. В образовавшийся дефект вводили муфтообразное кольцо (фиг. 1). Таким образом, у всех животных получали раны стандартного размера, площадью 300 мм2. Затем на рану накладывали раневое покрытие.
В качестве раневого покрытия использовали отсепарированную тонким слоем кожу свиней линии GAL-KO, в качестве сравнительного контроля - вариант аллогенной кожи в качестве положительного контроля и вариант с нелеченной раной в качестве отрицательного контроля.
Результат испытания оценивали на 4 сутки, что соответствует времени начала эпителизации в норме.
После 4 суток изымали образец ткани дна раны, выдерживали в 10% формалине, заливали парафином, срезы глубиной 4-5 мкм окрашивали гематоксилином и эозином, пикрофуксином по Ван-Гизону на коллагеновые волокна для дальнейшего проведения микроскопии и фотофиксации. Препараты с образцами просматривались на микроскопе CarlZeiss и фотографировались с помощью видеокамеры.
Морфометрически по компьютерной программе оценивалась толщина слоя грануляционной ткани в образце.
1) Результат испытания без применения раневого покрытия (нелеченная рана -отрицательный контроль).
Раневая поверхность покрыта относительно тонким фибринозно-лейкоцитарным слоем. Он состоит из сплетения тонких фибриновых нитей и нейтрофильных лейкоцитов с немногочисленными макрофагами. Под ним располагается сравнительно толстый слой созревающей грануляционной ткани, в которой видны фрагменты оставшейся жировой ткани.
Грануляционная ткань состоит из многочисленных сосудов, которые местами формируют вертикальные петли, и многочисленных веретеновидных фибробластов (фиг. 2). Фибробласты ориентируются горизонтально к поверхности, хотя часть их имеет неопределенное расположение. Воспалительные процессы в грануляционной ткани минимальны: отек отсутствует, нейтрофильная инфильтрация слабая, появляются макрофаги и лимфоциты. Сосуды представлены в основном капиллярами, реже артериалами и венулами, еще реже мелкими артериями мышечного типа. Коллагеновые волокна фуксинофильны по Ван-Гизону, что свидетельствует об их зрелости (фиг. 3).
В глубокой части грануляционной ткани количество сосудов и клеток уменьшено, а количество коллагеновых волокон увеличено. Это свидетельствует о начале фиброзирования глубокой части грануляционной ткани.
Оценка эффективности заживления по 4-х бальной системе: воспаление - 2 балла, содержание сосудов - 4 балла, зрелость грануляционной ткани - 3 балла.
2) Результат испытания с использованием раневого покрытия на основе кожи свиней линии GAL-KO.
Испытания проведены с использованием раневого покрытия, представляющего собой кожные лоскуты трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу. До проведения испытаний раневое покрытие, стерилизованное γ-излучением дозой 15 кГр, выдержано в течение 7-8 час при сверхнизкой температуре минус 190°С в среде, содержащей 10% ДМСО.
Гистологически отмечается, что покрытие состояло из поверхностного слоя кожи - эпидермиса и сосочкового слой дермы. Фибринозно-лейкоцитарный слой относительно толстый, без признаков инфицирования. Глубокая часть этого слоя состоит из уплотненного фибрина. Ткань умеренно зрелая, богата сосудами, часть которых приобретает вертикальную ориентацию. Среди веретеновидных фибробластов остаются еще нейтрофильные лейкоциты, макрофаги, лимфоциты и плазматические клетки. Коллагеновые волокна тонкие и не всегда фуксинофильны, что указывает на их незрелость.
При использовании образцов, состоящих из нижних слоев дермы, в препарате оставался виден имплантат (дерма, покрывающая рану). Структура коллагеновых волокон практически не нарушена. При окраске по Ван-Гизону они сохраняют отчетливую фуксинофилию. Между имплантатом и дефектом кожи располагается сравнительно тонкий слой фибринозно - лейкоцитарного экссудата, причем лейкоциты на небольшое расстояние инфильтрирует имплантированную дерму. Глубже экссудата располагается грануляционная ткань с разной степенью созревания.
Местами ткань зрелая с большим количеством фуксинофильных коллагеновых волокон, но сохраняется увеличенное количество лимфоцитов и макрофагов. Сосуды многочисленны, часть из них сохраняют и имеют вертикальную ориентацию. В других участках отмечается значительно повышенное содержание макрофагов, лимфоцитов и плазматических клеток.
Все это свидетельствует о том, что нет принципиальных различий в заживлении ран под кожей свиньи линии GAL-KO, срезанной на различной толщине.
Оценка эффективности заживления по 4-х бальной системе: воспаление - 1-2 балла, содержание сосудов 2-3 балла, зрелость грануляционной ткани - 2-3 балла.
3) Результат испытания с использованием раневого покрытия на основе аллогенной крысиной кожи.
Раневая поверхность представлена относительно толстым фибринозно- лейкоцитарным слоем. Грануляционная ткань также сравнительно тонкая и в основном незрелая, хотя в отдельных участках она созревает, и там увеличивается количество коллагеновых волокон и вертикальных сосудов. На некоторых участках фибринозно-лейкоцитарный слой покрыт трансплантированной крысиной кожей, коллагеновые волокна которой остаются фуксинофильны.
В одном случае наблюдается различная структура раневых тканей. В одних участках под фибринозно-лейкоцитарном слоем грануляционная ткань практически отсутствует, и экссудат непосредственно соприкасается с жировой клетчаткой. В других участках слой грануляционной ткани состоит из относительно незрелой грануляционной ткани с малым количеством коллагеновых волокон, но многочисленными фибробластами и сосудами, без вертикальной ориентации. Коллагеновые волокна очень тонкие и в основном не фуксинофильные.
Оценка эффективности заживления по 4-х бальной системе: воспаление 1-2 балла, содержание сосудов - 2 балла, зрелость грануляционной ткани - 1 балл.
В ходе проведенных исследований, было выявлено на основе контрольных сравнений, что кожа свиньи линии GAL-KO является эффективным раневым покрытием при заживлении кожных ран вследствие полученных допустимых значений 4-х бальной системы по признакам - наличия воспалительного процесса, общего количества сосудов и зрелости грануляционной ткани.
Пример 4.
Для подтверждения эффективности предлагаемого способа оперативного лечения ожоговых ран IIIA степени были проведены испытания в Автономной некоммерческой организации «Институт медико-биологических исследований и технологий» (АНО «ИМБИИТ).
Испытания проведены с использованием раневого покрытия на основе кожи трансгенных свиней линии GAL-KO для медицинских изделий, применяемых при лечении ожоговых ран.
Цель испытания: проверка показателей апирогенности образцов раневого покрытия. Касается биологически активных веществ экзогенного (бактериального и вирусного), а также эндогенного (клеточно-тканевого) происхождения, которые обладают свойством вызывать перестройку уровня регуляции температурного гомеостаза, что обуславливает развитие лихорадки и повышение температуры тела.
Испытания проводились при следующих климатических условиях: температура воздуха плюс 25°С; относительная влажность воздуха 54%; атмосферное давление 749 мм.рт.ст.
Нормативные документы:
ГОСТ Р 51148-98. Государственный стандарт Российской Федерации. «Изделия медицинские. Требования к образцам и документации, представляемым на токсикологические, санитарно-химические испытания, испытания на стерильность и пирогенность».
Описание материала:
Раневое покрытие представляет собой кожные лоскуты трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу, размером 4,0-4,5 на 5,0-5,5 см, толщиной до 1,0 мм, заготовленные в условиях стерильной операционной с соблюдением правил асептики и антисептики. До проведения испытаний материал хранился в течении 7 часов при сверхнизких температурах (минус 190°С) в среде содержащей 10% ДМСО.
Экспериментальные животные - мыши.
Выполнены эксперименты на 5 белых лабораторных мышах.
В соответствии с Европейской конвенцией (Страсбург, 1986) и Хельсинкской декларацией Всемирной медицинской ассоциации о гуманном обращении с животными (2000), а также с требованиями приказа №267 МЗ РФ от 19.06.2003 «Правила по обращению, содержанию, обезболиванию и умерщвлению экспериментальных животных» животные содержались в стандартных условиях вивария, по 1 особи в клетке, получали кормление комплексным гранулированным лабораторным кормом при постоянном доступе к воде.
В качестве экспериментальной модели использована модель полнослойной плоскостной раны (Л.И. Слуцкий, 1969, A.B. Shekhter et al., 2005). Животных наркотизировали внутримышечным введением раствора золетила с рометаром.
В течение 8 суток животным измеряли температуру тела. Предельно допустимые значения температуры животных: 37,5-39,5°С.
В ходе испытания температура крыс варьировалась от плюс 37,5 до плюс 39,2°С.
Результаты испытания.

Объекты испытаний не являются пирогенными, что соответствует требованиям технического задания и ГОСТ Р 51148-98.
Учитывая выявленную в ходе экспериментов возможность получения стерильных опытных образцов раневого покрытия, а также принадлежность разрабатываемого медицинского изделия по степени потенциального риска к классу 2а, проведение исследования по оценке апирогенности не представляется необходимым.
Экспериментально установлено, что лоскуты кожи трансгенной свиньи линии GAL-KO временно прилипают во второй фазе, но никогда не васкуляризируются по-настоящему, т.е. после наложения покрытия на иссеченную рану происходит образование новых сосудов путем разрастания и ветвления старых сосудов. Новые сосуды аутокожи экспериментального животного не внедряются в материал покрытия и не происходит сцепление с кожей трансгенной свиньи.
Выводы.
Таким образом, применение биологического покрытия в виде лоскутов кожи трансгенной свиньи линии GAL-KO на срок до 14 дней после получения травмы при последующем лечении известными методами в условиях специализированных ожоговых центров и в общехирургических стационарах имеет следующие преимущества:
- увеличивается в последующем средняя приживляемость аутотрансплантатов на 10-20%;
- нормализуется развитие грануляционной ткани и активизирование процесса краевой эпителизации;
- отсутствует аллергическое действие;
- не оказывается отрицательное влияние на реакцию тканей (биологическая безопасность);
- обеспечивается более быстрая по сравнению с другими покрытиями эпителизация ран.
Изобретение позволяет обеспечить улучшение и сокращение сроков заживления ран путем обеспечения четырех основных важных характеристик покрытия ожоговой раны: просачиваемость пара, газа, прилипания, бактериального торможения и васкуляризации при биологической безопасности и создает условия подготовки ожоговой раны к аутотрансплантации. Материалы для покрытия ран, следовательно, должны быть заменены на кожу пациента, либо должны быть использованы методы по пересадке кожи.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЙ ТРАНСПЛАНТАТ ДЕРМАЛЬНОГО МАТРИКСА С МЕЗЕНХИМАЛЬНЫМИ МУЛЬТИПОТЕНТНЫМИ СТРОМАЛЬНЫМИ КЛЕТКАМИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ РАН С ЕГО ИСПОЛЬЗОВАНИЕМ | 2013 |
|
RU2526813C1 |
| Ранозаживляющая мазь для лечения термических ожогов | 2022 |
|
RU2787377C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛУБОКОГО ОЖОГА КОЖИ | 2008 |
|
RU2372922C1 |
| Способ стимуляции заживления ожоговых травм в эксперименте | 2023 |
|
RU2811662C1 |
| СРЕДСТВО ДЛЯ ЗАМЕСТИТЕЛЬНОЙ КЛЕТОЧНОЙ ТЕРАПИИ | 2007 |
|
RU2342163C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ КОЛЛАГЕНАЗЫ МИКРОБНОГО ПРОИСХОЖДЕНИЯ | 2000 |
|
RU2166950C1 |
| Способ восстановления кожного покрова | 2019 |
|
RU2731313C1 |
| Композит для ускоренного заживления ран различной этиологии, применение композита в качестве косметического средства и в качестве лечебного средства в ветеринарии, средство для регенерации кожных покровов на основе композита | 2017 |
|
RU2693228C2 |
| ТЕХНОЛОГИЯ РЕГЕНЕРАТИВНОЙ БИОПЛАСТИКИ ДЕФЕКТОВ ПОКРОВНЫХ ТКАНЕЙ | 2013 |
|
RU2547386C1 |
| Фармацевтическая композиция для лечения ран и ожогов | 2016 |
|
RU2636530C2 |

Изобретение относится к медицине, а именно к хирургии и комбустиологии, и может быть использовано в ходе лечения ожоговых ран для временного закрытия ран различной этиологии. Способ оперативного лечения ожоговых ран включает хирургическую обработку раны и временное наложение биологического раневого покрытия с последующим проведением аутотрансплантации. При этом покрытие, выдержанное при температуре минус 65-70°С и стерилизованное γ- или β-излученим дозой от 12 до 18 кГр, охлаждают при 180-190°С 6-8 часов и накладывают на рану на срок не более 14 дней. В качестве биологического раневого покрытия используют лоскуты кожи трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу, обеспечивающие отсутствие иммунной реакции отторжения раневого покрытия. Изобретение позволяет сократить сроки заживления ожоговых ран кожи человека при одновременной биологической безопасности используемого материала. 3 ил., 1 табл., 4 пр.
Способ оперативного лечения ожоговых ран, включающий хирургическую обработку раны и временное наложение биологического раневого покрытия с последующим проведением аутотрансплантации, отличающийся тем, что в качестве биологического раневого покрытия используют лоскуты кожи трансгенных свиней линии GAL-KO, не содержащие альфа-1,3-галактозу, обеспечивающие отсутствие иммунной реакции отторжения раневого покрытия, при этом покрытие, выдержанное при температуре минус 65-70°С и стерилизованное γ- или β-излучением дозой от 12 до 18 кГр, дополнительно охлаждают при 180-190°С 6-8 ч и накладывают на рану на срок не более 14 дней.
| СПОСОБ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ ОЖОГОВЫХ РАН IIIA СТЕПЕНИ | 2010 |
|
RU2455997C2 |
| CN 103356705 B, 30.09.2015 | |||
| Зиновьева Н.А | |||
| и др | |||
| Использование трансгенных GAL-KO свиней в ксенотрансплантации: проблемы и перспективы Сельскохозяйственная биология, no | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Устройство для усиления микрофонного тока с применением самоиндукции | 1920 |
|
SU42A1 |
Авторы
Даты
2018-11-30—Публикация
2018-03-06—Подача