Область техники, к которой относится изобретение
Настоящее изобретение относится к устройству для тестирования на беременность и к способу выполнения тестирования на беременность, а также к способу изготовления этого устройства.
Уровень техники
Были разработаны и запущены в серийное производство простые устройства для латерального проточного иммуноанализа, предназначенные для обнаружения аналитов в жидких образцах, см., например, документ EP291194. Такие устройства обычно содержат пористый носитель, содержащий высушенный мобилизуемый меченый связывающий реагент, способный связываться с соответствующим аналитом, и иммобилизованный связывающий реагент, также способный связываться с этим аналитом, предусмотренный в зоне обнаружения ниже по потоку от меченого связывающего реагента. Обнаружение иммобилизованного меченого связывающего реагента в зоне обнаружения указывает на присутствие аналита в образце.
Альтернативно, если интересующий аналит представляет собой гаптен, в устройстве для иммунологического анализа может использоваться реакция конкуренции, в которой меченый аналит или аналог аналита конкурирует с аналитом, присутствующим в образце, за связывание с иммобилизованным связывающим реагентом в зоне обнаружения. Альтернативно, в устройстве для анализа может использоваться реакция ингибирования, в соответствии с которой в зоне обнаружения предусматривается иммобилизованный аналит или аналог аналита, при этом устройство для анализа содержит мобилизуемый меченый связывающий реагент для аналита.
Устройство для анализа может быть способным обнаруживать присутствие и/или количество более одного аналита. Например, в случае анализов, обнаруживающих присутствие веществ, вызывающих физическую и психическую зависимость, устройство может быть способным определять полный перечень таких веществ. Такие устройства для латерального проточного иммуноанализа обычно предусматриваются с несколькими зонами обнаружения, причем такие зоны предусматриваются на одном или более латеральных проточных носителях в устройстве для анализа.
Определение результата анализа традиционно выполнялось визуально. Однако такие устройства требуют интерпретации результата пользователем, что привносит нежелательную степень субъективности, в частности, при низких уровнях аналита, когда интенсивность окраски зоны обнаружения является слабой.
В связи с этим были разработаны цифровые устройства, содержащие оптические средства обнаружения, предназначенные для определения результата анализа, а также средства отображения, предназначенные для отображения результата анализа. Цифровые считывающие устройства для анализа, предназначенные для использования в сочетании с аналитическими тест-полосками для определения концентрации и/или количества аналита в жидком образце, известны как устройства для анализа, содержащие интегральное цифровое считывающее устройство для анализа. Пример такого устройства раскрыт в документе EP 1484601.
Свет от источника света, такого как светоизлучающий диод (LED), падает на часть пористого носителя, и либо отраженный, либо пропущенный свет обнаруживается фотодетектором. Обычно считывающее устройство будет иметь более одного LED для освещения различных зон носителя, и для каждого из нескольких LED предусматривается соответствующий фотодетектор. В документе EP1484601 раскрыта оптическая схема для цифрового устройства считывания тест-полосок для латерального проточного анализа, содержащее отражатель, позволяющее уменьшить число фотодетекторов в устройстве.
Технология анализа вышеупомянутого типа воплощена в устройствах для теста на наличие беременности, проводимого самостоятельно. Обычно это устройства, используемые женщинами, подозревающими, что могли забеременеть. В связи с этим их следует разрабатывать так, чтобы их можно было легко использовать (не требуют какой-либо медицинской или технической подготовки), и обычно их утилизируют после однократного использования. Устройство, как правило, представляет собой устройство для латерального проточного иммуноанализа, и обычно этот тест начинается с приведения в контакт части для ввода образца аналитической полоски для латерального проточного анализа с образцом мочи. Часть для ввода образца аналитической полоски может погружаться в образец мочи в емкости, или, более типично, пользователь может помочиться непосредственно на часть для ввода образца. Затем проходит анализ, который не требует от женщины совершения каких-либо дальнейших действий, и результат регистрируется и считывается визуально или, в случае цифрового устройства, определяется с помощью средства считывания результата анализа и демонстрируется пользователю посредством устройства отображения, такого как, например, жидкокристаллический дисплей (LCD).
Традиционные тесты на наличие беременности этого типа основаны на измерении хорионического гонадотропина человека (hCG) в образце. hCG вырабатывается развивающимся эмбрионом, и концентрация hCG в образце выше определенного порогового значения даст положительный результат (т. е. ʺбеременнаʺ).
Существует потребность в усовершенствованном тесте на наличие беременности, особенно в усовершенствованном тесте на наличие беременности, проводимого самостоятельно: многие женщины хотят знать как можно раньше, беременны ли они, и поэтому существует потребность в очень чувствительном тесте, способном обнаруживать hCG в образцах, таких как моча, при очень низкой концентрации. Однако это создает проблему, поскольку hCG иногда может присутствовать в моче при относительно низкой концентрации по причинам иным, нежели беременность, при этом очень чувствительный тест на наличие беременности может дать ложноположительный результат (т. е. специфичность анализа снижается).
Как иллюстрация этого, в образце мочи может присутствовать hCG, не связанный с беременностью. В частности, hCG может присутствовать в моче женщин в периоды перименопаузы и постменопаузы и происходить из гипофиза, а не развивающегося эмбриона. Обнаружение этого вырабатываемого гипофизом hCG или иного не связанного с беременностью hCG в тесте на наличие беременности даст ложноположительный результат относительно беременности. Во многих странах женщины откладывают создание семьи на более поздний возраст, например из-за работы или иных обязательств, и, таким образом, небольшую, но значимую прослойку потребителей устройств для теста на наличие беременности, проводимого самостоятельно или ʹʹв домашних условияхʹʹ, составляют женщины более старшего возраста, которые могут попадать в категорию женщин периода перименопаузы и постменопаузы, и, следовательно, могут иметь ложноположительные результаты при использовании чувствительного анализа на hCG. По данным одного исследования до 10% продаж безрецептурных тестов на наличие беременности приходились на женщин старше 40 лет (Leavitt SA 2006, ʺA private little revolution: the home pregnancy test in American Cultureʺ. Bull. Hist. Med. 2006; 80:317-45).
Согласно общепризнанным определениям Всемирной организации здравоохранения ʺменопаузаʺ и ʺперименопаузаʺ представляют собой следующее:
Менопауза (естественная менопауза) - определяется как постоянное прекращение менструации в результате утраты фолликулярной активности яичников. Естественная менопауза признается наступившей после 12 последовательных месяцев аменореи, для которой отсутствует иная очевидная патологическая или физиологическая причина. Менопауза совпадает с последним менструальным циклом (FMP), что становиться известно с определенностью лишь в ретроспективе спустя год или более после события.
Перименопауза - термин перименопауза включает период, непосредственно предшествующий менопаузе (когда начинают проявляться эндокринологические, биологические и клинические признаки приближающейся менопаузы), и первый год после менопаузы.
Соответственно, для целей настоящего изобретения женщин периода перименопаузы определяют как женщин, находящихся в перименопаузе согласно вышеприведенному определению ВОЗ, а женщин периода постменопаузы определяются как женщин, прошедших менопаузу согласно вышеприведенному определению ВОЗ.
Тесты на наличие беременности, проводимые самостоятельно или ʹʹв домашних условияхʹʹ, должны быть надежными, чтобы позволить женщинам предпринимать соответствующие действия при получении результата своего теста. Требуемым уровнем надежности является точность ≥ 99% (т. е. суммарная величина ложноположительных и ложноотрицательных результатов составляет 1% или менее). Доступные в настоящее время устройства для теста, проводимого самостоятельно или в домашних условиях, могут обнаруживать hCG в моче при концентрации 25 мМЕ/мл или более с чувствительностью ≥ 99%. Такие устройства могут добиваться требуемого уровня точности ≥ 99%, но лишь при использовании в тот день, когда субъект предполагает начало своего цикла (т. е. предполагаемый первый день менструального кровотечения), или позже, поскольку с этого момента времени почти все женщины, которые беременны, будут иметь концентрацию hCG в моче 25 мМЕ/мл или выше, а уровни не связанного с беременностью hCG никогда в норме этого уровня не достигают. Однако из этого следует, что если женщина использует устройство для теста, проводимого самостоятельно, до первого дня предполагаемого цикла, возможен ложноотрицательный результат, поскольку концентрация hCG в моче еще не достигла уровня, выявляемого тестом. Соответственно, доступные в настоящее время традиционные устройства для теста на наличие беременности, проводимого самостоятельно, не являются на 99% точными, если используются раньше первого дня предполагаемого цикла. Фактически, средний уровень hCG в моче через 10 дней после овуляции составляет примерно 8,4 мМЕ/мл, и лишь около 10% образцов, взятых в этот день, будут иметь концентрацию hCG > 25 мМЕ/мл. Следовательно, в этот ранний период беременности при использовании традиционного устройства для теста, проводимого самостоятельно, с чувствительностью 25 мМЕ/мл будет наблюдаться очень низкий показатель обнаружения беременности. На 11 день после овуляции средний уровень повышается до 19,8 мМЕ/мл, так что на этой стадии менее 50% женщин, вероятно, получат положительный результат. Показатели обнаружения для более позднего тестирования будут составлять приблизительно 70% (день 12), 80% (день 13) и почти 100% (день 14), исходя из чувствительности теста 25 мМЕ/мл. Просто использование более чувствительного теста не является оптимальным решением, поскольку это увеличит риск ложноположительного результата из-за возросшей вероятности выявления hCG, не связанного с беременностью, так что тест по-прежнему не будет иметь точность ≥ 99%.
Следовательно, существует потребность в устройстве для теста на наличие беременности, особенно в устройстве для теста, проводимого самостоятельно или в домашних условиях, способном обнаруживать беременность с точностью ≥ 99% даже при использовании в момент времени при беременности, более ранний чем первый день предполагаемого цикла.
В другом контексте, во многих странах тесты на hCG в сыворотке обычно выполняют у почти всех женщин-пациентов детородного возраста перед проведением любого медицинского вмешательства, которое могло бы причинить вред развивающемуся плоду. Признанной является проблема повышенных уровней hCG в сыворотке, обусловленных ʺгипофизарнымʺ hCG, у женщин периода пери- и постменопаузы. Snyder et al. (Clinical Chemistry 2005 51, 1830-1835) проверяли изменения с возрастом концентраций hCG в сыворотке у небеременных женщин и исследовали применение измерений фолликулостимулирующего гормона (FSH) в сыворотке как инструмент для интерпретации более высоких, чем ожидаемые, результатов для hCG. Они предположили, что комбинацию измерений hCG в сыворотке, знания возраста субъекта и измерений FSH в сыворотке можно применять для уменьшения или полного исключения ʺложноположительныхʺ результатов обнаружения беременности. Эти авторы, однако, не затрагивали вопросы тестов на наличие беременности, проводимых самостоятельно, и, в частности, не затрагивали вопросы обнаружения беременности на очень ранней стадии.
Раскрытие изобретения
В первом аспекте в настоящем изобретении представлено тестирующее устройство для обнаружения беременности у субъекта-женщины, причем тестирующее устройство содержит:
аналитическое средство для измерения абсолютного или относительного количества hCG в образце, взятом у субъекта;
аналитическое средство для измерения абсолютного или относительного количества FSH в образце, взятом у субъекта;
и аналитическое средство для измерения абсолютного или относительного количества одного или более метаболитов прогестерона в образце, взятом у субъекта.
Образец может представлять собой любую подходящую биологическую жидкость, такую как цельная кровь, плазма, сыворотка или моча. Однако весьма предпочтительным является образец мочи, поскольку этот образец легко получать и он не требует проведения инвазивной процедуры. Кроме того, использование образца мочи облегчает самостоятельное проведение тестирования пользователем.
В этом контексте количество аналита, присутствующего в образце, может определяться в абсолютном выражении (например, как численное значение на единицу объема) или в относительном выражении (например, по отношению к предварительно заданному пороговому значению). В частности, ʺотносительное количество одного или более метаболитов прогестеронаʺ не предназначено означать, что концентрации разных метаболитов прогестерона в образце сравниваются между собой, а означает, что концентрация одного или более таких аналитов может сравниваться с предварительно заданным пороговым значением. Аналитическое средство будет адаптироваться и конструктивно исполняться для измерения своих соответствующих аналитов, хотя, как объяснено ниже, одно аналитическое средство может адаптироваться и конструктивно исполняться для измерения количества двух или более разных аналитов.
В пояснение, после зачатия дальнейшие циклы овуляции не требуются, поскольку женщина уже забеременела. Соответственно, после зачатия развитие фолликулов ингибируется подавлением выработки FSH. Таким образом, у беременной женщины можно ожидать наличие повышенных уровней hCG и низких уровней FSH. Соответственно, измерение FSH можно использовать в помощь интерпретации значимости обнаружения слегка повышенных уровней hCG, в частности, если есть подозрение, что это могло быть вызвано источником, не связанным с беременностью.
Следует также отметить, что во время первых 10-12 недель беременности прогестерон, вырабатываемый желтым телом, стимулирует рост эндометрия, тем самым обеспечивая продолжение беременности. Уровень прогестерона повышается во время частей лютеиновой фазы менструальных циклов, но если беременность не происходит (т. е. если субъект менструирует), этот уровень падает обратно до исходных уровней. Однако если беременность происходит, уровни прогестерона (и его метаболитов в моче) будут оставаться повышенными, и будут продолжать повышаться на протяжении беременности, так что прогестерон (и его метаболиты в моче) можно использовать как вспомогательное средство для hCG в качестве дополнительного подтверждения беременности.
Предпочтительно, тестирующее устройство будет дополнительно содержать средства для интерпретации результатов анализов для определения результата теста на наличие беременности и, предпочтительно, средство отображения для отображения результата теста.
Во втором аспекте в настоящем изобретении представлен способ обнаружения беременности у субъекта-женщины, причем способ включает этап приведения в контакт образца, взятого у субъекта, с тестирующим устройством в соответствии с первым аспектом, определенным выше. Как отмечалось выше, образец предпочтительно представляет собой образец мочи.
Ниже приводится более подробное описание предпочтительных признаков настоящего изобретения. Следует отметить, что если эти признаки будут описываться в отношении тестирующего устройства в соответствии с первым аспектом, они в равной степени будут применимы и к способу в соответствии со вторым аспектом (и наоборот), если контекст не диктует иначе.
Тестирующее устройство может предусматривать микрофлюидный анализ с одним или более изготовленными капиллярными каналами (обычно определенного внутреннего диаметра), по которым может протекать жидкий образец, но более предпочтительно тестирующее устройство предусматривает латеральный проточный анализ. Тестирующее устройство может предусматривать как микрофлюидный анализ, так и латеральный проточный анализ. В одном варианте осуществления тестирующее устройство будет предусматривать три латеральных проточных анализа - по одному анализу для соответствующего каждого одного из трех аналитов (т. е. hCG, FSH и метаболита прогестерона).
В некоторых вариантах осуществления может потребоваться проведение более одного анализа для определения одного конкретного аналита. Например, одним анализом может быть микрофлюидный анализ, а другим анализом может быть латеральный проточный анализ. Альтернативно, оба анализа для определения аналита могут представлять собой микрофлюидные или могут представлять собой латеральные проточные анализы. Если оба анализа для определения аналита представляют собой латеральные проточные анализы, они могут выполняться на одной тест-полоске для латерального проточного анализа или на соответствующих тест-полосках для латерального проточного анализа.
Например, во время ранних стадий беременности уровни hCG повышаются экспоненциально, и, следовательно, концентрация hCG в образце мочи, взятом у беременного субъекта, может значительно варьировать в зависимости от того, насколько долго длиться беременность субъекта. Поэтому может быть желательным обеспечение одного анализа, являющегося анализом с относительно высокой чувствительностью в отношении hCG, и одного анализа, являющегося анализом с относительно низкой чувствительностью в отношении hCG, так что концентрацию hCG в образце можно определить в расширенном диапазоне концентрации. (В пояснение, высокие уровни аналита могут вызывать осложнения, известные как ʺхукʺ-эффект. Это может приводить к неточностям при анализах с высокой чувствительностью из-за ограниченного диапазона анализа, и, следовательно, наличие анализа с меньшей чувствительностью может быть полезным, позволяющим получать точные измерения при очень высоких уровнях аналита).
В норме прогестерон в моче в обнаруживаемых количествах не присутствует. Вместо этого он метаболизируется, и различные метаболиты прогестерона выводятся из организма с мочой. Поэтому анализ по настоящему изобретению адаптирован для измерения одного или более метаболитов прогестерона в моче. Метаболиты прогестерона можно разделить на 4 группы: прегнандиолы, прегнанолоны, прегнандионы и последнюю группу, содержащую соединения, более полярные, чем прегнандиол. Теоретически, для измерения в соответствии с настоящим изобретением могут подходить один или более метаболитов из любой одной из этих четырех групп. Предпочтительные примеры включают прегнанолон (3α-гидрокси-5β-прегнан-20-он) и прегнандиол (5β-прегнан-3α-20 α-диол). Последнее соединение является особенно предпочтительным для проведения теста, поскольку оно представляет собой метаболит прогестерона, обычно присутствующий в моче при самой высокой концентрации (Cooke, I.D. 1976, Progesterone and its metabolites. В: Lorraine, J.A. & Bell, E.T. (ред.) ʺHormone Assays and their Applicationʺ стр. 447-508). Специалистам в данной области будет понятно, что ссылки, например, на прегнандиол и прегнанолон охватывают, если контекст не диктует иначе, их обычно встречающиеся производные. В частности, метаболиты прогестерона обычно присутствуют в моче в виде глюкуронидов или, изредка, в виде сульфатов. Таким образом, ссылки в данном документе, например, на прегнандиол охватывают, в частности, прегнандиол-3-глюкуронид (ʺP-3-Gʺ), иногда называемый также PdG. Кроме того, ссылки в данном документе на ʺпрогестеронʺ или ʺанализ на прогестеронʺ, если контекст не диктует иначе, предназначены охватывать, в частности, метаболиты прогестерона и анализы на метаболиты прогестерона, соответственно.
Следует принимать во внимание, что степень структурной гомологии и, таким образом, антигенное подобие различных метаболитов прогестерона могут быть очень высокими. Соответственно, в иммунологическом анализе антитело, которое связывается с конкретным метаболитом прогестерона с первым сродством связывания, может связываться с другим метаболитом прогестерона со вторым сродством связывания, которое может быть не значительно ниже первого сродства связывания, так что антитело может в некоторой степени перекрестно реагировать. Альтернативно, можно было бы использовать высокоспецифичное антитело, обладающее намного более высоким (например, по меньшей мере в 10 раз или более) сродством связывания в отношении конкретного метаболита прогестерона, чем в отношении других метаболитов прогестерона, присутствующих в моче человека. Соответственно, анализ на ʺметаболит прогестеронаʺ зачастую может выявлять несколько разных метаболитов прогестерона. Определенная степень перекрестной специфичности любых реагентов в отношении разных метаболитов прогестерона не имеет принципиального значения для настоящего изобретения, но специалисту в данной области, будет ясно, что этот фактор, наряду с другими характеристиками, может потребоваться учитывать при выборе реагента и подборе соответствующего ʺпороговогоʺ значения, как будет объяснено ниже.
Подобным образом, у человека существует несколько вариантов FSH, которые могут присутствовать в моче (например, фрагменты, такие как отдельные β цепи), и разных изоформ (см. Walton W.J. et al., J Clin Endocrinol Metab., 86, 3675-85, 2001; Dahl, K.D. и Stone M.P. J Andrology, 13, 11, 1992; и Baenziger, J.U. и Green E.D Biochem. et Biophys. Acta, 947, 287-306, 1988), например, с варьирующими степенями гликолизирования, и в иммунологическом анализе можно использовать антитело, связывающееся относительно специфично с одним вариантом, фрагментом или одной изоформой FSH, или можно использовать менее специфичное антитело, связывающееся с приемлемо высоким сродством с несколькими разными вариантами FSH человека. Опять-таки, этот фактор может влиять на выбор реагента и/или выбор порогового значения, подобранного в анализе, но в целом не имеет принципиального значения для настоящего изобретения. Подобные замечания применимы и к hCG и его вариантам.
Вообще говоря, концепция, лежащая в основе настоящего изобретения, представляет собой реализацию того, что для очень раннего выявления беременности можно использовать анализ на hCG с очень высокой чувствительностью, и что посредством дополнительного измерения FSH и метаболита прогестерона специфичность теста можно поддерживать на приемлемо высоком уровне (т. е. избегая большого числа ложноположительных результатов, обусловленных обнаружением hCG из не связанных с беременностью источников), при этом не требуется знание возраста субъекта. Предлагаемое устройство для анализа особенно подходит как простой P°C или, в частности, устройство для теста, проводимого самостоятельно, не требующее для его использования какой-либо медицинской или технической подготовки. В частности, устройство для анализа предпочтительно утилизируется после однократного использования. Кроме того, устройство желательно представляет собой простое устройство для латерального проточного анализа или устройство для микрофлюидного анализа, в котором различные анализы выполняются автоматически после приведения в контакт устройства с достаточным объемом образца мочи без необходимости какого-либо дополнительного вмешательства пользователя. Также предпочтительно, чтобы устройство представляло собой цифровое устройство, т. е. считывало результат анализа и отображало его для пользователя.
В частности, устройство для анализа по настоящему изобретению предпочтительно представляет собой устройство для теста, проводимого самостоятельно или в домашних условиях. В предпочтительных вариантах осуществления устройство для анализа обладает точностью ≥99% при его использовании до первого дня предполагаемого цикла. В частности, устройство для анализа по настоящему изобретению может достигать точности ≥99% даже при использовании его за 2 дня до первого дня предполагаемого цикла, предпочтительно, даже при использовании его за 3 дня до первого дня предполагаемого цикла, предпочтительно, даже при использовании за 4 дня до первого дня предполагаемого цикла, предпочтительно, даже при использовании его за 5 дней до первого дня предполагаемого цикла и, более предпочтительно, даже при использовании его за 6 дней до первого дня предполагаемого цикла (например, рассчитанного с учетом пика LH или всплеска LH).
Тестирование на hCG показывает вероятно положительные (беременна) результаты (т. е. в случае образцов, в которых hCG в моче выше предварительно заданного порогового значения), которые могут подтверждаться (или опровергаться) результатами анализов на FSH и метаболит прогестерона. Таким образом, например, уровень hCG чуть выше предварительно заданного порогового значения на фоне повышенного уровня FSH и низкого уровня метаболита прогестерона указывает, что у субъекта беременность отсутствует (и подразумевает, что повышенный уровень hCG обусловлен источником, не связанным с беременностью).
Таким образом, в настоящем изобретении предложен тест на наличие беременности, с помощью которого можно обнаруживать беременность с высокой чувствительностью (т. е. выявлять 99% или более беременных субъектов), с высокой специфичностью (т. е. с долей ложноположительных результатов 1% или ниже) и, более того, который может достигать этих результатов, даже если субъекты включают женщин периода пери- и постменопаузы; и, что даже более удивительно, в один момент времени (день) на очень ранней стадии беременности (т. е. даже до первого дня предполагаемого цикла) и без какой-либо другой внешней информации (такой как, например, возраст субъекта).
Еще одно преимущество настоящего изобретения заключается в том, что оно позволяет избежать ложноотрицательных результатов, возможных при использовании портативных устройств для теста на наличие беременности, основанных на определении hCG, если субъект имеет очень высокие уровни β корового фрагмента hCG. Эта проблема была признана в данной области техники и описана, например, в работе Gronowski et al. (2009 Clinical Chemistry 55, 1389-1394). Это объясняется тем, что заниженный сигнал от hCG, обусловленный ингибиторным эффектом избытка β-корового фрагмента, будет компенсироваться результатами анализа на FSH и метаболит прогестерона, на которые избыток β-корового фрагмента не повлияет.
Преимущественно, один образец мочи будет использоваться для обеспечения образца для теста для каждого из (по меньшей мере) трех анализов на присутствие аналита, выполняемых устройством/способом анализа по настоящему изобретению. В целях удобства, все три анализа на присутствие аналита будут выполняться по существу одновременно, предпочтительно, с использованием одного образца мочи, наносимого на устройство для анализа. Это можно удобно осуществлять путем использования, inter alia, вариантов осуществления, описанных ниже.
Для целей настоящего изобретения три теста на присутствие аналита будут выполняться ʺпо существу одновременноʺ, т. е. тесты проводятся с использованием образцов мочи, полученных во время одного и того же эпизода мочеиспускания, и результаты анализов считываются с разницей во времени не более 10 минут, предпочтительно не более 5 минут, более предпочтительно не более 3 минут и наиболее предпочтительно не более 60 секунд. Целесообразно, чтобы все три теста на присутствие аналита начинались по существу одновременно (т. е. с разницей во времени не более 60 секунд) путем нанесения пользователем образца мочи на контактирующую с образцом часть тестирующего устройства.
В предпочтительном варианте осуществления различные аспекты настоящего изобретения обладают одной или более (желательно всеми) из следующих характеристик:
(i) чувствительность 99% или выше;
(ii) специфичность 99% или выше;
(iii) способность достигать (i) и (ii), даже если день тестирования приходится на ранний срок беременности (т. е. до первого дня предполагаемого цикла согласно определению в данном документе);
(iv) способность достигать (i) и (ii), даже если тест выполняется/устройство для анализа используется один раз, в один момент времени (т. е. в один день);
(v) устройство/способ анализа не требуют какой-либо внешней информации (например, знания возраста женщины или любого анамнеза субъекта, такого как предыдущее измерение уровня hCG, FSH или прогестерона); и
(vi) способность достигать (i) и (ii), даже если субъекты включают женщин периода пери- и/или постменопаузы (согласно определению в данном документе).
Для цели настоящего описания ʺранняя стадияʺ беременности означает до первого дня предполагаемого цикла, рассчитанного с учетом обнаруженного у женщины пикового уровня лютеинизирующего гормона [ʺпик LHʺ], наблюдаемого во время овуляции или примерно в это время. Для пояснения, первый день предполагаемого цикла обычно считают днем через 15 дней после пика LH.
Авторы настоящего изобретения рассчитали, что с помощью приспособления и способа по настоящему изобретению должно быть возможным установление состояния действительной беременности с чувствительностью 99% или выше и специфичностью 99% или выше даже у женщин периода перименопаузы и постменопаузы по результату анализа в один момент времени.
Первый день предполагаемого цикла может рассчитываться с учетом определенных моментов времени. В частности, первый день предполагаемого цикла может рассчитываться с учетом дня всплеска LH (т. е. дня, в который в менструальном цикле первый раз обнаружено четкое заметное повышение уровня LH); это событие обычно происходит примерно за 12-24 часов до пика LH. Первый день предполагаемого цикла может также рассчитываться путем прибавления обычной продолжительности менструального цикла (в днях) к дате последней менструации. Другие способы расчета предполагаемого цикла включают прибавление 28 дней к дате последней менструации.
В общем случае, результаты анализов на присутствие аналита будут определяться по истечении конкретного времени (обычно, но не обязательно, определяемого с учетом времени, в которое образец был приведен в контакт с зоной ввода образца устройства для анализа). Время, в которое определяется результат анализа на присутствие аналита, может обозначаться как tE. Устройство считывания результата анализа может содержать своего рода встроенный таймер, предназначенного для определения, когда достигается tE. Таймер может включаться автоматически при приведении в контакте образца с устройством для анализа (например, жидкого образца, обеспечивающего протекание тока), или может запускаться пользователем (например, нажатием выключателя и т. п.) или любым иным удобным способом. В целях удобства, реакция анализе может достигать равновесия в tE, но это не является обязательным. tE может достигаться одновременно в одно и то же время для всех анализов на присутствие аналита, или tE может быть разным для разных аналитов.
В некоторых вариантах осуществления, если сигнал анализа на присутствие аналита остается ниже верхнего порогового значения в tE, результат анализа является отрицательным (в тех форматах, в которых присутствие аналита, представляющего интерес, приводит к образованию сигнала). Конечная точка анализа не обязательно может приходиться на завершение реакции. В действительности обычно будет считаться, что конечная точка tE была достигнута до завершения реакции.
Для удобства, конечная точка tE может определяться считывающим устройством с учетом конкретного момента времени (т. е. может считаться, что tE наступает через конкретное количество времени после начала анализа, например, через конкретный промежуток времени после включения считывающего устройства и/или вставки аналитической полоски в считывающее устройство и/или нанесения образца на аналитической полоски для теста). В целях иллюстрации tE, как правило, будет наступать через 1-10 минут, предпочтительно через 1-5 минут после начала анализа.
Желательно, устройство считывания результата анализа будет программироваться таким образом, чтобы в случае получения промежуточного сигнала повторить тестовое измерение. В простом варианте осуществления измерение повторяется в tE. Однако предпочтительно измерение повторяется один или более раз до конечной точки. Наиболее предпочтительно, считывающее устройство программируется на повторение измерения с регулярными промежутками времени (скажем, например, с промежутками 1 секунда или 5 секунд) до тех пор, пока сигнал не превысит верхнее пороговое значение, или пока не будет достигнут tE, в зависимости от того, что произойдет раньше.
Введение часов или иного прибора для отсчета времени в устройство считывания результата анализа является желательным, чтобы считывающее устройство могло автоматически проводить измерения в предварительно заданные моменты времени без дополнительного ввода информации пользователем.
Таким образом, например, считывающее устройство может программироваться для проведения измерений в начальный момент времени to и, при необходимости, проводить затем повторные измерения с любым требуемым промежутком времени до тех пор, пока сигнал не превысит верхнее пороговое значение, или пока не будет достигнут tE, как описано выше.
Кроме того, часы или иной прибор для отсчета времени помогают считывающему устройству в определении скорости накопления сигнала. Если измерения количества сигнала проводятся в два или более моментов времени (с известным разделением по времени), то можно легко рассчитать скорость накопления сигнала.
Следует отметить, что скорость или количество накопления сигнала можно было бы измерять как в абсолютном выражении, так и в виде относительного значения (например, по сравнению с контрольным значением или иным значением для сравнения, необязательно полученным в ходе по существу одновременной реакции).
В частности, устройство считывания результата анализа в некоторых вариантах осуществления может определять результат анализа (т. е. беременна или не беременна) до достижения tE, если одно или более полученных показаний анализа на присутствие аналита значительно выше или ниже (в зависимости от обстоятельств) конкретного соответствующего порогового уровня. ʹРаннееʹʹ определение результата анализа таким путем описано в документе EP 1484613. В случае настоящего изобретения, например, если количество FSH в образце находится выше предварительно заданного верхнего порогового значения (на уровне, при котором беременность никогда не наблюдается), то сигнал анализа на FSH проявится очень быстро, и это может позволить устройству считывания результата анализа (или наблюдателю-человеку) определить результат анализа раньше tE как результат ʺне беременнаʺ, возможно, не дожидаясь рассмотрения результата анализа на hCG и/или метаболит прогестерона. Аналогичным образом, если уровень метаболита прогестерона в образце является очень низким (например, ниже 1 мкг/мл), сильный сигнал анализа на метаболит прогестерона проявится очень быстро, до того как будет достигнут tE для анализа на метаболит прогестерона, что обеспечивает раннее определение результата анализа как ʺне беременнаʺ, опять-таки, возможно, без полученного показания анализа на hCG и/или FSH.
ʺРаннееʺ определение результата анализа может выполняться до достижения tE для любого из трех аналитов (т. е. hCG, метаболита прогестерона и FSH); или может выполняться до достижения tE для любого сочетания двух из трех аналитов (т. е. hCG и прогестерона, hCG и FSH или прогестерона и FSH); или до достижения tE лишь для одного из трех аналитов (т. е. в tE или после него для других двух из трех аналитов).
Аналогичным образом, существуют нижнее, среднее и верхнее пороговые значения для всех трех анализов на присутствие аналита, или для любого из трех анализов на присутствие аналита, или для любого сочетания двух из трех анализов на присутствие аналита.
Тестирующее устройство будет содержать по меньшей мере один путь течения, предпочтительно, по меньшей мере два пути течения и обычно три или даже четыре пути течения.
Термин ʺпуть теченияʺ для целей настоящего изобретения означает субстрат, который способен перемещать жидкость из первого положения во второе положение и может, например, представлять собой капиллярный канал, микрофлюидный путь или пористый носитель, такой как латеральный проточный пористый носитель. Пористый носитель может содержать один или более материалов пористого носителя, которые могут перекрываться при линейном или послойном размещении, или которые соединение при помощи жидкостной системы. Материалы пористого носителя могут быть одинаковыми или разными. Различные анализы в тестирующем устройстве могут предусматриваться на отдельных субстратах, или же они могут предусматриваться на общем субстрате так, чтобы жидкость, перемещаемая по пути течения одного анализа, не могла перетекать в путь течения другого анализа. Например, первый и второй анализы могут предусматриваться на одном и том же пористом носителе так, чтобы первый и второй пути течения были изолированы друг от друга. Этого можно добиться, например, с помощью лазерной резки частей пористого носителя, чтобы сделать их непористыми, тем самым отделяют первый и второй анализы. Альтернативно, для обеспечения двух или более (обычно по существу параллельных) путей течения на одном и том же пористом носителе вдоль полоски может наноситься непористый блокирующий материал. В других вариантах осуществления на одном пути течения можно размещать тесты в отношении двух или даже трех разных аналитов. Например, один путь течения может включать реагенты для тестирования на hCG и может также включать реагенты для тестирования на метаболит прогестерона. Альтернативно, один путь течения может включать реагенты для теста на hCG и FSH; или один путь течения может включать реагенты для теста на FSH и метаболит прогестерона. В частности, путь течения может содержать две зоны обнаружения, по одной для каждого аналита, в которых меченый реагент обычно может накапливаться, в целом, пропорционально (прямо или обратно) концентрации соответствующего аналита в образце.
Путь течения или пути течения в тестирующем устройстве могут содержать латеральный проточный пористый носитель. Подходящие материалы, которые могут использоваться в качестве пористого носителя, включают нитроцеллюлозу, ацетатное волокно, целлюлозу или производные целлюлозы, сложный полиэфир, полиамид, полиолефин или стекловолокно. Пористый носитель может включать нитроцеллюлозу. Преимуществом такого решения является то, что связывающий реагент может быть надежно иммобилизован без предшествующей химической обработки. Если материал пористой твердой фазы включает бумагу, например, иммобилизация антитела может выполняться путем химического связывания с использованием, например, CNBr, карбонилдимидазола или трезилхлорида.
В устройстве/способе анализа по настоящему изобретению обычно используют один или более связывающих реагентов. Обычно в анализе на hCG используют связывающий реагент, который связывается с hCG, в анализе на FSH используют связывающий реагент, который связывается с FSH, а в анализе на метаболит прогестерона используют очередной связывающий реагент, который связывается с метаболитом прогестерона. В анализы, в частности, можно включать использование меченого связывающего реагента. Как объяснено в другой части настоящего описания, можно было бы использовать меченый связывающий реагент, который связывается как с hCG, так и с FSH, поскольку эти две молекулы имеют некоторую общую структуру.
Для целей настоящего изобретения термин ʺсвязывающий реагентʺ относится к члену пары связывания, т. е. двум различным молекулам, где одна молекула связывается со второй молекулой посредством химических и/или физических механизмов взаимодействия. Эти две молекулы взаимосвязаны в том смысле, что их связывание между собой является таковым, что они способны отличать своего партнера по связыванию от остальных компонентов анализа, имеющих аналогичные характеристики. Члены пары связывания называют лиганд и рецептор (антилиганд), член пары связывания и партнер по паре связывания и т. п. Молекула может также представлять собой член пары связывания для скопления молекул; например, антитело, выработанное против иммунного комплекса из второго антитела и его соответствующего антигена, может рассматриваться как член пары связывания для иммунного комплекса.
В дополнение к членам пары связывания антиген и антитело другие пары связывания включают, в качестве примеров и без ограничения, биотин и авидин, углеводы и лектины, комплементарные нуклеотидные последовательности, комплементарные пептидные последовательности, эффекторные и рецепторные молекулы, кофакторы ферментов и ферменты, ингибиторы ферментов и ферменты, пептидную последовательность и антитело, специфичное в отношении этой последовательности или всего белка, полимерные кислоты и основания, красящие вещества и белковые связывающие вещества, пептиды и специфические белковые связывающие вещества (например, рибонуклеаза, С-пептид и С-белок рибонуклеазы) и т. п. Кроме того, специфические пары связывания могут включать члены, которые аналогичны оригинальному специфичному члену связывания.
ʺМеткаʺ, если используется в контексте меченого связывающего реагента, относится к любому веществу, которое способно производить сигнал, выявляемый визуальными или приборными средствами. Различные метки, подходящие для использования в настоящем изобретении, включают метки, производящие сигналы посредством либо химических, либо физических механизмов действия, например, являются оптически обнаруживаемыми. Такие метки включают ферменты и субстраты, хромогены, катализаторы, флуоресцентные соединения, хемилюминесцентные соединения, электроактивные виды молекул, молекулы красящих веществ, радиоактивные метки и метки-частицы. Метки-частицы могут включать магнитные или электронно-заряженные метки, которые могут обнаруживаться магнитными или электрохимическими средствами. Метка может быть ковалентно прикреплена к связывающему реагенту. В частности, метка может быть оптически обнаруживаемой. Предпочтительные оптически обнаруживаемые метки включают метки-коллоидные частицы металлов и частицы, несущие красящие вещества, описанные ниже.
Метка может включать коллоидную частицу металла, как, например, золото, серебро, платину, обогащенный серебром золь золота, золь углерода или наночастицы углерода; коллоидные частицы металлоидов или неметаллов, как, например, теллур или селен; или окрашенные или цветные частицы, как, например, полимерная частица, содержащая красящее вещество, или золь красящего вещества. Красящее вещество может быть любого подходящего цвета, например, синего. Красящее вещество может быть флуоресцентным или содержать квантовую точку. Подходящие флуоресцентные материалы хорошо известны специалистам в данной области. Золи красящих веществ можно получать из коммерчески доступных гидрофобных красителей, таких как Foron Blue SRP (Sandoz) и Resolin Blue BBLS (Bayer). Подходящие полимерные метки можно выбирать из целого ряда синтетических полимеров, таких как полистирол, поливилтолуол, полистирол-акриловая кислота и полиакролеин. Используемые мономеры в норме не растворимы в воде, и их эмульгируют в водном поверхностно-активном веществе так, чтобы образовались мицеллы мономеров, которые затем индуцируют к полимеризации путем добавления в эмульсию инициатора полимеризации. При этом получают по существу сферические полимерные частицы. Идеальный диапазон размеров для таких полимерных частиц составляет от примерно 0,05 мкм до примерно 0,5 мкм. Согласно одному иллюстративному варианту осуществления метка представляет собой коллоид золота с предпочтительным средним диаметром частицы в диапазоне 0,02-0,25 мкм.
Высушенные связывающие реагенты могут предусматриваться в пути течения микрофлюидного устройства или на материале пористого носителя, предусмотренного выше по потоку от материала пористого носителя, содержащего зону обнаружения, в устройстве латерального проточного типа. Находящийся выше по потоку материал пористого носителя может быть макропористым. Материал макропористого носителя должен характеризоваться низким связывание с белком или вообще не связываться с ним, или должен легко поддаваться блокированию при помощи реагентов, таких как BSA или PVA, для минимизации неспецифического связывания и облегчения свободного перемещение меченого реагента после того, как макропористый носитель был увлажнен жидким образцом. При необходимости, материал макропористого носителя можно предварительно обрабатывать поверхностно-активным средством или растворителем для придания ему большей гидрофильности и для содействия быстрому впитыванию жидкого образца. Кроме того, чтобы стабилизировать и помочь мобилизовать меченый реагент, можно использовать один или более сахаров (например, сахарозу, трегалозу). Их можно удобно наносить на путь течения и/или материал пористого носителя как часть раствора, в котором меченый реагент наносится на пористый носитель. Подходящие материалы для макропористого носителя включают пласмассы, такие как полиэтилен и полипропилен, или другие материалы, такие как бумага или стекловолокно. В случае, если меченый связывающий реагент метят обнаруживаемой частицей, макропористый носитель может иметь размер пор по меньшей мере в десять раз больше максимального размера частицы метки-частицы. Бóльшие размеры пор приводят к лучшему высвобождению меченого реагента.
Для удобства, тестирующее устройство будет содержать три или более путей течения: соответствующий путь течения для каждого анализа на присутствие аналита. Возможно, однако, что два или более анализов на присутствие аналита могут совместно выполняться в общем пути течения (возможно, в дополнение к необязательной общей зоне нанесения образца, описанной ниже). Как правило, путь течения будет включать капиллярный или иной микрофлюидный проточный канал, или один или более пористых элементов, по которым может транспортироваться водная текучая среда, такая как образец мочи.
В одном варианте осуществления тестирующее устройство содержит три отдельных полоски для латерального проточного анализа, по одной для каждого анализа на присутствие аналита. В еще одном варианте осуществления тестирующее устройство может содержать две полоски для латерального проточного анализа; одна из полосок служит для проведения анализа на один из аналитов (например, hCG), а другая полоска служит для проведения соответствующего анализа на каждый из двух других аналитов. Также может быть предусмотрен вариант осуществления, в котором один путь течения или теста-полоска для латерального проточного анализа используется для теста на все три аналита.
Тестирующее устройство может, в частности, содержать зону для нанесения образца. Это зона из пористого (как правило, гигроскопичного) материала, на которую может наноситься водный образец, такой как моча. Зона для нанесения образца может быть общей зоной. То есть, жидкий образец, нанесенный на общую зону для нанесения образца, может транспортироваться в два или более разных путей течения для анализа.
Как правило, образец наносится на зону для нанесения образца пользователем, который мочится непосредственно на зону для нанесения образца.
В предпочтительном варианте осуществления устройство для анализа содержит корпус, в котором размещены большинство или все функциональные компоненты анализов и реагенты для анализов. Для удобства корпус выполнен из водонепроницаемой синтетической пластмассы и предпочтительно является по существу непрозрачным. Для достижения требуемой степени непрозрачности в пластмассу может добавляться замутняющее средство. Подходящие синтетические пластмассы для изготовления корпуса включают, в частности, поликарбонат, полистирол, сополимеры полистирола, полиолефины, полипропилен, полиэтилен и акрилонитрил. Желательно, корпус может изготавливаться состоящим из двух или более частей, которые соединяются, при этом большинство (или все) остальные компоненты устройства для анализа находятся внутри собранных частей корпуса или между ними. Части корпуса могут соединяться и скрепляться обычными крепежными средствами, такими как соединение на защелках, или сваркой пластмасс и т. п.
В предпочтительном варианте осуществления устройство для анализа содержит корпус (как правило, имеющий признаки, отмеченные выше), и при этом часть или зона для нанесения образца выступает за корпус для облегчения нанесения образца мочи на часть или зону для нанесения образца. Часть или зона для нанесения образца, которая выступает за корпус, до использования может закрываться съемной крышкой. Предпочтительно, крышка также может изготавливаться из синтетической пластмассы, которая может быть непрозрачной, или прозрачной, или полупрозрачной. После нанесения образца на зону для нанесения образца крышку обычно возвращают на место.
На дистальном, нижнем по потоку конце путей течения анализа может предусматриваться абсорбирующий ʺприемникʺ. Может предусматриваться общий приемник, или приемник может предусматриваться на дистальном конце каждого анализа. Абсорбирующий приемник предпочтительно может включать высокоабсорбирующий материал, такой как, например, ватманская бумага CF7, и должен обеспечивать достаточную поглощающую способность для удаления любой несвязанной метки поблизости зоны обнаружения. В качестве альтернативы такому приемнику может быть достаточным отрезок материала пористой твердой фазы, который продолжается за пределами зоны обнаружения. Преимущество в обеспечении высокоабсорбирующего приемника заключается в том, что он удаляет или по существу удаляет избыток меченого связывающего реагента из путей течения соответствующих анализов. Это позволяет уменьшить распространение несвязанного меченого связывающего реагента поблизости соответствующих зон и, следовательно, позволяет использовать пути течения анализов в устройстве, которое может иметь отличающиеся количества меченого связывающего реагента.
Для удобства тестирующее устройство будет содержать и другие компоненты, известные специалистам в данной области, и обычные в традиционных устройствах для теста на наличие беременности, проводимого самостоятельно или в домашних условиях, в том числе (но без ограничения) индикатор достаточного количества образца (например, описанный в документе PCT/EP2013/061178), прокладку, предотвращающую ʺпереполнениеʺ (например, раскрытую в документе WO2012/069610), использование потока образца в качестве контроля анализа (например, как описано в документе EP 1484611, US 6194222); ʺраннееʺ определение положительных или отрицательных результатов (например, как раскрыто в документе EP 1484613; US 5679584); автоматическое ʺпробуждениеʺ электронных устройств (например, автоматическое включение после смачивания устройства образцом, что замыкает электрическую цепь) и использование цифрового индикатора выполнения анализа (например, как промышленном образце Европейского Сообщества с регистрационным № 1367304) или ʺизменяющий цвет тампонʺ и т. п., которые обеспечивают для пользователя визуальную индикацию того, когда образец был нанесен на тестирующее устройство, и/или визуальную индикацию того, что анализ начался (например, как описано в документе WO 2003/058245). Преимущественно, тестирующее устройство будет представлено потребителю в водонепроницаемой упаковке, необязательно дополнительно содержащей поглотитель влаги, например пакетик с силикагелем.
Для удобства, элементы анализов будут находиться на некоторой опоре или защитном слое для обеспечения механической прочности и подходящей степени жесткости. Для удобства, элемент(ы) анализа плюс опора могут называться и поставляться как аналитическая полоске для теста. Элементы всех трех анализов могут располагаться на одной аналитической полоске, или на двух, трех или даже четырех (т. е. более одной аналитической полоске для одного аналита) аналитических полосках для теста. Аналитическая полоска или полоски для теста можно адаптировать и конструктивно исполнять для вставки пользователем в тестирующее устройство, или, более предпочтительно, аналитическая полоска или полоски для теста могут образовывать составляющую часть тестирующего устройства, которое покупается потребителем с аналитической полоской(ами) для теста, предварительно вставленными или загруженными в тестирующее устройство.
Результаты анализов могут считываться внешним средством считывания результатов анализов или непосредственно пользователем, но намного более предпочтительно, тестирующее устройство будет содержать встроенное устройство считывания результата анализа для считывания результата анализа. Устройство считывания результата анализа предпочтительно считывает результаты всех трех анализов на присутствие аналита. Преимущественно, устройство считывания результата анализа будет включать электронный компонент, в частности, цифровой электронный компонент, такой как микропроцессор. Как правило (хотя не обязательно), анализы считываются оптическими средствами, т. е. путем измерения количества света, отраженного и/или пропущенного зоной обнаружения, в которой оптически меченый реагент обычно скапливается пропорционально (прямо или обратно) концентрации аналита в образце. Альтернативно, анализы могут считываться, например, путем магнитных или электромагнитных измерений. Очевидно, что способ, посредством которого считывается анализа, может зависеть от свойств метки(меток), используемых для мечения реагента(ов) для анализа.
Внешнее средство считывания результата анализа может представлять собой специализированное устройство считывания результата (например, подобное устройству, описанному в документе EP 1066530). Альтернативно, внешнее средство считывания результата анализа может быть ʺнеспециализированнымʺ, таким как мобильный телефон или иное переносное электронное устройство (например, планшетный компьютер), предпочтительно снабженное камерой, где результат анализа считывается путем измерения интенсивности сигнала, вырабатываемого видимой меткой.
Устройство считывания результата анализа, будь то внешнее или образующее часть комбинированного устройства для анализа/устройства считывания результата анализа, может считывать и интерпретировать результаты анализов или может передавать данные результата анализа в дистанционно расположенное устройство для данных анализа, подлежащих интерпретации. Данные анализа могут передаваться в дистанционно расположенное устройство в режиме реального времени. Эти данные могут передаваться путем подключения к сети Интернет, или могут храниться в запоминающем устройстве (таком как флэш-накопитель и т. п.), которое физически транспортируется к удаленному устройству, или данные могут передаваться средствами беспроводной связи (например, Bluetooth, связь малого радиуса действия [NFC] и т. п.).
Микропроцессор может управлять работой компонентов оптического считывания или иного считывания анализа и, для удобства, будет запрограммирован с соответствующими пороговыми значениями для сигналов анализа для каждого из аналитов, или сможет иметь доступ к ним, при этом сравнивать фактические значения сигналов анализа с предварительно заданными пороговыми значениями и интерпретировать результаты анализов так, чтобы определить результат теста на наличие беременности.
Таким образом, устройство считывания результата анализа содержит компоненты, необходимые для считывания результата анализов. Также тестирующее устройство будет преимущественно содержать устройство отображения результата анализа, предназначенное для отображения пользователю результата теста на наличие беременности. Обычно устройство отображения будет включать LCD, но возможны и другие типы устройства отображения (например, c использованием ʺэлектронных чернилʺ). В тех вариантах осуществления, в которых устройство для анализа (или, конкретнее, его компонент) требует для работы источник питания, устройство для анализа предпочтительно будет оснащаться встроенным источником питания, таким как батарея. Очень маленькие и дешевые, батареи коммерчески легкодоступны. Также устройство может снабжаться выключателем для соединения с встроенным источником питания и включения устройства.
В альтернативных вариантах осуществления результаты анализов могут непосредственно считываться пользователем способом, известным по традиционным тестам на беременность, проводимым самостоятельно, например, пользователем, производящим осмотр одного или более окошек, расположенных над зонами обнаружения, для определения присутствия или отсутствия выявляемого сигнала в одной или более (или всех) зонах обнаружения. Каждая зона обнаружения может снабжаться отдельным окошком в непрозрачном корпусе, чтобы позволить пользователю произвести осмотр зоны обнаружения. Альтернативно, две или более (или все) зоны обнаружения могут охватываться одним большим окошком. Обычно в таких считываемых пользователем устройствах пользователь будет непосредственно проводить осмотр зон обнаружения латерального проточного или микрофлюидного анализов. В других форматах пользователь может определить результат с учетом цветовой таблицы или индикатора. Для удобства тестирующее устройство будет поставляться вместе с инструкциями или руководством по считыванию результата анализа (если устройство не интерпретирует результаты анализа для пользователя). Например, пользователю может предоставляться напечатанная цветовая таблица для облегчения интерпретации таких непосредственно считываемых визуальных тестов.
Комбинированные аналитические полоски для теста на наличие беременности/устройство считывания результата анализа с устройством отображения могут называться ʺцифровым тестом на наличие беременностиʺ, и такие цифровые тестирующие устройства являются коммерчески доступными, и их можно было бы адаптировать, с учетом преимущества по настоящему раскрытию, для создания тестирующего устройства в соответствии с настоящим изобретением.
Микропроцессор предпочтительно будет программироваться таким образом, чтобы компоненты для считывания результата анализа считывали результаты анализа(ов), интерпретировали результаты анализа и отображали заключение пользователю.
Компоненты для считывания результатов анализов предпочтительно будут содержать по меньшей мере один источник света и по меньшей мере один фотодетектор. По меньшей мере один источник света предпочтительно представляет собой светоизлучающий диод (LED). По меньшей мере один фотодетектор предпочтительно представляет собой фотодиод или фототранзистор. Источник света при анализе освещает зону обнаружения на анализе, в которой при проведении анализа обычно скапливается меченое вещество в зависимости от концентрации интересуемого аналита в образце, применяемом для анализа. Меченое вещество может накапливаться таким образом, что оно прямо коррелирует с концентрацией аналита (т. е. чем выше концентрация аналита, тем больше количество метки, накапливающее в зоне обнаружения). Обычно используется формат ʺсэндвичʺ-анализа, хорошо известный специалистам в данной области. Альтернативно, накопление меченого вещества может отрицательно коррелировать с концентрацией аналита (т. е. чем выше концентрация аналита, тем меньше количество метки, накапливающееся в зоне обнаружения). Эта отрицательная корреляция является типичной для анализов конкурентного или ингибиторного типа, который часто используется, когда интересуемый аналит представляет собой гаптен и/или слишком мал, чтобы допустить одновременное связывание двух разных антител (например, как в случае метаболитов прогестерона).
Как FSH, так и hCG представляют собой гетеродимерные молекулы, содержащие α- и β-субъединицы. α-субъединица FSH и hCG по существу идентична, так что антитела, направленные на α-субъединицу, могут связываться как с FSH, так и с hCG. Следовательно, в анализе на эти две молекулы потенциально можно использовать общий реагент, который может представлять собой, например, мобилизуемое, напрямую меченое (т. е. выявляемое оптически) антитело. Соответствующие зоны обнаружения могут содержать иммобилизованное антитело захвата, специфичное в отношении β субъединицы (которая отличается у FSH и hCG). Очевидно, что это относится к иммунологическому анализу типа ʺсэндвичʺ, но хорошо известны и другие форматы анализа, которые могли бы использоваться вместо него.
Может случиться, если образец содержит высокие уровни hCG (например, поскольку образец предоставлен субъектом с относительно продолжительным сроком беременности), что антитело, специфичное к общей α-субъединице, может ʹзаполнятьсяʹʹ высокими уровнями hCG, при этом эффективно снижается количество антитела, доступного для связывания с FSH, что, возможно, тем самым является причиной недооценки количества FSH, присутствующего в образце. На практике это, вероятно, не вызовет каких-либо проблем, поскольку такие высокие уровни hCG будут почти всегда (>99,9%) связаны с наличием беременности, которая будет точно обнаружена и интерпретирована тестирующим устройством независимо от любого результата анализа на FSH. Также возможно использовать двойную пару антител, специфичных к β субъединице, для анализа на hCG и двойную пару антител, специфичных к β субъединице, для анализа на FSH. Этот формат мог бы нейтрализовать вышеупомянутый эффект, наблюдаемый при высоких уровнях аналита.
С точки зрения необходимости снижения стоимости (особенно в тех вариантах осуществления, в который устройство утилизируют после однократного использования), предпочтительно использовать один фотодетектор для обнаружения света, испускаемого зоной обнаружения по меньшей мере двух, предпочтительно трех, разных анализов. Будет понятно, что на самом деле свет происходит не от зон обнаружения - он происходит от источников света - но он отражается зонами обнаружения и/или пропускается через них, в зависимости от ситуации, и поэтому кажется, что он испускается ими. Обычно, но не обязательно, каждая зона обнаружения освещается соответствующим источником света, таким как LED.
Один источник света, такой как LED, можно было бы использовать для освещения зоны обнаружения по меньшей мере двух разных анализов и, если возможно, трех разных анализов. Однако также возможно предусмотреть несколько LED. Например, для освещения каждой соответствующей зоны обнаружения может предусматриваться по одному LED. Если предусмотрены несколько LED, они могут производить освещение одним цветом или могут производить освещение с разной длиной волны. Возможны варианты осуществления, в которых число LED (или иных источников света) равно или даже превышает число зон обнаружения. Альтернативно, могут использоваться разные конфигурации, в которых один LED освещает две зоны обнаружения, при этом число LED меньше числа зон обнаружения.
В устройстве обычно может использоваться зона контроля. Это часть пути течения микрофлюидного или латерального проточного анализа, которая используется для сравнения с ней показания, полученного в зоне обнаружения. Использование зоны контроля хорошо известно специалистам в данной области. В частности, в устройстве может использоваться ʹобщаяʹʹ зона контроля (как описано в документе EP 2031376), при этом одна зона контроля используется как контроль для двух или более зон обнаружения, по меньшей мере одна из которых расположена в другом пути течения.
Микропроцессор или компьютеризованный орган управления может приводить к тому, что источник(и) света может освещать одну или более зон обнаружения последовательно так, чтобы различать свет, отраженный соответствующими зонами обнаружения и/или пропущенный через них. В одном варианте осуществления источники света излучают свет с разной длиной волны в разное время, и фотодетектор(ы) различают разные длины волны. Дополнительно или альтернативно, для регулирования зоны, освещаемой конкретным источником света, могут использоваться оптические отражатели (неподвижные или регулируемые). Более подробные сведения об этом типе оптических устройств, которые можно использовать, приведены, например, в документах EP 1484601, US 6055060 и US 5889585. Во избежание сомнений, термин ʺсветʺ, используемый в данном документе, не предназначен для обозначения исключительно излучения в той части электромагнитного спектра, которая видима наблюдателю-человеку, и охватывает, например, ультрафиолетовое и инфракрасное излучение. Тем не менее, может быть предпочтительной работа компонентов в видимой части спектра и чувствительность к ней.
Микропроцессор или средства компьютеризованного управления предпочтительно будет содержать несколько хранящихся пороговых значений для аналитов, с которыми буду сравниваться результаты анализов, чтобы позволить устройству считывания результатов анализов интерпретировать результаты и отображать пользователю соответствующее заключение (например, беременна или не беременна). Микропроцессор или средства управления преимущественно будут программироваться посредством алгоритма для измерения результатов теста, сравнения их с предварительно заданными пороговыми значениями и отображения заключения.
В одном варианте осуществления микропроцессор или средства управления будут вначале определять результат анализа на hCG и сравнивать его с предварительно заданным нижним пороговым значением hCG. Если результат, определенный в анализе на hCG, будет ниже предварительно заданного нижнего порогового значения hCG, можно будет сразу же установить отсутствие беременности у субъекта, и этот результат будет показан пользователю с помощью устройства отображения (например, в виде слов НЕ БЕРЕМЕННА или их эквивалента на любом языке; или посредством интуитивно-понятного символа, например, знака минус или нуль).
Однако если результат, определенный в анализе на hCG, будет выше предварительно заданного нижнего порогового значения, устройство считывания результата анализа может переходить к измерению результата анализа на FSH. Если результат анализа на FSH указывает, что концентрация FSH в образце выше его предварительно заданного порогового значения, можно будет удостовериться в отсутствии беременности у субъекта, и этот результат будет отображен для пользователя, как описано выше.
Однако если измеренный уровень FSH в образце будет ниже его соответствующего предварительно заданного порогового значения, устройство считывания результата анализа может затем измерять результат анализа на метаболит прогестерона (в этом случае, анализа на P3G). Если результат анализа указывает, что концентрация P3G в образце ниже его соответствующего предварительно заданного порогового значения, можно будет удостовериться в отсутствии беременности у субъекта. Если концентрация P3G в образце выше предварительно заданного порогового значения, субъект является беременным, и устройство считывания результата анализа будет отображать пользователю соответствующее заключение посредством устройства отображения.
Пороговые значения могут храниться в устройстве по настоящему изобретению в виде абсолютных концентраций аналита (т. е. в единицах массы или МЕ на единицу объема) и/или в виде значений оптической плотности, или любым иным удобным образом.
В одном варианте осуществления в устройстве может быть предусмотрено верхнее и нижнее пороговое значение для одного, двух или всех трех аналитов hCG/FSH/прогестерон. Например, в одном варианте осуществления устройство может иметь верхнее пороговое значение для hCG и нижнее пороговое значение для hCG. Если измеренная концентрация hCG превышает верхнее пороговое значение для hCG, устройство может утверждать, что субъект является беременным, без анализа результатов анализов на FSH/прогестерон. Это утверждение может делаться устройством на ʺраннемʺ этапе (например, до того как анализ достигнет равновесия), если очевидно, что результат анализа на аналит hCG будет превышать верхнее пороговое значение. В других вариантах осуществления результат ʹБеременнаʹʹ, тем не менее, подтверждается проверкой результатов анализов на FSH и прогестерон.
Если результат анализа на hCG ниже нижнего порогового значения для hCG, устройство утверждает, что субъект не является беременным (с подтверждением результатами анализа на FSH и прогестерон или без него). Если результат анализа на hCG выше нижнего порогового значения для hCG, но не превышает верхнее пороговое значение для hCG, устройство потребует результатов анализа на FSH и прогестерон, чтобы прийти к заключению относительно наличия или отсутствия беременности. Устройство может проверять эти результаты анализа на FSH и прогестерон последовательно (например, сначала один аналит, затем другой, в любом порядке) или параллельно.
В частности, устройство может иметь верхнее или нижнее пороговое значение для анализов на FSH и/или прогестерон. Возможно, что выбор какого-либо из нескольких пороговых значений для применения в конкретном случае будет зависеть от абсолютной или относительной концентрации аналита, обнаруженной в двух других анализах, так что может использоваться схема ʺвзвешиванияʺ или ʺкомпенсацииʺ. Например, концентрация hCG, которая, как определено, находится на более верхнем конце промежуточного диапазона между верхним и нижним пороговыми значениями для hCG, могла бы ʺкомпенсироватьʺ относительно низкую концентрацию прогестерона, заставляя устройство применить нижнее пороговое значение для прогестерона при определении состояния беременна/не беременна. И наоборот, низкий уровень FSH и/или высокий уровень прогестерона, например, могли бы компенсировать относительно низкую концентрацию hCG в образце.
Измерение в ходе анализа и/или интерпретация результата анализа могут включать один или более этапов обработки данных, на которых данные анализа подвергают одному или более вычислениям или иному типу обработки. Для удобства эту обработку будут выполнять с помощью цифрового электронного устройства, такого как микропроцессор и т. п., которое обычно образует часть внешнего или встроенного устройства считывания результата анализа. Например, обработка данных может представлять собой расчет отношения. В частности, этап обработки может включать расчет отношения FSH: метаболит прогестерона или vice versa. Отношение может основываться на относительных интенсивностях сигнала или на расчетах концентрации соответствующих аналитов по измеренным интенсивностям сигнала или иного подходящего соответствующего параметра. В частности, ʹграничнуюʹ интенсивность сигнала для hCG или выведенную концентрацию hCG можно подтвердить или проверить расчетом отношения FSH: метаболит прогестерона (или vice versa).
Кроме того, в дополнение к hCG, FSH и прогестерону устройство может проводить анализы на другие аналиты. Эти другие аналиты могли бы включать, в частности, гормоны, такие как, например, LH, hPL (плацентарный лактоген человека), и/или релаксин, и/или эстроген или его метаболит. Еще одним примером такого гормона служит тиреостимулирующий гормон (TSH). TSH связан с hCG, FSH (и LH) тем, что все эти гормоны содержат α-субъединицу, очень схожую с α-субъединицей остальных гормонов. TSH содержит также β субъединицу, уникальную для TSH. Уровни TSH в моче уже измеряли ранее (см., например, Yoshida et al., 1988 Endocrinol. Jpn. 35, 733-739), хотя концентрация весьма низка. Концентрация такого одного или более дополнительных аналитов также может учитываться устройством при определении беременна/не беременна, возможно с помощью воздействия на выбор применимых пороговых значений для одного или более аналитов из hCG/FSH/прогестерон. Может измеряться отношение одного или более дополнительных аналитов к одному или более из hCG, FSH и прогестерона. В частности, может измеряться отношение TSH к hCG (или vice versa). Измерение других аналитов может быть особенно полезным при усовершенствованиях настоящего изобретения, описанных ниже.
При усовершенствовании вышеописанных основных принципов может потребоваться указывать пользователю не только наличие или отсутствие беременности у субъекта, но также (в случае наличия беременности) срок беременности (т. е. внутриутробный возраст плода) с точки зрения приблизительного количества времени, прошедшего со времени зачатия. Это могло бы указываться путем показа числа дней или, более предпочтительно, числа недель. Для удобства, мог бы отображаться один из трех интервалов: 1-2 недели, 2-3 недели и >3 недель. Для содействия этому тестирующее устройство преимущественно может снабжаться несколькими разными пороговыми значениями концентрации hCG (или, точнее, пороговыми значениями для аналитического результата теста на hCG), соответствующими соответственному количеству недель после зачатия. Способы достижения этого раскрыты в документе WO 2009/147437. Опять-таки, для содействия этому варианту осуществления может быть желательным, чтобы тестирующее устройство могло тестировать концентрацию hCG в расширенном диапазоне (например, путем включения как теста с относительно высокой чувствительностью, так и теста с относительно низкой чувствительностью на hCG), и подходящие способы для достижения этого описаны в документе WO 2008/122796. Оценке гестационного срока беременности может содействовать измерение концентрации других аналитов в дополнение к hCG, например, hPL (см. документ WO2012/055355), и/или метаболита(ов) прогестерона.
В некоторых вариантах осуществления было бы желательным, чтобы тестирующее устройство выполняло своего рода функцию контроля. Традиционно, устройства для теста, проводимого самостоятельно, обеспечивают определенную индикацию, что тест функционировал правильно.
Типично, функция контроля будет включать использование контрольной зоны, в которой обычно будет скапливаться меченый реагент, если на зону нанесения образца тестирующего устройства было нанесено достаточное количество образца. Для удобства, меченым реагентом будет меченое антитело или иной реагент, который нанесен в высушенной форме на верхнюю по потоку или проксимальную часть тест-полоски, с возможностью дальнейшего высвобождения, и мобилизуется после регидратации образцом, и захватывается специфическим агентом захвата, иммобилизованным в контрольной зоне. Контроль показывает, достаточное ли количество образца было нанесено на тестирующее устройство, и показывает, что реагенты теста в достаточной степени сохранили свои связывающие свойства, и что меченый реагент был мобилизован в достаточной степени.
Различные признаки настоящего изобретения описываются далее посредством иллюстративного примера и со ссылками на сопутствующие графические материалы, в которых:
фиг. 1 представляет собой покомпонентный вид одного варианта осуществления устройства в соответствии с настоящим изобретением;
на фиг. 2-5 проиллюстрированы разные форматы аналитических тест-полосок для использования в разных вариантах осуществления устройства в соответствии с настоящим изобретением; и
на фиг. 6 схематически проиллюстрирован один вариант осуществления алгоритма/древовидной логической схемы использования в устройстве в соответствии с настоящим изобретением.
ПРИМЕРЫ
Пример 1
В первоначальных экспериментах hCG в моче, FSH в моче и P3G в моче измеряли у 119 небеременных добровольцев из группы периода пери- и постменопаузы (PP, возраст 41-90 лет), в которой всего 50 образцов имели [hCG] ≥ 2,5 мМЕ/мл, и у 72 беременных добровольцев, успешно вынашивающих беременность до родов (возраст 21-40 лет), от дня 7 EMP (ожидаемой, но не наступившей менструации) до дня +3 EMP. Образцы тестировали, при возможности, что дало всего 589 образцов для раннего срока беременности (ʺEPSʺ), из которых 434 имели [hCG] ≥ 2,5 мМЕ/мл, как определили с помощью анализа PerkinElmer® Delfia®.
Анализ этих результатов показал, что применяя для определения беременности пороговый уровень hCG в моче, составляющий по меньшей мере 2,5 мМЕ/мл, в сочетании как с пороговым значением для FSH, составляющим 10 мМЕ/мл или меньше, так и с пороговым значением для P3G, составляющим по меньшей мере 4 мкг/мл, действительную беременность можно было бы выявлять со 100% прогностичностью положительного результата (отсутствие ложноположительных результатов в группе небеременных). Пороговые уровни этих трех аналитов, применяемых для определения беременности, установленные настоящим исследованием, могут измениться при расширении базы данных, но результаты показывают, что используя hCG в сочетании с FSH и P3G, связанный с беременностью hCG можно было отличать от связанного с гипофизом hCG у женщин периода пери- и постменопаузы.
Результаты, полученные с применением этих пороговых значений, представлены в таблице 1.
Период пери/постменопаузы (PP)
(n=119)
(n =50)
Образцы для раннего срока беременности
(n=589)
(n=434)
Результаты в таблице 1 имеют очень большое значение. Они показывают, что в случае группы A очень чувствительный тест на hCG (выявляющий всего лишь 2,5 мМЕ/мл hCG) в сочетании с тестами на FSH и метаболит прогестерона (P3G) дал нулевую долю ложноположительных результатов в статистически значимой выборке женщин, при этом успешно идентифицировал всех беременных субъектов в группе B.
Пример 2
В одном варианте осуществления изобретения устройство для теста на наличие беременности будет содержать латеральный проточный иммуноанализ, выполненный в формате двух полосок из нитроцеллюлозы (NC), при этом сэндвич-анализ на hCG расположен на первой полоске. Сэндвич-анализ на FSH и конкурентный анализ на P3G будут расположены на второй отдельной полоске с двумя отдельными зонами захвата. Обе полоски будут запускать анализ одновременно, благодаря общей зоне для нанесения образца, контактирующей с пористой средой, которая будет контактировать с обеими полосками из нитроцеллюлозы. Устройство будет проводить цифровое измерение ответа на сигнал (связанная метка) на зонах захвата NC-полосок в ответ на количество интересуемого аналита. Встроенный алгоритм будет давать конечному пользователю цифровое отображение ответа на экране (Беременна/Не беременна и/или гестационный срок) в зависимости от уровней аналитов.
Пример возможного алгоритма схематически проиллюстрирован на фиг. 6. Следует отметить, что алгоритм, представленный на фиг. 6, представляет собой лишь один вариант осуществления, и могли бы применяться многие другие варианты осуществления. Следует также отметить, что абсолютные концентрации аналитов, представленные на фиг. 6, являются исключительно иллюстративными, и что могли бы использоваться другие концентрации аналитов.
Пример 3
Что касается фиг. 1, на которой показан покомпонентный вид одного варианта осуществления, устройство в соответствии с настоящим изобретением содержит состоящий из двух частей корпус, изготовленный из синтетической пластмассы. Корпус имеет верхнюю часть 2 и нижнюю часть 4. Корпус изготовлен из непрозрачной пластмассы, такой как поликарбонат или полипропилен. При необходимости может добавляться вещество, придающее непрозрачность.
Внутри корпуса находится источник питания, такой как маленький элемент 6 таблеточного типа, подающий электрическую энергию компонентам, закрепленных на блоке печатных плат (PCBA) 8. Эти компоненты включают, в частности, один или более LED и фотодиодов и жидкокристаллический дисплей 10. Компоненты, закрепленные на PCBA 8, включают компоненты, необходимые для считывания результатов анализов, выполняемых на двух полосках для латерального проточного анализа, закрепленных внутри корпуса. Одна из полосок 12 предназначена для выполнения анализа на hCG, а другая полоска 14 предназначена для выполнения анализа как на FSH, так и на прегнандиол-3-глюкуронид (P3G).
Верхняя и нижняя части 2, 4 корпуса взаимодействуют с образованием по существу не проницаемого для влаги герметичного соединения вокруг вышеупомянутых компонентов. Образец мочи достигает полосок 12, 14 для латерального проточного анализа посредством тампона 16 для ввода пробы. Одна концевая область тампона 16 для ввода пробы находится в сообщении посредством потока жидкости с прилегающей концевой областью каждой из полосок 12, 14 для анализа (так что тампон для ввода пробы действует как общая зона для нанесения образца).
Противоположная концевая область тампона 16 для ввода пробы выступает через отверстие на одном конце корпуса и расположена снаружи, что обеспечивает возможность нанесения пробы на тампон для ввода пробы. Выступающая часть тампона для ввода пробы защищена съемной крышкой 18, форма и размеры которой выполнены так, чтобы она взаимодействовала с концом корпуса, на который надевается, и создавала с ним плотное, точно подогнанное зацепление.
В проиллюстрированном варианте осуществления для нанесения образца мочи на тампон 16 для ввода пробы пользователь снимает крышку 18 и мочится непосредственно на тампон. Тампон изготовлен из абсорбирующего материала, и поэтому образец впитывается в тампон и пассивным образом течет вдоль тампона и в полоски 12, 14 для анализа. Затем пользователь, необязательно, надевает крышку 18 на место. Для содействия протеканию образца в полоски для анализа и вдоль них полоски для анализа на их дистальном конце (т. е. на конце, дальнем от тампона 16 для ввода проб) находятся в сообщении посредством потока жидкости с прокладкой-ʺприемникомʺ 20 из высокоабсорбирующего материала.
Латеральные проточные анализы продолжаются традиционным образом, что в результате приводит к накоплению меченого связывающего реагента, зависящему от концентрации аналита (пропорционально или обратно пропорционально, в зависимости от обстоятельств) в зоне(ах) обнаружения на тест-полосках 12, 14, что обнаруживается и считывается компонентами считывания анализа, закрепленными на PCBA 8. Микропроцессор, ASIC или подобный, анализирует и интерпретирует полученные показания и отображает результат анализа на LCD 10, который виден пользователю через окошко или отверстие 21, выполненное в подходящем месте в верхней части 2 корпуса.
Важно, чтобы до использования тест-полоски 12, 14 для латеральногопроточного анализа сохранялись сухими, и по этой причине в PCBA предусмотрено гнездо для влагопоглотителя 22, который поглощает влагу внутри корпуса.
Пример 4
Что касается фиг. 2, этот пример относится к варианту осуществления, в котором две разные полоски для латерального проточного анализа используются в сочетании с устройством в соответствии с настоящим изобретением или образуют его составную часть.
На фиг. 2 одна из полосок, 30, используется для выполнения анализа на hCG с высокой чувствительностью. Другая полоска 32 используется для выполнения анализа как на FSH, так и на P3G. Образец мочи попадает на обе полоски 30, 32 для анализа из общего элемента для ввода пробы (для упрощения не показан) и течет вдоль полосок в направлении, указанном стрелкой 34. На своих проксимальных концах (т. е. на тех концах, на которые образец мочи попадает вначале) обе полоски имеют прокладку 36 для конъюгата из стекловолокна, а вблизи дистального конца обе полоски находятся в сообщении посредством потока жидкости с высокоабсорбирующим ʺприемникомʺ 38, который стимулирует протекание образца вдоль полосок для анализа. Обе полоски также содержат после ʺприемникаʺ 38 пару установочных отверстий 40. Они способствуют правильной установке полосок внутри устройства, в частности, чтобы полоски для анализа могли правильно считываться компонентами для считывания результата анализа данного устройства. Обратите внимание, что пары установочных отверстий 40 не являются симметричными, так что полоски нельзя случайно поменять друг с другом.
Что касается полоски 30, прокладка 36 для конъюгата нагружена мобилизуемым моноклональным антителом к альфа-субъединице hCG, конъюгированным с золем золота (42). Этот конъюгат высушен на прокладке для конъюгата и высвобождается после смачивания образцом.
Зона 44 обнаружения содержит иммобилизованное моноклональное антитело, специфичное к β-субъединице hCG. Таким образом, любой hCG, присутствующий в образце, связывается меченым конъюгатом и образует сэндвич с антителом ʹзахватаʹʹ к β-субъединице hCG в зоне обнаружения, причем этот способ известен специалистам в данной области.
Зона 46, ограниченная пунктирными линиями, представляет собой зону контроля, которую средство считывания результата анализа использует для калибровки полученных показаний анализа. Одна и та же зона 46 контроля может использоваться для калибровки как полученных показаний анализа на hCG, так и показаний, полученных для анализов на FSH и P3G на полоске 32 (т. е. может использоваться общая зона контроля).
Что касается полоски 32, прокладка для конъюгата из стекловолокна имеет два разных конъюгата 48: один представляет собой золь золота, конъюгированный с моноклональным антителом к α-субъединице FSH, а другой представляет собой золь золота, конъюгированный с моноклональным антителом к P3G. (В этом примере антитело к α-субъединице hCG и антитело к α-субъединице FSH принадлежат к одному клону антител).
Иммобилизованное моноклональное антитело к β-субъединице FSH используется как антитело захвата в зоне 50 обнаружения FSH, тогда как иммобилизованный конъюгат P3G-овальбумина используется как молекула захвата в зоне 52 обнаружения P3G.
Основная часть каждой полоски 30, 32 для анализа выполнена из нитроцеллюлозы, как показано с помощью номера позиции 54.
Хотя в этом варианте осуществления зона 52 обнаружения P3G показана ниже по потоку зоны 50 обнаружения FSH, предусмотрено, что относительные положения этих двух зон обнаружения могут быть противоположными.
Дополнительным вариантом является формат, в котором анализы на hCG и P3G выполняются на одной полоске, а для анализа на FSH используется отдельная полоска.
Пример 4A
Можно предусмотреть другой формат анализа. Он по существу идентичен таковому, изображенному на фиг. 2 и описанному в примере 4, за исключением того, что в этом варианте один из мобилизуемых конъюгатов, нанесенных на прокладку 36 для конъюгата, представляет собой конъюгат P3G-овальбумин, меченый золем золота (вместо mAb к P3G), а иммобилизованная молекула захвата в зоне 52 обнаружения P3G представляет собой иммобилизованное mAb к P3G. При такой конфигурации P3G в образце конкурирует с меченым конъюгатом за связывание с антителом захвата в зоне 52 обнаружения.
Пример 5
Что касается фиг. 3 (на которой подобные компоненты обозначены номерами позиций, используемыми на фиг. 2), в этом варианте осуществления все 3 анализа выполняются с использованием одной полоски для анализа. Прокладка 36 для конъюгата из стекловолокна нагружена общим конъюгатом антитело к α-субъединице hCG и антитело к α-субъединице FSH - золь золота и конъюгатом mAb к P3G - золь золота (42, 48, соответственно).
Зона 44 обнаружения hCG содержит иммобилизованное mAb к β-субъединице hCG. Зона 50 обнаружения FSH содержит иммобилизованное mAb к β субъединице FSH, а зона 52 обнаружения P3G содержит иммобилизованный конъюгат P3G-овальбумин.
Как и раньше, относительные положения зон обнаружения могут меняться. Кроме того, как в примере 4A, мобильным реагентом на P3G может быть конъюгат P3G-овальбумин, меченый золем золота, а зона 52 обнаружения P3G может содержать иммобилизованное антитело к P3G.
С легкостью может предусматриваться еще один вариант, в котором мобилизуемые конъюгаты могут содержать первый золь золота, конъюгированный с моноклональным антителом, специфичным к β субъединице hCG, и второй золь золота, конъюгированный с моноклональным антителом, специфичным к β-субъединице FSH. Соответствующие зоны обнаружения содержат иммобилизованные антитело к α-субъединице hCG и антитело к α-субъединице FSH. Другим возможным вариантом является использование антитела к β-субъединице hCG, как в мобилизуемом конъюгате, так и в качестве иммобилизованного антитела захвата, при условии, что эти два антитела связываются с разными эпитопами и, таким образом, не мешают друг другу и не конкурируют между собой за связывание с hCG. Подобным образом также может проводиться анализ на FSH с использованием антител, специфичных к β-субъединице FSH, как в мобилизуемом конъюгате, так и в качестве иммобилизованного антитела захвата.
Пример 6
В этом примере, схематически проиллюстрированном на фиг. 4, для каждого аналита предусмотрена отдельная полоска для латерального проточного анализа. Анализ на hCG проводится на полоске 100, анализ на FSH проводится на полоске 102, а анализ на P3G проводится на полоске 104. Подобные компоненты обозначены теми же номерами позиций, как на фиг. 2.
Образец наносится на все три полоски дл анализа через общий элемент для ввода пробы (для упрощения не показан). Общая прокладка-ʹприемникʹ 38 находится в контакте посредством потока жидкости вблизи дистального конца каждой полоски для анализа. В отличие от фиг. 2, в этом варианте осуществления каждая полоска 100, 102, 104 для анализа имеет свою собственную зону 46 контроля. Кроме того, каждая полоска для анализа имеет зону 60 процедурного контроля, которая указывает, правильно ли был выполнен анализ в смысле того, сохранили ли связывающие реагенты свои связывающие свойства.
Пример 7
На фиг. 5 проиллюстрирован еще один вариант осуществления. В нем также используются три полоски для анализа. Однако две из трех полосок предназначены для измерения уровней hCG, таким образом, одна из полосок, 110, представляет собой анализ на hCG с высокой чувствительностью (для обнаружения низких уровней hCG), одна из полосок, 112, представляет собой анализ на hCG с низкой чувствительностью (для обнаружения высоких уровней hCG), а третья полоска 114 предназначена для анализа как на FSH, так и на P3G. Подобные компоненты обозначены теми же номерами позиций, что и на фиг. 2.
Чтобы снизить чувствительность анализа на hCG на полоске 112, прокладка 36 для конъюгата нагружена (42ʹʹ) не только мобилизуемым золем золота, конъюгированным с mAb к α-субъединице hCG, но также свободным (немеченым) mAb к β-субъединице hCG, которое связывается с hCG, присутствующем в образце и, таким образом, конкурирует с иммобилизованным антителом захвта к β-субъединице hCG, расположенным в зоне 44 обнаружения. Таким образом, при высоких уровнях аналита hCG в образце, система анализа не забивается. В этом случае немеченое моноклональное антитело к β-субъединице hCG действует в качестве средства-ʺуловителяʺ. Средство-уловитель не обязательно должно представлять собой антитело, но может быть любым немеченым средством, связывающимся с hCG и препятствующим (косвенно) отложению меченого реагента в зоне обнаружения. Средство-уловитель, например, может быть иммобилизованно на/в пути течения, или может быть смешано (в мобилизуемой форме) с меченым конъюгатом.
Использование анализов на hCG как с высокой, так и с низкой чувствительностью обеспечивает возможность устройству измерять hCG точно в пределах расширенного диапазона концентраций, и эта конфигурация применима в тех вариантах осуществления, в которых устройство может отображать результат, который показывает не только то, что субъект является беременным, но также может показывать пользователю количественную оценку того, насколько долго протекает беременность субъекта (например, в виде недель после зачатия).
Хотя вышеприведенные примеры иллюстрируют применение различных форматов латерального проточного анализа, будет очевидно, что в аналогичном устройстве для анализа мог бы использоваться микрофлюидный анализ или анализ, основанный как на латеральном проточном анализе, так и на микрофлюидном анализе.
Пример 8
В этом примере описаны этапы при получении полосок для латерального проточного анализа, пригодных для применения в устройстве в соответствии с настоящим изобретением, проиллюстрированном на фиг. 4.
Получение реагентов для анализа:
A. Подготовка меченого золем золота антитела:
1. Анализ на P3G:
Способ:
Боратный буфер (20 мл, 20 мМ, pH 8,5) добавляли в раствор золя золота с размером частиц 80 нм (20 мл, A550нм=OD 6,85, BBI International) с полученим конечного раствора, содержащего золь золота, с OD 3,425 в 10 мМ боратном буфере.
Раствор антитела к P3G (клон № 5806:2, Alere, г. Сан-Диего, 40 мл, 160 мкг/мл в 10 мМ боратном буфере) быстро смешивали с раствором золя золота на магнитной мешалке в течение 30 минут при комнатной температуре.
После 30 минут смешивания в реакционную смесь добавляли 610 мкл 65,6 мг/мл раствора β-казеина и смешивание продолжали в течение дополнительных 30 минут при комнатной температуре.
Конечная концентрация β-казеина в реакционной смеси составляла 0,5 мг/мл.
Раствор золя разливали в пробирки Falcon (50 мл), и растворы центрифугировали (4000 g, 10 мин, 15°C).
Прозрачные надосадочные жидкости сливали, а осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком.
Растворы золя переносили в пробирки Eppendorf и центрифугировали (4000 g, 7 мин, 15°C).
Надосадочные жидкости аккуратно удаляли, а осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком, добавляли промывочный буфер (1 мл, 0,5 мг/мл β-казеина в 10 мМ боратном буфере) дл ресуспендировани золь. После ресуспендирования растворы центрифугировали (4000 g, 7 мин, 15°C).
Надосадочные жидкости аккуратно удаляли, а осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком, добавляли промывочный буфер (1 мл, 0,5 мг/мл β-казеина в 10 мМ боратном буфере) для ресуспендирования золя. После ресуспендирования растворы центрифугировали (4000 g, 7 мин, 15°C).
Надосадочную жидкость удаляли, а осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком, золь ресуспендировали в небольшом объеме буфера для хранения (0,5 мг/мл BSA в PBS++азид [PBSA]), и конечный объем доводили до 2 мл. Хотя в первоначальных экпериментах использовали 0,5 мг/мл BSA в буфере для хранения, было установлено, что присутствие BSA мешает анализу на P3G. Поэтому впоследствии вместо BSA в буфере для хранения использовали 0,5 мг/мл казеина. В вариантах осуществления настоящего изобретения, в которых компоненты для анализа на P3G могли бы контактировать с компонентами для других анализов (например, в которых как анализ на P3G, так и анализ на hCG и/или FSH выполняются в одном пути течения или на одной полоске для латерального проточного анализа), тогда для других анализов также будет необходимо исключить использование BSA, чтобы предотвратить воздействие на анализ на P3G.
Конечную OD препарата золя определяли измерением поглощения при 550 нм.
2. Анализ на hCG и анализ на FSH:
Способ:
Боратный буфер (20 мл, 20 мМ, pH 8,5) добавляли в раствор золя золота с размером частиц 80 нм (20 мл, A550нм=OD 6,85, BBI International) с получением конечного раствора, содержащего золь золота, при OD 3,425 в 10 мМ боратном буфере.
Раствор антитела к α-субъединице hCG (клон № 3299:4, Alere, Сан-Диего, 40 мл, 20 мкг/мл в 10 мМ боратном буфере) быстро смешивали с раствором золя золота на магнитной мешалке в течение 30 минут при комнатной температуре.
После 30 минут смешивания в реакционную смесь добавляли 610 мкл 65,6 мг/мл раствора β-казеина и смешивание продолжали в течение дополнительных 30 минут при комнатной температуре. Конечная концентрация β-казеина в реакционной смеси составила 0,5 мг/мл.
Раствор золя разливали по пробиркам Falcon (50 мл) и растворы центрифугировали (4000g, 10 мин, 15°C).
Прозрачные надосадочные жидкости сливали, и осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком.
Растворы золя переносили в пробирки Eppendorf и центрифугировали (4000 g, 7 мин, 15°C).
Надосадочные жидкости аккуратно удаляли, и осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком, добавляли промывочный буфер (1 мл, 0,5 мг/мл раствор β-казеина в 10 мМ боратном буфере) для ресуспендирования золя. После ресуспендирования растворы центрифугировали (4000 g, 7 мин, 15°C).
Надосадочные жидкости аккуратно удаляли и осажденный золь перемешивали вихревым способом и подвергали обработке ультразвуком, добавляли промывочный буфер (1 мл, 0,5 мг/мл раствор β-казеина в 10 мМ боратном буфере) для ресуспендирования золя. После ресуспендирования растворы центрифугировали (4000 g, 7 мин, 15°C).
Надосадочную жидкость удаляли и осажденный золь перемешали вихревым способом и подвергали обработке ультразвуком, золь ресуспендировали в небольшом объеме буфера для хранения (0,5мг/мл BSA в PBSA) и окнечный объем доводили до 2 мл.
Конечную OD препарата золя определяли измерением поглощения при 550 нм.
B. Подготовка реагентов для иммобилизации на нитроцеллюлозу:
Хотя в примере ниже описывается подготовка и использование конъюгатов P3G-овальбумин, может предусматриваться, что могут использоваться другие белковые или синтетические полимерные конъюгаты P3G. Белковые конъюгаты P3G включают, но не ограничиваются ими, бычий сывороточный альбумин, иммуноглобулин G, желатин и бета-казеин. Типичные примеры полимерных носителей включают полиаллиламин, поливиниловый спирт, полилизин и полиэтиленимин.
Анализ на P3G:
Подготовка конъюгатов P3G-овальбумин (молярное отношение P3G к овальбумину 10:1)
Способ
Подготовка активированного NHS сложного эфира P3G (10 мг P3G, 10% шкала DMSO)
Водорастворимый карбодииимид, EDC, использовали для подготовки активированного NHS сложного эфира P3G. Реакцию проводили с молярным избытком EDC (1,1x) и NHS (1,5x) относительно P3G (2,01361×0-5 молей P3G).
Общий объем для проведения реакции составлял 600 мкл.
14,153 мг/мл раствор EDC (1-этил-3-[3-диметиламинопропил]карбодиимида гидрохлорида, Thermo Scientific, кат. № 77149, M.W.=191,7) готовили путем растворения 48 мг EDC в 3,39 мл DMSO (99,7% сверхсухой, Acros, кат. № 3484400).
11,6 мг/мл раствор NHS (N-гидроксисукцинимид, Sigma Aldrich, кат. № 130672, M.W.=115,09) готовили путем растворения 29 мг NHS в 2,5 мл DMSO.
10 мг P3G (5β-прегнан-3α, 20α-диол глюкуронид, P3G, Sigma, кат. № P3635, M.W.=496,63) отвешивали в стеклянный флакон и добавляли 300 мкл раствора EDC и 300 мкл раствора NHS, приготовленных, как описано выше, с получением реакционной смеси, содержавшей в 1,1× больше EDC и в 1,5× больше NHS, чем P3G. Реакционную смесь перемешивали при комнатной температуре в темноте в течение 4 часов, и реакцию оставляли продолжаться в течение ночи (приблизительно 16 часов) при температуре 20°C.
В этот раствор добавляли DMSO (400 мкл) и доводили общий объем раствора до 1000 мкл.
Исходя из 100% превращения P3G в сложный эфир P3G-NHS, в 1000 мкл будет содержаться 2,01361×0-5 молей активированного сложного эфира. Таким образом, 100 мкл этого раствора будут содержать 2,01361×0-6 молей.
Подготовка конъюгата P3G-овальбумин
Использовали 100 мкл активного сложного эфира (2,01361×0-6 молей).
4,43 мг/мл раствор овальбумина (Sigma, кат. № A5503, >98%, MW=44000) в буфере PBS (таблетки PBS, Sigma, кат. № P4417) готовили путем растворения 92,4 мг овальбумина в 20,858 мл PBS, и 2 мл этого раствора использовали для 10-кратного препарата.
В раствор овальбумина добавляли DMSO (100 мкл) непосредственно перед добавлением раствора активированного NHS P3G (100 мкл). Таким образом, конечная концентрация DMSO в реакционной смеси поддерживалась на уровне 10% (объем/объем).
Реакционный раствор перемешивали при комнатной температуре в течение 3,5 часа. После прохождения реакции в течение 3,5 часа реакцию гасили добавлением в раствор 1M буфера Tris pH 7,4 (100 мкл).
Затем P3G-овальбумин центрифугировали, и прозрачную надосадочную жидкость удаляли и очищали на колонке PD-10 (GE Healthcare, кат. № 17-0851-01), предварительно уравновешенной PBSA.
- Раствор конъюгата (2,5 мл) наносили на верхнюю часть уравновешенной колонки, и всему раствору позволили просочиться в слой геля.
- Затем в колонку внесли буфер для элюирования (PBSA, 3 мл) и элюат собирали в чистый стеклянный сосуд. Этот элюат содержал очищенный конъюгат P3G-овальбумин.
Для определения концентрации белка использовали коэффициент экстинкции (A280 0,1%), составляющий 0,7. Затем конъюгат P3G-овальбумин концентрировали до 3 мг/мл для иммобилизации на нитроцеллюлозе.
1. Анализ на hCG:
Перед иммобилизацией на нитроцеллюлозе антитело к β-субъединице hCG- (клон № 3468:2, Alere, Сан-Диего) разбавляли в PBSA до 3 мг/мл.
2. Анализ на FSH:
Перед иммобилизацией на нитроцеллюлозе антитело к β-субъединице FSH (клон № 5948:2, Alere, Сан-Диего) разбавляли в PBSA до 3 мг/мл.
C. Подготовка и средства для размещения и иммобилизации специфических связывающих веществ:
Способ
1. Анализ на P3G:
1.1. Подготовили блокирующий буфер PVA (pH 9) (Tris-основа 20 мМ (Sigma), 1% вес/объем PVA (80% PVA, гидролизованный, 9-10K MW (Sigma), 0,05% вес/объем Tween 20 (Sigma) и NaCl 150 мМ (Sigma)).
1.2. Подготовили блокирующий раствор PVA путем добавления 2% вес/объем сахарозы (Sigma) в 47,5 мл блокирующего буфера PVA с добавлением 2,5 мл этанола (Sigma).
1.3. Белые проклеенные нитроцеллюлозные (Whatman) листы нарезали на полосы 35 см ×40 мм с помощью резальной машины, и на одном конце полосы выбивали отверстия с шагом 6 мм (можно было бы использовать самую разную величину шага, однако для примеров, представленных в данному документе, использовали шаг отверстий 6 мм).
1.4. Устройство для нанесения BioDot установили для нанесения конъюгата P3G-овальбумин в требуемое место на нитроцеллюлозной полоске при концентрации 3 мг/мл со скоростью нанесения 1 мкл/см.
1.5. После нанесения полосы высушивали при 55°C и блокировали с использованием блокирующего раствора PVA, а затем сушили при температуре 65°C и хранили на протяжении ночи при комнатной температуре с влагопоглотителем в запечатанных саше из фольги.
2. Анализ на hCG:
Следовали этапам 1.1-1.3 включительно из раздела C.1.
Устройство для нанесения BioDot установили для нанесения антитела 3468 в требуемое место на нитроцеллюлозной полосе при концентрации 3 мг/мл со скоростью нанесения 1 мкл/см.
После нанесения полосы сушили при 55°C и блокировали с использованием блокирующего раствора PVA, а затем сушили при 65°C и хранили на протяжении ночи при комнатной температуре с влагопоглотителем в запечатанных саше из фольги.
3. Анализ на FSH:
Следовали этапам 1.1-1.3 включительно из раздела C.1.
Устройство для нанесения BioDot установили для нанесения антитела 5948 в требуемое место на нитроцеллюлозной полосе при концентрации 3 мг/мл со скоростью нанесения 1 мкл/см.
После нанесения полосы сушили при температуре 55°C и блокировали с использованием блокирующего раствора PVA, а затем сушили при температуре 65°C и хранили на протяжении ночи при комнатной температуре с влагопоглотителем в запечатанных саше из фольги.
D. Подготовка и средства для иммобилизации меченых золем золота связывающих реагентов (для использования в примере варианта осуществления 1):
Способ
1. Анализ на P3G:
Покрытый золем конъюгат 5806, подготовленный в разделе A.1, осаждали в центрифуге и надосадочную жидкость удаляли. Образовавшийся в результате осадок перемешивали вихревым способом и подвергали обработке ультразвуком, а затем осадок восстанавливали в буфере для распыления конъюгата золя золота до требуемого OD золота (в этом примере OD80). Буфер для распыления конъюгата золя золота (pH 7,6), применяемый в следующих примерах, содержал 10 мМ Tris (Sigma), 5% вес/объем сахарозы (Sigma) и 0,5% (вес/объем) BSA* (Proliant Biologicals, SKU № 68700). Однако другие примеры буферов для распыления, которые также можно использовать, могут содержать дополнительные вещества в разбавляющем растворе и могут также иметь более высокие или более низкие уровни составляющих частей, перечисленных в примере выше. (Впоследствии изменили на 0,5% вес/объем казеина).
Стекловолокно G041 Millipore (Surewick®) нарезали размером 26 мм ×35 см и загружали на распылитель BioDot.
Распылитель BioDot устанавливали на пропитывание/вливание в стекловолокно покрытого золем конъюгата 5806 в требуемое место на стекловолокне. В этом примере на стекловолокно распыляли за 4 последовательные прохода конъюгат с OD80 со скоростью нанесения 1,65 мкл/см на каждом проходе распыления.
Пропитанное золем золота стекловолокно сушили при 55°C и хранили на протяжении ночи при комнатной температуре с влагопоглотителем поглотителем в запечатанных саше из фольги.
2. Анализ на hCG:
Полосы пропитанного/влитого золем золота стекловолокна для анализа на hCG готовили аналогично описанному выше, за исключением того, что в данном случае использовали 3299, покрытое золем золота (см. раздел A.2), и OD конъюгата золя составлял OD111. В этом примере, приведенном в данном случае, на стекловолокно распыляли за 2 прохода конъюгата золота со скоростью нанесения 1,65 мкл/см.
3. Анализ на FSH:
Для анализа на FSH 3299, покрытое золем золота (см. раздел A.2), распыляли на стекловолокно с использованием 2 последовательных проходов при OD62 конъюгата золота при скорости дозирования 1,65 мкл/см. Полосы с нанесенными дозами сушили и хранили аналогично тому, как в примере выше.
E. Конструирование/получение полосок для анализа: примеры конструкций чипа для анализа с одной полоской (один анализ на чип/полоску)
Способ
1. Анализ на P3G:
Компоненты для анализа на P3G собирали в чипе для анализа (полоске) с помощью кинематического сборочного узла Universal Laminator Module.
Подкладочный ламинат (Ferrisgate) помещали на кинематический стол для карт, и к подкладочному ламинату в предварительно заданном положении прикрепляли заблокированную нитроцеллюлозную полосу с иммобилизованным P3G-овальбумином (раздел C.1).
К подкладочному ламинату прикрепляли полосу из стекловолокна, пропитанную конъюгатом 5806-золя (раздел D.1) с перекрытием 2 мм поверх нитроцеллюлозной полосы.
Прикаточный ролик обеспечивал надежный контакт всех компонентов чипа с подкладочным ламинатом.
Затем полосы нарезали на отдельные чипы размером 6 мм с использованием резальной машины BioDot и хранили с влагопоглотителем в саше из фольги до использования.
2. Анализ на hCG:
Компоненты для анализа на hCG собирали аналогично анализу на P3G, за исключением использования нитроцеллюлоазных полос с иммобилизованным 3468 (раздел C.2) и полос из стекловолокна, пропитанных конъюгатом золя золота-3299 (раздел D.2).
Затем полосы нарезали на отдельные чипы размером 6 мм с использованием резальной машины BioDot и хранили с влагопоглотителем в саше из фольги до использования.
3. Анализ на FSH:
Компоненты для анализа на FSH собрали аналогично анализу на P3G, за исключением использования нитроцеллюлозных полос с иммобилизованным 5948 (раздел C.3) и полос из стекловолокна, пропитанных конъюгатом золя золота-3299 (раздел D.3).
Затем полосы нарезали на отдельные чипы размером 6 мм с использованием резальную машину BioDot и хранили с влагопоглотителем в саше из фольги до использования.
Пример 9
В этом примере приводится дополнительная информация об иллюстративных алгоритмах использования в устройстве в соответствии с насятощим изобретением.
Устройство для анализа по настоящему изобретению обеспечивает более высокую вероятность обнаружения беременности до первого дня предполагаемого цикла по сравнению с традиционными тестами на наличие беременности, проводимыми самостоятельно, в то же время сохраняется специфичность в отношении беременности. Оно достигает этого не только с помощью большей чувствительности в отношении hCG, но также путем измерения FSH и одного или более метаболитов прогестерона, чтобы сохранить специфичность в отношении беременности при очень низких концентрациях hCG; у некоторых женщин периода пост- и перименопаузы могут наблюдаться повышенные уровни hCG, которые при слишком высокочувствительном тесте на hCG могли бы давать ложноположительные результаты. FSH действует в качестве критерия для исключения беременности, поскольку высокие уровни связаны с пери- и постменопаузным состоянием, а метаболиты прогестерона (например, P3G) действуют в качестве критерия наличия беременности, поскольку при беременности наблюдаются повышенные уровни.
В одном простом варианте осуществления этой концепции устройство могло бы функционировать, как показано в таблице 2. В этом примере анализируемый метаболит прогестерона представляет собой P3G:
Все тесты определены как тесты анализа и выражаются в виде обнаруженной концентрации. Для тестов с интенсивностью сформированной видимой линии в случае конкурентных анализов логика должна быть инвертированной, при этом при повышении концентрации аналита интенсивность линии снижается.
Улучшенных характеристик, возможно, можно было бы добиться при использовании более подробного алгоритма: важность (вес) уровня FSH или уровней метаболитов прогестерона могла бы зависеть от уровня hCG и/или пороговые значения, применяемые для тестирования на FSH и метаболит прогестерона, могли бы зависеть от уровня hCG. В более сложном случае пороговое значение для FSH могло бы зависеть от концентрации hCG, а пороговое значение для метаболита прогестерона могло бы зависеть от уровня FSH (и vice versa).
Этот алгоритм схематически представлен на фиг. 6. Что касается этой фигуры, алгоритм/древовидная логическая схема относится к варианту осуществления тестирующего устройства по настоящему изобретению, содержащего две тест полоски для латерального проточного анализа. Первая полоска используется для выполнения анализа на hCG, а вторая полоска используется для выполнения анализа на FSH и анализа на P3G.
В древовидной логической схеме устройство считывания результата анализа вначале проверяет результат анализа на hCG и сравнивает сигнал анализа с предварительно заданным значением сигнала, соответствующим концентрации hCG 2,5 мМЕ/мл. Если результат анализа меньше порогового значения 2,5 мМЕ/мл, считывающее устройство может сразу указать, что тестируемый субъект ʺНе беременна (после символа ʺ<ʺ на этой фигуре). [Однако результат полного анализа (т. е. ʺБеременнаʺ или ʺНе беременнаʺ) не обязательно может показываться пользователю, пока не будут определены результаты всех трех анализов на аналиты]. Альтернативно, если концентрация hCG, определенная в образце мочи, равна или выше порогового значения 2,5 мМЕ/мл, считывающее устройство приступает к проверке результата анализа на FSH (первая тестовая линия или зона обнаружения на второй полоске для анализа). Поскольку концентрация hCG выше 2,5 мМЕ/мл могла быть вызвана источниками, не связанными с беременностью, ʺраннееʺ определение общего окончательного результата анализа не может быть возможным на основании только результата анализа на hCG.
Анализ на FSH имеет пороговое значение 10 мМЕ/мл. Если концентрация FSH, определенная в образце, равна или выше порогового значения 10 мМЕ/мл, устройство для анализа/считывающее устройство объявляет результат теста как ʺНе беременнаʺ. Наоборот, если концентрация FSH в образце выше порогового значения 10 мМЕ/мл, устройство для анализа/считывающее устройство перейдет к проверке результата анализа на P3G.
Результат анализа на P3G считывается со второй тестовой линии или зоны обнаружения на второй полоске для латерального проточного анализа. Если анализ на P3G показывает, что концентрация P3G в образце ниже 4 мкг/мл, то субъект объявляется как ʺБеременнаʺ.
Специалистам в данной области будет ясно, что точные значения сигналов или пороговые концентрации, выбранные для конкретного варианта осуществления, будут зависеть, по меньшей мере частично, от специфических характеристик используемых анализов (например, реагентов, матриц потока, концентрации конъюгатов и т. д.), так что пороговые значения, указанные выше, в других вариантах осуществления могут слегка отличаться, хотя относительные количества будут, как правило, такими же.
Кроме того, на фигуре показано, что устройство для анализа/считывающее средство просматривает или проверяет результаты анализов на hCG, FSH и P3G последовательно. Будет ясно, что соответствующие результаты анализов могут просматриваться в любом порядке или по существу одновременно. Кроме того, ʺраннееʺ определение результатов одного или двух анализов может обеспечить определение окончательного результата полного результата анализа (т. е. ʺБеременнаʺ или ʺНе беременнаʺ), при этом необязательно требуется, чтобы был известен результат всех трех анализов на аналиты, если концентрации аналитов на очень сильно превышают (или намного ниже, в зависимости от обстоятельств) соответствующие пороговые концентрации.
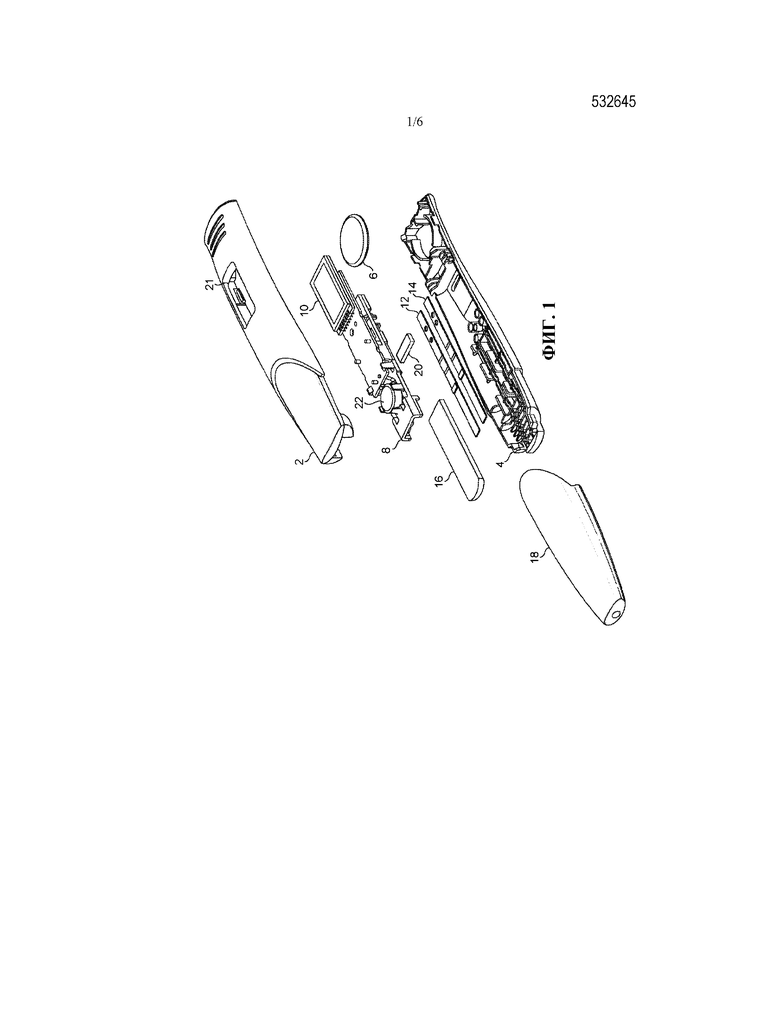
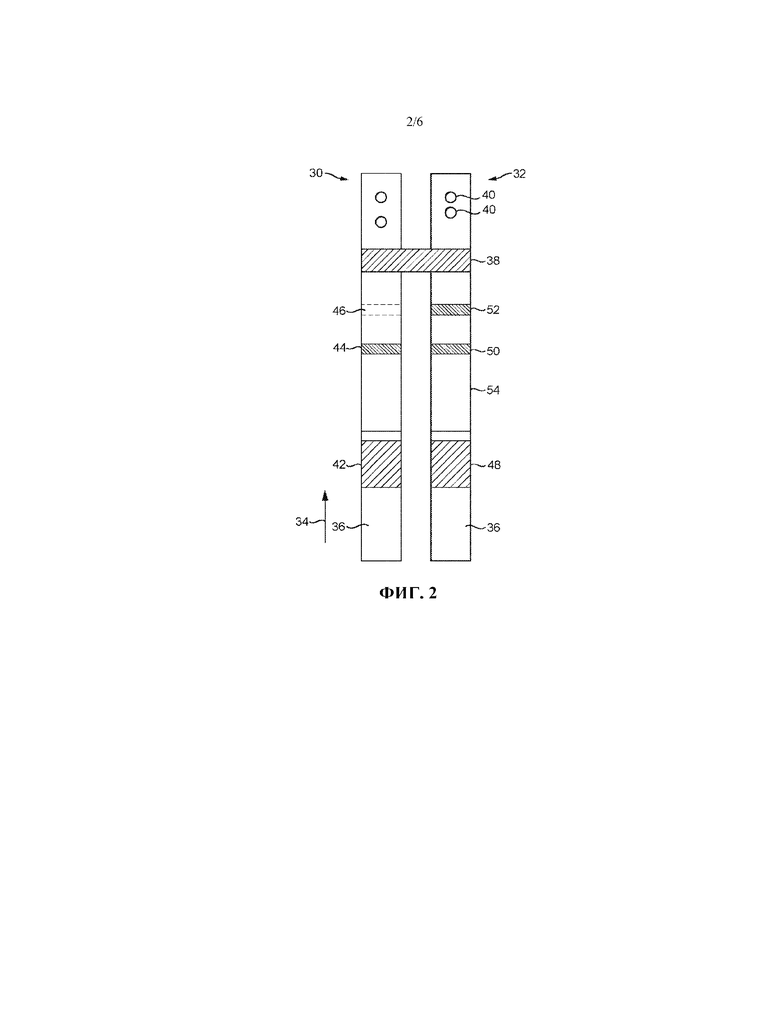
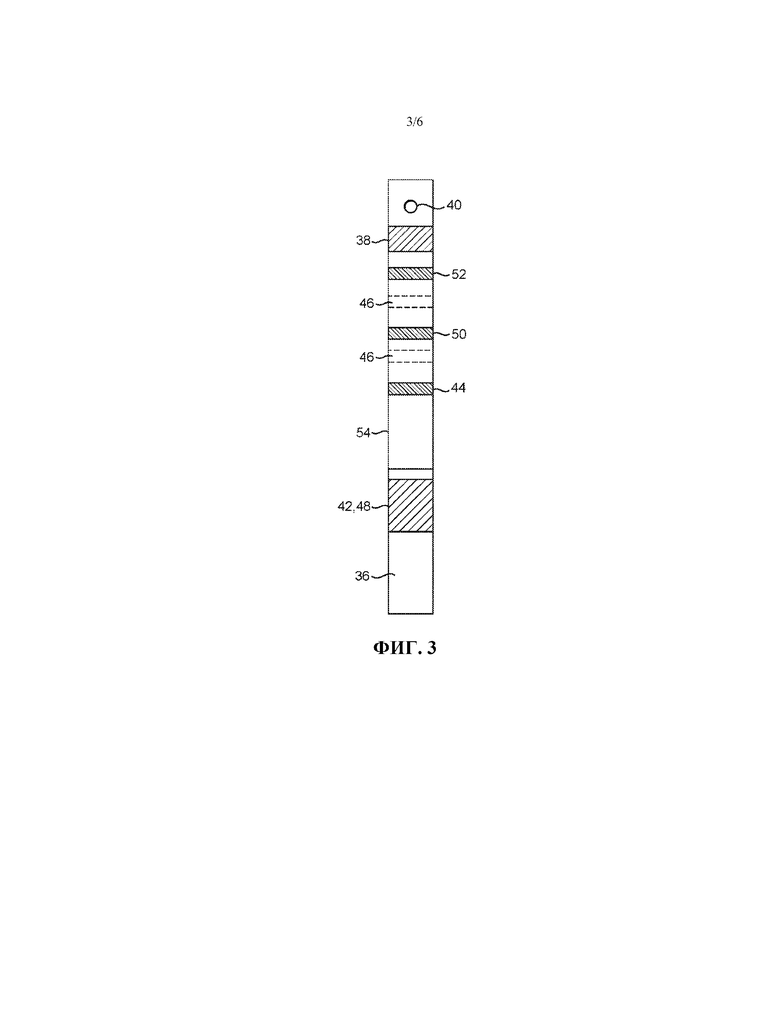
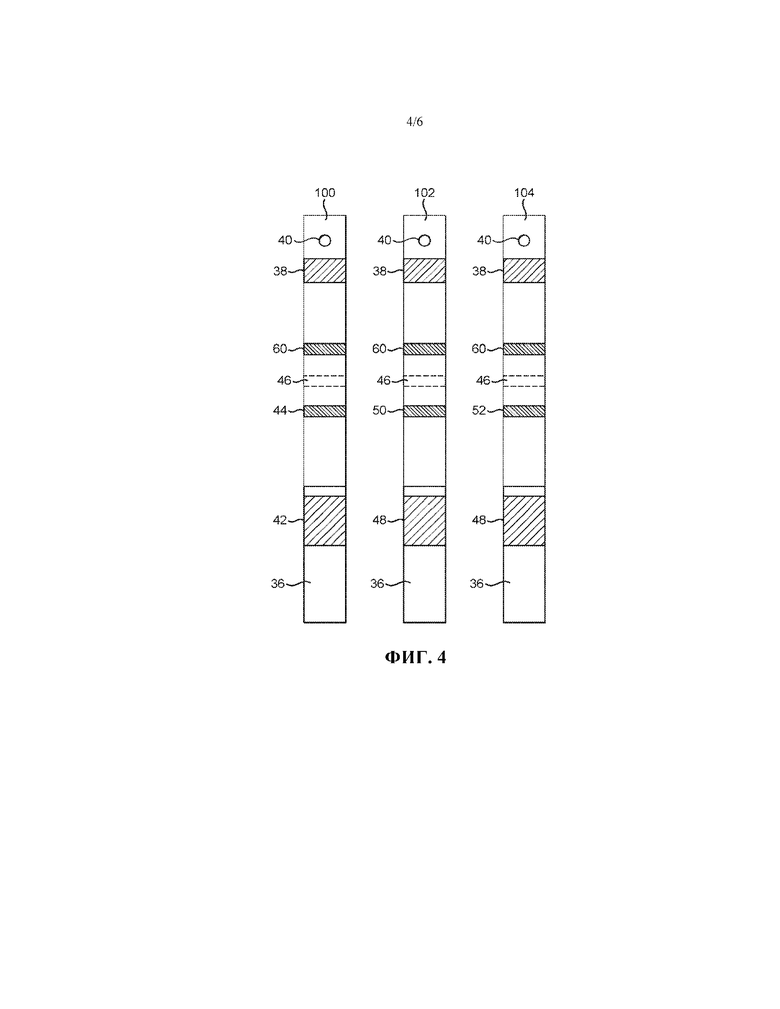
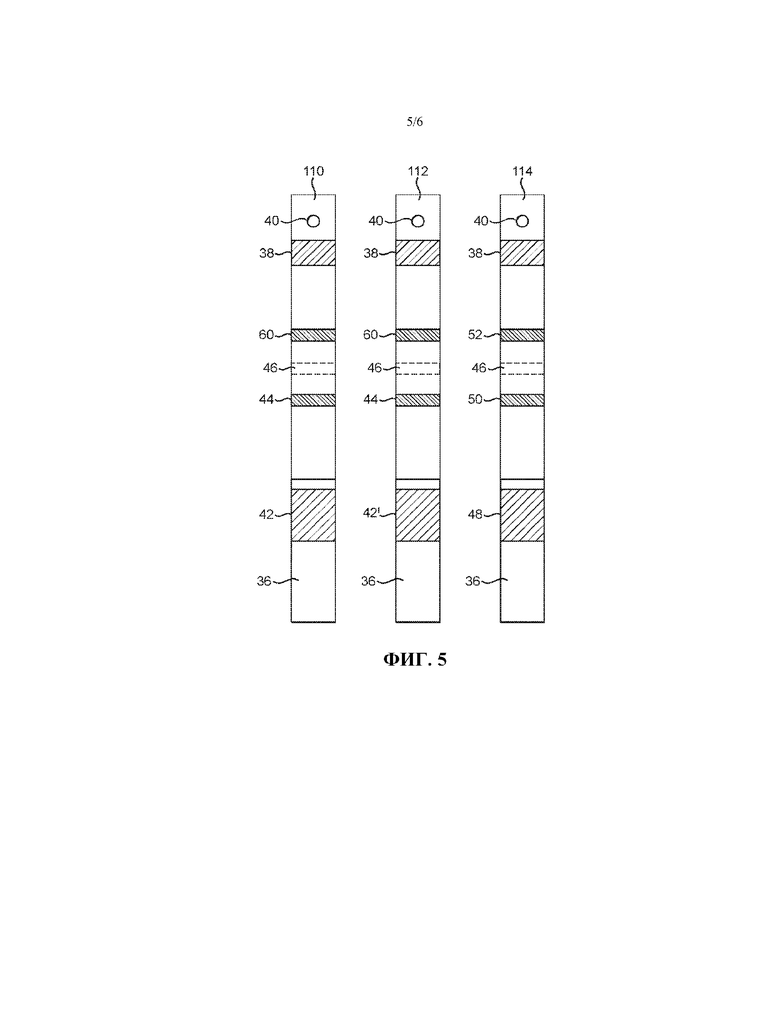
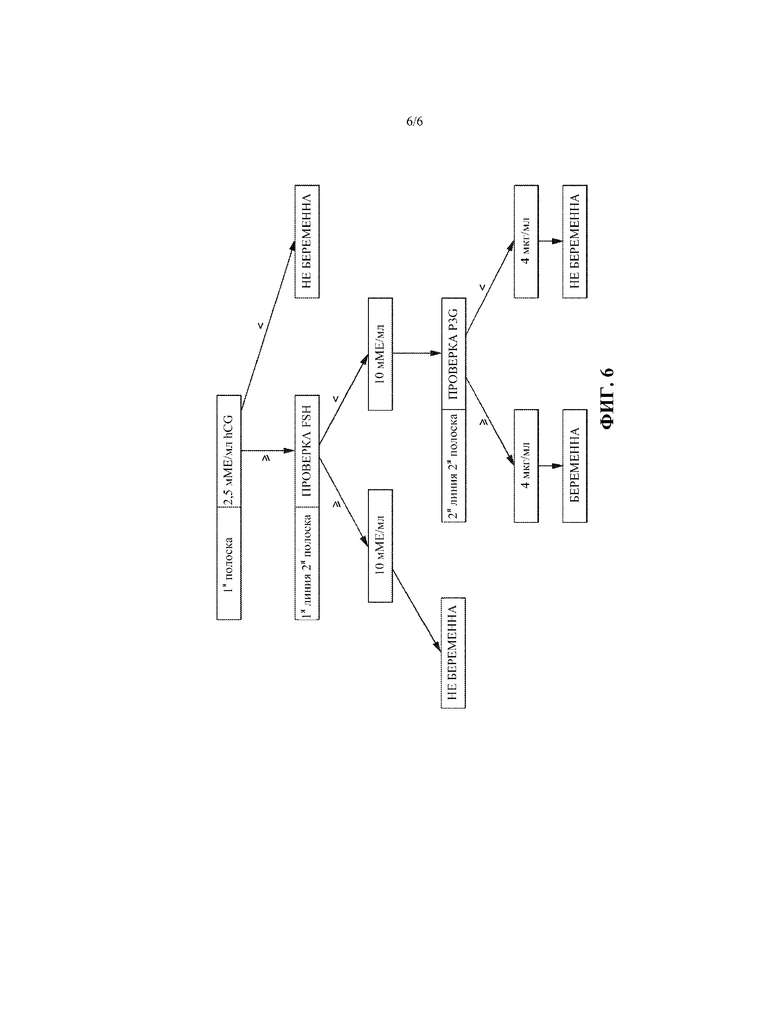
Группа изобретений относится к устройству для тестирования на беременность и способу выполнения тестирования на беременность. Цифровое тестирующее устройство для обнаружения беременности содержит аналитические средства для измерения количества hCG, FSH и метаболита прогестерона в образце, взятом у субъекта; устройство отображения результата анализа пользователю; компьютеризованное средство управления, запрограммированное с верхним и нижним пороговыми значениями для hCG, с по меньшей мере одним пороговым значением для FSH и/или с по меньшей мере одним пороговым значением метаболита прогестерона и с алгоритмом для интерпретации результатов анализа. Также раскрыт способ обнаружения беременности путем приведения в контакт образца с указанным цифровым тестирующим устройством. Группа изобретений обеспечивает возможность определения беременности с чувствительностью 99% и выше и специфичностью 99% и выше, а также не требует информации, касающейся возраста женщины или предыдущего измерения уровня hCG, FSH или метаболита прогестерона. 2 н. и 13 з.п. ф-лы, 6 ил., 2 табл., 9 пр.
1. Цифровое тестирующее устройство для обнаружения беременности у субъекта-женщины, причем тестирующее устройство содержит:
аналитическое средство для измерения абсолютного или относительного количества hCG в образце, взятом у субъекта;
аналитическое средство для измерения абсолютного или относительного количества FSH в образце, взятом у субъекта;
и аналитическое средство для измерения абсолютного или относительного количества метаболита прогестерона в образце, взятом у субъекта;
микропроцессор, ASIC или другое компьютеризованное средство управления, запрограммированное с верхним и нижним пороговыми значениями для hCG, с по меньшей мере одним пороговым значением для FSH и/или с по меньшей мере одним пороговым значением метаболита прогестерона и запрограммированное с алгоритмом для интерпретации результатов анализа, проведенного с помощью аналитического средства, и определения из результатов анализа, проведенного в один момент времени, является ли субъект беременным, посредством сравнения результатов анализа на hCG с верхним пороговым значением для hCG, причем результат анализа на hCG выше порогового значения для hCG побуждает устройство на индикацию того, что субъект является беременным без анализа результатов FSH и анализов метаболита прогестерона; и причем результат анализа на hCG ниже порогового значения для hCG побуждает устройство на индикацию того, что субъект не является беременным с или без подтверждения результатов FSH и анализов метаболита прогестерона; и причем результат анализа на hCG между верхним и нижним пороговыми значениями для hCG побуждает устройство на индикацию того, что субъект является беременным, если анализ результатов FSH ниже порогового значения для FSH и/или результат анализов метаболита прогестерона выше порогового значения для метаболита прогестерона, и
устройство отображения результата для отображения окончательного результата анализа пользователю.
2. Тестирующее устройство по п. 1, содержащее одну или более тест-полосок для латерального проточного анализа и/или один или более микрофлюидных анализов.
3. Цифровое тестирующее устройство по п. 2, содержащее средство считывания результатов анализов.
4. Цифровое тестирующее устройство по п. 1, которое представляет собой портативное устройство или устройство для теста, проводимого самостоятельно.
5. Цифровое тестирующее устройство по п. 1, которое утилизируется после однократного использования.
6. Цифровое тестирующее устройство по п. 1, содержащее по меньшей мере два анализа на hCG, причем один из анализов является анализом с относительно высокой чувствительностью, и один из анализов является анализом с относительно низкой чувствительностью, так что тестирующее устройство может измерять концентрацию hCG в пределах расширенного диапазона.
7. Цифровое тестирующее устройство по п. 6, в котором метаболит прогестерона, обнаруживаемый с помощью анализа на метаболит прогестерона, представляет собой прегнандиол или его производное, причем его производное предпочтительно представляет собой глюкуронид и более предпочтительно прегнандиол-3-глюкуронид.
8. Цифровое тестирующее устройство по п. 1, в котором тестирующее устройство запрограммировано с по меньшей мере одним дополнительным пороговым значением для hCG.
9. Цифровое тестирующее устройство по п. 1, адаптированное и выполненное с возможностью отображения приблизительного гестационного срока беременности для беременного субъекта, причем устройство отображает гестационный срок для беременного субъекта в виде интервалов 1-2 недели, 2-3 недели или более 3 недель.
10. Цифровое тестирующее устройство по п. 1, дополнительно содержащее функцию контроля для указания того, что устройство функционировало правильно.
11. Цифровое тестирующее устройство по п. 1, содержащее общую зону для нанесения образца, так что образец, нанесенный на общую зону для нанесения образца, попадает в два или более отдельных пути течения, при этом по меньшей мере один анализ на аналит расположен на соответствующем одном из двух или более отдельных путях течения.
12. Цифровое тестирующее устройство по п. 1, в котором все анализы на каждый из hCG, FSH и метаболита прогестерона предусмотрены на одном общем пути течения.
13. Цифровое тестирующее устройство по любому из пп. 1-12, в котором предусмотрен по меньшей мере один, предпочтительно два или более, более предпочтительно три или более и наиболее предпочтительно все признаки (i)-(v), изложенные ниже:
(i) чувствительность 99% или выше;
(ii) специфичность 99% или выше;
(iii) способность достигать (i) и (ii), даже если день тестирования приходится на ранний срок беременности до первого дня предполагаемого цикла;
(iv) устройство анализа не требует информации, касающейся возраста женщины или любого анамнеза субъекта, такого как предыдущее измерение уровня hCG, FSH или прогестерона; и
(v) способность достигать (i) и (ii), даже если субъекты включают в себя женщин периода перименопаузы и/или постменопаузы.
14. Способ обнаружения беременности у субъекта-женщины, причем способ содержит этап, на котором образец, взятый у субъекта, приводят в контакт с тестирующим устройством по любому из предыдущих пунктов.
15. Способ по п. 14, в котором предусмотрен по меньшей мере один, предпочтительно два или более, более предпочтительно три или более и наиболее предпочтительно все признаки (i)-(v), изложенные ниже:
(i) чувствительность 99% или выше;
(ii) специфичность 99% или выше;
(iii) способность достигать (i) и (ii), даже если день тестирования приходится на ранний срок беременности до первого дня предполагаемого цикла;
(iv) способ анализа не требует информации, касающейся возраста женщины или любого анамнеза субъекта, такого как предыдущее измерение уровня hCG, FSH или прогестерона; и
(v) способность достигать (i) и (ii), даже если субъекты включают в себя женщин периода перименопаузы и/или постменопаузы.
| US 7090802 B1, 15.08.2006 | |||
| Конденсаторная бумага | 1942 |
|
SU75193A1 |
| US 2010129935 A1, 27.05.2010 | |||
| US 2006019404 A1, 26.01.2006 | |||
| СПОСОБ ПРОИЗВОДСТВА КОНСЕРВОВ "ПИКША ТУШЕНАЯ С ЗЕЛЕНЫМ ЛУКОМ И ПОМИДОРАМИ" СПЕЦИАЛЬНОГО НАЗНАЧЕНИЯ (ВАРИАНТЫ) | 2007 |
|
RU2335983C1 |
| ТЕСТ-СИСТЕМА С ИСПОЛЬЗОВАНИЕМ ЭЛЕМЕНТОВ НЕЭНЗИМАТИЧЕСКОГО РАСПОЗНАВАНИЯ АНАЛИЗИРУЕМОГО ВЕЩЕСТВА | 2005 |
|
RU2398235C2 |
Авторы
Даты
2018-12-06—Публикация
2014-10-01—Подача