Изобретение относится к биохимии и медицине и представляет собой пептид с аминокислотной последовательностью (в однобуквенных кодах) H[isoD][pS]GYEVHH, где специальными кодами [isoD] и [pS] обозначены изомеризованный аминокислотный остаток аспарагиновой кислоты и фосфорилированный аминокислотный остаток серина, соответственно. Данный пептид способен образовывать стабильный цинк-опосредованный межмолекулярный комплекс с метал-связывающим доменом человеческого бета-амилоида. Автором настоящего изобретения показано, что указанный пептид может эффективно применяться для лечения болезни Альцгеймера.
Болезнь Альцгеймера - это нейродегенеративное заболевание, одна из распространенных форм деменции, «старческого слабоумия». Чаще всего болезнь Альцгеймера развивается после 50 лет, хотя есть и случаи диагностики в более ранних возрастных периодах. (Cummings, J.L. (2004). Alzheimer's disease. N Engl J Med 351, 56-67.)
Названная по имени немецкого психиатра Алоиса Альцгеймера болезнь на данный момент диагностирована у порядка 46 миллионов человек в мире.
У некоторых пациентов заболевание может быть связано с наследственными нарушениями, но у большинства пациентов заболевание встречается спорадически, без какой-либо определенной причины (Selkoe, DJ. (2001). Alzheimer's disease: genes, proteins, and therapy. Physiol Rev 81, 741-66).
Симптомы болезни Альцгеймера проявляются медленно, и первым симптомом может быть лишь слабая забывчивость. На этой стадии индивидуумы могут забывать последние события, действия, имена знакомых людей или названия вещей и могут быть не в состоянии решить простые математические задачи. При прогрессировании болезни симптомы становятся более заметными и более серьезными. Это вынуждают людей, пораженных болезнью Альцгеймера, прибегать к медицинской помощи. Симптомы, характерные для средней стадии болезни Альцгеймера, включают забывание того, как выполнять простые функции, такие как приводить себя в порядок, при этом возникают проблемы с речью, пониманием, чтением или письмом. Пациенты на поздней стадии болезни Альцгеймера могут становиться боязливыми или агрессивными, могут уходить далеко от дома и, в конце концов, нуждаться в полном уходе.
Гистологически это заболевание характеризуется нейритными бляшками, главным образом ассоциированными с корой головного мозга, лимбической системой и базальными ганглиями. Основным компонентом указанных бляшек является пептид амилоид-бета (Аβ), который является продуктом расщепления белка-предшественника амилоида-бета (βАРР или АРР). АРР является трансмембранным гликопротеидом типа I, который содержит крупный эктопический N-концевой домен, трансмембранный домен и небольшой цитоплазматический С-концевой хвост. Альтернативный сплайсинг транскрипта одного гена АРР в хромосоме 21 приводит к нескольким изоформам, которые отличаются количеством аминокислот.
Аβ пептид представляет собой соединение, которое обычно обнаруживается в биологических жидкостях, таких как кровь или цереброспинальная жидкость, в которых он присутствует в низких концентрациях от 0,5 до 5 нМ, и это одинаково как у здоровых людей, так и у пациентов, страдающих болезнью Альцгеймера (Mayeux, R. et al. (1999). Plasma amyloid beta-peptide 1-42 and incipient Alzheimer's disease. Ann Neurol 46, 412-6; Seubert, P. et al. (1992). Isolation and quantification of soluble Alzheimer's beta-peptide from biological fluids. Nature 359, 325-7)
На настоящий момент, по всем имеющимся данным, можно сделать вывод, что 1-16 N-концевая область пептида Аβ является областью, которая несомненно участвует в наиболее убедительном и определяющем пути феномена формирования амилоидных бляшек.
Было определено, что 1-16 N-концевая область бета-амилоида является металл-связывающим доменом, где цинк (Zn) и медь (Cu) присоединяются к Аβ пептиду (Guilloreau, L., Damian, L., Coppel, Y., Mazarguil, H., Winterhalter, M. and Faller, P. (2006). Structural and thermo dynamical properties of Cull amyloid-beta16/28 complexes associated with Alzheimer's disease. J Biol Inorg Chem 11, 1024-38; Kozin, S.A., Zirah, S., Rebuffat, S., Hoa, G.H. and Debey, P. (2001). Zinc binding to Alzheimer's Abeta(1-16) peptide results in stable soluble complex. Biochem Biophys Res Commun 285, 959-64). В настоящее время выявлено, что амилоидные бляшки характеризуются аномально высокой концентрацией двухвалентных металлов и, в частности, цинка (Lovell, М.А., Robertson, J.D., Teesdale, W.J., Campbell, J.L. and Markesbery, W.R. (1998). Copper, iron and Zinc in Alzheimer's disease senile plaques. J Neurol Sci 158, 47-52). Некоторое количество исследований и экспериментов, как in vivo так и in vitro, показали, что высокие концентрации цинка вызывают преципитацию Аβ пептида, приводящую к образованию амилоидных бляшек. Кроме того, было показано, что амилоидные бляшки более значимо образуются в окружении нейронов в присутствии высокой концентрации ионов цинка (Frederickson, C.J. and Bush, A.I. (2001). Synaptically released zinc: physiological functions and pathological effects. Biometals 14, 353-66; Frederickson, C.J., Suh, S.W., Silva, D. and Thompson, R.B. (2000). Importance of zinc in the central nervous system: the zinc-containing neuron. J Nutr 130, 1471S-83S).
Именно поэтому в настоящее время считается, что блокирование взаимодействия Аβ пептида с цинком должно привести к уменьшению агрегации Аβ пептида в виде амилоидных бляшек и тем самым предотвратить патологии, связанные с этим взаимодействием.
В патенте US 6001852 в качестве лекарственного средства для лечения болезни Альцгеймера предлагается Клиохинол, который является цинк-хелатирующим агентом.
В патенте US 7018797 представлен метод ингибирования связывания β-амилоидных пептидов с α-7 никотиновым рецептором ацетилхолина для лечения нейродегенеративных заболеваний. В US 7018797, соединения, полученные из нафталина, в частности, 5,8-дигидрокси-транс-2-ди (N-пропиламино)-3-метил-1,2,3,4-тетрагидронафталин, были предложены в качестве соединений, которые могут подавлять связывание Аβ пептида с α-7 никотиновым рецептором ацетилхолина.
В US 7314724 в качестве лекарства против болезни Альцгеймера было предложено использование растворимых форм ламининов и их фрагментов (>10 кДа), которые способны связываться с Аβ и держать его в мономерном состоянии.
Из документа WO 2010/115843, 14.10.2010 известна антигенная конструкция, содержащая антигенный пептид, соответствующий последовательности в пределах тау-белка, включающий фосфо-эпитоп, где пептидом является (а), модифицированный путем связывания с липофильным или гидрофобным фрагментом, который облегчает встраивание в липидный бислой липосомы, и (б), реконструированный в липосому так, что пептид презентирован на поверхности липосомы, для индукции иммунного ответа у животного, страдающего от нейродегенеративного расстройства. Указанная антигенная конструкция используется для лечения болезни Альцгеймера.
Из документа ЕА 12325, 28.08.2009 В1 известно использование 3-амино-1-пропансульфоновой кислоты в способе лечения болезни Альцгеймера.
Из документа WO 2013/041962 28.03.2013 известно получение антитела для использования при лечении болезни Альцнеймера.
В документе WO 2009/149485 17.12.2009 описана группа изобретений, которая относится к медицине и касается применения мимотопов для лечения β-амилоидозов, включая болезнь Альцгеймера, где вышеуказанные мимотопы являются полипептидами, содержащими от 4 до 20 аминокислотных остатков, и способны вызывать in vivo образование антител к неукороченному Аβ1-40/42 и укороченным с N-конца формам АβрЕ3-40/42, Аβ3-40/42, Aβ11-40/42, AβpE11-40/42 и Aβ14-40/42 без нарушения физиологических функций передачи сигнала БПА.
В документе WO 2006/121656 16.11.2006 описан способ для предотвращения или лечения заболевания, ассоциированного с отложениями амилоида Аβ в головном мозге пациента, нуждающегося в такой профилактике или лечении. Способ включает введение эффективной дозы иммуногенного фрагмента Аβ с отсутствием Т-клеточного эпитопа, способного вызывать иммунный ответ в форме антител к указанному фрагменту Аβ, где иммуногенный фрагмент содержит один или более линейных пептидов из 8 аминокислот (8-меров) Аβ, при этом указанный один или более 8-меров включают Аβ(21-28) (AEDVGSNK).
Из документа RU 2588143 С2, 27.06.2016 известно изобретение, которое относится к пептидному соединению Ra-R1-R2-R3-R4-Rb (I) или Ra-R4-R3-R2-R1-Rb (II), где Ra представляет собой N-концевую первичную аминную группу аминокислоты R1 или R4, либо свободную, либо замещенную аминозащитной группой, Rb представляет собой гидроксильную группу С-концевой карбоксильной группы аминокислоты R1 или R4, либо свободную, либо замещенную гидроксизащитной группой, и R1-R2-R3-R4 или R4-R3-R2-R1 представляют собой HADD, KADD, DDAK, RADD, DDAR, KAED, DEAK, RAED, DEAR, HADE, EDAH, KADE, EDAK, RADE, EDAR, HAEE, EEAH, KAEE, EEAK, RAEE и EEAR. Данные пептидные соединения применяются для связывания с β-амилоидными пептидами и ингибирования полимеризации их в виде амилоидных бляшек, а также в качестве лекарственного средства или для подготовки или определения препаратов с целью лечения нейродегенеративных заболеваний, в частности болезни Альцгеймера.
Однако, к сожалению, несмотря на успехи в предотвращении образования амилоидных бляшек, влияние известных препаратов на улучшение когнитивных функций при болезни Альцгеймера в среднем является очень ограниченным.
Исходя из вышеизложенного, на настоящий момент существует необходимость получения альтернативных эффективных средств для лечения болезни Альцгеймера, в том числе за счет снижения или предотвращения связывания ионов Zn(II) с β-амилоидным пептидом.
Автором настоящего изобретения был получен пептид, соответствующий по своему аминокислотному составу фрагменту 6-14 человеческого бета-амилоида, но в отличие от него пептид по настоящему изобретению содержит химически модифицировнные аминокислотные остатки, а именно фосфорилированый остаток серина (обозначаемый как "[pS]") и изомеризованный остаток аспарагиновой кислоты (обозначаемый как "[isoD]"). Пептид по настоящему изобретению имеет нонамерную (девяти-членную) аминокислотную последовательность H[isoD][pS]GYEVHH с открытыми или защищенными концами основной полипептидной цепи (например, с ацетилированным N-концевым амином и амидированным С-концевым гидроксилом) и обозначается далее как "isoD-pS-nAβ". Данный пептид способен образовывать стабильный цинк-опосредованный межмолекулярный комплекс с метал-связывающим доменом человеческого бета-амилоида. Автором настоящего изобретения показано, что указанный пептид может эффективно применяться для лечения болезни Альцгеймера. На основе пептида создана также фармацевтическая композиция для лечения болезни Альцгеймера. В качестве активного компонента в ней используется пептид "isoD-pS-nAβ" согласно изобретению. Остальные компоненты выбраны из круга нейтральных носителей и разбавителей и хорошо известны специалисту в данной области техники (например, физиологичекский раствор).
Таким образом, авторами настоящего изобретения к рассмотрению предложено следующее.
1. Пептид "isoD-pS-nAβ", способный образовывать стабильный цинк-опосредованный межмолекулярный комплекс с метал-связывающим доменом человеческого бета-амилоида.
2. Фармацевтическая композиция для лечения болезни Альцгеймера, содержащая эффективное количество пептида согласно изобретению и фармацевтически приемлемый носитель.
3. Способ снижения цинк-индуцированной агрегации бета-амилоида, включающий взаимодействие пептида согласно изобретению с бета-амилоидом.
4. Способ образования цинк-опосредованных межмолекулярных комплексов пептид-бета-амилоид, включающий в взаимодействие пептида согласно изобретению с бета-амилоидом.
5. Способ лечения болезни Альцгеймера, включающий введение пациенту эффективного колическтва фармацевтической композиции согласно изобретению.
Изобретение иллюстрируется следующими примерами.
ПРИМЕР 1. Экспериментальное свидетельство способности "isoD-pS-nAβ" образовывать стабильные цинк-опосредованные межмолекулярные комплексы с металл-связывающим доменом человеческого бета-амилоида.
Образование цинк-связанных комплексов между isoD-pS-nAβ (аналитом) и иммобилизованным пептидным фрагментом DAEFRHDSGYEVHHQK (лигандом), соответствующим металл-связывающему домену 1-16 бета-амилоида человека, Аβ(1-16), было исследовано с помощью биосенсора на эффекте поверхностного плазмонного резонанса (БППР) «BIAcore 3000» (GE Healthcare, США) в водных буферных системах при физиологических значениях рН. По результатам таких экспериментов рассчитывается значение константы диссоциации (Кд) взаимодействия субстанции и иммобилизованного лиганда. Если значение Кд равно или меньше 10-4 М, то такое взаимодействие рассматривается в качестве биологически значимого.
Перед каждым экспериментом лиофилизированные синтетические пептиды (чистота более 98%), которые использовались в качестве аналита или лиганда, растворяли в подходящей буферной системе. Концентрация каждого пептида в растворе определялась спектрофотометрически с использованием коэффициента экстинкции 1450 М-1 cm-1 при 276 нм (пик поглощения аминокислотного остатка Туг 10 в человеческом Аβ).
Сенсорный чип СМ5 с гидрофильной карбоксиметилированной декстрановой матрицей, подходящий буфер HBS (10 мМ HEPES, рН 7.4, 150 мМ NaCl, 3 мМ EDTA, 0.005% ПВА Р20), 1-ethyl-3-(3-dimethylaminopropyl)-25 carbodiimide (EDC), N-hydroxysuccinimide (NHS), 2-(2-pyridinyldithio)-ethaneamine (PDEA), и цистеин, используемые в анализах, были закуплены у компании-производителя (BIAcore, GE, USA). Иммобилизация лиганда проводилась в соотвтествие с протоколами компании-производителя и с использованием соотвтествующих рабочих растворов.
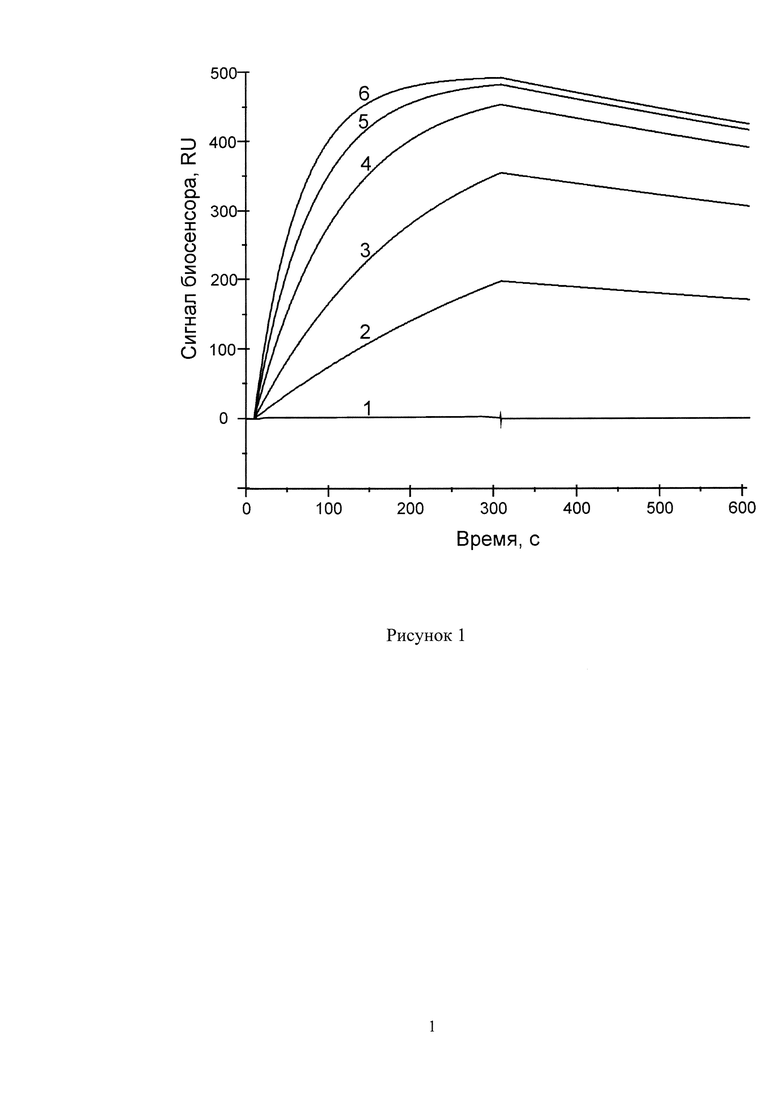
БППР эксперименты были проведен на инструменте «BIAcore 3000» (GE Healthcare, США). Синтетический пептид Ас-DAEFRHDSGYEVHHQKGGGGC-NH2 ("Aβ(1-16)-Gly-Gly-Gly-Gly-Cys") был использован в качестве лиганда, который иммобилизировали через дисульфидную связь тиоловой группы С-концевого остатка цистеина. В качестве аналита использовали синтетический пептид Ас-H[isoD][pS]GYEVHH-NH2 ("isoD-pS-nAβ"). Концентрации образцов растворов каждого аналита были 0, 2, 5, 10, 15 и 20 микромолей). На рисунке 1 представлены полученные наборы кинетических кривых связывания (сенсограммы БППР) аналита "isoD-pS-nAβ" c иммобилизованным Аβ(1-16)-Gly-Gly-Gly-Gly-Cys) после вычитания контрольного фона. Измерения проводились при 25°С в 10 мМ HEPES буфере (рН 6,8), содержащем различные концентрации аналита (0, 2, 5, 10, 15 и 20 микромолей, кривые 1-6, соответственно) в присутствии 100 мкМ Zn.
На основании полученых данных было найдено, что константа диссоциации цинк-опосредованных взаимодействий между "isoD-pS-nAβ" и иммобилизованным Aβ(1-16)-Gly-Gly-Gly-Gly-Cys составляет (5±0.7)×10-7 М.
Таким образом, показано образование стабильных межмолекулярных комплексов между металл-связывающим доменом бета-амилоида и тестируемым пептидом в присутствии ионов цинка. При этом в отсутствии ионов цинка никаких взаимодействий зафиксированно не было. Следовательно, пептид согласно изобретению представляет собой средство, способное образовать стабильный межмолекулярный комплекс с металл-связывающим доменом человеческого бета-амилоида.
ПРИМЕР 2. Анализ влияния "isoD-pS-nAβ" на образование цинк-индуцированных агрегатов человеческого бета-амилоида (Аβ42) методом корреляционной спектроскопии (динамического лазерного светорассеяния).
Размер цинк-индуцированных агрегатов пептидов Аβ42 определяли методом корреляционной спектроскопии, используя анализатор размера частиц Zetasizer Nano ZS (Malvern Instruments Ltd., Великобритания), позволяющий измерять диаметр частиц в диапазоне от 0.6 нм до 10 мкм. Измерения проводили при температуре 25°С в соответствии с инструкцией производителя. Метод корреляционной спектроскопии основан на определении коэффициента диффузии дисперсных частиц в жидкости путем анализа корреляционной функции флуктуаций интенсивности рассеянного света. Размер частиц определяется по формуле Стокса-Эйнштейна, которая связывает коэффициент диффузии с гидродинамическим радиусом частицы. При этом предполагается, что частица имеет сферическую форму.
Для полидисперсной популяции частиц анализатор Zetasizer Nano ZS дает распределение частиц по размеру, для чего используется программа CONTIN, являющаяся частью его программного обеспечения. Программа использует математический алгоритм, позволяющий из всех возможных распределений частиц по размеру выбрать то, которое наилучшим образом описывает экспериментально определяемую корреляционную функцию. Программа также определяет средний размер частиц в полидисперсной популяции, который использовался в данной работе для сравнительное анализа.
Пробы для определения размера агрегатов пептидов методом корреляционной спектроскопии готовились следующим образом. 100 мкл раствора пептида Аβ42 с концентрацией 30 мкМ в буфере А (10 мМ HEPES, 150 мМ NaCl, рН 7,4) смешивали с 20 мкл раствора хлорида цинка концентрацией 150 мМ в буфере А в одноразовой микрокювете BRAND UV (BRAND GMBH, Германия) и немедленно использовали для определения размера агрегатов. Для определения влияния пептида isoD-pS-nAβ на цинк-индуцированную агрегацию Аβ42 к 100 мкл раствора Аβ42 предварительно добавляли 1 мкл раствора пептида isoD-pS-nAβ в буфере А с концентрацией, позволяющей получать желаемое молярное соотношение данных пептидов и Аβ42 в интервале от 1 до 10, инкубировали смесь 10 мин при комнатной температуре, после чего вносили цинк как описано выше. Конечная концентрация Аβ42 в анализируемой пробе составляла 25 мкМ, молярное отношение цинк/Аβ42 было 1:1, а молярное отношение между isoD-pS-nAβ и Аβ42 составляло 1:1, 3:1 и 10:1.
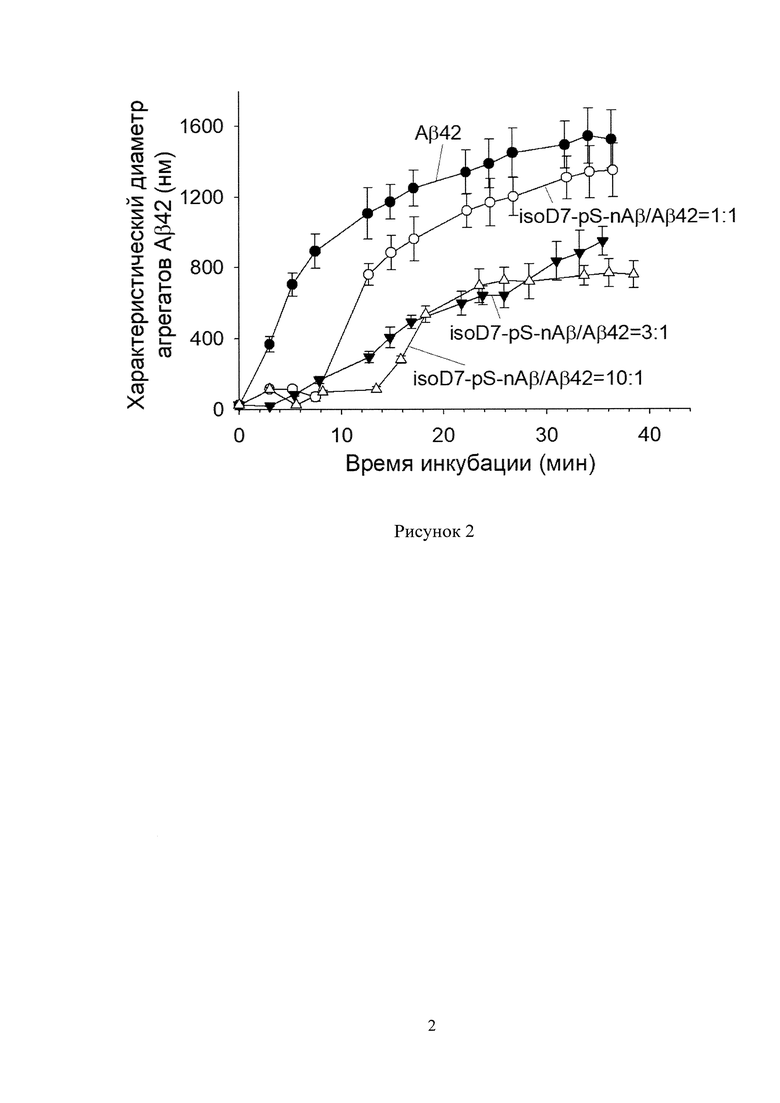
Результаты показаны на рис. 2 - влияние "isoD-pS-nAβ" на цинк-зависимую агрегацию человеческого бета-амилоида Аβ42.
Из приведенных на Рис. 2 данных следует, что добавление isoD-pS-nAβ существенно снижает способность Аβ42 подвергаться цинк-индуцированой агрегации. При этом при повышении концентрации субстанции в смесях процесс ингибирования такой агрегации усиливается.
ПРИМЕР 3. Улучшение когнитивных функций мышиной модели («АβРР/PS1») болезни Альцгеймера под действием внутривенного введения "isoD-pS-nAβ" экспериментальным животным.
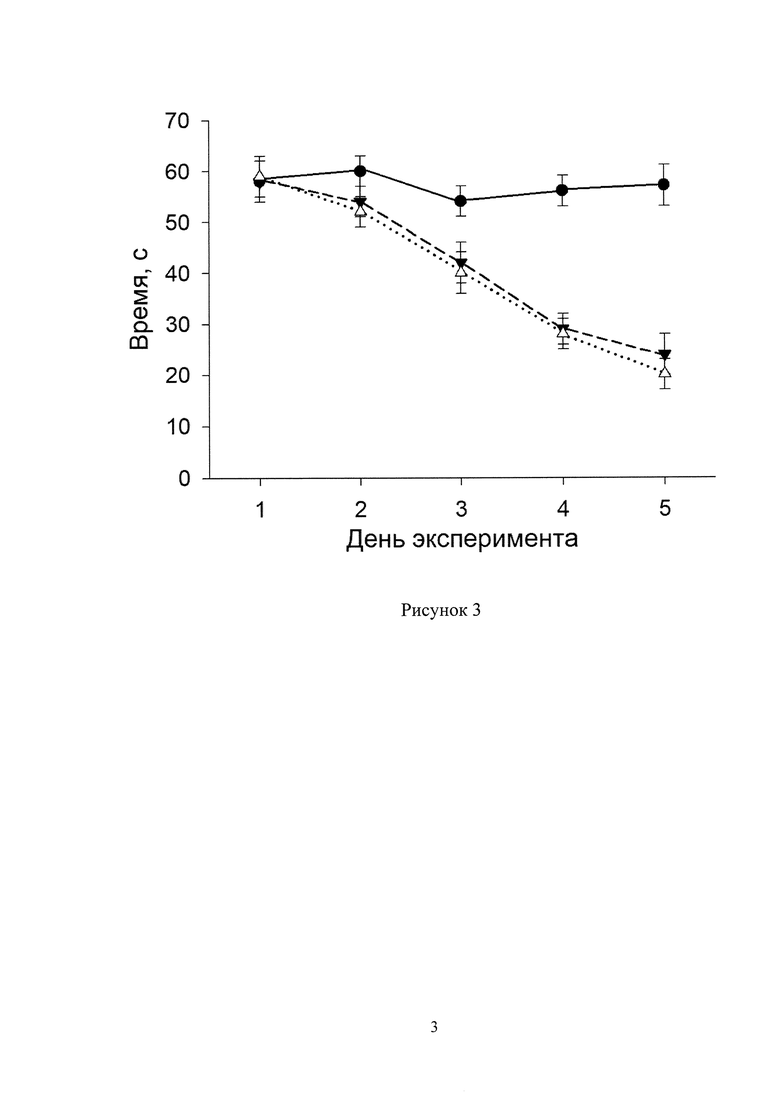
Для оценки влияния субстанции "isoD-pS-nAβ" на характеристики памяти и обучения экспериментальных животных была использована стандартная методика оценки пространственной памяти в водном лабиринте Морриса. Водный лабиринт Морриса является классическим инструментом для оценки пространственной памяти, зависящей от функции гиппокампа. Важно отметить, что именно в гиппокампе у пациентов при болезни Альцгеймера и у трасгенных мышей линии «АβРР/PS1» агрессивно развивается церебральный амилоидоз. Были использованы три группы семимесячных мышей: интактные животные линии «АβРР/PS1» (N «intact» = 9 голов), инъектированные препаратом "isoD-pS-nAβ" мыши линии «АβРР/PS1» (N «isoD-pS-nAβ» = 8 голов; препарат вводился внутривенно в дозе 5 мг/кг три раза - в возрасте 4, 5 и 6 месяцев), и контрольные мыши дикого типа (N «wt» = 10 голов). Результаты анализа пространственной памяти животных, полученные в этом тесте, продемонстрировали значительную разницу между интактными и инъектированными мышами линии «АβРР/PS1» (рис. 3) - анализ пространственной памяти интактных животных линии «АβРР/PS1» (N «intact» = 9 голов, сплошная линия, черные кружочки), инъектированных препаратом «isoD-pS-nAβ» мышей линии «АβРР/PS1» (N «isoD-pS-nAβ» = 8 голов, возраст 7 мес., прерывистая линия, черные треугольнички), и контрольных мышей дикого типа (N «wt» = 10 голов, пунктирная линия, пустые треугольнички) в водном лабиринте Морриса. Размер бассейна 180 см, платформа расположена стационарно. На оси ординат указано время, затраченное животными на поиск платформы при последовательных тестированиях в течение 5 дней.
Начиная с 3-го дня обучения время, которое требовалось контрольным животным (дикого типа) и инъектированным препаратом «isoD-pS-nAβ» трансгенным мышам для нахождения платформы, достоверно сокращалось. В то же время в группе интактных мышей линии «АβРР/PS1» это время оставалось таким же, как и на 1-й день обучения. Таким образом, было показано, что систематические внутривенные инъекции «isoD-pS-nAβ» (в дозах по 5 мг/кг) приводили к улучшению способности животных к обучению и поддержанию долговременной памяти по сравнению с интактной контрольной группой трансгенных мышей, что свидетельствует о существенном когнитивно-стимулирующем эффекте этой субстанции.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2018 |
|
RU2679080C1 |
| Фармацевтическая композиция на основе пептида HAEE для лечения нейродегенеративных заболеваний | 2019 |
|
RU2709539C1 |
| МАГНИЕВЫЙ КОМПЛЕКС ПЕПТИДА HAEE ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2784746C1 |
| ЦИНКОВЫЙ КОМПЛЕКС ПЕПТИДА HAEE ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2784319C1 |
| КАЛЬЦИЕВЫЙ КОМПЛЕКС ПЕПТИДА ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2785354C1 |
| МЕДНЫЙ КОМПЛЕКС ПЕПТИДА HAEE ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2784732C1 |
| АММОНИЕВАЯ СОЛЬ ПЕПТИДА HAEE ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2784249C1 |
| НАТРИЕВАЯ СОЛЬ ПЕПТИДА HAEE ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2784326C1 |
| КАЛИЕВАЯ СОЛЬ ПЕПТИДА HAEE ДЛЯ ЛЕЧЕНИЯ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2784425C1 |
| ЭКЗОГЕННО-ИНДУЦИРУЕМАЯ ЖИВОТНАЯ МОДЕЛЬ БОЛЕЗНИ АЛЬЦГЕЙМЕРА | 2012 |
|
RU2532525C2 |
Изобретение относится к биохимии и к медицине и представляет собой пептид формулы H[isoD][pS]GYEVHH, где остаток серина является фосфорилированным, а остаток аспарагиновой кислоты изомеризирован. Данный пептид способен образовывать стабильный цинк-опосредованный межмолекулярный комплекс с металлсвязывающим доменом человеческого бета-амилоида и используется для лечения болезни Альцгеймера. 5 н.п. ф-лы, 3 ил., 3 пр.
1. Пептид H[isoD][pS]GYEVHH с открытыми или защищенными концами основной полипептидной цепи (например, с ацетилированным N-концевым амином и амидированным С-концевым гидроксилом), способный образовывать стабильный цинк-опосредованный межмолекулярный комплекс с металлсвязывающим доменом человеческого бета-амилоида.
2. Фармацевтическая композиция для лечения болезни Альцгеймера, содержащая эффективное количество пептида по п. 1 и фармацевтически приемлемый носитель.
3. Способ снижения цинк-индуцированной агрегации бета-амилоида, включающий взаимодействие пептида по п. 1 с бета-амилоидом.
4. Способ образования цинк-опосредованных межмолекулярных комплексов пептид-бета-амилоид, включающий взаимодействие пептида по п. 1 с бета-амилоидом.
5. Способ лечения болезни Альцгеймера, включающий введение пациенту эффективного количества фармацевтической композиции по п. 2.
| WO 2006121656, 16.11.2006 | |||
| WO 2013041962, 28.03.2013 | |||
| ПЕПТИДНОЕ СОЕДИНЕНИЕ, ПОЛЕЗНОЕ ДЛЯ ИНГИБИРОВАНИЯ ОБРАЗОВАНИЯ АМИЛОИДНЫХ БЛЯШЕК | 2011 |
|
RU2588143C2 |
Авторы
Даты
2019-02-05—Публикация
2018-04-17—Подача