Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития ишемического инсульта.
Ишемический инсульт продолжает оставаться одним из самых разрушительных заболеваний во всем мире с точки зрения заболеваемости и смертности [Подтипы ишемических нарушений мозгового кровообращения: диагностика и лечение [Текст] / В.А. Пизова // Неврология, нейропсихиатрия, психосоматика, 2012. – №4. – С. 34-38]. На протяжении последних десятилетий инсульт занимает лидирующие позиции по заболеваемости, инвалидизации и смертности, поэтому исследование молекулярно-генетических механизмов предрасположения к данному заболеванию остается актуальной проблемой современной генетики человека [Хронические сосудистые заболевания головного мозга [Текст] / А.С. Кадыков, Л.С. Манвелов [и др.] // М.: ГЭОТАР-Медиа. – 2013. – 232 с.]. Цереброваскулярные заболевания, в том числе инсульт, являются этиологически гетерогенными заболеваниями, которые развиваются при взаимодействии внешнесредовых и генетических факторов [Факторы риска, первичная и вторичная профилактика острых нарушений мозгового кровообращения [Текст] / Л.А. Цукурова, Ю.А. Бурса // Российский медицинский журнал, 2012. – №10. – С. 494-499].
В формирование инсульта вовлечены такие средовые факторы риска, как курение, злоупотребление алкоголем, высокий уровень холестерина в крови, избыточное употребление соли. Наряду со средовыми факторами риска, идентифицированы гены-кандидаты, ассоциированные с восприимчивостью к инсульту, среди которых важное значение имеют гены цитокинов [Association between Tumor Necrosis Factor-α (-238G/A and -308G/A) Gene Polymorphisms and Risk of Ischemic Stroke: A Meta-Analysis [Text] / P. Kumar, S. Misra, A. Kumar [et al.] // Pulse (Basel), 2016. – Vol. 3, №3-4. – Р. 217-228]. Согласно данным литературы, цитокины продуцируются нейронами, микроглией, макрофагами, моноцитами, и отвечают за модуляцию размера ишемического повреждения при инсульте. Аллели A и G rs2162679 и rs6214 гена IFG1, были связаны с развитием ишемического инсульта в корейской популяции. [Polymorphisms of IGFI contribute to the development of ischemic stroke [Text] / H.J. Kim, S.K. Kim, H.J. Park [et al.] // Exp Ther Med., 2012. – Vol. 3, №1. – Р. 93-98].
Рецептор фактора некроза опухолей первого типа (TNFR1) – трансмембранный белок с молекулярной массой 55 кДа, опосредующий все процессы, запускаемые TNFα, в том числе регуляцию воспалительного ответа, апоптоза, клеточной пролиферации и дифференцировки [Tumor Necrosis Factor Alpha: A Link between Neuroinflammation and Excitotoxicity [Text] / G. Olmos, J. Lladó // Аm. J. Рhysiоl. Hеаrt Сirс. Рhysiоl. – 2015. – Vol. 11 (32). – P. 12].
Ген, кодирующий TNFR1, расположен на коротком плече 12 хромосомы (12p13.31). Согласно литературным данным, локус rs767455 TNFR1 вовлечен в развитие многих патологических состояний, в том числе, гипертонической болезни, ишемического инсульта, церебральной аневризмы [Genetic ablation of soluble tumor necrosis factor with preservation of membrane tumor necrosis factor is associated with neuroprotection after focal cerebral ischemia [Text] / Р. Madsen, M. Pernille, G. Clausen [et al.] // In Journal of Cerebral Blood Flow and Metabolism. – 2015. – Vol. 41, №4. – Р. 289-297].
Рецептор фактора некроза опухолей второго типа (TNFR2) – белок с молекулярной массой 75-80 кДа, являющийся членом суперсемейства TNF-рецепторов [Infliximab therapy balances regulatory T-cells, tumour necrosis factor receptor 2 (TNFR2) expression and soluble TNFR2 in sarcoidosis [Text] / A. Verwoerd, D. Hijdra, A.D. Vorselaars [et al.] // Clin Exp Immunol. – 2016. – Vol. 185, №2. – Р. 263-270]. Рецептор TNF второго типа опосредует процессы клеточной пролиферации, миграции и адаптации клеток, а также участвует в защите нейронов от апоптоза и активации антиоксидантных путей [Elevated remnant cholesterol causes both low-grade inflammation and ischemic heart disease, whereas elevated low-density lipoprotein cholesterol causes ischemic heart disease without inflammation / A. Varbo, M. Benn, A. Tybjеrg-Hansen [et al.] // Circulation. – 2013. – Vol. 128, №12. – Р. 1298-1309].
Цитогенетические координаты гена, кодирующего TNFR2 – 1р36.2, в его 3'-нетранслируемой области локализован таговый полиморфизм rs1061624 TNFR2. Согласно данным литературы, ген TNFR2 ассоциирован с ишемическим инсультом у населения США [Circulating biomarkers and incident ischemic stroke in the Framingham Offspring Study [Tехt] / A. Shoamanesh, S.R. Preis [еt аl.] // Neurology. – 2016. – Vol.87, №12. – P.1206-1211].
Недавние исследования показали, что важное модифицирующее влияние на характер взаимодействий полиморфизмов генов-кандидатов цитокинов при формировании цереброваскулярных заболеваний оказывает курение [Interaction between smoking and functional polymorphism in the cytokines gene is associated with ischaemic heart disease and myocardial infarction in patients with rheumatoid arthritis: a cross-sectional study [Tехt] / Y. Chen, P.T. Dawes, J.C. Packham [еt аl.] // Arthritis Research & Therapy. – 2012. – № 14 (2). – Р. 81-87], при этом у курильщиков регистрируются более высокие уровни цитокинов по сравнению с некурящими индивидуумами.
В Российской Федерации исследования вовлеченности генов цитокинов в формирование предрасположенности к ишемическому инсульту единичны и фрагментарны, а данные о роли генетических вариантов rs1061624 TNFR2, rs767455 TNFR1 и курения в развитии ишемического инсульта отсутствуют.
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития ишемического инсульта на основе данных о сочетаниях генетических полиморфизмов rs1061624 TNFR2, rs767455 TNFR1 и статуса курения.
Из области техники известен «Способ прогнозирования развития острого ишемического инсульта» по патенту РФ №2012134988 от 20.02.2014. Способ включает учет показателей ферментов антиокислительной защиты в периферической крови, при этом в качестве ферментов антиокислительной защиты определяют каталазу, пероксидазу и показатель перекисного окисления липидов. При увеличении показателей пероксидазы и перекисной резистентности эритроцитов и снижении показателя каталазы более, чем на 70% от референтных значений, судят о высоком риске развития ишемического инсульта. Однако данный способ не является достаточно информативным, так как не включает генетические маркеры и применим только на клиническом этапе, что исключает раннюю диагностику и проведение профилактических мероприятий по предотвращению развития инсульта.
За прототип выбран патент РФ № 2422523 от 22.04.2010 «Аллель SNP41 гена PDE4D, его применение для прогнозирования индивидуальной предрасположенности к инсульту в русской популяции, применение молекулярно-генетического маркера индивидуальной предрасположенности к инсульту и способ прогнозирования индивидуальной предрасположенности к инсульту». Способ включает получение ДНК, из венозной крови, анализ полиморфизма гена PDE4D на наличие аллеля А SNP41, прогноз предрасположенности к инсульту в русской популяции в случае выявления наличия указанного аллельного варианта, что позволяет своевременно назначать соответствующие медикаменты. Недостатками указанного способа являются:
- использование в качестве маркера только одного генетического полиморфизма, что снижает статистическую мощность проведенного исследования;
- для прогнозирования риска развития инсульта не используются средовые факторы риска.
Задачей настоящего исследования является расширение арсенала способов диагностики, а именно создание способа прогнозирования развития ишемического инсульта на основе комбинации генов рецепторов факторов некроза опухолей первого и второго типа и статуса курения.
Технический результат использования изобретения – получение критериев оценки риска развития ишемического инсульта у индивидуумов русской национальности, уроженцев Центрального Черноземья на основе данных о сочетаниях генетических вариантов локусов rs1061624 TNFR2, rs767455 TNFR1 и статуса курения.
Предполагаемое изобретение, включающее выделение ДНК из венозной крови и анализ полиморфизма гена, содержит следующие новые признаки:
- анализируют полиморфизмы генов цитокинов rs1061624 TNFR2 и rs767455 TNFR1;
- устанавливают наличие средовых факторов риска развития ишемического инсульта, а именно – выявляют статус курения;
- прогнозируют высокий риск развития ишемического инсульта при выявлении сочетания генотипа GG rs767455 TNFR1 с GG rs1061624 TNFR2 и с положительным статусом курения.
Новизна и изобретательский уровень заключаются в том, что из уровня техники не известна возможность прогноза риска развития ишемического инсульта по наличию сочетания генетических вариантов полиморфных маркеров цитокинов rs1061624 TNFR2, rs767455 TNFR1 и статуса курения.
Выделение геномной ДНК из периферической крови осуществляют методом фенольно-хлороформной экстракции (Mathew, 1984) в два этапа. На первом этапе к 4 мл крови с ЭДТА добавляют 25 мл лизирующего буфера, содержащего 320мМ сахарозы, 1% тритон Х-100, 5мМ MgCl2, 10мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4ºС, 4000 об./мин. в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10мг/мл) и инкубируют образец при 37ºС в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об./мин. в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. После лиофилизации полученную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -200С. Выделенную ДНК используют для проведения полимеразной цепной реакции синтеза ДНК.
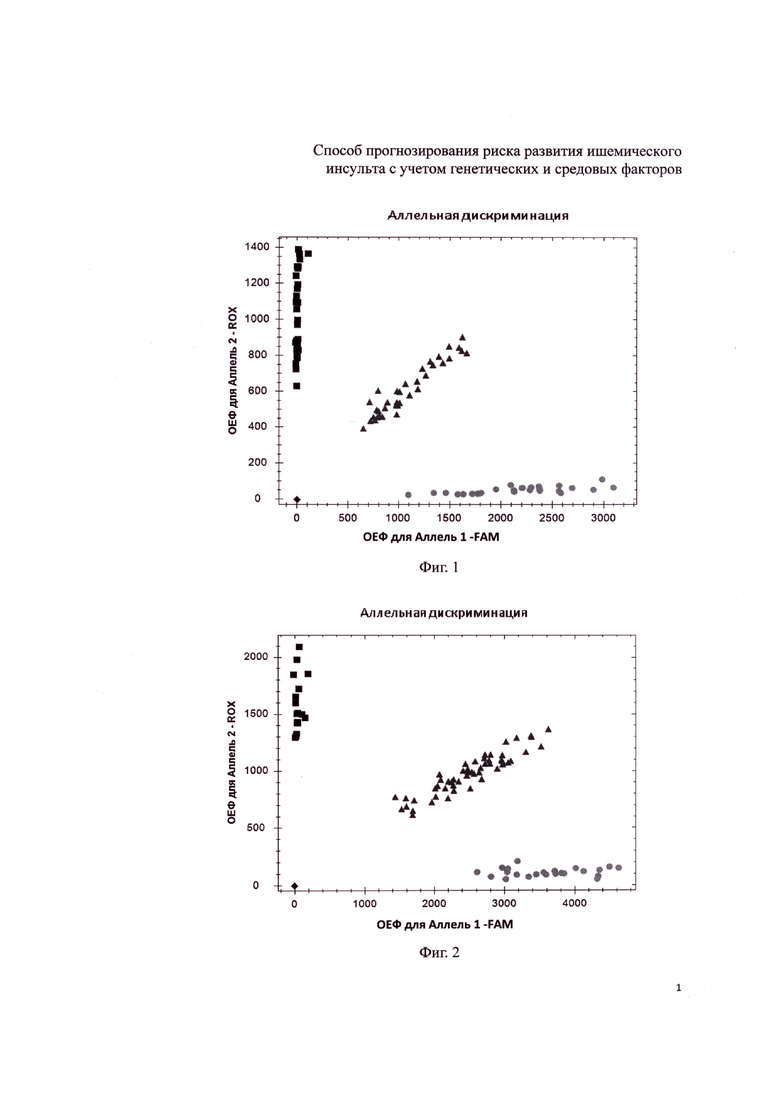
Анализ полиморфизма гена rs767455 TNFR1 проводят методом ПЦР-синтеза ДНК на амплификаторе СFX96 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 25 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (5 мин при 95°С) выполняют 40 циклов амплификации по схеме: отжиг праймеров – 1 мин. при t=54°С; денатурация – 15 сек при t=95°С. При проведении ПЦР в амплификаторе (CFX96) с флюоресцентной детекцией генотипирование осуществляют методом Tag Man зондов по данным величин ОЕФ (относительные единицы флуоресценции). Для rs767455 TNFR1 зонд с флуоресцентным красителем ROX соответствует аллелю G, зонд с красителем FAM – аллелю A (фиг.1).
Для исследования полиморфизма rs1061624 ТNFR2 используют наборы 2,5х реакционной смеси для проведения ПЦР-РВ в объеме 25 мкл на 1 образец, включающие 2,5х реакционную смесь (2,5х ПЦР буфер: (KСl, ТрисHСl (рH 8,8), 6,25 мМ MgСl2), SynTаq ДНК-полимеразу, дезоксинуклеозидтрифосфаты, глицерол, Twееn 20) в объеме 10мкл, 25мМ MgСl2 в объеме 1,5 мкл, ddH2О (деионизированная вода), по 10 пкмоль каждого праймера и по 5 пкмоль каждого зонда. При проведении ПЦР в амплификаторе с флюоресцентной детекцией (на амплификаторе CFX96) генотипирование осуществляют методом Tag Man зондов по данным величин ОЕФ (относительные единицы флуоресценции). Для rs1061624 ТNFR2 зонд с флуоресцентным красителем ROX соответствует аллелю A, зонд с красителем FAM – аллелю G (фиг.2).
Выделенную ДНК подвергают полимеразной цепной реакции с использованием стандартных олигонуклеотидных праймеров [Hulkkonen J., 2002; Mirjam M. de Jong et al., 2003].
Изобретение характеризуется фигурами.
Фиг. 1. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма TNFR1 (rs767455):  - АА,
- АА, - GG,
- GG,  - AG, ■ - отрицательный контроль
- AG, ■ - отрицательный контроль
Фиг. 2. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма ТNFR2 (rs1061624):  - GG,
- GG,  - АА,
- АА,  - AG, ■ - отрицательный контроль.
- AG, ■ - отрицательный контроль.
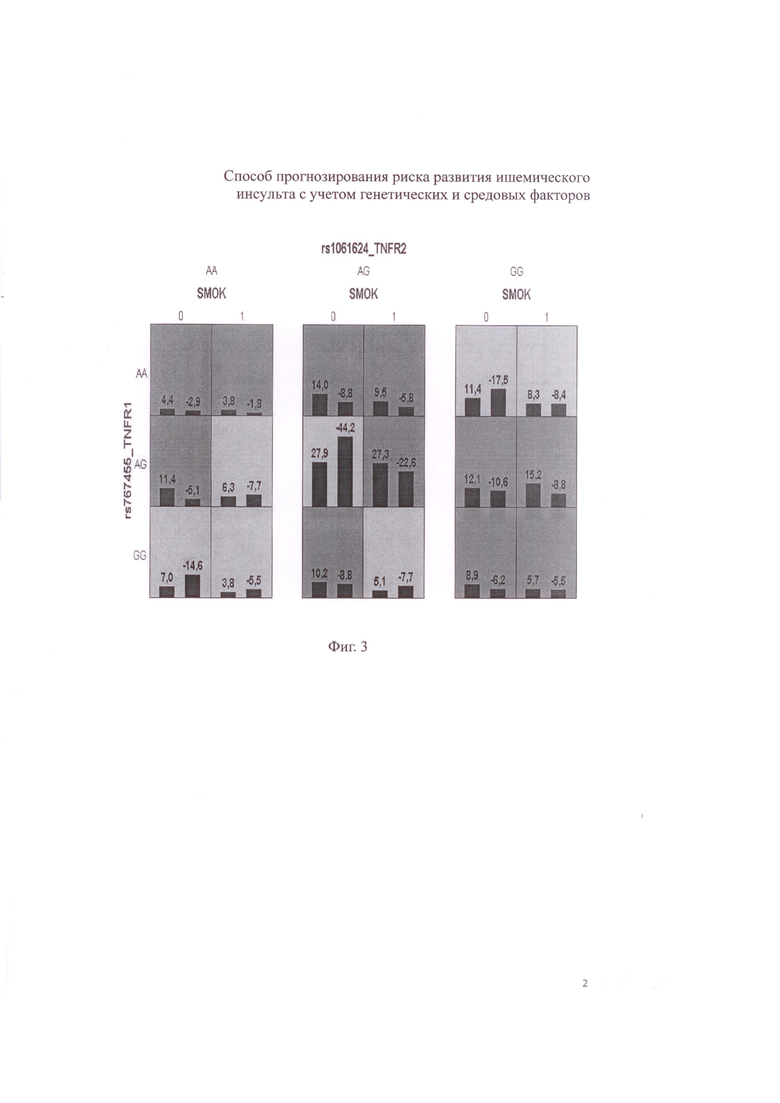
Фиг. 3. Диаграмма взаимодействий локусов рецепторов факторов некроза опухолей и курения (SMOK) в трехфакторной модели при формировании инсульта, полученная методом GMDR с коррекцией на коварианты, где столбики слева соответствуют группе больных, столбики справа соответствуют контрольной группе.
Генотипирование полиморфизмов rs767455 TNFR1, rs1061624 TNFR2 осуществляют методом детекции TagMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени.
Анализ ассоциаций сочетаний генетических вариантов и статуса курения с ишемическим инсультом проводят с помощью методов MDR (Multifactor Dimensionality Reduction) и его модификации GMDR (Generalized Multifactor Dimensionality Reduction) с использованием соответствующего программного обеспечения (MDR версии 3.0.2, http://www.epistasis.org/ mdr.html, и GMDR версии 0.9, http://www.ssg.uab.edu/gmdr/) (фиг. 3). В основе использованных методов лежит общий принцип выявления переменной, содержащей информацию о нескольких локусах, и формирование кластеров, содержащих комбинации генотипов высокого и низкого риска развития изучаемой патологии.
Возможность использования предложенного способа для оценки риска возникновения и развития ишемического инсульта подтверждает анализ результатов наблюдений 303 пациентов с инсультом и 527 индивидуумов контрольной группы. Общий объем исследуемой выборки составил 830 человек. Средний возраст пациентов с инсультом составил 59,58±8,21 лет, а средний возраст представителей контрольной группы – 58,81±7,74 лет. В группе больных с инсультом оказались 201 мужчина и 102 женщины, а в контрольной группе – 322 мужчины и 205 женщин. В исследуемые выборки включались индивидуумы русской национальности, являющиеся уроженцами Центрального Черноземья России и не имеющие родства между собой. Группа больных с инсультом и контрольная группа полностью сопоставимы по возрасту, полу, месту рождения и национальности.
Все клинические и клинико-лабораторные исследования проводили на базе неврологического и кардиологического отделений Белгородской областной клинической больницы Святителя Иоасафа, с информированного согласия пациентов на использование материалов лечебно-диагностических мероприятий, проводимых за период госпитализации и после нее для научно-исследовательских целей. В работе использовалась анкета-опросник, включающая антропометрические, социально-демографические показатели, а также сведения о наличии у респондентов средовых факторов риска цереброваскулярных заболеваний, таких как курение, злоупотребление алкоголем, низкий уровень физической активности, особенности питания, стрессовые ситуации [Промоторный полиморфизм -1293G>C гена CУР2E1 увеличивает риcк развития гипертоничеcкой болезни у мужчин, злоупотребляющих алкоголем [Текcт] / А.В. Полоников, В.П. Иванов, М.А. Cолодилова // Бюллетень экcпериментальной биологии и медицины. – 2013. – Т. 155, № 6. – C. 695-698]. Статус курения оценивался по двум категориям: отрицательный статус – обследуемый не курит/не курил, положительный статус – обследуемый курит ежедневно в течение последнего года и дольше. Полученные материалы протоколировали по стандартам этического комитета Российской Федерации.
Анализ ассоциаций сочетаний генетических вариантов цитокинов и статуса курения с ишемическим инсультом проводили с помощью методов MDR (Multifactor Dimensionality Reduction) и его модификации GMDR (Generalized Multifactor Dimensionality Reduction) с использованием соответствующего программного обеспечения (MDR версии 3.0.2, http://www.epistasis.org/ mdr.html, и GMDR версии 0.9, http://www.ssg.uab.edu/gmdr/), с коррекцией на индекс массы тела, уровни холестерина, триглицеридов, липопротеидов низкой плотности, липопротеидов высокой плотности, низкую физическую активность, предпочтение к жирной пище, редкое употребление овощей и фруктов. Для валидации полученных результатов проводили пермутационный тест – выполнено 1000 пермутаций при 10 кросс-валидациях, что обеспечивает рperm<0,001
Установлены особенности «конституции» больных с ишемическим инсультом на основе комбинаций генов рецепторов факторов некроза опухолей и курения. Выявлена модель генно-средовых взаимодействий полиморфизмов rs767455 TNFR1, rs1061624 TNFR2 и статуса курения, ассоциированная с высоким риском развития ишемического инсульта: воспроизводимость модели (CVC) составила 100%, точность предсказания модели (Test.Bal.Acc.) равна 56,33, отношение шансов OR=2,17 (95% CI 1,44-3,34) при уровне значимости р=0,01 (рреrm<0,001). В рамках данной модели выявлена комбинация, являющаяся фактором риска развития ишемического инсульта: сочетание генотипа GG rs767455 TNFR1 с генотипом GG rs1061624 TNFR2 наблюдается у 5,28% пациентов с инсультом и у 2,47% индивидуумов контрольной группы (Х2=5,82, р=0,02). Наличие данного сочетания генотипов с курением является фактором риска развития ишемического инсульта (ОR=2,41, 95% СI 1,16-5,04) независимо от влияния прочих средовых факторов.
В качестве примеров конкретного применения разработанного способа приведено обследование добровольцев русской национальности, являющихся жителями Центрального Черноземья и не являющихся родственниками между собой: определен статус курения и проведено генетическое обследование по локусам rs767455 TNFR1, rs1061624 TNFR2.
Пример 1.
У пациента С. была взята венозная кровь, при генотипировании ДНК-маркеров было выявлено, что генотип мужчины по локусу rs767455 TNFR1 – GG, генотип по локусу rs1061624 TNFR2 – GG. При анкетировании установлено, что пациент C. курит ежедневно в течение пяти лет. Сочетание генотипа GG (rs767455 TNFR1), генотипа GG (rs1061624 TNFR2) и положительный статус курения позволило отнести пациента в группу больных с высоким риском развития ишемического инсульта. Дальнейшее наблюдение и результаты ультразвукового дуплексного сканирования (УЗДС) выявили у пациента окклюзивное заболевание сонных артерий (нарушение мозгового кровоснабжения), что подтвердило высокий риск развития инсульта по ишемическому типу.
Пример 2.
У пациентки Ш. произведен забор венозной крови, при генотипировании ДНК-маркеров выявлено, что ее генотип по локусу rs767455 TNFR1 – АА, генотип по локусу rs1061624 TNFR2 – GG. При анкетировании установлено, что пациентка Ш. не курит. По данным генотипирования и отрицательному статусу курения пациентка Ш. не включается в группу больных с высоким риском развития инсульта. При дальнейшем наблюдении у пациентки не было зафиксировано нарушений мозгового кровообращения.
Пример 3.
У пациента Н. после забора венозной крови из локтевой вены и последующего генотипирования выявлен генотип АG по локусу rs767455 TNFR1 и генотип АG по локусу rs1061624 TNFR2. При анкетировании установлено, что пациент Н. курит больше года. По данным генотипирования пациент Н. не включается в группу больных с высоким риском развития ишемического инсульта. Дальнейшее обследование и результаты компьютерной томографии показали, что мозговое кровообращение пациента Н. соответствует норме.
Применение данного способа позволит на доклиническом этапе формировать среди индивидуумов группы риска и своевременно реализовывать в этих группах необходимые лечебно-профилактические мероприятия по предупреждению развития ишемического инсульта.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития ишемического инсульта | 2018 |
|
RU2685859C1 |
| Способ прогнозирования риска развития гипертонической болезни с учетом генетических и средовых факторов | 2018 |
|
RU2678441C1 |
| Способ прогнозирования риска развития ишемического инсульта с учетом генетических факторов | 2017 |
|
RU2653450C1 |
| Способ прогнозирования риска развития эссенциальной гипертензии | 2017 |
|
RU2661604C1 |
| Способ прогнозирования риска развития инсульта у мужчин на основе генетического тестирования | 2017 |
|
RU2664430C1 |
| Способ прогнозирования риска развития гипертонической болезни на основании молекулярно-генетических данных | 2018 |
|
RU2679401C1 |
| Способ прогнозирования риска развития эссенциальной гипертензии у женщин на основе генетических факторов | 2017 |
|
RU2664428C1 |
| Способ прогнозирования риска развития преэклампсии на основе комбинаций генов матриксных металлопротеиназ | 2017 |
|
RU2646448C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПРЕЭКЛАМПСИИ НА ОСНОВЕ КОМБИНАЦИЙ ГЕНОВ ЦИТОКИНОВ | 2014 |
|
RU2568891C1 |
| Способ прогнозирования риска развития ишемического инсульта у курящих женщин популяции Центральной России на основе генотипирования полиморфизма rs1136141 (G>A) гена HSPA8 | 2023 |
|
RU2806497C1 |
Изобретение относится к области медицинской диагностики и предназначено для прогнозирования риска развития ишемического инсульта. У индивидуумов русской национальности, являющихся жителями Центрального Черноземья, выделяют ДНК из венозной крови и проводят анализ полиморфизмов генов цитокинов rs1061624 TNFR2 и rs767455 TNFR1. Выявляют статус курения. Высокий риск развития ишемического инсульта прогнозируют при выявлении сочетания генотипа GG rs767455 TNFR1 с генотипом GG rs1061624 TNFR2 и с положительным статусом курения. Изобретение обеспечивает получение новых критериев оценки риска развития ишемического инсульта на основе данных о сочетаниях генетических вариантов локусов rs1061624 TNFR2, rs767455 TNFR1 и статуса курения. 3 ил., 3 пр.
Способ прогнозирования риска развития ишемического инсульта с учетом генетических и средовых факторов у индивидуумов русской национальности, являющихся жителями Центрального Черноземья, включающий выделение ДНК из венозной крови и анализ полиморфизмов генов, отличающийся тем, что анализируют полиморфизмы генов цитокинов rs1061624 TNFR2 и rs767455 TNFR1, устанавливают наличие средовых факторов риска развития ишемического инсульта, а именно – выявляют статус курения, прогнозируют высокий риск развития ишемического инсульта при выявлении сочетания генотипа GG rs767455 TNFR1 с генотипом GG rs1061624 TNFR2 и с положительным статусом курения.
| Машина для упаковки фруктов | 1930 |
|
SU21813A1 |
| СПОСОБ ДИАГНОСТИКИ ГЕНЕТИЧЕСКОЙ ПРЕДРАСПОЛОЖЕННОСТИ К РАЗВИТИЮ ИШЕМИЧЕСКОГО ИНСУЛЬТА У БОЛЬНЫХ С ФИБРИЛЛЯЦИЕЙ ПРЕДСЕРДИЙ | 2015 |
|
RU2602451C1 |
| АЛЛЕЛЬ SNP41 ГЕНА PDE4D, ЕГО ПРИМЕНЕНИЕ ДЛЯ ПРОГНОЗИРОВАНИЯ ИНДИВИДУАЛЬНОЙ ПРЕДРАСПОЛОЖЕННОСТИ К ИНСУЛЬТУ В РУССКОЙ ПОПУЛЯЦИИ, ПРИМЕНЕНИЕ МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКОГО МАРКЕРА ИНДИВИДУАЛЬНОЙ ПРЕДРАСПОЛОЖЕННОСТИ К ИНСУЛЬТУ И СПОСОБ ПРОГНОЗИРОВАНИЯ ИНДИВИДУАЛЬНОЙ ПРЕДРАСПОЛОЖЕННОСТИ К ИНСУЛЬТУ | 2010 |
|
RU2422523C1 |
| ALVARADO-ARNES L.E | |||
| et al | |||
| Single nucleotide polymorphisms of cytokine-related genes and association with clinical outcome in a Chagas disease case-control study from Brazil | |||
| Mem Inst Oswaldo Cruz | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
Авторы
Даты
2019-02-12—Публикация
2018-08-15—Подача