Область техники, к которой относится изобретение
Объектами настоящего изобретения являются:
- способ поперечного сшивания гиалуроновой кислоты или одной из ее солей и по выбору других биосовместимых полимеров,
- способ приготовления инъекционного гидрогеля, полученного указанным способом поперечного сшивания,
- гидрогель, полученный указанным способом поперечного сшивания, и
- применение гидрогеля, полученного указанным способом поперечного сшивания, в косметологии и медицине.
Уровень техники
Гиалуроновая кислота представляет собой полисахарид, образованный повторением дисахаридных звеньев, состоящих из D-глюкуроновой кислоты и N-ацетилглюкозамина. Ее структура является линейной и не имеет какой-либо видоспецифичности. Гиалуроновая кислота широко распространена в человеческих и животных живых организмах, где выполняет много биологический функций, таких как, например, контроль уровня гидратации или поддержание вязкоэластичности жидкостей или тканей. Особенно можно отметить, что она обнаружена в высокой концентрации в синовиальной жидкости, стекловидном теле глаза и в коже. В теле человека весом 70 кг содержится около 15 граммов гиалуроновой кислоты, половина из которых находится в коже, и это количество уменьшается по мере старения.
Гели на основе гиалуроновой кислоты известны и широко применяются в эстетической косметологии и медицине в течение многих лет. Можно отметить, что такие гели обычно вводят в виде инъекций:
- в глаза, во время офтальмологических хирургических операций для поддержания интраокулярного пространства и для защиты тканей глаза,
- в суставы, в случае артрозов, для компенсации дефицита синовиальной жидкости и временного восстановления хондропротекторных свойств указанной биологической жидкости,
- в кожу или под кожу для заполнения морщин или для увеличения объема определенных зон лица или тела.
В живых организмах гиалуроновая кислота имеет короткий полупериод существования (менее 1 недели). Применяемые в косметологии и медицине гидрогели для инъекций содержат гиалуроновую кислоту, стабилизированную поперечным сшиванием, что позволяет значительно увеличить период существования (далее называемый «реманентность») указанного полисахарида in vivo и, таким образом, продлить эффект воздействия введенного продукта. Таким образом, благодаря такой модификации поперечным сшиванием гидрогель на основе поперечно-сшитой гиалуроновой кислоты обладает, например, способностью заполнять морщины на срок до нескольких месяцев.
Специалисту в данной области техники понятно, что для увеличения реманентности in vivo инъекционного гидрогеля на основе гиалуроновой кислоты, можно увеличить степень поперечного сшивания гиалуроновой кислоты; однако эта модификация молекулы ведет и к увеличению вязкости геля, таким образом, затрудняя его продавливание через иглу и, следовательно, введение этого геля в область, выбранную специалистом. В этом случае необходимо:
- либо ограничить степень поперечного сшивания гиалуроновой кислоты и, таким образом, реманентность геля in vivo, с целью сохранения удовлетворительной силы выдавливания,
- либо использовать иглы большего диаметра, чтобы уменьшить силу выдавливания, требуемую для экструдирования геля через иглу, что является более болезненным для пациента, а также вызывает большее травмирование (кровоподтеки, красные пятна, воспалительный процесс, отеки…) области, где осуществляется инъекция.
Для преодоления этой проблемы было предложено множество различных решений, специалисты производили поиск возможностей для создания состава для инъекций, имеющего подходящую реманентность и вязкость, и таким образом обеспечивающего удовлетворительную силу продавливания геля через иглу. Например, можно упомянуть:
- составы на основе частиц поперечно-сшитой гиалуроновой кислоты, полученных путем разделения поперечно-сшитого геля на частицы, в целом, путем измельчения; описаны различные препарационные способы для получения такого типа составов, как в случае заявки WO 97/04012,
- составы на основе поперечно-сшитой гиалуроновой кислоты, содержащие различные сшивающие химические вещества согласно специальному способу приготовления, описанному в заявке WO 2005/085329,
- составы на основе поперечно-сшитой гиалуроновой кислоты, содержащие смеси поперечно-сшитых гелей, которые не сшиты друг с другом, т.е. не соединены друг с другом ковалентными связями; эти составы получают согласно специальному способу, описанному в заявке FR 2924615, и
- составы на основе поперечно-сшитой гиалуроновой кислоты, состоящие из частиц поперечно-сшитой гиалуроновой кислоты, которые сшиты с матрицей поперечно-сшитой гиалуроновой кислоты; такие составы приготавливают в соответствии с заявкой ЕР 2011816 или в соответствии с заявкой US 2010/0028435.
Однако данные решения не являются полностью удовлетворительными.
В заявке WO 97/04012 описан конкретный способ изготовления, позволяющий получить продукты на основе полисахаридов (которыми может быть гиалуроновая кислота) в форме частиц. Гранулированные гели на основе поперечно-сшитой гиалуроновой кислоты, именуемые в специализированной литературе также «двухфазными гелями», характеризуются наличием частиц с диаметром от 200 микрометров до более чем 1000 микрометров, диспергированных в растворе несшитой гиалуроновой кислоты, что дает возможность облегчить введение благодаря эффекту смазки. Эти гели не являются полностью удовлетворительными, поскольку выдавливание геля через иглу происходит неравномерно, особенно если продукт содержит частицы большого диаметра; при этом раствор на основе несшитой гиалуроновой кислоты, играющей роль носителя, быстро всасывается in vivo, что ведет к по меньшей мере частичной потере желаемого эффекта (можно отметить снижение объема заполнения в течение нескольких дней после инъекции продукта, предназначенного для создания объема); и, наконец, данный продукт имеет не очень хороший профиль безопасности (т.е. имеет больше побочных эффектов) по сравнению с гелями на основе гиалуроновой кислоты, не содержащими частиц, которые могут спровоцировать реакцию на инородное тело и/или вызвать миграцию этих частиц в результате механического воздействия на обработанную область.
В заявке WO 2005/085329 описан конкретный способ изготовления, содержащий этап инициирования поперечного сшивания определенного количества по меньшей мере одного полимера (которым может быть гиалуроновая кислота), за которым следует добавление дополнительного количества полимера (которым может быть гиалуроновая кислота) с молекулярной массой выше 500000 Да в растворе, с таким разбавлением реакционной смеси, чтобы уменьшить общую концентрацию полимера в растворе, продолжая реакцию поперечного сшивания. Такой раствор не дает возможности провести эффективное поперечное сшивание гиалуроновой кислоты. Естественно, добавление дополнительного количества полимера сопровождается разбавлением и, следовательно, уменьшением концентрации гиалуроновой кислоты в реакционной смеси. Таким образом, вероятность столкновения цепей гиалуроновой кислоты с сшивающим агентом понижается, и реакция сшивания не очень эффективна.
В заявке FR 2924615 описан способ изготовления, характеризующийся поперечным сшиванием гомогенной смеси идентичных или разных х полимеров (которыми может быть гиалуроновая кислота) перед смешиванием. Под смешиванием понимают размещение х полимеров в непосредственной близости друг от друга без образования ковалентных связей между ними. Этот раствор не является полностью удовлетворительным, поскольку полимеры не связаны друг с другом, и поэтому полученный таким образом гель может распасться внутри области инъекции, особенно под воздействием механической нагрузки, которая может быть достаточно значительной в указанной области. Например, можно упомянуть случай, если продукт вводят в губы с целью создания объема; при этом губы подвергаются высоким механическим нагрузкам. Испытанное механическое воздействие может вызвать миграцию имплантированного геля и привести к побочным эффектам не только в области инъекции, но и вокруг нее.
Заявка ЕР 2011816 относится к инъецируемым гелям полисахаридов (которыми может быть гиалуроновая кислота), содержащим по меньшей мере один первый сильно сшитый полисахаридный гель в форме частиц и по меньшей мере один слабо сшитый полисахаридный гель, образующий матрицу; при этом указанный по меньшей мере один первый гель связан ковалентными связями с указанным по меньшей мере одним вторым гелем. В отличие от продукта по заявке WO 97/04012, сильно сшитые частицы связаны со слабо сшитой полисахаридной матрицей; тем самым миграция частиц в данном решении значительно ограничена в краткосрочной и/или среднесрочной, но не в долгосрочной перспективе (высвобождение сильно сшитых частиц с возможностью миграции после рассасывания слабо сшитого полисахарида в ткани). Поскольку это решение предусматривает использование полисахаридных частиц с высокой степенью сшивания, существует высокий риск ответной реакции на инородное тело из-за гранулированного характера продукта и высокой степени сшивания этих частиц (производится существенная модификация гиалуроновой кислоты, что способствует нераспознаванию молекулы организмом).
В заявке US 2010/0028435 раскрыт способ приготовления составов на основе поперечно-сшитой гиалуроновой кислоты, изготовленных из частиц поперечно-сшитой гиалуроновой кислоты, совместно сшитых с матрицей поперечно-сшитой гиалуроновой кислоты. Так, в отношении данной заявки mutatis mutandis применимы те же замечания, что и в отношении заявки ЕР 2011816.
Раскрытие изобретения
Настоящее изобретение позволяет устранить указанные различные недостатки благодаря новому способу поперечного сшивания гиалуроновой кислоты или одной из ее солей и, по выбору, других биосовместимых полимеров; где способ дает возможность получить гидрогель, в частности, обладающий следующими характеристиками:
- хорошей способностью к продавливанию его через иглы и, за счет этого, легкостью их введения специалистом, выполняющим инъекцию, в область инъекции безболезненно и без существенного травмирования пациента,
- отсутствием перехода одной или большего числа конститутивных фаз гидрогеля в частицы в ходе выполнения поперечного сшивания (но при этом продукт характеризуется низкой силой выдавливания при инъекции, несмотря на отсутствие частиц, которые в целом понижают силу выдавливания);
- отсутствием в продукте совместно сшитых частиц, что ведет к существенному улучшению профиля безопасности (меньшее количество побочных эффектов и осложнений в краткосрочной и/или среднесрочной/долгосрочной перспективе), повышенной способности к интеграции/имплантированию гидрогеля в ткань (более равномерное распределение продукта в ткани), а также обеспечивает значительно более короткий и менее сложный способ изготовления (поскольку в процессе изготовления отсутствуют трудоемкие этапы измельчения),
- исключительными свойствами вязкоэластичности, происходящими из особой структуры полученного гидрогеля, что дает возможность предложить выполняющему инъекцию специалисту продукт с особыми механическими/реологическими свойствами, соответствующий его ожиданиям при обработке желаемого участка, учитывая его анатомию, управляющие физиологические механизмы и, если применимо, требуемые механические/реологические свойства, которые позволят скорректировать выявленные недостатки,
- способностью к имплантированию простым путем ткани в области, подлежащие обработке, благодаря особенной «мультиструктурированной» (и без совместно сшитых частиц) структуре полученного гидрогеля,
- повышенной безопасностью полученного гидрогеля из-за лучшей способности не рассасываться в обработанной области и, таким образом, не мигрировать в прилегающие либо более отдаленные области, особенно при воздействии механических нагрузок,
- сложной структурой матрицы полученного гидрогеля, характеризующейся как «мультиструктурированная», благодаря которой можно оптимизировать контролируемое высвобождение активных и/или биологических веществ, когда это применимо,
- оптимизированной реманентностью полученного гидрогеля с целью продления эффективности косметологического и терапевтического воздействия, что дает возможность ограничить количество введений продукта за одну медицинскую или хирургическую процедуру.
Поэтому объектом изобретения является новый способ поперечного сшивания гиалуроновой кислоты или одной из ее солей и, по выбору, других биосовместимых полимеров, содержащий этапы:
a) приготовления первой водной фазы гиалуроновой кислоты и, по выбору, других биосовместимых полимеров, частично сшитых, в котором:
- добавляют гиалуроновую кислоту или одну из ее солей и, по выбору, других биосовместимых полимеров в водный раствор для получения концентрации С1 гиалуроновой кислоты,
- добавляют количество Q1 сшивающего агента,
- обеспечивают частичное сшивание гиалуроновой кислоты путем управления температурой Т1 и продолжительностью t1 реакции сшивания,
- причем приготовленная первая водная фаза частично сшитой гиалуроновой кислоты в целом не переходит в гранулированное состояние;
b) приготовления по меньшей мере одной второй водной фазы гиалуроновой кислоты и, по выбору, других биосовместимых полимеров, частично сшитых, в котором:
- добавляют гиалуроновую кислоту или одну из ее солей и, по выбору, других биосовместимых полимеров для получения концентрации С2 гиалуроновой кислоты,
- добавляют количество Q2 сшивающего агента,
- обеспечивают частичное сшивание гиалуроновой кислоты путем управления температурой Т2 и продолжительностью t2 реакции сшивания,
причем приготовленная вторая водная фаза частично сшитой гиалуроновой кислоты в целом не переходит в гранулированное состояние,
c) добавления к первой фазе по меньшей мере второй фазы частично сшитой гиалуроновой кислоты, и затем перемешивания указанных по меньшей мере двух фаз с возможным добавлением дополнительного количества Qm сшивающего агента, и
d) продолжения поперечного сшивания приготовленной смеси путем управления температурой Tm и продолжительностью tm реакции поперечного сшивания.
После этого реакцию поперечного сшивания смеси прекращают, предпочтительно разбавляя водным раствором и/или удаляя непрореагировавший сшивающий агент путем выполнения очистки.
Следовательно, способ поперечного сшивания по изобретению предполагает смешивание во время сшивания по меньшей мере двух водных фаз гиалуроновой кислоты и, по выбору, других биосовместимых полимеров, которые уже частично сшиты, и последующее продолжение реакции сшивания для связывания указанных по меньшей мере двух фаз ковалентными связями.
Понятие «частично сшитый» подразумевает ситуацию, когда указанные по меньшей мере две водных фазы гиалуроновой кислоты, по выбору содержащие другие биосовместимые полимеры, все еще имеют доступные для реагирования сайты полимерных цепей, способные прореагировать со сшивающим агентом для поперечного сшивания (образования мостиков) между новыми цепями гиалуроновой кислоты и/или другими биосовместимыми полимерами.
Важно отметить, что способ поперечного сшивания по изобретению не подразумевает приготовление и/или добавление поперечно-сшитых частиц гиалуроновой кислоты или одной из ее солей, либо любого другого полимера во время выполнения этапов указанного способа поперечного сшивания, т.е. этапов а, b, с и d, описанных выше. Никакие частично сшитые фазы ни в какой момент в ходе выполнения способа не переводят в частицы, например, путем измельчения. Таким образом, способ поперечного сшивания по изобретению не дает возможности сшивания вместе поперечно-сшитых частиц с гелем гиалуроновой кислоты.
В одном из вариантов осуществления изобретения вторая водная фаза частично сшитой гиалуроновой кислоты характеризуется более высокой степенью сшивания, чем первая водная фаза частично сшитой гиалуроновой кислоты. Эта особенность дает возможность облегчения размешивания в первой фазе второй, более сильно сшитой фазы.
Понятие «степень частичного сшивания» подразумевает уровень поперечного сшивания фазы непосредственно перед ее смешиванием с другой фазой; уровень поперечного сшивания является лишь частичным, так как он будет еще развиваться при продолжении поперечного сшивания во время смешивания фаз. Уровень поперечного сшивания может быть определен для каждой релевантной фазы экспериментальным путем, измеряя степень сшивания и сравнивая ее с теоретически максимальной степенью сшивания (которую можно рассчитать, оценив соотношение числа молей введенного сшивающего агента и числа молей полимерных звеньев, способных к поперечному сшиванию). Экспериментальную оценку степени сшивания производят либо косвенно (например, измерением силы выдавливания, см. пример 2), либо непосредственно (например, спектрометрией ядерного магнитного резонанса (ЯМР)), например, способом, раскрытым в публикации Кенн и др. (Kenne et al. Modification and cross-linking parameters in hyaluronic acid hydrogels - definitions and analytical methods, Carbohyr. Polym. 2013, 91; 410-418).
Таким образом, в целом «степень частичного сшивания» частично сшитой фазы составляет менее 90% (от максимальной теоретически рассчитанной степени), или менее 70%, или даже менее 50%, или даже менее 30%, или даже менее 10%.
В одном из вариантов осуществления изобретения концентрация С2 гиалуроновой кислоты больше либо равна концентрации С1. Эта особенность дает возможность облегчить размешивание более высококонцентрированной второй фазы в первой фазе, но также достичь лучшего набухания второй фазы в первой фазе (гиалуроновая кислота способна набухать в воде, тем более, когда ее концентрация является значительной). Это дает возможность способствовать максимальному стерическому «встраиванию» за счет переплетения полимерных цепей второй фазы в первой фазе, а также способствует протеканию реакции сшивания, которая связывает полимерные цепи первой и второй фаз, в силу более близкого физического расположения данных цепей, и, тем самым, большей эффективности реакции образования мостиков между этими цепями.
В одном из вариантов осуществления изобретения фазы количество сшивающего агента Q2 больше либо равно количеству Q, чтобы получить степень частичного сшивания больше для второй фазы, чем для первой.
В одном из вариантов осуществления изобретения температура Т2 выше или равна температуре Т1, чтобы получить степени частичного сшивания больше для второй фазы, чем для первой. Температура Tm сшивания сама по себе выше, чем температура Т2, чтобы максимизировать эффективность реакции поперечного сшивания, позволяя связать первую и вторую фазы ковалентными связями.
В одном из вариантов осуществления изобретения продолжительность t2 реакции сшивания больше или равна продолжительности t1, чтобы получить более высокую степени частичного сшивания для второй фазы, чем для первой. Продолжительность tm реакции сшивания сама по себе может быть больше или равна продолжительностям t1 и t2, но также может быть и меньше их. Такая продолжительность tm зависит от выбранной температуры Tm для обеспечения сшивания смеси указанных по меньшей мере двух фаз.
Во время приготовления смеси массы первой и второй фаз могут быть равны либо отличаться. В зависимости от свойств, которые желательно придать получаемому гидрогелю в соответствии с изобретением, во время перемешивания присутствие одной фазы должно быть соответствующим образом промоутировано относительно другой, и, следовательно, должна быть использована большая масса этой фазы по сравнению с другой. Так, можно утверждать, что с точки зрения механических/реологических свойств, фаза, имеющая наиболее высокую степень сшивания, придает гелю по изобретению доминирующие свойства эластичности и реманентности относительно фазы с меньшей степенью сшивания. С другой стороны, фаза с наименьшей степенью сшивания обусловливает меньшую силу выдавливания этой фазы, за счет чего легче использовать продукт, предназначенный для инъекций. Таким образом, для гидрогеля в соответствии с изобретением наблюдается синергетический эффект результирующих механических/реологических свойств, реманентности и способности к выдавливанию. Эта синергия происходит благодаря оптимизации двух взаимно воздействующих параметров: низкая степень сшивания одной из фаз способствует более легкому выдавливанию, а также лучшей когезии и общей пластичности гидрогеля, и снижает реманентность и эластичность, в то время как более высокая степень сшивания другой фазы способствует лучшей реманентности и более выраженным в сторону упругости продукта вязкоэластичным свойствам и a contrario снижает способность к выдавливанию, когезию и пластичность. Следовательно, такая синергия позволяет комбинировать преимущества каждой из разных составляющих фаз, минимизируя их недостатки, и избежать возникновения недостатков, описанных ранее в отношении составов, содержащих поперечно-сшитые полимерные частицы. Оптимизация пропорционального содержания каждой из поперечно-сшитых фаз гидрогеля обеспечивает возможность для получения легко инъецируемый продукт, отвечающий различным существующим области косметологии и медицины требованиям к инъецируемости, механическим/реологическим качествам и реманентности.
В одном из вариантов осуществления изобретения сшивание смеси различных частично сшитых фаз останавливают, выполняя очистку для удаления остатков непрореагировавшего сшивающего агента. Такую очистку выполняют хорошо известными специалистам методами, например, при помощи диализной ванны, или промывая проточной водой. Предпочтительно выбирают очистку при помощи диализа, для которого используют изотонический раствор с подходящим рН. В конце реакции сшивания смеси различных частично сшитых фаз, но до этапа очистки смеси, иногда целесообразно нейтрализовать полученный гель традиционными способами, известными в данной области, например, путем добавления кислоты, если реакция сшивания протекала в щелочной среде, или путем добавления щелочи, если реакция сшивания протекала в кислой среде.
Изобретение относится к поперечному сшиванию гиалуроновой кислоты или одной из ее солей, в частности, физиологически приемлемых солей, таких как натриевая, кальциевая, цинковая, калиевая соли (предпочтительно, натриевой соли). Гиалуроновая кислота может иметь любое животное происхождение, либо получена бактериальной ферментацией. Она может иметь молекулярную массу от нескольких Да до нескольких миллионов Да, предпочтительно от около 0,1 до 4 млн Да.
Изобретение также касается поперечного сшивания других биосовместимых полимеров, комбинируемых с гиалуроновой кислотой. Эти полимеры природного или искусственного происхождения должны иметь химические свойства, позволяющие им сшиваться, и они должны быть биосовместимыми, чтобы иметь способность контактировать с биологическими жидкостями или тканями. Можно упомянуть, например, полисахариды, полиэфиры, полиангидриды, полифосфазены, поли-ε-капролактоны, полимолочные кислоты и их производные, поливиниловые кислоты, полиакриламиды, N-винил-пирролидон и акриловые полимеры, а также их биологически приемлемые производные.
Реакция поперечного сшивания протекает в водных растворах в кислой или щелочной среде, предпочтительно, в щелочной среде с рН предпочтительно от 8 до 13. Значения рН растворов может быть одинаковыми либо различными.
Сшивающие агенты, участвующие в различных реакциях поперечного сшивания, могут быть одинаковыми или различными. В качестве таких агентов, как правило, выступают би- либо полифункциональные сшивающие агенты различных типов, они, например, могут быть выбраны из дивинилсульфонов, би- или полифункциональных эпоксидных смол, карбодиимидов и формальдегидов. Предпочтительно, агенты выбирают из ряда би- или полифункциональных эпоксидных смол, особенно 1,4-бутандиол-диглицидилового эфира (БДДЭ), диэпокси-октана или 1,2-бис(2,3-эпоксипропил)-2,3-этилена. Для каждой из реакций поперечного сшивания наиболее предпочтительно использование БДДЭ.
Температуры поперечного сшивания, как правило, находятся в пределах 15-60°С. Для поперечного сшивания частично сшитых фаз температура предпочтительно ниже 35°С, а для поперечного сшивания смеси разных частично сшитых фаз - выше 45°С.
Продолжительность поперечного сшивания обычно составляет несколько часов, преимущественно от более 1 часа до приблизительно 12 часов.
Поперечное сшивание смеси разных частично сшитых фаз предпочтительно выполняется с двумя фазами, однако оно также может быть выполнено и с более чем двумя фазами, имеющими разные степени частичного сшивания.
Пропорциональный вес каждой частично сшитой фазы в смеси для сшивания может значительно варьироваться, особенно в зависимости от выбранного конкретного состава, от степени частичного сшивания соответствующих релевантных фаз и от целевых свойств готового продукта. В целом, в смеси, пропорциональный вес фазы с максимально высокой степенью частичного сшивания составляет от около 0,1 до 99,9%, или в пределах от около 5 до 95%, или в пределах от около 10 до 90%, или в пределах от около 20 до 80%, или в пределах от около 30 до 70%, или в пределах от около 40 до 60%, или в пределах от около 45 до 55% от общей массы разных фаз смеси.
Способ поперечного сшивания по изобретению отличается от способов, известных из уровня техники. Ни один из описанных способов не предусматривает поперечное сшивание, включающее в себя смешивание во время поперечного сшивания по меньшей мере двух водных фаз гиалуроновой кислоты и, по выбору, других биосовместимых полимеров, предварительно частично сшитых, и дальнейшего продолжения реакции поперечного сшивания для связывания указанных по меньшей мере двух фаз ковалентными связями без подготовки и/или добавления веществ из сшитой гиалуроновой кислоты, ее соли или иного полимера, на этапах указанного способа поперечного сшивания.
Публикациями из известного уровня техники, рассматриваемыми в роли наиболее близких аналогов заявленного изобретения, являются заявки, указанные ниже.
- Заявка WO 97/04012, в которой описан специальный способ поперечного сшивания полисахарида, которым может быть гиалуроновая кислота, где способ содержит этапы:
- помещения полисахарида в водный раствор,
- инициирования реакции поперечного сшивания путем добавления сшивающего агента,
- создания стерических условий, неблагоприятных для реакции поперечного сшивания, преимущественно представляющих собой разбавление реагирующей смеси во время сшивания, и
- создания стерических условий, благоприятных для реакции поперечного сшивания, преимущественно представляющих собой концентрирование реагирующей смеси путем выпаривания для завершения реакции поперечного сшивания.
В отличие от заявленного изобретения, указанное решение не предусматривает смешивание частично сшитых фаз гиалуроновой кислоты в процессе поперечного сшивания.
С другой стороны, настоящее изобретение не характеризуется созданием неблагоприятных стерических условий (например, разбавления), а затем благоприятных стерических условий (например, выпаривания) во время реакции поперечного сшивания: процесс поперечного сшивания по изобретению протекает в благоприятных условиях с целью оптимальной производительности процесса.
- Заявка WO 2005/085329, в которой описан специальный способ поперечного сшивания, способ характеризуется:
- этапом инициирования поперечного сшивания определенного количества по меньшей мере одного полимера, и
- добавлением в раствор дополнительного количества полимера молекулярной массой более 500000 Да, с разбавлением реакционной смеси, чтобы уменьшить общую концентрацию полимера в растворе при продолжении реакции поперечного сшивания.
В отличие от заявленного изобретения указанное решение не применяет этапы смешивания различных частично сшитых фаз гиалуроновой кислоты во время поперечного сшивания.
Указанная заявка предусматривает добавление полимера во время реакции поперечного сшивания, но этот полимер не подвергали предварительному поперечному сшиванию ни частично, ни полностью. С другой стороны, в отличие от настоящего изобретения, такое добавление полимера должно непременно сопровождаться разбавлением реакционной смеси, что ведет к неблагоприятным стерическим условиям и, как следствие, к не вполне эффективному продолжению реакции поперечного сшивания.
- Заявка FR 2924615 описывает способ приготовления гидрогеля, который характеризуется гомогенным смешиванием х полимеров, идентичных либо разных, сшитых перед смешиванием.
В отличие от заявленного изобретения, указанное решение не применяет этапы смешивания различных частично сшитых фаз гиалуроновой кислоты во время поперечного сшивания.
X полимеров, которые предварительно сшиты, и для каждого из которых реакция поперечного сшивания была остановлена, перемешивают, чтобы просто разместить указанные х полимеров в непосредственной близости друг к другу без образования ковалентных связей между ними: эти различные полимеры не подвергаются поперечному сшиванию.
Заявка ЕР 2011816 описывает способ приготовления гидрогеля, содержащий этапы:
- подготовки частиц из первого сильно сшитого полисахарида по известным специалистам методикам измельчения, чтобы получить частицы с необходимым размером зерна,
- взвешивания этих частиц,
- добавления по меньшей мере одного второго полисахарида, и
- поперечного сшивания указанного по меньшей мере одного второго полисахарида до степени поперечного сшивания Х2 для получения по меньшей мере одного второго слабо сшитого полисахарида и его поперечного сшивания с указанными частицами.
В отличие от этого решения, в заявленном изобретении не предусмотрено использование поперечно-сшитых частиц (приготовление и/или добавление в реакционную смесь) во время поперечного сшивания. Следует особо отметить, что в изобретении во время поперечного сшивания отсутствует этап измельчения, позволяющий получить частицы поперечно-сшитой гиалуроновой кислоты:
- для частично сшитых фаз перед смешиванием указанных фаз для продолжения поперечного сшивания, и
- для смешивания частично сшитых фаз во время продолжения реакции поперечного сшивания.
- В заявке US 2010/0028435 описан способ приготовления инъекционного геля, схожего с гелем, описанным в заявке ЕР 2011816.
Гель, описанный в заявке US 2010/0028435, получают путем взаимного поперечного сшивания поперечно-сшитых частиц гиалуроновой кислоты с гелем гиалуроновой кислоты.
В отличие от указанной заявки (и изобретения по заявке ЕР 2011816) способ поперечного сшивания по изобретению не предусматривает никакого приготовления и/или добавления поперечно-сшитых частиц гиалуроновой кислоты или одной из ей солей, или любого другого полимера, на этапах указанного метода поперечного сшивания. Таким образом, способ поперечного сшивания по изобретению не позволяет выполнить взаимное поперечное сшивание поперечно-сшитых частиц с гелем гиалуроновой кислоты.
Изобретение также относится к способу приготовления инъекционного гидрогеля, образуемого гиалуроновой кислотой или одной из ее солей и, по выбору, другими биосовместимыми полимерами, поперечно-сшитыми согласно описанному ранее способу поперечного сшивания. Этот способ характеризуется наличием по меньшей мере следующих последовательных этапов:
- поперечного сшивания гиалуроновой кислоты или одной из ее солей и, по выбору, других биосовместимых полимеров согласно описанному ранее способу поперечного сшивания;
- очистки смеси при помощи изотонического раствора с приемлемым рН;
- гомогенизации смеси с возможным добавлением одного или нескольких других биосовместимых полимеров и/или одного или нескольких веществ, которые могут оказать положительно воздействие на организм, например, активных веществ;
- по выбору, дегазации и/или лиофилизации;
- помещения в шприц, флакон или любой другой герметичный контейнер, и
- стерилизации.
Гидрогель для инъекций по изобретению предпочтительно помещают в шприцы и затем стерилизуют любым из способов, известных per se, преимущественно, автоклавированием для непосредственного использования и/или продажи.
Изобретение также относится к гидрогелю, полученному описанным выше способом поперечного сшивания. Этот гидрогель состоит, по меньшей мере, из поперечно-сшитой гиалуроновой кислоты или одной из ее солей и, по выбору, других биосовместимых полимеров, и характеризуется смесью нескольких фаз поперечно-сшитой гиалуроновой кислоты с разной степенью сшивания, где указанные фазы связаны друг с другом ковалентными связями. Таким образом, гидрогель, полученный способом поперечного сшивания по изобретению, может быть охарактеризован как состоящий из одной «мультиструктурированной» поперечно-сшитой фазы без сшитых друг с другом частиц.
Согласно одному из аспектов изобретения, гидрогель может быть основан на производном гиалуроновой кислоты, т.е. основан на молекуле, полученной модификацией молекулы гиалуроновой кислоты химическим или иным путем.
Гидрогель по изобретению обладает хорошей способностью к выдавливанию через иглы, и поэтому специалист может легко выполнить инъекцию в область введения, и она будет безболезненной и не будет значительно травмировать пациента. Это преимущество обусловлено «мультиструктурированной» комплексной матрицей, основанной на способе поперечного сшивания по изобретению, что позволяет способствовать более удобному инъецированию благодаря смазыванию, которое обусловлено присутствием в продукте фазы с меньшей степенью сшивания.
Гидрогель по изобретению не содержит и не состоит из поперечно-сшитых друг с другом частиц. Это обеспечивает преимущество значительно улучшенного профиля безопасности продукта в сравнении с продуктом, содержащим частицы (меньше побочных эффектов и осложнений в краткосрочной и/или среднесрочной/долгосрочной перспективе), и повышенной способности к интеграции /имплантированию гидрогеля в ткань (более равномерное распределение продукта в ткани).
Благодаря своему своей «мультиструктурированности», гидрогель по изобретению обладает отличными механическими/реологическими вязкоэластичными свойствами (т.е. вязкостью и эластичностью). Присутствие в гидрогеле по изобретению по меньшей мере двух фаз в равных или различных пропорциях, имеющих разную степень сшивания, позволяет оптимально соответствовать нуждам специалистов, выполняющих инъекцию в выбранную область, в плане наблюдения за анатомией, управляющими физиологическими механизмами и, если применимо, необходимыми механическими/реологическими свойствами, которые позволят скорректировать выявленные недостатки (например, повышенная эластичность для создания объема вокруг скуловой кости).
Гидрогель по изобретению имеет хорошую способность к «биологической имплантации» в ткани. «Мультиструктурированная» матрица обеспечивает превосходную гибкость, что позволяет достичь оптимального проникновения продукта в ткани и за счет этого ограничить возникновение пост-инъекционных травм и, следовательно, ограничить побочные эффекты, такие как боли в области инъекции, а также сопровождающую любые инъекции воспалительную реакцию.
Особая структура гидрогеля, характеризующаяся тем, что разные фазы связаны друг с другом ковалентными связями, также позволяет повысить безопасность введенного имплантата, улучшая способность продукта не распадаться и не мигрировать в прилегающие или более отдаленные области, особенно в результате воздействия на обработанную область механических нагрузок.
«Мультиструктурированная» матрица гидрогеля также позволяет получить фазы с более высокой степенью сшивания, сохранив при этом инъецируемый продукт, что ведет к лучшей реманентности гидрогеля и, таким образом, продлению эффекта от косметологического/терапевтического воздействия, и позволит еще более сократить количество введений препарата за одну медицинскую или хирургическую процедуру.
Высокий профиль безопасности имплантата по изобретению в сочетании с его особой комплексной структурой, наделяющей его механическими/реологическими качествами, а также качествами биологического интегрирования, адаптируемыми и оптимизируемыми в зависимости от характеристик области, подлежащей обработке, делает продукт предпочтительным выбором для контролируемого и/или отложенного высвобождения одного либо нескольких веществ, положительно воздействующих на организм, особенно активных субстанций и/или биологических организмов, таких как клетки, обогащенные тромбоциты, гены, фрагменты ДНК или факторы роста. Наличие в продукте различных фаз, фаз с разной степенью сшивания, а также концентрациями полимеров, позволяет высвобождать каждое из этих веществ в разное время, и тем самым оптимизировать профиль высаливания и воздействия одного либо нескольких активных ингредиентов или соединений биологического происхождения для местного или общего воздействия.
Гидрогель по изобретению предпочтительно имплантируют инъекцией в ткани и/или жидкости живого человеческого или животного организмов.
Гидрогель по изобретению может быть использован и в неинъецируемой форме. В этом случае специалист имплантирует стерильный продукт по изобретению, помещая его в подлежащую обработке область с помощью подходящих медицинских и/или хирургических инструментов.
Гидрогель по изобретению можно использовать в композициях для наружного применения в соответствии с приемлемыми составами, например, для нанесения на кожу, волосы, ногти, роговую оболочку глаза, зубы, губы, внутренние или наружные слизистые оболочки и на раны. В этом случае гель может содержать любые соединения, имеющие один или несколько положительных эффектов в отношении подлежащей обработке области, например, витамины, антиоксиданты, увлажняющие молекулы, протеины, активные субстанции, имеющие или не имеющие фармакологического действия, биологические организмы, такие как клетки, обогащенные тромбоциты, гены, фрагменты ДНК или факторы роста, красящие агенты, пигменты, молекулы пахучих веществ или ароматические молекулы. Эти соединения могут быть либо диспергированы в гидрогеле, либо присоединены к одному или нескольким полимерам гидрогеля, или могут быть заключены/инкапсулированы в другом материале, который сам диспергирован в гидрогеле.
Согласно одному из аспектов изобретения, общая концентрация гиалуроновой кислоты или одной из ее солей в гидрогеле составляет от 0,1 до 50 мг/мг, предпочтительно от 1 до 35 мг/мл, наиболее предпочтительно - от 8 до 30 мг/мл.
Согласно одному из аспектов изобретения, гидрогель по изобретению частично или полностью лиофилизируют для получения полутвердой формы или порошка.
Согласно одному из аспектов изобретения, гидрогель по изобретению содержит одно или несколько природных или искусственных активных веществ, обладающих или не обладающих фармакологическим действием, например, антиоксиданты, противовоспалительные средства, антисептики, антибактериальные агенты, противогрибковые агенты, противоопухолевые агенты, местные обезболивающие, протеины, гормоны, как по отдельности, так и в комбинациях. Эти активные вещества могут быть или диспергированы в гидрогеле, или присоединены к одному или нескольким полимерам гидрогеля, или заключены/инкапсулированы в другом материале, который сам диспергирован в гидрогеле. В качестве примера последнего случая можно привести инкапсулирование активного вещества, такого как противовоспалительное вещество, в микросферах на основе полимера, являющегося производным полимолочной кислоты или поли-ε-капролактона.
Согласно одному из аспектов изобретения, гидрогель содержит лидокаин, диспергированный в его поперечно-сшитой матрице.
Согласно одному из аспектов изобретения, гидрогель содержит одно или несколько соединений биологического происхождения, например, клетки, обогащенные тромбоциты, гены, фрагменты ДНК или факторы роста. Эти соединения предпочтительно диспергированы в гидрогеле, однако могут быть присоединены к одному или нескольким полимерам гидрогеля, или заключены/инкапсулированы в другом материале, который сам диспергирован в гидрогеле.
Согласно одному из аспектов изобретения, гидрогель содержит полимеры, диспергированные в поперечно-сшитой матрице гидрогеля. Например, можно упомянуть полисахариды, полиэфиры, полиангидриды, полифосфазены, поли-ε-капролактоны, полимолочные кислоты и их производные, поливиниловые кислоты, полиакриламиды, N-винил-пирролидон и акриловые полимеры, а также их биологически приемлемые производные.
Согласно одному из аспектов изобретения, гидрогель содержит минеральные вещества, диспергированные в поперечно-сшитой матрице гидрогеля. Например, можно упомянуть гидроксиапатиты или трикальций фосфаты, например, β-трикальций фосфаты.
Согласно одному из аспектов изобретения, гидрогель непосредственно перед введением пациенту смешивают с одним или несколькими другими предпочтительно стерильными веществами, которые могут положительно воздействовать на организм. Такое смешивание производит конечный пользователь, т.е. вводящий препарат специалист или уполномоченный персонал, согласно надлежащему способу и используя одно или несколько устройств для перемешивания, которые дают возможность получить удовлетворительную смесь и, при необходимости, сохранить ее стерильность. Например, можно упомянуть смешивание конечным пользователем гидрогеля по изобретению с одним или несколькими веществами, такими как активные субстанции, биологические организмы, либо минеральные вещества:
- попеременным извлечением материала из двух контейнеров (один наполнен гидрогелем по изобретению, а другой - веществом, которое необходимо диспергировать в гидрогеле), такими контейнерами могут быть, например, шприцы, и
- одновременным выдавливанием содержимого обоих контейнеров (один наполнен гидрогелем по изобретению, а другой - веществом, которое необходимо диспергировать в гидрогеле), чтобы соединить разные вещества и/или смешать их в еще одном контейнере перед введением пациенту.
Изобретение также относится к использованию гидрогеля, полученного описанным выше способом поперечного сшивания, в косметологических и терапевтических целях.
Положительный эффект, возможный благодаря изобретению, позволяет применять гидрогель, полученный описанным способом поперечного сшивания, в косметологических и медицинских целях, особенно в целях, уже подробно описанных в литературе, посвященной гиалуроновой кислоте (см., например, Volpi et al., Curr. Med. Chem. 2009, 16:1718-45).
Так, гидрогель по изобретению используют в косметологических (эстетических) и медицинских целях для человека или животных. Гидрогель предпочтительно имплантируют в организм пациента инъекцией, однако его также можно имплантировать и в неинъецируемой форме. В этом случае специалист помещает гидрогель в подлежащую обработке область при помощи подходящих медицинских и/или хирургических инструментов. Наконец, гидрогель может применяться наружно.
Гидрогель по изобретению используют, в частности:
- в качестве филлера,
- для создания пространств внутри определенных тканей, способствуя, тем самым, их оптимальному функционированию,
- для замены физиологических жидкостей или неполноценных тканей,
- для стимулирования или способствования регенерации тканей,
- увлажнения и защиты тканей, и
- доставки веществ, которые могут иметь положительное воздействие на организм, в частности, активных субстанций и/или биологических организмов.
В качестве примера можно упомянуть использование гидрогеля в следующих случаях:
- при приготовлении состава для интрадермальной или подкожной имплантации, для улучшения качества кожи либо заполнения морщин, либо восстановления объемов лица (скуловые кости, подбородок, губы, нос.) или тела,
- при приготовлении косметического либо космецевтического препарата, направленного на увлажнение и/или доставку в организм соединений различной природы, таких как: витамины, антиоксиданты, увлажняющие молекулы, протеины, активные субстанции, биологические организмы, красящие агенты, пигменты, молекулы пахучих веществ или ароматические молекулы.
- при приготовлении офтальмологической композиции для наружного применения, например, для длительного увлажнения роговицы глаза,
- при приготовлении стоматологической композиции для наружного применения либо имплантации, например, для заполнения пародонтальных карманов и/или для стимуляции регенерации тканей вокруг зуба,
- при приготовлении интраокулярно имплантируемой композиции, в частности для использования во время хирургических операций катаракты, глаукомы, пресбиопии или операций на стекловидном теле,
- при приготовлении внутрисуставно имплантируемой композиции для использования в ортопедии или ревматологии, в частности для восстановления вязкости или восполнения синовиальной жидкости при лечении артрозов, а также для реконструкции костей или регенерации хрящей,
- при приготовлении урологической имплантируемой композиции для использования при лечении энурезов и энкопрезов,
- при приготовлении состава композиции для наружного применения либо имплантации, используемой в медицине либо общей хирургии в рамках лечения фиброзов или для лучшего заживления ран, и
- при приготовлении состава композиции для наружного применения либо имплантирования, позволяющей осуществлять контролируемое и/или отложенное высвобождение активных веществ и/или биологических соединений для различных медицинских применений.
Краткое описание чертежей
На Фиг. 1 представлена фотография с 40-кратным увеличением поперечно-сшитой фазы С гидрогеля по изобретению.
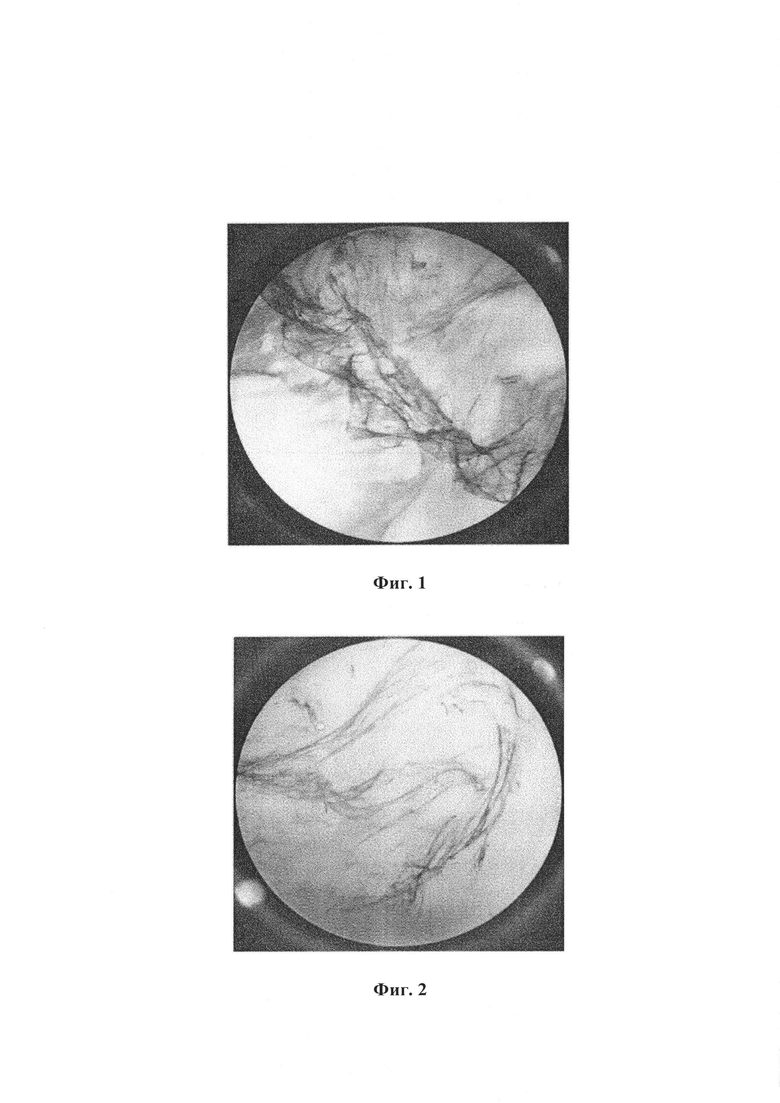
На Фиг. 2 представлена фотография с 40-кратным увеличением поперечно-сшитой фазы D гидрогеля по изобретению.
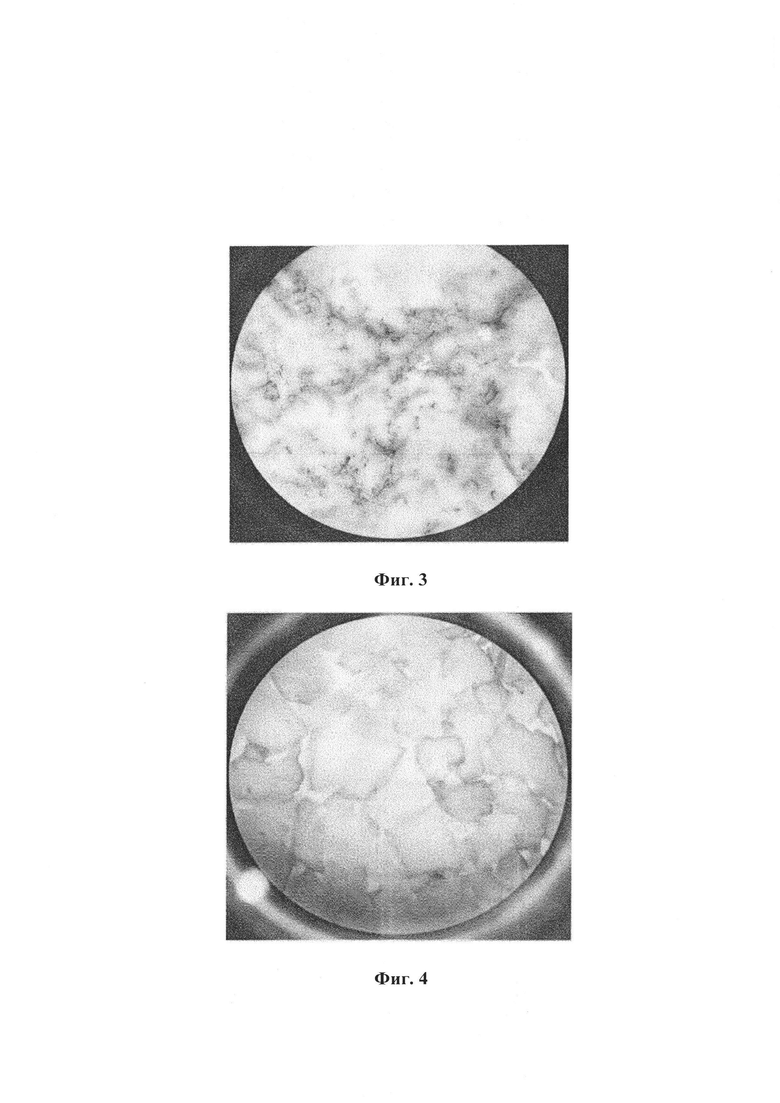
На Фиг. 3 представлена фотография с 40-кратным увеличением поперечно-сшитого продукта, полученного из частично сшитых фаз С и D гидрогеля по изобретению.
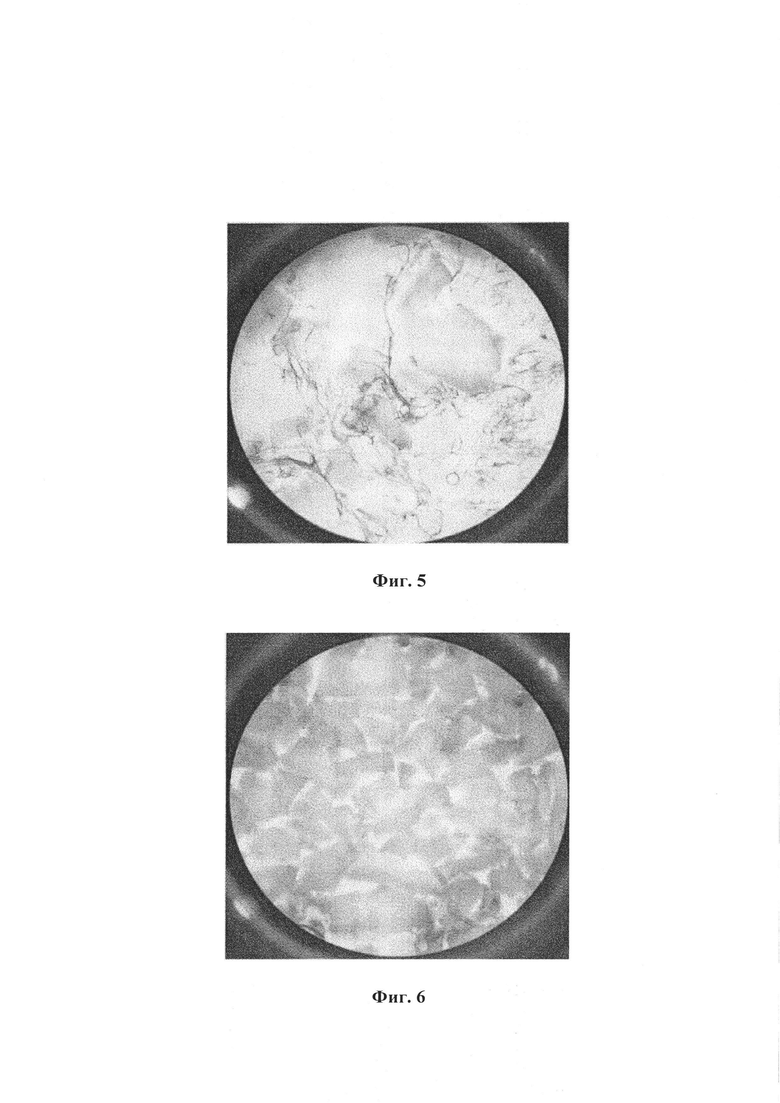
На Фиг. 4 представлена фотография с 40-кратным увеличением частиц Хр.
На Фиг. 5 представлена фотография с 40-кратным увеличением поперечно-сшитого продукта, полученного сшиванием частиц Хр.
На Фиг. 6 представлена фотография с 40-кратным увеличением частиц Yp.
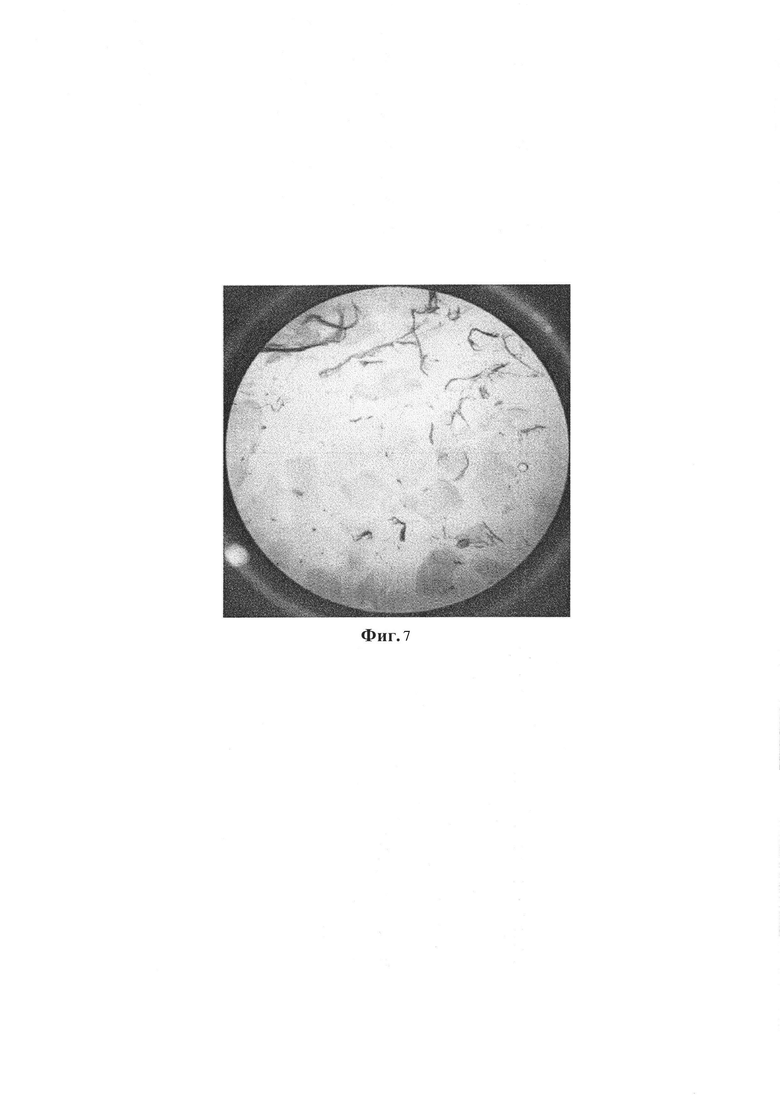
На Фиг. 7 представлена фотография с 40-кратным увеличением поперечно-сшитого продукта, полученного в результате совместного сшивания частиц Yp.
Осуществление изобретения
Настоящее изобретение не ограничивается, но может быть наглядно продемонстрировано на следующих примерах.
Гиалуронат натрия, натрий карбоксиметилцеллюлоза, лидокаина гидрохлорид, фосфокальций гидроксиапатит, а также весь спектр других соединений, используемых в примерах, имеют высокую степень очистки.
Способность к инъецированию приготовленных гелей была определена измерением требуемой силы (в Ньютонах), прилагаемой для выдавливания геля, содержащегося в стеклянном шприце емкостью 1 мл (шприц BD Hypak SCF, 1 мл RF-PRTC), через имеющуюся иглу со скоростью 12,5 мм/мин.
Реологические свойства гелей были измерены при температуре 25°С при помощи капиллярного вискозиметра AR2000 (инструментарий терапевтического направления) с использованием геометрии «плоскость-плоскость» 40 мм и зазора 1000 мкм.
Пример 1
Приготовление геля 1 по изобретению.
а) Приготовление частично сшитой фазы А
Приготовили навеску 4,7 г волокон гиалуроната натрия (NaHA) молекулярной массой около 3,0 МДа и влажностью 13,8%, к которой добавили 45,75 г 1% водного раствора NaOH (масс. %).
Гидратация волокон заняла 1 час 20 минут при регулярном ручном гомогенизировании при помощи лопатки.
К реакционной среде добавили 1,41 г раствора 1,4-бутандиол диглицидилового эфира (БДЦЭ), разбавленного в пропорции 1:5 в 1% растворе NaOH, после чего смесь гомогенизировали вручную в течение 15 мин.
Полученный таким образом гель разделили на три порции с равной массой для приготовления следующих трех фракций:
- Фракцию 1 поместили на 1 ч на термостатическую баню с температурой 30°С, а затем разбавили фосфатным буфером, содержащим HCl, доведя до концентрации NaHA 20 мг/мл и нейтрального рН (= фаза А'). Фазу А' механически гомогенизировали в течение 10 мин (= гель А').
- Фракцию 2 поместили на 2 ч на термостатическую баню с температурой 50°С, а затем разбавили фосфатным буфером, содержащим HCl, доведя до концентрации NaHA 20 мг/мл и нейтрального рН (= фаза Аʺ). Фазу Аʺ механически гомогенизировали в течение 10 мин (= гель Аʺ).
- Фракцию 3 поместили на 1 ч на термостатическую баню с температурой 30°С.
Обозначим полученную частично сшитую фазу А.
b) Приготовление частично сшитой фазы В
Приготовили навеску 5,25 г волокон гиалуроната натрия (NaHA) с молекулярной массой около 3,0 МДа и влажностью 13,8%, к которой добавили 45,75 г 1% водного раствора NaOH (масс. %).
Гидратация волокон заняла 1 час 20 минут при регулярном ручном гомогенизировании при помощи лопатки.
К реакционной среде добавили 2,73 г раствора 1,4-бутандиол-диглицидилового эфира (БДДЭ), разбавленного в пропорции 1:5 в 1% растворе NaOH, после чего смесь гомогенизировали вручную в течение 15 мин с помощью лопатки.
Полученный таким образом гель разделили на три порции с равной массой для приготовления следующих трех фракций:
- Фракцию 1 поместили на 1 ч на термостатическую баню с температурой 30°С, а затем разбавили фосфатным буфером, содержащим HCl, доводя до концентрации NaHA 20 мг/мл и нейтрального рН (= фаза В'). Фазу В' механически гомогенизировали в течение 10 мин (= гель В').
- Фракцию 2 поместили на 2 ч на термостатическую баню с температурой 50°С, а затем разбавили фосфатным буфером, содержащим HCl, доводя до концентрации NaHA 20 мг/мл и нейтрального рН (= фаза В"). Фазу В" механически гомогенизировали в течение 10 мин (= гель В").
- Фракцию 3 поместили на 1 ч на термостатическую баню с температурой 30°С.
Обозначим полученную частично сшитую фазу В.
с) Смешивание частично сшитых фаз А и В и продолжение процесса поперечного сшивания
9,0 г частично сшитой фазы А добавили к 13,0 г частично сшитой фазы В, и подвергли механическому перемешиванию в течение 15 мин при комнатной температуре перед помещением смеси на 2 часа на термостатическую баню с температурой 50°С.
Сшитый продукт нейтрализовали до рН=7,0 в фосфатном буферном растворе, содержащем HCl, где продукт был оставлен на 24 часа для набухания, после этого продукт в течение 24 часов проходил диализ в фосфатном буферном растворе с целью удаления непрореагировавшего БДДЭ.
После 10-минутной механической гомогенизации был получен гель 1 с концентрацией гиалуроната натрия, равной 20 мг/мл.
Пример 2
Исследование характеристик геля 1 из примера 1
Гели 1, А', Аʺ, В' и Вʺ поместили в стеклянные шприцы объемом 1 мл; значения усилия, необходимого для выдавливания геля через иглу 27G1/2 на скорости 12,5 мм/мин, приведены в таблице ниже.
Видно, что:
- реакция поперечного сшивания является частичной для фаз А и В. В действительности, силы выдавливания для Аʺ и Вʺ значительно выше, чем для А' и В, соответственно, что демонстрирует более высокую степень поперечного сшивания гелей Аʺ и Вʺ, чем у А' и В', и
- гель 1 по изобретению требует меньшей силы выдавливания, чем В", и, следовательно, обладает улучшенной способностью к инъецированию, чем гель, не подвергшийся поперечному сшиванию способом по изобретению.
Кроме того, были измерены реологические вязкоэластические свойства G' и Gʺ геля 1 при 1,0 Гц.
Пример 3
Приготовление геля 2 по изобретению
a) Приготовление частично-сшитой фазы С
Приготовили навеску 4,2 г порошка гиалуроната натрия (NaHA) молекулярной массой около 2,0 МДа и влажностью 6,3%, затем к нему добавили 0,3 г натрий карбоксиметилцеллюлозы (42 мПа*с, 2% в воде, при 20°С) с влажностью 2,0%, и 33,6 г 1% водного раствора NaOH (масс. %).
Гидратация порошка заняла 1 час 20 минут при регулярном ручном гомогенизировании при помощи лопатки.
Обозначим полученную гидратированную фазу Н.
К 27,0 г фазы Н добавили 1,80 г раствора 1,4-бутандиол-диглицидилового эфира (БДДЭ), разбавленного в пропорции 1:5 в 1% растворе NaOH, после чего смесь гомогенизировали вручную с помощью лопатки в течение 15 мин, а затем поместили на 1 ч 30 мин на термостатическую баню с температурой 50°С.
b) Приготовление частично сшитой фазы D
К 3,0 г фазы Н добавили 0,10 г раствора 1,4-бутандиол-диглицидилового эфира (БДДЭ), разбавленного в пропорции 1:5 в 1% растворе NaOH, после чего смесь гомогенизировали вручную с помощью лопатки в течение 15 мин, а затем поместили на 2 ч на термостатическую баню с температурой 50°С.
с) Смешивание частично сшитых фаз С и D и продолжение процесса поперечного сшивания
Частично сшитую фазу D добавили к частично сшитой фазе С, затем подвергали механическому перемешиванию в течение 15 мин при комнатной температуре перед помещением смеси на 2 ч 30 мин на термостатическую баню с температурой 50°С.
Сшитый продукт нейтрализовали до рН=7,0 в фосфатном буферном растворе, содержащем HCl, где продукт был оставлен на 24 часа для набухания, после этого продукт в течение 24 часов проходил диализ в фосфатном буферном растворе с целью удаления непрореагировавшего БДДЭ.
После 10-минутной механической гомогенизации был получен гель 2 с концентрацией гиалуроната натрия, равной 20 мг/мл.
Пример 4
Приготовление инъецируемого состава 1 по изобретению К 25% массы геля 2, полученной в примере 3, добавили 0,3 масс. % порошка гидрохлорида лидокаина, после чего смесь механическим путем гомогенизировали в течение 15 мин.
Полученный таким образом гель поместили в стеклянные шприцы объемом 1 мл, после чего шприцы в течение 20 мин стерилизовали в автоклаве при температуре 121°С.
Пример 5
Приготовление инъецируемого состава 2 по изобретению
К 25% массы геля 2, полученной в примере 3, добавили 30 масс. % порошка фосфокальциевого гидроксиапатита, размер частиц которого составляет 30-50 мкм, после чего смесь механическим путем гомогенизировали в течение 15 мин.
Полученный таким образом гель поместили в стеклянные шприцы объемом 1 мл, после этого шприцы в течение 20 мин стерилизовали в автоклаве при температуре 121°С.
Пример 6
Описание характеристик инъецируемого состава 1 по примеру 4
Было обнаружено, что стерильный состав, полученный в примере 4, является легко инъецируемым через иглу 27G1/2; усилие инъекции измеряли на скорости 12,5 мм/мин и получили значение 21,3 Н.
Значение рН и осмолярность этого состава соответствуют физиологическим:
- рН=6,9
- осмолярность=290 мОсм/кг H2O
Измерение реологических качеств показало, что модуль упругости G' равен 74 Па, 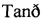 =0,25 при частоте 1,0 Гц.
=0,25 при частоте 1,0 Гц.
Важно отметить, что указанные реологические качества совместимы с инъецированием в кожу либо под кожу.
В две колбы F1 и F2 объемом по 10 мл, содержащих 8 мл очищенной воды, ввели:
- в колбу F1 - 1 мл геля Restylane® («Galderma Q-Med», г. Упсала, Швеция), Restylane® - продукт на основе поперечно-сшитой гиалуроновой кислоты в концентрации 20 мг/мл, известный в косметологической медицине уже более 10 лет, а
- в колбу F2 - 1 мл инъекционной композиции 1.
Содержимое колб F1 и F2 вручную взбалтывали в течение 5 секунд. Спустя еще 10 секунд можно было увидеть, что Restylane® полностью диссоциировал в воде (частицы поперечно-сшитой гиалуроновой кислоты взвешены в воде), чего не наблюдалось для инъекционной композиции 1, которая продолжала сохранять в воде форму геля. Таким образом, уровень когезии инъекционной композиции 1 гораздо выше, чем у Restylane®.
Пример 7
Сравнение изготовления геля по изобретению с известным уровнем техники (US 2010/0028435)
a) Приготовление геля 2 по изобретению См. пример 3.
b) Приготовление геля X, в соответствии с примером 4 заявки US 2010/0028435
Приготовили навеску 3,5 г порошка гиалуроната натрия (NaHA) молекулярной массой около 2,0 МДа и влажностью 6,3%, к которой добавили 24,0 г 1% водного раствора NaOH (масс. %).
Гидратация порошка заняла 1 час, после этого продукт в течение 10 минут гомогенизировали вручную при помощи лопатки.
К реакционной среде добавили 700 мкл БДДЭ, после чего смесь гомогенизировали вручную с помощью лопатки в течение 10 мин, а затем поместили на 2 ч на термостатическую баню с температурой 50°С.
Сшитый продукт нейтрализовали до рН=7,0 в фосфатном буферном растворе, содержащем HCl, где продукт был оставлен на 24 часа для набухания (конечный объем =92 мл).
Полученный таким образом гель был измельчен до частиц серийным пассажем через решетку 250 мкм.
Обозначим полученные частицы Хр.
Приготовили навеску 3,5 г порошка гиалуроната натрия (NaHA) молекулярной массой около 2,0 МДа и влажностью 6,3%, к которой добавили 30,5 г 1% водного раствора NaOH (масс. %).
Гидратация порошка заняла 1 час, после этого продукт в течение 10 минут гомогенизировали вручную при помощи лопатки.
К реакционной среде добавили 263 мкл БДДЭ, после чего смесь гомогенизировали вручную в течение 10 мин при помощи лопатки, а затем поместили на 2 ч на термостатическую баню с температурой 50°С.
Обозначим полученный сшитый продукт Xg.
58 г частиц Хр и 24 г 1% водного раствора NaOH добавили к поперечно-сшитому продукту Xg, после чего смесь гомогенизировали вручную в течение 10 мин при помощи лопатки, а затем поддерживали реакцию поперечного сшивания в течение 6 ч при температуре 25°С.
Сшитый продукт нейтрализовали до рН=7,0 в фосфатном буферном растворе, содержащем HCl, где продукт был оставлен на 24 часа для набухания, после этого продукт в течение 24 часов проходил диализ в фосфатном буферном растворе с целью удаления непрореагировавшего БДДЭ.
После механической гомогенизации в течение 30 мин был получен гель X.
с) Сравнение процессов изготовления геля 2 и геля X
Гель 2 и гель X поместили в стеклянные шприцы объемом 1 мл и выдавливали через иглы размером 27G1/2 (6 тестов для каждого геля / ручное выдавливание оператором). И гель 2, и гель X без усилий проходили через иглу, однако следует отметить, что гель 2 по изобретению оказался гораздо более гомогенным в шприце. Фактически, выполнявший тестирование оператор во время выдавливания отметил большое количество неравномерностей при работе с гелем X (в отличие от геля 2 по изобретению) в плане силы, с которой приходилось воздействовать на поршень шприца, охарактеризованной оператором как «надавливания». С другой стороны, из шести протестированных шприцев с гелем X содержимое двух шприцев оказалось невозможно выдавить полностью, поскольку игла была совершенно забита/перекрыта гелем (в отличие от геля 2 по изобретению).
Как уже описывалось ранее, из уровня техники известен переход поперечно-сшитого геля в гранулированное состояние для уменьшения силы выдавливания продукта и, таким образом, повышения способности к выдавливанию через иглу (сильно сшитый гидрогель измельчают до частиц малых размеров, имеющих больше шансов пройти через отверстие иглы). Было неожиданным, что гель 2 по изобретению, не подвергавшийся измельчению частично сшитых фаз (одна из которых является сильно сшитой, а вторая - менее сшитой), но имеющий сшитую фазу, полученную в результате смешивания и поперечного сшивания указанных двух частично сшитых фаз, также оказался удобным для выдавливания и гораздо более однородным. Сложная «мультиструктурированная» (без совместной поперечной сшивки) структура по изобретению позволяет решить известную из уровня техники проблему силы выдавливания, не прибегая к измельчению продукта для получения частиц.
Чтобы оценить, является ли структура геля гранулированной или нет, на образцах геля, отобранных во время приготовления геля 2 и геля X, были проведены тесты с толуидиновым синим. Для этой цели около 0,1 г тестируемого геля поместили на предметное стекло и добавили к нему 5 капель водного раствора толуидинового синего (0,1 г толуидинового синего на 100 г деионизованной воды), после чего первое предметное стекло накрыли вторым предметным стеклом. Затем визуально оценили результат под микроскопом и сделали фотографию с 40-кратным увеличением.
Были выполнены следующие цветовые тесты:
- Для геля 2: для частично сшитых фаз С и D (см. Фиг. 1 и 2) и для сшитого продукта, полученного из частично сшитых фаз С и D (см. Фиг. 3) после нейтрализации до нейтрального рН на трех образцах;
- Для геля X: для частиц Хр (см. Фиг. 4) и сшитого продукта, полученного в результате совместного поперечного сшивания частиц Хр (см. Фиг. 5), после нейтрализации до нейтрального рН на двух образцах.
В противоположность Фиг. 4 (а также Фиг. 5), где отчетливо видны поперечно-сшитые частицы NaHA, в гелевой структуре на Фиг. 1-3, относящихся к гелю 2 по изобретению, не просматриваются частицы. Отсутствие перехода частично сшитых фаз во время выполнения способа поперечного сшивания по изобретению позволяет получить гидрогель, не содержащий частиц совместно сшитого NaHa.
Это дает значительное преимущество перед продуктами, известными из уровня техники, и, в особенности, продуктами, описанными в US 2010/0028435, а также в ЕР 2011816. В действительности, как уже было описано в литературе, а также в заявках US 2010/0028435 и ЕР 2011816, поперечно-сшитые частицы вызывают возникновение побочных эффектов и осложнений как в краткосрочной, так и долгосрочной перспективе (в заявке ЕР 2011816 особо обозначено, что поперечно-сшитые частицы вызывают более или менее сильную реакцию на инородное тело). Отсутствие совместно сшитых частиц в настоящем изобретении, таким образом, является существенным усовершенствованием по сравнению с решениями, предложенными в US 2010/0028435 и ЕР 2011816, в плане профиля безопасности продукта с сохранением отличной способности к выдавливанию.
С другой стороны, важно отметить, что в заявках US 2010/0028435 и ЕР 2011816 указано, что миграция сильно сшитых частиц в организме ограничена благодаря совместному сшиванию этих частиц со слабо сшитой матрицей NaHA. Это утверждение справедливо лишь в краткосрочной перспективе, однако миграция сильно сшитых частиц становится возможной в долгосрочной перспективе после рассасывания матрицы из слабо сшитого NaHa. Последнее обстоятельство является еще одним доказательством улучшенного профиля безопасности заявленного инъецируемого гидрогеля, в котором проблема миграции совместно сшитых частиц в долгосрочной перспективе не возникает (гидрогель по изобретению не содержит совместно сшитых частиц).
Другим существенным преимуществом заявленного изобретения является улучшенная интеграция в ткани (= биоинтеграция/биоимплантация) продукта по изобретению в сравнении с продуктами, содержащими совместно сшитые частицы, известными из заявок US 2010/0028435 и ЕР 2011816. В действительности, согласно различным научным публикациям (напр., Tran С et al. In vivo bio-integration of three HA fillers in human skin: a histological study, Dermatology 2014, 228:4754; или Micheels, P. et al., Superficial dermal injection of HA soft tissue fillers: comparative ultrasound study, Dermatol. Surg. 2012, 38:1162-1169), при инъекции в кожу продуктов на основе гранулированного поперечно-сшитого NaHA (например, продуктов, описанных в заявках US 2010/0028435 и ЕР 2011816) продукты распределяются гораздо более гетерогенно по сравнению с продуктами на основе негранулированного поперечно-сшитого NaHA (как в случае с гидрогелем по изобретению).
Также необходимо отметить, что при выполнении способа приготовления гидрогеля по изобретению требуется гораздо меньше времени на изготовление продукта в сравнении со способами, описанными в US 2010/0028435 и ЕР 2011816. Наглядно демонстрирует данное утверждение тот факт, что на приготовление геля 2 по изобретению требуется около 55 ч, а на приготовление геля X по заявке US 2010/0028435 - около 85 часов. Так, настоящее изобретение обладает явным экономическим преимуществом и минимизирует опасность бактериального загрязнения геля в процессе изготовления, которая тем выше, чем дольше длится процесс изготовления.
Пример 8
Сравнение изготовления геля по изобретению с известным уровнем техники (ЕР 2011816)
a) Приготовление геля 2 по изобретению См. пример 3.
b) Приготовление геля Y, согласно примеру 1 заявки ЕР 2011816 Приготовили навеску 1,00 г порошка гиалуроната натрия (NaHA) молекулярной массой около 2,0 МДа и влажностью 6,3%, к которой добавили 6,2 г 1% водного раствора NaOH (масс. %).
Гидратация порошка заняла 1 ч 20 мин с регулярной гомогенизацией вручную при помощи лопатки.
В реакционную среду добавили 0,15 г БДДЭ, после чего смесь гомогенизировали вручную в течение 10 мин при помощи лопатки, а затем поместили на 2 ч 30 мин на термостатическую баню с температурой 50°С.
Сшитый продукт ввели в деионизированную воду на 24 часа, при этом для удаления непрореагировавшего БДДЭ были последовательно использованы три бани, каждая продолжительностью 8 часов.
Полученный таким образом гель был измельчен до частиц серийным пассажем через решетку 250 мкм, после чего частицы оставили для дренирования на 2 ч.
Обозначим полученные частицы Yp.
5,00 г частиц Yp добавили к 0,8 г порошка гиалуроната натрия (NaHA) молекулярной массой около 2,0 МДа и уровнем влажности 6,3%, а затем добавили 2,0 г 1% водного раствора NaOH (масс. %).
Смесь вручную гомогенизировали в течение 30 минут, после чего добавили 0,03 г БДДЭ и снова гомогенизировали в течение 30 минут, прежде чем поместить реакционную смесь на 2 ч 30 мин на термостатическую баню с температурой 50°С.
Обозначим полученный поперечно-сшитый продукт Yp.
Поперечно-сшитый продукт нейтрализовали до рН=7,0 в фосфатном буферном растворе, содержащем HCl, где продукт был оставлен на 24 часа для набухания, после этого продукт в течение 24 часов проходил диализ в фосфатном буферном растворе с целью удаления непрореагировавшего БДДЭ.
После ручной гомогенизации в течение 30 мин был получен гель Y.
с) Сравнение процессов изготовления геля 2 и геля Y
Как и в примере 7, гель 2 и гель Y поместили в стеклянные шприцы объемом 1 мл и выдавили через иглу размером 27G1/2. В результате было установлено, что оба геля без усилий проходят через иглу и в данном случае применимы те же замечания, что и в отношении примера 7: гель 2, изготовленный согласно изобретению, оказался гораздо более гомогенным и при выдавливании через иглу распределялся равномернее, чем гель Y. Примечательно, что гель 2 по изобретению хотя и не подвергался измельчению до частиц для облегчения выдавливания продукта, благодаря сложной «мультиструктурированной» структуре показал результат силы выдавливания, схожий с гелем Y, который прошел этап перехода сильно сшитой фазы в гранулированное состояние.
Как и в примере 7, на образцах геля, отобранных во время приготовления геля 2 и геля Y, были проведены тесты с толуидиновым синим.
Были выполнены следующие цветовые тесты:
- Для геля 2: для частично сшитых фаз С и D (см. Фиг. 1 и 2) и для поперечно-сшитого продукта, полученного из частично сшитых фаз С и D (см. Фиг. 3) после нейтрализации до нейтрального рН на трех образцах;
- Для геля Y: для частиц Yp (см. Фиг. 6) и поперечно-сшитого продукта, полученного в результате совместного поперечного сшивания частиц Yp (см. Фиг. 7), после нейтрализации до нейтрального рН на двух образцах.
Результаты испытаний аналогичны результатам примера 7. В противоположность Фиг. 6 (а также Фиг. 7), на которой отчетливо видны поперечно-сшитые частицы NaHA, в гелевой структуре на Фиг. 1-3, на которых приведен гель 2 по изобретению, частицы не просматриваются.
Таким образом, настоящее изобретение позволяет получить легко инъецируемый гидрогель, несмотря на то, что он не подвергается измельчению (частично или полностью) для образования частиц во время процесса поперечного сшивания. Так, благодаря отсутствию совместных сшитых частиц в геле достигается значительное усовершенствование по сравнению с гелем, полученным по ЕР 2011816:
- улучшен профиль безопасности в краткосрочной и долгосрочной перспективе, в частности, в долгосрочной перспективе не происходит миграция сильно сшитых частиц, как в заявке ЕР 2011816;
- улучшена биоинтеграция геля в ткани (более равномерное распределение) в силу отсутствия совместных сшитых частиц.
И наконец, аналогично примеру 7, необходимо отметить, что изобретение обладает явным экономическим преимуществом и позволяет минимизировать опасность бактериального загрязнения благодаря значительно более короткой продолжительности процесса изготовления, чем описанная в заявке ЕР 2011816 (около 55 часов на изготовление геля по изобретению, в сравнении с 83 часами, необходимыми для изготовления геля в соответствии с заявкой ЕР 2011816), и, в отличие от ЕР 2011816, не требует выполнения одного либо нескольких трудоемких этапов измельчения.
Группа изобретений относится к косметологии и медицине. Способ поперечного сшивания гиалуроновой кислоты или ее производного включает приготовление первой водной фазы частично сшитой гиалуроновой кислоты с использованием сшивающего агента, которая не конвертирована в частицы; приготовление по меньшей мере одной второй водной фазы частично сшитой гиалуроновой кислоты с использованием сшивающего агента, которая не конвертирована в частицы; где вторая фаза имеет степень частичного сшивания, отличную от степени сшивания первой фазы; добавление второй фазы к первой фазе и затем перемешивание указанных фаз, где массы первой и второй фаз в смеси равны или отличаются; продолжение реакции поперечного сшивания смеси путем управления температурой и продолжительностью реакции, при этом способ поперечного сшивания осуществляют без добавления частиц сшитой гиалуроновой кислоты. Также раскрыт инъецируемый гидрогель, способ его приготовления и его применение для приготовления композиции косметического, космецевтического и терапевтического назначения. Группа изобретений обеспечивает вязкоэластичный гидрогель с оптимизированной реманентностью. 6 н. и 15 з.п. ф-лы, 7 ил., 1 табл., 8 пр.
1. Способ поперечного сшивания гиалуроновой кислоты, или одной из ее физиологически приемлемых солей, или ее физиологически приемлемого производного, представляющего собой молекулу, полученную модификацией молекулы гиалуроновой кислоты химическим путем, который включает в себя по меньшей мере следующие этапы:
a) приготовление первой водной фазы частично сшитой гиалуроновой кислоты с использованием сшивающего агента, причем полученная первая водная фаза частично сшитой гиалуроновой кислоты не конвертирована в частицы;
b) приготовление по меньшей мере одной второй водной фазы частично сшитой гиалуроновой кислоты с использованием сшивающего агента, причем полученная по меньшей мере одна вторая водная фаза частично сшитой гиалуроновой кислоты не конвертирована в частицы;
где указанная вторая фаза имеет степень частичного сшивания, отличную от степени сшивания указанной первой водной фазы;
c) добавление указанной по меньшей мере одной второй фазы с этапа b) к первой фазе с этапа а) и затем перемешивание указанных по меньшей мере двух фаз, где соответствующие массы первой и второй фаз в смеси равны или отличаются; и
d) продолжение реакции поперечного сшивания смеси, полученной на этапе с), путем управления температурой и продолжительностью реакции,
при этом способ поперечного сшивания осуществляют без добавления частиц сшитой гиалуроновой кислоты во время выполнения этапов а, b, с и d.
2. Способ по п. 1, в котором сшивание гиалуроновой кислоты осуществляют с другим сшиваемым полисахаридом, причем:
на этапе а) первую водную фазу частично сшитой гиалуроновой кислоты готовят с добавлением другого сшиваемого полисахарида; и
на этапе b) по меньшей мере одну вторую водную фазу частично сшитых гиалуроновой кислоты готовят с добавлением другого сшиваемого полисахарида.
3. Способ по п.. 1 или 2, в котором на этапе с) при получении смеси указанных по меньшей мере двух фаз добавляют дополнительное количество сшивающего агента.
4. Способ по п. 1 или 2, в котором указанная вторая фаза имеет степень частичного сшивания больше, чем указанная первая водная фаза, и/или в котором концентрация гиалуроновой кислоты для приготовления второй фазы выше или равна концентрации гиалуроновой кислоты для приготовления первой фазы.
5. Способ по п.. 1 или 2, в котором количество сшивающего агента, используемое для приготовления второй фазы, больше или равно количеству сшивающего агента, используемому для приготовления первой фазы, и/или в котором температура поперечного сшивания при приготовлении второй фазы выше или равна температуре поперечного сшивания при приготовлении первой фазы, а температура поперечного сшивания для смеси выше температуры поперечного сшивания для второй фазы на этапе b).
6. Способ по п. 1 или 2, в котором продолжительность поперечного сшивания для второй фазы на этапе b) больше или равна продолжительности поперечного сшивания первой фазы на этапе а).
7. Способ по п.. 1 или 2, в котором поперечное сшивание смеси останавливают, разбавляя смесь водным раствором и/или удаляя непрореагировавший сшивающий агент путем выполнения очистки диализом.
8. Способ по п.. 1 или 2, в котором реакции поперечного сшивания осуществляют за счет действия одного или нескольких полифункциональных сшивающих агентов, выбранных из группы би- или полифункциональных эпоксидных смол, дивинилсульфонов, карбодиимидов или формальдегидов, предпочтительно 1,4-бутандиол-диглицидилового эфира (БДДЭ).
9. Способ по п. 1 или 2, в котором в качестве физиологически приемлемых солей гиалуроновой кислоты используют натриевые, кальциевые, цинковые или калиевые соли.
10. Способ по п. 1 или 2, в котором гиалуроновая кислота или одна из ее физиологически приемлемых солей имеет молекулярную массу в диапазоне 0,1-4 млн Да.
11. Способ приготовления инъецируемого гидрогеля, который включает в себя по меньшей мере следующие последовательные этапы:
- поперечное сшивание гиалуроновой кислоты или одной из ее физиологически приемлемых солей способом согласно любому из пп. 1-10,
- очистку смеси изотоническим раствором с приемлемым рН,
- гомогенизацию смеси,
- помещение в шприц, флакон или любой другой герметичный контейнер, и
- стерилизацию.
12. Способ по п. 11, в котором после гомогенизации смеси и перед ее помещением в контейнер смесь подвергают вакуумированию и/или лиофилизации.
13. Способ по п. 11 или 12, в котором смесь гомогенизируют с добавлением одного или нескольких других сшиваемых полисахаридов.
14. Гидрогель, полученный способом по любому из пп. 11-13, состоящий, по меньшей мере, из поперечно-сшитой гиалуроновой кислоты или одной из ее физиологически приемлемых солей, который представляет собой смесь нескольких фаз поперечно-сшитой гиалуроновой кислоты с разной степенью сшивания, где указанные фазы связаны друг с другом ковалентными связями.
15. Гидрогель по п. 14, состоящий, по меньшей мере, из поперечно-сшитой гиалуроновой кислоты или одной из ее физиологически приемлемых солей, или других сшиваемых полисахаридов, который представляет собой смесь нескольких фаз поперечно-сшитой гиалуроновой кислоты с разной степенью сшивания, где указанные фазы связаны друг с другом ковалентными связями.
16. Гидрогель по п. 14 или 15, в котором общая концентрация гиалуроновой кислоты или одной из ее солей составляет от 0,01 до 50 мг/мл.
17. Гидрогель по п. 14 или 15, который содержит одно или несколько активных веществ, обладающих или не обладающих фармакологическим действием, выбранных из группы, включающей в себя антиоксиданты, противовоспалительные вещества, антисептики, антибактериальные вещества, противогрибковые вещества, противоопухолевые вещества, протеины, гормоны, местные обезболивающие как по отдельности, так и в комбинациях.
18. Гидрогель по п. 14 или 15, который содержит лидокаин, диспергированный в поперечно-сшитой матрице гиалуроновой кислоты, и/или одно или несколько минеральных веществ, диспергированных в поперечно-сшитой матрице гиалуроновой кислоты.
19. Применение гидрогеля по любому из пп. 14-18 для приготовления композиции косметического назначения, такой как интрадермально или подкожно имплантируемая композиция для улучшения качества кожи, или для заполнения морщин, или для восстановления объемов лица.
20. Применение гидрогеля по любому из пп. 14-18 для разработки состава космецевтической композиции.
21. Применение гидрогеля по любому из пп. 14-18 для разработки состава композиции терапевтического назначения, такой как наружная или интраокулярная композиция для применения в офтальмологии; наружная или имплантируемая композиция для применения в стоматологии; внутрисуставная композиция для использования в ортопедии и ревматологии; имплантируемая композиция в урологии и для применения при лечении недержаний; наружная или имплантируемая композиция, используемая в медицине или общей хирургии в рамках лечения фиброзов или для улучшения заживления ран; наружная или имплантируемая фармацевтическая композиция, позволяющая осуществлять контролируемое и/или отложенное высвобождение активных веществ для различных медицинских применений.
| US 4716154 A, 29.12.87 | |||
| ПОПЕРЕЧНО СШИТЫЕ ПОЛИСАХАРИДНЫЕ И БЕЛКОВЫЕ МАТРИЦЫ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2006 |
|
RU2472809C2 |
Авторы
Даты
2019-03-27—Публикация
2014-06-10—Подача