ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к области терапии мастита, в частности на основе пробиотиков.
УРОВЕНЬ ТЕХНИКИ, ПРЕДШЕСТВУЮЩИЙ ИЗОБРЕТЕНИЮ
Мастит представляет собой воспаление или инфекцию ткани молочной железы или вымени, и его можно классифицировать как послеродовой и непослеродовой мастит. Послеродовой мастит связан с беременностью, грудным вскармливанием или отнятием от груди и часто возникает у лактирующих млекопитающих, как у животных, так и у людей. Непослеродовой мастит не имеет никакого отношения к лактации, но имеет очень сходные симптомы и может возникать, например, после пирсинга соска. По оценкам до 33% лактирующих женщин страдают маститом. Хотя мастит может возникать в любой момент во время лактации с пиком частоты возникновения во время второй и третьей недели послеродового периода. Большинство случаев мастита вызывает инфекция Staphylococcus, в основном S. aureus и S. epidermidis. Лечение часто включает введение антибиотиков. Мастит является крайне не желательным, т.к. во время мастита изменяется композиция грудного молока, например, повышенное содержание натрия и медиаторов воспаления, которые могут препятствовать оптимальному питанию, которое обеспечивает грудное молоко для ребенка. Кроме того, во время мастита продолжение грудного вскармливания может оказаться невозможным или может являться нежелательным для матери.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В настоящее время неожиданно было обнаружено, что штамм Lactobacillus salivarius, обозначаемый как PS2, или композиция, содержащая PS2 Lactobacillus salivarius, эффективно снижает мастит и/или симптомы, связанные с маститом. Штамм PS2 Lactobacillus salivarius был депонирован, и ему присвоен номер доступа LMG P-27027.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к новому штамму Lactobacillus salivarius, композициям, содержащим этот новый штамм и к способу лечения и/или профилактики воспаления и/или инфекции в ткани молочной железы или вымени, в частности мастита.
В первом аспекте изобретение относится к штамму Lactobacillus salivarius, обладающему по меньшей мере 80% идентичностью последовательности со штаммом с номером доступа LMG P-27027.
Во втором аспекте изобретение относится к композиции, содержащей штамм Lactobacillus salivarius по изобретению и физиологически приемлемый носитель или эксципиент. Предпочтительно композиция содержит 108 до 1010 КОЕ Lactobacillus salivarius на грамм сухой массы. Предпочтительно композиция дополнительно содержит по меньшей мере один, выбранный из группы трудноусваиваемых олигосахаридов, LC-PUFA, дополнительных пробиотиков и питательных микроэлементов. Предпочтительно композиция представляет собой порошок.
В третьем аспекте настоящее изобретение относится к применению штамма Lactobacillus salivarius по изобретению для получения лекарственного средства. Другими словами, изобретение относится к штамму Lactobacillus salivarius по изобретению для применения в качестве лекарственного средства. Другими словами, изобретение относится к способу профилактики и/или лечения заболевание, включающему введение нуждающемуся в этом индивидууму штамма Lactobacillus salivarius по изобретению.
В четвертом аспекте настоящее изобретение относится к применению композиции по изобретению для получения лекарственного средства. Другими словами, изобретение относится к композиции по изобретению для применения в качестве лекарственного средства. Другими словами, изобретение относится к способу профилактики и/или лечения заболевания, включающему введение нуждающемуся в этом индивидууму композиции по изобретению.
В пятом аспекте настоящее изобретение относится к применению штамма Lactobacillus salivarius по изобретению для получения композиции для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего. Другими словами, изобретение относится к штамму Lactobacillus salivarius по изобретению для применения в лечении и/или профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего. Другими словами, изобретение относится к способу лечения и/или профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего, включающему введение нуждающемуся в этом индивидууму штамма Lactobacillus salivarius по изобретению. Предпочтительно воспаление и/или инфекция ткани молочной железы или вымени представляет собой мастит. Предпочтительно млекопитающее представляет собой человека женского пола. Предпочтительно штамм Lactobacillus salivarius по изобретению вводят более одного раза в сутки, более предпочтительно два или три раза в сутки, наиболее предпочтительно три раза в сутки в дозе от 108 до 1010 колониеобразующих единиц (КОЕ) в дозе.
В шестом аспекте настоящее изобретение относится к применению композиции по изобретению для получения композиции для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего. Другими словами, изобретение относится к композиции по изобретению для применения в лечении и/или профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего. Другими словами, изобретение относится к способу лечения и/или профилактики воспаление и/или инфекция ткани молочной железы или вымени у млекопитающего, включающему введение нуждающемуся в этом индивидууму композиции по изобретению. Предпочтительно воспаление и/или инфекция ткани молочной железы или вымени представляет собой мастит. Предпочтительно млекопитающее представляет собой человека женского пола. В одном из вариантов осуществления человек женского пола подвергается риску, в частности высокому риску развития мастита, и композиция по изобретению предназначена для профилактики мастита у человека женского пола, подвергающегося риску, в частности высокому риску, развития мастита. Соответственно, человек женского пола ранее страдал воспалением и/или инфекцией ткани молочной железы или вымени, в частности маститом. Предпочтительно композицию по изобретению вводят более одного раза в сутки, более предпочтительно два или три раза в сутки, наиболее предпочтительно три раза в сутки, в дозе от 108 до 1010 колониеобразующих единиц (КОЕ) в дозе. Предпочтительно композиция дополнительно содержит по меньшей мере один выбранный из группы трудноусваиваемых олигосахаридов, LC-PUFA, дополнительных пробиотиков и питательных микроэлементов.
Lactobacillus salivarius
Штамм Lactobacillus salivarius по изобретению обозначают как PS2 Lactobacillus salivarius или PS2 L. salivarius. PS2 L. salivarius был депонирован Danone Research BV, Bosrandweg 20, 6704 PH Wageningen, Нидерланды в соответствии с Будапештским договором о международном признании депонирования микроорганизмов для целей процедуры выдачи патентов в BCCM/LMG (Belgian Coordinated Collections of Microorganisms, Laboratorium voor Microbiologie - Bacteriënverzameling (LMG), University of Gent, K.L. Ledeganckstraat 35, B-9000 Gent, Belgium) 23 мая 2012 г. PS2 L. salivarius был присвоен номер доступа BCCM/LMG LMG P-27027. Депозитор Danone Research BV дал разрешение заявителю ссылаться на депонированный биологический материал в этой патентной заявка. Ниже в настоящем описании PS2 L. salivarius также обозначают как LMG P-27027 Lactobacillus salivarius или LMG P-27027 L. salivarius.
Настоящее изобретение также относится к штаммам L. salivarius, обладающим по меньшей мере 80% идентичностью с последовательностью рРНК 16S штамма LMG P-27027 L. salivarius, предпочтительно по меньшей мере 85% идентичностью, более предпочтительно по меньшей мере 90% идентичностью, наиболее предпочтительно по меньшей мере 95% идентичностью (см.: Stackebrandt & Goebel, 1994, Int. J. Syst. Bacteriol. 44:846-849). В предпочтительном варианте осуществления штамм по настоящему изобретению обладает по меньшей мере 97% идентичностью с последовательностью рРНК 16S штамма LMG P-27027 L. salivarius, более предпочтиетьльно по меньшей мере 98% идентичностью, более предпочтительно по меньшей мере 99% идентичностью. В другом предпочтительном варианте осуществления штамм по настоящему изобретению обладает 100% идентичностью с последовательностью рРНК 16S LMG P-27027 L. salivarius. Другими словами, в предпочтительном варианте осуществления штамм по настоящему изобретению представляет собой штамм LMG P-27027 Lactobacillus salivarius.
Композиция
Предпочтительно настоящий штамм L. salivarius содержится в композиции, такой как пищевая композиция, пищевая добавка, фармацевтическая композиция или нутрицевтическая композиция, предпочтительно пищевая композиции или пищевая добавка. Предпочтительно настоящая композиция содержит штамм L. salivarius и физиологически приемлемый носитель или эксципиент и/или дополнительные ингредиенты, как дополнительно описано ниже. Предпочтительно штамм L. salivarius по изобретению находится в лиофилизированной форме.
Композиция по изобретению предпочтительно содержит от 102 до 1013 колониеобразующих единиц (КОЕ) настоящего штамма L. salivarius на грамм сухой массы композиции, предпочтительно от 104 до 1012, более предпочтительно от 105 до 1011, наиболее предпочтительно от 105 до 1010 КОЕ L. salivarius на грамм сухой массы композиции. Штамм L. salivarius по изобретению предпочтительно вводят в суточной дозе от 102 до 1013, более предпочтительно от 105 до 1012, более предпочтительно от 108 до 5×1010, наиболее предпочтительно от 108 до 1010 колониеобразующих единиц (КОЕ). Композиция по изобретению может содержать жизнеспособные и/или нежизнеспособные L. salivarius по изобретению, предпочтительно жизнеспособные L. salivarius по изобретению.
Настоящая композиция, содержащая штамм L. salivarius, может находиться в любой известной в данной области форме, такой как в твердой форме, в полутвердой форме или в жидкой форме. Предпочтительно композиция представляет собой питательную композицию или питательную добавку, предпочтительно в форме порошка, капсулы или таблетки, наиболее предпочтительно пищевой добавки. Подходящие пищевые композиции включают любой напиток или пищевой продукт, такой как питье, молочный напиток, йогурт, молочный продукт, хлебопродукт, продукт на основе сои, продукт на основе фруктов, продукт на основе овощей, мясопродукт или их сочетания, например, основное блюдо. В предпочтительном варианте осуществления композиция представляет собой пищевую добавку в форме порошка, капсулы или таблетки, наиболее предпочтительно в форме порошка. Предпочтительно композиция содержит штамм L. salivarius в лиофилизированной форме, которая является особенно подходящей, когда композиция находится в форме порошка, капсулы или таблетки. Настоящий штамм или настоящая композиция могут содержаться в контейнере, предпочтительно карандаше или пакетированной порционной форме или саше. Предпочтительно настоящая композиция, когда находится в форме порошка, капсулы или таблетки, особенно когда находится в форме порошка, предназначена для добавления в напиток или пищевой продукт перед приемом внутрь. Предпочтительно к настоящей композиции, когда она находится в форме порошка, капсулы или таблетки, особенно когда находится в форме порошка, прилагаются инструкции по добавлению композиции к напитку или пищевому продукту перед приемом внутрь. Напиток или пищевой продукт, к которому настоящую композицию необходимо добавлять, может представлять собой любой напиток или пищевой продукт, такой как питье, молочный напиток, йогурт, молочный продукт, хлебопродукт, продукт на основе сои, продукт на основе фруктов, продукт на основе овощей, мясопродукт или их сочетания, например, основное блюдо.
Дополнительные компоненты
Штамм L. salivarius по изобретению предпочтительно содержится в композиции, которая может содержать физиологически приемлемый носитель или эксципиент и/или дополнительные ингредиенты. Можно использовать любой физиологически приемлемый эксципиент или носитель, который известен в данной области. Подходящие эксципиенты или носители включают, но не ограничиваются ими, воду, глюкозу, лактозу, сахарозу, маннит, мальтодекстрин, (устойчивый) крахмал, целлюлозу или производные целлюлозы, например, метилцеллюлозу, стеарат магния, стеариновую кислоту, сахарин натрия, тальк, карбонат магния и т.п.
Предпочтительно вводят дополнительные ингредиенты, которые являются благоприятными для лактирующих женщин, более предпочтительно ингредиенты, которые являются благоприятными для иммунной системы и/или поддерживают иммунную систему. Такие ингредиенты, как правило, известны в данной области и включают, но не ограничиваются ими, пищевое волокно и трудноусваиваемые олигосахариды, LC-PUFA и питательные микроэлементы (например, витамины и минералы). В композицию изобретению также можно вводить макропитательные вещества (например, липиды, белок, усваиваемые углеводы).
Трудноусваиваемый олигосахарид
Настоящий штамм предпочтительно содержится в композиции, которая дополнительно содержит трудноусваиваемые олигосахариды. Термин "трудноусваиваемые", как используют в настоящем изобретении, относится к сахаридам, которые не расщепляются в кишечнике под действием кислот или пищеварительных ферментов, содержащихся в верхнем отделе желудочно-кишечного тракта (тонком кишечнике и желудке) человека, но который ферментируется кишечной флорой человека. Моно- и дисахариды, такие как глюкоза, галактоза, фруктоза, сахароза и лактоза являются усваиваемыми.
Предпочтительно настоящая композиция содержит трудноусваиваемые олигосахариды со степенью полимеризации (DP) от 2 до 250, более предпочтительно от 3 до 60. Предпочтительно трудноусваиваемые олигосахариды содержат по меньшей мере один олигосахарид, выбранный из группы из фруктоолигосахаридов (таких как инулин), галактоолигосахаридов (таких как транс-галактоолигосахариды или бета-галактоолигосахариды), глюкоолигосахариды (такие как гентио-, нигеро- и циклодекстринолигосахариды), арабиноолигосахариды, маннанолигосахариды, ксилоолигосахариды, фукоолигосахариды, арабиногалактоолигосахариды, глюкоманноолигосахариды, галактоманноолигосахариды, содержащие сиаловые кислоты олигосахариды и содержащие уроновые кислоты олигосахариды, более предпочтительно выбранные из группы из фруктоолигосахаридов, галактоолигосахаридов и содержащих уроновые кислоты олигосахаридов, наиболее предпочтительно выбранные из группы из фруктоолигосахаридов и галактоолигосахаридов. Предпочтительно композиция содержит галактоолигосахариды, более предпочтительно транс-галактоолигосахариды. В предпочтительном варианте осуществления композиция содержит смесь галактоолигосахаридов и фруктоолигосахаридов.
Предпочтительно галактоолигосахариды имеют от 2 до 10. Предпочтительно галактоолигосахариды имеют среднюю DP ниже 6. Галактоолигосахарид предпочтительно выбирают из группы, состоящей из транс-галактоолигосахаридов, лакто-N-тетраозы (LNT), лакто-N-неотетраозы (нео-LNT), фукозиллактозы, фукозилированной LNT и фукозилированной нео-LNT. Транс-галактоолигосахариды (TOS) продаются, например, под товарным знаком Vivinal™ (Borculo Domo Ingredients, Netherlands). Предпочтительно сахариды транс-галактоолигосахаридов являются β-связанными. Фруктоолигосахарид предпочтительно имеет DP от 2 до 250, более предпочтительно от 2 до 100, наиболее предпочтительно от 5 до 60. Предпочтительно фруктоолигосахариды имеют среднюю DP более 10. Фруктоолигосахариды включают инулин, леван и/или смешанный тип полифруктана. Особенно предпочтительный фруктоолигосахарид представляет собой инулин. Пригодный для использования в композициях фруктоолигосахарид является коммерчески доступным, например, как Raftiline®HP (Orafti). Предпочтительно настоящая композиция содержит галактоолигосахариды и фруктоолигосахариды в массовом отношении галактоолигосахариды:фруктоолигосахариды от 99: 1 до 1:99, более предпочтительно от 20:1 до 1:1, наиболее предпочтительно от 12:1 до 7:1.
В другом предпочтительном варианте осуществления композиция содержит смесь короткоцепочечных и длинноцепочечных фруктоолигосахаридов. Предпочтительно смесь фруктоолигосахаридов со средней DP менее 10 и фруктоолигосахаридоы со средней DP более 10. Фруктоолигосахарид со средней DP менее 10, пригодный для использования в композициях, является коммерчески доступным, например, как Raftilose®. Фруктоолигосахарид со средней DP более 10, пригодный для использования в композициях, является коммерчески доступным, например, как Raftiline®HP. Предпочтительно настоящая композиция содержит фруктоолигосахариды со средней DP менее 10 и фруктоолигосахариды со средней DP более 10 в массовом отношении от 20:1 до 1:20, более предпочтительно от 10:1 до 1:10, наиболее предпочтительно от 5:1 до 1:5 или в отношении приблизительно 1:1.
Предпочтительно композиция содержит от 0,25% масс. до 50% масс. трудноусваиваемых олигосахаридов, более предпочтительно от 0,5% масс. до 30% масс., даже более предпочтительно от 1,0% масс. до 20% масс. трудноусваиваемых олигосахаридов в пересчете на сухую массу. В случае жидкой формы композиция предпочтительно содержит от 50 мг до 5 г трудноусваиваемых олигосахаридов на 100 мл, более предпочтительно от 250 мг до 2 г, даже более предпочтительно от 500 мг до 1 г на 100 мл. Выраженное в терминах дозирования содержание трудноусваиваемых олигосахаридов составляет предпочтительно от 0,1 до 50 г в сутки, более предпочтительно от 1 до 35 г в сутки, даже более предпочтительно от 5 до 25 г в сутки, наиболее предпочтительно от 10 до 20 г в сутки.
Длинноцепочечные полиненасыщенные жирные кислоты (LC-PUFA)
Предпочтительно настоящая композиция дополнительно содержит длинноцепочечные полиненасыщенные жирные кислоты и/или длинноцепочечные полиненасыщенные жирные ацильные цепи (LC-PUFA). Термин LC-PUFA в настоящем изобретении относится к жирной кислоте или жирной ацильной цепи длиной 20 атомов углерода или более и по меньшей мере с двумя ненасыщенными связями. Предпочтительно композиция содержит LC-PUFA, выбранную из группы, состоящей из эйкозапентаеновых кислот и/или ацильной цепи (EPA), докозагексаеновой кислоты и/или ацильной цепи (DHA) и арахидоновой кислоты и/или ацильной цепи (AA). В одном из вариантов осуществления композиция содержит DHA. В другом варианте осуществления композиция содержит EPA. Более предпочтительно композиция содержит DHA и EPA. LC-PUFA преимущественно укрепляет иммунную систему. Таким образом, введение композиции, содержащей пищевое волокно и LC-PUFA, лактирующим женщинам будет оказывать улучшенный действие на иммунную систему.
Предпочтительно композиция содержит 5от 0 до 3000 мг LC-PUFA в суточной дозе, более предпочтительно от 100 до 1500 мг, наиболее предпочтительно от 200 до 700 мг.
Питательные микроэлементы
Предпочтительно настоящий штамм содержится в композиции, которая дополнительно содержит питательные микроэлементы, более предпочтительно витамины и минералы. Предпочтительные питательные микроэлементы представляют собой такие, которые являются благоприятными для лактирующих женщин, в частности такие, которые являются благоприятными для иммунной системы и/или поддерживают иммунную систему. Такие ингредиенты, как правило, известны в данной области и, как правило, включают добавки, предназначенные для лактирующих женщин или молодых матерей. Введение витаминов и минералов в настоящую композицию подходящим способом снижает количество композиций или добавок, которые необходимо принимать лактирующим женщинам.
Предпочтительные витамины представляют собой водорастворимые витамины; витамин B1 (тиамин), витамин B2 (рибофлавин), витамин B3 (ниацин), витамин B5 (пантотеновую кислоту), витамин B6 (пиридоксин), фолиевую кислоту, витамин B12 (цианокобаламин), биотин, холин и витамин C, и жирорастворимые витамины; витамин D3, витамин E и витамин K. Наиболее предпочтительные витамины представляют собой фолиевую кислоту, витамин B1, витамин B2, витамин B6, витамин B12, холин и витамин C.
Предпочтительные минералы представляют собой кальций, фосфор, цинк, йод, железо, марганец, селен, медь и магний. Наиболее предпочтительные минералы представляют собой кальций, йод, цинк и железо.
Дополнительные пробиотики
Композиция по изобретению наряду с настоящим штаммом of L. salivarius, как описано выше, может содержать дополнительные пробиотики.
Пробиотики в настоящем изобретении относятся к микроорганизмам, которые при введении оказывают положительное действие на хозяина. Пробиотики оказывают положительное действие на иммунную систему лактирующих женщин, таким образом, комбинация с пробиотиками будет оказывать лучшее действие на иммунную систему. Предпочтительно пробиотики выбраны из группы, состоящей из Lactobacillus и Bifidobacterium. Более предпочтительно пробиотик выбран из группы, состоящей из группы Lactobacillus accidophilus, L. rhamnosus, L. casei, L. paracasei, L. plantarum, L. reuteri, L. fermentum, Bifidobacterium infantis, B. animalis subsp. lactis, B. breve, B. longum и B. bifidum. Предпочтительно пробиотики содержаться в суточной дозе от 1×106 колониеобразующих единиц (КОЕ) до 1×1013 КОЕ, более предпочтительно от 1×107 до 1×1011, наиболее предпочтительно от 1×108 до 1×1010 каждого отдельного пробиотика.
В предпочтительном варианте осуществления композиция содержит только один штамм активный для лечения и/или профилактики мастита, т.е. штамм L. salivarius по изобретению. В одном из вариантов осуществления композиция не содержит штамм Lactobacillus gasseri.
Макропитательные вещества
Настоящая композиция также может содержать по меньшей мере один, предпочтительно по меньшей мере два, более предпочтительно по меньшей мере три макропитательных вещества, выбранных из белка, жира и усваиваемого углевода. Это является особенно предпочтительным в случае если штамм по изобретению содержится в пищевой композиции. В предпочтительном варианте осуществления настоящие пищевые композиции содержат по меньшей мере один, выбранный из группы трудноусваиваемых олигосахаридов, LC-PUFA, дополнительных пробиотиков и питательных микроэлементов, как описано выше.
Применение
Настоящий штамм и/или композиция является подходящей в качестве лекарственного средства, в частности для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего, более конкретно для лечения и/или профилактики мастита и/или симптомов, связанных с маститом. Предпочтительно настоящий штамм и/или композиция является особенно подходящей для лечения воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего, особенно для лечения мастита и/или симптомов, связанных с маститом. В одном из вариантов осуществления предпочтительно настоящий штамм и/или композиция является особенно подходящей для профилактики воспаления и/или инфекции ткани молочной железы или вымени у млекопитающего, особенно для профилактики мастита и/или симптомов, связанных с маститом. В контексте настоящего изобретения "профилактику" также можно формулировать как "снижение риска возникновения". Как используют в настоящем описании, фраза "лечение и/или профилактика мастита и/или болей в молочной железе, и других симптомов, связанных с маститом" (и аналогичных) включает уменьшение продолжительности периода времени, в течение которого индивидуум страдает маститом, снижение уровня боли, испытываемой индивидуумом, страдающим маститом, уменьшение времени выздоровления индивидуума, страдающего маститом, уменьшение периода времени (при наличии), в течение которого индивидуум прекращает грудное вскармливание своего грудного ребенка вследствие мастита, снижение риска того, что индивидуум выбирает прекращение грудного вскармливания вследствие мастита, увеличение периода времени, в течение которого индивидуум кормит грудью своего грудного ребенка и/или снижение риска того, что индивидуум прекращает грудное вскармливание своего грудного ребенка вследствие мастита.
Мастит, подлежащий лечению и/или профилактике, может являться послеродовым или непослеродовым, предпочтительно мастит является послеродовым. Связанные с маститом, симптомы включают (местную) боль в молочной железе, покраснение, набухание, нагрубание молочной железы и прилив жара молочной железы(з), застой молока, лихорадку, гриппоподобные симптомы и развитие абсцесса молочной железы. Настоящий штамм и/или композицию можно вводить женщине, которая страдает маститом, или женщине, которая подвергается риску, предпочтительно высокому риску, развития мастита. Женщины, подвергающиеся высокому риску развития мастита, включают, но не ограничиваются ими, женщин, у которых вырабатывается молоко или у которых будет вырабатываться молоко и которые имеют болезненные или потрескавшиеся соски, которые страдали маститом ранее (например, вовремя кормления грудью другого ребенка), которые проводят кормление грудью с нерегулярными интервалами времени, которые принимают или которые недавно принимали антибиотики (от другой инфекции), которые страдают диабетом, хроническим заболеванием, инфекцией ВИЧ, СПИД или нарушением иммунной системы. В одном из вариантов осуществления настоящий штамм и/или композицию необходимо вводить женщине, которая страдала маститом ранее. В контексте настоящего изобретения, "женщины" и "человек женского рода" используют взаимозаменяемо.
Настоящий штамм и/или композицию можно вводить женщине, которая планирует начать кормление грудью в течение нескольких недель (например, за четыре недели до планируемого начала кормления грудью), кормит грудью или недавно прекратила кормление грудью. Особенно предпочтительно вводить настоящий штамм и/или композиция до тех пор, пока симптомы мастита сохраняются, или более предпочтительно до тех пор, пока продолжается лактация. В некоторых вариантах осуществления настоящий штамм и/или композицию можно вводить женщине в последний триместр беременности (т.е. перед тем, как они начинают кормить грудью своего ребенка), в первые недели после родов или до тех пор, пока продолжается лактация. Соответственно, настоящий штамм и/или композицию можно вводить женщине начиная с 29 недели ее беременности, с 30 недели, с 31 недели, с 32 недели, с 32 недели, с 33 недели, с 34 недели, с 35 недели, с 36 недели, с 37 недели, с 38 недели, с 39 недели, с 40 недели, с 41 недели, с 42 недели, с рождения или с любого момента времени после родов во то время, как продолжается лактация до или после того, как любые симптомы мастита становятся очевидными и в дальнейшем.
Способ введения
Используемую в настоящем способе композицию предпочтительно вводят энтерально, более предпочтительно перорально. Композицию по изобретению можно вводить в однократной суточной дозе или в многократных доз в сутки, таких как по меньшей мере 2 дозы в сутки, по меньшей мере 3 дозы в сутки, по меньшей мере 4 дозы в сутки. Предпочтительно композицию по изобретению вводят более одного раза в сутки. В особенно предпочтительном варианте осуществления композицию по изобретению вводят в 2 или 3 дозах в сутки, наиболее предпочтительно в 3 дозах в сутки. В предпочтительном варианте осуществления композиция по изобретению представляет собой пищевую композицию или пищевую добавку. Добавка по изобретению может находиться в форме порошка, таблетки (включая жевательную таблетку) или капсулы. Пищевая композиция по изобретению может представлять собой любой пищевой продукт или напиток. Предпочтительно композиция, особенно пищевая добавка, по изобретению дополнительно содержит физиологически приемлемый эксципиент или носитель. В предпочтительном варианте осуществления композиция или добавка представляет собой порошок, упакованный в контейнер (предпочтительно саше), содержащий от 1 до 10 г, более предпочтительно от 1,5 до 7 г, наиболее предпочтительно от 2 до 5 г. Предпочтительно каждый контейнер содержит однократную дозу.
Предпочтительно пищевая композиция представляет собой жидкость на основе молока, содержащую жиры, белки и усваиваемые углеводы. Предпочтительно такую жидкость на основе молока упаковывают в бутылку или треугольные пакеты объемом от 50 до 1000 мл, более предпочтительно от 60 до 500, наиболее предпочтительно от 75 до 125 мл.
Предпочтительно композиция представляет собой порошок, упакованный контейнер, предпочтительно саше, содержащее от 1 до 10 г, более предпочтительно от 1,5 до 7 г, наиболее предпочтительно от 2 до 5 г.
В этом документе и в формуле изобретения глагол "содержать" и его спряжения используют в его неограничивающем смысле для обозначения того, что объект после слова является включенным, но объект, не упоминающийся конкретно, не исключают. Кроме того, описание элемента в форме единственного числа не исключает возможности того, что более чем один элемент присутствуют, если из контекста явно не следует, что присутствует один и только один из элементов. Таким образом, формы единственного числа, как правило, означают "по меньшей мере один".
ОПИСАНИЕ ЧЕРТЕЖЕЙ
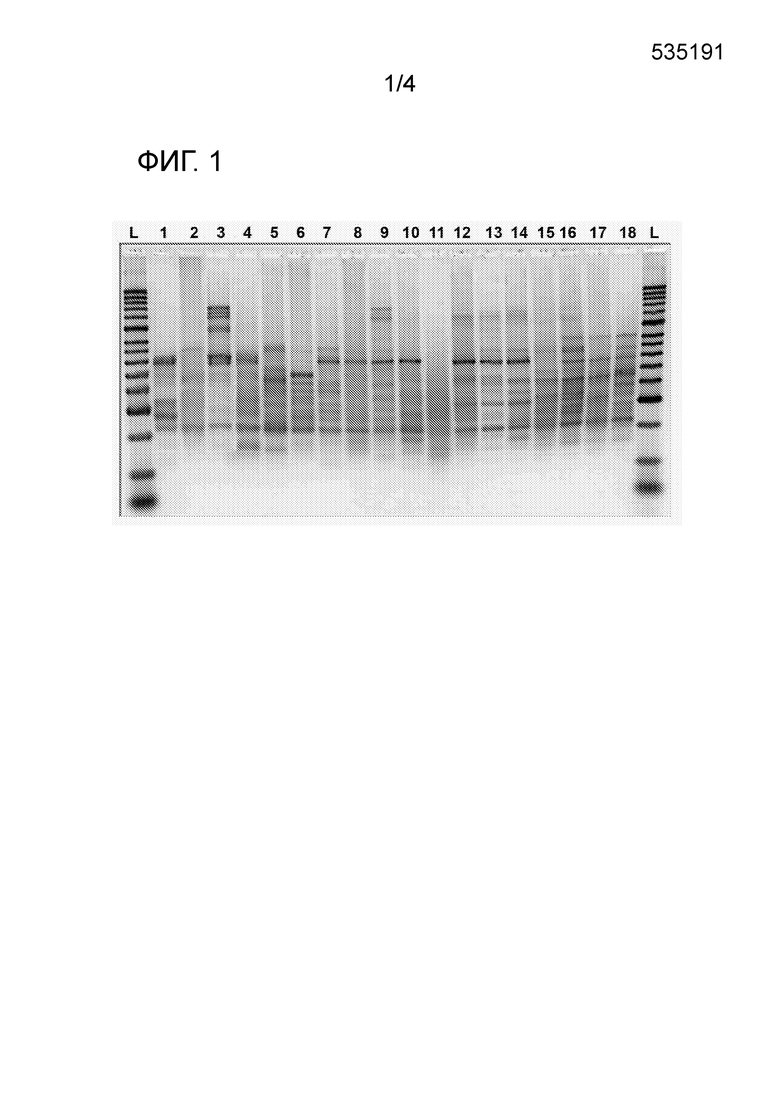
На фигуре 1 представлен анализ RAPD 18 различных штаммов Lactobacillus salivarius. Дорожки соответствуют: (1) ZH17-05; (2) CELA-2; (3) PS2; (4) CECT 5713; (5) CTC 2197; (6) FI 9810; (7) FI 9789; (8) CECT 4062; (9) CECT 4063; (10) V3-III-1; (11) V4-II-90; (12) V7-II-1; (13) V7-II-62; (14) V7-IV-1; (15) V7-IV-60; (16) V8-III-62; (17) V11-I-60; (18) V11-III-60; (L) HyperLadder™ II (50 п.о. - 2000 п.о.) (Bioline).
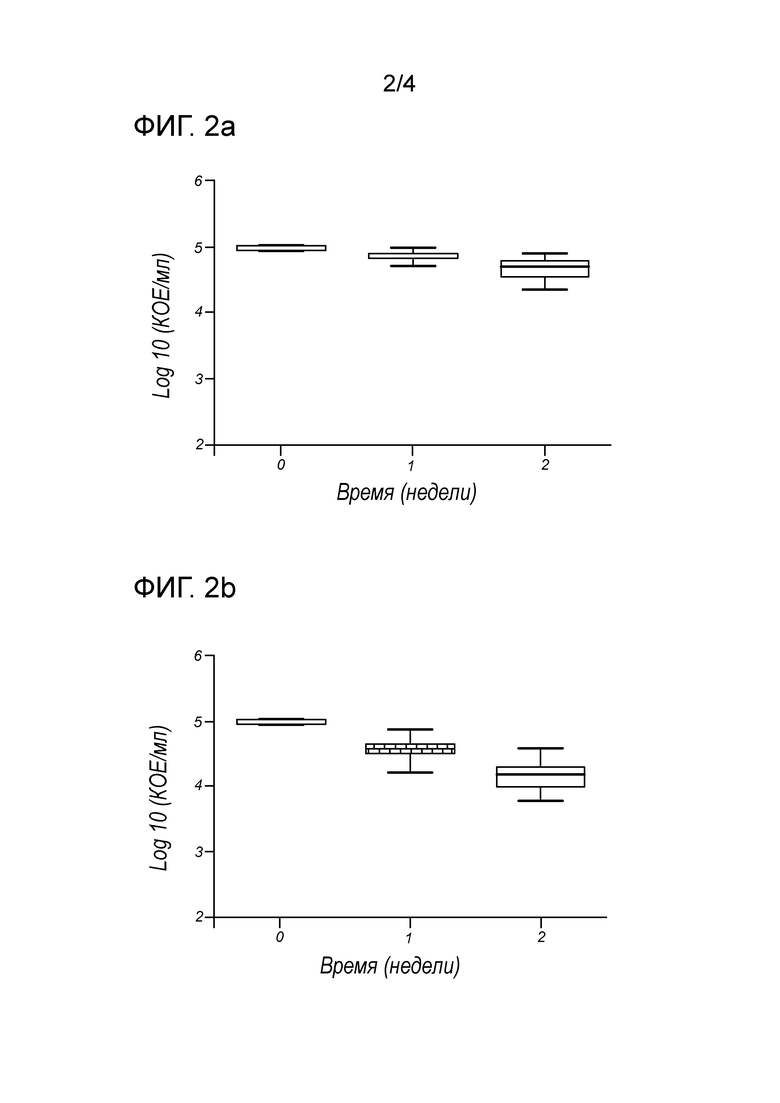
На фигуре 2 представлены диаграммы размаха общего содержания бактерий в образцах грудного молока, получаемых в клиническом испытании примера 2, на сутки 0, сутки 7 и сутки 14; фигура 2a=группа лечения 1, фигура 2b=группа лечения 2, фигура 2c=группа лечения 3, фигура 2d=группа сравнения.
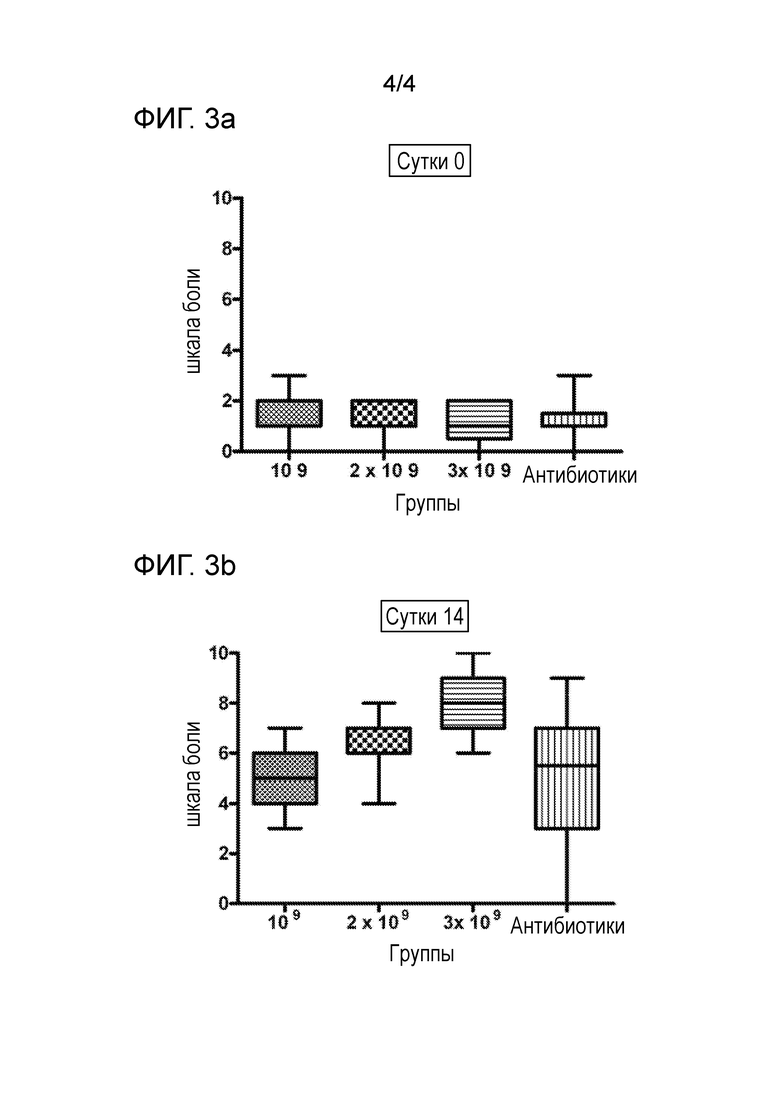
На фигуре 3 представлены диаграммы размаха оценок выраженности боли в баллах, получаемых в клиническом испытании примера 2, на сутки 0 (фигура 3a) и на сутки 14 (фигура 3b).
ПРИМЕРЫ
Пример 1: Анализ случайным образом амплифицированной полиморфной ДНК (RAPD)
Всего 28 штаммов Lactobacillus salivarius подвергали анализу случайным образом амплифицированной полиморфной ДНК (RAPD). Профили RAPD получали с использованием праймера OPL5 (5'-ACGCAGGCAC-3') (Veyrat A., Miralles M.C. and Perez-Martinez G.A. в J. Appl. Microbiol. 1999, 87:49-61). Компьютерный анализ проводили с использованием программного обеспечения InfoQuest FP (Bio-Rad Laboratories, Inc., Hercules, CA).
28 анализируемых штаммов включали одиннадцать штаммов, выделенных из молока человека (PS2; HN6; FN74M1; LA105 Te-1; WN70 M1; AP141 Me-2; AP141 Me-11; TM142 M1; TA143 Ma-1; TA143 Te-1; MV144 M1), один штамм, выделенный из кала грудных детей (ZH17-05), один штамм, выделенный из молока свиньи (CELA-2), один штамм, выделенный у домашней птицы (CTC 2197), десять штаммов, получаемых из выделений из влагалища человека (V3-III-1; V4-II-90; V7-II-1; V7-II-62; V7-IV-1; V7-IV-60; V8-III-62; V11-I-60; V11-III-60; V11-IV-60), пять штаммов из известных коллекций (FI 9810; FI 9789; CECT 4062; CECT 4063; CECT 5713).
Анализ выявлял, что профиль RAPD Lactobacillus salivarius PS2 (дорожка 3) отличался от профилей других штаммов, исследуемых в этом примере, см. фигура 1 для выбранного сравнения (другие профили RPAD не показаны).
Arroyo et al. в Clin. Infect. Dis. 2010, 50(12), 1551-1558 описывают использование бактериального штамма CECT5713 Lactobacillus salivarius для лечения мастита. Было продемонстрировано, что штамм PS2 Lactobacillus salivarius, который является целью настоящего изобретение, имеет профиль RAPD отличный от штамма CECT5713, а также обладает улучшенными свойствами по сравнению со штаммом CECT5713, такими как повышенная стабильность и отсутствие профагов в его геноме (Langa et al., в Appl. Microbiol. Biotechnol. 2012, 94, 1279-87).
Пример 2: Клиническое испытание I - лечение мастита
Способы. Проводили открытое исследование в целом со 108 лактирующими женщинами с симптомами мастита. Все они соответствовали следующим ниже критериям: воспаление молочной железы, болезненное грудное вскармливание, содержание бактерий в молоке >1×104 КОЕ/мл. Лактирующие женщины получали 1 (группа лечения 1, n=25), 2 (группа лечения 2, n=25) или 3 (группа лечения 3, n=25) капсулы, содержащие лиофилизированную добавку на основе пробиотиков, содержащую 1×109 КОЕ L. salivarius PS2 на г в сутки в течение 14 суток. Группа сравнения (n=33) получала лечение антибиотиком в течение 14 суток, как назначено их центрах первичной медицинской помощи. Ни один из индивидуумов не принимал внутрь коммерческие пробиотические пищевые продукты или добавки во время исследования. Женщины с абсцессом молочной железы, синдромом Рейно или любой другой патологией молочной железы исключали.
Образцы грудного молока отбирали до начала введения добавки или лечения (сутки 0) и каждую неделю до конца исследования (сутки 7 и сутки 14). Акушерки оценивали развитие симптомов в одни и те же моменты времени в их центрах первичной медицинской помощи; добровольцев просили оценить в баллах их боль в молочной железе от 0 (очень болезненно) до 10 (боль отсутствует).
Содержание бактерий измеряли в образцах молока так, как указано ниже. Образцы распределяли на чашках с агаром Baird-Parker, Columbia, Mac-Conkey и Sabouraud с декстрозой и хлорамфениколом для селективного выделения и количественного определения основных агентов, вовлеченных в инфекционный мастит, и параллельно на чашки MRS (Oxoid) с агаром, дополненные L-цистеином (0,5 г/л) (MRS-Cys) для выделения лактобактерий. Чашки инкубировали в течение 48 часов при 37°C в аэробных условиях, за исключением чашек MRS-Cys, которые инкубировали в анаэробных условиях.
Бактерии, выделенные из молока, сначала идентифицировали на уровне видов классическими морфологическими и биохимическими тестами. Идентификацию бактерий, принадлежащих к видам S. epidermidis или S. aureus, подтверждали способом мультиплексной полимеразной цепной реакции (ПЦР) на основе генов dnaJ. Идентификацию стрептококков проводили частичной амплификацией и секвенированием гена tuf. Оставшиеся изоляты идентифицировали секвенированием рРНК 16S. Их идентичность определяли на основании наиболее высоких баллов (>99%) среди последовательностей, депонированных в базе данных Европейской лаборатории по молекулярной биологии.
Идентификацию PS2 L. salivarius в образцах молока проводили анализом гибридизации ДНК-ДНК колоний. Для этой цели конструировали 2 видоспецифичных зонда на основе уникальных последовательностей рРНК 16S. Колонии, получаемые на чашках MRS-Cys, из образцов молока (сутки 14) точечно переносили в правильном расположении на 2 группы в чашки MRS-Cys методом отпечатков. Затем нейлоновые диски Hybond-N+ (GE Healthcare) укладывали непосредственно на поверхности культур и удерживали на них в течение 1 минуты. Гибридизацию и детекцию проводили, как описано ранее (Jimenez et al. в Appl. Environ. Microbiol. 2008, 74: 4650-4655). Идентичность изолятов, которые давали положительный сигнал после гибридизации колоний, подтверждали секвенированием рРНК 16S, как описано выше, и проводили генотипирование в гель-электрофорезе в пульсирующем поле (PFGE), как описано ранее (Jimenez et al., 2008). Их профили сравнивали с профилями CECT4062 L. salivarius, CECT4063 L. salivarius, DSM 20492 L. salivarius и CECT5713 L. salivarius.
Статистический анализ. Перед статистическим анализом микробиологические данные, записанные как число КОЕ на мл молока, трансформировали в логарифмические величины. Приводимые значения содержаний бактерий представляют собой средние значения определений в двух или трех повторениях. Непрерывные переменные "содержания бактерий" и "оценка выраженности боли в молочной железе в баллах" не имели нормального распределения. Использовали критерий Манна-Уитни для определения статистически значимых отличий между содержаниями бактерий (общих и основных видов бактерий) и между оценками выраженности боли в молочной железе в баллах в различные моменты времени испытания.
Содержания бактерий в образцах молока. На сутки 0 средние значения общего содержания бактерий в молоке являлись очень схожими в 4 группах и находились в диапазоне от 8,5 до 1,2×104 КОЕ/мл (таблица 1). На сутки 7 средние значения общего содержания бактерий в группах лечения 2 и 3, получавших 2 или 3 дозы в сутки, являлась значительно ниже (p<0,001), чем соответствующее значение в группе лечения 1, получавшей одну дозу в сутки. Этот параметр не анализировали в группе сравнения на 7 сутки. На сутки 14 средние значения общего содержания бактерий в группе сравнения имели тенденцию быть значимо меньшими, чем в группе лечения 1. Однако группы лечения 2 и 3 имели значительно меньшие средние значения общего содержания бактерий, чем группа сравнения, см. таблицу 1 и фигуру 2.
Среднее общее содержание бактерий (TBC) в группах лечения и сравнения
Развитие клинических симптомов. Средняя оценка в баллах выраженности боли в молочной железе, указываемые женщинами, являлась одинаковой на сутки 0 в 4 группах в диапазоне от 0 до 3, см. таблицу 2 и фигуру 3a. На сутки 14 оценка выраженности боли в молочной железе в баллах улучшалась у большинства участниц. Наблюдали статистически значимые отличия (p<0,001) между оценками выраженности боли в молочной железе в баллах в группе лечения 2 и 3, получавшей 2 и 3 дозы в сутки (средняя оценка в баллах 6,5 и 8,2 соответственно) и оценкой выраженности боли в молочной железе в баллах в группе лечения 1 (средняя оценка в баллах 4,08 и 5,03, соответственно) на сутки 14, см. таблицу 2 и фигуру 3b.
Средние оценки выраженности боли в молочной железе в баллах (BPS) в группах лечения и сравнения
Заключение. Эти результаты указывают на то, что добавление PS2 L. salivarius приводило к сниженному содержанию бактерий в грудном молоке и улучшению клинических симптомов (оценка выраженности боли в баллах) женщин, страдающих маститом. Результаты, получаемые с одной суточной дозой 109 КОЕ/мл PS2 L. salivarius, являются сравнимыми с результатами, получаемыми с антибиотиками, при этом две или три суточные дозы 109 КОЕ/мл PS2 L. salivarius явно работает лучше, чем регулярное лечение антибиотиками. Добавление двух или трех доз, в частности трех доз, этого штамма в сутки приводило к значительно большему снижению содержания бактерий по сравнению со стандартным лечением антибиотиком.
Пример 3: Клиническое испытание II - профилактика мастита у индивидуумов, подвергающихся высокому риску
Способы. Проводили рандомизированное, двойное слепое, плацебо-контролируемое интервенционное исследование проводили всего с 108 здоровыми беременными женщинами в возрасте 25-35 лет, которые готовились кормить грудью своих грудных детей. Все женщины соответствовали следующим ниже критериям: нормальная беременность, нормальное состояние здоровья и наличие в анамнезе лактационного мастита по меньшей мере после предшествующей беременности. Индивидуумов распределили случайным образом в группу тестирования (n=55) и группу плацебо (n=53). Группа тестирования принимала внутрь 1 саше, содержавшее лиофилизированную пробиотическую порошкообразную добавку, содержащую 1×109 КОЕ PS2 L. salivarius на г в сутки, и группа плацебо принимала внутрь 1 саше, содержащее добавку-плацебо, с 30-й недели беременности до 12 недель после родов. Ни один из индивидуумов не принимал внутрь коммерческие пробиотические пищевые продукты или добавки во время третьего триметра беременности и во время исследования. Женщин, принимавших коммерческие пробиотические пищевые продукты или добавки или получавших лечение антибиотиком в предшествующие 30 суток, и женщин с аллергией на белок коровьего молока или непереносимостью лактозы и женщин с абсцессом молочной железы, синдромом Рейно или любой другой патологией молочной железы исключали.
Симптомы мастита оценивали акушерки центров первичного здоровья во время первых 3 месяцев после рождения. Согласно последним критериям классификации инфекционного мастита [Fernández et al., Benef. Microbes. 2014, 5(2), 169-83] "острый мастит" определяли как острое воспаление молочной железы с местными (глотание с жадностью, боль, покраснение, сниженная секреция) и общими (гриппоподобными) симптомами, при этом "подострый мастит" определяли как воспаление молочной железы, характеризующееся наличием местным симптомов (глотание с жадностью, иглоподобная и/или жгучая боль, сниженная секреция) и отсутствием общих симптомов. Оба определения только включают такие случаи, связанные с высоким содержанием бактерий в молоке (>103 КОЕ/мл), определяемым как объясняется ниже, и высоким содержанием лейкоцитов (>104 клеток/мл). Количественное определение лейкоцитов проводили оптической микроскопией после дифференциального окрашивания по Май-Грюнвальду-Гимзе.
При возникновении мастита добровольцев просили оценить в баллах ощущение боли в своей молочной железе от 0 (очень болезненно) до 10 (боль отсутствует) в соответствии со стандартным способом оценки боли [Jensen and Karoly, Handbook of Pain Assessment, 2nd edition, New York: Guilford Press, 2001, pp 15-34; Jensen, Pain assessment in clinical trials. В H. Wittink and D. Carr (eds.), Pain Management: Evidence, Outcomes, and Quality of life. Amsterdam: Elsevier, 2008].
Образцы грудного молока (10 мл) собирали между 91 и 100 сутками после рождения в случае женщин, которые не страдали маститом в течение 3 месяцев периода последующего наблюдения. В случае женщин, которые страдали таким состоянием, образец молока собирали непосредственно после диагностики. Содержание бактерий в образцах молока измеряют так, как указано ниже. Образцы распределяют на чашках с агаром Baird-Parker, Columbia, Mac-Conkey и Sabouraud с декстрозой и хлорамфениколом для селективного выделения и количественного определения основных агентов, вовлеченных в инфекционный мастит и параллельно на чашках MRS (Oxoid) с агаром (Oxoid), дополненным L-цистеином (0,5 г/л) (MRS-Cys), для выделения лактобактерий. Чашки инкубируют в течение 48 часов при 37°C в аэробных условиях, за исключением чашек MRS-Cys, которые инкубируют в анаэробных условиях. Выделяемые из молока бактерии сначала идентифицируют на уровне видов классическими морфологическими и биохимическими тестами. После подсчета бактерий идентифицировали характерных представителей колоний каждого морфологического типа посредством MALDI-TOF точечным нанесением части бактериальной колонии (~1 мкл) на планшет для образца MALDI. Затем его покрывали 1 мкл насыщенного раствора α-циано-4-гидроксикоричной кислоты в ацетонитриле (28%) и оставляли сушиться при комнатной температуре. Для каждого изолята конструировали средний спектр по меньшей мере с 50 профилями спектра масса/заряд и использовали для идентификации путем сравнения со спектрами, содержащимися в базе данных Myla (Biomerieux). Идентификацию определяли как 99-100% совпадение с видоспецифичными значениями масса/заряд в базе данных.
Статистический анализ. Перед статистическим анализом микробиологические данные, записываемые как число КОЕ на мл молока, трансформировали в логарифмические величины. Непрерывные переменные выражали в виде среднего значения и 95% доверительного интервала (CI) средних значений после проверки на нормальное распределение. После апостериорного критерия Бонферрони использовали однофакторный дисперсионный анализ для сравнения возраста и времени начала (неделя беременности) исследования между группами пробиотиков и плацебо и для проверки эффекта введения пробиотика и типа мастита (подострый и острый) в оценках выраженности боли в молочной железе в баллах. Двухфакторный дисперсионный анализ использовали для исследования эффекта лечения и состояния здоровья молочной железы на содержание стафилококков/стрептококков, а также эффекта лечения и тип мастита на оценку выраженности боли в молочной железе в баллах и для исследования возможности взаимодействия двух исследуемых переменных. Количественные отношения сравнивали с использованием критерия χ2 или критерия точной вероятности Фишера при необходимости. Проводили корреляционный анализ для исследования взаимосвязи между содержанием стафилококков/стрептококков в грудном молоке и оценки выраженности боли в молочной железе в баллах. Статистическую значимость устанавливали при P<0,05.
Результаты. Не наблюдали значимого отличия между группой пробиотика и плацебо относительно возраста (среднее значение: 31,18 лет, 95% CI: 30,70-31,66 для группы пробиотика и среднее значение: 30,51 лет, 95% CI: 30,02-31,00 для группы плацебо; P=0,1699, однофакторный дисперсионный анализ) и недели беременности (среднее значение: 29,82 недели, 95% CI: 29,49-30,15 для группы пробиотика и среднее значение: 30,06 недели, 95% CI: 29,74-30,37 для контрольной группы; P=0,2953, однофакторный дисперсионный анализ) в начале исследования. На всем протяжении исследования не сообщали о нежелательных или побочны эффектах/явлениях, связанных приемом внутрь пробиотика.
Частоту возникновения мастита оценивали в течение первых 3 месяцев после родов. В целом 44 женщины из 108 (59,26%) страдали маститом; 77,27% случаев классифицировали как подострый, при этом острые случаи составляли оставшиеся 22,73%. Результаты частоты возникновения (подострого или острого) мастита в первые три месяца после родов представлены в таблице 3, а также среднее значение общего содержания бактерий (TBC) в грудном молоке и оценки выраженности боли в молочной железе в баллах (BPS). Статистически значимые отличия выявляли между группой пробиотика и контроля в отношении частоты мастита. Процент женщин, страдающих маститом в группе пробиотика являлся значительно ниже, чем в контрольной группе (P=0,0010, критерий χ2). Не выявляли значимых отличий между группой женщин, которые получали PS2 L. salivarius во время своей беременности, и контрольной группой, которая получала плацебо относительно типа мастита. В группе пробиотика частоты подострого и острого мастита составляли 79% и 21% соответственно, тогда как в контрольной группе эти проценты составляли 77% и 23% соответственно (P=1,000, критерий точной вероятности Фишера).
Среднее содержание бактерий в образцах молока, получаемых от всех участниц, составляло 2,63×103 КОЕ/мл (95% CI: 1,74×103-3,98×103). Употребление пробиотика или плацебо и состояние здоровья молочной железы (здоровая, подострый мастит или острый мастит) оказывало достоверный эффект (P=0,000 для обоих основных факторов, двухфакторный дисперсионный анализ) на содержание бактерий, детектируемых в грудном молоке. Кроме того, взаимосвязь между этими двумя факторами также являлась значимой (P=0,000, двухфакторный дисперсионный анализ), что указывает на то, что среднее содержание бактерий, выявляемое в грудном молоке от здоровых женщин и женщины с маститом, сильно зависело от лечения пробиотиком.
Когда содержание бактерий, регистрируемых в образцах молока от здоровых женщины, которые получали пробиотик (n=41), сравнивали со значениями здоровых женщин, входящих в контрольную группу, получавшую плацебо (n=23), наблюдали небольшое, но значимое отличие (P=0,0005, t-критерий). Различия, наблюдаемые между группами по содержанию бактерий молока, получаемого от женщин с подострым и острым маститом, являлись выше: среднее содержание бактерий в группах пробиотика и подострого (n=11) и острого (n=3) мастита составляло 6,76×103 КОЕ/мл и 6,17×103 КОЕ/мл соответственно, тогда как среднее содержание бактерий в группах плацебо и подострого (n=23) и острого (n=7) мастита достигало 4,07×104 КОЕ/мл подострого (n=11) и 1,05×105 КОЕ/мл соответственно (P=0,0001 и 0,0064 соответственно, t-критерий) (таблица 3). Не выявляли значимых отличий, когда содержание бактерий в образцах грудного молока, получаемых в случаях подострого мастита, сравнивали с содержание бактерий в случаях острого мастита в обеих группах пробиотика (P=0,770, t-критерий) или плацебо (P=0,0939, t-критерий).
Результаты клинического испытания II
(n=53)
[a] среднее значение и 95% доверительный интервал в 103 КОЕ/мл; [b] критерий χ2; [c] критерий точной вероятности Фишера; [d] t-критерий; [e] однофакторный дисперсионный анализ.
Большая часть участниц страдала маститом (43 из 44) оценивали степень выраженности боли в своей молочной железе от 0 до 4 по шкале в диапазоне от 0 (очень болезненно) до 10 (боль отсутствует). Наблюдали сильную корреляцию между сообщаемыми BPS и содержанием бактерий, выявляемых в молоке (r=-0,814, P=0,000, корреляция смешанных моментов Пирсона). Двухфакторный дисперсионный анализ, с использованием которого сравнивали все наблюдения, регистрируемые для боли в молочной железе, сообщаемые женщинами-участницами с маститом, демонстрировал, что употребление PS2 L. salivarius оказывало значительное влияние на степень выраженности боли в отличие от типа мастита (таблица 8). Более высокие значения BPS, указывают на менее выраженную боль, описывали у женщины в группе пробиотика (n=13) по сравнению с женщинами в группе плацебо (n=30). Как правило, тип мастита не вызывал значимых отличий в оценке выраженности боли в молочной железе в баллах (среднее значение BPS=1,97; 95% CI:1,50-2,44 у 33 женщин с подострым маститом в сравнении со средним значением BPS=1,30; 95% CI:0,40-2,20 у 10 женщины с острым маститом; P=0,1663, однофакторный дисперсионный анализ). Среди всех женщины с маститом, женщин, сообщающих о том, что они испытывали более выраженную боль в молочной железе (более низкий BPS), чаще всего выявляли в группе плацебо, чем в группе пробиотика (P=0,0327, критерий χ2). Фактически все женщины (n=9), которые указывали на то, что чувствуют сильную боль в своей молочной железе (BPS=0), не принимали PS2 L. salivarius и входили в группу плацебо.
Заключение. Введение PS2 L. salivarius приводит к значительному снижению частоты возникновения мастита, общего содержания бактерий материнского молока (для здоровых женщин, женщин, страдающих подострым и острым маститом) и оценок выраженности боли в молочной железе в баллах женщин, страдающих маститом, даже для целевой группы женщин, подвергающихся высокому риску развития мастита. Таким образом, штамм по изобретению способен оказывать профилактическое действие в отношении мастита.
Пример 4: Клиническое испытание III - лечение мастита
Способы. В исследовании участвовало всего 23 женщины с симптомами мастита. Все они соответствовали следующим ниже критериям: воспаление молочной железы, болезненное кормление грудью, содержание стафилококков/стрептококков в молоке >3 log10 колониеобразующих единиц (КОЕ)/мл и содержание лейкоцитов в молоке >4 log10 клеток/мл. Все индивидуумы ежесуточно употребляли ~9,5 log10 КОЕ PS2 Lactobacillus salivarius в течение 21 суток. Ни один из индивидуумов не принимал внутрь коммерческие пробиотические пищевые продукты или добавки во время исследования. Женщин с абсцессом молочной железы, синдром Рейно или любой другой патологией молочной железы исключали.
Мастит симптомы оценивали на сутки 0 и 21 акушерки центров первичного здоровья. Образцы грудного молока, крови и мочи получали в начала и в конце исследования. Образцы молока (30 мл) собирали в диапазоне 7-9 часов утра и по меньшей мере через 2 часа после последнего кормления. Первые 2 мл собирали посредством ручного сцеживания для микробиологического анализа и определения содержания соматических клеток, тогда как оставшееся молоко получали с использованием молокоотсоса для биохимического и иммунологического анализов. Первую фракцию объемом 22 мл образцов крови собирали в пробирки с Na-гепарином для анализа состава жирных кислот (FA) клеточной фракции и связанных с окислительным стрессом (OS) параметров в плазме. Вторую фракцию объемом 8 мл собирали в пробирки с ЭДТА для стандартного общего анализа крови и иммунологического анализа. Последние 4 мл использовали для получения сыворотки для стандартного биохимического анализа крови и количественного определения высокочувствительного C-реактивного белка (hs-CRP). Для стандартного анализа мочи собирали первую утреннюю мочу (плотность, pH, белки, глюкоза, кетоновые тела, нитриты, уробилиноген, эритроциты и лейкоциты).
Содержание бактерий измеряли в образцах молока так, как указано ниже. Образцы распределяли на чашках с агаром Baird-Parker, Columbia, Mac-Conkey и Sabouraud с декстрозой и хлорамфениколом и инкубировали в течение 48 часов при 37°C в аэробных условиях для селективного выделения и количественного определения основных агентов, вовлеченных в инфекционный мастит. После определения содержания бактерий идентифицировали характерных представителей колоний каждого морфологического типа посредством MALDI-TOF. Использовали образцы свежего молока для определения содержания соматических клеток (SCC) с использованием автоматического устройство для подсчета клеток. Анализ подпопуляций соматических клеток проводили оптической микроскопией после дифференциального окрашивания по Май-Грюнвальду-Гимзе свежего молока. Анализ проводили в двух повторениях два разных наблюдателя, и для каждого образца подсчитывали минимальное количество 100 клеток. Концентрации жира, белка, лактозы, общих твердых веществ и обезжиренных твердых веществ (NFS) образцов молока определяли с использованием устройства MilkoScan Minor, предварительно откалиброванного и утвержденного для анализа молока человека. Концентрации натрия, калия и хлорида определяли в образцах обезжиренного молока с использованием ионоселективного электрода на анализаторе Spotlyte. После оттаивания к 0,5 мл каждого образца молока добавляли 0,5 мл 40 мМ раствора NaCl. Каждое измерение повторяли три раза.
Жирные кислоты (FA), содержащиеся в образцах молока и в клеточной фракции крови непосредственно дериватизировали до сложных метиловых эфиров FA (FAME) и анализировали, как описано ранее [Rodríguez-Alcalá et al., Innov. Food Sci. Emerg. Technol. 2009, 10, 32-36]. Анализы проводили по меньшей мере в двух повторениях. Концентрации широкого диапазона цитокинов, хемокинов, факторов роста и иммуноглобулинов в молоке и образцах крови определяли в двух повторениях с использованием устройства система Bioplex 200 или посредством ELISA, как описано ранее [Espinosa-Martos et al., J. Pediatr. Gastroenterol. Nutr. 2013, 56, 560-8]. В образцах плазмы также анализировали антигены Льюиса крови. Метаболиты, связанные с осмотическим стрессом и конечными продуктами метаболизма оксида азота (NOx) в крови измеряли в двух повторениях, как описано ранее [Codoñer-Franch et al., Atherosclerosis 2011, 215, 475-480 and Nutr. Metab. Cardiovasc. Dis. 2012, 22, 237-243].
Статистический анализ. Перед статистическим анализом микробиологические данные, записываемые в виде числа КОЕ на мл молока, трансформировали в логарифмические величины. Для проверки нормального распределения использовали критерий Шапиро-Уилка. Концентрации выражают в виде средних значений и 95% доверительного интервала (CI) в данных с нормальным распределением или в виде медиан и интерквартильного размаха (IQR), когда они не соответствовали нормальному распределению. Эффект введения пробиотиков анализировали парным t-критерием Стьюдента или знаковым ранговым критерием Уилкоксона. Различия частот детекции аналитических параметров анализировали с использованием критериев χ2 с поправкой Йейтса при необходимости. Различия считали значимыми при P<0,05.
Анализы молока. Анализы образцов молока обобщены в таблицах 4 и 5. На сутки 0 среднее значение общего содержания бактерий в образцах молока составляло 4,08 log10 КОЕ/мл; это значение значительно снижалось к концу исследования (3,09 log10 КОЕ/мл; P<0,000) (таблица 4). Следует отметить, что содержание всех микроорганизмов, вовлеченных в мастит (Staphylococcus epidermidis, Staphylococcus aureus, viridans streptococci и corynebacteria), значительно снижалось на сутки 21 (таблица 4), тогда как лактобактерии, которые невозможно было детектировать в образцах молока, собираемых на сутки 0, выделяли более чем у половины женщин на сутки 21 (данные не показаны). Клинические симптомы исчезали или заметно улучшались у всех женщин к концу исследования (данные не показаны). В целом значения SCC не изменялись, хотя наблюдали значительное снижение процента полиморфноядерных (PMN) лейкоцитов (P=0,018) и тенденцию к снижению процента эпителиальных клеток после лечения пробиотиком (таблица 4).
Концентрации жира, лактозы, общих твердых веществ и обезжиренных твердых веществ в грудном молоке не изменялись на всем протяжении периода исследования, и хотя содержание белка снижалось на сутки 21, это все еще соответствовало диапазону нормальных физиологических значений (данные не показаны). Уровни калия в молоке снижались (P=0,000), а уровни хлорида повышались (P=0,002) после введения пробиотика, при этом концентрации натрия в молоке, а также отношение Na/K не изменялись (таблица 4). Основная жирная кислота, встречающаяся в образцах грудного молока, представляла собой олеиновую кислоту (C18:1 c9, ~40%), далее следовала пальмитиновая (C16, ~15-17%), линолевая (C18:2 c9, c12, ~13-14%) и лауриновая (C12, ~10%) кислоты (данные не показаны). Не выявляли изменений в композиции FA молока после лечения, за исключением небольшого повышения, наблюдаемого для пальмитиновой кислоты (1,9%, P=0,018).
IgA, IgG1, IgG3, IgG4 и IgM являлись иммуноглобулинами, которые наиболее часто детектировали в образцах молока. IgA детектировали во всех образцах и в самых высоких концентрациях (таблица 5). После лечения пробиотиком уровни IgE и IgG3 значительно повышались (P=0,041 и 0,020, соответственно) (таблица 5). Цитокины, хемокины и факторы роста выявляли в образцах грудного молока по существу с различными частотами: IL-1β, TGF-β2, GRO-α, IL-8, MCP-1, MIP-1β и EGF можно было детектировать более чем в 90% образцов, IL-6, IL-7 и GM-CSF in 57-87%, и оставшуюся часть этих соединений менее чем в 50% образцов (таблица 5). Прием пробиотика не изменял ни их наблюдаемые частоты детекции, ни их концентрации, за исключением IL-7 и EGF, которые значительно снижались (P=0,070 и 0,061, соответственно) (таблица 5). Следует отметить, что, среднее значение концентрации цитокинов IFN-γ, IL-1β, IL-6, IL-10, IL-12(p70) и TNF-α, и хемокины IL-8, MCP-1 и MIP-1β снижались, и их доверительный интервал значения сужался после введения, хотя эти изменения не достигали статистической значимости (таблица 5).
Содержание бактериальных, соматических клеток и электролитов в молоке
[a] парный t-критерий; [b] 95% доверительный интервал; [c] моноциты/макрофаги.
Концентрации иммуноглобулинов и цитокинов в молоке
[a] парный t-критерий; [b] 95% доверительный интервал; [c] Сокращенные обозначения: EGF=эпителиальный фактор роста; G-CSF=гранулоцитарный колониестимулирующий фактор; GM-CSF=гранулоцитарно-макрофагальный колониестимулирующий фактор; GRO-α=связанный с ростом онкоген-α; Ig=иммуноглобулин; IL=интерлейкин; IFN-γ=интерферон-γ; MCP-1= моноцитарный хемоаттрактантный белок; MIP-1β=макрофагальный белок воспаления-1β; TGF-β2=трансформирующий фактор роста-β2; TNF-α=фактор некроза опухоли-α.
Анализы крови. Анализы образцов крови обобщены в таблицах 6 и 7. У участниц детектировали три из четырех фенотипов антигенов Льюиса A/B, но ни у одной из них не выявляли фенотип A+/B+ (данные не показаны). Как правило, значения, получаемые для тестируемых гематологических и биохимических параметров, находились в физиологических диапазонах в оба момента времени отбора проб. Отмечали значительное снижение количественного отношения лимфоцитов (P=0,004) и повышение количественного отношения PMN клеток (P=0,011) после лечения пробиотиком (таблица 6). Следует отметить, что, основные изменения детектировали в липидном профиле крови участниц, т.к. триглицериды (P=0,012), а также общие уровни холестерина (P=0,003), LDL (P=0,006) и VLDL (P=0,010) в образцах крови являлись значительно ниже после лечения пробиотиком (данные не показаны). Не наблюдали существенных изменений в FA, детектируемых в клеточной фракции крови, за исключением адреновой кислоты (C22:4 n6), которая незначительно снижалась (P=0,047) (данные не показаны).
Анализ маркеров окислительного стресса демонстрировал незначительное снижение большинства из них после введения пробиотика, хотя только снижение конечных продуктов окисления белков (AOPP), при выражении в виде абсолютной концентрации и после нормализации на содержание белка, являлось статистически значимым (P=0,008 и P=0,003 соответственно; таблица 6). Корреляционный анализ параметров окислительного стресса демонстрировал, что после введения пробиотика AOPP положительно коррелировали с взаимодействующим с тиобарбитуровой кислотой веществом (TBARM, r=0,346, P=0,004) и уровнями нитритов (r=0,400; P=0,001) и отрицательно с изопростанами (r=-.254; P=0,035). Также отмечали отрицательные корреляции SH-групп с TBARM (r=-0,427; P=0,000) и с изопростанами и нитритом (r=-0,318; P=0,008).
Уровни различных иммунологических соединений в крови также находились в своих физиологических диапазонах (таблица 7). Все Ig присутствовали во всех образцах крови за исключением IgE, который не детектировали в двух образцах, собираемых на сутки 21. IL-4, IFN-γ, TNF-α и все хемокины детектировали более чем в 87% образцов; IL-6, IL-12(p70), IL-7 и G-CSF детектировали в 52-74% и остывшую часть этих соединений можно было измерять менее, чем в 50% из них. После лечения пробиотиком в образцах крови отмечали сниженные концентрации IgA (P=0,047), IgG1 (P=0,066), IL-2 (P=0,098) и MCP-1 (P=0,062) (таблица 7).
Гематологические и биохимические параметры крови
[a] парный t-критерий [b] 95% доверительный интервал для данных с нормальным распределением и знаковый ранговый критерий Уилкоксона, когда не 1; [c] Сокращенные обозначения: MCH=средний эритроцитарный гемоглобин; MCHC=средняя концентрация эритроцитарного гемоглобина; MCV=средний объем эритроцита; MPV=среднее объем тромбоцита; PMN=полиморфонуклеарные клетки; RDW=ширина распределения эритроцитов по объему; AOPP=конечные продукты окисления белков; TBARM=взаимодействующее с тиобарбитуровой кислотой вещество; MDA=малоновый диальдегид; NOx=конечные продукты метаболизма оксида азота; PG=простагландин; бл.=белок; SH=сульфгидрил; [d] Нормальное распределение отсутствует.
Таблица 7. Концентрации иммуноглобулинов и цитокинов в крови
[a] парный t-критерий; [b] 95% доверительный интервал; [c] Сокращенные обозначения: G-CSF=гранулоцитарный колониестимулирующий фактор; GM-CSF=гранулоцитарно-макрофагальный колониестимулирующий фактор; Ig=иммуноглобулин; IL=интерлейкин; IFN-γ=интерферон-γ; MCP-1=моноцитарный хемоаттрактантный белок; MIP-1β=макрофагальный белок воспаления-1β; TNF-α=фактор некроза опухоли-α.
Анализ мочи. Значения, получаемые для параметров мочи, находились в физиологических диапазонах, и не наблюдали различий, связанных с лечением пробиотиком (данные не показаны).
Заключение. Выявляли, что PS2 L. salivarius являлся эффективным для улучшения общего содержания бактерий в молоке человека, и наблюдали прямую взаимосвязь между снижением содержания стафилококков и стрептококков и клиническим исходом. Женщины, включенные в это исследование, сообщали полном или заметном улучшении после лечения. Эти результаты являются показателем способности PS2 L. salivarius лечить мастит.
Введение пробиотика не влияло на содержание макропитательных веществ грудного молока, которое находилось в нормальных диапазонах во время исследования. Электролиты, содержащиеся в молоке, отражают целостность эпителия молочной железы, которая достигается постепенно после родов через закрытие плотных контактов, и регулируется механизмами транспорта [Neville et al., Am. J. Clin. Nutr. 1991, 54, 81-92]. Сниженные уровни калия и повышенные уровни IgG3 после лечения PS2 L. salivarius подтверждают благоприятное действие на целостность эпителия молочной железы. Транспорт IgG1 и IgG3 представляет собой конкурентный механизм, опосредованный рецептором, который поддерживает подкласс IgG3 в молоке, которые имеет более выраженные эффекторные свойства [Stapleton et al., Nature Commun. 2011, 2, 599] и снижает скорость распространения инфекции у индивидуумов с иммунодефицитом [Shapiro, Immunotherapy, 2012, 4, 1835-9].
Уровни IL-8 и других цитокинов и хемокинов (таких как IFN-γ, IL-1β, IL-6, IL-12(p70), TNF-α, MCP-1 и MIP-1β) снижались в молоке вследствие лечения пробиотиком, что могло вызывать улучшение состояния воспаления, связанного с маститом. 95% доверительные интервалы различных параметров заметно сужались после лечения пробиотиком, что указывает на меньшую дисперсию данных и подтверждает более нормализованные уровни.
Повышение трофических факторов EGF и TGF-β2 могло способствовать иммуномодуляции в эпителии молочной железы, что также может являться благоприятным для ребенка. TGF-β2 является ключевым иммунорегуляторным фактором молочной железы, способствующим местной продукции IgA и индукции механизмов толерантности в полости у детей [Stavnezer, J. Immunol., 1995, 155, 1647-1651; Oddy and Rosales, Pediatr. Allergy Immunol. 2010, 21, 47-59]. В противоположность этому пероральная добавка со штаммом L. reuteri беременным женщинам снижала уровни TGF-β2 в молозиво [Böttcher et al., Pediatr. Allergy Immunol. 2008, 19, 497-504]. Этот явный противоречивый результат является показателем дифференциальных иммунных ответов, реализуемых различными бактериальными штаммами, и может объяснять, почему различные пробиотические штаммы находят разные виды применения.
Пример 5: Жидка композиция
100 мл жидкой композиции на основе молока, упакованной в 100 мл бутылку, содержащую 8,1 г транс-галактоолигосахарида, 0,9 г фруктополисахарида, 750 мл рыбьего жира и от 108 до 1010 колониеобразующих единиц (КОЕ) штамма Lactobacillus salivarius по настоящему изобретению, необязательно также содержащую питательные микроэлементы, рекомендуемые для лактации (например, фолиевая кислота, витамин B1, витамин B2, витамин B6, витамин B12, холин, витамин C, кальций, йод, цинк и железо), где композиция включает инструкции по добавлению содержимого карандаша или пакетированной порционной формы саше в напиток или еду, которую необходимо употреблять один или два раза в сутки для профилактики и/или лечения мастита или симптомов мастита.
Пример 6: Добавка
Карандаш или пакетированная порционная форма, или саше, содержащее от 108 до 1010 колониеобразующих единиц (КОЕ) штамма Lactobacillus salivarius по настоящему изобретению, с инструкциями по добавлению содержимого карандаша или пакетированной порционной формы саше в напиток или еду, которую необходимо употреблять один или два раза в сутки для профилактики и/или лечения мастита или симптомов мастита. Соответственно напиток представляет собой холодный напиток или теплый напиток.
Пример 7: Батончик мюсли
Батончик мюсли, содержащий злаки (например, овес, пшеницу, кукурузу, рис), соответственно включая злаки в форме хлопьев, экструдированных злаков и т.д., и штамм Lactobacillus salivarius по настоящему изобретению в диапазоне от 108-1010 колониеобразующих единиц (КОЕ) и необязательно также содержащий:
- фрукты (например, клюкву, изюм, ежевику, черную смородину, вишню, малину, клубнику и т.д.), соответственно включая сухие или лиофилизированные фрукты;
- семена и/или орехи;
- сиропы и/или масла;
- пребиотики (например, транс-галактоолигосахарид, фруктополисахарид);
- питательные микроэлементы, рекомендуемые для лактации (например, фолиевую кислоту, витамин B1, витамин B2, витамин B6, витамин B12, холин, витамин C, кальций, йод, цинк и железо).
Батончик мюсли может содержать инструкции, что батончик мюсли необходимо употреблять один или два раза в сутки для профилактики и/или лечения мастита или симптомов мастита.

Группа изобретений относится к области получения фармацевтических средств на основе пробиотиков. Предложены штамм Lactobacillus salivarius BCCM/LMG LMG P-27027, пригодный для лечения мастита, и его применение, а также способ лечения и/или профилактики воспаления и/или инфекции ткани молочной железы у женщин, композиция, содержащая указанный штамм, и ее применение. Композиция содержит от 102 до 1013 КОЕ указанного штамма и физиологически приемлемый носитель или эксципиент. Изобретения обеспечивают эффективное лечение и/или профилактику воспаления и/или инфекции ткани молочной железы у женщин. 5 н. и 4 з.п. ф-лы, 7 ил., 7 табл., 7 пр.
1. Штамм Lactobacillus salivarius с номером доступа BCCM/LMG LMG P-27027, где указанный штамм пригоден для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы у женщин.
2. Применение штамма Lactobacillus salivarius по п. 1 для получения композиции для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы у женщин.
3. Применение по п. 2 для лечения и/или профилактики мастита у женщин.
4. Способ лечения и/или профилактики воспаления и/или инфекции ткани молочной железы у женщин, где штамм Lactobacillus salivarius с номером доступа BCCM/LMG LMG P-27027 вводят в дозе от 108 до 1010 колониеобразующих единиц (КОЕ) на дозу.
5. Способ по п. 4, где штамм Lactobacillus salivarius вводят три раза в сутки в дозе от 108 до 1010 колониеобразующих единиц (КОЕ) на дозу.
6. Композиция для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы, содержащая от 102 до 1013 КОЕ штамма Lactobacillus salivarius по п. 1 и физиологически приемлемый носитель или эксципиент.
7. Композиция по п. 6, содержащая от 108 до 1010 КОЕ Lactobacillus salivarius на грамм сухой массы.
8. Композиция по п. 6, дополнительно содержащая по меньшей мере один, выбранный из группы трудноусваиваемых олигосахаридов, LC-PUFA, дополнительных пробиотиков и питательных микроэлементов.
9. Применение композиции по п. 6 для лечения и/или профилактики воспаления и/или инфекции ткани молочной железы у женщин.
| МИКРООРГАНИЗМЫ МОЛОКА МЛЕКОПИТАЮЩЕГО, ИХ СОДЕРЖАЩИЕ КОМПОЗИЦИИ И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ МАСТИТА | 2008 |
|
RU2446814C2 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| E.JIMENEZ et al, "Oral administration of Lactobacillus strains isolated from breast milk as an alternative for the treatment of infectious mastitis during lactation".//Applied and Environmental Microbiology, 2008, vol.74, N 15, р.4650-4655 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2019-04-09—Публикация
2014-12-19—Подача