Изобретение относится к ветеринарной медицине, а именно ветеринарной фармакологии, в частности для лечения ран различной этиологии у животных.
Известны способы применения препаратов серебра в качестве антисептиков в виде водных растворов: серебряная вода, AgNO3 или протаргол. В известных препаратах коллоидного серебра (колларгол и протаргол), обладающих антисептическими свойствами, стабилизатором высокодисперсных частиц серебра служат белковые полимеры казеин и желатин (М.Д. Машковский. Лекарственные средства. Т. 2, Новая волна, М., 2000).
Недостатком этих средств и способов их применения является то, что эти препараты, из-за наличия в их составе белков непостоянного состава, могут обладать аллергическим действием и не поддаются строгой стандартизации. Наличие же в их составе значительных количеств катионного серебра придает им обжигающее действие. Их единственная выпускная форма - только порошки, которые перед использованием необходимо растворять в асептической дистиллированной воде.
Известен препарат наноразмерных частиц серебра в водных растворах - Арговит (Витар) (ТУ 9310-13-00008064-00), который представляет собой комплекс серебра с медицинским поливинилпирролидоном («Применение препаратов серебра в медицине» - Сборник трудов по материалам научно-практической конференции «Новые химические системы и процессы в медицине», под. ред. Е.М. Благитко, Новосибирск, 2004, 115 с.). Препарат состоит из нанокластеров металлического серебра, стабилизированных поли-N-винил-пирролидоном-2, получаемых химическим восстановлением водорастворимой соли серебра с последующей сушкой до порошка. Получаемые частицы серебра имеют по данным авторов размеры несколько нанометров и вследствие этого повышенную активность, и агрегативную устойчивость. Арговит выпускается в виде стабилизированного концентрированного раствора, из которого путем разведения дистиллированной водой готовят разбавленные рабочие растворы для применения. По внешнему виду - концентрированный раствор темно-коричневого цвета, разбавленные растворы - от коричневого до желтого цвета различной интенсивности в зависимости от степени разбавления. По данным авторов, разбавленные растворы седиментационно устойчивы в течение не менее 2 недель (Патент РФ №2342120, 27.12.2008 г).
Недостатком лекарственных форм этих препаратов является жидкая консистенция, пригодная, в основном, для санации раны (полоскание, промывание) и не обеспечивающая пролонгированного действия. При этом расходуется много перевязочного материала, а растворы серебра дороги и имеют малый срок хранения в растворе. Требуется ежедневная санация раны, промывание 2-5% р-ром арговита, перевязки с 5% аргогелем или/и электрофорез серебра, что усложняет использование в том числе в домашних условиях не обученными людьми. Для аппликации препарата на поверхность раны требуются дополнительные материалы, марлевые повязки.
Известно также средство"Арголит" для лечения инфицированных ран (Патент РФ №2245151, 27.01.2005 г.). Средство представляет собой порошок цеолита, модифицированного серебром, с размерами частиц 17-20 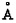 . Предложенная форма обеспечивает повышение лечебного эффекта средства за счет увеличения пористости цеолита и увеличения площади взаимодействия осажденного в нем серебра с поверхностью раны.
. Предложенная форма обеспечивает повышение лечебного эффекта средства за счет увеличения пористости цеолита и увеличения площади взаимодействия осажденного в нем серебра с поверхностью раны.
Однако недостатком данного средства и способа его применения является трудность очищения раны после применения.
Наиболее близким аналогом, принятым за прототип, является клеевая композиция на основе наночастиц серебра и способ ее применения (Патент RU №2623060 от 21.06.2017 г.). Недостатком данной композиции является отсутствие в ее составе компонентов повышающих биодоступность действующего антимикробного вещества для тканей. Присутствующие в ее составе композитные частицы из диоксида титана и ультрадисперсного серебра способны оказывать механическое раздражающее действие на раневую поверхность, препятствуя заживлению. Входящие в состав указанной клеевой композиции химические вещества (поливинилбутираль, дибутилфталат, канифоль) препятствуют равномерному нанесению препарата на всю поверхность поврежденных кожных покровов.
Техническая задача, на решение которой направлено предлагаемое изобретение, состоит в расширении арсенала средств и способов лечения ожоговых, мокнущих и рваных ран и чистых послеоперационных ран для их заживления, более эффективном и менее токсичным, чем те, что доступны в настоящее время для лечения кожных ран.
Сущность изобретения заключается в том, что средство для лечения кожных ран у животных, содержащее серебро, пролангатор, согласно изобретению, содержит водный раствор кластерного серебра, в качестве в качестве пролонгатора полиэтиленгликоль и диметилсульфоксид (ДМСО), и дополнительно глицерин, при следующем соотношении масс. %:
Сущность изобретения заключается также в том, что в способе применения средства для лечения кожных ран у животных, включающем нанесение препарата на раневую поверхность, согласно изобретению, наносят средство, состоящее из водного раствора кластерного серебра 5-20% масс., полиэтиленгликоля 5-10% масс., глицерина 5-10% масс., и диметилсульфоксида 5-15% масс., путем аэрозольного распыления на область раны, 2 раза в день, в количестве 200-300 мкл. в течение всего периода заживления
Способ осуществляется следующим образом.
1. Получение средства для лечения ран у животных.
В качестве компонентов предлагаемого средства были выбраны следующие вещества:
- Кластерное серебро, стабилизированное полимером, в виде водного раствора;
- Глицерин;
- Полиэтиленгликоль (ПЭГ-400);
- Диметиолсульфоксид (ДМСО).
Кластерное серебро обладает выраженной противомикробной активностью и представляет собой суспензию частиц высокодисперсного металлического серебра нанометрового размера (5-80 нм), стабилизированных полимером в дистиллированной воде, в соотношении:
- серебро 1-1,5% масс.
- полимер-стабилизатор 15-20% масс.
- вода дистиллированная - остальное до 100% масс.
Водный раствор кластерного серебра в качестве компонента вводили в готовый препарат в концентрации 5-20% масс. При снижении концентрации водного раствора кластерного серебра менее 5% масс. отмечали существенное снижение антимикробной активности компонента. При повышении концентрации более 20% масс. отмечали отсутствие положительной динамики повышения антимикробных свойств данного компонента.
Таким образом, исходным количеством водного раствора кластерного серебра приняли концентрацию 5-20% масс.
Глицерин в комплексе с полиэтиленгликолем (ПЭГ-400) улучшают смачивание и растекание препарата по раневой поверхности, формируя воздухо- и влагопроницаемое покрытие, способствующее улучшенному заживлению раны.
При снижении в составе готового препарата данных компонентов до концентрации менее 5% масс. пропадает эффект равномерного смачивания и растекание препарата по раневой поверхности. При повышении концентрации глицерина и полиэтиленгликоля (ПЭГ-400) более 10% масс. возрастает вязкость раствора и затрудняется его нанесение на поверхность раны.
Диметилсульфоксид в качестве компонента препарата оказывает противовоспалительное и местноанестезирующее действие, повышает проницаемость кожи и тканей для действующих веществ препарата.
При снижении концентрации диметилсульфоксида менее 5% масс. не обеспечивается должный эффект проницаемости кожных покровов и тканей для основного действующего вещества. При повышении концентрации более 15% масс. возрастает себестоимость конечного препарата, без существенного повышения терапевтической эффективности.
Исходя из этого был предложен следующий состав препарата:
Указанные ингредиенты, в стерильных условиях смешивали в следующей последовательности: к полиэтиленгликолю (ПЭГ-400) добавляли глицерин, через 15 мин перемешивания вносили водный раствор кластерного серебра 0,1%, затем через 15 мин перемешивания - диметилсульфоксид (ДМСО) и дистиллированную воду до необходимого объема. Через 20 мин перемешивания готовы препарат помещали в термостат на 24 ч при Т=37°C. для проверки стерильности.
Готовую смесь в стерильных условиях помещали в помповые распылители в объеме 15 мл.
Полученному средству было присвоено рабочее название «Арговит спрей - 3».
Эффективность препарата «Арговит спрей - 3» была подтверждена в следующих примерах.
Пример 1. Объектом исследования служили аэрозольные формы сереб-росодержащего препарата «Арговит», различающиеся составом:
- «Арговит спрей - 1» - глицерин 5-10% масс., кластерное серебро 0,1% - 5-20% масс.; вода дистиллированная до 100% масс.
- «Арговит спрей - 2» - глицерин 5-10% масс, ПЭГ-400 - 5-10% масс; кластерное серебро 0,1% - 5-20% масс; вода дистиллированная до 100% масс
- «Арговит спрей - 3» глицерин 5-10% масс, ПЭГ-400 - 5-10% масс; кластерное серебро 0,1% - 5-20% масс; диметилсульфоксид (ДМСО) - 5-20% масс; вода дистиллированная до 100% масс
Опыт по изучению антибактериального действия представленных препаратов проводился с использованием музейных штаммов возбудителей раневой инфекции - St. albus, Str.pyogenes, E.coli, Ps.aeruginosae.
Для постановки опыта в чашку Петри с питательной средой - мясопептонный агар (МПА) с случае с St. albus, Str.pyogenes, Ps.aeruginosae, и средой Эндо в случае с E.coli - вносили 100 мкл. взвеси суточной культуры тест-микробов (1 млрд. КОЕ/мл). Шпателем производили равномерное распределение внесенной микробной взвеси по всей поверхности питательной среды. Затем, на поверхность среды помещался алюминиевый трафарет и производилось распыление исследуемых аэрозольных форм серебросодержащих препаратов «Арговит спрей - 1», «Арговит спрей - 2», «Арговит спрей - 3».
Посевы инкубировали в термостате при Т=37°C в течение 24 часов.
Антибактериальный эффект оценивали по отсутствию роста тест-микробов на поверхности питательных сред в зонах распыления препаратов «Арговит спрей» трех модификаций.
В результате проведенного опыта было установлено, что все три формы препарат «Арговит спрей» обладают выраженной антибактериальной активностью в отношении тест-микробов (Таблица 1).


Примечание: (-) - отсутствие роста тест-микробов; (+) - сплошной рост тест-микробов.
В опытных чашках на месте внесения действующего вещества аэрозольных форм серебросодержащих препаратов «Арговит спрей - 1», «Арговит спрей - 2», «Арговит спрей - 3» наблюдается полное отсутствие роста тест-микробов. В контроле на всей поверхности питательной среды наблюдается сплошной рост колоний микроорганизмов.
Таким образом, установлен выраженное антибактериальное эффект действие представленных составов «Арговит спрей - 1», «Арговит спрей - 2», «Арговит спрей - 3».
Пример 2. Для оценки продолжительности антибактериального действия аэрозольных форм серебросодержащих препаратов «Арговит спрей - 1», «Арговит спрей - 2», «Арговит спрей - 3», в чашки Петри с МПА на всю поверхность среды нанесли исследуемые препараты (по 4 чашки Петри на каждый препарат). Затем с промежутками в три часа на поверхность среды производили посевы тест-микробов: St. albus, Str.pyogenes, Ps.aeruginosae, E.coli в дозе 20 мкл. (1 млрд. КОЕ/мл). Посевы инкубировали в термостате при Т=37°C в течение 24 часов.
Продолжительность антибактериального эффекта оценивали по наличию или отсутствию роста тест-микробов на поверхности питательных сред в зонах распыления препаратов «Арговит спрей - 1», «Арговит спрей - 2», «Арговит спрей - 3».
Результаты представлены в таблице 2.

Примечание: (-) - выраженный антибактериальный эффект (отсутствие роста тест-микроба);
(++) - сомнительный антибактериальный эффект (единичные колонии тест-микроба);
(++++) - отсутствие антибактериального эффекта (рост тест-микроба)
Как видно из представленных данных наиболее продолжительным антибактериальным эффектом обладает «Арговит спрей - 3». В отличие от остальных препаратов, он обеспечивает выраженное антибактериальное действие в отношении всех тест-микробов в течение 12 часов.
У препаратов «Арговит спрей - 1» и «Арговит спрей - 2» антибактериальное действие заканчивалось через 3 часа - в случае с Proteus vulgaris, и через 6 часов - в отношении других микроорганизмов.
Пример 3. Лечебно-профилактическая эффективность препаратов изучалась на морских свинках, разделенных по принципу аналогов на 6 групп (табл. 3).

Раны животным наносились с левой стороны на боковой поверхности брюшной стенки. В качестве средства для общего наркоза использовался «Золетил-100» в дозе рекомендованной производителем. Операционное поле готовили в соответствии с общими правилами асептики и антисептики: произвели удаление шерстного покрова и обработку кожных покровов спиртовым раствором йода. Раны наносились с помощью скальпеля и хирургических ножниц и тупой препаровки; ожоги - с помощью стального тавра (Р=220 мм), раскаленного на газовой горелке.
У животных опытных групп раны обрабатывались препаратом «Арговит спрей - 3», контрольных групп - клеевой композицией (прототип).
За всеми животными вели наблюдение: учитывали общее клиническое состояние, состояние раны и скорость ее заживления, наличие и отсутствие раневой инфекции или других осложнений.
В результате проведенного опыта было установлено, что применение препарата «Арговит спрей - 3» ускоряет заживление операционных ран на 14,28% по сравнению с контролем. В опытной группе полная герметизация раны наступала на 6 сутки опыта, в контрольной группе на 7 сутки. Осложнений в виде воспаления или развития гнойной инфекции не наблюдалось.
Результаты терапии лоскутных ран представлены в таблице 4.

На 7 сутки опыта, средняя площадь лоскутной раны в опытной группе составила 6,03% от первоначального повреждения, в контрольной - 8,3%. На 14 сутки площадь ран составила 0,6% и 2,2% соответственно.
Ожоговые раны.
На 7 сутки опыта, у животных первой опытной группы раны представляли собой четко ограниченные участки кожного покрова, покрытые струпом. На 14 сутки опыта раны имели грануляционную ткань, признаков гнойного воспаления не наблюдалось. На 21 день опыта у всех животных опытной группы, обрабатываемых препаратом «Арговит спрей - 3», ожоговые раны полностью были закрыты грануляционной тканью.
У животных контрольной группы наблюдается иная картина. На 14 сутки и опыта у двух животных на месте ожога развилось гнойное воспаление -при микроскопии содержимого раны, были обнаружены микроорганизмы рода Streptococcus и Ps.aeruginosa. На 21 сутки опыта одно животное в контрольной группе пало.
На 28 сутки, ожоговая рана морских свинок контрольной группы представляла собой рубцовую ткань, частично закрывающую собой участки изъязвления и гнойного воспаления.
Полное заживление ожоговых ран у животных контрольной группы наступало на 42 сутки опыта.
Исходя из полученных результатов можно сделать вывод, что препарат «Арговит-спрей-3» при нанесении на поверхность ожоговых ран, профилактирует развитие осложнений в виде гнойного воспаления, что положительно влияет на регенерацию тканей и сроки заживления ран.
Пример 4. Для проведения клинических исследований профилактических свойств антимикробного препарата препаратом «Арговит спрей - 3» были набраны 3 группы кошек (n=5): две опытных и одна контрольная. Животным первой опытной группы после проведения планового оперативного вмешательства (овариэктомия) проводили обработку послеоперационных швов препаратом «Арговит спрей - 3» 2 раза в сутки. Животным второй опытной группы операционную рану обрабатывали клеевой композицией (прототип) по схеме предложенной разработчиком - 1 раз в 3 дня. В контрольной группе операционную рану не обрабатывали.
Герметизацию операционных ран проводили путем наложения узловых швов на кожные покровы нерассасывающимся шовным материалом «Мед-Капрон» стерилизованным паром.
Эффективность заживления ран оценивали по числу осложнений, возникающих в раннем и позднем послеоперационных периодах, свидетельствующих о несостоятельности швов: фильтрация водянистой влаги; инфильтрация ткани вокруг шва; нагноение; рыхлое грубое рубцевание.
Результаты изменения клинического состояния животных и характера швов на 5 и 10 день опыта, представлены в таблицах 5.

При этом установлено, что на 5-день опыта у всех животных первой и второй опытных групп клиническое состояние оценивали как хорошее. В контрольной группе у одной кошки (20%) отмечалось угнетение, отказ от корма, что характеризовалось нами как удовлетворительное состояние.
Воспаление операционного шва в первой опытной группе отмечалось у 40% животных; во второй - 60%, в контроле данную патологию отмечали у 100% животных.
В первой опытной группе ни у одного животного на месте операционной раны не развилась гнойная инфекция. Во второй группе признаки гнойной инфекции также не отмечались. В контроле у 80% животных было отмечено послеоперационное осложнение в виде развития местного гнойного воспаления.
На 10-день опыта у всех животных отмечали хорошее клиническое состояние. Воспаление операционного шва в опытных группах не регистрировали, в контроле - у 40% животных отмечали плотный рубец на месте соединения кожных тканей.
Таким образом, предлагаемый нами способ послеоперационной обработки швов, позволяет исключить развитие послеоперационного воспаления в виду имеющихся у него бактерицидный свойств и длительного сохранения антибактериальных свойств, а также улучшает качество соединяемой поверхности.
Таким образом, использование «Арговит спрей - 3», в качестве средства для обработки послеоперационных ран способствует заживлению без осложнений и может применяться в домашних условиях.
«Арговит спрей - 3» расширяет реестр отечественных препаратов, по эффективности и удобству применения не уступает аналогам, а также имеет более низкую себестоимость.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ терапии послеродового эндометрита крупного рогатого скота | 2020 |
|
RU2735257C1 |
| Способ лечения субклинического мастита коров | 2018 |
|
RU2706124C1 |
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО | 1998 |
|
RU2143260C1 |
| СПОСОБ ЛЕЧЕНИЯ СЕРОЗНОГО МАСТИТА КРУПНОГО РОГАТОГО СКОТА | 2015 |
|
RU2598338C1 |
| Композит для ускоренного заживления ран различной этиологии, применение композита в качестве косметического средства и в качестве лечебного средства в ветеринарии, средство для регенерации кожных покровов на основе композита | 2017 |
|
RU2693228C2 |
| Способ терапии послеродового гнойно-катарального эндометрита коров | 2020 |
|
RU2745582C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТОВ НАНОДИСПЕРСИЙ НУЛЬВАЛЕНТНЫХ МЕТАЛЛОВ С АНТИСЕПТИЧЕСКИМИ СВОЙСТВАМИ | 2010 |
|
RU2445951C1 |
| АНТИСЕПТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ПОЛИВИНИЛПИРРОЛИДОН И УНИТИОЛ, ПРИМЕНЕНИЕ ТАКОЙ КОМПОЗИЦИИ И СПОСОБ ОБРАБОТКИ РАН С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2017 |
|
RU2649785C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ РАН, ОЖОГОВ И ИНФЕКЦИОННО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ КОЖИ, ПРИДАТКОВ КОЖИ И СЛИЗИСТЫХ ОБОЛОЧЕК | 2010 |
|
RU2452475C2 |
| СПОСОБ ТЕРАПИИ КАТАРАЛЬНОГО МАСТИТА КОРОВ КОМПЛЕКСНЫМ ПРЕПАРАТОМ, СОДЕРЖАЩИМ НАНОЧАСТИЦЫ СЕРЕБРА АРГОВИТ И ДИМЕКСИД | 2021 |
|
RU2757329C1 |
Группа изобретений относится к ветеринарии и может быть использована для лечения ран у животных. Предложено средство, содержащее водный раствор кластерного серебра при следующем соотношении компонентов в масс. %: водный раствор кластерного серебра 0,1%- 5-20, полиэтиленгликоль (ПЭГ-400)- 5-10, глицерин- 5-10, диметилсульфоксид (ДМСО)- 5-15, вода дистиллированная - остальное. Также предложено применение данного средства в виде аэрозоля для лечения кожных ран у животных. Группа изобретений позволяет лечить ожоговые, мокнущие, рваные и чистые послеоперационные раны, а также заявленное средство является более эффективным и менее токсичным, чем те, что доступны в настоящее время для лечения кожных ран. 2 н.п. ф-лы, 5 табл.
1. Средство для лечения ран у животных, содержащее серебро, пролангатор, отличающееся тем, что содержит водный раствор кластерного серебра, а в качестве пролонгатора полиэтиленгликоль и диметилсульфоксид, и дополнительно глицерин, при следующем соотношении масс. %:
2. Применение средства по п.1 в виде аэрозоля для лечения кожных ран у животных.
| Клеевая композиция и способ ее применения | 2015 |
|
RU2623060C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ РАН | 2006 |
|
RU2342120C2 |
| Водяной цепной лопастной двигатель | 1926 |
|
SU5240A1 |
| МАРЬИН Е | |||
| М.и др | |||
| Природные сорбенты в лечении гнойных ран у животных//Монография | |||
| Ульяновск, 2010 | |||
| MORYKWAS M | |||
| J | |||
| et al | |||
| Vacuum-assisted closure: a new method for wound control and treatment: animal studies and basic foundation //Annals of plastic surgery | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
Авторы
Даты
2019-06-11—Публикация
2017-11-21—Подача