Изобретение относится к области медицины и ветеринарии, а именно к онкологии и может найти применение в медицинских технологиях, основанных на реализации метода высокотемпературной деструкции (термоабляции) костной ткани путем высокотемпературного воздействия на патологически измененные участки кости человека или животного.
Во многих источниках научно-технической и патентной информации, в том числе и в [1. Патент РФ №2468796, МПК (2006.01), A61K 31/541, A61K 31/54, A61K 31/00, А61Р 35/00, А61Р 19/08, опубликовано 10.12.2012, Бюл. №34], [2. Мацко Д.Е. Саркомы костей классификация, гистологическое строение, особенности морфологической диагностик и // Практическая онкология. - 2010 - №1 - С. - 10], [3. Крживицкий П.И. Лучевая диагностика и оценка эффективности лечения остеосарком на современном этапе: Автореф. дисс. на соискание ученой степени канд. мед. наук. - Санкт-Петербург, 2009, - 26 с.] отмечено, что раковые опухоли (злокачественные новообразования ЗНО) костей относятся к злокачественному, не соответствующему норме, росту, обнаруженному в костях. Например, к ним относятся первичные опухоли костей, такие как остеосаркома (или остеома), хондросаркома, саркома Юинга и другие типы сарком. К опухолям костей также могут относиться вторичные, или метастатические, опухоли, обнаруженные в костях. При этом остеосаркома является наиболее часто встречаемым типом ЗНО, составляющим до 35% основных онкологических заболеваний костей, а хондросаркома - от 10 до 25% [2]. В [1] также отмечено, что остеосаркома занимает 6-е место среди онкологических заболеваний у детей в возрасте до 15 лет. Ежегодно в США остеосаркома поражает 400 детей и молодых людей в возрасте до 20 лет и 500 взрослых (большинство в возрасте 15-30 лет). Примерно 1/3 от 900 человек умирает ежегодно, т.е. примерно 300 человек каждый год. В [3] сказано, что удельный вес опухоли среди всех злокачественных новообразований скелета составляет от 30 до 38%. В [1] также отмечено, что остеосаркома является наиболее распространенной опухолью костей у собак и обычно поражает собак среднего возраста и крупного размера, например ирландских волкодавов, борзых грейхаундзов, немецких овчарок, ротвейлеров и немецких догов. Эта форма рака встречается у собак в десять раз чаще, чем у людей.
В связи с вышеизложенным можно сказать, что в данной области медицины существует потребность в развитии методов лечения злокачественных новообразований кости. В настоящее время существует несколько вариантов лечения ЗНО костей, которые применяются как самостоятельные виды лечения, так и в комплексе друг с другом, это:
1. Химиотерапия,
2. Лучевая терапия,
3. Хирургическое лечение,
1) Орган-уносящие операции (ампутации, экзартикуляции).
2) Орган-сохраняющие операции (эндопротезирование, краевые резекции, внутриочаговые резекции).
4. Реабилитация.
В [1] описан способ лечения ЗНО кости без применения термического воздействия. Согласно способу [1], частично удаляют опухоль кости у субъекта. После этого производят обработку области, примыкающей к тому участку кости, где опухоль была, по меньшей мере, частично удалена, гелем, содержащим тауролидин, таурултам, их смесь или их раствор, находящийся в равновесном состоянии. В предпочтительных вариантах осуществления этого изобретения гель является рассасывающимся. Особенно предпочтительно, если это гель на водной основе, включающий фибриллярный белок с поперечными сшивками или состоящий из него.
Недостатком данного способа является то, что удаление опухоли вместе с пораженной костью ослабляет ее механическую прочность, поэтому такая технология приемлема для небольших по объему ЗНО.
В настоящее время известен также способ локального интраоперационного гипертермического воздействия на ЗНО с использованием высокоинтенсивного сфокусированного ультразвука (HIFU). HIFU концентрирует ультразвуковые волны внутри организма, генерируя тепловую энергию (тепловой эффект) и кавитацию (нетепловой эффект), которые вызывают гибель опухолевых клеток. Например, из уровня техники известна система фокусированного воздействия ультразвуком высокой интенсивности для сканирования и лечения опухолей [4. Патент на изобретение RU №2210409, опубликован 20.08.2003, МПК A61N 7/02, A61F 7/00]. Согласно этому способу фокусируют ультразвук высокой интенсивности (HIFU), который используют как для сканирования (определения места положения и формы опухоли), так и для лечения опухолей. Для этого формируют из ультразвуковых волн объемную точку с высокой энергией (фокальную зону). Энергия в этой зоне достигает свыше 1000 Вт/см2 и температура мгновенно повышается до величины более 70°С. Воздействуют сформированной фокальной зоной на опухолевую ткань. При этом разрушающее воздействие проводят в фиксированной точке (для опухолей размером менее 1 см3), или в последовательных точках (для опухолей размером более 1 см3), при этом две соседние точки разрушения перекрываются на 1/10-1/2 часть для того, чтобы обеспечить полное разрушение опухолевой ткани. В случае, когда опухолевая ткань имеет форму длинных тяжей, осуществляют непрерывное разрушающее воздействие, то есть воздействие проводят однократно в течение 30 с. Принципиальные недостатки способа, описанного в [4], связаны с закономерностями распространения ультразвуковых колебаний в тканях человеческого тела и заключаются в следующем. Во-первых, при использовании метода деструкции с применением ультразвука практически невозможно избежать поражения здоровых клеток организма даже при сколь угодно высоком уровне фокусирования ультразвуковых колебаний, что требует в свою очередь проведения точного сканирования формы опухоли и ее места расположения. Во-вторых, ультразвук практически полностью отражается от кортикального слоя кости. В-третьих, ультразвук может изменять направление при переходе из одной среды в другую. Эти недостатки существенно ограничивают возможности применения данного способа случаями расположения опухоли на поверхности или около поверхности кости и практически делают невозможным его применение для случаев ЗНО большого объема и на большом протяжении костей. Кроме того, осуществление данного способа требует специального сложного дорогого оборудования и высококвалифицированных специалистов, как в области медицины, так и в области специальной техники. Большей частью этот способ воздействия используется как вариант паллиативного лечения костных метастатических опухолей с хорошим и стойким анальгезирующим эффектом.
Применение ультразвука для абляции костной ткани описано также в монографии [5. Vogl TJ, Helmberger TK, Mack MG, Reiser MF (eds) Percutaneous Tumor Ablation in Medical Radiology. 2008, Springer-Verlag, Berlin, Heidelberg, New York pp 258.], в которой отмечено, что в настоящее время наиболее распространенными являются способы прямого термического воздействия на опухолевую ткань с целью ее разрушения. К таким способам относятся радиочастотная абляция, ультразвуковая абляция, лазерная абляция, микроволновая абляция. Каждый из этих способов имеет свои достоинства и недостатки, однако для них характерен и один общий недостаток - это невозможность одномоментного гипертермического воздействия на опухоль кости большого объема и на большом ее протяжении.
Из уровня техники известен способ оперативного лечения опухолей костей [6. патент РФ №2087132, МПК А61В 17/56, А61В 17/22, опубликовано 20.08.1997 г]. Согласно этому способу опухоль удаляют путем резекции, после чего осуществляют пластику дефекта кости костными трансплантатами с применением дренажной системы. Для этого после удаления опухоли в стенках остаточной костной полости формируют дренажные отверстия в количестве, определяемом ее величиной и достаточном для свободного оттока крови в окружающие мягкие ткани. Этот способ позволяет предупредить формирование гематомы и нагноение в остаточной костной полости после удаления опухоли. Однако данный способ, основанный на таком хирургическом вмешательстве, существенно ослабляет кость, требует костных трансплантатов и не исключает метастазирование.
Из уровня техники известен патент [7. Патент РФ №2217088, опубликован 27.11.2003, МПК А61В 17/56, А61В 18/20], в котором описан способ лечения доброкачественных опухолей и опухолеобразных поражений костей у детей - [8. Л.В. Прокопова, Н.Г. Николаева. Сравнительная оценка результатов сохранных операций при доброкачественных опухолях и опухолеподобных поражениях костей у детей. Ортопедия, 5, 1991, с. 61-65]. Согласно способу [8] после определения места расположения и размера опухоли, в компактном слое кости образуют окно, через которое удаляют патологические ткани, а здоровые ткани остаточной костной полости подвергают обработке CO2-лазером (лазерная абляция). При резком истончении кортикальных стенок их удаляют вместе с патологическими тканями, а стенки, сохраняющие механическую прочность, подвергают лазерной обработке. Этот способ, как и аналог [6] позволяет предупредить формирование гематомы и нагноение в остаточной костной полости после удаления опухоли, благодаря обработке костной полости СО2-лазером. Однако способ [8] как и способ, описанный в [6], достаточно травматичен для пациентов, так как очень часто сильно ослабляется механическая прочность кости, что в определенных случаях требует осуществления пластики и ее укрепления. Лазерная обработка в [8] проводится высоко сфокусированным лучом, что допускает возможность появления необработанных участков поверхности остаточной костной полости (неравномерная термоабляция). Кроме того, этот способ не исключает метастазирования, потому что лазерную обработку костной полости проводят после удаления патологического очага, когда метастазы уже могут быть унесены кровотоком при проведении его резекции. Кроме того, для реализации данного способа требуется узкоспециализированное дорогостоящее оборудование - СО2-лазер. Эти недостатки снижают эффективность способа [8] и возможность его широкого применения.
Из уровня техники известны также способы воздействия на ЗНО путем локального гипертермического воздействия, например такие способы описаны в [9. Патент на изобретение RU №2317793, опубликовано 2008.02.27 бюл. №6, МПК А61В 18/14, А61В 18/12, А61М 1/00, А61М 25/00] или в [10. Патент на изобретение RU №2467720, МПК А61 В 18/12, A61N 7/00, опубликовано 27.11.2012 бюл. №33]. Согласно способу высокотемпературного разрушения биоткани, описанному в [9], в биоткань вводят теплоноситель (дистиллированную воду) через отверстия, выполненные в стенке полой металлической иглы, являющейся электродом. Введение и нагрев теплоносителя до температуры 100-110°С током высокой частоты осуществляют при повышенном давлении 1-2 бара и регулировании скорости введения теплоносителя. Использование изобретения [9] позволяет уменьшить травматичность процедуры высокотемпературного разрушения биоткани за счет увеличения объема коагуляции за одну процедуру (достигается сферический объем коагуляции диаметром до 5 см).
Согласно способу [10] по намеченным точкам в биологическую ткань вводят полые направляющие под воздействием ультразвуковых колебаний с частотой 19-25 кГц и амплитудой 3-30 мкм. После этого во внутреннюю полость каждой из направляющих через проксимальный конец вводят нагревательную иглу. Осуществляют нагрев и стабилизацию заданной температуры каждой нагревательной иглы.
Из уровня техники известен также способ реализации термоабляции опухоли костей [11. Патент РФ №2527363, МПК А61В 18/12, опубликовано 27.08.2014, бюллетень №24]. Согласно этому способу высокотемпературный нагрев (термоабляцию) проводят в два этапа. На первом этапе проводят термоабляцию вокруг опухоли в пределах здоровой ткани кости. Для этого в намеченные точки вокруг опухоли под воздействием ультразвуковых колебаний вводят основные нагреватели, определяя внутреннюю нагреваемую объемную область. После этого проводят первый этап термоабляции при температуре основных нагревателей не менее 65°С. Заданную температуру стабилизируют в течение всего времени воздействия. На втором этапе проводят полную термоабляцию всей внутренней нагреваемой объемной области ткани кости. Для этого в область кости, заключенную между основными нагревателями, в намеченные точки под воздействием ультразвуковых колебаний вводят дополнительные нагреватели. После этого осуществляют высокотемпературную абляцию при температуре всех (основных и дополнительных) нагревателей не менее 65°С. Заданную температуру нагревателей стабилизируют в течение всего времени воздействия. Способ позволяет обеспечить равномерную и стабильную высокотемпературную абляцию опухоли кости в пределах здоровых тканей, за счет чего снижается вероятность метастазирования, и появляется возможность уменьшения объема хирургического вмешательства.
Способы [9, 10, 11] позволяют осуществлять локальное гипертермическое воздействие непосредственно в зоне ЗНО и являются простыми с точки зрения их реализации. При этом имеется возможность регулирования температуры воздействия в режиме реального времени, а количество сеансов температурного воздействия во время одной операции не имеет ограничений. Самое главное - такой оперативный подход позволяет сохранить сегмент, пораженный опухолью, уничтожив при этом опухолевый очаг. Однако эти способы имеют и свои недостатки: во-первых, инвазивное многоточечное введение нагревателей (электродов) в зону воздействия приводит к ослаблению кости в области введения нагревателей и термического воздействия; во-вторых, практически эти способы невозможно применить при больших опухолевых площадях ЗНО плоских и трубчатых костей из-за необходимости использования большого количества нагревателей для обеспечения требуемой температуры во всей зоне воздействия.
В настоящее время перед онкоортопедами возникают проблемы, связанные с разработкой новых медицинских технологий интраоперационного воздействия на ЗНО костей, имеющих большие опухолевые площади и объемы, с обеспечением сохранения естественного костного каркаса и функциональности конечности. Из уровня техники известны способы, основанные на радикальной резекции костной опухоли с интраоперационной гипертермической обработкой резецированного сегмента кости и последующей его имплантацией в зону дефекта, описанные, например, в [12. Aponte-Tinao L, Ayerza MA, Muscolo DL, Farfalli GL. Survival, recurrence, and function after epiphyseal preservation and allograft reconstruction in osteosarcoma of the knee. Clin Orthop Relat Res. 2015 May; 473(5): 1789-96. doi: 10.1007/sl 1999-014-4028-5. Epub 2014 Oct 29. PubMed PMID: 25352262; PubMed Central PMCID: PMC4385338] или в [13. Yasin NF, Ajit Singh V, Saad M, Omar E. Which is the best method of sterilization for recycled bone autograft in limb salvage surgery: a radiological, biomechanical and histopathological study in rabbit. BMC Cancer. 2015 Apr 15;15:289. doi: 10.1186/sl2885-015-1234-9. PubMed PMID: 25884718; PubMed Central PMCID: РМС4407570]. Например, в источнике [12] описан способ радикальной резекции костной опухоли с замещением дефекта алло - или аутотрансплататом.
Наиболее близким к заявляемому способу, который взят за прототип, является способ резекции злокачественных опухолей костно-мышечной системы с последующей биологической реконструкцией, описанный в [14. Asada N, Tsuchiya Н, Kitaoka K, Mori Y, Tomita K. Massive autoclaved allografts and autografts for limb salvage surgery. A 1-8 year follow-up of 23 patients. Acta Orthop Scand. 1997 Aug; 68(4):392-5. PubMed PMID: 9310047.]. Техническая суть способа по [14] заключается в следующем: после определения места расположения и размера опухоли проводят широкомасштабную резекцию опухоли, осуществляют кюретаж (выскабливание) опухоли из резецированной кости, после чего проводят автоклавирование резецированной кости при 135°С в течение 10 минут. После этого осуществляют трансплантацию кости из малоберцовой кости (при этом используют как васкуляризированные, так и неваскуляризированные малоберцовые трансплантаты) либо проводят реимплантацию автоклавированной кости в дефект кости пациента и ее фиксацию пластинками и/или гвоздем IM. В этом способе высокотемпературному воздействию подвергают резецированную кость, что позволяет радикально уничтожить опухоль, уменьшить возможную инвалидизацию пациента, сохранить естественный костный каркас и функциональность конечности за счет исключения ее ампутации.
Недостатком прототипа [14] является, то, что этот способ является травматичным, так как требуется резекция кости, пораженной ЗНО. Необходимое высокотемпературное воздействие (автоклавирование при 135°С в течение 10 минут) проводят на предварительно резецированную кость, что, в свою очередь, требует решать вопросы реимплантации и биологической реконструкции резецированной кости или ее сегмента. При этом резецированная у пациента кость или сегмент не всегда могут быть использованы для реимплантации оперируемому пациенту из-за ее недостаточной структурной прочности, обусловленной как имеющимся заболеванием, так и предшествующим высокотемпературным воздействием. Все это требует дополнительного решения вопросов, связанных как с реимплантацией автоклавированной кости, так и с поиском и использованием алло - или аутотрансплантатов. В целом это приводит как к усложнению способа гипертермического воздействия и повышению его травмируемости для пациента, так и к затягиванию процесса восстановления подвижности конечности, что снижает эффективность как известных способов [12, 13], так и способа по прототипу [14].
Таким образом, отмеченные выше недостатки позволяют сформулировать техническую проблему, как проблему низкой эффективности известных способов интраоперационного гипертермического воздействия на кости, пораженные опухолями большой площади и объема, обусловленной, во-первых, сложностью известных способов, что сдерживает их широкое использование, во-вторых, повышенной травмируемостью пациента, приводящей к снижению прочности естественного костного каркаса и повышению срока процесса восстановления пациента.
Технический результат, достигаемый при решении вышеназванной проблемы, заключается в обеспечении равномерной и стабильной высокотемпературной абляции кости, имеющей большую площадь и объем, пораженные ЗНО, при одновременном упрощении способа, снижении травмируемости пациента и повышении возможности широкого использования этого способа.
Для решения технической проблемы и достижения технического результата заявляемый способ согласно изобретению, как и прототип, содержит общие операции, такие как определение места расположения и размера опухоли кости, проведение интраоперационного гипертермического воздействия на костную ткань, пораженную опухолью.
В отличие от прототипа согласно изобретению после установления места расположения и размера опухоли кости определяют область гипертермического воздействия, включающую область кости, пораженную опухолью и не менее 1 см здоровой костной ткани. После этого скелетируют кость в области гипертермического воздействия. Далее на область гипертермического воздействия кости накладывают соединенные с блоком стабилизации температуры гибкие поверхностные нагреватели, охватывая эту область кости со всех сторон. После этого осуществляют нагрев области гипертермического воздействия кости до значений температуры не менее 70°С. В течение первых 8-12 минут высокотемпературного воздействия температуру поднимают до величины не менее 50°С, а общее время высокотемпературного воздействия составляет не менее 30 минут, при этом заданную температуру стабилизируют в течение всего времени высокотемпературного воздействия на заданном уровне.
В частном случае мягкие ткани, сосуды и нервы, окружающие область гипертермического воздействия, теплоизолируют от гибких поверхностных нагревателей с помощью термоизоляционного материала.
В частном случае область гипертермического воздействия трубчатой кости охватывают гибким поверхностным нагревателем со всех сторон путем обвитая им трубчатой кости, а концы нагревателя закрепляют на поверхности кости.
В частных случаях гибкие поверхностные нагреватели выполняют в виде ленты требуемого размера или пластин разного размера и формы для обеспечения соответствия формы и площади гибких поверхностных нагревателей форме и площади области гипертермического воздействия.
В частном случае область гипертермического воздействия трубчатой кости охватывают несколькими гибкими поверхностными нагревателями путем наложения каждого нагревателя вокруг кости, при этом концы каждого из нагревателей соединяют друг с другом таким образом, что каждый из нагревателей образует кольцо вокруг кости.
В частном случае область гипертермического воздействия плоских костей охватывают несколькими (2 и более) гибкими поверхностными нагревателями, каждый из которых накладывают на противоположные стороны кости, при этом гибкие поверхностные нагреватели фиксируют к плоскости кости и/или между собой.
В частном случае для регистрации в режиме реального времени температуры гипертермического воздействия на пораженную опухолью кость через отверстие, выполненное в здоровой области кости, вводят термодатчик, соединенный с дисплеем.
Из уровня техники в общедоступных источниках информации не выявлен способ интраоперационного гипертермического воздействия на костную ткань, характеризующийся той же совокупностью признаков, что и заявляемый способ. Это подтверждает новизну заявляемого способа.
Из уровня техники не обнаружены способы интраоперационного гипертермического воздействия на костную ткань, имеющую большую опухолевую площадь, и объем, которые обеспечивали бы пониженную травмируемость пациента во время операции, сохранение прочности естественного костного каркаса и снижение времени восстановления пациента, при одновременном упрощении способа гипертермического воздействия. Это обеспечивается тем, что в заявляемом способе гипертермическому воздействию подвергают область ЗНО без разрушения целостности кости, т.е. не проводят резецирования кости, как это делается, например, в аналогах [12, 13] и в прототипе [14]. Для этого согласно изобретению область гипертермического воздействия на трубчатой кости охватывают со всех сторон гибким поверхностным нагревателем, обвивая ее этим нагревателем, выполненным, например, в виде ленты. Или вокруг трубчатой кости накладывают несколько гибких поверхностных нагревателей, выполненных, например, в виде пластин, при этом концы каждого из нагревателей соединяют друг с другом таким образом, что каждый из нагревателей образует кольцо вокруг кости (то есть охватывает кость). Если гипертермическому воздействию подвергают плоскую кость, то гибкие поверхностные нагреватели (2 и более) накладывают на противоположные стороны кости, при этом гибкие поверхностные нагреватели фиксируют к плоскости кости и/или между собой. Таким образом, в способе согласно изобретению гипертермическое воздействие осуществляют с помощью гибких поверхностных нагревателей, которые полностью охватывают область гипертермического воздействия на кости, при этом площадь и объем опухоли не имеет значения. Согласно изобретению гибкие поверхностные нагреватели выполняют разного размера и формы (например, в виде пластины или ленты), что позволяет обеспечить соответствие площади области гипертермического воздействия и площади гибких поверхностных нагревателей. Согласно изобретению нагрев области гипертермического воздействия на кости проводят до значений температуры не менее 70°С в течение времени не менее 30 минут. Такие параметры высокотемпературного воздействия согласно [15. Fan QY, Zhou Y, Zhang M, Ma В, Yang T, Long H, Yu Z, Li Z. Microwave ablation of malignant extremity bone tumors. Springerplus. 2016 Aug 20;5(1): 1373. doi: 10.1186/s40064-016-3005-8. eCollection 2016. PubMed PMID: 27606161; PubMed Central PMCID: PMC4992478.] позволяют уничтожить опухолевые клетки, не оказав при этом существенного повреждающего воздействия на коллагеновые и минеральные структуры кости и тем самым позволяют сохранить основные прочностные характеристики кости, что, в свою очередь, дает возможность для хорошей ревитализации (восстановления, оживления) кости, подвергнутой высокотемпературному воздействию, что также отмечено и в аналоге [13]. Кроме того в источнике [15] и в источнике [16. Agarwal М. CORR Insights(®): Is Limb Salvage With Microwave-induced Hyperthermia Better Than Amputation for Osteosarcoma of the Distal Tibia? Clin Orthop Relat Res. 2017 Jun; 475(6): 1678-1680. doi: 10.1007/sl 1999-017-5305-x. Epub 2017 Mar 6. PubMed PMID: 28265886; PubMed Central PMCID: PMC5406351.] отмечено, что высокотемпературное воздействие снижает прочностные характеристики кости, поэтому его следует проводить при определенной температуре. Согласно заявляемому изобретению температура воздействия составляет не менее 70°С. Требуемая температура обеспечивается тем, что в заявляемом способе гибкие поверхностные нагреватели соединяют с блоком стабилизации температуры, который поддерживает заданную температуру путем регулирования энергии, поступающей в нагреватели. Наблюдение за температурой воздействия в режиме реального времени осуществляют с помощью термодатчика, который вводят внутрикостно через зону кости, не пораженную опухолью, что позволяет дополнительно контролировать температуру воздействия во время операции. Кроме того в заявляемом способе обратная поверхность гибких пластинчатых нагревателей прилегает к окружающим тканям, вызывая их прогрев, обеспечивая появление радиосенсибилизации этих тканей, создавая тем самым хорошую основу для интраоперационного лучевого воздействия на ложе опухоли. Кроме того, заявляемый способ обеспечивает повышение чувствительности тканей к химиопрепаратам в рамках курсового применения химиотерапии. Таким образом, заявляемый способ позволяет провести высокотемпературную обработку опухоли кости с минимальным повреждающим воздействием на кость, что создает хорошие условия для последующей ревитализации области кости, подвергнутой высокотемпературному воздействию и снизить восстановительный послеоперационный период для пациента. Кроме того заявляемый способ является более простым и следовательно более доступным для широкого применения, так как гипертермическому воздействию подвергают область кости с ЗНО без разрушения целостности кости, т.е. не проводят резецирования кости, как это делается, например, в аналогах [12, 13] и в прототипе [14]. Все вышеизложенное позволяет говорить об эффективности заявляемого способа интраоперационного гипертермического воздействия на костную ткань.
Изобретение для специалиста явным образом не следует из уровня техники и соответствует, по мнению заявителей, требованиям критерия патентоспособности «изобретательский уровень».
Способ поясняется чертежами и примерами конкретного выполнения, в которых высокотемпературному воздействию подвергалась трубчатая кость фиг. 1, 2, а во втором случае - плоская кость фиг. 3.
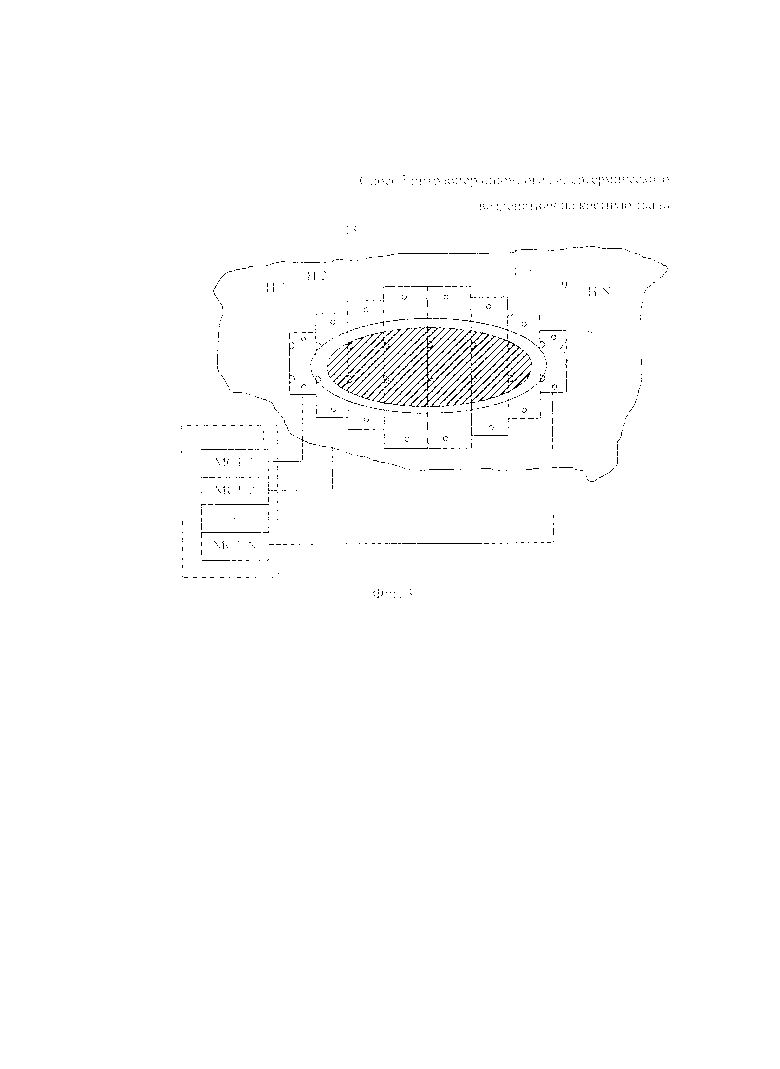
На фиг. 1 схематично показана реализация способа, где пораженную область трубчатой кости подвергают гипертермическому воздействию путем ее охвата несколькими гибкими поверхностными нагревателями, каждый из которых выполнен в виде пластины, образующей кольцо вокруг трубчатой кости. На фиг. 2 схематично показана реализация способа, где пораженную область трубчатой кости подвергают гипертермическому воздействию путем ее охвата гибким поверхностным нагревателем, выполненным в виде ленты, навитой на трубчатую кость. На фиг. 3 схематично показана реализация способа, где пораженную область плоской кости подвергают гипертермическому воздействию путем наложения гибких поверхностных нагревателей, выполненных в виде пластин, на одну из сторон плоской кости. Наложение пластин на другую сторону плоской кости выполнено симметрично и на фиг. 3 не показано.
Заявляемый способ может быть реализован с помощью комплекса 1 для высокотемпературного воздействия на биологическую ткань, показанного на фиг. 1. Комплекс 1 содержит модуль управления 2, блок стабилизации температуры (БСТ) 3 и N гибких поверхностных нагревателей Н-1, H-2, … H-N. Блок стабилизации температуры 3 состоит из N модулей стабилизации температуры МСТ-1, MCT-2, … MCT-N, каждый из которых соединен с соответствующим гибким поверхностным нагревателем Н-1, Н-2, … H-N. Управляющие воздействия У1-УN от модуля управления 2 подаются соответственно на каждый из модулей стабилизации температуры МСТ-1, МСТ-2, … MCT-N. Пораженная ЗНО область кости (трубчатой или плоской) обозначена позицией 4. Вокруг нее расположена область гипертермического воздействия 5. Отверстие 6, выполненное в здоровой области трубчатой кости 12, предназначено для введения термодатчика 7, соединенного с дисплеем 8 (при необходимости термодатчик 7 вводят и в плоскую кость 13 - на фиг. 3 не показано). Позицией 9 на фиг. 3 обозначены специальные сцепные устройства, предназначенные для соединения выполненных в виде пластин поверхностных нагревателей Н-1, H-2, … H-N друг с другом. Позицией 10 обозначены крепежные отверстия, предназначенные для крепления поверхностных нагревателей Н-1, Н-2, … Н-N к соответствующей поверхности кости. Позицией 11 на фиг. 2 обозначен гибкий поверхностный нагреватель, выполненный в виде ленты. Позицией 12 на фиг. 1-2 схематично обозначена трубчатая кость, а позицией 13 на фиг. 3 - фрагмент плоской кости.
Заявляемый способ технически может быть реализован следующим образом. Определяют (например, при помощи рентгенологического, томографического или ультразвукового исследования) место расположения области кости 4, пораженной ЗНО. После этого пациента готовят к оперативному вмешательству стандартным способом. После проведения анестезии и разреза в необходимой области осуществляют скелетирование кости, пораженной опухолью, таким образом, чтобы обеспечить доступ к пораженной ЗНО области кости 4 и к здоровой костной ткани, не менее чем на 1 см в каждую сторону от пораженной области 4, формируя, таким образом, область высокотемпературного воздействия 5. Мягкие ткани, сосуды и нервы, окружающие область гипертермического воздействия 5, теплоизолируют от гибких поверхностных нагревателей Н-1, H-2, … H-N с помощью термоизоляционного материала. При необходимости слежения за температурой в области высокотемпературного воздействия 5 в режиме реального времени в тело трубчатой или плоской кости устанавливают термодатчик 7, соединенный с дисплеем 8.
Область высокотемпературного воздействия 5 (в случае поражения ЗНО трубчатой кости) охватывают гибкими поверхностными нагревателями Н-1, H-2, … H-N, соединенными с соответствующими модулями стабилизации температуры МСТ-1, МСТ-2, … MCT-N, путем наложения каждой пластины гибкого поверхностного нагревателя вокруг кости. При этом концы каждой пластины нагревателя соединяют друг с другом таким образом, что каждая из пластин гибкого поверхностного нагревателя образует кольцо вокруг кости - фиг. 1. Трубчатую кость, пораженную опухолью, можно также охватить гибким поверхностным нагревателем 11, выполненным в виде ленты, как показано на фиг. 2. При этом гибким поверхностным нагревателем 11 обвивают область высокотемпературного воздействия 5, осуществляя сцепление витков друг с другом с помощью специальных сцепных устройств 9.
При гипертермическом воздействии на плоскую кость (фиг. 3) осуществляют наложение поверхностных нагревателей Н-1, H-2, … H-N на область высокотемпературного воздействия 5 таким образом, чтобы обеспечить максимальное соответствие площади и формы области гипертермического воздействия кости 5 с площадью гибких поверхностных нагревателей Н-1, H-2, … H-N. На противоположной стороне плоской кости симметрично располагают другие поверхностные нагреватели (на фиг. 3 не показано). В необходимых случаях (в зависимости от формы и площади пораженной ЗНО области кости 4) можно использовать несколько поверхностных нагревателей Н-1, H-2, … H-N одного или различных размеров. Для соединения гибких поверхностных нагревателей Н-1, Н-2, … H-N друг с другом используются специальные сцепные устройства 9. Гибкие поверхностные нагреватели Н-1, H-2, … H-N фиг. 3 имеют крепежные отверстия 10 для обеспечения их крепления к поверхности плоской кости.
После установки всех поверхностных нагревателей Н-1, H-2, … H-N на область высокотемпературного воздействия 5 осуществляют включение соответствующих модулей стабилизации температуры МСТ-1, МСТ-2, … MCT-N комплекса 1 для осуществления гипертермического воздействия на костную ткань. Модуль управления 2, по заданию оператора, подает управляющие воздействия У1, У2, … УN, задающие температуру стабилизации, на соответствующие модули стабилизации температуры МСТ-1, МСТ-2, … MCT-N. При этом заданная температура стабилизации поверхностных нагревателей Н-1, H-2, … H-N, обеспечивает температуру в области гипертермического воздействия 5 не менее 70°С. Общее время высокотемпературного воздействия составляет не менее 30 минут, при этом нагрев кости до температуры не менее 50°С обеспечивается за время, не превышающее 8-12 минут. Заявителями и авторами экспериментально установлено, что эффективное высокотемпературное воздействие на костную ткань реализуется при температуре не менее 70°С в течение времени не менее 30 минут. При более низких значениях температуры и времени воздействия эффективность разрушения (гибели) раковых клеток снижается, об этом же говорится также в источниках [15, 16]. После завершения сеанса гипертермического воздействия из раны удаляют все вспомогательные материалы, гибкие поверхностные нагреватели, термодатчик. Проводят этапный гемостаз, рану промывают раствором антисептика. В рану устанавливают трубчатый дренаж и зашивают послойно.
Таким образом, конкретные параметры высокотемпературного воздействия в заявляемом способе определены экспериментально и не противоречат сложившейся практике локального интраоперационного гипертермического воздействия на костную опухоль. Приведенный пример реализации способа высокотемпературного воздействия на ЗНО кости не исключает использования для этой цели других устройств (например, использование изобретения по патенту РФ №2636877 «Комплекс для высокотемпературного воздействия на биологическую ткань» по второму варианту). Изобретение промышленно применимо. Заявляемый способ является простым с точки зрения его применения, так как его реализация возможна с помощью известных и доступных устройств и блоков с достижением указанного технического результата.
Таким образом, заявляемый способ интраоперационного гипертермического воздействия на костную ткань, реализованный с помощью комплекса 1 для высокотемпературного воздействия на биологическую ткань, позволяет прогреть большую площадь и объем кости, пораженной ЗНО, на всю глубину до температуры и в течение времени, необходимых для уничтожения опухолевых клеток, сохраняя при этом прочностные характеристики кости. Заявляемый способ является более простым по сравнению с прототипом [14] и аналогами [12, 13], так как согласно изобретению в нем отсутствует такое сложное действие как резецирование и протезирование пораженного ЗНО участка кости. Это делает заявляемый способ, с одной стороны, менее травматичным для пациента и способствует его более быстрому выздоровлению, а, с другой стороны, обеспечивает возможность его широкого использования, что свидетельствует об эффективности заявляемого способа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕАЛИЗАЦИИ ТЕРМОАБЛЯЦИИ ОПУХОЛИ КОСТЕЙ | 2013 |
|
RU2527363C1 |
| КОМПЛЕКС ДЛЯ ВЫСОКОТЕМПЕРАТУРНОГО ВОЗДЕЙСТВИЯ НА БИОЛОГИЧЕСКУЮ ТКАНЬ (варианты) | 2016 |
|
RU2636877C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА ЯЗЫКА | 2009 |
|
RU2405462C2 |
| СПОСОБ РЕАЛИЗАЦИИ ЛОКАЛЬНОЙ ГИПЕРТЕРМИИ | 2011 |
|
RU2467720C1 |
| СПОСОБ ПРОФИЛАКТИЧЕСКОЙ ФИКСАЦИИ ПРОКСИМАЛЬНОГО ОТДЕЛА БЕДРЕННОЙ КОСТИ С ЦЕМЕНТНОЙ ПЛАСТИКОЙ ПОСЛЕ РАДИОЧАСТОТНОЙ АБЛЯЦИИ ПРИ МЕТАСТАТИЧЕСКОМ ПОРАЖЕНИИ И УГРОЗЕ ПАТОЛОГИЧЕСКОГО ПЕРЕЛОМА | 2013 |
|
RU2553497C1 |
| СПОСОБ ПРОТИВООПУХОЛЕВОЙ ИММУНОТЕРАПИИ | 2012 |
|
RU2530523C2 |
| СПОСОБ КОМБИНИРОВАННОГО ЛЕЧЕНИЯ РАКА ЯЗЫКА | 2010 |
|
RU2458651C2 |
| СПОСОБ ЛОКАЛЬНОЙ ДЕСТРУКЦИИ ПЕРВИЧНЫХ И МЕТАСТАТИЧЕСКИХ НОВООБРАЗОВАНИЙ ОРГАНОВ БРЮШНОЙ ПОЛОСТИ И ЗАБРЮШИННОГО ПРОСТРАНСТВА С ЛАПАРОСКОПИЧЕСКИМ ДОСТУПОМ | 2021 |
|
RU2770279C1 |
| Способ альтернативного лечения инсулин-продуцирующей доброкачественной опухоли поджелудочной железы | 2015 |
|
RU2613717C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ НА ОСНОВЕ КОНФОРМНОЙ КОНТАКТНОЙ ТЕРМОАБЛЯЦИИ | 2022 |
|
RU2785891C1 |

Изобретение относится к медицине, а именно к онкологии, и может быть использовано для интраоперационного гипертермического воздействия на костную ткань. Для этого устанавливают место расположения и размер опухоли кости. Далее определяют область гипертермического воздействия, включающую область кости, пораженную опухолью и не менее 1 см здоровой костной ткани. Скелетируют кость в области гипертермического воздействия. После этого на область гипертермического воздействия кости накладывают соединенные с блоком стабилизации температуры гибкие поверхностные нагреватели, охватывая эту область кости со всех сторон. Осуществляют нагрев области гипертермического воздействия кости до значений температуры не менее 70°С. При этом в течение первых 8-12 минут температуру поднимают до величины не менее 50°С, а общее время высокотемпературного воздействия составляет не менее 30 минут. При этом заданную температуру стабилизируют в течение всего времени высокотемпературного воздействия на заданном уровне. Способ обеспечивает эффективную равномерную стабильную высокотемпературную абляцию кости, пораженной злокачественным новообразованием, имеющую большую площадь и объем при упрощении способа, снижении его травматичности. 7 з.п. ф-лы, 3 ил.
1. Способ интраоперационного гипертермического воздействия на костную ткань, заключающийся в том, что устанавливают место расположения и размер опухоли кости, осуществляют высокотемпературное воздействие на костную ткань, пораженную опухолью, отличающийся тем, что после установления места расположения и размера опухоли кости определяют область гипертермического воздействия, включающую область кости, пораженную опухолью, и не менее 1 см здоровой костной ткани, скелетируют кость в области гипертермического воздействия, после чего на область гипертермического воздействия кости накладывают соединенные с блоком стабилизации температуры гибкие поверхностные нагреватели, охватывая эту область кости со всех сторон, и осуществляют нагрев области гипертермического воздействия кости до значений температуры не менее 70°С, причем в течение первых 8-12 минут температуру поднимают до величины не менее 50°С, а общее время высокотемпературного воздействия составляет не менее 30 минут, при этом заданную температуру стабилизируют в течение всего времени высокотемпературного воздействия на заданном уровне.
2. Способ по п. 1, отличающийся тем, что мягкие ткани, сосуды и нервы, окружающие область гипертермического воздействия, теплоизолируют от гибких поверхностных нагревателей с помощью термоизоляционного материала.
3. Способ по п. 1, отличающийся тем, что область гипертермического воздействия трубчатой кости охватывают гибким поверхностным нагревателем со всех сторон путем обвития им трубчатой кости, а концы нагревателя закрепляют на поверхности кости.
4. Способ по п. 3, отличающийся тем, что гибкий поверхностный нагреватель выполняют в виде ленты требуемого размера.
5. Способ по п. 1, отличающийся тем, что область гипертермического воздействия трубчатой кости охватывают гибкими поверхностными нагревателями путем наложения каждого нагревателя вокруг кости, при этом концы каждого из нагревателей соединяют друг с другом таким образом, что каждый из нагревателей образует кольцо вокруг кости.
6. Способ по п. 1, отличающийся тем, что область гипертермического воздействия плоских костей охватывают 2 и более гибкими поверхностными нагревателями, каждый из которых накладывают на противоположные стороны кости, при этом гибкие поверхностные нагреватели фиксируют к плоскости кости и/или между собой.
7. Способ по пп. 5, 6, отличающийся тем, что гибкие поверхностные нагреватели выполняют в виде пластин разного размера и формы для обеспечения соответствия площади области гипертермического воздействия кости и площади гибких поверхностных нагревателей.
8. Способ по п. 1, отличающийся тем, что для регистрации температуры гипертермического воздействия в режиме реального времени на пораженную опухолью кость в нее через отверстие, выполненное в здоровой области кости, вводят термодатчик, соединенный с дисплеем.
| ХУТОРНОЙ А.Ю | |||
| "Электронное устройство для высокотемпературного разрушения патологических образований ткани кости" - автореферат диссертации на соиск | |||
| уч | |||
| ст | |||
| к.т.н., Томск, 2014 | |||
| КОМПЛЕКС ДЛЯ ВЫСОКОТЕМПЕРАТУРНОГО ВОЗДЕЙСТВИЯ НА БИОЛОГИЧЕСКУЮ ТКАНЬ (варианты) | 2016 |
|
RU2636877C1 |
| Способ получения гексаалкилдисилоксанов | 1957 |
|
SU110968A1 |
| СПОСОБ РЕАЛИЗАЦИИ ТЕРМОАБЛЯЦИИ ОПУХОЛИ КОСТЕЙ | 2013 |
|
RU2527363C1 |
| US 6478793 B1, 12.11.2002 | |||
| JP 2010143923 A, 01.07.2010 | |||
| АНТИБАКТЕРИАЛЬНЫЕ ПРОИЗВОДНЫЕ ХИНОЛИНА | 2007 |
|
RU2446159C2 |
| CN 204909726 U, 30.12.2015 | |||
| КОБЗЕВ А.В | |||
| и др | |||
| "Управление электронными игольчатыми нагревателями при реализации метода локальной гипертермии и его экспериментальная проверка" // "Доклады ТУСУРа", N2(22), часть 2, декабрь 2010 г., стр.300-302 | |||
| LU S et al | |||
| "Limb salvage in primary malignant bone tumors by intraoperative microwave heat treatment" | |||
| Chin Med J (Engl) | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| LU S et al | |||
| "Microwave heating and neoadjuvant chemotherapy for malignant bone tumor" | |||
| Zhonghua Wai Ke Za Zhi | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
Авторы
Даты
2019-07-22—Публикация
2018-07-13—Подача