Область техники.
Изобретение относится к области медицины в частности к ортопедии, и может быть использовано для диагностики состояния при лечении больных с септическими артритами или инфекционными осложнениями после эндопротезирования суставов.
Уровень техники.
Известен способ гистологической экспресс-диагностики инфекции после эндопротезирования суставов (источник [1]: Feldman D.S., Lonner J.H., Desai P., Zuckerman J.D., опубл. в J BoneJointSurgAm. 1995; 77A: 1807-1813.), который проводится во время выполнения хирургического вмешательства и включает в себя забор периартикулярных тканей, в которых идентифицируют полиморфноядерные лейкоциты. В случае выявления более 5 полиморфноядерных лейкоцитов диагностируют наличие инфекции
Однако данный способ [1] предусматривает работу непосредственно с инфицированными тканями и не позволяет проводить малоинвазивную диагностику в предоперационном периоде.
Известен способ выбора тактики хирургического лечения больных с периимплантным воспалением в области крупных суставов (источник [2]: патент RU 2506592), где описан способ цитологического исследования (фибробластов, фиброцитов, остеобластов и синовиоцитов) отделяемого из свищевого отделяемого или пунктата перипротезной области. Сущность способа состоит в том, что проводят исследование материала, отобранного из очага поражения, а именно отделяемого из свища или пунктата из перипротезной области, каплю которого наносят на предметное стекло, высушивают и проводят цитологическое исследование при световой микроскопии. При наличии в исследуемом материале клеток фибробластов и фиброцитов по 1-3 в каждом поле зрения, остеобластов по 1-2 в редких полях зрения и синовиоцитов, расположенных в группах по 3-10 клеток, выбирают ревизионное эндопротезирование, а при наличии клеток фибробластов, фиброцитов, остеобластов по 1-2 в редких полях зрения, разрозненных синовиоцитов с дистрофическими изменениями по 1-2 в редких полях зрения, а также клеток остеокластов по 1-3 в препарате, выбирают резекционную артропластику.
Однако исследование с помощью данного способа [2] не учитывает, что цитологический состав свищевого (или раневого) отделяемого и клеточный состав периартикулярного экссудата могут существенно отличаться, особенно в случаях поражения гнойно-воспалительным процессом тазобедренного сустава из-за наличия большого массива околосуставных тканей. Кроме того данный способ не предусматривает количественной оценки клеточного состава забираемого экссудата в определенном объеме исследуемой жидкости и не позволяет объективно оценить степень контаминации сустава и периартикулярных тканей. В совокупности это снижает диагностические возможности известного способа.
Техническая проблема заключается, в том, что существующие способы не позволяют проводить малоинвазивную диагностику в предоперационном периоде, не позволяют объективно оценить степень контаминации сустава и периартикулярных тканей, не позволяют на основе диагностики выбрать технику хирургического лечения обеспечивающую снижение риска послеоперационных инфекционных осложнений.
Сущность технического решения.
Задачей, на решение которой направлено изобретение, является разработка способа, расширяющего диагностические возможности при оценке степени инфекционной контаминации сустава и периартикулярных тканей.
Технический результат - определение степени контаминации инфицированного сустава обеспечивающее возможность выбора техники хирургического лечения позволяющей снизить риск послеоперационных инфекционных осложнений.
Указанная задача решается тем, что в способе определения степени инфекционной контаминации сустава у больных с септическим артритом или перипротезной инфекцией (инфекционных осложнениях после эндопротезирования суставов) для обоснованного выбора необходимого хирургического лечения, включающем забор периартикулярного экссудата с последующим проведением его лабораторного исследования, изъятую жидкость периартикулярного экссудата делят на три части для проведения трех лабораторных исследований: определения уровня лейкоцитоза, определения процентного содержания нейтрофилов и определения концентрации колоний патогенного микроорганизма в объеме исследуемой жидкости и при установлении следующих значений:
- уровня лейкоцитов - менее 10000×10/9 мкл.;
- уровня нейтрофилов - менее 80%;
- концентрации колоний патогенного микроорганизма - менее 10*4 КОЕ/мл;
диагностируют слабую степень контаминации инфицированного сустава;
- уровня лейкоцитов - от 10000 до 20000×10/9 мкл.;
- уровня нейтрофилов - от 80 до 90%;
- концентрации колоний патогенного микроорганизма - от 10*4 до 10*5 КОЕ/мл
диагностируют среднюю степень контаминации инфицированного сустава;
- уровня лейкоцитов - более 20000×10/9 мкл.;
- уровня нейтрофилов - более 90%;
- концентрации колоний патогенного микроорганизма - более 10*5 КОЕ/мл;
диагностируют тяжелую степень контаминации инфицированного сустава. В зависимости от того какой является степень контаминации инфицированного сустава слабой, средней, или тяжелой выбирают хирургическую технику обеспечивающую снижение риска послеоперационных инфекционных осложнений.
Указанная сущность позволяет определить степень контаминации инфицированного сустава. Определение степени инфекционной контаминации сустава, в предоперационном и интраоперационном периодах, позволяет хирургу осуществить выбор необходимого хирургического пособия в каждом конкретном случае. В целом это расширяет диагностические возможности при оценке степени инфекционной контаминации сустава у больных с септическим артритом и перипротезной инфекцией. Это возможность осуществить малоинвазивной диагностику состояния сустава пациента в предоперационном периоде, провести необходимые подготовительные мероприятия к оперативному лечению и провести удаление компонентов инфицированного эндопротеза и реэндопротезирование снизив риск возможных осложнений.
Способ поясняется описанием, примером практического использования и иллюстрациями, на которых изображено:
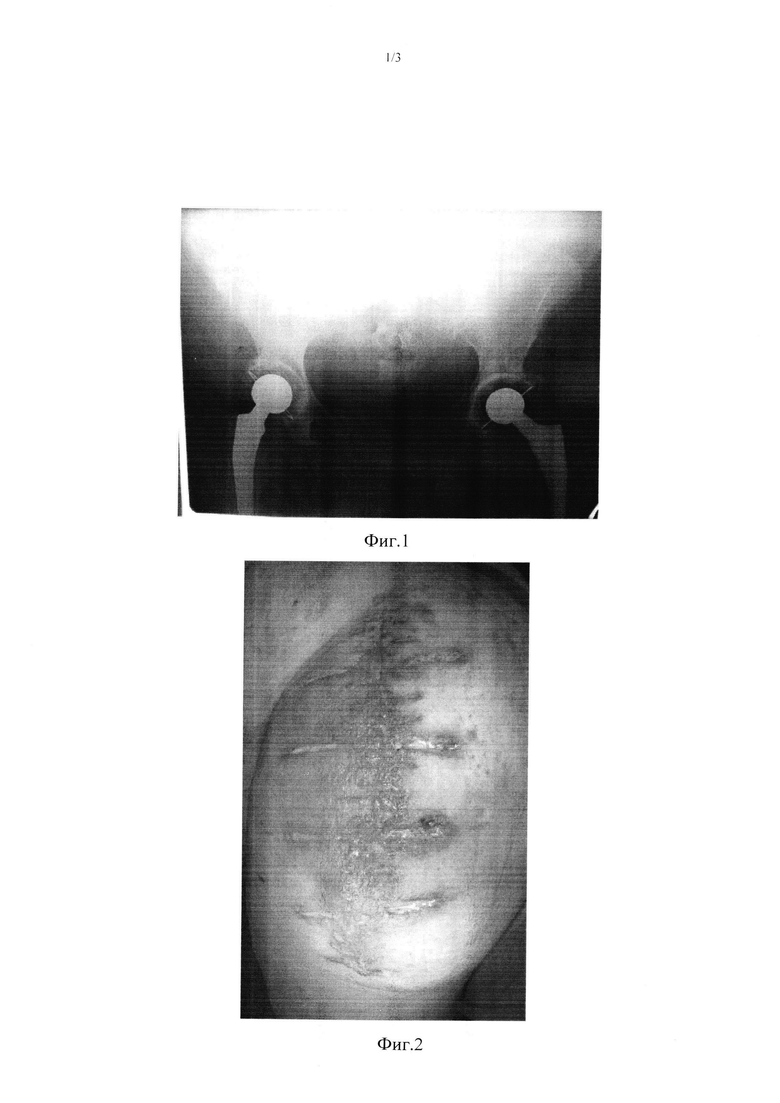
Фиг. 1 - рентгенограмма таза до лечения больной К. 57 лет;
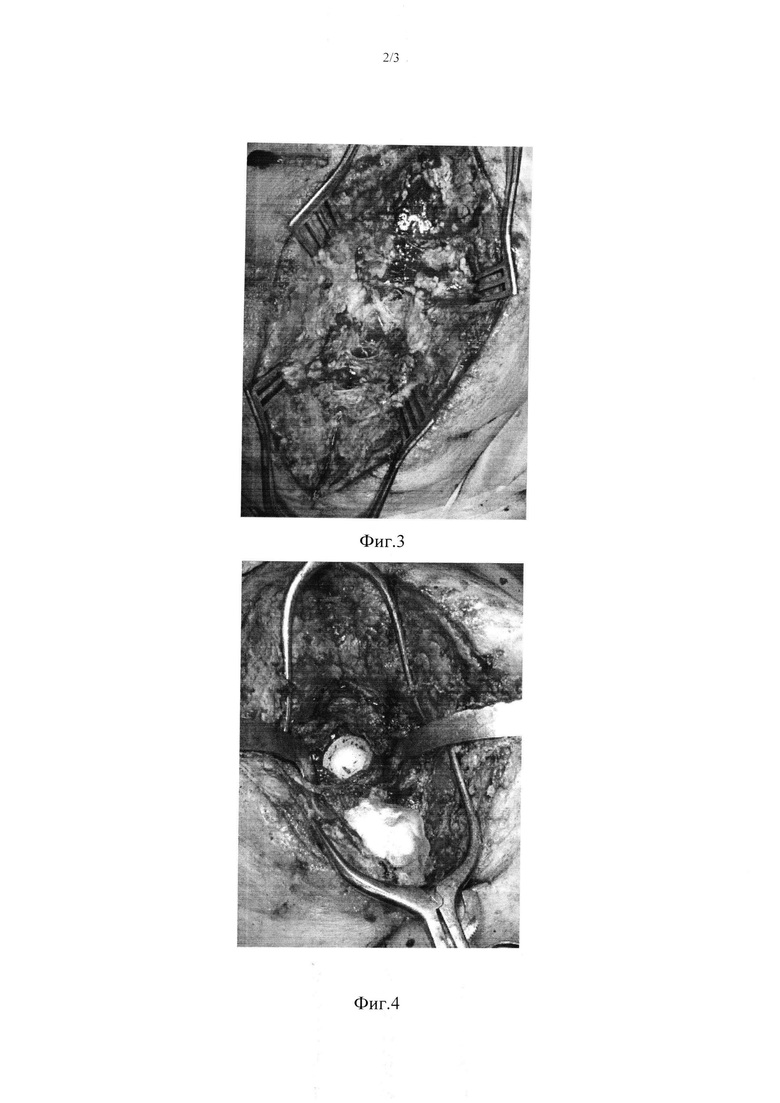
Фиг. 2 - локальный статус левого тазобедренного сустава;
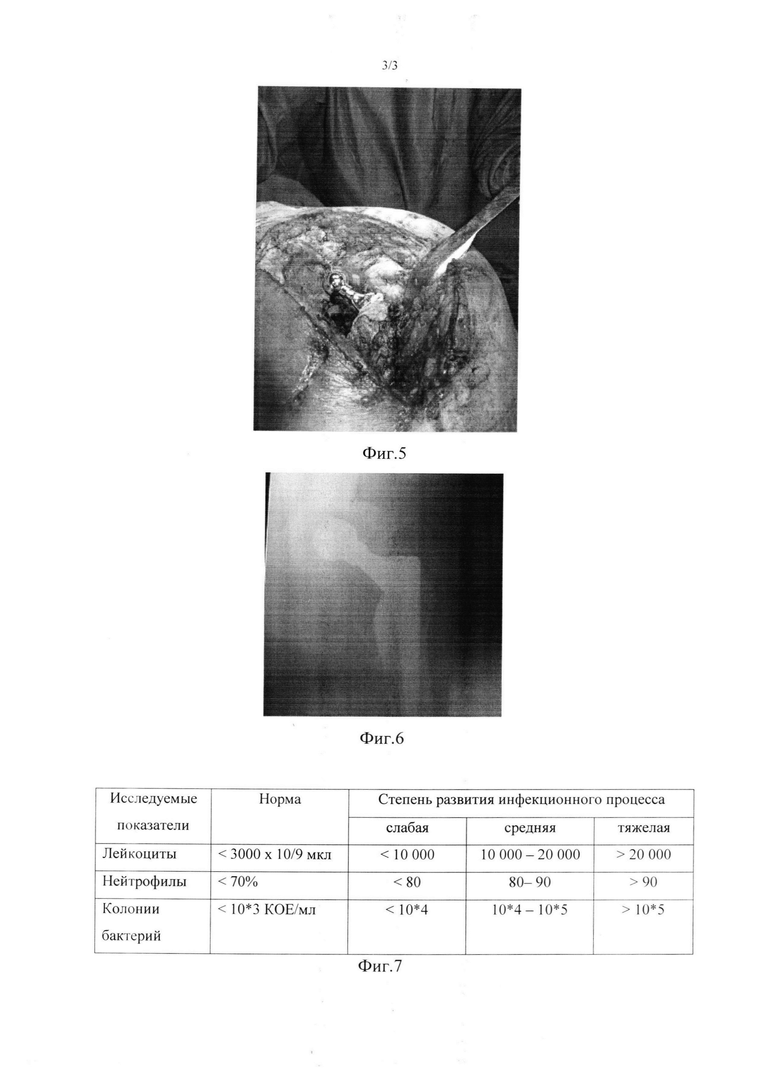
Фиг. 3 - артротомия тазобедренного сочленения;
Фиг. 4 - удаление компонентов инфицированного эндопротеза и хирургическая обработка тканей;
Фиг. 5 - имплантация цементного эндопротеза;
Фиг. 6 - рентгенограмма левого тазобедренного сустава после лечения;
Фиг. 7 - таблица, сводные данные показателей степени инфекционной контаминации сустава у больных с септическим артритом и перипротезной инфекцией.
Способ осуществляется следующим образом.
Способ осуществляется как в предоперационном периоде посредством диагностической пункции, так и непосредственно в ходе выполнения ревизионного вмешательства при лечении больных с септическим артритом или перипротезной инфекцией, инфекционными осложнениями после эндопротезирования суставов. Известными приемами выполняют артроцентез и забор жидкости периартикулярного экссудата. Далее, проводят лабораторное исследование изъятой жидкости с определением уровня лейкоцитоза и процентного содержания нейтрофилов, а так же концентрации колоний патогенного микроорганизма в объеме исследуемой жидкости периартикулярного экссудата. Изъятую жидкость периартикулярного экссудата делят на три части для проведения трех лабораторных исследований. При установлении по результатам лабораторного исследования в жидкости периартикулярного экссудата следующих значений:
- уровня лейкоцитов - менее 10000×10/9 мкл.;
- уровня нейтрофилов - менее 80%;
- концентрации колоний патогенного микроорганизма - менее 10*4 КОЕ/мл;
диагностируют слабую степень контаминации инфицированного сустава;
- уровня лейкоцитов - от 10000 до 20000×10/9 мкл.;
- уровня нейтрофилов - от 80 до 90%;
- концентрации колоний патогенного микроорганизма - от 10*4 до 10*5 КОЕ/мл
диагностируют среднюю степень контаминации инфицированного сустава;
- уровня лейкоцитов - более 20000×10/9 мкл.;
- уровня нейтрофилов - более 90%;
- концентрации колоний патогенного микроорганизма - более 10*5 КОЕ/мл;
диагностируют тяжелую степень контаминации инфицированного сустава.
Выбор необходимого хирургического пособия у больных с септическим артритом и перипротезной инфекцией зависит от степени контаминации инфицированного сустава. Определение слабой, средней, тяжелой, степени инфекционной контаминации сустава, в предоперационном и интраоперационном периодах, позволяет хирургу осуществить выбор необходимого хирургического пособия в каждом конкретном случае и провести удаление компонентов инфицированного эндопротеза и реэндопротезирование снизив риск возможных осложнений.
При исследовании уровня лейкоцитов в пробирку наливают 0,4 мл изотонического или гипотонического раствора NaCI. С помощью семплера или микропипетки вносили 20 мкл периартикулярного экссудата (ПЭ) (разведение 1:20) и аккуратно без пены размешивали. Если ПЭ был мутным с низкой вязкостью, его сразу наносили на предметное стекло. Заполняли камеру Горяева и подсчитывали количество клеточных элементов в 40 больших квадратах. Расчет производили по формуле:
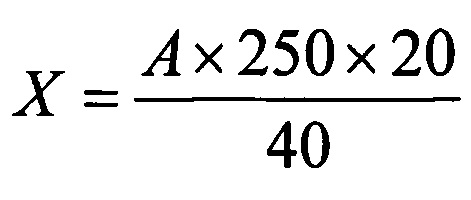 , где
, где
X - количество лейкоцитов в ПЭ;
А - количество клеточных элементов в 40 больших квадратах камеры Горяева;
250 - объем одного большого квадрата камеры;
20 - степень разведения ПЭ.
Оценку процентного соотношения нейтрофилов к общему количеству лейкоцитов осуществляют в следующей последовательности. Препараты для микроскопического исследования готовят из периартикулярного экссудата без центрифугирования. На край предметного стекла наносят каплю периартикулярного экссудата, шлифованным краем другого стекла (или пластиковым шпателем) под углом 45 градусов выравнивают каплю по стеклу. Покровное стекло закрывают каплю осадка без пузырей. Затем из этого осадка готовится мазок для окраски азур-эозином. После покраски препарата подсчитывают количество нейтрофилов и сопоставляют их с общим количеством лейкоцитов.
Родовую и видовую идентификацию выделенных бактериальных культур проводят как традиционным методом (на основании изучения их тинкториальных, культуральных и биохимических свойств), так и при помощи бактериологических анализаторов АТВ Expression ("BioMerieux", Франция) и «WalkAway 40 Plus» ("Siemens", США), с использованием соответствующих микротест систем. Для выделения аэробных и факультативно-анаэробных бактерий используют следующие питательные среды: агар с содержанием 5% крови; желточно-солевой агар; среду Левина; среду Сабуро. Посевы инкубировали при температуре 37о С в течение 24-48 часов. Для определения степени обсемененности посев делят на сектора пластинки питательной среды в чашке Петри, после инкубирования подсчитывают количество колоний каждого типа в секторах, результат выражают через десятичный логарифм величины выросших колоний (КОЕ/мл).
Практическое использование способа иллюстрирует следующее клиническое наблюдение.
Больная К. 57 лет поступила в клинику с диагнозом: острая послеоперационная перипротезная инфекция левого тазобедренного сустава (согласно Tsukayama). Гипертоническая болезнь 3 ст. 2 ст. риск 4. ИБС. Стенокардия напряжения 1 ФК. Гипертрофия левого желудочка. ХСН 2А ФК 2. Ожирение 3 ст. Лимфостаз обеих нижних конечностей. Хроническая железодефицитная анемия легкой степени тяжести. Рентгенологически: состояние после тотального эндопротезирования обоих тазобедренных суставов. Компоненты стабильны. Дефект левого бедра I типа и дефект левой вертлужной впадины I типа по Paprosky (Фиг. 1). Локальный статус: в области левого тазобедренного сустава отмечается гиперемия, отек послеоперационного рубца, обильное серозное отделяемое (Фиг. 2). Произведена диагностическая пункция инфицированного сустава, забор жидкости периартикулярного экссудата, жидкость отправлена на лабораторные, цитологическое и микробиологическое, исследования. По результатам цитологии, уровню лейкоцитов (лейкоцитоз), уровню нейтрофилов (содержание нейтрофилов), концентрации колоний патогенных микроорганизмов (микробиологические результаты аспирационного содержимого): pseudomonas aeruginosa, klebsiella pneumoniae БЛРС, enterococcus faecalis, степень инфекционной контаминации сустава была определена как средняя (см. фиг. 7 таблица). По результатам обследования больной выполнено одноэтапное реэндопротезирование левого тазобедренного сустава с полной заменой компонентов эндопротеза. В ходе операции осуществили доступ к пораженному суставу (Фиг. 3), после чего произвели удаление компонентов эндопротеза и хирургическую обработку тканей сустава (Фиг. 4). Далее имплантировали компоненты цементного эндопротеза (Фиг. 5). Операцию завершили установкой дренажа, послойным ушиванием раны и выполнением контроля рентгенографии (Фиг. 6). В послеоперационном периоде больная получила курс этиотропной терапии в течение 6 недель.
Сопоставление клинической ситуации в каждом конкретном случае с результатами лабораторного исследования периартикулярного экссудата инфицированного сустава, дает возможность выделения трех степеней инфекционной контаминации сустава, которые представлены и описаны в таблице (фиг. 7). Данные таблицы получены опытным путем. Определение степени инфекционной контаминации сустава, в предоперационном и интраоперационном периодах, позволяет хирургу в той или иной степени осуществить выбор необходимого хирургического пособия в каждом конкретном случае. В целом это расширяет диагностические возможности при оценке степени инфекционной контаминации сустава у больных с септическим артритом и перипротезной инфекцией.
Предложенный способ применяется авторами в Центре Илизарова г. Курган.
Практическое использование способа иллюстрируют следующие клинические наблюдения.
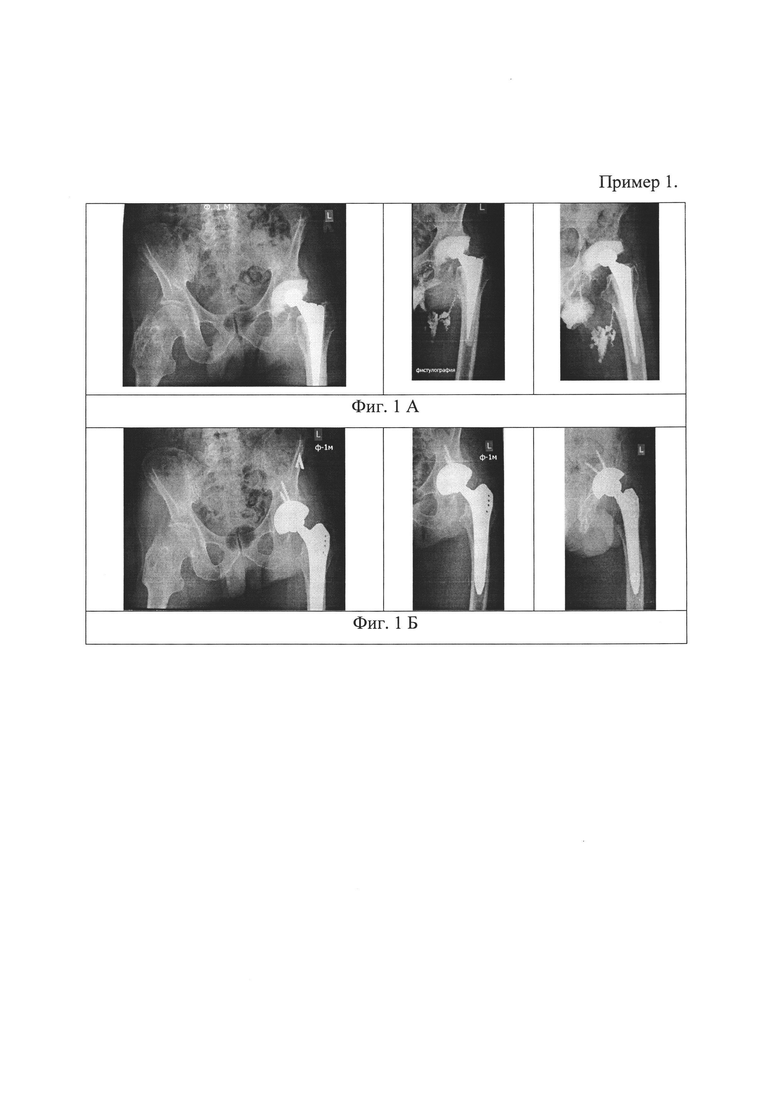
Пример 1. Больной И. 55 лет поступил в клинику с диагнозом: поздняя хроническая перипротезная инфекция тазобедренного сустава (согласно D.T. Tsukayama). Инфицированный спейсер. Хронический гематогенный остеомиелит левого бедра и таза, свищевая форма; Рентгенологически отмечался дефицит костной ткани бедра I типа и вертлужной впадины I типа по Paprosky (Фиг. 1А); Локальный статус: в области левого бедра отмечались два свищевых хода. Для обоснованного выбора необходимого хирургического лечения произведена диагностическая пункция инфицированного сустава, периартикулярная жидкость отправлена на цитологическое и микробиологическое исследования. Жидкость периартикулярного экссудата делили на три части для проведения трех лабораторных исследований: определения уровня лейкоцитоза, определения процентного содержания нейтрофилов и определения концентрации колоний патогенного микроорганизма в объеме исследуемой жидкости. Результаты цитологии: лейкоцитоз - 8425 клеток/мкл., содержание нейтрофилов - 42%; Микробиологический результат аспирационного содержимого - Staphylococcus aureus 10*3 КОЕ/мл. Диагностировали слабую степень контаминации инфицированного сустава. По результатам обследования больному назначено и выполнено удаление инфицированного спейсера, санация гнойно-воспалительного очага и одномоментная установка эндопротеза с шестинедельным курсом этиотропной терапии. Рентгенограммы таза и тазобедренного сустава после проведенного лечения (Фиг. 1Б). Послеоперационных инфекционных осложнений не наблюдалось.
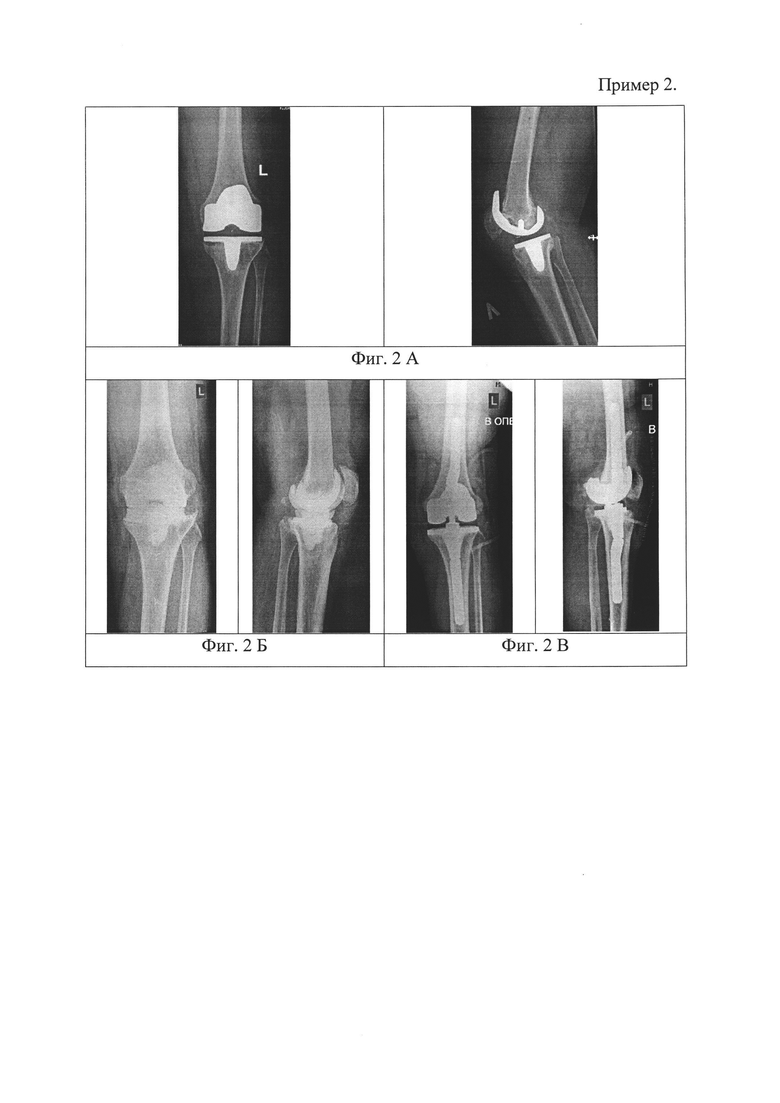
Пример 2. Больная В. 64 лет поступила в клинику с диагнозом: поздняя хроническая перипротезная инфекция коленного сустава (согласно D.T. Tsukayama). Хронический посттравматический остеомиелит левого бедра и большеберцовой кости; Рентгенологически отмечался дефицит костной ткани бедра F 1 и большеберцовой кости Т 1 по AORI (Фиг. 2А); Локальный статус: в области левого коленного сустава отмечался отек и гиперемия мягких тканей. Для обоснованного выбора необходимого хирургического лечения произведена диагностическая пункция инфицированного сустава, периартикулярная жидкость отправлена на цитологическое и микробиологическое исследования. Жидкость периартикулярного экссудата делили на три части для проведения трех лабораторных исследований: определения уровня лейкоцитоза, определения процентного содержания нейтрофилов и определения концентрации колоний патогенного микроорганизма в объеме исследуемой жидкости. Результаты цитологии: лейкоцитоз - 19500 клеток/мкл., содержание нейтрофилов - 83%; Микробиологический результат аспирационного содержимого - Enterobacter cloacae БЛРС 10*4 КОЕ/мл. Диагностировали среднюю степень инфекционной контаминации сустава. По результатам обследования больной назначено и выполнено удаление инфицированного эндопротеза, радикальная хирургическая обработка тканей и установка цементного спейсера в сочетании с курсом антибиотикотерапии в течение 6 недель. Рентгенограммы коленного сустава после операции (Фиг. 2Б) и рентгенограммы после замены цементного спейсера на постоянный эндопротез (Фиг. 2В). Послеоперационных инфекционных осложнений не наблюдалось.
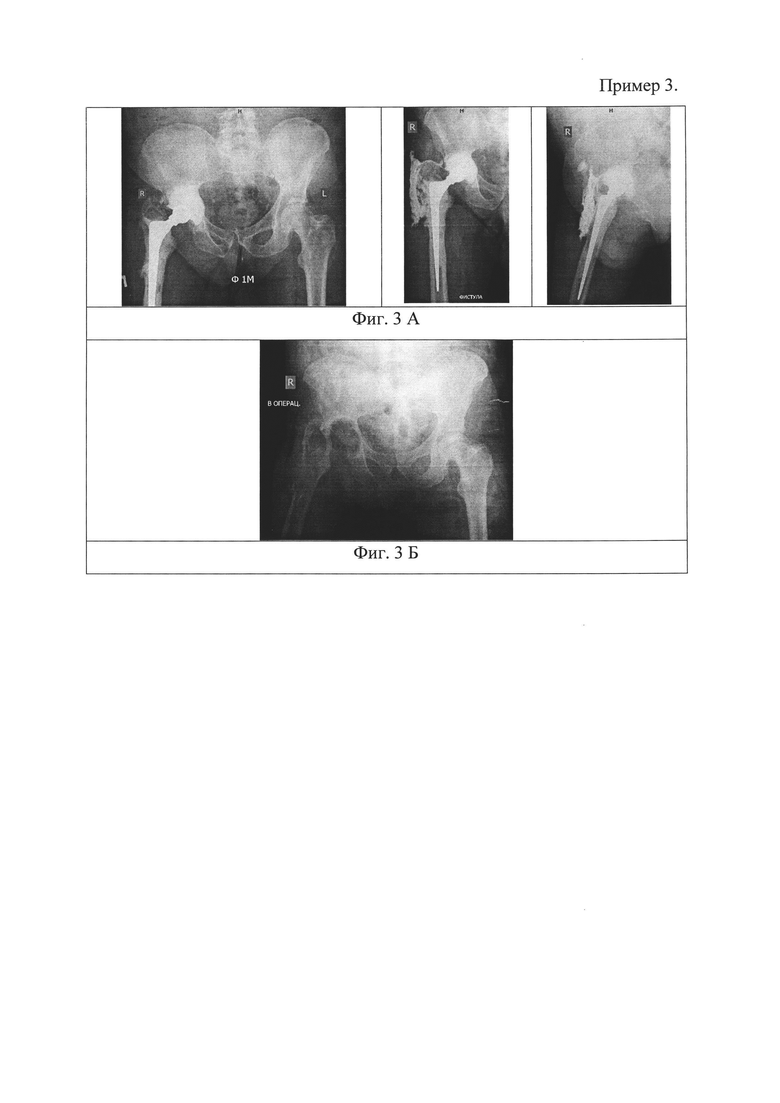
Пример 3. Больной К. 51 года поступил в клинику с диагнозом: поздняя хроническая перипротезная инфекция тазобедренного сустава (согласно D.T. Tsukayama). Инфицированный спейсер. Хронический посттравматический остеомиелит правого бедра и таза, свищевая форма; Рентгенологически отмечался дефицит костной ткани бедра III А типа и вертлужной впадины II С типа по Paprosky (Фиг. 3А); Локальный статус: в области правого бедра отмечался свищ с гнойным отделяемым. Для обоснованного выбора необходимого хирургического лечения, произведена диагностическая пункция инфицированного сустава, периартикулярная жидкость отправлена на цитологическое и микробиологическое исследования. Жидкость периартикулярного экссудата делили на три части для проведения трех лабораторных исследований: определения уровня лейкоцитоза, определения процентного содержания нейтрофилов и определения концентрации колоний патогенного микроорганизма. Результаты цитологии: лейкоцитоз - 46750 клеток/мкл., содержание нейтрофилов - 95%; Микробиологический результат аспирационного содержимого - Enterococcus faecalis 10*5 КОЕ/мл. Степень инфекционной контаминации сустава была определена как тяжелая. Учитывая высокую степень контаминации сустава и неоднократные безуспешные ревизионные вмешательства, больному произведена резекционная артропластика тазобедренного сустава с удаление всех элементов спейсера. Противомикробная терапия составила 6 недель. Рентгенограммы таза после операции (Фиг. 3Б). Послеоперационных инфекционных осложнений не наблюдалось.
Определение степени инфекционной контаминации сустава, в предоперационном и интраоперационном периодах, позволяет хирургу в степени осуществить выбор необходимого хирургического пособия в каждом конкретном случае и снизить послеоперационных риск осложнений.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ подготовки инфицированной периартикулярной раны для имплантации постоянного или временного стабилизирующего устройства | 2018 |
|
RU2712013C1 |
| СПОСОБ ВЫБОРА ТАКТИКИ ЛЕЧЕНИЯ БОЛЬНЫХ С ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ | 2016 |
|
RU2640391C1 |
| Способ определения хирургической тактики ревизионного эндопротезирования крупных суставов при инфекционном осложнении | 2018 |
|
RU2692960C1 |
| Способ определения вида инфекционных и асептических парапротезных/параимплантных послеоперационных осложнений после протезирования крупных суставов | 2020 |
|
RU2766803C2 |
| СПОСОБ ЛЕЧЕНИЯ РАННЕЙ ПАРАПРОТЕЗНОЙ ИНФЕКЦИИ | 2011 |
|
RU2478343C1 |
| Способ выбора тактики ревизионного эндопротезирования крупных суставов | 2018 |
|
RU2691142C1 |
| Способ диагностики перипротезной инфекции у больных с нестабильностью компонентов эндопротезов крупных суставов | 2020 |
|
RU2749685C1 |
| Способ диагностики инфекции при подозрении на инфекцию в области сустава | 2015 |
|
RU2627442C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЦЕМЕНТНОГО СПЕЙСЕРА ДЛЯ ЭТИОТРОПНОЙ МЕСТНОЙ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ ПРИ ИНФЕКЦИОННЫХ ПОРАЖЕНИЯХ КОСТЕЙ И СУСТАВОВ | 2020 |
|
RU2754075C1 |
| Способ прогнозирования инфекционных осложнений при эндопротезировании крупных суставов | 2016 |
|
RU2620047C1 |
Изобретение относится к области медицины и представляет собой способ определения степени инфекционной контаминации сустава у больных с перипротезной инфекцией для обоснованного выбора необходимого хирургического лечения, включающий забор периартикулярного экссудата с последующим проведением его лабораторного исследования, отличающийся тем, что изъятую жидкость периартикулярного экссудата делят на три части для проведения трех лабораторных исследований: определения уровня лейкоцитоза, определения процентного содержания нейтрофилов и определения концентрации колоний патогенного микроорганизма в объеме исследуемой жидкости и при установлении следующих значений:
- уровня лейкоцитов менее 10000×10/9 мкл.; уровня нейтрофилов менее 80%; концентрации колоний патогенных микроорганизмов менее 10*4 КОЕ/мл; диагностируют слабую степень контаминации инфицированного сустава; уровня лейкоцитов от 10000 до 20000×10/9 мкл.; уровня нейтрофилов от 80 до 90%; концентрации колоний патогенного микроорганизма от 10*4 до 10*5 КОЕ/мл; диагностируют среднюю степень контаминации инфицированного сустава; уровня лейкоцитов более 20000×10/9 мкл.; уровня нейтрофилов более 90%; концентрации колоний патогенного микроорганизма более 10*5 КОЕ/мл; диагностируют тяжелую степень контаминации инфицированного сустава. Использование заявленного изобретения позволяет быстро и точно определить степень контаминации инфицированного сустава и осуществить выбор необходимого хирургического пособия в каждом конкретном случае. 7 ил., 3 пр.
Способ определения степени инфекционной контаминации сустава у больных с перипротезной инфекцией для обоснованного выбора необходимого хирургического лечения, включающий забор периартикулярного экссудата с последующим проведением его лабораторного исследования, отличающийся тем, что изъятую жидкость периартикулярного экссудата делят на три части для проведения трех лабораторных исследований: определения уровня лейкоцитоза, определения процентного содержания нейтрофилов и определения концентрации колоний патогенного микроорганизма в объеме исследуемой жидкости и при установлении следующих значений:
- уровня лейкоцитов менее 10000×10/9 мкл.; уровня нейтрофилов менее 80%; концентрации колоний патогенных микроорганизмов менее 10*4 КОЕ/мл; диагностируют слабую степень контаминации инфицированного сустава;
- уровня лейкоцитов от 10000 до 20000×10/9 мкл.; уровня нейтрофилов от 80 до 90%; концентрации колоний патогенного микроорганизма от 10*4 до 10*5 КОЕ/мл; диагностируют среднюю степень контаминации инфицированного сустава;
- уровня лейкоцитов более 20000×10/9 мкл.; уровня нейтрофилов более 90%; концентрации колоний патогенного микроорганизма более 10*5 КОЕ/мл; диагностируют тяжелую степень контаминации инфицированного сустава.
| ТЕПЛЯКОВА О.В | |||
| И ДР | |||
| Септический артрит у взрослых// Клин | |||
| Микробиол | |||
| Антимикроб | |||
| Химиотер | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| КАРБЫШЕВА С.Б | |||
| D-лактат - маркер бактриального воспаления нативных и протезированных суставов// Травматология и ортопедия России | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Способ диагностики инфекции при подозрении на инфекцию в области сустава | 2015 |
|
RU2627442C2 |
Авторы
Даты
2019-07-29—Публикация
2018-10-09—Подача