ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Некоторые варианты осуществления настоящей заявки относятся к новым нуклеозидным или нуклеотидным линкерам для увеличения инкорпорации нуклеотидов в последовательности ДНК и других диагностических применений, например, секвенирования путем синтеза.
УРОВЕНЬ ТЕХНИКИ
[0002] Прогресс в исследовании молекул был достигнут, в частности, путем улучшения технологий, используемых для характеристики молекул или их биологических реакций. В частности, в исследовании нуклеиновых кислот ДНК и РНК были использованы развивающиеся технологии, используемые для анализа последовательностей и изучения событий гибридизации.
[0003] Примером технологий, которые позволили улучшить изучение нуклеиновых кислот, является разработка искусственно полученных чипов иммобилизованных нуклеиновых кислот. Эти чипы, как правило, имеют матрицу полинуклеотидов высокой плотности, иммобилизованную на подложке из твердого материала. См., например, Fodor с соавт., Trends Biotech. 12: 19-26, 1994, где описаны способы сборки различных нуклеиновых кислот с использованием химически сенсибилизированной стеклянной поверхности, защищенной маской, но подверженной воздействию в определенных областях, чтобы можно было прикрепить соответствующим образом модифицированные нуклеотидные фосфорамидиты. Искусственно полученные чипы также могут быть изготовлены с помощью метода "нанесения пятнами" известных полинуклеотидов на твердую подложку в заранее определенных положениях (например, Stimpson с соавт., Proc. Natl. Acad. Sci. 92: 6379-6383, 1995).
[0004] Один из способов определения нуклеотидной последовательности нуклеиновой кислоты, связанной с чипом, называется "секвенированием путем синтеза" или "SBS". Этот метод для определения нуклеотидной последовательности ДНК в идеале требует контролируемой (т.е., последовательной) инкорпорации правильного комплементарного нуклеотида напротив секвенируемой нуклеиновой кислоты. Это позволяет точно определять последовательность путем добавления нуклеотидов в несколько циклов, как если бы каждый нуклеотидный остаток секвенировали по одному, тем самым предотвращая инкорпорацию неконтролируемого ряда нуклеотидов. Каждый инкорпорированный нуклеотид считывается с использованием соответствующей метки, присоединенной к нему, перед удалением фрагмента метки и последовательного следующего этапа секвенирования.
[0005] Соответственно, в контексте реакций секвенирования нуклеиновых кислот было бы желательно иметь возможность увеличить скорость нуклеотидноой инкорпорации во время секвенирования путем синтеза таким образом, чтобы эффективность метода секвенирования могла быть улучшена.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0006] Некоторые варианты осуществления, раскрытые в настоящем описании, относятся к нуклеозиду или нуклеотиду, ковалентно присоединенному к флуорофору через линкер, где указанный линкер содержит структуру формулы (I) или (II), или комбинацию обоих:
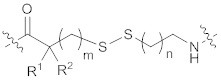 (I),
(I), 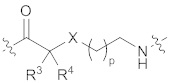 (II),
(II),
каждый из R1 и R2 независимо выбран из водорода или необязательно замещенного C1-6 алкила;
R3 выбран из водорода, необязательно замещенного С1-6 алкила, -NR5-C(=O)R6 или -NR7-C(=O)-OR8;
R4 выбран из водорода или необязательно замещенного C1-6 алкила;
каждый из R5 и R7 независимо выбран из водорода, необязательно замещенного C1-6 алкила, необязательно замещенного фенила или необязательно замещенного C7-12 аралкила;
каждый из R6 и R8 независимо выбран из необязательно замещенного C1-6 алкила, необязательно замещенного фенила, необязательно замещенного C7-12 аралкила, необязательно замещенного C3-7 циклоалкила или необязательно замещенного 5-10-членного гетероарила;
каждое из метиленовых повторяющихся звеньев в 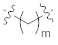 ,
, 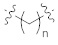 или
или 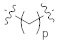 является необязательно замещенным;
является необязательно замещенным;
Х выбран из метилена (СН2), кислорода (О) или серы (S);
m представляет собой целое число от 0 до 20;
n представляет собой целое число от 1 до 20; и
p представляет собой целое число от 1 до 20.
[0007] В некоторых вариантах осуществления меченный флюорофором нуклеозид или нуклеотид, содержащий структуру формулы (I), не имеет структуру:
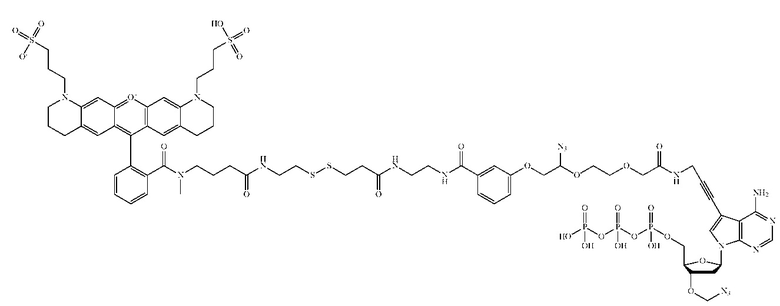
[0008] Некоторые варианты осуществления, раскрытые в настоящем описании, относятся к нуклеозиду или нуклеотиду, ковалентно присоединенному к флуорофору через линкер, в котором указанный линкер содержит структуру формулы (III)
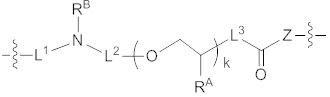 (III)
(III)
где L1 отсутствует или содержит линкер любой структуры, описанной в формуле (I) или (II), или защитный фрагмент, или их комбинации; L2 выбран из необязательно замещенного C1-20 алкилена, необязательно замещенного C1-20 гетероалкилена, необязательно замещенного C1-20 алкилена, прерванного замещенной ароматической группой, или необязательно замещенного C1-20 гетероалкилена, прерванного замещенной ароматической группой; L3 выбран из необязательно замещенного C1-20 алкилена или необязательно замещенного C1-20 гетероалкилена; RA выбран из водорода, циано, гидрокси, галогена, С1-6 алкила, C1-6 алкокси, C1-6 галогеналкила, C1-6 галогеналкокси или азидо, и где, по меньшей мере, одно из повторяющихся звеньев 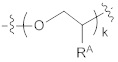 содержит азидогруппу; Z выбран из кислорода (O) или NRB; каждый из RB и RC независимо выбран из водорода или необязательно замещенного C1-6 алкила; и k представляет собой целое число от 1 до 50.
содержит азидогруппу; Z выбран из кислорода (O) или NRB; каждый из RB и RC независимо выбран из водорода или необязательно замещенного C1-6 алкила; и k представляет собой целое число от 1 до 50.
[0009] Некоторые варианты осуществления, раскрытые в настоящем описании, относятся к наборам, содержащим меченый нуклеозид или нуклеотид, содержащий линкер между флуорофором и нуклеозидом или нуклеотидом, где линкер содержит структуру любой из формул (I), (II) или (III), или их комбинации.
[0010] Некоторые варианты осуществления, раскрытые в настоящем описании, относятся к реагентам для модификации нуклеозида или нуклеотида, содержащего флуорофор и линкер, где линкер содержит структуру любой из формул (I), (II) или (III), или их комбинации.
[0011] Некоторые варианты осуществления, раскрытые в данном описании, относятся к способам обнаружения нуклеозида, который был инкорпорирован в полинуклеотид, включающий: (а) инкорпорацию меченого нуклеозида или нуклеотида, содержащего линкер, в полинуклеотид; и (b) обнаружение флуоресцентного сигнала от указанного меченого нуклеозида или нуклеотида, который был инкорпорирован на стадии (а), где линкер содержит структуру любой из формул (I), (II) или (III), или их комбинации. В некоторых вариантах осуществления способ дополнительно включает: предоставление матричной нити нуклеиновой кислоты и частично гибридизированной нити нуклеиновой кислоты, где стадия (а) инкорпорирует в гибридизированную нить, по меньшей мере, один нуклеозид или нуклеотид, который комплементарен нуклеозиду или нуклеотиду в соответствующем положении матричной нити, и где стадия (b) идентифицирует основание инкорпорированного нуклеозида или нуклеотида, таким образом, указывая на идентичность комплементарного нуклеозида или нуклеотида матричной нити.
[0012] Некоторые варианты осуществления, раскрытые в настоящем описании, относятся к способам секвенирования молекулы матричной нуклеиновой кислоты, включающим: инкорпорацию одного или нескольких меченых нуклеотидов в цепь нуклеиновой кислоты, комплементарной матричной нуклеиновой кислоте; определение идентичности основания, присутствующего в одном или нескольких инкорпорированных меченых нуклеотидах для того, чтобы определить последовательность молекулы матричной нуклеиновой кислоты; где идентичность основания, присутствующего в одном или нескольких меченых нуклеотидах, определяют путем детектирования флуоресцентного сигнала, создаваемого указанными мечеными нуклеотидами; и где, по меньшей мере, один инкорпорированный меченый нуклеотид, содержащий линкер, является таким, как описано выше, где линкер содержит структуру любой из формул (I), (II) или (III), или их комбинации. В некоторых вариантах осуществления настоящего изобретения идентичность основания, присутствующего в одном или нескольких нуклеотидах, определяют после каждой стадии инкорпорации нуклеотида.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
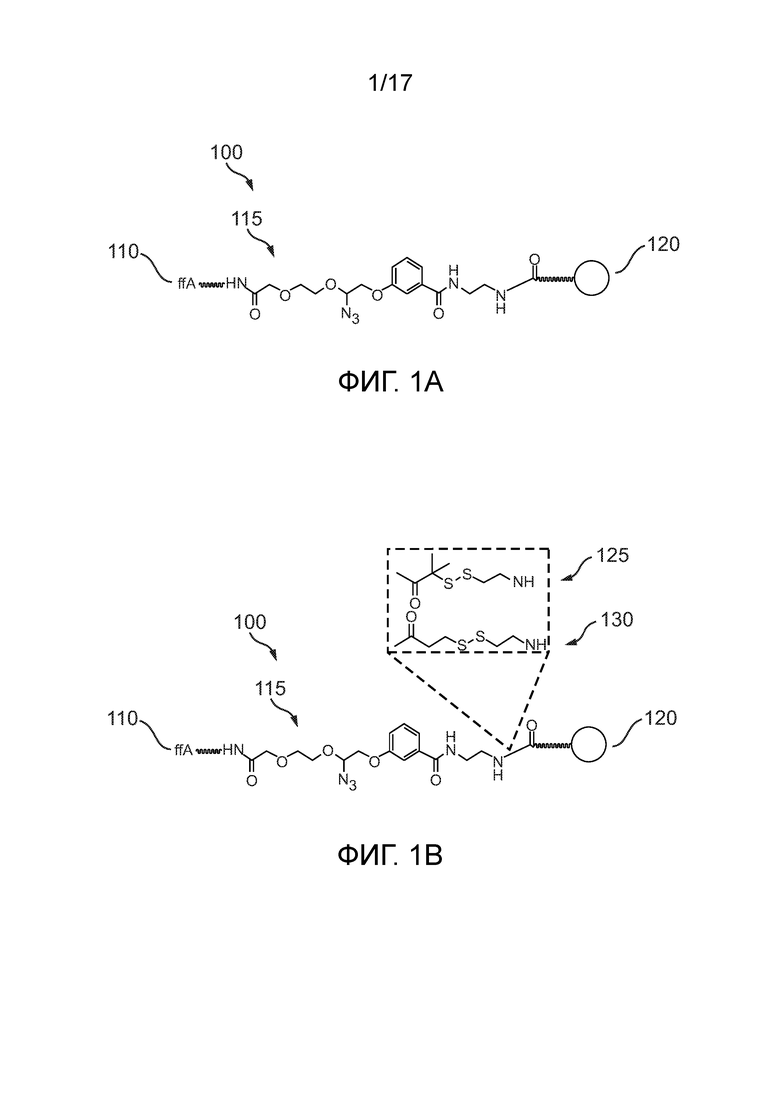
[0013] Фиг. 1А иллюстрирует частичную структурную формулу связывающей группы стандартного меченого нуклеотида.
[0014] Фиг. 1В иллюстрирует меченый нуклеотид, показанный на фиг. 1А, с двумя возможными линкерами 125 и 130, которые вставлены в стандартную связывающую группу, показанную на фиг. 1A.
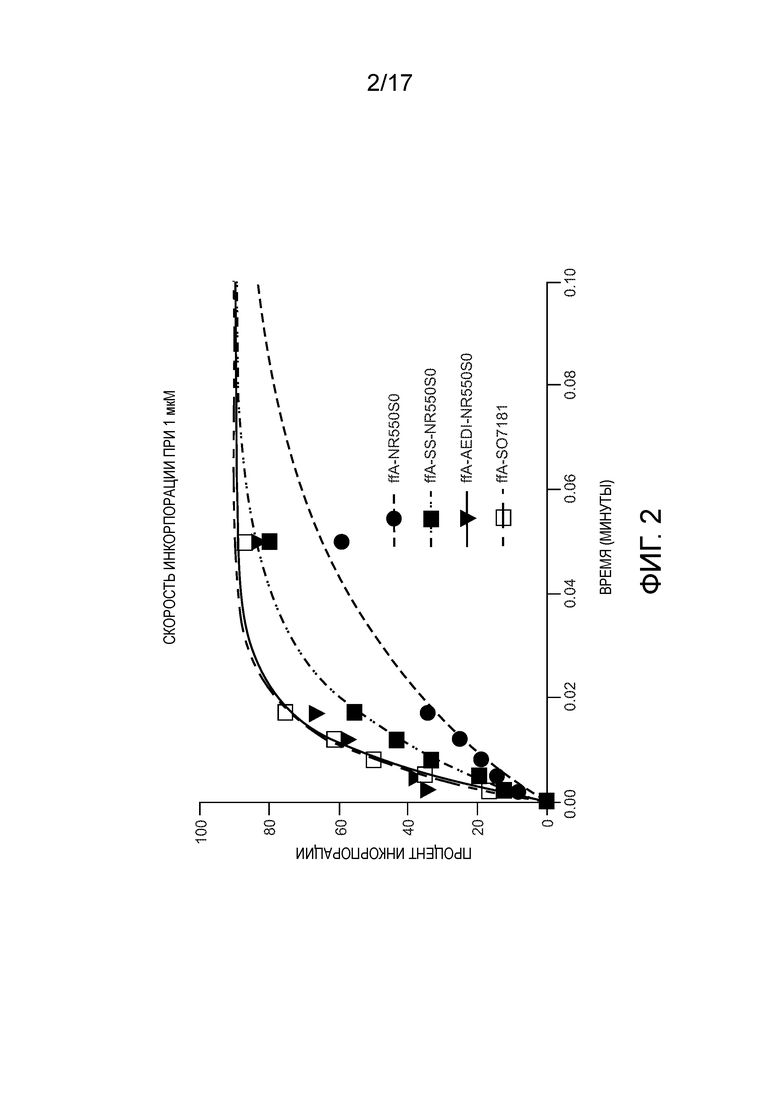
[0015] Фиг. 2 демонстрирует график скорости инкорпорации нуклеотида с использованием меченого нуклеотида, показанного на фиг. 1А, и модифицированных меченых нуклеотидов, показанных на фиг. 1B.
[0016] Фиг. 3А-3Е иллюстрируют структурные формулы дополнительных линкеров, которые вставлены в стандартную связывающую группу, показанную на фиг. 1А.
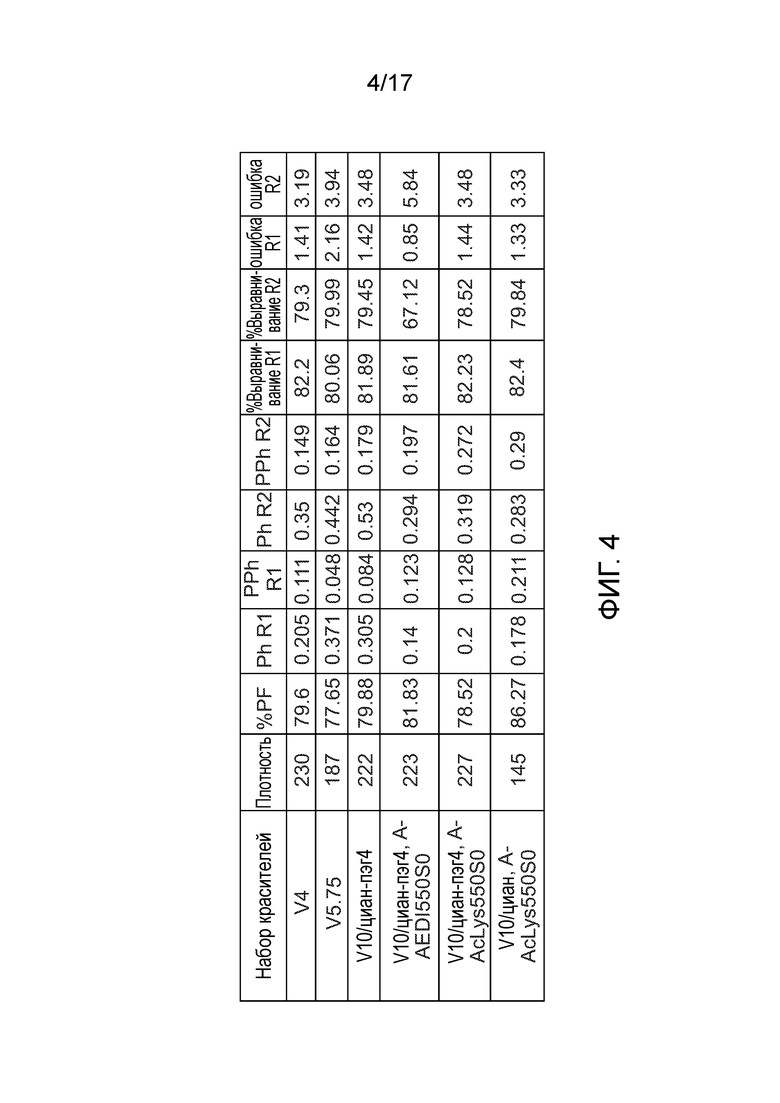
[0017] Фиг. 4 демонстрирует таблицу данных для хода секвенирования с применением двух красителей, используемого для оценки влияния вставки 125, показанной на фиг. 1В, и вставки 315, показанной на фиг. 3В, на качество секвенирования.
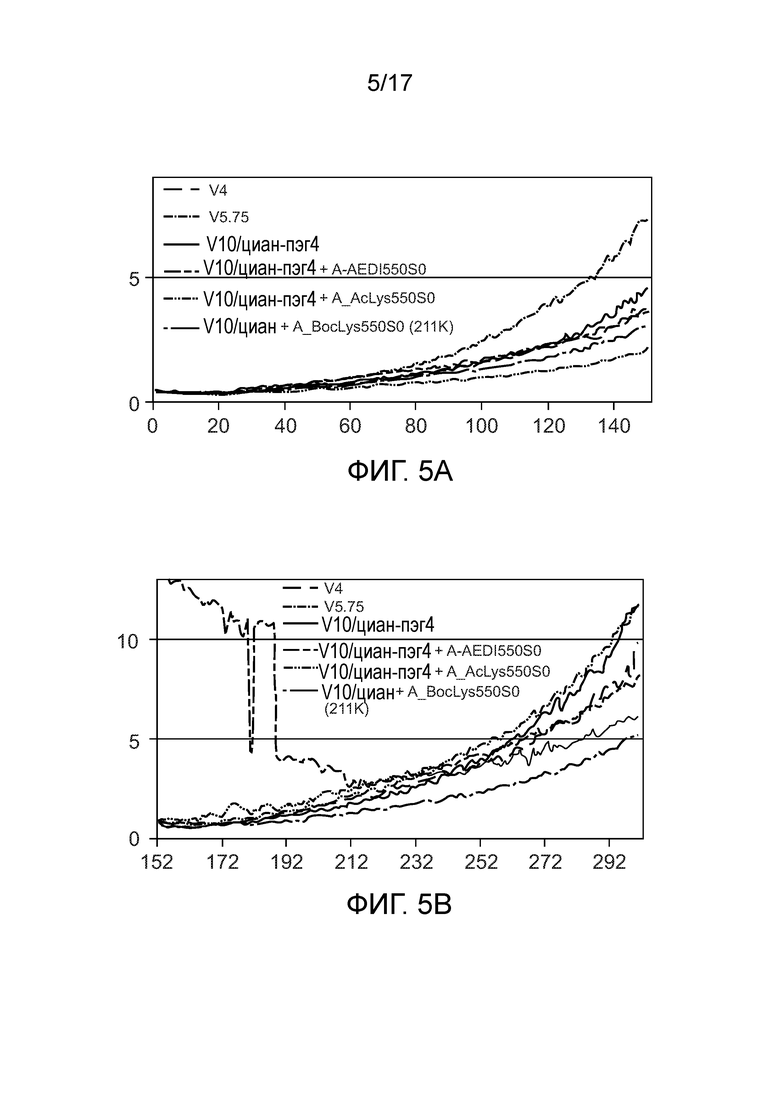
[0018] Фиг. 5A и 5B демонстрируют график частоты появления ошибок для считывания 1 и график частоты появления ошибок для считывания 2 хода секвенирования, показанного на фиг. 4, с использованием вставки линкеров 125 и 315.
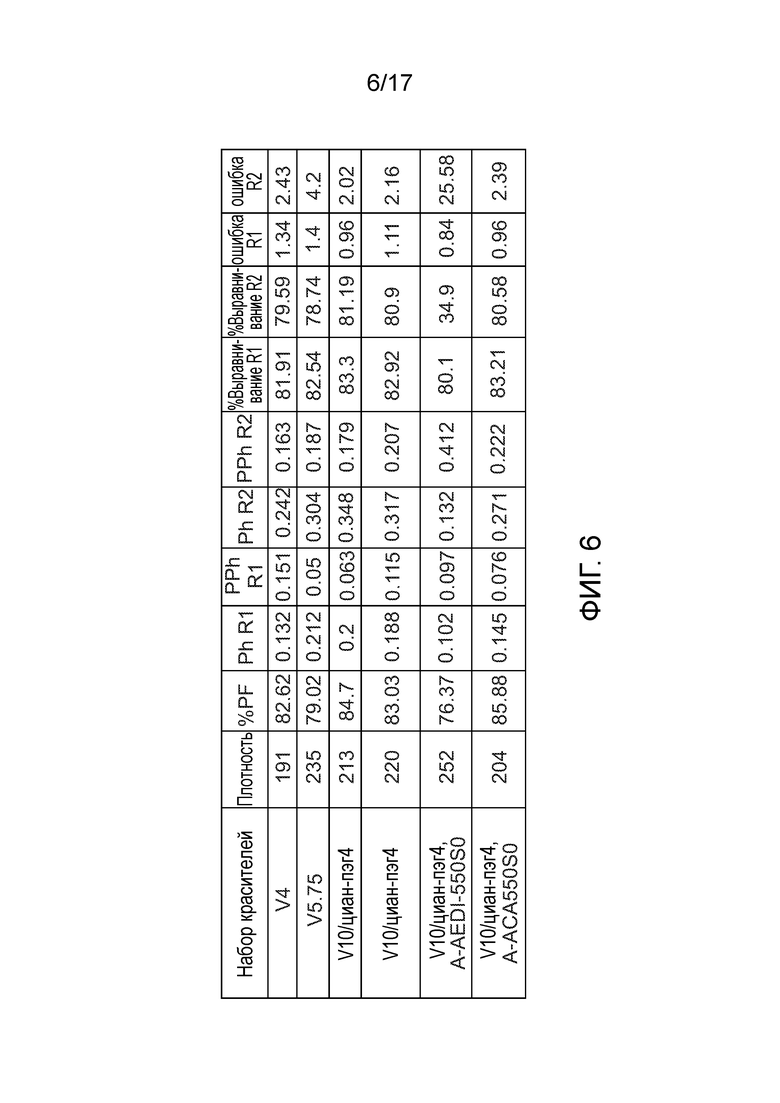
[0019] Фиг. 6 демонстрирует таблицу данных для хода секвенирования, используемого для оценки влияния вставки 125, показанной на фиг. 1В, и вставки 310, показанной на фиг. 3А, на качестве секвенирования.
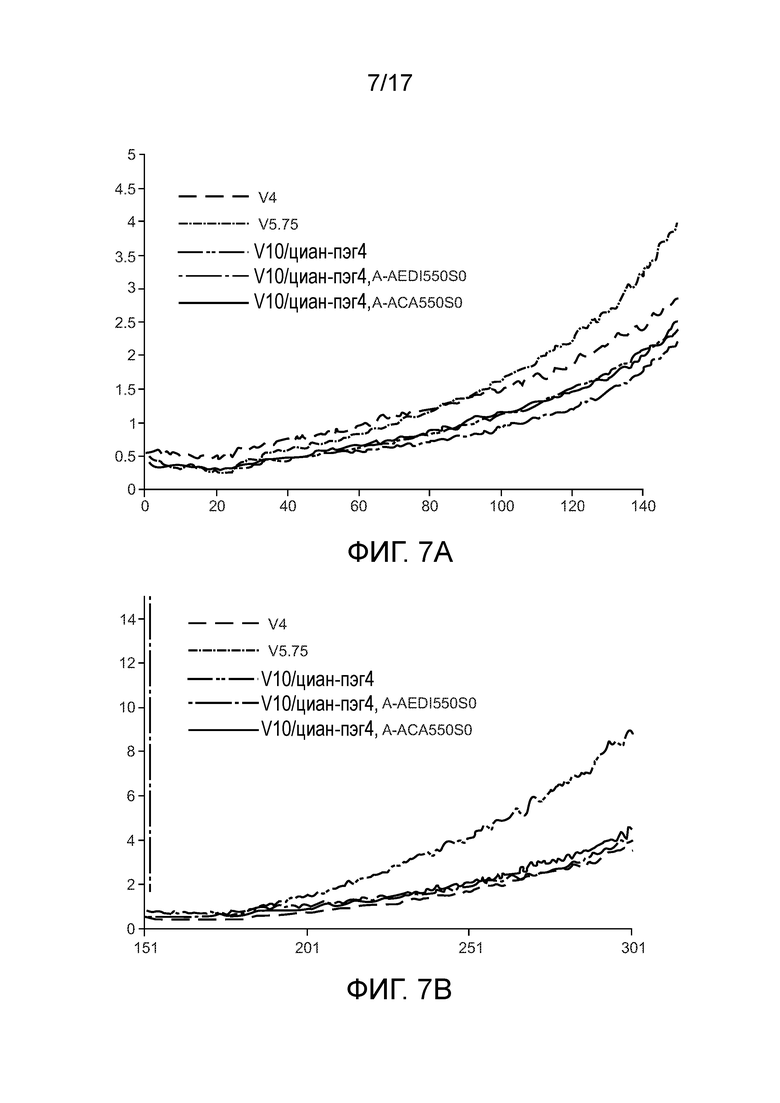
[0020] Фиг. 7А и 7В демонстрируют график частоты появления ошибок для считывания 1 и график частоты появления ошибок для считывания 2 хода секвенирования, показанного на фиг. 6, с использованием вставки линкера 125.
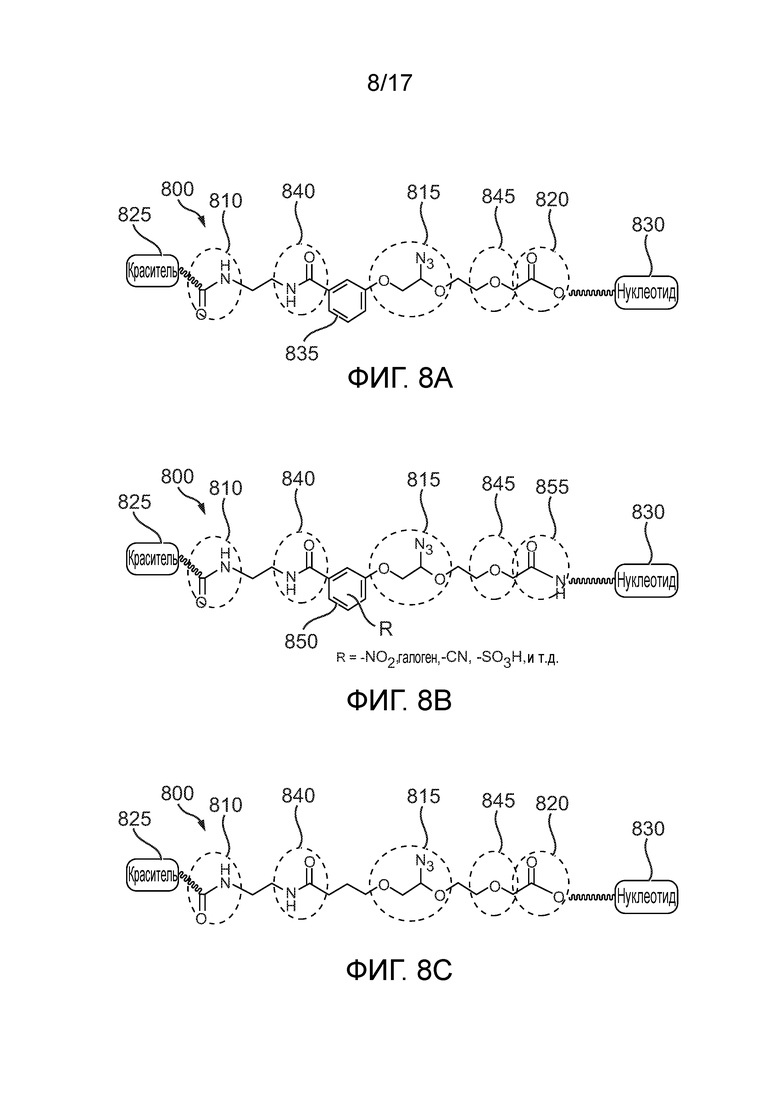
[0021] Фиг. 8А демонстрирует пример стандартной структуры линкера LN3.
[0022] Фиг. 8B, 8С и 8D демонстрируют три примера модифицированных структур линкера LN3, показанного на фиг. 8А.
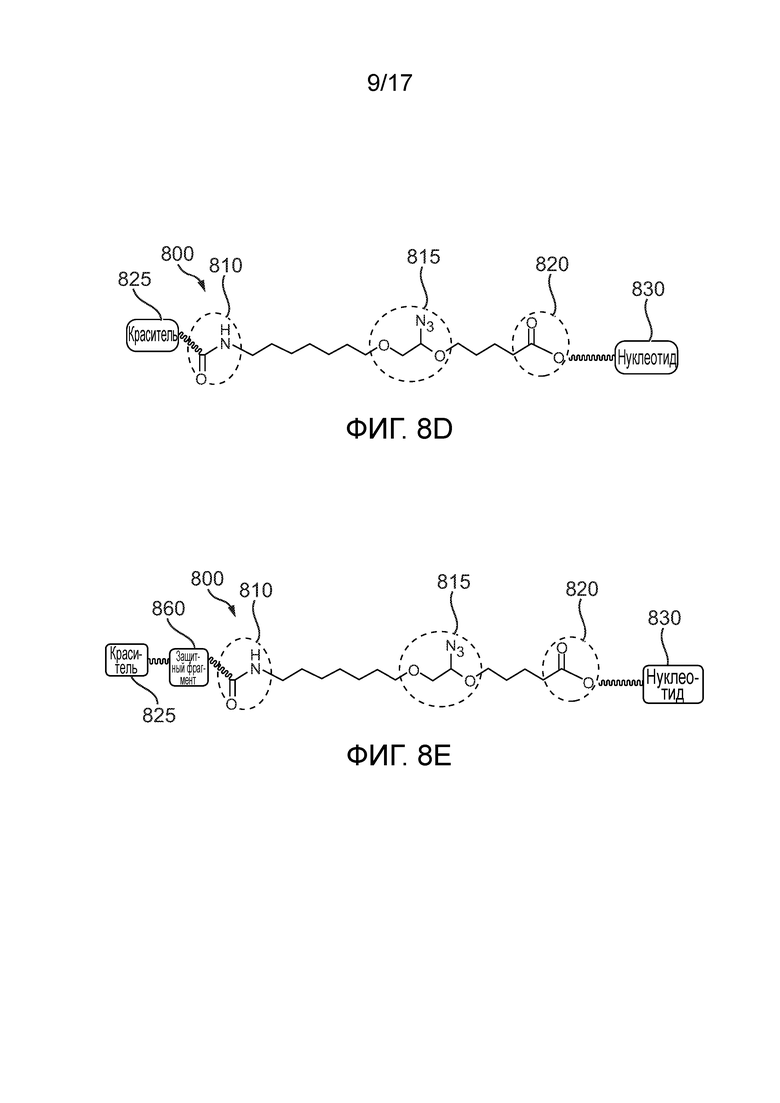
[0023] Фиг. 8Е иллюстрирует вставку защитного фрагмента в линкер, показанный на фиг. 8D.
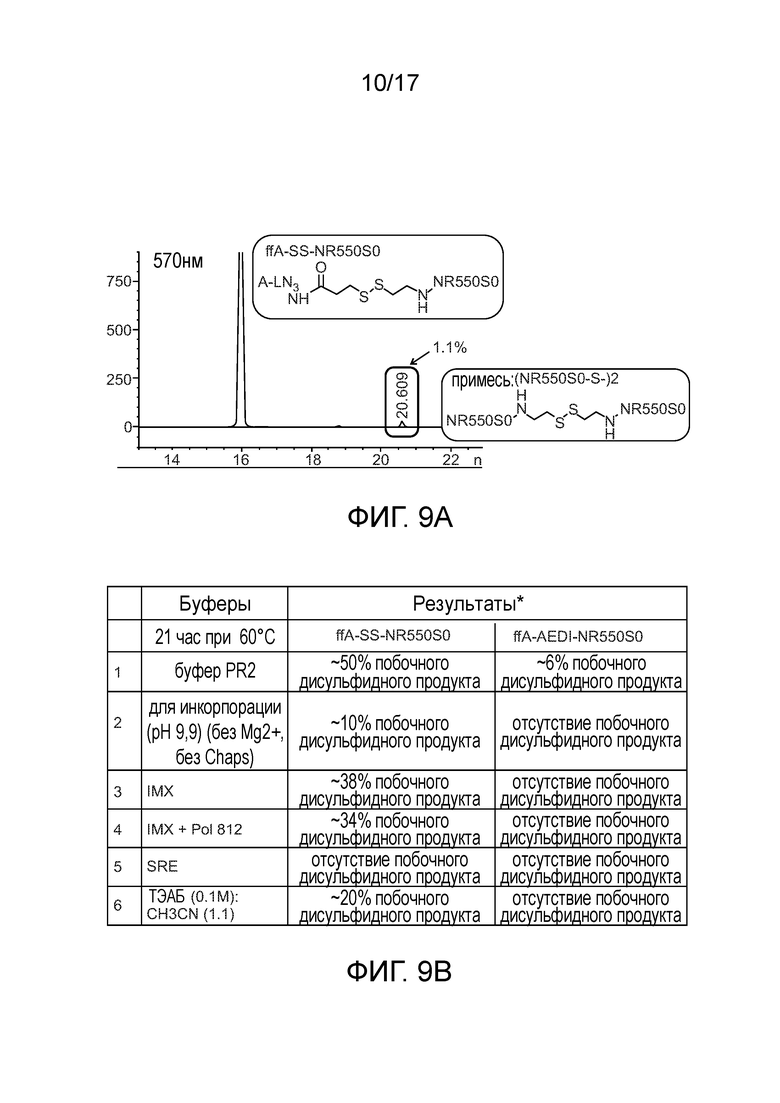
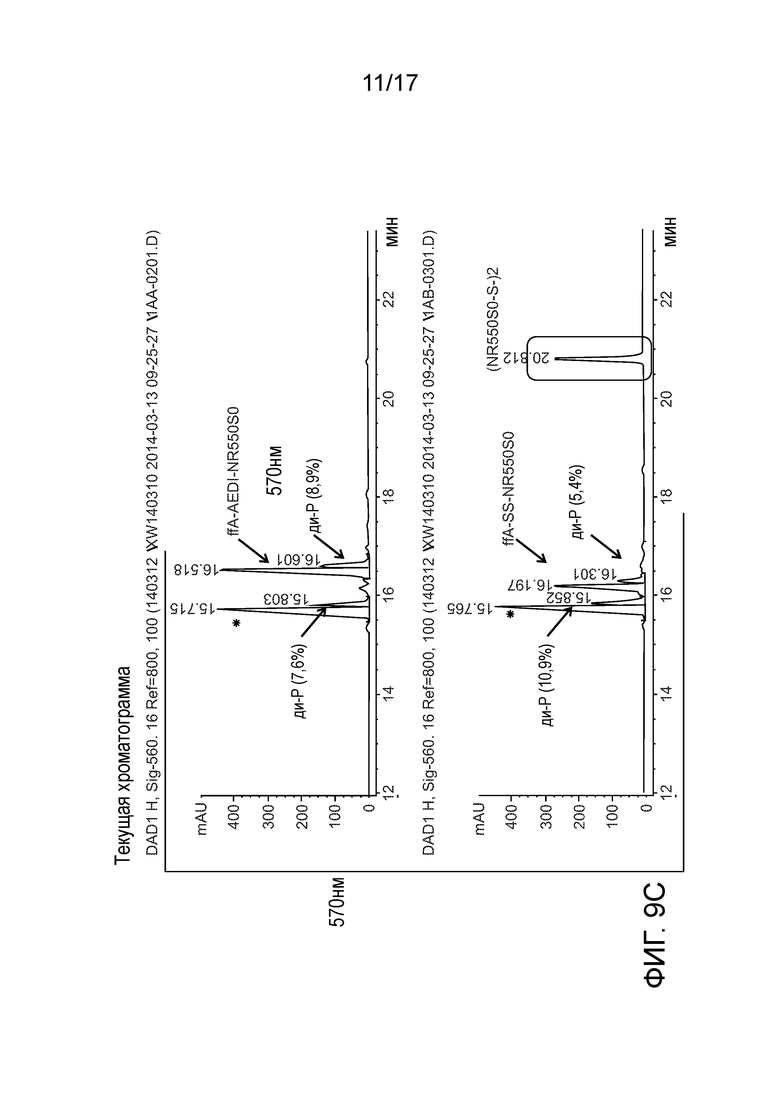
[0023А] Фиг. 9А представляет собой хроматограмму, демонстрирующую появление примеси в ffA с SS-линкером. Фиг. 9B представляет собой таблицу сравнения стабильности ffA с SS-диккерок и с AЕDI-линкером. Фиг. 9C представляет собой хроматограмму, демонстрирующую сравнение SS-линкера и AEDI-линкера ffA в IMX 60° в течение 22 часов, снова демонстрирующую примесь с SS-линкером.
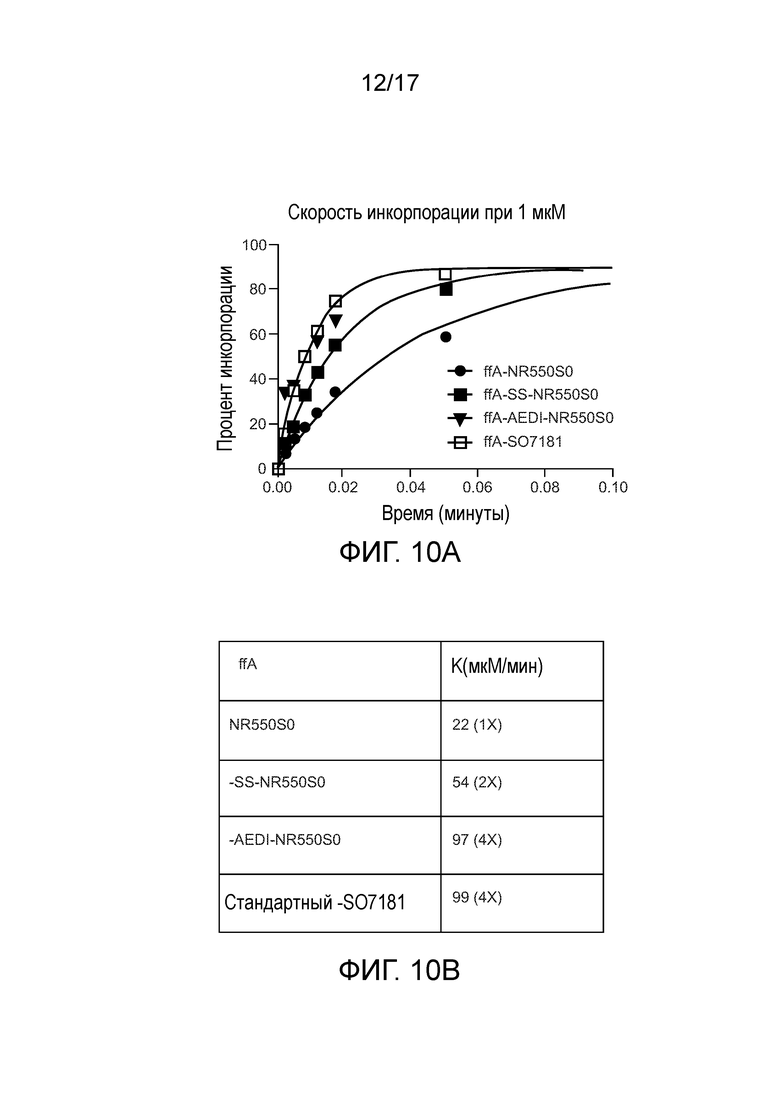
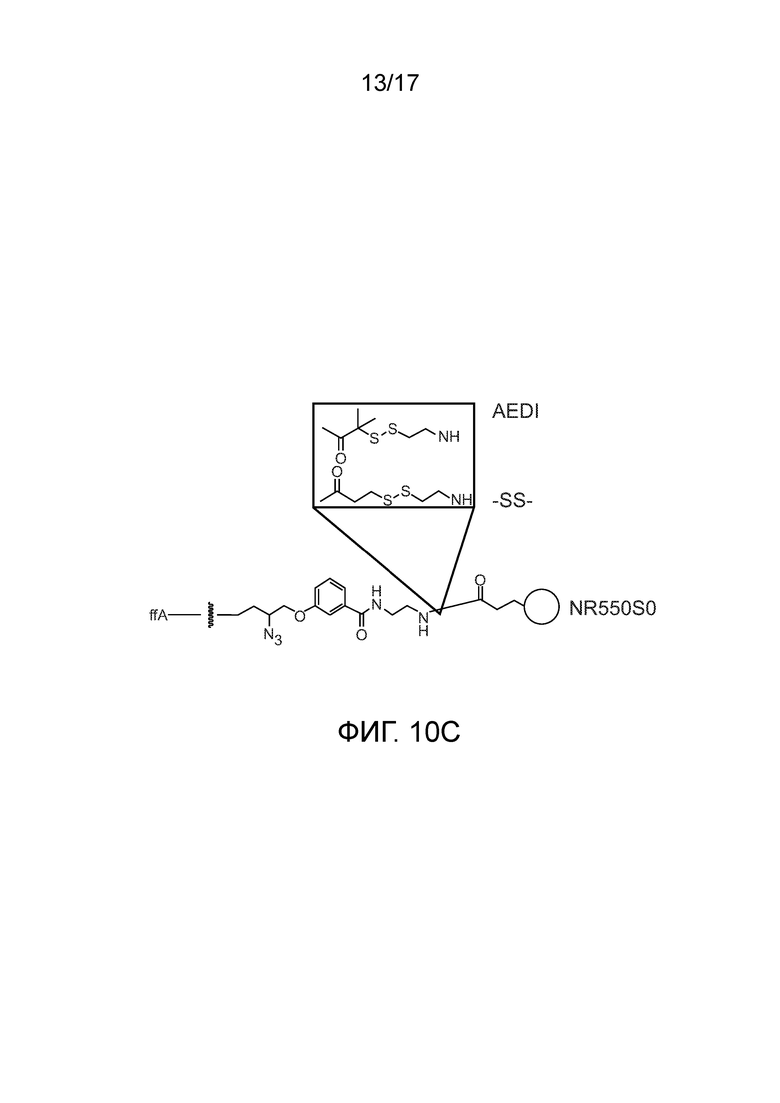
[0023В] Фиг. 10А, 10В и 10С демонстрируют неожиданное увеличение скорости нуклеотидной инкорпорации в растворе с изменениями линкера. Фиг. 10А представляет собой график, демонстрирующий степень инкорпорации при 1 мкМ с Фиг. 10В, демонстрирующей табулированные результаты. Фиг. 10С схематически демонстрирует линкеры AEDI и SS с MR550S0.
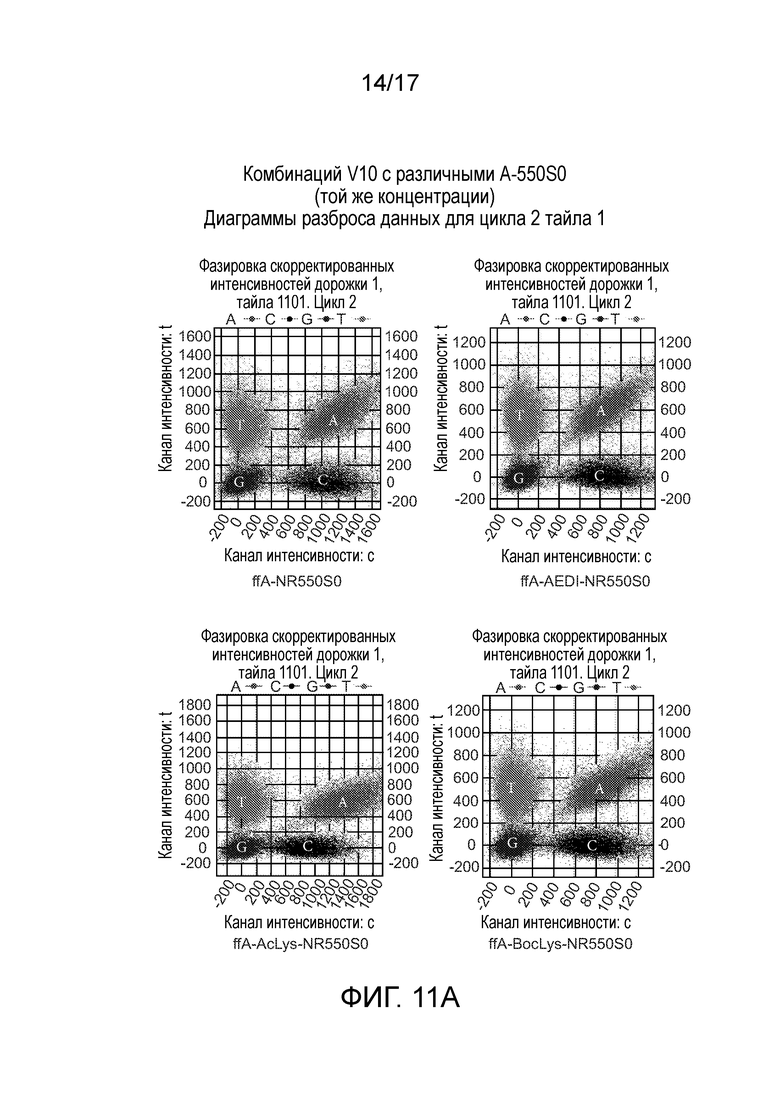
[0023С] Фиг. 11A демонстрирует диаграммы разброса.санных для комбинаций V10 с различными A-550S0 (той же концентрации). Фиг. 11В демонстрирует линкеры Kcat ETA в растворе.
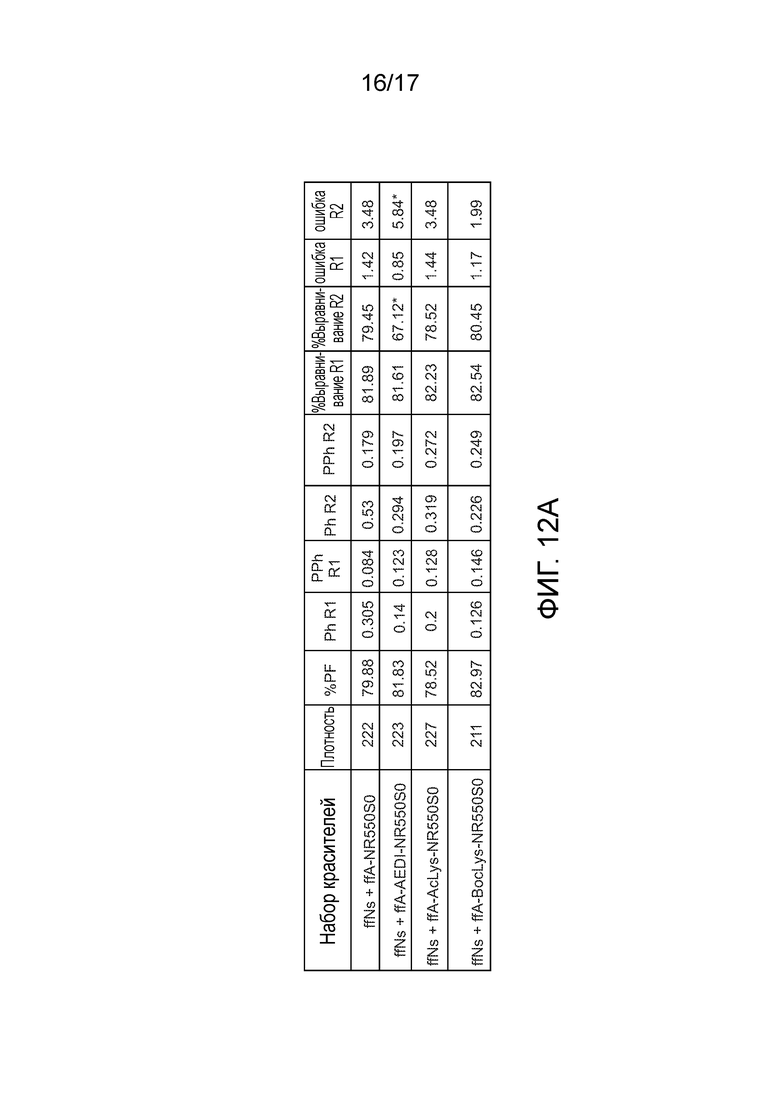
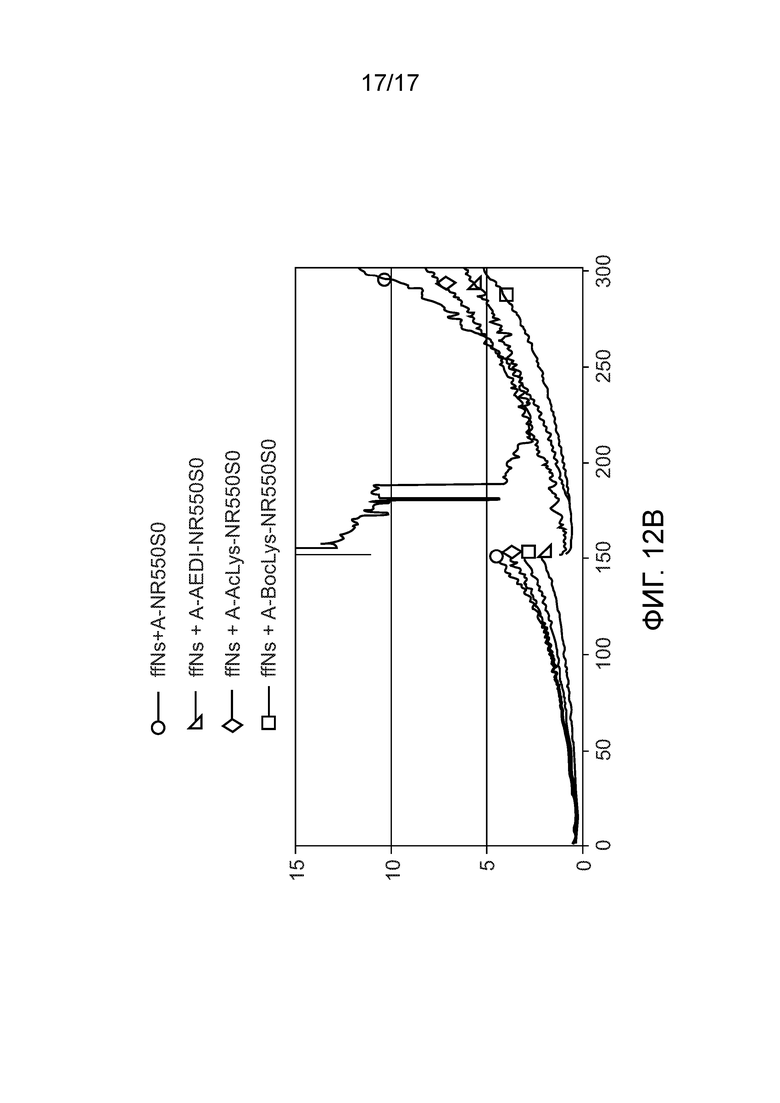
[0023D] Фиг. 12A и 12В демонстрируют метрики секвенирования на M111, Human550, 2×151 циклов.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
[0024] Некоторые варианты осуществления, раскрытые в данном документе, относятся к нуклеозиду или нуклеотиду, ковалентно присоединенному к флуорсфору через линкер, где линкер содержит структуру формулы (I) или (II), приведенных ниже, или комбинацию обоих, в которых определения переменных определены выше.
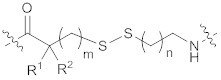 (I),
(I), 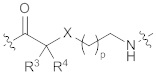 (II).
(II).
[0025] В некоторых вариантах осуществления структуры формулы (I) R1 представляет собой водород. В некоторых других вариантах осуществления R1 представляет собой необязательно замещенный C1-6 алкил. В некоторых таких вариантах осуществления R1 представляет собой метил.
[0026] В любых вариантах осуществления R1, как он описан в данном документе для формулы (I), R2 представляет собой водород. В некоторых других вариантах осуществления R2 представляет собой необязательно замещенный С1-6 алкил. В некоторых таких вариантах осуществления R2 представляет собой метил. В одном варианте осуществления как R1, так и R2 представляют собой метил. В другом варианте осуществления как R1, так и R2 представляют собой водород.
[0027] в некоторых вариантах осуществления структуры формулы (I) m равно 0. В некоторых других вариантах осуществления m равно 1.
[0028] В некоторых вариантах осуществления структуры формулы (I) n равно 1.
[0029] В некоторых вариантах осуществления структуры формулы (I) структура формулы (I) может также быть представлена формулой (Ia) или (Ib):
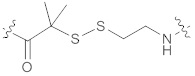 (Ia),
(Ia), 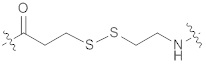 (Ib).
(Ib).
[0030] В некоторых вариантах осуществления, описанных в данном документе, формула (Ia) упоминается как "AEDI", и формула (Ib) упоминается как "SS".
[0031] В некоторых вариантах осуществления структуры формулы (II) R3 представляет собой водород. В некоторых других вариантах осуществления R3 представляет собой необязательно замещенный C1-6 алкил. В некоторых таких вариантах осуществления R3 представляет собой метил. В некоторых вариантах осуществления R3 представляет собой -NR5-C(=O)R6. В некоторых таких вариантах осуществления R5 представляет собой водород. В некоторых таких вариантах осуществления R6 представляет собой необязательно замещенный C1-6 алкил, например, метил. В некоторых вариантах осуществления R3 представляет собой -NR7-C(=O)OR8. В некоторых таких вариантах осуществления R7 представляет собой водород. В некоторых таких вариантах осуществления R8 представляет собой необязательно замещенный C1-6 алкил, например, трет-бутил.
[0032] В любых вариантах осуществления R3, как он описан в данном документе для формулы (II), R4 представляет собой водород. В некоторых других вариантах осуществления R4 представляет собой необязательно замещенный C1-6 алкил. В некоторых таких вариантах осуществления R4 представляет собой метил. В одном варианте осуществления как R3, так и R4 представляют собой метил. В другом варианте осуществления как R3, так и R4 представляют собой водород. В одном варианте осуществления R3 представляет собой -NH(C=O)CH3, и R4 представляет собой водород. В другом варианте осуществления R3 представляет собой -NH(C=O)O-tBu (Вос), и R4 представляет собой водород.
[0033] В некоторых вариантах осуществления структуры формулы (II) Х представляет собой метилен, который может быть необязательно замещен. В другом варианте осуществления Х представляет собой кислород (О). В еще одном варианте осуществления Х представляет собой серу (S).
[0034] В некоторых вариантах осуществления структуры формулы (II) p равно 1. В некоторых других вариантах осуществления p равно 2.
[0035] В некоторых вариантах осуществления структуры формулы (II) структура формулы (II) также может быть представлена формулой (IIа), (IIb), (IIc), (IId), (IIe) или (IIf):
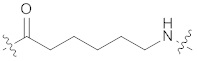 (IIa),
(IIa), 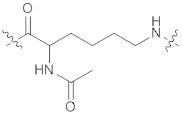 (IIb),
(IIb), 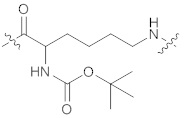 (IIc),
(IIc), 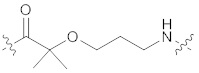 (IId),
(IId),
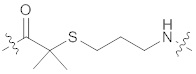 (IIe) или
(IIe) или 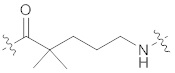 (IIf)
(IIf)
[0036] В некоторых вариантах осуществления, описанных в настоящем документе, формула (IIa) упоминается как "АСА", формула (IIb) упоминается как "AcLys", формула (IIc) упоминается как "BocLys", формула (IId) упоминается как "dMeO", формула (IIe) упоминается как "dMeS", и формула (IIf) упоминается как "DMP".
[0037] В любых вариантах осуществления нуклеозида или нуклеотида, меченного флуорофором через линкер, содержащий структуру формулы (I) или (II), как описано в настоящем документе, нуклеозид или нуклеотид может быть прикреплен к левой стороне линкера, либо непосредственно, либо через дополнительный связывающий фрагмент.
[0038] Некоторые варианты осуществления, раскрытые в данном документе, относятся к нуклеозиду или нуклеотиду, ковалентно присоединенному к флуорофору через линкер, причем указанный линкер содержит структуру формулы (III), и в котором определения переменных определены выше.
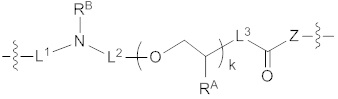 (III).
(III).
[0039] В некоторых вариантах осуществления структуры формулы (III) L1 отсутствует. В некоторых других вариантах осуществления L1 представляет собой линкер, описанный выше, содержащий структуру формулы (I) или (II), в частности формулы (Ia), (Ib), (II), (IIa), (IIb), (IIc), (IId), (IIe) или (IIf). В некоторых других вариантах осуществления L1 может представлять собой защитный фрагмент, содержащий молекулу, которая защищает от повреждения ДНК. В некоторых таких вариантах осуществления защитный фрагмент включает Тролокс, галловую кислоту, п-нитро-бензил (pNB) или аскорбат, или их комбинации.
[0040] В некоторых вариантах осуществления структуры формулы (III) L2 представляет собой необязательно замещенный С1-20 алкилен. В некоторых других вариантах осуществления L2 представляет собой необязательно замещенный C4-10 алкилен. В некоторых таких вариантах осуществления L2 представляет собой гептилен. В некоторых других вариантах осуществления L2 представляет собой необязательно замещенный C1-20 гетероалкилен. В некоторых таких вариантах осуществления необязательно замещенный C1-20 гетероалкилен содержит один или несколько атомов азота. В некоторых таких вариантах осуществления, по меньшей мере, один из атомов углерода C1-20 гетероалкилена замещен оксо (=O). В некоторых других вариантах осуществления L2 представляет собой необязательно замещенный C3-6 гетероалкилен. В некоторых вариантах осуществления L2 прерывается замещенной ароматической группой, такой как замещенная C6-10 арильная группа или 5-10-членная замещенная гетероарильная группа, содержащая от одного до трех гетероатомов. В некоторых таких вариантах осуществления L2 прерывается замещенным фенилом. В некоторых таких вариантах осуществления фенильная группа замещена одним или несколькими (до четырех) заместителями, выбранными из нитро, циано, галогена, гидрокси, C1-6 алкила, C1-6 алкокси, C1-6 галогеналкила, C1-6 галогеналкокси или сульфонилгидроксида. В некоторых других таких вариантах осуществления фенильная группа замещена одним-четырьмя заместителями, выбранными из нитро, циано, галогена или сульфонилгидроксида (т.е. -S(=O)2OH).
[0041] В некоторых вариантах осуществления структуры формулы (III) RA в 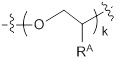 выбран из водорода или азидо. В некоторых таких вариантах осуществления k равно 2, при этом один RA представляет собой азидо, а другой - водород.
выбран из водорода или азидо. В некоторых таких вариантах осуществления k равно 2, при этом один RA представляет собой азидо, а другой - водород.
[0042] В некоторых вариантах осуществления структуры формулы (III) L3 представляет собой необязательно замещенный С1-20 алкилен. В некоторых других вариантах осуществления L3 представляет собой необязательно замещенный C1-6 алкилен. В некоторых таких вариантах осуществления L3 представляет собой этилен. В некоторых других вариантах осуществления L3 представляет собой необязательно замещенный C1-20 гетероалкилен. В некоторых таких вариантах осуществления необязательно замещенный C1-20 гетероалкилен содержит один или несколько атомов кислорода. В некоторых таких вариантах осуществления L1 представляет собой необязательно замещенный C1-6 алкиленоксид, например, C1-3 алкиленоксид.
[0043] В некоторых вариантах осуществления структуры формулы (III) RB представляет собой водород. В некоторых вариантах осуществления RC представляет собой водород. В некоторых других вариантах осуществления как RB, так и RC представляют собой водород.
[0044] В некоторых вариантах осуществления структуры формулы (III) структура формулы (III) может также быть представлена формулой (IIIa), (IIIb) или (IIIc):
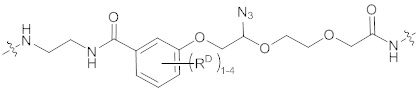 (IIIa)
(IIIa)
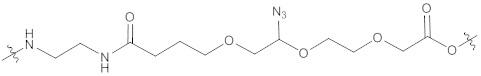 (IIIb),
(IIIb),
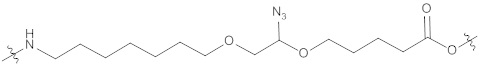 (IIIc);
(IIIc);
где RD выбран из нитро, циано, галогена, гидрокси, C1-6 алкила, C1-6 алкокси, C1-6 галогеналкила, C1-6 галогеналкокси или сульфонилгидроксида. В некоторых других вариантах осуществления RD выбран из нитро, циано, галогена или сульфонилгидроксида.
[0045] В любых вариантах осуществления нуклеозида или нуклеотида, меченного флуорофором через линкер, содержащий структуру формулы (III), как описано в настоящем документе, флуорофор может быть прикреплен к левой стороне линкера, либо непосредственно, либо через дополнительный связывающий фрагмент.
[0046] В любых вариантах осуществления, описанных в настоящем документе в отношении линкера, содержащего структуру формулы (I), (II) или (III), когда термин "необязательно замещенный" используется для определения переменной, такая переменная может быть незамещенной.
Определения
[0047] Если не указано иное, все технические и научные термины, используемые в настоящем документе, имеют то же значение, которое обычно понимается рядовым специалистом в данной области техники. Использование термина "включая", а также других форм, таких как "включать", "включает" и "включено", не является ограничивающим. Использование термина "имеющий", а также других форм, таких как "иметь", "имеет" и "имел", не является ограничивающим. В контексте настоящего описания, независимо от того, в переходной фразе или в теле формулы изобретения, термины "содержит" и "содержащий" должны интерпретироваться как имеющие неограничивающее значение. То есть, вышеуказанные термины должны интерпретироваться в качестве синонима фразы "имеющие, по меньшей мере" или "включающие, по меньшей мере". Например, при использовании в контексте процесса, термин "включающий" означает, что процесс включает, по меньшей мере, перечисленные стадии, но может включать дополнительные стадии. При использовании в контексте соединения, композиции или устройства, термин "содержащий" означает, что соединение, композиция или устройство содержит, по меньшей мере, указанные признаки или компоненты, но может также содержать дополнительные признаки или компоненты.
[0048] Заголовки разделов, используемые в данном документе, предназначены только организационных целей и не должны истолковываться как ограничивающие описанный объект.
[0049] В данном описании общепринятые органические аббревиатуры определены следующим образом:
[0050] В контексте настоящего описания термин "чип" относится к совокупности различных тест-молекул, которые подсоединены к одному или нескольким субстратам, таким, что различные тест-молекулы можно отличить друг от друга в соответствии с относительным расположением. Чип может содержать различные тест-молекулы, то есть каждая расположена в другом адресуемом местоположении на субстрате. В качестве альтернативы или дополнительно чип может содержать отдельные субстраты, каждый из которых несет другую тест-молекулу, где различные тест-молекулы могут быть идентифицированы в соответствии с местоположениями субстратов на поверхности, к которой субстраты прикреплены, или в соответствии с местоположениями субстратов в жидкости. Примерные чипы, в которых отдельные субстраты расположены на поверхности, включают, но не ограничиваются ими, те, в том числе "гранулы в ячейках", что описаны, например, в патенте США №6,355,431 B1, US 2002/0102578 и публикации РСТ № WO 00/63437. Примерные форматы, которые могут быть использованы в настоящем изобретении, чтобы отличить гранулы в жидком чипе, например, с помощью микрожидкостного устройства, такого как клеточный сортер с возбуждением флуоресценции (FACS), описаны, например, в патенте США № 6,524,793. Дополнительные примеры чипов, которые могут быть использованы в настоящем изобретении, включают, но не ограничиваются ими, те, которые описаны в патентах США №№ 5,429,807; 5,436,327; 5,561,071; 5,583,211; 5,658,734; 5,837,858; 5,874,219; 5,919,523; 6,136,269; 6,287,768; 6,287,776; 6,288,220; 6,297,006; 6,291,193; 6,346,413; 6,416,949; 6,482,591; 6,5147,51 и 6610482; и WO 93/17126; WO 95/11995; WO 95/35505; EP 742 287; и EP 799 897.
[0051] В контексте настоящего описания термин "ковалентно присоединенный" или "ковалентно связанный" относится к образованию химической связи, характеризующейся обобщением пары электронов между атомами. Например, ковалентно присоединенное полимерное покрытие относится к полимерному покрытию, которое образует химические связи с функционализированной поверхностью субстрата, по сравнению с прикреплением к поверхности с помощью других способов, например, адгезии или электростатического взаимодействия. Следует принять во внимание, что полимеры, которые присоединены ковалентно к поверхности, также могут быть присоединены с помощью способов в дополнение к ковалентному присоединению.
[0052] В контексте настоящего описания "с Са по Cb" или "Ca-b", где "а" и "b" представляют собой целые числа, относятся к числу атомов углерода в указанной группе. То есть, группа может содержать от "а" до "b", включительно, атомов углерода. Так, например, группа "с C1 по C4 алкил" или "C1-4 алкил" относится ко всем алкильным группам, имеющим от 1 до 4 атомов углерода, то есть, СН3-, CH3CH2-, CH3CH2CH2-, (СН3)2CH-, CH3CH2CH2CH2-, CH3CH2CH(СН3)- и (СН3)3C-.
[0053] Термин "галоген" или "гало" в контексте настоящего описания означает любой из радиостабильных атомов в колонке 7 Периодической Таблицы Элементов, например, фтор, хлор, бром или йод, с фтором и хлором, являющимися предпочтительными.
[0054] В контексте настоящего описания "алкил" относится к неразветвленной или разветвленной углеводородной цепи, которая является полностью насыщенной (т.е. не содержит двойных или тройных связей). Алкильная группа может содержать от 1 до 20 атомов углерода (всякий раз, когда она появляется в данном документе, числовой диапазон, такой как "от 1 до 20" относится к каждому целому числу в заданном диапазоне; например, "от 1 до 20 атомов углерода" означает, что алкильная группа может состоять из 1 атома углерода, 2 атомов углерода, 3 атомов углерода и т.д., вплоть до и включая 20 атомов углерода, хотя настоящее определение охватывает также случай употребления термина "алкил", где не обозначен числовой диапазон). Алкильная группа может быть также алкилом среднего размера, имеющим от 1 до 9 атомов углерода. Алкильная группа также может быть низшим алкилом, имеющим от 1 до 4 атомов углерода. Алкильная группа может быть обозначена как "С1-4 алкил" или подобными обозначениями. Только в качестве примера, "C1-4 алкил" указывает на то, что в алкильной цепи присутствует от одного до четырех атомов углерода, т.е. алкильная цепь выбрана из группы, состоящей из метила, этила, пропила, изопропила, н-бутила, изобутила, втор-бутила и трет-бутила. Типичные алкильные группы включают, но никаким образом не ограничиваются ими, метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, пентил, гексил и тому подобное. Алкильная группа может быть замещенной или незамещенной.
[0055] В контексте настоящего описания термин "алкокси" относится к формуле -OR, где R представляет собой алкил, как определено выше, такой как "C1-9 алкокси", включающий, но не ограничивающийся ими, метокси, этокси, н-пропокси, 1-метилэтокси (изопропокси), н-бутокси, изобутокси, втор-бутокси и трет-бутокси и тому подобное.
[0056] В контексте настоящего описания "гетероалкил" относится к неразветвленной или разветвленной углеводородной цепи, содержащей один или несколько гетероатомов, то есть элементов, отличных от углерода, включая, но не ограничиваясь ими, азот, кислород и серу, в основной цепи. Гетероалкильная группа может иметь от 1 до 20 атомов углерода, хотя настоящее определение охватывает также случаи употребления термина "гетероалкил", где не обозначен числовой диапазон. Гетероалкильная группа может также быть гетероалкилом среднего размера, имеющим от 1 до 9 атомов углерода. Гетероалкильная группа также может быть низшим гетероалкилом, имеющим от 1 до 4 атомов углерода. Гетероалкильная группа может быть обозначена как "С1-4 гетероалкил" или подобными обозначениями. Гетероалкильная группа может содержать один или несколько гетероатомов. Только в качестве примера, "C1-4 гетероалкил" указывает на то, что в гетероалкильной цепи присутствует от одного до четырех атомов углерода и дополнительно один или несколько гетероатомов в основной цепи.
[0057] В контексте настоящего описания "алкилен" означает разветвленную или неразветвленную цепь полностью насыщенной ди-радикальной химической группы, содержащей только углерод и водород, которая присоединена к остальной части молекулы через две точки присоединения (т.е., алкандиил). Алкиленовая группа может иметь от 1 до 20 атомов углерода, хотя настоящее определение охватывает также случаи употребления термина алкилен, где не обозначен числовой диапазон. Алкиленовая группа может быть также алкиленом среднего размера, имеющим от 1 до 9 атомов углерода. Алкиленовая группа может быть также низшим алкиленом, имеющим от 1 до 4 атомов углерода. Алкиленовая группа может быть обозначена как "С1-4 алкилен" или подобными обозначениями. Только в качестве примера "C1-4 алкилен" указывает на то, что в алкиленовой цепи присутствует от одного до четырех атомов углерода, то есть алкиленовая цепь выбрана из группы, состоящей из метилена, этилена, этан-1,1-диила, пропилена, пропан-1,1-диила, пропан-2,2-диила, 1-метил-этилена, бутилена, бутан-1,1-диила, бутан-2,2-диила, 2-метил-пропан-1,1-диила, 1-метил-пропилена, 2-метил-пропилена, 1,1-диметил-этилена, 1,2-диметил-этилена и 1-этил-этилена. В контексте настоящего описания, когда алкилен прерывается ароматической группой, он относится к вставке ароматической группы внутри одной углерод-углеродной связи алкиленовой цепи через две точки прикрепления или к присоединению ароматической группы к одному концу алкиленовой цепи через одну точку прикрепления. Например, когда н-бутилен прерывается фенильной группой, примерные структуры включают 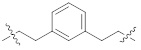 ,
, 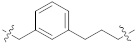 или
или 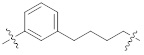 .
.
[0058] В контексте настоящего описания термин "гетероалкилен" относится к алкиленовой цепи, в которой один или несколько скелетных атомов алкилена выбраны из атома, отличного от углерода, например, кислорода, азота, серы, фосфора или их комбинаций. Гетероалкиленовая цепь может иметь длину от 2 до 20000. Типичные гетероалкилены включают, но не ограничиваются ими, -OCH2, -OCH(CH3)-, -O-С(СН3)2-, -OCH2CH2-, -CH(CH3)O-, -CH2OCH2-, -CH2OCH2CH2-, -SCH2-, -SCH(CH3)-, -SC(СН3)2-, -SCH2CH2-, -CH2SCH2CH2-, -NHCH2-, -NHCH(СН3)-, -NHC(СН3)2-, -NHCH2CH2-, -CH2NHCH2-, -CH2NHCH2CH2- и тому подобное. В контексте настоящего описания, когда гетероалкилен прерывается ароматической группой, он относится к вставке ароматической группы внутри одной углерод-углеродной связи или связи углерод-гетероатом гетероалкиленовой цепи через две точки прикрепления или к присоединению ароматической группы к одному концу гетероалкиленовой цепи через одну точку прикрепления. Например, когда н-пропиленоксид прерывается фенильной группой, примерные структуры включают 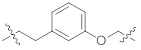 ,
, 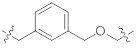 или
или 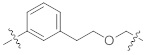 .
.
[0059] В контексте настоящего описания "алкенил" относится к алкильной группе, которая содержит в неразветвленной или разветвленной углеводородной цепи одну или несколько двойных связей. Алкенильная группа может быть незамещенной или замещенной.
[0060] В контексте настоящего описания "алкинил" относится к алкильной группе, которая содержит в неразветвленной или разветвленной углеводородной цепи одну или несколько тройных связей. Алкинильная группа может быть незамещенной или замещенной.
[0061] В контексте настоящего описания "циклоалкил" относится к полностью насыщенной (без двойных или тройных связей) моно- или мульти-циклической углеводородной кольцевой системе. Когда он состоит из двух или более колец, кольца могут быть соединены вместе в конденсированном виде. Циклоалкильные группы могут содержать от 3 до 10 атомов в кольце(кольцах). В некоторых вариантах осуществления циклоалкильные группы могут содержать от 3 до 8 атомов в кольце(кольцах). Циклоалкильная группа может быть незамещенной или замещенной. Типичные циклоалкильные группы включают, но никаким образом не ограничиваются ими, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил.
[0062] Термин "ароматический" относится к кольцу или кольцевой системе, имеющим сопряженную пи-электронную систему, и включает как карбоциклические ароматические (например, фенил), так и гетероциклические ароматические группы (например, пиридин). Термин включает моноциклические или конденсированные полициклические (т.е. кольца, которые имеют общие смежные пары атомов) группы при условии, что вся кольцевая система является ароматической.
[0063] В контексте настоящего описания "арил" относится к ароматическому кольцу или кольцевой системе (т.е. два или несколько конденсированных колец, которые имеют два общих смежных атома углерода), содержащим только углерод в каркасе кольца. Когда арил представляет собой кольцевую систему, каждое кольцо в системе является ароматическим. Арильная группа может иметь от 6 до 18 атомов углерода, хотя настоящее определение охватывает также случай употребления термина "алкил", где не обозначен числовой диапазон. В некоторых вариантах осуществления арильная группа имеет от 6 до 10 атомов углерода. Арильная группа может быть обозначена как "C6-10 арил", "C6 или C10 арил" или подобными обозначениями. Примеры арильных групп включают, но не ограничиваются ими, фенил, нафтил, азуленил и антраценил.
[0064] Термин "аралкил" или "арилалкил" означает арильную группу, присоединенную, в качестве заместителя, через алкиленовую группу, например, "C7-14 аралкил" и тому подобное, в том числе, но не ограничиваясь ими, бензил, 2-фенилэтил, 3-фенилпропил и нафтилалкил. В некоторых случаях, алкиленовая группа представляет собой низшую алкиленовую группу (т.е., C1-4 алкиленовую группу).
[0065] В контексте настоящего описания "гетероарил" относится к ароматическому кольцу или кольцевой системе (т.е. два или несколько конденсированных колец, которые имеют два общих смежных атома углерода), которые содержат один или несколько гетероатомов, то есть элементов, отличных от углерода, в том числе, но не ограничиваясь ими, азот, кислород и серу, в каркасе кольца. Когда гетероарил представляет собой кольцевую систему, каждое кольцо в системе является ароматическим. Гетероарил может иметь 5-18 кольцевых членов (то есть, число атомов, образующих каркас кольца, в том числе атомов углерода и гетероатомов), хотя настоящее определение охватывает также случай употребления термина "алкил", где не обозначен числовой диапазон. В некоторых вариантах осуществления, гетероарильная группа имеет от 5 до 10 членов в кольце или от 5 до 7 кольцевых членов. Гетероарильная группа может быть обозначена как "5-7-членный гетероарил", "5-10-членный гетероарил" или подобными обозначениями. Примеры гетероарильных колец включают, но не ограничиваются ими, фурил, тиенил, фталазинил, пирролил, оксазолил, тиазолил, имидазолил, пиразолил, изоксазолил, изотиазолил, триазолил, тиадиазолил, пиридинил, пиридазинил, пиримидинил, пиразинил, триазинил, хинолинил, изохинолинил, бензимидазолил, бензоксазолил, бензотиазолил, индолил, изоиндолил и бензотиенил.
[0066] "Гетероаралкил" или "гетероарилалкил" означает гетероарильную группу, присоединенную, в качестве заместителя, через алкиленовую группу. Примеры включают, но не ограничиваются ими, 2-тиенилметил, 3-тиенилметил, фурилметил, тиенилэтил, пирролилалкил, пиридилалкил, изоксазолилалкил и имидазолилалкил. В некоторых случаях алкиленовая группа представляет собой низшую алкиленовую группу (т.е., C1-4 алкиленовую группу).
[0067] В контексте настоящего описания "циклоалкил" означает полностью насыщенное карбоциклическое кольцо или кольцевую систему. Примеры включают циклопропил, циклобутил, циклопентил и циклогексил.
[0068] Группа "О-карбокси" относится к группе "-OC(=O)R", в которой R выбран из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, С3-7 карбоциклила, С6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании.
[0069] Группа "С-карбокси" относится к группе "C(=O)OR", в которой R выбран из водорода, С1-6 алкила, С2-6 алкенила, С2-6 алкинила, C3-7 карбоциклила, C6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании. Не ограничивающий пример включает карбоксил (т.е. -C(=O)ОН).
[0070] Группа "циано" относится к группе "CN".
[0071] Группа "азидо" относится к группе "-N3".
[0072] Группа "O-карбамоил" относится к группе "-OC(=O)NRARB", в которой RA и RB каждый независимо выбран из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-7 карбоциклила, С6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании.
[0073] Группа "N-карбамоил" относится к группе "-N(RA)OC(=O)RB", в которой RA и RB каждый независимо выбран из водорода, С1-6 алкила, С2-6 алкенила, C2-6 алкинила, С3-7 карбоциклила, С6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании.
[0074] Группа "С-амидо" относится к группе "C(=O)NRARB", в которой RA и RB каждый независимо выбран из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, C3-7 карбоциклила, С6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании.
[0075] Группа "N-амидо" относится к группе "-N(RA)C(=O)RB", в которой RA и RB каждый независимо выбран из водорода, С1-6 алкила, С2-6 алкенила, C2-6 алкинила, С3-7 карбоциклила, С6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании.
[0076] Группа "амино" относится к группе "-NRARB", в которой RA и RB каждый независимо выбран из водорода, C1-6 алкила, C2-6 алкенила, C2-6 алкинила, С3-7 карбоциклила, С6-10 арила, 5-10-членного гетероарила и 5-10-членного гетероциклила, как определено в данном описании. Не ограничивающий пример включает свободный амино (т.е. -NH2).
[0077] В контексте настоящего описания термин "Тролокс" относится к 6-гидрокси-2,5,7,8-тетраметилхроман-2-карбоновой кислоте.
[0078] В контексте настоящего описания термин "аскорбат" относится к соли аскорбиновой кислоты.
[0079] В контексте настоящего описания термин "галловая кислота" относится к 3,4,5-тригидроксибензойной кислоте.
[0080] В контексте настоящего описания, замещенную группу получают из незамещенной исходной группы, в которой происходит обмен одного или нескольких атомов водорода на другой атом или группу. Если не указано иное, когда группа считается "замещенной", это означает, что группа замещена одним или несколькими заместителями, независимо выбранными из C1-C6 алкила, C1-C6 алкенила, С1-С6 алкинила, С1-С6 гетероалкила, С3-С7 карбоциклила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и С1-С6 галогеналкокси), С3-С7 карбоциклилил-С1-С6-алкила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и C1-C6 галогеналкокси), 5-10-членного гетероциклила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и С1-C6 галогеналкокси), 5-10-членного гетероциклил-С1-С6-алкила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, С1-С6-галогеналкилом и С1-С6 галогеналкокси), арила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и C1-C6 галогеналкокси), арил(С1-С6)алкила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и C1-C6 галогеналкокси), 5-10-членного гетероарила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и C1-C6 галогеналкокси), 5-10-членного гетероарил(С1-С6)алкила (необязательно замещенного галогеном, C1-C6 алкилом, C1-C6 алкокси, C1-C6 галогеналкилом и C1-C6 галогеналкокси), галогена, циано, гидрокси, С1-С6 алкокси, С1-С6 алкокси(С1-С6)алкила (т.е., простого эфира), арилокси, сульфгидрила (меркапто), галоген(С1-С6)алкила (например, -CF3), галоген(С1-С6)алкокси (например, -OCF3), C1-C6 алкилтио, арилтио, амино, амино(С1-С6)алкила, нитро, О-карбамила, N-карбамила, О-тиокарбамила, N-тиокарбамила, С-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, С-карбокси, О-карбокси, ацила, цианато, изоцианато, тиоцианато, изотиоцианато, сульфинила, сульфонила и оксо (=O). Везде, где группа описана как "необязательно замещенная", эта группа может быть замещена вышеуказанными заместителями.
[0081] Следует понимать, что некоторые соглашения о присвоении имен радикалам могут включать либо моно-радикал, либо ди-радикал, в зависимости от контекста. Например, когда заместителю требуется две точки присоединения к остальной части молекулы, следует понимать, что заместитель представляет собой ди-радикал. Например, заместитель, определенный как алкил, которому требуется две точки присоединения, включает ди-радикалы, такие как -CH2-, -CH2CH2-, -CH2CH(CH3)CH2- и тому подобное. Аналогичным образом, группа, определенная как амино, которому требуется две точки присоединения, включает ди-радикалы, такие как -NH-, -N(СН3)- и тому подобное. Другие соглашения о присвоении имен радикалам четко указывают, что радикал представляет собой ди-радикал, такой как "алкилен" или "алкенилен".
[0082] Везде, где заместитель, изображен как ди-радикал (то есть, имеет две точки присоединения к остальной части молекулы), следует понимать, что заместитель может быть присоединен в любой направленной конфигурации, если не указано иное. Так, например, заместитель, изображенный как -AE- или  включает заместитель, сориентированный таким образом, что А присоединен к крайней левой точке присоединения молекулы, а также случай, в котором А присоединен к крайней правой точке присоединения молекулы.
включает заместитель, сориентированный таким образом, что А присоединен к крайней левой точке присоединения молекулы, а также случай, в котором А присоединен к крайней правой точке присоединения молекулы.
[0083] Когда соединения, раскрытые в данном описании, имеют, по меньшей мере, один стереоцентр, они могут существовать в виде отдельных энантиомеров и диастереомеров или в виде смеси таких изомеров, включая рацематы. Разделение индивидуальных изомеров или селективный синтез индивидуальных изомеров осуществляется путем применения различных способов, которые хорошо известны специалистам в данной области техники. Если не указано иное, все такие изомеры и их смеси включены в объем соединений, раскрытых в настоящем документе.
[0084] В контексте настоящего описания "нуклеотид" включает азотсодержащее гетероциклическое основание, сахар и один или несколько фосфатных групп. Они являются мономерными звеньями последовательности нуклеиновой кислоты. В РНК сахар представляет собой рибозу, а в ДНК - дезоксирибозу, т.е. сахар, у которого отсутствует гидроксильная группа, которая присутствует в рибозе. Азотсодержащее гетероциклическое основание может представлять собой пуриновое или пиримидиновое основание. Пуриновые основания включают аденин (А) и гуанин (G), а также их модифицированные производные или их аналоги. Пиримидиновые основания включают цитозин (С), тимин (Т) и урацил (U), а также их модифицированные производные или их аналоги. Атом С-1 дезоксирибозы связан с N-1 пиримидина или N-9 пурина.
[0085] В контексте настоящего описания "нуклеозид" структурно подобен нуклеотиду, но отсутствуют фосфатные остатки. Примером нуклеозидного аналога будет тот, в котором метка связана с основанием, и никакая фосфатная группа не присоединена к молекуле сахара. Термин "нуклеозид" используется в данном описании в его обычном смысле, как он понимается специалистами в данной области техники. Примеры включают, но не ограничиваются ими, рибонуклеозид, содержащий фрагмент рибозы, и дезоксирибонуклеозид, содержащий фрагмент деоксирибозы. Модифицированный фрагмент пентозы представляет собой фрагмент пентозы, в котором атом кислорода был заменен на углерод, и/или углерод был заменен на атом серы или кислорода. "Нуклеозид" представляет собой мономер, который может иметь замещенное основание и/или остаток сахара. Кроме того, нуклеозид может быть инкорпорирован в более крупные ДНК- и/или РНК-полимеры и олигомеры.
[0086] В контексте настоящего описания термин "полинуклеотид" относится к нуклеиновым кислотам в целом, включая ДНК (например, геномную ДНК кДНК), РНК (например, мРНК), синтетические олигонуклеотиды и синтетические аналоги нуклеиновых кислот. Полинуклеотиды могут включать природные или неприродные основания, или их комбинации, и природные или неприродные связи остова, например, фосфоротиоаты, ПНК или 2'-O-метил-РНК, или их комбинации.
[0087] В контексте настоящего описания термин "фазирование" относится к явлениям в SBS, что обусловлено неполным удалением 3'-терминаторов и флуорофоров, а также невозможностью завершить инкорпорацию части нитей ДНК внутри кластеров посредством полимераз при заданном цикле секвенирования. Предварительное фазирование обусловлено инкорпорацией нуклеотидов без эффективных 3'-терминаторов, и событие инкорпорации идет на 1 цикл впереди. Фазирование и предварительное фазирование являются причиной того, что выведенные интенсивности для конкретного цикла состоят из сигнала текущего цикла, а также фона от предшествующих и последующих циклов. По мере увеличения числа циклов возрастает доля последовательностей в кластере, подвергшихся воздействию фазирования, что затрудняет идентификацию подходящего основания. Предварительное фазирование может быть вызвано присутствием следовых количеств незащищенных или деблокированных 3'-ОН-нуклеотидов в процессе секвенирования путем синтеза (SBS). Незащищенные 3'-ОН-нуклеотиды могут быть образованы в ходе производственных процессов или, возможно, в процессе хранения и обработки реагентов. Соответственно, модификации нуклеотидных аналогов или связывающих групп, которые приводят к более быстрому времени цикла SBS, более низким значениям фазирования и предварительного фазирования и большей длине считывания последовательности, обеспечивают большие преимущества в применениях SBS.
[0088] В контексте настоящего описания термин "защитный фрагмент" включает, но не ограничивается ими, молекулы, которые могут защитить от повреждений ДНК (например, фото-повреждения или других химических повреждений). Некоторые конкретные примеры включают антиоксиданты, такие как витамин C, производные витамина E, фенольная кислота, полифенолы и их производные и аналоги. Следует понимать, что в некоторых контекстах, где термин "защитный фрагмент" определен, он относится к фрагменту, полученному в результате реакции между одной или несколькими функциональными группами защитного фрагмента с соответствующей функциональной группой линкера, как описано в настоящем документе. Например, когда защитная часть представляет собой "галловую кислоту", он может относиться к амидам и сложным эфирам галловой кислоты, а не к самой галловой кислоте со свободной карбоксильной группой.
Детектируемые метки
[0089] Некоторые варианты осуществления, описанные в данном документе, относятся к использованию обычных детектируемых меток. Детектирование может быть осуществлено любым подходящим способом, в том числе флуоресцентной спектроскопией или другими оптическими средствами. Предпочтительная метка представляет собой флуорофор, которая после поглощения энергии, испускает излучение на определенной длине волны. Многие подходящие флуоресцентные метки известны. Например, Welch с соавт. (Chem. Eur. J. 5(3):951-960, 1999) раскрывает данзил-функционализированные флуоресцентные фрагменты, которые могут быть использованы в настоящем изобретении. Zhu с соавт. (Cytometry 28:206-211, 1997) описывает использование флуоресцентных меток Cy3 и Cy5, которые также могут быть использованы в настоящем изобретении. Метки, пригодные для использования, также раскрыты в Prober с соавт. (Science 238:336-341, 1987); Connell с соавт. (BioTechniques 5(4):342-384, 1987), Ansorge с соавт. (Nucl. Acids Res. 15(11):4593-4602, 1987) и Smith с соавт. (Nature 321:674, 1986). Другие коммерчески доступные флуоресцентные метки включают, но не ограничиваются ими, флуоресцеин, родамин (в том числе, TMR техасский красный и Rox), адекса, бодипи, акридин, кумарин, пирен, бензантрацен и цианины.
[0090] Различные метки могут быть также использованы в настоящей заявке, например, бифлуорофорные FRET-кассеты Tet. Let. 46:8867-8871, 2000). Мультифлуорофорные дендримерные системы (J. Am. Chem. Soc. 123:8101-8108, 2001) также могут быть использованы. Несмотря на то, флуоресцентные метки являются предпочтительными, другие формы детектируемых меток будут очевидны для обычных специалистов в данной области техники в качестве пригодных. Например, микрочастицы, в том числе квантовые точки (Empodocles с соавт., Nature 399:126-130, 1999), наночастицы золота (Reichert с соавт.., Anal. Chem. 72:6025-6029, 2000) и микрогранулы (Lacoste с соавт., Proc. Natl. Acad. Sci USA 97(17):9461-9466, 2000), могут быть использованы.
[0091] Мультикомпонентные метки также могут быть использованы в настоящей заявке. Мультикомпонентной меткой является та, которая зависит от взаимодействия с дополнительным соединением для обнаружения. Наиболее распространенной мультикомпонентной меткой, используемой в биологии, является система биотин-стрептавидин. Биотин используют в качестве метки, прикрепленной к нуклеотиду. Стрептавидин затем добавляют отдельно, чтобы произошла активизация детектирования. Доступны другие многокомпонентные системы. Например, динитрофенол имеет коммерчески доступное флуоресцентное антитело, которое может быть использовано для детектирования.
[0092] Если не указано иное, то ссылка на нуклеотиды также предназначена для применения к нуклеозидам. Настоящая заявка также будет дополнительно описана со ссылкой на ДНК, хотя описание будет также применимо к РНК, ПНК и другим нуклеиновым кислотам, если не указано иное.
Способы секвенирования
[0093] В нуклеозиды или нуклеотиды, описанные в данном документе, могут быть использованы в сочетании с различными методами секвенирования. В некоторых вариантах осуществления способ для определения нуклеотидной последовательности нуклеиновой кислоты-мишени может быть автоматизированным процессом.
[0094] Нуклеотидные аналоги, представленные в данном описании, могут быть использованы в методике секвенирования, такой как методика секвенирования путем синтеза (SBS). Если кратко, то SBS может быть инициировано путем контактирования целевой нуклеиновой кислоты с одним или несколькими мечеными нуклеотидами, ДНК-полимеразой и т.д. Те признаки, когда праймер удлиняется с использованием нуклеиновой кислоты-мишени в качестве матрицы, будут включать меченый нуклеотид, который может быть обнаружен. Необязательно меченые нуклеотиды могут дополнительно включать обратимое свойство терминации, терминирующее дальнейшее удлинение праймера, как только нуклеотид был добавлен в качестве праймера. Например, аналог нуклеотида, имеющий фрагмент обратимого терминатора, может быть добавлен в качестве праймера таким образом, что последующее удлинение не может произойти до тех пор, пока не будет доставлен деблокирующий агент, чтобы удалить фрагмент. Таким образом, для вариантов осуществления, которые используют обратимую терминацию, деблокирующий агент может быть доставлен в проточную кювету (до или после того, как происходит детектирование). Промывания могут осуществляться между различными стадиями доставки. Затем цикл может быть повторен n раз, чтобы удлинить праймер посредством n нуклеотидов, тем самым определяя последовательность длины n. Примерные методики SBS, жидкостные системы и платформы детектирования, которые могут быть легко адаптированы для использования с чипом, полученным способами в соответствии с настоящим раскрытием, описаны, например, в Bentley с соавт., Nature 456:53-59 (2008), WO 04/018497; WO 91/06678; WO 07/123744; в патентах США №№ 7,057,026; 7,329,492; 7,211,414; 7,315,019 или 7,405,281, а также в заявке на патент США № публикации 2008/0108082 А1, каждый из которых включен в настоящую заявку посредством ссылки.
[0095] Другие методики секвенирования, использующие циклические реакции, могут быть использованы, например, пиросеквенирование. Пиросеквенирование обнаруживает высвобождение неорганического пирофосфата (PPi), так как отдельные нуклеотиды инкорпорированы в образующуюся цепь нуклеиновой кислоты (Ronaghi, с соавт., Analytical Biochemistry 242(1), 84-9 (1996); Ronaghi, Genome Res. 11(1), 3-11 (2001); Ronaghi с соавт. Science 281(5375), 363 (1998); патенты США №№ 6,210,891; 6,258,568 и 6,274,320, каждый из которых включен в настоящую заявку посредством ссылки). В пиросеквенировании высвобождающийся PPi может быть обнаружен путем преобразования в аденозинтрифосфат (АТФ) с помощью АТФ-сульфурилазы, и полученный в результате АТФ может быть обнаружен с помощью люцифераза-продуцируемых фотонов. Таким образом, реакцию секвенирования можно контролировать с помощью системы детектирования люминесценции. Источники возбуждения излучения, используемые для систем детектирования на основе флуоресценции, не являются необходимыми для методик пиросеквенирования. Пригодные жидкостные системы, детекторы и методики, которые могут быть использованы для применения пиросеквенирования к чипам в соответствии с настоящим раскрытием, описаны, например, в заявке на патент ВОИС с серийным № PCT/US11/57111, заявке на патент США № публикации 2005/0191698 А1, патенте США № 7,595,883 и патенте США № 7,244,559, каждый из которых включен в настоящую заявку посредством ссылки.
[0096] Реакции секвенирования путем лигирования также могут быть использованы в том числе, например, те, которые описаны в Shendure с соавт. Science 309:1728-1732 (2005); в патенте США № 5,599,675; и в патенте США № 5,750,341, каждый из которых включен в настоящую заявку посредством ссылки. Некоторые варианты осуществления могут включать методики секвенирования путем гибридизации, как описано, например, в Bains с соавт., Journal of Theoretical Biology 135(3), 303-7 (1988); Drmanac с соавт., Nature Biotechnology 16, 54-58 (1998); Fodor с соавт., Science 251(4995), 767-773 (1995); и WO 1989/10977, каждый из которых включен в настоящую заявку посредством ссылки. Как в методиках секвенирования путем лигирования, так и в методиках секвенирования путем гибридизации, нуклеиновые кислоты, которые присутствуют в гель-содержащих лунках (или других вогнутых объектах), подвергают многократным циклам доставки олигонуклеотида и детектирования. Жидкостные системы для способов SBS, изложенные в настоящем документе, или в ссылках, приведенных в настоящем документе, могут быть легко адаптированы для доставки реагентов для методик секвенирования путем лигирования или секвенирования путем гибридизации. Как правило, олигонуклеотиды являются флуоресцентно мечеными и могут быть обнаружены с помощью флуоресцентных детекторов, аналогичных тем, которые описаны в отношении методик SBS в настоящем документе или в ссылках, приведенных в настоящем документе.
[0097] Некоторые варианты осуществления могут использовать способы, включающие мониторинг в режиме реального времени активности ДНК-полимеразы. Например, инкорпорации нуклеотидов могут быть обнаружены с помощью взаимодействий резонансного переноса энергии флуоресценции (FRET) между флуорофор-несущей полимеразой и γ-фосфат-меченых нуклеотидов, или с помощью волноводов zeromode. Методики и реагенты для секвенирования на основе FRET описаны, например, в Levene с соавт. Science 299, 682-686 (2003); Lundquist с соавт. Opt. Lett. 33, 1026-1028 (2008); Korlach с соавт. Proc. Natl. Acad. Sci. USA 105, 1176-1181 (2008), раскрытие которых включено в настоящую заявку посредством ссылки.
[0098] Некоторые варианты осуществления SBS включают обнаружение протона, высвобождаемого при инкорпорации нуклеотида в инсерционный продукт. Например, секвенирование, основанное на обнаружении высвобождаемых протонов, может использовать электрический детектор и связанные с ним методики, которые являются коммерчески доступными от Ion Torrent (Гилфорд, штат Коннектикут, дочерняя компания Technologies Life), или способы и системы секвенирования, описанные в заявке на патент США № публикаций 2009/0026082 A1; 2009/0127589 A1; 2010/0137143 A1; или 2010/0282617 А1, каждый из которых включен в настоящую заявку посредством ссылки.
Примерные модифицированные линкеры
[0099] Дополнительные варианты осуществления раскрыты более подробно в следующих примерах, которые ни в коей мере не предназначены для ограничения объема притязаний.
[0100] Фиг. 1А иллюстрирует частичную структурную формулу меченого нуклеотида 100. Меченый нуклеотид 100 включает полностью функционализированный аденозиновый нуклеотид (ffA) 110, стандартный линкерный фрагмент 115 и флуоресцентный краситель 120. Стандартный линкерный фрагмент 115 может представлять собой линкерный фрагмент, обычно используемый в синтезе меченых нуклеотидов для секвенирования путем синтеза (SBS). В одном примере флуоресцентный краситель 120 представляет собой NR550S0. В этом примере меченый нуклеотид 100 может быть описан как "ffA-NR550S0". В другом примере флуоресцентный краситель 120 представляет собой SO7181, и меченый нуклеотид 100 может быть описан как "FFA-SO7181".
[0101] Фиг. 1В иллюстрирует меченый нуклеотид 100, показанный на фиг. 1А, с двумя возможными структурными модификациями в стандартном линкерном фрагменте 115. В одном примере стандартный линкерный фрагмент 115 включает вставку AEDI 125 между карбонильной (то есть, -C(=O)-) и амино- (т.е. -NH-) частью амидного фрагмента. В этом примере модифицированный меченый нуклеотид может быть описан как "ffA-AEDI-NR550S0". В другом примере стандартный линкерный фрагмент 115 включает вставку SS 130, и модифицированный меченый нуклеотид может быть обозначен как "ffA-SS-NR550S0".
[0102] Фиг. 2 демонстрирует график скорости инкорпорации нуклеотида с использованием меченого нуклеотида, показанного на фиг. 1А, и модифицированных меченых нуклеотидов, показанных на фиг. 1B. Анализ проводили при 55°С, в 40мМ этаноламине (рН 9,8), 9 мМ MgCl, 40 мМ NaCl, 1 мМ ЭДТА, 0,2% CHAPS, с 20нМ праймером: матричная ДНК и 30мкг/мл полимеразы 812 (MiSeq Kit V2), 1 мМ нуклеотид. Фермент связывается с ДНК и затем быстро смешивается с нуклеотидом в модуле гашения потока в течение короткого промежутка времени (до 10 секунд) перед гашением с помощью 500 мМ ЭДТА. Берут несколько временных точек для каждого нуклеотида. Полученные образцы затем анализируют на денатурирующем геле, и процент ДНК, преобразованного в ДНК+1, определяют и наносят на график в зависимости от времени, чтобы определить константу скорости первого порядка для каждого нуклеотида. Данные приведены ниже в таблице 1. Данные показывают, что скорость инкорпорации для меченого нуклеотида, содержащего вставку SS 130 (ffA-SS-NR550S0), была приблизительно в 2 раза быстрее по сравнению со скоростью инкорпорации для меченого нуклеотида, содержащего стандартный линкер 115 (ffA-NR550S0). Скорость инкорпорации для меченого нуклеотида, содержащего вставку AEDI 125 (ffA-AEDI-NR550S0), была приблизительно в 4 раза быстрее по сравнению со скоростью инкорпорации ffA-NR550S0. Данные также показывают, что скорость инкорпорации для меченого нуклеотида, содержащего стандартный линкер 115 и флуоресцентный краситель SO7181 (ffA-SO7181), была приблизительно в 4 раза быстрее по сравнению со скоростью инкорпорации ffA-NR550S0.
[0103] Фиг. 3А-3F иллюстрируют структурные формулы дополнительных вставок 310, 315, 320, 325, 330 и 335 для стандартного линкерного фрагмента 115, показанного на фиг. 1A. Во вставке ACA 310 диметиловые замещения удаляют, и связь сера-сера (SS) заменяют углерод-углеродной связью по сравнению со вставкой 125. Связь сера-сера не является необходимой для SBS (например, SBS с применением 2 красителей или 4 красителей).
[0104] Во вставке AcLys 315, ацетил-защищенный лизин используют для замены вставки 125.
[0105] Во вставке BocLys 320, трет-бутоксикарбонил-защищенный лизин используют для замены вставки 125.
[0106] Во вставке dMeO 325, связь сера-сера (S-S) заменяют связью кислород-углерод (O-CH2) по сравнению со вставкой 125.
[0107] Во вставке dMeS 330, связь сера-сера (S-S) заменяют связью сера-углерод (S-CH2) по сравнению со вставкой 125.
[0108] Во вставке DMP 335, связь сера-сера (S-S) заменяют связью сера-углерод (CH2) по сравнению со вставкой 125.
[0109] В различных примерах, описанных в настоящем документе, вставки, включая тип с диметил-замещением (например, вставка AEDI 125, вставка dMeO 325 и вставка dMeS 330), как было установлено, увеличивали скорость нуклеотидной инкорпорации в процессе SBS.
[0110] В различных примерах, описанных в настоящем документе, длина углеродных цепей во вставках также может быть изменена.
[0111] Фиг. 4 демонстрирует таблицу данных для хода секвенирования с применением двух красителей, используемого для оценки влияния вставки AEDI 125, показанной на фиг. 1B, и вставки AcLys 315, показанной на фиг. 3B, на качество секвенирования. Секвенирование проводили на гибридной платформе Miseq с помощью матрицы Human 550bp и 2 раза по 150 циклов. Новый набор красителей, V10/циан-пэг4 A-AEDI550S0, V10/циан-пэг4 A-AcLys550S0 и V10/циан A-AcLys 550S0, сравнивали со стандартным коммерческим набором красителей V4 и улучшенным набором красителей платформы Nova V5.75. Для каждого из образцов V10/циан-пэг4 A-AEDI550S0, V10/циан-пэг4 A-AcLys550S0 и V10/циан A-AcLys 550S0 значение фазирования (Ph R1) было ниже, чем значения фазирования образцов без вставок AEDI или AcLys. Таким образом, меченые нуклеотиды, содержащие дополнительные вставки 125 и 315, продемонстрировали улучшение качества секвенирования.
[0112] Фиг. 5А и 5В демонстрируют график частоты появления ошибок для считывания 1 и график частоты появления ошибок для считывания 2 хода секвенирования, показанного на фиг. 4, соответственно. Для считывания 1 частота появления ошибок V10/циан-пэг4 A-AEDI550S0 и V10/циан-пэг4 А-AcLys550S0 была ниже, чем того же набора красителей V10/циан-пэг4 без вставки. Для считывания 2 она становится еще более очевидной, когда используется вставка AcLys 315, где конечная частота появления ошибок была снижена на 30% по сравнению с набором красителей без вставки. Таким образом, вставки 125 и 315, как было доказано, значительно улучшают качество секвенирования.
[0113] Фиг. 6 демонстрирует таблицу данных для хода секвенирования, используемого для оценки влияния вставки AEDI 125 и вставки ACA 310 на качество секвенирования. Секвенирование проводили на гибридной платформе Miseq с матрицей Human 550bp и 2 раза по 150 циклов. Новый набор красителей, V10/циан-пэг4 A-AEDI550S0, V10/циан-пэг4 A-ACALys550S0, сравнивали со стандартным коммерческим набором красителей V4 и улучшенным набором красителей платформы Nova V5.75. Опять же, каждый из образцов V10/циан-пэг4 A-AEDI550S0 и V10/циан-пэг4 А-ACA550S0 имеет более низкое значение фазирования (Ph R1) по сравнению с образцами без вставок AEDI или ACA, и, таким образом, продемонстрировал улучшение качества секвенирования.
[0114] Фиг. 7A и 7B демонстрируют график частоты появления ошибок для считывания 1 и график частоты появления ошибок для считывания 2 хода секвенирования, показанного на фиг. 6, соответственно. Частота появления ошибок для считывания 1 для набора, содержащего новую вставку AEDI (V10/циан-пэг4 A-AEDI550S0), была ниже, чем того же набора красителей без вставки, V10/циан-пэг4. Вставка ACA (V10/циан-пэг4 ACA550S0) дала график частоты появления ошибок в обоих считываниях аналогичный стандартному V10/циан-пэг4. AEDI снова показала улучшение качества секвенирования. Эти данные также показали, что сама структура вставки оказывает влияние на улучшение качества секвенирования.
[0115] Фиг. 8А демонстрирует структурную формулу стандартного линкера LN3 800. Линкер LN3 800 включает первый замещенный амидо-функциональный фрагмент 810, второй азидо-замещенный ПЭГ-функциональный фрагмент 815 и третий сложноэфирный функциональный фрагмент 820, который может быть необходим в структуре линкера для связывания молекулы красителя 825 с нуклеотидом 830. Первый функциональный фрагмент 810 может, например, использоваться для присоединения молекулы красителя 825 к линкеру LN3 800. Второй функциональный фрагмент 815 может, например, быть расщепляемой функциональной группой, которая может использоваться для отщепления молекулы красителя 825 от линкера LN3 800. Третий функциональный фрагмент 820 может, например, использоваться для присоединения нуклеотида 830 к линкеру LN3 800. Фиг. 8B иллюстрирует определенную модификацию стандартного линкера LN3, где фенокси-фрагмент 850 замещен одним-четырьмя заместителями, выбранными из -NO2, -CN, галогена или -SO3H. Кроме того, сложноэфирный фрагмент 820 заменен амидным фрагментом 855.
[0115A] Фиг. 9А представляет собой график, показывающий появление примеси в ffA с SS-линкером. С ffA-SS-NR550S0 после очистки ВЭЖХ: примеси появились в течение ночи в слабощелочных условиях (pH8-9). К.т. в течение ночи в 0,1М ТЭАБ/CH3CN. Фиг. 9В сравнивает стабильность ffA с SS-линкером и AEDI-линкером, с AEDI-линкером демонстрирует значительно улучшенную стабильность
по сравнению с SS-линкерами. ffA-LN3-NR550S0 использовали в качестве внутреннего стандарта. Побочный дисульфидный продукт: (NR550S0 -S-)2. Фиг. 9С демонстрирует сравнение ffA с SS-линкером и AEDI-линкером в IMX 60° в течение 22 часов, снова показывая примесь с SS-линкером. Внутренним контролем является ffA-LN3-NR550S0. Ди-Р: дифосфат.
[0115B] Фиг. 10А, 10В и 10C демонстрируют неожиданное увеличение скорости нуклеотидной инкорпорации в растворе с изменениями линкера. Фиг. 10А демонстрирует скорость инкорпорации при 1 мкМ. Результаты показывают, что краситель и линкер оказывали значительное влияние на кинетику инкорпорации с таблицей 10B, ясно показывающей преимущество AEDI-линкера в кинетике инкорпорации. Фиг. 10C схематически демонстрирует линкеры AEDI и SS с NR550S0.
[0115C] Фиг. 11А демонстрирует диаграммы разброса данных для комбинаций V10 с различными А-550S0 (той же концентрации). Диаграммы разброса данных для цикла 2 тайла 1. Фиг. 11B демонстрирует линкеры Kcat FFA в растворе. Можно видеть, что на поверхности с точки зрения скорости инкорпорации AEDI-линкер быстрее, чем в отсутствие линкера: 'А'-облако (на диаграмме разброса данных) слегка движется в сторону центра. AcLys-линкер медленнее, чем AEDI и в отсутствие линкера: 'А'-облако движется в направлении оси х. BocLys-линкер похож на отсутствие линкера и не далеко от AEDI-линкера. В растворе можно видеть, что ACA-линкер был самым медленным, в то время как AEDI и ACLys имеют сходный Kcat, за ними следует BocLys.
[0115D] Фиг. 12А и 12B демонстрируют метрики секвенирования на M111, Human550, 2×151 циклов. Использование ffN в сочетании с различными А-550S0 (той же концентрации). Можно видеть, что как линкер AEDI, так и линкер BocLys дали сходные хорошие результаты секвенирования. Хотя Kcat раствора AEDI и AcLys похожи, результат секвенирования AEDI немного лучше.
[0116] Линкер LN3 800 включает дополнительный фенокси-фрагмент 835, который может быть удален из линкера LN3 800, как показано на фиг. 8C. Линкер LN3 800 также включает дополнительный амидо-фрагмент 840 и необязательный сложноэфирный фрагмент 845, оба из которых могут быть удалены из линкера LN3 800, как показано на фиг. 8D. Целью для удаления определенных функциональных групп, подобно амидному фрагменту 810, фенокси-фрагменту 835, является проверка того, имеют ли они негативные взаимодействия с ферментом во время нуклеотидной инкорпорации, что может снизить эффективность инкорпорации.
[0117] Фиг. 8E иллюстрирует вставку или добавление защитного фрагмента 860 в линкер. Защитный фрагмент 860 вставляют между функциональным фрагментом 810 (или может быть присоединен к фенокси-фрагменту 835 или 850 на фиг. 8A-8C) и молекулой красителя 825. Защитный фрагмент 860 может, например, представлять собой молекулу, которая защищает от повреждения ДНК. Повреждение ДНК, включая фото-повреждения или другие химические повреждения, является одним из кумулятивных эффектов (то есть, цикл за циклом) SBS. Существенное снижение или устранение повреждений ДНК может обеспечить более эффективное SBS и более долгие считывания секвенирования. В некоторых вариантах осуществления защитный фрагмент 860 может быть выбран из гасителя триплетного состояния, такого как Тролокс, галловая кислота, 2-меркаптоэтанол (BME) и т.д. В некоторых других вариантах осуществления защитный фрагмент 860 может быть выбран из реагента для гашения или защитного реагента, такого как 4-нитробензиловый спирт или соль аскорбиновой кислоты, такая как аскорбат натрия. В некоторых других вариантах осуществления защитный агент может быть физически примешан в буфер, а не образует ковалентные связи с меченым нуклеозидом или нуклеотидом. Тем не менее, этот подход может потребовать более высокую концентрацию защитного агента и может быть менее эффективным. В качестве альтернативы, защитный фрагмент, ковалентно присоединенный к нуклеозидам или нуклеотидам, может обеспечить лучшую защиту от повреждения ДНК. В некоторых других вариантах осуществления, показанных на фиг. 8С, 8D и 8Е, сложноэфирный фрагмент 820 может также быть заменен на амидо-фрагмент 855 и фенокси-фрагмент 835 и быть дополнительно замещенным.
[0118] В любом из примеров, продемонстрированных на фиг. 8A-8E, вставка AEDI 125 и вставка SS 130, показанные на фиг. 1В, и вставка 300, показанная фиг. 3A-3F, могут, например, быть вставлены между первым функциональным фрагментом 810 и молекулой красителя 825 линкера 800.
ПРИМЕРЫ
[0119] Дополнительные варианты осуществления раскрыты более подробно в следующих примерах, которые ни в коей мере не предназначены для ограничения объема формулы изобретения.
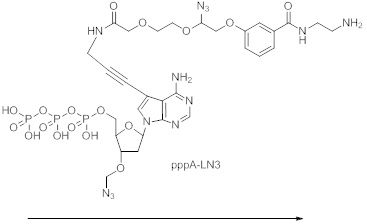
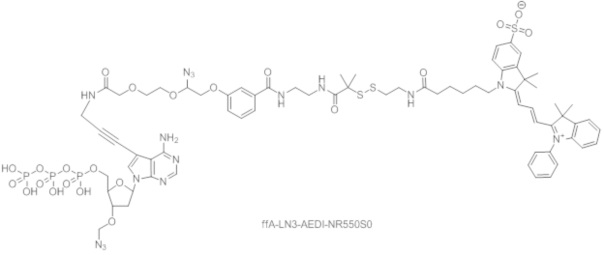
Общая методика реакции получения ffA-LN3-AEDI-NR550S0:
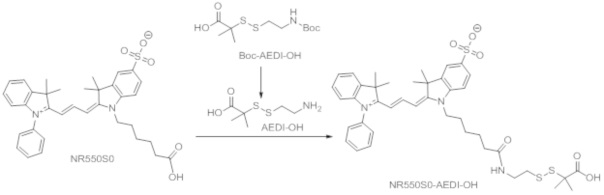
[0120] В 50 мл круглодонной колбе, растворяли Вос-AEDI-ОН (1 г, 3,4 ммоль) в ДХМ (15 мл) и добавляли ТФУК (1,3 мл, 17 мл) к раствору при комнатной температуре. Реакционную смесь перемешивали в течение 2-х часов. ТСХ (ДХМ:МеОН=9:1) указывала на полный расход Вос-AEDI-ОН. Реакционную смесь упаривали досуха. Затем к остатку добавляли ТЭАБ (2М, ~15 мл), и рН контролировали до нейтрального уровня. Смесь затем растворяли в H2O/CH3CN (1:1, ~15 мл) и упаривали досуха. Процедуру повторяли 3 раза, чтобы удалить избыток соли ТЭАБ. Твердый остаток белого цвета обрабатывали с помощью CH3CN (20 мл) и перемешивали в течение 0,5 часа. Отфильтровывая раствор и промывая твердое вещество с помощью CH3CN, получали чистую соль AEDI-ОН-ТФУК (530 мг, 80%). 1H ЯМР (400 МГц, D2O, δ (м.д.)): 3,32 (т, J=6,5 Гц, 2H, NH2-CH2); 2,97 (т, J=6,5 Гц, 2H, S-CH2); 1,53 (с, 6H, 2× СН3). 13С ЯМР (400 МГц, D2O, δ (м.д.)): 178,21 (с, СО); 127,91, 117,71 (2с, ТФУК); 51,87 (с, С-(CH3)2); 37,76 (т, СН2-NH2); 34,23 (т, S-CH2); 23,84 (д, 2× СН3). 19F ЯМР (400 МГц, D2O, δ (м.д.)): -75,64.
[0121] В 50 мл круглодонной колбе краситель NR550S0 (114 мг, 176 мкмоль) растворяли в ДМФА (безводный, 20 мл) и упаривали досуха. Процедуру повторяли в 3 раза. Безводный ДМА (10 мл) и основание Хаггиса (92 мкл, 528 мкмоль, 3 эквивалента) затем прикапывали с помощью пипетки в круглодонную колбу. TSTU (69 мг, 228 мкмоль, 1,3 эквивалента) добавляли в виде одной порции. Реакционную смесь выдерживали при комнатной температуре. Через 30 мин анализ ТСХ (CH3CN:H2O=85:15) показал, что реакция завершена. AEDI-OH (68 мг, 352 мкмоль, 2 эквивалента) в 0,1 М ТЭАБ добавляли к реакционной смеси и перемешивали при комнатной температуре в течение 3 ч. ТСХ (CH3CN:H2O=8:2) показала полный расход активированного сложного эфира, и красное пятно появилось ниже активированного сложного эфира. В то же время аналитическая ВЭЖХ также показала полный расход активированного сложного эфира и образование продукта. Реакцию гасили с помощью буфера ТЭАБ (0,1М, 10 мл), и летучий растворитель удаляли при пониженном давлении испарения (HV) и очищали на колонке Axia с получением NR550S0-AEDI-ОН. Выход: 60%.
[0122] В 25 мл круглодонной колбе NR550S0-AEDI-ОН (10 мкмоль) растворяли в ДМФА (безводный, 5 мл) и выпаривали досуха. Процедуру повторяли 3 раза. Затем безводный ДМА (5 мл) и ДМАП (1,8 мл, 15 мкмоль, 1,5 эквивалента) добавляли в круглодонную колбу. ДСК (5,2 мг, 20 мкмоль, 2 эквивалента) добавляли в виде одной порции. Реакционную смесь выдерживали при комнатной температуре. Через 30 мин анализ ТСХ (CH3CN:H2O=8:2) показал, что реакция завершена. Основание Хаггиса (3,5 мкл, 20 мкмоль) прикапывали с помощью пипетки к реакционной смеси. Затем раствор pppA-LN3 (20 мкмоль в 0,5 мл H2O, 2 эквивалента) и Et3N (5 мкл) добавляли к реакционной смеси и перемешивали при комнатной температуре в течение ночи. ТСХ (CH3CN:H2O=8:2) показала полный расход активированного сложного эфира, и красное пятно появилось на нулевой линии. В то же время аналитическая ВЭЖХ также показала полный расход активированного сложного эфира и образование конечного продукта. Реакцию гасили с помощью буфера ТЭАБ (0,1М, 10 мл) и наносили на колонку DEAE Sephadex (25 г колонка Biotage). Колонку элюировали с градиентом, как показано ниже в таблице 2.
A: 0,1 M буфер ТЭАБ (10% CH3CN)
B: 1 М буфер ТЭАБ (10% CH3CN).
Градиент:
[0123] Целевой продукт элюировали из 45%-100% 1 М буфера ТЭАБ. Фракцию, содержащую продукт, объединяли, упаривали и очищали с помощью ВЭЖХ (колонка YLC, 8 мл/мин). Выход: 53%.
[0124] Таким образом, настоящее изобретение может относиться к нуклеозиду или нуклеотиду, ковалентно присоединенному к флуорофору через линкер, где указанный линкер содержит структуру формулы (I) или (II), или комбинацию обоих:
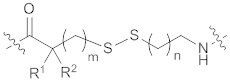 (I),
(I), 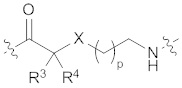 (II),
(II),
где
каждый из R1 и R2 независимо выбран из водорода или необязательно замещенного C1-6 алкила;
R3 выбран из водорода, необязательно замещенного С1-6 алкила, -NR5-C(=O)R6 или -NR7-C(=O)-OR8;
R4 выбран из водорода или необязательно замещенного C1-6 алкила;
каждый из R5 и R7 независимо выбран из водорода, необязательно замещенного C1-6 алкила, необязательно замещенного фенила или необязательно замещенного C7-12 аралкила;
каждый из R6 и R8 независимо выбран из необязательно замещенного C1-6 алкила, необязательно замещенного фенила, необязательно замещенного C7-12 аралкила, необязательно замещенного C3-7 циклоалкила или необязательно замещенного 5-10-членного гетероарила;
каждое из метиленовых повторяющихся звеньев в 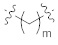 ,
, 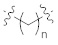 или
или 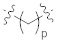 является необязательно замещенным;
является необязательно замещенным;
Х выбран из метилена (СН2), кислорода (О) или серы (S);
m представляет собой целое число от 0 до 20;
n представляет собой целое число от 1 до 20; и
p представляет собой целое число от 1 до 20, при условии, что меченый флюорофором нуклеозид или нуклеотид не имеет структуру:
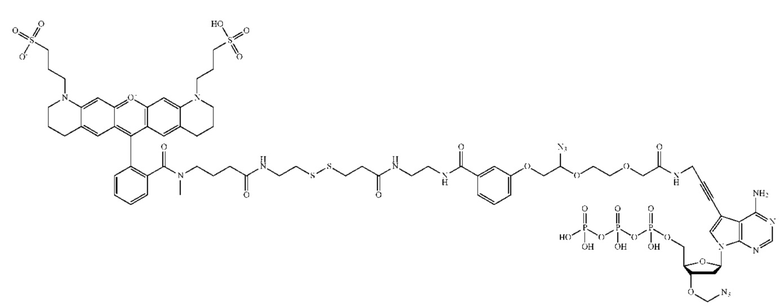
[0125] В некоторых случаях нуклеозида или нуклеотида, указанного выше, структура формулы (I) также представлена формулой (Ia) или (Ib):
 (Ia),
(Ia),  (Ib).
(Ib).
Кроме того, структура формулы (II) также может быть представлена формулой (IIа), (IIb), (IIc), (IId), (IIe) или (IIf):
 (IIa),
(IIa),  (IIb),
(IIb),  (IIc),
(IIc),  (IId),
(IId),
 (IIe) или
(IIe) или  (IIf).
(IIf).
[0126] Более конкретно настоящее изобретение может относиться к нуклеозиду или нуклеотиду, ковалентно присоединенному к флуорофору через линкер, где указанный линкер содержит структуру формулы (I) или (II), или комбинацию обоих:
 (I),
(I), 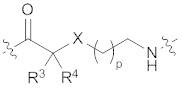 (II),
(II),
где
R1 выбран из необязательно замещенного C1-6 алкила;
R2 выбран из водорода или необязательно замещенного C1-6 алкила;
R3 выбран из необязательно замещенного C1-6 алкила, -NR5-C(=O)R6 или -NR7-C(=O)-OR8;
R4 выбран из водорода или необязательно замещенного C1-6 алкила;
каждый из R5 и R7 независимо выбран из водорода, необязательно замещенного C1-6 алкила, необязательно замещенного фенила или необязательно замещенного C7-12 аралкила;
каждый из R6 и R8 независимо выбран из необязательно замещенного C1-6 алкила, необязательно замещенного фенила, необязательно замещенного C7-12 аралкила, необязательно замещенного C3-7 циклоалкила или необязательно замещенного 5-10-членного гетероарила;
каждое из метиленовых повторяющихся звеньев в 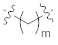 ,
, 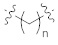 или
или 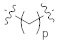 является необязательно замещенным;
является необязательно замещенным;
Х выбран из метилена (СН2), кислорода (О) или серы (S);
m представляет собой целое число от 0 до 20;
n представляет собой целое число от 1 до 20; и
р представляет собой целое число от 1 до 20.
[0127] Предпочтительно, чтобы структура формулы (I) также была представлена формулой (Ia):
 (Ia).
(Ia).
Кроме того, структура формулы (II) также представлена формулой (IIb), (IIc), (IId), (IIe) или (IIf):
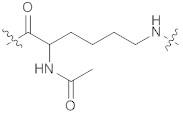 (IIb),
(IIb),  (IIc),
(IIc),  (IId),
(IId),
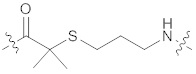 (IIe) или
(IIe) или  (IIf).
(IIf).
| название | год | авторы | номер документа |
|---|---|---|---|
| НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ С 3’-ГИДРОКСИ БЛОКИРУЮЩИМИ ГРУППАМИ И ИХ ПРИМЕНЕНИЕ В СПОСОБАХ СЕКВЕНИРОВАНИЯ ПОЛИНУКЛЕОТИДОВ | 2019 |
|
RU2818762C2 |
| МУЛЬТИПЛЕКСНОЕ ФЛУОРЕСЦЕНТНОЕ ОБНАРУЖЕНИЕ АНАЛИТОВ | 2020 |
|
RU2816515C2 |
| ПОЛИМЕТИНОВЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФЛУОРЕСЦЕНТНЫХ МЕТОК | 2016 |
|
RU2696562C1 |
| КУМАРИНЫ, ЗАМЕЩЕННЫЕ ВТОРИЧНЫМИ АМИНАМИ, И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФЛУОРЕСЦЕНТНЫХ МЕТОК | 2018 |
|
RU2756272C2 |
| ТАГМЕНТАЦИЯ С ПРИМЕНЕНИЕМ ИММОБИЛИЗОВАННЫХ ТРАНСПОСОМ С ЛИНКЕРАМИ | 2018 |
|
RU2783536C2 |
| НОВЫЕ КОМБИНАЦИИ ГАСИТЕЛЯ И РЕПОРТЕРНОГО КРАСИТЕЛЯ | 2019 |
|
RU2795062C2 |
| МОДИФИЦИРОВАННЫЕ НУКЛЕОЗИДЫ, НУКЛЕОТИДЫ И НУКЛЕИНОВЫЕ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2707251C2 |
| МОДИФИЦИРОВАННЫЕ НУКЛЕОЗИДЫ, НУКЛЕОТИДЫ И НУКЛЕИНОВЫЕ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2648950C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ХИМИЧЕСКОГО РАСЩЕПЛЕНИЯ И СНЯТИЯ ЗАЩИТЫ ДЛЯ СВЯЗАННЫХ С ПОВЕРХНОСТЬЮ ОЛИГОНУКЛЕОТИДОВ | 2019 |
|
RU2766688C2 |
| ХЕМОСЕЛЕКТИВНАЯ ТИОЛ-КОНЪЮГАЦИЯ С АЛКЕН- ИЛИ АЛКИН-ФОСФОНОТИОЛАТАМИ И -ФОСФОНАТАМИ | 2019 |
|
RU2825582C2 |


Изобретение относится к нуклеотиду, ковалентно присоединенному к флуорофору через линкер А, который может быть использован в технологиях анализа нуклеиновых кислот, соответствующему формуле:
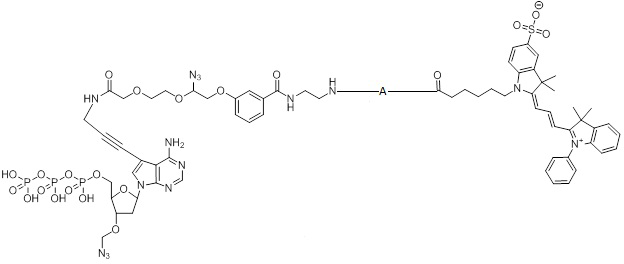 ,
,
где линкер А имеет структуру формулы (I) или (II):
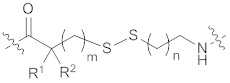 (I),
(I), 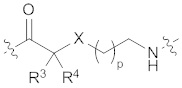 (II),
(II),
каждый из R1 и R2 представляет собой метил, m представляет собой 0, n представляет собой 1; R3 представляет собой -NH-C(=O)O-трет-бутил, R4 представляет собой водород, Х представляет собой СН2 и p равен 2; или R3 представляет собой -NH-C(=O)СН3, R4 представляет собой водород, Х представляет собой СН2 и p равен 2. Предложен новый модифицированный нуклеотид и набор на его основе для повышения эффективности нуклеотидной инкорпорации в секвенирования путем синтеза. 2 н. и 2 з.п. ф-лы, 12 ил., 2 табл., 1 пр.
1. Нуклеотид, ковалентно присоединенный к флуорофору через линкер А и соответствующий формуле:
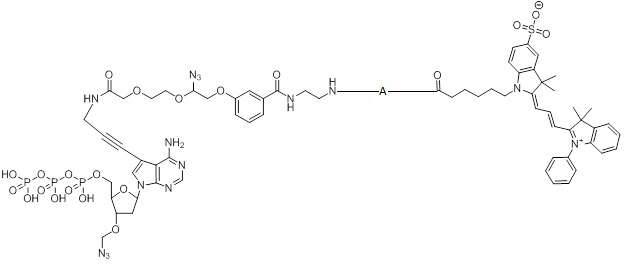 ,
,
где линкер А имеет структуру формулы (I) или (II):
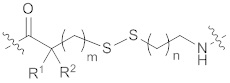 (I),
(I), 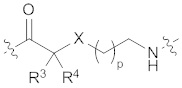 (II),
(II),
где
каждый из R1 и R2 представляет собой метил, m представляет собой 0, n представляет собой 1;
R3 представляет собой -NH-C(=O)O-трет-бутил, R4 представляет собой водород, Х представляет собой СН2 и p равен 2; или
R3 представляет собой -NH-C(=O)СН3, R4 представляет собой водород, Х представляет собой СН2 и p равен 2.
2. Нуклеотид по п.1, где линкер А имеет структуру формулы (Ia):
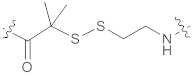 (Ia).
(Ia).
3. Нуклеотид по п.1, где линкер А имеет структуру формулы (IIb) или (IIc):
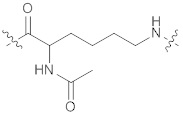 (IIb),
(IIb), 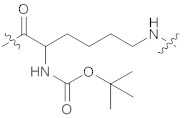 (IIc).
(IIc).
4. Набор, содержащий нуклеотид по любому из пп.1-3.
| МЕТАЛЛОРЕЖУЩИЙ СТАНОК ГЛУБОКОГО СВЕРЛЕНИЯ | 1995 |
|
RU2088381C1 |
| WO 2013044018 A1, 28.03.2013 | |||
| WO 2005044836 A2, 19.05.2005 | |||
| US 2007166705 A1, 19.07.2007 | |||
| WO 03048387 A2, 12.06.2003 | |||
| CN 103087131 A, 08.05.2013 | |||
| WO 2009051807 A1, 23.04.2009 | |||
| WO 2004090154 A2, 21.10.2004 | |||
| WO 2002086088 A2, 31.10.2002 | |||
| WO 2012159072 A2, 22.11.2012 | |||
| P | |||
| SURESH JAYASEKARA et al | |||
| Journal of medicinal chemistry, 2014, vol | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| СНЕГОВОЙ ПЛУГ ДЛЯ ЛОКОМОТИВА | 1925 |
|
SU3874A1 |
| US 20120252691 A1, 04.10.12 | |||
| WO 2000036152 A1, 22.06.2000 | |||
| RU 2009121089 A, 20.01.2011. | |||
Авторы
Даты
2019-09-12—Публикация
2015-08-06—Подача