Изобретение относится к ветеринарной микробиологии, в частности к лабораторной диагностике возбудителей инфекционных заболеваний, а именно к средствам диагностики инфекции у животных.
Известен способ выявления вируса лейкоза КРС по нуклеотидным последовательностям консервативных областей вирусного генома с использованием полимеразной цепной реакции в реальном времени (патент РФ №2521330, кл. C12Q 1/68, G01N 33/569, 2013 г. ), включающий выделение ДНК вируса лейкоза из биологического материала от инфицированных животных сорбционным методом, постановку полимеразной цепной реакции - с добавлением внутреннего положительного контроля и проведением последовательно 40 циклов амплификации с флуоресцентной детекцией в реальном времени с использованием специфичных для участка генома возбудителя олигонуклеотидных праймеров, флуоресцентно-меченного зонда, положительного и отрицательного контрольных образцов, измерение накопления флуоресцентного сигнала по каналам соответствующих флуоресцентных красителей для специфического сигнала и сигнала внутреннего контроля и интерпретацию результатов на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией
Также известен способ диагностики лейкоза крупного рогатого скота методом полимеразной цепной реакции, заключается в том, что используют прямой и обратный олигонуклеотидные праймеры для выявления фрагмента гена pol провируса лейкоза крупного рогатого скота (патент РФ №2445370, кл. C12Q 1/68, G01N 33/569, 2012 г. - прототип). В известном способе проводят электрофоретическое определение размера амплифицируемого фрагмента нуклеотидной последовательности, выделяют ДНК провируса сорбционным методом, осуществляют постановку одноэтапной полимеразной цепной реакции - с одновременным проведением не более 40 циклов амплификации с детекцией с использованием специфичных для участка генома провируса лейкоза крупного рогатого скота олигонуклеотидных праймеров, зондов, красителей и контрольных образцов в виде внутреннего и положительного, измерение специфического сигнала и сигнала контроля по каналам соответствующих красителей и интерпретацию результатов.
Однако в известном способе последовательность непосредственно читается по электрофореграмме. Длина фрагмента, который может быть расшифрован этим методом, ограничивается разрешающей способностью метода гель-электрофореза.
Общим недостатком известных технических решений является отсутствие возможности получения достоверной диагностики выявления генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) с целью выявления лейкоза на ранней стадии.
Техническим результатом заявляемого технического решения является получение достоверной диагностики выявления генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) с целью выявления лейкоза на ранней стадии.
Технический результат достигается тем, что в способе выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) включающий выделение ДНК из биологического материала от инфицированных животных сорбционным методом, постановку одноэтапной полимеразной цепной реакции - с одновременным проведением циклов амплификации с детекцией с использованием специфичных для участка генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) олигонуклеотидных праймеров, зондов, красителей и контрольных образцов в виде внутреннего и положительного, измерение специфического сигнала и сигнала контроля по каналам соответствующих красителей и интерпретацию результатов, согласно изобретению проводят флуоресцентную детекцию, измеряют по каналу JOE(HEX)/Yellow накопление флуоресцентного сигнала для специфического сигнала тестирования наличия генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), а по каналу FAM/Green - сигнал внутреннего контрольного образца и осуществляют интерпретацию результатов на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией, если кривые накопления флуоресцентного сигнала выходят до 35 цикла, то результат реакции считается положительным, а если кривые не пересекают пороговую линию или пересекают ее после 35 цикла, то результат реакции - отрицательный, при этом для внутреннего контрольного образца используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, а для положительного контрольного образца используют смесь рекомбинантных плазмидных ДНК, содержащих фрагмент генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) и фрагмент генома бактериофага Т4 взятых в соотношении 1:1, со следующими нуклеотидными последовательностями:
TMBLV-F CCTACTTTCAGACCCCCTTGAC прямой праймер
TMBLV-R CATAAGAGCTTAAGGCCTGAG обратный праймер
TMBLV-P R6G CCAAGCCTCACCTTGGGGCCTCCT BHQ1 зонд
T4F TACATATAAATCACGCAAAGC
T4R TAGTATGGCTAATCTTATTGG
Т4Р FAM ACATTGGCACTGACCGAGTTC BHQ1ЗОНД.
Новизна заявляемого технического решения заключается в том, что для получения достоверной диагностики генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) проводят реакцию в одной ПРЦ-пробирке (one-tube) с использованием специфичных для участка генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) олигонуклеотидных праймеров флуоресцентно-меченного зонда и разных видов контроля для которых используют различные формы материала бактериофага Т4: суспензия и фрагмент генома со специфическими к нему праймерами и зондом. Такая постановка ПЦР в реальном времени сокращает и упрощает процедуру анализа, снижает риск контаминации. Кроме того, флуоресцентная детекция продуктов амплификации осуществляется с использованием принципа выщепления флуоресцентной метки на 5' конце олигонуклеотидного зонда.
Признаки, отличающие заявляемое техническое решение от прототипа, направлены на достижение технического результата и не выявлены при изучении данной и смежной областей науки и техники и, следовательно, соответствуют критерию «изобретательский уровень».
Заявляемый способ рекомендовано использовать в ветеринарной вирусологии, так как относится к средствам диагностики генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), что соответствует критерию «промышленная применимость».
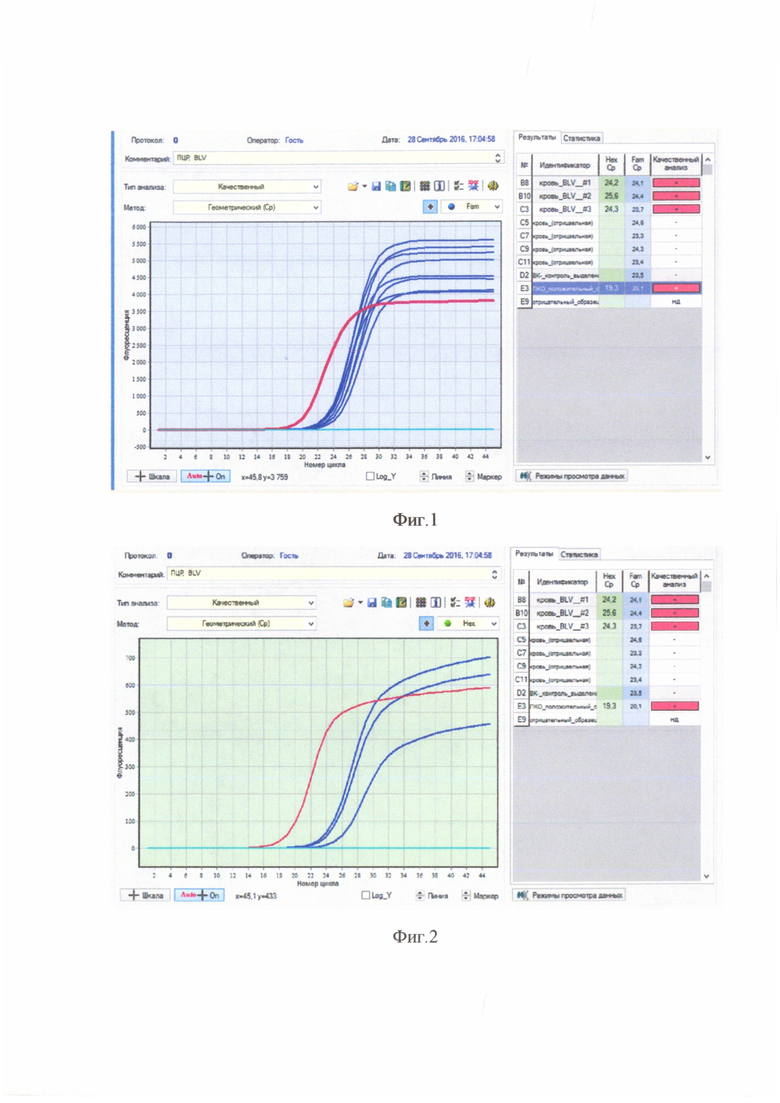
Сущность изобретения поясняется чертежами, где представлены скриншоты графиков, на фиг. 1 - представлен канал FAM/Green - для тестирования сигнала от внутреннего контрольного образца - ВКО; на фиг. 2 Канал JOE(HEX)/Yellow накопление флуоресцентного сигнала для специфического сигнала тестирования наличия генома (Bovine leukosis virus, BLV). Способ выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) осуществляется следующим образом.
Предварительно сорбционным методом выделяют из биологического материала, геном провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), взятый от животных.
Далее проводят постановку одноэтапной полимеразной цепной реакции - с одновременным проведением циклов амплификации с флуоресцентной детекцией с использованием специфичных для участка генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) олигонуклеотидных праймеров, зондов, красителей и контрольных образцов в виде внутреннего и положительного, измерение специфического сигнала и сигнала контроля по каналам соответствующих красителей и интерпретацию результатов, измеряют по каналу JOE(HEX)/Yellow накопление флуоресцентного сигнала для специфического сигнала тестирования наличия генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), а по каналу FAM/Green - сигнал внутреннего контрольного образца. Затем осуществляют интерпретацию результатов проводят на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией, если кривые накопления флуоресцентного сигнала выходят до 35 цикла, то результат реакции считается положительным, а если кривые не пересекают пороговую линию или пересекают ее после 35 цикла, то результат реакции - отрицательный, при этом для внутреннего контрольного образца используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, а для положительного контрольного образца используют смесь рекомбинантных плазмидных ДНК, содержащих фрагмент генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) и фрагмент генома бактериофага Т4 взятых в соотношении 1:1, со следующими нуклеотидными последовательностями:
TMBLV-F CCTACTTTCAGACCCCCTTGAC прямой праймер
TMBLV-R CATAAGAGCTTAAGGCCTGAG обратный праймер
TMBLV-P R6G CCAAGCCTCACCTTGGGGCCTCCT BHQ1 зонд
T4F TACATATAAATCACGCAAAGC
T4R TAGTATGGCTAATCTTATTGG
Т4Р FAM ACATTGGCACTGACCGAGTTC BHQ1ЗОНД.
Использование для разных видов контроля различные формы материала бактериофага Т4: суспензии и фрагмента генома со специфическими к нему праймерами и зондом обусловлено тем, что это позволяет контролировать корректное прохождение реакции в каждой пробирки, а также контролируется этап выделения ДНК из образцов.
Выбор последовательности и расчет первичной структуры олигонуклеотидных праймеров и зондов.
Праймеры, специфичные для ДНК Bovine leukosis virus были отобраны на основе консервативного участка гена "pol" (Bovine leukemia virus complete genome, AF033818.1) и спроектированы с использованием Primer Express Software v3.0 (Applied Biosystems). С помощью BLAST праймеры были проверены на отсутствие гомологии с последовательностями других вирусов и генома человека. Термодинамический анализ выбранных праймеров был выполнен с помощью Vector NTI. Расчетная длина специфического фрагмента составила 98 пар нуклеотидов.
Для детекции продуктов амплификации был подобран олигонуклеотидный флуоресцентно-меченный зонд TMBLV-P (комплементарный участку нуклеотидной последовательности, ограниченной позициями отжига праймеров TMBLV-F и TMBLV-R). Зонд был помечен красителем R6G. Для гашения самопроизвольной флуоресценции на 3`-конце олигонуклеотидного зонда прикреплен гаситель BHQ-1. Основные свойства рассчитанных олигонуклеотидов, определившие возможность их использования в ПЦР были описаны с помощью программы "Oligo 6.0".
В качестве внутреннего контрольного образца использовался бактериофаг Т4, имеющий геномную ДНК порядка 169 - 170 тысяч пар нуклеотидов (Enterobacteria phage Т4Т, complete genome GenBank: HM137666.1). В результате анализа был выбран участок между 400 и 500 нуклеотидами, содержащий уникальные нуклеотидные последовательности, рассчитаны первичные структуры олигонуклеотидных праймеров, фланкирующих выбранный участок генома. Праймеры были спроектированы с использованием Primer Express Software v3.0 (Applied Biosystems) и исследованы с использованием BLAST, чтобы подтвердить их специфичность.
Пример конкретного осуществления способа выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV)
Для исследования используют цельную кровь. Исследования проводили для взрослых особей и телят старше 14-ти дневного возраста. Кровь отбирали из яремной или хвостовой вены в стерильные пробирки с 3% раствором ЭДТА из расчета 10:1.
Для взятия крови использовали одноразовые системы.
Пробы цельной крови с ЭДТА использовали для экстракции ДНК без предварительной подготовки.
Для исследования использовали набор реагентов в соответствии инструкцией по применению набора реагентов «ПЦР-ЛЕЙКО3-КРС-ФАКТОР» для выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) в биологическом материале методом полимеразной цепной реакции (ПЦР) с флуоресцентной детекцией в режиме реального времени ТУ 21.10.60-118-51062356-2016, для диагностики in vitro, (http://www.vetfaktor.ru/.).
Набор состоит из комплекта реагентов для проведения мультиплексной ПЦР РВ (комплект №1) и комплекта контрольных образцов (комплект №2).
Состав набора приведен в таблицах 1 и 2.
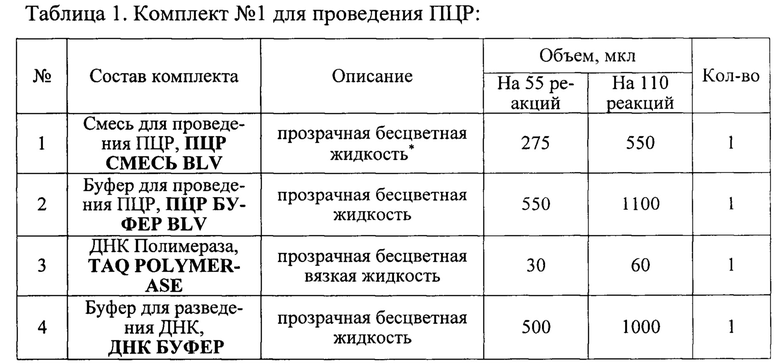
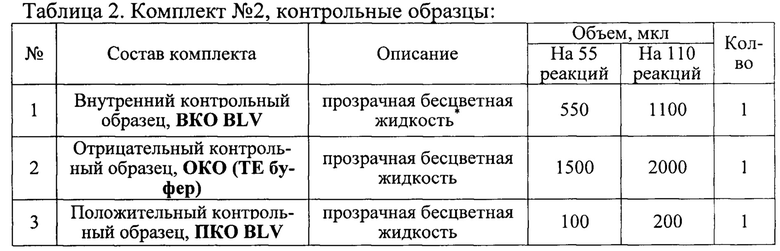
* Возможна легкая опалесценция
В набор не входят реактивы для экстракции нуклеиновых кислот.Выделение ДНК может проводиться, например, с помощью наборов на основе сорбционного метода, в состав которых входит силика или микроцентрифужные колонки, и также наборов на основе фенол-хлороформной экстракции и т.п.Рекомендуется использовать набор «ДНК/РНК-С-ФАКТОР» либо аналогичный.
Анализ исследуемых проб состоял из трех этапов:
- экстракция нуклеиновых кислот (НК);
- проведение ПЦР РВ;
- учет результатов анализа.
Экстракцию (выделение) НК из исследуемых проб проводили следующим образом. Отбирают необходимое количество одноразовых пробирок объемом 1,5 мл, включая отрицательный контроль выделения. Вносят во все пробирки с исследуемыми образцами, включая пробирку для отрицательного контрольного образца (ОКО) по 10 мкл внутреннего контрольного образца (ВКО) BLV.
Вносят исследуемые пробы в объеме согласно инструкции к набору для выделения НК, в пробирку отрицательного контроля выделения (ВК-) вместо исследуемой пробы вносят ОКО, в качестве которого используют деионизированную воду (пробирку обозначить как ВК-).
Подготовка образцов к проведению ПЦР Общий объем реакционной смеси должен быть 25 мкл, а объем ДНК-пробы - 10 мкл. Успешное прохождение реакции контролируют использованием положительного контрольного образца (ПКО) BLV, ВКО BLV и ДНК буфера, где для внутреннего контрольного образца (ВКО) используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, если концентрация копий нуклеотидных последовательностей отклоняется в большую или меньшую сторону, то наблюдаются повторности сомнительных образцов. Для положительного контрольного образца (ПКО) используют смесь рекомбинантных плазмидных ДНК, содержащих фрагмент генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) и фрагмент генома бактериофага Т4, взятых в соотношении 1:1, по 5 ООО копий специфического фрагмента в 10 мкл (в соотношении 1:1), если соотношение фрагментов отклоняется в большую или меньшую сторону, то также наблюдаются повторности сомнительных образцов
В отдельной пробирке смешивают компоненты набора из расчета на каждую реакцию ПЦР: 5 мкл ПЦР СМЕСЬ BLV; 10 мкл смеси ПЦР БУФЕР BLV; 0,5 мкл TAQ POLYMERASE
Перемешивают смесь на вортексе и сбрасывают капли кратковременным центрифугированием.
Отбирают необходимое количество пробирок для амплификации ДНК исследуемых и контрольных проб. Вносят по 15 мкл приготовленной реакционной смеси.
Используя наконечники с фильтром, в подготовленные пробирки вносят:
а) в пробирку отрицательного контроля ПЦР (К-) 10 мкл ДНК буфера;
б) в ряд пробирок для исследуемых проб - в каждую внести по 10 мкл ДНК соответствующей пробы, полученной по п. 7.1 (включая пробу ВК-);
в) в пробирку с положительным контролем ПЦР (К+) 10 мкл ПКО BLV. Далее проводят ПЦР РВ с флуоресцентной детекцией с помощью прибора «Rotor-Gene Q».

Помещают подготовленные для проведения ПЦР пробирки в ячейки амплификатора и программируют прибор согласно инструкции производителя.
После завершения программы амплификации отработанные пробирки утилизируют в соответствии с МУ 1.3. 2569 -09. и проводят интерпретацию результатов анализа.
Полученные данные - кривые накопления флуоресцентного сигнала анализируются с помощью программного обеспечения используемого прибора для проведения ПЦР в режиме «реального времени» в соответствии с инструкцией производителя к прибору.
Учет результатов ПЦР-анализа проводится по наличию или отсутствию пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией (что соответствует наличию или отсутствию значения порогового цикла «Ct» для исследуемого образца).
Результат считается достоверным в случае корректного прохождения положительных и отрицательных контролей амплификации и экстракции ДНК в соответствии с таблицей 4, фиг. 1, 2.

Появление любого значения Ct в таблице результатов для отрицательного контроля этапа экстракции ВК- на канале JOE(HEX)/Yellow (фиг. 2) и для отрицательного контроля этапа ПЦР К- на любом из каналов свидетельствует о наличии контаминации реактивов или образцов. В этом случае результаты анализа по всем пробам считаются недействительными. Требуется повторить анализ всех проб, а также предпринять меры по выявлению и ликвидации источника контаминации.
Образцы, для которых по каналу FAM/Green (фиг. 1) значение Ct отсутствует или превышает 32 цикл (и при этом по каналу JOE(HEX)/Yellow отсутствует значение Ct) требуют повторного проведения исследования с этапа ПЦР. Задержка в значениях пороговых циклов для исследуемых образцов на канале FAM/Green указывает на присутствие ингибиторов в пробе(ах) или на ошибки при экстракции ДНК или при постановке реакции. Требуется провести исследование, начиная с этапа экстракции ДНК.
Образец считается положительным (ДНК провируса лейкоза КРС присутствует), если наблюдается экспоненциальный рост сигнала на канале JOE(HEX)/Yellow (фиг. 2), при этом значения Ct контрольных образцов находятся в пределах нормы (табл. 4). Если для исследуемого образца по каналу JOE(HEX)/Yellow значение Ct определяется позднее 32 цикла при корректном прохождении положительных и отрицательных контролей - он считается спорным и исследуется повторно с этапа выделения НК. Если при повторной постановке наблюдается схожий результат (Ct на канале JOE(HEX)/Yellow более 32), требуется повторное взятие материала от того же животного для проведения ПЦР-исследования и (или) использование альтернативных методов диагностики.
В случае получения значения Ct на канале JOE(HEX)/Yellow менее 32 при исследовании повторно взятого от животного материала - образец считать положительным.
Образец считается отрицательным (ДНК провируса лейкоза КРС отсутствует), если не наблюдается рост сигнала флуоресценции на канале JOE(HEX)/Yellow, при этом значения Ct по каналу FAM/Green и Ct контрольных образцов находятся в пределах нормы (Табл. 4).
Для доказательства эффективности использования ПЦР с флуоресцентной детекцией в режиме реального времени проводился сравнительный анализ чувствительности заявляемого с прототипом, в котором использовался метод ПЦР с электрофоретической детекцией. Оказалось чувствительность ПЦР с флуоресцентной детекцией при обнаружении ДНК провируса лейкоза КРС на 4,2-5% выше, чем ПЦР с электрофоретической детекцией.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) в продуктах питания методом полимеразной цепной реакции в режиме реального времени | 2022 |
|
RU2794654C1 |
| Тест-система для выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) | 2018 |
|
RU2700450C1 |
| Тест-система для выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) в продуктах питания методом полимеразной цепной реакции в режиме реального времени | 2022 |
|
RU2782573C1 |
| Способ выявления ДНК вируса ринотрахеита (bovine herpes virus 1, BoHV-1) у крупного рогатого скота | 2018 |
|
RU2700449C1 |
| Тест-система для выявления ДНК вируса ринотрахеита (bovine herpes virus 1, BoHV-1) у крупного рогатого скота | 2018 |
|
RU2700254C1 |
| Способ диагностики вируса лейкоза крупного рогатого скота | 2018 |
|
RU2694966C1 |
| Способ выявления генома возбудителя вируса парагриппа 3 типа у крупного рогатого скота | 2018 |
|
RU2696069C2 |
| Тест-система для обнаружения генома вируса парагриппа 3 типа у крупного рогатого скота с помощью мультиплексной полимеразной цепной реакции с флуоресцентной детекцией в режиме реального времени | 2018 |
|
RU2681473C1 |
| Способ диагностики лейкоза крупного рогатого скота методом полимеразной цепной реакции | 2018 |
|
RU2694617C1 |
| Тест-система для выявления ДНК возбудителя криптоспоридиоза (Cryptosporidiosis) в биологическом материале животных и кормах с помощью полимеразной цепной реакции в режиме реального времени | 2021 |
|
RU2785381C1 |
Изобретение относится к области биотехнологии. Изобретение представляет собой способ выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), включающий выделение ДНК из биологического материала от инфицированных животных сорбционным методом, постановку одноэтапной полимеразной цепной реакции с одновременным проведением циклов амплификации с детекцией с использованием специфичных для участка генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) олигонуклеотидных праймеров, зондов, красителей и контрольных образцов в виде внутреннего и положительного, измерение специфического сигнала и сигнала контроля по каналам соответствующих красителей и интерпретацию результатов, согласно изобретению проводят флуоресцентную детекцию, измеряют по каналу JOE(HEX)/Yellow накопление флуоресцентного сигнала для специфического сигнала тестирования наличия генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), а по каналу FAM/Green - сигнал внутреннего контрольного образца и осуществляют интерпретацию результатов на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией, если кривые накопления флуоресцентного сигнала выходят до 35 цикла, то результат реакции считается положительным, а если кривые не пересекают пороговую линию или пересекают ее после 35 цикла, то результат реакции - отрицательный, при этом для внутреннего контрольного образца используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, а для положительного контрольного образца используют смесь рекомбинантных плазмидных ДНК, содержащих фрагмент генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) и фрагмент генома бактериофага Т4, взятых в соотношении 1:1. Изобретение позволяет достоверно диагностировать выявление генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) с целью выявления лейкоза на ранней стадии. 2 ил., 4 табл.
Способ выявления ДНК провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), включающий выделение ДНК из биологического материала от инфицированных животных сорбционным методом, постановку одноэтапной полимеразной цепной реакции с одновременным проведением циклов амплификации с детекцией с использованием специфичных для участка генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) олигонуклеотидных праймеров, зондов, красителей и контрольных образцов в виде внутреннего и положительного, измерение специфического сигнала и сигнала контроля по каналам соответствующих красителей и интерпретацию результатов, отличающийся тем, что проводят флуоресцентную детекцию, измеряют по каналу JOE(HEX)/Yellow накопление флуоресцентного сигнала для специфического сигнала тестирования наличия генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV), a по каналу FAM/Green - сигнал внутреннего контрольного образца и осуществляют интерпретацию результатов на основании наличия/отсутствия пересечения кривой флуоресценции с пороговой линией, если кривые накопления флуоресцентного сигнала выходят до 35 цикла, то результат реакции считается положительным, а если кривые не пересекают пороговую линию или пересекают ее после 35 цикла, то результат реакции - отрицательный, при этом для внутреннего контрольного образца используют суспензию бактериофага Т4 с концентрацией 5×103 копий нуклеотидных последовательностей на 1 мкл, а для положительного контрольного образца используют смесь рекомбинантных плазмидных ДНК, содержащих фрагмент генома провируса лейкоза крупного рогатого скота (Bovine leukosis virus, BLV) и фрагмент генома бактериофага Т4, взятых в соотношении 1:1, со следующими нуклеотидными последовательностями:
TMBLV-F CCTACTTTCAGACCCCCTTGAC прямой праймер
TMBLV-R CATAAGAGCTTAAGGCCTGAG обратный праймер
TMBLV-P R6G CCAAGCCTCACCTTGGGGCCTCCT BHQ1 зонд
T4F TACATATAAATCACGCAAAGC
T4R TAGTATGGCTAATCTTATTGG
Т4Р FAM ACATTGGCACTGACCGAGTTC BHQ1 зонд.
| СПОСОБ ДИАГНОСТИКИ ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2010 |
|
RU2445370C1 |
| СПОСОБ ВЫЯВЛЕНИЯ ВИРУСА ЛЕЙКОЗА КРС ПО НУКЛЕОТИДНЫМ ПОСЛЕДОВАТЕЛЬНОСТЯМ КОНСЕРВАТИВНЫХ ОБЛАСТЕЙ ВИРУСНОГО ГЕНОМА | 2012 |
|
RU2521330C2 |
Авторы
Даты
2019-09-13—Публикация
2018-10-01—Подача