Предлагаемое изобретение относится к медицине, а именно к хирургии, комбустиологии, пластической хирургии, и может быть использовано у больных, которым требуется выполнение кожной пластики ран полнослойным кожным аутотрансплантатом.
Современные возможности комбустиологии позволяют успешно лечить пострадавших с глубокими ожогами на площади более 50% поверхности тела. При больших площадях ожоговых поражений актуальным аспектом лечения является рациональное использование донорских ресурсов кожи. При обширных ожогах восстановить кожный покров сплошными трансплантатами часто не удается. Пластика целыми аутотрансплантатами в таких случаях производится лишь на важных в функциональном и косметическом отношениях участках тела (Ожоги: Руководство для врачей / Под ред. Б.С. Вихриева и В.М. Бурмистрова. - Л.: Медицина, 1981. - С. 158). При выборе свободной пересадки кожи необходимо учитывать, что склонность полнослойных трансплантатов к вторичной ретракции по сравнению с расщепленными меньше (Азолов В.В., Дмитриев Г.И. Хирургическое лечение последствий ожогов. - Н. Новгород: ОАО «Дзержинская типография», 1995. - С. 42, С. 57), в связи с чем использовать полнослойные кожные трансплантаты на функционально и эстетически значимых участках тела предпочтительнее.
Аналогом предполагаемого изобретения является способ пластики полнослойным кожным трансплантатом. (Казарезов М.В., Королева А.Н., Головнев В.А. Контрактуры. - Новосибирск: Новосибирская ГМА, 2002. - С.119). С помощью дерматома берется лоскут необходимых размеров на всю толщу кожи, а образовавшийся дефект замещается расщепленным лоскутом. В результате происходит приживление и того, и другого кожных лоскутов.
К недостаткам способа относятся:
1. Недостаточный размер полнослойного кожного трансплантата, ширина которого ограничена техническими характеристиками дерматома (до 10 см).
2. Необходимость взятия нескольких кожных трансплантатов для закрытия больших раневых дефектов с последующим рубцеванием по линиям стыков (участков прилегания трансплантатов друг к другу).
3. Технические трудности или невозможность взятия полнослойного кожного трансплантата дерматомом в области пупка при отсутствии донорских ресурсов в других областях.
4. Снижение результатов приживления расщепленных кожных трансплантатов на донорскую рану после взятия полнослойного кожного трансплантата до подкожно-жировой клетчатки.
В качестве ближайшего аналога нами принят способ забора кожного аутотрансплантата (Богданов СБ., Бабичев Р.Г., Патент РФ на изобретение №2618166, заявка №2016103838 от 05.02.2016, опубл. 02.05.2017, Бюл. №13). Способ включает выполнение модели воспринимающего ложа в асептических условиях, наложение модели на место взятия аутотрансплантата, прошивание трансплантата на держалки и его отделение от клетчатки, выполнение разреза кожи до верхних слоев подкожно-жировой клетчатки, фрагменты которой затем удаляют с помощью ножниц, а со стороны дермы трансплантат выравнивают дерматомом, с иссечением слоя в 0,1 мм, при этом общую толщину трансплантата формируют в 1,0-2,0 мм. При необходимости в цельном полнослойном кожном аутотрансплантате формируют прорези (для рта, носовых ходов, глаз). Через 3-5 дней на первой перевязке оценивают рост грануляций на донорском участке, через 5-10 дней при формировании грануляционной ткани выполняют пластическое закрытие гранулирующей донорской раны расщепленными кожными трансплантатами, толщиной 0,2-0,3 мм.
К недостаткам способа относятся:
1. Риск случайной перфорации полнослойного кожного трансплантата при его отделении на уровне верхних слоев подкожно-жировой клетчатки, что в дальнейшем приведет к образованию грубого рубца в области перфорации и значительно ухудшит эстетический результат кожной пластики.
2. Невозможность выполнения одномоментного пластического закрытия раны донорского участка, т.к. результат приживления кожных трансплантатов при пересадке на подкожно-жировую клетчатку значительно хуже.
3. Необходимость выполнения кожной пластики донорского участка отсрочено, после созревания грануляционной ткани, что требует дополнительного лечения раны донорского участка и повышает риск гнойно-септических осложнений.
4. В предложенном способе не указана возможность взятия полнослойного кожного трансплантата на животе с уже имеющимся дефектом от пупка, что актуально у пациентов с дефицитом донорских ресурсов.
Задачи:
- усовершенствовать методику забора полнослойного кожного трансплантата;
- оптимизировать использование донорских ресурсов кожи путем взятия полнослойного кожного трансплантата необходимого размера с дефектом от пупка в незаметной (закрытой одеждой) области;
- обеспечить условия для одномоментного пластического закрытия раны донорского участка;
- снизить риск гнойно-септических осложнений при заборе полнослойного кожного трансплантата;
- улучшить результаты оперативного лечения при кожной пластике полнослойным кожным трансплантатом эстетически значимых зон с имеющимися естественными физиологическими отверстиями.
Сущностью изобретения, включающего предоперационную разметку кожных покровов, рассечение кожи и подкожно-жировой клетчатки окаймляющим разрезом на животе, отделение кожного трансплантата от донорского ложа, гемостаз, обезжиривание и истончение изнутри кожного трансплантата, пластическое закрытие донорской раны, является следующее: забор кожи осуществляют вокруг пупка, выполняют дополнительный окаймляющий разрез кожи и подкожно-жировой клетчатки вокруг пупка, иссекают единым блоком кожу и всю подлежащую под кожным трансплантатом жировую клетчатку до поверхностной фасции, а сформированное при заборе кожного трансплантата отверстие от пупка в дальнейшем располагают над естественными физиологическими отверстиями (глазная или ротовая щель, носовые ходы).
Технический результат: данный способ позволяет выполнить забор полнослойного кожного трансплантата с дефектом от пупка при наличии дефицита непораженных участков кожи необходимого размера, обеспечить локализацию донорского участка в незаметной (закрытой одеждой) области, произвести аутопластику полнослойным кожным трансплантатом ран эстетически значимых участков. тела с имеющимися естественными физиологическими отверстиями (на лице), снизить риск гнойно-септических осложнений за счет одномоментного пластического закрытия раны донорского участка, улучшить функциональные и эстетические результаты оперативного лечения.
Осуществление способа забора кожного трансплантата производят следующим образом. После стандартной подготовки и обработки операционного поля на животе выполняют предоперационную разметку кожных покровов, обозначая границы забора кожного трансплантата и границы иссечения кожи вокруг пупка для дальнейшего расположения данного дефекта в кожном трансплантате над ' естественными физиологическими отверстиями. Скальпелем по линиям предоперационной разметки производят рассечение кожи и подкожно-жировой клетчатки, т.е. выполняют один окаймляющий разрез по наружному краю трансплантата, а другой окаймляющий разрез - вокруг пупка. Выкраиваемый трансплантат берут на швы-держалки. Далее отделяют кожный трансплантат от донорского ложа, иссекая единым блоком кожу и всю подлежащую под кожным трансплантатом жировую клетчатку до поверхностной фасции. Производят гемостаз и пластическое закрытие донорской раны расщепленными перфорированными кожными трансплантатами, накладывают асептические повязки. Кожный трансплантат обезжиривают и истончают изнутри ножницами и дерматомом. Выполняют хирургическую обработку раны лица, гемостаз. Подготовленный полнослойный кожный трансплантат укладывают на обработанную рану лица таким образом, чтобы сформированное при заборе кожного трансплантата отверстие от пупка было расположено над естественными физиологическими отверстиями (глазная или ротовая щель, носовые ходы). По показаниям дополнительно рассекают кожный трансплантат над другими естественными физиологическими отверстиями, после чего производят фиксацию кожного трансплантата швами и накладывают повязки. На 7-е сутки после операции наблюдали приживление расщепленных кожных трансплантатов на донорском участке живота, на 9-11 сутки - приживление полнослойного кожного трансплантата на лице.
По данному способу в клинических условиях оперированы 6 больных с глубокими термическими ожогами лица.
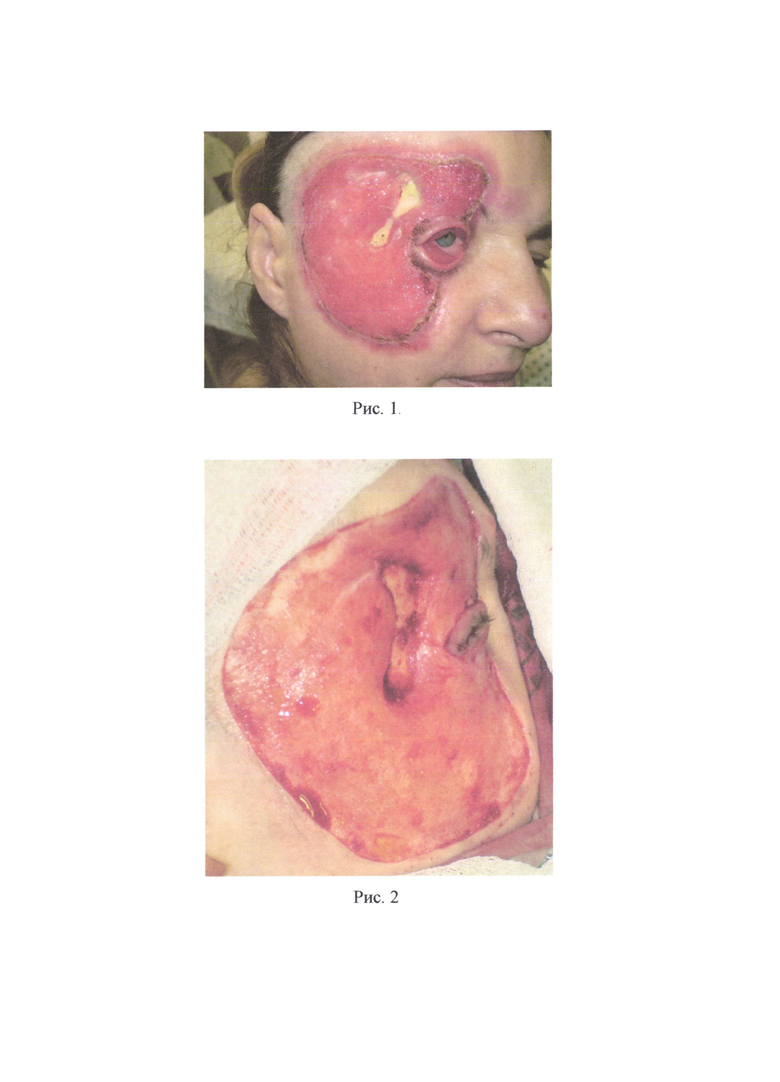
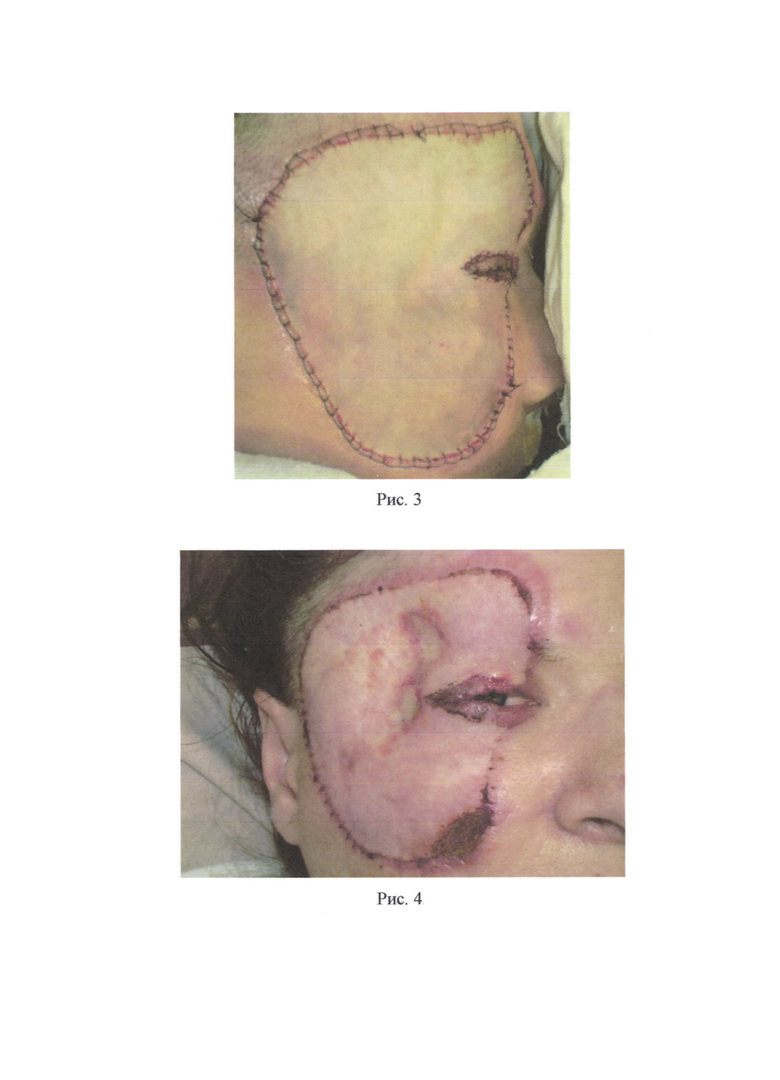
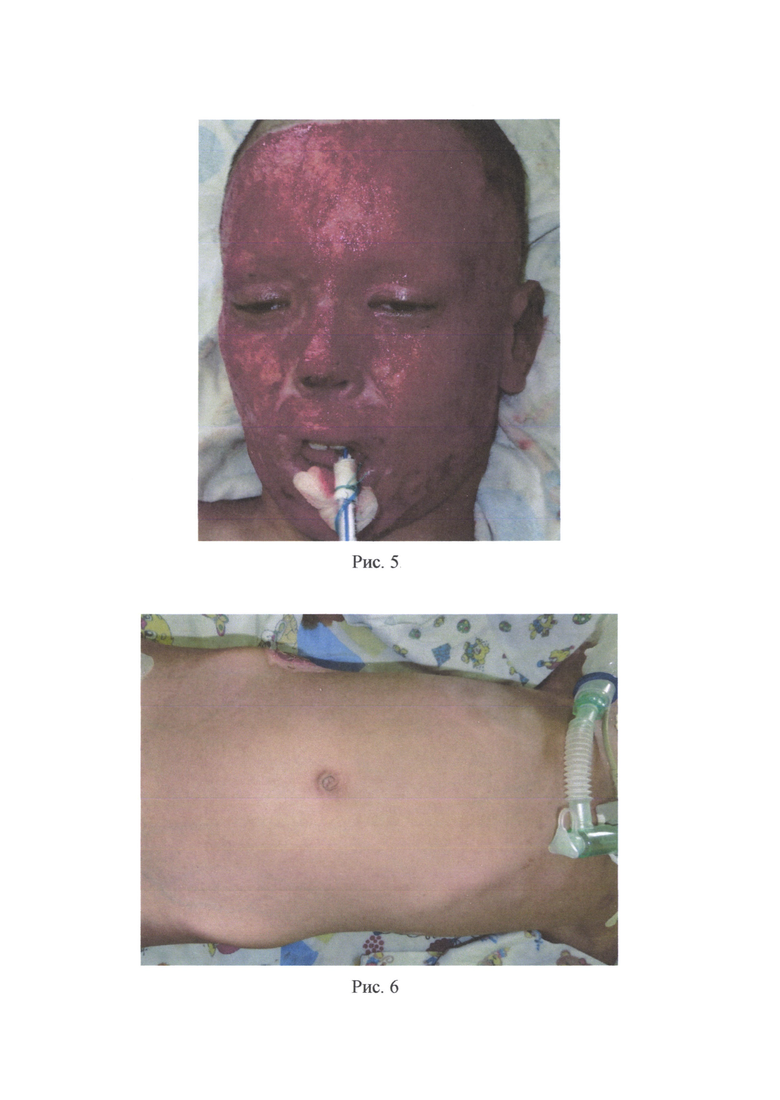
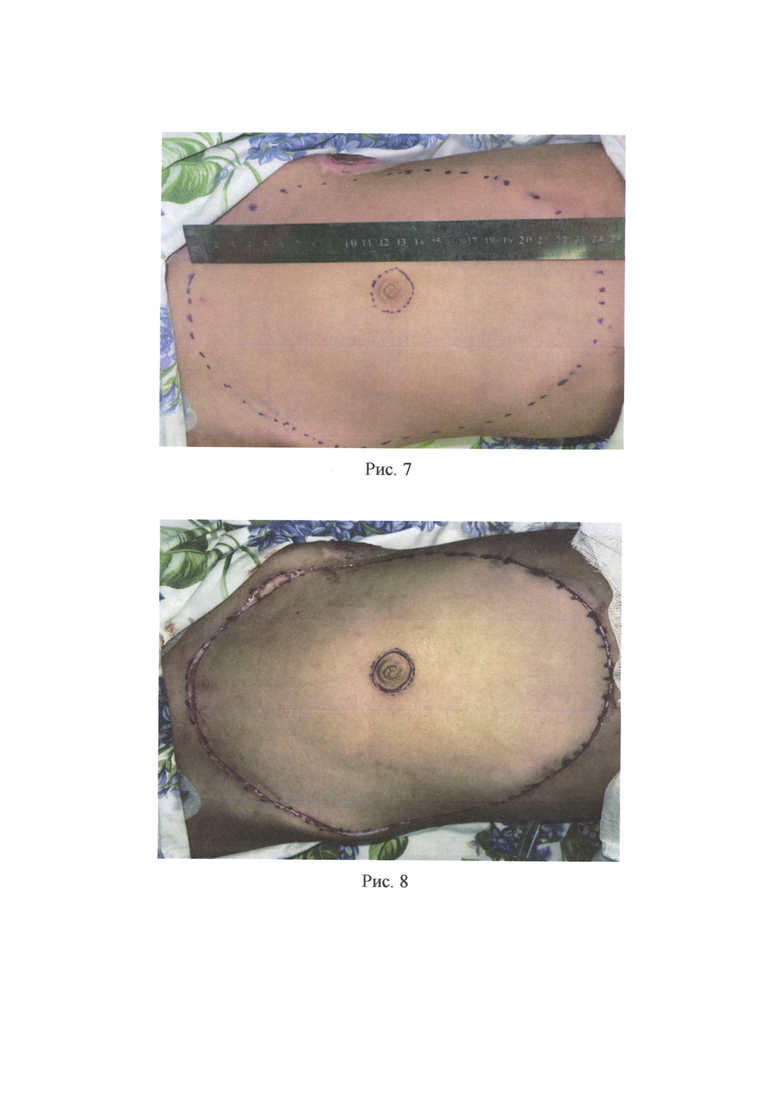
Пример 1 (см. приложение 1). Пациентка С. 44 лет, поступила в ожоговое отделение ГБУЗ «НИИ - ККБ №1 им. проф. СВ. Очаповского» с диагнозом: термический ожог (пламенем) лица, туловища, конечностей 28% I-II-III степени, ожоговая болезнь. После выполнения этапных некрэктомий на лице на 23-е сутки после травмы (рис. 1) больная была взята в операционную. После стандартной подготовки и обработки операционного поля на животе была выполнена предоперационная разметка кожных покровов, обозначая границы забора кожного трансплантата и границы иссечения кожи вокруг пупка для дальнейшего расположения данного дефекта в кожном трансплантате над правой глазной щелью. Скальпелем по линиям предоперационной разметки было произведено рассечение кожи и подкожно-жировой клетчатки, т.е. выполнен один окаймляющий разрез по наружному краю трансплантата, а другой окаймляющий разрез - вокруг пупка. Выкраиваемый трансплантат был взят на швы-держалки. Далее кожный трансплантат был отделен от донорского ложа путем иссечения единым блоком кожи и всей подлежащей под кожным трансплантатом жировой клетчатки до поверхностной фасции. Был произведен гемостаз и пластическое закрытие донорской раны расщепленными перфорированными кожными трансплантатами, наложены асептические повязки. Кожный трансплантат был обезжирен и истончен изнутри ножницами и дерматомом. Была выполнена хирургическая обработка раны лица, гемостаз (рис.2). Подготовленный полнослойный кожный трансплантат был уложен на обработанную рану лица таким образом, чтобы сформированное при заборе кожного трансплантата отверстие от пупка было расположено над естественным физиологическим отверстием (правая глазная щель), после чего была произведена фиксация кожного трансплантата швами (рис. 3) и были наложены повязки. На 7-е сутки после операции наблюдали приживление расщепленных кожных трансплантатов на донорском участке живота, на 10 сутки - приживление полнослойного кожного трансплантата на лице (рис. 4).
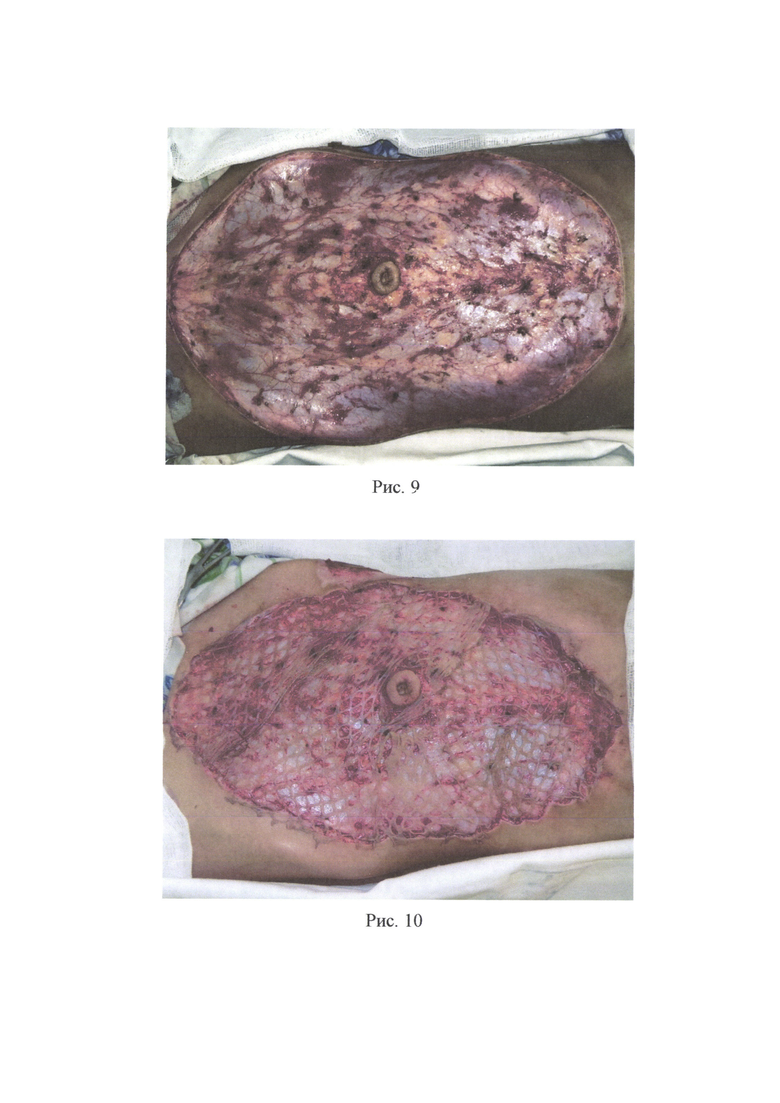
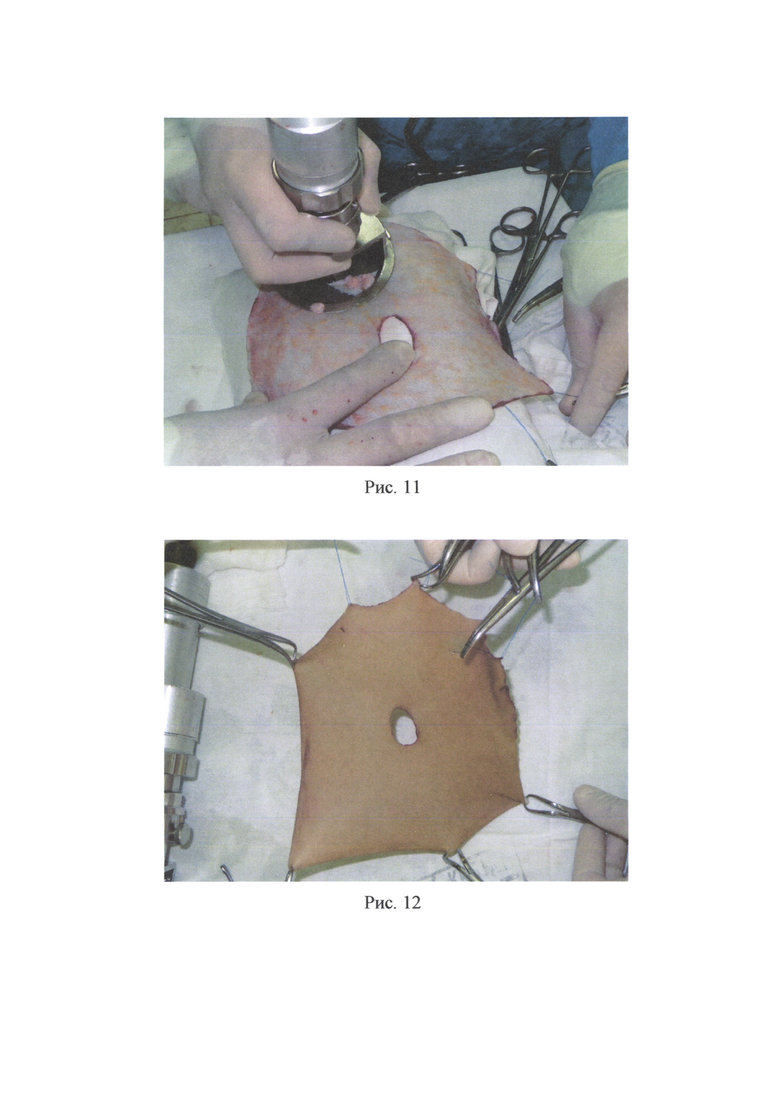
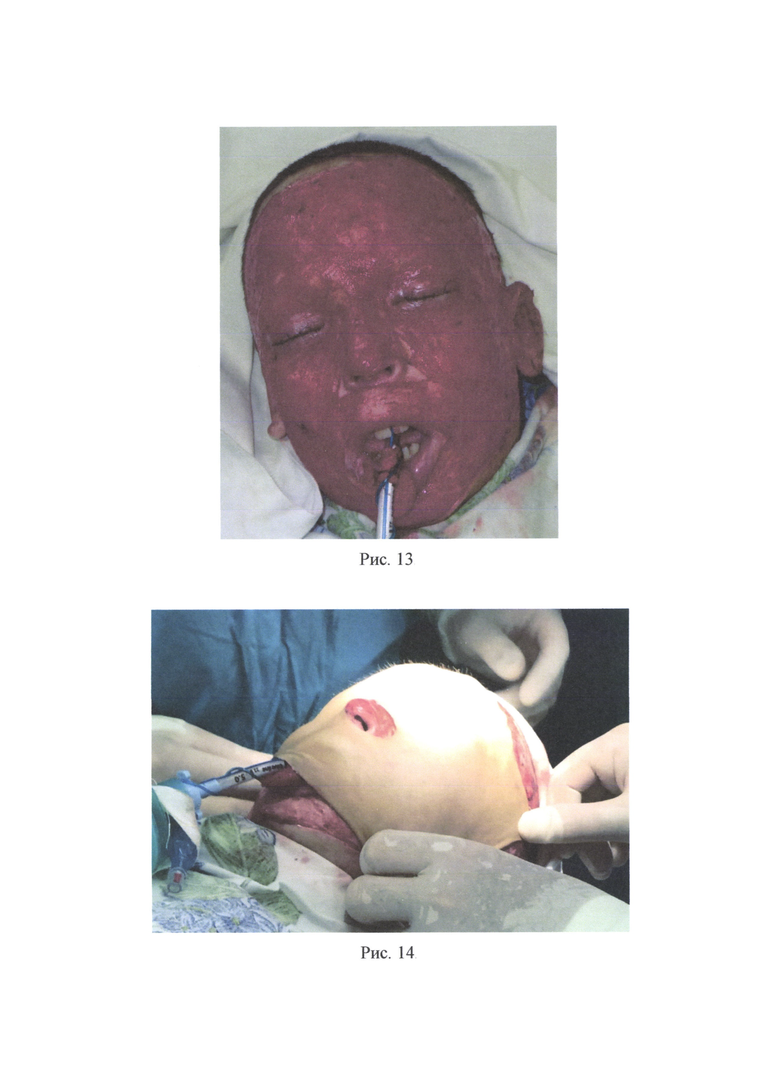
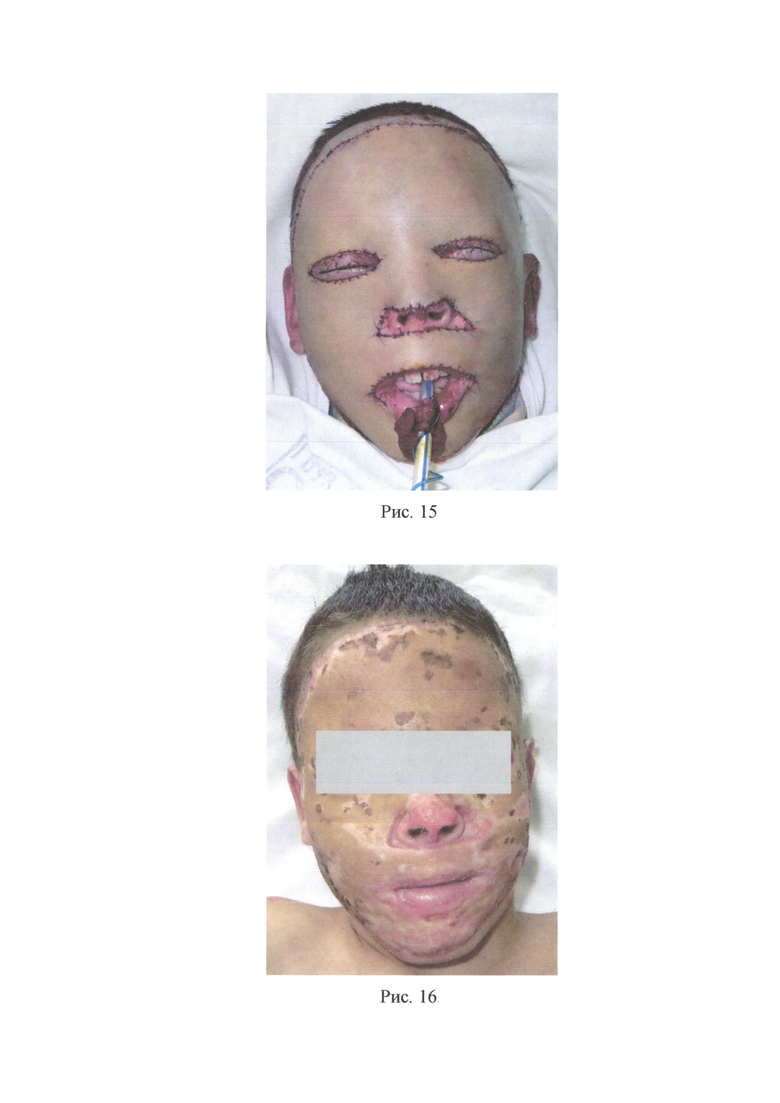
Пример 2. Пациент А., 9 лет, поступил в ожоговое отделение ГБУЗ «НИИ - ККБ №1 им. проф. СВ. Очаповского» с диагнозом: термический ожог (пламенем) головы, шеи, туловища, ягодиц, конечностей 41% I-II-III степени, термоингаляционная травма, ожоговая болезнь. После выполнения этапных некрэктомий на лице на 21-е сутки после травмы (рис. 5) больной был взят в операционную. После стандартной подготовки и обработки операционного поля (рис. 6) на животе была выполнена предоперационная разметка кожных покровов (рис. 7), обозначая границы - забора кожного трансплантата и границы иссечения кожи вокруг пупка для дальнейшего расположения данного дефекта в кожном трансплантате над носовыми ходами. Скальпелем по линиям предоперационной разметки было произведено рассечение кожи и подкожно-жировой клетчатки, т.е. выполнен один окаймляющий разрез по наружному краю трансплантата, а другой окаймляющий разрез - вокруг пупка (рис. 8). Выкраиваемый трансплантат был взят на швы-держалки. Далее кожный трансплантат был отделен от донорского ложа путем иссечения единым блоком кожи и всей подлежащей под кожным трансплантатом жировой клетчатки до поверхностной фасции (рис. 9). Был произведен гемостаз и пластическое закрытие донорской раны расщепленными перфорированными кожными трансплантатами (рис. 10), наложены асептические повязки. Кожный трансплантат был обезжирен и истончен изнутри ножницами и дерматомом (рис. 11). Была выполнена хирургическая обработка ран лица, гемостаз (рис. 13). Подготовленный полнослойный кожный трансплантат (рис. 12) был уложен на обработанную рану лица (рис. 14) таким образом, чтобы сформированное при заборе кожного трансплантата отверстие от пупка было расположено над естественными физиологическими отверстиями (носовые ходы), после чего была произведена фиксация кожного трансплантата швами (рис. 15) и были наложены повязки. На 7-е сутки после операции наблюдали приживление расщепленных кожных трансплантатов на донорском участке живота, на 10 сутки - приживление полнослойного кожного трансплантата на лице. Пациент был выписан на 63-е сутки после травмы после полного восстановления, поврежденного ожогом кожного покрова и заживления донорских ран. Наблюдали полное приживление полнослойного кожного трансплантата на лице без склонности к ретракции (рис. 16) и удовлетворительное состояние восстановленного кожного покрова на донорском участке живота (рис. 17).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ДОНОРСКОЙ РАНЫ ЖИВОТА | 2018 |
|
RU2702152C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ РУБЦОВЫХ ДЕФОРМАЦИЙ ШЕИ | 2018 |
|
RU2694332C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ МНОЖЕСТВЕННЫХ РУБЦОВЫХ ДЕФОРМАЦИЙ КИСТИ | 2019 |
|
RU2701602C1 |
| СПОСОБ ЛЕЧЕНИЯ ОБШИРНЫХ РАН ГОЛОВЫ | 2019 |
|
RU2734048C1 |
| СПОСОБ СВОБОДНОЙ ОТСРОЧЕННОЙ ПЛАСТИКИ КОЖНЫМ АУТОТРАНСПЛАНТАТОМ ПРИ ТРАВМАТИЧЕСКИХ ОТСЛОЙКАХ КОЖИ | 2017 |
|
RU2665676C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТОТАЛЬНЫХ ГЛУБОКИХ ОЖОГОВ ТУЛОВИЩА | 2019 |
|
RU2701625C1 |
| СПОСОБ ЗАБОРА КОЖНОГО ТРАНСПЛАНТАТА И ВОССТАНОВЛЕНИЯ ДОНОРСКОЙ РАНЫ | 2016 |
|
RU2618907C1 |
| СПОСОБ ПЛАСТИКИ ПОЛНОСЛОЙНЫМ КОЖНЫМ АУТОТРАНСПЛАНТАТОМ | 2017 |
|
RU2655201C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГЛУБОКИХ ТОТАЛЬНЫХ ОЖОГОВ ЛИЦА | 2016 |
|
RU2632776C1 |
| СПОСОБ ХИРУРГИЧЕСКОЙ ТРЕНИРОВКИ КОЖНО-ЖИРОВОГО ЛОСКУТА НА ВРЕМЕННОЙ ПИТАЮЩЕЙ НОЖКЕ | 2021 |
|
RU2781109C1 |

Изобретение относится к медицине, а именно к хирургии, комбустиологии и пластической хирургии. Осуществляют предоперационную разметку кожных покровов, рассечение кожи и подкожно-жировой клетчатки окаймляющим разрезом на животе, отделение кожного трансплантата от донорского ложа, гемостаз, обезжиривание и истончение изнутри кожного трансплантата, пластическое закрытие донорской раны. При этом забор кожи осуществляют вокруг пупка. Выполняют дополнительный окаймляющий разрез кожи и подкожно-жировой клетчатки вокруг пупка. Иссекают единым блоком кожу и всю подлежащую под кожным трансплантатом жировую клетчатку до поверхностной фасции, а сформированное при заборе кожного трансплантата отверстие от пупка в дальнейшем располагают над естественными физиологическими отверстиями лица - глазная или ротовая щель, носовые ходы. Способ позволяет выполнить забор полнослойного кожного трансплантата с дефектом от пупка при наличии дефицита непораженных участков кожи необходимого размера, обеспечить локализацию донорского участка в незаметной области, произвести аутопластику полнослойным кожным трансплантатом ран эстетически значимых участков тела с имеющимися естественными физиологическими отверстиями, снизить риск гнойно-септических осложнений за счет одномоментного пластического закрытия раны донорского участка, улучшить функциональные и эстетические результаты оперативного лечения. 2 пр., 17 ил.
Способ забора кожного трансплантата на животе, включающий предоперационную разметку кожных покровов, рассечение кожи и подкожно-жировой клетчатки окаймляющим разрезом на животе, отделение кожного трансплантата от донорского ложа, гемостаз, обезжиривание и истончение изнутри кожного трансплантата, пластическое закрытие донорской раны, отличающийся тем, что забор кожи осуществляют вокруг пупка, выполняют дополнительный окаймляющий разрез кожи и подкожно-жировой клетчатки вокруг пупка, иссекают единым блоком кожу и всю подлежащую под кожным трансплантатом жировую клетчатку до поверхностной фасции, а сформированное при заборе кожного трансплантата отверстие от пупка в дальнейшем располагают над естественными физиологическими отверстиями лица (глазная или ротовая щель, носовые ходы).
| СПОСОБ ЗАБОРА КОЖНОГО АУТОТРАНСПЛАНТАТА | 2016 |
|
RU2618166C1 |
| СПОСОБ КОМБИНИРОВАННОЙ КОЖНОЙ ПЛАСТИКИ ПРИ УСТРАНЕНИИ РУБЦОВЫХ КОНТРАКТУР ШЕИ | 1994 |
|
RU2108064C1 |
| БОГДАНОВ С.Б | |||
| И ДР | |||
| Современные способы выполнения свободной кожной пластики полнослойными аутотрансплантатами | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| САРЫГИН П.В | |||
| Хирургическое лечение последствий ожогов шеи и лица | |||
| Москва | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Автореферат дисс | |||
| на соиск | |||
| уч | |||
| степ | |||
| КМН, с.29 | |||
| SHAHRIAR LOGHMANI ET AL | |||
| The Supraclavicular Flap for Reconstruction of Post-Burn Mentosternal Contractures | |||
| Iran Red Crescent Med J | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| ПРИСПОСОБЛЕНИЕ ДЛЯ УСТРАНЕНИЯ СКОЛЬЖЕНИЯ КОЛЕС АВТОМОБИЛЕЙ | 1920 |
|
SU292A1 |
Авторы
Даты
2019-10-07—Публикация
2018-09-28—Подача