УРОВЕНЬ ТЕХНИКИ
[0001] Воспаление тканей полости рта может быть вызвано хирургическим вмешательством, локализованным поражением, травмой, некрозом, неправильной гигиеной полости рта или различными системными процессами. Гингива (десна) является, частью мягкой ткани, которая выстилает ротовую полость, окружая зубы. Гингивит представляет собой воспаление десен, при котором, как правило, наблюдается их отек, покраснение или кровоточивость. Гингивит - это воспаление или инфекция десен и альвеолярных костей, которые поддерживают зубы. При периодонтите, по сравнению с гингивитом, патологическое состояние прогрессивно ухудшается, при этом десны воспаляются и начинают отступать от зубов и форм карманов, что в конечном итоге может привести к разрушению кости и периодонтальной связки.
[0002] Считается общепринятым, что налетообразующие бактерии, которые живут в ротовой полости и на поверхности зубов, являются причиной воспалительного процесса полости рта, такого как гингивит, а определенные вещества, выделяемые этими бактериями, непосредственно обуславливают это воспаление. Помимо всего прочего, бактерии, ассоциированные с воспалением полости рта, продуцируют, в качестве продуктов жизнедеятельности, метаболиты, включая газы, такие как сероводород, метилмеркаптан и других сернистые газы. Как полагают, эти газы и метаболиты являются ключевыми факторами, способствующими неприятному запаху изо рта.
[0003] Клинические наблюдения, которые начались с 1960-х годов, установили взаимосвязь между накопленным зубным налетом и развитием гингивита. Признание этих взаимосвязей сыграли ключевую роль для клинической практики в стоматологии и способствовали открытию терапевтических средств, таких как триклозан, хлоргексидин, хлорид цетилпиридиния и других для проведения профилактических мероприятий. Несмотря на эти успехи, очевидно, что клиническая оценка гингивита имеет некоторые ограничения и не позволяет обнаруживать определенные клинические проявления, связанные с гингивитом, на самых ранних этапах.
[0004] В литературе описаны исследования о роли полиморфноядерных нейтрофилов (ПЯН) в механизмах защиты при воспалительных процессах в полости рта (Kornman et al., 1997). При том, что исследования в основном сосредоточены на роли ПЯН в механизмах защиты, данные об оценке ПЯН в ротовой полости или в слюне недостаточны. Кроме того, существует не так много информации, которая описывает эффекты определенных лекарственных форм на уровне ПЯН, предназначенных для гигиены полости рта.
[0005] Как и при большинстве патологических состояний, желательно диагностировать воспаление полости рта как можно раньше, чтобы начать лечение на ранней стадии и избежать прогрессирования процесса воспаления. Это особенно важно при гингивите и периодонтите, но хотя гингивит и является патологическим состоянием, его развитие может быть обратимым. В противоположность этому, в отличие от гингивита, периодонтит является более серьезным заболеванием полости рта, при котором поражение ткани ротовой полости является по существу необратимым.
[0006] Кроме того, у многих пациентов по всему миру осложняющим фактором в определении степени воспаления полости рта является ограниченный доступ к профессиональной стоматологической помощи либо из-за отдаленности такой профессиональной стоматологической помощи, либо из-за стоимости диагностических и лечебных процедур.
[0007] Таким образом, актуальной остается потребность в безопасной, неинвазивной, простой и экономически эффективной методике мониторинга за состоянием воспаления полости рта у пациента и/или мониторинга за ходом лечения воспаления полости рта.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0008] Неожиданно было обнаружено, что количество, число или уровень полиморфноядерных лейкоцитов (ПЯН) или индикаторного вещества ПЯН в слюне субъекта коррелирует с уровнем или степенью воспаления полости рта у указанного субъекта. Соответственно, настоящее изобретение относится к способу определения наличия, отсутствия или степени тяжести воспаления полости рта, или мониторинга за патологическим воспалительным состоянием полости рта у субъекта, при этом спопоб включает:
(a) получение образца материала для анализа из полости рта от указанного субъекта,
(b) определение количества ПЯН или индикаторного вещества ПЯН в указанном анализируемом образце,
(c) сравнение количества ПЯН или индикаторного вещества ПЯН в анализируемом образце с контролем.
[0009] Способы настоящего изобретения легко осуществить в учреждениях предоставления медицинской помощи, например, в присутствии пациента, стоматологических клиниках, стоматологических центрах и тому подобное. Учитывая простоту, безопасность и неинвазивность способов по настоящему изобретению, в некоторых вариантах реализации изобретения способы могут выполняться пациентом, который может записывать/сообщать результаты.
[0010] Дополнительные области применения настоящего изобретения станут очевидными из подробного описания, представленного ниже. Следует понимать, что подробное описание и конкретные примеры, раскрывающие предпочтительный вариант реализации настоящего изобретения, предназначены только для целей иллюстрации и никак не ограничивают объем настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0011] Следующее описание предпочтительного варианта (вариантов) реализации изобретения носит лишь иллюстративный характер и никоим образом не предназначено для ограничения данного изобретения, его заявки или вариантов применения.
[0012] Во всем тексте настоящей заявки диапазоны используются в качестве сокращенного обозначения для описания каждого значения, которое находится в пределах диапазона. В качестве значения диапазона можно выбрать любое значение в пределах диапазона. Кроме того, все ссылочные источники, цитируемые в настоящем документе, полностью включены в настоящий документ посредством ссылок. В случае противоречия определений в настоящем описании и в процитированной ссылке настоящее описание является определяющим. Если не указано иное, все проценты и количества, выраженные в этом разделе и в любом другом месте описания, необходимо понимать как обозначающие проценты по массе. Все проценты, выраженные в данном документе, являются массовыми по сухому веществу, если специально не оговорено иное.
[0013] В контексте данного изобретения термин "лечить" или "лечение", как он используется в данном документе, означает реверсию, облегчение, смягчение или подавление прогрессирования нарушения или патологического состояния, к которому применяется такой термин, или одного или более симптомов такого нарушения или патологического состояния. При использовании по тексту данного документа и прилагаемой формуле изобретения, слова в единственном числе означают также множественное число, если из контекста явно не следует иное.
[0014] Термин "нормальный контроль" относится к субъекту или группе субъектов, которые не имеют воспаления полости рта.
[0015] Термин "тампон" относится к любому устройству, изготовленному из абсорбирующего материала и пригодному для сбора жидкости из полости рта. Предпочтительно, абсорбирующий материал прикреплен к держателю, но термин "тампон" в данном контексте включает автономные приборы, изготовленные из абсорбирующего материала, которые могут быть помещены в рот или на поверхность слизистой оболочки рта для абсорбции слюны, расположенной там.
[0016] Термин "материал полости рта" относится к любому веществу из полости рта, которое может быть собрано, например, слюна, жидкость из десневой борозды, оральные соскобы из языка или щеки, десневой налет, и тому подобное. Предпочтительным материалом из полости рта в способах настоящего изобретения является слюна.
[0017] В данном контексте термин "измерить" и "определить" относится к любым качественным или количественным определениям.
[0018] В способах по настоящему изобретению субъектом может быть любое животное и, предпочтительно, млекопитающее, такое как человек, мышь, крыса, кошка, собака, лошадь, корова, осел, овца или свинья. Люди являются наиболее предпочтительными.
[0019] В некоторых аспектах способы включают получение анализируемого образца материала ротовой полости, такого как слюна, взятая у субъекта. Слюна может быть получена любым способом, используемым в данной области техники. Например, в данной области техники известны и коммерчески доступны различные устройства для сбора жидкости полости рта и наборы. Устройство для сбора жидкости полости рта может состоять или иным образом иметь форму или изготавливаться из частиц, волокон, пластинок, и тому подобное. Слюна может быть собрана с помощью аспирации или абсорбции. Пригодными устройствами для сбора жидкости полости рта являются коммерчески доступные устройства компании Oasis Diagnostics Corp., Ванкувер, штат Вашингтон, такие как Super-SAL™, VerOFy®, Versi-SAL® и UltraSal-2™.
[0020] В некоторых аспектах, материал из полости рта, например, слюну, получают с помощью устройства, такого как тампон. Тампон может состоять из любого материала, пригодного для использования в данной области, такого как альгинат, губка, капиллярная матрица, фильтровальная бумага, кальциевые волокна, материалы на основе целлюлозы или синтетические полимеры, такие как полиуретан, полиэфир, вискоза или полимер этиленгликоля и терефталевой кислоты. Для осуществления настоящего изобретения особенно пригодны полимеры этиленгликоля и терефталевой кислоты (т.е., полиэтилентерефталат), существующие на рынке под торговым наименованием DACRON® (DuPont), Предпочтительно, чтобы тампон не содержал хлопок или другие природные материалы на основе целлюлозы, поскольку хлопок может быть загрязнен металлами из почвы, в которой этот хлопок выращивали, и вследствие этого возможно потенциальное загрязнение анализа и получение неточных или ложных положительных результатов. С целью облегчения абсорбции абсорбирующий материал тампона может быть пропитан солями или гипертоническим раствором. Абсорбирующий материал также может быть пропитан ароматизатором, чтобы сделать взятие образцов более приятной процедурой для субъекту. Тампон может быть на конце держателя или аппликатора, изготовленного из пластика, дерева, алюминия и тому подобное, с применением синтетических материалов, таких как пластик, что является предпочтительным. Затем тампон можно поместить в водный раствор, предпочтительно, стерильный и буферный. Для отделения ПЯН и/или их производных, или компонентов из материала тампона в водный раствор, тампон можно покрутить, встряхнуть и т.д.
[0021] В другом варианте реализации изобретения слюну получают при сплевывании. Например, субъект полощет полость рта водным раствором, предпочтительно, стерильным и/или буферным. Примеры буферных растворов включают сбалансированный солевой раствор Хэнкса, фосфатно-буферный раствор, буфер TRIS и тому подобное. Содержимое полости рта, т.е. образцы слюны, затем сплевывают в контейнеры, предпочтительно, стерильные.
[0022] Количество ПЯН может быть определено в образцах с использованием обычных методов, известных в данной области, например, с помощью устройство для подсчета клеток, микроскопии и тому подобное. При использовании микроскопии, образцы слюны могут впоследствии концентрировать, например, с помощью центрифугирования, фильтрации и т.п., и затем снова суспендировать. Чтобы сделать ПЯН более заметными, для их окрашивания могут использоваться красители для клеток: обычные или флюоресцентные, такие как акридиновый оранжевый и тому подобные. В одном варианте реализации изобретения количество ПЯН может быть определено по методике, описанной в статье: Bender JS, Thang Н, Glogauer М, (2006) "Novel rinse assay for the quantification of oral neutrophils and the monitoring of chronic periodontal disease", J. Periodontal Res. 2006, 41:214-220, включенной в данный документ посредством ссылки.
[0023] Время, необходимое для сбора слюны субъекта, может варьироваться. В некоторых аспектах, устройство для сбора жидкости ротовой полости или буферный раствор необходимо оставлять во рту субъекта в течение по меньшей мере около 5 секунд, или по меньшей мере около 10 секунд, или по меньшей мере около 15 секунд, или по меньшей мере около 20 секунд, или по меньшей мере около 30 секунд. В некоторых аспектах, устройство для сбора жидкости ротовой полости или буферный раствор может оставаться во рту субъекта в течение по меньшей мере около 1 минуты или более.
[0024] Способ по настоящему изобретению предназначен для упрощения диагностики, прогнозирования и мониторинга воспалительных заболеваний полости рта, таких как гингивит или периодонтит, и ассоциированных состояний, например, зловонное дыхание или неприятный запах изо рта. Способы по настоящему изобретению могут быть также использованы для оценки потенциальных терапевтических агентов для лечения и/или облегчения симптомов, ассоциированных с воспалением в полости рта. Способы настоящего изобретения могут быть использованы для определения наличия, отсутствия или тяжести воспаления в полости рта.
[0025] В одном варианте реализации настоящего изобретения количество ПЯН или индикаторного вещества ПЯН в анализируемом образце сравнивается с контролем. Если способ согласно изобретению заключается в обнаружении наличия, отсутствия или тяжести воспаления в полости рта, контрольная группа представляет собой нормальных здоровых субъектов, т.е. субъектов, которые, как известно, не имеют воспаления в полости рта.
[0026] В конкретном аспекте изобретение относится к способу диагностики воспаления в полости рта, гингивита или пародонтита, и/или определения их тяжести в исследуемом субъекте, путем получения образца материала изо рта, такого как образец слюны от нормального здорового человека или образцы материала изо рта, такие как образцы слюны из множества нормальных здоровых субъектов, определению количества ПЯН или индикаторного вещества ПЯН в образцах здорового субъекта(ов), а также получение одного или более образцов из исследуемого субъекта и определение количества ПЯН в анализируемом материале изо рта, и сравнение количества ПЯН или индикаторного вещества ПЯН в нормальном образце (ах) материала изо рта с количеством ПЯН или индикаторного вещества ПЯН в образце (ах) анализируемого материала изо рта,
[0027] Если способ согласно изобретению заключается в мониторинге эффективности лечения воспаления в полости рта или мониторинге патологического воспалительного процесса в полости рта, то контроль представляет собой анализируемый образец, полученный от того же субъекта в предшествующий момент времени, который может быть до или после того, как начато лечение. Результаты, полученные при осуществлении способа мониторинга по настоящему изобретению, могут быть использованы для коррекции и модификации лечения воспаления в полости рта, то есть, изменения методики, режима, схемы, дозы и/или вещества, например, средства для чистки зубов или лекарственного препарата, используемого для лечения воспаления.
[0028] В дополнительном аспекте настоящее изобретение относится к способу мониторинга патологического состояния субъекта, имеющего воспаление в полости рта, путем сравнения уровня ПЯН или индикаторного вещества ПЯН в одном или более образцах материала из полости рта в первый момент времени, с уровнем ПЯН или индикаторного вещества ПЯН во второй момент времени; и коррелирования снижения уровня ПЯН или индикаторного вещества ПЯН во второй момент времени, по сравнению с первым моментом времени, с улучшением патологического состояния у субъекта, и/или коррелирования увеличения уровня ПЯН или индикаторного вещества ПЯН во второй момент времени, по сравнению с первым моментом времени, с увеличением степени тяжести патологического состояния у субъекта.
[0029] Настоящее изобретение включает измерение индикаторного вещества ПЯН вместо непосредственного измерения ПЯН. Количествами индикаторных веществ ПЯН являются количества любых веществ, которые могут быть измерены в материалах полости рта, таких как слюна, и в которых количество вещества коррелирует с количеством ПЯН. Такие индикаторные вещества ПЯН включают, например, метаболиты, компоненты, ферменты, цитокины, выделения ПЯН, продукты распада ПЯН, и тому подобное. Конкретные примеры индикаторных веществ ПЯН включают слюнной лактоферрин, калпротектин и слюнная лейкоцитарная эстераза. В большинстве вариантов реализации изобретения корреляция с ПЯН является положительной, например, чем большее количество лактоферрина и/или лейкоцитарной эстеразы, тем больше количество ПЯН. Тем не менее, также предполагается, что может существовать отрицательная корреляция, т.е. чем больше количество конкретного измеряемого вещества, тем меньше количество ПЯН. В любом случае, для сравнения количества конкретного вещества в полости рта при наличии, отсутствии или разной степени тяжести воспаления в полости рта, с помощью методик, известных в данной области техники, могут быть разработаны стандарты, например, разработка таблиц данных или стандартных кривых.
[0030] В данной области техники известны анализы для определения наличия и/или количества лейкоцитарной эстеразы, калпротектина и/или лактоферрина в биологических образцах. Такие анализы могут быть основаны на обнаружении реакции вещества, подлежащего измерению, или комплексов, образованные с ним, по изменению цвета, с помощью флуоресценции, люминесценции, радиоизотопного обнаружения, ELSIA и тому подобное.
[0031] В патенте США 5776780, который включен в настоящее описание в качестве ссылки, описана система реагентов для обнаружения и измерения лейкоцитарной эстеразы. Генерирующий цвет механизм или индикатор системы реагента является результатом активности лейкоцитарной эстеразы, направленной на совместимые сложные эфиры. В результате этой эфир/эстеразной реакции продуцируется относительно нестабильный индоксиловый фрагмент, который окисляется с образованием цвета индиго, что улавливается с помощью монохроматической спектрофотометрии. Добавление дегидрогеназы к реагенту увеличивает скорость реакции и полноту реакции индоксилового фрагмента. Дегидрогеназа окисляет спиртовую группу на индоксиловой группе и способствует образованию кетона. Этот переходный индоксиловый кетоновый радикал усиливает развитие цвета, специфичность, точность и чувствительность реакции. Система реагента может содержать одно или более из следующих соединений: 2,4-динитрофенилгидразин, гидроксиламин или семикарбизид, которые в присутствии индоксидовых кетонов обуславливают развитие цвета, что можно отследить при той же длине волны, что и индиго. Дальнейшее усовершенствование метода, касающегося индоксилового промежуточного продукта, предусматривает добавление п-диметиламинобензальдегида или п-нитробензенедиазония тетрафторбората или других азо-индикаторов.
[0032] В одном варианте реализации настоящего изобретения предлагается диагностический набор для определения количества ПЯН в образце слюны путем определения количества лейкоцитарной эстеразы в указанном образце, включающий:
(a) сложный эфир, соответствующий лейкоцитарной эстеразе;
(b) средства для приведения в контакт сложного эфира с образцом для получения индоксиловых фрагментов, которые формируются из реакции сложного эфира с любой лейкоцитарной эстеразой, присутствующей в образце; а также
(c) средства для измерения продукции индоксиловых фрагментов.
[0033] В одном варианте реализации изобретения способы определения продукции индоксиловых фрагментов осуществляются путем обнаружения изменения цвета.
[0034] Анализы на лактоферрин могут быть основаны на обнаружении комплексов антитело/антиген. В дополнительном аспекте настоящего изобретения предлагается диагностический набор для определения количества ПЯН в образце слюны путем определения количества лактоферрина в указанном образце, специфически взаимодействующим с антителом, специфичным для лактоферрина, включающий:
(a) лактоферрин-специфическое антитело;
(b) средства для приведения в контакт лактоферрин-специфического антитела с образцом для получения комплексов, содержащих лактоферрин-специфическое антитело и лактоферрин, присутствующий в образце; а также
(c) средства для измерения продукции таких комплексов.
[0035] Лактоферрин-специфические антитела являются коммерчески доступными или могут быть получены способами, известными в данной области, например:
(a) введение лактоферрина по меньшей мере одной мыши для получения по меньшей мере одной иммунизированной мыши;
(b) извлечение В-лимфоцитов по меньшей мере из одной иммунизированной мыши;
(c) слияние В-лимфоцитов по меньшей мере одной иммунизированной мыши с миеломными клетками, с получением таким образом гибридомы;
(d) клонирование гибридом;
(e) отбор клонов, которые продуцируют анти-лактоферриновые антитела;
(f) культивирование клонов, продуцирующих анти-лактоферриновое антитело; а затем
(g) изоляция анти-лактоферриновых антител из культур.
[0036] В одном варианте реализации изобретения лактоферрин представляет собой антиген в иммунологических анализах, включая твердофазный иммуноферментный анализ (ELISA), РИА и другие не связанные с ферментами анализы связывания антитела или способах, известных в данной области техники для выявления антител.
[0037] В анализах ELISA, лактоферрин-специфическое антитело иммобилизуют на выбранной поверхности, например на поверхности, способной связывать белки, такой как фильтровальная бумага или лунки полистирольного микротитрационного планшета. После промывания для удаления не полностью адсорбированного лактоферрин-специфического антитело, неспецифический белок, такой как раствор бычьего сывороточного альбумина (БСА), который, как известно, является антигенно нейтральным в отношении анализируемого образца, может быть связан с выбранной поверхностью. Это позволяет блокировать сайты неспецифической адсорбции на иммобилизирующей поверхности и таким образом снижать фон, обусловленный неспецифическим связыванием на поверхности. Иммобилизирующую поверхность затем подвергают контакту с образцом слюны, анализируемым с помощью способа, который способствует формированию иммунного комплекса (антиген/антитело). Этот этап может включать разбавление образца разбавителями, такими как растворы BSA, бычий гамма-глобулин (BGG) и/или фосфатно-солевой буфер (PBS)/Твин. Затем образец инкубируют в течение от около 2 до 4 часов при температурах, таких как порядка от около 25°С до 37°С. После инкубации поверхность, контактирующую с образцом, промывают для удаления неиммунокомплексного материала. Процедура промывания может включать промывание раствором, таким как PBS/Твин или боратным буфером. После образования специфических иммунокомплексов между анализируемым образцом и связанным лактоферриновым специфическим антителом, и последующего промывания, появление и даже количество иммунокомплексной формации может быть определено путем воздействия на иммунокомплекс вторым антителом, имеющим специфичность к лактоферриновому специфическому антителу.
[0038] Если лактоферриновое специфическое антитело имеет человеческое происхождение, второе антитело может быть антителом, имеющим специфичность в отношении иммуноглобулинов человека и, как правило, IgG. Для обеспечения способа обнаружения, второе антитело может иметь ассоциированную активность, такую как ферментативная активность, которая будет генерировать, например, развитие цвета при инкубировании с соответствующим хромогенным субстратом. Затем может быть проведено количественное определение путем измерения степени генерации цвета, используя, например, спектрометр видимой области спектра. Модификации этой методики могут быть выполнены с помощью способов, известных в данной области техники. Например, могут применяться хроматографические сэндвич-иммуноанализы бокового потока.
[0039] В других вариантах реализации изобретения анализы для определения индикаторных веществ ПЯН, таких как лактоферрин, калпротектин и лейкоцитарная эстераза, могут быть минимализированы и/или упрощены. Например, необходимые реагенты могут быть включены в материал, абсорбирующий слюну, каким является материал, абсорбирующий воду, такой как целлюлоза. Материал, абсорбирующий слюну, может быть в виде листов или полос, или быть в составе устройства, такого как погружаемый зонд, который может непосредственно контактировать с материалом полости рта, таким как слюна. В таких вариантах реализации изобретения полоска или погружаемый зонд могут непосредственно контактировать со слюной в ротовой полости, тем самым устраняя необходимость в сборе отдельного образца. В таких анализы наличие и/или количество индикаторного вещества ПЯН может быть определено по изменению цвета и путем сравнивания анализируемого цвета со стандартной цветовой схемой.
[0040] Такие анализы являются коммерчески доступными для обнаружения веществ в моче или кале, например, быстрые тест-кассеты OnSite FOB (OnSite FOB Hi Rapid Test-Cassette), производимые компанией CTK Biotech, Inc; реагентные индикаторные полоски для мочи (Urinalysis Reagent Test Strips), производимые компанией Tigermedical; индикаторные полоски для мочи CLIA-URS-10 (CLIA-URS-10 Urine Reagent Strips), производимые компанией CLIAwaived, Inc., наборы ELISA для калпротектина, производимые компанией Alpha Laboratories, такие как CALcheck Blue™ и Quantum Blue®; и тому подобное. С помощью некоторых коммерчески доступных анализов есть возможность определять индикаторные вещества ПЯН, такие как лейкоцитарная эстераза, как правило, к тому же одновременно с другими веществами, при этом такие анализы могут быть использованы в способах по настоящему изобретению без модификации. Тем не менее, в некоторых вариантах реализации изобретения анализы приспособлены для тестирования слюны и только для индикаторных веществ ПЯН.
[0041] Уровень лактоферрина в материале из полости рта, таком как слюна, коррелирует с количеством ПЯН в материале из полости рта, таком как слюна. Таким образом, настоящее изобретение в другом варианте реализации относится к способу диагностики воспаления в полости рта, гингивита или пародонтита, и/или определения их тяжести в исследуемом субъекте, путем получения образца материала изо рта, такого как образец слюны от нормального здорового человека или образцы материала изо рта, такие как образцы слюны из множества нормальных здоровых субъектов, определению количества лактоферрина в образце (ах) здорового субъекта(ов), а также получение одного или более образцов от исследуемого субъекта и определение количества лактоферрина в анализируемом образце (ах) субъекта, и сравнение количества лактоферрина в нормальном образце (ах) с количеством лактоферрина в анализируемом образце (ах).
[0042] В другом варианте реализации изобретения предлагается способ мониторинга патологического состояния субъекта, имеющего воспаление в полости рта, путем сравнения уровня лактоферрина в одном или более образцах материала из полости рта в первый момент времени, с уровнем лактоферрина во второй момент времени; и коррелирования снижения уровня лактоферрина во второй момент времени, по сравнению с первым моментом времени, с улучшением патологического состояния у субъекта, и/или коррелирования увеличения уровня лактоферрина во второй момент времени, по сравнению с первым моментом времени, с увеличением степени тяжести патологического состояния у субъекта.
[0043] Уровень лейкоцитарной эстеразы в материале из полости рта, таком как слюна, коррелирует с количеством ПЯН в материале из полости рта, таком как слюна. Таким образом, настоящее изобретение относится к способу диагностики воспаления в полости рта, гингивита или пародонтита, и/или определения их тяжести в исследуемом субъекте, путем получения образца материала изо рта, такого как образец слюны от нормального здорового человека или образцы из множества нормальных здоровых субъектов, определению количества лейкоцитарной эстеразы в образце (ах) здорового субъекта (ов), а также получение одного или более образцов от исследуемого субъекта и определение количества лейкоцитарной эстеразы в анализируемом образце (ах) субъекта, и сравнение количества лейкоцитарной эстеразы в нормальном образце (ах) с количеством лейкоцитарной эстеразы в анализируемом образце (ах).
[0044] В другом варианте реализации изобретения предлагается способ мониторинга патологического состояния субъекта, имеющего воспаление в полости рта, путем сравнения уровня лейкоцитарной эстеразы в одном или более образцах материала из полости рта в первый момент времени, с уровнем лейкоцитарной эстеразы во второй момент времени; и коррелирования снижения уровня лейкоцитарной эстеразы во второй момент времени, по сравнению с первым моментом времени, с улучшением патологического состояния у субъекта, и/или коррелирования увеличения уровня лейкоцитарной эстеразы во второй момент времени, по сравнению с первым моментом времени, с увеличением степени тяжести патологического состояния у субъекта.
[0045] Уровень калпротектина в материале из полости рта, таком как слюна, коррелирует с количеством ПЯН в материале из полости рта, таком как слюна. Таким образом, настоящее изобретение в другом варианте реализации относится к способу диагностики воспаления в полости рта, гингивита или пародонтита, и/или определения их тяжести в исследуемом субъекте, путем получения образца материала изо рта, такого как образец слюны от нормального здорового человека или образцы материала изо рта, такие как образцы слюны из множества нормальных здоровых субъектов, определению количества калпротектина в образце (ах) здорового субъекта(ов), а также получение одного или более образцов от исследуемого субъекта и определение количества калпротектина в анализируемом образце (ах) исследуемого субъекта, и сравнение количества калпротектина в нормальном образце (ах) с количеством калпротектина в анализируемом образце (ах).
[0046] В другом варианте реализации изобретения предлагается способ мониторинга патологического состояния субъекта, имеющего воспаление в полости рта, путем сравнения уровня калпротектина в одном или более образцах материала из полости рта в первый момент времени, с уровнем калпротектина во второй момент времени; и коррелирования снижения уровня калпротектина во второй момент времени, по сравнению с первым моментом времени, с улучшением патологического состояния у субъекта, и/или коррелирования увеличения уровня калпротектина во второй момент времени, по сравнению с первым моментом времени, с увеличением степени тяжести патологического состояния у субъекта.
[0047] Способы по настоящему изобретению для мониторинга патологического состояния у субъекта могут быть использованы для начала, изменения или модификации способов лечения воспаления в полости рта.
[0048] В одном варианте реализации настоящее изобретение относится к способу выбора схемы лечения у субъекта с подозрением на воспаление полости рта, включающему
(a) получение образца материала для анализа, такого как слюна, из полости рта от указанного субъекта,
(b) определение количества ПЯН или индикаторного вещества ПЯН в указанном анализируемом образце,
(c) сравнение количества ПЯН или индикаторного вещества ПЯН в анализируемом образце с контролем,
(d) выбор схемы лечения на основе сравнения, осуществленного на этапе (с).
[0049] В выборе способа, дополнительный этап для субъекта, принимающего лечение согласно выбранной схеме, является предпочтительным, в одном варианте реализации изобретения, в консультации со стоматологом.
[0050] Схема лечения будет варьироваться в зависимости от сравнения анализируемого образца с контролем (этап (с)). В некоторых случаях сравнение продемонстрирует незначительное воспаление или вообще его отсутствие, и в этом случае схема лечения может включать чистку зубов один раз или два раза в день с использованием пригодного средства для чистки зубов. Если сравнение демонстрирует определенную степень воспаления в полости рта, после этого может быть выбран один или более из нескольких видов схем лечения, например:
1. Чистка зубов чаще, чем в два раза в день, например, 3, 4, 5 или 6 раз.
2. Применение противомикробных агентов. Противомикробный агент может быть в составе средства для чистки зубов, например, зубной пасты или жидкости для полоскания рта, или может вводиться с помощью других способов, например, таблеток, суппозиториев, трансдермальных пластырей или в инъекционной форме. Вводимое количество будет эффективным противомикробным количеством, т.е. количеством, достаточным для устранения или уменьшения тяжести воспаления в полости рта.
3. Применение противовоспалительных агентов. Противовоспалительный агент может быть в составе средства для чистки зубов, например, зубной пасты или жидкости для полоскания рта, или может вводиться с помощью других способов, например, таблеток, суппозиториев, трансдермальных пластырей или в инъекционной форме. Вводимое количество будет эффективным противовоспалительным количеством, т.е. количеством, достаточным для устранения или уменьшения тяжести воспаления в полости рта.
[0051] Противомикробный агент, используемый в настоящем изобретении, не имеет особых ограничений, и может быть выбран из галогенированного дифенилового эфира (например, триклозана), растительных экстрактов или эфирных масел (например, экстракта розмарина, тимола, ментола, эвкалиптола, метилового эфира салициловой кислоты), бигуанидных антисептиков (например, хлоргексидина (СНХ), алексидина или октенидина), фенольных антисептиков, гексетидина, повидон иода, делмопинола, салифлора, ионов металлов и их солей (например, хлорида цинка, лактата цинка, цитрата цинка, фторида олова и хлорида олова), сангвинарина, прополиса, окислительных агентов (например, пероксида водорода, буферного пероксибората натрия, или пероксикарбоната), цетилпиридинийхлорида, экстракта магнолии, магнолола, гонокиола, бутила магнолола, пропил гонокиола и их смесей. В состав средства для чистки зубов также могут быть включены агенты, препятствующее присоединению, такие как Солрол (Solrol), а также агенты, диспергирующие налет, такие как ферменты (папаин, глюкоамилаза и т.д.).
[0052] Пригодные противовоспалительные агенты включают без ограничения стероидные агенты, такие как флуцинолон и гидрокортизон, нестероидные агенты (НПВП), такие как кеторолак, флурбипрофен, ибупрофен, напроксен, индометацин, диклофенак, этодолак, индометацин, сулиндак, толметин, кетопрофен, фенопрофен, пироксикам, набуметон, аспирин, дифлунизал, меклофенамат, мефенамовая кислота, оксифенбутазон и фенилбутазон.
[0053] В композициях для ухода за полостью рта в схемах лечения также могут использоваться другие известные активные вещества, таких как источник ионов фтора (например, фторид амина, фторид натрия, монофторфосфат натрия, фторид олова и т.д.) или основная аминокислота (например, аргинин, активный компонент технологии Рго-Argin™ компании Colgate.
[0054] Преимуществом настоящего изобретения является то, что учитывая простоту, безопасность и неинвазивность способов по настоящему изобретению, в некоторых вариантах реализации изобретения способы могут выполняться самим пациентом, который может записывать/сообщать результаты. Пациенты постоянно нуждаются в определенных мотивированных и основанных на комплаенсных подходах для содействия поддержке и мониторингу состояния здоровья их полости рта. Способы, описанные в этом документе, представляют собой несложные, экономически эффективные, быстрые и удобные средства для выполнения рутинных оценок состояния здоровья полости рта самими пациентами в домашних условиях. Таким образом, способы, описанные в настоящем документе, обеспечивают соответствующие подходы, которые могут быть реализованы в домашних условиях, т.е. способы и наборы являются "домашними". Эти способы позволяют субъектам повседневно следить за здоровьем их ротовой полости и вести периодический учет результатов, которые могут обсуждаться и использоваться при консультации со специалистом-стоматологом. Эти способы могут быть использованы после посещения стоматолога для мониторинга и оценки состояния здоровья полости рта и обращения или модулирования стоматологической помощи на основе результатов этих способов. В некоторых вариантах реализации изобретения результаты могут быть компьютеризированы, сохраняться в электронном виде и/или автоматически представлены врачу-стоматологу.
[0055] В способах настоящего изобретения, образцы материала из полости рта, такие как образцы слюны, сравнивают на той же единичной основе, например, 1; 0,1; 0,001 или 0,0001 мл или другие объемы материала из полости рта до тех пор, пока эти объемы одинаковы.
[0056] Таким образом, в одном из вариантов реализации настоящего изобретения предлагается способ (Способ 1). Для определения наличия, отсутствия или степени тяжести воспаления в полости рта, или мониторинга за патологическим воспалительным состоянием полости рта у субъекта, при этом способ включает:
(a) получение образца материала для анализа, такого как слюна, из полости рта от указанного субъекта,
(b) определение количества ПЯН или индикаторного вещества ПЯН в указанном анализируемом образце,
(c) сравнение количества ПЯН или индикаторного вещества ПЯН в анализируемом образце с контролем.
[0057] К примеру, в изобретении предложен:
1.1. Способ по способу 1, отличающийся тем, что контроль представляет собой образец от нормального здорового субъекта или множества здоровых субъектов;
1.2. Способ по способу 1, отличающийся тем, что контроль представляет собой другой анализируемый образец от того же субъекта, взятый заблаговременно;
1.3. Способ по любому из предшествующих способов, отличающийся тем, что количество ПЯН или индикаторного вещества ПЯН относительно контроля указывает на наличие воспаление в полости рта;
1.4. Способ по любому из предшествующих способов, отличающийся тем, что повышенный уровень ПЯН или индикаторного вещества ПЯН в анализируемом образце указывает на неэффективное лечение воспаления в полости рта; а пониженный уровень ПЯН или индикаторного вещества ПЯН в анализируемом образце указывает на эффективное лечение воспаления в полости рта;
1.5. Способ по любому из предшествующих способов, отличающийся тем, что воспаление в полости рта представляет собой гингивит;
1.6. Способ по любому из предшествующих пунктов, отличающийся тем, что воспаление в полости рта представляет собой периодонтит;
1.7. Способ по любому из предшествующих способов, отличающийся тем, что состояние, ассоциированное с воспалением в полости рта, представляет собой галитоз.
1.8. Способ по любому из предшествующих способов, отличающийся тем, что образец для анализа получают с помощью тампона;
1.9. Способ по любому из предшествующих способов, отличающийся тем, что образец для анализа получают с помощью отхаркивания;
1.10. Способ по любому из предшествующих способов, отличающийся тем, что количество полиморфноядерных нейтрофилов определяют с помощью микроскопии;
1.11. Способ по любому из предшествующих способов, отличающийся тем, что индикаторное вещество полиморфноядерных нейтрофилов представляет собой лактоферрин;
1.12. Способ по любому из предшествующих способов, отличающийся тем, что индикаторное вещество полиморфноядерных нейтрофилов представляет собой лейкоцитарную эстеразу;
1.13. Способ по любому из предшествующих способов, отличающийся тем, что индикаторное вещество полиморфноядерных нейтрофилов представляет собой калпротектин;
1.14. Способ по любому из предшествующих способов, отличающийся тем, что количество индикаторного вещества ПЯН определяется путем приведения в контакт слюны с материалом, абсорбирующим слюну, который содержит необходимые реагенты для определения наличия и/или количества индикаторного вещества ПЯН;
1.15. Способ по непосредственно предшествующему способу, отличающийся тем, что наличие и/или количество индикаторного вещества ПЯН идентифицируют по изменению цвета.
1.16. Способ выбора схемы лечения у субъекта с подозрением на воспаление в полости рта, включающий:
(a) получение образца материала для анализа, такого как слюна, из полости рта от указанного субъекта,
(b) определение количества ПЯН или индикаторного вещества ПЯН в указанном анализируемом образце,
(c) сравнение количества ПЯН или индикаторного вещества ПЯН в анализируемом образце с контролем,
(d) выбор схемы лечения на основе сравнения, осуществленного на этапе (с).
1.17. Способ по п. 1.16, включающий один или более вариантов реализации изобретения по пп. 1.1-1.16;
1.18. Способ по 1.16 и 1.17, включающий дополнительный этап для субъекта, получающего лечение согласно выбранной схеме;
1.19. Способ по 1.16 или 1.17, отличающийся тем, что схему лечения выбирают из чистки зубов два раза в день, чистки зубов чаще, чем в два раза в день, лечения субъекта противовоспалительными агентами, лечения субъекта противомикробными агентами или их комбинацией;
1.20. Способ по п. 1.19, отличающийся тем, что противомикробный агент выбирают из галогенированного дифенилового эфира (например, триклозана), растительных экстрактов или эфирных масел (например, экстракта розмарина, тимола, ментола, эвкалиптола, метилового эфира салициловой кислоты), бигуанидных антисептиков (например, хлоргексидина, алексидина или октенидина), фенольных антисептиков, гексетидина, повидон иода, делмопинола, салифлора, ионов металлов и их солей (например, хлорида цинка, лактата цинка, цитрата цинка, фторида олова и хлорида олова), сангвинарина, прополиса, окислительных агентов (например, пероксида водорода, буферного пероксибората натрия, или пероксикарбоната), цетилпиридинийхлорида, экстракта магнолии, магнолола, гонокиола, бутила магнолола, пропил гонокиола и их комбинаций. Также могут быть включены агенты, препятствующее присоединению, такие как Солрол (Solrol), а также агенты, диспергирующие налет, такие как ферменты (папаин, глюкоамилаза и т.д.).
1.21. Способ по п. 1.19 или 1.20, отличающийся тем, что противовоспалительные агенты выбирают из стероидных агентов, таких как флуцинолон и гидрокортизон, нестероидных агентов (НПВП), таких как кеторолак, флурбипрофен, ибупрофен, напроксен, индометацин, диклофенак, этодолак, индометацин, сулиндак, толметин, кетопрофен, фенопрофен, пироксикам, набуметон, аспирин, дифлунизал, меклофенамат, мефенамовая кислота, оксифенбутазон и фенилбутазон и их комбинаций.
1.22. Способ по любому из предшествующих способов, который является способом, реализуемым в домашних условиях.
[0058] Изобретение также относится к наборам для осуществления предлагаемых способов, например, наборам для проведения анализов у субъекта. В одном из вариантов реализации изобретения диагностический набор для идентификации субъекта, имеющего воспаление в полости рта или повышенный риск развития заболевания или состояния в результате воспаления в полости рта, при этом набор включает материал, абсорбирующий слюну, и содержащий необходимые реагенты для определения наличия и/или количества индикаторного вещества ПЯН вместе с инструкцией по применению.
[0059] Изобретение проиллюстрировано следующими неограничивающими его примерами.
ПРИМЕРЫ
Пример 1.
[0060] Цель. В этом клиническом исследовании оценивали уровни полиморфноядерных лейкоцитов (ПЯН), тип иммунных клеток, в сравнении с клиническими параметрами зубного налета (индекс зубного налета) и гингивита (индекс гингивита) соответственно.
[0061] Методика. В этом исследовании субъекты оценивались с помощью этих методов на исходном уровне, Визите 1 (7 дней), и Визите 2 (14 дней). На протяжении всего периода исследования всем субъектам были предоставлены коммерчески доступные фторсодержащие зубные пасты для гигиены полости рта.
[0062] Оценка зубного налета.
[0063] Зубной ряд обрабатывали раствором для окрашивания налета, после этого зубной налет оценивали на дисто-, медио-, мезиобуккальной и дисто-, медио-, мезиоязычной поверхности каждого зуба в соответствии с критериями модифицированного индекса Quigley и Hein (Turesky et al., 1970 и Quigley & Hein, 1962), который предусматривает шкалу от 0 до 5 баллов. Общий балл субъекта рассчитывали путем суммирования всех баллов для всех участков и деления на общее количество оцениваемых участков.
[0064] Оценка гингивита
[0065] Степень гингивита оценивали на 6 участках каждого зуба (те же участки, что перечисленные выше) согласно критериям Системы индекса гингивита  и Silness, 1963), которая предусматривает шкалу от 0 до 3 баллов. Общий балл субъекта рассчитывали путем суммирования всех баллов для всех участков и деления на общее количество оцениваемых участков.
и Silness, 1963), которая предусматривает шкалу от 0 до 3 баллов. Общий балл субъекта рассчитывали путем суммирования всех баллов для всех участков и деления на общее количество оцениваемых участков.
[0066] Измерение ПЯН
[0067] Перед проведением клинических оценок субъекты были проинструктированы относительно энергичного полоскания ротовой полости сбалансированным солевым раствором Хэнкса (Gibco® HBSS, Life Technologies) в течение 30 секунд, с последующим сплевыванием в стерильные пробирки. К образцам добавляли формальдегид, после этого образцы центрифугировали. Полученные гранулы ресуспендировали и окрашивали акридиновым оранжевым в темной комнате при комнатной температуре в течение 20 минут перед анализом с помощью флуоресцентной микроскопии.
[0068] Результаты. В исследование были включены сто пятьдесят девять (159) взрослых субъектов (61 мужчин и 98 женщин; возрастной диапазон 19-61 лет).
[0069] Демографические показатели субъектов приведены в Таблице 1. Сводные результаты клинических оценок приведены в Таблицах 2-4 ниже.

[0070] Для сравнения ПЯН с индексом зубного налета и индексом гингивита выполняли графическое отображение и проводили соответствующий корреляционный анализ. Перед проведением анализа, из-за смещенного распределения баллов ПЯН, использовали логарифмическое (log10) преобразование данных. Проведенный анализ показал, что корреляционный коэффициент Log (ПЯН) с индексом зубного налета составляет 0,57, а корреляционный коэффициент Log (ПЯН) с индексом гингивита составляет 0,66. Оба корреляционных коэффициента достоверно (Р < 0,0001) отличаются от нуля.
[0071] Приведенный выше анализ показал, что Log (ПЯН) демонстрирует результаты, которые убедительно коррелируют с индексом зубного налета и индексом гингивита. Заключительный этап анализа предназначался для оценки статистической чувствительности Log (ПЯН) по сравнению с индексом зубного налета и индексом гингивита, в отношении правомочности такой системы измерений для выявления изменений в сравнении с исходным уровнем. В Таблицах 2, 3 и 4 приводятся сводные данные, которые анализируются, и результаты анализа.
[0072] В Таблице 2 приведены исходные данные, сгруппированные для каждого из трех индексов.

[0073] В Таблицах 3 и 4 обобщены изменения для визитов 1 и 2, соответственно, по сравнению с исходными данными, а анализ представлен посредством t-статистики и Р-значения для статической значимости среднего изменения по сравнению с исходным уровнем, t-статистика является критерием результата этого анализа, и применяется для определения Р-значения, используемого для оценки статистической значимости изменения по сравнению с исходным уровнем.
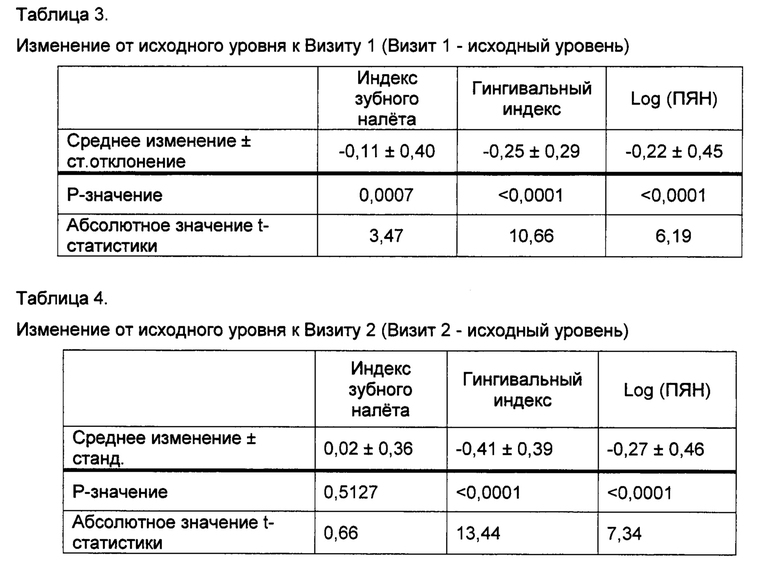
[0074] Сводные данные, приведенные в Таблице 2, представляют средний показатель и стандартное отклонение значения исходного уровня для каждого измерения. В Таблицах 3 и 4 все анализы демонстрируют статистически значимые (р < 0,0001) средние изменения по сравнению с исходным уровнем за исключением изменения между Визитом 2 и исходным уровнем для индекса зубного налета. Тем не менее, в обеих таблицах 3 и 4 наибольшая t-статистика ассоциирована с индексом гингивита. Поскольку чем больше t-статистика, тем больше статистическая чувствительность системы измерений, можно сделать вывод, что в данном исследовании индекс гингивита имеет большую статистическую чувствительность, чем две другие системы измерений, с точки зрения обнаружения изменений по сравнению с исходным уровнем. Log (ПЯН), демонстрируя большую статистическую чувствительность, чем индекс зубного налета, оказывается менее чувствительным, чем индекс гингивита.
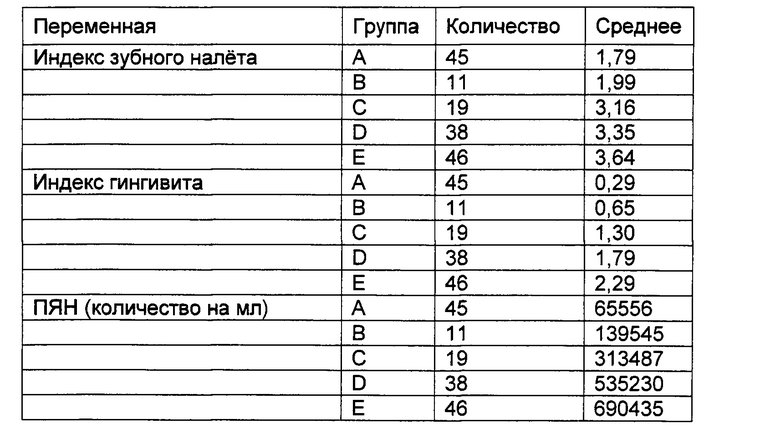
[0075] Анализируемую группу из 159 взрослых субъектов можно было разделить на отдельные группы на основе индекса зубного налета, индекса гингивита и количества ПЯН с более низкими числовыми индексами, которые свидетельствуют о здоровой среде полости рта.
Пример 2.
[0076] Цель. В этом клиническом исследовании оценивали уровни полиморфноядерных лейкоцитов (ПЯН) в сочетании с клиническими параметрами, такими как зубной налет (3Н), воспаление десен (ВД) и глубина при зондировании зубодесневого кармана (ГК) среди следующих групп субъектов, стратифицированных на основе их первоначального клинического статуса:
- здоровые: субъекты с хорошим состоянием здоровья полости рта, не имеющие гингивита
- гингивит: субъекты с гингивитом, диагностированным на основе клинической оценки
- заболевания пародонта: субъекты из заболеваниями пародонта, диагностированными на основании клинической оценки
[0077] В таблицах ниже приведены демографические характеристики исследуемых пациентов (таблица 5), результаты клинических оценок (таблица 6) и уровни полиморфноядерных лейкоцитов (таблица 7) до и после 28 дней использования зубной пасты на основе триклозана/сополимера (Colgate®Total - сополимер триклозан и полиметилвинилэфир/малеиновый ангидрид) для гигиены полости рта. Методики описаны в данном документе или аналогичны тем, которые приведены в
Примере 1.
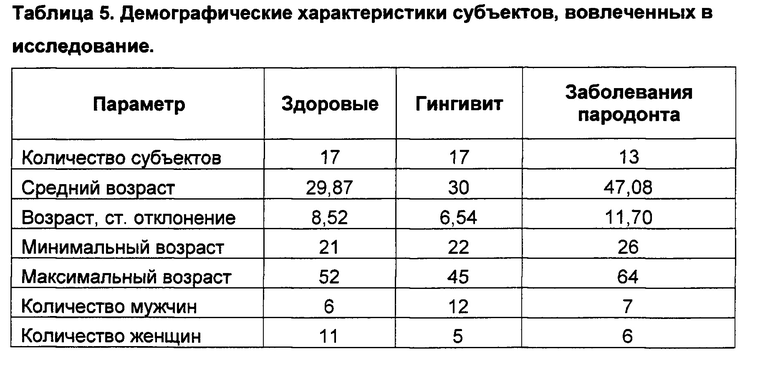
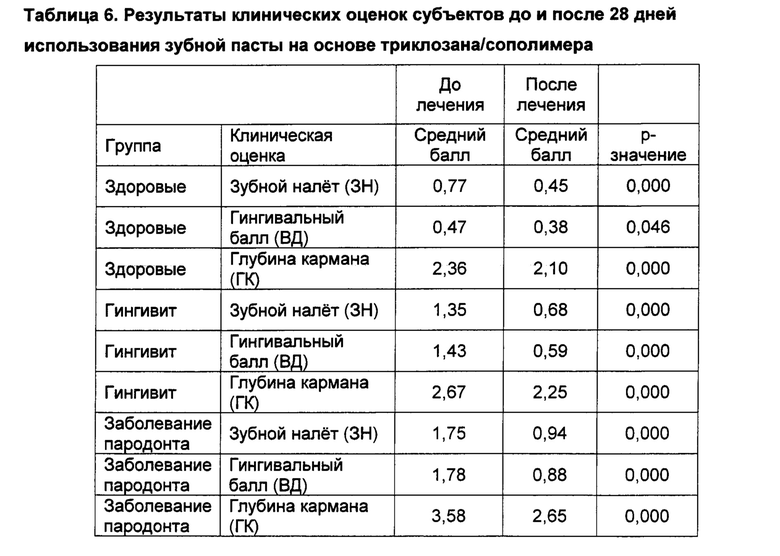
Результаты указывают на значимое снижение каждого из оцениваемых клинических параметров для всех групп исследуемых субъектов.
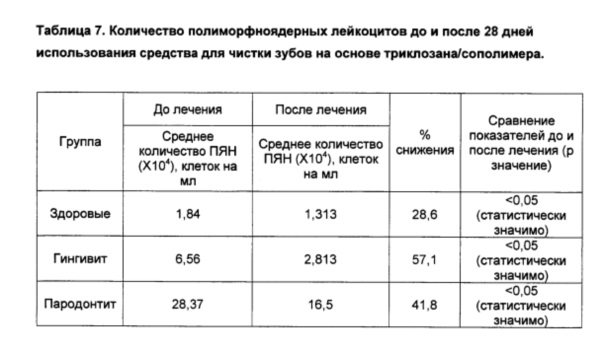
Результаты указывают на значимое снижение количества ПЯН для каждой группы исследуемых субъектов.
Пример 3.
[0078] Цель. В этом клиническом исследовании оценивали уровни полиморфноядерных лейкоцитов (ПЯН) у субъектов, которым для гигиены полости рта назначалась либо коммерчески доступная фторсодержащая зубная паста, либо зубная паста на основе триклозана/сополимера. Субъектов оценивали до и после 30 дней использования каждой зубной пасты.
[0079] В таблице 8 представлены результаты этого исследования.
[0080] Методики описаны в данном документе или аналогичны тем, которые приведены в предыдущих примерах.
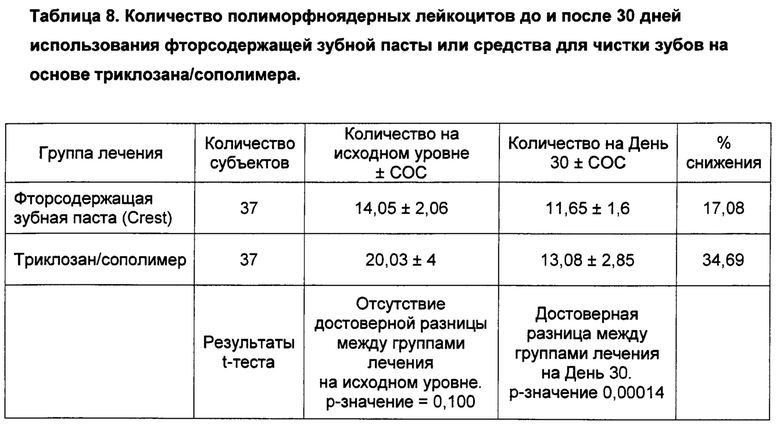
[0081] Результаты указывают на значимое снижение количества ПЯН у субъектов, которые для гигиены полости рта использовали зубную пасту на основе триклозана/сополимера. Аналогичный эффект не наблюдался среди тех субъектов, которые использовали фторсодержащие зубные пасты.
Пример 4.
[0082] В этом клиническом исследовании оценивали уровни полиморфноядерных лейкоцитов (ПЯН) в сочетании со следующими общепринятыми клиническими и микробиологическими параметрами до и после 2-х недельного использования для гигиены полости рта 0,12% хлоргексидина (СНХ) для полоскания:
- Клинические параметры:
- Неприятный запах на основе органолептических данных и оценки уровня неприятного запаха изо рта галиметром.
- Оценка налета на языке на основе клинического индекса налета на языке.
- Микробиологические параметры:
- Общее количество жизнеспособных организмов в зубном налете, слюне и на поверхности языка.
- Организмы, обуславливающие неприятный запах, в зубном налете, слюне и на поверхности языка.
Демографические характеристики субъектов, вовлеченных в исследование, представлены в таблице 9.

[0083] Определяли количество полиморфноядерных лейкоцитов (ПЯН) у всех субъектов до и после использования СНХ для полоскания полости рта. Результаты указывают на снижение количества ПЯН во всех группа субъектов после двух недель использования СНХ для полоскания полости рта.
[0084] В таблицах 10-12 представлены результаты клинической оценки субъектов с помощью галиметра, органолептических показателей и по индексу налета на языке.
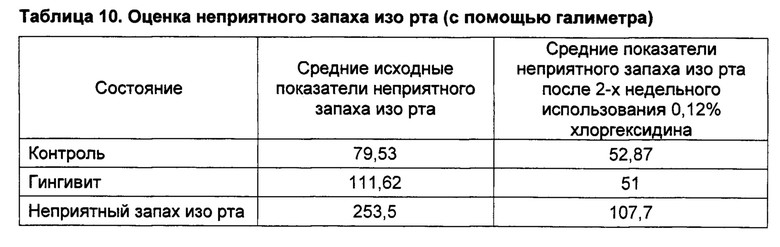
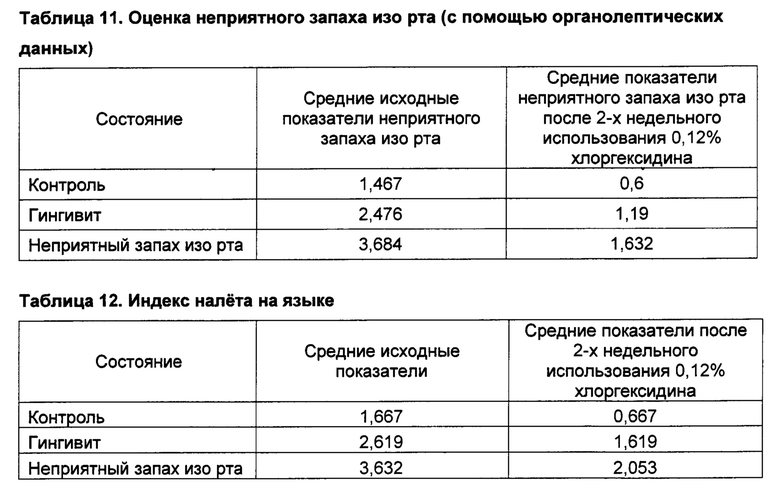
[0085] Результаты показывают, что у субъектов, которым было назначено полоскание раствором СНХ, отмечалось значимое снижение показателя неприятного запаха изо рта при всех клинических оценках.
[0086] В таблицах 13-18 приведены результаты микробиологических оценок субъектов относительно наличия жизнеспособных организмов в зубном налете, слюне и на поверхности языка в дополнение к организмам, обуславливающим неприятный запах в каждом из этих образцов.
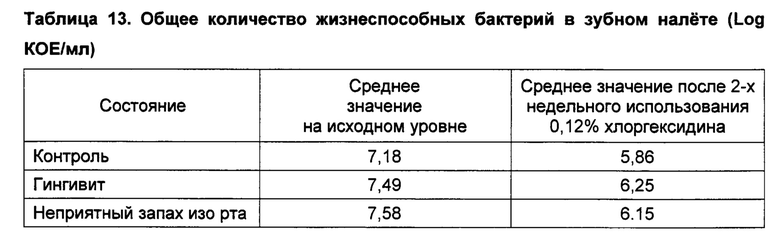
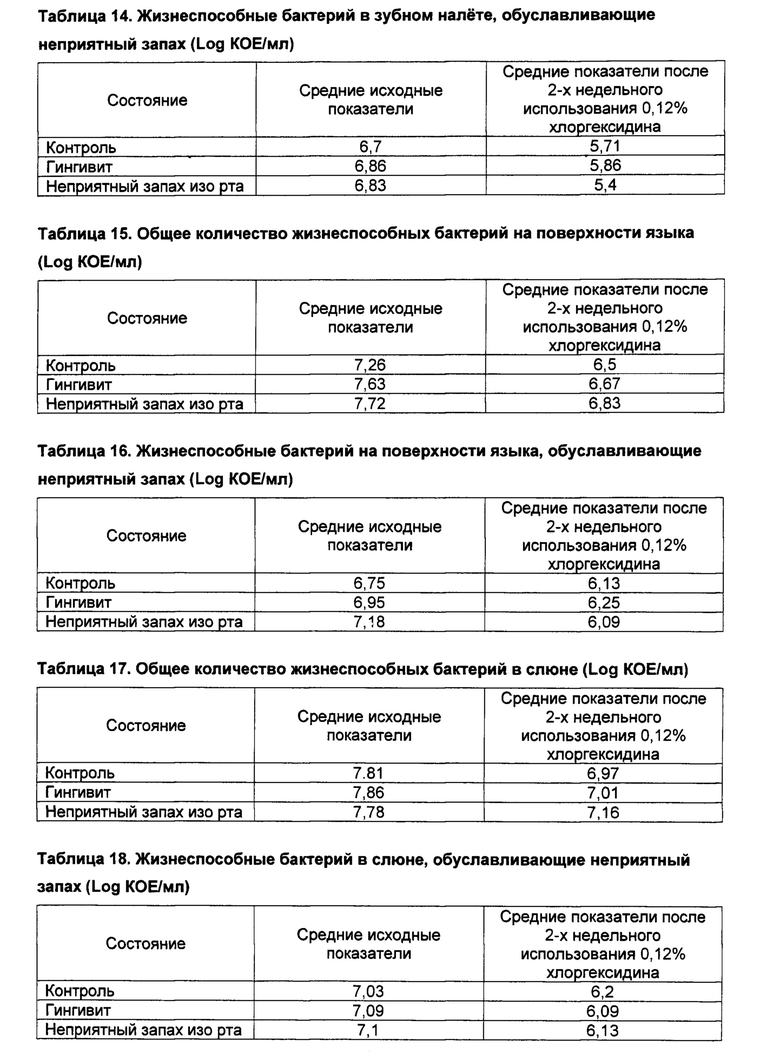
[0087] У субъектов отмечалось значимое снижение количества всех видов организмов в каждом образце из полости рта, оцениваемом после применения полосканий раствором СНХ.
Пример 5
[0088] В этом исследовании определяли, как быстро начинают проявляться изменения количества ПЯН в полости рта и клинические результаты у субъектов, использующих для чистки зубов зубную пасту Total или фторсодержащую зубную пасту.
Дизайн исследования.
1. Субъекты использовали для чистки зубов фторсодержащую зубную пасту или зубную пасту Total.
2. Субъектов оценивали на момент начала исследования (исходный уровень или до применения какой-либо зубной пасты) и также после чистки зубов пастой в течение 1 недели и 2 недель.
Следующие оценки проводились для всех субъектов на исходном уровне и по истечении 1 недели и 2 недель использования назначенной зубной пасты:
1. ПЯН
2. Клинические параметры (индекс зубного налета, индекс гингивита, индекс кровоточивости).
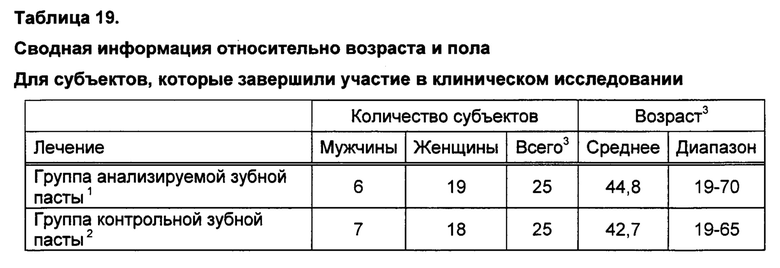
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеинового ангидрида), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Статистически значимых различий между группами лечения по полу или возрасту не выявлено.
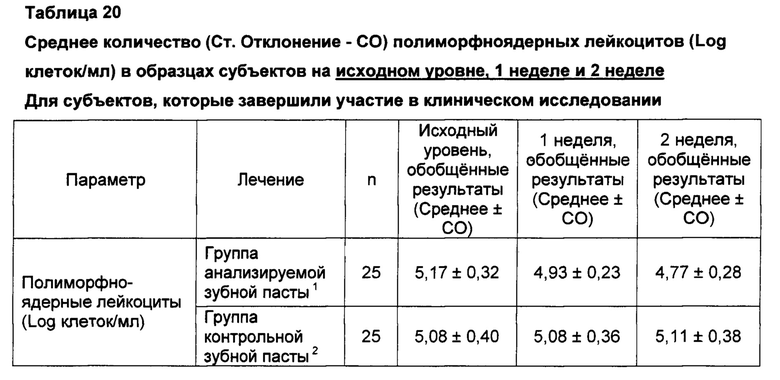
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Статистически значимых различий между двумя группами лечения на исходном уровне по отношению к полиморфноядерных лейкоцитам (log клетка/мл) не выявлено.
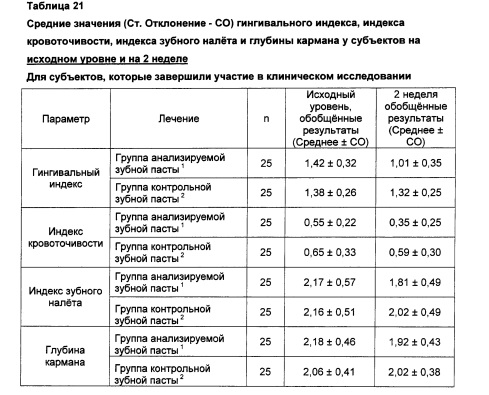
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Статистически значимых различий между двумя группами лечения на исходном уровне по показателям гингивального индекса, индекса кровоточивости, индекса зубного налета и глубины кармана (мм) не выявлено.
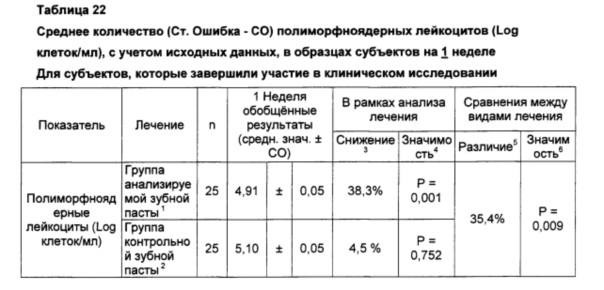
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
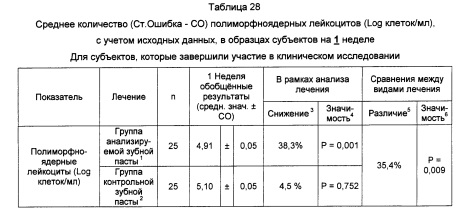
3. Снижение, представленное как среднее значение на 1 неделе, относительно исходного среднего значения. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) на 1 неделе обследования.
4. Значимость парного t-теста сравнения результатов обследования на исходном уровне и 1 неделе.
5. Различие между средними значениями на 1 неделе, представленными как снижение среднего значения на 1 неделе для группы, использующей контрольную зубную пасту. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) в группе, использующей анализируемую зубную пасту, относительно группы, использующей контрольную зубную пасту.
6. Статистическая значимость сравнения ANCOVA средних значений с учетом исходных данных.
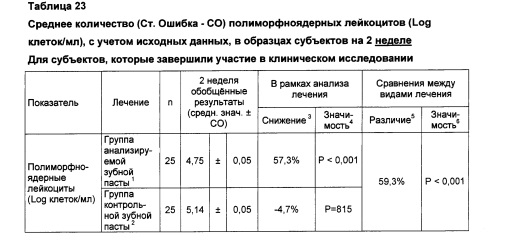
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
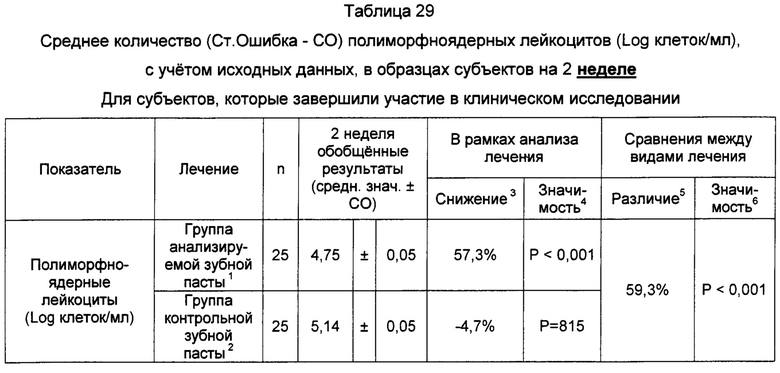
3. Снижение, представленное как среднее значение на 2 неделе относительно исходного среднего значения. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) на 2 неделе обследования.
4. Статистическая значимость парного t-теста сравнения результатов обследования на исходном уровне и 2 неделе.
5. Различие между средними значениями на 2 неделе, представленными как снижение среднего значения на 2 неделе для группы, использующей контрольную зубную пасту. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) в группе, использующей анализируемую зубную пасту, относительно группы, использующей контрольную зубную пасту.
6. Статистическая значимость сравнения ANCOVA средних значений с учетом исходных данных.
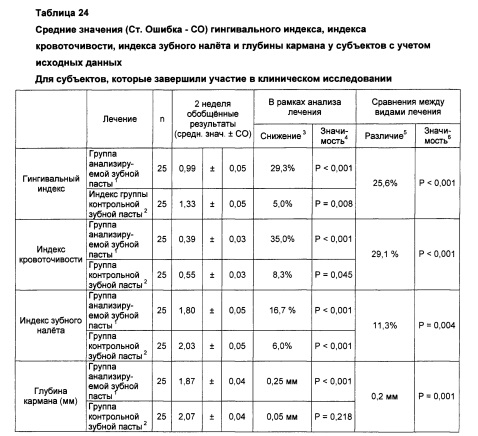
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
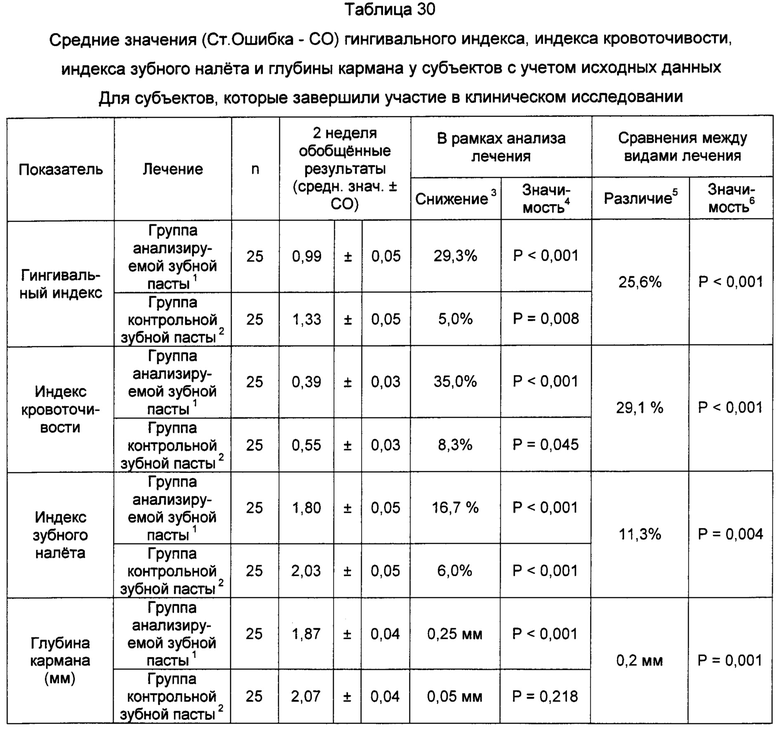
3. Снижение, представленное как среднее значение на 2 неделе относительно исходного среднего значения. Положительное значение указывает на снижение баллов индексов на 2 неделе обследования.
4. Статистическая значимость парного t-теста сравнения результатов обследования на исходном уровне и 2 неделе.
5. Различие между средними значениями на 2 неделе, представленными как снижение среднего значения на 2 неделе для группы, использующей контрольную зубную пасту. Положительное значение указывает на снижение показателей индекса в группе, использующей анализируемую зубную пасту, относительно группы, использующей контрольную зубную пасту.
6. Статистическая значимость сравнения ANCOVA средних значений с учетом исходных данных.
Сводная информация по результатам:
- у субъектов, использующих для чистки зубов зубную пасту Total, отмечалось снижение количества ПЯН уже после одной недели использования этой зубной пасты.
- дополнительное снижение количества ПЯН у субъектов, использующих для чистки зубов зубную пасту Total, отмечалось в течение второй недели ее использования. Другими словами, эффекты зубной пасты Total становились более выраженными между 1 и 2 неделями.
Значимость полученных результатов:
1. Изменения количества ПЯН (или нейтрофилов) начинают происходить в первые дни после использования эффективной зубной пасты (Total).
2. Кроме того, % изменений количества ПЯН отмечается выше при использовании Total, чем фторсодержащей зубной пасты.
3. % различий в количестве ПЯН в группе Total отмечается значительно выше, чем в показателях обычных клинических индексов, т.е. индекса гингивита, индекса кровоточивости и индекс зубного налета.
Пример 6
Цель исследования - определить, как быстро у субъектов, использующих для чистки зубов зубную пасту Total или фторсодержащую зубную пасту, начинают проявляться изменения количества ПЯН в полости рта и клинические результаты.
Дизайн исследования.
1. Субъекты использовали для чистки зубов фторсодержащую зубную пасту или зубную пасту Total
2. Субъектов оценивали на момент начала исследования (исходный уровень или до применения какой-либо зубной пасты) и также после чистки зубов пастой в течение 1 недели и 2 недель.
Следующие оценки проводились для всех субъектов на исходном уровне и по истечении 1 недели и 2 недель использования назначенной зубной пасты:
1. ПЯН
2. Клинические параметры (индекс зубного налета, индекс гингивита, индекс кровоточивости).
Результаты представлены в следующих таблицах.
Выводы
- у субъектов, использующих для чистки зубов зубную пасту Total, отмечалось снижение количества ПЯН уже после одной недели использования этой зубной пасты.
- дополнительное снижение количества ПЯН у субъектов, использующих для чистки зубов зубную пасту Total, отмечалось в течение второй недели ее использования, т.е. эффекты Total становились более выраженными от 1 недели до 2 недели.
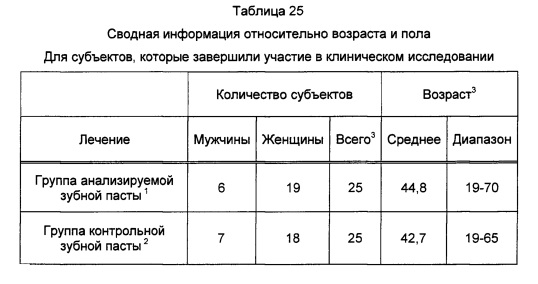
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Статистически значимых различий между группами лечения по полу или возрасту не выявлено.
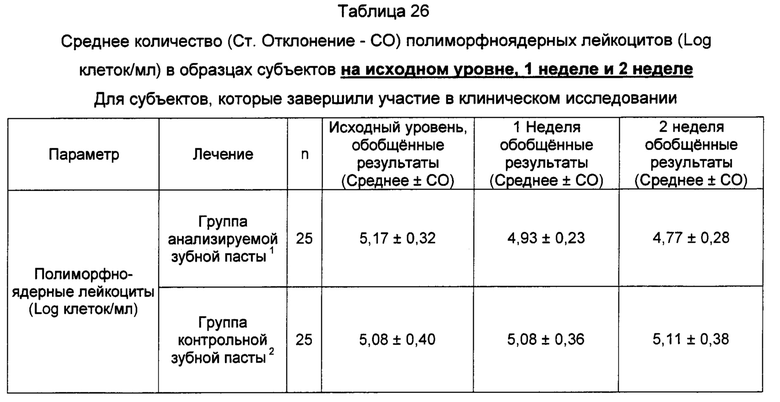
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Статистически значимых различий между двумя группами лечения на исходном уровне по отношению к полиморфноядерных лейкоцитам (log клетка/мл) не выявлено.
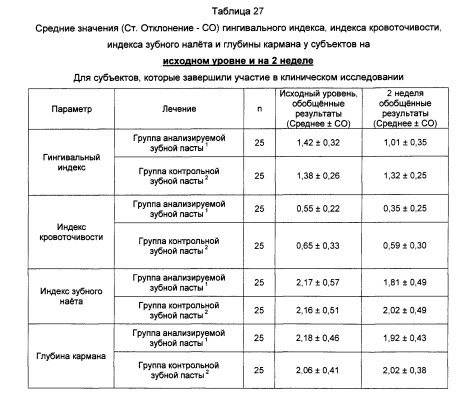
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Статистически значимых различий между двумя группами лечения на исходном уровне по показателям гингивального индекса, индекса кровоточивости, индекса зубного налета и глубины кармана (мм) не выявлено.
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Снижение, представленное как среднее значение на 1 неделе, относительно исходного среднего значения. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) на 1 неделе обследования.
4. Значимость парного t-теста сравнения результатов обследования на исходном уровне и 1 неделе.
5. Различие между средними значениями на 1 неделе, представленными как снижение среднего значения на 1 неделе для группы, использующей контрольную зубную пасту. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) в группе, использующей анализируемую зубную пасту, относительно группы, использующей контрольную зубную пасту.
6. Статистическая значимость сравнения ANCOVA средних значений с учетом исходных данных.
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера, 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Снижение, представленное как среднее значение на 2 неделе относительно исходного среднего значения. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) на 2 неделе обследования.
4. Статистическая значимость парного t-теста сравнения результатов обследования на исходном уровне и 2 неделе.
5. Различие между средними значениями на 2 неделе, представленными как снижение среднего значения на 2 неделе для группы, использующей контрольную зубную пасту. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) в группе, использующей анализируемую зубную пасту, относительно группы, использующей контрольную зубную пасту.
6. Статистическая значимость сравнения ANCOVA средних значений с учетом исходных данных.
1. В составе средства для чистки зубов содержится 0,3% триклозана, 2,0% сополимера (сополимер полиметилвинилэфир/малеиновый ангидрид), 0,243% натрия фторида в расчете на диоксид кремния (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
2. Зубная паста Colgate Cavity Protection Great Regular Flavor (Colgate-Palmolive Co., Нью-Йорк, штат Нью-Йорк)
3. Снижение, представленное как среднее значение на 2 неделе относительно исходного среднего значения. Положительное значение указывает на снижение количества полиморфноядерных лейкоцитов (Log клеток/мл) на 2 неделе обследования.
4. Статистическая значимость парного t-теста сравнения результатов обследования на исходном уровне и 2 неделе.
5. Различие между средними значениями на 2 неделе, представленными как снижение среднего значения на 2 неделе для группы, использующей контрольную зубную пасту.
Положительное значение указывает на снижение показателей индекса в группе, использующей анализируемую зубную пасту, относительно группы, использующей контрольную зубную пасту.
6. Статистическая значимость сравнения ANCOVA средних значений с учетом исходных данных.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПЛЕКС ДЛЯ ПРОФИЛАКТИКИ ОКСИДАТИВНОГО СТРЕССА ПОЛОСТИ РТА | 2019 |
|
RU2748338C2 |
| Способ оценки степени галитоза полости рта | 2020 |
|
RU2755170C1 |
| СПОСОБЫ И КОМПЛЕКТЫ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2007 |
|
RU2493816C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ПРЕДУПРЕЖДЕНИЯ ИЛИ УМЕНЬШЕНИЯ ЗУБНОГО НАЛЕТА И/ИЛИ ГИНГИВИТА | 2004 |
|
RU2378023C2 |
| Способ комплексного лечения и профилактики воспалительных заболеваний пародонта и слизистой оболочки рта у лиц с йододефицитом | 2023 |
|
RU2813153C1 |
| ЗУБНАЯ ПАСТА, СОДЕРЖАЩАЯ КОМПЛЕКС ГИДРОЛАЗ | 2013 |
|
RU2527692C1 |
| СПОСОБ ПРОФИЛАКТИКИ ГИНГИВИТА И ГИПОСИАЛИИ У БОЛЬНЫХ ЮВЕНИЛЬНЫМ РЕВМАТОИДНЫМ АРТРИТОМ | 2017 |
|
RU2685787C1 |
| БЕЗАБРАЗИВНАЯ ЗУБНАЯ ПАСТА, СОДЕРЖАЩАЯ ФЕРМЕНТЫ ПАПАИН, ДЕКСТРАНАЗУ, АЛЬФА-АМИЛАЗУ, КАЛИЯ ИЛИ АММОНИЯ ТИОЦИАНАТ, ИНВЕРТАЗУ ИЛИ ГЛЮКОАМИЛАЗУ, ГЛЮКОЗООКСИДАЗУ, ЛАКТОПЕРОКСИДАЗУ, ЛИЗОЦИМ ИЛИ ЛАКТОФЕРРИН И ЛАКТУЛОЗУ | 2009 |
|
RU2407512C1 |
| ЗУБНАЯ ПАСТА, СОДЕРЖАЩАЯ БУФЕРНУЮ СМЕСЬ | 2013 |
|
RU2527691C1 |
| СОДЕРЖАЩАЯ МИРТ КОМПОЗИЦИЯ ДЛЯ ГИГИЕНЫ ПОЛОСТИ РТА | 2007 |
|
RU2469703C2 |
Изобретение относится к области стоматологии и раскрывает способ определения эффективности лечения субъекта, у которого определено воспаление в полости рта. Способ включает получение тестового образца материала из полости рта, такого как слюна, от указанного субъекта, определение количества полиморфноядерных нейтрофилов или индикаторного вещества полиморфноядерных нейтрофилов в указанном анализируемом образце, сравнение количества полиморфноядерных нейтрофилов или индикаторного вещества полиморфноядерных нейтрофилов в указанном анализируемом образце с контролем и выбор режима лечения. Способ позволяет осуществлять мониторинг хода лечения воспаления ротовой полости. 16 з.п. ф-лы, 30 табл.
1. Способ определения эффективности лечения субъекта, у которого определено воспаление в полости рта, включающий:
(a) получение тестового образца материала из полости рта, такого как слюна, от указанного субъекта,
(b) определение количества полиморфноядерных нейтрофилов или индикаторного вещества полиморфноядерных нейтрофилов в указанном анализируемом образце,
(c) сравнение количества полиморфноядерных нейтрофилов или индикаторного вещества полиморфноядерных нейтрофилов в указанном анализируемом образце с контролем,
(d) выбор режима лечения на основании сравнения, осуществленного в шаге (с),
в котором анализируемый образец взят после начала лечения, и в котором контрольный образец представляет собой образец материала из ротовой полости того же субъекта, взятый до начала лечения, и в котором режим лечения выбирается из чистки зубов два раза в день, чистки зубов более двух раз в день, лечения субъекта противовоспалительными агентами, лечения субъекта противомикробными агентами, или их комбинации, при этом повышенное количество полиморфноядерных нейтрофилов или индикаторного вещества полиморфноядерных нейтрофилов в указанном анализируемом образце указывает на неэффективное лечение воспаления в полости рта; а пониженный уровень полиморфноядерных нейтрофилов или индикаторного вещества полиморфноядерных нейтрофилов в анализируемом образце указывает на эффективное лечение воспаления в полости рта, и в котором индикаторное вещество полиморфноядерных нейтрофилов выбрано из лактоферрина, эстеразы лейкоцитов и калпротектина.
2. Способ по п. 1, отличающийся тем, что материал из полости рта представляет собой слюну.
3. Способ по п. 1, отличающийся тем, что воспаление в полости рта представляет собой гингивит.
4. Способ по п. 1, отличающийся тем, что воспаление в полости рта представляет собой периодонтит.
5. Способ по п. 1, отличающийся тем, что состояние, ассоциированное с воспалительным процессом в полости рта, представляет собой галитоз.
6. Способ по п. 1, отличающийся тем, что образец для анализа получают с помощью тампона.
7. Способ по п. 1, отличающийся тем, что образец для анализа получают с помощью отхаркивания.
8. Способ по п. 1, отличающийся тем, что индикаторное вещество полиморфноядерных нейтрофилов представляет собой лактоферрин.
9. Способ по п. 1, отличающийся тем, что индикаторное вещество полиморфноядерных нейтрофилов представляет собой лейкоцитарную эстеразу.
10. Способ по п. 1, отличающийся тем, что индикаторное вещество полиморфноядерных нейтрофилов представляет собой калпротектин.
11. Способ по п. 1, отличающийся тем, что материал из полости рта приводят в контакт с абсорбирующим материалом, содержащим реагенты для определения наличия или количества индикаторного вещества полиморфноядерных нейтрофилов.
12. Способ по п. 11, отличающийся тем, что абсорбирующий материал представляет собой полоску или индикаторную полоску.
13. Способ по п. 1, включающий дополнительные этапы применения субъектом терапевтически эффективного количества композиции для ухода за зубами.
14. Способ по п. 13, отличающийся тем, что композиция для ухода за полостью рта содержит активный агент, выбранный из группы, состоящей из противомикробного агента, противовоспалительного агента, источника ионов фтора, основной аминокислоты и их смесей.
15. Способ по п. 1, отличающийся тем, что противомикробный агент выбирают из группы, состоящей из галогенированного дифенилового эфира, триклозана, растительных экстрактов, эфирных масел, экстракта розмарина, тимола, ментола, эвкалиптола, метилового эфира салициловой кислоты, бигуанидных антисептиков, хлоргексидина, алексидина, октенидина, фенольных антисептиков, гексетидина, повидон иода, делмопинола, салифлора, ионов металлов и их солей, хлорида цинка, лактата цинка, цитрата цинка, фторида олова и хлорида олова, сангвинарина, прополиса, окислительных агентов, пероксида водорода, буферного пероксибората натрия, пероксикарбоната, цетилпиридинийхлорида, экстракта магнолии, магнолола, гонокиола, бутил магнолола, пропил гонокиола и их комбинаций; а противовоспалительные агенты выбирают из группы, состоящей из стероидных агентов, флуцинолона, гидрокортизона, нестероидных агентов (НПВП), кеторолака, флурбипрофена, ибупрофена, напроксена, индометацина, диклофенака, этодолака, индометацина, сулиндака, толметина, кетопрофена, фенопрофена, пироксикама, набуметона, аспирина, дифлунизала, меклофенамата, мефенамовой кислоты, оксифенбутазона и фенилбутазона и их комбинаций.
16. Способ по п. 14, отличающийся тем, что активный агент выбирают из группы, состоящей из триклозана, хлоргексидина, источника ионов фтора, аргинина и их смесей.
17. Способ по п. 1, являющийся способом, реализуемым в домашних условиях.
| ADONOGIANAKI E | |||
| et al | |||
| Lactoferrin in the gingival crevice as a marker of polymorphonuclear leucocytes in periodontal diseases | |||
| Journal of Clinical Periodontology, vol | |||
| Прибор для промывания газов | 1922 |
|
SU20A1 |
| MARTINS C.A | |||
| et al | |||
| Correlation of lactoferrin with neutrophilic inflammation in Body Fluids | |||
| Сlinical and diagnostic laboratory immunology, Nov | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| Мяльно-трепальная машина | 1924 |
|
SU763A1 |
| MURRAY M.C | |||
| et al | |||
| The relationship between elastase and lactoferrin in healthy, gingivitis and periodontitis sites | |||
| Oral Diseases | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| УСТРОЙСТВО ДЛЯ ИДЕНТИФИКАЦИИ ЗАБОЛЕВАНИЙ РОТОВОЙ ПОЛОСТИ | 2010 |
|
RU2526672C2 |
| УСТАНОВКА ВИБРАЦИОННАЯ ДЛЯ ПРИГОТОВЛЕНИЯ КОРМОВ | 2013 |
|
RU2548888C1 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛИТЕЛЬНЫХ И ВОСПАЛИТЕЛЬНО-ДЕСТРУКТИВНЫХ ЗАБОЛЕВАНИЙ ПАРОДОНТА | 2002 |
|
RU2223088C1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| RU 2012124153 A, 27.04.2015 | |||
| ПЕРОРАЛЬНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ОКИСЛЕННУЮ КАМЕЛИЮ | 2005 |
|
RU2390329C2 |
Авторы
Даты
2019-10-10—Публикация
2014-06-05—Подача