Изобретение относится к урологии и предназначено для уменьшения солевой обструкции мочеточниковых стентов.
Внутреннее дренирование верхних мочевыводящих путей давно и с успехом используется в урологии [Trapeznikova M.F., Dutov.V., Rumyantsev A.А., et al. Choice of urinary tract drainage in different age groups of patients with urolithiasis. Urologiia. 2011;2:3-7.]. Оно рекомендовано по завершению различных эндоурологических вмешательств, при выполнении различных реконструктивно-пластических вмешательств на мочеточнике, лоханочно-мочеточниковом сегменте [Wilson С.Н., Rix D.A., Manas D.M. Routine intraoperative ureteric stenting for kidney transplant recipients. CochraneDatabaseSystRev. 2013; 6: CD004925]. Преимущества этого вида дренирования очевидны: малая инвазивность, отсутствие обязательного рутинного применения рентген- и ультразвукового контроля, отсутствие наружного дренажа у пациента значительно снижает риск инфекционных осложнений, повышает качество его жизни.
С другой стороны, существуют и не менее очевидные проблемы применения внутренних стентов верхних мочевыводящих путей, главными из которых, являются обструкция стента и инфекция. Одной из основных причин, лежащих в основе этих двух осложнений, является отложение солей на внутренней и внешней поверхностях стента, образование биопленок между поверхностью стента и слизистой мочеточника [Liatsikos E.N., Karnabatidis D., Katsanos K., et al.Ureteral metal stents: 10-year experience with malignant ureteral obstruction treatment. J. Urol. 2009; 182(6): 2613-2617.].
Существует два принципиальных подхода к профилактике солевой обструкции мочеточниковых стентов:
- использование стентов из современных материалов с нанопокрытиями,
- применение лекарственных препаратов и физических методов воздействия при использовании стандартных «потоковых» стентов.
Известны попытки нивелировать негативные эффекты использованием металлических стентов, а также различных покрытий, наносимых на стент [Kogan M.I., Moisyuk Ja. G., Shkodkin S.V., et al. Effectiveness of ureteral stents with nanostructured coating in renal transplantation (preliminary results). Urologiia. 2015; 1: 58-61.], но проблема все еще далека от окончательного решения.
Наиболее близким способом, взятым в качестве прототипа, является способ неинвазивной санации мочеточниковых стентов путем ультразвукового озвучивания с поверхности тела над проекцией мочеточникового стента (П.И. Шустер, А.А. Новиков, Я.Б. Шустер, О.Г. Новикова. Изменения ультраструктуры биопленок и гидродинамических показателей при неинвазивной ультразвуковой санации мочеточниковых стентов. В кн.: Материалы XVI Конгресса Российского Общества Урологов «Урология в XXI веке». Уфа, 20-22 октября 2016. С. 393.) Акустическое воздействие осуществляется неинвазивно, но из-за высокой частоты воздействия (42 кГц) и ограничений по амплитуде воздействия с поверхности тела эффективность процесса санации существенно снижается.
Техническим результатом изобретения является повышение эффективности неинвазивной санации мочеточниковых стентов, снижение их солевой обструкции и создание условий для профилактики обструктивного пиелонефрита.
Указанный технический результат повышения эффективности неинвазивной санации мочеточниковых стентов достигается тем, что осуществляют ультразвуковое озвучивание с поверхности тела над проекцией мочеточникового стента, причем озвучивание осуществляют амплитудно-импульсным модулированным сигналом, у которого в качестве несущей частоты используют низкочастотную часть ультразвукового спектра 16-30 кГц, а качестве модулирующей применяют частоты, кратные частоте сетевого питающего напряжения и сформированные на его основе.
Вариант реализации предлагаемого способа неинвазивной санации мочеточниковых стентов заключается в следующем. Поскольку особенностями применения способа в данном медико-технологическом процессе являются:
- неинвазивность процесса, что определяет задачу обеспечения эффективности воздействия с поверхности тела пациента в глубине гетерогенной среды;
- необходимость снижения теплового эффекта воздействия на поверхности кожного покрова, поскольку предыдущее условие требует, с одной стороны, значительного повышения амплитуды ультразвуковых колебаний на рабочем торце инструмента, а, с другой стороны, повышения площади рабочей поверхности ультразвукового инструмента.
Первая особенность требует учета эффекта затухания акустических колебаний при их распространении по биотканями здесь необходимо учитывать как коэффициенты затухания разных типов тканей, так и специфику распространения акустических волн и, в первую очередь, квадратичную зависимость затухания от частоты. Поэтому представляется рациональным выбор наиболее низкой несущей частоты из разрешенных к применению. Поэтому, для повышения эффективности процесса, частота ультразвукового воздействия выбирается в нижней части ультразвукового диапазона от 16 до 30 кГц.
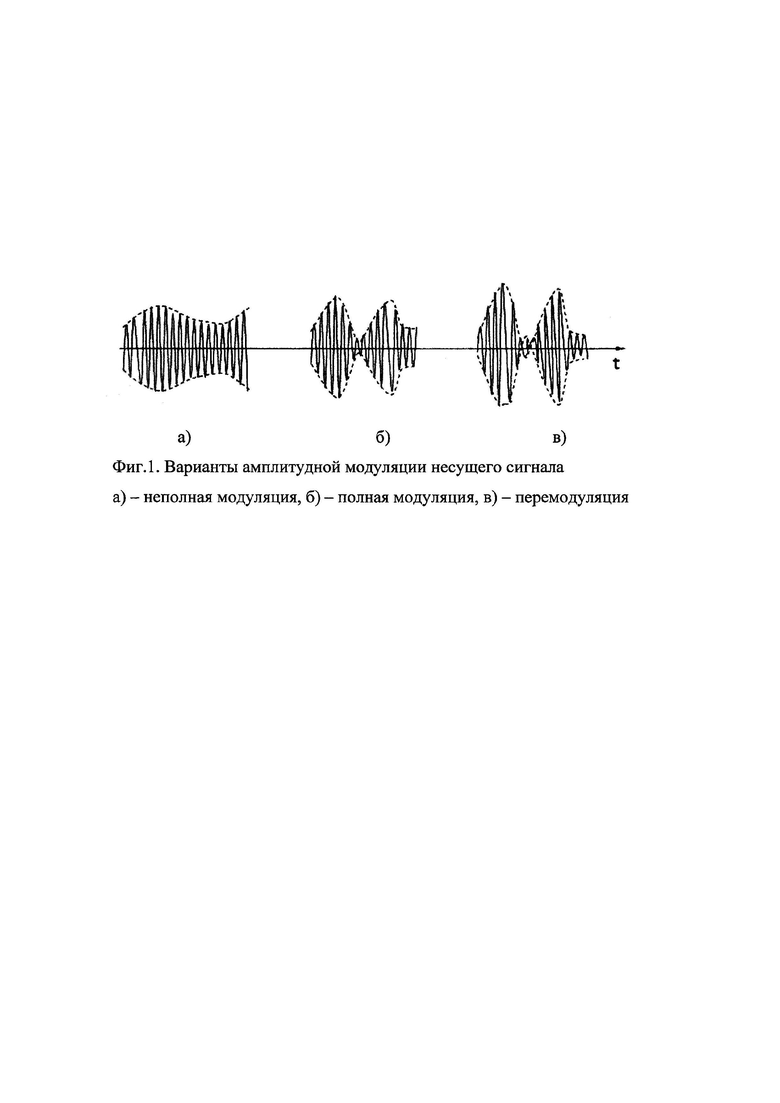
С другой стороны, для обеспечения компромисса между противоречивыми требованиями вышеперечисленных условий, предлагается использовать для питания ультразвукового излучателя амплитудно-модулированный сигнал, приближенный к импульсному режиму работы. Для упрощения вопроса реализации предлагаемого способа, была принята частота модуляции, кратная частоте сетевого питающего напряжения в 50 Гц. Такой режим работы, как показано на фиг. 1, обеспечивает возможность, с одной стороны, повысить пиковую амплитуду ультразвуковых колебаний почти в полтора раза, а с другой, обеспечить снижение теплового поверхностного эффекта при работе излучателя на кожный покров.
Особенность такого типа сигнала в том, что за счет комплексного эффекта двухчастотного воздействия, с одной стороны, обеспечивается глубокое проникновение его даже в неоднородную гетерогенную среду с незначительными отражениями и затуханием на границах сред, а с другой стороны, высокочастотная составляющая препятствует или, по крайней мере, существенно затрудняет, образование биопленок на поверхностях стента, что значительно повышает их резистентность к инкрустации солей.
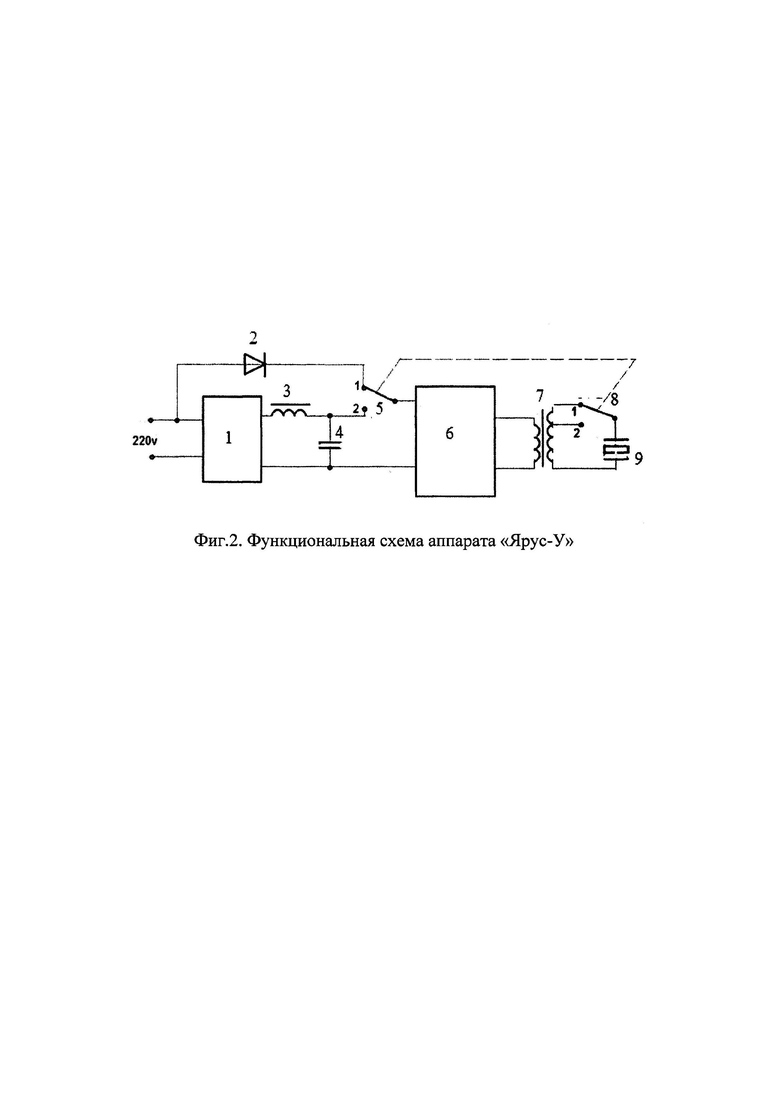
На фиг. 2 приведена функциональная схема устройства, позволяющая реализовать такой режим работы аппарата в целом.
Как следует из приведенной схемы, амплитудная модуляция выходного сигнала генератора обеспечивается по цепи питания высокочастотного генератора за счет запитывания его от обычного однополупериодного выпрямителя на диоде 2. Благодаря дополнительному переключателю 5 в режиме работы 1, силовой выпрямитель и сглаживающий фильтр 3-4 отключаются, и питающее напряжение поступает на вход высокочастотного инвертора 6 через диод 2. Одновременно срабатывающий переключатель 8 переводит выходной высокочастотный трансформатор в режим повышенной мощности, обеспечивая тем самым на пиках питающего напряжения увеличение амплитуды колебаний рабочего торца ультразвукового инструмента по сравнению с непрерывным режимом работы генератора.
С использованием разработанного оборудования были проведены исследования по оценке эффективности ультразвукового воздействия на стент мочеточника для уменьшения солевой обструкции и профилактики атаки обструктивного пиелонефрита, путем сравнения ультраструктур биопленок и гидродинамических показателей.
В исследование было включено 40 пациентов с уролитиазом, которым было выполнено стентирование стандартным «потоковым» стентом по ОМС для дренирования почки с целью профилактики обструктивного пиелонефрита. Продолжительность стояния стента у всех пациентов - один месяц. В течение всего месяца все больные амбулаторно получали назначенное лечение. Пациенты были разделены на 4 группы по 10 пациентов в каждой: группа 1 - получали только мочегонные травы или Фитолизин по стандартной схеме, группа 2 - получали мочегонные травы в сочетании с Роватинексом в дозировке по 2 капсулы 3 раза в день до еды, группа 3 - получали мочегонные травы в сочетании с ультразвуковым воздействием на проекцию стента и группа 4 - мочегонные травы, Роватинекс и ультразвуковое воздействие на проекцию стента. С помощью аппарата «Ярус-У» производилось озвучивание над проекцией стента в течение 15 минут 3 раза в неделю. Физические характеристики ультразвукового воздействия: частота - 26 КГц, мощность - 100-150 Вт, максимальная амплитуда в пике амплитудно-модулированного сигнала - 20 мкм. Оценивались: наличие атак обструктивного пиелонефрита, морфология удаленного через один месяц мочеточникового стента (диаметр просвета, протекаемость мл/мин, объемная скорость потока), наличие побочных эффектов. В лаборатории нанотехнологий оценивались ультраструктурная плотность и пластичность биопленки.
В течение месяца наблюдения: в группе 1 - три атаки пиелонефрита, в группе 2 - одна атака пиелонефрита, в группах 3 и 4 - атак пиелонефрита не наблюдали. Исследуя морфологию удаленного стента: лучшие физические параметры протекаемости были в 4 группе и несколько хуже в 3 группе. И на порядок хуже были показатели в 1 и 2 группах. При электронной микроскопии на стенде оценивались ультраструктурная плотность (Ultrastructuraldensity) с определением коэффициента UD-1 и коффициент пластичности DF (Ductilityfactor). На стентах, подвергшихся ультразвуковому озвучиванию, ультраструктурная плотность биопленки была значительно ниже, так же как и коэффициент пластичности, что свидетельствует о более слабых внутренних связях в ультраструктуре биопленки. Побочных эффектов от ультразвуковой терапии не наблюдали ни у одного пациента.
Таким образом, предложенный способ ультразвукового озвучивания над проекцией мочеточникового стента является дешевым, эффективным и безопасным способом уменьшения солевой обструкции и может быть рекомендован к применению в составе комплекса лечебных мероприятий, направленных на профилактику обструктивного пиелонефрита.
Литература.
1. Trapeznikova M.F., Dutov V.V., Rumyantsev A.A., et al. Choice of urinary tract drainage in different age groups of patients with urolithiasis. Urologiia. 2011; 2:3-7.
2. Wilson C.H., Rix D.A., Manas D.M. Routine intraoperative ureteric stenting for kidney transplant recipients. Cochrane Database Syst Rev. 2013; 6: CD004925.
3. Liatsikos E.N., Karnabatidis D., Katsanos K., et al. Ureteral metal stents: 10-year experience with malignant ureteral obstruction treatment. J. Urol. 2009; 182(6): 2613-2617.
4. Kogan M.I., Moisyuk Ja.G., Shkodkin S.V., et al. Effectiveness of ureteral stents with nanostructured coating in renal transplantation (preliminary results). Urologiia. 2015;1:58-61.
5. П.И. Шустер, А.А. Новиков, Я.Б. Шустер, О.Г. Новикова. Изменения ультраструктуры биопленок и гидродинамических показателей при неинвазивной ультразвуковой санации мочеточниковых стентов. В кн.: Материалы XVI Конгресса Российского Общества Урологов «Урология в XXI веке». Уфа, 20-22 октября 2016. С. 393.
| название | год | авторы | номер документа |
|---|---|---|---|
| УСТРОЙСТВО НЕИНВАЗИВНОЙ САНАЦИИ МОЧЕТОЧНИКОВЫХ СТЕНТОВ | 2018 |
|
RU2693002C1 |
| СПОСОБ АКУСТИЧЕСКОГО УДАРНО-ВОЛНОВОГО ВОЗДЕЙСТВИЯ НА БИОТКАНИ ЧЕЛОВЕКА | 2017 |
|
RU2683153C1 |
| Способ удаления стентов без цистоскопии у детей после реконструктивно-пластической операции на мочевом пузыре и устьях мочеточников | 2022 |
|
RU2796129C1 |
| Способ эндоскопического лечения больных нефролитиазом с применением альфа-адреноблокаторов | 2021 |
|
RU2779496C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ НОРМАЛЬНОЙ И СНИЖЕННОЙ СОКРАТИТЕЛЬНОЙ ФУНКЦИИ МОЧЕТОЧНИКА ПРИ ВРОЖДЕННОМ НЕРЕФЛЮКСИРУЮЩЕМ МЕГАУРЕТЕРЕ У ДЕТЕЙ | 2012 |
|
RU2483679C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ У ДЕТЕЙ С ОБСТРУКТИВНЫМИ УРОПАТИЯМИ | 2010 |
|
RU2427384C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ВАРИКОЗНОЙ БОЛЕЗНИ ВЕН НИЖНИХ КОНЕЧНОСТЕЙ У СОБАК | 2023 |
|
RU2823139C1 |
| Способ малоинвазивного лечения недержания мочи | 2015 |
|
RU2629717C2 |
| Способ прогнозирования течения острого гестационного пиелонефрита, обусловленного пузырно-мочеточниковым рефлюксом | 2021 |
|
RU2760885C1 |
| Способ оценки процесса ремоделирования паренхимы почки после разрешения обструкции при мочекаменной болезни | 2019 |
|
RU2735812C1 |
Изобретение относится к урологии и может быть использовано для неинвазивной санации мочеточниковых стентов. Осуществляют ультразвуковое озвучивание с поверхности тела над проекцией мочеточникового стента амплитудно-импульсным модулированным сигналом. Причем в качестве несущей частоты используют низкочастотную часть ультразвукового спектра 16-30 кГц. В качестве модулирующей частоты применяют частоту, кратную частоте сетевого питающего напряжения и сформированную на его основе Способ обеспечивает повышение эффективности неинвазивной санации мочеточниковых стентов, снижение их солевой обструкции за счет использования амплитудно-импульсного модулированного сигнала. 2 илл.
Способ неинвазивной санации мочеточниковых стентов путем ультразвукового озвучивания с поверхности тела над проекцией мочеточникового стента, отличающийся тем, что озвучивание осуществляют амплитудно-импульсным модулированным сигналом, причем в качестве несущей частоты используют низкочастотную часть ультразвукового спектра 16-30 кГц, а качестве модулирующей применяют частоту, кратную частоте сетевого питающего напряжения и сформированную на его основе.
| RU 2016110102 A, 13.11.2017 | |||
| Разводной гаечный ключ | 1930 |
|
SU20570A1 |
| US 7857766 B2, 28.12.2010 | |||
| ШКОДКИН С.В | |||
| и др | |||
| Рентгенофизиология сегментарного дренирования мочеточника в эксперименте | |||
| Курский научно-практический вестник "Человек и его здоровье" | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| NAAMA DROR et al | |||
| Advances in Microbial Biofilm Prevention on Indwelling Medical Devices with Emphasis on Usage of Acoustic Energy | |||
| Sensors | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2019-10-17—Публикация
2017-11-24—Подача