Изобретение относится к медицине, а именно к нейрохирургии, и может быть использовано при хирургическом лечении дефектов черепа после наложения фрезевого отверстия и проведения костно-пластической трепанации.
Показаниями к костно-пластической трепанации черепа являются опухоли мозга, последствия открытой и закрытой травмы черепа и головного мозга, абсцессы головного мозга, арахноидиты, гидроцефалия.
Целостное закрытие фрезевых отверстий важно не только для устранения косметических дефектов, но и для восстановления защитной функции черепа.
Основным лечебным показанием к закрытию дефекта черепа является необходимость герметизации полости черепа и защита головного мозга от внешних воздействий.
Учитывая увеличение количества и сложности хирургических вмешательств, выполняемых на головном мозге, необходима разработка простого и эффективного способа закрытия фрезевых отверстий.
Существуют разные способы закрытия фрезевых отверстий.
Известно устройство для краниопластики, которое состоит из пластины и не менее трех фиксирующих элементов, выполненных в виде шплинтов из пористого никелида титана, каждый из которых имеет уплощенную головку с шипами и трапециевидный стержень с расходящимся концом (Авторское свидетельство. №1655477, «Устройство для краниопластики», опубл. 15.06.91).
Недостатки заключаются в том, что устройство для краниопластики очень громоздкое по размерам, в данном устройстве применяются два материала никелид-титан и самотвердеющая пластмасса, трансплантат из самотвердеющей пластмассы не обладает биоинертностью и, как следствие, происходит отторжение трансплантата. При этом для фиксации устройства необходимо дополнительно формировать отверстия со стороны костей свода черепа для фиксации трансплантата.
Существуют различные фиксаторы для закрепления эндопротезов, закрывающих дефекты костей черепа, выполненные из металла с памятью формы: омегообразные, S-образные, волнообразные скобки (Патент РФ №2133113, опубл. 20.07.1999).
Недостатки:
- при установке указанных скоб, возможно смещение трансплантата в сторону места фиксации устройства;
- не создает надежной фиксации и не предотвращается возможное смещение трансплантата в направлении полости черепа;
- значительная толщина указанных скобок иногда создает видимость нахождения инородного тела под кожными покровами головы пациента, что уменьшает косметические свойства операции;
- указанные фиксаторы не заполняют пространство (промежуток) между костным трансплантатом и краем костного дефекта свода черепа, который был ранее выпилен пилкой Джигли;
- фиксация трансплантата к донорскому участку происходит только с одной - наружной стороны, что не создает достаточную прочность и неподвижность трансплантата;
- для установки указанных фиксаторов необходимо произвести дополнительные отверстия в трансплантате и по периметру костного дефекта.
Известны способы закрытия фрезевых отверстий путем заполнения их костной стружкой пациента, смешанной с кровью (Авторское свидетельство SU №1222249, «Способ костно-пластической трепанации черепа у детей» Казахский НИИ педиатрии и детской хирургии, опубл 20.07.1999), и смешанной с кровью и физиологичесим раствором (Method for cranial bone
reconstruction, Danaila Leon, appl.26.02.1997, №appl. RO019970000367, publ. 02.27.1998).
Применение вышеуказанных методик в детском возрасте оправдано, покольку существует риск миграции трансплантата во время роста из нерезорбируемого материала в том числе и эпидурально. Данные осложнения в части случаев приводят к повторным операциям.
Недостатком методики является резорбция костной стружки, примерно в 20%-40% случаев. В большинстве случаев костная стружка постепенно замещается соединительной тканью, образование кости, как правило, не происходит.
Также известен способ пластики фрезевых отверстий черепа аутотрансплантатом (Авторское свидетельство SU №1097291, Киевский НИИ нейрохирургии, опубл. 15.06.1984). Наложение фрезевого отверстия проводится корончатой фрезой с образованием костного уступа шириной 2-3 мм. После проведения манипуляций, аутотрансплантант укладывается во фрезевое отверстие и расклинивается штифтом, выкушенным из аутотрансплантата.
При использовании корончатой фрезы существует вероятность повреждения твердой мозговой оболочки, какие-либо ограничители глубины пропила не предусмотрены. Методика технологически не удобна и несовершенна, поскольку необходимо пропилить кость не полностью, извлечь выпиленный фрагмент и сформировать костный уступ.
К недостаткам методики относится высокая вероятность резорбции аутокости, ограниченный контакт аутотрансплантата и костей черепа. Это приводит к снижению вероятности остеоинтеграции и сращения с костями черепа.
Наиболее близким способом (Патент US2012283771 (А1) - 2012-11-08) закрытия фрезевого отверстия является использование биодеградируемых имплантатов изготовленных из материалов, таких как коллаген, полигликолид, сополимеры молочной кислоты и гликолевой кислоты, поли-L-лактид, поли-L-молочную кислоту, кристаллические полимеры. Срок биологической деградации таких материалов варьирует от 3 до 6 месяцев. На боковой части имплантатат предусмотрены распорные элементы, которые должны удерживать имплантатат в отверстии. Распорные элементы изготавливаются разных размеров для универсальности и возможности использовать имплантат в отверстиях разного диаметра. Имплантат изготавливается гибким и в зоне контакта с костью имеется перфорация для улучшения остеоинтеграции. Предусмотрена возможность использовать различные биологически активные субстанции для улучшения осеоинтеграции.
Недостатком методики можно считать развитие гранулем в послеоперационном периоде, которое встречается примерно в 10% случаев. Это происходит в результате индивидуальной реакции на биологическую деградацию и ферментативный гидролиза трансплантата. Материал подвергающийся гидролизу, нельзя назвать биологически инертным. При развитии гранулемы появляется отек мягких тканей, болезненность и покраснение кожи. Данные явления регрессируют примерно через 12 месяцев. Резорбируемые материалы в основном используют у детей, где существенно выше регенераторный потенциал и имеется потенциал роста. У взрослых не доказано, что после резорбции имплантат заместится костной тканью. Соответственно останется фрезевое отверстие, которое в известной степени закроется соединительной тканью.
Таким образом, проблема пластики фрезевого отверстия черепа по-прежнему остается актуальной.
Задачей изобретения является разработка эффективного и безопасного способа целостного закрытия фрезевого отверстия после трепанации черепа или после диагностического доступа.
Предлагается способ закрытия фрезевого отверстия с использованием имплантата из пористого никелида титана, с процентным содержанием Ni-55%, Ti-45%. Материал длительно используется в травматологии, успешно используется свойство «память формы», обладает биологической инертностью и является идеальным материалом для создания биологически и механически совместимых с организмом человека имплантатов. Никелид титана не является ферромагнетиком, не наносит вреда пациентам, практически не искажает магнитно-резонансный эффект при выполнении МРТ и КТ головного мозга и биоэлектрическую активность головного мозга. Микропористость имплантата достигается благодаря спеканию порошка никелида титана в керамических формах при температуре около 1700 градусов. По структуре он напоминает губчатую костную ткань. Имеет открытую сквозную пористую структуру, близкую к структуре пор костной ткани: пористость 40-70% с размером пор, оптимальным для врастания тканевых элементов. Поры и пространство в имплантате легко заполняются костными тканями. Имплантат выполнен перфорированным с целью улучшения остеоинтеграции.
Проведено исследование толщины теменной, затылочной и лобной костей на 20 паспортизированных черепах. В ходе анатомического исследования выяснено, что средняя толщина костей в зоне наиболее частого наложения фрезевых отверстий составляет: лобной кости 4.5 мм, теменной кости 6 мм, затылочной кости 5 мм. Учитывая экспериментальные данные, целесообразно использовать никелид титановые микропористые имплантаты выполненные в виде дисков, толщиной 3-5 мм. и диаметром 10 мм.
В пористые края имплантата втирается стерилизованная костная стружка пациента, с добавлением плазмы крови, обогащенной тромбоцитами, а затем имплантат плотно помещается во фрезевое отверстие, за счет неровной шероховатой структуры имплантат надежно и плотно фиксируется внутри фрезевого отверстия.
Способ осуществляют следующим образом.
Накладывают фрезевое отверстие. Костную стружку собирают на этапе формирования костного доступа и стерилизуют в сухожаровом шкафу.
После проведения трепанации в случае использования пилы Джигли остается 4-5 фрезевых отверстий, при использовании автоматических трепанов 1 фрезевое отверстие. Указанные отверстия представляют собой дефекты кости круглой формы 12 мм диаметром. Дефекты видны на конвекситальной поверхности свода черепа.
Затем имплантат из пористого никелида титана диаметром 10 мм и толщиной 3-5 мм, в зависимости от толщины кости свода черепа, примеряют к фрезевому отверстию. При проведении хирургической операции имеются имплантаты разной толщины. Предварительно имплантат стерилизуют автоклавированием при стандартных температурных режимах.
При проведении операции проводят подготовку плазмы обогащенной тромбоцитами по следующей методике. Методика предусматривает 2-х этапное центрифугирование.
1 этап: центрифугирование 3600 оборотов в минуту 4 минуты, перерыв 2 минуты.
2 этап: центрифугирование 3600 оборотов в минуту 2 минуты. Далее шприцом набирают слой плазмы обогащенной тромбоцитами.
В боковую контактную пористую поверхность имплантата втирают костную стружку, в которую добавлена плазма крови, обогащенная тромбоцитами.
Во фрезевое отверстие на твердую мозговую оболочку помещают гемостатическую губку, сверху имплантат. Затем мягкие ткани ушивают отдельными швами послойно.
За счет неровной шероховатой структуры поверхности имплантат из никелида титана надежно и плотно фиксируется внутри фрезевого отверстия. А благодаря тому, что предварительно в контактную поверхность втирается костная стружка с добавлением плазмы крови, обогащенной тромбоцитами, увеличивается скорость остеоинтеграции. Это подтверждено экспериментальными данными. Формирование рубцов, сращений с твердой мозговой оболочкой и развитие послеоперационной ликвореи профилактируется использованием защитного слоя из гемостатической губки. Также остеоинтеграция ускоряется за счет использования in-lay техники установки имплантата. In-lay техника реализуется путем вкладывания имплантата во фрезевое отверстие таким образом, чтобы имплантат и поверхности черепа находились на одном уровне без ступеньки. Только в этом случае пористая поверхность имплантата максимально контактирует с губчатой костью черепа.
Техническим результатом применения предлагаемого способа является достижение полного восстановления целостности и защитной функции черепа. За счет использования бионертного материала исключается токсическое воздействие, отторжение имплантата, нагноение и возникновение других осложнений. За счет применения гемостатической губки снижается уровень ликвореи и профилактируется образование рубцов и сращений с твердой мозговой оболочкой. Преимуществом является также то, что благодаря шероховатой боковой поверхности краев имплантата и втиранию костной стружки удается получить жесткую фиксацию и максимальный контакт имплантата с костью черепа. А за счет пористости имплантата достигается прорастание имплантата костью уже на 40-й день эксперимента в 100% случаев.
При этом применение данной методики не увеличивает время операции, так как костная стружка собирается на этапе формирования костного доступа, а имплантаты разной толщины легко доступны для использования хирургом в необходимых количествах и не требуют сложной и продолжительной подготовки к использованию.
Кроме того при использовании предлагаемого способа устраняются косметические дефекты, что благоприятно влияет на качество жизни пациента и существенно снижается риск послеоперационной ликвореи.
При экспериментальных операциях по пластике дефекта черепа у кроликов с помощью пористого никелида титана, выяснено, что дефект черепа в диаметре 10 мм при средней толщине кости 0.9 мм при использовании in-lay техники, полностью зарастает на 24-й день в 50% наблюдений и на 40-й день в 100% наблюдений.
Краткое описание рисунков.
На фото показано проведение экспериментальной трепанации у кролика (Фиг. 1).
В результате проведения краниопластики установлен экспериментальный имплантат из пористого никелида титана (Фиг. 2).
Взятие гистологиии на 24-й день после краниопластики (Фиг. 3).
Виден экспериментальный имплантат из пористого никелида титана, обрастающий костью.
Взятие гистологии на 40-й день после краниопластики (Фиг. 4). Стрелкой указано место экспериментальной трепанации, закрытой пористым имплантатом. Экспериментальный имплант из пористого никелида титана полностью обрастает костью.
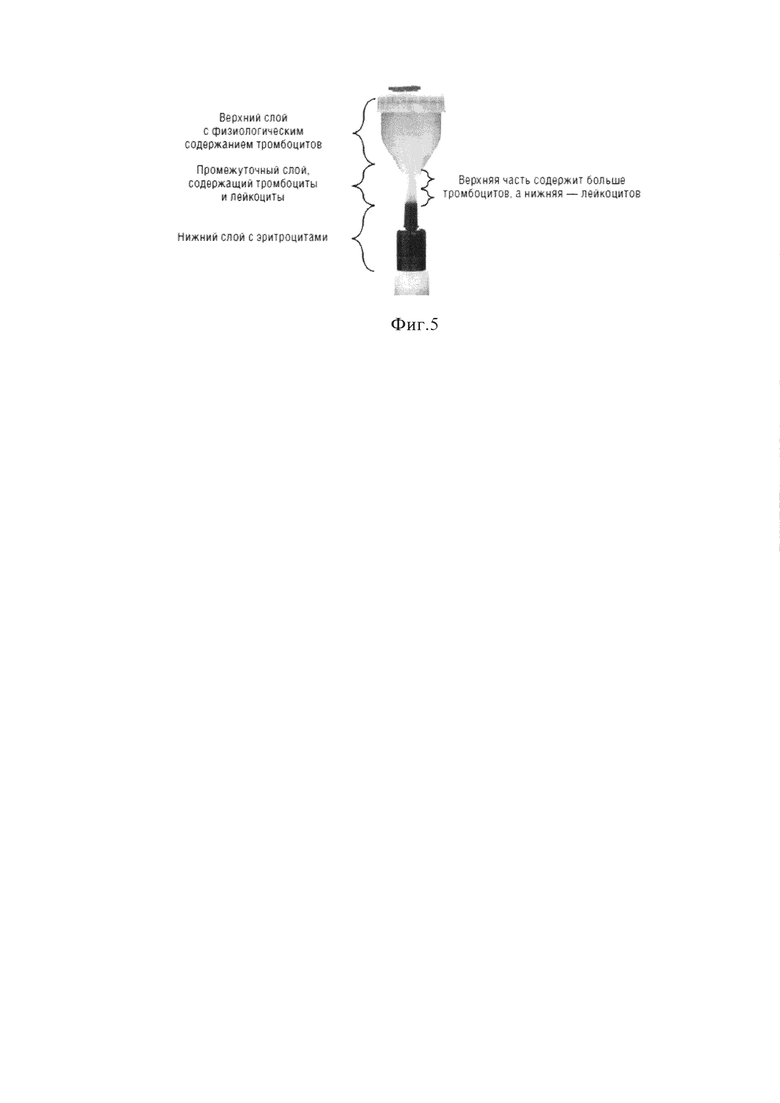
Пробирка с PRP плазмой после центрифугирования. (Фиг. 5)
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КРАНИОПЛАСТИКИ | 2004 |
|
RU2279252C2 |
| Способ обработки вдавленного перелома костей черепа у детей по Пшеничному А.А. | 2017 |
|
RU2683067C1 |
| Способ устранения дефектов и деформаций нижней челюсти | 2018 |
|
RU2734756C2 |
| Способ створчатой трепанации черепа | 2017 |
|
RU2640996C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПРИ ОБШИРНОЙ ГЕМАТОМЕ В ПОЛОСТИ ЧЕРЕПА | 2008 |
|
RU2376939C1 |
| Способ реконструктивной операции при вдавленном переломе костей свода черепа | 2023 |
|
RU2821664C1 |
| ДЕРЖАТЕЛЬ ДЛЯ КОСТНОГО ТРАНСПЛАНТАТА | 2012 |
|
RU2487679C1 |
| СПОСОБ ХРАНЕНИЯ КОСТНОГО ТРАНСПЛАНТАТА ДЛЯ КРАНИОПЛАСТИКИ | 2004 |
|
RU2279253C2 |
| СПОСОБ ПЛАСТИКИ КОСТНОГО ДЕФЕКТА ОСНОВАНИЯ ЧЕРЕПА | 2019 |
|
RU2722406C1 |
| БИОИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ ЗАКРЫТИЯ КОСТНЫХ ДЕФЕКТОВ С ВОССТАНОВЛЕНИЕМ В НИХ КОСТНОЙ ТКАНИ И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОЙ КОНСТРУКЦИИ | 2009 |
|
RU2416434C1 |


Изобретение относится к медицине, а именно к нейрохирургии, и может быть использовано при хирургическом лечении дефектов черепа. На твердую мозговую оболочку укладывают гемостатическую губку. Затем в контактный пористый край дисковидного имплантата втирают костную стружку, смешанную с плазмой крови, обогащенной тромбоцитами. После достижения гемостаза имплантат из пористого никелида титана плотно вводят во фрезевое отверстие черепа. Мягкие ткани ушивают послойно. Изобретение обеспечивает полное восстановление целостности и защитной функции черепа, снижение уровня ликвореи и профилактику образования рубцов и сращений с твердой мозговой оболочкой, жесткую фиксацию имплантата во фрезевом отверстии, ускорение остеоинтеграции, исключение токсического воздействия, отторжения имплантата, нагноения и возникновения других послеоперационных осложнений. 5 ил.
Способ закрытия фрезевого отверстия черепа, включающий введение во фрезевое отверстие имплантата из пористого никелида титана, отличающийся тем, что на твердую мозговую оболочку укладывается гемостатическая губка, затем в контактный пористый край дисковидного имплантата втирают костную стружку, смешанную с плазмой крови, обогащенной тромбоцитами, и после достижения гемостаза имплантат плотно вводят во фрезевое отверстие; после этого мягкие ткани ушивают послойно.
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Роторный двигатель внутреннего сгорания | 1960 |
|
SU131592A1 |
| Устройство для краниопластики | 1985 |
|
SU1655477A1 |
| ОСТРОВЕРХОВ Г.Е | |||
| и др | |||
| Оперативная хирургия и топографическая анатомия: Учебник для студентов медицинских вузов | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| - М.: ООО "Медицинское информационное агентство", 2015, с | |||
| Чемодан с сигнальным замком | 1922 |
|
SU338A1 |
| JAZAYERI MA et al | |||
| Comparison of various delivery systems for | |||
Авторы
Даты
2019-11-14—Публикация
2019-03-13—Подача