Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения фторзамещенного органического алифатического соединения и к способу очистки фторзамещенного органического алифатического соединения. В частности, настоящее изобретение относится к способу получения фторзамещенного органического алифатического соединения с использованием нового многофункционального растворителя и к способу очистки фторзамещенного органического алифатического соединения с использованием твердофазной экстракции (ТФЭ). Кроме того, настоящее изобретение относится к способу получения радиофармацевтических препаратов с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости.
Уровень техники
Развитие современной цивилизации ведет к повышению качества жизни, а развитие медицинской науки ведет к увеличению продолжительности жизни. С другой стороны, все большее распространение стали получать болезни головного мозга, такие как болезнь Паркинсона, депрессивное расстройство, шизофрения и болезнь Альцгеймера; болезни сердца, вызванные стрессом и нарушением режима питания; и различные виды рака, вызванные воздействием на организм человека вредных материалов. Таким образом, возникла потребность в разработке метода визуальной диагностики, пригодной для диагностирования подобных болезней на ранних стадиях.
Существует несколько методов визуальной диагностики. В частности, непосредственно применимым в клинических условиях методом является позитронно-эмиссионная томография (ПЭТ), которая позволяет визуализировать процесс распределения и биохимического изменения радиофармацевтического препарата in vivo путем внутривенной инъекции органического соединения, меченного радиоактивным изотопом, который излучает позитроны в организм человека. Следовательно, с помощью подобной позитронно-эмиссионной томографии можно проводить количественное определение биохимического изменения в очаге поражения внутри организма человека и таким образом установить степень прогрессирования болезни и предсказать уровень лечебного воздействия (A. Agool, R.H. Slart, K.K. Thorp, A.W. Glaudemans, D.C. Cobben, L.B. Been, F.R. Burlage, P.H. Elsinga, R.A. Dierckx, E. Vellenga, J.L. Holter, Nucl. Med. Commun. 2011, 32, 14.; N. Aide, K. Kinross, C. Cullinane, P. Roselt, K. Waldeck. O.Neels, D. Dorow, G. McArthur, R.J. Hicks, J. Nucl. Med. 2011, 51, 1559.; A. Debucquoy, E. Devos, P. Vermaelen, W. Landuyt, S. De Weer, F. Van Den Heuvel, K. Haustermans, Int. J. Radiat. Biol. 2009, 85, 763.).
Радиофармацевтический препарат представляет собой материал, вводимый в организм человека после мечения радиоактивным изотопом и предназначенный для диагностирования или лечения болезней. Радиоактивный изотоп, используемый для подобного радиофармацевтического препарата, нестабилен и превращается в стабильный изотоп, испуская радиационное излучение. Испускаемое при распаде излучение можно использовать для диагностики и лечения болезней. Испускаемое радиационное излучение может быть альфа-излучением (α-лучами), бета-излучением (β-лучами), гамма-излучением (γ-лучами), позитронным излучением (β+-лучами) или другими видами излучения. При этом для позитронно-эмиссионной томографии используют фтор ([18F] F), углерод ([15С] С), азот ([13N] N), кислород ([15O] О), галлий ([68Ga] Ga) и другие радиоактивные изотопы. Среди этих радиоактивных изотопов [18F] фторид сходен по размеру с водородом, образует прочную связь с атомом углерода в органических соединениях, его легко получать, и он обладает подходящим периодом полураспада (110 минут). Таким образом, его считают вполне подходящим для использования в позитронно-эмиссионной томографии (Lasne, М.С.; Perrio, С.; Rouden, J.; Barre, L.; Roeda, D.; Dolle, F.; Crouzel, C. Contrast Agents II, Topics in Current Chemistry, Springer-Verlag, Berlin, 2002, 222, 201-258.; Bolton, R. J. Labeled Compd. Radiopharm. 2002, 45 485-528).
Для образования [18F] фторида используют циклотрон, который представляет собой циклический коллайдер и обычно используется для излучения позитронов в [18O] H2O (M.R. Kilbourn, J.T. Hood, M.J. Welch, Int. J. Appl. Radiat. Isot. 1984, 35, 599.; G.K. Mulholland, R.D. Hichwa, M.R. Kilbourn, J. Moskwa, J. Label. Compd. Radiopharm. 1989, 26, 140.). Обычно [18F] фторид получают в виде раствора в [18O] H2O с очень низкой концентрацией. Кроме того, его раствор в [18O] H2O стоит очень дорого, поэтому его подвергают рециркуляции и повторному использованию (K. -I, Nishijima, Y. Kuge, Е. Tsukamoto, K.-I. Seki, К. Ohkura, Y. Magata, A. Tanaka, K. Nagatsu, N. Tamaki. Appl. Radiat. Isot. 2002, 57, 43; D. Schoeller, Obes. Res. 1999, 7, 519.; SNM Newsline, J. Nucl. Med. 1991, 32, 15N).
Чтобы удалить небольшое количество металлических примесей, попадающих во время рециркуляции вышеупомянутой [18O] H2O и образования [18F] фторида, и обеспечить использование только [18F] фторида при проведении реакции мечения, обычно используют метод анионного обмена с четвертичной алкиламмониевой солью, нанесенной на полимерный картридж (Chromafixor QMA) в качестве носителя (D.J. Schlyer, М. Bastos, A.P. Wolf, J. Nucl. Med. 1987, 28, 764.; S.A. Toorongian, G.K. Mulholland, D.M. Jewett, M.A. Bachelor, M.R. Kilbourn, Nucl. Med. Biol. 1990, 17, 273.; D.M. Jewett, S.A. Toorongian, G.K. Mulholland, G.L. Watkins, M.R. Kilbourn, Appl. Radiat. Isot. 1988, 39, 1109.; G.K. Mulholland, R.D.T.J. Mangner, D.M. Jewett, M.R. Kilbourn, J. Label. Compd. Radiopharm. 1989, 26, 378.; K. Ohsaki, Y. Endo, S. Yamazaki, M. Tomoi, R. Iwata, Appl. Radiat. Isot. 1998, 49, 373-378.).
Для элюирования [18F] фторида, удерживаемого четвертичной алкиламмониевой солью, нанесенной на полимерный картридж, используют соль металла, такую как K2CO3, или водный раствор аммониевой соли, такой как ТВАНСО3 (гидрокарбонат тетрабутиламмония). Из-за основности используемых для элюирования солей протекают такие побочные реакции, как взаимодействие со спиртом или образование алкена, приводящие к нежелательному снижению эффективности мечения. Кроме того, при использовании ЖХВР (жидкостной хроматографии высокого разрешения) для очистки полученного 18-фторорганического соединения может наблюдаться перекрытие со сложным побочным продуктом, являющимся слабым источником неионизируюшего излучения (S.M. Okarvi, Eur. J. Nucl. Med. 2001, 28, 929.; J.C. Walsh, K.M. Akhoon, N. Satyamurthy, J.R. Barrio, M.M. Phelps, S.S. Gambhir, T. Toyokuni, J. Label. Compds. Radiopharm. 1999, 42, S1.; L. Lang, W.C. Eckelman, Appl. Radiat. Isot. 1994, 45, 1155.; L. Lang, W.C. Eckelman, Appl. Radiat. Isot. 1997, 48, 169.).
Как известно, реакцию нуклеофильного замещения обычно проводят в присутствии полярного апротонного растворителя, такого как ацетонитрил (CH3CN), диметилформамид (DMF) или диметилсульфоксид (DMSO), способного повышать реакционную способность нуклеофила, т.е. фторида. С другой стороны, согласно недавнему отчету, спиртовой растворитель ослабляет ионную связь между катионом металла и фтор-анионом из-за образования водородной связи с солью фтора, повышая реакционную способность соли фтора в реакциях нуклеофильного замещения, понижая основность оснований, используемых при проведении реакции мечения [18F] фторида, и тем самым ингибируя побочные реакции (D.W Kim, D.S. Ahn, Y.H. Oh, S. Lee, H.S. Kil, S.J. Oh, S.J. Lee, J.S. Kim, J.S. Ryu, D.H. Moon, D.Y. Chi. J. Am. Chem. Soc. 2006, 128, 16394.; S.J. Lee, S.J. Oh, D.Y. Chi, H.S. Kil, E.N. Kim, J.S. Ryu, D.H. Moon, Eur. J. Nucl. Med. Mol. Imaging. 2007, 34, 1406.).
Вышеупомянутая проблема повышает расход прекурсора из-за использования основания при мечении. Для решения этой проблемы можно использовать способ мечения органического соединения [18F] фторидом с использованием в качестве реакционной среды третичного спирта, способного понижать основность основания и ограничивать расход прекурсора. Однако трет-бутанол, который является самым простым представителем подобных третичных спиртов, имеет низкую температуру кипения, составляющую 83°С, а следовательно, не позволяет повышать температуру реакции. Другой представитель подобных третичных спиртов, трет-амиловый спирт имеет более высокую температуру кипения, составляющую около 100°С. Однако трет-амиловый спирт нельзя считать оптимальным растворителем, применимым в качестве реакционный среды, с точки зрения температуры кипения, поскольку реакцию мечения [18F] фторидом проводят при температуре 100°С или при более высокой температуре.
Кроме того, трет-амиловый спирт не смешивается с водой. После проведения реакции мечения [l8F] фторидом спиртовой растворитель следует удалить в том случае, если необходимо провести процесс гидролиза и процесс очистки с использованием жидкостной хроматографии высокого разрешения (ЖХВР) или твердофазной экстракции (ТФЭ). Если растворитель удален не полностью, то он может смешиваться с примесями в процессе очистки.
Обычно спиртовой растворитель, используемый в качестве реакционной среды, удаляют путем выпаривания. Но поскольку такой процесс занимает много времени, то фактический выход реакции снижается из-за спада радиоактивности, обусловленного периодом полураспада радиоактивного изотопа, используемого для мечения, когда радиоактивный изотоп имеет относительно короткий период полураспада. Кроме того, в этом случае при испарении радиоактивного изотопа вместе с органическим растворителем возникает проблема загрязнения окружающей среды. А при многократном использовании трет-амилового спирта в системе автоматического синтеза та часть системы, которая не обладает стойкостью к трет-амиловому спирту, может быть повреждена при его испарении, что приводит к нарушению процесса изготовления радиофармацевтического препарата.
Между тем, чтобы защитить работников от радиоактивного излучения в процессе изготовления радиофармацевтического препарата, используют систему автоматического синтеза, расположенную в экранированном свинцом пространстве, называемом горячей камерой, и подобные системы автоматического синтеза можно разделить на системы бескассетного типа (TracerLab FXFN, GE Healthcare, Modular Lab, E & Z и др.) и системы кассетного типа (TracerLab MX, GE Healthcare, FastLab, GE Healthcare, AIO module, Trasis и др.).
Системы автоматического синтеза бескассетного типа используют в основном для проведения исследований и они неудобны тем, что нуждаются в промывке после каждого использования. В системе автоматического синтеза кассетного типа используются сменные кассеты и она не нуждается в дополнительной промывке. Кроме того, проводя смену кассет, можно использовать систему автоматического синтеза кассетного типа несколько раз в сутки. Прежде всего, система автоматического синтеза кассетного типа соответствует правилам надлежащей производственной практики (GMP). Поэтому в случае радиофармацевтического препарата, нуждающегося в частом изготовлении, предпочтительно использовать систему автоматического синтеза кассетного типа, а не систему автоматического синтеза бескассетного типа.
Но чтобы можно было использовать подобную автоматизированную систему синтеза кассетного типа, условия, при которых изготавливают требуемый радиофармацевтический препарат, а именно, вид реакционной среды, температура реакции, продолжительность реакции и другие параметры, должны быть подходящими для кассеты. В противном случае кассета может повреждаться в процессе изготовления радиофармацевтического препарата и это может приводить к нарушению процесса изготовления радиофармацевтического препарата.
Реакционный контейнер 10а (см. поз. А на фиг. 2), установленный в кассету автоматизированной системы синтеза кассетного типа, содержит трубку 11а подачи реагентов, используемую для извлечения реагентов после завершения реакции. Обычно трубка подачи реагентов доходит до дна реакционного контейнера 10а, что позволяет увеличить коэффициент извлечения реагентов (см. поз. А на фиг. 2). Кроме того, дно может иметь закругленную или V-образную форму, чтобы еще более увеличить коэффициент извлечения реагентов. Когда температура внутри реакционного контейнера 10а повышается и раствор испаряется настолько, что в реакционном контейнере 10а создается повышенное давление, реакционная среда подвергается противоточному движению в трубку 11a подачи реагентов, доходящую до дна. В результате кассета, присоединенная к другому концу трубки 11а подачи реагентов, заполняется растворителем, используемым в качестве реакционной среды, во время реакции. Причем, если кассета изготовлена из нестойкого к растворителю материала или если реакция протекает при температуре, значительно превышающей температуру кипения растворителя, кассета разрушается под действием возникшего давления, что может привести к нарушению процесса изготовления радиофармацевтического препарата. Кроме того, раствор, совершающий противоточное движение в трубку 11а подачи реагентов, не участвует в реакции, так что в реакцию вступают не все реагенты, что приводит к большому колебанию выхода продукта реакции. Это не позволяет добиться стабильного выхода продукта реакции. В результате не удается получать радиофармацевтический препарат, отвечающий требованиям GMP.
За границей для решения вышеупомянутых проблем разработаны кассеты из материала, обладающего стойкостью к различным растворителям. Кассеты, изготовленные из подобного нового материала, слишком дороги, чтобы использовать их однократно. Таким образом, экономически невыгодно использовать такие кассеты одноразового использования в большом количестве. Согласно другому способу на трубку, по которой происходит противоточное движения жидкости из реактора, устанавливают запорный клапан, чтобы раствор не мог попасть в кассету. Однако этим способом не удается полностью устранить явление противоточного движения жидкости, и он является всего лишь временным средством, не позволяющим совершающему противоточное движение раствору попасть в кассету.
Кроме того, в таком реакционном контейнере 10а, где трубка 11а подачи реагентов доходит до дна реакционного контейнера 10а (см. поз. А на фиг. 2), реагенты разбрызгиваются по стенкам реакционного контейнера 10а из-за высокой скорости подачи реагентов по трубке 11а подачи реагентов. Кроме того, во время получения радиофармацевтического препарата, меченного F-18, проводят выпаривание, чтобы обеспечить реакционную способность F-18 после его элюирования из анионообменного картриджа. Во время выпаривания, когда по той же трубке подают азот, он поступает в раствор, содержащийся в реакционном контейнере 10а, и вызывает образование пузырьков. Поэтому при проведении выпаривания реагенты разбрызгиваются по стенкам реакционного контейнера. Когда раствор, содержащий прекурсор, поступает обратно в реакционный контейнер 10а по трубке 11а подачи реагентов после выпаривания F-18, прекурсор тоже разбрызгивается по стенкам реакционного контейнера 10а. Таким образом, участие во взаимодействии разбрызганных по стенкам реагентов всякий раз меняется, что приводит к изменению выхода радиофармацевтического препарата. В частности, в случае радиофармацевтического препарата, чувствительного к количеству реагентов, происходит не только изменение выхода, но часто вовсе нарушается процесс изготовления. В результате, добиться стабильного изготовления радиофармацевтического препарата оказывается трудно.
Раскрытие изобретения
Техническая проблема
Технической проблемой, которую призвано решить настоящее изобретение, является создание способа изготовления фторзамещенного органического алифатического соединения с использованием нового многофункционального растворителя. В частности, целью настоящего изобретения является создание способа получения органического фторзамещенного алифатического соединения с использованием многофункционального растворителя, имеющего функциональную группу, способную повысить эффективность мечения радиоактивным изотопом, и функциональную группу, способную повысить эффективность очистки, и тем самым устранить вышеупомянутые проблемы, возникающие при использовании полярного апротонного растворителя и полярного протонного растворителя при мечении радиоактивным изотопом.
Другой технической проблемой, которую призвано решить настоящее изобретение, является создание способа эффективной очистки фторзамещенного органического алифатического соединения путем проведения твердофазной экстракции (ТФЭ) с использованием ионообменного ТФЭ картриджа.
Еще одной технической проблемой, которую призвано решить настоящее изобретение, является создание способа изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости. В частности, целью настоящего изобретения является создание способа изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, который позволяет стабильно подавать в реакционный контейнер реагент, используемый для изготовления радиофармацевтического препарата, в количестве, предназначенном для участия в реакции.
И еще одной технической проблемой, которую призвано решить настоящее изобретение, является создание способа изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, который предотвращает противоточное движение реакционной среды из-за испарения растворителя или по какой-либо иной причине во время проведения мечения при высокой температуре, чтобы исключить повреждение кассеты и чтобы весь растворитель мог участвовать в реакции.
Техническое решение
В соответствии с одним аспектом настоящего изобретения предлагается способ изготовления фторзамещенного органического алифатического соединения, включающий в себя стадию обеспечения взаимодействия алифатического соединения, содержащего замещаемую группу, с солью фтора в многофункциональном растворителе, имеющем химическую формулу 1, с получением алифатического соединения, меченого [18F] фторидом, присоединенным вместо замещаемой группы:
(химическая формула 1)

где каждая из групп R1 и R2 независимо друг от друга представляет собой Н, C1-C10-алкильную группу или ту же функциональную группу, что и группа X1; группа Ln представляет собой C1-C10-алкильную группу или полиэтиленгликолевую группу СН2(ОСН2СН2)n, где n является целым числом в диапазоне 1-10; группа X1 представляет собой полярную группу, выбранную из следующего: алкоксильная группа (OR3), нитрильная группа (CN) и галоид, а группа R3 представляет собой C1-C10-алкильную группу.
Предпочтительно Ln может являться C1-C3-алкильной группой или полиэтиленгликолевой группой СН2(OCH2CH2)n, где n является целым числом в диапазоне 1-3.
Алкоксильная группа (OR3) может содержать любое из следующего: метокси-группа, этоксигруппа, пропоксигруппа, изопропоксигруппа и трет-бутоксигруппа.
Галоид может содержать любое из следующего: хлорид (Cl), бромид (Br) и йодид (I).
Предпочтительно каждая из групп R1 и R2 может содержать метальную группу или этильную группу.
Многофункциональный растворитель, имеющий химическую формулу 1, может содержать любое из следующего: 1-метокси-2-метил-2-пропанол, 1-этокси-2-метил-2-пропанол, 1-пропокси-2-метил-2-пропанол, 1-изопропокси-2-метил-2-пропанол, 1-трет-бутокси-2-метил-2-пропанол, 1-нитрил-2-метил-2-пропанол, 1-хлор-2-метил-2-пропанол, 1-бром-2-метил-2-пропа- нол, 1-йод-2-метил-2-пропанол, 1-(2-метоксиэтокси)-2-метил-2-пропанол и 3-(метоксиметил)-3-пентанол.
Соль фтора, используемая в качестве источника [18F] фторида, может представлять собой соединение, содержащее фтор-18.
Алифатическое соединение может являться соединением, содержащим алкилгалоидную группу или алкилсульфонатную группу, причем галоидная группа или сульфонатная группа является замещаемой группой.
Алифатическое соединение может представлять собой соединение, содержащее алкилгалоидную группу или алкилсульфонатную группу, причем галоидная группа или сульфонатная группа представляет собой первичную замещаемую группу или вторичную замещаемую группу.
Алифатическое соединение может иметь формулу N-(CH2)n-X2 или O-(СН2)n-X2, где группа X2 представляет собой замещаемую группу, а n является целым числом в диапазоне 1-10.
Группа Х2 может являться галоидной группой или сульфонатной группой.
Галоидная группа может быть выбрана из группы, состоящей из следующего: Cl, Br и I.
Сульфонатная группа может иметь формулу -SO3R12 (где группа R12 выбрана из следующего: C1-C12-алкил, C1-C12-алкилгалоид, фенил, C1-C4-алкилфенил, галогенфенил, C1-C4-алкоксифенил и нитрофенил).
Предлагаемый способ может также включать в себя стадию очистки алифатического соединения, меченого [18F] фторидом, с использованием, по меньшей мере, одного ионообменного ТФЭ картриджа.
Ионообменный ТФЭ картридж может содержать любое из следующего: анионообменный ТФЭ картридж и анионообменный ТФЭ картридж.
Ионообменный ТФЭ картридж может содержать твердофазный носитель, содержащий полимер с фенильной группой и C1-C20-углеводород, или кремнезем.
Катионообменный ТФЭ картридж может содержать любое из следующего: ТФЭ картридж для SCX (сильный катионообменник на кремнеземе), ТФЭ картридж МСХ (сильный катионообменник на полимере) и ТФЭ картридж WCX (слабый катионообменник на полимере).
Анионообменный ТФЭ картридж может содержать любое из следующего: ТФЭ картридж SAX (сильный анионообменник на кремнеземе), ТФЭ картридж МАХ (сильный анионообменник на полимере) и ТФЭ картридж WAX (слабый анионообменник на полимере).
В соответствии с другим аспектом настоящего изобретения предлагается способ очистки фторзамещенного органического алифатического соединения, включающий в себя стадию очистки фторзамещенного органического алифатического соединения путем проведения твердофазной экстракции (ТФЭ) с использованием ионообменного ТФЭ картриджа, имеющего химическую формулу 2:
(химическая формула 2)
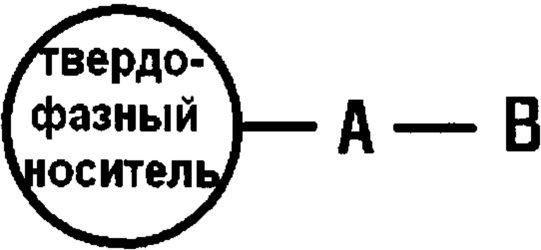
где твердофазный носитель представляет собой полимер, содержащий фенильную группу и C1-C20-углеводород, или кремнезем;
группа А может отсутствовать, когда твердофазный носитель является полимером, или представлять собой фенил либо С1-C20-углеводородную группу, когда твердофазный носитель является кремнеземом; и
группа В может представлять собой органический катион или органический анион,
причем органический катион имеет формулу  , где Е представляет собой азот или фосфор, группы R1, R2 и R3 могут быть одинаковыми или могут отличаться друг от друга и каждая из них выбрана из C2-C20-гетероароматических катионов, имеющих формулу
, где Е представляет собой азот или фосфор, группы R1, R2 и R3 могут быть одинаковыми или могут отличаться друг от друга и каждая из них выбрана из C2-C20-гетероароматических катионов, имеющих формулу  и
и  и содержащих C1-C20-углеводородную группу
и содержащих C1-C20-углеводородную группу  , арильную группу, содержащую, по меньшей мере, один атом азота, азот и кислород или азот и серу, а также содержащую C1-C20-углеводородную группу в качестве заместителя у одного атома азота, а органический анион является анионом серной кислоты (-SO3-) или карбоновой кислоты (-COO-).
, арильную группу, содержащую, по меньшей мере, один атом азота, азот и кислород или азот и серу, а также содержащую C1-C20-углеводородную группу в качестве заместителя у одного атома азота, а органический анион является анионом серной кислоты (-SO3-) или карбоновой кислоты (-COO-).
Очистку можно проводить, используя для очистки фторзамещенного органического алифатического соединения ионообменный ТФЭ картридж, имеющий химическую формулу 2, где группа В является органическим катионом, в сочетании с ионообменным ТФЭ картриджем, имеющим химическую формулу 2, где группа В является органическим анионом.
Фторзамещенное органическое алифатическое соединение может представлять собой [I8F] фторпропилкарбометокситропан.
В соответствии с еще одним аспектом настоящего изобретения предлагается способ очистки фторзамещенного органического алифатического соединения, включающий в себя стадию очистки путем проведения твердофазной экстракции (ТФЭ) с использованием, по меньшей мере, одного ионообменного ТФЭ картриджа, причем фторзамещенное органическое алифатическое соединение представляет собой [18F] фторпропилкарбометокситропан.
Ионообменный ТФЭ картридж может содержать любое из следующего: катионообменный ТФЭ картридж и анионообменный ТФЭ картридж.
Ионообменный ТФЭ картридж может содержать твердофазный носитель, включая полимер, содержащий фенильную группу и C1-C20-углеводород, или кремнезем.
Катионообменный ТФЭ картридж может содержать любое из следующего: ТФЭ картридж SCX (сильный катионообменник на кремнеземе), ТФЭ картридж МСХ (сильный катионообменник на полимере) и ТФЭ картридж WCX (слабый катионообменник на полимере).
Анионообменный ТФЭ картридж может содержать любое из следующего: ТФЭ картридж SAX (сильный анионообменник на кремнеземе), ТФЭ картридж МАХ (сильный анионообменник на полимере) и ТФЭ картридж WAX (слабый анионообменник на полимере).
В соответствии с еще одним аспектом настоящего изобретения предлагается способ изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, причем этот способ включает в себя следующие стадии: элюирование [18F] фторида через реакционный контейнер, предотвращающий противоточное движение жидкости; выпаривание элюента в реакционном контейнере, предотвращающем противоточное движение жидкости, подачу радиофармацевтического прекурсора и растворителя, используемого в качестве реакционной среды, в реакционный контейнер, предотвращающий противоточное движение жидкости, и обеспечение взаимодействия выпаренного [18F] фторида с радиофармацевтическим прекурсором в присутствии растворителя, используемого в качестве реакционной среды, причем реакционный контейнер, предотвращающий противоточное движение жидкости, содержит первую трубку для подачи реагентов, используемых для изготовления радиофармацевтического препарата, и вторую трубку для создания разрежения, при этом конец первой трубки расположен, по меньшей мере, над поверхностью реагентов для изготовления радиофармацевтического препарата, подаваемых в реакционный контейнер, предотвращающий противоточное движение жидкости.
Конец первой трубки может отстоять от поверхности реагентов на расстояние не более 5 см.
Кассета, содержащая реакционный контейнер, предотвращающий противоточное движение жидкости, может представлять собой кассету коллекторного типа.
Растворитель, используемый в качестве реакционной среды, может содержать любое из следующего: апротонный растворитель, протонный растворитель и многофункциональный растворитель.
Апротонный растворитель может содержать любое из следующего: ацетонитрил, диметилформамид и диметилсульфоксид.
Протонный растворитель может содержать любое из группы, состоящей из следующего: первичные спирты, в том числе метанол, этанол, н-пропанол, н-бутанол, н-амиловый спирт, н-гексиловый спирт, н-гептанол и н-октанол; вторичные спирты, в том числе изопропанол, изобутанол, изоамиловый спирт и 3-пентанол; и третичные спирты, в том числе трет-бутанол, трет-амиловый спирт, 2,3-диметил-2-бутанол, 2-(трифторметил)-2-пропанол, 3-метил-3-пентанол, 3-этил-3-пентанол, 2-метил-2-пентанол, 2,3-диметил-3-пентанол, 2,4-диметил-2-пентанол, 2-метил-2-гексанол, 2-циклопропил-2-пропанол, 2-циклопропил-2-бутанол, 2-циклопропил-3-метил-2-бутанол, 1-метилциклопентанол, 1-этилциклопентанол, 1-пропилциклопентанол, 1-метилциклогексанол, 1-этилциклогексанол и 1-метилциклогептанол.
Многофункциональный растворитель может представлять собой соединение, имеющее химическую формулу 1:
(химическая формула 1)

где каждая из групп R1 и R2 независимо друг от друга представляет собой Н, C1-C10-алкильную группу или ту же функциональную группу, что и группа X1;
группа Ln представляет собой C1-C10-алкильную группу или полиэтиленгликолевую группу СН2(ОСН2СН2)n, где n является целым числом в диапазоне 1-10;
группа X1 представляет собой полярную группу, выбранную из следующего: алкоксильная группа (OR3), нитрильная группа (CN) и галоид, при этом группа R3 представляет собой C1-C10-алкильную группу, а галоид может содержать любое из следующего: хлорид (Cl), бромид (Br) и йодид (I).
Многофункциональный растворитель, имеющий химическую формулу 1, может содержать любое из следующего: 1-метокси-2-метил-2-пропанол, 1-этокси-2-метил-2-пропанол, 1-пропокси-2-метил-2-пропанол, 1-изопропокси-2-метил-2-пропанол, 1-трет- бутокси-2-метил-2-пропанол, 1-нитрил-2-метил-2-пропанол, 1-хлор-2-метил-2-пропанол, 1-бром-2-метил-2-пропанол и 1-йод-2-метил-2-пропанол.
Преимущества, обеспечиваемые настоящим изобретением
В соответствии с вариантами осуществления настоящего изобретения предлагается способ изготовления фторзамещенного органического алифатического соединения с использованием многофункционального растворителя, содержащего функциональную группу, способную повышать эффективность мечения радиоизотопом, и функциональную группу, способную повышать эффективность очистки. Функциональная группа, способная повышать эффективность мечения радиоизотопом, подавляет побочные реакции, обусловленные побочным действием основания, и тем самым позволяет повысить выход при мечении радиоизотопом. Функциональная группа, способная повышать эффективность очистки, увеличивает полярность растворителя, используемого в качестве реакционной среды, чтобы он мог смешиваться с водой, и устраняет необходимость в дополнительном процессе удаления растворителя. В результате удается сократить продолжительность изготовления радиофармацевтического препарата и упростить процесс его изготовления. Кроме того, удается повысить эффективность очистки. Более того, линкер, с помощью которого присоединяются функциональные группы, вызывает повышение температуры кипения, что позволяет устанавливать температуру, оптимальную для мечения фтором-18, и тем самым оптимизировать изготовление радиофармацевтического препарата.
Кроме того, в соответствии с вариантами осуществления настоящего изобретения предлагается способ очистки фторзамещенного органического алифатического соединения путем проведения твердофазной экстракции (ТФЭ) с использованием ионообменного ТФЭ картриджа. Это позволяет эффективно удалять почти все примеси, оставшиеся после изготовления фторзамещенного органического алифатического соединения.
Кроме того, в соответствии с вариантами осуществления настоящего изобретения предлагается способ изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, который позволяет стабильно подавать в реакционный контейнер реагенты, используемые для изготовления радиофармацевтического препарата, в количестве, предназначенном для участия в реакции без потерь, и тем самым обеспечивать высокий выход.
Помимо того, в соответствии с вариантами осуществления настоящего изобретения предлагается способ изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, который предотвращает противоточное движение растворителя из-за испарения во время проведения мечения при высокой температуре, чтобы исключить повреждение кассеты и чтобы весь растворитель мог участвовать в реакции.
Следовательно, реагенты, используемые для изготовления радиофармацевтического препарата, могут стабильно принимать участие в мечении полностью в том количестве, которое подано в реакционный контейнер. Таким образом, возможно изготавливать радиофармацевтический препарат с небольшими колебаниями выхода продуктов синтеза без сбоев в работе. Это позволит в будущем изготавливать радиофармацевтический препарат в соответствии с правилами надлежащей производственной практики (GMP). Кроме того, поскольку противоточное движение растворителя, используемого в качестве реакционной среды, отсутствует, то отпадает необходимость в кассете, стойкой к растворителю, используемому в качестве реакционной среды. Это обеспечивает высокую экономическую эффективность изготовления радиофармацевтического препарата.
Краткое описание чертежей
На фиг. 1 приведено схематичное изображение процесса получения радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, согласно одному из вариантов осуществления изобретения.
На фиг. 2 приведено схематичное изображение процесса получения радиофармацевтического препарата с использованием кассеты, содержащей обычный реакционный контейнер.
Осуществление изобретения
Далее приведено более подробное описание изобретения со ссылкой на приложенные чертежи, где показаны характерные примеры его осуществления. Однако это изобретение может быть осуществлено во множестве разных форм и не ограничено приведенными здесь характерными примерами осуществления. В этом описании могут быть опущены подробности широко известных признаков и методов. На чертежах одинаковые элементы обозначены одинаковыми числами.
Первым следует подробное описание способа изготовления фторзамещенного органического алифатического соединения с использованием нового многофункционального растворителя и способа очистки фторзамещенного органического алифатического соединения с использованием ТФЭ.
В соответствии с одним аспектом настоящего изобретения предлагается способ изготовления фторзамещенного органического алифатического соединения, включающий в себя стадию обеспечения взаимодействия алифатического соединения, содержащего замещаемую группу, с солью фтора в многофункциональном растворителе, имеющем химическую формулу 1, с получением алифатического соединения, меченого [18F] фторидом, присоединенным вместо замещаемой группы:
(химическая формула 1)

где R1 и R2 независимо друг от друга представляют собой Н, C1-C10-алкильную группу или ту же функциональную группу, что и группа X1; группа Ln представляет собой C1-C10-алкильную группу или полиэтиленгликолевую группу СН2(ОСН2СН2)n, где n является целым числом в диапазоне 1-10; группа X1 представляет собой полярную группу, выбранную из следующего: алкоксильная группа (OR3), нитрильная группа (CN) и галоид, а группа R3 представляет собой C1-C10-алкильную группу.
Соль фтора используется в качестве источника [18F] фторида и представляет собой соединение, содержащее фтор-18. Соль фтора может быть выбрана из следующего: фториды щелочного металла, содержащие щелочной металл, выбранный из группы, состоящей из следующего: литий, натрий, калий, рубидий и цезий; фториды щелочноземельного металла, содержащие щелочноземельный металл, выбранный из группы, состоящей из следующего: магний, кальций, стронций и барий; и фториды аммония. Более предпочтительно, соль фтора представляет собой фторид калия или фторид аммония. Фторид щелочного металла, содержащий калий, или фторид тетраалкиламмония предпочтительно адсорбируют на носитель, выбранный из следующего: Целит, молекулярные сита, глинозем и силикагель. Предпочтительно, фторид аммония может быть выбран из группы, состоящей из следующего: фториды четвертичного аммония, в том числе фторид тетрабутиламмония и фторид бензилтриметиламмония; фториды третичного аммония, в том числе фторид триэтиламмония и фторид трибутиламмония; фториды вторичного аммония, в том числе фторид дибутиламмония и фторид дигексиламмония; и фториды первичного аммония, в том числе фторид бутиламмония и фторид гексиламмония. Более предпочтительно, фторид аммония представляет собой фторид тетрабутиламмония.
Согласно настоящему изобретению, алифатическое соединение, содержащее замещаемую группу, представляет собой алифатическое соединение, содержащее алкилгалоидную группу или алкилсульфонатную группу, причем замещаемой группой является галоидная группа или сульфонатная группа. С другой стороны, галоидная группа или сульфонатная группа могут являться первичной замещаемой группой или вторичной замещаемой группой. Галоидная группа может быть выбрана из группы, состоящей из следующего: Cl, Br и I, а сульфонатная группа имеет формулу -SO3R12 (где группа R12 выбрана из группы, состоящей из следующего: С1-С12-алкил, С1-С12-алкилгалоид, фенил, С1-С4-алкилфенил, галогенфенил, С1-С4-алкоксифенил и нитрофенил). Конкретными примерами алкилсульфонатной группы (где группа R12 представляет собой С1-С12-алкил или С1-С12-алкилгалоид) могут являться метансульфонат, этансульфонат, изопропансульфонат, хлорметансульфонат, трифторметансульфонат или хлорэтансульфонат. Конкретными примерами арилсульфонатной группы (где группа R12 представляет собой фенил, C1-C4-алкилфенил, галогенфенил, C1-C4-алкоксифенил или нитрофенил) могут являться метилфенилсульфонат, этилфенилсульфонат, хлорфенилсульфонат, бромфенилсульфонат, метоксифенилсульфонат или нитрофенилсульфонат.
Согласно другому варианту осуществления, алифатическое соединение, содержащее замещаемую группу, может представлять собой алифатическое соединение, имеющее формулу N-(N-(CH2)n-X2 или O-(СН2)n-X2 (где группа X2 является замещаемой группой и n является целым числом в диапазоне 1-10).
Группа X2 представляет собой галоидную группу или сульфонатную группу, при этом галоидная группа выбрана из группы, состоящей из следующего: Cl, Br и I, а сульфонатная группа имеет формулу -SO3R12 (где группа R12 выбрана из группы, состоящей из следующего: С1-С12-алкил, С1-С12-алкилгалоид, фенил, С1-С4-алкилфенил, галогенфенил, С1-С4-алкокси-фенил и нитрофенил). Конкретными примерами алкилсульфонатной группы (где группа R12 представляет собой C1-C12-алкил или С1-С12-алкилгалоид) могут являться метансульфонат, этансульфонат, изопропансульфонат, хлорметансульфонат, трифторметансульфонат или хлорэтансульфонат. Конкретными примерами арилсульфонатной группы (где группа R12 представляет собой фенил, С1-С4-алкилфенил, галогенфенил, С1-С4-алкоксифенил или нитрофенил) могут являться метилфенилсульфонат, этилфенилсульфонат, хлорфенилсульфонат, бромфенилсульфонат, метоксифенилсульфонат или нитрофенилсульфонат.
В частности, конкретными примерами алифатического соединения, содержащего замещаемую группу, могут являться следующие соединения:
1-фенил-4-(3-тозилпропил)-фенилпиперазин  , представляющий собой органическое соединение, содержащее OTs (О-тозил) в качестве первичной замещаемой группы;
, представляющий собой органическое соединение, содержащее OTs (О-тозил) в качестве первичной замещаемой группы;
2-(3-метансульфонилоксипропокси)нафталин  , представляющий собой органическое соединение, содержащее OMs (О-мезил) в качестве первичной замещаемой группы;
, представляющий собой органическое соединение, содержащее OMs (О-мезил) в качестве первичной замещаемой группы;
2-(2-метансульфонилоксипропокси)нафталин  , представляющий собой органическое соединение, содержащее OMs в качестве вторичной замещаемой группы;
, представляющий собой органическое соединение, содержащее OMs в качестве вторичной замещаемой группы;
(3-толуолсульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропан, представляющий собой органическое соединение, содержащее OTs в качестве первичной замещаемой группы;
(3-метансульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропан, представляющий собой органическое соединение, содержащее OMs в качестве первичной замещаемой группы;
3-(2-нитроимидазол-1-ил)-2-O-тетрагидропиранил-1-О-толуолсульфонилпропандиол, представляющий собой органическое соединение, содержащее OTs в качестве вторичной замещаемой группы;
5'-О-диметокситритил-2'-деокси-3'-O-носил-β-D-трео-пентофураноксил)-3-N-бутилоксикарбонил-тимин, представляющий собой органическое соединение, содержащее ONs (О-нозил) в качестве вторичной замещаемой группы;
трифлатманноза (1, 3, 4, 6-тетра-O-ацетил-2-O-трифтор-метансульфонил-бета-D-маннопираноза), содержащий OTf (трифлат) в качестве вторичной замещаемой группы;
(Е)-4-хлорбут-2-енил-2-β-карбометокси-3-β-(4-йодфенил)тропан, представляющий собой органическое соединение, содержащее Cl в качестве первичной замещаемой группы, и т.п.
Фторзамещенное органическое алифатическое соединение, изготовленное по способу согласно настоящему изобретению, может также представлять собой радиофармацевтический препарат. Радиофармацевтический препарат может представлять собой, по меньшей мере, один препарат, выбранный из следующих соединений:
[18F] фторпропилкарбометокситропан 
[18F] фтормизонидазол 
[18F] фтортимидин 
[18F] фтордезоксиглюкоза 
и [18F] LBT999 
Многофункциональный растворитель согласно одному из вариантов осуществления содержит спиртовую группу (спиртовая группа в химической формуле 1) в качестве функциональной группы, способной повышать эффективность мечения радиоизотопом, функциональную группу, способную повышать эффективность очистки, и линкер (группа Ln в химической формуле 1), способный обеспечить оптимальную температуру реакции.
Когда мечение [18F] фторидом осуществляют путем нуклеофильного замещения, следует использовать определенное количество основания, типичными примерами которого являются карбонат калия и гидрокарбонат калия. Подобные основания вызывают побочную реакцию с прекурсором, что приводит к увеличению расхода прекурсора и к снижению эффективности мечения [18F] фторидом. Однако спиртовая группа, имеющаяся в многофункциональном растворителе согласно одному варианту осуществления, ингибирует подобную побочную реакцию с прекурсором, вызванную основанием, снижает расход прекурсора и тем самым обеспечивает изготовление радиофармацевтического препарата с высоким выходом.
Кроме того, поскольку группа X1 (группа X1 в химической формуле 1), имеющаяся в многофункциональном растворителе согласно одному варианту осуществления, увеличивает его полярность, растворимость многофункционального растворителя в воде возрастает, что позволяет использовать различные способы очистки, например, простые способы очистки путем проведения твердофазной экстракции (ТФЭ) с использованием ТФЭ картриджа и способы очистки с использованием жидкостной хроматографии высокого разрешения (ЖХВР), что позволяет изготавливать радиофармацевтический препарат высокой чистоты. Согласно уровню техники, растворитель, используемый в качестве реакционной среды, обладает низкой растворимостью в воде и для его удаления приходится проводить выпаривание. Однако многофункциональный растворитель не нуждается в выпаривании, что уменьшает продолжительность реакции.
Кроме того, линкер (группа Ln в химической формуле 1), имеющийся в многофункциональном растворителе согласно одному варианту осуществления, повышает температуру кипения, что позволяет устанавливать оптимальную температуру реакции и тем самым обеспечивает изготовление радиофармацевтического препарата с высоким выходом.
Кроме того, способ изготовления фторзамещенного органического алифатического соединения согласно одному варианту осуществления, может дополнительно включать в себя стадию очистки полученного алифатического соединения, меченного [18F] фторидом, с использованием, по меньшей мере, одного ионообменного ТФЭ картриджа.
Как было указано выше, когда фторзамещенное органическое алифатическое соединение изготавливают с использованием многофункционального растворителя согласно настоящему изобретению, полученное фторзамещенное органическое алифатическое соединение можно подвергать очистке с применением как ЖХВР, так и ТФЭ. Однако в отличие от ТФЭ, при проведении ЖХВР может происходить потеря радиоактивности в процессе очистки и под действием радиоактивности могут образоваться продукты распада при массовом производстве. Эта проблема особенно обостряется при изготовлении [18F] фторпропилкарбометокситропана. В этом случае продукты радиоактивного распада имеют такое же время удержания, что и [18F] фторпропилкарбометокситропан, и снижают его радиохимическую чистоту. Кроме того, при проведении очистки с использованием ЖХВР выход может меняться в зависимости от квалификации работника или исследователя, что затрудняет получение радиофармацевтического препарата стабильно высокого качества. Чтобы решить вышеуказанные проблемы, можно проводить очистку с использованием обращеннофазового ТФЭ картриджа, широко применяемого при изготовлении лекарственных средств. При этом, несмотря на то, что при использовании обращенно-фазового ТФЭ картриджа радиохимическая чистота выше, чем при использовании ЖХВР, затруднительно освободиться от примесей, имеющих такую же полярность, что и [18F] фторпропилкарбометокситропан (от промежуточных соединений, которые остаются после фторирования прекурсоров, используемых для получения [18F] фторпропилкарбометокситропана, и претерпевают изменение в химической структуре, хотя и не подвергаются фторированию). Иными словами, несмотря на то, что подобные примеси и отличаются по структуре от получаемого [18F] фторпропилкарбометокситропана, они обладают почти такой же олеофильностью, что и [18F] фторпропилкарбометокситропан. Таким образом, при использовании обращенно-фазового ТФЭ картриджа почти не удается избавиться от подобных органических примесей, образовавшихся из прекурсора, как будет показано в приведенных ниже примерах.
Однако при использовании ионообменного ТФЭ способа очистки, согласно настоящему изобретению, удается провести эффективную очистку [18F] фторпропилкарбометокситропан от органических примесей, имеющих такую же полярность, что и [18F] фторпропилкарбометокситропан.
Ионообменный ТФЭ способ очистки, согласно настоящему изобретению, использует ионообменный ТФЭ картридж, который может содержать любое из следующего: катионообменный ТФЭ картридж и анионообменный ТФЭ картридж. Ионообменный ТФЭ картридж может содержать твердофазный носитель, включая полимер, содержащий фенильную группу и C1-C20-углеводород, или кремнезем. При этом катионообменный ТФЭ картридж может содержать любое из следующего: ТФЭ картридж SCX (сильный катионообменник на кремнеземе), ТФЭ картридж МСХ (сильный катионообменник на полимере) и ТФЭ картридж WCX (слабый катионообменник на полимере), а анионообменный ТФЭ картридж может содержать любое из следующего: ТФЭ картридж SAX (сильный анионообменник на кремнеземе), ТФЭ картридж МАХ (сильный анионообменник на полимере) и ТФЭ картридж WAX (слабый анионообменник на полимере).
Согласно другому варианту осуществления, ионообменный ТФЭ картридж представляет собой ионообменный ТФЭ картридж, имеющий химическую формулу 2:
(химическая формула 2)
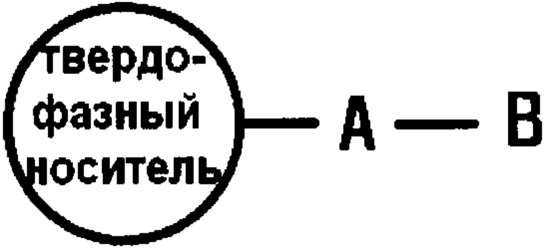
где твердофазный носитель представляет собой полимер, содержащий фенильную группу и С1-С20-углеводород или кремнезем; группа А может отсутствовать, когда твердофазный носитель является полимером, или представляет собой фенил либо С1-С20-углеводородную группу, когда твердофазный носитель является кремнеземом; а группа В может представлять собой органический катион или органический анион, причем органический катион имеет формулу 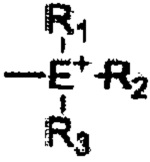 , где Е представляет собой азот или фосфор, группы R1, R2 и R3 могут быть одинаковыми или могут отличаться друг от друга и каждая из них выбрана из С2-С20-гетероароматических катионов, имеющих формулу
, где Е представляет собой азот или фосфор, группы R1, R2 и R3 могут быть одинаковыми или могут отличаться друг от друга и каждая из них выбрана из С2-С20-гетероароматических катионов, имеющих формулу  и
и 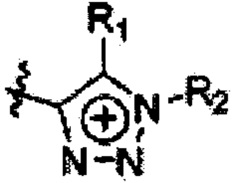 и содержащих С2-С20-углеводородную группу, арильную группу
и содержащих С2-С20-углеводородную группу, арильную группу 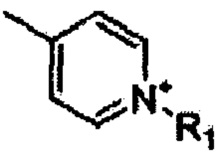 , содержащую, по меньшей мере, один атом азота, азот и кислород или азот и серу, а также содержащую С2-С20-углеводородную группу в качестве заместителя у одного атома азота, а органический анион является анионом серной кислоты (-SO3-) или карбоновой кислоты (-COO-).
, содержащую, по меньшей мере, один атом азота, азот и кислород или азот и серу, а также содержащую С2-С20-углеводородную группу в качестве заместителя у одного атома азота, а органический анион является анионом серной кислоты (-SO3-) или карбоновой кислоты (-COO-).
Как было указано выше, согласно настоящему изобретению, при использовании многофункционального растворителя в качестве реакционной среды возможно получать фторзамещенное органическое алифатическое соединение высокого качества с высоким выходом и высокой эффективностью мечения путем фторирования органического алифатического соединения, имеющего замещаемую группу. Кроме того, согласно настоящему изобретению, многофункциональный растворитель, используемый в качестве реакционной среды, обладает большим сродством с водой, что позволяет проводить очистку фторзамещенного органического алифатического соединения без использования дополнительной стадии выпаривания растворителя. Несмотря на то, что согласно настоящему изобретению, очистку фторзамещенного органического алифатического соединения можно проводить с использованием как ЖХВР, так и ТФЭ, возможно дополнительно повысить эффективность удаления примесей, оставшихся после фторирования, если проводить очистку с использованием ионообменной ТФЭ.
Далее настоящее изобретение объяснено более подробно со ссылкой на следующие примеры. Однако эти примеры всего лишь поясняют сущность изобретения и не служат для ограничения объема изобретения. Специалистам в данной области техники понятно, что в него могут быть внесены различные изменения, касающиеся формы и деталей, которые не выходят за пределы объема этого изобретения, определяемого прилагаемой формулой изобретения. Следовательно, предполагается, что в объем настоящего изобретения входят все варианты осуществления в пределах сущности и объема приложенной формулы изобретения.
Пример 1. Использование 1-метокси-2-метил-2-пропанола в качестве растворителя при проведении реакции
Пример 1-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
В реакционный контейнер подают 0,1 мл раствора 1-фенил-4-(3-тозилпропил)-фенилпиперазина в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды, согласно настоящему изобретению. Затем проводят реакцию при температуре 120°С и получают l-(3-[18F] фторпропил)-4-фенилпиперазин.
Эффективность мечения определяют методом радиоизотопной тонкопленочной хроматографии. После проведения реакции продукт разбавляют без выпаривания и подвергают очистке способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
Пример 1-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Используют тот же способ, что и в примере 1-1, за исключением того, что в реакционный контейнер подают 0,1 мл раствора 2-(3-метансульфонилоксипропокси)нафталина (алифатического соединения, содержащего OMs в качестве первичной замещаемой группы) или 2-(2-метансульфонилоксипропокси)нафталина (алифатического соединения, содержащего OMs в качестве вторичной замещаемой группы) и 1,0 мл 1-метокси-2-метил-2-пропанола -многофункционального растворителя, используемого в качестве реакционной среды, согласно настоящему изобретению. Затем проводят реакцию при температуре 120°С и получают 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.
Эффективность мечения определяют методом радиоизотопной тонкопленочной хроматографии. После проведения реакции продукт разбавляют без выпаривания и подвергают очистке способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
Сравнительный пример 1. Использование ацетонитрила в качестве растворителя при проведении реакции
Сравнительный пример 1-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
Используют те же материалы и тот же способ, что и в примере 1-1, за исключением того, что в качестве растворителя при проведении реакции используют ацетонитрил и получают l-(3-[18F] фторпропил)-4-фенилпиперазин.
Сравнительный пример 1-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Используют те же материалы и тот же способ, что и в примере 1-2, за исключением того, что в качестве растворителя при проведении реакции используют ацетонитрил и получают 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.
Сравнительный пример 2. Использование трет-амилового спирта в качестве растворителя при проведении реакции
Сравнительный пример 2-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
Используют те же материалы и тот же способ, что и в примере 1-1, за исключением того, что в качестве растворителя при проведении реакции используют трет-амиловый спирт и получают l-(3-[18F] фторпропил)-4-фенилпиперазин.
Сравнительный пример 2-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Используют те же материалы и тот же способ, что и в примере 1-2, за исключением того, что в качестве растворителя при проведении реакции используют трет-амиловый спирт и получают 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.
Полученные результаты приведены в таблице 1.


Как показано в табл. 1, когда фторзамещенное органическое алифатическое соединение получают с использованием многофункционального растворителя, 1-метокси-2-метил-2-пропанола, согласно настоящему изобретению, эффективность мечения составляет, по меньшей мере, 90%, а выход составляет, по меньшей мере, 61%, что свидетельствует об изготовлении фторзамещенного органического алифатического соединения высокого качества с высоким выходом и высокой эффективностью мечения. С другой стороны, когда в качестве реакционной среды используют обычный растворитель, трет-амиловый спирт (сравнительный пример 2), эффективность мечения органического алифатического соединения, содержащего OMs в качестве замещаемой группы, в случае О-алкильных алифатических соединений составляет, по меньшей мере, 90%, но выход составляет всего 10%; это означает, что эффективное изготовление фторзамещенного органического алифатического соединения невозможно. В случае N-алкил-алифатического соединения, содержащего OTs в качестве замещаемой группы, эффективность мечения фторзамещенного органического алифатического соединения низка (9,1%) и выход весьма низок (6,2%). Кроме того, при использовании обычного растворителя, ацетонитрила (сравнительный пример 1), эффективность мечения фторзамещенного органического алифатического соединения в случае N-алкил-алифатического соединения, содержащего OMs в качестве замещаемой группы, недостаточно высока, составляя 56,5% или 43,7%, а выход в этом случае низок (31,1% или 20,4%), что свидетельствует о невозможности эффективного изготовления фторзамещенного органического алифатического соединения.
Пример 2. Использование 1-хлор-2-метил-2-пропанола в качестве растворителя при проведении реакции
Пример 2-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
В реакционный контейнер подают 0,1 мл раствора 1-фенил-4-(3-тозилпропил)-фенилпиперазина в ацетонитриле и 1,0 мл 1-хлор-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды, согласно настоящему изобретению. Затем проводят реакцию при температуре 120°С и получают l-(3-[,8F] фторпропил)-4-фенилпиперазин.
Эффективность мечения определяют методом радиоизотопной тонкопленочной хроматографии. После проведения реакции продукт разбавляют без выпаривания и подвергают очистке способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
Пример 2-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
В реакционный контейнер подают 0,1 мл раствора 2-(3-метансульфонилоксипропокси)нафталина (алифатического соединения, содержащего OMs в качестве первичной замещаемой группы) или 2-(2-метансульфонилоксипропокси)нафталина (алифатического соединения, содержащего OMs в качестве вторичной замещаемой группы) в ацетонитриле и 1,0 мл 1-хлор-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды, согласно настоящему изобретению. Затем проводят реакцию при температуре 120°С и получают 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.
Эффективность мечения определяют методом радиоизотопной тонкопленочной хроматографии. После проведения реакции продукт разбавляют без выпаривания и подвергают очистке способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
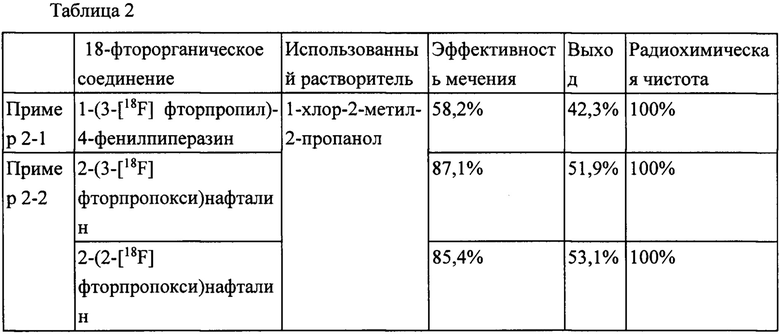
Как показано в табл. 1, в примере 2 - многофункционального растворителя для получения фторзамещенного органического алифатического соединения согласно настоящему изобретению, используют 1-хлор-2-метил-2-пропанол. В примере 2-1 эффективность мечения и выход составляют 58,2% и 42,3%, соответственно, что приблизительно в 6-7 раз больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 3 раза больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
В примере 2-2 эффективность мечения составляет 87,1% или 85,4%, а выход составляет 51,9% или 53,1%, что приблизительно в 2-3 раза больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 5 раз больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
Пример 3. Использование 1-нитрил-2-метил-2-пропанола в качестве растворителя
Пример 3-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OTs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-1, за исключением того, что в качестве растворителя используют 1-нитрил-2-метил-2-пропанол и получают фторзамещенное органическое алифатическое соединение l-(3-[18F] фторпропил)-4-фенилпиперазин.
Пример 3-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OMs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-2, за исключением того, что в качестве растворителя используют 1-нитрил-2-метил-2-пропанол и получают фторзамещенное органическое алифатическое соединение 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.

Как показано в табл. 3, в примере 3 - многофункционального растворителя для получения фторзамещенного органического алифатического соединения согласно настоящему изобретению, используют 1-нитрил-2-метил-2-пропанол. В примере 3-1 эффективность мечения и выход составляют 42,8% и 30,2%, соответственно, что приблизительно в 5 раз больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 4-5 раз больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
В примере 3-2 эффективность мечения составляет 81,3% или 83,8%, а выход составляет 51,9% или 53,1%, что приблизительно в 2-3 раза больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 4-5 раз больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
Пример 4. Использование 3-(метоксиметил)-3-пентанола в качестве растворителя
Пример 4-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OTs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-1, за исключением того, что в качестве растворителя используют 3-(метоксиметил)-3-пентанол и получают фторзамещенное органическое алифатическое соединение l-(3-[18F] фторпропил)-4-фенилпиперазин.
Пример 4-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OMs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-2, за исключением того, что в качестве растворителя используют 3-(метоксиметил)-3-пентанол и получают фторзамещенное органическое алифатическое соединение 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.


Как показано в табл. 4, в примере 4 - многофункционального растворителя для получения фторзамещенного органического алифатического соединения согласно настоящему изобретению, используют 3-(метоксиметил)-3-пентанол. В примере 4-1 эффективность мечения и выход составляют 64,7% и 43,8%, соответственно, что приблизительно в 7 раз больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 4 раза больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
В примере 4-2 эффективность мечения составляет 84,3% или 83,4%, а выход составляет 54,9% или 51,7%, что в обоих случаях больше, чем в сравнительном примере 1-2 (использование ацетонитрила) и в сравнительном примере 2-2 (использование трет-амилового спирта).
Пример 5. Использование 1-(2-метоксиэтокси)-2-метил-2-пропанола в качестве растворителя
Пример 5-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OTs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-1, за исключением того, что в качестве растворителя используют 1-(2-метоксиэтокси)-2-метил-2-пропанол и получают фторзамещенное органическое алифатическое соединение l-(3-[18F] фторпропил)-4-фенилпиперазин.
Пример 5-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OMs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-2, за исключением того, что в качестве растворителя используют 1-(2-метоксиэтокси)-2-метил-2-пропанол и получают фторзамещенное органическое алифатическое соединение 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.


Как показано в табл. 5, в примере 5 - многофункционального растворителя для получения фторзамещенного органического алифатического соединения согласно настоящему изобретению используют 1-(2-метоксиэтокси)-2-метил-2-пропанол. В примере 5-1 эффективность мечения и выход составляют 58,7% и 47,0%, соответственно, что приблизительно в 8 раз больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 4 раза больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
В примере 5-2 эффективность мечения составляет 85,3% или 81,8%, а выход составляет 52,1% или 50,3%, что в обоих случаях больше, чем в сравнительном примере 1-2 (использование ацетонитрила) и в сравнительном примере 2-2 (использование трет-амилового спирта).
Пример 6. Использование 1-этокси-2-метил-2-пропанола в качестве растворителя
Пример 6-1. Фторирование органического алифатического соединения, имеющего OTs в качестве первичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OTs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-1, за исключением того, что в качестве растворителя используют 1-этокси-2-метил-2-пропанол и получают фторзамещенное органическое алифатическое соединение l-(3-[18F] фторпропил)-4-фенилпиперазин.
Пример 6-2. Фторирование органического алифатического соединения, имеющего OMs в качестве первичной или вторичной замещаемой группы
Для проведения фторирования органического алифатического соединения, содержащего OMs в качестве замещаемой группы, используют те же материалы и тот же способ, что и в примере 2-2, за исключением того, что в качестве растворителя используют 1-этокси-2-метил-2-пропанол и получают фторзамещенное органическое алифатическое соединение 2-(3-[18F] фторпропокси)нафталин или 2-(2-[18F] фторпропокси)нафталин.

Как показано в табл. 6, в примере 6 - многофункционального растворителя для получения фторзамещенного органического алифатического соединения согласно настоящему изобретению, используют 1-этокси-2-метил-2-пропанол. В примере 6-1 эффективность мечения и выход составляют 50,1% и 39,8%, соответственно, что приблизительно в 6 раз больше, чем при использовании в качестве реакционной среды обычного растворителя (ацетонитрила в сравнительном примере 1-2 в табл. 1). Кроме того, выход приблизительно в 3 раза больше, чем при использовании трет-амилового спирта согласно сравнительному примеру 2-2 в табл. 1.
В примере 6-2 эффективность мечения составляет 87,3% или 80,1%, а выход составляет 55,2% или 53,2%, что в обоих случаях больше, чем в сравнительном примере 1-2 (использование ацетонитрила) и в сравнительном примере 2-2 (использование трет-амилового спирта).
Пример 7. Изготовление [18F] фторпропилкарбометокситропана
Пример 7-1. Использование в качестве прекурсора алифатического соединения, имеющего OTs в качестве замещаемой группы
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
В реакционный контейнер подают в качестве прекурсора 0,1 мл раствора (3-толуолсульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды, согласно настоящему изобретению. Затем проводят реакцию при температуре 120°С и получают [18F] фторпропилкарбометокситропан.
Эффективность мечения определяют методом радиоизотопной тонкопленочной хроматографии. После проведения реакции продукт разбавляют без выпаривания и подвергают очистке способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
Пример 7-2. Использование в качестве прекурсора алифатического соединения, имеющего OMs в качестве замещаемой группы
Используют тот же способ, что и в примере 3, за исключением того, что в качестве прекурсора используют (3-метансульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропан, имеющий OMs в качестве замещаемой группы, и получают [18F] фторпропилкарбометокситропан.
Сравнительный пример 4. Использование ацетонитрила в качестве растворителя
Сравнительный пример 4-1
Используют те же материалы и тот же способ, что и в примере 7-1, за исключением того, что в качестве растворителя при проведении реакции используют ацетонитрил и получают [18F] фторпропилкарбометокситропан.
Сравнительный пример 4-2
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что в качестве растворителя при проведении реакции используют ацетонитрил и получают [18F] фторпропилкарбометокситропан.
Сравнительный пример 5. Использование трет-амилового спирта в качестве растворителя
Сравнительный пример 5-1
Используют те же материалы и тот же способ, что и в примере 7-1, за исключением того, что в качестве растворителя при проведении реакции используют трет-амиловый спирт и получают [18F] фторпропилкарбометокситропан.
Сравнительный пример 5-2
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что в качестве растворителя при проведении реакции используют трет-амиловый спирт и получают [18F] фторпропилкарбометокситропан.
Полученные результаты приведены в таблице 7.

Как показывают приведенные выше результаты, когда в качестве реакционной среды используют обычный растворитель, ацетонитрил (сравнительные примеры 4-1 и 4-2), выход составляет всего 5-7%, а эффективность мечения составляет всего 6-12%. Когда в качестве реакционной среды используют обычный растворитель, трет-амиловый спирт (сравнительные примеры 5-1 и 5-2), эффективность мечения составляет не менее 40%, но выход достаточно мал (2-3%). Таким образом, можно видеть, что обычные растворители, используемые в качестве реакционной среды, не пригодны для изготовления фторзамещенного органического алифатического соединения. С другой стороны, в примерах 7-1 и 7-2 используется 1-метокси-2-метил-2-пропанол - многофункционального растворителя в соответствии с настоящим изобретением и обеспечивается выход 74,2% и 65,7%, соответственно, что значительно выше, чем в сравнительных примерах. Кроме того, в примерах 7-1 и 7-2 обеспечивается эффективность мечения 92,7% и 77,4%, соответственно, что значительно выше, чем в сравнительных примерах, а чистота составляет 100%. Следовательно, при использовании многофункционального растворителя в соответствии с настоящим изобретением можно получать фторзамещенное органическое алифатическое соединение высокой чистоты с высокой эффективностью мечения и высоким выходом.
Пример 8. Изготовление препарата [18F] LBT 999
В этом примере в качестве прекурсора для получения препарата [18F] LBT 999 используется алифатическое соединение, имеющее С1 в качестве замещаемой группы.
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора (Е)-4-хлорбут-2-енил-2-β-карбометокси-3-β-(4-йодфенил)тропана в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола -многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию при температуре 120°С и получают [18F] LBT 999.
Эффективность мечения определяют методом радиоизотопной тонкопленочной хроматографии. После проведения реакции продукт разбавляют без выпаривания и подвергают очистке способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
Пример 9. Изготовление [18F] фтормизонидазола
В этом примере в качестве прекурсора для получения [18F] фтормизонидазола используется алифатическое соединение, имеющее OTs в качестве вторичной замещаемой группы.
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора 3-(2-нитроимидозол-1-ил)-2-O-тетрагидропиранил-1-O-толуолсульфонилпропандиола в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола -многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения [18F] фторидом при температуре 120°С и определяют эффективность мечения методом радиоизотопной тонкопленочной хроматографии. После проведения реакции добавляют 1М соляной кислоты и проводят гидролиз при температуре 100°С в течение 5 мин, далее добавляют 2М раствора гидроксида натрия для нейтрализации. Затем продукт разбавляют водой и проводят очистку способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта. Полученные результаты приведены в таблице 8.
Пример 10. Изготовление [18F] фтортимидина
В этом примере в качестве прекурсора для получения [18F] фтортимидина используется алифатическое соединение, имеющее ONs в качестве вторичной замещаемой группы.
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора 5'-O-диметокситрифенилметил-2'-дезокси-3'-O-нозил-b-D-трео-пентофуранозил-3-N-бутоксикарбонил-тимина в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения [18F] фторидом при температуре 120°С и определяют эффективность мечения методом радиоизотопной тонкопленочной хроматографии. После проведения реакции добавляют 1М соляной кислоты и проводят гидролиз при температуре 100°С в течение 5 мин, а затем добавляют 2М раствора гидроксида натрия для нейтрализации. Затем продукт разбавляют водой и проводят очистку способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта. Полученные результаты приведены в таблице 8.
Пример 11. Изготовление [18F] фтордезоксиглюкозы В этом примере в качестве прекурсора для получения [18F] фтордезоксиглюкозы используется алифатическое соединение, имеющее OTf в качестве вторичной замещаемой группы.
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора трифлатманнозы (1,3,4,6-тетра-O-ацетил-2-O-трифторметансульфонил-бета-D-маннопиранозы), который является алифатическим соединением, имеющим OTf в качестве вторичной замещаемой группы, в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения [18F] фторидом при температуре 120°С и определяют эффективность мечения методом радиоизотопной тонкопленочной хроматографии. После проведения реакции добавляют 1М соляной кислоты и проводят гидролиз при температуре 100°С в течение 5 мин, а затем добавляют 2М раствора гидроксида натрия для нейтрализации. Затем продукт разбавляют водой и проводят очистку способом твердофазной экстракции. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
В примерах 8-11 показано получение различных радиофармацевтических препаратов с использованием 1-метокси-2-метил-2-пропанола - многофункционального растворителя в соответствии с настоящим изобретением. В таблице 8 указаны также эффективность мечения, способ очистки, продолжительность очистки и выход для каждого примера.

Препарот [18F] LBT 999 в соответствии с примером 8, [18F] фтормизонидазол в соответствии с примером 9, [18F] фтортимидин в соответствии с примером 10 и [18F] фтордезоксиглюкоза в соответствии с примером 11 представляют собой радиофармацевтические препараты, используемые в настоящее время в клиниках Кореи и других стран. Их изготавливают с использованием 1-метокси-2-метил-2-пропанола - многофункционального растворителя в соответствии с настоящим изобретением. Как показано в таблице 8, все радиофармацевтические препараты имеют чистоту 100%, демонстрируют достаточно высокую эффективность мечения, составляющую 97,4%, 95,7%, 90,5% и 93,7%, соответственно, и высокий выход, составляющий 65,1%, 63,4%, 61,7% и 66,4%, соответственно. Таким образом, как можно видеть из приведенных выше результатов, с использованием многофункционального растворителя в соответствии с настоящим изобретением возможно получать радиофармацевтические препараты высокой чистоты с высоким выходом и высокой эффективностью мечения.
Пример 12. Очистка [18F] фторпропилкарбометокситропана
Пример 12-1. Очистка с использованием твердофазной экстракции (ТФЭ)
Чтобы провести очистку (пример 12-1-1) [18F] фторпропилкарбометокситропана, полученного в примере 7-1, и очистку (пример 12-1-2) [18F] фторпропилкарбометокситропана, полученного в примере 7-2, продукты реакции разбавляют водой без выпаривания и подвергают очистке способом обращенно-фазовой твердофазной экстракции (ТФЭ) после завершения синтеза [18F] фторпропилкарбометокситропана, проводимого путем добавления прекурсора и растворителя, используемого в качестве реакционной среды, согласно примерам 7-1 и 7-2. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продуктов.
Пример 12-2. Очистка с использованием жидкостной хроматографии высокого разрешения (ЖХВР)
Чтобы провести очистку (пример 12-2-1) [18F] фторпропилкарбометокситропана, полученного в примере 7-1, и очистку (пример 12-2-2) [18F] фторпропилкарбометокситропана, полученного в примере 7-2, продукты реакции разбавляют водой без выпаривания и подвергают очистке способом жидкостной хроматографии высокого разрешения после завершения синтеза [18F] фторпропилкарбометокситропана, проводимого путем добавления прекурсора и растворителя, используемого в качестве реакционной среды, согласно примерам 7-1 и 7-2. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продуктов.
Результаты, полученные в примере 12, приведены в таблице 9.
Сравнительный пример 6. Очистка [18F] фторпропилкарбометокситропана
Сравнительный пример 6-1. Очистка с использованием твердофазной экстракции (ТФЭ)
Чтобы провести очистку (сравнительный пример 6-1-1) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 4-1, и очистку (сравнительный пример 6-1-2) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 4-2, продукты реакции разбавляют водой без выпаривания и подвергают очистке способом обращенно-фазовой твердофазной экстракции (ТФЭ) после завершения синтеза [18F] фторпропилкарбометокситропана, проводимого путем добавления прекурсора и растворителя, используемого в качестве реакционной среды, согласно сравнительным примерам 4-1 и 4-2. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продуктов.
Сравнительный пример 6-2. Очистка с использованием жидкостной хроматографии высокого разрешения (ЖХВР)
Чтобы провести очистку (сравнительный пример 6-2-1) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 4-1, и очистку (сравнительный пример 6-2-2) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 4-2, продукты реакции разбавляют водой без выпаривания и подвергают очистке способом жидкостной хроматографии высокого разрешения после завершения синтеза [18F] фторпропилкарбометокситропана, проводимого путем добавления прекурсора и растворителя, используемого в качестве реакционной среды, согласно сравнительным примерам 4-1 и 4-2. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продуктов.
Результаты, полученные в сравнительном примере 6, приведены в таблице 9.
Сравнительный пример 7. Очистка [l8F] фторпропилкарбометокситропана
Сравнительный пример 7-1. Очистка с использованием твердофазной экстракции (ТФЭ). Чтобы провести очистку (сравнительный пример 7-1-1) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 5-1, и очистку (сравнительный пример 7-1-2) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 5-2, продукты реакции разбавляют водой без выпаривания и подвергают очистке способом обращенно-фазовой твердофазной экстракции (ТФЭ) после завершения синтеза [18F] фторпропилкарбометокситропана, проводимого путем добавления прекурсора и растворителя используемого в качестве реакционной среды, согласно сравнительным примерам 5-1 и 5-2. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продукта.
Сравнительный пример 7-2. Очистка с использованием жидкостной хроматографии высокого разрешения (ЖХВР)
Чтобы провести очистку (сравнительный пример 7-2-1) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 5-1, и очистку (сравнительный пример 7-2-2) [18F] фторпропилкарбометокситропана, полученного в сравнительном примере 5-2, продукты реакции разбавляют водой без выпаривания и подвергают очистке способом жидкостной хроматографии высокого разрешения после завершения синтеза [18F] фторпропилкарбометокситропана, проводимого путем добавления прекурсора и растворителя, используемого в качестве реакционной среды, согласно сравнительным примерам 5-1 и 5-2. После очистки проводят жидкостную хроматографию высокого разрешения для определения чистоты продуктов.
Результаты, полученные в сравнительном примере 7, приведены в таблице 9.
Сравнительный пример 8. Очистка [18F] фторпропилкарбометокситропана
Сравнительный пример 8-1. Очистка с использованием твердофазной экстракции (ТФЭ)
Используют те же материалы и тот же способ, что и в сравнительных примерах 7-1-1 и 7-1-2, за исключением того, что [18F] фторпропилкарбометокситропан подвергают выпариванию после изготовления, а затем проводят очистку. Далее определяют выход и радиохимическую чистоту.
Сравнительный пример 8-2. Очистка с использованием жидкостной хроматографии высокого разрешения (ЖХВР)
Используют те же материалы и тот же способ, что и в сравнительных примерах 7-1-1 и 7-1-2, за исключением того, что [18F] фторпропилкарбометокситропан подвергают выпариванию после изготовления, а затем проводят очистку. Далее определяют выход и радиохимическую чистоту.
Результаты, полученные в сравнительном примере 8, приведены в таблице 9.


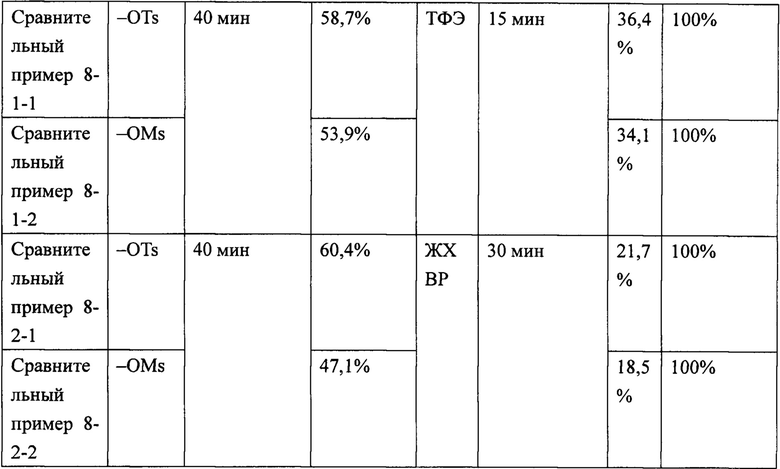
Как показано в табл. 9, когда согласно настоящему изобретению для изготовления [I8F] фторпропилкарбометокситропана используют многофункциональный растворитель, эффективность мечения, выход и радиохимическая чистота существенно выше, чем при использовании обычных растворителей - ацетонитрила (сравнительный пример 6) и трет-амилового спирта (сравнительный пример 7), даже если проводят последующую стадию очистки с использованием ТФЭ (пример 12-1) и ЖХВР (пример 12-2).
При этом многофункциональный растворитель согласно настоящему изобретению обеспечивает более высокий выход, когда очистку проводят с использованием ТФЭ (пример 12-1), а не с использованием ЖХВР (пример 12-2).
Между тем, в примере 12, в сравнительном примере бив сравнительном примере 7 не используют выпаривание, а очистку [I8F] фторпропилкарбометокситропана производят указанными способами. В сравнительном примере 8 проводят выпаривание, а затем производят очистку [18F] фторпропилкарбометокситропана указанными способами. В результате, в примере 8 наблюдается некоторое увеличение продолжительности синтеза из-за выпаривания по сравнению с теми примерами, где выпаривание не используется. При проведении выпаривания общая продолжительность синтеза увеличивается приблизительно на 15 минут.Выход снижается приблизительно на 50% по сравнению с примером 12 из-за потери радиоактивности во время выпаривания.
Пример 13. Способ обращенно-фазовой очистки [18F] фторпропилкарбометокситропана
При использовании для очистки обращенно-фазовой ТФЭ в примере 12-1 удается получать [I8F] фторпропилкарбометокситропан высокой радиохимической чистоты с высокой эффективностью мечения и высоким выходом. Однако после синтеза остаются примеси, имеющие такую же полярность, что и [18F] фторпропилкарбометокситропан. Поэтому способ обращенно-фазовой очистки используют, чтобы определить, удается ли выполнить очистку от подобных примесей.
Пример 13-1. Очистка с использованием обращенно-фазовой жидкостной хроматографии высокого разрешения (ЖХВР)
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления после синтеза [18F] фторпропилкарбометокситропана используют 8 мл 70% метанола. Разбавленную реакционную смесь подвергают очистке с использованием колонки С18. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 13-2. Очистка с использованием картриджа для обращенно-фазовой твердофазной (ТФЭ) экстракции на кремнеземной основе
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления после синтеза [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картридж С 18, чтобы [18F] фторпропилкарбометокситропан мог остаться в ТФЭ картридж С 18. Чтобы удалить остатки органического растворителя и полярные примеси, ТФЭ картридж С18 промывают водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картридже С18, элюируют этанолом в количестве не менее 2 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 13-3. Очистка с использованием картриджа для обращенно-фазовой твердофазной (ТФЭ) экстракции на полимерной основе
Для изготовления [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 7-2. Затем используют для очистки [18F] фторпропилкарбометокситропана те же материалы и тот же способ, что и в примере 13-2, за исключением того, что используют картридж ТФЭ типа HLB.
Результаты, полученные в примере 13, приведены в таблице 10.

Как показано в табл. 10, когда очистку проводят с использованием обращенно-фазовой ЖХВР на кремнеземной основе согласно примеру 13-1, степень удаления органических примесей, образовавшихся и прекурсора, достаточно высока. Однако в этом случае извлечение радиоактивности после очистки происходит слишком медленно и полученное соединение малопригодно в качестве радиофармацевтического препарата. Между тем, в примерах 13-2 и 13-3 извлечение радиоактивности происходит достаточно быстро, но степень удаления органических примесей, образовавшихся из прекурсора, чрезвычайно мала.
Пример 14. Очистка с использованием катионообменной ТФЭ на кремнеземной основе
Пример 14-1. Очистка с использованием катионообменного ТФЭ картриджа типа СМ на кремнеземной основе
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картридж типа СМ, чтобы удержать [I8F] фторпропилкарбометокситропан в ТФЭ картридже типа СМ. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджа типа СМ водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картридже типа СМ, элюируют этанолом в количестве не менее 2 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 14-2. Очистка с использованием катионообменного ТФЭ картриджа типа SCX на кремнеземной основе
Используют те же материалы и тот же способ, что и в примере 14-1, за исключением того, что в качестве картриджа для очистки [18F] фторпропилкарбометокситропана используют ТФЭ картридж типа SCX.
Пример 14-3. Очистка с использованием катионообменного ТФЭ картриджа типа WCX на кремнеземной основе
Используют те же материалы и тот же способ, что и в примере 14-1, за исключением того, что в качестве картриджа для очистки [18F] фторпропилкарбометокситропана используют ТФЭ картридж типа WCX.
Полученные в примере 14 результаты приведены в таблице 11.
Пример 15. Очистка с использованием катионообменной ТФЭ на полимерной основе
Пример 15-1. Очистка с использованием катионообменного ТФЭ картриджа типа МСХ на полимерной основе
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картридж типа МСХ, чтобы удержать [18F] фторпропилкарбометокситропан в ТФЭ картридже типа МСХ. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджа типа МСХ водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картридже типа МСХ, элюируют этанолом в количестве не менее 2 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 15-2. Очистка с использованием катионообменного ТФЭ картриджа типа WCX на полимерной основе
Используют те же материалы и тот же способ, что и в примере 15-1, за исключением того, что в качестве картриджа для очистки [18F] фторпропилкарбометокситропана используют ТФЭ картридж типа WCX.
Полученные в примере 15 результаты приведены в таблице 11.
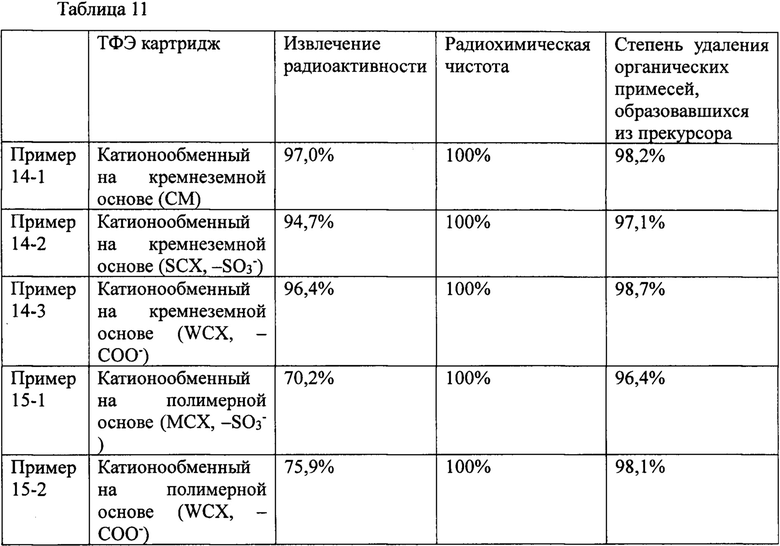
Как показано в табл. 11, при использовании катионообменных смол на кремнеземной основе и на полимерной основе, степень удаления органических примесей, образовавшихся из прекурсора составляет не менее 96% в обоих случаях. В примере 13 в табл. 10 можно видеть, что катионообменный ТФЭ картридж удаляет органические примеси, образовавшиеся из прекурсора, более эффективно, чем обращенно-фазовый ТФЭ картридж. Кроме того, когда очистку проводят с использованием катионообменного ТФЭ картриджа, коэффициент извлечения радиоактивности при ТФЭ на кремнеземной основе составляет не менее 95%, а коэффициент извлечения радиоактивности при ТФЭ на полимерной основе составляет не менее 70%, следовательно, эти соединения можно использовать в качестве радиофармацевтических препаратов в обоих случаях.
Пример 16. Очистка с использованием анионообменной ТФЭ на кремнеземной основе
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картридж типа SAX, чтобы удержать [18F] фторпропилкарбометокситропан в ТФЭ картридже типа SAX. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджа типа SAX водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картридже типа SAX, элюируют этанолом в количестве не менее 5 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Полученные в примере 16 результаты приведены в таблице 12.
Пример 17. Очистка с использованием анионообменной ТФЭ на полимерной основе
Пример 17-1. Очистка с использованием анионообменного ТФЭ картриджа типа МАХ на полимерной основе
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картридж типа МАХ, чтобы удержать [18F] фторпропилкарбометокситропан в ТФЭ картридже типа МАХ. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджа типа МАХ водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картридже типа МАХ, элюируют этанолом в количестве не менее 2 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 17-2. Очистка с использованием анионообменного ТФЭ картриджа типа WAX на полимерной основе
Используют те же материалы и тот же способ, что и в примере 17-1, за исключением того, что в качестве картриджа для очистки [18F] фторпропилкарбометокситропана используют ТФЭ картридж типа WAX.
Полученные в примере 17 результаты приведены в таблице 12.

Как показано в табл. 12, при использовании анионообменной смолы степень удаления органических примесей, образовавшихся из прекурсора, составляет не менее 87%, что несколько меньше, чем при использовании катионообменных смол согласно примерам 14 и 15 (см. табл. 11). Кроме того, коэффициент извлечения радиоактивности составляет от 70% до 98%, подобно тому, что наблюдается при использовании катионообменных смол в примерах 14 и 15.
Пример 18. Очистка с совместным использованием катионообмена и анионообмена
Пример 18-1. ТФЭ очистка с совместным использованием катионообмена и анионообмена
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картриджи типа SCX+SAX (два картриджа, соединенные друг с другом), чтобы удержать [18F] фторпропилкарбометокситропан в соединенных ТФЭ картриджах. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджей водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картриджах, элюируют этанолом в количестве не менее 2 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 18-2. ТФЭ очистка с совместным использованием катионообмена и анионообмена на полимерной основе
Используют те же материалы и тот же способ, что и в примере 7-2, за исключением того, что для разбавления [18F] фторпропилкарбометокситропана используют не менее 20 мл воды. Разбавленную реакционную смесь пропускают через ТФЭ картриджи типа МСХ+МАХ (два картриджа, соединенные друг с другом), чтобы удержать [18F] фторпропилкарбометокситропан в соединенных ТФЭ картриджах. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджей водой в количестве не менее 5 мл. Наконец, [18F] фторпропилкарбометокситропан, удержанный в ТФЭ картриджах, элюируют этанолом в количестве не менее 2 мл, чтобы провести его очистку. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Кроме того, после очистки используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Полученные в примере 18 результаты приведены в таблице 13.

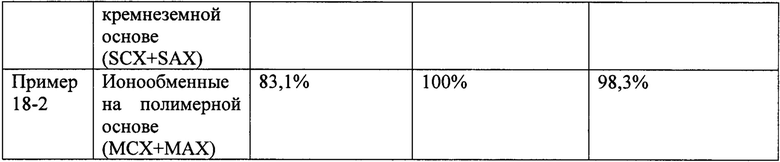
Как показано в таблице 13, виды и количество органических примесей, образовавшихся из прекурсора могут меняться в зависимости от условий мечения [18F] фторпропилкарбометокситропана [18F] фторидом (т.е. от основания и растворителя, используемого в качестве реакционной среды). Даже при одних и тех же условиях виды и количество органических примесей могут меняться в зависимости от характера радиофармацевтического препарата. Следовательно, органические примеси можно удалять более успешно, используя совместно катионообменный картридж и анионообменный картридж.
Пример 19. Очистка с использованием анионообменного ТФЭ картриджа на кремнеземной основе
Пример 19-1. Очистка после синтеза, проводившегося с использованием 1-метокси-2-метил-2-пропанола в качестве растворителя
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора (3-метансульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенилтропана) в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола -многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения при температуре 120°С и получают [18F] фторпропилкарбометокситропан.
Полученный [18F] фторпропилкарбометокситропан разбавляют водой в количестве не менее 20 мл. Разбавленную реакционную смесь пропускают через ТФЭ картриджи SCX+SAX (два картриджа, соединенные друг с другом), чтобы удержать [18F] фторпропилкарбометокситропан на соединенных ТФЭ картриджах. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку соединенных ТФЭ картриджей водой в количестве не менее 5 мл. Наконец, элюируют [18F] фторпропилкарбометокситропан из соединенных ТФЭ картриджей этанолом в количестве не менее 2 мл и разбавляют физиологическим раствором, чтобы получить [18F] фторпропилкарбометокситропан. Затем используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 19-2. Очистка после синтеза, проводившегося с использованием ацетонитрила в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 19-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл ацетонитрила.
Пример 19-3. Очистка после синтеза, проводившегося с использованием трет-амилового спирта в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 19-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл трет-амилового спирта.
Полученные в примере 19 результаты приведены в таблице 14.
Пример 20. Очистка с использованием ионообменного ТФЭ картриджа на полимерной основе
Пример 20-1. Очистка после синтеза, проводившегося с использованием 1-метокси-2-метил-2-пропанола в качестве растворителя
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора (3-метансульфонилоксипропил)-2-β-карбометокси-3-β-4-йодфенилтропан) в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения при температуре 120°С и получают [18F] фторпропилкарбометокситропан.
Полученный [18F] фторпропилкарбометокситропан разбавляют водой в количестве не менее 20 мл. Разбавленную реакционную смесь пропускают через ТФЭ картриджи МСХ+МАХ (два картриджа, соединенные друг с другом), чтобы удержать [18F] фторпропилкарбометокситропан на соединенных ТФЭ картриджах. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку соединенных ТФЭ картриджей водой в количестве не менее 5 мл. Наконец, элюируют [18F] фторпропилкарбометокситропан из соединенных ТФЭ картриджей этанолом в количестве не менее 2 мл и разбавляют физиологическим раствором, чтобы получить [18F] фторпропилкарбометокситропан. Затем используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 20-2. Очистка после синтеза, проводившегося с использованием ацетонитрила в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 20-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл ацетонитрила.
Пример 20-3. Очистка после синтеза, проводившегося с использованием трет-амилового спирта в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 20-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл трет-амилового спирта.
Полученные в примере 20 результаты приведены в таблице 14.
Сравнительный пример 9. Очистка с использованием обращенно-фазовой ЖХВР
Сравнительный пример 9-1. Очистка после синтеза, проводившегося с использованием 1-метокси-2-метил-2-пропанола в качестве растворителя
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора (3-метансульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенилтропана) в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения при температуре 120°С и получают [18F] фторпропилкарбометокситропан.
Полученный [18F] фторпропилкарбометокситропан разбавляют 70% метанолом в количестве 8 мл. Разбавленную реакционную смесь подвергают очистке способом ЖХВР с использованием колонки С18. Определяют эффективность мечения и радиоактивность реакционной смеси перед очисткой и радиоактивность [18F] фторпропилкарбометокситропана после очистки, чтобы установить степень извлечения радиоактивности. Затем [18F] фторпропилкарбометокситропан разбавляют водой в количестве не менее 20 мл. Разбавленную реакционную смесь пропускают через ТФЭ картридж С18, чтобы удержать [18F] фторпропилкарбометокситропан в ТФЭ картридже С18. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджа С18 водой в количестве не менее 5 мл. Наконец, элюируют [18F] фторпропилкарбометокситропан из ТФЭ картриджа С18 этанолом в количестве 2 мл и разбавляют физиологическим раствором, чтобы получить [18F] фторпропилкарбометокситропан. Затем используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Сравнительный пример 9-2. Очистка после синтеза, проводившегося с использованием ацетонитрила в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 9-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл ацетонитрила.
Сравнительный пример 9-3. Очистка после синтеза, проводившегося с использованием трет-амилового спирта в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 9-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл трет-амилового спирта.
Полученные в примере 9 результаты приведены в таблице 14.
Сравнительный пример 10. Очистка с использованием обращенно-фазового ТФЭ картриджа
Сравнительный пример 10-1. Очистка после синтеза, проводившегося с использованием 1-метокси-2-метил-2-пропанола в качестве растворителя
На носитель четвертичной аммониевой соли (Chromafix или QMA) адсорбируют [18F] фторид путем пропускания через него [18F] фторида, чтобы провести ионообмен, а [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, элюируют смешанным раствором метансульфоната калия, имеющим контролируемый рН, в реакционный контейнер. После элюирования элюент полностью удаляют путем азеотропной отгонки, подавая азот при температуре 100°С.
Согласно настоящему изобретению, в реакционный контейнер подают в качестве прекурсора 0,1 мл раствора (3-метансульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенилтропана) в ацетонитриле и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя, используемого в качестве реакционной среды. Затем проводят реакцию мечения при температуре 120°С и получают [18F] фторпропилкарбометокситропан.
Полученный [18F] фторпропилкарбометокситропан разбавляют водой в количестве не менее 20 мл. Разбавленную реакционную смесь пропускают через ТФЭ картридж С18, чтобы удержать [18F] фторпропилкарбометокситропан на ТФЭ картридже С18. Чтобы удалить остатки органического растворителя и полярные примеси, проводят промывку ТФЭ картриджа С18 водой в количестве не менее 5 мл. Наконец, элюируют [18F] фторпропилкарбометокситропан из ТФЭ картриджа С18 этанолом в количестве не менее 2 мл и разбавляют физиологическим раствором, чтобы получить [18F] фторпропилкарбометокситропан. Затем используют жидкостную хроматографию высокого разрешения для определения радиохимической чистоты и степени удаления органических примесей, образовавшихся из прекурсора.
Пример 10-2. Очистка после синтеза, проводившегося с использованием ацетонитрила в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 10-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл ацетонитрила.
Сравнительный пример 10-3. Очистка после синтеза, проводившегося с использованием трет-амилового спирта в качестве растворителя
Для получения [18F] фторпропилкарбометокситропана используют те же материалы и тот же способ, что и в примере 10-1, за исключением того, что в качестве растворителя при проведении реакции используют 1 мл трет-амилового спирта.
Полученные в примере 10 результаты приведены в таблице 14.


Как показано в табл. 14, когда очистку [18F] фторпропилкарбометокситропана проводят с использованием ЖХВР, обеспечивается самая высокая степень удаления органических примесей. Однако в случае очистки с использованием ЖХВР начальная точка и конечная точка разделения задаются работниками, и результат может зависеть от количества использований ЖХВР колонки или от тщательности подготовки подвижной фазы. Иначе говоря, ЖХВР может приводить к разным результатам в зависимости от квалификации работника. В случае очистки с использованием ТФЭ работник не вмешивается в проведение очистки, поскольку ТФЭ полностью выполняется системой. Таким образом, ТФЭ очистка не подвержена влиянию квалификации работника и всегда обеспечивает воспроизводимость результатов, поэтому она более пригодна для изготовления радиофармацевтических препаратов. При этом используемая в настоящее время обратно-обращенная ТФЭ на С18 может обеспечить высокий выход и радиохимическую чистоту. Однако использовать обратно-обращенную ТФЭ на С18 для очистки [18F] фторпропилкарбометокситропана, требующего высокой удельной радиоактивности (мКи/мкмоль), затруднительно. С другой стороны, при использовании катионообменного и анионообменного картриджей можно удалить большинство ионогенных органических примесей. Таким образом, удается удалить большую часть органических примесей, образовавшихся из прекурсора.
Ниже приведено более подробное описание способа изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, согласно одному из вариантов осуществления изобретения.
На фиг. 1 приведено схематичное изображение процесса получения радиофармацевтического препарата, проводимого с использованием кассеты, содержащей реакционный контейнер, предотвращающий противоточное движение жидкости, согласно одному из вариантов осуществления изобретения.
Предотвращающий противоточное движение жидкости реакционный контейнер 10 согласно настоящему варианту осуществления содержит первую трубку 11, по которой подают реагенты, используемые для синтеза радиофармацевтического препарата, и вторую трубку 13 для создания разрежения внутри реакционного контейнера. Первая трубка 11 присоединена к входным патрубкам для подачи каждого реагента, в том числе раствора, содержащего [18F] фторид, прекурсор для радиофармацевтического препарата и растворитель, используемый в качестве реакционной среды при мечении прекурсора [18F] фторидом, и к патрубку в виде коллектора для подачи азота или воздуха, что определяет форму кассеты. Следовательно, кассета может содержать один коллектор или несколько коллекторов. Кассета, используемая для изготовления радиофармацевтического препарата, может иметь и другие известные составные части, при условии, что реакционный контейнер для изготовления радиофармацевтического препарата представляет собой реакционный контейнер, предотвращающий противоточное движение жидкости, согласно настоящему изобретению.
Конечная точка Е первой трубки 11 расположена на такой высоте, чтобы она находилась на некотором расстоянии от дна предотвращающего противоточное движение жидкости реакционного контейнера 10. Предпочтительно, конечная точка Е первой трубки 11 расположена на такой высоте, чтобы она находилась на определенном расстоянии от поверхности материалов, подаваемых в предотвращающий противоточное движение жидкости реакционный контейнер 10. Более предпочтительно, если расстояние между конечной точкой Е первой трубки 11 и поверхностью всех реагентов, загруженных в предотвращающий противоточное движение жидкости реакционный контейнер 10 для синтеза радиофармацевтического препарата, составляет не более 5 см. Иначе говоря, конечная точка Е первой трубки 11 может находиться на высоте от 0 см до 5 см над поверхностью всех реагентов, подаваемых в предотвращающий противоточное движение жидкости реакционный контейнер 10 для синтеза радиофармацевтического препарата.
Как показано на фиг. 1, конечная точка Е первой трубки 11 расположена на высоте, отстоящей от нижней поверхности предотвращающего противоточное движение жидкости реакционного контейнера 10 на заранее определенное расстояние, а содержащий F-18 раствор 20 подают по первой трубке 11 (поз. А на фиг. 1). Поскольку конечная точка Е первой трубки 11 расположена на заранее определенном расстоянии от нижней поверхности предотвращающего противоточное движение жидкости реакционного контейнера 10, содержащий F-18 раствор 20 поступает ровной струей без разбрызгивания (поз. В на фиг. 1), так что раствор может стабильно подаваться на дно предотвращающего противоточное движение жидкости реакционного контейнера 10 (поз. С на фиг. 1). Когда же азот или воздух подают по первой трубке 11 для выпаривания содержащего F-18 раствора, поданного в реакционный контейнер (поз. D на фиг. 1), в содержащем F-18 растворе пузырьки не образуются, поскольку конечная точка Е первой трубки расположена на определенном расстоянии от дна предотвращающего противоточное движение жидкости реакционного контейнера 10. Таким образом, удается избежать разбрызгивания содержащего F-18 раствора по стенкам предотвращающего противоточное движение жидкости реакционного контейнера 10 (поз. Е на фиг. 1). После выпаривания содержащего F-18 раствора 20 по первой трубке 11 подают прекурсор 30 радиофармацевтического препарата. Аналогично, прекурсор 30 радиофармацевтического препарата поступает на содержащий F-18 раствор 20 ровной струей без разбрызгивания (поз. F и G на фиг. 1). Затем по трубке 11 подают растворитель 40, используемый в качестве реакционной среды, чтобы провести реакцию мечения прекурсора радиофармацевтического препарата фтором-18. При проведении этой реакция конечная точка Е первой трубки 11 расположена на высоте, отстоящей на заранее определенное расстояние от поверхности всех реагентов, подаваемых в предотвращающий противоточное движение жидкости реакционный контейнер 10, так что растворитель 40 не подвергается противоточному движению в первую трубку 11 даже в том случае, когда температура при проведении реакции мечения повышается до 100-140°С. Таким образом, растворитель может принимать участие в реакции мечения в том количестве, в котором он подан в предотвращающий противоточное движение жидкости реакционный контейнер 10. В результате удается стабильно изготавливать радиофармацевтический препарат и повысить его выход. Кроме того, поскольку растворитель 40 не подвергается противоточному движению в первую трубку 11, растворитель 40 не проникает в кассету, к которой присоединен другой участок первой трубки 11, не имеющий конечной точки Е, и кассета не подвергается повреждению под действием растворителя 40.
Для сопоставления с настоящим изобретением далее дано описание способа изготовления радиофармацевтического препарата, проводимого с использованием кассеты, содержащей обычный реакционный контейнер. На фиг. 2 приведено схематичное изображение процесса получения радиофармацевтического препарата, проводимого с использованием кассеты, содержащей обычный реакционный контейнер. Как показано на фиг. 2, конечная точка Еа трубки Па подачи реагентов, предназначенной для подачи и отвода реагентов, установлена таким образом, что доходит до дна реакционного контейнера 10а, чтобы увеличить коэффициент извлечения (поз. А на фиг. 2). Следовательно, когда содержащий F-18 раствор подают по трубке 11а подачи реагентов, содержащий F-18 раствор 20а разбрызгивается по стенкам реакционного контейнера 10а (поз. В на фиг. 2) и некоторое количество содержащего F-18 раствора остается на стенках реакционного контейнера 10а (поз. С на фиг. 2). Кроме того, когда по трубке Па подачи реагентов подают азот или воздух в содержащий F-18 раствор 20а для выпаривания, в нем образуются воздушные пузырьки (поз. D на фиг. 2). Из-за этого содержащий F-18 раствор еще сильнее разбрызгивается по стенкам реакционного контейнера (поз. Н на фиг. 2). Это происходит потому, что трубка Па подачи реагентов соприкасается с дном реакционного контейнера 10а. После этого по трубке 11а подачи реагентов нагнетают растворитель 40а, используемый в качестве реакционной среды, чтобы провести мечение прекурсора радиофармацевтического препарата фтором-18. Обычно подобное мечение проводят при температуре 100-140°С, которая превышает температуру кипения растворителя 40а, используемого в качестве реакционной среды. В результате растворитель 40а испаряется, создавая повышенное давление и вызывая противоточное движение растворителя 40а в трубку 11а подачи реагентов, так что некоторое количество растворителя 40а не участвует в реакции мечения (поз. I на фиг. 2). Другой участок трубки 11а подачи реагентов, не имеющий конечной точки Еа, подключен к кассете, и кассета может повреждаться при проведении вышеуказанного процесса, если только кассета не обладает стойкостью к растворителю 40а, причем степень стойкости зависит от типа кассеты. В этом случае невозможно использовать все предназначенные для реакции материалы, что приводит к нарушению процесса изготовления радиофармацевтического препарата.
Таким образом, когда радиофармацевтический препарат изготавливают с использованием кассеты, содержащей предотвращающий противоточное движение жидкости реакционный контейнер 10, согласно настоящему изобретению, растворитель, используемый в качестве реакционной среды, не подвергается противоточному движению в первую трубку 11 и тем самым решается проблема повреждения кассеты, возникающая из-за подобного противотока. Кроме того, отсутствует потребность в разработке материала для изготовления кассеты, стойкого к используемому в качестве реакционной среды растворителю, что снижает ее стоимость. При этом большая часть используемого в качестве реакционной среды растворителя может принимать участие в реакции мечения, что повышает выход радиофармацевтического препарата. Более того, удается обеспечить изготовление радиофармацевтического препарата с соблюдением правил надлежащей производственной практики (GMP).
Как показано на фиг. 1, растворитель, используемый в качестве реакционной среды, при изготовлении радиофармацевтического препарата с использованием кассеты, содержащей предотвращающий противоточное движение жидкости реакционный контейнер 10, согласно настоящему изобретению, может содержать любое из следующего: апротонные растворители, протонные растворители и многофункциональные растворители.
Апротонный растворитель может содержать любое из следующего: ацетонитрил, диметилформамид и диметилсульфоксид.
Протонный растворитель может содержать любое вещество из группы, состоящей из следующего: первичные спирты, в том числе метанол, этанол, н-пропанол, н-бутанол, н-амиловый спирт, н-гексиловый спирт, н-гептанол и н-октанол; вторичные спирты, в том числе изопропанол, изобутанол, изоамиловый спирт и 3-пентанол; и третичные спирты, в том числе трет-бутанол, трет-амиловый спирт, 2,3-диметил-2-бутанол, 2-(трифторметил)-2-пропанол, 3-метил-3-пентанол, 3-этил-3-пентанол, 2-метил-2-пентанол, 2,3-диметил-3-пентанол, 2,4-диметил-2-пентанол, 2-метил-2-гексанол, 2-циклопропил-2-пропанол, 2-циклопропил-2-бутанол, 2-циклопропил-3-метил-2-бутанол, 1-метилциклопентанол, 1-этилциклопентанол, 1-пропилциклопентанол, 1-метилциклогексанол, 1-этилциклогексанол и 1-метилциклогептанол.
Многофункциональный растворитель может представлять собой соединение, имеющее химическую формулу 1:
(химическая формула 1)
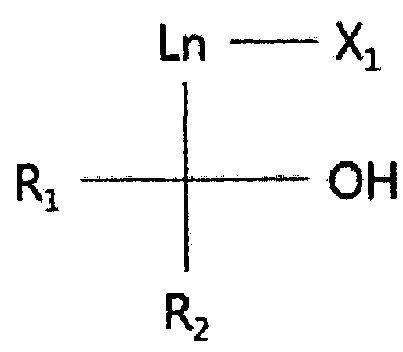
где каждая из групп R1 и R2 независимо друг от друга представляет собой Н, C1-C10-алкильную группу или ту же функциональную группу, что и группа X1;
группа Ln представляет собой C1-C10-алкильную группу или полиэтиленгликолевую группу СН2(OCH2CH)n, где n является целым числом в диапазоне 1-10; и
группа X1 представляет собой полярную группу, выбранную из следующего: алкоксильная группа (OR3), нитрильная группа (CN) и галоид;
при этом Ln предпочтительно представляет собой C1-C3-алкильную группу или полиэтиленгликолевую группу СН2(OCH2CH2)n, где n является целым числом в диапазоне 1-3.
Предпочтительно, алкоксильная группа выбрана из следующего: метокси-, этокси-, пропокси-, изопропокси- и трет-бутоксигруппы.
Предпочтительно, галоид выбран из следующего: хлорид (Cl), бромид (Br) и йодид (I).
Предпочтительно, каждая из групп R1 и R2 представляет собой метил или этил.
Предпочтительно, многофункциональный растворитель, имеющий химическую формулу 1, выбран из группы, состоящей из следующего: 1-метокси-2-метил-2-пропанол, 1-этокси-2-метил-2-пропанол, 1-пропокси-2-метил-2-пропанол, 1-изопропокси-2-метил-2-пропанол, 1-трет-бутокси-2-метил-2-пропанол, 1-нитрил-2-метил-2-пропанол, 1-хлор-2-метил-2-пропанол, 1-бром-2-метил-2-пропанол, 1-йод-2-метил-2-пропанол, 1-(2-метоксиэтокси)-2-метил-2-пропанол и 3-(метоксиметил)-3-пентанол.
Таким образом, способ изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер 10, предотвращающий противоточное движение жидкости, согласно настоящему изобретению, включает в себя стадии элюирования [18F] фторида через предотвращающий противоточное движение жидкости реакционный контейнер 10 (поз. А-С на фиг. 1); выпаривание элюента в предотвращающем противоточное движение жидкости реакционном контейнере 10 (поз. D и Е на фиг. 1); и подачи прекурсора радиофармацевтического препарата и используемого в качестве реакционной среды растворителя в предотвращающий противоточное движение жидкости реакционный контейнер, чтобы выпаренный [18F] фторид мог вступить в реакцию с прекурсором радиофармацевтического препарата в присутствии используемого в качестве реакционной среды растворителя (поз. F-H на фиг. 1). Например, стадию элюирования проводят, пропуская [18F] фторид через носитель четвертичной аммониевой соли (Chromafix или QMA) для проведения ионообмена и элюируя [18F] фторид, адсорбированный на носителе четвертичной аммониевой соли, в предотвращающий противоточное движение жидкости реакционный контейнер 10 смешанным раствором метансульфоната калия, имеющим контролируемый рН. Стадию выпаривания проводят, подавая азот или воздух по первой трубке 11 при определенной температуре, например, 100-140°С. Стадию проведения реакции проводят, вводя прекурсор радиофармацевтического препарата и растворитель, используемый в качестве реакционной среды, по первой трубке 11, чтобы обеспечить реакцию при температуре 100-140°С с получением радиофармацевтического препарата, меченного фтором F-18. После синтеза этот способ может дополнительно включать в себя стадию очистки, проводимой с использованием твердофазной экстракции (ТФЭ) или жидкостной хроматографии высокого разрешения (ЖХВР). При использовании твердофазной экстракции (ТФЭ) или жидкостной хроматографии высокого разрешения (ЖХВР), этот способ возможно осуществлять согласно одному из примеров 12-19. Кроме того, стадии элюирования, выпаривания, синтеза и очистки можно осуществлять с использованием методов, обычно применяемых при изготовлении радиофармацевтических препаратов.
Способ изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер 10, предотвращающий противоточное движение жидкости, согласно настоящему изобретению, можно использовать для изготовления любых органических соединений, меченных фтором F-18.
Так, соль фтора, используемая здесь в качестве источника фторида F-18, представляет собой соединение, содержащее фтор-18, и может быть выбрана из следующего: фториды щелочного металла, содержащие щелочной металл, выбранный из группы, состоящей из следующего: литий, натрий, калий, рубидий и цезий; фториды щелочноземельного металла, содержащие щелочноземельный металл, выбранный из группы, состоящей из следующего: магний, кальций, стронций и барий; и фториды аммония. Более предпочтительно, соль фтора представляет собой фторид калия или фторид аммония. Фторид щелочного металла, содержащий калий, или фторид тетраалкиламмония предпочтительно адсорбируют на носитель, выбранный из следующего: Целит, молекулярные сита, глинозем и силикагель. Предпочтительно фторид аммония может быть выбран из группы, состоящей из следующего: фториды четвертичного аммония, в том числе фторид тетрабутиламмония и фторид бензилтриметиламмония; фториды третичного аммония, в том числе фторид триэтиламмония и фторид трибутиламмония; фториды вторичного аммония, в том числе фторид дибутиламмония и фторид дигексиламмония; и фториды первичного аммония, в том числе фторид бутиламмония и фторид гексиламмония. Более предпочтительно, фторид аммония представляет собой фторид тетрабутиламмония. Соль фтора может использоваться в количестве от 1 пг до 10 нг [18F] фторида на миллиграмм прекурсора радиофармацевтического препарата, описанного ниже.
Кроме того, используемый здесь прекурсор радиофармацевтического препарата предпочтительно может представлять собой алкилгалоид или алкилсульфонат. В алкилгалоиде или алкилсульфонате галоид выбран из Cl, Br и I, но не F, а сульфонат имеет формулу -SO3R12, где группа R12 является алкильной или арильной группой. В частности, алкильная группа представляет собой С1-С12-алкилсульфонат или С1-С12-галогеналкилсульфонат, а конкретные ее примеры выбраны из группы, состоящей из следующего: метансульфонат, этансульфонат, изопропансульфонат, хлорметансульфонат, трифторметансульфонат и хлорэтансульфонат. Кроме того, арильную группу предпочтительно выбирают из следующего: фенил, С1-С4-алкилфенил, галогенфенил, C1-C4-алкоксифенил и нитрофенил, а конкретными ее примерами являются метилфенилсульфонат, этилфенилсульфонат, хлорфенилсульфонат, бромфенилсульфонат, метоксифенилсульфонат и нитрофенилсульфонат. Кроме того, используемый здесь прекурсор радиофармацевтического препарата может представлять собой алифатическое соединение, имеющее замещаемую группу, которое используется в способе изготовления фторзамещенного органического алифатического соединения в примерах 1-11.
Например, радиофармацевтический препарат, который можно получить в соответствии со способом изготовления радиофармацевтического препарата с использованием кассеты, содержащей реакционный контейнер 10, согласно настоящему изобретению, может быть выбран из группы, состоящей из следующих радиофармацевтических препаратов:
[18F] фторпропилкарбометокситропан 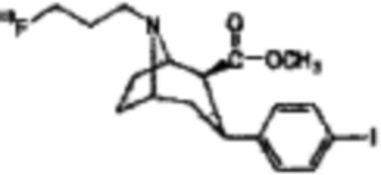
[18F] фтормизонидазол 
[18F] фтортимидин 
[18F] фторэстрадиол 
[18F] фтордезоксиглюкоза 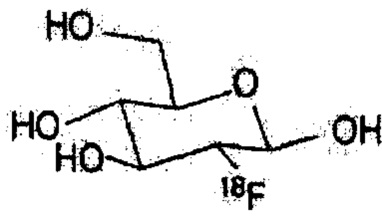
[18F] фтордиазодинитрофенол 
[18F] флорбетабен 
[18F] флорбетапир 
[I8F] FHBG 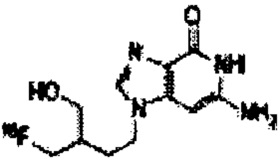
[18F] HX4 
[18F] LBT999 
[18F] флутеметамол 
и [18F] FC119S 
Далее настоящее изобретение описано более подробно со ссылкой на следующие примеры. Однако эти примеры лишь поясняют сущность изобретения и не служат для ограничения объема изобретения. Специалистам в данной области техники понятно, что в него могут быть внесены различные изменения, касающиеся формы и деталей, которые не выходят за пределы объема этого изобретения, определяемого прилагаемой формулой изобретения. Следовательно, предполагается, что в объем настоящего изобретения входят все варианты его осуществления в пределах сущности и объема прилагаемой формулы изобретения.
Примеры 21 и 22. Изготовление [18F] фторпропилкарбометокситропана
Предотвращающий противоточное движение жидкости реакционный контейнер 10, показанный на фиг. 1, помещают в кассету TRACERlab MXFDG (фирмы GE healthcare) и используют автоматизированную систему синтеза TRACERlab MX для получения [18F] фторпропилкарбометокситропана.
Сначала вводят 0,1 мл ацетонитрильного раствора, содержащего 4 мг (3-метансульфонилокси- пропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана или (3-толуолсульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана, и 1,0 мл 1-метокси-2-метил-2-пропанола - многофункционального растворителя в качестве реакционной среды. Затем проводят реакцию при температуре 120°С в течение 10-20 мин с получением [18F] фторпропилкарбометокситропана.
Примеры 23 и 24. Изготовление [18F] фторпропилкарбометокситропана
Предотвращающий противоточное движение жидкости реакционный контейнер 10, показанный на фиг. 1, помещают в кассету TRACERlab MXFDG (фирмы GE healthcare) и используют автоматизированную систему синтеза TRACERlab MX для получения [18F] фторпропилкарбометокситропана.
Сначала вводят 0,1 мл ацетонитрильного раствора, содержащего 4 мг (3-метансульфонилокси- пропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана или (3-толуолсульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана, и 1,0 мл трет-амилового спирта в качестве протонного растворителя. Затем проводят реакцию при температуре 120°С в течение 10-20 мин с получением [18F] фторпропилкарбометокситропана.
Примеры 25 и 26. Изготовление [18F] фторпропилкарбометокситропана
Предотвращающий противоточное движение жидкости реакционный контейнер 10, показанный на фиг. 1, помещают в кассету TRACERlab MXFDG (фирмы GE healthcare) и используют автоматизированную систему синтеза TRACERlab MX для получения [18F] фторпропилкарбометокситропана.
Сначала вводят 0,1 мл ацетонитрильного раствора, содержащего 4 мг (3-метансульфонилокси-пропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана или (3-толуолсульфонилоксипропил)-2-β-карбометокси-3-β-(4-йодфенил)тропана. Затем проводят реакцию при температуре 120°С в течение 10-20 мин с получением [18F] фторпропилкарбометокситропана.
Сравнительные примеры 11-16. Изготовление [18F] фторпропилкарбометокситропана Для получения [18F] фторпропилкарбометокситропана используют обычную кассету TRACERlab MXFDG (фирмы GE healthcare) с реакционным контейнером 10а, показанным на фиг. 2, и автоматизированную систему синтеза TRACERlab MX. Загружают те же реагенты и проводят реакцию в тех же условиях, что и в примерах 21-26.
В таблице 15 приведены полученные результаты, включая выход радиофармацевтического препарата, для каждого из примеров 21-26 и сравнительных примеров 11-16, а также указано, наблюдалось ли повреждение кассеты.

Как показано в таблице 15, когда радиофармацевтический препарат изготавливают с использованием предотвращающего противоточное движение жидкости реакционного контейнера согласно настоящему изобретению (примеры 21-26), удается получать радиофармацевтический препарат с неизменно высоким выходом без повреждения кассеты. В частности, даже при использовании ацетонитрила (примеры 25 и 26) удается получать радиофармацевтический препарат с выходом приблизительно 10%. В случае трет-амилового спирта (пример 23 и 24) ФП-КИТ получают с выходом 20-23%. В случае 1-метокси-2-метил-2-пропанола (пример 21 и 22) удается добиться высокого выхода 31-33%, увеличенного приблизительно на 10% благодаря сокращению продолжительности изготовления.
С другой стороны, когда радиофармацевтический препарат изготавливают с использованием обычного реакционного контейнера в том виде, как он есть, (сравнительные примеры 11-16), обычная кассета, не обладающая стойкостью против 1-метокси-2-метил-2-пропанола и трет-амилового спирта, повреждается из-за противотока растворителя во время проведения реакции, приводя к нарушению процесса изготовления радиофармацевтического препарата. Даже при использовании ацетонитрила в качестве реакционной среды выход составляет всего приблизительно 1-2%, поскольку реагенты не могут полностью участвовать в реакции, так что использовать обычный реакционный контейнер нецелесообразно.
Пример 27. Изготовление [18F] фтортимидина
Предотвращающий противоточное движение жидкости реакционный контейнер 10, показанный на фиг. 1, помещают в кассету TRACERlab MXFDG (фирмы GE healthcare) и используют автоматизированную систему синтеза TRACERlab MX для получения [18F] фтортимидина.
Сначала вводят 1,1 мл ацетонитрильного раствора, содержащего 5 мг 5'-O-диметокситрифенил-метил-2'-дезокси-3'-O-нозил-β-D-треопентофуранозил)-3-N-бутоксикарбонил-тимина. Затем проводят реакцию при температуре 120°С в течение 10-20 мин с получением [18F] фтортимидина.
Сравнительный пример 17. Изготовление [18F] фтортимидина
Для получения [18F] фтортимидина используют обычную кассету TRACERlab MXFDG (фирмы GE healthcare) с реакционным контейнером 10а, показанным на фиг. 2, и автоматизированную систему синтеза TRACERlab MX. Загружают те же реагенты и проводят реакцию в тех же условиях, что и в примере 27.
Пример 28. Изготовление [18F] фтормизонидазола Предотвращающий противоточное движение жидкости реакционный контейнер 10, показанный на фиг. 1, помещают в кассету TRACERlab MXFDG (фирмы GE healthcare) и используют автоматизированную систему синтеза TRACERlab MX для получения [18F] фтормизонидазола.
Сначала вводят 1,1 мл ацетонитрильного раствора, содержащего 1-2 мг 3-(2-нитроимидазол-1-ил)-2-O-тетрагидропиранил-1-О-толуолсульфонилпропандиола. Затем проводят реакцию при температуре 100°С в течение 10-20 мин с получением [18F] фтормизонидазола.
Сравнительный пример 18. Изготовление [18F] фтормизонидазола
Для получения [18F] фтормизонидазола используют обычную кассету TRACERlab MXFDG (фирмы GE healthcare) с реакционным контейнером 10а, показанным на фиг. 2, и автоматизированную систему синтеза TRACERlab MX. Загружают те же реагенты и проводят реакцию в тех же условиях, что и в примере 28.
Пример 29. Изготовление [18F] фторэстрадиола
Предотвращающий противоточное движение жидкости реакционный контейнер 10, показанный на фиг. 1, помещают в кассету TRACERlab MXFDG (фирмы GE healthcare) и используют автоматизированную систему синтеза TRACERlab MX для получения [18F] фторэстрадиола.
Сначала вводят 1,1 мл ацетонитрильного раствора, содержащего 0,5-1 мг 3-(метоксиметокси)-1,3,5(10)-гонатриен-16-β,17-β-диол-16,17-циклосульфата. Затем проводят реакцию при температуре 100°С в течение 10-20 мин с получением [18F] фторэстрадиола.
Сравнительный пример 19. Изготовление [18F] фторэстрадиола
Для получения [18F] фторэстрадиола используют обычную кассету TRACERlab MXFDG (фирмы GE healthcare) с реакционным контейнером 10а, показанным на фиг. 2, и автоматизированную систему синтеза TRACERlab MX. Загружают те же реагенты и проводят реакцию в тех же условиях, что и в примере 29.
В таблице 16 показан выход радиофармацевтического препарата для каждого из примеров 27-29 и для сравнительных примеров 17-19.


Как показано в табл. 16, когда используют прекурсор в небольшом количестве (0,5-5 мг), в сравнительных примерах 17-19 не все реагенты могут участвовать в реакции, что приводит к существенно сниженному выходу - приблизительно 1-3%. В примерах 27-29 все реагенты могут участвовать в реакции, что приводит к увеличению выхода радиофармацевтического препарата от 5 до 30 раз по сравнению с выходом в сравнительных примерах 17-19.
Несмотря на то, что настоящее изобретение описано на конкретных примерах его осуществления, для специалиста в данной области техники очевидно, что в него могут быть внесены различные изменения, не выходящие за пределы сущности и объема изобретения, определяемые следующей формулой изобретения и эквивалентами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РАДИОМЕЧЕНИЯ | 2014 |
|
RU2690848C2 |
| Способ получения флутеметамола | 2016 |
|
RU2733398C2 |
| СПОСОБ ПОЛУЧЕНИЯ [F]ФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В СПИРТОВЫХ РАСТВОРИТЕЛЯХ | 2005 |
|
RU2357947C2 |
| Способ радиоактивного мечения | 2014 |
|
RU2675371C2 |
| СПОСОБ ПРОИЗВОДСТВА ФТОРСОДЕРЖАЩЕГО ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ | 2021 |
|
RU2807182C1 |
| КОМПОЗИЦИЯ 18F- ФЛУЦИКЛОВИНА В ЦИТРАТНЫХ БУФЕРАХ | 2012 |
|
RU2623163C2 |
| НОВЫЕ ПРЕКУРСОРНЫЕ МОЛЕКУЛЫ ДЛЯ МЕЧЕННЫХ F-18 ПЭТ РАДИОАКТИВНЫХ ИНДИКАТОРОВ | 2010 |
|
RU2538276C2 |
| НУКЛЕОФИЛЬНОЕ ФТОРИРОВАНИЕ В ТВЕРДОЙ ФАЗЕ | 2002 |
|
RU2315769C9 |
| РАДИОФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2008 |
|
RU2475267C2 |
| АВТОМАТИЧЕСКИЙ СПОСОБ ВВЕДЕНИЯ РАДИОАКТИВНЫХ ИЗОТОПОВ | 2006 |
|
RU2459632C2 |
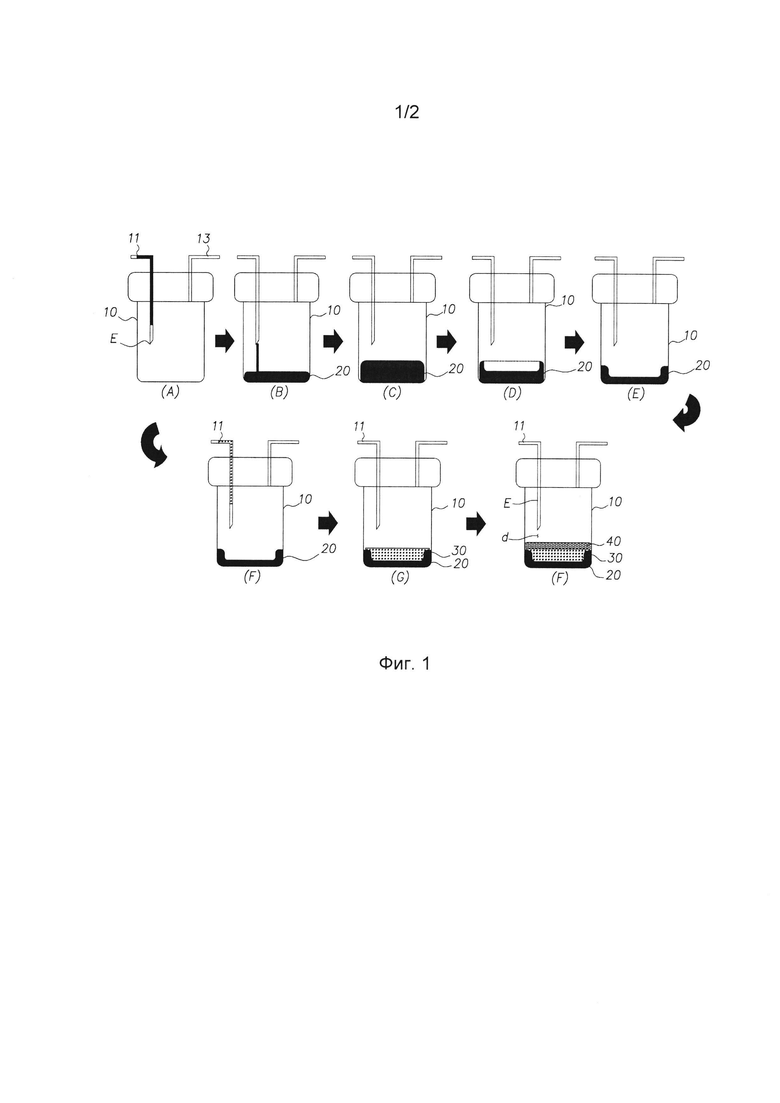
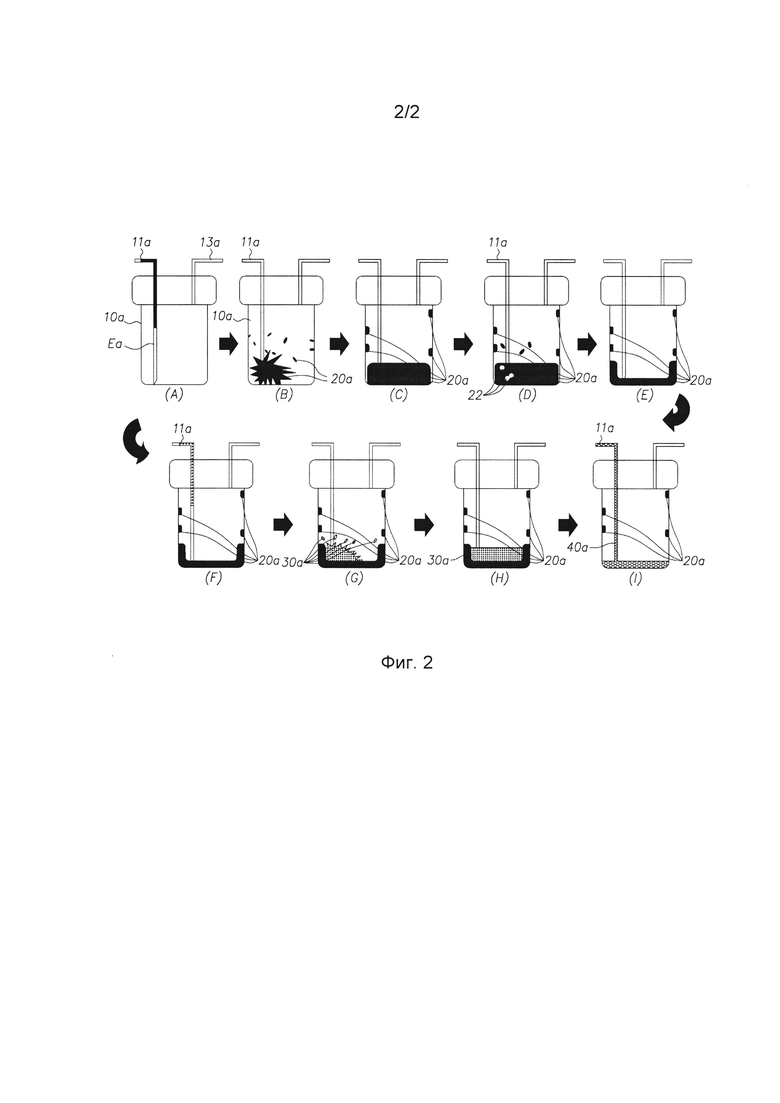
Изобретение относится к способу изготовления фторзамещенного органического алифатического соединения (в частности, [18F] фторпропилкарбометокситропан), пригодного для использования в качестве радиофармацевтического препарата, включающему в себя стадию обеспечения взаимодействия соли фтора с алифатическим соединением, содержащим замещаемую группу, с использованием многофункционального растворителя, имеющего химическую формулу 1, с получением алифатического соединения, меченного [18F] фторидом. При этом алифатическое соединение, содержащее замещаемую группу, имеет формулу N-(CH2)n-Х2 или O-(СН2)n-Х2, где группа Х2 является замещаемой группой, а n является целым числом в диапазоне 1-10, а соль фтора используется в качестве источника [18F] фторида, представляет собой соединение, содержащее фтор-18. Способ может дополнительно включать стадию очистки путем проведения твердофазной экстракции (ТФЭ) с использованием ионообменного ТФЭ картриджа формулы 2. Технический результат – высокие эффективность мечения, выход и чистота продукта. 3 н. и 22 з.п. ф-лы, 2 ил., 16 табл., 29 пр.
1. Способ изготовления фторзамещенного органического алифатического соединения, включающий в себя стадию обеспечения взаимодействия соли фтора с алифатическим соединением, содержащим замещаемую группу, с использованием многофункционального растворителя, имеющего химическую формулу 1, с получением алифатического соединения, меченного [18F] фторидом, замещающим замещаемую группу:
(химическая формула 1)
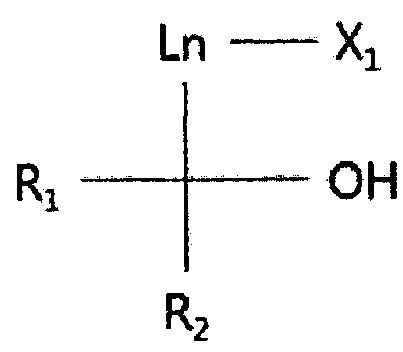 ,
,
где каждая из групп R1 и R2 независимо друг от друга представляет собой Н, C1-C10-алкильную группу или ту же функциональную группу, что и группа X1; группа Ln представляет собой C1-C10-алкильную группу или полиэтиленгликолевую группу СН2(ОСН2СН2)n, где n является целым числом в диапазоне 1-10; группа X1 представляет собой полярную группу, выбранную из следующего: алкоксильная группа (OR3), нитрильная группа (CN) и галоид, а группа R3 представляет собой C1-C10-алкильную группу.
2. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором Ln представляет собой C1-C10-алкильную группу или полиэтиленгликолевую группу CH2(ОСН2СН2)n, где n является целым числом в диапазоне 1-3.
3. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором алкоксильная группа (OR3) выбрана из следующего: метоксигруппа, этоксигруппа, пропоксигруппа, изопропоксигруппа и трет-бутоксигруппа.
4. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором галоид выбран из следующего: хлорид (Cl), бромид (Br) и йодид (I).
5. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором каждая из групп R1 и R2 является метильной группой или этильной группой.
6. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором многофункциональный растворитель, имеющий химическую формулу 1, выбран из группы, состоящей из следующего: 1-метокси-2-метил-2-пропанол, 1-этокси-2-метил-2-пропанол, 1-пропокси-2-метил-2-пропанол, 1-изопропокси-2-метил-2-пропанол, 1-трет-бутокси-2-метил-2-пропанол, 1-нитрил-2-метил-2-пропанол, 1-хлор-2-метил-2-пропанол, 1-бром-2-метил-2-пропанол, 1-йод-2-метил-2-пропанол, 1-(2-метоксиэтокси)-2-метил-2-пропанол и 3-(метоксиметил)-3-пентанол.
7. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором соль фтора, используемая в качестве источника [18F] фторида, представляет собой соединение, содержащее фтор-18.
8. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором алифатическое соединение представляет собой соединение, содержащее алкилгалоидную группу или алкилсульфонатную группу, причем галоидная группа или сульфонатная группа является замещаемой группой.
9. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором алифатическое соединение представляет собой соединение, содержащее алкилгалоидную группу или алкилсульфонатную группу, причем галоидная группа или сульфонатная группа является первичной замещаемой группой или вторичной замещаемой группой.
10. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, в котором алифатическое соединение имеет формулу N-(CH2)n-Х2 или O-(СН2)n-Х2, где группа Х2 является замещаемой группой, а n является целым числом в диапазоне 1-10.
11. Способ изготовления фторзамещенного органического алифатического соединения по п. 10, в котором группа Х2 является галоидной группой или сульфонатной группой.
12. Способ изготовления фторзамещенного органического алифатического соединения по любому из пп. 8, 9 и 11, в котором галоидная группа выбрана из группы, состоящей из следующего: Cl, Br и I.
13. Способ изготовления фторзамещенного органического алифатического соединения по любому из пп. 8, 9 и 11, в котором сульфонатная группа имеет формулу -SO3R12, где группа R12 выбрана из следующего: С1-С12-алкил, С1-С12-алкилгалоид, фенил, С1-С4-алкилфенил, галогенфенил, С1-С4-алкоксифенил и нитрофенил.
14. Способ изготовления фторзамещенного органического алифатического соединения по п. 1, дополнительно включающий в себя стадию очистки меченного [18F] фторидом алифатического соединения с использованием, по меньшей мере, одного ионообменного ТФЭ картриджа.
15. Способ изготовления фторзамещенного органического алифатического соединения по п. 14, в котором ионообменный ТФЭ картридж выбран из следующего: катионообменный ТФЭ картридж и анионообменный ТФЭ картридж.
16. Способ изготовления фторзамещенного органического алифатического соединения по п. 15, в котором ионообменный ТФЭ картридж содержит твердофазный носитель, включая полимер, содержащий фенильную группу и С1-С20-утлеводород, или кремнезем.
17. Способ изготовления фторзамещенного органического алифатического соединения по п. 16, в котором катионообменный ТФЭ картридж выбран из следующего: ТФЭ картридж SCX (сильный катионообменник на кремнеземе), ТФЭ картридж МСХ (сильный катионообменник на полимере) и ТФЭ картридж WCX (слабый катионообменник на полимере).
18. Способ изготовления фторзамещенного органического алифатического соединения по п. 16, в котором анионообменный ТФЭ картридж выбран из следующего: ТФЭ картридж SAX (сильный анионообменник на кремнеземе), ТФЭ картридж МАХ (сильный анионообменник на полимере) и ТФЭ картридж WAX (слабый анионообменник на полимере).
19. Способ очистки фторзамещенного органического алифатического соединения по п.1, включающий в себя стадию очистки фторзамещенного органического алифатического соединения путем проведения твердофазной экстракции (ТФЭ) с использованием ионообменного ТФЭ картриджа, имеющего химическую формулу 2:
(химическая формула 2)
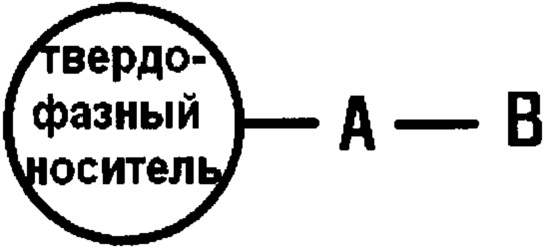 ,
,
где твердофазный носитель представляет собой полимер, содержащий фенильную группу и C1-С20-углеводород, или кремнезем;
группа А может отсутствовать, когда твердофазный носитель является полимером, или представляет собой фенил либо С1-C20-углеводородную группу, когда твердофазный носитель является кремнеземом; и
группа В может представлять собой органический катион или органический анион,
причем органический катион имеет формулу  , где Е представляет собой азот или фосфор, группы R1, R2 и R3 могут быть одинаковыми или могут отличаться друг от друга и каждая из них выбрана из C2-С20-гетероароматических катионов, имеющих формулу
, где Е представляет собой азот или фосфор, группы R1, R2 и R3 могут быть одинаковыми или могут отличаться друг от друга и каждая из них выбрана из C2-С20-гетероароматических катионов, имеющих формулу 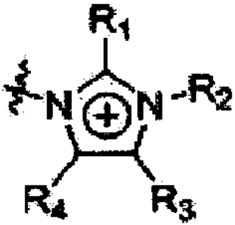 и
и 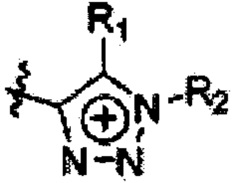 и содержащих C1-С20-углеводородную группу, арильную группу, содержащую, по меньшей мере, один атом азота, азот и кислород или азот и серу, а также содержащую С1-C20-углеводородную группу в качестве заместителя у одного атома азота, а органический анион является анионом сульфоновой кислоты (-SO3-) или карбоновой кислоты (-СОО-).
и содержащих C1-С20-углеводородную группу, арильную группу, содержащую, по меньшей мере, один атом азота, азот и кислород или азот и серу, а также содержащую С1-C20-углеводородную группу в качестве заместителя у одного атома азота, а органический анион является анионом сульфоновой кислоты (-SO3-) или карбоновой кислоты (-СОО-).
20. Способ очистки фторзамещенного органического алифатического соединения по п. 19, в котором очистку фторзамещенного органического алифатического соединения проводят используя ионообменный ТФЭ картридж, имеющий химическую формулу 2, где группа В является органическим катионом, в сочетании с ионообменным ТФЭ картриджем, имеющим химическую формулу 2, где группа В является органическим анионом.
21. Способ очистки фторзамещенного органического алифатического соединения по п.1, включающий в себя стадию очистки фторзамещенного органического алифатического соединения путем проведения твердофазной экстракции (ТФЭ) с использованием, по меньшей мере, одного ионообменного ТФЭ картриджа, причем фторзамещенное органическое алифатическое соединение представляет собой [18F] фторпропилкарбометокситропан.
22. Способ очистки фторзамещенного органического алифатического соединения по п. 21, в котором ионообменный ТФЭ картридж выбран из следующего: катионообменный ТФЭ картридж и анионообменный ТФЭ картридж.
23. Способ очистки фторзамещенного органического алифатического соединения по п. 22, в котором ионообменный ТФЭ картридж содержит твердофазный носитель, включая полимер, содержащий фенильную группу и С1-С20-углеводород, или кремнезем.
24. Способ очистки фторзамещенного органического алифатического соединения по п. 23, в котором катионообменный ТФЭ картридж выбран из следующего: ТФЭ картридж SCX (сильный катионообменник на кремнеземе), ТФЭ картридж МСХ (сильный катионообменник на полимере) и ТФЭ картридж WCX (слабый катионообменник на полимере).
25. Способ очистки фторзамещенного органического алифатического соединения по п. 23, в котором анионообменный ТФЭ картридж выбран из следующего: ТФЭ картридж SAX (сильный анионообменник на кремнеземе), ТФЭ картридж МАХ (сильный анионообменник на полимере) и ТФЭ картридж WAX (слабый анионообменник на полимере).
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| СПОСОБ ПОЛУЧЕНИЯ [F]ФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В СПИРТОВЫХ РАСТВОРИТЕЛЯХ | 2005 |
|
RU2357947C2 |
Авторы
Даты
2019-12-27—Публикация
2015-11-06—Подача