Область техники
Изобретение относится к биотехнологии и медицине. Более подробно изобретение относится к области создания и применения в хирургии биорезорбируемых, биосовместимых биополимерных структур в виде трубок, полученных фотоотверждением смеси метакрилированного производного желатина и метакрилированного производного фиброина шелка Bombyx mori и предназначенных для закрытия анастомоза с целью повышения состоятельности.
Уровень техники
Благодаря достижению современной анестезиологии и реанимации, количество реконструктивных операций на органах брюшной полости растет с каждым днем. Но, несмотря на это, процент осложнений, таких как несостоятельность анастомозов достигает 20%, а летальность при этом осложнении может достигать 80%. В настоящее время для решения данной проблемы предложено большое количество профилактических мероприятий, таких как превентивные стомы, защита анастомоза изнутри и снаружи, интубация зоны анастомоза. Сущность всех этих методов сводится к повышению прочности, герметичности анастомоза и снижению нагрузки на сформированный анастомоз.
Учитывая большой спектр профилактических мероприятий несостоятельности анастомозов желудочно-кишечного тракта перспективным является использование подходов регенеративной медицины для решения данной проблемы.
Впервые упоминание об ушивании кишечной раны появилось около 2000 лет до нашей эры. Первые операции в Европе, при повреждении кишечника, были связаны с использованием методики перчаточников. Сущность данного метода заключалась в сшивании кишечных стенок непрерывным обвивным швом. При этом концы нитей не срезались, а выводились через рану брюшной стенки, а сшитый фрагмент фиксировался к париетальной брюшине. Нить извлекалась тогда, когда цирюльник считал это безопасным [Гординский М.Б. К столетию Лемберовского кишечного шва. Новый хирургический архив, 1926, 11, 3, 270-273]. В XVII веке для восстановления пассажа по кишечнику, кроме сшивания краев кишечной трубки, улучшение результатов лечения пытались достичь путем введения внутрипросветных стентов (Lanfrank). Кишечный анастомоз в то время был очень редкой и опасной операцией. Основным методом лечения на тот момент являлось формирование кишечного свища с последующим его закрытием (Paracelsus, La Peyronie, В. Bell). Такой подход оставался до середины XIX века [Однорядный непрерывный шов анастомозов в абдоминальной хирургии. Под редакцией Егиева В.Н. - М.: Медиапрактика-М, 2002, с. 6-12].
В 1824 году Jobert А. предложил узловой однорядный, сквозной инвагинирующий кишечный шов. Позже Lambert А., в 1826 году - однорядный узловой, инвертирующий шов с узлами на серозе.
Одним из первых этот шов модернизировал Пирогов Н.И. и описал методику прецизионного серозно-мышечно-подслизистого экстрамукозного кишечного шва [Burch, J.M. Single-layer continuous versus two-layer interrupted intestinal anastomosis: a prospective randomized trial / J.M. Burch, R.J. Franciose, E.E. Moore // Ann. Surg. - 2000. -Vol. 231, N 6. - P. 832-837].
Однорядный кишечный шов прошел через множество модификаций, но низкое качество шовного материала того времени приводило к частым осложнениям.
Параллельно с методикой совершенствования однорядного шва развивалась техника механического соединения органов. В XVIII веке Du Verger для стентирования анастомоза применял гусиную трахею, в XIX веке применялись цилиндры из картона, смоченный маслом или эссенцией (Sabatier), Watson предложил каучуковый стент.
В дальнейшем были разработаны и применены в клинике компрессионные механизмы, данные устройства давали хороший результат при использовании их на тонкой кишке. При использовании данной методики на толстой кишке летальность достигала 50%. В 1908 году V. Fisher разработал первый сшивающий аппарат. Н. Hult в 1908 году сообщил о применении данного устройства для пересечения желудка с формированием линейного скобочного шва [Гординский М.Б. К столетию Лемберовского кишечного шва. Новый хирургический архив, 1926, 11, 3, 270-273]. В 1951 году в СССР был открыт НИИ хирургических аппаратов и инструментов, где были созданы компрессионые аппраты АКА [Каншин Н.Н., Горский В.А., Куприков С.В. и др. // Современные достижения и новые технологии в хирургии: Сб. науч. тр. - М., 2005. - С. 67-72]. В настоящее время сшивающие аппараты заняли определенную нишу в современной хирургии, но полностью перекрыть потребности абдоминальной хирургии в настоящее время не могут.
В связи с этим фактором в начале XX века появилась методика двурядного кишечного шва, которая стала основным методом соединением полых органов. Дальнейшие исследования двурядных межкишечных анастомозов показали, что заживление их происходит вторичным натяжением [Семенов Г.М. Хирургический шов / Г.М. Семенов, В.Л. Петришин, М.В. Ковшова. - 2-е изд. - СПб.: Питер, 2006. - 256 с.]. Споры о рядности кишечного шва остаются актуальными по настоящее время, так как ни один из предложенных методов не дает отсутствие осложнений на 100%.
«Кишечный шов» является термином, который объединяет в себе все виды швов, используемых для восстановления полых органов брюшной полости.
Причины развития несостоятельности кишечного шва многообразны, ведущими из них является: особенности строение стенки анастомозируемых органов, нарушение техники наложения швов, несовершенство шовного материала, воздействие патогенной микрофлоры, возраст больного, нарушение гомеостаза, наличие сопутствующей патологии.
Учитывая высокую актуальность проблемы несостоятельности анастомозов и высокую летальность при развитии данного осложнения, в настоящее время активно разрабатываются и вводятся в практику разные способы профилактики несостоятельности анастомозов. Все профилактические мероприятия направлены на повышение прочности, герметичности формируемых анастомозов и снижение нагрузки на сформированный анастомоз.
Для достижения данных целей в настоящее время используются следующие мероприятия: превентивные стомы, изделия, направленные на снижение внутрипросветного давления в области анастомоза, защита последнего изнутри, укрепление кишечного шва снаружи, использование синтетического шовного материала, который усиливает регенерацию сшиваемых тканей [Способ хирургической профилактики несостоятельности кишечного шва / А.Г. Семенов, В.Л. Мартынов, М.Г. Рябков [и др.] // Мед. альманах. - 2013. - №5 (28). - С. 138-144].
Формирование классической превентивной стомы сопряжено с рядом проблем. Таких как: сложный уход в послеоперационном периоде, частичная социальная изоляция пациента, возникновение парастомических осложнений, необходимость повторной госпитализации и операции. Суммируя изложенное, можно сказать, что в 19% случаев временная стома становится постоянной [Chow A., Tilney H.S., Paraskeva P. et al. The morbidity surrounding reversal of defunctioning ileostomies: a systematic review of 48 studies including 6,107 cases. Int. J. Colorectal Dis. - 2009. - №24 (6). - p. 711-23].
Трансанальная декомпрессия зоны анастомоза при помощи дренажа. Сущность данного метода заключается в декомпресии зоны анастомоза при помощи силиконовой трубки, заведенной выше зоны анастомоза, последнюю фиксируют к перианальной области узловым швом. На 5-7-е сутки после операции силиконовый дренаж удаляют. При ретроспективном исследовании одни авторы не видят существенного вклада данного метода на частоту несостоятельности анастомозов [Kim М-К., Won D-Y., Lee J-К. et al. Comparative study between transanal tube and loop ileostomy in low anterior resection for mid rectal cancer: a retrospective single center trial. Ann. Surg. Treat. Res. - 2015. - №88 (5). - p. 260-8]. В то время как в других исследованиях эффективность трансанальной интубации в отношении снижения частоты несостоятельности колоректального анастомоза была достоверна доказана [Hidaka Е., Ishida F., Mukai S. et al. Efficacy of transanal tube for prevention of anastomotic leakage following laparoscopic low anterior resection for rectal cancers: a retrospective cohort study in a single institution. Surg. Endosc. - 2015. - №29. - p. 863-7]. Во всех этих исследованиях сравнивались группы пациентов с проведением трансананльной декомпрессии и без ее проведения.
Другой известный из уровня техники метод повышения состоятельности ананстомоза - Valtrac. Данный способ профилактики заключается в проведении зоны анастомоза специального устройства в виде биофрагментируемого кольца (Valtrac) с презервативом. Данное устройство фиксируется внутри кишки на 5 см проксимальнее анастомоза рассасывающимся шовным материалом. Кишечное содержимое проходит внутри презерватива, не соприкасаясь со сформированным анастомозом. В среднем, самостоятельное отхождение устройства наблюдалось на 14 день после операции. В сравнительных исследованиях проведенных по данной методики авторами Ye et al. [Ye F., Chen D., Wang D. et al. Use of ValtracTMSecured Intracolonic Bypass in Laparoscopic Rectal Cancer Resection. Medicine. - 2014. - №93 (29). - p. 224], эффективность методики Valtrac не была доказана, так как частота несостоятельности анастомоза не различалась между группами с применением Valtrac и превентивной стома и только с формированием превентивной стомы (4,5% и 5,1%, Р=1; 8,3% и 0%, Р=0,5).
Также из уровня техники известна методика C-seal. Сущность метода заключается в защите анастомоза при помощи C-seal (биофрагментированный полиуретановый «пакетик»). C-seal крепится к головке сшивающего аппарата и проводится в просвет низводимой кишки. После формирования анастомоза C-seal выворачивается в просвет прямой кишки, при этом прикрывая сформированный анастомоз от каловых масс, тем самым снижая частоту несостоятельности. В среднем, самостоятельное отхождение устройства наблюдается на 11 день после операции. По результатам исследований [Morks A.N., Havenga К., ten Cate Hoedemaker H.O. et al. Thirty-seven patients with C-seal: protection of stapled colorectal anastomoses with a biodegradable sheath. Int. J. Colorectal Dis. - 2013. - №28 (10). - p. 1433-8] сложно судить об эффективности методики, поскольку они не носили сравнительный характер и всем пациентам, как правило, формировалась превентивная стома.
В настоящее время в экспериментальных и клинических исследованиях широко распространение получило укрепление линии шва мембранами, которые имеют разный химический состав и строение. Сущность метода заключается в укрепление однорядного шва полимерной пленочной мембраной, что приводит к повышению герметичности последнего в 1-е сутки, а следовательно, снижает риск развития несостоятельности на ранних сроках эксперимента. Преимущество метода состоит в профилактике биологической несостоятельности развития гнойно-некротического процесса и, как следствие, несостоятельности анастомоза. Недостатки метода заключается в механической несостоятельности, которая в равной мере приводит к недостаточности швов анастомоза. Кроме этого не все мембраны обладают хорошими адгезивными свойствами и легки в применении [Kannelos I., Blouhos K., Demetriades Н., Pramateftakis MG, Mantzoros I, Zacharakis E, Betsis D.The failed intraperitoneal colon anastomosis after colon resection // Tech. Coloproct. 2004. Vol. 8. P. 53-55].
Учитывая большой спектр профилактических мероприятий несостоятельности анастомозов желудочно-кишечного тракта и отсутствие согласия исследователей в данном направлении весьма перспективным является использование подходов регенеративной медицины для решения данной проблемы. При данном подходе используются биосовместимый каркас, который служит субстратом для миграции, пролиферации и дифференцировки клеток поврежденного органа [С.А. Маркосьян, Н.М. Лысяков, М.Ю. Беляева. Изучение влияния большого сальника на заживление кишечного анастомоза в условиях нарушенного кровоснабжения тонкой кишки. Вестник экспериментальной и клинической хирургии. Том 11, №4 (37), с. 288-292, 2017 г]. В настоящее время есть огромное количество биорезорбируемого материала, такие как коллаген, PLA, хитазан и др., но каждый из них обладает рядом недостатков, среди которых иммуногенность, аллергенность, недостаточная механическая прочность, токсичность продуктов распада и т.д. Одно из ведущих мест занимают изделия из фиброина шелка. Скафолды, основанные на фиброине шелка обладают высокой биосовместимостью, программированной скоростью деградации, легкостью химической модификации [Kapoor S., Kundu S.C. Silk protein-based hydrogels: Promising advanced materials for biomedical applications // Acta Biomater. - 2016. - Vol. 31. - P. 17-32.]. Изделия из фиброина шелка обладают высокой прочностью на растяжение, которое составляет 740 МПа. в то время как у коллагена 0.9-7.4 МПа и PLA - 28-50 МПа. Кроме того, скорость разложения фиброина шелка может быть скорректирована путем изменения режима обработки фиброина, влияющего на степень β-складчатости, при этом наблюдается следующая зависимость - скорость разложения уменьшается с увеличением общего содержания β-слоев. Уникальные свойства шелка тутового шелкопряда, такие как доступность, легкость химической модификации, способность к биодеградации в живом организме и возможность получения из него материалов различных форматов из водных и органических растворов привлекли внимание исследователей. В связи с этим последние несколько лет ведутся активные работы по изучению возможностей использования природного полимера фиброина шелка в качестве основы скаффолдов для регенеративной медицины. Была показана высокая биологическая совместимость, низкая иммуногенность и контролируемая биодеградация фиброина шелка. В результате ряда исследований были разработаны методы получения разных видов скаффолдов из фиброина шелка. В настоящее время ведутся исследования по возможности их использования в регенерации тканей.
Наиболее близкое решение по отношению к заявляемому способу, известное из уровня техники, раскрыто в патентном документе US 4719916 A «Intraintestinal bypass tube» Раскрыт кишечный трансплантат, образованный из тонкостенной латексной или эластичной трубки различной ширины и длины. Верхний круговой конец трубки и вертикальный шов усилены тканью, которая содержит рентгеноконтрастную нить. Трансплантат соединяют с подслизистым слоем кишечника, проксимальным к обычному анастомозу, что предотвращает контакт пищеварительного тракта: пищевода, желудочно-кишечного тракта, пищи и фекалий с местом закрытия анастомоза. Таким образом, использование такого трансплантата предотвращает утечку содержимого ЖКТ из любого кишечного анастомоза и гарантирует заживление анастомоза, при этом сам трансплантат естественным образом удаляется через прямую кишку.
Недостатками данного изобретения является использование синтетических материалов, что может привести к дополнительным послеоперационным осложнениям. Кроме того, используемые в представленных изобретениях материалы не являются биодеградируемыми и/или биорезорбируемыми, что может также привести к осложнениям, в том числе фиброзу окружающих тканей и, в перспективе, к прободению кишечной стенки.
Раскрытие изобретения
В заявляемом изобретении предложено использование биодеградируемого имплантата на основе метакрилированного фиброина шелка для снижения вероятности несостоятельности анастомозов ЖКТ. Изделия из данного материала обладают такими свойствами как: программируемая скорость деградация, низкая иммуногенность, легкость модификации, особенность строения позволяет витализировать данный имплантат.
Предлагается новый подход к решению проблемы несостоятельности анастомоза, где помимо механической защиты зоны анастомоза, имплантат активно встраивается в процесс регенерации. Имплантат становится основой для регенерации стенки кишки. В экспериментальных исследованиях на крысах показана полная регенерация стенки кишки с сохранением архитектоники и функции органа.
Задачей изобретения является разработка способа применения имплантатов на основе фиброина для снижения вероятности несостоятельности анастомозов.
Техническим результатом, достигаемым заявленным изобретением, является обеспечение возможности коррекции циркулярного дефекта кишки за счет использования трубчатого биодеградируемого имплантата, выполненного из метакрилированных производных фиброина шелка и желатина. Имплантат (биорезорбируемая трубка на основе метакрилированного желатина и метакрилированного фиброина) обеспечивает герметичность кишечника в течение всего периода заживления дефекта.
Заявляемый способ характеризуется простотой, низкой стоимостью, отсутствием необходимости дополнительных расходных материалов и специальных навыков, что позволит быстро и широко внедрить его в клиническую практику.
Поставленная задача решается тем, что, способ получения биорезорбируемой трубки на основе метакрилированного желатина и метакрилированного фиброина, согласно техническому решению, включает следующие шаги:
а) растворение в гексафторизопропаноле макромономеров: метакрилированного желатина (ЖМА) из расчета 10 масс. % и метакрилированного фиброина (ФМА) из расчета 4 масс. % при 55°С±5 в течение 18-36 часов;
б) получение смеси, включающей равные части растворов ЖМА и ФМА, и фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин из расчета 5 масс. % от массы макромономеров;
в) подготовка направляющей для формирования трубки посредством обезжиривания с последующим высушиванием поверхности стеклянной палочки с круглым сечением диаметром 2-15 см;
г) подготовка армировочной нити посредством выдерживания шелковой некрученой нити 8/0-4/0 в смеси, полученной на шаге б);
д) формирование первых слоев биорезорбируемой трубки на направляющей посредством ее погружения в смесь, полученную на шаге б), на 5-10 секунд с последующим вращением и экспонированием полученной заготовки в свете ультрафиолетовой лампы не менее 2 минут;
е) армирование нитью концевых участков трубки посредством укладывания нити витками на расстоянии 2-5 мм от концов формируемой трубки на заготовку, полученную на шаге д);
ж) формирование наружных слоев биорезорбируемой трубки посредством погружения полученной на шаге е) заготовки в смесь, полученную на шаге б), на 5-10 секунд, с последующим вращением и экспонированием полученной трубки в свете ультрафиолетовой лампы не менее 2 минут;
з) обработка сформированной трубки выдерживанием в дистиллированной воде в течение 1-1.5 часа, с последующим выдерживанием в 96%-ом этаноле в течение 12-18 часов и повторным выдерживанием в дистиллированной воде в течение 1-1.5 часа, обработкой внутренней поверхности сформированной трубки хлороформом.
Растворение ЖМА и ФМА проводят в течение 24 часов при 50°С. Направляющая преимущественно имеет диаметр 4 мм, при этом на шаге д) ее выдерживают в смеси в течение 7 секунд, экспонируют в свете ультрафиолетовой лампы мощностью 36 Вт в течение 2 мин, вращая направляющую со скоростью 15 об./мин, а шаг д) повторяют 4-6 раз в зависимости от формируемого количества слоев. На шаге е) равномерно укладывают по 10 витков нити на концевые участки трубки длиной 2,5 мм, отступив от одного края 2 мм и 7,5 мм, при этом плотность витков армирования составляет 10-15 витков на 3 мм трубки. На шаге з) сформированную трубку выдерживают в дистиллированной воде в течение 1 часа, затем 12 часов выдерживают в 96%-ом этаноле и еще 1 час в дистиллированной воде. Сформированная трубка имеет следующие параметры: толщина стенки трубки: от 150 мкм до 700 мкм, длина армированных участков 2-15 мм, длина неармированного участка: 1-6 мм, количество армированных участков: 2, расположение армированных участок: по краям трубки на расстоянии 1-6 мм от края, внутренний диаметр: от 2 мм до 15 см. Обезжиривание направляющей ведут 70% этанолом. Шаг ж) повторяют 4-20 раз в зависимости от формируемого количества слоев.
Поставленная задача также решается тем, что способ повышения состоятельности кишечного анастомоза, согласно техническому решению, включает следующие шаги:
а) подготовка биорезорбируемой трубки, полученной в соответствии с п. 1 для закрытия анастомоза посредством ее инкубации в стерильном физиологическом растворе в течение 15-30 минут с многократной заменой физиологического раствора;
б) предоперационная подготовка экспериментальных животных, посредством питания 10% раствором глюкозы без ограничения в течение 2 суток.
в) закрытие анастомоза трубкой, для чего животных фиксируют в положении на спине, внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела, формируют операционную рану, в которую выводят участок тонкой кишки (7 см дистальнее желудка), после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника биорезорбируемую трубку и фиксируют с помощью хирургической нити, после чего в месте имплантации удаляют участок кишечной трубки длиной 1-3 мм и проводят послойное ушивание полости с помещением кишки брюшную полость;
г) послеоперационный уход посредством ежедневных инъекций цефтриаксона из расчета 50 мг/кг массы тела в течение 4-х суток. Используемая биорезорбируемая трубка может иметь следующие параметры: внутренний диаметр - 4 мм, длина неармированного участка - 3 мм, длина армированных участков - 2,5 мм, толщина стенки - 300 мкм. В месте имплантации удаляют участок кишечной трубки длиной 1 мм. В качестве экспериментальных животных используют крыс линии Wistar, при этом за 15 мин до начала хирургического вмешательства крыс подвергают общей анестезии с премедикацией атропина сульфатом в дозе 0.04 мг/кг, подкожно.
В заявляемом изобретении может быть использован фиброин шелка каркасной нити пауков, фиброин шелка тутового шелкопряда и других видов шелкопрядов, фиброин рекомбинантного шелка, а также искусственные аналоги шелка.
В качестве фотоинициатора был выбран дифенил(2,4,6-триметилбензоил)фосфин оксид (97%), являющийся высокореактивным, нерастворимым в воде соединением, применяемым для быстрого фотоотверждения, например, для лазерной стерео литографии. Биорезорбируемой трубки, полученные в соответствии с заявляемым изобретением могут применяться для повышения состоятельности анастомозов полых органов.
Краткое описание чертежей
Изобретение поясняется чертежами.
На фиг. 1 представлена биорезорбируемая трубка, получаемая заявляемым способом.
На фиг. 2 представлен анастомоз дополнительно закрытый биорезорбируемой трубкой диаметра 4 мм.
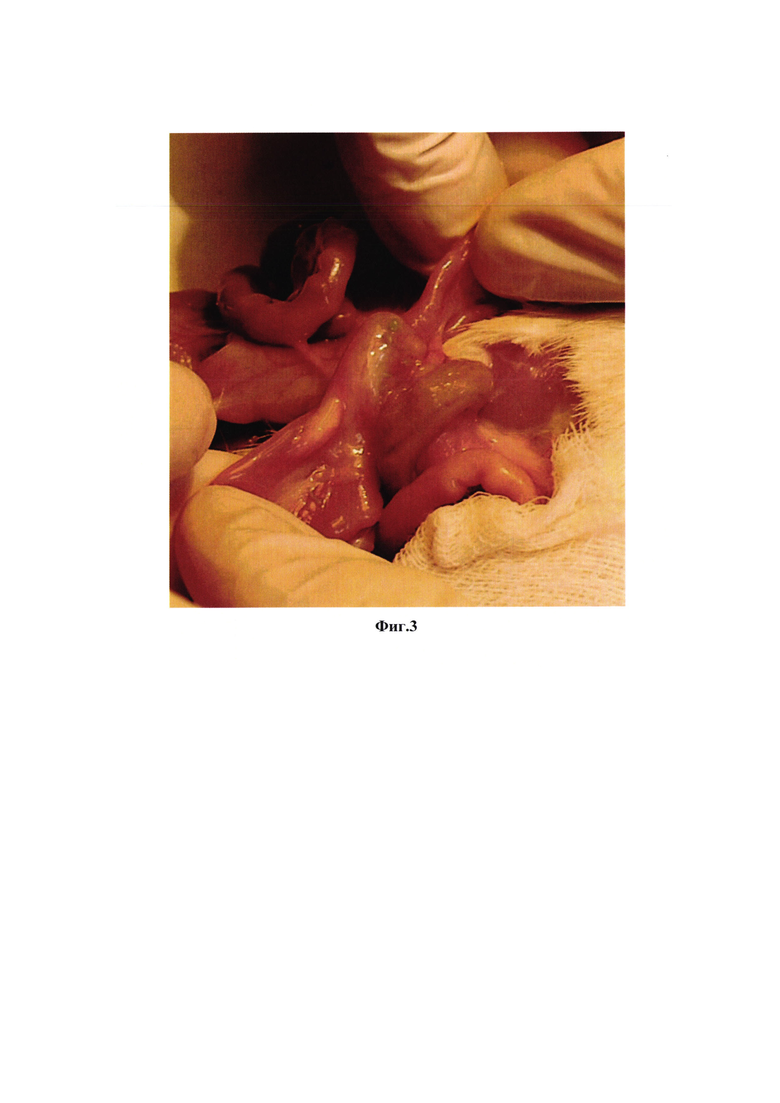
На фиг. 3 представлено состояние кишечника через 2 недели после операции.
Осуществление изобретения
Навеску метакрилированного желатина (ЖМА) растворяют в гексафторизопропаноле на водяной бане при 55°С±5 в течение 18-36 часов из расчета 10 масс. %. Навеску метакрилированного фиброина (ФМА) растворяют в гексафторизопропаноле на водяной бане при 55°С±5 в течение 18-36 часов из расчета 4 масс. %. Полученные растворы ЖМА и ФМА смешивают в равных объемных соотношениях и вносят фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин оксид (ТРО) в количестве 5% от массы макромономеров: ЖМА и ФМА. Формирование трубки диаметром 2-15 мм и длиной 4-36 мм выполняют на предварительно обработанной стеклянной палочке с круглым сечением соответствующей длины и диаметра. Обработка стеклянной палочки включает обезжиривание 70% этанолом, высушивание и обработку вакуумной смазкой, растворенной в хлороформе (5 мг/мл). Для этого палочку погружают в раствор вакуумной смазки в хлороформе на 10-30 секунд и затем высушивают на воздухе при комнатной температуре 30-60 минут. Далее формируют на направляющей - обработанной соответствующей стеклянной полочке, первые 4-6 слоев. Для этого погружают ее в смесь ЖМА/ФМА/ТРО на 5-10 секунд, извлекают и проводят фотополимеризацию нанесенного на направляющую слоя смеси ЖМА/ФМА/ТРО посредством экспонирования в свете УФ-лампы (мощность 36 Вт) не менее 2 минут. Направляющую при этом вращают со скоростью 10-20 об. мин. В зависимости от требуемого количества слоев процедуру повторяют 4-6 раз. Затем осуществляют армирование концевых участков формируемой трубки нанесением витков некрученой шелковой нити, предварительно обработанной в смеси ЖМА/ФМА/ТРО не менее 2 минут, из расчета 10-15 витков на 3 мм на расстоянии 2-5 мм от края. При этом количество витков и расстояние между ними определяется требуемыми параметрами получаемой трубки: длина армированного участка и длина неармированного участка. Далее формируют наружные слои трубки. Количество наружных слоев определяют исходя из требуемой толщины стенки трубки, считая, что каждый слой составляет 30 мкм. Заготовку помещают в смесь ЖМА/ФМА/ТРО на 5-10 секунд, извлекают и вращая со скоростью 10-20 об./мин. экспонируют в свете УФ-лампы (мощность 36 Вт) не менее 2 минут. Сформированную трубку на оправке переносят в дистиллированную воду на 1-1.5 часа, затем 12-18 часов выдерживают в 96%-ом этаноле и еще 1-1.5 часа в дистиллированной воде. Полученную трубку снимают с направляющей, обрабатывают внутреннюю поверхность хлороформом и переносят в 96%-ый этанол для хранения.
Полученную биорезорбируемую трубки используют для закрытия анастомоза. Для крыс линии Wistar массой 190-230 г используют трубку со следующими параметрами: диаметр - 4 мм, длина неармированного участка - 3-5 мм, длина армированных участков - 2,5 мм, толщина стенки - 280-320 мкм. Перед операцией трубку отмывают от этанола. Для этого переносят трубку из 96%-ого этанола в стерильный физиологический раствор, инкубируют при 37°С 15-30 минут, заменяют физиологический раствор на свежий и выдерживают трубку в нем еще 30 минут. Процедуру повторяют 3 раза. Животных начинают готовить к операции за 2 суток до хирургического вмешательства. За 2 суток до операции животных лишают твердой пищи и дают им 10% раствор глюкозы без ограничения (per os). Операция проводят под общей анестезией (Золетил + Ксилазин), премедикация - атропина сульфат в дозе 0.04 мг/кг, подкожно за 15 мин до начала хирургического вмешательства. Животных фиксируют в положении на спине. В начале операции внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела. Операционное поле ограничивают стерильными марлевыми салфетками, выполняют лапаротомию. В операционную рану выводят участок тонкой кишки (7 см дистальнее желудка), после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника стерильную трубку и узловыми швами герметично фиксируют имплантат с помощью хирургической нити (полиэстер, 4/0). После чего в месте имплантации удаляют участок кишечной трубки длиной 1-3 мм. Кишку помещают в брюшную полость и проводят послойное ушивание полости. В течение 4-х суток после операции выполняют ежедневные инъекции цефтриаксона из расчета 50 мг/кг массы тела. В течение 2-х суток животные получают 10-% раствор глюкозы, твердую пищу не получают, на третьи сутки их переводят на стандартную диету.
Таким образом, применение трубчатого биодеградируемого имплантата, выполненного из метакрилированных производных фиброина шелка и желатина, обеспечивает возможность коррекции циркулярного дефекта кишки. При этом имплантат (биорезорбируемая трубка на основе метакрилированного желатина и метакрилированного фиброина) обеспечивает герметичность кишечника в течение всего периода заживления дефекта. Ниже приведены примеры конкретного выполнения. Специалисту в данной области техники понятно, что данные примеры не являются ограничивающими изобретение, а лишь показывают возможность его реализации.
Пример 1
Получение трубки
Навеску лиофилизированного метакрилированного желатина (ЖМА) помещают в 1,5 мл гексафторизопропанола (ГФИП) из расчета 4 масс. % и помещают в закрытой посуде на водяную баню. Инкубируют смесь ЖМА с ГФИП до полного растворения в течение 24 часов при 50°С. Навеску лиофилизированного метакрилированного фиброина (ФМА) помещают в 1,5 мл ГФИП из расчета 10 масс. % и помещают в закрытой посуде на водяную баню. Инкубируют смесь ЖМА с ГФИП до полного растворения в течение 24 часов при 50°С. Смешивают растворы макромономеров: 1,5 мл ЖМА и 1,5 мл ФМА и добавляют к ним фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин оксид (ТРО) в количестве 5% от массы макромономеров. Поверхность стеклянной палочки диаметром 4 мм обезжиривают 70%-ым этиловым спиртом. Далее готовят смазку для оправки - стеклянной палочки диаметром 4 мм: в 1 мл хлороформа вносят 5 мг вакуумной смазки и растворяют на водяной бане при 50°С. Сухую стеклянную палочку диаметром 4 мм, обезжиренную спиртом, погружают в смазку на 20 секунд и затем высушивают на воздухе при комнатной температуре 30 минут. Обработанную смазкой стеклянную палочку используют в качестве направляющей для формирования трубки. Направляющую погружают в смесь ЖМА/ФМА/ТРО на 7 секунд, извлекают из раствора и облучают в свете УФ-лампы (мощность 36 Вт) в течение 2 мин, вращая направляющую со скоростью 15 об/мин. Повторяют процедуру погружения-экспонирования 4 раза. Для армирования концевых участков трубки используют хирургическую некрученую шелковую нить, смоченную в растворе ЖМА/ФМА/ТРО. Равномерно укладывают по 10 витков нити на концевые участки трубки длиной 2,5 мм, отступив от одного края 2 мм и 7,5 мм. Таким образом получают заготовку со следующими параметрами: длина армированных участков - 2,5 мм, длина неармированного участка - 3 мм. Вновь погружают заготовку в раствор ЖМА/ФМА/ТРО на 5 секунд, извлекают и вращая со скоростью 15 об/мин экспонируют в свете УФ-лампы (мощность 36 Вт) 2 минуты. Повторяют процедуру еще 4 раза. Сформированную трубку на оправке переносят в дистиллированную воду на 1 час, затем 12 часов выдерживают в 96%-ом этаноле и еще 1 час в дистиллированной воде. Полученную трубку снимают с направляющей, обрабатывают внутреннюю поверхность хлороформом для удаления остатков смазки и переносят в 96%-ый этанол для хранения. Сформированная таким образом трубка представлена на фиг. 1.
Пример 2
Коррекция анастомоза биорезорбируемой трубкой
Биорезорбируемую трубку со следующими параметрами: диаметр - 4 мм, длина неармированного участка - 3 мм, длина армированных участков - 2,5 мм, толщина стенки - 300 мкм, отмывают от этанола: переносят трубку из 96%-ого этанола в стерильный физиологический раствор, инкубируют при 37°С 20 минут, заменяют физиологический раствор на свежий и выдерживают трубку в нем еще 30 минут. Процедуру повторяют 3 раза. Крыс линии Wistar массой 190-230 г начинают готовить к операции за 2 суток до хирургического вмешательства. За 2 суток до операции животных лишают твердой пищи и дают им 10% раствор глюкозы без ограничения (per os). Операцию проводят под общей анестезией (Золетил + Ксилазин), премедикация - атропина сульфат в дозе 0.04 мг/кг, подкожно за 15 мин до начала хирургического вмешательства. Животных фиксируют в положении на спине. В начале операции внутримышечно вводят цефтриаксон из расчета 100 мг/кг массы тела. Операционное поле ограничивают стерильными марлевыми салфетками, выполняют лапаротомию. В операционную рану выводят участок тонкой кишки (7 см дистальнее желудка), после чего с противобрыжеечного края кишки выполняют разрез на половину диаметра кишечной трубки, вводят в просвет кишечника стерильную трубку и узловыми швами герметично фиксируют имплантат с помощью хирургической нити (полиэстер, 4/0). После чего в месте имплантации удаляют участок кишечной трубки длиной 1 мм. Кишку помещают в брюшную полость и проводят послойное ушивание полости. В течение 4-х суток после операции выполняют ежедневные инъекции цефтриаксона из расчета 50 мг/кг массы тела. В течение 2-х суток животные получают 10-% раствор глюкозы, твердую пищу не получают, на третьи сутки их переводят на стандартную диету. В качестве контроля используют животных, которым ушивают анастомоз с помощью хирургической нити (полиэстер, 4/0). Закрытый биорезорбируемой трубкой анастомоз представлен на фиг. 2. На вторые сутки после операции 70% животных контрольной группы умерли, на третьи сутки умерло еще 30%. Таким образом, смертность в контрольной группе составила 100%. При вскрытии животных контрольной группы наблюдались характерные признаки перитонита, анастомоз несостоятелен. Выживаемость животных из экспериментальной группы составили 100%. Через 2 недели после коррекции анастомоза биорезорбируемой трубкой животных выводили из эксперимента. У животных контрольной группы через 2 недели после операции выраженного спаечного процесса и несостоятельности анастомоза не наблюдалось. Состояние кишечника в области операции через 2 недели представлено на фиг. 3. Таким образом, применение биорезорбируемых трубок, описанных в настоящем изобретении, обеспечивает состоятельность анастомоза.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ СОСТОЯТЕЛЬНОСТИ КИШЕЧНОГО АНАСТОМОЗА С ИСПОЛЬЗОВАНИЕМ БИОРЕЗОРБИРУЕМОЙ ТРУБКИ НА ОСНОВЕ МЕТАКРИЛИРОВАННОГО ЖЕЛАТИНА И МЕТАКРИЛИРОВАННОГО ФИБРОИНА | 2019 |
|
RU2749871C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОРЕЗОРБИРУЕМОЙ ТРУБКИ НА ОСНОВЕ МЕТАКРИЛИРОВАННОГО ЖЕЛАТИНА И МЕТАКРИЛИРОВАННОГО ФИБРОИНА И СПОСОБ ВОССТАНОВЛЕНИЯ СТЕНКИ ТОНКОЙ КИШКИ В ЭКСПЕРИМЕНТЕ С ПОМОЩЬЮ ТАКОЙ ТРУБКИ | 2018 |
|
RU2714200C1 |
| СПОСОБ ФОРМИРОВАНИЯ БИОРЕЗОРБИРУЕМЫХ ФИБРОИНОВЫХ ПЛЕНОК С ИСПОЛЬЗОВАНИЕМ МЕТАКРИЛИРОВАННОГО ЖЕЛАТИНА | 2016 |
|
RU2645200C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ ТОНКОЙ КИШКИ | 2013 |
|
RU2559921C2 |
| СПОСОБ ФОРМИРОВАНИЯ БИОРЕЗОРБИРУЕМЫХ ТРЕХМЕРНЫХ СТРУКТУР | 2017 |
|
RU2691752C1 |
| ИМПЛАНТАТ ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2692578C1 |
| СПОСОБ ПОЛУЧЕНИЯ МИНЕРАЛИЗОВАННЫХ КОМПОЗИТНЫХ МИКРОСКАФФОЛДОВ ДЛЯ РЕГЕНЕРАЦИИ КОСТНОЙ ТКАНИ | 2016 |
|
RU2660558C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОДЕГРАДИРУЕМОГО КОМПОЗИТНОГО МАТРИКСА НА ОСНОВЕ РЕГЕНЕРИРОВАННОГО ФИБРОИНА ШЕЛКА Bombyx mori И ЕГО ПРИМЕНЕНИЕ | 2012 |
|
RU2483756C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ КОЖНОГО ПОКРОВА | 2016 |
|
RU2658707C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ДЕФЕКТА ТОНКОЙ КИШКИ ПОСРЕДСТВОМ ПРИМЕНЕНИЯ АЛЛОГЕННОГО ДЕЦЕЛЛЮЛЯРИЗИРОВАННОГО БИОМАТЕРИАЛА | 2024 |
|
RU2821237C1 |


Изобретение относится к биотехнологии и медицине. Более подробно изобретение относится к области хирургии, а именно к методам снижения вероятности несостоятельности кишечных анастомозов. Изобретение относится к способу получения биорезорбируемой трубки на основе метакрилированного желатина и метакрилированного фиброина, включающему следующие шаги: а) растворение в гексафторизопропаноле макромономеров: метакрилированного желатина (ЖМА) из расчета 10 масс. % и метакрилированного фиброина (ФМА) из расчета 4 масс. % при 55°С±5 в течение 18-36 часов; б) получение смеси, включающей равные части растворов ЖМА и ФМА и фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин из расчета 5 масс. % от массы макромономеров; в) подготовка направляющей для формирования трубки посредством обезжиривания с последующим высушиванием поверхности стеклянной палочки с круглым сечением диаметром 2-15 см; г) подготовка армировочной нити посредством выдерживания шелковой некрученой нити 8/0-4/0 в смеси, полученной на шаге б); д) формирование первых слоев биорезорбируемой трубки на направляющей посредством ее погружения в смесь, полученную на шаге б), на 5-10 секунд с последующим вращением и экспонированием полученной заготовки в свете ультрафиолетовой лампы не менее 2 минут; е) армирование нитью концевых участков трубки посредством укладывания нити витками на расстоянии 2-5 мм от концов формируемой трубки на заготовку, полученную на шаге д); ж) формирование наружных слоев биорезорбируемой трубки посредством погружения полученной на шаге е) заготовки в смесь, полученную на шаге б), на 5-10 секунд, с последующим вращением и экспонированием полученной трубки в свете ультрафиолетовой лампы не менее 2 минут; з) обработка сформированной трубки выдерживанием в дистиллированной воде в течение 1-1,5 часа, с последующим выдерживанием в 96%-ом этаноле в течение 12-18 часов и повторным выдерживанием в дистиллированной воде в течение 1-1,5 часа, обработкой внутренней поверхности сформированной трубки хлороформом. Технический результат – получение изделий, обладающих программируемой скоростью деградация, низкой иммуногенностью, легкостью модификации; разработка нового подхода к решению проблемы несостоятельности анастомоза, где, помимо механической защиты зоны анастомоза, имплантат активно встраивается в процесс регенерации. 10 з.п. ф-лы, 3 ил., 2 пр.
1. Способ получения биорезорбируемой трубки на основе метакрилированного желатина и метакрилированного фиброина, включающий следующие шаги:
а) растворение в гексафторизопропаноле макромономеров: метакрилированного желатина (ЖМА) из расчета 10 масс. % и метакрилированного фиброина (ФМА) из расчета 4 масс. % при 55°С±5 в течение 18-36 часов;
б) получение смеси, включающей равные части растворов ЖМА и ФМА и фотоинициатор дифенил(2,4,6-триметилбензоил)фосфин из расчета 5 масс. % от массы макромономеров;
в) подготовка направляющей для формирования трубки посредством обезжиривания с последующим высушиванием поверхности стеклянной палочки с круглым сечением диаметром 2-15 см;
г) подготовка армировочной нити посредством выдерживания шелковой некрученой нити 8/0-4/0 в смеси, полученной на шаге б);
д) формирование первых слоев биорезорбируемой трубки на направляющей посредством ее погружения в смесь, полученную на шаге б), на 5-10 секунд с последующим вращением и экспонированием полученной заготовки в свете ультрафиолетовой лампы не менее 2 минут;
е) армирование нитью концевых участков трубки посредством укладывания нити витками на расстоянии 2-5 мм от концов формируемой трубки на заготовку, полученную на шаге д);
ж) формирование наружных слоев биорезорбируемой трубки посредством погружения полученной на шаге е) заготовки в смесь, полученную на шаге б), на 5-10 секунд, с последующим вращением и экспонированием полученной трубки в свете ультрафиолетовой лампы не менее 2 минут;
з) обработка сформированной трубки выдерживанием в дистиллированной воде в течение 1-1,5 часа, с последующим выдерживанием в 96%-ом этаноле в течение 12-18 часов и повторным выдерживанием в дистиллированной воде в течение 1-1,5 часа, обработкой внутренней поверхности сформированной трубки хлороформом.
2. Способ по п. 1, характеризующийся тем, что растворение ЖМА и ФМА проводят в течение 24 часов при 50°С.
3. Способ по п. 1, характеризующийся тем, что направляющая имеет диаметр 4 мм.
4. Способ по п. 1, характеризующийся тем, что на шаге д) направляющую выдерживают в смеси в течение 7 секунд, экспонируют в свете ультрафиолетовой лампы мощностью 36 Вт в течение 2 минут, вращая направляющую со скоростью 15 об/мин.
5. Способ по п. 1, характеризующийся тем, что на шаге е) равномерно укладывают по 10 витков нити на концевые участки трубки протяженностью по 2,5 мм, с отступлением от конца трубки 2 мм и 7,5 мм.
6. Способ по п. 1, характеризующийся тем, что на шаге з) сформированную трубку выдерживают в дистиллированной воде в течение 1 часа, затем 12 часов выдерживают в 96%-ом этаноле и еще 1 час в дистиллированной воде.
7. Способ по п. 1, характеризующийся тем, что сформированная трубка имеет следующие параметры: толщина стенки трубки: от 150 мкм до 700 мкм, длина армированных участков 2-15 мм, длина неармированного участка: 1-6 мм, количество армированных участков: 2, расположение армированных участок: по краям трубки на расстоянии 1-6 мм от края, внутренний диаметр: от 2 мм до 15 см.
8. Способ по п. 1, характеризующийся тем, что шаг д) повторяют 4-6 раз в зависимости от формируемого количества слоев.
9. Способ по п. 1, характеризующийся тем, что обезжиривание направляющей ведут 70% этанолом.
10. Способ по п. 1, характеризующийся тем, что плотность витков армирования составляет 10-15 витков на 3 мм трубки.
11. Способ по п. 1, характеризующийся тем, что шаг ж) повторяют 4-20 раз в зависимости от формируемого количества слоев.
| US 4719916 A, 19.01.1988 | |||
| СПОСОБ ВОССТАНОВЛЕНИЯ ЦЕЛОСТНОСТИ ТОНКОЙ КИШКИ | 2013 |
|
RU2559921C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИОДЕГРАДИРУЕМОГО КОМПОЗИТНОГО МАТРИКСА НА ОСНОВЕ РЕГЕНЕРИРОВАННОГО ФИБРОИНА ШЕЛКА Bombyx mori И ЕГО ПРИМЕНЕНИЕ | 2012 |
|
RU2483756C1 |
Авторы
Даты
2020-01-17—Публикация
2018-12-29—Подача