Изобретение относится к экспериментальной медицине, а именно к акушерству и гинекологии, и может быть использовано для лечения эндометриоза на основании экспериментальной модели у крыс.
В настоящее время не существует единого подхода и универсального метода лечения, который гарантировал бы полное излечение и отсутствие рецидивов заболевания [Генитальный эндометриоз: Различные грани проблемы /М.И. Ярмолинская, Э.К. Айламазян. - Спб.: ЭкоВектор, 2017. - 615 с.].
Известен способ лечения наружного генитального эндометриоза (НГЭ) путем хирургического лечения, значительно уменьшающий выраженность болевого синдрома и диспареунии у больных [Comptour A. etal. Patient Quality of Life and Symptoms after Surgical Treatment for Endometriosis. JMinimInvasiveGynecol. 2019;26(4):717-726. doi: 10.1016/j.jmig.2018.08.005].
Недостатком данного способа является то, что неоднократные оперативные вмешательства могут вызывать развитие спаечного процесса, значительно снижать овариальный резерв и, соответственно, оказывать непосредственное влияние на возможность реализации репродуктивной функции в будущем. В целом, частота возникновения рецидивов эндометриоза после хирургического лечения достигает от 21,5% через 2 года и до 50% спустя 5 лет [Brown J, Farquhar С. Endometriosis: an overview of Cochrane Reviews. Cochrane Database Syst Rev. 2014 Mar 10;(3):CD009590. doi: 10.1002/1465185 8.CD0095 90.pub2].
Гормональная терапия НГЭ включает разнообразный спектр препаратов, относящийся к различным линиям терапии: прогестины, комбинированные оральные контрацептивы, агонисты гонадолиберинов (ГнРГ), внутриматочная спираль с левоноргестрелом, антигонадотропины, ингибиторы ароматаз, нестероидные противовоспалительные препараты и анальгетики. Гормональные методы лечения являются эффективными, но имеют серьезные побочные эффекты, которые ограничивают их долгосрочное применение, при этом высок процент рецидивов заболевания [Генитальный эндометриоз: Различные грани проблемы /М.И. Ярмолинская, Э.К. Айламазян. - Спб.: ЭкоВектор, 2017. - 615 с.].
Таким образом, необходимо дальнейшее изучение патогенеза заболевания и разработка альтернативных методов патогенетически обоснованного медикаментозного лечения.
Техническим результатом изобретения является расширение арсенала средств лечения эндометриоза, возможность избежать использования гормональных средств и недостатков их применения.
Указанный технический результат достигается в способе лечения эндометриоза на основании экспериментальной модели у крыс, в котором на модели эндометриоза, полученной путем хирургического вмешательства, выполняют внутрибрюшинное введение антагониста окситоциновых рецепторов в дозировке 0.35 мг/кг каждые сутки в течение 21 дня.
Способ иллюстрируется фиг. 1-5, где:
на фиг. 1 - эндометриоидная гетеротопия с шовным материалом и реактивным гигантоклеточным воспалением. Г-Э, ×200;
на фиг. 2 - поперечно-полосатая мускулатура с шовным материалом. Г-Э, ×100;
на фиг. 3 - поперечно-полосатая мускулатура с шовным материалом в стадии резорбции и экссудативным воспалением. Г-Э, ×100;
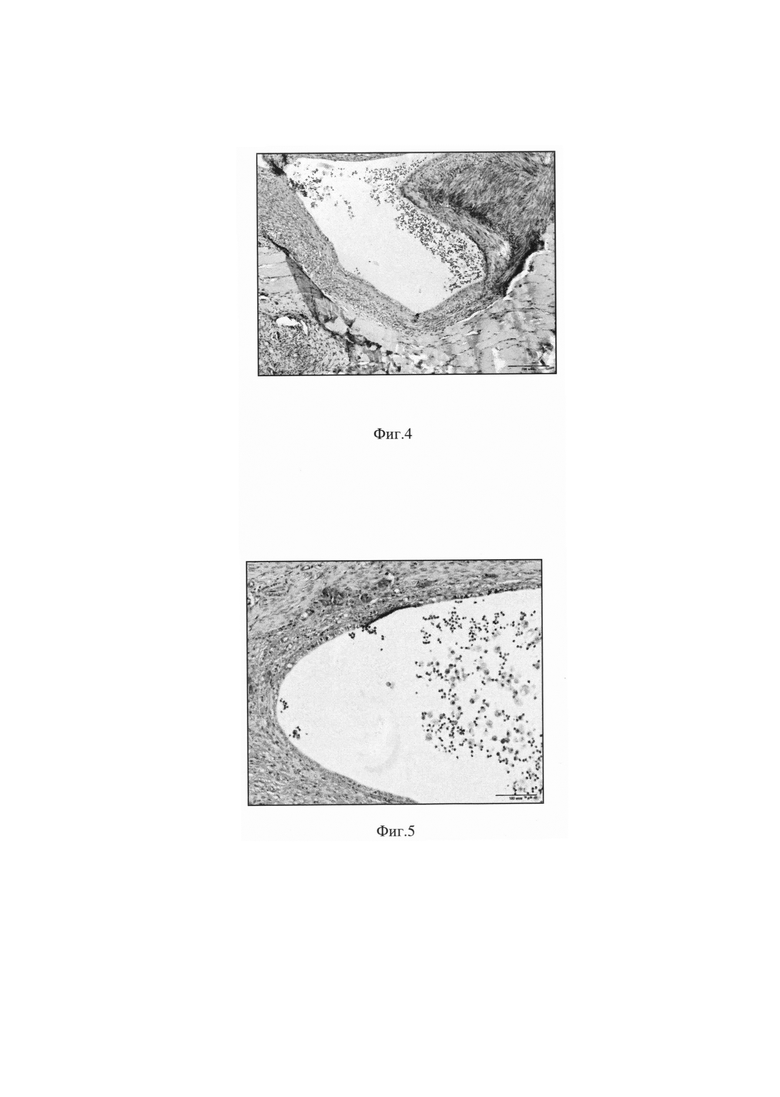
на фиг. 4 - сформированная эндометриоидная гетеротопия. Г-Э, ×100;
на фиг. 5 - очаг эндометриоза в виде "кисты" с гемосидерофагами. Г-Э, ×200.
Согласно литературным данным [Mechsner S., Bartley J. et al. Oxytocin receptor expression in smooth muscle cells of peritoneal endometriotic lesions and ovarian endometriotic cysts. Fertil Steril. 2005;83 Suppl 1:1220-31. doi: 10.1016/j.fertnstert.2004.11.038], в эндометриоидных гетеротопиях, кроме железистых клеток эндометрия в окружении стромальных клеток и/или макрофагов, верифицированы также гладкомышечные клетки. Клетки гладкой мускулатуры обнаружены в эндометриоидных имплантатах, располагающихся на брюшине, яичниках, при глубоком инфильтративном эндометриозе и аденомиозе. В гладкомышечных и эпителиальных клетках эндометриоидных гетеротопий были идентифицированы рецепторы окситоцина (OXTR). Отмечено, что женщины с эндометриозом имеют более высокий уровень окситоцина (ОХТ) в сыворотке крови [HuangM. etal.The abnormalexpressionofoxytocin receptors in the uterine junctional zone in women with endometriosis. ReprodBiolEndocrinol. 2017 3;15(1):1. doi: 10.1186/s12958-016-0220-7]. Известно, что окситоцин способен запускать синтез простагландина Е2 и F2a в гладкомышечных клетках, при этом простагландин Е2 является одним из мощных стимуляторов экспрессии мРНК фермента ароматазы (цитохрома р450) в строме эндометрия, что сопровождается повышенной ароматазной активностью в очаге эндометриоза и локальным синтезом эстрогенов.
В настоящее время большинство экспериментальных моделей эндометриоза проводится с использованием крыс. Моделирование эндометриоза на крысах, по нашему мнению, является наиболее обоснованным, так как эти лабораторные животные имеют схожее течение физиологических и патологических процессов с человеком, что позволяет использовать результаты исследований на животных для создания новых методов лечения этого заболевания у человека. Было отмечено, что «эндометриоидоподобные» имплантаты у крысы демонстрируют регрессию эпителиальных клеток и стромальную фибробластную трансформацию, аналогичную гистологическим данным в эндометриоидных поражениях человека.
Заявляемый способ основан на экспериментальных исследованиях на 24 крысах-самках линии Wistar. Все лабораторные животные были выведены в ФГУП «Питомник лабораторных животных «Рапполово» и содержались в регламентированных условиях вивария при соблюдении всех правил содержания лабораторных животных (время и порядок проведения карантина, маркировка всех особей, постоянный санитарный контроль, стандартный рацион питания, свободный доступ к воде и пище, автоматический режим освещения «день/ночь»). Уход за животными и проведение экспериментов осуществлялись согласно основным морально-этическим принципам проведения биомедицинских экспериментов на животных, сформулированных в следующих документах: «Правила лабораторной практики в РФ» (Good Laboratory Practice), утвержденные приказом Министерства здравоохранения и социального развития от 23.08.2010 №708н, и «Международные рекомендации по проведению биомедицинских исследований с использованием животных», принятые Международным советом медицинских научных обществ (CIOMS) в 1985 г.
На первом этапе эксперимента было проведено формирование модели заболевания у крыс линии Wistar массой 200±50 г. согласно существующей методике [Сравнительная оценка эффективности перспективных препаратов для таргетной терапии эндометриоза на основании экспериментальной модели заболевания. / Ярмолинская М.И., Петросян М.А. и соавт. // Гинекология. - 2018; 20 (5). - С. 46-51]. Оперативное вмешательство проводилось в фазу эструса. С целью анестезии при операции использовали золазепама гидрохлорид 100 в дозировке 30 мг/кг, после операции проводилась профилактика инфекционных осложнений путем внутримышечного введения цефтриаксона, обезболивание после операции выполнялось 2% раствором кеторолака внутримышечно.
В ходе операции после обработки передней брюшной стенки выполнены послойный срединный разрез, затем ревизия брюшной полости. На уровне бифуркации маточных рогов было произведено выделение и перевязка с последующим удалением левого маточного рога и левого яичника, после чего выполнена овариоэктомия справа. Удаленный рог матки рассекали продольно и из полученного участка вырезали 2 фрагмента размером 3×3 мм. Далее выполнена аутотрансплантация фрагментов маточной стенки на внутреннюю поверхность брюшной стенки.
Через две недели была выполнена лапароскопия для подтверждения формирования модели и оценки стартовых размеров эндометриоидных имплантатов.
После рандомизации было начато ежедневное внутрибрюшинное введение препарата-Атозибан (Atosiban),Фармидея ООО (Латвия), 12 крысам основной группы в дозировке 0.35 мг/кг/день.
Вторая группа (контрольная - 12 крыс) получала инъекции физиологического раствора. На 21-е сутки лечения экспериментальных животных выводили из опыта. После вскрытия проводили визуальную оценку формирования эндометриоидных гетеротопий в местах имплантации. Имплантированные ткани замеряли в двух плоскостях, иссекали из окружающих тканей и фиксировали в нейтральном 10% формалине для последующего гистологического исследования.
В 89,5% случаев при моделировании заболевания визуализировались эндометриоидоподобные имплантаты. У 5 крыс эндометриоидные очаги визуализировались только с одной стороны. У 24 крыс было сформировано 43 эндометриоидных имплантата. В начале лечения средние площади поверхности эндометриоидных имплантатов были сопоставимы в обеих группах - 18,3±2,5 мм2 в основной группе и 17,5±3,5 мм2 в группе контроля. В основной группе из 22 эндометриоидных гетеротопий в 27,3% случаев была обнаружена полная резорбция имплантатов, в 68,2% наблюдалось достоверное уменьшение площади гетеротопий на 62,4±11,2%. В контрольной группе было отмечено увеличение размеров очагов эндометриоза в 95,2% случаев на 29±7,2%. Средняя площадь эндометриоидных имплантатов в основной группе после лечения была достоверно меньше, чем в контрольной группе (7,3±1,8 мм и 22,2±1,2 мм соответственно, р<0,05).
Операционно-биопсийный материал фиксировали в 10% нейтральном забуференном формалине (рН 7.2) в течение 24 часов. Проводку материала осуществляли с помощью автоматической станции Leica TP 1020 (Leica, Германия). Полученный после проводки материал заливали в парафин, из которого изготавливали срезы толщиной 3 мкм. Для обзорной окраски использовали гематоксилин и эозин. При световой микроскопии оценивали наличие сформированных эндометриоидных гетеротопий в виде "кист", выстилку "кист", присутствие гемосидерофагов, наличие реактивного и патологического воспаления. Исследование проводили на микроскопе Olympus СХ31 (Olympus, Япония) при увеличении ×100, ×200, ×400.
Исследовано 43 образца эндометриоидных гетеротопий, сформированных в результате эксперимента (22 образца, полученных с правой стороны брюшины и 21 образец, полученный с левой стороны брюшины) от 24 животных. Исследуемые образцы разделены на 2 группы: 1 группа - основная - после лечения ингибиторами окситоциновых рецепторов (22 образца от 12 животных), 2 группа - контрольная (получавшая инъекции физиологического раствора), 21 образец от 12 животных.
В основной группе (после лечения ингибиторами окситоциновых рецепторов) отмечено достоверное уменьшение размеров гетеротопий с единичными спавшимися "кистами" (68.2%) или полная резорбция эндометриоидных очагов (27.3%), в одном случае (4.5%) достоверного уменьшения площади эндометриоидной гетеротопий отмечено не было (фиг. 1). В случаях полной резорбции эндометриоидных гетеротопий было отмечено наличие поперечно-полосатой мускулатуры и шовного материала.
Во всех образцахэндометриоидных очагов после лечения определялась поперечно-полосатая мускулатура с шовным материалом в разной стадии резорбции, а также гигантоклеточное воспаление и экссудативное воспаление (фиг. 2, 3).
Во всех исследованных образцах контрольной группы присутствовали поперечно-полосатые мышцы с шовным материалом, в 95,2% выявлены сформированные эндометриоидные гетеротопий в виде "кист", выстланные эндометриодноподобным эпителием (фиг. 4).
В 50% случаев присутствовали гемосидерофаги (фиг. 5), в 35% случаев выявлена гиперваскуляризация эндометриоидной гетеротопий. В 15% случаев определялась экссудативная инфильтрация и плазмоцитарная инфильтрация.
Полученные результаты продемонстрировали высокую эффективность антагониста окситоциновых рецепторов в терапии хирургически-индуцированного эндометриоза у крыс (полная резорбция или достоверный регресс эндометриоидных гетеротопий). Представленные данные являются основанием для дальнейшего продолжения экспериментальных исследований с целью оценки наиболее эффективных минимальных доз, длительности терапиии возможности применения антагониста окситоциновых рецепторов в клинической практике у больных эндометриозом.
Заявляемый способ расширяет арсенал средств лечения эндометриоза, позволяет избежать применения гормональных препаратов и проявления их недостатков, проводить исследования по выявлению наиболее эффективных минимальных доз, длительности терапии, возможности применения антагониста окситоциновых рецепторов в клинической практике у больных эндометриозом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА В ЭКСПЕРИМЕНТЕ У КРЫС | 2023 |
|
RU2816983C1 |
| ПРЕПАРАТ НА ОСНОВЕ СТЕРОИДНЫХ ЭСТРОГЕНОВ ДЛЯ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА | 2021 |
|
RU2755250C1 |
| СПОСОБ ЛЕЧЕНИЯ НАРУЖНОГО ГЕНИТАЛЬНОГО ЭНДОМЕТРИОЗА | 2019 |
|
RU2732251C1 |
| СПОСОБ ФОРМИРОВАНИЯ ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ КОМБИНАЦИИ САХАРНОГО ДИАБЕТА 1 ТИПА И ЭНДОМЕТРИОЗА | 2021 |
|
RU2776727C1 |
| СПОСОБ ЛЕЧЕНИЯ НАРУЖНОГО ГЕНИТАЛЬНОГО ЭНДОМЕТРИОЗА | 2018 |
|
RU2693050C1 |
| СПОСОБ ЛЕЧЕНИЯ НАРУЖНОГО ГЕНИТАЛЬНОГО ЭНДОМЕТРИОЗА | 2019 |
|
RU2711658C1 |
| Способ прогнозирования рецидива эндометриоидных кист яичника | 2018 |
|
RU2694882C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ НАРУЖНОГО ГЕНИТАЛЬНОГО ЭНДОМЕТРИОЗА | 2013 |
|
RU2541089C1 |
| СПОСОБ ЛЕЧЕНИЯ НАРУЖНОГО ГЕНИТАЛЬНОГО ЭНДОМЕТРИОЗА | 2019 |
|
RU2727299C1 |
| Способ прогнозирования развития рецидива инфильтративного эндометриоза малого таза на основании результата экспрессии иммуногистохимического маркера Musashil в эндометриоидной ткани | 2016 |
|
RU2636506C1 |

Настоящее изобретение относится к области медицины, а именно к способу лечения эндометриоза на основании экспериментальной модели у крыс, который заключается в том, что на модели эндометриоза, полученного путем хирургического вмешательства, выполняют внутрибрюшинное введение антагониста окситоциновых рецепторов в дозировке 0,35 мг/кг каждые сутки в течение 21 дня. Настоящее изобретение обеспечивает лечение эндометриоза с возможностью не использовать гормональные средства и избежать недостатков их применения и обеспечивает расширение арсенала средств лечения эндометриоза. 5 ил.
Способ лечения эндометриоза на основании экспериментальной модели у крыс, заключающийся в том, что на модели эндометриоза, полученного путем хирургического вмешательства, выполняют внутрибрюшинное введение антагониста окситоциновых рецепторов в дозировке 0,35 мг/кг каждые сутки в течение 21 дня.
| N-АЦЕТИЛ-L-ЦИСТЕИН ДЛЯ ЛЕЧЕНИЯ ЭНДОМЕТРИОЗА | 2010 |
|
RU2549433C2 |
| Прибор для одновременного испытания нескольких ткацких гонкой | 1928 |
|
SU14693A1 |
| KR 20180100120 A, 07.09.2018. | |||
Авторы
Даты
2020-01-17—Публикация
2019-09-12—Подача