Область техники, к которой относится изобретение
Изобретение относится к комбинации ингибитора FGFR и ингибитора IGF1R.
Комбинация предназначена для применения в лечении пролиферативного нарушения, в особенности для применения в лечении рака.
Ингибитор FGFR и ингибитор IGFR могут применяться одновременно, отдельно или последовательно.
Изобретение также относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и комбинацию согласно изобретению.
Сущность изобретения
Настоящее изобретение относится к комбинации первого соединения, которое является ингибитором FGFR, и второго соединения, которое является ингибитором IGF1R.
Было обнаружено, что комбинация первого соединения, которое является ингибитором FGFR, и второго соединения, которое является ингибитором IGF1R, может применяться для предотвращения развития резистентности опухоли или рака к ингибитору FGFR комбинации, или для задержки развития резистентности опухоли или рака к ингибитору FGFR комбинации.
Уровень техники
FGFR
Семейство протеинтирозинкиназных (PTK) рецепторов фактора роста фибробластов (FGF) регулирует различные типы физиологических функций, включающих митогенез, заживление ран, дифференцировку клеток, ангиогенез и развитие. Как нормальный, так и злокачественный рост клеток, а также пролиферация находятся под воздействием изменений в локальной концентрации факторов FGF, молекул внеклеточной сигнализации, которые действуют как аутокринные, а также паракринные факторы. Аутокринная сигнализация FGF может быть особенно важной в развитии раковых опухолей, зависимых от стероидных гормонов, до гормононезависимого состояния. Факторы FGF и их рецепторы экспрессируются при повышенных уровнях в нескольких линиях тканей и клеток, при этом повышенная экспрессия, как полагают, вносит вклад в злокачественный фенотип. Кроме того, ряд онкогенов являются гомологами генов, кодирующих рецепторы факторов роста, и существует вероятность аномальной активации FGF-зависимой сигнализации при раке поджелудочной железы человека (Knights et al., Pharmacology and Therapeutics 2010 125:1 (105-117); Korc. et al Current Cancer Drug Targets 2009 9:5 (639-651)).
Двумя типичными представителями являются кислотный фактор роста фибробластов (aFGF или FGF1) и основный фактор роста фибробластов (bFGF или FGF2), и на сегодняшний день идентифицированы по меньшей мере двадцать различных предствителей семейства FGF. Клеточный ответ на факторы FGF передается через четыре типа трансмембранных протеинтирозин-киназных рецепторов факторов роста фибробластов (FGFR) с высоким сродством, обозначенных номерами от 1 до 4 (от FGFR1 до FGFR4).
Прерывание сигнального пути FGFR1 должно влиять на пролиферацию опухолевых клеток, поскольку данная киназа активируется во многих типах опухолей в добавление к пролиферирующим эндотелиальным клеткам. Повышенная экспрессия и активация FGFR1 в опухолеассоциированной сосудистой сети указывает на роль этих молекул в ангиогенезе опухоли.
Недавнее исследование продемонстрировало связь между экспрессией FGFR1 и туморогенностью в классических дольковых карциномах (КДК). Карциномы КДК являются причиной 10-15% всех опухолей молочной железы и, как правило, недостатка экспрессии p53 и Her2 при сохранении экспрессии рецептора эстрогена. Амплификация гена 8p12-p11.2 была продемонстрирована в ~50% случаев КДК, причем было показано, что она связана с повышенной экспрессией FGFR1. Предварительные исследования с миРНК, направленными против FGFR1, или низкомолекулярным ингибитором рецептора показали, что клеточные линии, имеющие указанную амплификацию, особенно чувствительны к ингибированию данного сигнального пути. Рабдомиосаркома (RMS) является наиболее распространенной саркомой мягких тканей у детей, которая вероятно, возникает в результате нарушения пролиферации и дифференцировки в течение миогенеза скелета. Рецептор FGFR1 оверэкспрессирован в первичных рабдомиосаркомах и ассоциирован с гипометилированием 5'CpG-островков и нарушенной экспрессией генов AKT1, NOG и BMP4. Рецептор FGFR1 также связывали с плоскоклеточным раком легкого, колоректальным раком, глиобластомой, астроцитомой, раком предстательной железы, мелкоклеточным раком легкого, меланомой, раковыми опухолями головы и шеи, раком щитовидной железы, раком матки.
Рецептор 2 фактора роста фибробластов проявляет высокое сродство к кислотному и/или основному факторам роста фибробластов, а также к лигандам фактора роста кератиноцитов. Рецептор 2 фактора роста фибробластов также распространяет мощные остеогенные эффекты факторов FGF в процессе роста и дифференцировки остеобластов. Мутации в рецепторе 2 фактора роста фибробластов, приводящие к сложным функциональным изменениям, как было показано, вызывают аномальное окостенение черепных швов (краниосиностоз), что свидетельствует о главной роли FGFR сигнализации в костеобразовании в соединительнотканной мембране. Например, при синдроме Аперта (AP), который характеризуется преждевременным окостенением черепных швов, большинство случаев связано с точечными мутациями, приводящими к приобретению новой и патологической функции в рецепторе 2 фактора роста фибробластов. Кроме того, скрининг мутаций у больных синдромной формой краниосиностоза указывает на то, что повторные мутации FGFR2 служат причиной тяжелых форм синдрома Пфейфера. Конкретные мутации FGFR2 включают W290C, D321A, Y340С, C342R, C342S, C342W, N549H, K641R в FGFR2.
Несколько тяжелых нарушений в развитии скелета человека, включая синдромы Аперта, Крузона, Джексона-Вейсса, Бира-Стивенсона (синдром складчатой кожи) и Пфейфера, ассоциированы с наличием мутаций в рецепторе 2 фактора роста фибробластов. Большинство случаев, если не все, синдрома Пфейфера (PS) также вызваны de novo мутацией гена рецептора 2 фактора роста фибробластов, и недавно было показано, что мутации в рецепторе 2 фактора роста фибробластов нарушают один из критериев, обусловливающих лигандную специфичность. А именно, две мутантные сплайс-формы рецептора фактора роста фибробластов, FGFR2c и FGFR2b, приобретают способность связывать атипичные лиганды FGF и активироваться ими. Такая потеря лигандной специфичности приводит к нарушению сигнализации, и, как полагают, тяжелый фенотип указанных синдромов заболевания является результатом эктопической лиганд-зависимой активации рецептора 2 фактора роста фибробластов.
Генетические аберрации рецепторной тирозинкиназы FGFR3, такие как хромосомные транслокации или точечные мутации, приводят к эктопически экспрессируемым или нерегулируемым, конститутивно активным FGFR3-рецепторам. Такие нарушения связаны с подгруппой множественных миелом и наблюдаются при карциноме мочевого пузыря, гепатоклеточной карциноме, плоскоклеточной карциноме полости рта и цервикальных карциномах. Соответственно, ингибиторы FGFR3 могут применяться в лечении множественной миеломы, карциномы мочевого пузыря и цервикальной карциномы. Экспрессия FGFR3 также повышена при раке мочевого пузыря, в частности, при инвазивном раке мочевого пузыря. Рецептор FGFR3 часто активирован при мутациях в уротелиальной карциноме (UC). Повышенную экспрессию ассоциировали с мутацией (85% опухолей с мутациями обнаружили высокий уровень экспрессии), но также 42% опухолей без обнаружимой мутации показывали оверэкспрессию, включая многие мышечно-инвазивные опухоли. Рецептор FGFR3 также связан с раком эндометрия и щитовидной железы.
Повышенную экспрессию FGFR4 связывали с карциномами предстательной железы и щитовидной железы. Кроме того, зародышевый полиморфизм (Gly388Arg) ассоциирован с повышением частоты возникновения рака легкого, молочной железы, толстой кишки, печени (ГЦК) и предстательной железы. Кроме того, усеченная форма FGFR4 (включающая киназный домен), как было обнаружено, также присутствует в 40% опухолей гипофиза, но не присутствует в нормальной ткани. Повышенную экспрессию FGFR4 наблюдали в опухолях печени, толстой кишки и легкого. Рецептор FGFR4 связан с колоректальным раком и раком печени, где экспрессия его лиганда FGF19 часто повышена. Рецептор FGFR4 также связан с астроцитомами, рабдомиосаркомой.
Фиброзные состояния представляют главную медицинскую проблему, возникающую в результате аномального или избыточного отложения фиброзной ткани. Такие отложения встречаются при многих заболеваниях, включая цирроз печени, гломерулонефрит, легочный фиброз, системный фиброз, ревматоидный артрит, а также при естественном процессе заживления ран. Механизмы развития фиброза не полностью изучены, но, как полагают, он возникает в результате действий различных цитокинов (включающих фактор некроза опухоли (TNF), факторы роста фибробластов (FGF), фактор роста тромбоцитов (PDGF) и трансформирующий фактор роста бета). Фактор (TGFβ) вовлечен в пролиферацию фибробластов и отложение белков внеклеточного матрикса (включающих коллаген и фибронектин). Это приводит к изменению структуры ткани и функции и последующей патологии.
Ряд доклинических исследований продемонстрировал активацию факторов роста фибробластов в доклинических моделях фиброза легкого. Как было показано, TGFβ1 и PDGF вовлечены в процесс фиброгенеза, и в последующей опубликованной работе предполагается, что повышение факторов FGF и последующее усиление пролиферации фибробластов могут происходить в ответ на повышение TGFβ1. Потенциальный терапевтический эффект, направленный на фиброзный механизм при таких состояниях, как идиопатический легочный фиброз (IPF), предполагается на основе описанного клинического эффекта противофиброзного средства пирфенидона. Идиопатический легочный фиброз (также называемый криптогенным фиброзирующим альвеолитом) является прогрессирующим заболеванием, включающим рубцевание легкого. Постепенно альвеолярные мешочки легких замещаются фиброзной тканью, которая становится толще, что вызывает необратимую потерю способности ткани переносить кислород в кровоток. Симптомы заболевания включают одышку, хронический сухой кашель, утомляемость, боль в груди и потерю аппетита, приводящую к быстрой потере массы тела. Заболевание является крайне серьезным, с приблизительно 50% смертности после 5 лет.
В таком качестве, соединения, которые ингибируют FGFR-рецептор, будут пригодными в представлении средств для предотвращения роста опухолей или индуцирования апоптоза в опухолях, в особенности путем ингибирования ангиогенеза. Поэтому ожидается, что соединения окажутся полезными в лечении или предотвращении пролиферативных нарушений, таких как раковые опухоли. В частности, опухоли с активирующими мутантными формами рецепторных тирозинкиназ или апрегуляцией рецепторных тирозинкиназ могут быть особенно чувствительными к ингибиторам. Больные с активирующими мутантными формами любой из изоформ специфических RTK (рецепторных тирозинкиназ), обсуждаемых в описании, могут также найти лечение ингибиторами RTK особенно благоприятным.
Примеры ингибиторов FGFR
*) N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамин (соединение A) представлен следующей формулой:
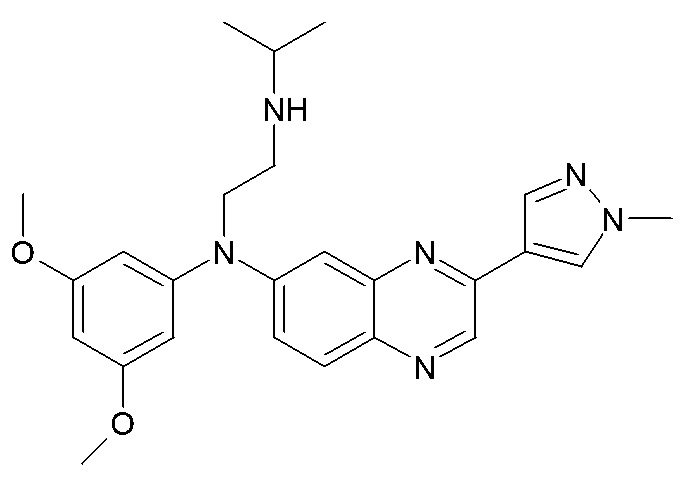 соединение A
соединение A
*) N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амин (соединение B) представлен следующей формулой:
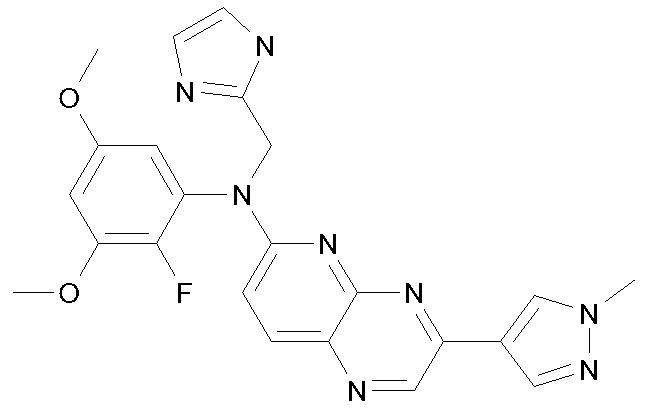 соединение B
соединение B
Соединения N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамин (соединение A) или его фармацевтически приемлемая соль или его сольват и N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амин (соединение B) или его фармацевтически приемлемая соль или его сольват, а также их химический синтез, описаны в WO2011/135376 и WO2013/061080, которые включены в настоящее описание посредством отсылки. Они описаны как ингибиторы или модуляторы активности некоторых тирозиновых протеинкиназ, в особенности FGFR, и, таким образом, соединения могут применяться в лечении или профилактике, в особенности лечении, заболеваний или состояний, опосредованных такими тирозинкиназами, в особенности FGFR. Соединения могут применяться в лечении или профилактике, в особенности лечении, рака.
В WO2011/135376 настоящее соединение A также представлено как гидрохлоридная соль. В WO2013/061080 настоящее соединение B также представлено как сульфатная соль, как гидрохлоридная соль, как фосфатная соль, как лактатная соль, как фумаратная соль.
Ингибиторы FGFR-киназы, соединения A и B, описанные в настоящей заявке, обладают дифференцированным профилем селективности, что обеспечивает новую возможность применения таких средств направленного действия в подгруппах больных, у которых болезнь вызвана нарушением регуляции FGFR. Ингибиторы FGFR-киназы, соединения A и B, описанные в настоящей заявке, демонстрируют пониженное ингибирующее действие на дополнительные киназы, в особенности VEGFR, более конкретно VEGFR2 и PDGFR, в частности PDGFR-бета, и обеспечивают дифференцированный профиль побочных эффектов или токсичности и, таким образом, обеспечивают более эффективное лечение при таких показаниях. Ингибиторы VEGFR2 и PDGFR-бета ассоциируются с токсическими эффектами, такими как артериальная гипертензия или отек, соответственно. В случае ингибиторов VEGFR2 такое гипертензивное действие часто ограничивает дозу, может служить противопоказанием у некоторых групп больных и требует клинического контроля. Ингибиторы киназы FGFR, соединения A и B, описанные в настоящей заявке, являются ингибиторами FGFR1, 2, 3 и 4.
Фактор роста эндотелия сосудов (VEGFR)
Фактор роста эндотелия сосудов (VEGF), полипептид, является митогенным в отношении эндотелиальных клеток in vitro и стимулирует ангиогенные ответы in vivo. VEGF также связывали с нарушенным ангиогенезом. Рецепторы VEGFR представляют собой тирозиновые протеинкиназы (PTK). PTK-киназы катализируют фосфорилирование специфических остатков тирозина в белках, участвующих в клеточной функции, и таким образом регулируют рост клеток, их выживание и дифференцировку.
Было идентифицировано три PTK рецептора VEGF: VEGFR-1 (Flt-1), VEGFR-2 (Flk-1 или KDR) и VEGFR-3 (Flt-4). Указанные рецепторы вовлечены в ангиогенез и участвуют в сигнальной трансдукции. Особый интерес представляет рецептор VEGFR-2, который является трансмембранной рецепторной PTK, экспрессируемой в основном в эндотелиальных клетках. Активация VEGFR-2 посредством VEGF является критической стадией пути передачи сигнала, которая инициирует ангиогенез опухоли. Экспрессия VEGF может быть конститутивной по отношению к опухолевым клеткам и может быть также апрегулирована в ответ на некоторые стимулы. Одним таким стимулом является гипоксия, при которой экспрессия VEGF апрегулируется как в опухолевых, так и ассоциированных тканях хозяина. Лиганд VEGF активирует VEGFR-2 путем связывания с его внеклеточным VEGF-связывающим сайтом. Такое связывание приводит к димеризации рецепторов VEGFR и аутофосфорилированию остатков тирозина на внутриклеточном киназном домене VEGFR-2. Киназный домен функционирует, перенося фосфат от АТФ к остаткам тирозина, представляя, таким образом, сайты связывания для сигнальных белков, активируемых ниже по каскаду после VEGFR-2, что, в конечном счете, приводит к инициации ангиогенеза.
PDGFR
Злокачественная опухоль является результатом неконтролируемой пролиферации клеток. Рост клеток контролируется посредством хрупкого баланса между стимулирующими рост и ингибирующими рост факторами. В нормальной ткани продукция и активность указанных факторов приводит к дифференцированным клеткам, растущим в контролируемых и регулируемых условиях, которые поддерживают нормальную целостность и функционирование органа. Злокачественная клетка избегает этого контроля; природный баланс нарушается (посредством различных механизмов) и становится нерегулируемым, происходит аберрантный рост клеток. Фактором роста, играющим важную роль в развитии опухоли, является фактор роста тромбоцитов (PDGF), который включает семейство пептидных факторов роста, которые передают сигнал посредством тирозинкиназных рецепторов клеточной поверхности (PDGFR) и стимулируют различные клеточные функции, включая рост, пролиферацию и дифференцировку.
*) BGJ398 (3-(2,6-дихлор-3,5-диметоксифенил)-1-[6-[4-(4-этилпиперазин-1-ил)анилино]пиримидин-4-ил]-1-метилмочевина), имеющая следующую формулу:
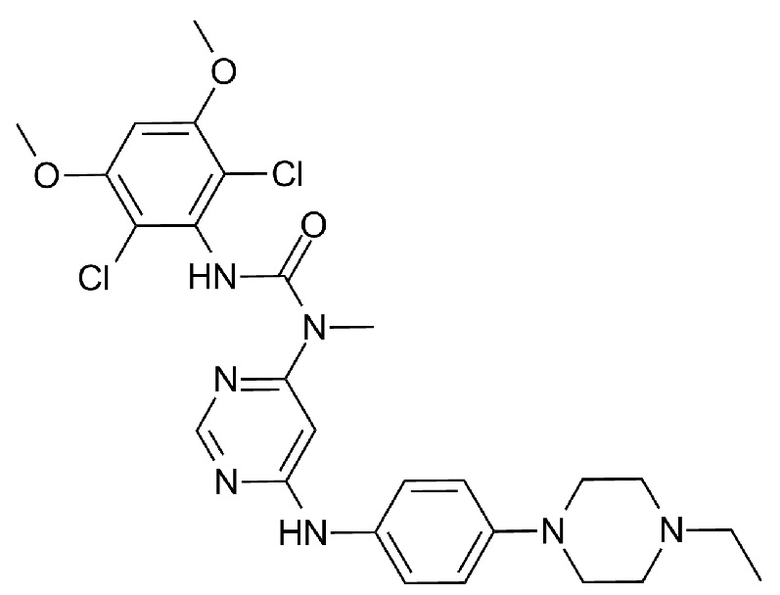
*) AZD-4547 (N-(5-(3,5-диметоксифенэтил)-1H-пиразол-3-ил)-4-((3S,5R)-3,5-диметилпиперазин-1-ил)бензамид), имеющий следующую формулу:
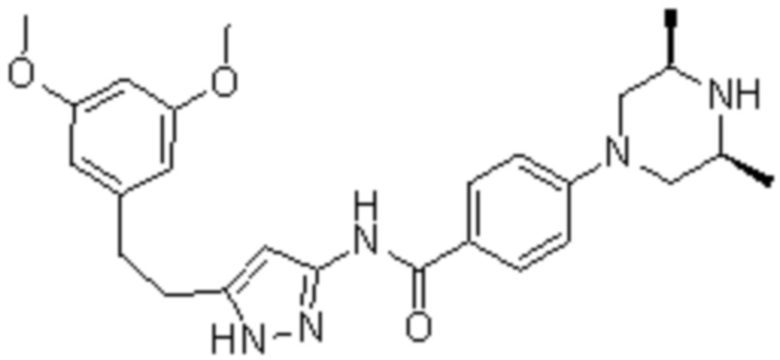
*) PD 173074 (N-[2-[[4-(диэтиламино)бутил]амино]-6-(3,5-диметоксифенил)пиридо[2,3-d]пиримидин-7-ил]-N'-(1,1-диметилэтил)мочевина), имеющая следующую формулу:
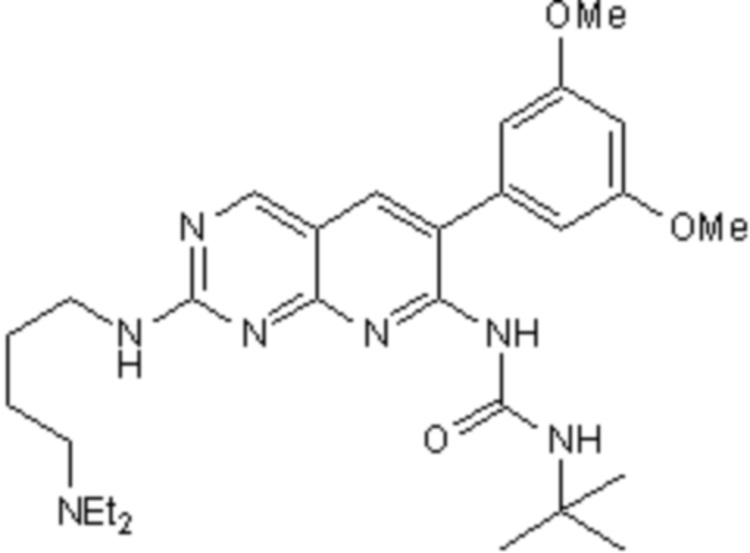
*) LY-2874455 ((R,E)-2-(4-(2-(5-(1-(3,5-дихлорпиридин-4-ил)этокси)-1H-индазол-3-ил)винил)-1H-пиразол-1-ил)этанол), имеющий следующую формулу:
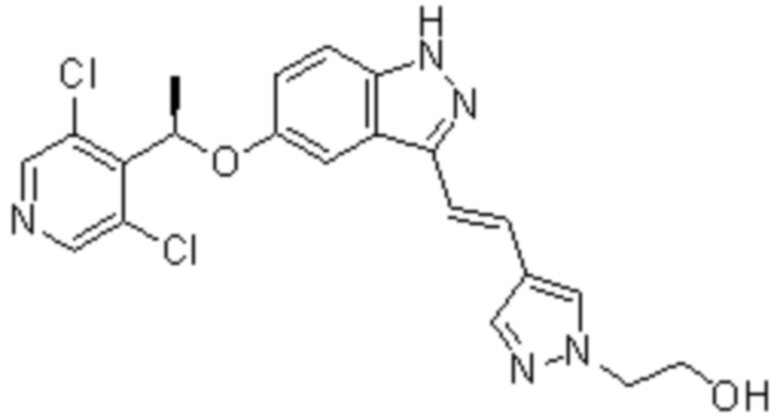
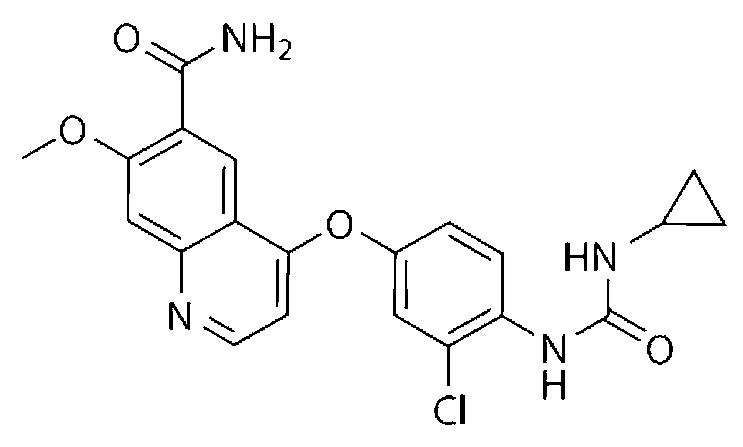
*) Бриваниб (аланинат) (S)-(R)-1-((4-((4-фтор-2-метил-1H-индол-5-ил)окси)-5-метилпирроло[2,1-f][1,2,4]триазин-6-ил)окси)пропан-2-ил 2-аминопропаноат.
*) Интеданиб
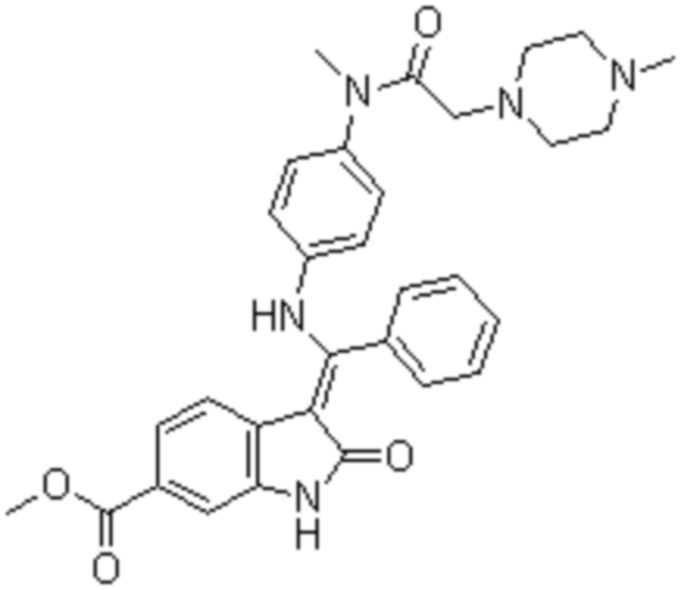
*) Довитиниб
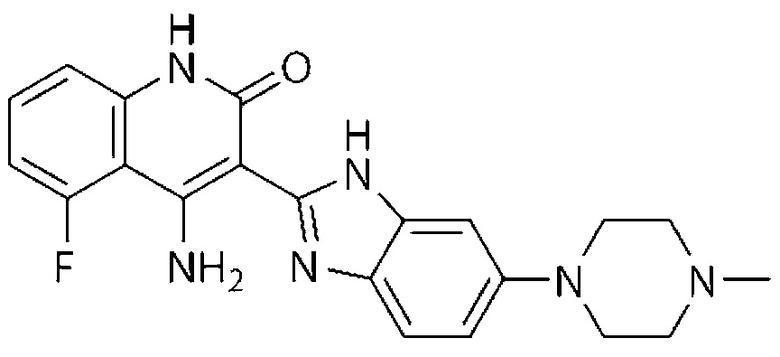
*) Цедираниб
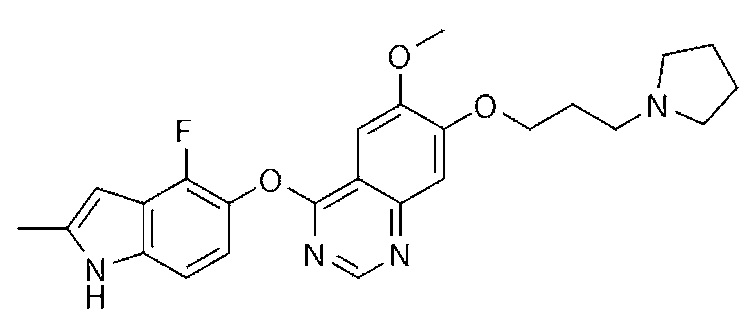
*) Маситиниб
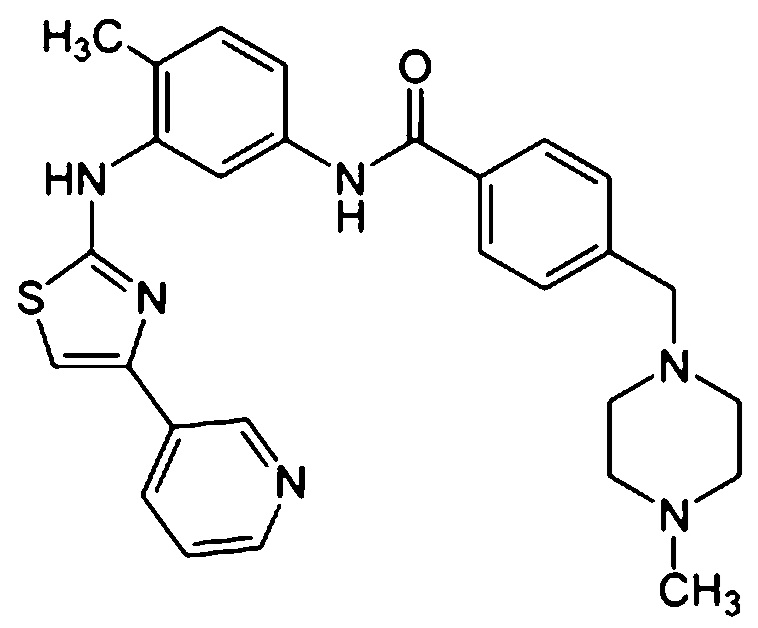
*) Орантиниб
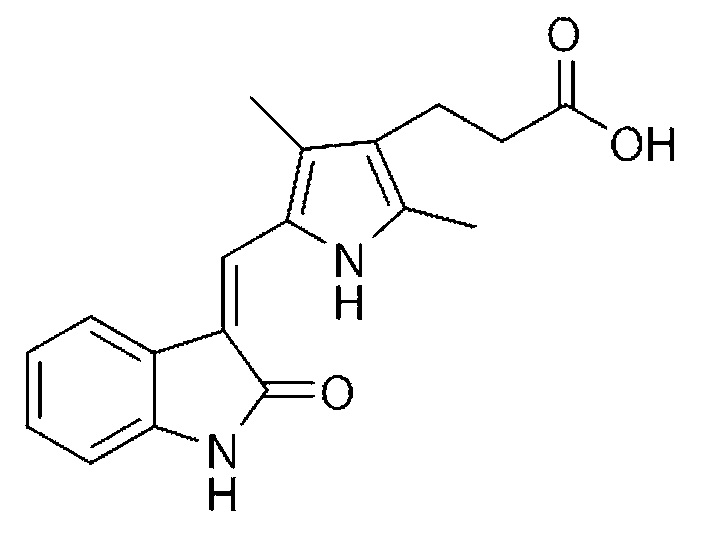
*) Ponatinib (AP24534)
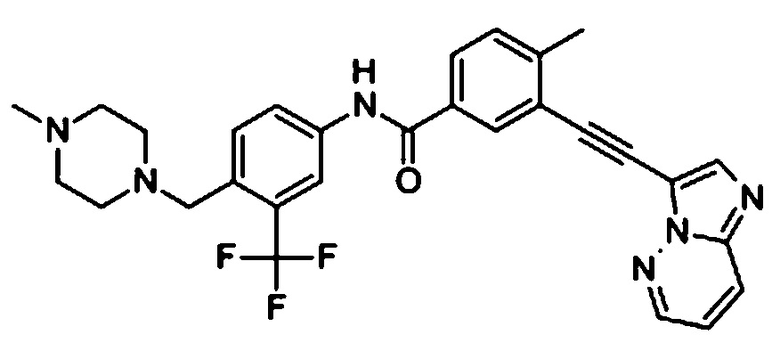
*) E-7080 (lenvatinib)
*) BAY1163877, TAS-120, ARQ087, ASP5878, FF284,
*) Антитела или связанные соединения, такие как, например, HGS1036/FP-1039; MFGR1877S; AV-370; GP369/AV-396b; HuGAL-FR21; моноклональные антитела (BAY1179470, RG-7444).
IGF1R
Инсулиноподобные факторы роста, также известные как соматомедины, включают инсулиноподобный фактор роста I (IGF-I) и инсулиноподобный фактор роста (IGF-II). Эти факторы роста проявляют митогенную активность в отношении различных типов клеток, включая опухолевые клетки, при связывании с общим рецептором, называемым рецептором инсулиноподобного фактора роста 1 (IGF1R). IGF1R принадлежит к большому классу рецепторов тирозинкиназ. Взаимодействие IGF с IGF1R активирует рецептор, вызывая аутофосфорилирование рецептора по остаткам тирозина. После активации, IGF1R, в свою очередь, фосфорилирует внутриклеточные мишени, активируя клеточные сигнальные пути. Эта активация рецептора важна для стимуляции роста и выживания опухолевых клеток. Поэтому ингибирование активности IGF1R представляет ценный потенциальный способ лечения или предотвращения роста человеческих раковых опухолей и других пролиферативных заболеваний.
Несколько источников указывают, что IGF-I, IGF-II и их рецептор IGF1R являются важными медиаторами злокачественного фенотипа. Было обнаружено, что уровни IGF-I в плазме являются ниболее сильным прогностическим фактором риска развития рака предстательной железы, причем подобные эпидемиологические исследования решительно связывают уровни IGF-I в плазме с риском развития рака молочной железы, толстой кишкой и легкого.
Оверэкспрессия рецептора инсулиноподобного фактора роста 1 также была продемонстрирована в нескольких линиях раковых клеток и опухолевых тканей. IGF1R оверэкспрессирован в 40% всех линий клеток рака молочной железы и в 15% линий клеток рака легкого. В опухолевой ткани рака молочной железы IGF1R оверэкспрессирован в 6-14 раз, при этом IGF1R проявляет в 2-4 раза более высокую киназную активность по сравнению с нормальной тканью. Биоптаты тканей рака толстой и прямой кишки демонстрируют повышенные уровни IGF1R, при этом уровень экспрессии IGF1R коррелирует с тяжестью заболевания. Анализ культур клеток первичного рака шейки матки и линий клеток рака шейки матки показал 3- и 5-кратную оверэкспрессию IGF1R, соответственно, по сравнению с нормальными эктоцервикальными клетками. Экспрессия IGF1R в клетках синовиальной саркомы также коррелирует с агрессивным фенотипом (то есть метастаз и высокая скорость пролиферации). Кроме того, акромегалия, медленно развивающееся заболевание, вызвано гиперсекрецией соматотропина и IGF-I. Антагонизм функции IGF1R может быть полезным в лечении данного заболевания.
Ингибиторы IGF/IGF1R главным образом относятся к трем основным классам: (1) моноклональные антитела против IGF1R, (2) моноклональные антитела против лигандов IGF1R (IGF-1 и IGF-2) и (3) ингибиторы тирозинкиназы IGF1R. Эти IGF1R-направленные средства оказывают одинаковые воздействия на сигнализацию IGF1R, но отличаются по механизмам действия, спектру ингибирования мишеней и фармакологическим свойствам.
Блокада рецептора с применением терапии моноклональными антителами против IGF1R до настоящего времени была наиболее клинически исследованным подходом.
Примеры ингибиторов IGF/IGF1R
GSK1838705A является низкомолекулярным ингибитором киназы, имеющим следующую формулу:
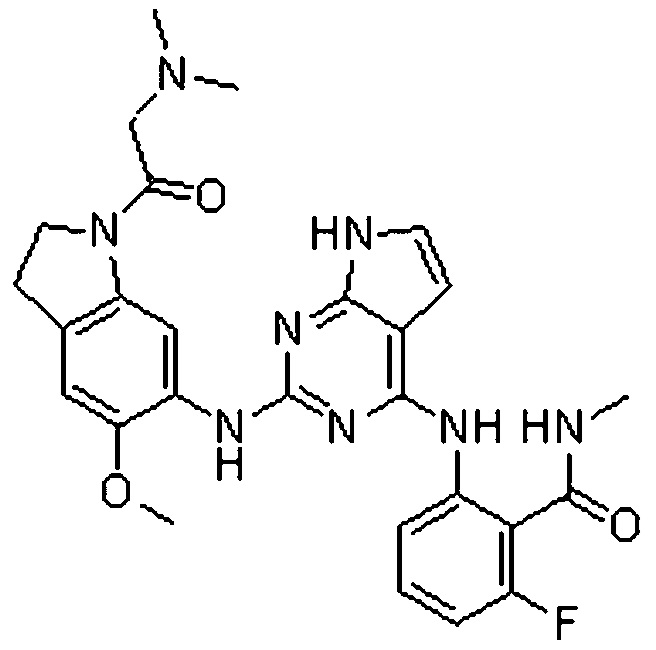 ;
;
BMS-754807 является низкомолекулярным ингибитором, имеющим следующую формулу:
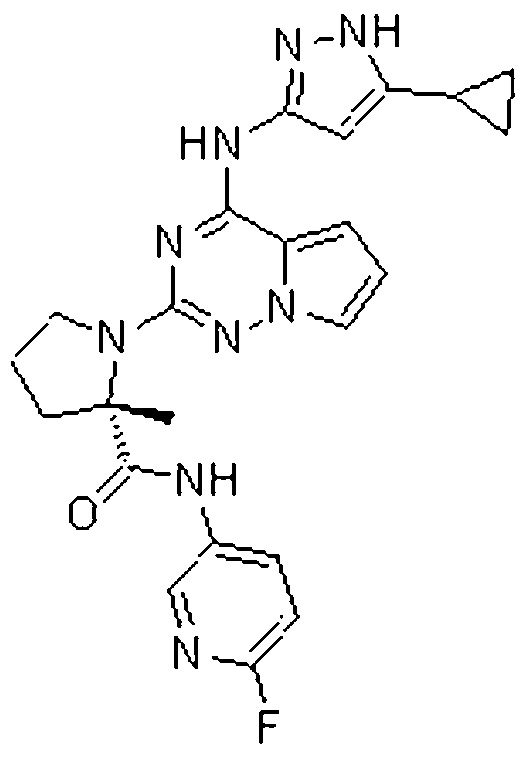 ;
;
NVP-AEW541; моноклональное антитело против IGF1R CP-751,871; моноклональное антитело против IGF1R IMC-A12 (циксутумумаб); моноклональное антитело AMG-479 (ганитумумаб); гуманизированное моноклональное антитело AVE-1642; R1507; MK-0646 (далотузумаб); INSM18, низкомолекулярный ингибитор IGF1R; Insm-18 (NDGA); пероральный ингибитор IGF-1R PL225B; OSI-906 (линситниб); XL-228; GSK 1904529A; ABDP; A-928605; AXL1717 (PPP) (пикроподофиллин); KW-2450; CP 751,871 (фигитумумаб); Sch717454 (робатумумаб); BIIB022 (моноклональное антитело против IGF1R); h10H5; MEDI-573; BI836845;
или их фармацевтически приемлемая соль или их сольват.
http://www.ncbi.nlm.nih.gov/entrez/eutils/elink.fcgi?dbfrom=pubmed&retmode=ref&cmd=prlinks&id=19023648http://dx.doi.org/10.1007%2Fs10911-008-9104-6
Описание чертежей
Фигура 1: График Incucyte (% конфлюэнтности с течением времени), на котором представлена пролиферация клеток DMS114, обработанных отдельными средствами (соединение [1 мкМ] с или без контроля ДМСО, GSK1838705A [1 мкМ] с или без контроля ДМСО), обработанных комбинацией соединения A [1 мкМ] и GSK1838705A [1 мкМ], и ДМСО в качестве контроля растворителем.
Фигура 2: График Incucyte (% конфлюэнтности с течением времени), на котором представлена пролиферация клеток DMS114, обработанных отдельными средствами (соединение [1 мкМ] с или без контроля ДМСО, BMS-754807 [300 нм] с или без контроля ДМСО), обработанных комбинацией соединения A [1 мкМ] и BMS-754807 [300 нм], и ДМСО в качестве контроля растворителем.
Фигура 3: График Incucyte (% конфлюэнтности с течением времени), на котором представлена пролиферация резистентных клеток DMS114, поддерживаемых в присутствии соединения A [1 мкМ] с или без ДМСО, и резистентных клеток DMS114, поддерживаемых в присутствии соединения A [1 мкМ] и обработанных GSK1838705A [1 мкМ] (длительная обработка).
Подробное описание изобретения
Изобретение относится к комбинации ингибитора FGFR и ингибитора IGF1R.
В одном варианте осуществления настоящее изобретение относится к комбинации ингибитора FGFR, описанного в настоящей заявке, и ингибитора IGF1R, в особенности ингибитора IGF1R, описанного в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к комбинации первого соединения, выбранного из N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина (соединения A) или его фармацевтически приемлемой соли или его сольвата и N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина (соединения B) или его фармацевтически приемлемой соли или его сольвата; и второго соединения, которое является ингибитором IGF1R, в особенности ингибитором IGF1R, описанным в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина (соединения A) или его фармацевтически приемлемой соли или его сольвата и ингибитора IGF1R, в особенности ингибитора IGF1R, описанного в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина (соединения A) или его фармацевтически приемлемой соли или его сольвата и второго соединения, выбранного из GSK1838705A и BMS-754807.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина (соединения A) или его фармацевтически приемлемой соли или его сольвата и GSK1838705A.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина (соединения A) или его фармацевтически приемлемой соли или его сольвата и BMS-754807.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина (соединения B) или его фармацевтически приемлемой соли или его сольвата и ингибитора IGF1R, в особенности ингибитора IGF1R, описанного в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина (соединения B) или его фармацевтически приемлемой соли или его сольвата и второго соединения, выбранного из GSK1838705A и BMS-754807.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина (соединения B) или его фармацевтически приемлемой соли или его сольвата и GSK1838705A.
В одном варианте осуществления настоящее изобретение относится к комбинации N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина (соединения B) или его фармацевтически приемлемой соли или его сольвата и BMS-754807.
В одном варианте осуществления ингибитор FGFR, в особенности ингибитор FGFR, описанный в настоящей заявке, более конкретно соединение A или его фармацевтически приемлемая соль или его сольват, или соединение B или его фармацевтически приемлемая соль или его сольват, и ингибитор IGF1R, в особенности ингибитор IGF1R, описанный в настоящей заявке, более конкретно GSK1838705A или GSK1838705A комбинаций настоящего изобретения, вводят одновременно (например, в отдельных или единых композициях) или последовательно в любом порядке, в приблизительно одно и то же время. В данном случае два соединения будут вводить в количестве и способом, которые являются достаточными, чтобы обеспечить предпочтительный или синергический эффект.
В одном варианте осуществления ингибитор FGFR, в особенности ингибитор FGFR, описанный в настоящей заявке, более конкретно соединение A или его фармацевтически приемлемая соль или его сольват, или соединение B или его фармацевтически приемлемая соль или его сольват, и ингибитор IGF1R, в особенности ингибитор IGF1R, описанный в настоящей заявке, более конкретно GSK1838705A или GSK1838705A комбинаций настоящего изобретения, вводят последовательно в любом порядке, в отдельных схемах применения. В данном случае два соединения будут вводить в течение периода и в количестве и способом, которые являются достаточными, чтобы обеспечить предпочтительный или синергический эффект.
Следует понимать, что предпочтительный способ и порядок введения и соответствующие дозы и схемы применения для каждого компонента комбинации будут зависеть от конкретного применяемого химиотерапевтического средства, их пути введения, конкретной опухоли, которую подвергают лечению, и конкретного носителя, которого подвергают лечению.
Оптимальный способ и порядок введения, а также дозы и схема применения могут быть с легкостью определены специалистом в данной области при использовании стандартных методов и с учетом информации, представленной в настоящей заявке.
В комбинациях настоящего изобретения ингибитор FGFR и ингибитор IGF1R могут быть включены в отдельные лекарственные формы, которые могут поступать в продажу независимо друг от друга, но с показаниями или инструкцией по их комбинированному применению. Указанные показания или инструкция могут быть в форме листка-вкладыша или подобного, или в форме любой информации, например, в письменной или голосовой форме.
В комбинациях настоящего изобретения ингибитор FGFR и ингибитор IGF1R могут вводить одним путем введения или различными путями введения.
В одном варианте осуществления ингибитор FGFR и ингибитор IGF1R в комбинациях настоящего изобретения вводят одним путем введения, в особенности пероральным путем.
Настоящее изобретение также относится к фармацевтическому продукту или коммерческой упаковке, включающим комбинацию согласно настоящему изобретению, в особенности вместе с инструкциями по одновременному, отдельному или последовательному применению в лечении заболевания, опосредованного активностью FGFR тирозинкиназы, в особенности рака.
В одном варианте осуществления, в комбинациях настоящего изобретения, ингибитор FGFR и ингибитор IGF1R вводят одновременно.
В одном варианте осуществления, в комбинациях настоящего изобретения, ингибитор FGFR и ингибитор IGF1R вводят отдельно, в особенности в течение промежутка времени, который выбран таким образом, чтобы эффект комбинированного применения был больше, чем эффект, полученный при введении ингибитора FGFR или ингибитора IGF1R отдельно.
В случае комбинации настоящего изобретения, включающей соединение A или его фармацевтически приемлемую соль или его сольват в качестве ингибитора FGFR, может быть предпочтительным вводить указанное соединение реже, чем ингибитор IGF1R, поскольку соединение A проявляет лизосомотропные свойства и пролонгированное блокирование мишени.
Ингибитор FGFR и ингибитор IGF1R комбинаций настоящего изобретения также могут быть объединены в одну лекарственную форму.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, ингибитор FGFR, в особенности ингибитор FGFR, описанный в настоящей заявке, и, в качестве второго действующего вещества, ингибитор IGF1R, в особенности ингибитор IGF1R, описанный в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, соединение, выбранное из N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина (соединения A) или его фармацевтически приемлемой соли или его сольвата и N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина (соединения B) или его фармацевтически приемлемой соли или его сольвата; и, в качестве второго действующего вещества, соединение, которое является ингибитором IGF1R, в особенности ингибитором IGF1R, описанным в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамин (соединение A) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, ингибитор IGF1R, в особенности ингибитор IGF1R, описанный в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамин (соединение A) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, соединение, выбранное из GSK1838705A и BMS-754807.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамин (соединение A) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, GSK1838705A.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамин (соединение A) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, BMS-754807.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амин (соединение B) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, ингибитор IGF1R, в особенности ингибитор IGF1R, описанный в настоящей заявке.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амин (соединение B) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, соединение, выбранное из GSK1838705A и BMS-754807.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амин (соединение B) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, GSK1838705A.
В одном варианте осуществления настоящее изобретение относится к фармацевтической композиции, включающей фармацевтически приемлемый носитель и, в качестве первого действующего вещества, N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амин (соединение B) или его фармацевтически приемлемую соль или его сольват, и, в качестве второго действующего вещества, BMS-754807.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения вводят перорально.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора FGFR, соединение A или его фармацевтически приемлемую соль или его сольват, в частности соединение A.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора FGFR, соединение B или его фармацевтически приемлемую соль или его сольват, в частности соединение B.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора FGFR, малую молекулу.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора FGFR, большую молекулу, такую как, например, антитело.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора IGF1R, малую молекулу.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора IGF1R, большую молекулу, такую как, например, антитело.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают, в качестве единственных действующих веществ, ингибитор FGFR и ингибитор IGF1R, в том числе описанные в любом из вариантов осуществления настоящего изобретения.
В одном варианте осуществления комбинации настоящего изобретения или фармацевтические композиции настоящего изобретения включают по меньшей мере одно дополнительное терапевтическое средство, в особенности по меньшей мере одно дополнительное противоопухолевое средство или вспомогательное средство, специально для применения в качестве лекарственного, более конкретно для применения в лечении рака или связанных с раком заболеваний.
Примеры противоопухолевых средств или вспомогательных средств (поддерживающих средств в терапии), которые могут входить в состав комбинаций или фармацевтических композиций настоящего изобретения, включают, без ограничения:
- комплексные соединения платины, например, цисплатин, необязательно в комбинации с амифостином, карбоплатином или оксалиплатином;
- соединения таксана, например, паклитаксел, частицы паклитаксела, связанного с белком (AbraxaneTM) или доцетаксел;
- ингибиторы топоизомеразы I, такие как соединения камптотецина, например, иринотекан, SN-38, топотекан, топотекан hcl;
- ингибиторы топоизомеразы II, такие как противоопухолевые эпиподофиллотоксины или производные подофиллотоксина, например, этопозид, этопозида фосфат или тенипозид;
- противоопухолевые алкалоиды барвинка, например, винбластин, винкристин или винорелбин;
- противоопухолевые нуклеозидные производные, например, 5-фторурацил, лейковорин, гемцитабин, гемцитабин hcl, капецитабин, кладрибин, флударабин, неларабин;
- алкилирующие средства, такие как азотистый иприт или нитрозомочевину, например, циклофосфамид, хлорамбуцил, кармустин, тиотепу, мефалан (мелфалан), ломустин, алтретамин, бусульфан, дакарбазин, эстрамустин, ифосфамид необязательно в комбинации с месной, пипоброман, прокарбазин, стрептозоцин, телозоломид, урацил;
- противоопухолевые производные антрациклина, например, даунорубицин, доксорубицин, необязательно в комбинации с дексразоксаном, доксил, идарубицин, митоксантрон, эпирубицин, эпирубицин hcl, валрубицин;
- производные тетракарцина, например, тетракарцин A;
- глюкокортикоид, например, преднизон;
- антитела, например, трастузумаб (антитело к HER2), ритуксимаб (антитело к СD20), гемтузумаб, гемтузумаб озогамицин, цетуксимаб, пертузумаб, бевацизумаб, алемтузумаб, экулизумаб, ибритумомаб тиуксетан, нофетумомаб, панитумумаб, тозитумомаб, CNTO 328;
- антагонисты рецепторов эстрогена или селективные модуляторы рецепторов эстрогена или ингибиторы синтеза эстрогена, например, тамоксифен, фулвестрант, торемифен, дролоксифен, фазлодекс, ралоксифен или летрозол;
- ингибиторы ароматазы, такие как эксеместан, анастрозол, летразол, тестолактон и ворозол;
- средства, влияющие на дифференцировку, такие как ретиноиды, витамин D или ретиноевую кислоту, и средства, блокирующие метаболизм ретиноевой кислоты (RAMBA), например, аккутан;
- ингибиторы ДНК-метилтрансферазы, например, азацитидин или децитабин;
- антифолаты, например, преметрексед динатрия;
- антибиотики, например, актиномицин D, блеомицин, митомицин C, дактиномицин, карминомицин, дауномицин, левамизол, пликамицин, митрамицин;
- антиметаболиты, например, клофарабин, аминоптерин, цитозина арабинозид или метотрексат, азацитидин, цитарабин, флоксуридин, пентостатин, тиогуанин;
- средства, индуцирующие апоптоз, и антиангиогенные средства, такие как ингибиторы Bcl-2, например, YC 137, BH 312, ABT 737, госсипол, HA 14-1, TW 37 или декановую кислоту;
- тубулинсвязывающие средства, например, комбрестатин, колхицины или нокодазол;
- ингибиторы киназы (например, ингибиторы EGFR (рецептор фактора роста эпителия), MTKI (многонаправленные ингибиторы киназы), ингибиторы mTOR), например, флавоперидол, иматиниба мезилат, эрлотиниб, гефитиниб, дасатиниб, лапатиниб, лапатиниба дитозилат, сорафениб, сунитиниб, сунитиниба малеат, темсиролимус;
- ингибиторы фарнесилтрансферазы, например, типифарниб;
- ингибиторы гистондеацетилазы (HDAC), например, бутират натрия, субероиланилид гидроксамовой кислоты (SAHA), депсипептид (FR 901228), NVP-LAQ824, R306465, JNJ-26481585, трихостатин A, вориностат;
- ингибиторы убиквитин-протеасомного пути, например, PS-341, MLN.41 или бортезомиб;
- Йонделис;
- ингибиторы теломеразы, например, теломестатин;
- ингибиторы матриксных металлопротеиназ, например, батимастат, маримастат, приностат или метастат.
- Рекомбинантные интерлейкины, например, алдеслейкин, денилейкина дифтитокс, интерферон-альфа 2a, интерферон-альфа 2b, пегинтерферон-альфа 2b
- ингибиторы MAPK
- Ретиноиды, например, алитретиноин, бексаротен, третиноин
- Триоксид мышьяка
- Аспарагиназу
- Стероиды, например, дромостанолона пропионат, мегестрола ацетат, нандролон (деканоат, фенпропионат), дексаметазон
- Агонисты или антагонисты гонадотропин-рилизинг гормона, например, абареликс, гозерелина ацетат, гистрелина ацетат, лейпролида ацетат
- Талидомид, леналидомид
- Меркаптопурин, митотан, памидронат, пэгадемас, пэгаспаргазу, расбуриказу
- Миметики ВH3, например, ABT-737
- Ингибиторы MEK, например, PD98059, AZD6244, Cl-1040
- аналоги колониестимулирующего фактора, например, филграстим, пэгфилграстим, сарграмостим; эритропоэтин или его аналоги (например, дарбепоэтин альфа); интерлейкин 11; опрелвекин; золедронат; золедроновая кислота; фентанил; бисфосфонат; палифермин.
- стероидный ингибитор цитохром Р450 17-альфа-гидроксилазы-17,20-лиазы (CYP17), например, абиратерон, абиратерона ацетат.
Комбинации или фармацевтические композиции настоящего изобретения также имеют терапевтические применения в сенсибилизации опухолевых клеток для лучевой терапии и химиотерапии.
Таким образом, комбинации или фармацевтические композиции настоящего изобретения могут применяться в качестве "радиосенсибилизатора" и/или "хемосенсибилизатора" или могут быть представлены в комбинации с другим "радиосенсибилизирующим" и/или "хемосенсибилизирующим" соединением.
Термин "радиосенсибилизатор" или "радиосенсибилизирующее" соединение при использовании в настоящем описании определяют как комбинацию или фармацевтическую композицию настоящего изобретения, или молекулу, предпочтительно молекулу с низкой молекулярной массой, которая при введении животным в терапевтически эффективных количествах повышает чувствительность клеток к ионизирующему излучению и/или способствует лечению заболеваний, которые поддаются лечению ионизирующим излучением.
Термин "хемосенсибилизатор" или "хемосенсибилизирующее" соединение при использовании в настоящем описании определяют как комбинацию или фармацевтическую композицию настоящего изобретения, или молекулу, предпочтительно молекулу с низкой молекулярной массой, которая при введении животным в терапевтически эффективном количестве повышает чувствительность клеток к химиотерапии и/или способствует лечению заболеваний, которые поддаются лечению химиотерапевтическими средствами.
Некоторые механизмы способа действия радиосенсибилизаторов были предложены в литературе, включая: гипоксические клеточные радиосенсибилизаторы (например, соединения 2-нитроимидазола и соединения бензотриазина диоксида), имитирующие кислород или, альтернативно, ведущие себя подобно биовосстановительным средствам при гипоксии; негипоксические клеточные радиосенсибилизаторы (например, галогенированные пиримидины) могут быть аналогами оснований ДНК и предпочтительно могут встраиваться в ДНК раковых клеток и, тем самым, стимулировать индуцированное излучением разрушение молекул ДНК и/или блокировать нормальные механизмы репарации ДНК; и различные другие потенциальные механизмы действия были предположены в качестве радиосенсибилизаторов в лечении заболевания.
В настоящее время во многих методиках лечения рака применяют радиосенсибилизаторы в сочетании с рентгеновским излучением. Примеры радиосенсибилизаторов, активируемых рентгеновским излучением, включают, без ограничения, следующие соединения: метронидазол, мизонидазол, десметилмизонидазол, пимонидазол, этанидазол, ниморазол, митомицин C, RSU 1069, SR 4233, EО9, RB 6145, никотинамид, 5-бромдезоксиуридин (BUdR), 5-иоддезоксиуридин (IUdR), бромдезоксицитидин, фтордезоксиуридин (FudR), гидроксимочевину, цисплатин и терапевтически эффективные аналоги и производные перечисленных соединений.
В фотодинамической терапии (ФДТ) раковых опухолей видимый свет используется в качестве радиационного активатора сенсибилизирующего средства. Примеры фотодинамических радиосенсибилизаторов включают, без ограничения, следующие соединения: производные гематопорфирина, фотофрин, производные бензопорфирина, этиопорфирин олова, феоборбид-a, бактериохлорофилл-a, нафталоцианины, фталоцианины, фталоцианин цинка и терапевтически эффективные аналоги и производные перечисленных соединений.
Радиосенсибилизаторы могут быть введены в сочетании с терапевтически эффективным количеством одного или более других соединений, включающих, без ограничения: соединения, которые способствуют включению радиосенсибилизаторов в клетки-мишени; соединения, которые регулируют поток терапевтических средств, питательных веществ и/или кислорода к клеткам-мишеням; химиотерапевтические средства, которые действуют на опухоль с дополнительным облучением или без него; или другие терапевтически эффективные соединения, предназначенные для лечения рака или других заболеваний.
Хемосенсибилизаторы могут быть введены в сочетании с терапевтически эффективным количеством одного или более других соединений, включающих, без ограничения: соединения, которые способствуют включению хемосенсибилизаторов в клетки-мишени; соединения, которые регулируют поток терапевтических средств, питательных веществ и/или кислорода к клеткам-мишеням; химиотерапевтические средства, которые действуют на опухоль, или другие терапевтически эффективные соединения, предназначенные для лечения рака или других заболеваний. Антагонисты кальция, например, верапамил, как было обнаружено, могут применяться в комбинации с антинеопластическими средствами для достижения чувствительности к химиотерапевтическим препаратам в опухолевых клетках, резистентных к общепринятым химиотерапевтическим средствам, и для повышения эффективности таких соединений в чувствительных к лекарственным средствам злокачественных опухолях.
Настоящее изобретение также относится к применению комбинации настоящего изобретения для производства лекарственного средства для лечения нарушения, опосредованного FGFR, в частности рака.
Настоящее изобретение также относится к применению фармацевтической композиции настоящего изобретения для производства лекарственного средства для лечения нарушения, опосредованного FGFR, в частности рака.
Настоящее изобретение также относится к применению комбинации настоящего изобретения для производства лекарственного средства для профилактики резистентности опухоли или рака к ингибитору FGFR комбинации или для задержки резистентности опухоли или рака к ингибитору FGFR комбинации.
Настоящее изобретение также относится к применению фармацевтической композиции настоящего изобретения для производства лекарственного средства для профилактики резистентности опухоли или рака к ингибитору FGFR фармацевтической композиции или для задержки резистентности опухоли или рака к ингибитору FGFR фармацевтической композиции.
Настоящее изобретение также относится к применению комбинации настоящего изобретения для производства лекарственного средства для профилактики развития резистентности опухоли или рака к ингибитору FGFR комбинации или для задержки развития резистентности опухоли или рака к ингибитору FGFR комбинации.
Настоящее изобретение также относится к применению фармацевтической композиции настоящего изобретения для производства лекарственного средства для профилактики развития резистентности опухоли или рака к ингибитору FGFR фармацевтической композиции или для задержки развития резистентности опухоли или рака к ингибитору FGFR фармацевтической композиции.
Настоящее изобретение также относится к применению комбинации настоящего изобретения для производства лекарственного средства для профилактики или лечения, в особенности для лечения опухоли или рака, где активация сигнального пути IGF является механизмом резистентности опухоли или рака к ингибитору FGFR.
Настоящее изобретение также относится к применению фармацевтической композиции настоящего изобретения для производства лекарственного средства для профилактики или лечения, в особенности для лечения опухоли или рака, где активация сигнального пути IGF является механизмом резистентности опухоли или рака к ингибитору FGFR.
Настоящее изобретение также относится к применению ингибитора IGF1R, в особенности ингибитора IGF1R, описанного в настоящей заявке, для предотвращения резистентности, задержки резистентности, предотвращения развития резистентности или задержки развития резистентности опухоли или рака к ингибитору FGFR, в особенности ингибитору FGFR, описанному в настоящей заявке, более конкретно соединения A или его фармацевтически приемлемой соли или его сольвата, или соединения B или его фармацевтически приемлемой соли или его сольвата.
Соединения в фоме солей в комбинациях или фармацевтических композициях настоящего изобретения обычно являются фармацевтически приемлемыми солями, при этом примеры фармацевтически приемлемых солей обсуждаются в публикации Berge et al. (1977) "Pharmaceutically Acceptable Salts", J. Pharm. Sci., Vol. 66, pp. 1-19. Впрочем, соли, которые не являются фармацевтически приемлемыми, также могут быть получены в форме промежуточных соединений, которые затем могут быть превращены в фармацевтически приемлемые соли. Такие, не являющиеся фармацевтически приемлемыми, солевые формы, которые могут оказаться пригодными, например, при очистке или разделении соединений согласно изобретению, также составляют часть изобретения.
Соли согласно настоящему изобретению могут быть синтезированы из исходного соединения, которое содержит основную или кислотную группу, с помощью стандартных химических способов, таких как способы, описанные в Pharmaceutical Salts: Properties, Selection, and Use, P. Heinrich Stahl (Editor), Camille G. Wermuth (Editor), ISBN: 3-90639-026-8, Hardcover, 388 pages, August 2002. Как правило, такие соли могут быть получены при взаимодействии указанных соединений в форме свободной кислоты или основания с соответствующим основанием или кислотой в воде или в органическом растворителе, или в их смеси; обычно используют неводные среды, такие как эфир, этилацетат, этанол, изопропанол или ацетонитрил. Соединения согласно изобретению могут существовать в виде моно- или ди-солей в зависимости от pKa кислоты, из которой образуется соль.
Соли присоединения кислот могут быть образованы с использованием целого ряда кислот, как неорганических, так и органических. Примеры солей присоединения кислот включают соли, образованные с кислотой, выбранной из группы, состоящей из уксусной, 2,2-дихлоруксусной, адипиновой, альгиновой, аскорбиновой (например, L-аскорбиновой), L-аспарагиновой, бензолсульфоновой, бензойной, 4-ацетамидобензойной, бутановой, (+)камфорной, камфорсульфоновой, (+)-(1S)-камфор-10-сульфоновой, каприновой, капроновой, каприловой, коричной, лимонной, цикламовой, додецилсерной, этан-1,2-дисульфоновой, этансульфоновой, 2-гидроксиэтансульфоновой, муравьиной, фумаровой, галактаровой, гентизиновой, глюкогептоновой, D-глюконовой, глюкуроновой (например, D-глюкуроновой), глутаминовой (например, L-глутаминовой), α-оксоглутаровой, гликолевой, гиппуровой, бромоводородной, хлороводородной, иодоводородной, изетионовой, молочной (например, (+)-L-молочной, (±)-DL-молочной), лактобионовой, малеиновой, яблочной, (-)-L-яблочной, малоновой, (±)-DL-миндальной, метансульфоновой, нафталинсульфоновой (например, нафталин-2-сульфоновой), нафталин-1,5-дисульфоновой, 1-гидрокси-2-нафтойной, никотиновой, азотной, олеиновой, оротовой, щавелевой, пальмитиновой, памовой, фосфорной, пропионовой, L-пироглутаминовой, пировиноградной, салициловой, 4-аминосалициловой, себациновой, стеариновой, янтарной, серной, танниновой, (+)-L-винной, тиоциановой, толуолсульфоновой (например, p-толуолсульфоновой), ундециленовой и валериановой кислот, а также ацилированных аминокислот и катионообменных смол.
Одна отдельная группа солей состоит из солей, образованных из уксусной, хлороводородной, иодоводородной, фосфорной, азотной, серной, лимонной, молочной, янтарной, малеиновой, яблочной, изетионовой, фумаровой, бензолсульфоновой, толуолсульфоновой, метансульфоновой (мезилат), этансульфоновой, нафталинсульфоновой, валериановой, уксусной, пропановой, бутановой, малоновой, глюкуроновой и лактобионовой кислот. Другая группа солей присоединения кислот включает соли, образованные из уксусной, адипиновой, аскорбиновой, аспарагиновой, лимонной, DL-молочной, фумаровой, глюконовой, глюкуроновой, гиппуровой, хлороводородной, глутаминовой, DL-яблочной, метансульфоновой, себациновой, стеариновой, янтарной и винной кислот.
Если соединение является анионным или имеет функциональную группу, которая может быть анионной, то тогда соль может быть образована с подходящим катионом. Примеры подходящих неорганических катионов включают, без ограничения, ионы щелочных металлов, такие как Na+ и K+, катионы щелочноземельных металлов, такие как Ca2+ и Мg2+, и другие катионы, такие как Al3+. Примеры подходящих органических катионов включают, без ограничения, ион аммония (т.e. NH4+) и ионы замещенного аммония (например, NH3R+, NH2R2+, NHR3+, NR4+).
Примерами некоторых подходящих ионов замещенного аммония являются ионы, которые получены из: этиламина, диэтиламина, дициклогексиламина, триэтиламина, бутиламина, этилендиамина, этаноламина, диэтаноламина, пиперазина, бензиламина, фенилбензиламина, холина, меглумина и трометамина, а также аминокислот, таких как лизин и аргинин. Примером обычного иона четвертичного аммония является N(CH3)4+.
В одном варианте осуществления фармацевтически приемлемые соли ингибиторов FGFR, соединения A и соединения B, комбинаций или фармацевтических композиций настоящего изобретения являются солями присоединения кислот.
В одном варианте осуществления, где комбинации или фармацевтические композиции настоящего изобретения включают, в качестве ингибитора FGFR, соединение A или его фармацевтически приемлемую соль или его сольват, или соединение B или его фармацевтически приемлемую соль или его сольват, указанное соединение A или соединение B присутствуют в форме соли, в особенности такой соли соединения A и соединения B, как описано выше в разделе уровень техники изобретения.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают ингибитор FGFR в форме свободного основания.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают ингибитор IGF1R в форме свободного основания.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения включают ингибитор FGFR и ингибитор IGF1R в форме свободного основания.
Соединения комбинаций или фармацевтических композиций настоящего изобретения могут образовывать сольваты, например, с водой (т.e. гидраты) или с обычными органическими растворителями. При использовании в настоящем описании, термин "сольват" означает физическую ассоциацию соединений согласно настоящему изобретению с одной или более молекулами растворителя. Указанная физическая ассоциация включает различные степени ионного и ковалентного связывания, включая образование водородных связей. В некоторых случаях сольват можно выделять, например, когда одна или более молекул растворителя включены в кристаллическую решетку твердого кристаллического вещества. Термин "сольват" охватывает как сольваты в фазе раствора, так и выделяемые сольваты. Неограничивающие примеры подходящих сольватов включают соединения согласно изобретению в комбинации с водой, изопропанолом, этанолом, метанолом, ДМСО, этилацетатом, уксусной кислотой или этаноламином и подобным. Соединения согласно изобретению могут проявлять свое биологическое действие, когда они находятся в растворе. Сольваты фармацевтически приемлемых солей соединений в комбинациях или фармацевтических композициях настоящего изобретения также охвачены термином "сольват".
Сольваты хорошо известны в фармацевтической химии. Они могут играть важную роль в способах получения вещества (например, в отношении его очистки, хранения вещества (например, его стабильности) и легкости обращения с веществом) и часто образуются как часть стадий выделения или очистки химического синтеза. Специалист в данной области сможет определить посредством стандартных и длительно используемых методик, образовался ли гидрат или другой сольват в условиях выделения или условиях очистки, применяемых для получения данного соединения. Примеры таких методик включают термогравиметрический анализ (ТГА), дифференциальную сканирующую калориметрию (ДСК), рентгеновскую кристаллографию (например, рентгеновскую кристаллографию монокристаллов или порошковую рентгеновскую дифракцию) и ЯМР твердого тела (ЯМР-ТТ, также известную как ЯМР с вращением образца под магическим углом или ЯМР-ВМУ). Такие методики представляют собой такую же часть стандартного аналитического инструментального набора опытного химика, как и ЯМР, ИК, ВЭЖХ и МС. В альтернативе, специалист в данной области может получить сольват искусственно, при использовании условий кристаллизации, которые включают количество растворителя, требуемое для конкретного сольвата. Далее описанные выше стандартные методы могут быть использованы для установления факта образования сольватов. Также соединения, описанные в настоящей заявке, охватывает любые комплексы (например, комплексы включения или клатраты с соединениями, такими как циклодекстрины, или комплексы с металлами) соединений.
Кроме того, соединения комбинаций или фармацевтических композиций настоящего изобретения могут иметь одну или более полиморфных (кристаллических) или аморфных форм и, в таком качестве, должны быть включены в объем изобретения.
При использовании в настоящем описании, термин "модуляция", применительно к активности киназы, определяет изменение уровня биологической активности протеинкиназы. Таким образом, модуляция охватывает физиологические изменения, которые вызывают увеличение или уменьшение соответствующей протеинкиназной активности. В последнем случае модуляция может быть описана как "ингибирование". Модуляция может проявляться прямо или косвенно, и может быть опосредована любым механизмом и на любом физиологическом уровне, в том числе, например, на уровне экспрессии генов (включая, например, транскрипцию, трансляцию и/или посттрансляционную модификацию), на уровне экспрессии генов, кодирующих регуляторные элементы, которые прямо или косвенно влияют на уровни киназной активности. Таким образом, модуляция может предполагать повышенную/подавленную экспрессию или оверэкспрессию или недостаточную экспрессию киназы, включая амплификацию гена (т.е. множество копий гена) и/или повышенную или пониженную экспрессию под влиянием транскрипционного эффекта, а также гипер- (или гипо-) активность и (де)активацию протеинкиназы(киназ) (включая (де)активацию) под действием мутации(ий). Термины "модулированный", "модулирующий" и "модулировать" следует интерпретировать соответствующим образом.
При использовании в настоящем описании, термин "опосредованный", применительно к киназе, описанной в настоящей заявке (и применяемый, например, к различным физиологическим процессам, заболеваниям, состояниям, патологическим состояниям, терапиям, лечениям или вмешательствам), предназначен для ограничительного использования в силу того, что различные процессы, заболевания, состояния, патологические состояния, лечения и вмешательства, к которым применяется термин, являются такими, при которых киназа играет биологическую роль. В случаях, когда термин применяют к заболеванию, состоянию или патологическому состоянию, биологическая роль, которую играет киназа, может быть прямой или косвенной и может быть необходимой и/или достаточной для проявления симптомов заболевания, состояния или патологического состояния (или его этиологии или прогрессии). Таким образом, активность киназы (и, в частности, аберрантные уровни активности киназы, например, оверэкспрессия киназы) необязательно должна быть ближайшей причиной заболевания, состояния или патологического состояния: скорее предполагается, что опосредованные киназой заболевания, состояния или патологические состояния включают такие, которые имеют многофакторные этиологии и сложное прогрессирование, при которых рассматриваемая киназа участвует лишь частично. В случаях, когда термин применяют к лечению, профилактике или вмешательству, роль, которую играет киназа, может быть прямой или косвенной и может быть необходимой и/или достаточной для проведения лечения, профилактики или исхода вмешательства. Таким образом, заболевание или патологическое состояние, опосредованное киназой, включает развитие резистентности к любому конкретному противоопухолевому средству или лечению рака.
Таким образом, например, комбинации или фармацевтические композиции настоящего изобретения могут применяться в ослаблении или уменьшении заболеваемости раком.
Ингибиторы FGFR, соединение A и соединение B, комбинаций и фармацевтических композиций обладают активностью против FGFR1, FGFR2, FGFR3 и/или FGFR4, и, в особенности, против FGFR1, FGFR2, FGFR3 и FGFR4.
Как следствие их активности в модулировании или ингибировании FGFR, комбинации или фармацевтические композиции настоящего изобретения смогут применяться в предоставлении средств предотвращения роста или индукции апоптоза неоплазий, в особенности путем ингибирования ангиогенеза. Таким образом, следует ожидать, что комбинации или фармацевтические композиции настоящего изобретения окажутся полезными в лечении или предотвращении пролиферативных нарушений, таких как раковые опухоли. Кроме того, комбинации или фармацевтические композиции настоящего изобретения смогут применяться в лечении заболеваний, при которых имеется нарушение пролиферации, апоптоза или дифференцировки.
Примеры типов рака, которые можно лечить (или ингибировать) комбинациями или фармацевтическими композициями настоящего изобретения, включают, без ограничения, карциному, например, карциному мочевого пузыря, молочной железы, толстой кишки (например, колоректальные карциномы, такие как аденокарциному толстой кишки и аденому толстой кишки), почки, уротелиальную, матки, эпидермиса, печени, легкого (например, аденокарциному, мелкоклеточный рак легкого и немелкоклеточные карциномы легких, плоскоклеточный рак легкого), пищевода, головы и шеи, желчного пузыря, яичника, поджелудочной железы (например, карциному экзокринного отдела поджелудочной железы), желудка, желудочно-кишечный (также называемый раком желудка) рак (например, желудочно-кишечные стромальные опухоли), шейки матки, эндометрия, щитовидной железы, предстательной железы или кожи (например, плоскоклеточную карциному или возвышающуюся дерматофибросаркому); рак гипофиза, гемобластоз лимфоидного происхождения, например, лейкоз, острый лимфолейкоз, хронический лимфолейкоз, B-клеточную лимфому (например, диффузную В-крупноклеточную лимфому), T-клеточную лимфому, лимфому Ходжкина, неходжкинскую лимфому, волосатоклеточную лимфому или лимфому Беркитта; гемобластоз миелоидного происхождения, например, лейкозы, острые и хронические миелолейкозы, хронический миеломоноцитарный лейкоз (ХММЛ), миелопролиферативное нарушение, миелопролиферативный синдром, миелодиспластический синдром или промиелоцитарный лейкоз; множественную миелому; фолликулярный рак щитовидной железы; гепатоцеллюлярный рак, опухоль мезенхимального происхождения (например, саркому Юинга), например, фибросаркому или рабдомиосаркому; опухоль центральной или периферической нервной системы, например, астроцитому, нейробластому, глиому (такую как мультиформная глиобластома) или шванному; меланому; семиному; тератокарциному; остеосаркому; ретикуллярный прогрессирующий меланоз; кератоакантому; фолликулярный рак щитовидной железы или саркому Капоши. В частности, плоскоклеточный рак легких, рак молочной железы, рак толстой и прямой кишки, глиобластому, астроцитомы, рак предстательной железы, мелкоклеточный рак легких, меланому, злокачесвенные опухоли головы и шеи, рак щитовидной железы, рак матки, рак желудка, гепатоцеллюлярный рак, рак шейки матки, множественную миелому, рак мочевого пузыря, рак эндометрия, уротелиальный рак, рак толстой кишки, рабдомиосаркому, рак гипофиза.
Примеры типов рака, который можно лечить (или ингибировать), включают, без ограничения, рак мочевого пузыря, уротелиальный рак, метастатический уротелиальный рак, хирургически неоперабельный уротелиальный рак, рак молочной железы, глиобластому, рак легкого, немелкоклеточный рак легкого, плоскоклеточный рак легкого, аденокарциному легкого, легочную аденокарциному, мелкоклеточный рак легкого, рак яичника, рак эндометрия, рак шейки матки, саркому мягких тканей, плоскоклеточный рак головы и шеи, рак желудка, рак пищевода, плоскоклеточный рак пищевода, аденокарциному пищевода, холангиокарциному, гепатоцеллюлярный рак.
Некоторые типы рака являются резистентными к лечению определенными лекарственными средствами. Это может быть обусловлено типом опухоли или может возникать вследствие лечения соединением. В этой связи, ссылки на множественную миелому включают чувствительную к бортезомибу множественную миелому или рефрактерную множественную миелому. Аналогичным образом, ссылки на хронический миелолейкоз включают чувствительный к иматинибу хронический миелолейкоз и рефрактерный хронический миелолейкоз. Хронический миелолейкоз также известен как хронический миелобластный лейкоз, хронический гранулоцитарный лейкоз или ХМЛ. Аналогично, острый миелолейкоз также назвают острым миелобластным лейкозом, острым гранулоцитарным лейкозом, острым нелимфоцитарным лейкозом или ОМЛ.
Комбинации или фармацевтические композиции настоящего изобретения также могут применяться в лечении заболеваний системы кроветворения с нарушенной клеточной пролиферацией, будь то предзлокачественные или стабильные заболевания, такие как миелопролиферативные заболевания. Миелопролиферативные заболевания ("МПЗ") представляют собой группу заболеваний костного мозга, в котором продуцируются избыточные клетки. Они связаны с и могут переходить в миелодиспластический синдром. Миелопролиферативные заболевания включают истинную полицитемию, эссенциальную тромбоцитемию и первичный миелофиброз. Другим гематологическим нарушением является гиперэозинофильный синдром. Т-клеточные лимфопролиферативные заболевания включают заболевания, которые обусловлены натуральными киллерными клетками.
Кроме того, комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения желудочно-кишечного рака (также известного как рак желудка), например, желудочно-кишечных стромальных опухолей. Желудочно-кишечный рак относится к злокачественным заболеваниям желудочно-кишечного тракта, включая пищевод, желудок, печень, желчную систему, поджелудочную железу, кишечник и анус.
Таким образом, в комбинациях, фармацевтических композициях, применениях или способах настоящего изобретения для лечения заболевания или патологического состояния, включающих аномальный рост клеток, заболевание или патологическое состояние, включающее аномальный рост клеток, в одном варианте осуществления являются раком.
Определенные подгруппы типов рака включают множественную миелому, карциному мочевого пузыря, шейки матки, предстательной железы и щитовидной железы, рак легкого, молочной железы и толстой кишки.
Другая подгруппа типов рака включает множественную миелому, карциному мочевого пузыря, гепатоцеллюлярную карциному, плоскоклеточную карциному ротовой полости и карциномы шейки матки.
Другая подгруппа типов рака включает злокачественные новообразования мочевого пузыря, легкого, молочной железы, желудка, гепатоцеллюлярные злокачественные новообразования, злокачественные новообразования толстой кишки, гемобластозы, новообразования яичников, глиобластому.
Другая подгруппа типов рака включает рак мочевого пузыря, легкого, молочной железы, желудка и гепатоцеллюлярный рак.
Комбинации или фармацевтические композиции настоящего изобретения, обладающие FGFR, например, FGFR1 ингибирующей активностью, могут быть особенно полезными при лечении или профилактике рака молочной железы, в частности классической дольковой карциномы (КДК).
Если комбинации или фармацевтическии композиции настоящего изобретения обладают FGFR4 активностью, они также смогут применяться при лечении раковых опухолей предстательной железы или гипофиза, или они будут применяться при лечении рака молочной железы, рака легкого, рака предстательной железы, рака печени (ГЦК) или рака легкого.
В частности, комбинации или фармацевтические композиции настоящего изобретения, включающие ингибиторы FGFR, могут применяться при лечении множественной миеломы, миелопролиферативных нарушений, рака эндометрия, рака предстательной железы, рака мочевого пузыря, рака легкого, рак яичника, рака молочной железы, рака желудка, рака толстой и прямой кишки и плоскоклеточной карциномы ротовой полости.
Другими подгуппами типов рака является множественная миелома, рак эндометрия, рак мочевого пузыря, рак шейки матки, рак предстательной железы, рак легкого, рак молочной железы, рак толстой и прямой кишки и карциномы щитовидной железы.
В частности, комбинации или фармацевтические композиции настоящего изобретения могут применяться при лечении множественной миеломы (в частности, множественной миеломы с транслокацией t(4;14) или оверэкспрессией FGFR3), рака предстательной железы (гормонорезистентных карцином предстательной железы), рака эндометрия (в частности, опухолей эндометрия с активирующими мутациями в FGFR2) и рака молочной железы (в частности, долькового рака молочной железы).
В частности, комбинации или фармацевтические композиции настоящего изобретения могут применяться при лечении дольковых карцином, таких как КДК (классическая дольковая карцинома).
Если комбинации или фармацевтические композиции настоящего изобретения обладают активностью против FGFR3, они смогут применяться при лечении множественной миеломы и рака мочевого пузыря.
В частности, соединения обладают активностью против опухолей с транслокацией FGFR3-TACC3, в частности, опухолей мочевого пузыря или головного мозга с транслокацией FGFR3-TACC3.
В частности, комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения t(4;14)-транслокация-положительной множественной миеломы.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения саркомы. В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения рака легкого, например, плоскоклеточной карциномы.
Если комбинации или фармацевтические композиции настоящего изобретения обладают активностью против FGFR2, они смогут применяться при лечении рака эндометрия, яичника, желудка, гепатоцеллюлярного рака, рака матки, шейки матки и рака толстой и прямой кишки. FGFR2 также оверэксрессирован в эпителиальном раке яичника, поэтому комбинации или фармацевтические композиции настоящего изобретения могут, в частности, применяться при лечении рака яичника, такого как эпителиальный рак яичника.
В одном варианте осуществления комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения рака легкого, в особенности НМРЛ (немелкоклеточного рака легкого), плоскоклеточной карциномы, рака печени, рака почки, рака молочной железы, рака толстой кишки, рака толстой и прямой кишки, рака предстательной железы.
Комбинации или фармацевтические композиции настоящего изобретения могут также применяться при лечении опухолей, ранее подвергавшихся лечению ингибитором VEGFR2 или антителом к VEGFR2 (например, авастином).
В частности, комбинации или фармацевтические композиции настоящего изобретения могут применяться при лечении VEGFR2-резистентных опухолей. Ингибиторы VEGFR2 и антитела применяют при лечении карцином щитовидной железы и почечно-клеточных карцином, поэтому комбинации или фармацевтические композиции настоящего изобретения могут применяться при лечении VEGFR2-резистентных карцином щитовидной железы и почечно-клеточных карцином.
Раковые опухоли могут быть раковыми опухолями, которые чувствительны к ингибированию одного или более FGFR, выбранных из FGFR1, FGFR2, FGFR3, FGFR4, например, одного или более FGFR, выбранных из FGFR1, FGFR2 или FGFR3.
Является ли конкретный тип рака или не является таким типом рака, который чувствителен к ингибированию сигнализации FGFR, можно определить посредством анализа роста клеток, как описано ниже, или способом, представленным в разделе, озаглавленном "Способы диагностики".
Соединения изобретения, и в особенности соединения, обладающие FGFR-ингибирующей активностью, могут быть особенно полезными в лечении или предотвращении типов рака, ассоциированных с наличием или характеризующихся наличием повышенных уровней FGFR, например, раковых опухолей, указанных в данном контексте во вводном разделе настоящей заявки.
Комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения взрослых больных. Комбинации или фармацевтические композиции настоящего изобретения могут применяться для лечения больных детского возраста.
Комбинации или фармацевтические композиции настоящего изобретения могут применяться в лечении других состояний, которые вызваны нарушением пролиферации, таких как сахарный диабет II типа или инсулинонезависимый сахарный диабет, аутоиммунные заболевания, черепно-мозговая травма, инсульт, эпилепсия, нейродегенеративные заболевания, такие как болезнь Альцгеймера, болезнь двигательного нейрона, прогрессирующий супрануклеарный паралич, кортико-базальная дегенерация и болезнь Пика, например, аутоиммунные заболевания и нейродегенеративные заболевания.
Одна подгруппа заболеваний и состояний, при которых могут применяться комбинации или фармацевтические композиции настоящего изобретения, состоит из воспалительных заболеваний, сердечнососудистых заболеваний и заживления ран.
Также известно, что FGFR играет роль в апоптозе, ангиогенезе, пролиферации, дифференцировке и транскрипции, и поэтому соединения, комбинации, фармацевтические композиции изобретения могут применяться в лечении следующих заболеваний помимо рака; хронических воспалительных заболеваний, например, системной красной волчанки, аутоиммунно-опосредованного гломерулонефрита, ревматоидного артрита, псориаза, воспалительного заболевания кишечника, аутоиммунного сахарного диабета, реакций гиперчувствительности в виде экземы, астмы, ХОБЛ, ринита и заболевания верхних дыхательных путей; сердечнососудистых заболеваний, например, гипертрофии сердца, рестеноза, атеросклероза; нейродегенеративных нарушений, например, болезни Альцгеймера, СПИД-ассоциированной деменции, болезни Паркинсона, амиотрофического бокового склероза, пигментного ретинита, спинальной мышечной атрофии и мозжечковой дегенерации; гломерулонефрита; миелодиспластических синдромов, ассоциированного с ишемическим повреждением инфаркта миокарда, инсульта и реперфузионного повреждения, аритмии, атеросклероза, заболеваний печени, вызванных токсинами и связанных с алкоголем, гематологических заболеваний, например, хронической анемии и апластической анемии; дегенеративных заболеваний костно-мышечной системы, например, остеопороза и артрита, аспирин-чувствительного риносинусита, муковисцидоза, рассеянного склероза, заболеваний почек и боли при раке.
Кроме того, мутации FGFR2 ассоциированы с несколькими тяжелыми нарушениями в развитии скелета человека, и, таким образом, соединения согласно изобретению могут применяться в лечении нарушений развития скелета человека, включающих аномальную оссификацию черепных швов (краниосиностоз), синдром Аперта (АР), синдром Крузона, синдром Джексона-Вейсса, синдром складчатой кожи Бира-Стивенсона и синдром Пфейффера.
Комбинации или фармацевтические композиции настоящего изобретения, обладающие FGFR, например, FGFR2 или FGFR3, ингибиторующей активностью, могут быть особенно полезными при лечении или предотвращении скелетных заболеваний. Конкретными скелетными заболеваниями являются ахондроплазия или танатофорная карликовость (также известная как танатофорная дисплазия).
Комбинации или фармацевтические композиции настоящего изобретения, обладающие FGFR, например, FGFR1, FGFR2 или FGFR3, ингибиторующей активностью, могут быть особенно полезными при лечении или предотвращении патологий, при которых прогрессирующий фиброз является симптомом. Фиброзные состояния, при лечении которых могут применяться соединения настоящего изобретения, включают заболевания, характеризующиеся аномальным или избыточным отложением фиброзной ткани, например, при циррозе печени, гломерулонефрите, фиброзе легких, системном фиброзе, ревматоидном артрите, а также при естественном процессе заживления ран. В частности, соединения согласно изобретению также могут применяться при лечении фиброза легких, в частности, идиопатического фиброза легких.
Оверэкспрессия и активация рецепторов FGFR в опухолеассоциированной сосудистой сети также предполагает наличие роли комбинаций или фармацевтических композиций настоящего изобретения в предотвращении и нарушении инициации ангиогенеза в опухоли. В частности, комбинации или фармацевтические композиции настоящего изобретения могут применяться в лечении рака, метастазирования, лейкоза, такого как ХЛЛ, заболеваний глаз, таких как возрастная макулодистрофия, в частности, влажная форма возрастной макулодистрофии, ишемические пролиферативные ретинопатии, такие как ретинопатия недоношенных (ROP) и диабетическая ретинопатия, ревматоидный артрит и гемангиома.
В одном варианте осуществления предложена комбинация или фармацевтическая композиция, определенная в настоящем описании, для применения в терапии, для применения в качестве лекарственного средства. В другом варианте осуществления предложена комбинация или фармацевтическая композиция, определенная в настоящем описании, для применения в профилактике или лечении, в особенности в лечении, заболевания или состояния, опосредованного FGFR-киназой.
Таким образом, например, комбинации или фармацевтические композиции настоящего изобретения могут применяться в ослаблении тяжести или уменьшении случаев рака. Следовательно, в другом варианте осуществления предложена комбинация или фармацевтическая композиция, определенная в настоящем описании, для применения в профилактике или лечении, в частности в лечении, рака. В одном варианте осуществления комбинация или фармацевтическая композиция, определенная в настоящем описании, предназначена для применения в профилактике или лечении FGFR-зависимого рака. В одном варианте осуществления комбинация или фармацевтическая композиция, определенная в настоящем описании, предназначена для применения в профилактике или лечении рака, опосредованного FGFR-киназами.
Таким образом, в изобретении помимо прочего предложено следующее:
Способ профилактики или лечения заболевания или состояния, опосредованного FGFR-киназой, где способ включает введение субъекту, нуждающемуся в этом, комбинации или фармацевтической композиции, как определено в настоящем описании.
-Способ профилактики или лечения заболевания или состояния, как описано в настоящей заявке, где способ включает введение субъекту, нуждающемуся в этом, комбинации или фармацевтической композиции, как определено в настоящем описании.
Способ профилактики или лечения рака, где способ включает введение субъекту, нуждающемуся в этом, комбинации или фармацевтической композиции, как определено в настоящем описании.
Способ ослабления тяжести или уменьшения случаев заболевания или состояния, опосредованного FGFR-киназой, где способ включает введение субъекту, нуждающемуся в этом, комбинациии или фармацевтической композиции, как определено в настоящем описании.
Способ ингибирования FGFR-киназы, где способ включает контакт киназы с ингибирующей киназу комбинацией или фармацевтической композицией, как определено в настоящем описании.
Способ модуляции клеточного процесса (например, деления клеток) посредством ингибирования активности FGFR-киназы с применением комбинации или фармацевтической композиции, как определено в настоящем описании.
Комбинация или фармацевтическая композиция, как определено в настоящем описании, для применения в качестве модулятора клеточного процесса (например, деление клеток) посредством ингибирования активности FGFR-киназы.
Комбинация или фармацевтическая композиция, как определено в настоящем описании, для применения в профилактике или лечении рака, в особенности лечении, рака.
Комбинация или фармацевтическая композиция, как определено в настоящем описании, для применения в качестве модулятора (например, ингибитора) FGFR.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения заболевания или состояния, опосредованного FGFR-киназой.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения заболевания или состояния, как описано в настоящем описании.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения, в особенности лечения, рака.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для модуляции (например, ингибирования) активности FGFR.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, в производстве лекарственного средства для модуляции клеточного процесса (например, деления клеток) посредством ингибирования активности FGFR-киназы.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения заболевания или патологического состояния, характеризуемого апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4).
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения рака, где рак характеризуется апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4).
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения рака у пациента, выбранного из субпопуляции, обладающей генетическими аберрациями FGFR3-киназы.
Применение комбинации или фармацевтической композиции, как определено в настоящем описании, для производства лекарственного средства для профилактики или лечения рака у пациента, который согласно поставленному диагнозу является частью субпопуляции, обладающей генетическими аберрациями FGFR3-киназы, в особенности имеет транслокацию FGFR3-TACC3, более конкретно имеет рак мочевого пузыря с транслокацией FGFR3-TACC3.
Способ профилактики или лечения заболевания или патологического состояния, характеризуемого апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), где способ включает введение комбинации или фармацевтической композиции, как определено в настоящем описании.
Способ ослабления тяжести или уменьшения случаев заболевания или патологического состояния, характеризуемого апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), где способ включает введение комбинации или фармацевтической композиции, как определено в настоящем описании.
Способ профилактики или лечения (или ослабления тяжести или уменьшения случаев) рака у пациента, страдающего раком или подозреваемого на наличие рака; где способ включает: (i) прохождение пациентом диагностического исследования с целью определения, имеет ли пациент генетические аберрации гена FGFR3, в частности транслокацию FGFR3-TACC3, более конкретно рак мочевого пузыря с транслокацией FGFR3-TACC3; и (ii) в случае присутствия у пациента указанного варианта, последующее введение пациенту комбинации или фармацевтической композиции, как определено в настоящем описании, обладающей ингибиторующей активностью в отношении FGFR3-киназы.
Способ профилактики или лечения (или ослабления тяжести или уменьшения случаев) заболевания или состояния, характеризуемого апрегуляцией FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), включающий: (i) прохождение пациентом диагностического исследования с целью определения маркера, характерного для апрегуляции FGFR-киназы (например, FGFR1 или FGFR2, или FGFR3, или FGFR4), и (ii) в случае, когда результат диагностического исследования свидетельствует о наличии апрегуляции FGFR-киназы, последующее введение пациенту комбинации или фармацевтической композиции, как определено в настоящем описании, обладающей ингибиторующей активностью в отношении FGFR-киназы.
В одном варианте осуществления заболеванием, опосредованным FGFR-киназами, является связанное с онкологией заболевание (например, рак). В одном варианте осуществления заболеванием, опосредованным FGFR-киназами, является не связанное с онкологией заболевание (например, любое представленное в описании заболевание, исключая рак). В одном варианте осуществления заболеванием, опосредованным FGFR-киназами, является состояние, описанное в настоящей заявке. В одном варианте осуществления изобретения заболеванием, опосредованным FGFR-киназами, является патологическое состояние скелета, описанное в настоящей заявке. Конкретные нарушения развития скелета человека включают нарушение оссификации черепных швов (краниосиностоз), синдром Аперта (AP), синдром Крузона, синдром Джексона-Вейсса, синдром складчатой кожи Бира-Стивенсона, синдром Пфейффера, ахондроплазию и танатофорную карликовость (также известную как танатофорная дисплазия).
Мутантные киназы
Лекарственно-устойчивые мутации киназы могут возникать в группах больных, которые проходили лечение ингибиторами киназы. Такие мутации образуются, частично, в областях белка, который связывается или взаимодействует с конкретным ингибитором, используемым в терапии. Такие мутации снижают или повышают способность ингибитора связываться и ингибировать данную киназу. Эти мутации могут возникать по любым аминокислотным остаткам, которые взаимодействуют с ингибитором или представляют важность для поддержания связывания указанного ингибитора с мишенью. Ингибитор, который связывается с киназой-мишенью без необходимости взаимодействия с мутировавшим аминокислотным остатком, вероятно, не будет затронут мутацией, и будет оставаться эффективным ингибитором фермента.
Изучение образцов больных раком желудка выявило присутствие двух мутаций в FGFR2, Ser167Pro в экзоне IIIa и мутацию сайта сплайсинга 940-2A-G в экзоне IIIc. Указанные мутации идентичны гаметным активирующим мутациям, которые вызывают синдромы краниосиностоза, и которые наблюдали в 13% исследованных тканях первичного рака желудка. Кроме того, активирующие мутации в FGFR3 наблюдали в 5% исследованных образцов пациентов, при этом оверэкспрессия рецепторов FGFR коррелировала с неблагоприятным прогнозом в данной группе пациентов.
Кроме того, существуют хромосомные транслокации или точковые мутации, которые наблюдали в FGFR, которые приводят к биологическим состояниям приобретения функции, оверэкспрессии или конститутивной активности.
Соединения, комбинации или фармацевтические композиции изобретения, таким образом, могут найти конкретное применение в отношении раковых опухолей, которые экспрессируют мутантную молекулярную мишень, такую как FGFR. Диагностика опухолей с такими мутациями может быть выполнена с применением методик, известных специалисту в данной области и описанных в настоящей заявке, таких как ОТПЦР и FISH.
Было сделано предположение, что мутации консервативного остатка треонина в АТФ-связывающем сайте FGFR должны приводить к устойчивости к ингибиторам. Аминокислотный остаток валин 561 был мутирован до метионина в FGFR1, что соответствует предыдущим сообщениям о мутациях, найденных в Abl (T315) и EGFR (T766), которые, как было показано, придают устойчивость к селективным ингибиторам. Данные анализа FGFR1 V561M показали, что указанная мутация придавала устойчивость к ингибитору тирозинкиназы по сравнению с диким типом.
Способы диагностики
Перед введением комбинации или фармацевтической композиции, как описано в настоящей заявке, пациент может быть подвергнут скринингу с целью определения, является ли заболевание или состояние, которым пациент страдает или может страдать, заболеванием или состоянием, которое может быть чувствительным к лечению соединением, обладающим активностью против FGFR.
Например, биологический образец, полученный у пациента, может быть проанализирован с целью определения, является ли заболевание или состояние, такое как рак, которым пациент страдает или может страдать, заболеванием или состоянием, которое характеризуется генетическим нарушением или аномальной белковой экспрессией, что приводит к апрегуляции уровней или активности FGFR или к сенсибилизации пути до нормальной активности FGFR, или к апрегуляции указанных путей сигнализации, связанных с фактором роста, таких как уровни лиганда фактора роста или активность лиганда фактора роста, или к апрегуляции биохимического пути, следующего после активации FGFR.
Примеры таких нарушений, которые приводят к активации или сенсибилизации сигнала от FGFR, включают потерю или ингибирование апоптических путей, апрегуляцию рецепторов или лигандов или присутствие мутантных вариантов рецепторов или лигандов, например, вариантов PTK. Опухоли с мутациями в FGFR1, FGFR2 или FGFR3, или FGFR4, или апрегуляцией, в частности оверэкспрессией FGFR1, или мутанты FGFR2 или FGFR3 с приобретением функции, могут быть особенно чувствительными к ингибиторам FGFR.
Например, точковые мутации с приобретением функции в FGFR2 были идентифицированы при ряде заболеваний. В частности, активирующие мутации в FGFR2 были идентифицированы в 10% опухолей эндометрия.
Кроме того, генетические аберрации рецепторной тирозинкиназы FGFR3, такие как хромосомные транслокации или точковые мутации, приводящие к эктопически экспрессированным или нерегулируемым, конститутивно активным рецепторам FGFR3, были идентифицированы и связаны с подгруппой множественных миелом, карцином мочевого пузыря и шейки матки. Конкретная мутация T674I рецептора PDGF была идентифицирована у больных, проходивших лечение иматинибом. Кроме того, амплификация гена 8p12-p11.2 была продемонстрирована в ~50% случаев долькового рака молочной железы (КДК), и, как было показано, она была связана с повышенной экспрессией FGFR1. Предварительные исследования с миРНК, направленными против FGFR1, или низкомолекулярным ингибитором рецептора, показали, что клеточные линии, несущие такую амплификацию, особенно чувствительны к ингибированию данного сигнального пути.
В альтернативе биологический образец, полученный у пациента, может быть проанализирован на предмет потери негативного регулятора или супрессора FGFR. В данном контексте термин "потеря" охватывает делецию гена, кодирующего регулятор или супрессор, усечение гена (например, в результате мутации), усечение транскрибируемого продукта гена или инактивацию транскрибируемого продукта (например, в результате точковой мутации) или секвестрацию другим генным продуктом.
Термин апрегуляция включает повышенную экспрессию или оверэкспрессию, включающую амплификацию гена (т.е. множественные копии гена) и повышенную экспрессию посредством транскрипционного эффекта, а также гиперактивность и активацию, включающую активацию в результате мутаций. Таким образом, больной может быть подвергнут диагностическому исследованию с целью определения маркера, характерного для апрегуляции FGFR. Термин диагностика включает скрининг. Под маркером подразумеваются генетические маркеры, включающие, например, измерение состава ДНК для идентификации мутаций FGFR. Термин маркер также включает маркеры, которые характерны для апрегуляции FGFR, включая ферментативную активность, уровни фермента, состояние фермента (например, фосфорилированное или нет) и уровни мРНК указанных выше белков.
Диагностические испытания и скрининги обычно проводят на биологическом образце, выбранном из биоптатов опухоли, образцов крови (выделение и обогащение выделенных опухолевых клеток), образцов кала, мокроты, анализа хромосом, плевральной жидкости, перитонеальной жидкости, соскоба со щеки, биоптата и мочи.
Способы идентификации и анализ мутаций и апрегуляции белков известны специалисту в данной области. Способы скрининга могут включать, без ограничения, стандартные методы, такие как полимеразную цепную реакцию с обратной транскриптазой (ОТ-ПЦР) или гибридизацию in situ, такую как флуоресцентная гибридизация in situ (FISH).
Идентификация индивида, несущего мутацию в FGFR, может означать, что больной может быть особенно подходящим для лечения ингибитором FGFR. Опухоли могут быть предпочтительно подвергнуты скринингу на присутствие варианта FGFR перед лечением. Способ скрининга обычно включает прямое секвенирование, анализ с олигонуклеотидными микрочипами или мутант-специфичным антителом. Кроме того, диагностика опухолей с такими мутациями может быть выполнена с использованием способов, известных специалисту в данной области и описанных в настоящей заявке, таких как ОТ-ПЦР и FISH.
Кроме того, мутантные формы, например, FGFR, могут быть идентифицированы путем прямого секвенирования, например, опухолевых биоптатов при использовании ПЦР и способов прямого секвенирования продуктов ПЦР, как описано выше. Специалисту в данной области будет очевидно, что все такие хорошо известные способы определения оверэкспрессии, активации или мутаций указанных выше белков могут быть применены к данному случаю.
В скрининге с помощью ОТ-ПЦР, уровень мРНК в опухоли оценивают путем создания кДНК копии мРНК с последующей амплификацией кДНК с помощью ПЦР. Методы ПЦР амплификации, выбор праймеров и условия амплификации хорошо известны специалисту в данной области. Манипуляции с нуклеиновыми кислотами и ПЦР осуществляют стандартными способами, как описано, например, в руководстве Ausubel, F.M. et al., eds. (2004) Current Protocols in Molecular Biology, John Wiley & Sons Inc., or Innis, M.A. et al., eds. (1990) PCR Protocols: a guide to methods and applications, Academic Press, San Diego. Реакции и манипуляции, включающие методы исследования нуклеиновых кислот, также описаны в руководстве Sambrook et al., (2001), 3rd Ed, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press. В альтернативе может быть использован коммерчески доступный набор для ОТ-ПЦР (например, Roche Molecular Biochemicals) или методики, описанные в патентах США 4,666,828; 4,683,202; 4,801,531; 5,192,659, 5,272,057, 5,882,864 и 6,218,529 и включенные в настоящее описание посредством отсылки. Примером способа гибридизации in situ для оценки экспрессии мРНК может быть флуоресцентная гибридизация in situ (FISH) (см., Angerer (1987) Meth. Enzymol., 152:649).
Как правило, гибридизация in situ включает следующие основные стадии: (1) фиксацию анализируемой ткани; (2) предварительную гибридизацию образца для повышения доступности целевой нуклеиновой кислоты и снижения неспецифического связывания; (3) гибридизацию смеси нуклеиновых кислот с нуклеиновой кислотой в биологической структуре или ткани; (4) промывки после гибридизации для удаления фрагментов нуклеиновой кислоты, не связавшихся при гибридизации, и (5) детектирование гибридизованных фрагментов нуклеиновой кислоты. Зонды, используемые в таких способах, обычно являются меченными, например, радиоизотопами или флуоресцентными репортерами. Предпочтительные зонды являются достаточно длинными, например, имеют длину от приблизительно 50, 100 или 200 нуклеотидов до приблизительно 1000 или более нуклеотидов, для осуществления специфической гибридизации с заданной нуклеиновой кислотой(ами) в жестких условиях. Стандартные методы проведения FISH описаны в руководстве Ausubel, F.M. et al., eds. (2004) Current Protocols in Molecular Biology, John Wiley & Sons Inc and Fluorescence In Situ Hybridization: Technical Overview by John M. S. Bartlett in Molecular Diagnosis of Cancer, Methods and Protocols, 2nd ed.; ISBN: 1-59259-760-2; March 2004, pps. 077-088; Series: Methods in Molecular Medicine.
Способы анализа уровня экспрессии генов описаны в DePrimo et al. (2003), BMC Cancer, 3:3. Кратко, методика является следующей: двухцепочечную кДНК синтезируют из суммарной РНК с использованием олигомера (dT)24 для праймирования синтеза первой цепи кДНК с последующим синтезом второй цепи кДНК со случайными гексамерными праймерами. Двухцепочечную кДНК используют в качестве матрицы для in vitro транскрипции кРНК с использованием биотинилированных рибонуклеотидов. кРНК химически фрагментируют согласно методикам, описанным Affymetrix (Santa Clara, CA, USA), а затем подвергают гибридизации в течение ночи на чипах Human Genome.
В альтернативе белковые продукты, экспрессированные из мРНК, могут быть проанализированы с помощью иммуногистохимического анализа образцов опухоли, твердофазного иммуноферментного анализа с микротитровальными планшетами, Вестерн-блоттинга, 2-мерного электрофореза в полиакриламидном геле с ДСН, ELISA, проточной цитометрии и других методов, известных в данной области для определения специфических белков. Способы определения могут включать сайтспецифические антитела. Специалисту в данной области будет очевидно, что все такие хорошо известные методы определения апрегуляции FGFR или определения вариантов или мутантов FGFR могут быть применены к данному случаю.
Аномальные уровни белков, таких как FGFR, могут быть измерены при использовании стандартных ферментных анализов, например, таких анализов, которые описаны в настоящей заявке. Активацию или оверэкспрессию также можно определять в образце ткани, например, ткани опухоли. При измерении активности тирозинкиназы с помощью такого анализа, как анализ Chemicon International, представляющая интерес тирозинкиназа должна быть иммунопреципитирована из лизата образца и измерена ее активность.
Альтернативные способы измерения оверэкспрессии или активации FGFR, включая его изоформы, включают измерение плотности микрососудистой сети. Плотность можно измерить, например, с помощью методов, описанных Orre and Rogers (Int J Cancer (1999), 84(2) 101-8).
Таким образом, все перечисленные способы также могут быть применены для идентификации опухолей, особенно подходящих для лечения комбинациями или фармацевтическими композициями согласно изобретению.
Комбинации или фармацевтические композиции согласно изобретению особенно пригодны в лечении пациента, имеющего мутантный FGFR. Мутация G697C в FGFR3 наблюдается в 62% плоскоклеточных карцином полости рта, при этом она вызывает конститутивную активацию киназной активности. Активирующие мутации FGFR3 также были идентифицированы в случаях карциномы мочевого пузыря. Указанные мутации включали 6 типов с различными степенями распространенности: R248C, S249C, G372C, S373C, Y375C, K652Q. Кроме того, полиморфизм Gly388Arg в FGFR4, как было обнаружено, ассоциирован с увеличением числа случаев и агрессивностью рака предстательной железы, толстой кишки, легкого, печени (ГЦК) и молочной железы.
Таким образом, в другом аспекте изобретение включает применение комбинации или фармацевтической композиции согласно изобретению с целью производства лекарственного средства для лечения или профилактики заболевания или состояния у пациента, прошедшего скрининг, показавший, что он страдает или подвергается риску развития заболевания или состояния, которое может поддаваться лечению соединением, обладающим активностью против FGFR.
Конкретные мутации, на наличие которых пациент проходит скрининг, включают G697C, R248C, S249C, G372C, S373C, Y375C, K652Q в FGFR3 и полиморфизм Gly388Arg в FGFR4.
В другом аспекте изобретение включает соединение, комбинацию или фармацевтическую композицию согласно изобретению для применения в профилактике или лечении рака у пациента, выбранного из субпопуляции, обладающей вариантом гена FGFR (например, мутация G697C в FGFR3 и полиморфизм Gly388Arg в FGFR4).
Ввиду своих полезных фармакологических свойств ингибиторы FGFR и ингибиторы IGF1R могут быть включены в различные лекарственные формы в целях применения.
В одном варианте осуществления фармацевтическая композиция (например, лекарственная форма) включает по меньшей мере один ингибитор FGFR или по меньшей мере один ингибитор IGF1R, или по меньшей мере один ингибитор FGFR и один ингибитор IGF1R изобретения вместе с одним или более фармацевтически приемлемыми носителями, адъювантами, вспомогательными веществами, разбавителями, наполнителями, буферами, стабилизаторами, консервантами, смазывающими веществами или другими материалами, известными специалистам в данной области, и, необязательно, другими терапевтическими или профилактическими средствами.
Для получения фармацевтической композиции согласно изобретению, эффективное количество соединения согласно настоящему изобретению, в качестве действующего вещества, объединяют с фармацевтически приемлемым носителем в виде однородной смеси, причем носитель может иметь различные формы в зависимости от формы препарата, требуемого для введения. Фармацевтические композиции могут находиться в любой форме, подходящей для перорального, парентерального, наружного, интраназального, офтальмологического, ушного, ректального, интравагинального или трансдермального введения. Указанные фармацевтические композиции предпочтительно находятся в стандартной дозированной лекарственной форме, подходящей, предпочтительно, для введения перорально, ректально, подкожно или посредством парентеральной инъекции. Например, при приготовлении композиций в лекарственной форме для перорального применения, может быть применена любая стандартная фармацевтическая среда, такая как, например, вода, гликоли, масла, спирты и тому подобное в случае пероральных жидких препаратов, таких как суспензии, сиропы, настойки и растворы; или твердые носители, такие как крахмалы, сахара, каолин, смазывающие вещества, связующие вещества, разрыхлители и тому подобное в случае порошков, пилюль, капсул и таблеток.
Благодаря легкости применения, таблетки и капсулы представляют собой наиболее предпочтительную пероральную стандартную лекарственную форму, при этом, безусловно, используются твердые фармацевтические носители. В случае парентеральных композиций носитель, как правило, будет содержать стерильную воду, по меньшей мере, в значительной степени, хотя могут быть включены другие ингредиенты, например для увеличения растворимости. Например, могут быть приготовлены растворы для инъекций, в которых носитель включает раствор хлорида натрия, раствор глюкозы или смесь раствора хлорида натрия и раствора глюкозы. Также могут быть приготовлены суспензии для инъекций, при этом могут быть использованы соответствующие жидкие носители, суспендирующие средства и тому подобное. В композициях, подходящих для подкожного введения, носитель необязательно представляет собой вещество, усиливающее проникновение, и/или подходящее смачивающее вещество, необязательно в комбинации с подходящими добавками любой природы в малых пропорциях, не оказывающими значительного повреждающего воздействия на кожу. Указанные добавки могут облегчать введение в кожу и/или могут применяться для приготовления требуемых композиций. Указанные композиции могут быть введены различными путями, например, в виде трансдермального пластыря, в виде капель, в виде мази. Они являются наиболее предпочтительными для приготовления указанных выше фармацевтических композиций в стандартной лекарственной форме благодаря легкости введения и однородности дозировки. Стандартная лекарственная форма, при использовании в настоящем описании и формуле изобретения, относится к физически дискретным единицам, подходящим в качестве единичных доз, при этом каждая единица содержит заданное количество действующего вещества, рассчитанное на достижение требуемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включающие таблетки с риской или таблетки с оболочкой), капсулы, пилюли, пакеты с порошком, облатки, растворы или суспензии для инъекций, чайные ложки, столовые ложки и тому подобное, а также их раздельное множество.
Наиболее предпочтительно приготавливать вышеуказанные фармацевтические композиции в стандартной лекарственной форме для легкости введения и однородности дозировки. Стандартная лекарственная форма, при использовании в описании и формуле изобретения, относится к физически дискретным единицам, подходящим в качестве единичных дозировок, при этом каждая единица содержит заданное количество действующего вещества, рассчитанное на достижение требуемого терапевтического эффекта, в сочетании с требуемым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включающие таблетки с риской или таблетки с оболочкой), капсулы, пилюли, пакеты с порошком, облатки, растворы или суспензии для инъекций, чайные ложки, столовые ложки и тому подобное, а также их раздельное множество.
Комбинацию или фармацевтическую композицию изобретения вводят в количестве, достаточном для проявления их противоопухолевой активности.
Специалисты в данной области смогут легко определить эффективное количество ингибитора FGFR и ингибитора IGF1R, как описано в настоящей заявке. Обычно предполагается, что терапевтически эффективное количество составляет от 0,005 мг/кг до 100 мг/кг массы тела и, в частности, от 0,005 мг/кг до 10 мг/кг массы тела. Может быть предпочтительным вводить требуемую дозу в виде одной, двух, трех, четырех или более субдоз с соответствующими интервалами в течение дня. Указанные субдозы могут быть приготовлены в виде стандартных лекарственных форм, например, содержащих 0,5-500 мг, в частности от 1 мг до 500 мг, более конкретно от 10 мг до 500 мг действующего вещества на стандартную лекарственную форму.
В зависимости от способа введения фармацевтическая композиция предпочтительно будет содержать от 0,05 до 99% по весу, более предпочтительно от 0,1 до 70% по весу, еще более предпочтительно от 0,1 до 50% по весу ингибитора FGFR, ингибитора IGF1R или комбинации ингибитора FGFR и ингибитора IGF1R, как описано в настоящей заявке, и от 1 до 99,95% по весу, более предпочтительно от 30 до 99,9% по весу, еще более предпочтительно от 50 до 99,9% по весу фармацевтически приемлемого носителя, где все проценты основаны на полном весе композиции.
Для лечения указанных выше патологических состояний комбинации или фармацевтические композиции изобретения могут предпочтительно применяться, как указано выше, в комбинации с одним или более другими лекарственными средствами, более конкретно с другими противоопухолевыми средствами или вспомогательными средствами в противоопухолевой терапии.
Настоящее изобретение, таким образом, также относится к фармацевтической композиции, включающей одно или более других лекарственных средств и комбинацию согласно настоящему изобретению вместе с фармацевтическим носителем.
Настоящее изобретение также относится к применению комбинации согласно изобретению в производстве фармацевтической композиции для ингибирования роста опухолевых клеток.
Настоящее изобретение также относится к продукту, содержащему, в качестве первого действующего вещества, ингибитор FGFR, в особенности ингибитор FFGR, как описано в настоящей заявке, более конкретно соединение A или его фармацевтически приемлемую соль или его сольват, или соединение B или его фармацевтически приемлемую соль или его сольват, в качестве второго действующего вещества - ингибитор IGF1R, в особенности ингибитор IGF1R, как определено в настоящем описании, и в качестве другого действующего вещества одно или более противоопухолевых средств, в качестве комбинированного препарата для одновременного, раздельного или последовательного применения в лечении пациентов, страдающих раком.
Одно или более других лекарственных средств и комбинация согласно настоящему изобретению могут применяться одновременно (например, в отдельных или единых композициях) или последовательно в любом порядке. В последнем случае три или более соединения будут применяться в течение периода и в количестве и таким способом, которые являются достаточными, чтобы гарантировать обеспечение предпочтительного или синергического эффекта. Следует понимать, что предпочтительный способ и порядок введения, а также соответствующие количества доз и схемы для каждого компонента комбинации будут зависеть от конкретного другого лекарственного средства и соединений комбинаций настоящего изобретения, которые вводят, от их пути введения, конкретной опухоли, которую подвергают лечению, и конкретного носителя, которого подвергают лечению. Оптимальный способ и порядок введения, а также количества доз и схема могут быть с легкостью определены специалистами в данной области при использовании стандартных методов и с учетом информации, представленной в настоящей заявке.
Весовое соотношение соединений в комбинациях согласно настоящему изобретению и одного или более других противоопухолевых средств, в случае их применения в комбинации, может быть определено специалистом в данной области. Указанное соотношение и точная доза, и частота введения зависят от конкретных соединений комбинаций согласно изобретению и другого используемого противоопухолевого средства (средств), конкретного состояния, которое подвергают лечению, тяжести состояния, которое подвергают лечению, возраста, веса, пола, питания, времени введения и общего физического состояния конкретного пациента, способа введения, а также другого лечения, которое может проходить индивид, как известно специалистам в данной области. Кроме того, очевидно, что эффективное ежедневное количество может быть уменьшено или увеличено в зависимости от ответа подвергаемого лечению субъекта и/или в зависимости от оценки врача, назначающего комбинации настоящего изобретения. Конкретное весовое соотношение для каждой пары ингибитора FGFR, ингибитора IGF1R и другого противоопухолевого средства может изменяться в пределах от 1/10 до 10/1, более конкретно от 1/5 до 5/1, еще более конкретно от 1/3 до 3/1.
Комплексное соединение платины предпочтительно вводят в дозировке, составляющей от 1 до 500 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 50 до 400 мг/м2, конкретно для цисплатина - в дозировке приблизительно 75 мг/м2, и для карбоплатина - приблизительно 300 мг/м2 на курс лечения.
Соединение таксана предпочтительно вводят в дозировке от 50 до 400 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 75 до 250 мг/м2, конкретно для паклитаксела - в дозировке приблизительно от 175 до 250 мг/м2, и для доцетаксела - приблизительно от 75 до 150 мг/м2 на курс лечения.
Соединение камптотецина предпочтительно вводят в дозировке от 0,1 до 400 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 1 до 300 мг/м2, конкретно для иринотекана - в дозировке приблизительно от 100 до 350 мг/м2, и для топотекана - приблизительно от 1 до 2 мг/м2 на курс лечения.
Противоопухолевое производное подофиллотоксина предпочтительно вводят в дозировке от 30 до 300 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 50 до 250 мг/м2, конкретно для этопозида - в дозировке приблизительно от 35 до 100 мг/м2, и для тенипозида - приблизительно от 50 до 250 мг/м2 на курс лечения.
Противоопухолевый алкалоид барвинка предпочтительно вводят в дозировке от 2 до 30 мг на квадратный метр (мг/м2) площади поверхности тела, конкретно для винбластина - в дозировке приблизительно от 3 до 12 мг/м2, для винкристина - в дозировке приблизительно от 1 до 2 мг/м2, и для винорелбина - в дозировке приблизительно от 10 до 30 мг/м2 на курс лечения.
Противоопухолевое нуклеозидное производное предпочтительно вводят в дозировке от 200 до 2500 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 700 до 500 мг/м2, конкретно для - 5-ФУ в дозировке от 200 до 500 мг/м2, для гемцитабина - в дозировке приблизительно от 800 до 1200 мг/м2, и для капецитабина - приблизительно от 1000 до 2500 мг/м2 на курс лечения.
Алкилирующие средства, такие как азотистый иприт или нитрозомочевину, предпочтительно вводят в дозировке от 100 до 500 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 120 до 200 мг/м2, конкретно для циклофосфамида - в дозировке приблизительно от 100 до 500 мг/м2, для хлорамбуцила - в дозировке приблизительно от 0,1 до 0,2 мг/м2, для кармустина - в дозировке приблизительно от 150 до 200 мг/м2, и для ломустина - в дозировке приблизительно от 100 до 150 мг/м2 на курс лечения.
Противоопухолевое антрациклиновое производное предпочтительно вводят в дозировке от 10 до 75 мг на квадратный метр (мг/м2) площади поверхности тела, например, от 15 до 60 мг/м2, конкретно для доксорубицина - в дозировке приблизительно от 40 до 75 мг/м2, для даунорубицина - в дозировке приблизительно от 25 до 45 мг/м2, и для идарубицина - в дозировке приблизительно от 10 до 15 мг/м2 на курс лечения.
Антиэстрогенное средство предпочтительно вводят в дозировке приблизительно от 1 до 100 мг ежедневно в зависимости от конкретного средства и состояния, подвергаемого лечению. Тамоксифен предпочтительно вводят перорально в дозировке от 5 до 50 мг, предпочтительно от 10 до 20 мг дважды в день, продолжая терапию в течение достаточного времени для достижения и сохранения терапевтического эффекта. Торемифен предпочтительно вводят перорально в дозировке приблизительно 60 мг один раз в день, продолжая терапию в течение достаточного времени для достижения и сохранения терапевтического эффекта. Анастрозол предпочтительно вводят перорально в дозировке приблизительно 1 мг один раз в день. Дролоксифен предпочтительно вводят перорально в дозировке приблизительно 20-100 мг один раз в день. Ралоксифен предпочтительно вводят перорально в дозировке приблизительно 60 мг один раз в день. Эксеместан предпочтительно вводят перорально в дозировке приблизительно 25 мг один раз в день.
Антитела предпочтительно вводят в дозировке приблизительно от 1 до 5 мг на квадратный метр (мг/м2) площади поверхности тела, или как известно в данной области, если есть различия. Трастузумаб предпочтительно вводят в дозировке от 1 до 5 мг на квадратный метр (мг/м2) площади поверхности тела, конкретно от 2 до 4 мг/м2 на курс лечения. Указанные дозировки могут быть введены, например, один раз, два раза или более на курс лечения, который может быть повторен, например, каждые 7, 14, 21 или 28 дней.
Соединения комбинаций или фармацевтических композиций настоящего изобретения могут обладать ценными диагностическими свойствами, благодаря которым они могут применяться для определения или идентификации образования комплекса между меченым соединением и другими молекулами, пептидами, белками, ферментами или рецепторами.
В способах определения или идентификации могут применяться соединения, меченные такими метками, как радиоактивные изотопы, ферменты, флуоресцентные вещества, люминесцентные вещества и т.д. Примеры радиоактивных изотопов включают 125I, 131I, 3H и 14C. Возможность детектирования ферментов обычно обеспечивают посредством конъюгирования соответствующего субстрата, который, в свою очередь, катализирует детектируемую реакцию. Соответствующие примеры включают, например, бета-галактозидазу, бета-глюкозидазу, щелочную фосфатазу, пероксидазу и малатдегидрогеназу, предпочтительно пероксидазу хрена. Люминесцентные вещества включают, например, люминол, производные люминола, люциферин, экворин и люциферазу.
Биологические образцы могут быть определены как ткань тела или физиологические жидкости. Примерами физиологических жидкостей являются спинномозговая жидкость, кровь, плазма, сыворотка, моча, мокрота, слюна и тому подобное.
Экспериментальная часть
При оценке описанных выше соединений A и B в качестве ингибиторов FGFR, при тестировании соединений в клеточном анализе пролиферации (анализ аламаровым синим, см. ниже), было обнаружено, что даже самые чувствительные линии раковых клеток (IC50<10 нМ) включали субпопуляцию клеток, которые не были чувствительны к соединениям. Например, это наблюдали по плато на кривой пролиферации приблизительно при ~10-20% ДМСО контроля (значение, наблюдаемое в анализе для ДМСО, взято за 100%, и значения, наблюдаемые для обработок дозами соединения, вычислены как % от 100% ДМСО). Например, при обработке клеток DMS114, линии клеток мелкоклеточного рака легкого с амплификацией FGFR1, в анализе пролиферации N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамином кривая показала плато при ~10-20% ДМСО контроля, что указывает на то, что ~10-20% клеток были нечувствительны к обработке соединением.
Нечувствительные клетки выделяли и профилировали с целью определить активные сигнальные пути, которые действуют в качестве факторов, способствующих их выживанию и/или пролиферации. Таким образом, клетки DMS114, линии клеток мелкоклеточного рака легкого с амплификацией FGFR1, сеяли в 10 см культуральные планшеты и помещали в инкубатор при 37°C, 5% CO2. Клетки выращивали в питательной среде (см. ниже), в случае исходных клеток с или без контроля ДМСО, или в питательной среде с добавкой высокой дозы соединения A (конечная концентрация соединения A в среде 1 мкМ, соединение A добавляли в виде образца, разбавленного из стокового раствора в ДМСО), в случае резистентных клеток, в течение длительного периода времени. В течение времени роста клеток, нечувствительных к соединению, среду с добавкой соединения A [1 мкМ] меняли два раза в неделю. В случае исходных клеток с или без контроля ДМСО, когда клетки достигали конфлюэнтности, близкой к 100%, их трипсинизировали и переносили обратно на чашку. В обработанных соединением чашках наблюдали рост резистентных клонов. Приблизительно через 2-3 недели после начальной обработки клетки собирали с чашки с помощью трипсинизирования и переносили на новую чашку для дальнейшего размножения. Резистентные клетки, такие же как исходные клетки, переносили два раза в неделю, но при этом в среду для резистентных клеток всегда добавляли соединение A [1 мкМ] (тест 1).
Питательная среда
RPMI-1640 (Gibco, 31870-025) 500 мл; 10% FCS (Hyclone, SV30160.03) 57 мл; 1 мМ пирувата натрия (Gibco, 11360) 5,7 мл; 2 мМ L-глутамина (Gibco, 25030) 5,7 мл; Гентамицин 50 мкг/мл (Gibco, 15750) 5,7 мл.
Резистентные клетки профилировали по генам, которые дифференцированно экспрессировали по сравнению с исходными клетками, с применением технологии микрочипов. Были выполнены два эксперимента на микрочипах. В первом эксперименте исходные и резистентные клетки профилировали с целью определения генов и путей, различных в этих двух популяциях, и исследования путей, которые способствуют развитию резистентности к соединению A. Во втором эксперименте на микрочипах профилировали изменения экспрессии генов с течением времени после обработки соединением A. С этой целью клетки DMS114 обрабатывали ДМСО или 1 мкМ соединения A или оставляли без обработки на 1 день, 1 неделю и 2 недели, 6 недель и 7 недель.
В обоих исследованиях на микрочипах обнаружили незначительное повышение экспрессии IGF1R в резистентных клетках.
В дополнение к этим экспериментам исходные и резистентные клетки профилировали на чипах фосфоРТК (рецепторная тирозинкиназа). Было обнаружено, что в резистентных клетках DMS114 только IGF1R сильно фосфорилирован по сравнению с исходными клетками DMS114, где не было обнаружено фосфорилирования IGF1R. Для оценки, играет ли IGF1R роль в выживании и пролиферации резистентных клеток DMS114, анализ пролиферации с аламаровым синим выполняли с исходными и резистентными клетками в присутствии ингибиторов IGF1R GSK1838705A и BMS-754807. Было обнаружено, что оба ингибитора IGF1R сильно ингибировали пролиферацию резистентных клеток DMS114, но не ингибировали пролиферацию исходных клеток, что дает возможность предположить, что клетки DMS114, резистентные к ингибитору FGFR, соединению A, имели активированный IGF1R и являлись зависимыми от сигнального пути IGF1R для своей пролиферации (см. Таблицу ниже).
Обнаружение активации сигнализации IGF1R в качестве фактора устойчивости к тестируемым ингибиторам FGFR в DMS114 говорит в пользу комбинированной терапии ингибиторами FGFR и IGF1R для преодоления развития резистентности к ингибитору FGFR в клетках DMS114.
Провели эксперимент, в котором эти два средства (ингибитор FGFR: 1 мкМ соединения A, и ингибитор IGF1R: 300 нМ BMS-754807; или ингибитор FGFR: 1 мкМ соединения A, и ингибитор IGF1R: 1 мкМ GSK1838705A) применяли в комбинации с начала. Также проводили обработку клеток отдельными средствами с или без ДМСО, или проводили обработку только ДМСО, служащим в качестве контроля растворителем. Пролиферацию клеток наблюдали при использовании системы IncuCyte, измеряя % конфлюэнтности клеток в динамике. В данном эксперименте, который проводили аналогичным способом, как описано выше для теста 1, наблюдали, что обработка ингибиторами IGF1R в отдельности, как и обработка ДМСО, не воздействовала на пролиферацию клеток DMS114. Обработка клеток ингибитором FGFR (1 мкМ соединения A) первоначально блокировала пролиферацию, но приблизительно через две-три недели наблюдали рост нечувствительных к соединению клеток, таким образом, клетки снова приобретали способность к пролиферации, что соответствует указанному выше обнаружению, что приблизительно через две-три недели непрерывного ингибирования пути FGFR соединением A нечувствительная резистентная субпопуляция клеток в клетках DMS114 приобретала способность к росту. Важно, что комбинированная обработка ингибитором FGFR (1 мкМ соединения A) и ингибитором IGF1R (BMS-754807 или GSK1838705A) полностью предотвращала появление резистентности. См. Фигуру 1 и 2.
Проводили дополнительный эксперимент, в котором резистентные клетки DMS114 подвергали обработке 1 мкМ GSK1838705A, и рост/пролиферацию клеток наблюдали с помощью системы IncuCyte. Клетки выдерживали в таких условиях более 33 дней, при этом среду заменяли два раза в неделю. Было обнаружено, что пролиферация резистентных клеток, поддерживаемых в присутствии соединения A, при обработке ингибитором IGF1R была полностью блокирована, и при длительной обработке (>30 дней) клетки не приобретали способность к росту. См. Фигуру 3.
В результате было обнаружено, что ингибитор FGFR, соединение A, ингибирует пролиферацию клеток DMS114 (IC50 8,54E-09 M). Однако присутствует первичная резистентность, которая приводит к росту нечувствительных к соединению клеток приблизительно через две-три недели после начального и непрерывного воздействия ингибитора FGFR. Активацию IGF1R идентифицировали как механизм резистентности к ингибированию FGFR в клетках DMS114. Было установлено, что предварительная обработка ингибитором FGFR и ингибитором IGF1R является мощным и эффективным подходом к блокированию развития первичной резистентности.
АНАЛИЗ С АЛАМАРОВЫМ СИНИМ
Клетки сеяли в 180 мкл среды при оптимизированной плотности клеток в черные 96-луночные планшеты с прозрачным плоским дном. Внешние лунки заполняли 180 мкл среды. Клетки инкубировали в течение 24 часов при 37°C и 5% CO2.
На следующий день разведения соединения приготавливали в 96-луночном круглодонном планшете (Corning #3365). 50× разведение соединения приготавливали в среде, 4 мкл стокового раствора соединения в 196 мкл среды в 96-луночном планшете (Corning #3585). Планшеты с соединениями/средой помещали в шейкер на 10 минут, а затем 20 мкл соединения в среде добавляли к клеткам (10× разведение). Клетки инкубировали при 37°C и 5% CO2 в течение 4 дней перед считыванием аламарового синего (Alamar Blue®).
Приготовление аламарового синего:
Материалы:
Таблетки резазурина (100 таблеток) (PROLABO)
Ферроцианид калия (Sigma)
Феррицианид калия (Sigma)
KH2PO4 (Sigma)
K2HPO4 (Sigma)
Калий-фосфатный буфер (PPB) 1 литр
20 мМ KH2PO4 2,72 г
80 мМ K2HPO4 13,86 г
pH 7,4 (несколько капель 5M KOH)
Добавить MilliQ до 500 мл
Довести раствор до pH 7,4 и довести конечный объем до 1 литра.
Реактив PPB-A
1 таблетка резазурина на мл PPB (1 таблетка+800 мкл PPB)
Реактив PPB-B 30 мМ феррицианида калия в PPB
0,987 г феррицианида калия+100 мл PPB
Стерилизовать фильтрованием через 0,22 мкм фильтр и хранить при 4°C
Реактив PPB-C 30 мМ ферроцианида калия в PPB
1,266 г феррицианида калия+100 мл PPB
Стерилизовать фильтрованием через 0,22 мкм фильтр и хранить при 4°C
Готовая к применению смесь аламарового синего
1 мл альтернативного PPB-A+1 мл PPB-B+1 мл PPB-C
Добавить 57 мл PPB
Стерилизовать фильтрованием через 0,22 мкм фильтр и хранить при 4°C
Через 4 дня инкубирования с соединением: Добавить 40 мкл готовой к применению смеси аламарового синего в каждую лунку. Инкубировать планшеты при 37°C и 5% CO2. Сканировать планшеты через 4 или 6 часов инкубирования (зависит от линии клеток). Встряхнуть планшеты и измерить RFU при возб.: 544 нм и эм.: 590 нм
Анализ с аламаровым синим включает флуориметрический/колориметрический индикатор роста, основанный на обнаружении метаболической активности. В частности, система включает окислительно-восстановительный (редокс) индикатор, который флуоресцирует и изменяет цвет в ответ на химическое восстановление питательной среды, происходящее вследствие роста клеток.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНАЦИИ | 2015 |
|
RU2715236C2 |
| НОВЫЕ СОЕДИНЕНИЯ | 2016 |
|
RU2747645C2 |
| СПОСОБ ТЕРАПИИ И ПРОФИЛАКТИКИ ОПУХОЛИ, ПОДДАЮЩЕЙСЯ ЛЕЧЕНИЮ ЭНДОКРИННОЙ ТЕРАПИЕЙ, С ПОМОЩЬЮ КОМБИНИРОВАННОГО ПРИМЕНЕНИЯ ИНГИБИТОРА РЕЦЕПТОРА ФАКТОРА РОСТА ФИБРОБЛАСТОВ И ЭНДОКРИННОЙ ТЕРАПИИ | 2019 |
|
RU2825636C2 |
| БИГЕТЕРОАРИЛ-ЗАМЕЩЕННЫЕ 1,4-БЕНЗОДИАЗЕПИНЫ И ПУТИ ИХ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2016 |
|
RU2747644C2 |
| ПТЕРИДИНЫ В КАЧЕСТВЕ FGFR ИНГИБИТОРОВ | 2013 |
|
RU2702906C2 |
| СОЕДИНЕНИЯ ТИЕНОПИРИДИНОНА | 2019 |
|
RU2827549C2 |
| ЗАМЕЩЕННЫЕ БЕНЗОПИРАЗИНОВЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ FGFR-КИНАЗ ДЛЯ ЛЕЧЕНИЯ РАКОВЫХ ЗАБОЛЕВАНИЙ | 2011 |
|
RU2602233C2 |
| ПРОИЗВОДНЫЕ БИЦИКЛИЧЕСКИХ АМИНОВ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗЫ | 2007 |
|
RU2465275C2 |
| ИНДАЗОЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ FGFR, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2015 |
|
RU2719428C2 |
| ЭКСПРЕССИЯ FGFR И ЧУВСТВИТЕЛЬНОСТЬ К ИНГИБИТОРУ FGFR | 2016 |
|
RU2728674C2 |
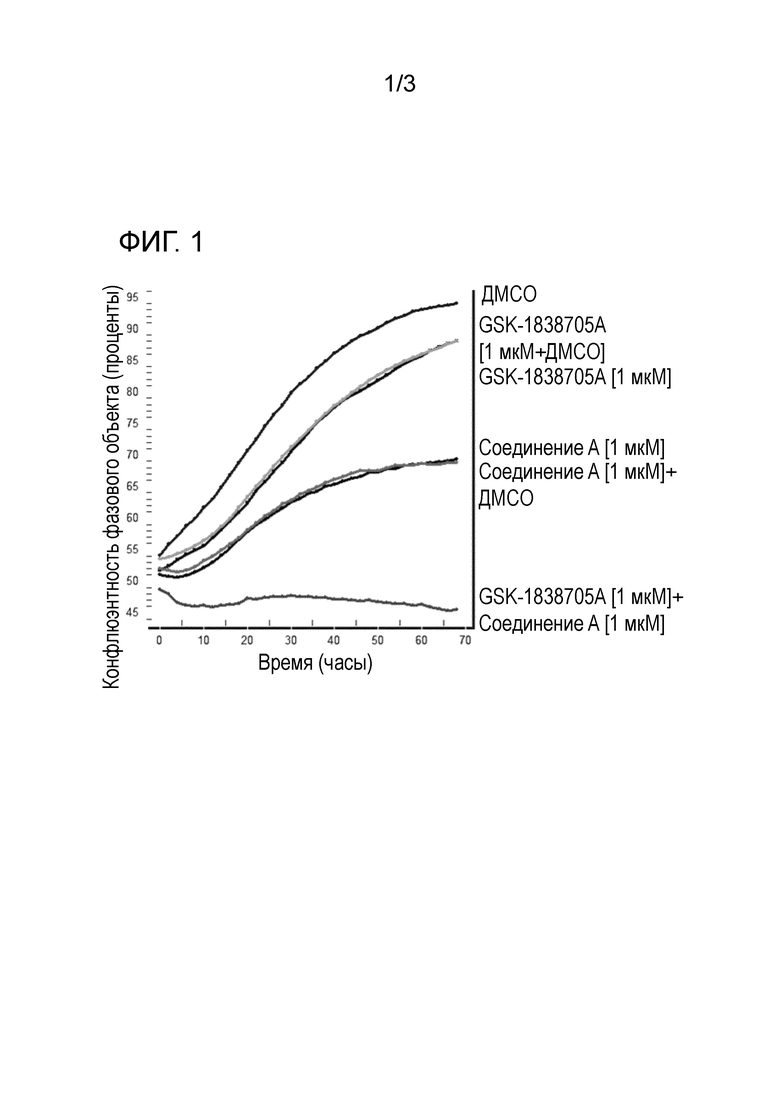
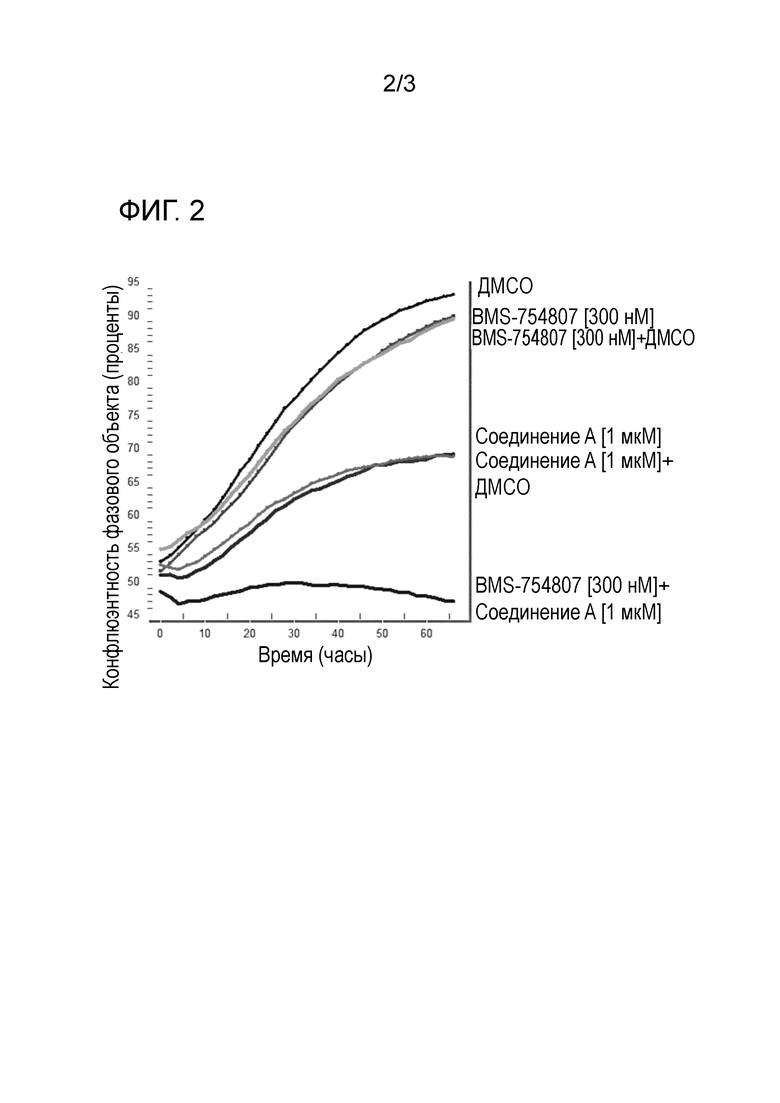
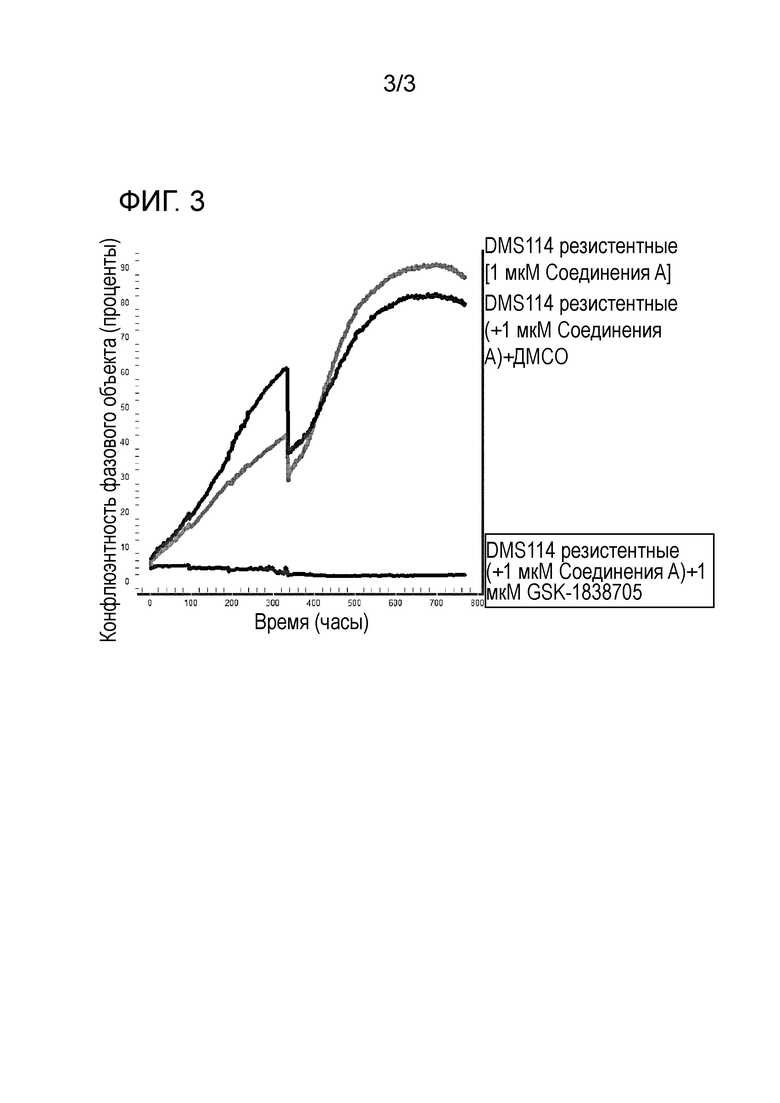
Группа изобретений относится к фармации и онкологии. Предложены: комбинация ингибитора FGFR, выбранного из N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина или его соли, сольвата и N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина или его соли, сольвата и ингибитора IGF1R для профилактики или лечения рака, композиция того же назначения, включающая указанную комбинацию, их применение для производства лекарственного средства для профилактики или лечения рака (варианты), способ лечения с их использованием (варианты) и комбинированный препарат того же назначения. Технический результат: комбинация указанных ингибиторов FGFR с ингибитором IGF1R (согласно примерам – GSK1838705A, BMS-754807) блокирует развитие первичной резистентности к лечению опухолевых клеток мелкоклеточного рака лёгкого. 7 н. и 17 з.п. ф-лы, 3 ил., 1 табл.
1. Комбинация ингибитора FGFR, выбранного из N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамина или его фармацевтически приемлемой соли или его сольвата и N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амина или его фармацевтически приемлемой соли или его сольвата, и ингибитора IGF1R, для профилактики или лечения рака.
2. Комбинация по п. 1, где ингибитор FGFR является N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамином или его фармацевтически приемлемой солью или его сольватом.
3. Комбинация по п. 2, где ингибитор FGFR является N-(3,5-диметоксифенил)-N'-(1-метилэтил)-N-[3-(1-метил-1H-пиразол-4-ил)хиноксалин-6-ил]этан-1,2-диамином в форме свободного основания.
4. Комбинация по п. 1, где ингибитор FGFR является N-(2-фтор-3,5-диметоксифенил)-N-(1H-имидазол-2-илметил)-3-(1-метил-1H-пиразол-4-ил)пиридо[2,3-b]пиразин-6-амином или его фармацевтически приемлемой солью или его сольватом.
5. Комбинация по любому из пп. 1-4, где ингибитор IGF1R выбран из GSK1838705A и BMS-754807.
6. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и комбинацию по любому из пп. 1-5 для профилактики или лечения рака.
7. Применение комбинации по любому из пп. 1-5 для производства лекарственного средства для профилактики или лечения рака.
8. Применение фармацевтической композиции по п. 6 для производства лекарственного средства для профилактики или лечения рака.
9. Применение по п. 7 или 8 для лечения рака легкого, мочевого пузыря, молочной железы, желудка или гепатоцеллюлярного рака.
10. Комбинация по любому из пп. 1-5, где
(i) рак представляет собой рак мочевого пузыря;
(ii) рак представляет собой рак мочевого пузыря с хромосомной транслокацией FGFR3; или
(iii) рак представляет собой рак мочевого пузыря с точечной мутацией FGFR3.
11. Комбинация по любому из пп. 1-5, где
(i) рак представляет собой опухоль с мутацией FGFR1, FGFR2, FGFR3 или FGFR4, или
(ii) рак представляет собой опухоль с мутантом FGFR2 или FGFR3 с приобретением функции; или
(iii) рак представляет собой опухоль со сверхэкспрессией FGFR1.
12. Комбинация по любому из пп. 1-5, где рак представляет собой рак мочевого пузыря, уротелиальный рак, метастатический уротелиальный рак, хирургически неоперабельный уротелиальный рак, рак молочной железы, глиобластому, рак легкого, немелкоклеточный рак легкого, плоскоклеточный рак легкого, аденокарциному легкого, легочную аденокарциному, мелкоклеточный рак легкого, рак яичника, рак эндометрия, рак шейки матки, саркому мягких тканей, плоскоклеточный рак головы и шеи, рак желудка, рак пищевода, плоскоклеточный рак пищевода, аденокарциному пищевода, холангиокарциному или гепатоцеллюлярный рак.
13. Комбинация по п. 12, где рак представляет собой уротелиальный рак, метастатический уротелиальный рак или хирургически неоперабельный уротелиальный рак.
14. Фармацевтическая композиция по п. 6, где
(i) рак представляет собой рак мочевого пузыря;
(ii) рак представляет собой рак мочевого пузыря с хромосомной транслокацией FGFR3; или
(iii) рак представляет собой рак мочевого пузыря с точечной мутацией FGFR3.
15. Фармацевтическая композиция по п. 6, где
(i) рак представляет собой опухоль с мутацией FGFR1, FGFR2, FGFR3 или FGFR4, или
(ii) рак представляет собой опухоль с мутантом FGFR2 или FGFR3 с приобретением функции; или
(iii) рак представляет собой опухоль со сверхэкспрессией FGFR1.
16. Фармацевтическая композиция по п. 6, где рак представляет собой рак мочевого пузыря, уротелиальный рак, метастатический уротелиальный рак, хирургически неоперабельный уротелиальный рак, рак молочной железы, глиобластому, рак легкого, немелкоклеточный рак легкого, плоскоклеточный рак легкого, аденокарциному легкого, легочную аденокарциному, мелкоклеточный рак легкого, рак яичника, рак эндометрия, рак шейки матки, саркому мягких тканей, плоскоклеточный рак головы и шеи, рак желудка, рак пищевода, плоскоклеточный рак пищевода, аденокарциному пищевода, холангиокарциному или гепатоцеллюлярный рак.
17. Фармацевтическая композиция по п. 16, где рак представляет собой уротелиальный рак, метастатический уротелиальный рак или хирургически неоперабельный уротелиальный рак.
18. Способ профилактики или лечения рака, включающий введение субъекту, нуждающемуся в этом, комбинации по любому из пп. 1-5.
19. Способ профилактики или лечения рака, включающий введение субъекту, нуждающемуся в этом, фармацевтической композиции по п. 6.
20. Способ по п. 18 или 19 для лечения рака легкого, мочевого пузыря, молочной железы, желудка или гепатоцеллюлярного рака.
21. Комбинированный препарат для лечения пациента, страдающего от рака, содержащий комбинацию по любому из пп. 1-5, для одновременного, раздельного или последовательного применения в лечении рака.
22. Комбинация по любому из пп. 1-5 для лечения рака.
23. Фармацевтическая композиция по п. 6 для лечения рака.
24. Применение комбинации по п. 7 для лечения рака.
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| SABBATINI P | |||
| et al | |||
| Установка для взаимодействия с потоком | 1989 |
|
SU1838705A3 |
| Mol.Cancer Ther | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
Авторы
Даты
2020-03-04—Публикация
2015-03-26—Подача