Изобретение относится к области [1,3]тиазолоазиниевых систем, обладающих биологической активностью и способных найти применение в медицинской практике.
Значительное число лекарственных препаратов содержат в своей структуре всевозможные гетероциклические фрагменты, при этом первенствующее положение занимают гетероциклы, содержащие в своей структуре атом азота, которые обладают широким спектром биологической активности. Как известно, проблема поиска новых антибактериальных препаратов, несмотря на большое число уже синтезированных веществ, до сих пор являются одной из важнейших задач медицины. При лечении бактериальных инфекций сложность подбора лекарственных препаратов обусловлена антибиотикорезистентностью, которая связана с появлением новых бактерий, устойчивых к применяющимся средствам, в том числе видов с множественной лекарственной устойчивостью. В связи с этим существенную роль играет поиск хорошо растворимых и малотоксичных соединений, которые могли бы применяться парентерально. Известны антибактериальные лекарственные средства, являющиеся представителями следующих классов органических соединений: производные β-лактамов (пенициллины, цефалоспорины, цефамицины), аминосахара (канамицин, гентамицин, неомицин, стрептомицин), поликетиды (тетрациклин, окситетрациклин, хлортетрациклин) и т.д [1].
В последние десятилетия отмечается существенное увеличение грибковых заболеваний, что, в частности, обусловлено с повсеместным применением в лечебной практике антибактериальных препаратов широкого спектра действия и других групп лекарственных средств. Ввиду этой тенденции к росту грибковых заболеваний (в том числе ассоциированных с ВИЧ-инфекцией), развитием резистентности возбудителей к имеющимся препаратам, растет спрос на эффективные антимикотические препараты. Несмотря на уменьшение токсичности последних поколений противогрибковых средств, остается открытым вопрос снижения количества побочных эффектов.
Производные пиридинкарбоновых кислот, в частности витамина В3 (РР) - 3-пиридинкарбоновая (никотиновая) кислота - участвуют во многих окислительно-восстановительных реакциях, в образовании ферментов и обмене липидов и углеводов в живых клетках [2]. Производные [1,3]тиазоло[3,2-а]пиридиния проявляют анальгезирующую, противовоспалительную, гипогликемическую [3], антиоксидантную активность и цитотоксичность для клеток карциномы НСТ-116 [4] и применяются в качестве хелатообразующих лигандов, обладающих фармакологической активностью [5].
Известно, что пурин-6-тион (пурин-6-тиол, 6-меркаптопурин) и его конденсированные производные проявляют противоопухолевую активность [6-8]. Было обнаружено, что [1,3]тиазоло[2,3-i]пурины являются ингибиторами ксантиноксидазы [9].
Однако в литературе отсутствует информация об изучении антимикотической и антибактериальной активности производных [1,3]тиазоло[3,2-а]пиридинов и [1,3]тиазоло[2,3-i]пуринов.
В настоящее время в медицинской практике широко используется противогрибковый препарат клотримазол (1-[(2-хлорфенил)дифенилметил]-1H-имидазол), который в зависимости от концентрации проявляет фунгицидный или фунгистатический эффект. Препарат оказывает антимикотическое действие в концентрации 10-20 мг/л, проявляет антибактериальные свойства в отношении грамположительных кокков [10].
В качестве побочных эффектов при применении клотримазола возможны различные аллергические реакции.
Никаких данных об одновременной антибактериальной и противогрибковой активности производных конденсированных [1,3]тиазолов не найдено. В патенте РФ (RU 2674581) имеются данные о способе получения тиазоло- и оксазолосодержащих пептидов и их антибактериальной активности в отношении грамотрицательных бактерий - способности ингибировать бактериальную рибосому Escherichia Coli, Klebsiella Pneumoniae и Yersinia Pseudotuberculosis. Какие-либо указания на возможность наличия антимикотической активности этих соединений в патенте отсутствуют.
Задачей изобретения является синтез новых соединений, обладающих высокой фунгицидной активностью в отношении культур Candida Albicans и Aspergillus Niger, в сочетании с антибактериальным действием на грамположительные микроорганизмы, т.е. активностью в отношении такого вида патогенной микрофлоры, как Staphylococcus Aureus.
Решение этой задачи позволит значительно увеличить возможность воздействия на бактериальную флору и расширить ассортимент веществ с противогрибковой активностью.
Заявляется четыре варианта конденсированных [1,3]тиазолоазиниевых систем с узловым атомом азота.
Вариант I. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота:
иодид 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния формулы:
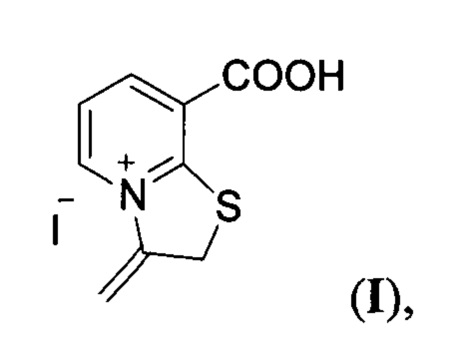
обладающий фунгицидной (Candida Albicans, Aspergillus Niger) и бактерицидной (Staphylococcus Aureus) активностью.
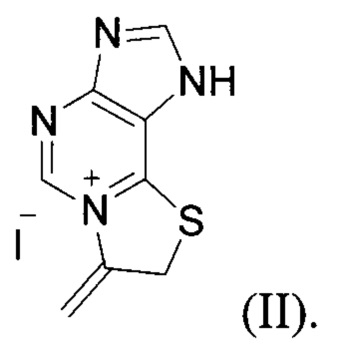
Вариант II. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота: иодид 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния формулы:
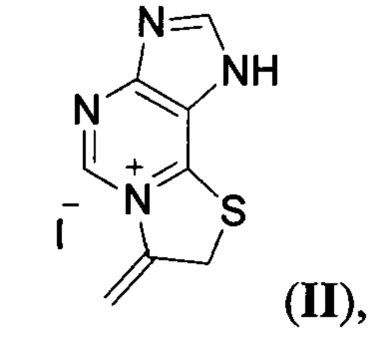
обладающий фунгицидной (Candida Albicans) и бактерицидной (Staphylococcus Aureus) активностью.
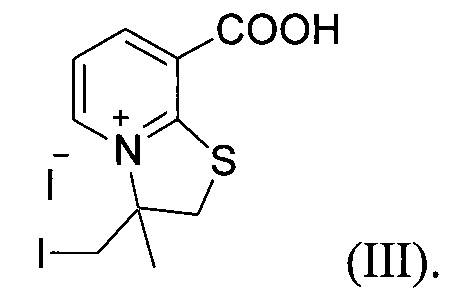
Вариант III. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота: иодид 3-иодметил-8-карбокси-3-метил-2,3-Дигидро[1,3]тиазоло[3,2-а]пиридиния формулы:
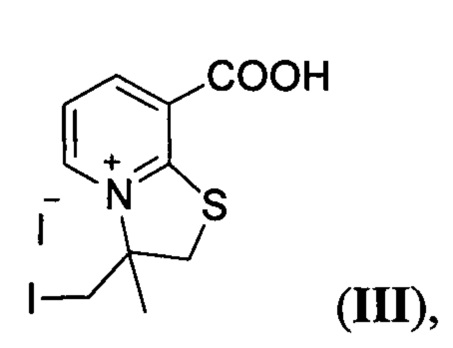
обладающий фунгицидной (Candida Albicans, Aspergillus Niger) и бактерицидной (Staphylococcus Aureus) активностью.
Вариант IV. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота: иодид 7-иодметил-7-метил-7,8-дигидротиазоло[2,3-i]пуриния формулы:
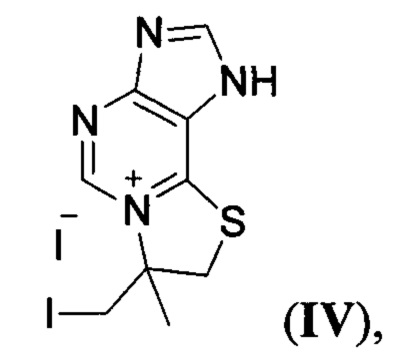
обладающий фунгицидной (Candida Albicans, Aspergillus Niger) и бактерицидной (Staphylococcus Aureus) активностью.
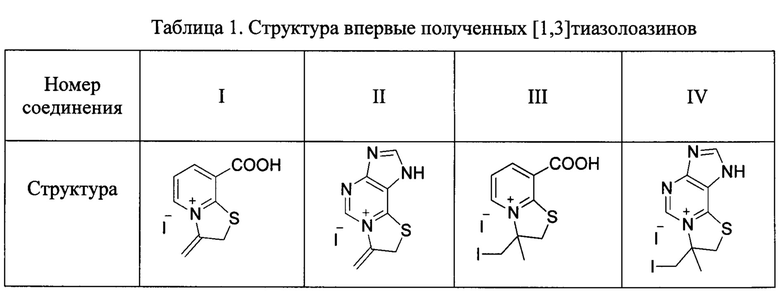
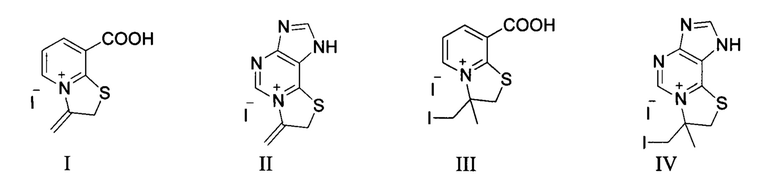
Задача решается на основе синтеза иодидов 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния (I), 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния (И), 3-иодметил-8-карбокси-3-метил-2,3-Дигидро[1,3]тиазоло[3,2-а]пиридиния (III) и 7-иодметил-7-метил-7,8-дигидротиазоло[2,3-i]пуриния (IV) (таблица 1), не описанных ранее в литературе новых соединений, проявляющих эффективную фунгицидную активность в отношении культур Candida Albicans и Aspergillus Niger и одновременно антибактериальные свойства в отношении Staphyllococcus Aureus.
На первой стадии биологическая активность новых тиазолоазинов I-IV была предсказана с помощью онлайн-сервиса PASS [11] и был обнаружен широкий спектр возможных фармакологических действий. Предсказание основано на теории появления биологической активности при наличии в молекуле определенной комбинации фармакофорных групп или фрагментов. Нами была замечена связь между появлением в молекуле метилиденового фрагмента и увеличением антибактериальных свойств синтезированных производных пиридина (соединение I). При этом в случае пуриновых производных увеличение активности наблюдалось в случае наличия иодметильного фрагмента (соединение IV).
Соединения (I-IV) получают взаимодействием (2-бромпроп-2-енилсульфанил)азинов или (2-метилпроп-2-енилсульфанил)азинов с иодом в хлороформе и последующем выделением в виде моноиодида путем взаимодействия с иодидом натрия в ацетоне. Соединения (I-IV) выпадают из раствора в виде порошка от белого до светло-желтого цветов.
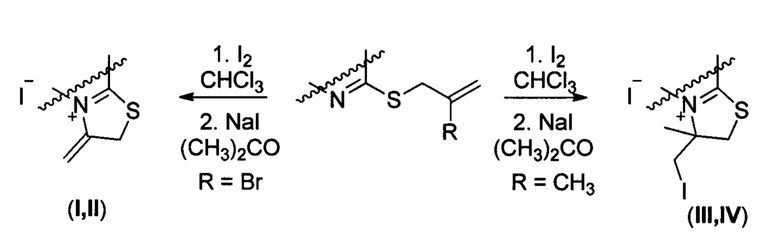
Очистку соединений (I-IV) осуществляют с использованием известного приема -перекристаллизации из подходящего растворителя.
Пример 1. Растворяют 508 мг (2 ммоль) иода в 10 мл растворителя (хлороформа, уксусной кислоты, дихлорметана, изопропилового спирта), добавляют раствор 1 ммоль (2-бромпроп-2-енилсульфанил)азина или (2-метилпроп-2-енилсульфанил)азина в 5 мл растворителя. Через сутки выпадает осадок в виде темно-фиолетовых кристаллов. Осадок фильтруют, промывают 6 мл Et2O, растворяют в 3 мл ацетона, добавляют 2 ммоль Nal. Через 1 сутки выпадает желтый осадок, который фильтруют, промывают 3 мл ацетона.
Анализ спектральных данных ИК и ЯМР 1Н подтверждает структуру иодидов I-IV. Состав соединений I-IV подтвержден элементным анализом.
I: иодид 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-a]пиридиния

II: иодид 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния

III: иодид 3-иодметил-8-карбокси-3-метил-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния

IV: иодид 7-иодметил-7-метил-7,8-дигидротиазоло[2,3-i]пуриния

Пример 2. Определение антимикробной (Staphylococcus Aureus) и противогрибковой (Candida Albicans, Aspergillus Niger) активности.
Для исследования противогрибкового и антибактериального действия веществ использовали культуры Staphyllococcus Aureus, Candida Albicans и Aspergillus Niger. Контролем служили известные противогрибковые и антибактериальные средства - клотримазол и цефазолин, также обладающие противогрибковыми и антибактерильными эффектами. После автоклавирования среды для культивирования микроорганизмов подсушивали 15 мин при температуре 37-40°С в термостате. После на питательные среды наносили сплошной слой исследуемых культур. На отдельные сектора со сплошным слоем культуры наносили исследуемые вещества. Контролем служили клотримазол и цефазолин. Процент подавления площади сектора каждой из культур микроорганизмов и грибов представлен в таблице 2.

Высоким антибактериальным и противогрибковым эффектом обладало соединение I. Во всех случаях было получено 100% подавление роста культур. В несколько меньшей степени антибактериальный и противогрибковый эффект проявлялся у соли III. Иодид IV отличался в большей степени антибактериальным эффектом.
Также у исследуемых веществ было выявлено подавление биопленкообразования. Выделенную чистую культуру засевали на поверхность агара сплошным газоном [12-14]. Затем стерильным пинцетом накладывали на агар бумажные диски пропитанные раствором каждого вещества. Чашки ставили в термостат при температуре 37°С. Отсутствие зоны роста микробов определялось вокруг пропитанных соответствующим веществом дисков. Эксперименты повторялись в 5-кратной повторности (таблица 3).

Полученные нами вещества (I, III) проявили более интенсивное действие в отношения подавления биопленкообразования, чем используемые в практической медицине клотримазол и цефазолин. Преимуществом полученных нами веществ является более высокая степень подавления биопленкообразования по сравнению с другими использующимися на практике аналогами.
Таким образом, впервые синтезированы иодиды 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния (I), 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния (II), 3-иодметил-8-карбокси-3-метил-2,3-дигидро[1,3]тиазоло[3,2-a]пиридиния (III) и 7-иодметил-7-метил-7,8-дигидротиазоло[2,3-i]пуриния (IV), обладающие фунгицидной активностью в отношении культур Candida Albicans и Aspergillus Niger. Их одновременное, наряду с фунгицидным, антибактериальное действие в отношении такого вида патогенной микрофлоры, как Staphyllococcus Aureus, является оригинальным сочетанием биологических свойств вещества и позволяет расширить ассортимент используемых в медицинской практике противогрибковых и антибактериальных препаратов на качественно новом уровне.
Таким образом, полученные иодиды 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния (I) общей формулы C9H8INO2S, 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния (II) общей формулы C8H7IN4S, 3-иодметил-8-карбокси-3-метил-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния (III) общей формулы C10H11I2NO2S и 7-иодметил-7-метил-7,8-дигидротиазоло[2,3-i]пуриния (IV) общей формулы C9H10I2N4S, обладают фунгицидным действием в отношении культур Candida Albicans и Aspergillus Niger в сочетании с антибактериальными свойствами в отношении Staphyllococcus Aureus.
Литература
1. Лоуренс Д.Р., Бенитт П.Н. Клиническая фармакология. - М.: Медицина, 1991. -.Т. 1. - С. 364.
2. Покровский В.И. Малая медицинская энциклопедия. Ред.; Сов. энциклопедия: Москва, 1991, т. 1, с. 330.
3. Litvinov V.P.; Sharanin Y.A.; Apenova Е.; Shestopalov А.М.; Mortikov V. Yu.; Nesterov V.N.; Shklover V.E.; Strachkov Yu. T. Chem. Heterocycl. Compd. 1987, 23, 574. [Химия гетероцикл. соединений 1987, 690.]
4. Shi F., Li C, Xia M., Miao K., Zhao Y., Tu S., Zheng W., Zhang G., Ma N. Bioorg. Med. Chem. Lett., 2009,19 (19), 5565. doi: 10.1016/j.bmcl.2009.08.046.
5. Poola В.; Choung W.; Nantz M. H. Tetrahedron, 2008, 64, 10798.
6. Hassan A.Y., Sarg M.T., Bayoumi A.H., Kalaf F.G.A. J. Heterocycl. Chem. 2017, 54, 3458. doi.org/10.1002/jhet.2969
7. Hassan A.Y. Asian J. Chem. 2010, 22, 689.
8. Ashour F.A., Rida S.M., El-Hawash S.A.M., ElSemary M. M., Badr M.H. Med Chem. Res., 2012, 21(7), 1107. doi.org/10.1007/s00044-011-9612-6
9. Biagi, G.; Costantini, A.; Costantino, L.; Giorgi, I.; Livi, O.; Pecorari, P.; Rinaldi, M.; Scartoni, V.J. Med. Chem. 1996, 39, 2529.
10. Справочник ВИДАЛЬ. Лекарственные препараты в России. - М.: АстраФармСервис, 1995. - 1170 с.
11. http://www.pharmaexpert.ru/passonline/index.php
12. Кузнецов СИ., Дубинина Г.А. Методы изучения водных микроорганизмов. - М.: Наука, 1989. - 285 с.
13. Кашкин П.Н., Блинков К.П. Безбородое A.M., Цыганов В.А., Антибиотики. Л. Медицина. - Ленинградское отделение, 1970. - 375 с.
14. Гэйл Э., Кандлифф Э., Рейнолдс П., Ричмонд М., Уоринг М. Молекулярные основы действия антибиотиков. - М. Мир, 1975. - 501 с.
Изобретение относится к конденсированным [1,3]тиазолоазиниевым системам: иодиду 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния, иодиду 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния и иодиду 3-иодметил-8-карбокси-3-метил-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния. Технический результат – производные конденсированных [1,3]тиазолоазиниевых систем, обладающие фунгицидной (Candida Albicans, Aspergillus Niger) и бактерицидной активностью (Staphyllococcus Aureus). 3 н.п. ф-лы, 3 табл., 2 пр.
1. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота: иодид 8-карбокси-3-метилидено-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния формулы
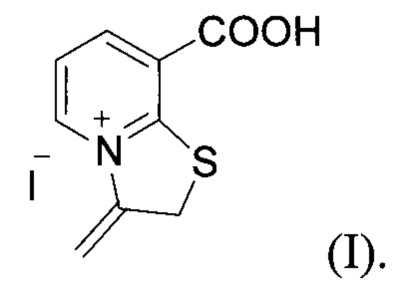
2. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота: иодид 7-метилидено-7,8-дигидро[1,3]тиазоло[2,3-i]пуриния формулы
3. Конденсированные [1,3]тиазолоазиниевые системы с узловым атомом азота: иодид 3-иодметил-8-карбокси-3-метил-2,3-дигидро[1,3]тиазоло[3,2-а]пиридиния формулы
| OSHEKO K | |||
| YU | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| КИМ Д.Г | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| KIM D.G | |||
| et al | |||
| "Synthesis of | |||
Авторы
Даты
2020-03-27—Публикация
2019-09-09—Подача