Изобретение относится к области синтеза биологически активных аналогов природных соединений, а именно к получению (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметилгонан-17-илиден]-6-метилгепт-5-еновой кислоты (1), обладающей антибактериальной активностью по отношению к Staphylococcus aureus (MRSA) и ингибирующей рост грибковой культуры Cryptococcus neoformans:

Известны примеры получения производных фузидовой кислоты, содержащих разветвленный полиаминовый фрагмент в молекуле, посредством реакции восстановительного аминирования с использованием NaBH(ОАс)3 в качестве восстанавливающего агента. Метод заключается во взаимодействии 1 экв. 3-кетофузидовой кислоты (2) с 3 экв. полиамина линейной или разветвленной структуры и 3 экв. NaBH(OAc)3 в растворе метанола. Реакция протекает при комнатной температуре в присутствии уксусной кислоты в течение 6-16 часов и приводит к образованию смеси α- и β-изомерных аминов (3-8) с выходом от 70 до 85%:
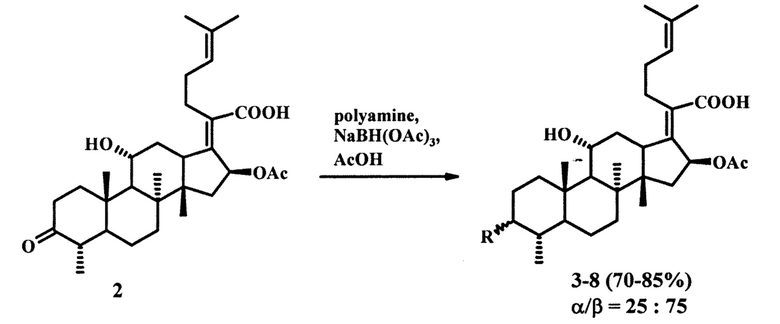
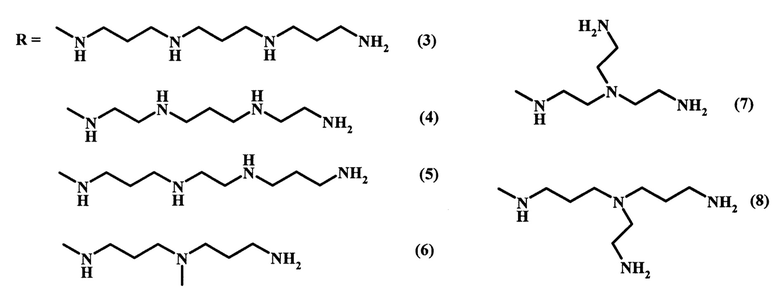
Была изучена биологическая активность полученных производных в отношении грамм-положительных и грамм-отрицательных бактерий (Staphylococci, Streptococci, Corynebacteriae, Mycobacteriae, Proteus, Propionibacterium, Pseudomonas, Neisseriae, E. coli), а также грибковых штаммов (Candida, Aspergillus) и установлено, что они не обладают антимикробным и фунгицидным действием по отношению к штаммам возбудителей бактериальных и грибковых инфекций человека и животных ([1] Т. Duvold. Blanched polyamine steroid derivatives. Patent WO 03/087121 A1, 2003; [2] T. Duvold. Novel fusidic acid derivatives. Patent WO 02/077007 A2, 2002).
Известны примеры синтеза производных фузидовой кислоты, содержащих N-(3-аминопропил)бутан-1,4-диаминовый заместитель в молекуле. Метод заключается во взаимодействии производных N-сукцинимидного эфира тетрагидрофузидовой кислоты (9) с 3 экв. N-(3-аминопропил)бутан-1,4-диамина (спермидина) в сухом хлороформе. Реакция протекает при комнатной температуре в течение 16 часов и приводит к образованию амидов (10-15) с выходами от 60 до 90%:
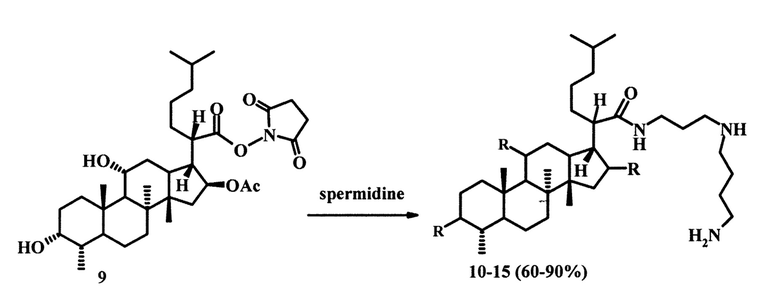
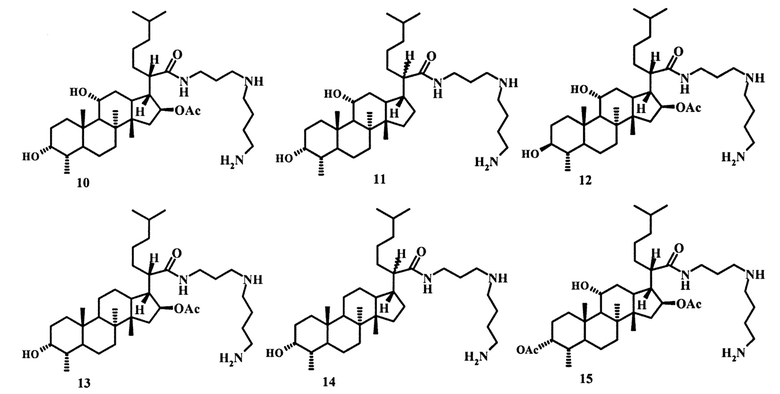
Изучение биологической активности полученных производных показало, что соединения (10) и (14) проявляют антибактериальное действие в отношении штаммов Staphylococcus aureus, Escherichia coli и Pseudomonas aeruginosa, a также ингибируют рост грибковых культур Candida albicans и Aspergillus niger [Т. Duvold. Novel fusidic acid derivatives. Patent WO 02/077007 A2, 2002].
Таким образом, синтез и биологические свойства 3β-N-(3-аминопропил)бутан-1,4-диаминового производного фузидовой кислоты (1) в литературе не описаны.
Задачей предлагаемого изобретения является разработка способа получения нового соединения - ((2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметилгонан-17-илиден]-6-метилгепт-5-еновой кислоты, обладающего антимикробной и противогрибковой активностью.
Синтез заявленного соединения (1) осуществляли следующим образом: 3,11-диоксопроизводное фузидовой кислоты (16) вовлекали во взаимодействие с 3 экв. N-(3-аминопропил)бутан-1,4-диамина (спермидина) и 0.3 экв. изопропоксида титана (IV) в среде сухого метанола, с последующей обработкой реакционной массы 2 экв. борогидрида натрия. После выделения и хроматографической очистки, получали производное (1), структура которого установлена с помощью 1D и 2D спектроскопии ЯМР 1Н и 13С и масс-спектрометрии MALDI TOF/TOF:
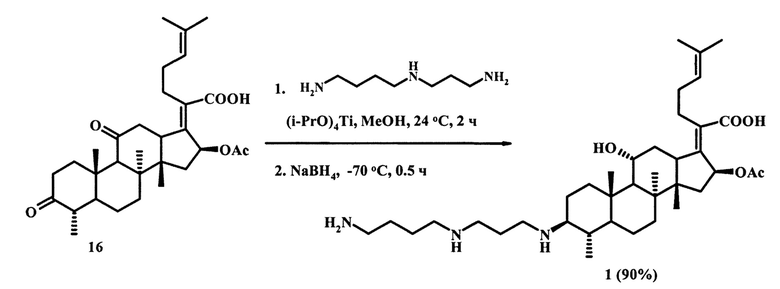
Преимущества предлагаемого способа:
В известном способе аминопроизводные (3-8) получены в виде смеси α- и β-стереоизомеров в соотношении 25:75, соответственно.
В отличие от известного, предлагаемый метод позволяет получать 3β-N-(3-аминопропил)бутан-1,4-диаминовое производное (1) в виде индивидуального стереоизомера с количественным выходом.
Сущность изобретения поясняется следующими примерами.
Пример 1. Смесь дикетона (16) (0.26 г, 0.5 ммоль), изопропоксида титана (IV) (55 мг, 0.15 ммоль) и 3β-N-(3-аминопропил)бутан-1,4-диамина (0.22 г, 1.5 ммоль) в 5 мл абсолютного метанола перемешивали в атмосфере аргона при комнатной температуре 2 часа. Реакционную массу охлаждали до -70°С и добавляли борогидрид натрия (0.04 г, 1.0 ммоль). Полученную смесь перемешивали в течение 0.5 часа при -70°С, после чего температуру постепенно повышали до комнатной и добавляли в реакционную массу 5 мл воды. Выпавший осадок отфильтровывали, промывали метанолом. Маточный раствор концентрировали в вакууме, получая сырой амин, который очищали колоночной хроматографией на силикагеле, элюируя метанолом. После хроматографической очистки получали триаминопроизводное (1) с выходом 90%, которое представляло собой кристаллическое вещество светло-желтого цвета, т.пл. 248-250°С, 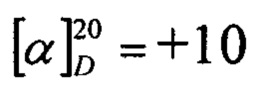 (с 1.13, МеОН). Структура соединения (1) подтверждена с помощью 1D и 2D спектроскопии ЯМР 1Н и 13С и масс-спектрометрии MALDI TOF/TOF. На основании спектральных данных установлено, что реакция проходит с высокой хемо- и стереоселективностью по 3 положению молекулы, в то время как кето-группа в 11-положении в реакцию аминирования не вступает и восстанавливается до гидроксильной. Аминогруппа в полученных соединениях имеет β-конфигурацию, что подтверждается спектрами NOESY.
(с 1.13, МеОН). Структура соединения (1) подтверждена с помощью 1D и 2D спектроскопии ЯМР 1Н и 13С и масс-спектрометрии MALDI TOF/TOF. На основании спектральных данных установлено, что реакция проходит с высокой хемо- и стереоселективностью по 3 положению молекулы, в то время как кето-группа в 11-положении в реакцию аминирования не вступает и восстанавливается до гидроксильной. Аминогруппа в полученных соединениях имеет β-конфигурацию, что подтверждается спектрами NOESY.
Спектральные характеристики ((2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметилгонан-17-илиден]-6-метилгепт-5-еновой кислоты (1)1.
Спектр ЯМР 1Н (CDCl3), δ, м.д.: 0.94-0.98 м (1Н, Н6), 0.96 с (3Н, H18), 1.07 с (3Н, Н19), 1.08 д (3Н, Н28, 3J 6.4 Гц), 1.14-1.27 м (1Н, Н7), 1.19-1.28 м (1H, Н6), 1.21-1.30 м (1H, Н15), 1.36 с (3Н, H30), 1.60-1.67 м (1Н, Н9), 1.63 с (3Н, Н27), 1.69 с (3Н, Н26), 1.72-1.84 м (1Н, H4), 1.74-1.84 м (1H, Н5), 1.74-1.86 м (2Н, Н34), 1.75-1.84 м (1Н, Н2), 1.76-1.87 м (1Н, Н7), 1.83-1.93 м (1Н, Н12), 1.92-1.99 м (1H, Н1), 2.00 с (3Н, Н32), 2.04-2.11 м (1H, Н2), 2.06-2.19 м (2Н, Н23), 2.10-2.20 м (2Н, H38), 2.10-2.20 м (1Н, Н15), 2.13-2.22 м (1H, Н1), 2.21-2.34 м (2Н, Н37), 2.29-2.36 м (1H, Н12), 2.33-2.43 м (1Н, Н22), 2.51-2.61 м (1Н, Н22), 2.77-2.82 м (1Н, Н36), 2.96-3.06 м (2Н, Н33), 3.01-3.08 м (1Н, Н13), 3.01-3.15 м (2Н, Н35), 3.06-3.14 м (2Н, Н39), 3.11-3.23 м (1H, Н36), 5.16 т (1Н, H24, 3J 7.5 Гц), 5.84 д (1Н, Н16, 3J 8.2 Гц).
Спектр ЯМР 13C (CDCl3), δ, м.д.: 14.36 (C28), 16.55 (С18), 16.55 (С27), 19.52 (С32), 21.08 (С6), 22.53 (С30), 22.82 (С19), 22.92 (С37), 22.99 (С38), 24.06 (С2, С34), 24.51 (С26), 27.87 (С23), 28.85 (С22), 31.69 (С7), 33.35 (С1), 34.95 (С4), 35.80 (С12), 36.05 (С10), 36.62 (С39), 38.65 (С15), 38.71 (С33), 39.12 (С8), 42.98 (С5), 43.15 (С13), 44.58 (С36), 46.90 (С35), 48.46 (С14), 48.84 (С9), 63.03 (С3), 66.82 (С11), 74.33 (С16), 123.31 (С24), 131.85 (С20), 131.56 (С25), 133.56 (С17), 171.56 (С31), 175.66 (С21). Масс-спектр (MALDI TOF/TOF), m/z (Iотн., %): 644 (100) [М+Н]+, 683 (55.3) [М+K]+.
1Контроль реакции осуществляли методом ТСХ на пластинах Sorbfil (Сорбполимер, Краснодар, Россия), проявляли 10% раствором серной кислоты. Для колоночной хроматографии использовали силикагель L (50-160 мкм) марки КСКГ. Температура плавления определена на приборе РНМК 80/2617. Спектры ЯМР 1D (1Н, 13С) и 2D (COSY, NOESY, HSQC, НМВС) сняты на спектрометре Bruker Avance 500 (125.78 МГц для 13С и 500.17 МГц для 1Н) с использованием стандартных импульсных последовательностей фирмы Bruker, внутренний стандарт Me4Si, растворитель - CD3OD. Оптические углы измерены на поляриметре Perkin-Elmer 341. Масс-спектры MALDI TOF/TOF получены на спектрометре Bruker Autoflex ТМ III Smartbeam с использованием матрицы 3-(4-гидрокси-3,5-диметоксифенил)проп-2-еновой кислоты (синапиновая кислота).
Противомикробный скрининг соединения (1) проводили в СО-ADD (The Community for Antimicrobial Drug Discovery), финансируемым Wellcome Trust (Великобритания) и Университетом Квинсленда (Австралия), на пяти бактериальных штаммах: Escherichia coli (Е. coli) АТСС 25922, Klebsiella pneumoniae (K. pneumoniae) АТСС 700603, Acinetobacter baumannii (A. baumannii) ATCC 19606, Pseudomonas aeruginosa (P. aeruginosa) ATCC 27853 и Staphylococcus aureus (S. aureus) ATCC 43300. Противогрибковую активность определяли на двух грибковых штаммах: Candida albicans (С. albicans) ATCC 90028 и Cryptococcus neoformans (С. neoformans) ATCC 208821.
Первичный скрининг противомикробной активности проводился путем тестов на ингибирование размножения клеток, используя образцы в одной (32 мкг/мл) концентрации. Аликвоту каждого образца в ДМСО помещали в 384-луночный планшет и обрабатывали соответствующей бактериальной культурой. Ингибирование роста бактерий определяли спектрофотометрически при 600 нм на монохромном микропланшетном ридере Tecan M1000 Pro. Процент ингибирования роста рассчитывали для каждой лунки с использованием отрицательного контроля (только для среды) и положительного контроля (бактерии без ингибиторов) на той же пластинке. В случае если один или оба раза наблюдалось ингибирование роста ≥80%, соединение считалось активным (Таблица 1).
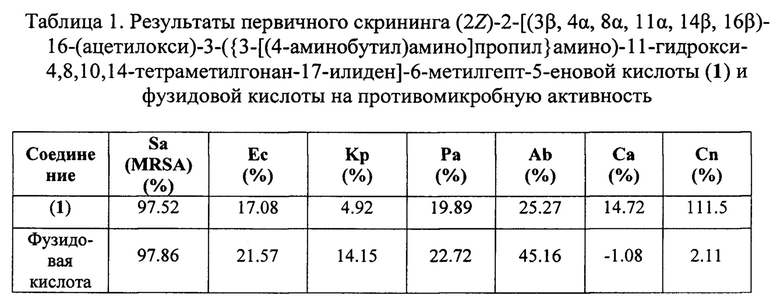
При первичном скрининге было выявлено наличие противомикробной и фунгицидной активности у (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметил-гонан-17-илиден]-6-метилгепт-5-еновой кислоты (1) в отношении культуры бактерий Staphylococcus aureus и грибковой культуры Cryptococcus neoformans. Для соединения (1) была определена минимальная ингибирующая концентрация в отношении вышеуказанных культур, а также изучена цитотоксическая и гемолитическая активности.
Минимальную ингибирующую концентрацию (MIC; мкг/мл) устанавливали в соответствии с рекомендациями Института клинических и лабораторных стандартов (Clinical and Laboratory Standards Institute (CLSI), США), определяя наименьшую концентрацию, при которой было обнаружено полное ингибирование бактерий или грибов. Скрининг проводился методом серийных разведений. Образцы готовились в ДМСО в тестовой концентрации 32 мкг/мл. Все бактерии культивировались на агаре Мюллера Хинтона при 37°С в течение ночи. Образец каждой культуры затем разбавлялся в 40 раз и инкубировался при 37°С в течение 1,5-3 ч. Полученные культуры добавлялись в каждую лунку 384-луночного планшета, содержащую исследуемый образец (плотность клеток 5×105 КОЕ / мл и общий объем 50 мкл). Все планшеты накрывались и инкубировались при 37°С в течение 18 ч без встряхивания. Ингибирование роста бактерий определялось измерением поглощения при 600 нм с использованием монохромного микропланшетного ридера Tecan M1000 Pro. Процент ингибирования роста рассчитывался для каждой лунки с использованием отрицательного контроля (только для среды) и положительного контроля (бактерии без ингибиторов) на той же пластине. Значения ингибирования определялись с помощью модифицированных Z-показателей, рассчитанных с использованием медианы и медианного абсолютного отклонения (MAD) образцов (без контроля) на той же пластине. Образцы с величиной ингибирования выше 80% и Z-оценкой выше 2,5 для обеих реплик классифицировались как активные вещества. Образцы с показателями ингибирования от 50 до 80% и Z-оценкой выше 2,5 для обеих реплик классифицировались как частично активные.
Тесты проводились в двойном повторе. Максимальный процент ингибирования роста обозначался как DMax. Хиты были классифицированы при MIC ≤ 16 мкг/мл или MIC ≤ 10 мкМ в любой реплике (n=2 на разных пластинах).
Цитотоксическое действие определяли на клеточной линии эмбриональных почек человека HEK293 путем определения концентрации, вызывающей гибель 50% клеток (Hk СС50). Ингибирование роста клеток HEK293 определяли, измеряя флуоресценцию после добавления 5 мкл 25 мкг / мл резазурина (конечная концентрация 2.3 мкг/мл) и после инкубации в течение еще 3 ч при 37°С в 5% СО2. Интенсивность флуоресценции измеряли с использованием монохромного микропланшетного ридера Tecan M1000 Pro с использованием автоматического вычисления коэффициента усиления. Максимальный процент цитотоксичности обозначали как DMax. Соединение считалось токсичным при СС50 ≤ 32 мкг / мл или СС50 ≤ 10 мкМ. Кроме того, образцы были отмечены как частичные цитотоксические, если DMax ≥ 50%, даже при СС50 выше максимальной тестируемой концентрации.
Гемолитическую активность (Hm НС10 и НС50 - концентрация при 10% и 50% гемолизе, соответственно) определяли путем измерения поглощения при 405 мм супернатанта - надосадочной жидкости, образованной после инкубации в течение 1 ч при 37°С планшетов, содержащих образцы соединений с добавленными к ним промытыми клетками крови человека, и последующего центрифугирования при 1000 об/мин в течение 10 мин. Абсорбцию измеряли с использованием монохромного микропланшетного ридера Tecan M1000 Pro.
Максимальный процент гемолиза представлен как DMax. Низкое значение DMax при НС10 > 32 мкг/мл (максимально испытанная концентрация) указывает на образцы без гемолитической активности. Образцы, обладающие гемолитической активностью, были охарактеризованы при НС10 ≤ 32 мкг/мл. Кроме того, образцы были помечены как частично гемолитические, если DMax ≥ 50%, даже при НС10 > максимальной тестируемой концентрации.
«Колистин» и «Ванкомицин» были использованы в качестве положительных стандартов бактериального ингибирования для грамотрицательных и грамположительных бактерий, соответственно. «Флуконазол» использовали в качестве стандартного ингибитора гриба для С. albicans и С. neoformans. «Тамоксифен» использовали в качестве положительного стандарта цитотоксичности. «Мелиттин» использовали в качестве положительного гемолитического стандарта.
Методика тестирования противомикробной, фунгицидной, цитотоксической и гемолитической активности in vitro соединений приведена также на сайте http://www.co-add.org.
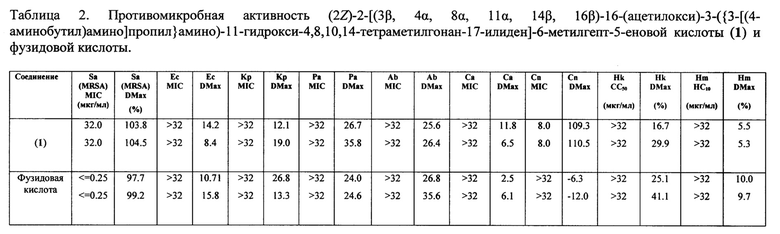
Образец (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметил-гонан-17-илиден]-6-метилгепт-5-еновой кислоты (1) в концентрации 8.0 мкг/мл показал фунгицидную активность, отсутствующую у фузидовой кислоты, ингибируя рост и размножение > 100% грибковой культуры Cryptococcus neoformans. В концентрации 32.0 мкг/мл соединение (1) ингибирует рост и размножение грамм-положительных бактерий Staphylococcus aureus, что, по критериям CO-ADD, является слабовыраженной антибактериальной активностью. Гемолитическая активность соединения (1) не превышает 5.5% даже при максимально тестируемой концентрации >32 мкг/мл, что ниже таковой у фузидовой кислоты в 1.8 раза, а цитотоксичность соединения (1) в 1.5 раза ниже по сравнению с нативным антибиотиком (Таблица 2).
Таким образом, соединение (1) проявляет фунгицидную активность в отношении патогенной грибковой культуры Cryptococcus neoformans при низкой токсичности и обладает минимальным гемолитическим действием при максимально тестируемой концентрации.
Изобретение относится к области синтеза биологически активных аналогов природных соединений, а именно к получению нового представителя азотсодержащих производных фузидовой кислоты - (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметил-гонан-17-илиден]-6-метилгепт-5-еновой кислоты (соединение (1)), обладающей антибактериальной активностью по отношению к Staphylococcus aureus (MRSA) и ингибирующей рост грибковой культуры Cryptococcus neoformans. Соединение (1) получено на основе соответствующего диоксо-производного фузидовой кислоты взаимодействием с 6 эквивалентами спермидина в присутствии изопропоксида титана (IV) в среде сухого метанола при перемешивании в течение 2 часов. Выход соединения (1) составил 90%. Соединение (1) проявляет фунгицидную активность в отношении патогенной грибковой культуры Cryptococcus neoformans при низкой токсичности и обладает минимальным гемолитическим действием при максимально тестируемой концентрации. 2 н.п. ф-лы, 2 табл., 1 пр.
1. Способ получения (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметил-гонан-17-илиден]-6-метилгепт-5-еновой кислоты (1),

заключающийся во взаимодействии (2Z)-2-[(4α,5α,8α,9β,13α,14β,16β)-16-(ацетилокси)-4,8,10,14-тетраметил-3,11-диоксогонан-17-илиден]-6-метилгепт-5-еновой кислоты с 6 эквивалентами N-(3-аминопропил)бутан-1,4-диамина и 0.3 эквивалентами изопропоксида титана (IV) в течение 2 часов.
2. (2Z)-2-[(3β,4α,8α,11α,14β,16β)-16-(Ацетилокси)-3-({3-[(4-аминобутил)амино]пропил}амино)-11-гидрокси-4,8,10,14-тетраметилгонан-17-илиден]-6-метилгепт-5-еновая кислота, обладающая антибактериальной активностью по отношению к Staphylococcus aureus (MRSA) и фунгицидной активностью в отношении грибковой культуры Cryptococcus neoformans.
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ 8-(МЕТОКСИКАРБОНИЛ)-4b,8-ДИМЕТИЛ-3-(2-МЕТИЛПРОПАНОИЛ)-ТЕТРАДЕКАГИДРОФЕНАНТРЕН-1,2,10a-ТРИКАРБОНОВУЮ КИСЛОТУ, ПРОЯВЛЯЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНУЮ И ПРОТИВОЯЗВЕННУЮ АКТИВНОСТЬ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2426720C1 |
| ПРОИЗВОДНЫЕ РАЗВЕТВЛЕННОГО ПОЛИАМИНОСТЕРОИДА | 2003 |
|
RU2334758C2 |
| WO 2002077007 A2, 03.10.2002. | |||
Авторы
Даты
2020-08-24—Публикация
2019-10-08—Подача