Изобретение относится к медицинской технике, а именно к ультразвуковой интерферометрии, и предназначено для ультразвуковой спектрометрии при исследовании биологических жидкостей.
Исследование физических характеристик биологических жидкостей является актуальной задачей, имеющей как самостоятельное научное (т.к. организм создает уникальные по своим свойствам жидкости и структуры), так и прикладное значение в области медицины и биологии. В настоящее время известен целый ряд физических методов, с помощью которых можно получать разнообразную информацию о биологических средах, т.е. средах, содержащих малые молекулы (органические и неорганические), макромолекулы (биополимеры: белки, полипептиды, нуклеиновые кислоты), клеточные и субклеточные элементы, которые имеют биологическое происхождение. Примерами жизненно важных биосред являются кровь, лимфа, желудочный сок, слюна, различные внутренние органы и ткани человека.
Экспериментальные исследования физических характеристик биосред имеют, некоторые особенности, которые связаны с их спецификой, поэтому это накладывает определенные ограничения на выбор физического метода их исследования. Определенные успехи при изучении биосред были сделаны при использовании ультразвуковых методов для измерения их акустических характеристик. Именно акустические исследования этих биологических сред позволяют изучить тонкие структурные характеристики, их межмолекулярные взаимодействия и конформационные перестройки.
Исследование физических характеристик биологических жидкостей является актуальной задачей, имеющей как самостоятельное научное (т.к. организм создает уникальные по своим свойствам жидкости и структуры), так и прикладное значение в области медицины и биологии. В настоящее время известен целый ряд физических методов, с помощью которых можно получать разнообразную информацию о биожидкостях (Буров В.А. и др., Активная и пассивная медицинская акустическая томография сильно неоднородных сред, Биомедицинские технологии и радиоэлектроника. 2002. №3. с. 5-13), т.е. водных растворах и суспензиях, содержащих малые молекулы (органические и неорганические), макромолекулы (биополимеры: белки, полипептиды, нуклеиновые кислоты), клеточные и субклеточные элементы, которые имеют биологическое происхождение. Примерами жизненно важных биожидкостей являются кровь, лимфа, желудочный сок, слюна.
Экспериментальные исследования физических характеристик биожидкостей имеют, по сравнению с обычными жидкостями, некоторые особенности, которые связаны с их спецификой.
Компоненты биожидкостей сохраняют нативное (естественное) состояние в ограниченном интервале внешних условий. Поэтому физические методы, не позволяющие работать с биожидкостями в нативном состоянии, заведомо дадут искаженную информацию. Измерения их физических характеристик необходимо производить в условиях, близких к условиям организма. Биожидкость, постоянно взаимодействуя с организмом, отражает изменения, которые происходят в нем под действием внешних факторов. Следовательно, в каждый момент времени их физические характеристики различны и, несмотря на то, что в нормальном состоянии адаптационные системы организма поддерживают постоянство внутренней среды, всегда приходится иметь дело с усредненными физическими характеристиками биологических жидкостей. Физический метод исследования биожидкостей, основанный на взаимодействии какого-либо вида энергии с биологической средой, должен незначительно возмущать равновесные состояния, существующие в жидкости, чтобы не вызвать необратимых изменений. Отсюда вытекает требование высокой чувствительности приемного устройства в установке, реализующей метод исследования биожидкостей.
Небольшие изменения внешних условий приводят к незначительным изменениям биосред. Тем не менее, эти небольшие изменения могут повлечь за собой серьезные последствия для организма. Это означает, что для исследования необходим метод, позволяющий регистрировать крайне малые изменения их свойств, т.е. обладающий повышенной точностью изменения регистрируемых параметров.
Биожидкости могут иметь как высокую (кровь, лимфа), так и низкую (желудочный сок) концентрацию компонентов. Поэтому, при выборе физического метода их исследования желательно, чтобы была возможность извлекать информацию о физических свойствах как в высоко-, так и в низко-концентрированных биожидкостях.
Все выше сказанное накладывает определенные ограничения на выбор физического метода исследования свойств биожидкостей.
Определенные успехи при изучении биосред были сделаны при использовании ультразвуковой интерферометрии для измерения акустических характеристик растворов белков и аминокислот. Именно акустические исследования этих биологических жидкостей позволяют изучить тонкие структурные характеристики и гидратацию биологических макромолекул в растворе, их межмолекулярные взаимодействия и конформационные перестройки биополимеров.
Ультразвуковые методы с целью их применения для исследования биологических сред использовались еще с девятнадцатого века, однако для медико-биологических приложений, в частности, в области медицинской диагностики известные технические решения применять не представляется возможным из-за того, что биосреды организма человека, используемые для медицинской диагностики (кровь, образцы внутренних органов), как правило, могут быть использованы в очень ограниченном объеме, а также точность измерений скорости и поглощения ультразвука должна быть предельно высокой для высококонцентрированных биосред (Клемин В.А Безреагентная диагностика: акустические технологии, Н. Новгород, 2014 г., 12 с.).
Ряд патологических процессов, сопровождающихся изменениями относительного содержания белка, липидов и воды, может приводить к изменению не только абсолютных значений скорости и затухания ультразвука, но и их зависимостей от частоты (Буров В.А. и др., Моделирование томографического восстановления термоакустических источников. Итерационно-корреляционные методы, Акустический журнал. 2003. том 49. №2. с. 167-177).
Большинство методов, которые используются в молекулярной акустике для измерения ультразвуковых характеристик различных сред (импульсный, фазовый и другие), мало пригодны при исследованиях биологических тканей и жидкостей, т.к. требуют использования больших объемов изучаемого материала. Резонаторный метод или метод интерферометра фиксированной длины, основанный на использовании стоячих ультразвуковых волн в цилиндрическом резонаторе, позволяет определять скорость и затухание ультразвука в малых объемах образца. С помощью резонаторного метода в диапазоне частот 1,7-17,4 МГц исследованы частотные зависимости скорости распространения и коэффициента затухания ультразвука в печени, селезенке и сердечной мышце крысы (Буров В.А. и др., Активная и пассивная медицинская акустическая томография сильно неоднородных сред, Биомедицинские технологии и радиоэлектроника. 2002. №3. С. 5 13).
Позже стали изучать и различные биологические жидкости. Например, с помощью резонаторного метода исследованы акустические свойства желудочного сока человека при различной патологии. Определены вклады различных компонентов желудочного сока (белки, ионы натрия) в величины его акустических характеристик. Применение для исследования биологических жидкостей дифференциального интерферометрического метода, позволившего довести относительную точность измерения скорости до 10-6 при объеме исследуемого образца порядка 100-1000 мкл (Greenleaf J.F. Computerized transmission tomography, Methods of experimental physics. Academic press. New York. 1981. Vol. 19) кардинально изменило ситуацию в ультразвуковых исследованиях белков. Высокоточные относительные измерения скорости ультразвука позволили четко дифференцировать фибриллярные и глобулярные белки, поскольку они имеют различную макромолекулярную структуру.
Еще в 50-е гг. было впервые показано, что поглощение ультразвука в жидкостях в значительной степени определяется содержащимися в ней белками (Уэбб С., Физика визуализации изображений в медицине, М.: «Мир». 1994. Том 1-410 с. Том 2 - 400 с.). Авторы исследовали кровь, плазму крови и водные растворы альбумина и гемоглобина в концентрациях, встречающихся в крови, в диапазоне ультразвуковых частот 0,3-10,0 МГц при температуре от 5 до 45°С. В дальнейшем более детально были изучены растворы гемоглобина, а также суспензия эритроцитов крови в физиологическом растворе. Анализировались и температурные зависимости акустических характеристик.
Так, из уровня техники известно использование интерферометра постоянной длины для измерения скорости ультразвука в биологических тканях и жидкостях (Carstensen E.L., Law W.K., McKay N.D., Muir T.G. Demonstration of nonlinear acoustical effects at biomedical frequencies and intensities, Ultrasound in Med. & Biol. 1980. V. 6. P. 359-368). Между преобразователями датчика специальной конструкции располагается образец среды минимального объема. Датчик, представляющий собой акустический резонатор, включен в цепь положительной обратной связи полосового усилителя. Когда датчик погружен в исследуемый раствор, в системе устанавливается генерация с частотой, соответствующей максимуму заданного резонансного пика, находящегося в полосе пропускания усилителя. Частота регистрируется электронносчетным частотомером. Скорость ультразвука в среде определяется по установившейся частоте генерации с помощью калибровки, построенной на измерениях в эталонных в водно-солевых растворах. Величина коэффициента поглощения ультразвука в среде регистрируется по смещению частоты генерации при введении фиксированного сдвига фазы сигнала в цепь обратной связи усилителя. Смещение частоты генерации определяется крутизной фазо-частотной характеристики резонатора, которая в свою очередь связана с затуханием ультразвука в исследуемой среде. пьезоэлектрический излучатель в качестве приемника, поставить перед излучающим кристаллом плоский отражатель, расположив его так, чтобы между ним и излучающей поверхностью кристалла установилась стоячая волна, то при перемещении отражателя воздействие отраженной волны на излучатель будет меняться, что можно регистрировать различными способами. Такое устройство позволяет весьма точно измерять длину волны и используется очень часто однако затруднения при определении длины камеры и тем самым при измерении абсолютных значений скорости и поглощения, предопределяют основную область применения интерферометра постоянной длины: автоматическое измерение изменений скорости и поглощения ультразвука.
Также из уровня техники известен ультразвуковой спектрометр (Клемин В.А Безреагентная диагностика: акустические технологии, Н. Новгород, 2014 г., 12 с.), принятый нами за прототип. Ультразвуковой спектрометр содержит корпус, расположенную в нем измерительную камеру с установленными в ней преобразователями ультразвуковых колебаний, нагревательный элемент, датчик температуры, при этом измерительная камера выполнена в виде одинаковых термостатируемых ячеек, каждая из них выполнена с возможностью соединения с независимым каналом измерения, каждый из которых содержит фазо-чувствительную схему, включающую в себя генератор сигналов, управляемый напряжением (ГУН) с цепью фазовой автоподстройки частоты (ФАПЧ), перестройка частоты генераторов производится модулем управления через цифроаналоговый преобразователь (ЦАП), выполненный с возможностью соединения с ГУН, при этом выходы фазо-чувствительных схем каждой ячейки выполнены с возможностью попеременного соединения через коммутатор ко входу частотомера, и управляющий модуль управления и обработки результатов (персональный компьютер), выполненный с возможностью соединения с ЦАП, нагревательным элементом и датчиком температуры. К недостаткам устройства можно отнести зависимость характеристик зависимости фаза-напряжение и напряжение-частота от диапазона частот и температурно-климатических условий работы измерительной установки за счет таких конструктивных элементов, как аналоговые фазо-чувствительных цепи и генераторы, управляемых напряжением. Кроме того, программный контроль частоты генератора исключает возможность перехода резонансной частоты между соседними резонансными пиками, который характерен для цепи ФАПЧ.
Таким образом, существует потребность в устройстве, позволяющем избежать вышеуказанных недостатков.
Техническим результатом настоящего изобретения является создание ультразвукового спектрометра, позволяющего быстро и с высокой точностью производить измерения резонансной частоты и ширины резонансного пика образца исследуемой биологической жидкости.
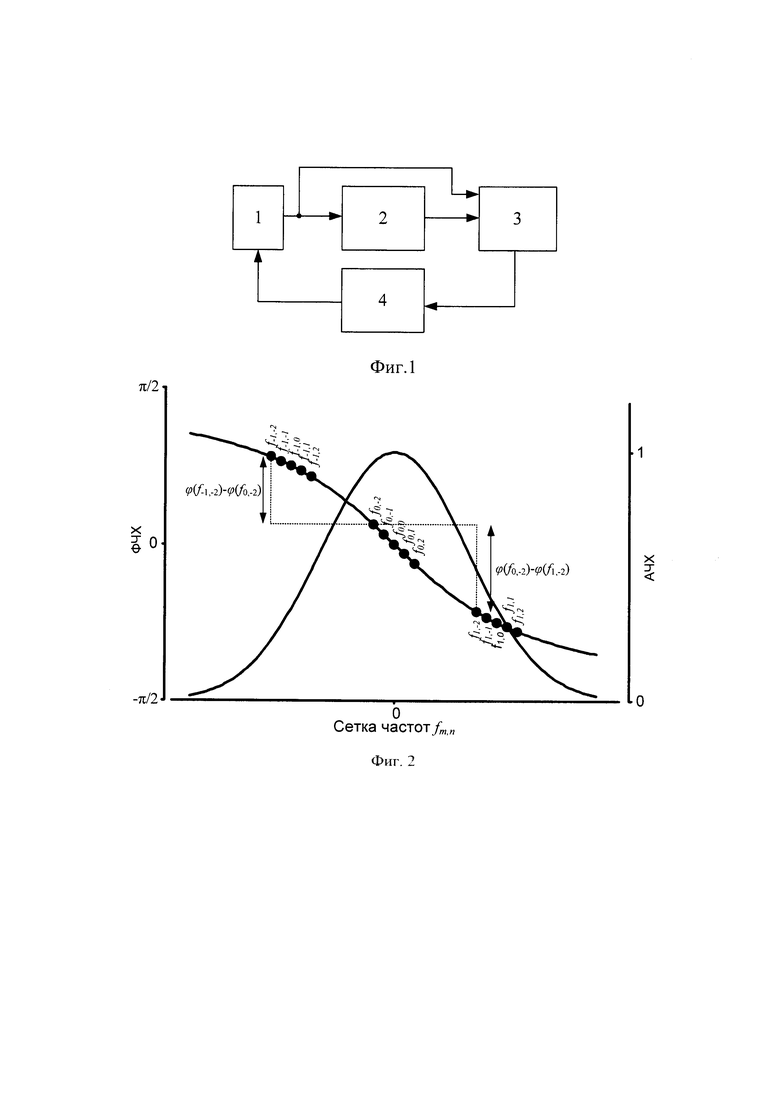
Этот технический результат достигается тем, что в ультразвуковом спектрометре, содержащем корпус, нагревательный элемент, датчик температуры, измерительную камеру с установленными в ней двумя резонаторами, представленными преобразователями ультразвуковых колебаний и термостатируемыми ячейками; каждый из резонаторов выполнен с возможностью соединения с независимым каналом измерения, представленным фазо-чувствительной схемой; и управляющий модуль, выполненный с возможностью соединения с нагревательным элементом и датчиком температуры, фазо-чувствительная схема представлена генератором сигналов с прямым цифровым синтезом (DDS) и прямым высокочастотным двухканальным синхронным аналого-цифровым преобразователем, содержащим первый вход и второй вход, при этом генератор сигналов DDS выполнен с возможностью соединения со входом резонатора и первым входом аналого-цифрового преобразователя, а выход резонатора выполнен с возможностью соединения со вторым входом аналого-цифрового преобразователя, модуль управления выполнен с возможностью соединения с генератором сигналов DDS.
На фиг. 1 представлена схема устройства.
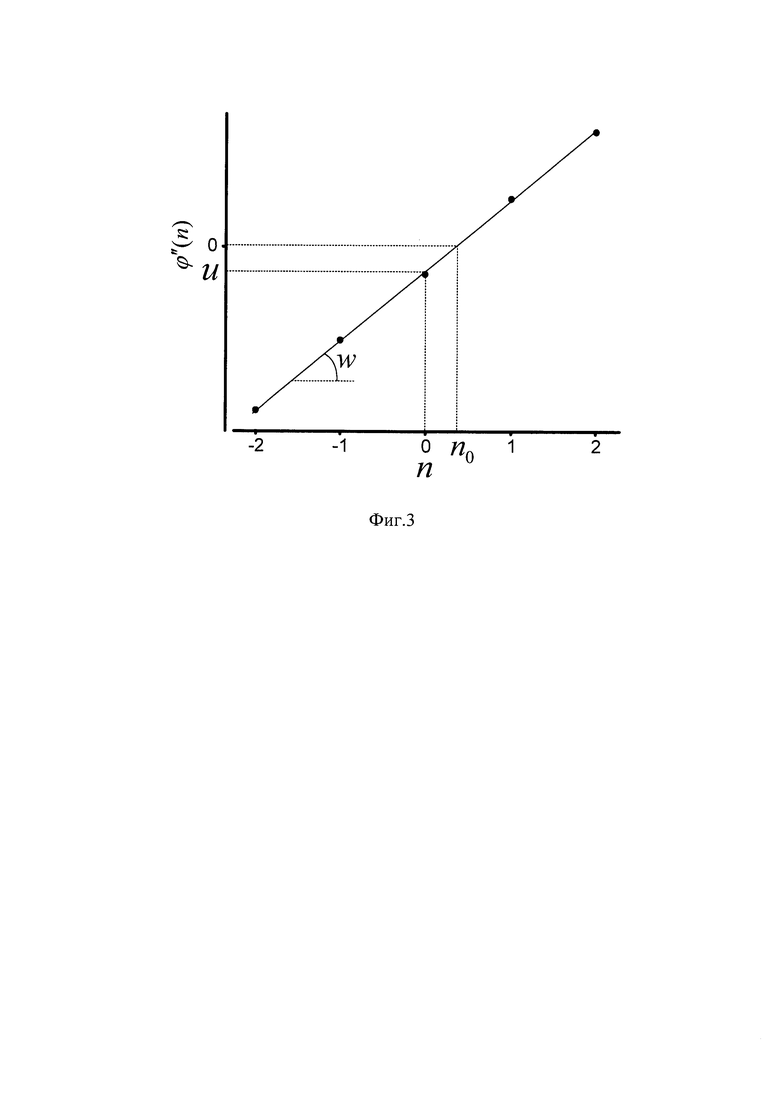
Фиг. 2-3 иллюстрируют обработку получаемого массива данных.
Устройство включает в себя корпус, нагревательный элемент, датчик температуры, измерительную камеру с установленными в ней двумя резонаторами Каждый резонатор представлен преобразователями ультразвуковых колебаний и термостатируемой ячейкой. Резонансные ячейки для исследования жидких образцов отличаются следующими характеристиками: они имеют малый объем камеры для исследуемого жидкого образца (0,1÷1 мл), они имеют малую длину камеры (4÷10 мм) и высокую рабочую частоту (1÷10 МГц), в пределах которой возможна регистрация резонансных пиков АЧХ камеры. Выражение для резонансной частоты в камере имеет вид:

где V - скорость звука в исследуемом образце, ƒn - частота резонансного пика с номером n, 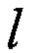 - длина камеры. Указанные характеристики резонансных ячеек приводят к тому, что в исследуемый частотный диапазон попадают резонансные пики с номерами n=70÷100. Резонансный пик ячейки при исследовании малопоглощающей жидкости (дистиллированной воды) имеет ширину около 700 Гц.
- длина камеры. Указанные характеристики резонансных ячеек приводят к тому, что в исследуемый частотный диапазон попадают резонансные пики с номерами n=70÷100. Резонансный пик ячейки при исследовании малопоглощающей жидкости (дистиллированной воды) имеет ширину около 700 Гц.
Каждый из двух резонаторов выполнен с возможностью соединения с независимым каналом измерения, каждый из которых содержит фазо-чувствительную схему, при этом выходы фазо-чувствительных схем (фиг. 1) каждого резонатора выполнены с возможностью попеременного соединения через коммутатор ко входу частотомера, фазо-чувствительная схема образована генератором сигналов с прямым цифровым синтезом (DDS) (1) и прямым высокочастотным двухканальным синхронным аналого-цифровым преобразователем (3), содержащим первый вход и второй вход, при этом генератор сигналов (1) выполнен с возможностью соединения со входом резонатора (2) и первым входом аналого-цифрового преобразователя (3), а выход резонатора (2) выполнен с возможностью соединения со вторым входом аналого-цифрового преобразователя (3). Управляющий модуль (4) (персональный компьютер) выполнен с возможностью соединения с аналого-цифровым преобразователем (3), нагревательным элементом и датчиком температуры (не показаны), а также с генератором сигналов (1).
Работа устройства осуществляется следующим образом.
Проводят измерение резонансной частоты и ширины резонансного пика образца биологической жидкости в акустической ячейке ультразвукового спектрометра фиксированной длины.
Программа управляющего модуля записывает в генератор (1) значение частоты, которую необходимо подать на пластины пьезопреобразователей резонатора (2). Проведение измерения резонансной частоты ячейки с исследуемым образцом проводят последовательно относительно ячейки с дистиллированной водой.
С выхода генератора (1) сигнал гармонических колебаний заданной частоты поступает на вход резонатора (2) и одновременно на первый вход аналого-цифрового преобразователя (3). После окончания переходного процесса в резонаторе (2) и установления в нем стационарных колебаний, на выходе резонатора (2) появляется стабильный по амплитуде и фазе гармонический сигнал, который поступает на второй вход аналого-цифрового преобразователя (3). В этот момент программа управляющего модуля (4) запускает процесс синхронной дискретизации сигналов с обоих каналов аналого-цифрового преобразователя (3). Результат дискретизации сохраняется в буферной памяти аналого-цифрового преобразователя (3) и затем передается в управляющий модуль и подвергается обработке программой. В результате измерения получается два массива цифровых данных регистрации гармонических сигналов.
Вычислительная часть измерителя резонансной частоты реализована в виде компьютерной или микропроцессорной программы, осуществляющей следующие действия. Для построения амплитудо-частотной характеристики вычисляют значение коэффициента передачи амплитуды в резонаторе по формуле:
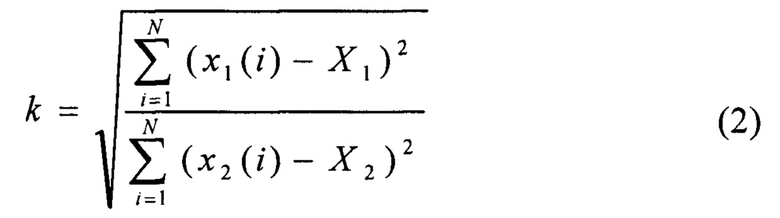
где i - номер измерения, x1(i) - значения, измеренные в первом канале, x2(i) - значения, измеренные во втором канале, Х1 - среднее значений x1(i), X2 - среднее значений x1(i).
Для построения фазо-частотной характеристики, значение фазового сдвига для заданной частоты вычисляют по формулам:
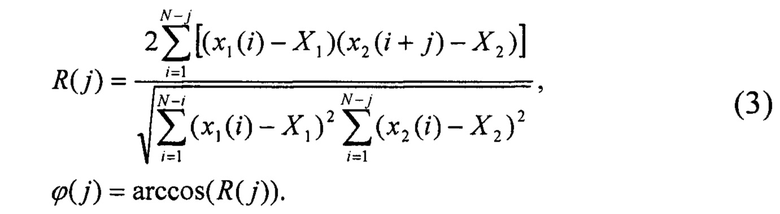
Формула для вычисления R(j) является формулой для вычисления корреляции Пирсона с введенным виртуальным сдвигом фазы j. График зависимости ϕ(j) имеет вид пилообразной линии. Для определения фазового сдвига между каналами аналого-цифрового преобразователя выбирают ближайший к оси ординат участок линии с положительным наклоном, аппроксимируют его прямой линией и определяют точку пересечения с осью абсцисс j0. Фазовый сдвиг определяют по формуле:

Таким образом, для любой заданной частоты, подаваемой в резонатор определяют точку амплитудной и фазовой характеристики.
Для определения положения резонансного пика, определяется фазо-частотная характеристика его окрестности. На рисунке 2 поясняется принцип построения сетки частот и способ приближенного вычисления второй производной фазы по частоте. Для этого в окрестности предполагаемой резонансной частоты формируется сетка частот по формуле:

где ƒp - предполагаемая резонансная частота, m=-1, 0, 1, n=-2, -1, 0, 1, 2,

где Δƒ - полуширина резонансного пика на полувысоте максимальной амплитуды пика, а - коэффициент размаха сканирования, обычно равный ~0,5, b - коэффициент размаха сканирования, обычно равный ~0,1.
В соответствии с этой сеткой (матрицей) частот проводят измерения фазо-частотной характеристики способом, указанным выше. Перебор частот производят следующим образом: фиксируют n=-2 и изменяют m от -1 до 1, затем увеличивают n на единицу и т.д. Такой способ исследования резонансного пика дает минимальную погрешность измерения при изменении резонансной частоты в ячейке во время измерения.
Положение резонансного пика определяют по нулю второй производной фазо-частотной характеристики в окрестности резонансной частоты. Для этого приближенно определяют (см. Фиг. 2) вторую производную фазы по формуле:
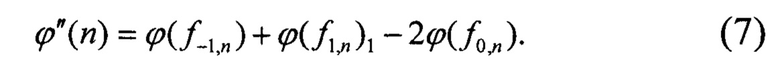
Таким образом, получают зависимость ϕ''(n), которую аппроксимируют прямой (Фиг. 3):

и определяют точку пересечения с осью абсцисс:

Текущую резонансную частоту определяют по формуле:

Текущую ширину резонансного пика определяют по наклону характеристики ϕ''(n):

Описанный выше режим измерений позволяет отслеживать изменения резонансной частоты со временем при выполнении условия

что накладывает ограничения на скорость измерения и стабильность условий измерения резонансной частоты в ячейке с исследуемой жидкостью.
При определении общего белка сыворотки крови была выполнена проверка воспроизводимости, правильности (сравнением с контрольными сыворотками «Randox») и чувствительности предлагаемого способа. В качестве метода сравнения использовался биуретовый метод определения концентрации общего белка в сыворотке крови. Был проведен регрессионный анализ и рассчитан коэффициент корреляции для оценки связи показателей, полученных двумя методами. Получена высокая степень корреляции (r=0,98) для выборки n=100 (количество проб). Все полученные значения соответствуют нормам аналитической точности клинических лабораторных исследований. Чувствительность предлагаемого способа составила менее 10 г/л в интервале концентраций общего белка 10-150 г/л. Анализ полученных данный свидетельствует, что результаты вполне удовлетворяют нормам аналитической точности клинических лабораторных исследований.
Воспроизводимость определения параметров липидограммы (определение холестерина общего, холестерина ЛПВП, холестерина ЛПНП и триглицеридов) производили в сыворотке больных с различным содержанием липидов и контрольных сыворотках. Для оценки правильности определения липидных компонентов были использованы контрольные сыворотки «Serodos» и проведены сопоставительные исследования акустического метода определения липидных компонентов сыворотки крови с традиционными биохимическими методами. Результаты сопоставительных исследований имеют по всем измеренным липидным компонентам коэффициенты корреляции от 0,77 до 0,85, что соответствует высокой корреляционной связи, достаточной для правильной диагностики нарушений липидного обмена. Статистическая обработка данных показала, что средние величины смещения находятся в пределах допустимых значений для показателей липидного обмена.
Таким образом, применение предлагаемого ультразвукового спектрометра фиксированной длины позволяет быстро и с высокой точностью производить измерения резонансной частоты и ширины резонансного пика образца исследуемой биологической жидкости.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ ультразвуковой спектрометрии при исследовании биологических жидкостей | 2019 |
|
RU2723152C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АПОЛИПОПРОТЕИНА А1 И АПОЛИПОПРОТЕИНА В СЫВОРОТКИ КРОВИ | 2013 |
|
RU2535142C1 |
| СПОСОБ ДИАГНОСТИКИ ЗАБОЛЕВАНИЙ ОПУХОЛЕВОГО ПРОИСХОЖДЕНИЯ ВНУТРЕННИХ ОРГАНОВ И СПОСОБ ПОЛУЧЕНИЯ КОНТРОЛЬНОГО ОБРАЗЦА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ (ВАРИАНТЫ) | 1993 |
|
RU2082318C1 |
| Способ оценки эффективности лечения отслойки сетчатки у пациентов с тампонадой силиконовым маслом и нарушением прозрачности оптических сред глаза | 2018 |
|
RU2696041C1 |
| СПОСОБ И СИСТЕМА ДЛЯ ОПРЕДЕЛЕНИЯ ПЛОТНОСТИ ЖИДКОСТИ | 1994 |
|
RU2144183C1 |
| УСТРОЙСТВО ДЛЯ УЛЬТРАЗВУКОВОГО КОНТРОЛЯ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 1992 |
|
RU2039978C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФИЗИЧЕСКИХ ПАРАМЕТРОВ СОСТОЯНИЯ СРЕДЫ | 1991 |
|
RU2029265C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАРАМЕТРИЧЕСКИХ ХАРАКТЕРИСТИК БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 2001 |
|
RU2206091C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЧЕСТВА КЛЕЙКОВИНЫ | 1997 |
|
RU2130179C1 |
| Устройство для метрологического контроля состояния приборов оптической флоуметрии | 2021 |
|
RU2777514C1 |
Изобретение относится к медицинской технике, а именно к ультразвуковой интерферометрии, и предназначено для ультразвуковой спектрометрии при исследовании биологических жидкостей. Техническим результатом является повышение точности измерений резонансной частоты и ширины резонансного пика образца исследуемой биологической жидкости. Ультразвуковой спектрометр содержит корпус, нагревательный элемент, датчик температуры, измерительную камеру с установленными в ней двумя резонаторами, представленными преобразователями ультразвуковых колебаний и термостатируемыми ячейками, каждый из резонаторов выполнен с возможностью соединения с независимым каналом измерения, представленным фазочувствительной схемой, и управляющий модуль, выполненный с возможностью соединения с нагревательным элементом и датчиком температуры. Фазочувствительная схема содержит генератор сигналов с прямым цифровым синтезом (DDS) и аналого-цифровой преобразователь, содержащий первый вход и второй вход. Генератор сигналов DDS выполнен с возможностью соединения с входом резонатора и первым входом аналого-цифрового преобразователя. Выход резонатора выполнен с возможностью соединения со вторым входом аналого-цифрового преобразователя, модуль управления выполнен с возможностью соединения с генератором сигналов DDS. 3 ил.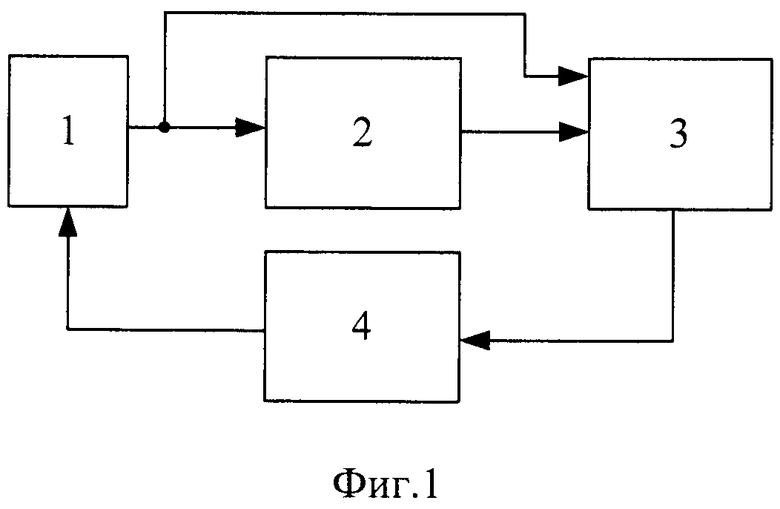
Ультразвуковой спектрометр, содержащий корпус, нагревательный элемент, датчик температуры, измерительную камеру с установленными в ней двумя резонаторами, представленными преобразователями ультразвуковых колебаний и термостатируемыми ячейками; каждый из резонаторов выполнен с возможностью соединения с независимым каналом измерения, представленным фазочувствительной схемой; и управляющий модуль, выполненный с возможностью соединения с нагревательным элементом и датчиком температуры, отличающийся тем, что фазочувствительная схема представлена генератором сигналов с прямым цифровым синтезом (DDS) и прямым высокочастотным двухканальным синхронным аналого-цифровым преобразователем, содержащим первый вход и второй вход, при этом генератор сигналов DDS выполнен с возможностью соединения с входом резонатора и первым входом аналого-цифрового преобразователя, а выход резонатора выполнен с возможностью соединения со вторым входом аналого-цифрового преобразователя, модуль управления выполнен с возможностью соединения с генератором сигналов DDS.
| СПОСОБ УЛЬТРАЗВУКОВОГО КОНТРОЛЯ СТРУКТУРНОГО СОСТОЯНИЯ ПОВЕРХНОСТЕЙ РАЗДЕЛА СРЕД | 1992 |
|
RU2049330C1 |
| УСТРОЙСТВО ДЛЯ УЛЬТРАЗВУКОВОГО КОНТРОЛЯ БИОЛОГИЧЕСКИХ ЖИДКОСТЕЙ | 1992 |
|
RU2039978C1 |
| Дифференциальный акустический интерферометр | 1988 |
|
SU1631407A1 |
| US 5804698 A1, 08.09.1998 | |||
| Запоминающая электронно-лучевая трубка | 1977 |
|
SU695417A1 |
Авторы
Даты
2020-06-04—Публикация
2019-10-24—Подача