Изобретение относится к медицине, в частности к технологии получения композиционного биомедицинского материала "никелид титана - полилактид" с возможностью контролируемой доставки лекарственных средств.
В последние годы все больше применяются такие медицинские изделия как стенты различной конфигурации, как правило, представляющие собой цилиндры из нескольких переплетенных проволок или тонких свернутых пластин с множеством отверстий и служащие для расширения сузившихся или полностью перекрытых полостей организма (сосудов, ЖКТ и др.).
Чаще всего стенты устанавливаются, когда атеросклеротические бляшки блокируют кровеносный сосуд. Эти бляшки состоят из холестерина и других веществ, которые прикрепляются к стенкам сосуда и там накаливаются. Закупорка может привести к инфаркту миокарда или апоплексии. Помимо кровеносных сосудов, стенты могут открыть любой из следующих проходов: желчные протоки, которые несут желчь, бронхи, которые представляют собой небольшие дыхательные пути в легких, мочеточники, которые несут мочу от почек до мочевого пузыря и другие. Вблизи или внутри этих проходов может появится новообразование, которое приведет к сужению или закупорке просвета.
Из-за постоянного контакта имплантатов с тканями живого человеческого организма материал для их изготовления должен обладать рядом физико-химических свойств, которые обеспечивали бы биосовместимость изделия. Примерно 30 лет назад для использования в медицине впервые начали применять новый класс материалов - сверхэластичные сплавы с памятью формы. Основой для них явился никелид титана, а также его сплавы. Новый материал обладал нужными физико-механическими свойствами, схожими с тканями организма.
Но медицинский имплантат типа «стент», как чужеродное тело, при контакте с кровью может вызвать развитие повторного сужения просвета (рестеноза). Существует три разные причины рестеноза, вызванные имплантатом:
а) В течении первых нескольких дней после имплантации поверхность стента находится в прямом контакте с кровью, что может привести к острому тромбозу, который снова закрывает просвет из-за присутствующей внешней поверхности.
б) Имплантация стента может вызывать повреждения сосудов, которые вызовут воспалительные реакции, в течение первых семи дней, в дополнение к вышеупомянутому тромбозу.
в) Через пару недель стент может начать прорастать в ткань кровеносного сосуда. Это означает, что стент полностью будет окружен гладкомышечными клетками и не будет иметь контакта с кровью. Данный эффект может привести не только к покрытию поверхности стента, но и к окклюзии всего внутреннего пространства стента.
Сейчас используются стенты, отличающиеся различным дизайном исполнения, материалом изготовления, а также видом (саморасширяющиеся, расширяемые воздушным баллончиком; растворимые и нет; с лекарственным покрытием и без), но ни один из них не может полностью обеспечить устранение проблемы (рестеноза).
Решение состоит в нанесении полимерного слоя (полилактида) на медицинское изделие типа «стент», которое обладает биосовместимостью, относительной инертностью, хорошими механическими свойствами, биодеградацией, а также он способен удерживать в своей структуре растворенное вещество (лекарство), и за счет этого производить доставку лекарств локально в нужной концентрации в течении определенного времени для дополнительного медикаментозного воздействия и предотвращения воспалительных реакций и избавления от рестеноза. Полилактид, т.е. полилактическая кислота, которую обычно получают из димера молочной кислоты, т.е. лактида, уже в течение многих лет используется в медицинских целях, например, при изготовлении хирургических швов, для разлагаемых нитей и для контролируемого высвобождения лекарственных средств.
В патенте CN 10405629 7А получали пленки полилактида методом растворения 10% полимера в дихлорметане, перемешивая его в магнитной мешалке в течение 24 часов до получения гомогенной системы. В специальном устройстве получали волокнистые мембраны и сушили их при 40°С в течении 12 часов. Данный метод требует достаточно длительного количества времени производства пленок.
В патенте US 611792 8А механические свойства пленок полилактида были усовершенствованы путем добавления к полимеру глицерол эфирных пластификаторов, но эти пластификаторы приводят к быстрому гидролизу и вызывают проблемы с адгезией. Также механические свойства пленок достаточны для применения в качестве поверхностного слоя на стент, поэтому в добавлении пластификаторов нет необходимости.
В патенте US 20040034409 А1 полилактид, с молекулярной массой более 200 кДа, наносился на стент для предотвращения рестеноза. Было обнаружено, что применение высокомолекулярного полилактида приводит к снижению воспалительных процессов. В патенте упоминается о том, что можно вводить лекарственные вещества в полимер и локально доставлять их к месту поражения, но конкретные исследования этого не проводились.
В патенте US 20050060028 А1, который является наиболее близким, стенты покрываются одним или несколькими поверхностными слоями, которые содержат антипролиферативный и/или противовоспалительный и при необходимости антитромботический активный агент.Гемосовместимое покрытие стента обеспечивает требуемую совместимость с кровью, а активный агент (или комбинация активных агентов), который равномерно распределяется по всей поверхности стента, обеспечивает покрытие поверхности стента клетками. Таким образом, на поверхности стента не происходит быстрой популяции и чрезмерного роста клеток, которое может привести к рестенозу, однако покрытие поверхности стента клетками может повысить риск возникновения тромбоза.
Задача данного изобретения состоит в получении композиционного биомедицинского материала "никелид титана - полилактид" для изготовления медицинского изделия типа «стент» с возможностью контролируемой доставки лекарственных средств в течении определенного времени, достаточного для предотвращения отторжения имплантата тканями.
Технический результат заключается в получении композиционного материала и изучении поверхностного слоя, а именно в получении однородных пленок полилактида с лекарством и контроль скорости выхода лекарственного средства в течении определенного времени.
Достижение технического результата включает в себя следующие этапы:
1) Приготовление гомогенного раствора полимера (полилактида), добавление лекарственного средства, нанесение полимера с лекарственным средством на проволоку методом окунания и дальнейшая сушка.
2) Используется полилактид с различной молекулярной массой (45 кДа, 90 кДа, 180 кДа)
3) В качестве растворителя для приготовления растворов используется хлороформ в количестве 100, 150 и 200 миллилитров.
4) Лекарственные вещества, а именно гентамицин, цефотаксим и линкомицин, добавляются в количестве от 1 до 8% вес.
5) Фиксация полимера достигается сушкой при комнатной температуре (20°С - 22°С)
Сущность изобретения
Поддержание определенного уровня лекарства, не смотря на ток крови, достигается контролируемой биодеградацией и выходом лекарственного средства из поверхностного полимерного слоя.
В качестве исходных материалов использовали следующие реактивы: Поли-D,L-лактид (45 кДа, ООО "МЕДИН-Н, Россия), Поли-D,L-лактид (90 кДа, ООО "МЕДИН-Н, Россия), Поли-D,L-лактид (180 кДа, ООО "МЕДИН-Н, Россия), Хлороформ (ОСЧ, поставщик ООО «Компонент-Реактив», Россия), проволока TiNi диаметром 280 мкм после отжига и полировки (ИМЕТ РАН).
Растворы полилактида готовят на основе особо чистого хлороформа в количестве от 100 до 200 миллилитров. Было установлено, что количество хлороформа, в данном диапазоне, не влияет на свойства получаемых полимерных пленок, поэтому для получения пленок с лекарственным средством использовалось 100 миллилитров растворителя. Был использован полилактид с различной молекулярной массой (45, 90 и 180 кДа) и установлено, что оптимальными прочностными и пластическими свойствами для применения в качестве поверхностного слоя на стент обладает полилактид с молекулярной массой 180 кДа. Полимерные пленки создавались с использованием 1, 3 и 5 грамм полимера. Оптимальной выбрана концентрация 3 грамма, способствующая формированию толщины 82-125 мкм. В качестве наполнителя используются антибиотики (линкомицин, цефотоксим, гентамицин), которые вводили в остывший (+30°С) раствор полилактида в концентрации 1, 3, 5 и 8% вес. При испарении хлороформа полимер с лекарственным средством образуют связку с равномерным распределением лекарства. Скорость биодеградации полимерной пленки из полилактида зависит от среды и типа антибиотика и составляет от 180 до 358 дней, а скорость выхода лекарственного средства зависит от антибиотика и его концентрации от 1 до 8% вес. Варьируя состав и толщину полимерного слоя можно добиться различной биодеградации и подобрать под конкретное применение.
Пример 1.
Композиционный материал получали нанесением поверхностного слоя из полилактида с введнным лекаственным средством (гентамицином) на проволоку из никелида титана.
Растворы полилактида готовят на основе особо чистого хлороформа объемом 100 миллилитров, который наливали в колбу объемом 300 миллилитров и нагревали до 50°С на магнитной мешалке. После нагрева в колбу помещался полимер (полилактид 180 кДа) навеской массы 3 грамма (±0,001 г). Для достижения гомогенного состояния раствор полимера в течении 1 часа перемешивается на электронной верхнеприводной мешалке при температуре 50°С. Затем полученному гомогенному раствору давали остыть до 30°С и вводили в него лекарственное средство (гентамицин) в количестве 1, 3, 5, 8% от массы полимера (в раствор с 3000 мг полимера добавляется 30,303 мг - 1%, 92,784 мг - 3%, 157,895 мг - 5% или 260,870 мг - 8% лекарства). Измельчение лекарства в растворе и достижение гомогенности осуществляется с помощью диспергатора при скорости 5000 об/мин в течении 10 минут.
Обезжиренная TiNi проволока окунается в остывший (+30°С) раствор полилактида с лекарственным средством и выдерживается в течение 5 минут. Затем проводится извлечение материала из раствора и сушка при комнатной температуре (20-22°С) в течение 24 часов.
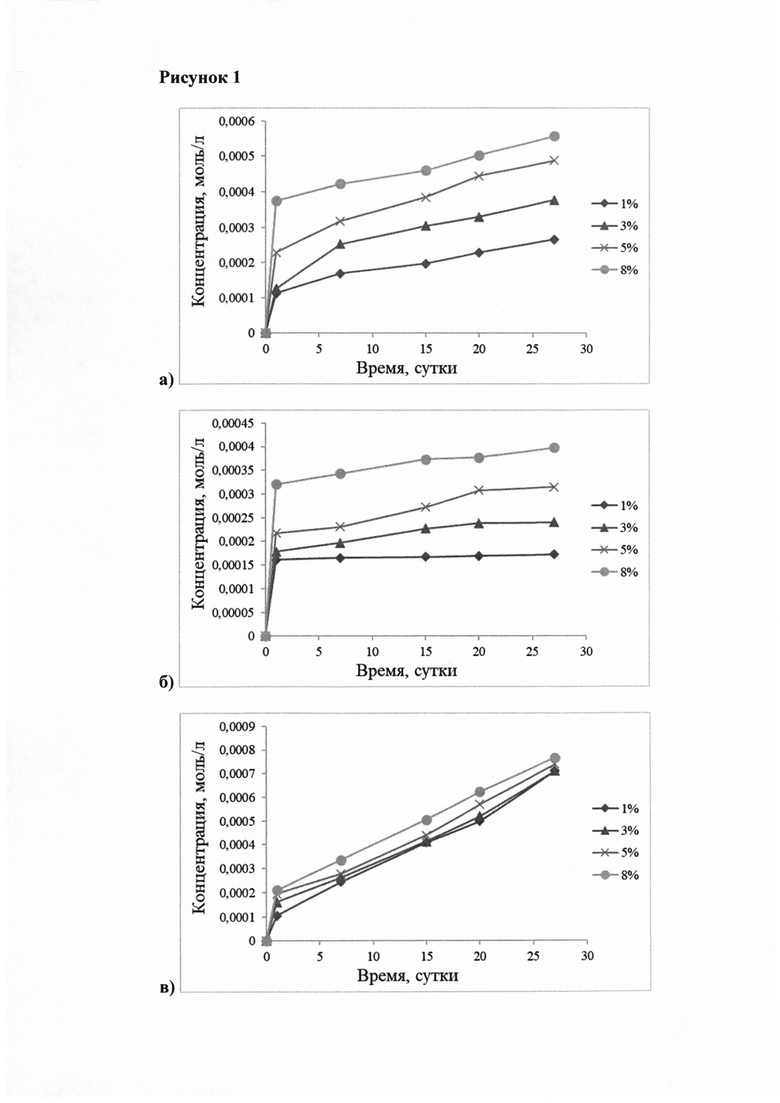
На рисунке 1 можно наблюдать кинетику выхода гентамицина из полимерного слоя в растворы моделирующие внеклеточные жидкости организма (рис. 1а - рН 5,3; рис. 1б - рН 7,4; рис. 1в - рН 9,0). Можно видеть, что спустя 1 сутки наблюдалось скачкообразное появление антибиотика, а затем его равномерный выход. Увеличение концентрации антибиотика приводило к большему количеству выхода лекарства в 1 сутки.
Пример 2.
Композиционный материал получали нанесением поверхностного слоя из полилактида с введнным лекаственным средством (цефотаксимом) на проволоку из никелида титана.
Растворы полилактида готовят на основе особо чистого хлороформа объемом 100 миллилитров, который наливали в колбу объемом 300 миллилитров и нагревали до 50°С на магнитной мешалке. После нагрева в колбу помещался полимер (полилактид 180 кДа) навеской массы 3 грамма (±0,001 г). Для достижения гомогенного состояния раствор полимера в течении 1 часа перемешивается на электронной верхнеприводной мешалке при температуре 50°С. Затем полученному гомогенному раствору давали остыть до 30°С и вводили в него лекарственное средство (цефотаксим) в количестве 1, 3, 5, 8% от массы полимера (в раствор с 3000 мг полимера добавляется 30,303 мг - 1%, 92,784 мг - 3%, 157,895 мг - 5% или 260,870 мг - 8% лекарства). Измельчение лекарства в растворе и достижение гомогенности осуществляется с помощью диспергатора при скорости 5000 об/мин в течении 10 минут.
Обезжиренная TiNi проволока окунается в остывший (+30°С) раствор полилактида с лекарственным средством и выдерживается в течение 5 минут. Затем проводится извлечение материала из раствора и сушка при комнатной температуре (20-22°С) в течение 24 часов.
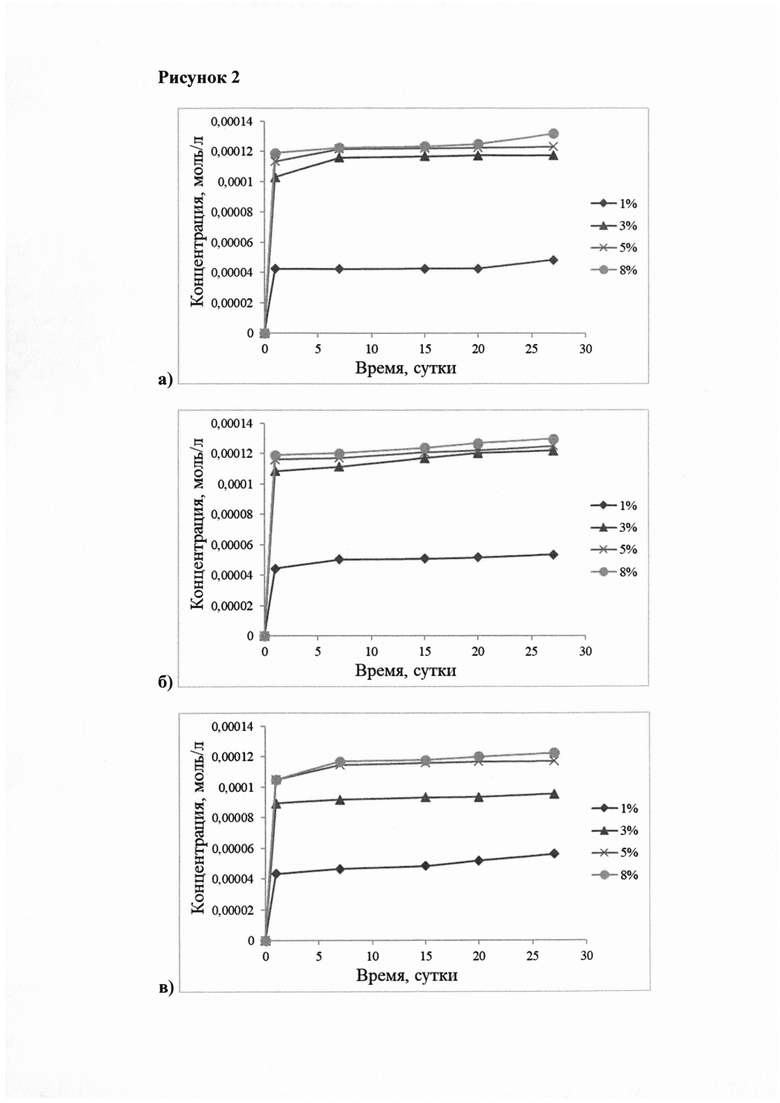
На рисунке 2 можно наблюдать кинетику выхода цефотаксима из полимерного слоя в растворы моделирующие внеклеточные жидкости организма (рис. 2а - рН 5,3; рис. 2б - рН 7,4; рис. 2в - рН 9,0). Можно видеть, что спустя 1 сутки наблюдалось скачкообразное появление антибиотика, а затем его равномерный выход. Увеличение концентрации антибиотика приводило к большему количеству выхода лекарства в 1 сутки.
Пример 3.
Композиционный материал получали нанесением поверхностного слоя из полилактида с введнным лекаственным средством (линкомицином) на проволоку из никелида титана.
Растворы полилактида готовят на основе особо чистого хлороформа объемом 100 миллилитров, который наливали в колбу объемом 300 миллилитров и нагревали до 50°С на магнитной мешалке. После нагрева в колбу помещался полимер (полилактид 180 кДа) навеской массы 3 грамма (±0,001 г). Для достижения гомогенного состояния раствор полимера в течении 1 часа перемешивается на электронной верхнеприводной мешалке при температуре 50°С. Затем полученному гомогенному раствору давали остыть до 30°С и вводили в него лекарственное средство (линкомицин) в количестве 1, 3, 5, 8% от массы полимера (в раствор с 3000 мг полимера добавляется 30,303 мг - 1%, 92,784 мг - 3%, 157,895 мг - 5% или 260,870 мг - 8% лекарства). Измельчение лекарства в растворе и достижение гомогенности осуществляется с помощью диспергатора при скорости 5000 об/мин в течении 10 минут.
Обезжиренная TiNi проволока окунается в остывший (+30°С) раствор полилактида с лекарственным средством и выдерживается в течение 5 минут. Затем проводится извлечение материала из раствора и сушка при комнатной температуре (20-22°С) в течение 24 часов.
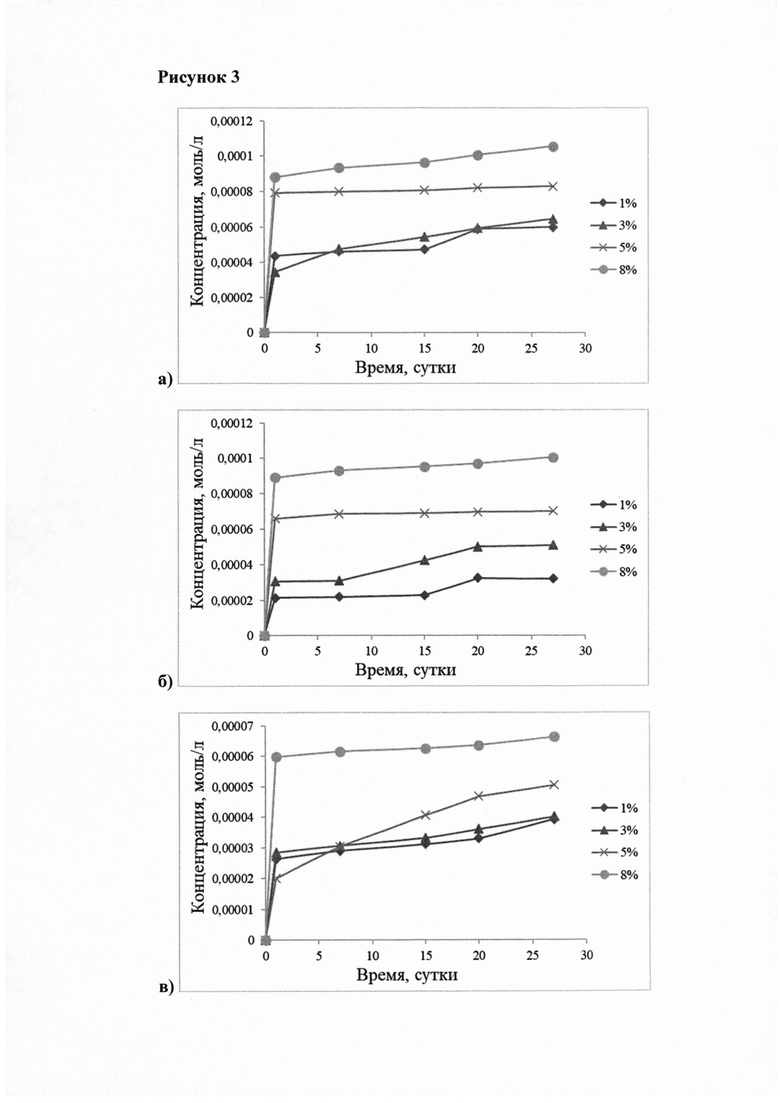
На рисунке 3 можно наблюдать кинетику выхода линкомицина из полимерного слоя в растворы моделирующие внеклеточные жидкости организма (рис. 3а - рН 5,3; рис. 3б - рН 7,4; рис. 3в - рН 9,0). Можно видеть, что спустя 1 сутки наблюдалось скачкообразное появление антибиотика, а затем его равномерный выход. Увеличение концентрации антибиотика приводило к большему количеству выхода лекарства в 1 сутки.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения композиционного биомедицинского материала «никелид титана-полилактид» с возможностью контролируемой доставки лекарственных средств | 2020 |
|
RU2733708C1 |
| Способ получения биосовместимого композиционного материала с основой из наноструктурного никелида титана и биодеградируемым лекарственным слоем полилактид с гепарином | 2019 |
|
RU2737827C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОДЕГРАДИРУЕМОГО ПОЛИМЕРНОГО ПОКРЫТИЯ С КОНТРОЛИРУЕМЫМ ВЫХОДОМ ЛЕКАРСТВЕННОГО СРЕДСТВА ДЛЯ МАЛОИНВАЗИВНОЙ ХИРУРГИИ | 2015 |
|
RU2585576C1 |
| Способ получения биодеградируемого полимерного покрытия на основе полилактида на проволоке TiNbTaZr | 2018 |
|
RU2686747C1 |
| Способ получения композиционного материала "Ti-Nb-Ta-Zr - полигликолидлактид с введенным лекарственным препаратом" | 2019 |
|
RU2730531C1 |
| Медицинское изделие стент с полимерными покрытиями | 2019 |
|
RU2737505C1 |
| Стент с лекарственным покрытием и способ его получения | 2021 |
|
RU2775427C1 |
| Способ получения биоактивного покрытия c бактерицидными свойствами на имплантате из титана | 2019 |
|
RU2719475C1 |
| СТЕНТ | 2007 |
|
RU2432183C9 |
| ЭНДОПРОТЕЗЫ, ИМЕЮЩИЕ ПОКРЫТИЕ АКТИВНЫМ СОЕДИНЕНИЕМ | 2012 |
|
RU2592367C2 |
Изобретение относится к технологии получения композиционного биомедицинского материала никелид титана-полилактид с возможностью контролируемой доставки лекарственных средств. Предложенный способ получения биомедицинского материала никелид титана-полилактид включает получение раствора полилактида с молекулярной массой 180 кДа в хлороформе. В остывший до 30°С раствор полилактида добавляют лекарственное средство гентамицин, цефотаксим или линкомицин в концентрации от 1% до 8% вес. Окунают проволоку из никелида титана (TiNi) в остывший до 30°С раствор полилактида с лекарственным средством, выдерживают в течение 5 мин. Извлекают полученный материал и сушат при комнатной температуре 20-22°С в течение 24 ч. Изобретение позволяет получать однородные по толщине пленки полилактида с лекарством с возможностью контролируемой доставки лекарственных средств в течение определенного времени, достаточного для предотвращения отторжения имплантата тканями. 3 ил., 3 пр.
Способ получения биомедицинского материала никелид титана-полилактид с возможностью контролируемой доставки лекарственного средства, включающий растворение полилактида в хлороформе, добавление лекарственного средства, окунание проволоки в раствор из полилактида с лекарством, выдержку и дальнейшую сушку, отличающийся тем, что получают раствор полилактида с молекулярной массой 180 кДа, в остывший до 30°С раствор полилактида добавляют лекарственное средство гентамицин, цефотаксим или линкомицин в концентрации от 1% до 8% вес., окунают проволоку из никелида титана (TiNi) в остывший до 30°С раствор полилактида с лекарственным средством, выдерживают в течение 5 мин, извлекают полученный материал и сушат при комнатной температуре 20-22°С в течение 24 ч.
| US 2005060028 A1, 17.03.2005 | |||
| СПОСОБ ПОЛУЧЕНИЯ БИОДЕГРАДИРУЕМОГО ПОЛИМЕРНОГО ПОКРЫТИЯ С КОНТРОЛИРУЕМЫМ ВЫХОДОМ ЛЕКАРСТВЕННОГО СРЕДСТВА ДЛЯ МАЛОИНВАЗИВНОЙ ХИРУРГИИ | 2015 |
|
RU2585576C1 |
| СЕВОСТЬЯНОВ М.А | |||
| и др | |||
| "Кинетика высвобождения антибиотика линкомицин из биодеградируемых биополимерных мембран на основе полилактида в водных растворах" | |||
| Успехи современного естествознания, 2016, no.5 (часть 1), с.43-46 | |||
| КАПЛАН М | |||
| А | |||
| "Нитинол с биодеградируемым поверхностным слоем." | |||
Авторы
Даты
2020-06-16—Публикация
2019-01-17—Подача