ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит список последовательностей, представленный в электронном виде в формате ASCII через EFS-Web и включенный в настоящий документ в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 19 ноября 2014 года, называется 11634.6003.00000_SL.txt и имеет размер 284497 байт.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к области биохимии, молекулярной биологии и диагностики, профилактики и лечения болезни Альцгеймера. В настоящем документе предложены гуманизированные антитела против тау-белка человека, которые способны различать нормальный (здоровый) и патологический (связанный с заболеванием) тау-белок.
УРОВЕНЬ ТЕХНИКИ
Болезнь Альцгеймера (AD) является прогрессирующим нейродегенеративным расстройством, которое разрушает высокие структуры головного мозга, такие как структуры, связанные с памятью и мыслительным процессом. Заболевание приводит к дефициту когнитивных функций и снижению памяти, обучения, языковых навыков и способности выполнять преднамеренные и целенаправленные движения. Существует потребность в эффективных способах и композициях для лечения и профилактики AD.
AD гистологически характеризуется наличием экстранейрональных бляшек и внутриклеточных и внеклеточных нейрофибриллярных клубков в головном мозге. Бляшки главным образом состоят из β амилоида (Αβ), тогда как клубки содержат патологические формы тау-белка, такие как патологические конформеры тау-белка и их агрегаты. Подтвержденная роль тау-белка в патологии AD была продемонстрирована в многочисленных исследованиях. Например, в статье Braak показано, что ближайшим аналогом нейродегенерации AD является наличие клубков тау-белка, а не амилоидных бляшек (Braak, H., et al. Neuropathological stageing of Alzheimer-related changes. Acta Neuropathol 82:239-259 (1991)).
Тау-белок относится к семейству белков, отличающихся неупорядоченной структурой и характеризующихся отсутствием жесткой трехмерной структуры в их физиологической среде (Skrabana et al., 2006).Однако усечение тау-белка и гиперфосфорилирование может вызвать патологические трансформации состояния, отличающегося неупорядоченной структурой, во множественные растворимые и нерастворимые патологические беспорядочные структуры, включая парные спиральные нити (PHF) и другие агрегаты (Wischik, C.M., Novak, M., Edwards, P.C., Klug, A., Tichelaar, W., Crowther, R.A. (1988). Structural characterization of the core of the paired helical filament of Alzheimer disease, Proc Natl Acad Sci USA 85,4884-8; Wischik, C.M., Novak, M. Thøgersen, H.C., Edwards, P.C., Runswick, M.J., Jakes, R., Walker, J.E., Milstein, C., Roth, M., Klug, A.(1988).Isolation of a fragment of tau derived from the core of the paired helical filament of Alzheimer disease, Proc Natl Acad Sci USA 85, 4506-10; Novak et al., 1993; Skrabana et al.,2006; Zilka, N., et al. Chaperone-like Antibodies Targeting Misfolded Tau Protein: New Vistas in the Immunotherapy of Neurodegenerative Foldopathies. Journal of Alzheimer's disease 15 (2008) 169-179; Kovacech B, Novak M.(2010). Tau truncation is a productive posttranslational modification of neurofibrillary degeneration in Alzheimer's disease. Curr Alzheimer Res Dec;7(8):708-16); Kovacech B, Skrabana R, Novak M.(2010). Transition of tau protein from disordered to misordered in Alzheimer's disease. Neurodegener Dis 7:24-27). Эти структурные изменения приводят к токсическому усилению функции, к потере физиологической функции нативного белка или к тому и другому (Zilka et al., 2008; Kovacech B, Novak M. (2010). Tau truncation is a productive posttranslational modification of neurofibrillary degeneration in Alzheimer's disease. Curr Alzheimer Res Dec;7(8):708-16); Kovacech B, Skrabana R, Novak M. (2010).Transition of tau protein from disordered to misordered in Alzheimer's disease. Neurodegener Dis 7:24-27).).
Физиологическая функция тау-белка заключается в опосредовании сборки мономеров тубулина в микротрубочки, которые составляют сеть микротрубочек нейронов (Buee, L., Bussiere, T., Buee-Scherrer, V., Delacourte, A., Hof, P.R.(2000). Tau protein isoforms, phosphorylation and role in neurodegenerative disorders. Brain Research.Brain Research Reviews.33, 95-130).Tau binds to microtubules through repetitive regions located in the C-terminal portion of the protein. Butner KA, Kirschner MW.1991.Tau protein binds to microtubules through a flexible array of distributed weak sites. J Cell Biol 115:717-730; Lee G, Neve RL, Kosik KS. 1989.The microtubule binding domain of tau protein. Neuron 2:1615-1624..Эти повторяющиеся домены (R1-R4) не идентичны друг другу, но содержат высококонсервативные 31-32 аминокислоты (Taniguchi T, Sumida M, Hiraoka S, Tomoo K, Kakehi T, Minoura K, Sugiyama S, Inaka K, Ishida T, Saito N, Tanaka C 2005 (Effects of different anti-tau antibodies on tau fibrillogenesis:RTA-1 and RTA-2 counteract tau aggregation. FEBS Lett 579:1399-1404; Taniguchi S, Suzuki N, Masuda M, Hisanaga S, Iwatsubo T, Goedert M, Hasegawa M. Inhibition of heparin-induced tau filament formation by phenothiazines, polyphenols, and porphyrins. J Biol Chem 280:7614-7623 (2005)). В человеческом мозге существует шесть уникальных изоформ тау-белка, которые отличаются друг от друга наличием или отсутствием определенных аминокислот в N-концевой части тау-белка в комбинации либо с тремя (R1, R3 и R4), либо с четырьмя (R1-R4) повторяющимися доменами на С-конце белка. См. также фигуру1, на которой показано шесть изоформ человека (2N4R, 1N4R, 2N3R, 0N4R, 1N3R и 0N3R с SEQ ID NO:151-156, соответственно, по порядку).).Было высказано предположение, что наиболее сильнодействующей частью тау-белка, вызывающей полимеризацию микротрубочек, является последовательность 306-VQIVYK-311 (SEQ ID NO:146) и 274-KVQIINKK-281 (SEQ ID NO:144), перекрывающие R1-R2.(von Bergen M, Friedhoff P, Biernat J, Heberle J, Mandelkow EM, Mandelkow E. 2000.Assembly of tau protein into Alzheimer paired helical filaments depends on a local sequence motif ((306)VQIVYK(311)) forming beta structure. Proc Natl Acad Sci U S A 97:5129-5134.)
Кроме того, патологические и физиологические функции тау-белка, по-видимому, влияют на специфическую структурную конформацию и природную неупорядоченную структуру, которую принимают полноразмерные изоформы белка и их фрагменты. Например, в статье Kontsekova et al. описан конформационный участок (включающий остатки 297-IKHVPGGGSVQIVYKPVDLSKVTSKCGSL-325 (SEQ ID NO:145) в пределах некоторых усеченных молекулах тау, которые отказывают значительное влияние на функцию этих укороченных молекул тау при сборке микротрубочек (WO 2004/007547).
Кроме их физиологической роли, считается, что повторы тау-белка связаны с формированием патологических агрегатов и других структур тау-белка. Таким образом, существует потребность в терапевтических и диагностических подходах, направленных на тау-белок, которые способны различать физиологическую и патологическую активность микротрубочек по связыванию с повторяющимися областями. Например, устойчивое к действию протеиназы ядро патологических спаренных спиральных филаментов (PHF) состоит из областей связывания микротрубочек с 3- и 4-повторами изоформ тау-белками (Jakes, R., Novak, M., Davison, M., Wischik, C.M. (1991).Identification of 3- and 4-repeat tau isoforms within the PHF in Alzheimer's disease. EMBO J 10, 2725-2729; Wischik, et al. 1988a; Wischik, et al. 1988b).Кроме того, в статье Novak et al. показано, что устойчивое к действию протеазы ядро PHF, длина которого составляет 93-95 аминокислот, ограничено тремя тандемными повторами (Novak, M., Kabat, J., Wischik, C.M.(1993). Molecular characterization of the minimal protease resistant tau unit of the Alzheimer's disease paired helical filament. EMBO J 12, 365-70). В статье Von Bergen et al. был определен минимальный тау-пептидный/взаимодействующий мотив (306-VQIVYK-311; SEQ ID NO:146), а также второй сайт тау-белка (275-VQIINK-280) (SEQ ID NO:147), которые образуют структуры бета-листов и описаны как вероятно ответственные за инициирование образования PHF, патологического агрегата тау-белка (von Bergen M, Friedhoff P, Biernat J, Heberle J, Mandelkow EM, Mandelkow E. 2000.Assembly of tau protein into Alzheimer paired helical filaments depends on a local sequence motif ((306)VQIVYK(311)) forming beta structure. Proc Natl Acad Sci U S A 97:5129-5134); EP 1214598; WO 2001/18546).См. фигуру 2, где показана функциональная карта тау-белка. Следовательно, современные стратегии нацелены на получение лекарственных средств против агрегатов, которые не нарушают внутриклеточную роль тау-белка в стабилизации микротрубочек.
Более того, в то время как при физиологических условиях тау-белок считается внутриклеточным цитоплазматическим белком, внутриклеточный тау-белок может высвобождаться во внеклеточное пространство и способствовать нейродегенерации (Gómez-Ramos, A., Díaz-Hernández, M., Cuadros, R., Hernández, F., and Avila, J.(2006). Extracellular tau is toxic to neuronal cells. FEBS Lett 580(20), 4842-50).Действительно, потеря нейронов связана с топографическим распределением нейрофибриллярных клубков (состоящих из тау-белка) в мозге при AD (West, M.J., Coleman, P.D., Flood, D.G.,Troncoso, J.C. (1994).Differences in the pattern of hippocampal neuronal loss in normal ageing and Alzheimer's disease. Lancet 344,769-72; Gómez-Isla, T., Price, J.L., McKeel Jr, D.W., Morris, J.C., Growdon, J.H., Hyman, B.T.(1996).Profound loss of layer II entorhinal cortex neurons occurs in very mild Alzheimer's disease. J Neurosci 16(14),4491-500; Gomez-Isla T, Hollister R, West H, Mui S, Growdon JH, Petersen RC, Parisi JE, Hyman BT. Neuronal loss correlates with but exceeds neurofibrillary tangles in Alzheimer's disease. Ann Neurol 41:17-24 (1997)).Кроме того, уровни общего тау-белка и фосфорилированного тау-белка увеличиваются в цереброспинальной жидкости (CSF) у пациентов с AD (Hampel, H., Blennow, K., Shaw, L.M., Hoessler, Y.C., Zetterberg, H., Trojanowski, J.Q. (2010).Total and phosphorylated tau protein as biological markers of Alzheimer's disease. Exp Gerontol 45(1), 30-40) и внеклеточный тау-белок был описан как "призрачные клубкиʺ в мозге (Frost, B., Diamond, M.I. (2009).The expanding realm of prion phenomena in neurodegenerative disease. Prion 3(2):74-7), что указывает на то, что внутриклеточный тау-белок высвобождается во внеклеточное пространство. Кроме того, внеклеточные агрегаты тау-белка могут проникать в клетки и стимулировать образование фибрилл внутриклеточного тау-белка, дополнительно распространяя тау мономер для продукции агрегатов патологического тау-белка (Frost et al.,2009).Такие исследования показали что внеклеточный нерастворимый тау-белок может выступать в качестве трансмиссивного агента, распространяя патологию, вызываемую тау-белком, по всему мозгу прионо-подобным образом (Frost, B., Jacks, R.L., Diamond, M.I. (2009).Propagation of tau misfolding from the outside to the inside of a cell. J Biol Chem 284(19),12845-52; Frost et al., 2009; Frost, B., Diamond, M.I. (2009).The expanding realm of prion phenomena in neurodegenerative disease. Prion 3(2):74-7). Нацеливание на патологический тау-белок может уменьшить патологию, связанную с внеклеточным и внутриклеточным тау-белком. См. Eva Kontsekova, Norbert Zilka, Branislav Kovacech, Petr Novak, Michal Novak. 2014.First-in-man tau vaccine targeting structural determinants essential for pathological tau-tau interaction reduces tau oligomerisation and neurofibrillary degeneration in an Alzheimer's disease model. Alzheimer's Research & Therapy, 6:44.Таким образом существует необходимость в лечебных подходах, способных уменьшать внеклеточный тау-белок либо предотвращая его формирование, либо ускоряя его выведение, либо и то, и другое, а также в лечебных подходах, которые уменьшают патологический внутриклеточный тау-белок. Более ясное понимание молекулярных механизмов, лежащих в основе патологической трансформации тау-белка, делает возможным специфическое нацеливание на патологические модификации тау-белка в терапевтических целях.
В международной публикации №WO 2013141962, Novak et al., описано обнаружение четырех областей тау-белка, которые стимулируют агрегацию тау-тау при AD, и раскрыты антитела, которые предотвращают агрегацию тау-белка за счет связывания этих четырех областей.
Не смотря на то, что в других исследованиях описаны антитела, которые связываются с последовательностями тау-белка, и сообщается о том, что некоторые из этих антител, влияют на агрегацию и выведение тау-белка (Asuni AA, Boutajangout A, Quartermain D, Sigurdsson EM. Immunotherapy targeting pathological tau conformers in a tangle mouse model reduces brain pathology with associated functional improvements. J Neurosci 27:9115-9129 (2007)), о моноклональных антителах против тау-белка, с которыми проводят клинические испытания для лечения AD, не сообщалось.
Успеху чужеродных (мышиных) моноклональных антител при лечении человека отчасти препятствовали иммуногенные антиглобулиновые ответы, индуцируемые человеком-реципиентом против таких чужеродных терапевтических средств. Они ухудшают как безопасность, так и фармакокинетические свойства антител. Эти проблемы привели к разработке антител с более низким риском иммунных реакций методами генной инженерии. Целый ряд запатентованных технологий генной инженерии (например, химеризация, гуманизация, трансплантация CDR, трансплантация каркасной области, созревание аффинности, фаговый дисплей, трансгенные мыши) постоянно разрабатываются для облегчения этого процесса. Недавний обзор см. в статье Safdari Y1, Farajnia S, Asgharzadeh M, Khalili M.Antibody humanization methods - a review and update. 2013.Biotechnol Genet Eng Rev. 29:175-86. doi:10.1080/02648725.2013.801235 and Almagro JC1, Fransson J. Humanization of antibodies. 2008.Front Biosci. 13:1619-33.
Гуманизированные антитела сконструированы, в первую очередь, для сохранения специфичности и аффиности исходного антитела, при этом имеющего константные области человека, что в идеале должно давать меньшую иммуногенную мишень для пациента. Типичное гуманизированное антитело содержит области, определяющие комплементарность (CDR) исходного антитела, имеющего мышиное или крысиное происхождение, и каркасные (FR) и константные области, которые в основном имеют человеческое происхождение, но часто мутированные для сохранения связывающих свойств исходного антитела. Однако антиген-связывающая аффинность и специфичность не являются единственными факторами, влияющими на биологическую активность и клиническую эффективность антитела. Улучшение активации антител иммунной системой пациента является важным фактором для некоторых гуманизированных антител, тогда как в других случаях целью является снизить клеточную токсичность. В конечном счете, более глубокое понимание структуры и активности антител позволяет исследователям создавать методами генной инженерии, часто посредством мутаций, гуманизированные антитела с улучшенными свойствами, которые являются более гомогенными и имеют улучшенные антиген-связывающие свойства (аффинность связывания, специфичность к мишени), эффекторные функции, стабильность, уровень экспрессии, свойства очистки, фармакокинетические и фармакодинамические свойства.Многие из этих улучшений важны для коммерческой жизнеспособности данного антитела. Иногда после того, как достигается аффинность связывания с мишенью и специфичность, необходимо мутировать некоторые из аминокислот в CDR или FR для уменьшения способности к агрегации гуманизированных антител. В других случаях изменяют (переключают или мутируют) константные области для улучшения эффекторных функций. Эти и другие аспекты функции и активности антител все еще создают проблемы при разработке антител для клинического применения. Ниже раскрыт набор гуманизированных антител против тау-белка, которые в результате конструирования обладают неожиданными благоприятными свойствами. Также ниже представлены новые способы и композиции, содержащие эти высокоспецифичные и высокоэффективные антитела, обладающие способностью специфически распознавать и связываться с патологическим тау-белком, препятствуя его агрегации. Все эти антитела, способы и композиции могут использоваться для диагностики и лечения AD и связанных таупатий.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Эти и другие объекты, признаки и преимущества настоящего изобретения станут очевидными после рассмотрения нижеследующего подробного описания раскрытого варианта осуществления и прилагаемой формулы изобретения.
Объектом изобретения является гуманизированное антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3 соответственно, и каркасную область иммуноглобулина человека M65092 (SEQ ID NO:71);
вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и каркасную область иммуноглобулина человека X72449 (SEQ ID NO:65); а также
константные области тяжелой цепи и легкой цепи, каждая из иммуноглобулина человека; и где каркасная область тяжелой цепи замещена в одном или нескольких положениях, выбранных из 9, 21, 27, 28, 30, 38, 48, 67, 68, 70 и 95; указанная каркасная область легкой цепи либо не замещена, либо замещена в положении 5; и где указанные положения соответствую нумерации Kabat. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Такие антитела и связывающие фрагменты также рассматриваются в форме, когда положение 9 тяжелой цепи занято P, положение 21 занято P, положение 27 занято Y, положение 28 занято I, положение 30 занято T, положение 38 занято K, положение 48 занято I, положение 67 занято K, положение 68 занято A, положение 70 занято L, и/или положение 95 занято F. В одном из вариантов осуществления положение 5 легкой цепи занято S. В некоторых вариантах осуществления по сути только два из этих 11 положений заняты. В некоторых вариантах осуществления по сути только три из этих 11 положений заняты. В некоторых вариантах осуществления по сути только четыре из этих 11 положений заняты. В некоторых вариантах осуществления по сути только пять из этих 11 положений заняты. В некоторых вариантах осуществления по сути только шесть из этих 11 положений заняты. В некоторых вариантах осуществления по сути только семь из этих 11 положений заняты. В некоторых вариантах осуществления по сути только восемь из этих 11 положений заняты. В некоторых вариантах осуществления по сути только девять из этих 11 положений заняты. В некоторых вариантах осуществления по сути только десять из этих 11 положений заняты. В некоторых вариантах осуществления по сути все 11 из этих 11 положений заняты. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в которых последовательность вариабельной области тяжелой цепи выбрана из RHA-RHM, SEQ ID NO:13-25, соответственно; и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26 (RKA).
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в которых последовательность вариабельной области тяжелой цепи выбрана из RHA-RHM, SEQ ID NO:13-25, соответственно; и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27 (RKB).
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:13, RHA, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:15, RHC, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:18, RHF, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:19, RHG, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:20, RHH, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:21, RHI, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:22, RHJ, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:23, RHK, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:24, RHL, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:13, RHA, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:15, RHC, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:18, RHF, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:19, RHG, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:20, RHH, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:21, RHI, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:22, RHJ, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:23, RHK, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:24, RHL, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
Также раскрыто гуманизированное антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3 соответственно, и каркасную область иммуноглобулина человека M65092 (SEQ ID NO:71); и
вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и каркасную область иммуноглобулина человека X72449 (SEQ ID NO:65); и
константные области тяжелой цепи и легкой цепи иммуноглобулина человека, предпочтительно IgG1 или IgG4.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с любой аминокислотной последовательностью из SEQ ID NO:28-40; и
вариабельный домен легкой цепи с любой аминокислотной последовательностью из SEQ ID NO:26 и 27. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с любой аминокислотной последовательностью из SEQ ID NO:43-55; и
легкую цепь, содержащую вариабельный домен легкой цепи с любой аминокислотной последовательностью из SEQ ID NO:26 и 27. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с любой аминокислотной последовательностью из SEQ ID NO:43-55; и
легкую цепь с любой аминокислотной последовательностью из SEQ ID NO:57 и 58. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:31; и
легкую цепь с аминокислотной последовательностью SEQ ID NO:57. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:32; и
легкую цепь с любой аминокислотной последовательностью из SEQ ID NO:57. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:31; и
легкую цепь с аминокислотной последовательностью SEQ ID NO:58. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:32; и
легкую цепи с аминокислотной последовательностью SEQ ID NO:58 и 27. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:46; и
легкую цепь с аминокислотной последовательностью SEQ ID NO:57. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:47; и
легкую цепь с аминокислотной последовательностью SEQ ID NO:57. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:46; и
легкую цепь с аминокислотной последовательностью SEQ ID NO:58. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Дополнительно раскрыто антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или связывающий фрагмент содержит следующие полные цепи:
тяжелую цепь с аминокислотной последовательностью SEQ ID NO:47; и
легкую цепь с аминокислотной последовательностью SEQ ID NO:58. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Также раскрыто антитело, содержащее:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3, и которая по меньшей мере на 85% идентична любой из SEQ ID NO: RHA, SEQ ID RHB, SEQ ID RHC, SEQ ID RHD, SEQ ID RHE, SEQ ID RHF, SEQ ID RHG, SEQ ID RHH, SEQ ID RHI, SEQ ID RHJ, SEQ ID RHL, SEQ ID RHM, то есть, SEQ ID NO:13-25;
и вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и которая по меньшей мере на 85% идентична SEQ ID NO:26, RKA, где антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
Также раскрыто антитело, содержащее:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3, и которая по меньшей мере на 90% идентична любой из SEQ ID NO: RHA, SEQ ID RHB, SEQ ID RHC, SEQ ID RHD, SEQ ID RHE, SEQ ID RHF, SEQ ID RHG, SEQ ID RHH, SEQ ID RHI, SEQ ID RHJ, SEQ ID RHL, SEQ ID RHM, то есть, SEQ ID NO:13-25;
и вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и которая по меньшей мере на 90% идентична SEQ ID NO:26, RKA, где антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
Также раскрыто антитело, содержащее:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3, и которая по меньшей мере на 95% идентична любой из SEQ ID NO: RHA, SEQ ID RHB, SEQ ID RHC, SEQ ID RHD, SEQ ID RHE, SEQ ID RHF, SEQ ID RHG, SEQ ID RHH, SEQ ID RHI, SEQ ID RHJ, SEQ ID RHL, SEQ ID RHM, то есть, SEQ ID NO:13-25;
и вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и которая по меньшей мере на 95% идентична SEQ ID NO:26, RKA, где антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
Такие антитела и связывающие фрагменты согласно трем предыдущим параграфам также предусматриваются в форме, когда положение 9 тяжелой цепи занято P, положение 21 занято P, положение 27 занято Y, положение 28 занято I, положение 30 занято T, положение 38 занято K, положение 48 занято I, положение 67 занято K, положение 68 занято A, положение 70 занято L, и/или положение 95 занято F. В одном из вариантов осуществления положение 5 легкой цепи занято S. В некоторых вариантах осуществления по сути только два из этих 11 положений заняты. В некоторых вариантах осуществления по сути только три из этих 11 положений заняты. В некоторых вариантах осуществления по сути только четыре из этих 11 положений заняты. В некоторых вариантах осуществления по сути только пять из этих 11 положений заняты. В некоторых вариантах осуществления по сути только шесть из этих 11 положений заняты. В некоторых вариантах осуществления по сути только семь из этих 11 положений заняты. В некоторых вариантах осуществления по сути только восемь из этих 11 положений заняты. В некоторых вариантах осуществления по сути только девять из этих 11 положений заняты. В некоторых вариантах осуществления по сути только десять из этих 11 положений заняты. В некоторых вариантах осуществления по сути все 11 из этих 11 положений заняты. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Также раскрыто антитело, содержащее:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3, и которая по меньшей мере на 85% идентична любой из SEQ ID NO: RHA, SEQ ID RHB, SEQ ID RHC, SEQ ID RHD, SEQ ID RHE, SEQ ID RHF, SEQ ID RHG, SEQ ID RHH, SEQ ID RHI, SEQ ID RHJ, SEQ ID RHL, SEQ ID RHM, то есть, SEQ ID NO:13-25;
и зрелую вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и которая по меньшей мере на 85% идентична SEQ ID NO:27, RKB, где антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
Также раскрыто антитело, содержащее:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3, и которая по меньшей мере на 90% идентична любой из SEQ ID NO: RHA, SEQ ID RHB, SEQ ID RHC, SEQ ID RHD, SEQ ID RHE, SEQ ID RHF, SEQ ID RHG, SEQ ID RHH, SEQ ID RHI, SEQ ID RHJ, SEQ ID RHL, SEQ ID RHM, то есть, SEQ ID NO:13-25;
и вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и которая по меньшей мере на 90% идентична SEQ ID NO:27, RKB, где антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
Также раскрыто антитело, содержащее:
вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2, 3, и которая по меньшей мере на 95% идентична любой из SEQ ID NO: RHA, SEQ ID RHB, SEQ ID RHC, SEQ ID RHD, SEQ ID RHE, SEQ ID RHF, SEQ ID RHG, SEQ ID RHH, SEQ ID RHI, SEQ ID RHJ, SEQ ID RHL, SEQ ID RHM, то есть, SEQ ID NO:13-25;
и вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5, 6, соответственно, и которая по меньшей мере на 95% идентична SEQ ID NO:27, RKB, где антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
Такие антитела и связывающие фрагменты согласно трем предыдущим параграфам также предусматриваются в форме, когда положение 9 тяжелой цепи занято P, положение 21 занято P, положение 27 занято Y, положение 28 занято I, положение 30 занято T, положение 38 занято K, положение 48 занято I, положение 67 занято K, положение 68 занято A, положение 70 занято L, и/или положение 95 занято F. В одном из вариантов осуществления положение 5 легкой цепи занято S. В некоторых вариантах осуществления по сути только два из этих 11 положений заняты. В некоторых вариантах осуществления по сути только три из этих 11 положений заняты. В некоторых вариантах осуществления по сути только четыре из этих 11 положений заняты. В некоторых вариантах осуществления по сути только пять из этих 11 положений заняты. В некоторых вариантах осуществления по сути только шесть из этих 11 положений заняты. В некоторых вариантах осуществления по сути только семь из этих 11 положений заняты. В некоторых вариантах осуществления по сути только восемь из этих 11 положений заняты. В некоторых вариантах осуществления по сути только девять из этих 11 положений заняты. В некоторых вариантах осуществления по сути только десять из этих 11 положений заняты. В некоторых вариантах осуществления по сути все 11 из этих 11 положений заняты. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В настоящем описании также представлено и раскрыто антитело всех предыдущих параграфов этого раздела ("Сущность изобретения"), где указанное антитело или связывающий фрагмент представляет собой Fab, Fab', F(ab')2, Fd, scFv, (scFv)2 или scFv-Fc. В некоторых вариантах осуществления такое антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент представляет собой антитело IgG1, IgG2, IgG3, или IgG4. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В настоящем описании также представлено и раскрыто антитело всех предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент представляет собой антитело IgG1. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент является гликозилированным. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В настоящем описании также представлено и раскрыто антитело всех предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент связывается с тау 151-391/4R с аффинностью (KD), равной по меньшей мере 5×10-7. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным. В некоторых вариантах осуществления аффинность связывания измеряют с помощью SPR. В некоторых вариантах аффинность связывания измеряют с помощью ELISA.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент связывается с тау по меньшей мере на 80% с той же аффинностью связывания, по существу с той же аффинностью связывания или с большей аффинностью связывания, чем антитело DC8E8, секретируемое гибридомой PTA-11994, депонированной в Американской коллекции типовых культур. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным. В некоторых вариантах осуществления аффинность связывания измеряют с помощью SPR. В некоторых вариантах аффинность связывания измеряют с помощью ELISA.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело конкурирует за связывание с тау-белком по меньшей мере на одном и том же эпитопе с антителом DC8E8, секретируемым гибридомой PTA-11994, депонированной в Американской коллекции типовых культур. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело получают рекомбинантным путем. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами. В некоторых вариантах осуществления антитело является химерным. В некоторых вариантах осуществления антитело является гуманизированным.
В некоторых вариантах осуществления антитело и связывающий фрагмент предыдущих четырех параграфов также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент первых четырех из предыдущих пяти абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент первых четырех из предыдущих шести абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент первых четырех из предыдущих семи абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент, первых четырех из предыдущих восьми абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент первых четырех из предыдущих девяти абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент первых четырех из предыдущих десяти абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент первых четырех из предыдущих одиннадцати абзацев также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело получают рекомбинантным путем в линии клеток яичника китайского хомяка (CHO). В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент содержит Fс-область, в которой была изменена эффекторная функция, время полураспада, протеолиз и гликозилирование. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих двух абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело или связывающий фрагмент модифицирован с целью модуляции функциональной характеристики, выбранной из группы, состоящей из антитело-зависимой клеточной цитотоксичности, комплемент-зависимой цитотоксичности, времени полураспада в сыворотке, биораспределения и связывания с Fc-рецепторами. В некоторых вариантах осуществления антитело связывается с одним или двумя эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150). В некоторых вариантах осуществления антитело связывается со всеми тремя эпитопами.
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В настоящем описании также представлено и раскрыто антитело предыдущих параграфов этого раздела, где указанное антитело обладает термостабильностью при температуре, равной или выше 69°C.
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В другом аспекте настоящего изобретения раскрыта композиция, содержащая одно из антител и/или связывающих фрагментов по настоящему изобретению или еще один компонент.
В другом аспекте настоящего изобретения раскрыта фармацевтическая композиция, содержащая антитело и/или связывающий фрагмент, как описано в этом разделе, и фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или стабилизатор.
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих двух абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
Также раскрыт дополнительный вариант любой вышеуказанной композиции, где композиция содержит лиофилизированный порошок антитела или связывающего фрагмента.
Также раскрыта любая их вышеуказанных композиций, где композиция составлена для инфузии или подкожного введения.
Также раскрыты любые из этих композиций, дополнительно содержащие второе терапевтическое средство (также называются комбинациями).
Ниже приведены четырнадцать примеров дополнительных композиций вариантов осуществления предыдущих трех абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых из этих композиций терапевтическое средство и антитело или связывающий фрагмент химически конъюгированы.
В некоторых из этих композиций второе терапевтическое средство может использоваться для профилактики или лечения AD.
Также раскрыто, что второе терапевтическое средство может быть выбрано из, например, бета-амилоидных пептидов (например, N-концевые бета-амилоидные пептиды), которые могут быть конъюгированы или нет с другими соединениями, таких как мутированный дифтерийный токсин; других антител против тау-белка, антител против бета-амилоида, таких как бапинезумаб, соланезумаб, гантенерумаб, кренезумаб и иммуноглобулин IVIG, других иммунологических лекарственных средств, нацеливающихся на олигомеры Aбета, соединений, предотвращающих гиперфосфорилирование тау-белка, соединений, предотвращающих олигомеризацию и агрегацию тау-белка или деполимеризацию тау-олигомеров (например, метилтиониний, рембер или LMTX) и других активных и пассивных иммунологических лекарственных средств, нацеливающихся на тау-агрегаты; и любых их фармацевтически приемлемых солей.
Также предполагается, что второе терапевтическое средство может быть выбрано из ингибиторов агрегации бета-амилоида (например,трамипросат), ингибиторов гамма-секретазы (например, семагацестат) и модуляторов гамма-секретазы (таренфлурбил); и их любой фармацевтически приемлемой соли.
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих четырех абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых случаях второе терапевтическое средство выбрано из ингибиторов ацетилхолинэстеразы (например, донепезил, ривастигмин, галантамин, такрин, пищевые добавки), антагонистов рецептора N-метил-D-аспартата (NMDA) (например, мемантин), ингибиторов репарации ДНК (например, пирензепин или его метаболит), хелаторов переходных металлов, факторов роста, гормонов, нестероидных противовоспалительных лекарственных средств (NSAID), антиоксидантов, средств, снижающих липиды, селективных ингибиторов фосфодиэстеразы, ингибиторов агрегации тау-белка, ингибиторов протеинкиназы, ингибиторов антимитохондриальной дисфункции, нейротрофинов, ингибиторов белков теплового шока, ингибиторов, связанных с липопротеином фосфолипазы А2, мемантина, антиапоптотического соединения, хелатора металла, ингибитора восстановления ДНК, 3-амино-1-пропансульфокислоты (3APS), 1,3-пропандисульфоната (1,3PDS), активатора секретазы, ингибитора бета-секретазы, ингибитора гамма-секретазы, бета-амилоидного пептида, бета-амилоидного антитела, тау-пептида, нейротрансмиттера, средства, разрушающего структуру бета-листа, противовоспалительной молекулы; и их любых фармацевтически приемлемых солей.
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
Также раскрыты композиции, в которых второе терапевтическое средство выбрано из соединений, описанных в WO 2004/058258 (см. в частности стр.16 и 17), включая мишень-нацеленные терапевтические средства (стр.36-39), алкансульфоновые и алканолсульфуровые кислоты (стр.39-51), ингибиторы холинэстеразы (стр.51-56), антагонисты рецептора NMDA (стр.56-58), эстрогены (стр.58-59), нестероидные противовоспалительные препараты (стр.60-61), антиоксиданты (стр.61-62), агонисты рецептора, активируемого пролифераторами пероксисом (PPAR) (стр.63-67), средства, снижающие холестерин (стр.68-75); ингибиторы амилоида (стр.75-77), ингибиторы образования амилоида (стр.77-78), хелаторы металлов (стр.78-79), антипсихотические препараты и антидепрессанты (стр.80-82), пищевые добавки (стр.83-89) и соединения, повышающие доступность биологически активных веществ в мозге (см. стр.89-93) и пролекарства (стр.93 и 94); и их любые фармацевтически приемлемые соли.
Также раскрыты композиции, в которых второе терапевтическое средство выбрано из соединений, предотвращающих олигомеризацию и агрегацию тау-белка, и соединений, которые деполимеризуют тау-олигомеры (например, метилтиониний, рембер или LMTX).
Ниже приведены четырнадцать примеров вариантов осуществления предыдущих двух абзацев:
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В другом аспекте в описании раскрыт диагностический реагент, содержащий антитело и/или связывающий фрагмент, описанные в настоящем документе, и фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество или стабилизатор.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления этих диагностических реагентов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В еще одном аспекте настоящее изобретение относится к иммуноконъюгату формулы (A)-(L)-(C), где: (A) представляет собой антитело или его связывающий фрагмент по настоящему изобретению; (L) представляет собой линкер; и (C) представляет собой агент; и где указанный линкер (L) соединяет (A) и (C). В некоторых случаях (C) представляет собой терапевтическое средство, визуализирующий агент, детектируемый агентом или диагностический агент. В некоторых случаях (C) представляет собой терапевтическое средство.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых других вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG1.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:26, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых других вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG1.
В некоторых вариантах осуществления этих иммуноконъюгатов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB, и константная область представляет собой изотип IgG4.
В изобретении раскрыты молекулы нуклеиновой кислоты (РНК и ДНК), кодирующие любое антитело и тау-связывающие фрагменты, описанные выше. В одном из вариантов осуществления такие молекулы нуклеиновых кислот содержат одну или несколько последовательностей нуклеиновых кислот, выбранных из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 85% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 90% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 95% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 96% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 97% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 98% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140. В других вариантах осуществления такие молекулы нуклеиновой кислоты содержат одну или более последовательностей нуклеиновых кислот, выбранных из последовательностей, которые по крайней мере на 99% идентичны любой из SEQ ID NO:96-124, 141-142 и 127-140.
В одном из вариантов осуществления в описании раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична любой аминокислотной последовательности от SEQ ID NO:RHA до SEQ ID NO:RHM, то есть, SEQ ID NO:13-25. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1. В других вариантах осуществления антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG4.
Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:26, RKA, или SEQ ID NO:27, RKB. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область каппа.
В одном из вариантов осуществления в описании раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична любой аминокислотной последовательности от SEQ ID NO:RHA до SEQ ID NO:RHM, то есть, SEQ ID NO:13-25. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1. В других вариантах осуществления антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG4.
Молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:26, RKA, или SEQ ID NO:27, RKB. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область каппа.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:14, RHB. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:16, RHD. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:17, RHE. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:25, RHM. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:14, RHB. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:16, RHD. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:17, RHE. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:25, RHM. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
В некоторых вариантах осуществления любая молекула нуклеиновой кислоты, только что описанная в этом разделе, является такой, что антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область IgG1.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:26, RKA. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область каппа.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:RKB. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область каппа.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:26, RKA. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область каппа.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая идентична аминокислотной последовательности SEQ ID NO:RKB. В каждом из этих вариантов осуществления также может быть случай, когда антитело или его фрагмент содержит тяжелую цепь, дополнительно содержащую константную область каппа.
В некоторых вариантах осуществления последовательность нуклеиновой кислоты кодирует HCVR с любой из SEQ ID NO:13-25 (RHA-RHM).
В еще одном варианте осуществления последовательность нуклеиновой кислоты кодирует HCVR с SEQ ID NO:14, RHB.
В одном из вариантов осуществления этих нуклеиновых кислот последовательность нуклеиновой кислоты кодирует HCVR с SEQ ID NO:16, RHD
В одном из вариантов осуществления этих нуклеиновых кислот последовательность нуклеиновой кислоты кодирует HCVR с SEQ ID NO:17, RHE.
В одном из вариантов осуществления этих нуклеиновых кислот последовательность нуклеиновой кислоты кодирует HCVR с SEQ ID NO:25, RHM.
В одном из вариантов осуществления этих нуклеиновых кислот последовательность нуклеиновой кислоты кодирует LCVR с любой из SEQ ID NO:26, RKA, и SEQ ID NO:27, RKB.
Также раскрыта последовательность нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO: 71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична любой аминокислотной последовательности от SEQ ID NO:RHA до SEQ ID NO:RHM (то есть, SEQ ID NO:13-25) и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью любой из SEQ ID NO:RHA до SEQ ID NO:RHM (то есть, SEQ ID NO:96-108), где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта последовательность нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO: 71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:14, RHB, и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью SEQ ID NO:97, RHB, где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта последовательность нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO: 71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:16, RHD, и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью SEQ ID NO:99, RHD, где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта последовательность нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO: 71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:17, RHE, и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью SEQ ID NO:100, RHE, где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта последовательность нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO: 71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности от SEQ ID NO:25, RHM, и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью SEQ ID NO:108, RHM, где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:26, RKA; и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью SEQ ID NO:109, RKA, где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:14, RKB; и, кроме того, такая последовательность нуклеиновой кислоты содержит нуклеотидную последовательность, которая гибридизуется в жестких условиях с комплементарной цепью SEQ ID NO:110, RKB, где жесткие условия гибридизации включают гибридизацию в 5× SSPE, 1% SDS, 1× раствор Денхардта при 65°C и промывку в 2× SSC, 1% SDS и затем 0,2× SSC при 65°C.
Также раскрыта популяция молекул нуклеиновых кислот, содержащая первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где:
первая молекула нуклеиновой кислоты представляет собой молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи (HCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3, и где указанная HCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична любой аминокислотной последовательности от SEQ ID NO:RHA до SEQ ID NO:RHM (то есть, SEQ ID NO:13-25);
и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6.
Также раскрыта популяция молекул нуклеиновых кислот, содержащая первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где:
молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:26, RKA;
и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3.
Также раскрыта популяция молекул нуклеиновых кислот, содержащая первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где:
молекула нуклеиновой кислоты, содержащая нуклеотидную последовательность, кодирующую вариабельную область легкой цепи (LCVR) или ее тау-связывающий фрагмент антитела против тау-белка, где указанная LCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека X72449 (SEQ ID NO:65), (ii) CDR1 LCVR, содержащую аминокислотную последовательность SEQ ID NO:4, (iii) LCVR CDR2, содержащую аминокислотную последовательность SEQ ID NO:5, и (iv) CDR3 LCVR, содержащую аминокислотную последовательность SEQ ID NO:6, и где указанная LCVR или ее фрагмент содержит аминокислотную последовательность, которая по меньшей мере на 98% идентична аминокислотной последовательности SEQ ID NO:27, RKB;
и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка, где указанная HCVR или ее фрагмент содержит: (i) каркасную область, полученную из иммуноглобулина человека M65092 (SEQ ID NO:71), (ii) CDR1 HCVR, содержащую аминокислотную последовательность SEQ ID NO:1, (iii) CDR2 HCVR, содержащую аминокислотную последовательность SEQ ID NO:2, и (iv) CDR3 HCVR, содержащую аминокислотную последовательность SEQ ID NO:3.
Также раскрыты молекулы нуклеиновых кислот, кодирующие любые вариабельные области тяжелой цепи RHA-RHM (SEQ ID NO:13-25), где эти последовательности нуклеиновых кислот выбраны из любой SEQ ID NO:28-40, соответственно, или 43-55, соответственно. Любая из этих молекул нуклеиновых кислот может быть комбинирована с молекулами нуклеиновых кислот следующего абзаца.
Также раскрыты молекулы нуклеиновых кислот, кодирующие любую легкую цепь RKA или RKB, где молекулы нуклеиновых кислот кодируют последовательности, выбранные из SEQ ID NO:57 и 58, соответственно.
Настоящее изобретение включает все возможные комбинации нуклеиновых кислот, раскрытых выше, которые кодируют аминокислоты или тау-связывающий фрагмент, вариабельную область легкой цепи, полноразмерную легкую цепь, вариабельную область тяжелой цепи, полноразмерную тяжелую цепь, как раскрыто в настоящем документе.
В некоторых примерах таких популяций нуклеиновых кислот они содержат первую молекулу нуклеиновой кислоты вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:14, RHB, и где вторую молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:26, RKA.
В некоторых примерах таких популяций они включают содержат первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:16, RHD, и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:26, RKA.
В некоторых примерах таких популяций они включают содержат первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:17, RHE, и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:26, RKA.
В некоторых примерах таких популяций они включают содержат первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:25, RHM, и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:26, RKA.
В некоторых примерах таких популяций они включают содержат первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:16, RHD, и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:27, RKB.
В некоторых примерах таких популяций они включают содержат первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:17, RHE, и где вторая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:27, RKB.
В некоторых примерах таких популяций они включают содержат первую молекулу нуклеиновой кислоты и вторую молекулу нуклеиновой кислоты, где первая молекула нуклеиновой кислоты содержит нуклеотидную последовательность, кодирующую HCVR или ее тау-связывающий фрагмент антитела против тау-белка с SEQ ID NO:14, RKB, и где вторую молекулу нуклеиновой кислоты, содержащую нуклеотидную последовательность, кодирующую LCVR или ее тау-связывающий фрагмент с SEQ ID NO:27, RKB.
Также раскрыт набор векторов, где каждый вектор содержит нуклеиновую кислоту, кодирующую тяжелую цепь антитела или связывающего фрагмента, как описано в вышеуказанных абзацах настоящего раздела. Раскрыт еще один набор векторов, содержащих нуклеиновую кислоту, кодирующую легкую цепь антитела или связывающего фрагмента, как описано в любому из вышеуказанных абзацев настоящего раздела. Раскрыт еще один набор векторов, содержащих нуклеиновую кислоту, кодирующую легкую цепь антитела или связывающего фрагмента, как описано в любому из вышеуказанных абзацев настоящего раздела, и тяжелую цепь антитела или связывающего фрагмента, как описано в предыдущих абзацах настоящего раздела.
Также раскрыты клетки-хозяева, содержащие любой из этих векторов. В некоторых вариантах осуществления клетка-хозяин является прокариотической. В других вариантах осуществления клетка-хозяин является эукариотической. Рассматривается также клетка-хозяин, содержащая любую популяцию молекул нуклеиновых кислот, описанных выше.
В некоторых вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих клеток-хозяев антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Любая из вышеуказанных раскрытых нуклеиновых кислот, антител, векторов и клеток-хозяев и их соответствующих композиций предусмотрены для применения в качестве лекарственного средства:
для профилактики или лечение AD или другой таупатии;
для лечения болезни Альцгеймера или другой таупатии у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии;
для замедления прогрессирования AD или другой таупатии у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии;
для улучшения симптомов AD или связанных с ней симптомов у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии; и
для снижения риска или задержки наступления AD или другой таупатии у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии.
Еще одним аспектом настоящего раскрытия является способ получения антитела или его тау-связывающего фрагмента, который связывается с тау-белком человека, включающий культивирование любой клетки-хозяина, только что описанной, для экспрессии нуклеиновой кислоты и, таким образом, получения антитела или его тау-связывающего фрагмента.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Еще в одном аспект раскрыт способ лечения болезни Альцгеймера или другой таупатии у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, включающий введение индивиду терапевтически эффективного количества композиции, содержащей любое из антител или связывающих фрагментов, описанных в этом разделе.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Еще в одном аспекте раскрыт способ усиления клиренса тау-агрегатов из мозга индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, включающий введение индивиду терапевтически эффективного количества композиции, содержащей любое из антител или связывающих фрагментов, описанных в этом разделе.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Еще в одном аспект раскрыт способ замедления прогрессирования AD или другой таупатии у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, включающий введение индивиду терапевтически эффективного количества композиции, содержащей любое из антител или связывающих фрагментов, описанных в этом разделе.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Еще в одном аспекте раскрыт способ улучшения симптомов AD или связанных с ней симптомов у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, включающий введение индивиду терапевтически эффективного количества композиции, содержащей любое из антител или связывающих фрагментов, описанных в этом разделе.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Еще в одном аспекте раскрыт способ лечения, профилактики или обратного развития когнитивного расстройства у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, включающий введение индивиду терапевтически эффективного количества композиции, содержащей любое из антител или связывающих фрагментов, описанных в этом разделе.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Еще в одном аспекте раскрыт способ уменьшения риска или замедления наступления AD или другой таутопатии у индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, включающий введение индивиду терапевтически эффективного количества композиции, содержащей любое из антител или связывающих фрагментов, описанных в этом разделе.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых вариантах осуществления любую из этих композиций, антител и/или связывающих фрагментов вводят посредством инъекции. В других вариантах осуществления любую из этих композиций, антител и/или связывающих фрагментов вводят посредством внутривенной инфузии.
Настоящее изобретение также предусматривает варианты осуществления, когда любую из этих композиций, антител и/или связывающих фрагментов вводят указанному индивиду в дозе антитела или связывающего фрагмента от 0,1 мг/кг массы тела до 20 мг/кг массы тела и с частотой от еженедельного введения до введения раз в месяц, таким образом, осуществляя лечение индивида. В предпочтительном варианте осуществления антитело или связывающий фрагмент вводят в дозе от 0,1 мг/кг массы тела до 10 мг/кг массы тела. В некоторых предпочтительных вариантах осуществления антитело или связывающий фрагмент вводят в течение по меньшей мере трех месяцев, предпочтительно по меньшей мере шести месяцев, по меньшей мере двенадцати месяцев, возможно, в течение двадцати четырех месяцев, в любой из указанных ранее доз. В еще одном варианте осуществления любую из этих композиций, антител и/или связывающих фрагментов вводят указанному индивиду в дозе антитела или связывающего фрагмента от 0,1 мг/кг массы тела до 10 мг/кг массы тела и с частотой от еженедельного введения до введения раз в месяц, предпочтительно, каждые две недели, таким образом, осуществляя лечение индивида. В еще одном варианте осуществления любую из этих композиций, антител и/или связывающих фрагментов вводят указанному индивиду в дозе антитела или связывающего фрагмента от 0,01 мг/кг массы тела до 100 мг/кг массы тела и с частотой от еженедельного введения до введения раз в месяц, таким образом, осуществляя лечение индивида.
В некоторых вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В другом аспекте любой терапевтический способ, только что описанный в этом разделе, дополнительно включает мониторинг прогресса лечения у индивида с помощью по крайней мере одного типа оценки, выбранного из группы, состоящей из краткой шкалы оценки психического статуса (MMSE), шкалы оценки когнитивных функций при болезни Альцгеймера (ADAS-COG), шкалы оценки состояния пациента на основании впечатления врача и ухаживающих за пациентами лиц (CIBI), набора неврологических тестов (NTB), шкалы инвалидизации при деменции (DAD), шкалы клинической оценки деменции по "сумме боксов" (CDR-SOB), опросника для оценки нейропсихиатрического состояния (NPI), сканирования позитронно-эмиссионной томографией (PET-изображение), и сканирования с помощью магнитного резонанса (MRI). В одном из вариантов осуществления типом оценки является набор неврологических тестов (NTB). В другом варианте осуществления типом оценки является краткая шкала оценки психического статуса (MMSE).
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых вариантах осуществления практика любого из этих способов дополнительно включает введение указанному индивиду, одновременно или последовательно, эффективного количества, по меньшей мере одного дополнительного терапевтического средства.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Например, в некоторых из этих вариантов осуществления дополнительное терапевтическое средство выбрано из группы, состоящей из антиапоптотического соединения, хелатора металла, ингибитора репарации ДНК, 3-амино-1-пропансульфоновой кислоты (3APS), 1,3-пропандисульфоната (1,3PDS), активатора секретазы, ингибитора бета-секретазы, ингибитора гамма-секретазы, бета-амилоидного пептида, антитела против бета-амилоида, нейромедиатора, средства, разрушающего структуру бета-листа, противовоспалительной молекулы и ингибитора холинэстеразы; и любой их фармацевтически приемлемой соли.
В некоторых других из этих вариантов осуществления ингибитором холинэстеразы является такрин, ривастигмин, донепезил, галантамин или пищевая добавка; и их любые фармацевтически приемлемые соли.
В некоторых вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В еще некоторых других этих вариантах осуществления дополнительное терапевтическое средство выбрано из бета-амилоидных пептидов (например, N-концевые бета-амилоидные пептиды), которые могут быть конъюгированы или нет с другими соединениями, таких как мутированный дифтерийный токсин; антител против бета-амилоида, таких как бапинезумаб, соланезумаб, гантенерумаб, кренезумаб, понезумаб и иммуноглобулин IVIG, других иммунологических лекарственных средств, нацеливающихся на олигомеры A-бета, соединений, предотвращающих гиперфосфорилирование тау-белка, соединения, предотвращающего олигомеризацию и агрегацию тау-белка или стимулирующего деполимеризацию тау-олигомеров (например, метилтиониний, рембер или LMTX) и других активных и пассивных иммунологических лекарственных средств, нацеливающихся на патологические формы тау-белка (например, агрегаты); и любых их фармацевтически приемлемых солей.
В некоторых из этих других вариантов осуществления дополнительное терапевтическое средство выбрано из ингибиторов агрегации амилоидного бета (например, трамипросат), ингибиторов гамма-секретазы (например, семагацестат) и модуляторов гамма-секретазы (таренфлурбил); и их любой фармацевтически приемлемой соли.
В некоторых вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых из этих вариантов осуществления дополнительное терапевтическое средство выбрано из ингибиторов ацетилхолинэстеразы (например, донепезил, ривастигмин, галантамин, такрин, пищевые добавки), антагонистов рецептора N-метил-D-аспартата (NMDA) (например, мемантин), ингибиторов восстановления ДНК (например, пирензепин или его метаболит), хелаторов переходных металлов, факторов роста, гормонов, нестероидных противовоспалительных лекарственных средств (NSAID), антиоксидантов, средств, уменьшающих уровень липидов, селективных ингибиторов фосфодиэстеразы, ингибиторов агрегации тау-белка, ингибиторов протеинкиназы, лекарственных средств ингибиторов митохондриальной дисфункции, нейротрофинов, ингибиторов белков теплового шока, ингибиторов липопротеин-связанной фосфолипазы A2, мемантина, антиапоптотического соединения, хелатора металла, ингибитора репарации ДНК, 3-амино-1-пропансульфоновой кислоты (3APS), 1,3-пропандисульфоната (1,3PDS), активатора секретазы, ингибитора бета-секретазы, ингибитора гамма-секретазы, бета-амилоидного пептида, бета-амилоидного антитела, нейротрансмиттера, средства, разрушающего структуру бета-листа, противовоспалительной молекулы; и их любых фармацевтически приемлемых солей.
В некоторых вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых из этих вариантов осуществления дополнительное терапевтическое средство выбрано из ингибиторов BACE; мускариновых антагонистов; ингибиторов холинэстеразы; ингибиторов гамма-секретазы; модуляторов гамма-секретазы; ингибиторов HMG-CoA-редуктазы; нестероидных противовоспалительных средств; антагонистов рецептора N-метил-D-аспартата; антител против амилоида; витамина Е; агонистов никотинацетилхолинового рецептора; обратных агонистов рецептора CB1 или антагонистов рецептора CB1; антибиотика; стимуляторов секреции гормона роста; антагонистов гистамина Н3; агонистов АМРА; ингибиторов PDE4; обратных агонистов GABAA; ингибиторов амилоидной агрегации; ингибиторов гликогенсинтаза-киназа бета; промоторов активности альфа секретазы; ингибиторов PDE-10, ингибиторов абсорбции холестерина, и их любых фармацевтически приемлемых солей.
В некоторых из этих вариантов осуществления дополнительное терапевтическое средство представляет собой второе антитело. В других вариантах осуществления второе антитело выбрано из бапинезумаба, соланезумаба, гантенерумаба, кренизумаба, понезумаба и иммуноглобулина IVIG.
В некоторых вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этих двух способов антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также включает способ оценки индивида, у которого предполагают или который предрасположен к болезни Альцгеймера или другой таупатии, где способ включает стадию детекции связывания любого антитела или тау-связывающего фрагмента, описанного в этом разделе, с компонентом биологического образца индивида, где детекция связывания с биологическим образом указывает на болезнь Альцгеймера или другую таупатию у индивида. В некоторых из этих вариантов биологический образец представляет собой материал биопсии, CSF, кровь, сыворотку или образец плазмы.
В некоторых вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
В некоторых других вариантах осуществления этого способа антитело и связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также предусматривает тот факт, что терапевтические способы, описанные в предыдущих абзацах, могут быть осуществлены с помощью антитела или тау-связывающего фрагмента, где антитело или связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:14, RHB, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также предусматривает тот факт, что терапевтические способы, описанные в предыдущих абзацах, могут быть осуществлены с антителом или тау-связывающим фрагментом, где антитело или связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также предусматривает тот факт, что терапевтические способы, описанные в предыдущих абзацах, могут быть осуществлены с помощью антитела или тау-связывающего фрагмента, где антитело или связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHE, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также предусматривает тот факт, что терапевтические способы, описанные в предыдущих абзацах, могут быть осуществлены с помощью антитела или тау-связывающего фрагмента, где антитело или связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:25, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:26, RKA. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также предусматривает тот факт, что терапевтические способы, описанные в предыдущих абзацах, могут быть осуществлены с помощью антитела или тау-связывающего фрагмента, где антитело или связывающий фрагмент также представляют собой антитело и связывающий фрагмент, в котором последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:16, RHD, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
Изобретение также предусматривает тот факт, что терапевтические способы, описанные в предыдущих абзацах, могут быть осуществлены с антителом или тау-связывающим фрагментом, где антитело или связывающий фрагмент также представляют собой антитело и связывающий фрагмент, где последовательность вариабельной области тяжелой цепи представляет собой SEQ ID NO:17, RHM, и последовательность вариабельной области легкой цепи представляет собой SEQ ID NO:27, RKB. Необязательно, антитело и связывающий фрагмент представляют собой изотип IgG4 или IgG1.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигура 1:Схема шести изоформ тау-белка человека
Фигура 2: Схематическая функциональная карта тау-белка человека (2N4R); описывает "VQIINK» и «VQIVYK» как SEQ ID NO:147 и 146, соответственно.
Фигура 3: Белок (SEQ ID NO:8) и последовательность ДНК (SEQ ID NO:91) вариабельной области легкой цепи каппа DC8E8
Фигура 4: Белок (SEQ ID NO:7) и последовательность ДНК (SEQ ID NO:90) вариабельной области тяжелой цепи DC8E8
Фигура 5: Анализ легкой цепи каппа DC8E8 зародышевой линии (SEQ ID NO:167 и 168, соответственно, по порядку)
Фигура 6: Анализ тяжелой цепи DC8E8 зародышевой линии (SEQ ID NO:66 и 169, соответственно, по порядку)
Фигура 7: Связывание химерного и мышиного DC8E8 с тау 151-391/4R
Фигура 8: Стратегия гуманизации тяжелой цепи DC8E8.Структурно важные остатки (пролин, цистеин и аспарагин) выделены жирным шрифтом и курсивом. Полужирные подчеркнутые остатки указывают обратную трансляцию в остаток мыши. Области CDR представлены строчными буквами и обозначены точками в заголовке таблицы. Остатки в пределах 4Å от CDR указаны звездочками в заголовке таблицы. На фигуре 8 описаны SEQ ID NO:7, 71 и 13-25, соответственно, по порядку. Следует обратить внимание, что SEQ ID NO:71 (номер доступа M65092 в базе данных IMGT) показан без лидерного пептида MDWTWRFLFVVAAVTGVQS (SEQ ID NO:174).
Фигура 9: Стратегия гуманизации легкой цепи каппа DC8E8.Структурно важные остатки (пролин, цистеин и аспарагин) выделены жирным шрифтом и курсивом. Полужирные подчеркнутые остатки указывают обратную трансляцию в остаток мыши. Области CDR представлены строчными буквами и обозначены точками в заголовке таблицы. Остатки в пределах 4Å от CDR указаны звездочками в заголовке таблицы. На фигуре 9 раскрыты SEQ ID NO:8, 65 и 26-27, соответственно, по порядку. Следует обратить внимание, что SEQ ID NO:65 (номер доступа X72449 в базе данных IMGT) показан без лидерного пептида QLLGLLMLWVSGSSG (SEQ ID NO:175).
Фигура 10: Связывание гуманизированного и химерного DC8E8 с тау 151-391/4R.Сравнение связывания антитела антителами, кодируемыми комбинациями RHA или RHB DC8E8, экспрессированными вместе с RKA DC8E8 или RKB DC8E8, с полностью химерным антителом.
Фигура 11: Связывание гуманизированного и химерного DC8E8 с тау 151-391/4R: Варианты RKA.
Фигура 12: Связывание гуманизированного и химерного DC8E8 с тау 151-391/4R: Варианты RKB.
Фигура 13: Связывание гуманизированного и химерного DC8E8 с тау 151-391/4R: Варианты Vкаппа (с химерной легкой цепью).
Фигура 14: Связывание гуманизированного и химерного DC8E8 с тау 151-391/4R: Варианты RHM.
Фигура 15: Термическая стабильность гуманизированных антител-кандидатов DC8E8: Очищенные антитела нагревали в течение 10 мин при указанной температуре, а затем охлаждали до 4°C перед проведением тау-связывающего анализа ELISA.
Фигура 16: Анализ термического сдвига очищенных гуманизированных антител-кандидатов DC8E8: Определение Tm очищенных антител-кандидатов и сравнение с химерным и мышиным DC8E8.
Фигура 17: Кинетика связывания антител DC8E8, проанализированных с помощью поверхностного плазмонного резонанса: Определение KD: DC8E8 мыши.
Фигура 18: Кинетика связывания антител DC8E8, проанализированных с помощью поверхностного плазмонного резонанса: Определение KD: Химерное DC8E8
Фигура 19: Кинетика связывания антител DC8E8, проанализированных с помощью поверхностного плазмонного резонанса: Определение KD: Гуманизированное RHD/RKA DC8E8 (AX004)
Фигура 20: Кинетика связывания антител DC8E8, проанализированных с помощью поверхностного плазмонного резонанса: Определение KD: гуманизированное RHE/RKA DC8E8 (AX005)
Фигура 21: Кинетика связывания антител DC8E8, проанализированных с помощью поверхностного плазмонного резонанса: Определение KD: Гуманизированное RHD/RKB DC8E8 (AX016)
Фигура 22: Кинетика связывания антител DC8E8, проанализированных с помощью поверхностного плазмонного резонанса: Определение KD: Гуманизированное RHЕ/RKB DC8E8 (AX017);
Фигура 23: Краткое изложение результатов анализа Biacore
Фигура 24: Анализ агрегации полностью гуманизированных антител-кандидатов:A.AX004 (DA); B.AX005 (EA); C.AX016 (DB); D.AX017 (EB).
Фигура 25: Очищенные гуманизированные антитела-кандидаты DC8E8, оцененные на растворимость: Профиль растворимости во время концентрирования.
Фигура 26: Очищенные гуманизированные антитела-кандидаты DC8E8, оцененные на растворимость: Профиль растворимости во время концентрирования: Связывающая активность после концентрирования.
Фигура 27: Анализ стресса при заморозке/оттаивании гуманизированных антител-кандидатов.
Фигура 28: Анализ стресса при нагревании полностью гуманизированных антител-кандидатов: A.AX004 (DA); B.AX005 (EA); C.AX0016 (DB); D.AX017 (EB).
Фигура 29: Связывание (А) химерного DC8E8 и (B) DC8E8 мыши с патологическим беспорядочным усеченным тау 151-391/4R и физиологическим тау 2N4R, как определено с помощью ELISA. (C) значения EC50 химерных и мышиных антител для проанализированных тау-белков.
Фигура 30: Ассоциативное равновесие констант связывания мышиного и химерного DC8E8 с патологическим беспорядочным укороченным тау 151-391/4R и полноразмерным физиологическим тау 2N4R определяли при помощи поверхностного плазмонного резонанса.
Фигура 31: Связывание (А) химерного DC8E8 и (B) мышиного DC8E8 с тау-пептидами, полученными из повторяющихся доменов тау-белка, как определено с помощью ELISA.(C) значения EC50 химерных и мышиных антител для проанализированных тау-пептидов.
Фигура 32: Химерное DC8E8 ингибирует патологическое взаимодействие тау-тау в анализе фибриллизации тау-белка in vitro.Патологический беспорядочный усеченный тау-белок 151-391/4R индуцировали гепарином для стимуляции конформационного изменения и фибрилляции, степень которых была измерена флуоресценцией с помощью Thioflavin T; химерный DC8E8 тестировали на способность предотвращать патологическое конформационное изменение и тау-тау взаимодействие.
Фигура 33: Связывание гуманизированных вариантов DC8E8 (изотип IgG4) и химерного DC8E8 и патологического беспорядочного тау 151-391/4R и полноразмерного физиологического тау 2N4R, как определено с помощью ELISA.(A) связывание гуманизированного антитела AX004; (B) связывание гуманизированного антитела AX005; (C) связывание гуманизированного антитела AX016; (D) связывание гуманизированного антитела AX017.(E) связывание химерного DC8E8.(F) значения EC50 химерного DC8E8 и гуманизированных вариантов AX004, AX005, AX016, AX017 к проанализированным тау-белкам.
Фигура 34: Связывание гуманизированных вариантов DC8E8 (изотип IgG1) и патологического беспорядочного тау 151-391/4R и полноразмерного физиологического тау 2N4R, как определено с помощью ELISA.(A) связывание гуманизированного антитела AX004; (B) связывание гуманизированного антитела AX005; (C) связывание гуманизированного антитела AX016; (D) связывание гуманизированного антитела AX017.(E) значения EC50 гуманизированных вариантов AX004, AX005, AX016, AX017 к проанализированным тау-белкам.
Фигура 35: Поверхностный плазмонный резонанс (SPR) для характеристики гуманизированных вариантов DC8E8 AX004, AX005, AX016, AX017, связывающихся с патологическим беспорядочным тау 151-391/4R и полноразмерным 2N4R.(A) варианты IgG4, (B) варианты IgG1.
Фигура 36: Связывание гуманизированных антител (изотип IgG4) с тау-пептидами, полученными из повторяющихся областей связывания с микротрубочками тау-белка, как определено с помощью ELISA.(A) связывание гуманизированного антитела AX004; (B) связывание гуманизированного антитела AX005; (C) связывание гуманизированного антитела AX016; (D) связывание гуманизированного антитела AX017.(E) связывание химерного DC8E8.(F) значения EC50 химерного DC8E8 и гуманизированных вариантов AX004, AX005, AX016, AX017 для проанализированных тау-белков.
Фигура 37: Связывание гуманизированных антител (изотип IgG1) с тау-пептидами, полученными из повторяющихся областей связывания с микротрубочками тау-белка, как определено с помощью ELISA.(A) связывание гуманизированного антитела AX004; (B) связывание гуманизированного антитела AX005; (C) связывание гуманизированного антитела AX016; (D) связывание гуманизированного антитела AX017.(E) значения EC50 химерного DC8E8 и гуманизированных вариантов AX004, AX005, AX016, AX017 для проанализированных тау-белков.
Фигура 38: Гуманизированные варианты DC8E8 ингибируют патологическое взаимодействие тау-тау при флуоресцентном анализе процесса образования фибрилл тау-белком. Патологический беспорядочный тау 151-391/4R индуцировали для стимуляции изменения конформации и образования фибрилл, как измерено по флуоресценции тиофлавина T; гуманизированные антитела добавляли к реакции образования фибрилл и тестировали их способность предотвращать патологическое конформационное изменение. Все тестированные гуманизированные антитела способны ингибировать патологическую тау-тау агрегацию. (A) ингибирование патологической агрегации, индуцированной гуманизированными вариантами DC8E8 изотипа IgG4, и (B) ингибирование патологической агрегации, индуцированной гуманизированными антителами изотипа IgG1.
Фигура 39: Иммуногистохимическое окрашивание мозга при болезни Альцгеймера с использованием гуманизированных антител DC8E8 (IgG1), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень нейрофибриллярной патологии в гиппокампе AD человека (CA1). Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали меньше патологических структур в мозге при AD. Панель инструментов:100 мкм
Фигура 40: Иммуногистохимическое окрашивание мозга при болезни Альцгеймера с использованием гуманизированных антител DC8E8 (IgG4), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень нейрофибриллярной патологии в гиппокампе AD человека (CA1). Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали меньше патологических структур в мозге при AD. Панель инструментов:100 мкм
Фигура 41: Иммуногистохимическое окрашивание мозга при TDP-17 (мутация тау-белка R406W) с использованием гуманизированных антител DC8E8 (IgG1), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень нейрофибриллярной патологии в энторинальной коре человека. Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали меньше патологических структур в мозге FTDP-17. Панель инструментов:100 мкм
Фигура 42: Иммуногистохимическое окрашивание мозга при TDP-17 (мутация тау-белка R406W) с использованием гуманизированных антител DC8E8 (IgG4), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень нейрофибриллярной патологии в энторинальной коре человека. Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8.AX005 (D) и AX017 (F) не распознавали патологические структуры в мозге FTDP-17.Панель инструментов:100 мкм
Фигура 43: Иммуногистохимическое окрашивание кортикобазальной дегенерации с использованием гуманизированных антител DC8E8 (IgG1), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень глиальной тау-патологии в хвостатом ядре мозга человека. Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали меньше патологических структур в мозге при CBD, однако интенсивность окрашивания сравнима с DC8E8.Панель инструментов:50 мкм
Фигура 44: Иммуногистохимическое окрашивание кортикобазальной дегенерации с использованием гуманизированных антител DC8E8 (IgG4), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень глиальной тау-патологии в хвостатом ядре мозга человека. Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали меньше патологических структур в мозге при CBD, однако интенсивность окрашивания сравнима с DC8E8.Панель инструментов:50 мкм
Фигура 45: Иммуногистохимическое окрашивание прогрессивного супрануклеарного паралича с использованием гуманизированных антител DC8E8 (IgG1), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень глиальной тау-патологии в хвостатом ядре мозга человека. Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали незначительно меньше патологических структур. Интенсивность окрашивания сравнима с DC8E8.Панель инструментов:50 мкм
Фигура 46: Иммуногистохимическое окрашивание прогрессивного супрануклеарного паралича с использованием гуманизированных антител DC8E8 (IgG4), как DC8E8 (A), так и химерного DC8E8 (B), показало высокий уровень глиальной тау-патологии в хвостатом ядре мозга человека. Гуманизированные антитела AX004 (C) и AX016 (E) отображали сходные параметры окрашивания с DC8E8. В целом, гуманизированные антитела AX005 (D) и AX017 (F) распознавали незначительно меньше патологических структур. Интенсивность окрашивания сравнима с DC8E8.Панель инструментов:50 мкм
Аминокислотные последовательности, соответствующие изомерам тау-белка человека, приведены в SEQ ID NO:151-156, соответственно, по порядку:
SEQ ID NO:151 (2N4R):
MAEPRQEFEV MEDHAGTYGL GDRKDQGGYT MHQDQEGDTD AGLKESPLQT PTEDGSEEPG SETSDAKSTP TAEDVTAPLV DEGAPGKQAA AQPHTEIPEG TTAEEAGIGD TPSLEDEAAG HVTQARMVSK SKDGTGSDDK KAKGADGKTK IATPRGAAPP GQKGQANATR IPAKTPPAPK TPPSSGEPPK SGDRSGYSSP GSPGTPGSRS RTPSLPTPPT REPKKVAVVR TPPKSPSSAK SRLQTAPVPM PDLKNVKSKI GSTENLKHQP GGGKVQIINK KLDLSNVQSK CGSKDNIKHV PGGGSVQIVY KPVDLSKVTS KCGSLGNIHH KPGGGQVEVK SEKLDFKDRV QSKIGSLDNI THVPGGGNKK IETHKLTFRE NAKAKTDHGA EIVYKSPVVS GDTSPRHLSN VSSTGSIDMV DSPQLATLAD EVSASLAKQG L
SEQ ID NO:152 (1N4R):
MAEPRQEFEV MEDHAGTYGL GDRKDQGGYT MHQDQEGDTD AGLKESPLQT PTEDGSEEPG SETSDAKSTP TAEAEEAGIG DTPSLEDEAA GHVTQARMVS KSKDGTGSDD KKAKGADGKT KIATPRGAAP PGQKGQANAT RIPAKTPPAP KTPPSSGEPP KSGDRSGYSS PGSPGTPGSR SRTPSLPTPP TREPKKVAVV RTPPKSPSSA KSRLQTAPVP MPDLKNVKSK IGSTENLKHQ PGGGKVQIIN KKLDLSNVQS KCGSKDNIKH VPGGGSVQIV YKPVDLSKVT SKCGSLGNIH HKPGGGQVEV KSEKLDFKDR VQSKIGSLDN ITHVPGGGNK KIETHKLTFR ENAKAKTDHG AEIVYKSPVV SGDTSPRHLS NVSSTGSIDM VDSPQLATLA DEVSASLAKQ GL
SEQ ID NO:153 (2N3R):
MAEPRQEFEV MEDHAGTYGL GDRKDQGGYT MHQDQEGDTD AGLKESPLQT PTEDGSEEPG SETSDAKSTP TAEDVTAPLV DEGAPGKQAA AQPHTEIPEG TTAEEAGIGD TPSLEDEAAG HVTQARMVSK SKDGTGSDDK KAKGADGKTK IATPRGAAPP GQKGQANATR IPAKTPPAPK TPPSSGEPPK SGDRSGYSSP GSPGTPGSRS RTPSLPTPPT REPKKVAVVR TPPKSPSSAK SRLQTAPVPM PDLKNVKSKI GSTENLKHQP GGGKVQIVYK PVDLSKVTSK CGSLGNIHHK PGGGQVEVKS EKLDFKDRVQ SKIGSLDNIT HVPGGGNKKI ETHKLTFREN AKAKTDHGAE IVYKSPVVSG DTSPRHLSNV SSTGSIDMVD SPQLATLADE VSASLAKQGL
SEQ ID NO:154 (0N4R):
MAEPRQEFEV MEDHAGTYGL GDRKDQGGYT MHQDQEGDTD AGLKAEEAGI GDTPSLEDEA AGHVTQARMV SKSKDGTGSD DKKAKGADGK TKIATPRGAA PPGQKGQANA TRIPAKTPPA PKTPPSSGEP PKSGDRSGYS SPGSPGTPGS RSRTPSLPTP PTREPKKVAV VRTPPKSPSS AKSRLQTAPV PMPDLKNVKS KIGSTENLKH QPGGGKVQII NKKLDLSNVQ SKCGSKDNIK HVPGGGSVQI VYKPVDLSKV TSKCGSLGNI HHKPGGGQVE VKSEKLDFKD RVQSKIGSLD NITHVPGGGN KKIETHKLTF RENAKAKTDH GAEIVYKSPV VSGDTSPRHL SNVSSTGSID MVDSPQLATL ADEVSASLAK QGL
SEQ ID NO:155 (1N3R):
MAEPRQEFEV MEDHAGTYGL GDRKDQGGYT MHQDQEGDTD AGLKESPLQT PTEDGSEEPG SETSDAKSTP TAEAEEAGIG DTPSLEDEAA GHVTQARMVS KSKDGTGSDD KKAKGADGKT KIATPRGAAP PGQKGQANAT RIPAKTPPAP KTPPSSGEPP KSGDRSGYSS PGSPGTPGSR SRTPSLPTPP TREPKKVAVV RTPPKSPSSA KSRLQTAPVP MPDLKNVKSK IGSTENLKHQ PGGGKVQIVY KPVDLSKVTS KCGSLGNIHH KPGGGQVEVK SEKLDFKDRV QSKIGSLDNI THVPGGGNKK IETHKLTFRE NAKAKTDHGA EIVYKSPVVS GDTSPRHLSN VSSTGSIDMV DSPQLATLAD EVSASLAKQG L
SEQ ID NO:156 (0N3R):
MAEPRQEFEV MEDHAGTYGL GDRKDQGGYT MHQDQEGDTD AGLKAEEAGI GDTPSLEDEA AGHVTQARMV SKSKDGTGSD DKKAKGADGK TKIATPRGAA PPGQKGQANA TRIPAKTPPA PKTPPSSGEP PKSGDRSGYS SPGSPGTPGS RSRTPSLPTP PTREPKKVAV VRTPPKSPSS AKSRLQTAPV PMPDLKNVKS KIGSTENLKH QPGGGKVQIV YKPVDLSKVT SKCGSLGNIH HKPGGGQVEV KSEKLDFKDR VQSKIGSLDN ITHVPGGGNK KIETHKLTFR ENAKAKTDHG AEIVYKSPVV SGDTSPRHLS NVSSTGSIDM VDSPQLATLA DEVSASLAKQ GL
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Термин "аффинность" относится к силе суммы нековалентных взаимодействий между одиночным сайтом связывания молекулы (например, антитело) и ее партнера по связыванию (например, антиген).Аффинность молекулы X к ее партнеру Y в целом можно выразить с помощью равновесной константы диссоциации (KD) (или обратной равновесной константы диссоциации, KA).Сродство можно измерить с помощью общепринятых в данной области способов, включая способы, описанные в настоящем документе. См., например, Pope ME, Soste MV, Eyford BA, Anderson NL, Pearson TW. (2009) J Immunol Methods. 341(1-2):86-96, и способы, описанные в настоящем документе. Конкретные иллюстративные и характерные варианты осуществления измерения аффинности связывания раскрыты в настоящем документе ниже.
Термин «аминокислота» относится к природным, модифицированным и синтетическим аминокислотам, а также к аналогам аминокислот и миметикам аминокислот, которые функционируют по аналогии с природными аминокислотами. Природными аминокислотами являются такие аминокислоты, которые кодируются генетическим кодом, а также такие аминокислоты, которые затем модифицированы, например, гидроксипролин, гамма-карбоксиглутамат и O-фосфосерин. Аминокислотные аналоги относятся к соединениям, которые обладают такой же базовой химической структурой, что и природная аминокислота, то есть содержат альфа-углерод, который связан с водородом, карбоксильной группой, аминогруппой и группой R, например, гомосерин, норлейцин, метионинсульфоксид, метионинметилсульфоний. Такие аналоги имеют модифицированные группы R (например, норлейцин) или модифицированные пептидные скелеты, но сохраняют ту же основную химическую структуру, что и природная аминокислота. Аминокислотные миметики относятся к химическим соединениям, которые имеют структуру, которая отличается от общей химической структуры аминокислоты, но которые действуют аналогично природной аминокислоте. Подходящие аминокислоты включают, но этим не ограничиваясь, как D-, так и L-изомеры 20 общих природных аминокислот, находящихся в пептидах, а также природные и неприродные аминокислоты, полученные органическим синтезом или альтернативными метаболическими путями. Примеры таких неприродных аминокислот включают, но не ограничиваются ими, N-ацетилглюкозаминил-L-серин, N-ацетилглюкозаминил-L-треонин и O-фосфотирозин.Модифицированные аминокислоты включают, но не ограничиваются ими, гидроксипролин, пироглутамат, гамма-карбоксиглутамат, O-фосфосерин, азетидинкарбоновую кислоту, 2-аминоадипиновую кислоту, 3-аминоадипиновую кислоту, бета-аланин, аминопропионовую кислоту, 2-аминомасляную кислоту, 4-аминомасляную кислоту, 6-аминокапроновую кислоту, 2-аминогептановую кислоту, 2-аминоизомасляную кислоту, 3-аминоизомасляную кислоту, 2-аминопимелиновую кислоту, трет-бутилглицин, 2,4-диаминоизомасляную кислоту, десмозин, 2,2'-диаминопимелиновую кислоту, 2,3-диаминопропионовую кислоту, N-этилглицин, N-метилглицин, N-этиласпарин, гомопролин, гидроксилизин, алло-гидроксилизин, 3-гидроксипролин, 4-гидроксипролин, изодесмозин, алло-изолейцин, N-метилаланин, N-метилглицин, N- метилизолейцин, N-метилпентилглицин, N-метилвалин, нафталанин, норвалин, норлейцин, орнитин, пентилглицин, пипеколиновую кислоту и тиопролин. Термин аминокислота также включает природные аминокислоты, которые являются метаболитами в некоторых организмах, но не кодируются генетическим кодом для включения в белки. Такие аминокислоты включают, но не ограничиваются ими, орнитин, D-орнитин и D-аргинин.
«Антителозависимая клеточно-опосредованная цитотоксичность» и «ADCC» относятся к клеточно-опосредованному взаимодействию, в котором неспецифические цитотоксические клетки экспрессируют рецепторы Fc (FcRs) (например, природные клетки-киллеры (NK), нейтрофилы и макрофаги), распознают связанные антитела на клетке-мишени и затем вызывают лизис клетки-мишени. Основные клетки, опосредующие ADCC, NK-клетки, экспрессируют только Fc.гамма.RIII, в то время как моноциты экспрессируют Fc.гамма.RI, Fc.гамма.RII и Fc.гамма.RIII.Сводная информация об экспрессии FcR на кроветворных клетках приведена в таблице 3 на странице 464 статьи Ravetch and Kinet, Annu.Rev.Immunol 9:457-92 (1991).Чтобы оценить ADCC-активность молекулы, представляющей интерес, может быть выполнен ADCC анализ in vitro, как описано в патентеСША№5500362 или патентеСША№5821337.Эффекторные клетки, подходящие для такого анализа, включают мононуклеарные клетки периферической крови (PBMC) и природные клетки-киллеры (NK). В качестве альтернативы или дополнения, ADCC-активность молекулы, представляющей интерес, можно оценить in vivo, например, на животной модели, как описано в публикации Clynes et al. PNAS (США) 95:652-656 (1998).
«Обратная мутация» представляет собой мутацию, введенную в нуклеотидную последовательность, которая кодирует гуманизированное антитело, где мутация дает аминокислоту, соответствующую аминокислоте исходного антитела (например, донорское антитело, например, антитело мыши).Некоторые остатки каркасного участка исходного антитела могут быть сохранены в процессе гуманизации антител по изобретению, чтобы в значительной степени сохранить связывающие свойства исходного антитела, в то же время минимизируя потенциальную иммуногенность полученного антитела. В одном из вариантов осуществления, раскрытого в настоящем документе, исходное антитело имеет мышиное происхождение. Например, обратная мутация меняет остаток каркасного участка человека на исходный остаток мыши. Примеры остатков каркасных участков, которые могут быть обратно мутированы, включают, но ими не ограничиваются, канонические остатки, поверхностные остатки для упаковки, необычные исходные остатки, которые расположены вблизи с сайтом связывания, остатки в "Варньер-зоне" (которая образует платформу, на которой остаются CDR) (Foote& Winter, 1992, J.Mol.Biol. 224, 487-499) и остатки, которые расположены вблизи с CDR H3.
Термин «химерные» антитела относится к антителам, в которых часть тяжелых и/или легких цепей идентична или гомологична соответствующим последовательностям в антителах, полученных из конкретных образцов или принадлежащих конкретному классу или подклассу антител (например, химерные гуманизированные, антитела с переключением класса), тогда как остальная часть цепи(ей) идентична или гомологична соответствующим последовательностям в антителах, полученных из других образцов или принадлежащих другим классам или подклассам антител, а также относится к фрагментам таких антител, при условии, что они проявляют желаемую биологическую активность (патентСША№4816567; и Morrison et al., Proc.Natl.Acad.Sci.USA, 81:6851-6855 (1984)). В одном из вариантов осуществления термин «химерные антитела» относится к моноклональным антителам, состоящим из вариабельной области, то есть области связывания, полученной из одного источника или образцов, и по крайней мере части константной области, полученной из другого источника или образцов, которые получают обычно с помощью технологий рекомбинантных ДНК. Иногда предпочтительными являются химерные антитела, содержащие вариабельную область мыши и константную область человека. Такие химерные антитела мыши/человека представляют собой продукт экспрессируемых генов иммуноглобулина, содержащих сегменты ДНК, кодирующие вариабельные области иммуноглобулина мыши, и сегменты ДНК, кодирующие константные области иммуноглобулина человека. Другие виды «химерных антител», охватываемых настоящим изобретением, представляет собой антитела, в которых класс или подкласс был модифицирован или изменен по сравнению с классом исходного антитела. Такие «химерные» антитела также упоминаются как «антитела с переключением класса». Способы получения химерных антител включают традиционные технологии рекомбинантных ДНК и методы трансфекции генов, известные в данной области. См., например, Morrison, S.L., et al., Proc.Natl.Acad Sci.USA 81 (1984) 6851-6855; патенты США №№5202238 и 5204244.
«Конкурентное связывание» определяют в анализе, в котором тестируемый иммуноглобулин/антитело/связывающий фрагмент ингибирует специфическое связывание эталонного антитела с обычным антигеном, таким как тау-белок (например, тау 151-391/4R).Известны различные виды анализов на конкурентное связывание, например: твердофазный прямой или непрямой радиоиммунологический анализ (RIA), твердофазный прямой или косвенный иммуноферментный анализ (EIA), конкурентный сэндвич-анализ (см. Stahli et al., Methods in Enzymology 9: 242 (1983)); твердофазный прямой биотин-авидиновый EIA (см., Kirkland et al.,J.Immunol. 137: 3614 (1986)); твердофазный прямой анализ с мечением, твердофазный прямой сэндвич-анализ с мечением (см. Harlow and Lane, Antibodies: A Laboratory Manual, Cold Spring Harbor Press (1988)); твердофазный прямой RIA, используя мечение с помощью I125 (см. Morel et al., Mol.Immunol.25 (1): 7 (1988)); твердофазный прямой биотин-авидиновый EIA (Cheung et al., Virology 176: 546 (1990)); и прямой RIA с мечением. (Moldenhauer et al., Scand.J.Immunol. 32:77 (1990)).Как правило, такой анализ включает использование очищенного антигена, связанного с твердой поверхностью, или клеток, несущих любой, как немеченый тестируемый иммуноглобулин, так и меченый эталонный иммуноглобулин. Конкурентное ингибирование измеряют путем определения количества метки, связавшейся с твердой поверхностью или клетками в присутствии тестируемого иммуноглобулина. Обычно тестируемый иммуноглобулин присутствует в избытке. Обычно, когда конкурирующее антитело присутствует в избытке, оно ингибирует специфическое связывание эталонного антитела с обычным антигеном по меньшей мере на 50-55%, 55-60%, 60-65%, 65-70%, 70-75% или более.
«Комплемент-зависимая цитотоксичность» или «CDC» относится к способности молекулы лизировать мишень в присутствии комплемента. Путь активации комплемента инициируется связыванием первого компонента системы комплемента (C1q) с молекулой (например, антителом), объединенной с распознаваемым антигеном. Для оценки активации комплемента может быть осуществлен анализ CDC, например, как описано в Gazzano-Santoro et al., J.Immunol. Methods 202:163 (1996).
Используемый в настоящем документе термин «конъюгация» относится к связи или химическому фрагменту, образованному в результате химического взаимодействия между функциональной группой первой молекулы (например, антителом) и функциональной группой второй молекулы (например, терапевтическим агентом или лекарственным средством).Такие связи включают, но этим не ограничиваются, ковалентные связи и нековалентные связи, при этом такие химические фрагменты включают, но ими не ограничиваются, сложные эфиры, карбонаты, имины, фосфатные эфиры, гидразоны, ацетали, ортоэфиры, пептидные связи и олигонуклеотидные связи. Выражение «гидролитически стабильные связи» означает, что связи по существу стабильны в воде и не реагируют с водой при практически используемых значениях рН, что включает, но этим не ограничивается, физиологические условия в течение длительного периода времени. Выражение «гидролитически нестабильные или расщепляемые связи» означает, что связи способны расщепляться в воде или в водных растворах, включая, например, кровь. Выражение «ферментативно нестабильные или расщепляемые связи» означает, что связи способны расщепляться одним или несколькими ферментами. Только в качестве примера, некоторые ПЭГ и соответствующие полимеры содержат способные к расщеплению связи в полимерном скелете или в линкерной группе, имеющейся между полимерным скелетом ПЭГ и одной или несколькими концевыми функциональными группами белка, полипептида или пептида, представленными в настоящем документе. Такие способные к разложению связи включают, но этим не ограничиваются, сложноэфирные связи, образованные путем взаимодействия ПЭГ карбоновых кислот или активированных ПЭГ карбоновых кислот со спиртовыми группами на биологически активном агенте, где такие сложноэфирные группы обычно гидролизуются в физиологических условиях с высвобождением биологически активного агента. Другие гидролитически расщепляемые связи включают, но этим не ограничиваются, карбонатные связи; иминовые связи, образованные при взаимодействии амина и альдегида; фосфатноэфирные связи, образованные при взаимодействии спирта с фосфатной группой; гидразоновые связи, которые являются продуктом взаимодействия гидразида и альдегида; ацетальные связи, которые являются продуктом взаимодействия альдегида и спирта; ортоэфирные связи, которые являются продуктом взаимодействия формиата и спирта; пептидные связи, образованные при взаимодействии аминогруппы, включая, но этим не ограничиваясь, на конце полимера, такого как ПЭГ, и карбоксильной группы пептида; и олигонуклеотидные связи, образованные фосфорамидитной группой, включая но этим не ограничиваясь, на конце полимера, и 5' гидроксильной группой олигонуклеотида.
Термин «DC8E8» относится к антителу, описанному в WO 2013/191962, и произведенному гибридомой, депонированной в Американской коллекции типовых культур, патентное депонирование №PTA-11994.Как описано в WO2013/041962, было обнаружено, что антитела (например,DC8E8), которые специфически связаны с одним или несколькими из четырех ранее неидентифицированных функциональных областей тау-белка, выбранных из 268-HQPGGG-273 (SEQ ID NO:148) (в пределах 1-го повторяющегося домена тау-белка), 299-HVPGGG-304 (SEQ ID NO:149) (в пределах 2-го повторяющегося домена тау-белка), 330-HKPGGG-335 (SEQ ID NO:150) (в пределах 3-го повторяющегося домена тау-белка), 362-HVPGGG- 367 (SEQ ID №:149) (в пределах 4-го повторяющегося домена тау-белка), cпособны ингибировать образование патологических агрегатов тау-белка и выявлять различные патологические формы тау-белка, некоторые из которых образуются на самых ранних стадиях заболевания (например, патологические мономеры). Гибридомы, полученные против патологического беспорядочного тау-белка II человека (тау 151-391/4R), которое также упоминается в настоящей заявке как тауΔ(1-150; 392-441)/4R, скринировали на получение моноклональных антител, специфичных к парным спиральным филаментам (PHF), как с помощью иммуногистохимических (IHC), так и с помощью иммуноферментных анализов (ELISA).Полученный набор включал моноклональное антитело против мыши (mAb) DC8E8, которое относится к подклассу IgG1.Эпитопное картирование DC8E8 показало, что оно связывает четыре ранее неидентифицированных эпитопа тау-белка человека. Более того, дополнительный функциональный анализ DC8E8 показал, что каждый эпитоп представляет собой отдельную функциональную область внутри тау-белка. Эти области, которые были описаны как новые мишени для диагностики и терапии AD, находятся в функциональных областях тау-белка, выбранных из 268-HQPGGG-273 (SEQ ID NO:148) (в пределах 1-го повторяющегося домена тау-белка), 299-HVPGGG-304 (SEQ ID NO:149) (в пределах 2-го повторяющегося домена тау-белка), 330-HKPGGG-335 (SEQ ID NO:150) (в пределах 3-го повторяющегося домена тау-белка), 362-HVPGGG-367 (SEQ ID NO:149) (в пределах 4-го повторяющегося домена тау-белка).
Как используется в настоящем описании термины «диагностирование» и «диагноз» относятся к способам, с помощью которых квалифицированный специалист может оценить и даже определить, страдает ли пациент данным заболеванием или состоянием, в данном случае болезнью Альцгеймера и связанными таупатиями. Специалист в данной области как правило ставит диагноз на основании одного или нескольких диагностических показателей, таких как, например, биомаркер, количество (включая наличие или отсутствие) которого указывает на наличие, тяжесть или отсутствие состояния.
Наряду с диагнозом, клинический мониторинг и прогнозирование заболевания также являются предметом большой важности и интереса. Важно знать стадию и скорость прогрессирования AD, чтобы спланировать наиболее эффективную терапию. Если можно сделать более точный прогноз, то может быть выбрана подходящая терапия и в некоторых случаях менее жесткая терапия для пациента. Измерение уровней патологического тау-белка, как раскрыто в настоящем документе, может быть полезно для того, чтобы классифицировать индивидов по прогрессированию AD, на тех, которым конкретные средства будут эффективны, и дифференцировать их от индивидов для которых может быть более подходящими альтернативные или дополнительные способы лечения.
Например, DC8E8 способен различать доклиническую AD, клиническую AD и полностью прогрессировавшую AD на конечной стадии (см. WO2013/041962).DC8E8 показало окрашивание на ранних стадиях (тау-мономеры, димеры) патологического тау-белка в доклинической стадии AD человека - I стадия по Браак. Антитело распознавало стадию патологических тау-олигомеров и стадию патологических тау-полимеров (клубки).При полностью прогрессировавшей болезни Альцгеймера (конечная стадия - VI стадия по Браак) DC8E8 распознавало, главным образом, патологические тау-полимеры в формах нейрофибриллярных клубков, невритических бляшек и сенильных нитей.DC8E8 распознавало все стадии развития клубков при болезни Альцгеймера.DC8E8 распознало ранние стадии развития образования клубков - мономерную, димерную и раннюю олигомерную стадию и позднюю олигомерную, до клубковую стадию, а также поздние стадии развития патологических тау-полимеров - внутриклеточные и внеклеточные нейрофибриллярные клубки.
Соответственно, «диагностирование» или «постановка диагноза», как используется в настоящем документе, дополнительно включает прогнозирование, которое может предусматривать прогнозирование клинического результата (наряду с или без медицинского лечения), выбор подходящего лечения (или же эффективность лечения), или мониторинг проводимого лечения и, возможно, изменение лечения, основанного на измерении уровней патологического тау-белка.
«Эффекторные функции» антитела относятся к биологической активности, характерной для области Fc (нативный участок области Fc или вариант аминокислотной последовательности области Fc) антитела. Примеры эффекторных функций антител включают связывание C1q; комплемент-зависимую цитотоксичность; связывание с рецептором Fc; антитело-зависимую клеточную цитотоксичность (ADCC); фагоцитоз; и подавление рецепторов поверхности клетки (например, рецептора В-клетки; BCR).
Термин «эпитоп» или «антигенная детерминанта» относится к сайту на антигене, с которым специфически связывается иммуноглобулин или антитело (или его антиген-связывающий фрагмент).Эпитопы могут быть образованы как смежными аминокислотами, так и несмежными аминокислотами, помещающимися рядом при третичной укладке белка. Эпитопы, образованные смежными аминокислотами, обычно сохраняются при воздействии денатурирующих растворителей, тогда как эпитопы, образованные третичной укладкой, обычно теряются при обработке денатурирующими растворителями. Эпитоп обычно включает по меньшей мере 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15 аминокислот, часто в уникальной пространственной конформации. Способы определения пространственной конформации эпитопов включают, например, рентгеновскую кристаллографию и двумерный ядерный магнитный резонанс. См., например, Epitope Mapping Protocols in Methods in Molecular Biology, Vol.66, G.E.Morris, Ed.(1996). "Конформационный эпитоп" представляет собой эпитоп, с которым антитело или его тау-связывающий фрагмент связывается конформационно-специфическим образом. Для эпитопов на основе белков связывание может зависеть от вторичной, третичной или четвертичной структуры белка, несущего эпитоп. Другими словами, антитело связывается структурно-специфическим способом, специфичным для третичной структуры способом или специфичным для четвертичной структуры способом. Конформационный эпитоп представляет собой эпитоп, который присутствует в патологическом тау-белке (например, присутствует в тау 151-391/4R).
Антитела и тау-связывающие фрагменты, описанные в настоящем документе, имеют в качестве своего «эпитопа» любой, один или несколько, следующих четырех тау-сайтов, некоторые или все из которых являются конформационными эпитопами:268-HQPGGG-273 (SEQ ID NO:148) (в пределах 1-го повторяющегося домена тау-белка), 299-HVPGGG-304 (SEQ ID NO:149) (в пределах 2-го повторяющегося домена тау-белка), 330-HKPGGG-335 (SEQ ID NO:150) (в пределах 3-го повторяющегося домена тау-белка), 362-HVPGGG- 367 (SEQ ID №:149) (в пределах 4-го повторяющегося домена тау-белка).Эти эпитопы также указаны в настоящем документе как QT1, QT2, QT3 и QT4, соответственно.DC8E8 связывается со всеми QT1-QT4; на самом деле, эпитоп DC8E8 представляет собой HXPGGG, где X представляет собой любую аминокислоту (SEQ ID NO:157).
Расщепление папаином антител дает два идентичных антиген-связывающих фрагмента, называемых фрагментами Fab, каждый с единственным антиген-связывающим сайтом, и остаточный фрагмент «Fc», название которого отражает его способность быстро кристаллизоваться (фрагмент (F) способный кристаллизоваться (c)).Обработка пепсином дает фрагмент F(ab')2, который имеет два антиген-связывающих сайта и сохраняет способность к перекрестному связыванию с антигеном. «Fv» представляет собой ту часть тяжелой цепи, которая входит в состав фрагмента Fab. Любой из этих фрагментов также может быть получен рекомбинантным путем. Часть Fc антитела связана с эффекторными функциями антитела, включая антитело-зависимую клеточную цитотоксичность (ADCC) и комплемент-зависимую цитотоксичность или фагоцитоз. Изменения (например, мутации или изменения гликозилирования) в Fc-области антитела могут быть использованы для модуляции любой из эффекторных функций, а также для повышения его полураспада в сыворотке и других фармакокинетических свойств.
Фрагмент Fab также содержит константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Фрагменты Fab' отличаются от фрагментов Fab добавлением нескольких остатков на карбоксильном конце домена CH1 тяжелой цепи, включающем один или несколько цистеинов шарнирной области антитела. Fab'-SH обозначает в настоящем описании Fab', в котором остаток(и) цистеина константных доменов несет по меньшей мере одну свободную тиольную группу. Фрагменты F(ab')2 антитела первоначально были получены как пары фрагментов Fab', которые имеют шарнирные цистеины между ними. Также известны другие химические соединения фрагментов антитела.
Как используется в настоящем описании термин «Fc» включает полипептид, содержащий константную область антитела, исключая первую константную область домена иммуноглобулина. Таким образом, Fc относится к двум последним константным областям доменов иммуноглобулинов IgA, IgD и IgG и к трем последним константным областям доменов иммуноглобулинов IgE и IgM и гибкому шарнирному N-концу этих доменов. В случае IgA и IgM, Fc может включать J-цепь. В случае IgG, Fc содержит иммуноглобулиновые домены C гамма 2 и C гамма 3 (Cгамма2 и Cгамма3) и шарнир между C гамма 1 (Cгамма1) и C гамма 2 (Cгамма2).Несмотря на то, что границы области Fc могут изменяться, область Fc тяжелой цепи IgG человека обычно определена как содержащая остатки C226 или P230 на карбоксильном конце, где нумерация соответствует системе нумерации ЕС. В одном из вариантов осуществления, для IgG1 человека область Fc в данном случае определена как содержащая остаток Р232 на карбоксильном конце, где нумерация соответствует системе нумерации ЕС (Edelman G M et al.,(1969) Proc Natl Acad Sci USA, 63(1):78-85).С-концевой лизин (остаток 447 в соответствии с системой нумерации ЕС) области Fc можно удалить, например, во время получения или очистки антитела или рекомбинантными способами генной инженерии нуклеиновой кислоты, кодирующей тяжелую цепь антитела. Соответственно, композиция интактных антител может содержать популяции антител со всеми удаленными остатками K447, популяции антител без удаленных остатков K447 и популяции антител со смесью антител с остатком K447 и без него. Fc может относиться к этой области сам по себе или к этой области в контексте полипептида Fc, например, антитела. Fc может быть нативной последовательностью Fc или вариантом Fc. Замены аминокислотных остатков в части Fc для изменения эффекторной функции антитела известны в данной области (см., например, Winter et al., патенты США №№ 5648260 и 5624821).Один подходящий Fc, описанный в заявке РСТ WO93/10151 (включена в настоящее описание в качестве ссылки), представляет собой одноцепочечный полипептид, расположенный на протяжении от N-концевой шарнирной области до нативного C-конца области Fc антитела IgG1 человека. Другим эффективным полипептидом Fc является мутеин Fc, описанный в патентеСША№5457035 и в статье Baum et al., 1994, EMBO J. 13:3992-4001.Аминокислотная последовательность этого мутеина идентична аминокислотной последовательности нативного Fc, представленной в WO93/10151, за исключением того, что аминокислота 19 была заменена с Leu на Ala, аминокислота 20 была заменена на с Leu на Glu и аминокислота 22 была изменена с Gly на Ala. Мутеин демонстрирует пониженную аффинность к Fc-рецепторам.
Термины «Fc-рецептор» или «FcR» используются для описания рецептора, который связывается с областью Fc антитела. Предпочтительным FcR является природная последовательность FcR человека. Более того, предпочтительным FcR является FcR, который связывается с антителом IgG (гамма-рецептор) и содержит подклассы рецепторов Fc.гамма.RI, Fc.гамма.RII и Fc.гамма.RIII, включая аллельные варианты и формы альтернативного сплайсинга этих рецепторов. Рецепторы Fc.гамма.RII включают Fc.гамма.RIIA («активирующий рецептор») и Fc.гамма.RIIB («ингибирующий рецептор»), которые имеют сходные аминокислотные последовательности, которые отличаются главным образом цитоплазматическими доменами. Активирующий рецептор Fc.гамма.RIIA содержит иммунорецепторный мотив активации на основе тирозина (ITAM) в своем цитоплазматическом домене. Ингибирующий рецептор Fc.гамма.RIIВ содержит иммунорецепторный мотив ингибирования на основе тирозина (ITIM) в своем цитоплазматическом домене (см. обзор M. в Daeron, Annu.Rev.Immunol 15:203-234 (1997)). FcR рассмотрен в Ravetch and Kinet, Annu.Rev.Immunol 9:457-92 (1991); Capel et al, Immunomethods 4:25-34 (1994); и de Haas et al, J.Lab.Clin; Med. 126:330-41 (1995). Термин «FcR» в настоящем описании охватывает другие FcR, включая FcR, которые будут идентифицированы в будущем. Этот термин также включает неонатальный рецептор, FcRn, который ответственен за перенос IgG матери плоду (Guyer et al.,J.Immunol. 117:587 (1976) и Kim et al., J.Immunol.24: 249 (1994)) и регулирует гомеостаз иммуноглобулинов.
«Fv» также представляет собой минимальный фрагмент антитела, который содержит полноразмерный антиген-распознающий и антиген-связывающий сайт. Эта область состоит из димера одного вариабельного домена тяжелой цепи и вариабельного домена легкой цепи в плотной нековалентной ассоциации. Именно в этой конфигурации три гипервариабельные области каждого вариабельного домена взаимодействуют и определяют антиген-связывающий сайт на поверхности димера VH-VL. В совокупности шесть гипервариабельных областей придают антиген-связывающую специфичность антителу. Однако даже один вариабельный домен (или половина Fv, содержащая только три гипервариабельные области, специфичные для антигена) обладает способностью распознавать и связывать антиген, хотя и с меньшей аффинностью, чем весь сайт связывания.
Как используется в настоящем описании гуманизированное антитело, которое содержит «каркасную область» вариабельного домена тяжелой или легкой цепи из конкретной последовательности иммуноглобулина зародышевой линии человека, может содержать аминокислотные различия по сравнению с каркасной областью вариабельного домена тяжелой или легкой цепи конкретной последовательности зародышевой линии из-за, например, природных соматических мутаций или преднамеренного введение сайт-направленной мутации. Однако выбранное гуманизированное антитело обычно идентично по меньшей мере на 90% по аминокислотной последовательности каркасной области вариабельного домена тяжелой или легкой цепи аминокислотной последовательности, кодируемой каркасной областью вариабельного домена тяжелой или легкой цепи гена иммуноглобулина зародышевой линии человека, и содержит аминокислотные остатки, которые идентифицируют гуманизированное антитело как происходящее от человека по сравнению с аминокислотными последовательностями иммуноглобулина зародышевой линии других видов (например, последовательностями зародышевой линии мыши). В некоторых случаях гуманизированное антитело может предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, более предпочтительно по меньшей мере на 96%, наиболее предпочтительно по меньшей мере на 97%, в частности по меньшей мере на 98%, наиболее предпочтительно по меньшей мере на 99% идентично по аминокислотной последовательности каркасной области вариабельного домена тяжелой или легкой цепи аминокислотной последовательности каркасной области вариабельного домена тяжелой или легкой цепи, кодируемой геном иммуноглобулина зародышевой линии. Как правило, каркасная область вариабельной области тяжелой или легкой цепи гуманизированного антитела, полученная из конкретной последовательности зародышевой линии человека, будет иметь не более 11 аминокислот, предпочтительно не более 5 или даже более предпочтительно не более 4, 3, 2 или 1 отличий от аминокислотной последовательности каркасной области вариабельного домена тяжелой или легкой цепи, кодируемой геном иммуноглобулина зародышевой линии человека.
«Эффекторные клетки человека» представляют собой лейкоциты, которые экспрессируют один или несколько FcR и выполняют эффекторные функции. Предпочтительно, клетки по меньшей мере экспрессируют Fc.гамма.RIII и осуществляют ADCC эффекторные функции. Примеры лейкоцитов человека, которые опосредуют ADCC, включают мононуклеарные клетки периферической крови (PBMC), клетки природные киллеры (NK), моноциты, цитотоксические Т-клетки и нейтрофилы; причем предпочтительными являются РВМС и NK-клетки. Эффекторные клетки могут быть выделены из природного источника, например, из крови или РВМС, как описано в настоящем документе.
«Последовательности зародышевой линии человека» встречаются естественным образом в популяции человека. Комбинация этих генов зародышевой линии дает разнообразие антител. Последовательности антител зародышевой линии для легкой цепи антитела происходят из консервативных v-генов и j-генов каппа или лябда зародышевой линии человека. Аналогично, последовательности тяжелой цепи происходят от v-, d- и j-генов зародышевой линии (LeFranc, M-P, and LeFranc, G, "The Immunoglobulin Facts Book" Academic Press, 2001). Для всех известных последовательностей существуют общедоступные, хорошо известные базы данных.
Термин «шарнир» или «шарнирная область» или «шарнирная область антитела» в настоящем документе включает гибкий полипептид, содержащий аминокислоты между первым и вторым константными доменами антитела или его тау-связывающего фрагмента. Термин «шарнирная область», как указано в настоящем документе, представляет собой часть последовательности длиной 6-62 аминокислот, присутствующую только в IgA, IgD и IgG, которая включает остатки цистеина, которые соединяют две тяжелые цепи. Структурно, в одном из вариантов осуществления домен CH1 IgG заканчивается положением 220 по EU, а домен CH2 IgG начинается с положения 237 по EU. Таким образом, для IgG шарнир антитела определен в настоящем документе в одном из вариантов, как включающий положения от 221 (D221 в IgG1) до 231 (A231 в IgG1), где нумерация соответствует системе нумерации ЕС.
Термин «гуманизированное антитело» относится к антителам, в которых каркасные области (FR) и/или области, определяющие комплементарность (CDR), были модифицированы и содержат CDR иммуноглобулина различной специфичности (мыши) по сравнению с исходным иммуноглобулином (человека). В одном из вариантов осуществления CDR мыши прививают в каркасную область антитела человека с получением «гуманизированного антитела». В другом варианте осуществления каркасные области человека «привиты» или сплайсированы в мышиные антитела, сохраняя CDR мышиного антитела и заменяя каркасные домены каркасными доменами человеческого происхождения. Прививку и сплайсинг можно проводить с помощью различных технологий рекомбинантной ДНК, включая ПЦР и мутагенез. В уровне техники существуют различные способы гуманизации (например, CDR-трансплантация, перестройка, трансгенные животные, комбинаторные библиотеки). См., например, Riechmann, L., et al., Nature 332 (1988) 323-327; Neuberger, M.S., et al., Nature 314 (1985) 268-270; Sastry L, Alting-Mess M, Huse WD, Short JM, Sorge JA, Hay BN,Janda KD, Benkovic SJ, Lerner RA (1989) Cloning of the immunological repertoire in for generation of monoclonal catalytic antibodies:construction of a heavy chain variable region-specific cDNA library.Proc Natl Acad Sci USA 86, 5728-5732; и Huse WD, Sastry S, Iverson SA, Kang AS, Alting-Mees M, Burton DR, Benkovic SJ, Lerner RA (1989) Generation of a large combinatorial library of the immunoglobulin repertoire in phage lambda. Science 246, 1275-1281. Гуманизированные антитела являются результатом генно-инженерных манипуляций с другим антителом, которое делают более человеко-подобным, сохраняя при этом его первоначальные антиген-связывающие свойства. Presta, L.G. Engineering of therapeutic antibodies to minimize immunogenicity and optimize function.Advanced Drug Delivery Reviews, Volume 58, Issues 5-6:640-656 (2006).Выбор вариабельных доменов человека, как легких, так и тяжелых, для использования при получении гуманизированных антител очень важен для уменьшения антигенности. Согласно методу так называемого приближения последовательность вариабельного домена антитела грызуна скринируют против библиотеки известных последовательностей вариабельного домена человека или библиотеки последовательности зародышевой линии человека. Последовательность человека, наиболее близкую к последовательности грызуна, может быть затем принята как каркасная область человека для гуманизированного антитела (Sims et al., J.Immunol. 1993; 151:2296 et seq.; Chothia et al, Chothia and Lesk, J.Mol.Biol. 1987; 196:901-917). В другом способе используют конкретную каркасную область, полученную из консенсусной последовательности всех человеческих антител конкретной подгруппы легких или тяжелых цепей. Та же каркасная область может быть использована для нескольких различных гуманизированных антител (Carter et al., PNAS USA, 1992; 89:4285 et seq.; Presta et al., J Immunol 1993; 151:2623 et seq.). Другие способы, предназначенные для снижения иммуногенности молекулы антитела у пациента человека, включают венированные антитела (см., например, патент США № 6797492 и публикации патентных заявок США 20020034765 и 20040253645) и антитела, которые были модифицированы анализом и удалением Т-клеточных эпитопов (см., например, публикации патентных заявок США 20030153043 и патентСША№5712120).
Особенно предпочтительные CDR гуманизированных антител, описанные в настоящем документе, соответствуют последовательностям CDR моноклонального антитела DC8E8 мыши, а именно SEQ ID NO:1-6.Копия гуманизированных антител и их тау-связывающих фрагментов, описанных в настоящем документе (например, иммуноглобулин с тем же самым вариабельным участком тяжелой или легкой цепи, что и описанные в настоящем документе), полученные рекомбинантными способами или любыми другими способами (кроме природного антитела), также представляет собой гуманизированное антитело или его тау-связывающий фрагмент в рамках этого термина.
Термин «гипервариабельная область», если используется в настоящем документе, относится к аминокислотным остаткам антитела, которые ответственны за связывание антигена. В одном из вариантов осуществления, согласно Кабат, гипервариабельная область обычно содержит аминокислотные остатки из «определяющей комплементарность области» или «CDR» (например, остатки 24-34 (L1), 50-56 (L2) и 89-97 (L3) в вариабельной области легкой цепи и 31-35 (H1), 50-65 (H2) и 95-102 (H3) в вариабельном домене тяжелой цепи, Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md.(1991)) и/или эти остатки из «гипервариабельной петли» (например, остатки 26-32 (L1), 50-52 (L2) и 91-96 (L3) в вариабельном домене легкой цепи и 26-32 (H1), 53-55 (Н2) и 96-101 (Н3) в вариабельном домене тяжелой цепи, Chothia and Lesk J.Mol.Biol. 196:901-917 (1987)).
Остатки «каркасной области» или «FR» являются остатками вариабельного домена, отличными от остатков гипервариабельной области, как определено в настоящем документе. В уникальной системе нумерации IMGT консервативные аминокислоты всегда имеют одинаковое положение, например, цистеин 23 (1ый-CYS), триптофан 41 (консервативный-TRP), гидрофобная аминокислота 89, цистеин 104 (2ой-CYS), фенилаланин или триптофан 118 (J-PHE или J-TRP).См., например, Lefranc M.-P., Immunology Today 18, 509 (1997); Lefranc M.-P., The Immunologist, 7, 132-136 (1999); Lefranc, M.-P., Pommié, C.,Ruiz, M., Giudicelli, V., Foulquier, E., Truong, L., Thouvenin-Contet, V. and Lefranc, Dev.Comp.Immunol., 27, 55-77 (2003). В другом варианте осуществления уникальная нумерация IMGT обеспечивает стандартизованное разграничение каркасных областей (FR1-IMGT:положения 1-26, FR2-IMGT:39-55, FR3-IMGT:66-104 и FR4-IMGT:118-128) и областей, определяющих комплементарность:CDR1-IMGT:27-38, CDR2-IMGT:56-65 и CDR3-IMGT:105-117.Поскольку пробелы являются незанятыми положениями, длины CDR-IMGT (показаны между скобками и разделены точками, например[8.8.13]) становятся важной информацией. Уникальная нумерация IMGT используется в двумерных графических изображениях, обозначенных как IMGT Colliers de Perles. См., например, Ruiz, M. and Lefranc, M.-P., Immunogenetics, 53, 857-883 (2002); Kaas, Q. and Lefranc, M.-P., Current Bioinformatics, 2, 21-30 (2007). Она также используется для представления 3D-структур. См., например, IMGT/3Dstructure-DB Kaas, Q.,Ruiz, M. and Lefranc, M.-P.,T cell receptor and MHC structural data.Nucl.Acids.Res., 32, D208-D210 (2004).Остатки каркасной области или FR представляют собой остатки вариабельного домена, отличные от заключенных в скобках гипервариабельных доменов.
Используя систему нумерации Kabat, настоящая линейная аминокислотная последовательность может содержать несколько или дополнительные аминокислоты, соответствующие сокращению, или вставке, FR или HVR вариабельного домена. Например, вариабельный домен тяжелой цепи может содержать одну аминокислотную вставку (остаток 52а по Кабат) после остатка 52 H2 и вставленные остатки (например, остатки 82a, 82b и 82c и тому подобное, по Кабат) после остатка 82 FR тяжелой цепи. Нумерация остатков по Кабат может быть определена для заданного антитела путем выравнивания в областях гомологии последовательности антитела со «стандартной» нумерованной по Кабат последовательностью.
Термин «иммуногенность» или иммуноген, как используется в настоящем документе, относится к антительному ответу на введение терапевтического лекарственного средства. Иммуногенность в отношении антител и тау-связывающих фрагментов, приведенных в настоящем документе, получена с использованием количественных и качественных анализов для детекции антител против указанных терапевтических белков, полипептидов и пептидов в биологических жидкостях. Такие анализы включают, но не ограничиваются ими, радиоиммуноанализ (RIA), ферментный иммуносорбентный анализ (ELISA), люминесцентный иммуноанализ (LIA) и флуоресцентный иммуноанализ (FIA). Анализ такой иммуногенности включает сравнение антительного ответа на введение антител и тау-связывающих фрагментов, представленных в настоящем документе, с антительным ответом на введение контрольного терапевтического белка, полипептида или пептида или носителя для доставки или буфера для доставки.
«Легкие цепи» антител любых видов позвоночных могут быть отнесены к одному из двух четко определенных типов, называемых каппа (κ) и лямбда (λ), основанный на аминокислотных последовательностях их константных доменов.
«Нативные антитела» обычно представляют собой гетеротетрамерные гликопротеины, размером приблизительно 150000 Дальтон, состоящие из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Каждая легкая цепь связана с тяжелой цепью одной ковалентной дисульфидной связью, в то время как количество дисульфидных связей изменяется среди тяжелых цепей различных изотипов иммуноглобулина. Каждая тяжелая и легкая цепь также имеет регулярные интервальные внутрицепочечные дисульфидные мостики. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH), за которым следует ряд константных доменов. Каждая легкая цепь имеет вариабельный домен на одном конце (VL) и константный домен на другом конце. Константный домен легкой цепи выровнен с первым константным доменом тяжелой цепи, а вариабельный домен легкой цепи выровнен с вариабельным доменом тяжелой цепи. Считается, что конкретные аминокислотные остатки образуют границу раздела между вариабельными доменами легкой цепи и тяжелой цепи.
Как используется в настоящем изобретении термин «нуклеиновая кислота» включает молекулы ДНК и молекулы РНК. Молекула нуклеиновой кислоты может быть одноцепочечной или двухцепочечной, но предпочтительно является двухцепочечной ДНК.
«Процент идентичности» двух последовательностей нуклеиновых кислот или аминокислот означает процент идентичных нуклеотидов или аминокислотных остатков двух последовательностей, подлежащих сравнению, полученными после оптимального выравнивания, этот процент является чисто статистическим и различия между двумя последовательностями являются беспорядочно распределенными по длине. Сравнение двух последовательностей нуклеиновой кислоты или аминокислот традиционно проводят путем сравнения последовательностей после оптимального их выравнивания, причем указанное сравнение можно проводить по сегменту или используя "окно выравнивания». Оптимальное выравнивание последовательностей для сравнения может быть выполнено, помимо сравнения вручную, с помощью алгоритма локальной гомологии Smith and Waterman (1981) [Ad.App.Math.2: 482], с помощью алгоритма локальной гомологии Neddleman and Wunsch (1970) [J.Mol.Biol.48: 443], с помощью метода поиска подобия в работе Pearson and Lipman (1988) [Proc.Natl.Acad.Sci.USA 85:2444] или с помощью компьютерного программного обеспечения с использованием этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в программном пакете Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Dr., Madison, WI, или с помощью программного обеспечения для сравнения BLAST NR или BLAST P).Например, идентичность последовательности может существовать в области, которая составляет по меньшей мере приблизительно 75-100 последовательных единиц в длину, в области, которая составляет приблизительно 50 последовательных единиц в длину или, если не указано, по всей последовательности полипептидной последовательности.
Процент идентичности двух последовательностей нуклеиновых кислот или аминокислот определяется сравнением двух оптимально выровненных последовательностей, в которых сравниваемая нуклеиновая кислота или аминокислота может иметь дополнения или делеции по сравнению с эталонной последовательностью для оптимального выравнивания между двумя последовательностями. Процент идентичности рассчитывается путем определения числа положений, в которых аминокислотный или нуклеотидный остаток идентичен между двумя последовательностями, например, между двумя полными последовательностями, разделяя количество идентичных положений на общее количество положений в окне выравнивания и умножая результат на 100 с получением процента идентичности между двумя последовательностями. В одном из вариантов осуществления процент идентичности последовательности антител определяют с последовательностями антител, максимально выравненными по соглашению о нумерации Кабат. После выравнивания, если область исследуемого антитела (например, полноразмерный зрелый вариабельный домен тяжелой или легкой цепи) сравнивается с той же областью эталонного антитела, то процентная идентичность последовательности между областями исследуемого и эталонного антитела представляет собой число положений, занятых одной и той же аминокислотой, как в области исследуемого, так и эталонного антитела, разделенное на общее количество выровненных положений двух областей, причем пробелы не учитываются, умноженное на 100 для преобразования в проценты.
Например, программа BLAST, «последовательности BLAST 2» (Tatusova et al., ʺBlast 2 sequences - a new tool for comparing protein and nucleotide sequencesʺ, FEMS Microbiol., 1999, Lett.174:247-250) доступная на сайте http://www.ncbi.nlm.nih.gov/gorf/bl2.html, может использоваться с параметрами по умолчанию (особенно для параметров «штраф за внесение пропуска»: 5 и «штраф за продление пропуска»: 2; выбранной матрицей, например, матрица «BLOSUM 62", предложенная программой); процент идентичности между двумя последовательностями для сравнения рассчитывается непосредственно программой.
Для аминокислотной последовательности с по меньшей мере 80%, например, 85%, 90%, 95% и 98% идентичностью со ссылочной аминокислотной последовательностью, предпочтительные примеры включают последовательности, которые содержат ссылочную последовательности, определенные изменения, особенно удаление, добавление или замену по крайней мере одной аминокислоты, усечение или расширение. В случае замены одной или нескольких последовательных или непоследовательных аминокислот предпочтительны замены, в которых замещенные аминокислоты заменены на «эквивалентные» аминокислоты. В данном случае выражение «эквивалентные аминокислоты» предназначено для обозначения любых аминокислот, которые могут быть замещены одной из структурных аминокислот, однако без изменения биологической активности соответствующих антител и тех конкретных примеров, которые определены ниже.
Эквивалентные аминокислоты могут быть определены либо по их структурной гомологии с аминокислотами, для которых они замещены, либо по результатам сравнительных испытаний биологической активности различных антител, которые могут быть получены. В качестве неограничивающего примера в нижеприведенной таблице 1 суммированы возможные замены, которые могут быть осуществлены, не приводя к существенной модификации биологической активности соответствующего модифицированного антитела; обратные замены, естественно, возможны при тех же условиях.
В контексте данного описания термины «патологический тау-белок» и «болезненный тау-белок» включают патологические тау-конформеры и структуры и включают все следующие: тау-белок типа IA, IB, IIA и IIB (подробно описаны в WO2004/007547 A2), беспорядоченный, патологический беспорядочный тау-белок (мономер, димер, тример, олигомер), патологический беспорядочный растворимый тау--белок, саркозил-нерастворимый тау-белок, внеклеточные тау-депозиты, тау-агрегаты, парные спиральные филаменты, нейрофибриллярные патологические формы, включая нейрофибриллярные поражения, клубки, нити, фибриллы, аксонные сфероиды, высокофосфорилированные формы усеченного тау-белка и полноразмерного тау-белка или любую другую форму тау-белка, связанную с AD или другой тауопатией, которая определяется антителами и/или тау-связывающими фрагментами, описанными в настоящем документе. Тау 151-391/4R (также называемый тауΔ(1-150; 392-441)/4R) представляет собой форму патологического тау-белка.
Термин «фармацевтически приемлемый» означает биологически или фармакологически совместимый для использования in vivo у животных или людей и предпочтительно означает одобренный регулирующим агентством федерального правительства или правительства штата или зарегистрированный в фармакопеи США или в другой общепризнанной фармакопеи для использования у животных и, в частности, у людей.
Термин «рекомбинантная клетка-хозяин» (или просто «клетка-хозяин»), как используется в настоящем документе, предназначен для обозначения клетки, в которую был введен рекомбинантный экспрессионный вектор. Следует понимать, что такие термины предназначены не только для конкретной рассматриваемой клетки, но и для потомства такой клетки. Поскольку некоторые модификации могут произойти в последующих поколениях из-за мутаций или влияния окружающей среды, такое потомство не может фактически быть идентичным родительской клетке, но тем не менее включено в объем термина «клетка-хозяин», как он используется в настоящем документе.
Термин «другая таупатия» включает все неврологические заболевания, которые сопровождаются появлением аномальных форм связанного с микротрубочками тау-белка в мозге пациентов. Термин включает, но не ограничивается ими, следующие заболевания: болезнь Альцгеймера, болезнь Герстманна-Штраусслера-Шейнкера, британскую деменцию, датскую деменцию, болезнь Пика, прогрессирующий надъядерный паралич, кортико-базальную дегенерацию, болезнь Аргирофильного зерна, комплекс болезнь Гуам-деменция, деменцию с преобладанием нейрофибриллярных клубков, таупатию белого вещества с глобулярными глиальными включениями, лобно-височную деменцию (например,FTDP-17) и паркинсонизм, связанный с хромосомой 17. См., например, Goedert M, Clavaguera F and Tolnay M. The propagation of prion-like protein inclusions in neurodegenerative diseases. Trends Neurol.Sci. В одном из вариантов осуществления одна или несколько из этих патологических форм тау-белка распознаются одним из антител или связывающих фрагментов, описанных в настоящем документе, по меньшей мере, в одном анализе. В некоторых вариантах осуществления анализ представляет собой IHC. В других вариантах осуществления анализ представляет собой ELISA.
Как используется в настоящем описании «специфически связывает» в отношении антитела означает, что антитело связывается с его целевым антигеном или эпитопом с большей аффинностью, чем это происходит со структурно отличающимся антигеном(ами) или эпитопом.
Как используется в настоящем описании термин «поверхностный плазмонный резонанс» относится к оптическому явлению, которое позволяет анализировать биоспецифические взаимодействия в реальном времени путем обнаружения изменений концентраций белка в биосенсорной матрице, например, с использованием системы BIAcore (Pharmacia Biosensor AB, Uppsala, Sweden and Piscataway, N.J.). Дальнейшее описание приведено в Примере 1 и в Jonsson, U., et al. (1993) Ann.Biol.Clin.51:19-26; Jonsson, U., et al. (1991) Biotechniques 11:620-627; Johnsson, B., et al. (1995) J.Mol.Recognit.8:125-131; and Johnnson, B., et al. (1991) Anal.Biochem.198:268-277.
«Одноцепочечные Fv» или «scFv» фрагменты антитела включают VH- и VL-домены антитела, где эти домены присутствуют в единственной полипептидной цепи. Предпочтительно, полипептид Fv дополнительно содержит полипептидный линкер между доменами VH и VL, который дает возможность scFv образовывать желаемую структуру для связывания антигена. Обзор scFv см. Pluckthun in The Pharmacology of Monoclonal Antibodies, том 113, Rosenburg and Moore eds., Springer-Verlag, New York, стр.269-315 (1994).
Как используется в настоящем описании термин «лечение» определяется как применение или введение терапевтического агента индивиду, у которого есть болезнь, признак заболевания или предрасположенность к заболеванию, с целью лечения, исцеления, облегчения, ослабления, изменения, коррекции, улучшения, нормализации или воздействия на болезнь, симптомы болезни или предрасположенность к болезни. Кроме того, если композиции по изобретению, либо сами по себе, либо в сочетании с другим терапевтическим агентом, излечивают, исцеляют, облегчают, ослабляют, изменяют, корректируют, улучшают, нормализуют или воздействуют по меньшей мере на один симптом болезни Альцгеймера или другой тауопатии, в отношении которой проводят лечение, по сравнению с таким симптомом при отсутствии использования композиции гуманизированного антитела против антитела или его тау-связывающего фрагмента, результат следует рассматривать как лечение основного расстройства независимо от того, все ли симптомы расстройства излечены, исцелены, облегчены, ослаблены, изменены, корректированы, улучшены, нормализованы или на которые было осуществлено воздействие.
Термин «вариабельный» относится к тому факту, что некоторые конкретные части вариабельных доменов широко различаются по последовательности среди антител и используются для связывания и специфичности каждого конкретного антитела для определенного антигена. Однако вариабельность неравномерно распределена по вариабельным доменам антител. Она сосредоточена в трех сегментах, называемым гипервариабельными доменами вариабельных доменов легкой цепи и тяжелой цепи. Более высококонсервативные части вариабельных доменов называются каркасными областями (FR).Каждый из вариабельных доменов нативных тяжелых и легких цепей содержит четыре FR, в основном использующие конфигурацию бета-структуры, соединенные тремя гипервариабельными областями, которые образуют петли, соединяющие и в некоторых случаях составляющие часть структуры бета-структуры. Гипервариабельные области (HVR) каждой цепи удерживаются вместе в непосредственной близости с помощью FR и вместе с гипервариабельными областями другой цепи вносят вклад в образование антиген-связывающего участка антител (см. Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed.Public Health Service, National Institutes of Health, Bethesda, Md.(1991)).Константные домены не участвуют непосредственно в связывании антитела с антигеном, но проявляют различные эффекторные функции, такие как участие антитела в антитело-зависимой клеточной цитотоксичности (ADCC).
Термин «вектор», как используется в настоящем описании, относится к молекуле нуклеиновой кислоты, способной переносить другую нуклеиновую кислоту, с которой он связан. Одним из типов векторов является «плазмида», которая относится к круглой двухцепочечной петле ДНК, в которую могут быть лигированы дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, в котором дополнительные сегменты ДНК могут быть лигированы в вирусный геном. Некоторые векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальное происхождение репликации, и эписомальные векторы млекопитающих). Другие векторы (например, неэпизомальные векторы млекопитающих) могут быть интегрированы в геном клетки-хозяина при введении в клетку-хозяина и, таким образом, реплицируются вместе с геномом хозяина. Более того, некоторые векторы способны управлять экспрессией нуклеиновых кислот, с которыми они функционально связаны. Такие векторы называются в настоящем документе «рекомбинантными векторами экспрессии» (или просто «векторы экспрессии»). В общем, экспрессирующие векторы, используемые в методах рекомбинантной ДНК, часто находятся в форме плазмид. В настоящем описании «плазмида» и «вектор» могут использоваться взаимозаменяемо, поскольку плазмида является наиболее часто используемой формой вектора. Однако предполагается, что изобретение включает такие другие формы векторов экспрессии, такие как вирусные векторы (например, дефектные по репликации ретровирусы, аденовирусы и адено-ассоциированные вирусы), которые выполняют эквивалентные функции.
Настоящее описание может быть легче понято со ссылкой на следующее подробное описание конкретных вариантов осуществления, включенных в настоящее описание. Хотя настоящее описание было описано со ссылкой на конкретные детали некоторых его вариантов осуществления, не предполагается, что такие детали следует рассматривать как ограничения объема раскрытия.
Гуманизированные антитела, которые связываются с болезненным тау-белком
Приведенные в настоящем документе представляют собой первые гуманизированные антитела против болезненного/патологического тау-белка, которые способны распознавать четыре различные области тау-белка в зависимости от конформации. Более конкретно, гуманизированные антитела, описанные в настоящем документе, способны связывать по меньшей мере один, два, три или четыре QT1-QT4 таким образом, что они отличаются от дикого типа/нормального тау-белка и конформации тау-белка, которые связаны с AD (болезненный тау-белок). В некоторых вариантах осуществления два, три или четыре из QT1-QT4 могут быть одновременно заняты этими антителами. Другими словами, антитела и тау-связывающие фрагменты, описанные в настоящем документе, имеют в качестве своего «эпитопа» любой, один или несколько, следующих четырех тау-сайтов, некоторые или все из которых являются конформационными эпитопами:268-HQPGGG-273 (SEQ ID NO:148) (в пределах 1-го повторяющегося домена тау-белка), 299-HVPGGG-304 (SEQ ID NO:149) (в пределах 2-го повторяющегося домена тау-белка), 330-HKPGGG-335 (SEQ ID NO:150) (в пределах 3-го повторяющегося домена тау-белка), 362-HVPGGG- 367 (SEQ ID №:149) (в пределах 4-го повторяющегося домена тау-белка).Эти эпитопы также указаны в настоящем документе как QT1, QT2, QT3 и QT4, соответственно.DC8E8 связывается со всеми QT1-QT4; на самом деле, эпитоп DC8E8 представляет собой HXPGGG, где X представляет собой любую аминокислоту.
В одном варианте осуществления антитела и тау-связывающие фрагменты обладают аффиностью к тау 151-139/4R, которые по меньшей мере на 80% так же эффективны, если не больше, чем исходное моноклональное антитело DC8E8 мыши. В одном из вариантов осуществления антитела и тау-связывающие фрагменты сохраняют специфичность в отношении эпитопов, распознаваемых антителом DC8E8 мыши. В одном из вариантов осуществления эти антитела обладают одним или более благоприятными биохимическими свойствами (например, константными областями человека и, таким образом, сниженной иммуногенностью, высокими уровнями экспрессии, высокой растворимостью, отсутствием значительной агрегации белка при очистке, высокой стабильностью), что делает их оптимальными для использования при лечении AD и связанных с ним таупатий у людей.
Гуманизация DC8E8 была эмпирически оптимизирована путем манипуляции с остатками каркасной области. Исходный гуманизированный вариант RHA/RKA (AX001) обнаруживал 10-кратное снижение аффинности связывания в отношении тау-белка по сравнению с химерной конструкцией DC8E8.Эти данные подразумевают, что один или несколько аминокислотных остатков каркасных областей имеют важное значение для гуманизации DC8E8 с незначительной результирующей потерей активности связывания. В противоположность этому однократная обратная мутация каркасной области была достаточной для восстановления аффинности связывания в гуманизированном антителе RHD (AX004). Это превосходство было неожиданным. Другие одноточечные обратные мутации не имели такого же неожиданного преимущества при связывании аффинности. См., например, конструкции RHF/RKA (AX006) и RHG/RKA (AX007).И следующее лучшее антитело несло 10 обратных мутаций. См. AX002.Из всех тестированных комбинаций обратных мутаций AX004 показал лучшую аффинность связывания с тау-белком (в анализе, описанном в настоящем документе), несмотря на наличие одной обратной мутации и в отличие от других одиночных конструкций с обратной мутацией. Другие гуманизированные конструкции с улучшенной аффинностью включают, например, AX002, AX005, AX037 и AX014, AX016, AX017, AX038 в вариантах легкой цепи RKA и RKB, соответственно.
Также представлены тау-связывающие фрагменты (например, фрагменты антител) гуманизированных антител, описанных в настоящем документе. Эти фрагменты также способны связывать по меньшей мере один, два, три или четыре QT1-QT4 (как определено выше) таким образом, что они отличаются от дикого типа/нормального тау-белка и конформации тау-белка, которые связаны с AD. В некоторых вариантах осуществления все четыре эпитопа QT1-QT4 могут быть заняты четырьмя антителами или тау-связывающими фрагментами, описанными в настоящем документе. В некоторых вариантах осуществления фрагменты или части связываются с тау-белком с одинаковой аффинностью и свойствами моноклонального антитела DC8E8 мыши. Например, в настоящем изобретении представлены фрагменты или части антитела, способные связываться с одним или несколькими QT1-QT4, включают, но ими не ограничиваются, Fab (например, путем расщепления папаином), Fd, Fab' (например, путем расщепления пепсином и частичного восстановления) и F(ab')2 (например, путем расщепления пепсином), facb (например, путем расщепления плазмином), pFc' (например, путем расщепления пепсином или плазмином), Fd (например, путем расщепления пепсином, частичное восстановление и повторная агрегация), Fv или scFv (например, с помощью методов молекулярной биологии). См. также, William E.Paul (ed.) Fundamental Immunology, 6th Edition, Lippincott Williams & Wilkins, NY, N.Y. (2008), включенную в настоящий документ в качестве ссылки в полном объеме. Любые другие фрагменты, время полужизни которых было увеличено путем конъюгации с другими молекулами, включая ПЭГилированные фрагменты, также входят в объем настоящего изобретения. Определенные фрагменты могут быть получены ферментативным расщеплением, синтетическими или рекомбинантными способами, которые известны в данной области техники или в соответствии с настоящим изобретением. Антитела также могут быть получены в различных усеченных формах с использованием генов антитела, в которых один или несколько стоп-кодонов введены выше природного стоп-сайта. Например, комбинированный ген, кодирующий часть тяжелой цепи F(ab')2, может быть сконструирован так, чтобы включать последовательности ДНК, кодирующие домен CH1 и/или шарнирную область тяжелой цепи. Различные части антител могут быть соединены вместе химическим образом обычными методиками или могут быть получены в виде непрерывного белка с использованием обычных способов генной инженерии.
В зависимости от аминокислотной последовательности константного домена тяжелых цепей интактные антитела могут быть отнесены к разным «классам». В одном из вариантов осуществления существует шесть основных классов интактных антител: IgA, IgD, IgE, IgG, IgY и IgM, и некоторые из них могут быть далее разделены на «подклассы» (изотипы), например,IgG1, IgG2, IgG3, IgG4, IgA и IgA2.Константные домены тяжелой цепи, которые соответствуют различным классам антител, называются альфа (α), дельта (δ), эпсилон (ε), гамма (γ) и мю (μ), соответственно. Структуры субъединиц и трехмерные конфигурации различных классов иммуноглобулинов хорошо известны. В одном из вариантов осуществления описанные в настоящем документе антитела имеют константные области любого из существующих иммуногенных изотипов. Например, константные области могут быть лямбда- или каппа-областью и гамма-1, гамма-2, гамма-3 или гамма-4 областями. Константные области смешанных изотипов также входят в объем настоящего описания (например,IgG1, смешанный с IgG4).Было замечено, что некоторые изотипы превосходят другие. Bruggemann M, Williams GT, Bindon CI, Clark MR, Walker MR, Jefferis R, Waldmann H, Neuberger MS (1987) Comparison of the effector functions of human immunoglobulins using a matched set of chimeric antibodies.J.Exp.Med. 166, 1351-1361; Bindon CI, Hale G, Bruggemann M, Waldmann H (1988) Human monoclonal IgG isotypes differ incomplement activating function at the level of C4 as well as C1q.J.Exp.Med.168, 127-42; Shaw DR, Khazaeli MB, LoBuglio AF (1988) Mouse/human chimeric antibodies to a tumor associated antigen:biologic activity of the four human IgG subclasses.J.Natl.Cancer Inst.80, 1553-9; Steplewski Z, Sun LK, Shearman CW, Ghrayeb J, Daddona P, Koprowski,H (1988) Biological activity of human-mouse IgG1, IgG2, IgG3, and IgG4 chimeric monoclonal antibodies with antitumor specificity.Proc.Natl.Acad.Sci.USA 85, 4852-6. В одном из экспериментов, описанных в этих ссылках, изотипы IgM, IgG1, IgG2, IgG3 человека (два аллотипа), IgG4, IgA и IgE сравнивали на аутологичный опресредованный комплементом лизис, а также на антителозависимую клеточную цитотоксичность (ADCC).Для опосредованного комплементом лизиса IgM и IgG1 человека оказались наиболее эффективными с двумя лучшими аллотипами IgG3.IgG2 дал слабый лизис, тогда как другие изотипы, по-видимому, не давали лизиса. Результаты для ADCC заключались в том, что IgG1 опять оказался очень эффективным, за ним шел IgG2, IgG3, или IgG4, в зависимости от анализа (например, тип клеток). Другие изотипы, включая IgM, оказались неэффективными. Но антитела имеют много других активностей (например, способствуют опсонизации макрофагами), и в конечном итоге трудно или даже невозможно предсказать, какой изотип будет иметь наилучший набор свойств для его желаемого использования.
Другим фактором, влияющим на иммуногенность гуманизированного антитела, является существование полиморфных детерминант в константной области. Эти различия могут быть сведены к минимуму для снижения антигенности. В популяции имеется 18 аллотипов IgG человека, наблюдаемых с разумной частотой: IgG1 имеет 4; IgG2 имеет 1; IgG3 имеет 13; IgG4 имеет 0. WHO (1976) Review of the notation for the allotypic and related markers of human immunoglobulins.Eur.J.Immunol. 6, 599-601. Кроме того, существуют три аллотипа легких цепей человека.Некоторые аллотипы присутствуют у некоторых людей и отсутствуют у других. Некоторые из них преимущественно экспрессированы среди японского населения.
В данной области описано множество способов гуманизирования не-человеческих антител. В одном из вариантов осуществления гуманизированное антитело содержит один или несколько аминокислотных остатков, введенных в него из источника, который не является человеком. Эти нечеловеческие аминокислотные остатки часто упоминаются как «импортные» остатки, которые обычно берут из "импортного" вариабельного домена. В одном из вариантов осуществления гуманизирование может быть по существу выполнено в соответствии со способом Winter et al. (Jones et al, Nature, 321:522-525 (1986); Riechmann et al, Nature, 332:323-327 (1988); Verhoeyen et al., Science, 239: 1534-1536 (1988)), путем замены последовательностей гипервариабельной области соответствующими последовательностями антитела человека. Соответственно, такими «гуманизированными» антителами являются химерные антитела (патентСША№4816567), в которых существенно меньше, чем в интактном вариабельном домене человека, заменено соответствующей последовательностью из видов, отличных от человека. В некоторых вариантах осуществления гуманизированные антитела являются антителами человека, в которых некоторые остатки гипервариабельной области и, возможно, некоторые остатки FR, заменены остатками из аналогичных сайтов антител грызунов.
Выбор вариабельных доменов человека, как легких, так и тяжелых, для использования при получении гуманизированных антител важен для уменьшения антигенности. Согласно методу так называемого "приближения" последовательность вариабельного домена антитела грызуна скринируют против полной библиотеки известных последовательностей вариабельного домена человека. Последовательность человека (полноразмерная вариабельная область или только каркасные области), которые наиболее близки к грызунам, затем принимают в качестве человеческой каркасной области (FR) для гуманизированного антитела (Sims et al., J.Immunol.,151:2296 (1993); Chothia et al, J.Mol.Biol.,196:901 (1987)). В другом способе используют конкретную каркасную область, полученную из консенсусной последовательности всех человеческих антител конкретной подгруппы легких или тяжелых цепей.Та же каркасная область может быть использована для нескольких различных гуманизированных антител (Carter et al., Proc.Natl.Acad.Sci.USA, 89:4285 (1992); Presta et al., J.Immunol, 151:2623 (1993)).
В некоторых вариантах осуществления важно, чтобы антитела были гуманизированы с сохранением высокой аффиности к антигену и других благоприятных биологических свойств исходного (например, антитела мыши). Для достижения этой цели согласно одному варианту осуществления гуманизированные антитела получают путем анализа родительских последовательностей и различных концептуальных гуманизированных продуктов, используя трехмерные модели родительских и гуманизированных последовательностей. Трехмерные модели иммуноглобулинов общедоступны и известны специалистам в данной области техники. Имеются компьютерные программы, которые иллюстрируют и отображают вероятные трехмерные конформационные структуры выбранных кандидатных последовательностей иммуноглобулина. Проверка этих дисплеев позволяет проанализировать вероятную роль остатков в функционировании последовательности иммуноглобулина-кандидата, т.е. анализ остатков, которые влияют на способность иммуноглобулина-кандидата связывать антиген. Таким образом, остатки FR могут быть выбраны и объединены из последовательностей реципиента и последовательностей для "импорта", так что достигается желаемая характеристика антитела, такая как повышенная аффинность к целевому антигену(ам).Как правило, остатки гипервариабельной области непосредственно и наиболее существенно оказывают влияние на связывание антигена.
В предыдущей таблице 2 представлены SEQ ID NO для некоторых аминокислотных последовательностей, описанных в настоящем документе. В другом варианте осуществления гуманизированное антитело или тау-связывающий фрагмент, как описано в настоящем документе, содержит SEQ ID NO:1, 2, 3, в качестве CDR 1, 2 и 3 тяжелой цепи, соответственно, и SEQ ID NO:4, 5, 6, в качестве CDR 1, 2 и 3 легкой цепи, соответственно. В некоторых вариантах осуществления это антитело или фрагмент содержит по меньшей мере один CDR, как определено в соответствии с Кабат, чья последовательность по меньшей мере на 80%, предпочтительно по меньшей мере на 85, 90, 95 и 98% идентична после оптимального выравнивания с CDR любой из SEQ ID NO:1-6.
В одном из вариантов осуществления антитело (AX001) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHA (SEQ ID NO:13) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет константные области либо IgG1 (AX001-IgG1), либо IgG4 (AXON001-IgG4).
В одном из вариантов осуществления антитело (AX002) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHB (SEQ ID NO:14) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет константные области либо IgG1 (AX002-IgG1), либо IgG4 (AXON002-IgG4).
В одном из вариантов осуществления антитело (AX003) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHС (SEQ ID NO:15) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX003-IgG1), либо IgG4 (AXON003-IgG4).
В одном из вариантов осуществления антитело (AX004) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHD (SEQ ID NO:16) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX004-IgG1) или IgG4 (AXON004-IgG4).
В одном из вариантов осуществления антитело (AX005) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHE (SEQ ID NO:17) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет константные области либо IgG1 (AX005-IgG1), либо IgG4 (AXON005-IgG4).
В одном из вариантов осуществления антитело (AX006) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHF (SEQ ID NO:18) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX006-IgG1) или IgG4 (AXON006-IgG4).
В одном из вариантов осуществления антитело (AX007) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHG (SEQ ID NO:19) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX007-IgG1) или IgG4 (AXON007-IgG4).
В одном из вариантов осуществления антитело (AX008) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHH (SEQ ID NO:20) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX008-IgG1) или IgG4 (AXON008-IgG4).
В одном из вариантов осуществления антитело (AX009) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHI (SEQ ID NO:21) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX009-IgG1) или IgG4 (AXON009-IgG4).
В одном из вариантов осуществления антитело (AX010) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHJ (SEQ ID NO:22) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX010-IgG1) или IgG4 (AXON010-IgG4).
В одном из вариантов осуществления антитело (AX011) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHK (SEQ ID NO:23) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX011-IgG1) или IgG4 (AXON011-IgG4).
В одном из вариантов осуществления антитело (AX012) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHL (SEQ ID NO:24) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX012-IgG1) или IgG4 (AXON012-IgG4).
В одном из вариантов осуществления антитело (AX013) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHA (SEQ ID NO:13) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX013-IgG1) или IgG4 (AXON013-IgG4).
В одном из вариантов осуществления антитело (AX014) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHB (SEQ ID NO:14) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX014-IgG1) или IgG4 (AXON014-IgG4).
В одном из вариантов осуществления антитело (AX015) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHС (SEQ ID NO:15) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX015-IgG1) или IgG4 (AXON015-IgG4).
В одном из вариантов осуществления антитело (AX016) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHD (SEQ ID NO:16) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX016-IgG1) или IgG4 (AXON016-IgG4).
В одном из вариантов осуществления антитело (AX017) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHE (SEQ ID NO:17) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX017-IgG1) или IgG4 (AXON017-IgG4).
В одном из вариантов осуществления антитело (AX018) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHF (SEQ ID NO:18) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX018-IgG1), либо IgG4 (AXON018-IgG4).
В одном из вариантов осуществления антитело (AX019) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHG (SEQ ID NO:19) и вариабельный домен легкой цепи RKA (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX019-IgG1), либо IgG4 (AXON019-IgG4).
В одном из вариантов осуществления антитело (AX020) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHH (SEQ ID NO:20) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX020-IgG1) или IgG4 (AXON020-IgG4).
В одном из вариантов осуществления антитело (AX021) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHI (SEQ ID NO:21) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX021-IgG1), либо IgG4 (AXON021-IgG4).
В одном из вариантов осуществления антитело (AX022) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHJ (SEQ ID NO:22) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX022-IgG1), либо IgG4 (AXON022-IgG4).
В одном из вариантов осуществления антитело (AX023) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHK (SEQ ID NO:23) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX023-IgG1), либо IgG4 (AXON023-IgG4).
В одном из вариантов осуществления антитело (AX024) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHL (SEQ ID NO:24) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX024-IgG1), либо IgG4 (AXON024-IgG4).
В одном из вариантов осуществления антитело (AX025) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHA (SEQ ID NO:13) и вариабельный домен легкой цепи VK (SEQ ID NO:8)). Это антитело имеет либо константные области IgG1 (AX025-IgG1), либо IgG4 (AXON025-IgG4).
В одном из вариантов осуществления антитело (AX026) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHB (SEQ ID NO:14) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX026-IgG1) или IgG4 (AXON026-IgG4).
В одном из вариантов осуществления антитело (AX027) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHС (SEQ ID NO:15) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX027-IgG1), либо IgG4 (AXON027-IgG4).
В одном из вариантов осуществления антитело (AX028) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHD (SEQ ID NO:16) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX028-IgG1), либо IgG4 (AXON028-IgG4).
В одном из вариантов осуществления антитело (AX029) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHE (SEQ ID NO:17) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX029-IgG1), либо IgG4 (AXON029-IgG4).
В одном из вариантов осуществления антитело (AX030) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHF (SEQ ID NO:18) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX030-IgG1), либо IgG4 (AXON030-IgG4).
В одном из вариантов осуществления антитело (AX031) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHG (SEQ ID NO:19) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX031-IgG1), либо IgG4 (AXON031-IgG4).
В одном из вариантов осуществления антитело (AX032) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHH (SEQ ID NO:20) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX032-IgG1), либо IgG4 (AXON032-IgG4).
В одном из вариантов осуществления антитело (AX033) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHI (SEQ ID NO:21) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX033-IgG1), либо IgG4 (AXON033-IgG4).
В одном из вариантов осуществления антитело (AX034) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHJ (SEQ ID NO:22) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX034-IgG1), либо IgG4 (AXON034-IgG4).
В одном из вариантов осуществления антитело (AX035) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHK (SEQ ID NO:23) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX035-IgG1), либо IgG4 (AXON035-IgG4).
В одном из вариантов осуществления антитело (AX036) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHL (SEQ ID NO:24) и вариабельный домен легкой цепи VK (SEQ ID NO:8). Это антитело имеет либо константные области IgG1 (AX036-IgG1), либо IgG4 (AXON036-IgG4).
В одном из вариантов осуществления антитело (AX037) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHM (SEQ ID NO:25) и вариабельный домен легкой цепи RKA (SEQ ID NO:26). Это антитело имеет либо константные области IgG1 (AX037-IgG1), либо IgG4 (AXON037-IgG4).
В одном из вариантов осуществления антитело (AX038) или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи RHM (SEQ ID NO:25) и вариабельный домен легкой цепи RKB (SEQ ID NO:27). Это антитело имеет либо константные области IgG1 (AX037-IgG1), либо IgG4 (AXON037-IgG4).
В еще одном варианте осуществления настоящее изобретение относится к тяжелой цепи антитела, содержащей вариабельный домен, выбранный из любого вариабельного домена тяжелой цепи RHA, RHB, RHC, RHD, RHE, RHF, RHG, RHH, RHI, RHJ, RHK, RHL и RHM. Любой из этих вариабельных доменов может быть связан с константной областью любого изотипа человека, включая константные области со смешанными изотипами.
В еще одном варианте осуществления изобретение относится к легкой цепи антитела, содержащей вариабельный домен, выбранный из RKA и RKB. Любой из этих вариабельных доменов может быть связан с константной областью любого изотипа человека, включая константные области со смешанными изотипами.
В другом варианте осуществления настоящее изобретение относится к тяжелой цепи антитела с любой SEQ ID NO:28-40 и 43-55.
В еще одном варианте осуществления изобретение относится к легкой цепи антитела, выбранной из SEQ ID NO:57-59.
Вариабельные домены тяжелых и легких цепей гуманизированных антител могут быть связаны по меньшей мере с частью константной области человека. Как описано выше в разделе "Определения", выбор константной области частично зависит от того, являются ли желательными антитело-зависимая клеточная цитотоксичность, антитело-зависимый клеточный фагоцитоз и/или комплемент-зависимая цитотоксичность. В одном из вариантов осуществления изотопы IgG1 и IgG3 человека имеют комплемент-зависимую цитотоксичность и изотипы IgG2 и IgG4 человека этого не имеют. В одном из вариантов осуществления IgG1 и IgG3 человека также индуцируют более сильные клеточные эффекторные функции, чем IgG2 и IgG4 человека. Константными областями легкой цепи могут быть лямбда или каппа. Пример константной области легкой цепи каппа человека имеет аминокислотную последовательность SEQ ID NO:170.N-концевой аргинин с SEQ ID NO:170 может быть пропущен, и в этом случае константная область легкой цепи каппа имеет аминокислотную последовательность SEQ ID NO: 171.Пример константной области тяжелой цепи IgG1 человека имеет аминокислотную последовательность SEQ ID NO:172.Пример константной области тяжелой цепи IgG4 человека имеет аминокислотную последовательность SEQ ID NO:173.Антитела могут быть экспрессированы в виде тетрамеров, содержащих две легкие и две тяжелые цепи, в виде отдельных тяжелых цепей, легких цепей, как Fab, Fab', F(ab')2 и Fv, или в виде одноцепочечных антител, в которых зрелые вариабельные домены тяжелой и легкой цепи связаны посредством спейсера.
Последовательности кДНК, кодирующие константные области человеческих антител, известны специалистам в данной области. В одном из вариантов осуществления примеры последовательностей кДНК, доступные, например, из GenBank, каждый включен в качестве ссылки в полном объеме, являются следующими: константная область тяжелой цепи IgG1 человека: Номер доступа в GenBank:J00228; константная область тяжелой цепи IgG2 человека: Номер доступа в GenBank:J00230; константная область тяжелой цепи IgG3 человека: Номер доступа в GenBank:X04646; константная область тяжелой цепи IgG4 человека: Номер доступа в GenBank:K01316; и константной области легкой цепи каппа человека: Номер доступа в GenBank:J00241. В одном из вариантов осуществления константная область может быть дополнительно модифицирована в соответствии с известными способами. Например, в константной области IgG4 остаток S241 может быть мутирован в остаток пролина (Р), чтобы обеспечить полное образование дисульфидного мостика в шарнирной области (см., например, Angel et al.,Mol.Immunol.1993; 30:105-8).
Для большей ясности в приведенной ниже таблице 3 суммированы различные аминокислотные последовательности, соответствующие различным вариабельным областям некоторых гуманизированных антител, описанных в настоящем документе.
На таблице 4 ниже приведены аминокислотные последовательности, соответствующие различным полноразмерным последовательностям мышиных и гуманизированных антител, описанных в настоящем документе.
На таблице 5 ниже приведены различные аминокислотные последовательности, соответствующие различным полноразмерным последовательностям легких цепей гуманизированных антител, описанных в настоящем документе.
Также в изобретении раскрыты химерные антитела и их тау-связывающие фрагменты. В одном из вариантов осуществления химерное антител или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи DC8E8 VH (SEQ ID NO:9) и вариабельный домен легкой цепи DC8E8 VK (SEQ ID NO:10) вместе с константной областью IgG1 человека (SEQ ID NO:172) тяжелой цепи и константной областью каппа (SEQ ID NO:170) легкой цепи. В еще одном варианте осуществления химерное антител или его тау-связывающий фрагмент содержит вариабельный домен тяжелой цепи DC8E8 VH (SEQ ID NO:9) и вариабельный домен легкой цепи DC8E8 VK (SEQ ID NO:10) вместе с константной областью IgG4 человека (SEQ ID NO:173) тяжелой цепи и константной областью каппа (SEQ ID NO:170) легкой цепи.
В одном из вариантов осуществления гуманизированное антитело или его тау-связывающий фрагмент/часть получен рекомбинантным способом. В другом варианте осуществления гуманизированное антитело или его тау-связывающий фрагмент/часть получен, по меньшей мере частично, путем химического синтеза. В одном из вариантов осуществления химерное антитело или его тау-связывающий фрагмент/часть получен рекомбинантным способом. В другом варианте осуществления химерное антитело или его тау-связывающий фрагмент/часть получен, по меньшей мере частично, путем химического синтеза.
В таблице 6 суммированы последовательности некоторых других молекул, связанных с гуманизацией, описанных в настоящем документе.
Рассматриваются модификации(я) аминокислотных последовательностей антител, описанных в настоящем документе. Например, может быть желательным улучшение аффинности и/или других биологических свойств антитела. Варианты аминокислотных последовательностей антитела получают путем введения соответствующих нуклеотидных изменений в нуклеиновую кислоту антитела или, или путем пептидного синтеза. Такие модификации включают, например, делеции и/или вставки и/или замены остатков в аминокислотных последовательностях антитела. Для получения конечной конструкции можно ввести любую комбинацию делеций, вставок и замен при условии, что конечная конструкция будет обладать желательными характеристиками. Аминокислотные изменения также могут изменять посттрансляционные процессы антитела, такие как изменение количества или положения сайтов гликозилирования.
Также в настоящем описании представлены антитела и связывающие фрагменты, последовательность которых была изменена путем введения по меньшей мере одной, в частности, по меньшей мере двух, более предпочтительно, по меньшей мере 3 или более консервативных замен в последовательности SEQ ID NO:13-25 и SEQ ID NO:26 и 27, соответственно, так что антитело по существу сохраняет свою полную функциональность.
Некоторые аминокислоты из остатков каркасной области зрелого вариабельного домена человека могут быть выбраны для замещения на основании их возможного влияния на конформацию CDR и/или на связывание с антигеном, опосредования взаимодействия между тяжелыми и легкими цепями, взаимодействия с константной областью, являющейся сайтом для желательной или нежелательной посттрансляционной модификации, являющейся необычным остатком для ее положения в последовательности вариабельного домена человека и, следовательно, потенциально иммуногенной, среди других причин. Специалисту в данной области известно как выбирать определенные аминокислоты для замены, а затем оценивать результат такой замены. Во многих вариантах осуществления положения замен в каркасных областях и аминокислоты для замены выбраны эмпирически.
Аминокислотные замены также могут быть сделаны в CDR. Одним из возможных вариантов является замена определенных остатков в CDR мышиного антитела DC8E8 соответствующими остатками из последовательностей CDR человека, обычно из CDR акцепторных последовательностей человека, используемых при конструировании характерных гуманизированных антител. В некоторых антителах для сохранения связывания в гуманизированном антителе необходима только часть CDR, а именно подмножество остатков CDR, необходимых для связывания, называемых SDR. Остатки CDR, не контактирующие с антигеном, и не находящиеся в SDR, могут быть определены на основе результатов предыдущих исследований (например, остатки H60-H65 в H2 CDR часто не являются обязательными), из областей CDR по Кабат, лежащих за пределами гипервариабельных петлей по Chothia (Chothia, J.Mol.Biol.196:901, 1987), путем молекулярного моделирования и/или эмпирически, или как описано Gonzales et al.,Mol.Immunol.41:863 (2004). В таких гуманизированных антителах в положениях, в которых отсутствует один или несколько донорных остатков CDR или в которых отсутствует весь донорный CDR, аминокислота, занимающая это положение, может быть аминокислотой, занимающей соответствующее положение (по нумерации Кабат) в акцепторной последовательности антитела. Количество таких замен акцептора для донорных аминокислот, которые должны быть включены в CDR, отражает баланс различных соображений. Такие замены потенциально выгодны для уменьшения количества аминокислот мыши в гуманизированном антителе и, следовательно, уменьшают вероятность иммуногенности. Однако замены также могут вызвать изменения аффинности, а значительное уменьшение аффинности желательно избегать. Положения замены в CDR и аминокислоты для замены выбраны эмпирически.
В одном из вариантов осуществления антитела и их тау-связывающие фрагменты содержат тяжелую цепь, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2 и 3, соответственно, и которая по крайней мере на 90% идентична зрелой тяжелой цепи с SEQ ID NO:28-40 (полноразмерные RHA-RHM); и легкую цепь, содержащую CDR-L1, CDR-L2 и CDR-L3 SEQ ID NO:4, 5 и 6, соответственно, и которая по меньшей мере на 90% идентична зрелой легкой цепи с SEQ ID NO:57 (RKA) или SEQ ID NO:58 (RKB). В некоторых вариантах осуществления зрелая тяжелая цепь по меньшей мере на 95%, 96%, 97%, 98% или 99% идентична любой из SEQ ID NO:28-40. В некоторых вариантах осуществления зрелая легкая цепь по меньшей мере на 95%, 96%, 97%, 98% или 99% идентична любой SEQ ID NO:57 или SEQ ID NO:58.
Подходящий способ идентификации определенных остатков или областей антитела, которые могут быть предпочтительными местами мутагенеза, называется «мутагенезом с аланиновым сканированием», как описано в статье Cunningham and Wells Science, 244:1081-1085 (1989). В данном случае, остаток или группу остатков-мишеней идентифицировали (например, заряженные остатки, такие как Arg, Asp, His, Lys и Glu) и замещали на нейтрально или отрицательно заряженные аминокислоты (наиболее предпочтительно, аланин или полиаланин) для того, чтобы повлиять на взаимодействие аминокислот и антигена. Эти места аминокислот, проявляющих функциональную чувствительность к заменам, затем уточняются путем введения дополнительных или других вариантов на сайтах замещения. Таким образом, хотя сайт введения варианта аминокислотной последовательности предопределен, природа мутации per se необязательно должна быть предопределена. Например, для того, чтобы проанализировать эффективности мутации на данном сайте на целевом кодоне или в области проводят ala-сканирование или случайный мутагенез, и экспрессированные варианты антитела скринируют на желаемую активность.
Вставки в аминокислотную последовательность включают амино- и/или карбокси-концевые слитые варианты длиной от одного остатка до полипептидов, содержащих сто или более остатков, а также вставки одного или множества аминокислотных остатков внутри последовательности. Примеры концевых вставок включают антитело с N-концевым остатком метионина или антитело, слитое с другим терапевтическим агентом. Другие варианты вставок молекулы антитела включают слитый с N- или C-концом антитела фермент (например, в случае ADEPT) или полипептид, что повышает период полураспада антитела из сыворотки.
Другим типом варианта является вариант замены аминокислоты. Эти варианты имеют по меньшей мере один аминокислотный остаток в молекуле антитела, замененный другим остатком. В одном из вариантов осуществления сайты, представляющие наибольший интерес для замещающего мутагенеза, включают гипервариабельные области, но также рассматриваются изменения в FR. Консервативные замены показаны в таблице выше, а также ниже. Могут быть введены более существенные изменения, обозначенные в классах аминокислот, а продукты скринированы.
Существенные изменения биологических свойств антитела осуществляют путем выбора замен, которые значительно отличаются по своему эффекту на поддержание (a) структуры полипептидного скелета в области замещения, например, бета-структуры или спиральной конформации (b) заряда или гидрофобности молекулы на целевом сайте, или (c) объема боковой цепи. Аминокислоты могут быть сгруппированы по сходству свойств своих боковых цепей (в A.L.Lehninger, in Biochemistry, second ed., стр.73-75, Worth Publishers, New York (1975)):
(1) неполярные: Ala (A), Val (V), Leu (L), Ile (I), Pro (P), Phe (F), Trp (W), Met (M)
(2) незаряженные полярные: Gly (G), Ser (S), Thr (T), Cys (C), Tyr (Y), Asn (N), Gln (Q)
(3) кислые: Asp (D), Glu (E)
(4) основные: Lys (K), Arg (R), His (H)
Альтернативно, природные остатки можно разделить на группы на основе других общих свойств боковой цепи:
(1) гидрофобные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) нейтральные гидрофильные:Cys, Ser, Thr, Asn, Gln;
(3) кислые:Asp, Glu;
(4) основные: His, Lys, Arg;
(5) остатки, влияющие на ориентацию цепи: Gly, Pro;
(6) ароматические: Trp, Tyr, Phe.
Неконсервативные замены обычно приводят к замене представителя одного из этих классов на представителя другого класса.
Любой остаток цистеина, не участвующий в поддержании корректной конформации антитела, также может быть замещен, обычно серином, для улучшения окислительной стабильности молекулы и предотвращения аберрантного перекрестного связывания. И наоборот, цистеиновые связи могут быть добавлены к антителу для улучшения его стабильности (в частности, когда антитело представляет собой фрагмент антитела, такой как фрагмент Fv).
Особенно предпочтительный тип замены включает замену одного или более остатков гипервариабельной области исходного антитела (например, гуманизированного антитела или антитела человека).Как правило, получающийся вариант(ы), выбранные для дальнейшей разработки, будут иметь улучшенные биологические свойства по сравнению с исходным антителом, из которого они получены. Удобный способ получения таких вариантов замещения включает созревание аффинности с использованием фагового дисплея.Вкратце, несколько сайтов гипервариабельных областей (например,6-7 сайтов) мутируют с получением всех возможных аминокислотных замен в каждом сайте.Полученные таким образом варианты антител моновалентным образом представлены на поверхности частиц нитевидных фагов в виде слияний с продуктом гена III M13, упакованным в каждой частице. Затем варианты, представленные на поверхности фага скринируют на их биологическую активность (например, аффинность связывания), как описано в настоящем документе. Для идентификации кандидатных сайтов гипервариабельной области для модификации может быть выполнен мутагенез со сканированием на аланин для идентификации остатков гипервариабельной области, вносящих существенный вклад в связывание с антигеном. Альтернативно, или дополнительно, может быть полезным проанализировать кристаллическую структуру комплекса антиген-антитело для выявления точек контакта между антителом и тау-белком человека. Такие контактные остатки и соседние остатки являются кандидатами для замены в соответствии с методами, разработанными в настоящем документе. После получения таких вариантов панель вариантов подвергают скринингу, как описано в настоящем документе, и антитела с превосходными свойствами в одном или нескольких соответствующих анализах могут быть выбраны для дальнейшей разработки.
Другой тип варианта аминокислоты антитела изменяет исходную структуру гликозилирования антитела. Под изменением понимают удаление одного или нескольких углеводных групп, обнаруженных в этом антителе, и/или добавление одного или нескольких сайтов гликозилирования, которые отсутствуют в этом антителе.
Гликозилирование антител обычно является N-связанным или O-связанным.N-связанным является присоединение углеводной группы к боковой цепи аспарагинового остатка. Трипептидные последовательности аспарагин-X-серин и аспарагин-Х-треонин, где Х представляет собой любую аминокислоту, кроме пролина, являются распознающими последовательностями для ферментативного присоединения углеводной группы к боковой цепи аспарагина. Таким образом, присутствие любой из этих трипептидных последовательностей в полипептиде создает потенциальный сайт гликозилирования.O-связанное гликозилирование относится к присоединению одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, чаще всего серину или треонину, хотя можно также использовать 5-гидроксипролин или 5-гидроксилизин.
Добавление сайтов гликозилирования к антителу удобно осуществлять путем изменения аминокислотной последовательности таким образом, чтобы она содержала одну или несколько описанных выше трипептидных последовательностей (для сайтов N-связанного гликозилирования). Изменение также может быть сделано путем добавления или замены одного или нескольких остатков серина или треонина на последовательность исходного антитела (для сайтов O-связанного гликозилирования).
Если антитело содержит Fc-область, то можно модифицировать углевод, присоединенный к ней. Например, антитела со зрелой углеводородной структурой, которые не содержат фукозу, присоединенную к Fc-области антитела, описаны в патенте США 2003/0157108 A1, Presta, L. См. также США 2004/0693621 A1 (Kyowa Hakko Kogyo Co., Ltd).Антитела с делящимся на пополам N-ацетилглюкозамином (GlcNAc) в углеводе, присоединенном к Fc-области антитела, указаны в WO 03/011878, Jean-Maire et al. и патентеСША№6602684, Umana et al. Антитела с по меньшей мере одним остатком галактозы в олигосахариде, присоединенном к Fc-области антитела, описаны в WO 97/30087, Patel et al. См. также WO98/58964 (Raju, S.) и WO 99/27644 (Raju, S.) в отношении антител с измененным углеводом, присоединенным к Fc-области.
Может быть желательным изменить период полураспада антител или тау-связывающих фрагментов по настоящему изобретению. В одном из вариантов осуществления одну или несколько аминокислот Fc мутируют для повышения периода полураспада антитела в крови, или где одну или несколько групп сахара Fc удаляют, или одну или несколько групп сахара добавляют для увеличения период полураспада антитела в крови. Обычные белки плазмы, такие как сывороточный альбумин человека (HSA) и иммуноглобулины (Ig), включая гуманизированные антитела, показывают длительный период полураспада, обычно от 2 до 3 недель, что связано с их специфическим взаимодействием с неонатальным Fc-рецептором (FcRn), что приводит к эндосомальной рециркуляции (Ghetie (2002) Immunol Res, 25: 97-113).Напротив, большинство других белков, представляющих фармацевтических интерес, в частности фрагменты рекомбинантных антител, гормоны и интерфероны, страдают высоким клиренсом (кровь). Это особенно справедливо для белков, размер которых ниже порогового значения для фильтрации почек приблизительно 70 кДа (Caliceti (2003) Adv Drug Deliv Rev 55: 1261-1277). В этих случаях период полураспада в плазме немодифицированного фармацевтического белка может быть значительно меньше часа. Это может ограничить их использование для большинства терапевтических применений. Для достижения устойчивого фармакологического действия, а также для удобства пациента - с необходимыми интервалами дозирования, растянутыми на несколько дней или даже недель - в данной области было разработано и описано несколько стратегий для разработки биофармацевтических препаратов.
В других вариантах осуществления антитела или их тау-связывающие фрагменты могут быть модифицированы так, чтобы влиять на время полураспада или время циркуляции посредством ПЭГилирования или другого конъюгирования с другими полимерами. Полимер может иметь любую молекулярную массу и быть разветвленным или неразветвленным. Для полиэтиленгликоля предпочтительная молекулярная масса составляет от около 1 кДа до около 100 кДа (термин «приблизительно» указывает на то, что в препаратах полиэтиленгликоля вес некоторых молекул будет больше, меньше, чем указанный молекулярный вес) для облегчения обработки и производства. Могут быть использованы другие размеры в зависимости от желаемого терапевтического профиля (например, продолжительность желательного замедленного высвобождения, эффекты, если таковые имеются, на биологическую активность, легкость в обработке, степень или отсутствие антигенности и другие известные эффекты полиэтиленгликоля на терапевтический белок или аналог).Например, полиэтиленгликоль может иметь среднюю молекулярную массу, равную приблизительно 500, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000, 5500, 6000, 6500, 7000, 7500, 8000, 8500, 9000, 9500, 10000, 10500, 11000, 11500, 12000, 12500, 13000, 13500, 14000, 14500, 15000, 15500, 16000, 16500, 17000, 17500, 18000, 18500, 19000, 19500, 20000, 25000, 30000, 35000, 40000, 50000, 55000, 60000, 65000, 70000, 75000, 80000, 85000, 90000, 95000 или 100000 Да. Разветвленные полиэтиленгликоли описаны, например, в патентеСША№5643575; Morpurgo et al., Appl.Biochem.Biotechnol. 56:59-72 (1996); Vorobjev et al., Nucleosides Nucleotides 18:2745-2750 (1999); and Caliceti et al., Bioconjug.Chem.10: 638-646 (1999). Полиэтиленгликоль может быть присоединен к белкам посредством связи с любым из ряда аминокислотных остатков. Например, полиэтиленгликоль может быть связан с полипептидами посредством ковалентных связей с остатками лизина, гистидина, аспарагиновой кислоты, глутаминовой кислоты или цистеина. Одна или несколько химических реакций может использоваться для присоединения полиэтиленгликоля к конкретным аминокислотным остаткам (например, лизин, гистидин, аспарагиновая кислот, глутаминовая кислота или цистеин) или к более чем одному типу аминокислотных остатков (например, лизина, гистидин, аспарагиновая кислота, глутаминовая кислота, цистеин и их комбинации).
Альтернативно, антитела или их фрагменты могут иметь повышенное время жизни in vivo за счет слияния с альбумином (включая, но ими не ограничиваясь рекомбинантный альбумин сыворотки человека или его фрагменты или варианты (см., например, патент США №5876969, выданный 2 марта 1999, патент EP 0413622 и патент США №5766883, выданный 16 июня 1998, включенный в настоящее описание в качестве ссылки в полном объеме)) или другие белки циркулирующей крови, такие как трансферрин или ферритин. В одном из вариантов осуществления полипептиды и/или антитела по настоящему изобретению (включая их фрагменты или варианты) слиты со зрелой формой сывороточного альбумина человека (то есть, аминокислоты 1-585 сывороточного альбумина человека, как показано на фиг.1 и 2 патента EP 0 322 094), который приведен в настоящем описание посредством ссылки в полном объеме. Полинуклеотиды, кодирующие слитые белки согласно изобретению, также включены в объем настоящего изобретения.
Антитела или их тау-связывающие фрагменты также могут быть химически модифицированы для обеспечения дополнительных преимуществ, таких как повышенная растворимость, стабильность и время циркуляции (период полужизни in vivo) полипептида или пониженной иммуногенности (см., например, патентСША№4179337).Химические фрагменты для дериватизации могут быть выбраны из водорастворимых полимеров, таких как полиэтиленгликоль, сополимеры этиленгликоля и пропиленгликоля, карбоксиметилцеллюлоза, декстран, поливиниловый спирт и тому подобное. Антитела и их тау-связывающие фрагменты могут быть модифицированы в произвольных положениях внутри молекулы или в заданных положениях внутри молекулы и могут включать одну, две, три или более присоединенных химических групп
Может быть желательным модифицировать антитела или тау-связывающие фрагменты по изобретению по отношению к эффекторной функции, например, для усиления антиген-зависимой клеточной цитотоксичности (ADCC) и/или комплемент-зависимой цитотоксичности (CDC) антитела. Это может быть достигнуто путем введения одной или нескольких аминокислотных замен в Fc-область антитела. Альтернативно или дополнительно цистеиновый остаток (остатки) можно вводить в область Fc, тем самым обеспечивая образование межцепочечной дисульфидной связи в этой области. Полученное таким образом гомодимерное антитело может обладать улучшенной способностью к интернализации и/или повышенной комплемент-опосредованной гибелью клеток и антитело-зависимой клеточной цитотоксичностью (ADCC).См. Caron et al, J.Exp Med.176:1191-1195 (1992) and Shopes, B.J.Immunol.148:2918-2922 (1992).Альтернативно, может быть сконструировано антитело, которое имеет две области Fc и, таким образом, может обладать улучшенной способностью к лизису комплемента и ADCC. См. Stevenson et al. Anti-Cancer Drug Design 3:219-230 (1989).
В WO00/42072 (Presta, L.) описаны антитела с улучшенной функцией ADCC в присутствии эффекторных клеток человека, где антитела содержат аминокислотные замены в Fc-области. Предпочтительно, антитело с улучшенной ADCC содержит замены в положениях 298, 333 и/или 334 области Fc. Предпочтительно, измененная область Fc представляет собой область Fc IgG1 человека, содержащую или состоящую из замещений в одном, двух или трех из этих положений.
Антитела с измененным связыванием C1q и/или комплементарной цитотоксичностью (CDC) описаны в WO 99/51642, патенте США № 6194551B1, патенте США № 6242195B1, патенте США № 6528624B1 и патенте США № 6538124 (Idusogie et al.). Антитела содержат аминокислотную замену в одном или нескольких положениях аминокислот 270, 322, 326, 327, 329, 313, 333 и/или 334 области Fc.
Для увеличения периода полураспада в сыворотке антитела, в антитело (особенно во фрагмент антитела) можно ввести эпитоп связывания рецептора реутилизации, как описано в патентеСША№5739277, например. Используемый в настоящем документе термин «эпитоп связывания рецептора реутилизации» относится к эпитопу области Fc молекулы IgG (например,IgG1, IgG2, IgG3 или IgG4), который ответственен за увеличение периода полураспада молекулы IgG в сыворотке in vivo.
Антитела с улучшенным связыванием с Fc-рецептором новорожденных (FcRn) и увеличенными периодами полураспада описаны в WO 00/42072 (Presta, L.). Указанные антитела содержат Fc область с одной или несколькими заменами, которые улучшают связывание Fc-области с FcRn. Например, область Fc может иметь замены в одном или более из положений 238, 256, 265, 272, 286, 303, 305, 307, 311, 312, 317, 340, 356, 360, 362, 376, 378, 380, 382, 413, 424 или 434.Предпочтительный вариант с Fc-областью антитела с улучшенным связыванием FcRn включает аминокислотные замены в одном, двух или трех положениях 307, 380 и 434 области Fc.
В одном из вариантов осуществления гуманизированное антитело или его тау-связывающий фрагмент/часть является моноклональным. Моноклональные антитела (mAb), описанные в настоящем документе, являются антителами, полученными из популяции по существу гомогенных антител, то есть отдельные антитела, содержащиеся в популяции, идентичны, за исключением возможных мутаций природного происхождения, которые могут присутствовать в небольших количествах. Моноклональные антитела являются высокоспецифичными направленными против одного антигенного сайта. Каждое mAb направлено против одного детерминанта (эпитопа) на антигене. Помимо их специфичности, моноклональные антитела предпочтительны тем, что они могут быть синтезированы гибридомной культурой, незагрязненной другими иммуноглобулинами. Определение "моноклональное" указывает на то, что антитело получено из по существу однородной популяции антител и его не следует интерпретировать как требование о продукции антитела посредством какого-либо конкретного способа.Например, моноклональные антитела, которые должны использоваться в соответствии с настоящим изобретением, могут быть получены в иммортализованной В-клетке или их гибридоме, или могут быть получены методами рекомбинантной ДНК. В других случаях моноклональные антитела получают из растущего клона одной клетки, такого как эукариотическая клетка-хозяин, трансфецированная молекулой ДНК, кодирующей антитело или ее тау-связывающий фрагмент или часть. Нуклеиновые кислоты, кодирующие антитела и фрагменты по настоящем изобретению, также могут быть доставлены индивиду-хозяину для экспрессии антитела и фрагментов клетками индивида-хозяина. Примеры стратегий доставки полинуклеотидов и экспрессии антисенилиновых антител в центральной нервной системе индивида-хозяина описаны в заявке РCTWO 98/44955, опубликованной 15 октября1998.Любую нуклеиновую кислоту можно модифицировать для повышения стабильности in vivo. Возможные модификации включают, но не ограничиваются ими, добавление фланкирующих последовательностей на 5'- и/или 3'-концы; использование фосфоротиоата или 2'-O-метила, а не фосфодиэстеразных связей в скелете; и/или включение нетрадиционных оснований, таких как инозин, квеузин и вибутозин, а также ацетил-, метил-, тио- и других модифицированных форм аденина, цитидина, гуанина, тимина и уридина.
В одном из аспектов антитело или тау-связывающий фрагмент, как описано в настоящем документе, может проявлять более высокое сродство к патологическому тау-белку, чем к физиологическому тау-белку.
В другом аспекте антитело или тау-связывающий фрагмент, как описано в настоящем документе, способно ингибировать агрегацию тау-тау.
В другом аспекте антитело или тау-связывающий фрагмент, как описано в настоящем документе, способно опосредовать захват и деградацию патологического тау-белка микроглией.
В одном из аспектов антитело или тау-связывающий фрагмент, как описано в настоящем документе, может проявлять более высокое сродство к патологическому тау-белку, чем к физиологическому тау-белку, и ингибировать тау-тау агрегацию.
В одном из аспектов антитело или тау-связывающий фрагмент, как описано в настоящем документе, способе проявлять более высокое сродство к патологическому тау-белку, чем к физиологическому тау-белку, ингибировать тау-тау агрегацию и опосредовать обратный захват и деградацию патологического тау-белка микроглией.
В приведенных ниже таблицах 7, 8 и 9 суммированы последовательности нуклеиновых кислот CDR и вариабельных областей и полноразмерных цепей некоторых из описанных в настоящем документе антител:
В другом наборе вариантов осуществления изобретение относится к нуклеиновым кислотам, кодирующим описанные в настоящем документе антитела, или их части. Нуклеиновые кислоты, кодирующие вариабельные домены тяжелых цепей VH DC8E8, RHA, RHB, RHC, RHD, RHE, RHF, RHG, RHH, RHI, RHJ, RHK, RHL и RHM и вариабельные домены легких цепей VK DC8E8, RKA и RKB, были оптимизированы по кодонам, используя запатентованную технологию GeneScript. В контексте настоящего изобретения оптимизация кодонов представляет собой процесс модификации нуклеотидной последовательности таким образом, чтобы улучшить ее экспрессию, содержание G/C, вторичную структуру РНК и трансляцию в эукариотических клетках без изменения кодируемой ею аминокислотной последовательности.
В одном из вариантов осуществления изобретение относится к нуклеиновым кислотам (ДНК или РНК), которые кодируют вариабельный домен тяжелой цепи гуманизированного антитела, как описано в настоящем документе. В одном из вариантов осуществления нуклеиновая кислота содержит ДНК, которая кодирует любую из вариабельных доменов тяжелой цепи RHA, RHB, RHC, RHD, RHE, RHF, RHG, RHH, RHI, RHJ, RHK, RHL и RHM. Эти нуклеиновые кислоты представлены в таблицах ниже. Нуклеиновые кислоты, имеющие процентную идентичность по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% и по меньшей мере 98%, также входят в объем этого варианта осуществления.
На таблице 10 ниже приведены последовательности различных нуклеиновых кислот, соответствующие различным полноразмерным последовательностям легких цепей гуманизированных антител, описанных в настоящем документе.
В еще одном из вариантов осуществления изобретение относится к нуклеиновым кислотам (ДНК или РНК), которые кодируют вариабельный домен легкой цепи гуманизированного антитела, как описано в настоящем документе. В одном варианте осуществления нуклеиновая кислота содержит ДНК, которая кодирует любую из вариабельных доменов легкой цепи RKA и RKB. Эти нуклеиновые кислоты представлены в таблицах выше. Нуклеиновые кислоты, имеющие процентную идентичность по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% и по меньшей мере 98%, также входят в объем этого варианта осуществления.
Специалистам в данной области будет понятно, что в результате вырожденности генетического кода существует много нуклеотидных последовательностей, которые кодируют антитело или его тау-связывающий фрагмент, как описано в настоящем документе. Некоторые из этих нуклеиновых кислот имеют минимальную гомологию с нуклеотидной последовательностью любого «дикого» антитела или его тау-связывающего фрагмента, как описано в настоящем документе. Тем не менее, нуклеиновые кислоты, которые изменяются из-за различий в использовании кодонов, конкретно рассматриваются в настоящем изобретении.
В одном из вариантов осуществления изобретение относится к нуклеиновым кислотам (ДНК или РНК), которые кодируют вариабельный домен тяжелой цепи гуманизированного антитела, как описано в настоящем документе. В одном из вариантов осуществления нуклеиновая кислота содержит ДНК, которая кодирует любой из вариабельных доменов тяжелой цепи RHA, RHB, RHC, RHD, RHE, RHF, RHG, RHH, RHI, RHJ, RHK, RHL и RHM, связанный с константной областью IgG1 человека. Нуклеиновые кислоты, имеющие процентную идентичность по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% и по меньшей мере 98%, также входят в объем этого варианта осуществления.
В одном из вариантов осуществления изобретение относится к нуклеиновым кислотам (ДНК или РНК), которые кодируют вариабельный домен тяжелой цепи гуманизированного антитела, как описано в настоящем документе. В одном из вариантов осуществления нуклеиновая кислота содержит ДНК, которая кодирует любой из вариабельных доменов тяжелой цепи RHA, RHB, RHC, RHD, RHE, RHF, RHG, RHH, RHI, RHJ, RHK, RHL и RHM, связанный с константной областью IgG4 человека. Нуклеиновые кислоты, имеющие процентную идентичность по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% и по меньшей мере 98%, также входят в объем этого варианта осуществления.
В еще одном из вариантов осуществления изобретение относится к нуклеиновым кислотам (ДНК или РНК), которые кодируют вариабельный домен легкой цепи гуманизированного антитела, как описано в настоящем документе. В одном варианте осуществления нуклеиновая кислота содержит ДНК, которая кодирует любой вариабельный домен легкой цепи RKA и RKB, связанный с каппа областью человека. Нуклеиновые кислоты, имеющие процентную идентичность по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 95% и по меньшей мере 98%, также входят в объем этого варианта осуществления.
В еще одном варианте осуществления изобретение относится к нуклеиновым кислотам (ДНК или РНК), которые кодируют каждый CDR DC8E8 кодоно-птимизированным образом.
Последовательности нуклеиновых кислот, имеющие процент идентичности по меньшей мере 80%, например 85%, 90%, 95% и 98%, после оптимального выравнивания с предпочтительной последовательностью, обозначают последовательности нуклеиновых кислот, имеющие относительно эталонной последовательности нуклеиновой кислоты, определенные изменения, в частности, делецию, усечение, расширение, химерное слияние и/или замену, особенно точно. В некоторых вариантах осуществления этими последовательностями являются последовательности, чей код одинаков для аминокислотных последовательностей и эталонной последовательности, что связано с дегенерацией генетического кода, или комплементарные последовательности, которые могут специфически гибридизоваться с эталонными последовательностями, например, в очень жестких условиях, особенно тех, как определено ниже.
Гибридизация в очень жестких условиях означает, что условия, связанные с температурой и ионной силой, выбраны так, что они обеспечивают и поддерживают гибридизацию двух комплементарных фрагментов ДНК. Только в качестве примера, очень жесткие условия стадии гибридизации для цели определения полинуклеотидных фрагментов, описанных в настоящем документе, преимущественно являются следующими.
Гибридизацию ДНК-ДНК или ДНК-РНК проводят в две стадии:(1) прегибридизация при 42°С в течение трех часов в фосфатном буфере (20 мМ, pH 7,5), содержащем 5×SSC (1×SSC соответствует раствору 0,15 М NaCl+0,015 М цитрата натрия), 50% формамида, 7% додецил сульфата натрия (SDS), 10× раствор Денхарда, 5% декстрансульфат и 1% ДНК спермы лосося; (2) первичная гибридизация в течение 20 часов при температуре, зависящей от длины зонда (то есть:42°С для зонда длиной > 100 нуклеотидов), затем две 20-минутные промывки при 20°С в 2×SSC+2% SDS, одна 20-минутная промывка при 20°С в 0,1×SSC+0,1% SDS. Последняя промывка осуществляется в 0,1×SSC+0,1% SDS в течение 30 минут при температуре 60°C для зонда длиной > 100 нуклеотидов. Условия жесткой гибридизации, описанные выше для полинуклеотида определенного размера, могут быть адаптированы специалистом в данной области для более длинных или более коротких олигонуклеотидов в соответствии с процедурами, описанными в Sambrook et al.(Molecular cloning:a laboratory manual, Cold Spring Harbor Laboratory; 3rd edition, 2001).
Экспрессионные системы
Антитела и их тау-связывающие фрагменты могут быть получены синтетически или с помощью любой из нескольких систем экспрессии, известных среднему специалисту в данной области. С этой целью также предусмотрены варианты осуществления, которые охватывают векторы клонирования, векторы экспрессии, клетки-хозяева и трансгенные животные (отличные от человека), трансфецированные, трансформированные или иным образом генетически или рекомбинантно модифицированные и, таким образом, содержащие одну или несколько последовательностей нуклеиновых кислот, описанных выше. В одном из вариантов осуществления клетками-хозяевами являются эукариотические клетки. В другом варианте осуществления клетками-хозяевами являются прокариотические клетки. В еще одном варианте осуществления клетки-хозяева экспрессируют один или более антител и их тау-связывающих фрагментов. Выбранные клетки могут быть культивировали и, при необходимости, белковый продукт интересующего гена выделен из культуры, используя обычные методики. В некоторых вариантах осуществления системы экспрессии были адаптированы для экспрессии антитела или его тау-связывающего фрагмента на оптимальном уровне. В некоторых вариантах антитела и их тау-связывающие фрагменты экспрессируют на основе контракта с компаниями, занимающимися экспрессией антител (например, Лонза), которые используют методики для экспрессии антител и их тау-связывающих фрагментов в качестве предоставляемой услуги. В другом варианте осуществления антитела и их тау-связывающие фрагменты экспрессируются в бесклеточной системе.
Примеры обычно используемых систем экспрессии антител включают рекомбинантный бакуловирус, лентивирус, простейшее (например, эукариотический паразит Leishmania tarentolae), микробную систему экспрессии, включая систему на основе дрожжей (например, Pichia pastoris, Saccharomyces cerevisiae, Yarrowia lipolytica, Hansenula polymorpha, Aspergillus и Trichoderma Fungi) и систему на основе бактерии (например, E. coli, Pseudomonas fluorescens, Lactobacillus, Lactococcus, Bacillus megaterium, Bacillus subtilis, Brevibacillus, Corynebacterium glutamicum), клетки яичников китайского хомяка (CHO), CHOK1SVNSO (Lonza), BHK (почка новорожденного хомяка), PerC.6 или Per.C6 (например, Percivia, Crucell), различные линии клеток HEK 293, Expi293F™ (Life Technologies), GenScript's YeastHIGH™ Technology (GenScript), клетки линии нейрональных предшественников человека AGE1.HN (Probiogen) и другие клетки млекопитающих, растений (например, кукуруза, люцерна и табак), клетки насекомых, яйца птиц, водоросли и трансгенные животные (например, мыши, козы, овц, свиньи, коровы).
Характер гликозилирования антител, экспрессируемых этими различными системами, значительно изменяется в зависимости от системы экспрессии. Например, механизмы гликозилирования клеток СНО несколько схож с механизмами гликозилирования клеток человека, но с некоторыми отличиями. Кроме выбора клеток-хозяев факторы, которые влияют на гликозилирование при рекомбинантной продукции антител, включают способ роста, состав среды, плотность культуры, оксигенацию, рН, схемы очистки и тому подобное. Были предложены различные способы изменения характера гликозилирования конкретного организма-хозяина, включая введение или сверхэкспрессию определенных ферментов, участвующих в продукции олигосахаридов (патент СШ А№№ 5047335; 5510261 и 5278299). Гликозилирование, или определенные типы гликозилирования, может быть ферментативно удалено из гликопротеина, например, используя эндогликозидазу H (Endo H).Кроме того, рекомбинантная клетка-хозяин может быть генетически получены с дефектом при обработке определенных типов полисахаридов. Эти и подобные методики хорошо известны в данной области и могут быть использованы для изменения антител и их тау-связывающих фрагментов, описанных в настоящем документе.
Преимущества и недостатки этих различных систем рассмотрены в литературе и известны специалистам в данной области. Некоторые из них описаны в следующих ссылках, каждая из которых включена в настоящее описание в качестве ссылки в полном объеме: Chadd et al. Therapeutic antibody expression technology. Curr Opin Biotechnol. 2001 Apr;12(2):188-94; Ma et al. Human antibody expression in transgenic rats: comparison of chimeric IgH loci with human VH, D and JH but bearing different rat C-gene regions. J Immunol Methods.2013 Dec 31;400-401:78-86; Zhang et al. Monoclonal antibody expression in mammalian cells. Methods Mol Biol. 2012;907:341-58.
Фармацевтические композиции и составы
В настоящем документе представлены композиции, содержащие гуманизированное антитело или его тау-связывающий фрагмент, как описано в настоящем описании, и другой компонент, такой как носитель. Также предложены фармацевтические композиции/терапевтические составы, содержащие гуманизированное антител или его тау-связывающий фрагмент, как описано в настоящем документе, а также вспомогательное вещество и/или фармацевтический носитель. В одном из вариантов осуществления носитель является неприродным соединением. В одном из вариантов осуществления вспомогательное вещество является неприродным соединением. В другом варианте осуществления разбавитель является неприродным соединением. В другом варианте осуществления состав, содержащий гуманизированное антитело или его тау-связывающий фрагмент, как описано в настоящем документе, не содержит природного соединения, за исключением, необязательно, воды.
В одном из вариантов осуществления терапевтические составы антител, используемых в соответствии с настоящим изобретением, получают для хранения и/или введения путем смешивания антитела или его тау-связывающего фрагмента, имеющего желаемую степень чистоты, с необязательными фармацевтически приемлемыми носителями, разбавителями, вспомогательными веществами или стабилизаторами (Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980)) в форме лиофилизированных композиций или водных растворов. В одном из вариантов осуществления, приемлемые носители, вспомогательные вещества или стабилизаторы в используемых дозах и концентрациях являются нетоксичными для реципиентов и включают буферы, такие как фосфатный, цитратный буфер и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как хлорид октадецилдиметилбензиламмония; хлорид гексаметония; хлорид бензалкония, хлорид бензетония; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехол; резорцин; циклогексанол; 3-пентанол и м-крезол); низкомолекулярные (менее чем около 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; сахара, такие как сахароза, маннит, трегалоза или сорбит; сольобразующий противоионы, такие как натрий; комплексы металлов (например, Zn-белковые комплексы); и/или неионные поверхностно-активные вещества, такие как TWEEN PLURONICS или полиэтиленгликоль (ПЭГ).Примеры лиофилизированных составов антител описаны в WO97/04801, специально включенном в настоящее описание в качестве ссылки.
В дополнительном варианте осуществления состав также содержит поверхностно-активное вещество. Поверхностно-активное вещество может быть выбрано, например, из детергента, этоксилированного касторового масла, полигликолизированных глицеридов, ацетилированных моноглицеридов, эфиров сорбита и жирных кислот, блоксополимеров полиоксипропилен-полиоксиэтилен (например, полоксамеры, такие как Pluronic®,F68, полоксамер 188 и 407, Triton X-100), эфиров полиоксиэтиленсорбитана и жирных кислот, производных полиоксиэтилена и полиэтилена, таких как алкилированные и алкоксилированные производные (твины, например,Tween-20, Tween-40, Tween-80 и Brij-35), моноглицеридов или их этоксилированных производных, диглицеридов и их оксиэтилированных производных, спиртов, глицерина, лектинов и фосфолипидов (например, фосфатидилсерин, фосфатидилхолин, фосфатидилэтаноламин, фосфатидилинозитол, дифосфатидилглицерин и сфингомиелин), производных фосфолипидов (например, дипальмитоилфосфатидная кислота) и лизофосфолипидов (например, пальмитоил-лизофосфатидил-L-серин и 1-ацил-sn-глицеро-3-фосфатные эфиры этаноламина, холин, серин или треонин) и алкил-, алкоксил-(алкиловый эфир), алкокси (алкиловый эфир)-производных лизофосфатидила и фосфатидилхолинов, например, лауроильные и миристоильные производные лизофосфатидилхолина, дипальмитоилфосфатидилхолина, и модификации полярной головной группы, то есть холины, этаноламины, фосфатидная кислота, серины, треонины, глицерин, инозитол, и положительно заряженные DODAC, DOTMA, DCP, BISHOP, лизофосфатидилсерин и лизофосфатидилтреонин и глицерофосфолипиды (например, цефалины), глицерогликолипиды (например, галактопираноид), сфингогликолипиды (например, церамиды, ганглиозиды), додецилфосфохолин, лизолецитин куриного яйца, производные фузидиевой кислоты (например, тауродигидрофузидат натрия и тому подобное), длинноцепочечные жирные кислоты и их соли C6-C12 (например, олеиновая кислота и каприловая кислота), ацилкарнитины и производные, N-ацилированные производные лизина, аргинин или гистидин или ацилированные на боковой цепи производные лизина или аргинина, N альфа-ацилированные производные дипептидов, содержащих любую комбинацию лизина, аргинина или гистидина и нейтральной или кислой аминокислоты, N альфа-ацилированные производные трипептида, содержащего любую комбинацию нейтральной аминокислоты и двух заряженных аминокислот, DSS (докузат натрия, регистрационный номер CAS [577-11-7]), докузат кальция, регистрационный номер CAS [128-49-4]), докузат калия, регистрационный номер CAS [7491-09-0]), SDS (додецилсульфат натрия или лаурилсульфат натрия), каприлат натрия, холевая кислота или ее производные, желчные кислоты и их соли и конъюгаты глицина или таурина, урсодезоксихолевая кислота, холат натрия, дезоксихолат натрия, таурохолат натрия, гликохолат натрия, N-гексадецил-N, N-диметил-3-аммонио-1-пропансульфонат, анионные (алкил-арил-сульфонаты) одновалентные поверхностно-активные вещества, цвиттерионные поверхностно-активные вещества (например,N-алкил-N,N-диметиламмоний-1-пропансульфонат, 3-холамидо-1-пропилдиметиламмоний-1-пропансульфорнат, катионные поверхностно-активные вещества (четвертичные аммониевые основания) (например, цетиловый триметиламмония бромид, хлорид цетилпиридина), неионогенные поверхностно-активные вещества (например, додецил бета-D-глюкопиранозид), полоксамины (например, Tetronic), которые являются тетрафункциональными блок-сополимерами, полученными в результате последовательного добавления пропиленоксида и этиленоксида к этилендиамину, или поверхностно-активное вещество может быть выбрано из группы производных имидазолина или их смесей. В одном из вариантов осуществления поверхностно-активное вещество не является природным соединением. Каждое из этих конкретных поверхностно-активных веществ представляет собой альтернативный вариант осуществления описания.
Один вариант из вариантов осуществления относится к стабильным составам антител и/или их тау-связывающих фрагментов, которые содержат предпочтительно фосфатный буфер с солевым раствором или выбранной солью, а также консервированные растворы и составы, содержащие консервант, а также многоцелевые консервированные композиции, подходящие для фармацевтического или ветеринарного применения, включая по меньшей мере одно антитело и/или его тау-связывающие фрагменты в фармацевтически приемлемом составе. В одном из вариантов осуществления консервированные составы содержат по меньшей мере один известный консервант или необязательно выбранный из группы, состоящей из по меньшей мере одного фенола, м-крезола, п-крезола, о-крезола, хлоркрезола, бензилового спирта, фенилмеркуринового нитрита, феноксиэтанола, формальдегида, хлорбутанола, хлорида магния (например, гексагидрат), алкилпарабена (метил, этил, пропил, бутил и тому подобное), хлорида бензалкония, хлорида бензетония, дегидроацетата натрия и тимерозала или их смесей в водном разбавителе. Любую подходящую концентрацию или смесь можно использовать, как известно в данной области, например 0,001-5%, или любой диапазон или значение в нем, например, но не ими ограничиваясь, 0,001, 0,003, 0,005, 0,009, 0,01, 0,02, 0,03, 0,05, 0,09, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,3, 4,5, 4,6, 4,7, 4,8, 4,9 или любой диапазон или значение в нем. Не ограничивающие примеры включают, без консерванта, 0,1-2% м-крезол (например,0,2, 0,3, 0,4, 0,5, 0,9, 1,0%), 0,1-3% бензиловый спирт (например,0,5, 0,9, 1,1, 1,5, 1,9, 2,0, 2,5%), 0,001-0,5% тимеросал (например, 0,005, 0,01), 0,001-2,0% фенол (например,0,05, 0,25, 0,28, 0,5, 0,9, 1,0%), 0,0005-1,0% алкилпарабен(ы) (например,0,00075, 0,0009, 0,001, 0,002, 0,005, 0,0075, 0,009, 0,01, 0,02, 0,05, 0,075, 0,09, 0,1, 0,2, 0,3, 0,5, 0,75, 0,9, 1,0%) и тому подобное. В одном из вариантов осуществления консервант или консерванты не являются природными соединениями.
В одном из вариантов осуществления антитела и их тау-связывающие фрагменты по настоящему описанию могут быть введены в фармацевтические композиции, подходящие для введения индивиду. В общем варианте осуществления фармацевтическая композиция содержит антитело или его тау-связывающий фрагмент по изобретению и фармацевтически приемлемый носитель. В одном из вариантов осуществления "фармацевтически приемлемый носитель" включает любые и все растворители, суспензионную среду, покрытия, противобактериальные и противогрибковые агенты, агенты для поддержания изотоничности и задержки абсорбции и тому подобное, которые являются физиологически совместимыми. Дополнительные примеры фармацевтически приемлемых носителей включают один или более из воды, солевого раствора, забуференного фосфатом физиологического раствора, декстрозы, глицерина, этанола и тому подобное, а также их комбинации. Во многих случаях предпочтительно вводить в композицию изотонические агенты, например, сахара, полиспирты, такие как маннит, сорбит или натрия хлорид. Фармацевтически приемлемые носители могут дополнительно содержать небольшие количества вспомогательных веществ, таких как смачивающие или эмульгирующие агенты, консерванты или буферы, которые увеличивают срок хранения или эффективность антитела или его тау-связывающего фрагмента.
В одном из варианте осуществления, подходящее количество фармацевтически приемлемую соль используется в составе для придания изотоничности состава. Примеры носителя включают солевой раствор, раствор Рингера и раствор декстрозы. В одном из вариантов осуществления рН раствора составляет от примерно 5 до примерно 8. В другом варианте осуществления рН составляет от примерно 7 до примерно 7,5.Другие носители включают препараты пролонгированного высвобождения, такие как полупроницаемые матрицы твердых гидрофобных полимеров, содержащие антитело или его тау-связывающий фрагмент, причем эти матрицы находятся в форме формованных изделий, например пленок, липосом или микрочастиц. Матрица замедленного высвобождения, как используется в настоящем изобретении, представляет собой матрицу, изготовленную из материалов, обычно полимеров, которые разлагаются ферментативным или кислотно/основным гидролизом или путем растворения. После введения в организм на матрицу воздействуют ферменты и биологические жидкости. Желательно, чтобы матрица с замедленным высвобождением была выбрана с помощью биосовместимых материалов, таких как липосомы, полилактиды (полилактидная кислота), полигликолид (полимер гликолевой кислоты), сополимеры молочной кислоты и гликолевой кислоты, полиангидриды, поли(орто) сложные эфиры, полипептиды, гиалуроновая кислота, коллаген, хондроитинсульфат, карбоновые кислоты, жирные кислоты, фосфолипиды, полисахариды, нуклеиновые кислоты, полиаминокислоты, аминокислоты, такие как фенилаланин, тирозин, изолейцин, полинуклеотиды, поливинилпропилен, поливинилпирролидон и силикон. Предпочтительной биодеградируемой матрицей является матрица одного из сополимеров гликолида и полилактида, полигликолида или полилактида (сополимеры молочной кислоты и гликолевой кислоты).
Специалистам в данной области будет очевидно, что некоторые носители могут быть более предпочтительными в зависимости, например, от способа введения и концентрации вводимого антитела.
Композиции по изобретению могут быть в различных формах. Они включают, например, жидкие, полутвердые и твердые лекарственные формы, такие как жидкие растворы (например, инъекционные и инфузионные растворы), дисперсии или суспензии, таблетки, пилюли, порошки, липосомы и суппозитории. В некоторых вариантах осуществления такие композиции могут также содержать буферы (например, нейтральный буферный солевой раствор или забуференный фосфатом физиологический раствор), углеводы (например, глюкозу, маннозу, сахарозу или декстраны), маннит, белки, полипептиды или аминокислоты, такие как глицин, антиоксиданты, хелатные агенты, такие как EDTA или глутатион, адъюванты (например, гидроксид алюминия) и/или консерванты. Альтернативно, композиции по настоящему изобретению могут быть введены в состав в виде лиофилизата. Антитела и их тау-связывающие фрагменты также могут быть инкапсулированы в липосомы, используя хорошо известные технологии.
Дозированные формы, подходящие для внутреннего введения, обычно содержат от 0,1 до 500 мг антитела или его тау-связывающего фрагмента (активного ингредиента) на единицу или в контейнере. В этих фармацевтических композициях активный ингредиент обычно присутствует в количестве примерно 0,5-99,999% по массу в пересчете на общую массу композиции.
Терапевтические композиции/составы обычно должны быть стерильными и стабильными в условиях производства и хранения. Композиция может быть составлена в виде раствора, микроэмульсии, дисперсии, липосомы или другой упорядоченной структуры, подходящей для высокой концентрации лекарственного средства. Стерильные инъекционные растворы могут быть получены путем объединения активного соединения (то есть, антитело или его тау-связывающий фрагмент) в необходимом количестве в подходящем растворителе с одним или комбинацией ингредиентов, перечисленных выше, по необходимости, с последующей стерилизующей фильтрацией. В общем, дисперсии получают путем введения активного соединения в стерильный растворитель, который содержит основную дисперсионную среду и необходимые другие ингредиенты из перечисленных выше. В случае стерильных порошков для получения стерильных растворов для инъекций предпочтительными способами получения являются вакуумная сушка и сушка вымораживанием, что дает порошок активного ингредиента плюс любой дополнительный желаемый ингредиент из ранее стерильно отфильтрованного раствора. Надлежащая текучесть раствора может поддерживаться, например, за счет применения материала покрытия, такого как лецитин, поддерживая необходимого размера частиц в случае дисперсий и используя поверхностно-активные вещества. Пролонгированная абсорбция инъекционных композиций может быть обеспечена введением в композицию агента, который замедляет абсорбцию, например, моностеарата алюминия и желатина.
Предпочтительная лекарственная форма зависит от предполагаемого способа введения и терапевтического использования. Специалисты в данной области знакомы с методиками определения таких доз. Обычные композиции находятся в форме растворов для инъекций или инфузий, например, композиций, сходных с композициями для пассивной иммунизации людей другими антителами. Самым обычным режимом введения является парентеральный (например, внутривенный, подкожный, внутрибрюшинный, внутримышечный). В предпочтительном варианте осуществления антитело вводят путем внутривенной инфузии или инъекции. В другом предпочтительном варианте осуществления антитело вводят внутримышечной или подкожной инъекцией.
Антитела и их тау-связывающие фрагменты по настоящему изобретению можно вводить различными способами, известными в данной области, хотя для многих терапевтических применений предпочтительным способом/путем введения является внутривенная инъекция или инфузия. Как будет понятно специалисту в данной области, путь и/или способ введения может изменяться в зависимости от желаемых результатов. В некоторых вариантах осуществления антитело или его тау-связывающий фрагмент могут быть получены вместе с носителем, который будет защищать соединение от быстрого высвобождения, например, состав с контролируемым высвобождением, включая имплантанты, трансдермальные пластыри и микрокапсулированные системы доставки. Можно использовать поддающиеся биологическому разложению, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие методы получения таких составов запатентованы или хорошо известны специалистам в данной области. См., например, Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978.
В некоторых вариантах осуществления антитело или его тау-связывающий фрагмент по изобретению можно вводить перорально, например, с инертным разбавителем или усвояемым съедобным носителем. Антитело или его тау-связывающий фрагмент (и при необходимости другие ингредиенты) также могут быть заключены в твердую или мягкую желатиновую капсулу с оболочкой, прессованы в таблетки или непосредственно введены в питание индивида. Для перорального терапевтического введения антитело или его тау-связывающий фрагмент могут быть включены с вспомогательными агентами и использованы в форме проглатываемых таблеток, буккальных таблеток, пастилок, капсул, эликсиров, суспензий, сиропов, вафель и тому подобное. При введении антитела или его тау-фрагмента по изобретению путем, отличным от парентерального введения, может быть необходимо покрыть антитело или его тау-связывающий фрагмент или совместно вводить антитело или его тау-связывающий фрагмент с веществом, предотвращающим ее инактивацию.
Некоторые варианты осуществления изобретения относятся к антителу или тау-связывающему фрагменту для переноса через гематоэнцефалический барьер. Некоторых нейродегенеративные заболевания, включая AD и связанные таутопатии, связаны с повышением проницаемости гематоэнцефалического барьера, таким образом, что антитело или его тау-связывающий фрагмент могут быть легко введены в мозг. Если гематоэнцефалический барьер остается интактным, то существует несколько известных в данной области подходов для переноса молекул через него, включая, но не ограничиваясь ими, физические методы, методы на основе липидов и методы на основе рецепторов и каналов.
Физические методы переноса антитела или его тау-связывающего фрагмента через гематоэнцефалический барьер включают, но ими не ограничиваются, полный обход гематоэнцефалического барьера или создание отверстий в гематоэнцефалическом барьере. Способы обхода включают, но ими не ограничиваются, непосредственную инъекцию в мозг (см., например, Papanastassiou et al., Gene Therapy 9:398-406 (2002)) and implanting a delivery device in the brain (see, e.g., Gill et al., Nature Med. 9:589-595 (2003); and Gliadel Wafers.TM., Guildford Pharmaceutical).Методы создания отверстий в барьере включают, но ими не ограничиваются, УЗИ (см., например, патент США №2002/0038086), осмотическое давление (например, путем введения гипертонического маннита (Neuwelt, E.A., Implication of the Blood-Brain Barrier and its Manipulation, Vols 1 & 2, Plenum Press, N.Y.(1989))), пермеабилизацию, например, брадикинином или пермеабилизатором A-7 (см., например, патенты США №№ 5112596, 5268164, 5506206 и 5686416) и трансфекцию нейронов, которые находятся снижу гематоэнцефалического барьера с помощью векторов, содержащих гены, кодирующие антитело или его тау-связывающий фрагмент (см., например, патент США №2003/0083299).
Способы переноса антитела или его тау-связывающего фрагмента, основанные на липидах, через их гематоэнцефалический барьер включают, но ими не ограничиваются, инкапсуляцию антитела или его тау-связывающего фрагмента в липосомы, которые связаны с активными фрагментами, которые связывают с рецепторами васкулярного эндотелия гематоэнцефалического барьера (см., например, патент США №20020025313), и покрытия антитела или его тау-связывающего фрагмента частицами из липопротеинов низкой плотности (см., например, патент США №20040204354) или аполипопротеином E (см., например, патент США №20040131692).
Способы переноса антитела или его тау-связывающего фрагмента, основанные на рецепторах и каналах, через гематоэнцефалический барьер включают, но ими не ограничиваясь, использование глюкокортикоидных блокаторов для увеличения проницаемости гематоэнцефалического барьера (см., например, патент США №2002/0065259, 2003/0162695 и 2005/0124533); активацию калиевых каналов (см., например, патент США №2005/0089473), ингибирование ABC-транспортеров (см., например, патент США №2003/0073713); покрытие антител трансферрином и модулирование активности одного или нескольких рецепторов трансферрина (см., например, патент США №2003/0129186) и катионизацию антитела (см., например, патент США №5004697).
Для эффективного введения соединения в мозг в данной области известен целый ряд других методик. Например, антитело или его тау-связывающий фрагмент может быть введен непосредственно внутрь желудочка или интратекально, предпочтительно посредством медленной инфузии для сведения к минимуму воздействия на паренхиму мозга.Желаемое антитело или его тау-связывающий фрагмент также может быть доставлен с помощью имплантата с медленным высвобождением в головном мозге, или имплантированных рекомбинантных клеток, которые продуцируют антитело или его тау-связывающий фрагмент. Гематоэнцефалический барьер (BBB) может быть пермеабилизирован одновременно с введением антитела или его тау-связывающего фрагмента, чтобы обеспечить перемещение антитела или его тау-связывающего фрагмента через BBB. Пермеабилизирующие агенты включают осмотические агенты, такие как гипертонический маннит или другой пермеабилизирующий агент, такой как брадикинин, алкилглицерин, ультразвук, электромагнитное излучение или парасимпатическая иннервация.
Кроме того, и без соблюдения какого-либо конкретного механизма также рассматривается возможность того, что антитело, в крови, может иметь эффект "впитывания" при удалении целевого белка из мозга. См., например, Опубликованная заявка США 20110158986, абзац [0017]. Если это так, то антитела и их тау-связывающие фрагменты могут быть эффективны для удаления патологического тау из мозга в циркуляцию, эффективно предотвращая дальнейшее повреждение нейронных клеток и тканей.
Дополнительные или комбинированные активные соединения или терапевтические агенты, как описано в других разделах этой заявки, могут также вводиться в композиции, вводиться одновременно или вводиться последовательно с антителом или его тау-связывающим фрагментом. В некоторых вариантах антитело или его тау-связывающий фрагмент по изобретению вводят в состав вместе с одним или более дополнительными терапевтическими агентами и/или вводят вместе с одним или более дополнительными терапевтическими агентами. Эти дополнительные терапевтические агенты также могут быть химически конъюгированы с антителами или их тау-связывающими фрагментами, описанными в настоящем документе.
В одном из вариантов осуществления раскрыт иммуноконъюгат с формулой (A)-(L)-(C), где: (A) представляет собой антитело или его связывающий фрагмент по настоящему изобретению; (L) представляет собой линкер; и (C) представляет собой агент; и где указанный линкер (L) соединяет (A) и (C). В одном из вариантов осуществления (C) представляет собой эффекторную молекулу, например, терапевтическое средство, визуализирующий агент, детектируемый агентом или диагностический агент. В некоторых вариантах осуществления эти конъюгаты упоминаются в настоящем документе как конъюгаты антитело-лекарственное средство (ADC).
(L) линкер, как используется в настоящем документе, представляет собой молекулу, которая используется для присоединения (A) к (C). Линкер способен образовывать ковалентные связи как с антителом, так и с эффекторной молекулой. Подходящие линкеры хорошо известны специалистам в данной области и включают, но не ограничиваются ими, углеродные линкеры с прямой или разветвленной цепью, гетероциклические углеродные линкеры или пептидные линкеры. Если антитело и эффекторная молекула представляют собой полипептиды, то линкеры могут быть связаны с составляющими аминокислотами посредством их боковых групп (например, посредством дисульфидной связи к цистеину). Однако в предпочтительном варианте осуществления линкеры присоединены к альфа-углероду аминокислотных и карбоксильных групп концевых аминокислот.
В некоторых обстоятельствах желательно, чтобы эффекторные молекулы высвободились из антитела, когда иммуноконъюгат достигнет своего целевого сайта. Таким образом в этих обстоятельствах, иммуноконъюгаты содержат связи, которые отщепляются вблизи от целевого сайта. Расщепление линкера с высвобождением эффекторной молекулы из антитела может быть вызвано ферментативной активностью или условиями, которые воздействуют на иммуноконъюгат либо внутри клетки-мишени, либо рядом с целевым сайтом. В других же вариантах осуществления линкерная единица не расщепляется, но лекарственное средство высвобождается, например, за счет деградации антитела.
Целый ряд различных реакций доступен для ковалентного присоединения лекарственных средств и/или линкеров к антителам или их фрагментам. Присоединение зачастую осуществляют путем взаимодействия аминокислотных остатков молекулы антитела, включая аминогруппы лизина, свободные карбоксильные группы глутаминовой и аспарагиновой кислот, сульфгидрильные группы цистеина и различные группы ароматических аминокислот. Одним из наиболее часто используемых неспецифических способов ковалентного присоединения является карбодиимидная реакция для связывания карбокси (или амино) группы соединения с амино (или карбокси) группами антитела. Кроме того, для связывания аминогруппы соединения с аминогруппами молекулы антитела используют бифункциональные агенты, такие как диальдегиды или имидоэфиры. Также для прикрепления лекарственных средств к антителам доступна реакция основания Шиффа. Этот способ включает окисление периодатом лекарственного средства, которое содержит гликоль или гидроксигруппы, в результате чего образуется альдегид, который затем взаимодействует со связующим агентом. Присоединение происходит через образование основания Шиффа с аминогруппами связывающего агента. Изотиоцианаты также могут использоваться в качестве связующих агентов для ковалентно присоединения лекарственных средств к связывающим агентам.
В некоторых вариантах осуществления линкер расщепляется под действием агента расщепления, который присутствует во внутриклеточной среде (например, в лизосоме или эндосоме или кавеоле). Линкер может быть, например, пептидильным линкером, который расщепляется под действием внутриклеточной пептидазы или протеазного фермента, включая, но ими не ограничиваясь, лизосомальную или эндосомальную протеазу. В некоторых вариантах осуществления длина пептидильного линкера составляет по меньшей мере две аминокислоты или по меньшей мере три аминокислоты. Агенты расщепления могут включать катепсины B и D и плазмин, каждый из которых известен как гидролизующий дипептидные производные лекарственных средств, что приводит к высвобождению активного лекарственного средства внутрь клетки-мишени (см., например, Dubowchik and Walker, 1999, Pharm. Therapeutics 83:67-123).Наиболее характерными являются пептидильные линкеры, которые расщепляются ферментами, присутствующими в 191P4D12-экспрессирующих клетках. Другие примеры таких линкеров описаны, например, в патенте США № 6214345. В конкретном варианте осуществления пептидильный линкер, расщепляемый внутриклеточной протеазой, представляет собой линкер Val-Cit или линкер Phe-Lys (см., например, патент США №6214345, в котором описан синтез доксорубицина с линкером Val-Cit).Одно из преимуществ использования внутриклеточного протеолитического высвобождения терапевтического агента состоит в том, что агент обычно ослабляется при конъюгировании и стабильность конъюгатов в сыворотке обычно является высокой.
В других вариантах осуществления расщепляемый линкер является pH-чувствительным, т.е. чувствительным к гидролизу при определенных значениях рН. Как правило, рН-чувствительный линкер гидролизуется в кислых условиях. Например, можно использовать кислото-лабильный линкер, который гидролизуется в лизосоме (например, гидразон, семикарбазон, тиосемикарбазон, цис-аконитовый амид, ортоэфир, ацеталь, кеталь или тому подобное).(См., например, патенты США №№5122368; 5824805; 5622929; Dubowchik and Walker, 1999, Pharm.Therapeutics 83:67-123; Neville et al., 1989, Biol.Chem. 264:14653-14661.)Такие линкеры являются относительно стабильными при нейтральном pH, например при рН крови, но нестабильны при рН ниже 5,5 или 5,0, приблизительном рН лизосомы. В некоторых вариантах осуществления гидролизуемый линкер представляет собой тиоэфирный линкер (такой как, например, тиоэфир, присоединенный к терапевтическому агенту через ацилгидразоновую связь (см., например, патент США № 5622929).
В других вариантах осуществления линкер является расщепляемым в восстанавливающих условиях (например, дисульфидный линкер). В данной области известен целый ряд дисульфидных линкеров, включая, например, линкеры, которые могут быть образованы с помощью SATA (N-сукцинимидил-S-ацетилтиоацетат), SPDP (N-сукцинимидил-3-(2-пиридилдитио)пропионат), SPDB (N-сукцинимидил-3-(2-пиридилдитио)бутират) и SMPT (N-сукцинимидил-оксикарбонил-альфа-метил-альфа-(2-пиридилдитио)толуол)-, SPDB и SMPT. (См., например, Thorpe et al.,1987, Cancer Res.47:5924-5931; Wawrzynczak et al., In Immunoconjugates: Antibody Conjugates in Radioimagery and Therapy of Cancer (C.W.Vogel ed., Oxford U.Press, 1987. Также см. патент США № 4880935.)
В других конкретных вариантах осуществления линкер представляет собой малонатный линкер (Johnson et al., 1995, Anticancer Res. 15: 1387-93), малеимидобензоиловый линкер (Lau et al., 1995, Bioorg-Med-Chem. 3 (10): 1299-1304) или 3'-N-амидный аналог (Lau et al.,1995, Bioorg-Med-Chem. 3 (10): 1305-12).
В других же вариантах осуществления линкерная единица не расщепляется, но лекарственное средство высвобождается за счет деградации антитела. (См. патентную публикацию США №2005/0238649).
В одном из вариантов осуществления линкер по существу чувствителен к внеклеточной среде. Как используется в настоящем описании термин «по существу нечувствительный к внеклеточной среде» в контексте линкера означает, что не более приблизительно 20%, обычно не более 15%, еще чаще не более приблизительно 10% и еще чаще не более приблизительно 5%, не более приблизительно 3% или не более 1% линкеров, в образце соединения конъюгата антитело-лекарственное средство расщепляются, когда соединение конъюгата антитело-лекарственное средство попадает во внеклеточную среду (например, в плазму).Является ли линкер по существу нечувствительным к внеклеточной среде можно определить, например, путем инкубации с плазмой соединения конъюгата антитело-лекарственное средство в течение заранее определенного периода времени (например, 2, 4, 8, 16 или 24 часа) и затем путем количественной оценки свободного лекарственного средства в плазме.
В других, не взаимоисключающих вариантах осуществления, линкер способствует клеточной интернализации. В некоторых вариантах осуществления линкер стимулирует клеточную интернализацию при конъюгировании с терапевтическим агентом (т.е. в условиях линкер-группа терапевтического агента конъюгата антитело-лекарственное средство, как описано в настоящем документе).
Различные примеры линкеров, которые можно использовать с настоящими композициями и способами, описаны в WO 2004-010957, патентная публикация США 2006/0074008, США 20050238649 и США 2006/0024317 (каждая из которых включена в настоящий документ в качестве ссылки в полном объеме и для всех целей).
Некоторые примеры конъюгатов антитело-лекарственное средство (ADC), существующие в настоящее время в клинической практике, можно найти в статье Feng, Y. et al. Conjugates of Small Molecule Drugs with Antibodies and Other Proteins. Biomedicines 2014, 2, 1-13; doi:10.3390/biomedicines2010001.
Ввиду большого количества способов, описываемых для присоединения разнообразных терапевтических агентов, визуализирующих агентов, детектируемых агентов, диагностических агентов, рентгенодиагностических соединений, радиотерапевтических соединений, лекарственных средств, токсинов и других агентов к антителам и их фрагментам, специалисту в данной области не составит труда определить подходящий способ для присоединения такого агента к антителу или его тау-связывающему фрагменту. В другом варианте осуществления (A) и (C) непосредственно связаны друг с другом.
В другом варианте осуществления (L) представляет собой спейсерную группу или связывающую группу, такую как полиальдегид, глутаровый альдегид, этилендиаминтетрауксусная кислота (EDTA) или диэтилентриаминпентауксусная кислота (DPTA).Другие способы присоединения антитела или фрагмента с другому соединению включают образование дисульфидных связей с использованием N-сукцинимидил-3-(2-пиридилтио)пропионата (SPDP) и сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилата (SMCC) или производных (если пептид не содержит сульфгидрильную группу, то это может быть осуществлено при добавлении остатка цистеина).Эти реагенты создают дисульфидную связь между собой и пептидным остатком цистеином, находящемся на одном белке, и амидную связь через.эпсилон.-амино на лизине или другую свободную аминогруппу в других аминокислотах. Множество таких дисульфидных/амид-образующих агентов описано в Immun.Rev.62, 185 (1982). Другие бифункциональные связывающие агенты образуют тиоэфир, а не дисульфидную связь. Многие из таких тио-эфир-образующих агентов являются коммерчески доступными и включают реакционноспособные сложные эфиры 6-малеимидокапроновой кислоты, 2-бромуксусной кислоты и 2-йодуксусной кислоты, 4- (N-малеимидометил)циклогексан-1-карбоновой кислоты. Карбоксильные группы могут быть активированы путем объединения с сукцинимидом или 1-гидроксил-2-нитро-4-сульфоновой кислотой, натриевой солью.
Нагрузка лекарственным средством представлена р и представляет собой среднее количество молекул лекарственного средства на антитело в молекуле (например, A-L-Dp). Нагрузка лекарственным средством может составлять от 1 до 20 групп лекарственного средства (D) на антитело. ADC по изобретению включают коллекции антител, конъюгированных с рядом молекул лекарственного вещества в количестве от 1 до 20. Среднее количество молекул лекарственного средства на антитело в препаратах ADC в результате реакций конъюгирования можно охарактеризовать обычными средствами, например, масс-спектроскопией и ИФА. Также может быть определено количественное распределение ADC по отношению к р. В некоторых случаях путем таких средств, как электрофорез, можно получить разделение, очистку и оценку характеристик гомогенного ADC, в котором p представляет собой определенное значение, от ADC с другими значениями лекарственной нагрузки.
Для некоторых конъюгатов антитело-лекарственное средство p может быть ограничен количеством сайтов присоединения на антителе. Например, если присоединяемая группа представляет собой тиоловую группу цистеина, как в характерных вышеприведенных вариантах осуществления, то антитело может содержать только одну или несколько тиоловых групп цистеина, или может содержать только одну или несколько достаточно реакционноспособных тиоловых групп, к которым может быть присоединен линкер. В некоторых вариантах осуществления высокая лекарственная нагрузка, например, p > 5, может привести к агрегации, нерастворимости, токсичности или потере способности некоторых конъюгатов антитело-лекарственное вещество проникать в клетку. В некоторых вариантах осуществления изобретения лекарственная нагрузка для ADC по изобретению составляет от 1 до 8; от примерно 2 до примерно 6; от примерно 3 до примерно 5; от примерно 3 до примерно 4; от примерно 3,1 до примерно 3,9; от примерно 3,2 до примерно 3,8; от примерно 3,2 до примерно 3,7; от примерно 3,2 до примерно 3,6; от примерно 3,3 до примерно 3,8; или от примерно 3,3 до примерно 3,7.Показано, что для некоторых ADC фактическое оптимальное соотношение молекул лекарственного вещества на антитело может быть менее 8 и может составлять от приблизительно 2 до приблизительно 5. См. патентСША№7498298.
В некоторых вариантах осуществления количество молекул лекарственного вещества, конъюгированных с антителом в ходе реакции конъюгирования, составляет меньше теоретического максимального значения. Антитело может содержать, например, остатки лизина, которые не реагируют с промежуточным соединением лекарственное средство-линкер или линкерным реагентом, как обсуждается ниже. Как правило, антитела не содержат большого количества свободных и реакционноспособных тиоловых групп цистеина, которые могут связываться с молекулой лекарственного средства; фактически, большинство тиоловых остатков цистеина в составе антител существуют в виде дисульфидных мостиков. В некоторых вариантах осуществления антитело может быть восстановлено с помощью восстанавливающего агента, например, дитиотрейтола (ДТТ) или трикарбонилэтилфосфина (TCEP) при частично или полностью восстановительных условиях с получением реакционноспособных тиоловых групп цистеина. В некоторых вариантах осуществления антитело подвергают воздействию денатурирующих условий для выявления реакционноспособных нуклеофильных групп, таких как лизин или цистеин.
Нагрузку (соотношение лекарственное средство/антитело) в ADC можно контролировать различными способами, например:(i) ограничивая молярный избыток промежуточного соединения лекарственное средство-линкер или линкерного реагента по отношению к антителу, (ii) ограничивая время или температуру реакции конъюгирования и (iii) посредством частичных или лимитирующих восстановительных условий для модификации тиоловых групп цистеина, (Iv) конструирование рекомбинантными методиками аминокислотной последовательности антитела таким образом, чтобы количество и положение остатков цистеина было модифицировано для контроля количества и/или положения присоединений линкер-лекарственное средство (таких как тиоMab или тиоFab, полученных как описано в настоящем документе и в WO2006/034488.
Следует понимать, что при реакции более чем одной нуклеофильной группы с промежуточным соединением лекарственное средство-линкер или с линекрным реагентом, а затем реагентом молекулы лекарственного средства, полученный продукт представляет собой смесь соединений ADC с распределением одной или нескольких молекул лекарственного средства, присоединенных к антителу. Среднее количество лекарственного средства на антитело в смеси можно рассчитать с помощью двойного твердофазного анализа антитела ELISA, специфичного по отношению к антителу и лекарственному средству. Отдельные молекулы ADC могут быть идентифицированы в смеси с помощью масс-спектроскопии и разделены с помощью ВЭЖХ, например хроматографией гидрофобного взаимодействия (см., например, Hamblett, K J., et al."Effect of drug loading on the pharmacology, pharmacokinetics, and toxicity of an anti-CD30 antibody-drug conjugate," Abstract No.624, American Association for Cancer Research, 2004 Annual Meeting, Mar.27-31, 2004, Proceedings of the AACR, Volume 45, March 2004; Alley, S.C., et al."Controlling the location of drug attachment in antibody-drug conjugates," Abstract No.627, American Association for Cancer Research, 2004 Annual Meeting, Mar.27-31, 2004, Proceedings of the AACR, Volume 45, March 2004). В некоторых вариантах осуществления из конъюгационной смеси можно выделить гомогенный ADC с одинаковым значением нагрузки посредством электрофореза или хроматографии.
В некоторых вариантах осуществления антитело или его тау-связывающий фрагмент, описанные в настоящем документе, могут быть введены в состав вместе с одним или более дополнительными соединениями и/или могут быть введены вместе с одним или более дополнительными соединениями, которые используются для профилактики/лечения AD.К ним относятся, но ими не ограничиваются, соединения, которые могут использоваться для активной и пассивной иммунотерапии при AD, такие как бета-амилоидные пептиды (например,N-концевые бета-амилоидные пептиды), тау-пептиды, которые могут быть конъюгированны или нет с другими соединениями, таких как мутированный дифтерийный токсин; другие антитела против бета-амилоида, такие как бапинезумаб, соланезумаб, гантенерумаб, кренезумаб, понезумаб и иммуноглобулин IVIG, другие иммунологические лекарственные средства, нацеливающиеся на олигомеры A-бета, другие антитела против тау-белка, соединения, предотвращающие гиперфосфорилирование тау-белка, и другие активные и пассивные иммунологические лекарственные средства, нацеливающиеся на тау-агрегаты. Другие лекарственные средства, которые должны быть эффективны при комбинированной терапии с антителами и тау-связывающими фрагментами, описанными в настоящем документе, представляют собой ингибиторы агрегации бета-амилоида (например, трамипросат), ингибиторы гамма-секретазы (например, семагацестат) и модуляторы гамма-секретазы (таренфлурбил). Кроме того, одно или больше антител по изобретению могут быть использованы в сочетании с двумя или более из вышеупомянутых терапевтических средств. На ранних стадиях заболевания комбинированная терапия может быть эффективной. На более поздних стадиях заболевания, также эффективна комбинированная терапия, например, комбинации hAb и факторов роста и других биологически активных молекул, вызывающих пластичность нейронов и регенерацию. Такая комбинированная терапия может преимущественно использовать более низкие дозы вводимых терапевтических агентов, что позволяет избежать возможных токсических эффектов или осложнений, связанных с различной монотерапией. Согласно соответствующему варианту осуществления антитело или его тау-связывающий фрагмент, описанные в настоящем документе, используются в комбинации (вводятся раздельно, до, одновременно с другим или после другого) с по меньшей мере одним агентом комбинации, выбранным из ингибиторов ацетилхолинэстеразы (например, донепезил, ривастигмин, галантамин, такрин, пищевые добавки), антагонистов рецептора N-метил-D-аспартата (NMDA) (например, мемантин), ингибиторов восстановления ДНК (например, пирензепин или его метаболит), хелаторов переходных металлов, факторов роста, гормонов, нестероидных противовоспалительных препаратов (NSAID), антиоксидантов, агентов, уменьшающих уровень липидов, селективных ингибиторов фосфодиэстеразы, ингибиторов агрегации тау-белка, ингибиторов протеинкиназы, лекарственных средств ингибиторов лекарств митохондриальной дисфункции, нейротрофинов, ингибиторов белков теплового шока, ингибиторов липопротеин-связанной фосфолипазы A2 и любой их фармацевтически приемлемой соли. В одном из вариантов осуществления лечение антителом и/или его тау-связывающим фрагментом комбинировано с лечением ингибиторами холинэстеразы (ChEI) и/или мемантином, которые дают скромный симптоматический эффект. В одном из вариантов осуществления терапевтический агент для комбинации выбран из группы, состоящей из антиапоптотического соединения, хелатора металла, ингибитора репарации ДНК, 3-амино-1-пропансульфоновой кислоты (3APS), 1,3-пропандисульфоната (1,3PDS), активатора секретазы, ингибитор бета-секретазы, ингибитора гамма-секретазы, бета-амилоидного пептида, антитела против бета-амилоида, нейромедиатора, разрушителя бета-структуры, противовоспалительной молекулы и ингибитора холинэстеразы. В одном из вариантов осуществления ингибитором холинэстеразы является такрин, ривастигмин, донепезил, галантамин или пищевая добавка. В других вариантах осуществления дополнительное терапевтическое средство выбрано из ингибиторов BACE; мускариновых антагонистов; ингибиторов холинэстеразы; ингибиторов гамма-секретазы; модуляторов гамма-секретазы; ингибиторов HMG-CoA-редуктазы; нестероидных противовоспалительных средств; антагонистов рецептора N-метил-D-аспартата; антител против амилоида; витамина Е; агонистов никотинацетилхолинового рецептора; обратных агонистов рецептора CB1 или антагонистов рецептора CB1; антибиотика; стимуляторов секреции гормона роста; антагонистов гистамина Н3; агонистов АМРА; ингибиторов PDE4; обратных агонистов GABAA; ингибиторов амилоидной агрегации; ингибиторов гликогенсинтаза-киназа бета; промоторов активности альфа секретазы; ингибиторов PDE-10 и ингибиторов абсорбции холестерина.
Другие соединения, которые подходят для применения в комбинации с антителом или тау-связывающим фрагментом, описанными в настоящем документе, описаны в WO 2004/058258 (см. в частности стр.16 и 17), включая мишень-нацеленные терапевтические средства (стр.36-39), алкансульфоновые и алканолсульфуровые кислоты (стр.39-51), ингибиторы холинэстеразы (стр.51-56), антагонисты рецептора NMDA (стр.56-58), эстрогены (стр.58-59), нестероидные противовоспалительные препараты (стр.60-61), антиоксиданты (стр.61-62), гамма-рецепторы, активируемые пролифераторами пероксисом (стр.63-67), средства, снижающие холестерин (стр.68-75); ингибиторы амилоида (стр.75-77), ингибиторы образования амилоида (стр.77-78), хелаторы металлов (стр.78-79), антипсихотические препараты и антидепрессанты (стр.80-82), пищевые добавки (стр.83-89) и соединения, повышающие доступность биологически активных веществ в мозге (см. стр.89-93) и пролекарства (стр.93 и 94).
В одном из вариантов осуществления антитело и/или его тау-связывающий фрагмент используются в сочетании с существующим стандартом лечения во время лечения, который включает ингибиторы холинэстеразы и антагонист NMDA мемантин (Namenda).
Фармацевтические композиции по изобретению могут включать «терапевтически эффективное количество» или «профилактически эффективное количество» антитела или его тау-связывающего фрагмента по изобретению. «Терапевтически эффективное количество» относится к количеству эффективному, в дозах и в течение необходимого периода времени, для достижения желаемого терапевтического результата. Терапевтически эффективное количество антитела или его тау-связывающего фрагмент может изменяться в зависимости от таких факторов, как болезненное состояние, возраст, пола и вес индивиддума и способность антитела или его тау-связывающего фрагмента вызывать желаемый ответ у индивидума. Терапевтически эффективное количество также является количеством, при котором любые токсичные или вредные эффекты антитела или его тау-связывающего фрагмента перевешивают терапевтический эффект. «Профилактически эффективное количество» относится к количеству эффективному, в дозах и в течение необходимого периода времени, для достижения желаемого профилактического результата. Как правило поскольку профилактическая доза используется у индивидуума до или на ранней стадии заболевания, профилактически эффективное количество будет меньше терапевтически эффективного количества.
Режимы дозирования можно регулировать для получения оптимального желаемого ответа (например, терапевтического или профилактического ответа). Например, может быть проведен протокол инфузии или введен единичный болюс, могут быть введены несколько разделенных доз в течение определенного времени или доза может быть пропорционально уменьшена или увеличена, на что указывает острота терапевтической ситуации. Особенно предпочтительно получить парентеральные композиции в единичной дозированной форме для простоты введения и однородности дозы. Дозированная лекарственная форма, как используется в настоящем описании, относится к физически дискретным единицам, подходящим в качестве единичных доз для индивидов, в отношении которых проводится лечение; причем каждая единица содержит заданное количество активного соединения, рассчитанного для получения желаемого терапевтического эффекта в сочетании с необходимым фармацевтическим носителем. Требования к дозированным лекарственным формам по изобретению связаны и напрямую зависят от (a) уникальных характеристик активного соединения и необходимости достичь конкретный терапевтический или профилактический эффект, и (b) ограничений в области получения такого активного соединения для лечения болезненной реакции у индивидов.
Следует отметить, что значения дозы могут изменяться в зависимости от тяжести состояния, которое необходимо облегчить. Кроме того, необходимо понимать, что для любого конкретного индивида, конкретные схемы введения должны быть скорректированы через некоторое время согласно индивидуальной потребности и на усмотрение медицинского работника, который осуществляет введение или контролирует введения композиций, и что диапазоны дозы, приведенные в данном описании, приведены только в качестве примера и не предназначены для ограничения объема или практики заявленной композиции.
Например, эффективные дозы композиций по настоящему изобретению для лечения состояний, описанных ниже, изменяются в зависимости от многих факторов, включая способы введения, место назначения, физиологическое состояние пациента, независимо от того, является ли пациент человеком или животным, введения других лекарственных средств и является ли лечение профилактическим или терапевтическим. Как правило, пациентом является человека. Дозировки для лечения должны быть титрированы для оптимизации безопасности и эффективности. Соответственно, лечение антителом или его тау-связывающим фрагментом обычно влечет за собой прием множественных доз в течение периода времени.
Примерный неограничивающий диапазон терапевтически или профилактически эффективного количества антитела или его тау-связывающего фрагмента по изобретению для людей составляет 0,1-20 мг/кг, более предпочтительно 1-10 мг/кг. В одном из предпочтительных вариантов осуществления антитело вводят в множественных доз в течение по меньшей мере трех месяцев, предпочтительно, по меньшей мере шести месяцев и дозы от 1 до 10 мг/кг. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,01-0,6 мг/кг и с частотой от еженедельного введения до ежемесячного. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,05-0,5 мг/кг. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,05-0,25 мг/кг. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,015-0,2 мг/кг раз в неделю или раз в две недели. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,05-0,15 мг/кг раз в неделю или раз в две недели. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,05-0,07 мг/кг раз в неделю. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,06 мг/кг раз в неделю. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,1-0,15 мг/кг раз в две недели. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,1-0,3 мг/кг раз в неделю. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 0,2 мг/кг раз в неделю. Необязательно, антитело или его тау-связывающий фрагмент вводят один раз в год. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 1-40 мг и с частотой от раз в неделю до раз в месяц. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 5-25 мг. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 2,5-15 мг. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 1-12 мг раз в неделю или раз в две недели. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 2,5-10 мг в неделю или раз в две недели. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 2,5-5 мг раз в неделю. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 4-5 мг раз в неделю. Необязательно, антитело или его тау-связывающий фрагмент вводят в дозе 7-10 мг раз в две недели.
В других вариантах осуществления пассивной иммунизации антителом или тау-связывающим фрагментом, как описано в настоящем документе, доза колеблется от приблизительно 0,0001 до 100 мг/кг и чаще от 0,01 до 5 мг/кг массы тела хозяина. В некоторых вариантах применения количество антитела или его тау-связывающего фрагмента можно вводить в дозе по меньшей мере 0,1 мг/кг массы тела, в дозе по меньшей мере 0,5 мг/кг массы тела, 1 мг/кг массы тела или любой комбинации доз от 0,1 до 10 мг/кг массы тела. В некоторых способах антитело или его тау-связывающий фрагмент можно вводить в нескольких дозах (одинаковых или разных) в течение по меньшей мере 1 месяца, по меньшей мере 3 месяцев или по меньшей мере 6 месяцев. Общее количество доз за любой период лечения может составлять, например, от 4 до 6, хотя в зависимости от факторов, описанных выше, могут использоваться другие числа. Лечение можно контролировать с помощью любого из способов, описанных ниже.
Подходящие составы антител можно также определить, исследуя опыт других, уже разработанных, терапевтических моноклональных антител. Например, было доказано, что несколько моноклональных антител, таких как Ритуксан (Ритуксимаб), Герцептин (Трастузумаб), Ксолар (Омализумаб), Бексар (Тозитумомаб), Кампат (Алемтузумаб), Зевалин, Онколим, Ремикейд (Инфликсимаб), Луцентис (Ранибизумаб), Синагиз (Паливизумаб), Солирис (Экулизумаб), Кадсила (адо-трастузумаб эмтанзин), Авастин (Бевацизумаб), Эрбитукс (Цетуксимаб), Симпони (Голимумаб), Тисабри (Натализумаб), МабТера (Ритуксимаб), Стелара (Устекинумаб), Притумумаб и Адуканумаб, являются эффективными в клинических ситуациях, а также могут быть использованы аналогичные составы с антителами по изобретению. Например, моноклональное антитело можно вводить в концентрации 10 мг/мл в одноразовых флаконах по 100 мг (10 мл) или 500 мг (50 мл), приготовленных для в.в. введения в 9,0 мг/мл хлорида натрия, 7,35 мг/мл дигидрата цитрата натрия, 0,7 мг/мл полисорбата 80 и стерильной воды для инъекций. Значение рН доводят до 6,5. В другом варианте осуществления антитело поставляется в составе, содержащем приблизительно 20 мМ Na-цитрата, приблизительно 150 мМ NaCl, при рН около 6,0.
Способы лечения и профилактики
Антитела и композиции, описанные в настоящем документе, могут быть использованы для различных способов лечения и профилактики AD и связанных таупатий. Кроме полезного свойства снижения иммуногенности эти антитела имеют по меньшей мере 80% связывающую аффинность в отношении патологического тау-белка, чем исходное антитело DC8E8 мыши.DC8E8 мыши подробно описано в в WO 2013/041962, где показано, что оно обладает терапевтическими свойствами на модели AD in vivo. Таким образом, есть разумные основания полагать, что гуманизированное DC8E8 также будет эффективно для терапии и профилактики AD человека, при этом вероятно вызывая менее негативный иммунологический ответ.
В одном из вариантов осуществления способ включает введение антител, нуклеиновых кислот, кодирующих их, или фармацевтических композиций, как описано в настоящем документе, индивиду/пациенту. При профилактическом применении фармацевтические композиции или лекарственные средства вводят пациенту, подверженному болезни Альцгеймера или другой таупатии, или имеющему риск их возникновения, в количестве, достаточном для устранения или снижения риска, уменьшения тяжести или задержки развития заболевания, включая биохимические, гистологические и/или поведенческие симптомы заболевания, его осложнения и промежуточные патологические фенотипы, проявляющиеся при развитии заболевания. При терапевтическом применении композиции или лекарственные средства вводят пациенту, у которого предполагают наличие, или который уже страдает таким заболеванием, в количестве, достаточном для лечения или по меньшей мере частичного прекращения симптомов заболевания (биохимических, гистологических и/или поведенческих), включая осложнения и промежуточные патологические фенотипы при развитии заболевания.
Как используется в настоящем описании «лечение» включает применение или введение терапевтического агента индивиду, у которого есть болезнь, признак заболевания или предрасположенность к заболеванию, с целью лечения, исцеления, облегчения, ослабления, изменения, коррекции, улучшения, нормализации или воздействия на болезнь, симптомы болезни или предрасположенность к болезни. Кроме того, если композиции по изобретению, либо сами по себе, либо в сочетании с другим терапевтическим агентом, излечивают, исцеляют, облегчают, ослабляют, изменяют, корректируют, улучшают, нормализуют или воздействуют по меньшей мере на один симптом болезни Альцгеймера или другую тауопатию, в отношении которой проводят лечение, по сравнению с таким симптомом при отсутствии использования композиции гуманизированного антитела против антитела или его тау-связывающего фрагмента, результат следует рассматривать как эффективное лечение основного расстройства независимо от того, все ли симптомы расстройства излечены, исцелены, облегчены, ослаблены, изменены, корректированы, улучшены, нормализованы или на которые было осуществлено воздействие.
У индивидуума "с риском" болезнь может быть обнаружена или нет, или заболевание у него может проявляться или нет перед проведением способов лечения, описанных в настоящем документе. «С риском» означает, что у индивида есть один или несколько так называемых факторов риска, которые являются измеримыми параметрами, которые коррелируют с развитием болезни Альцгеймера. Индивиды с один или несколькими этими факторами риска имеет более высокую вероятность развития болезни Альцгеймера, чем индивиды без этого фактора(ов) риска. Эти факторы риска включают, но ими не ограничиваются, возраст, пол, расу, диету, предшествующее заболевание в анамнезе, наличие предшествующего заболевания, генетическую (то есть, наследственную) предрасположенность и воздействие окружающей среды, и хорошо известны среднему специалисту в данной области.
В одном из вариантов осуществления настоящее изобретение относится к способу лечения или профилактики прогрессирования болезни Альцгеймера или другой тауопатии у индивида, причем способ включает введение указанному индивиду эффективного количества по меньшей мере одного антитела и/или его тау-связывающего фрагмента, как предусмотрено в настоящем описании. В некоторых вариантах способ способен уменьшить двигательные нарушения, улучшить двигательную функцию, уменьшить когнитивное нарушение, улучшить когнитивную функцию, или их комбинации.
В других вариантах осуществления в описании раскрыт способ улучшения по крайней мере одного симптома, связанного с болезнью Альцгеймера или другой таупатии у индивида, способ включает введение указанному индивиду эффективного количества по крайней мере одного антитела и/или его тау-связывающего фрагмента, как раскрыто в настоящем документе.
В одном из вариантов осуществления настоящее изобретение относится к способу задержки прогрессирования болезни Альцгеймера. В одном из вариантов осуществления «задержка» развития болезни Альцгеймера означает отсрочку, торможение, замедление, сдерживание, стабилизирование и/или отложение развитие заболевания. Эта задержка может быть различной по времени, в зависимости от истории болезни и/или индивиду, получающего лечение. Как очевидно специалисту в данной области достаточная или значительная задержка может, по существу, включать профилактику, поскольку у индивидуума не начинается заболевание. В одном из вариантов осуществления способ, который «задерживает» развитие болезни Альцгеймера, представляет собой способ, который уменьшает вероятность развития заболевания в заданные временные рамки и/или уменьшает степень заболевания в заданные временные рамки по сравнению с отсутствием проведения способа. Такие сравнения, как правило, основаны на клинических исследованиях с использованием статистически значимого числа индивидов.
Пациенты, индивиды или индивидуумы включают млекопитающих, таких как человек, крупный рогатый скот, лошади, собаки, кошки, свиньи и овцы. Индивидом предпочтительно является человек, который может страдать или не страдать болезнью или в настоящее время проявлять симптомы. В случае болезни Альцгеймера практически у любого есть риск развития болезни Альцгеймера, если он или она живет достаточно долго. Следовательно, способы по настоящему изобретению могут проводиться профилактически в общей популяции без необходимости какой-либо оценки риска пациента-индивидума.
В одном из вариантов осуществления пациенту необязательно проводят диагностический тесту перед началом лечения. В одном из вариантов осуществления способы по настоящему изобретению эффективны для индивидуумов, у которых существует известный генетический риск развития болезни Альцгеймера. К таким индивидам относятся индивиды, чьи родственники страдали этим заболеванием, и индивиды, чей риск определяется анализом генетических или биохимических маркеров. Генетические маркеры риска болезни Альцгеймера включают мутации в гене APP, в частности мутации в положении 717 и положениях 670 и 671, называемые мутациями Hardy и Swedish, соответственно (см. Hardy (1997) Trends Neurosci.20:154-9). Другими маркерами риска являются мутации в генах пресенилина, PS1 и PS2, и ApoE4, семейный анамнез AD, гиперхолестеринемия или атеросклероз. Индивиды, в настоящее время страдающие болезнью Альцгеймера, могут быть распознаны по характерной деменции, а также по наличию факторов риска, описанных выше. Кроме того, существует ряд диагностических тестов для выявления лиц, страдающих AD.К ним относятся измерение CSF тау-белка и уровни амилоида-бета42.Повышенный тау-белок и пониженные уровни амилоида-бета42 означают наличие AD. В одном из вариантов осуществления индивиды, страдающие болезнью Альцгеймера, могут быть диагностированы по критериями ADRDA (болезнь Альцгеймера и связанные с ней расстройства). У бессимптомных больных лечение можно начинать в любом возрасте (например,10, 20, 30).Обычно, однако, нет необходимости начинать лечение, до тех пор пока возраст пациента не достигнет 40, 50, 60 или 70.Обычно лечение предусматривает несколько доз в течение определенного периода времени. В течение времени лечение может контролироваться различными способами, известными в данной области. В случае возможных пациентов с синдромом Дауна лечение может начаться во внутриутробном периоде путем введения терапевтического агента матери или сразу после рождения.
Отбор пациентов может быть осуществлен с помощью любого из критериев отбора, используемых в области лечения AD и связанных с ней таупатий. В одном из вариантов осуществления критериями являются критерии, определенные конкретным клиническим испытанием. В другом варианте осуществления критериями являются критерии, определенные утвержденным режимом лечения. Может применяться комбинация критериев включения и исключения. Примеры критериев включения включают, но ими не ограничиваются: диагностика возможной болезни Альцгеймера на основе критериев NINCDS/ADRDA; подтвержденная АД легкой или умеренной степени, если показатель MMSE находится в диапазоне от 15 до 26; результат магнитно-резонансной томографии (МРТ) головного мозга пациента согласуется с диагнозом AD; наличие тау-патологии в мозге пациентов, определяемое подходящими методами визуализации, например, используя радиоактивные препараты на основе (11)C-PBB3 или лансопразола; и возраст от 50 до 85 лет.
В одном из вариантов осуществления выбор пациента проводят по способу, описанному в статье Rollin-Sillaire et al. Reasons that prevent the inclusion of Alzheimer's disease patients in clinical trials. Br J Clin Pharmacol. Apr 2013; 75(4):1089-1097.
Ряд итоговых показателей и основной определяемый параметр приведен в настоящем описании для некоторых вариантов осуществления того как оценивать лечение и определять эффективное количество. В одном из вариантов осуществления измерения первичных результатов в заданном временном периоде включают показатели среднего изменения согласно шкале оценки болезни Альцгеймера - когнитивной субшкале 13 (ADAS-Cog13) и показатели среднего изменения по шкале оценки повседневной деятельности при болезни Альцгеймера в ходе совместного исследования (ADCS-ADL), а измерения вторичных результатов включают изменение биомаркеров (общий тау-белок, фосфорилированный тау-белок, уровни Aбета 1-42) в церебро-спинальной жидкости, изменение волюметрии МРТ, оцененной на структурной МРТ, изменение в рейтинге клинической деменции (CDR-SB/CDR-GS), изменение в нейропсихиатрическом поведении: общее число баллов и групповые баллы в опроснике для оценки нейропсихиатрического состояния (NPI), изменение когнитивной функции: общий балл MMSE и/или безопасность: частота нежелательных событий, серьезных побочных эффектов и прекращение лечения. В другом варианте осуществления первичные конечные точки включают любое из следующего: время до наступления смерти, институционализацию, потерю способности к выполнению повседневную деятельность, тяжелую деменцию, замедление уровня прогрессирования заболевания, ADCS-ADL, балл ADAS-cog, баллы MMSE, когнитивную деятельность, биомаркеры CSF в плазме, общий балл ADAS, балл качества жизни, оцененного по шкале качества жизни при болезни Альцгеймера, баллы поведенческих тестов, и Клиническая рейтинговая шкала деменции - сумма боксов FDA США.
В одном из вариантов осуществления лечение болезни Альцгеймера относится к уменьшению или профилактике ухудшения поведенческих, функциональных и познавательных функций со временем. В некоторых вариантах поведенческие, функциональные и когнитивные аспекты болезни Альцгеймера могут быть оценены одним или несколькими тестами из ряда стандартизированных тестов, известных среднему специалисту в данной области, включая, но ими не ограничиваясь, нейропсихологическое тестирование, мини-тест на умственное состояние, мини-тест на когнитивное состояние, опросник для оценки нейропсихиатрического состояния, шкала оценки деменции Блесседа-Рота, испанская и английская шкала нейропсихологической оценки (SENAS), психиатрическая поведенческая оценка, функциональная оценка, тест "рисования часов", Бостонский тест на называние, Калифорнийский тест вербального научения, список когнитивных симптомов, тест на непрерывную деятельность, контролируемый устный тест на словесную ассоциацию, Когнистат (шкала оценки нейроповеденческих и когнитивных функций), d2-тест на внимание, система оценки управляющих функций Делис-Каплан, шкала оценки слабоумия, цифровой тест на бдительность, фигуральный тест на беглость, тест на "постукивание", тест категории Халстеда, батарея нейропсихологическиз тестов Халстеда-Рейгана, тест зрительной ориентации Хупера, нейрокогнитивная оценка Каплана Бейкреста, короткая нейропсихологическая оценка Кауфмана, батарея нейропсихологических тестов Лурия-Небраска, шкалы оценки памяти, быстрый неврологический скрининг-тест, повторяемая батарея для оценки нейропсихологического статуса, тест Струпа, тест на сопоставление символов и цифр, тестирование осязательного восприятия, тематический апперцептивный тест, формы А и В теста "оставления следов", Вербальный (устный) тест на беглость, и висконсинский тест сортировки карточек. Также используются дополнительные тесты на депрессию, тревожное состояние, афазию, ажитацию и поведенческие параметры, известные специалистам в данной области.
В другом варианте осуществления лечение болезни Альцгеймера определяется по улучшению или отсутствию ухудшения или уменьшению скорости ухудшения по меньшей мере в одной из оценок, выбранных из группы, состоящей из шкалы оценки тяжести болезни Альцгеймера - когнитивная подшкала (ADAS-cog), рейтинга клинической оценки слабоумия по сумме боксов (CDR-sb), шкалы оценки повседневной деятельности при болезни Альцгеймера в ходе совместного исследования (ADCS-ADL), опросника для оценки нейропсихиатрического состояния (NPI) и минитеста на психическое состояние (MMSE). В некоторых вариантах осуществления лечение приводит к уменьшению скорости ухудшения показателей ADAS-cog. В других вариантах осуществления лечение приводит к среднему уменьшению скорости ухудшения показателей ADAS-cog от двух до пяти баллов.
В одном из вариантов осуществления пациенты идентифицированы и/или выбраны на основе ʺGuidance for Industry, Alzheimer's Disease: Developing Drugs for the Treatment of Early Stage Disease,ʺ FDA, доступного в исправленной редакции от Управления по контролю за продуктами и лекарствами США.
В одном из вариантов осуществления диагностику болезни Альцгеймера у человека осуществляют согласно критериям, разработанных Национальными институтами неврологических и коммуникативных нарушений и инсульта (National Institutes of Neurological and Communicative Disorders and Stroke - NINCDS) и Ассоциацией болезни Альцгеймера и родственных нарушений (Alzheimer's disease and Related Disoders Association - ADRDA (NINCDS-ADRDA).
Периодическое использование одного или нескольких из этих тестов может быть рекомендовано врачом или другим медицинским работником для оценки прогрессии или регрессию болезни Альцгеймера и связанных с ней таупатий и для необходимости дальнейшего лечения. Выбор теста и определение эффективности лечения находятся в компетенции медицинских работников в области болезни Альцгеймера. Улучшенный показатель в одном или нескольких тестах указывает на снижение тяжести болезни Альцгеймера у этого индивида.
Способы диагностики
Благодаря способности обнаруживать патологические формы тау-белка антитела и их тау-связывающие фрагменты, описанные в настоящем документе, эффективны для многих других практических применений. Примеры таких применений включают, но не ограничиваются ими, анализ патологического тау-белка, скрининг предрасположенности к заболеванию, диагностирование заболевания, прогноз заболевания, мониторинг прогрессирования заболевания, определение терапевтических стратегий, основанных на типе индивидуума и уровне патологического тау-белка, разработка терапевтических агентов на основе уровней патологического тау-белка и типа, связанного с заболеванием, или вероятностью ответа на лекарственное средство, стратификации популяции пациентов для клинических испытаний для лечения, и прогнозирования вероятности того, что индивид будет отвечать на терапевтический агент. Методы in vitro для выявления патологических тау-белков, связанных с болезнью Альцгеймера и связанного с ней таупатий, с помощью антител и тау-связывающих фрагментов, которые раскрыты в настоящем документе, включают, но ими не ограничиваются, твердофазные иммуноферментные анализы (ELISA), радиоиммунологические анализы (RIA), Вестерн-блоты, иммунопреципитации, иммунофлуоресценцию, сэндвич-анализы и тканевые массивы.
В одном из вариантов осуществления описанные в настоящем документе антитела и их тау-связывающие фрагменты могут быть использованы для оценки распределения патологического тау-белка в ткани, патологической экспрессии во время развития или экспрессии при патологическом состоянии, таком как болезнь Альцгеймера и связанные с ней таупатии. Кроме того, детекция с помощью антител циркулирующего патологического тау-белка может быть использована для определения кругооборота тау-белка во время лечения AD и связанных с ним таупатий.
В соответствующих вариантах осуществления изобретение относится к способу диагностики или скрининга индивида на наличие болезни Альцгеймера или другой тауопатии у индивида или для определения риска развития болезни Альцгеймера или другой таупатии у индивида, включающему:
приведение в контакт организма или клетки, ткани, органа, жидкости или любой другого образца индивида с эффективным количеством по меньшей мере одного антитела и/или тау-связывающего фрагмента, как предусмотрено в настоящем документе; а также
определение наличия комплекса, содержащего патологический тау-белок и антитело и/или его тау-связывающий фрагмент, где наличие комплекса является диагностическим для болезни Альцгеймера или другой тауопатии, связанной с наличием патологического тау.
В некоторых вариантах осуществления антитела и/или их тау-связывающие фрагменты могут быть использованы для обнаружения патологического тау-белка in vivo, ex vivo, in situ, in vitro, в жидкости организма (например, в крови, сыворотке, моче, плазме, цереброспинальной жидкости, слюне) или в клеточном лизате или супернатанте, для оценки уровня и характера экспрессии. В одном из вариантов осуществления антитела и их тау-связывающие фрагменты используют в диагностических тестах in vivo, таких как визуализация in vivo. В некоторых из этих вариантов осуществления антитело мечено радионуклидом (таким как 111In, 99Tc, 14C, 131I, 125I или 3H), так что клетки или ткань, представляющие интерес, отмеченная присутствием антитела (и патологического тау-белка), могут быть локализованы, используя иммуносцинтиграфию. Другие обнаруживаемые метки включают метку, которую можно обнаруживать с помощью аналитических методов, включая, но не ограничиваясь ими, флуоресценцию, хемилюминесценцию, электронно-спиновый резонанс, спектроскопию поглощения ультрафиолетового/видимого света, инфракрасную спектроскопию, масс-спектрометрию, ядерный магнитный резонанс, магнитный резонанс, радиометрический и электрохимический способы.
В одном из вариантов осуществления антитела и их тау-связывающие фрагменты могут быть использованы в способе оценки эффективности лечения болезни Альцгеймера или другой таупатии. В одном из вариантов осуществления способ включает применение одного из антител и его тау-связывающих фрагментов для мониторинга наличия патологического тау-белка перед, во время и после лечения. В одном из вариантов осуществления снижение уровня или типа патологического тау-белка указывает на положительный ответ на проводимое лечение. В другом варианте осуществления отсутствие изменения или увеличение уровня или типа патологического тау-белка указывает на то, что лечение должно продолжаться.
В некоторых вариантах осуществления первая временная точка может быть выбрана до начала профилактики или лечения, а вторая временная точка может быть выбрана через некоторое время после начала профилактики или лечения. Патологические уровни тау-белка могут быть измерены в каждом из образцов, взятых в разные временные точки, и отмечены качественные и/или количественные различия. Изменение количеств одного или более измеренных уровней патологического тау-белка первого и второго образцов может быть сопоставлено с прогнозом, используемым для определения эффективности лечения и/или используемым для определения прогрессирования заболевания у индивида.
Обнаружение антитела или его тау-связывающего фрагмента, как описано в настоящем документе, может быть упрощено путем связывания (т.е. физической связи) антитела или его тау-связывающего фрагмента с обнаруживаемым веществом. Обнаруживаемые вещества включают, но не ограничиваются ими, различные ферменты, протезные молекулы, флуоресцентные вещества, люминесцентные вещества, биолюминесцентные вещества и радиоактивные вещества. Примеры подходящих ферментов включают пероксидазу хрена, щелочную фосфатазу, бета-галактозидазу или ацетилхолинэстеразу; примеры подходящих комплексов с простетическими группами включают стрептавидин/биотин и авидин/биотин; примеры подходящих флуоресцентных веществ включают умбеллиферон, флуоресцеин, флуоресцеин изотиоцианат, родамин, дихлортриазиниламин флуоресцеин, данзил хлорид или фикоэритрин; пример люминесцентного вещества включает лиминол; примеры биолюминесцентных веществ включают люциферазу, люциферин и экворин, а примеры подходящих радиоактивных веществ включают 125I, 131I, 35S и 3H.
Другие варианты применения
Антитела и тау-связывающие фрагменты, описанные в настоящем документе, также могут использоваться для выделения патологических тау-белков из природного клеточного источника или из рекомбинантных клеток-хозяев с помощью стандартных методов, таких как аффинная хроматография или иммунопреципитация. В другом варианте осуществления антитела и тау-связывающие фрагменты, описанные в настоящем документе, могут быть использованы для идентификации других антител, которые связываются с патологическим тау-белком посредством конкурентных анализов.
В одном варианте осуществления антитела могут быть использованы в качестве аффинно-очищающих агентов. В одном из вариантов осуществления антитела или их тау-связывающие фрагменты иммобилизуют на твердой фазе, такой как смола SEPHADEX TM. или магнитных бусах (например, марки Dynal) или на фильтровальной бумаге, используя способы, хорошо известные в данной области. Иммобилизованное антитело контактирует с образцом, содержащим тау-белок (или его фрагмент), который должен быть очищен, и после этого носитель промывают подходящим растворителем, который удаляет практически все вещество в образце, за исключением тау-белка, который связан с иммобилизованным антителом. Наконец, носитель промывают другим подходящим растворителем, таким как глициновый буфер, pH 5,0, который высвобождает тау-белок из антитела.
Также раскрыты наборы для применения антител и их тау-связывающих фрагментов, такие как наборы для определения наличия патологического тау-белка в тестируемом образце. Примерный набор может содержать антитела и их тау-связывающие фрагменты, такие как меченые антитела или антитела, которые могут быть помечены, и соединение или агент для обнаружения вариантов белков в биологическом образце; средство для определения количества или наличия/отсутствия варианта белка в образце; средство для сравнения количества варианта белка в образце со стандартом; и инструкции по применению.
В некоторых вариантах осуществления изобретение относится к медицинскому устройству, содержащему антитело или тау-связывающий фрагмент, как предусмотрено в настоящем документе, где устройство подходит для приведения в контакт или введения антитела или тау-связывающего фрагмента по меньшей мере одним из путей, выбранных из парентерального, подкожного, внутримышечного, внутривенного, внутрисуставного, внутрибронхиального, внутрибрюшного, внутрикапсульного, внутрихрящевого, внутриполостного, внутричревного, внутримозжечкового, интрацеребровентрикулярного, интратекального, интраколического, интрацервикального, внутрижелудочного, внутрипеченочного, интрамиокардиального, внутрикостного, внутритазового, интраперикардиального, интраперитонеального, интраплеврального, интрапростатического, внутрилегочного, ректального, внутрипочечного, интраретинального, интраспинального, интрасиновиального, интраторакального, внутриматочного, интравезикулярного, интралезионального, болюсного, вагинального, ректального, трансбуккального, сублингвального, интраназального, и трансдермального. В одном из вариантов осуществления устройство содержит шприц (например, предварительно заполненный шприц). В другом варианте осуществления устройство содержит пластырь. В другом варианте осуществления устройство содержит насос (например, мини-насос). В другом варианте осуществления устройство содержит ингалятор. В другом варианте осуществления устройство содержит распылитель.
В другом варианте осуществления изделие, содержащее вещества, могут использоваться для лечения AD и связанных с ним таупатий. Изделие может содержать флакон с фиксированной дозой гуманизированного антитела и/или его тау-связывающего фрагмента, содержащегося в нем, и, необязательно, листок-вкладыш. Флакон может быть образован из разнообразных веществ, таких как стекло или пластик, и может быть герметично закрыт пробкой, прокалываемой шприцем. Например, флакон может быть формальным стеклянным флаконом витрум I типа (например,20 см3 флакона для определенной фиксированной дозы или 50 мл флакона для другой фиксированной дозы), с ламинированной пробкой из фторопласта DAIKYO GREY и 20 мм алюминиевой крышкой с откидной крышкой. Изделие также может содержать другие вещества, желательные с коммерческой и пользовательской точки зрения, включая другие буферы, разбавители, фильтры, иглы и шприцы, и тому подобное. В одном из вариантов осуществления изделие содержит два флакона, где первый флакон содержит заданную фиксированную дозу гуманизированного антитела и/или его тау-связывающего фрагмента, а второй флакон содержит другую фиксированную дозу гуманизированного антитела и/или его тау-связывающего фрагмента.
Антитела могут быть использованы для антиидиотипических антител.(см., например, Greenspan & Bona, FASEB J.7(5):437-444, 1989; and Nissinoff, J.Immunol.147:2429-2438, 1991). Такие антиидиотипические антитела можно использовать в фармакокинетических, фармакодинамических, биораспределительных исследованиях, а также в исследованиях клинических ответов на антитела человека (HAHA) у индивидов, получавших антитела. Например, антиидиотипические антитела специфически связываются с вариабельной областью гуманизированных антител DC8E8 и поэтому могут быть использованы для детектирования гуманизированных антител DC8E8 в фармакокинетических исследованиях и помогают количественно оценить реакции на антитела человека (HAHA) у индивидов, получающих лечение.
Все публикации, патентные заявки и патенты, цитированные в настоящем описании, включены в качестве ссылки в той же степени, как если бы каждая отдельная публикация или заявка на патент была конкретно и индивидуальна указана и включена в качестве ссылки. В частности, все публикации, патентные заявки и патенты, цитируемые в настоящем документе, явно включены в настоящее описание в качестве ссылки для описания и раскрытия композиций и методик, которые могут быть использованы в связи с раскрытыми изобретениями.
Следующие сокращения использовали в Примерах, приведенных ниже.
Expi293 клетки эмбриональной почки человека (HEK293 с высокой плотностью/без сыворотки)
A Аденин
по пары оснований
°C Цельсия
C Цитозин
MEM Минимальная необходимая среда
ДНК Дезоксирибонуклеиновая кислота
ELISA иммуноферментный анализ
EC50 Концентрация антитела, обеспечивающая полумаксимальный ответ
EC80 Концентрация антитела, обеспечивающая 80% максимального ответа
ECD Внеклеточный домен
г грамм
G гуанин
HRP Пероксидаза хрена
IgG иммуноглобулин-G
KG или T (конвенция IUPAC)
мин минуты
M A или C (конвенция IUPAC)
нм нанометр
OD Оптическая плотность
PBS фосфатно-солевой буфер
ПЦР полимеразная цепная реакция
R A или G (конвенция IUPAC)
РНК Рибонуклеиновая кислота
комн.темп. комнатная температура
с секунда
SC или G (конвенция IUPAC)
T Тимин
TBS Буферный солевой раствор Tris
УФ ультрафиолет
VA или C или G (конвенция IUPAC)
VH вариабельная область тяжелой цепи иммуноглобулина
VK вариабельная область легкой цепи каппа иммуноглобулина
W A или T (конвенция IUPAC)
Y C или T (соглашение IUPAC)
ПРИМЕРЫ
Пример 1: Получение химерного варианта антитела DC8E8
Общую РНК выделяли из клеток гибридомы DC8E8, используя протокол RNeasy Mini для выделения полной РНК (Qiagen).РНК DC8E8 (3 мкг) подвергали обратной транскрипции с получением кДНК DC8E8,используя набор для синтеза кДНК 1-й цепи GE Life Sciences по протоколу изготовителя. кДНК DC8E8 амплифицировали с помощью ПЦР в 3 отдельных реакциях, как описано в разделе 8.3.кДНК вариабельной области тяжелой цепи иммуноглобулина (VH) амплифицировали с помощью ПЦР с помощью праймеров тяжелой цепи M13-MHV6 плюс MHCmix и праймеров ПЦР легкой цепи каппа M13-MKV5 плюс MKC с использованием Phusion High-Fidelity PCR Master Mix (Thermo Scientific).Результатом каждой реакции ПЦР был единственный продукт амплификации, который очищали с использованием набора для очистки ПЦР QIAquick и секвенировали в обоих направлениях с использованием прямой праймер M13 (TGTAAAACGACGGCCAGT (SEQ ID NO:158)) и обратный праймер M13 (CAGGAAACAGCTATGACC (SEQ ID NO:159)).
MHV указывает праймеры, которые гибридизуются с лидерными последовательностями генов вариабельной области тяжелой цепи мыши, MHCG указывает праймеры, которые гибридизуются с генами константной области мыши. Последовательности, указанные курсивом, указывают прямой M13 или обратный M13 праймер для сиквенса.
MKV обозначает праймер, который гибридизуется с лидерными последовательностями генов вариабельной области легкой цепи каппа мыши; MKC указывает праймер, который гибридизуется с геном константной области каппа мыши. Цветная часть указывает прямой M13 или обратный M13 праймер для сиквенса. Консенсусную последовательность VK DC8E8 ПЦР обозначили VK DC8E8 (фиг.3) и консенсусная последовательность ДНК VH обозначили VH DC8E8 (фиг.4). Анализ линии зародышевой линии показал, что легкая цепь каппа представляет собой VK8 мыши без соматических мутаций (фиг. 5).Тяжелая цепь представляет собой VH1 мыши и демонстрирует ряд соматических мутаций как в CDR, так и в каркасных областях (фиг.6).Появление двух остатков пролина в каркасной области 1 рассматривалось как значимое. Эти остатки могут иметь структурную роль за пределами расстояния 4Å остатков.
Конструирование химерных векторов экспрессии привело к рутинному клонированию амплифицированных вариабельных областей в векторы IgG/каппа (в настоящем документе обозначены как pHuG1, pHuG4 и pHuK, множество которых коммерчески доступны). Клоны, генерирующие правильные конструкции, были выбраны и секвенированы.
Суспендированные клетки Expi293 (Invitrogen), растущие в среде для трансфекции Expi293, и антибиотики ко-трансфицировали вместе с VH.pHuG1 DC8E8 и VK.pHuK DC8E8 или VH.pHuG4 DC8E8 и VK.pHuK DC8E8 (50 мкг ДНК каждый), используя реагент ExpiFectamine 293.Клетки выращивали в 100 мл среды для роста в течение 10 дней. Присутствие γ1κ и γ4κ (химерные антитела DC8E8) измеряли в кондиционированной среде с помощью стандартных методов ELISA.
Тау-связывающую активность каждого химерного антитела измеряли с помощью связывания ELISA и сравнивали с активностью исходного антитела DC8E8 мыши. Каждую лунку 94-луночного планшета MaxiSorp (Nunc) покрывали 50 мкл аликвотами 330 нг/мл Tau 151-391/4R в PBS и инкубировали в течение ночи при 4°С.Лунки промывали 3 раза PBS-T (0,1% Tween20). Свежий планшет блокировали 250 мкл PBS/0,2% BSA/0,05% Tween20 на лунку и инкубировали в течение 1 часа при комнатной температуре. Лунки промывали 3 раза PBS-T (0,1% Tween20). В лунки колонки 1 добавляли 240 мкл антитела (разбавляли в PBS/0,2% BSA/0,05% Tween 20, если необходимо); 120 мкл буфера (PBS/0,2% BSA/0,05% Tween 20) в другие лунки. 120 мкл переносили из колонки 1 в соседние лунки колонки 2.Процедуру продолжали в колонке 12 с серией 2-кратных разведений экспериментальных образцов. 100 мкл на лунку переносили из планшета для разведения в экспериментальный планшет. Планшеты инкубировали в течение 1 часа при комнатной температуре. Лунки промывали 3× PBS-T. Конъюгат козьего антитела против Fc человека с пероксидазой разбавляли 10000× (или антимышиное при 10000-кратном разведении) в PBS/0,2% BSA/0,05% Tween 20 и 100 мкл добавляли в каждую лунку. Планшеты инкубировали в течение 1 часа при комнатной температуре и повторно промывали. В каждую лунку добавляли 150 мкл субстрата (K-Blue) и инкубировали в течение 150 минут при комнатной температуре. Реакцию останавливали, добавляя 50 мкл раствора RED STOP в каждую лунку. Оптическую плотность считывали при 650 нм. Оба химерных антитела связывали Tau 151-391/4R с сопоставимыми значениями EC50, сравнимыми с антителом DC8E8 мыши (фиг.7). Последовательность была использована для конструирования гуманизированного варианта антитела DC8E8.
Пример 2: Гуманизированные варианты мыши DC8E8
Последовательность иммуноглобулина M65092 выбирали в качестве кандидата-донора человека для гуманизированной каркасной области тяжелой цепи (FW) из-за его большей идентичности последовательности и сходства с вариабельной областью тяжелой цепи DC8E8 (VH).Выравнивание последовательностей этих двух вариантных доменов может быть найдено на фиг.8. Следующей стадией была трансплантация CDR1, 2 и 3 из VH DC8E8 в акцептор FW M65092.Остатки человека в положениях 9, 21, 27, 28, 30, 38, 48, 67, 68, 70 и 95 по Кабата не сохраняются в области вариабельной тяжелой цепи дикого типа (RHA) M65092.Из-за их положения (в пределах 4Å от CDR Kabat, используя программу Discovery Studio (Accelrys), за исключением Pro в положениях 9 и 21), эти остатки проверяли на из важность для связывании тау-белка. Эта стадия является одной из самых непредсказуемых процедур при гуманизации моноклональных антител и требует идентификации важных остатков каркасной области исходного антитела, которые необходимо сохранить для значительного сохранения связывающих свойств исходного антитела, при этом минимизируя возможную иммуногенность полученного гуманизированного антитела. Каждый из этих неконсервативных остатков обратно мутировали в эквивалентный мышиный остаток DC8E8, в результате чего были получены различные рекомбинантные вариабельные области тяжелой цепи RHA-RHM. (Фигура 8).
Для того, чтобы гуманизировать легкую цепь, идентифицировали каппа (легкую) цепь человека аналогично процедуре идентификации тяжелой цепи. Первоначальный анализ выявил несколько возможных кандидатов-доноров, но все они оказались VK4 человека со слабой экспрессией. Расширенный анализ с включением CDR1 без одного остатка дал единственный кандидат, X72449, который показал более высокую степень гомологии последовательностей с антителом мыши, чем кандидаты VK4.Последовательность вариабельной легкой цепи каппа легкой цепи (VK) DC8E8 выравнивали с вариабельной областью легкой цепью каппа X72449.Фигура 9.RKA демонстрирует рекомбинантную вариабельную область легкой цепи с CDR DC8E8, привитыми на каркасную область X72449. В альтернативном варианте CDR RKB, DC8E8, привитые на каркас X72449 и остаток 5 по Кабату, обратно мутировали в соответствующий остаток мышиной цепи DC8E8.
Гены RHA-RHM, RKA и RKB синтезировали с помощью GenScript и/или с помощью мутагенеза PCR. Гены были оптимизированы по кодонам с помощью сайленс мутагенеза, чтобы использовать кодоны, преимущественно используемые клетками человека, используя программные алгоритмы, являющиеся собственностью GenScript. Затем каждый из генов RHA-RHM вставляли в векторы экспрессии IgG1 и IgG4 человека, используя способы, обычно используемые в данной области. Гены RKA и RKB вводили в вектор экспрессии легкой цепи K таким же образом. Множество примеров таких векторов экспрессии хорошо известны и коммерчески доступны среднему специалисту в данной области. Клоны секвенировали и получали экспрессионную плазмидную ДНК, используя наборы QIAGEN Plasmid Miniprep/Maxiprep. Препараты экспрессирующей плазмиды, кодирующие все различные гуманизированные и химерные последовательности VH и VK, использовали для трансфекции клеток Expi293, используя набор для экспрессионной системы Invitrogen Expi293, культивировали в течение 10 дней в бессывороточной среде, после чего собирали кондиционированную среду, содержащую каждое секретированное антитело. При желании концентрации антител IgG1k и IgG4k в кондиционированной среде Expi293 измеряли с помощью ELISA, используя стандартные способы количественного определения антител.
Пример 3: Свойства гуманизированных вариантов DC8E8
Связывание тау-белка антителами DC8E8
Связывающую активность с тау-белком (151-139/4R) измеряли методом связывания ELISA, как описано в примере 5. Данные, показанные на рисунке 10, указывают на эффективность связывания исходных вариантов гуманизированного DC8E8. Хотя все варианты связывались с тау-белком, этого исходного набора, антитела, содержащие вариант тяжелой цепи RHB, по-видимому, связываются лучше. Этот вариант тяжелой цепи содержит обратные мутации остатков мыши во всех положениях 9, 21, 27, 28, 30, 38, 48, 67, 68, 70 и 95 по Кабат, что свидетельствует о важности одного или нескольких из этих остатков для поддержания связывающей активности полноразмерного антитела.
Были синтезированы другие версии гуманизированной тяжелой цепи, каждая с единственной обратной мутацией, и их тестировали на связывание с помощью ELISA. Результаты для вариантов IgG4 показаны и суммированы на фигурах 11, 12 и 13. Варианты антитела с RHB, RHD и RHE были сопоставимо лучше любой из гуманизированных легких цепей (RKA и RKB) или химерной легкой цепи (cDC8E8). Поскольку варианты RHD и RHE содержат только одну мышиную обратную мутацию, в отличие от 11 мышиных обратных мутаций в варианте RHB, эти два варианта были выбраны в качестве возможных лидирующих кандидатов в сочетании с вариантом легкой цепи RKA (без мышиной обратной мутации).Удивительно, что эти обратные мутации были достаточны для восстановления связывающей аффинности к гуманизированным антителам. Объединение мутаций RHD и RHE (вариант RHM) не привело к заметному улучшению связывания патологического тау-белка по сравнению с каждой отдельной мутацией.
В свете результатов, описанных выше, вариант с тяжелой цепью (RHM), содержащий как мышиные обратные мутации, присутствующие в RHD и RHE, был получен с помощью сайт-направленного мутагенеза. На фигуре 14 показано связывание тау-белка 151-391/4R варианта RHM гуманизированного антитела DC8E8 и указано, что его сродство к белку не лучше, чем у главного кандидата AX004 (RHD/RKA).
Термостабильность гуманизированных антител-кандидатов к высоким температурам
Целью этого эксперимента является сравнение термостабильности гуманизированных антител. При воздействии более высоких температур, изменяющихся от 30 до 85°С в течение 10 минут, охлаждали до 4°С и использовали в анализе связывания ELISA при концентрации ЕС80 каждого кандидата. Все протестированные антитела по-видимому были одинаково стабильными (фигура 15), и все они становились неактивными только при 70°C, но без какого-либо неблагоприятного эффекта на тау-связывающие свойства.
Определение Tm гуманизированных антител-кандидатов
Для определения температуры плавления основных антител-кандидитов AX004 (DA), AX005 (EA), AX016 (DB) и AX017 (DE), гуманизированные, химерные и мышиные антитела очищали с помощью 2-ступенчатой аффинной хроматографии и системы гель-фильтрации (как описано в Примере 4) и тестировали в тепловом сдвиге. Анализ теплового сдвига представляет собой анализ связывания микропланшетов для контроля кривых термического плавления. В этом способе используют экологически чувствительный краситель SYPRO Orange, свойства связывания белка которого повышаются при денатурации белка. Следовательно, при тепловой денатурации анализируемого белка связывание красителя возрастает и достигает максимума, когда белок полностью денатурирован/развернут. Интенсивность флуоресценции, построенная как функция температуры, таким образом, дает типичную сигмоидную кривую, где точка перегиба кривой (половина максимальной интенсивности) соответствует температуре плавления (Tm) белка. Образцы инкубировали с флуоресцентным красителем (Sypro Orange) в течение 71 цикла при увеличении на 1°C за цикл в термоциклере qPCR.Tm для химерных и четырех гуманизированных антител указаны на фигуре 16 и подтверждают результаты, полученные в тесте на термостабильность: все антитела-кандидаты имеют очень похожие Tm (69-70°C) и сходные с данными химерного антитела (70°C), но немного ниже, чем для антитела мыши (73°C).
Аффинность гуманизированных антител-кандидатов
Определение аффинности антител проводили путем анализа SPR, используя Biacore T200.IgG против человека (GE Healthcare, номер в каталоге BR-1008-39) или IgG против мыши (GE Healthcare, номер в каталоге BR-1008-38) ковалентно иммобилизовали на чип CM5 (номер в каталоге BR-1005-30) до точки насыщения и в соответствии с инструкциями изготовителя. Антитела мыши DC8E8, химерные DC8E8, AX004, AX005, AX016 и AX017 разбавляли в буфере HBS-EP [0,01 М HEPES pH 7,4, 0,15 М NaCl, 3 мМ EDTA, 0,005% об./об. поверхностно-активное вещество P20, GE Healthcare] и иммобилизовали с помощью аффинного связывания до уровня между 144 и 177 RU. Рекомбинантный мономерный тау 151-391/4R (в PBS, насыщенном аргоном) разбавляли в HBS-EP в концентрациях от 20 нМ до 0,312 нМ с двухкратными разведениями и затем вводили со скоростью потока 100 мкл/мин. Время ассоциации устанавливали равным 150 сек, а время диссоциации - 300 сек. Концентрации тау-белка были выбраны эмпирически для того, чтобы получить кривизну во время фазы ассоциации. Первоначально кинетику связывания/диссоциации анализировали в соответствии с моделью взаимодействия 1:1, используя программный пакет для оценки BIAcore T200 2.0.
Сенсограммы показаны на фигурах 17-22. К сожалению, из-за двухфазной природы фазы диссоциации и некоторых доказательств дополнительного связывания на фазе ассоциации кинетику не удалось проанализировать. Показанные данные были получены с использованием анализа устойчивого состояния. Как мышиный, так и химерный DC8E8 показывают сродство приблизительно 10 нМ. Основные гуманизированные антитела-кандидаты демонстрируют сходную аффинность, изменяющуюся от 9 мМ (RHD/RKB) до приблизительно 16 нМ (RHE/RKA), суммированную на фигуре 23.На основании этих результатов можно предположить, что при гуманизации связывающая активность успешно сохранялась в пределах желаемых параметров.
Агрегация гуманизированных антител-кандидатов
Агрегация считается серьезной проблемой при разработке лекарственных средств, поскольку агрегация может снижать выход во время получения, ограничивать срок хранения и приводить к снижению эффективности у пациентов из-за повышенной иммуногенности. Образцы антител вводили путем инъекции со скоростью 0,4 мл/мин в эксклюзионную колонку в системе ВЭЖХ и анализировали путем многоуглового светорассеяния для определения абсолютных молярных масс и проверки агрегации (см. фигуры 24A, B, C и D).Все варианты показывают отсутствие признаков агрегации при средней молекулярной массе от 160 до 169,8 кДа, что является ожидаемым диапазоном для мономера IgG при этих установка анализа. Все образцы монодиспергированы (Mw/Mn <1,05).Массовое выделение составляет от 99,6 до 99,9% (расчетная масса по сравнению с введенной массой), что свидетельствует о хорошем извлечении белка и о том, что образцы, по видимому, не прилипают к колонке или содержат нерастворимые агрегаты, которые будут удерживаться защитной колонной. В целом данные свидетельствуют о том, что в любом анализируемом образце антител против DC8E8 нет никаких проблем с агрегацией.
Растворимость гуманизированных антител-кандидатов
Очищенные антитела-кандидаты концентрировали с использованием концентраторов поглощения растворителя (MWCO 7500 кДа) и измеряли концентрацию через определенные промежутки времени. Все образцы сконцентрировали между 35 и 41 мг/мл без видимого осаждения и тестировали в анализе связывания ELISA, который показал, что ни один из них не утратил активность связывания с тау-пептидом (фигура 25 и 26).Полученные данные свидетельствуют о том, что антитела не имеют тенденцию к осаждению при концентрациях вплоть до по меньшей мере 35 мг/мл.
Анализ стресса при заморозке/оттаивании антител-кандидатов
Образцы очищенных антител-кандидатов подвергали 10 циклам в течение 15 минут при -80°C с последующим оттаиванием в течение 15 минут при комнатной температуре. Затем образцы анализировали с помощью SEC-MALS для анализа агрегации (фигура 27).Данные свидетельствуют о том, что замораживание/оттаивание не вызывает агрегацию для всех четырех тестированных антител. В целом, данные свидетельствуют о том, что в любом анализируемом образце антител против DC8E8 нет никаких проблем с агрегацией.
Термический стресс-анализ антител-кандидатов
Образцы очищенных антител-кандидатов подвергали тепловой обработке при a) комнатной температуре, b) 37°C и c) при 50°C в течение 20 дней. Затем образцы анализировали с помощью SEC-MALS для анализа агрегации (фигура 28). В целом, данные свидетельствуют о том, что в любом анализируемом образце антител против DC8E8 нет никаких проблем с агрегацией.
Пример 4: Получение рекомбинантной изоформы полноразмерного тау-белка 2N4R и патологического беспорядочного тау 151-391/4R
Рекомбинантные белки тау получали из клона τ40 (Goedert, 1989), который субклонировали в плазмиду экспрессии pET-17b (Novagen) и экспрессировали в бактериях. Патологический беспорядочный тау 151-391/4R и все тау-пептиды нумеровали согласно самой длинной изоформе 2N4R тау-белка человека, которая составляет в длину 441 аминокислот и поэтому также называется тау441 (D'Souza, 2005).Получение тау-белков включает следующие стадии: а) экспрессию тау-белка бактериями; b) очистку тау-белка методом ионообменной хроматографии; с) очистку тау-белка гель-фильтрацией; d) концентрацию и хранение выделенного тау-белка;
а) Бактериальная экспрессия полноразмерного тау 2N4R человека и патологического беспорядочного тау 151-391/4R: плазмиды экспрессии трансформировали в производственный штамм Escherichia coli BL21 (DE3).Бактериальные клетки, содержащие соответствующую плазмиду экспрессии, культивировали и индуцировали, как описано в «Molecular Cloning: A Laboratory Manualʺ by Sambrook and Russell (2001). Одну колонию бактерии BL21 (DE3), трансформированную плазмидой pET-17b, осуществляющую экспрессию тау-белка или его фрагмента, выращивали при 37°С в 500 мл бульона Luria с 100 мкг/мл ампициллина при 300 об./мин и индуцировали, добавляя изопропил-β-D-1-тиогалактопиранозид (IPTG) до конечной концентрации 0,4 мМ. После дальнейшей инкубации при 37°С в течение 3 часов бактерии собирали центрифугированием при 3000 × g в течение 15 мин при 4°С.
b) Катионообменная хроматографическая очистка основных и нейтральных тау-белков (полноразмерные изоформы тау и тау151-391/4R) проводили по существу так же, как описано ранее (Krajciova et al.,2008). После экспрессии бактериальные осадки ресуспендировали в 10 мл лизирующего буфера (50 мМ 1,4-пиперазиндиэтансульфокислоты (PIPES) с pH 6,9, 50 мМ хлорида натрия (NaCl), 1 мМ этилендиаминтетрауксусной кислоты (EDTA), 5 мМ дитиотреитола (DTT ), 0,1 мМ фенилметилсульфонилфторида (PMSF), 5% (об./об.) глицерина), быстро замораживали в жидком азоте и хранили при -80°C перед использованием для очистки тау-белков. Для очистки тау-белка замороженные бактериальные суспензии быстро размораживали и помещали на лед. Стенки бактериальных клеток разрушали ультразвуком на льду, используя Sonopuls HD 2200, наконечник TT-13 (Bandelin, Германия), установленный на 50% рабочий цикл, выходная мощность 50 Вт, 6 раз в течение 30 с с паузами в 30 с. Лизаты осветляли центрифугированием (21000 × g в течение 15 мин при 4°C), и супернатанты фильтровали через 0,45 мкм мембранный фильтр. Крупномасштабную очистку рекомбинантных тау-белков проводили при 6°С, используя рабочую станцию ÄKTA-FPLC (Amersham Biosciences, Sweden).Отфильтрованные лизаты загружали со скоростью потока 3 мл/мин на колонку HiTr ap SP HP объемом 5 мл (GE Healthcare, Уппсала, Швеция), уравновешенную буфером для лизиса, и интенсивно промывали 60 мл лизирующего буфера до тех пор, пока исходный уровень при 280 нм не становится стабильным. Связанные тау-белки элюировали градиентом (0-30% в пределах 15 мл) буфера В (буфер для лизиса, дополненный 1 М NaCl).Отдельные фракции по 1 мл собирали и анализировали с помощью электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE).Для удаления нуклеиновых кислот, которые очищаются совместно с положительно заряженными тау-белками, фракции, содержащие тау-белок, объединяли и очищали второй стадией катионообменной хроматографии, используя колонку HiTrap SP HP объемом 5 мл (GE Healthcare, Упсала, Швеция), используя менее крутой градиент буфера В (0-30% в 45 мл).
с) На конечной стадии очистки гель-фильтрацией (то же самое для всех тау-белков) объединенные фракции тау-белка, полученные ионообменной хроматографией, вводили путем инъекции в колонку для гель-фильтрации (HiLoad 26/60 Superdex 200, Healthcare) со скоростью 3 мл/мин либо в PIPES, либо в буфере для лизиса гистидина для основных/нейтральных или кислых тау-белков, соответственно, с добавлением 100 мМ NaCl. Элюированные тау-белки собирали.
d) Для концентрации тау-белка после очистки гель-фильтрацией объединенные фракции разбавляли 1,5 объемами 2,5% глицерина и опять нагружали на колонку HiTrap SP HP (основные и нейтральные тау-белки) или на колонку HiTrap Q HP (кислые тау-белки).Концентрированный рекомбинантный тау-белок затем элюировали из колонки с помощью 1 М градиента NaCl. Наконец, буфер заменяли на фосфатно-буферный солевой раствор (PBS, 8,09 мМ динатрийфосфат (Na2HPO4), 1,47 мМ дигидрофосфат калия (KH2PO4), 136,89 мМ NaCl, 2,7 мМ хлорид калия (KCl)), насыщенным аргоном, используя колонка HiTrap Desalting с объемом 5 мл (GE Healthcare). Количественное определение белков очищенных образцов проводили с использованием наборов для количественного определения бицинхониновой кислоты (BCA) (Pierce, USA) с альбумином бычьей сыворотки в качестве стандарта. Тау-белки аликвотуют в рабочие аликвоты, быстро замораживают в жидком азоте и хранят при -70°С.
Пример 5: Свойства химерного DC8E8
а/ Химерный DC8E8 демонстрирует более высокую аффинность к патологическому беспорядочному тау 151-391/4R, чем к полноразмерному тау 2N4R.
Избирательную способность химерного DC8E8 в отношении иммунореактивности патологического тау-белка и физиологического тау-белка определяли ELISA и поверхностным плазмонным резонансом (SPR).
Для экспериментов с ELISA и SPR DC8E8 мыши очищали от супернатанта гибридомы, не содержащего сыворотку, на аффинной колонке с белком G следующим образом. Супернатант гибридомы доводили до рН 7,5 путем добавления 0,2 объема PBS и проверяли с помощью бумажной полоски для определения pH (при необходимости рН доводили, добавляя 4 М NaOH), раствор подвергали предварительному центрифугированию (20000 × g, 4°С, 10 мин), фильтровали через мембранный фильтр 0,45 мкм и загружали на колонку протеин G-сефароза объемом 5 мл (со скоростью потока 1-0,5 мл/мин).DC8E8 элюировали из колонки 0,1 М глицин-HCl, pH 2,7.Элюированные фракции немедленно нейтрализовали 1 М Трис-HCl с рН 9,0.Объединенные фракции диализовали против PBS, концентрировали ультрафильтрацией и хранили при -70°C.Концентрацию антитела определяли, измеряя оптическую плотность при 280 нм, используя формулу c(мг/мл)=A280 нм/1,43.
Химерное DC8E8 экспрессировали в клетках Expi293 и очищали от не содержащей сыворотки кондиционированной среды с помощью аффинной хроматографии и эксклюзионной хроматографии, как описано выше для DC8E8 мыши с некоторыми модификациями. Среду для культивирования клеток доводили до рН 7,5, подвергали предварительному центрифугированию, фильтровали через мембранный фильтр 0,45 мкм и загружали на колонку HiTrap MabSelect SuRe Protein A, используя PBS по Дульбекко в качестве связывающего и промывочного буфера. Химерное mAb DC8E8 элюировали из колонки 0,1 М цитратом натрия pH 2,5, дополненным 150 мМ NaCl. Элюированные фракции немедленно нейтрализовали 1 М Трис-HCl с рН 9,0.Объединенные фракции обрабатывали эксклюзионной хроматографией на колонке HiLoad 16/600 Superdex 200 пг, PBS по Дульбекко в качестве рабочего буфера. Концентрацию антитела определяли, измеряя оптическую плотность при 280 нм, используя формулу c(мг/мл)=A280 нм/1,37.
Для прямого анализа ELISA патологический беспорядоченный тау151-391/4R или полноразмерный тау-белок 2N4R иммобилизовали на планшеты ELISA (Nunc, MediSorp) при 5 мкг/мл в PBS, 50 мкл/лунку и инкубировали в течение ночи при 37°C.После блокирования PBS-0,05% Tween 20 (1 час при 20-25°C) для уменьшения неспецифического связывания планшеты инкубировали с 50 мкл/лунку трехкратных серийных разведений антитела (диапазон концентраций 10000 нг/мл - 0,17 нг/мл) в блокирующем буфере (PBS, 0,05% Tween 20) в течение 1 часа при 37°C.После инкубации и промывки вторичное антитело, конъюгированное с пероксидазой (антитело против Ig человека, Pierce, ThermoScientific) разбавляли 1:4000 в буфере PBS-Tween и наносили на лунки (50 мкг/лунка) в течение 1 часа при 37°C.После промывки реакционную смесь в течение 20 мин обрабатывали раствором Colorburst Blue (50 мкг/лунку) в качестве пероксидазного субстрата и останавливали 50 мкл 2 М H2SO4.Абсорбцию измеряли при 450 нм, используя ридер Multiscan MCC/340 ELISA (Labsystems). Данные со значением оптической плотности, по крайней мере вдвое превышающим значение отрицательных контролей (PBS), считали положительными.
Анализ показал, что химерное антитело DC8E8 способно различать патологический беспорядочный тау 151-391/4R и физиологический тау 2N4R (фигура 29А).Химерное DC8E8 распознавало физиологический тау 2N4R в значительно меньшей степени, чем патологический/патологический беспорядочный тау 151-391/4R.Важно отметить, что иммунореактивность химерного DC8E8 была сравнима с иммунореактивностью мышиного DC8E8 (фигура 29B).Как химерное, так и мышиное DC8E8 показали связывание тау-белков (патологический и физиологический тау-белок) с подобными значениями EC50, как показано на фигуре 29C.Вместе эти данные свидетельствуют о том, что связывающие свойства химерного DC8E8 сравнимы со связывающими свойствами исходного DC8E8 мыши.
Поверхностный плазмонный резонанс (SPR) используется для обнаружения и количественного определения связывания белка и для определения термодинамических параметров белковых комплексов (например, комплексов антитело-антиген) путем прямого мониторинга события связывания в реальном времени. Эта технология обычно используется для характеристики как диагностических, так и терапевтических антител (см., например, Karlsson and Larsson, Affinity Measurement Using Surface Plasmon Resonance, in Methods in Molecular Biology, Vol.248: Antibody Engineering:Methods and Protocols. Под редакцией: B.К.C.Lo © Humana Press Inc., Totowa, NJ, (2008)).
Аппарат BIACORE3000 с сенсорным чипом CM5 (Biacore AB, Уппсала) использовали для анализов SPR. Амино-связывающие реагенты (EDC, NHS, этаноламин с pH 8,5), детергент P20 и 10 мМ ацетат натрия с pH 5,0 получали от Biacore AB. Эти эксперименты проводили при 25°С в PBS pH 7,4 с 0,005% P20 (PBS-P) в качестве рабочего буфера. Для химерного DC8E8 поликлональное козье антитело против Fc человека (SIGMA, номер в каталоге I2136) соединяли при рН 5,0 через первичные амины одновременно в двух измерительных ячейках до 5000 RU (единиц реакции), одну из которых использовали для эталонного измерения. Для DC8E8 мыши аналитическую измерительную ячейку покрывали поликлональным антимышиным антителом (No.Z 0420; DakoCytomation, Glostrup, Denmark).
В каждом аналитическом цикле очищенное химерное DC8E8 и DC8E8 мыши отдельно захватывались в аналитической измерительной ячейке для достижения уровня иммобилизации 200-250 RU. Для определения равновесной константы ассоциации связывания (KA), а также для определения констант кинетической скорости (kON и kOFF) вводили инъекцией двукратные серийные разведения либо тау151-391/4R, либо физиологического тау 2N4R (против которого тестировали аффинность DC8E8) или PBS-P в качестве контроля со скоростью потока 100 мкл/мин над сенсорным чипом. Данные по кинетическому связыванию дублировали, как описано Myszka (1999) и подгоняли с помощью программного обеспечения для оценки BIA 4.1 (Biacore AB), независимо, для получения константы скорости диссоциации и константы скорости ассоциации. Равновесную константу ассоциации KA получали как отношение константы скорости ассоциации и диссоциации.
Для количественного определения аффинности химерного DC8E8 в отношении тестируемых тау-белков определяли равновесные константы ассоциации связывания (KA) для связывания DC8E8 с физиологической изоформой тау-белка 2N4R в четырех повторах, а также с патологическим беспорядочным тау 151-391/4R.Оба тау-белка, используемые для SPR, получали, как описано в примере 4.Химерное антитело DC8E8 различает патологический беспорядочный тау-белок 151-391/4R и физиологический тау-белок 2N4R (фигура 30).Степень отличительной активности химерного DC8E8 даже немного выше, чем у исходного антитела DC8E8 мыши. Эти результаты подтвердили:(1) специфичность гуманизированного DC8E8 для патологической беспорядочной формы тау-белка и (2) селективность DC8E8 для патологического беспорядочного тау (т.е. патологического тау или тау при заболевании) по сравнению с полноразмерным тау-белком (т.е. нормальный или физиологический тау-белок).
b/ Химерное DC8E8 связывает тау-пептиды, каждый из которых несет один из четырех эпитопов DC8E8 в повторяющихся областях домена, связывающего микротрубочки тау-белка
Предыдущие результаты показали, что DC8E8 мыши имеет четыре сайта связывания или эпитопы (267-273, 298-304, 329-335 и 361-367) на тау-белка человека, каждый из которых независимо расположен в одном из повторяющихся областях домена, связывающего микротрубочки тау-белка (WO/2013/041962, Kontsekova et al.,2014).С целью проверки способности химерного DC8E8 связываться с любым из четырех эпитопов, тау-пептиды 256-285, 282-311, 314-342, 352-380 были синтезированы EZBiolabs (США) с чистотой выше 95%.Каждый из пептидов включает один из четырех независимых эпитопов DC8E8.Связывающую активность химерного DC8E8 в отношении тау-пептидов измеряли прямым ELISA, как описано в примере 5 а/.Химерное DC8E8 связывало все тестируемые пептиды, полученные из MTBR (фигура 31A), аналогично первоначальному DC8E8 мыши (фигура 31B).Важно отметить, что наивысшую иммунореактивность была показана химерным и мышиным DC8E8 в отношении пептида 282-311, который был получен из MTBRII и который содержит эпитоп DC8E8 в положении 298-304.Иммунореактивность химерного антитела к дополнительно тестированным пептидам (256-285, 314-342, 352-380) была даже выше, чем исходного DC8E8 мыши, на что указывают значения ЕС50 (фигура 31С).
с/ Химерное DC8E8 ингибирует патологическое взаимодействие тау-тау
Анализ in vitro фибрилляции тау-белка использовали для определения, оказывает ли химерное антитело ингибирующее действие на патологические взаимодействия тау-тау. Анализ основан на внутреннем свойстве тау-белков, а именно на их способности подвергаться конформационным изменениям при взаимодействии с полианионами, такими как сульфатированный гликозаминогликановый гепарин. Эта измененная конформация на одной молекуле тау затем приводит к патологическим взаимодействиям с другой молекулой тау, стабилизации комплекса тау-тау путем образования поперечных β-структур в областях связывания микротрубочек взаимодействующих тау-молекул и, наконец, образования спаренных спиральных нитей (PHF), подобных нитям, образующихся при болезни Альцгеймера (Skrabana, R.,Sevcik, l.,Novak, M.(2006). Intrinsically disordered proteins in the neurodegenerative processes:formation of tau protein paired helical filaments and their analysis.Cell Mol Neurobiol 26, 1085-1097).Формирование структур, богатых бета-конформацией, может быть обнаружено с помощью флуоресцентных красителей, каких как тиофлавин Т (Friedhoff P, Schneider A, Mandelkow EM, Mandelkow E.Rapid assembly of Alzheimer-like paired helical filaments from microtubule-associated protein tau monitored by fluorescence in solution.Biochemistry 37(28):10223-30 (1998)).
Для анализа фибриллизации тау-белка in vitro мышиное и химерное DC8E8 очищали способами, описанными в примере 5.Анализ для определения эффекта химерного DC8E8 на патологические взаимодействия тау-тау проводили в PBS (профильтрованный через фильтр 0,2 мкм), содержащий:10 мкМ (конечная концентрация) патологического беспорядочного тау 151-391/4R; 10 мкМ гепарина (натриевая соль гепарина из слизистой оболочки кишечника свиньи, ≥ 150 МЕ/мг, сухая основа, средняя молекулярная масса 6000 Да, от SIGMA); и 12,5 мкМ (конечная концентрация) тиофлавина Т. Каждую реакционную смесь (50 мкл конечного объема) инкубировали в течение 20 ч при 37°С в закрытых черных твердых полистироловых пластинах (384 лунки, Greiner BioOne).Флуоресценцию тиофлавина T измеряли с использованием флуоресцентного ридера (Fluoroskan Ascent FL (Labsystems)) с длиной волны возбуждения 450 нм, эмиссией при 510 нм и временем измерения 200 мс. Для определения ингибирующей активности химерного DC8E8 в отношении патологических взаимодействий тау-тау, к реакционной смеси добавляли очищенное химерное DC8E8 до конечной концентрации 10 мкМ для инкубации при 37°С.Количество конформационно измененного и фибриллизованного тау измеряли флуоресценцией тиофлавина Т в отсутствие («отсутствие антитела») и в присутствии химерного антитела (фиг. 32).И химерное DC8E8, и мышиное DC8E8, добавленные при конечной концентрации 10 мкМ, предотвращали патологическое конформационное изменение и фибриллизацию патологического беспорядочного тау-белка. Химерное DC8E8 уменьшало количество фибриллизованных патологических форм тау-белка до менее чем 5,9%, мышиное DC8E8 уменьшало количество фибриллизованных патологических форм тау-белка до менее 4,7%.Данные показывают, что химерное антитело предотвращало патологическое конформационное изменение и фибриллизацию патологического беспорядочного тау-белка с характеристиками, сравнимыми с характеристиками исходного DC8E8.
Пример 6: Свойства гуманизированных вариантов DC8E8
а/ Гуманизированные варианты DC8E8 показывают более высокую аффинность к патологическому беспорядочному тау 151-391/4R, чем к полноразмерному тау 2N4R.
Чтобы оценить избирательную способность гуманизированных вариантов DC8E8 в отношении иммунореактивности патологического и физиологического тау-белков, использовали ELISA и SPR, как описано в примере 5.Все гуманизированные варианты DC8E8, а именно AX004, AX005, AX016, AX017 (оба изотипа IgG4 и IgG1) очищали согласно способу очистки химерного DC8E8, как описано в примере 5.
ELISA показал, что все гуманизированные варианты AX004, AX005, AX016 и AX017 (изотипы IgG4 и IgG1) были способны распознавать патологический тау151-391/4R (фигура 33A-D, фигура 34A-D).Важно отметить, что связывание каждого гуманизированного варианта DC8E8 было выше в отношении патологического тау151-391/4R, чем в отношении физиологического тау2N4R.Однако варианты, содержащие вариант RHE тяжелой цепи (AX005 и AX017), по-видимому, связывают физиологический тау-белок слабее, чем варианты AX004 и AX016, содержащие вариант RHD тяжелой цепи (фигура 33F; фигура 34E).Хотя AX005 и AX017 связывают физиологический тау-белок слабее, степень избирательной активности гуманизированных вариантов AX004, AX005, AX016 и AX017 аналогична активности химерного антитела DC8E8, на что указывают значения EC50. В целом свойства связывания тестируемых гуманизированных антител сравнимы со свойствами связывания химерного антитела (и исходного DC8E8 мыши, фигура 29).
Для экспериментов с SPR, выполненных, как описано выше для химерного DC8E8, были использованы гуманизированные варианты моноклонального антитела DC8E8 и химерного DC8E8. В каждом аналитическом цикле очищенный гуманизированный вариант DC8E8 фиксировали в аналитической измерительной ячейке для достижения уровня иммобилизации 200-250 RU. Для количественного определения аффинности гуманизированного DC8E8 для каждого тестированного тау-белка определяли равновесные константы ассоциации связывания (KA) для связывания антител с физиологической изоформой тау-белка 2N4R в четырех повторах, а также с патологическим беспорядочным тау 151-391/4R.Все тау-белки, использованные для SPR, получали в соответствии с примером 4.Аффинность каждого гуманизированного варианта DC8E8 была выше в отношении патологического беспорядочного тау151-391/4R, чем для полноразмерного тау2N4R.(фигура 35А, В).Эти результаты подтвердили:(1) специфичность гуманизированного DC8E8 для патологической беспорядочной формы тау-белка и (2) селективность DC8E8 для патологического беспорядочного тау (т.е. патологического тау или тау при заболевании) по сравнению с полноразмерным тау-белком (т.е. нормальный или физиологический тау-белок).
b/ гуманизированные варианты DC8E8 связывают тау-пептиды, каждый из которых несет один из четырех эпитопов DC8E8 в домене, связывающем микротрубочки тау-белка
Цель этого эксперимента состояла в том, чтобы определить способность гуманизированных вариантов DC8E8 (AX004, AX005, AX016, AX017, изотип IgG4 и изотип IgG1) связывать тау-пептиды 256-285, 282-311, 314-342, 352- 380.Каждый из этих пептидов охватывал один из четырех отдельных эпитопов DC8E8 в повторяющихся областях домена, связывающего микротрубочки (MTBR), тау-белка. Связывающую активность гуманизированных вариантов DC8E8 в отношении тау-пептидов измеряли прямым ELISA, как описано в примере 5.Каждое из тестируемых гуманизированных антител связывало все пептиды, полученные из MTBR (фигура 36A-D, фигура 37A-D), аналогично химерному DC8E8 (фигура 36E). Это справедливо как для вариантов с изотипом IgG1, так и с изотипом IgG4.Гуманизированные антитела-кандидаты показали наивысшую иммунореактивность в отношении пептида 282-311, который был получен из MTBRII и который содержит эпитоп DC8E8 в положениях 298-304, на что указывают значения EC50 (фигура 36F, фигура 37E).Варианты, содержащие вариант RHE тяжелой цепи (AX005 и AX017) связывают другие тестируемые пептиды (256-285б 314-342б 352-380) слабее, чем варианты AX004 и AX016, содержащие вариант RHD тяжелой цепи (фигура 36F; фигура 37E). В целом данные свидетельствуют о то, что иммунореактивность гуманизированного антитела AX004 и AX016 в отношении тестированных пептидов аналогично иммунореактивности химерного DC8E8, на что указывают значения EC50 (фигура 36F).
с/ гуманизированные варианты DC8E8 способны ингибировать патологическое взаимодействие тау-тау
Для того, чтобы определить влияние гуманизированных антител-кандидатов (а именно AX004, AX005, AX016, AX017, изотип IgG4 и изотип IgG1) на фибрилляцию тау-белка и на образование тау-агрегатов, был проведен анализ in vitro фибриллизации тау-белка (как описано в примере 5). Все гуманизированные варианты DC8E8 очищали, как описано в примере 5.Патологический тау-белок 151-391/4R, использованный для анализа на фибриллизацию, получали согласно примеру 4.
Для определения ингибирующей активности гуманизированных антител-кандидатов на патологические взаимодействия тау-тау очищенные гуманизированные варианты AX004, AX005, AX016, AX017 (изотип IgG4 и изотип IgG1) независимо добавляли к реакционной смеси при конечной концентрации 10 мкМ, а затем инкубировали при 37°C.Количество конформационно измененного и фибриллизованного тау-белка измеряли флуоресценцией тиофлавина Т в отсутствие («нет антитела») и в присутствии тестируемых антител. Результаты показали, что все гуманизированные антитела, добавленные при конечной концентрации 10 мкМ, предотвращали патологическое конформационное изменение и фибриллизацию патологического беспорядочного тау-белка (фигура 38А, В). Изотип антител не влиял на ингибирующий потенциал гуманизированных антител. Гуманизированные варианты AX004, AX005, AX016 и AX017, как изотипа IgG4, так и изотипа IgG1, уменьшали количество фибриллизованных патологических тау-форм до менее 3%. Данные свидетельствуют о том, что гуманизированные антитела предотвращали патологическое конформационное изменение и фибриллизацию патологического беспорядочного тау-белка с характеристиками, сравнимыми с характеристиками исходного DC8E8 мыши.
ПРИМЕР 7: химерный DC8E8 и гуманизированный вариант DC8E8 распознает патологию в мозге человека, страдающего болезнью Альцгеймера и другими таутопатиями
Образцы ткани мозга человека (на парафиновых блоках) получали из банка мозга Нидерландов. Блоки разрезали на микротоме. Для исследования использовали парафиновые срезы (8 мкм) коры гиппокампа-энторинальной коры мозга индивида с болезнью Альцгеймера (стадия VI по Браак) и FTDP17 (мутация R406W), хвостатого ядра индивида с кортикобазальной дегенерацией и прогрессирующим супрануклеарным параличом. Срезы обрабатывали холодной (+4°С) 98% муравьиной кислотой в течение 1 мин, а затем подвергали термической обработке в варочном автоклаве (2100 Retriever) в течение 20 мин при 121°С.Тканевые срезы инкубировали в блокирующем растворе (Section blok, Aptum) в течение 10 мин при комнатной температуре, а затем в течение ночи с использованием первичного антитела DC8E8 мыши (1:200), антител AX004, AX005, AX016, AX017 человека и химерного DC8E8 (все 1:1000).Затем срезы инкубировали с биотинилированным вторичным антителом (Vectastain Elite ABC Kit, Vector Laboratories) при комнатной температуре в течение часа, а затем проводили реакцию с комплексом авидин-биотин-пероксидаза в течение 60 минут (набор Vectastain Elite ABC, Vector Laboratories), оба при комнатной температуре (25°C).Иммунореакцию визуализировали набором с пероксидазным субстратом (Vector VIP, Vector laboratories, Ca, США) и контрастно окрашивали метил-зеленым (Vector Laboratories).Оценку иммунореактивности проводили световой микроскопией при увеличении ×100-400.Морфологические характеристики тау-иммуноположительных срезов определяли на основе клеточной локализации и картины окрашивания. Цифровые изображения были сделаны с использованием микроскопа Olympus BX51, оснащенного цифровой фотокамерой Olympus DP50 (Olympus Optical Co., Ltd., Токио, Япония).
Иммуногистохимическое окрашивание мозга человека при болезни Альцгеймера, прогрессирующем супрануклеарном параличе, кортикобазальной дегенерации и у пациентов FTDP-17 показало, что химерное антитело DC8E8 имеет такую же окраску, что и DC8E8 мыши (фигура 39-46, A, B). Авторы сравнили иммуногистохимическое окрашивание химерного антитела с гуманизированными антителами DC8E8 - AX004, AX005, AX016 и AX017. В целом, гуманизированные антитела AX004 и AX016 (IgG1 и IgG4) демонстрируют очень сходную картину окрашивания с мышиным или химерным DC8E8.Гуманизированные антитела AX004 и AX016 распознавали обширное количество нейрофибриллярных клубков, нейрофибриллярных нитей и сенильных бляшек в мозге человека при AD (фигура 39C, E; 40C, E). В случае FTDP-17 человека с мутацией тау-белка R406W, AX004 и AX016 иммунометили нейрофибриллярные клубки и нейропильные нити в энторинальной и височной коре (фигура 41 C, E; 42 C, E). При кортикобазальной дегенерации AX004 и AX016 окрашивали глиальную тау-патологию в хвостатом ядре (фигура 43 C, E; 44 C, E).При прогрессивном супрануклеарном параличе AX004 и AX016 распознавали большое количество олигодендроглиальных спиральных тел и астроцитические бляшки (фигура 45C, E; 46C, E). Напротив, AX005 и AX017 показали снижение иммунного окрашивания при болезни Альцгеймера (фигура 39D, F; 40D, F), FTDP-17 (фигура 41D, F), при кортикобазальной дегенерации (фигура 43D, F; 44D, F) и при прогрессирующем супрануклеарном параличе (Фигура 45D, F; 46D, F). Интересно, что изотип IgG4 AX005 и AX017 не окрашивал патологические структуры при FTDP17 (фигура 42D, F). Таким образом, гуманизированные антитела AX004 и AX016 имеют такую же окраску, что и DC8E8.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГУМАНИЗИРОВАННЫЕ АНТИ-ТАУ-АНТИТЕЛА | 2015 |
|
RU2743152C2 |
| АНТИТЕЛА ПРОТИВ TFR И ИХ ПРИМЕНЕНИЕ ПРИ ЛЕЧЕНИИ ПРОЛИФЕРАТИВНЫХ И ВОСПАЛИТЕЛЬНЫХ РАССТРОЙСТВ | 2016 |
|
RU2737637C2 |
| БЕЗОПАСНЫЕ И ФУНКЦИОНАЛЬНЫЕ ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА | 2011 |
|
RU2607368C2 |
| АНТИТЕЛА К ИНТЕГРИНУ АЛЬФА-2 И ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2545401C2 |
| ГУМАНИЗИРОВАННОЕ ТАУ-АНТИТЕЛО | 2013 |
|
RU2644242C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ИНФЕКЦИЙ, ВЫЗВАННЫХ Staphylococcus aureus | 2015 |
|
RU2636780C1 |
| АНТИТЕЛА ПРОТИВ CD40 И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2796413C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К CTLA4 | 2012 |
|
RU2629768C2 |
| АНТИТЕЛО ПРОТИВ ЛИГАНДА 1 ЗАПРОГРАММИРОВАННОЙ ГИБЕЛИ КЛЕТОК (PD-L1), ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2016 |
|
RU2727914C2 |
| АНТИТЕЛА ПРОТИВ БЕЛКА РЕЦЕПТОРА С-МЕТ | 2011 |
|
RU2608644C2 |
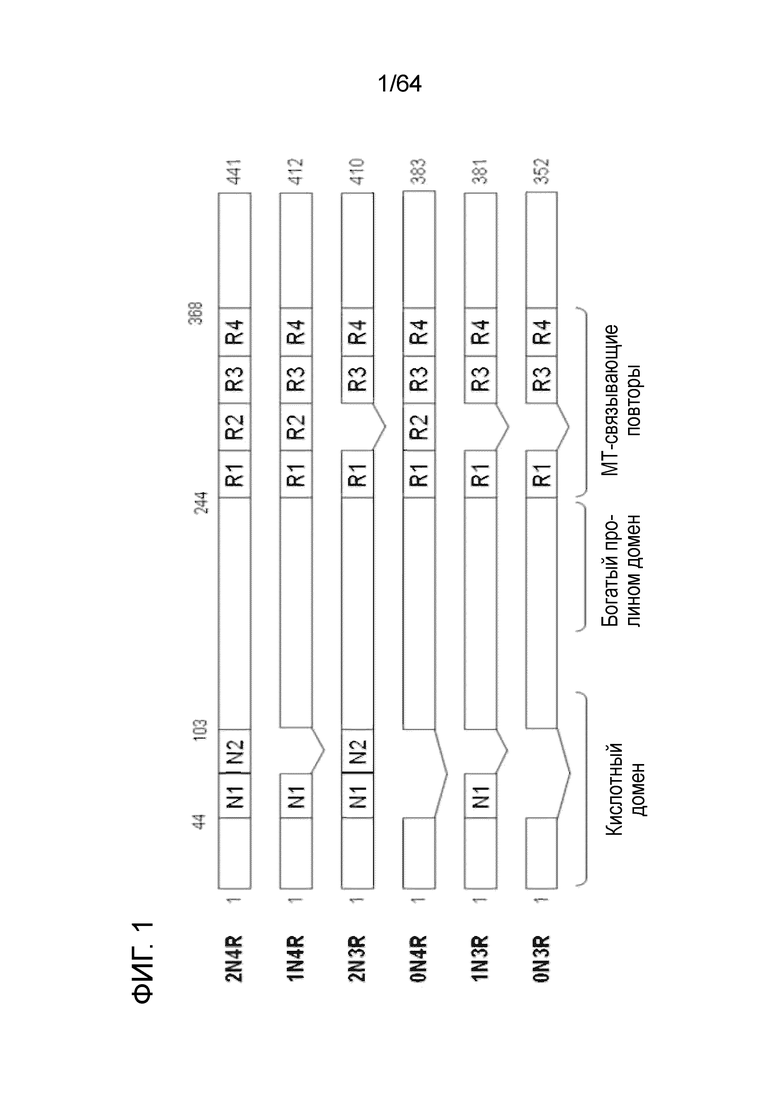
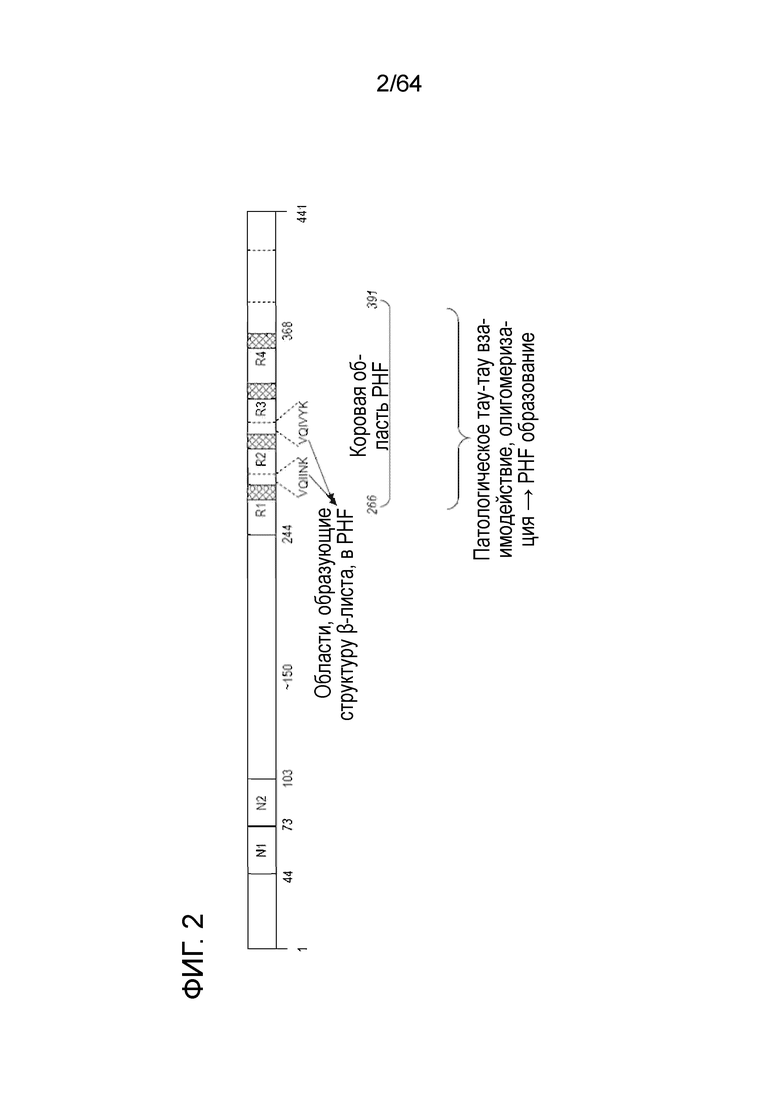




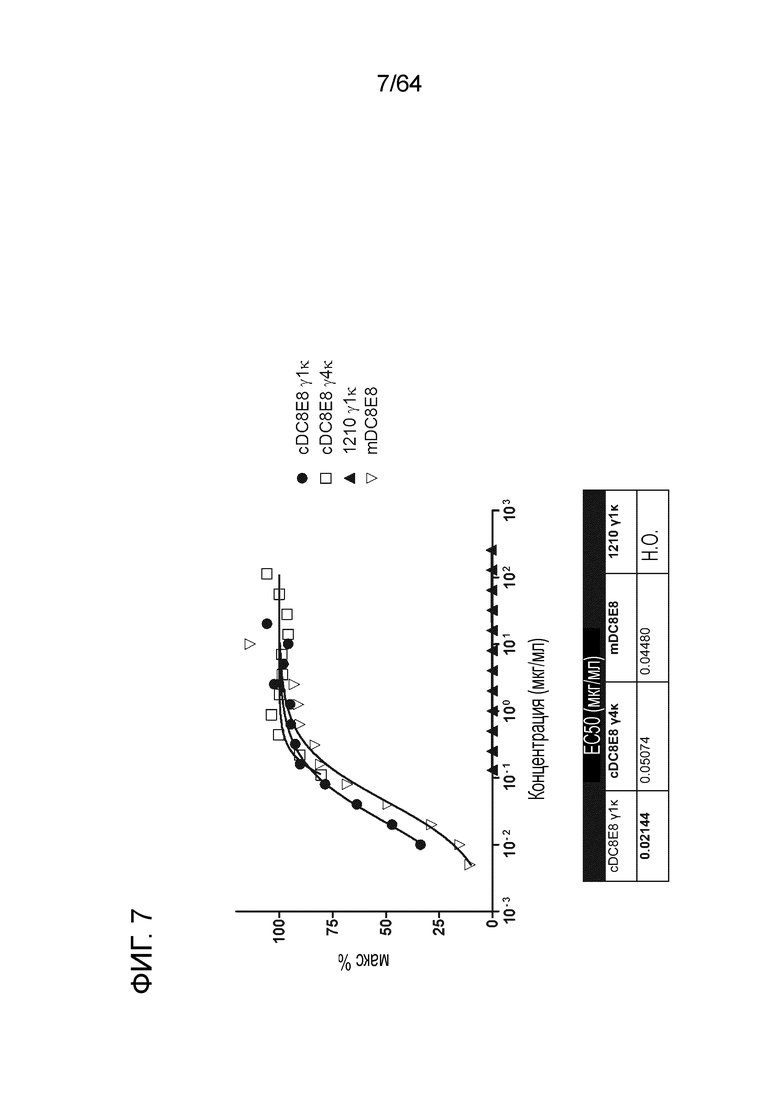

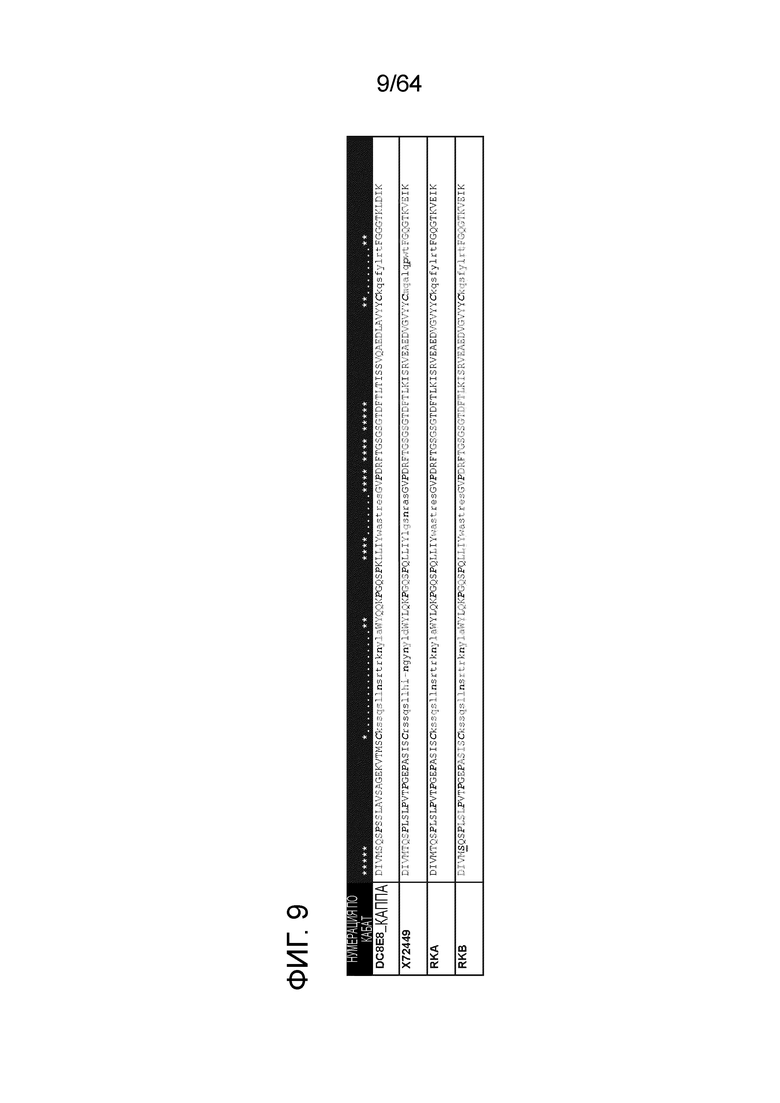
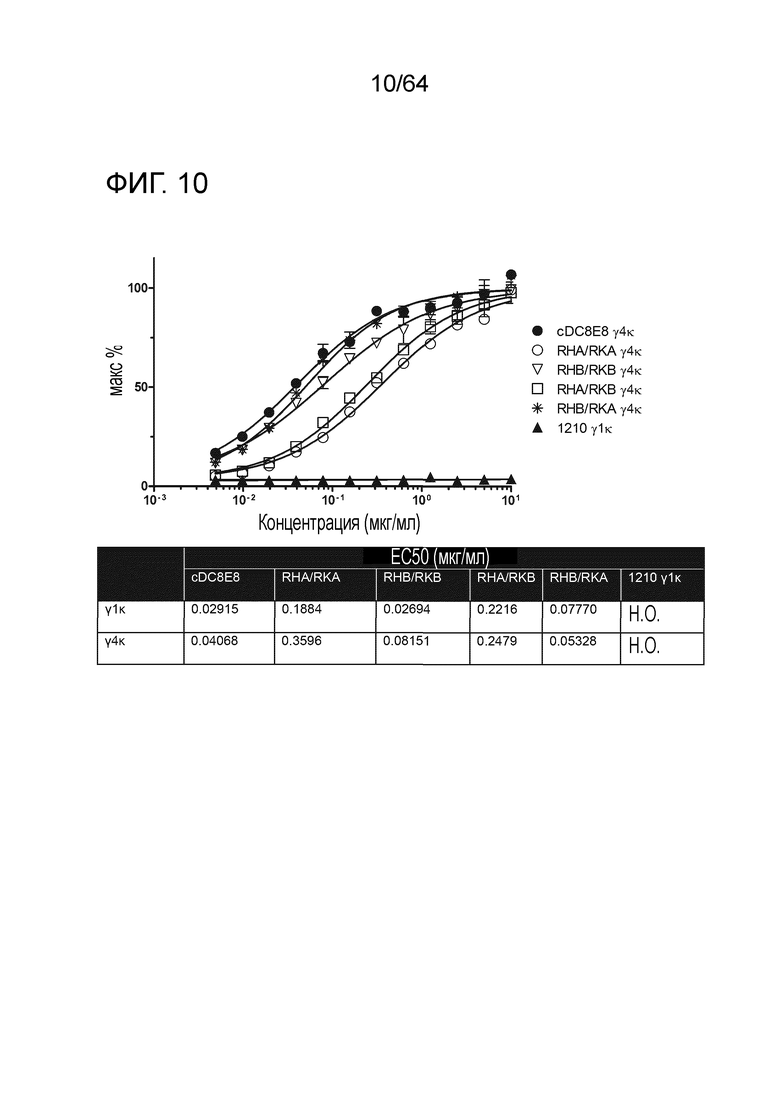
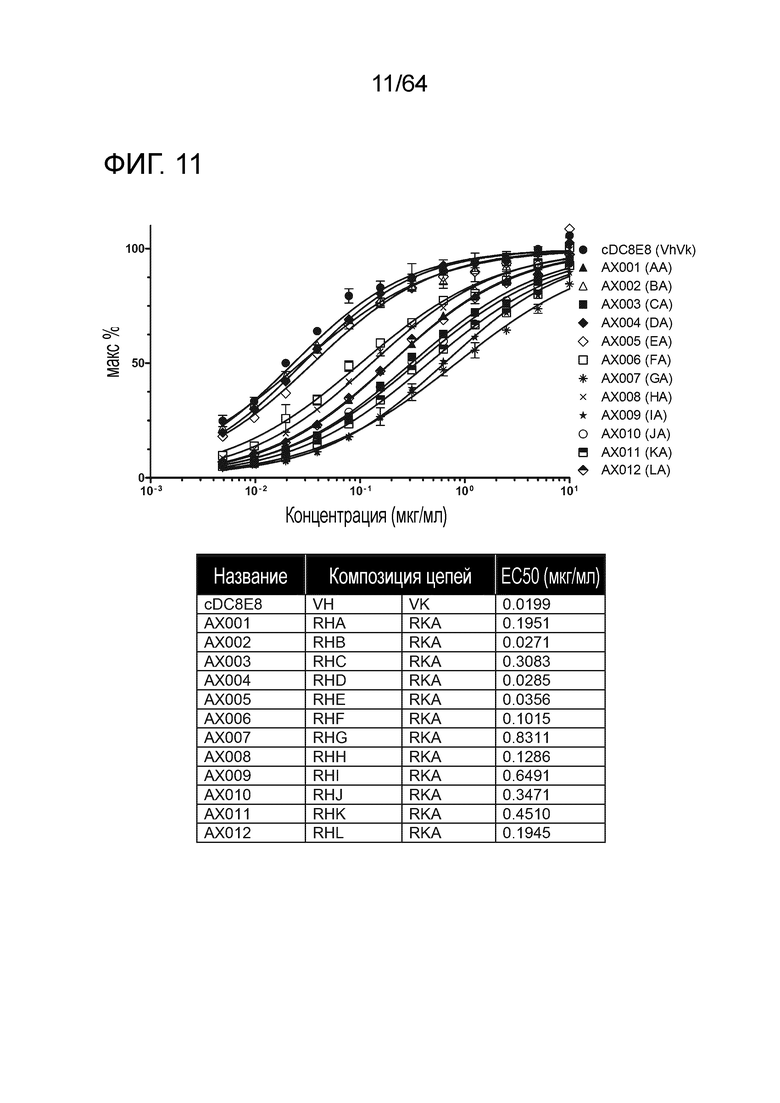
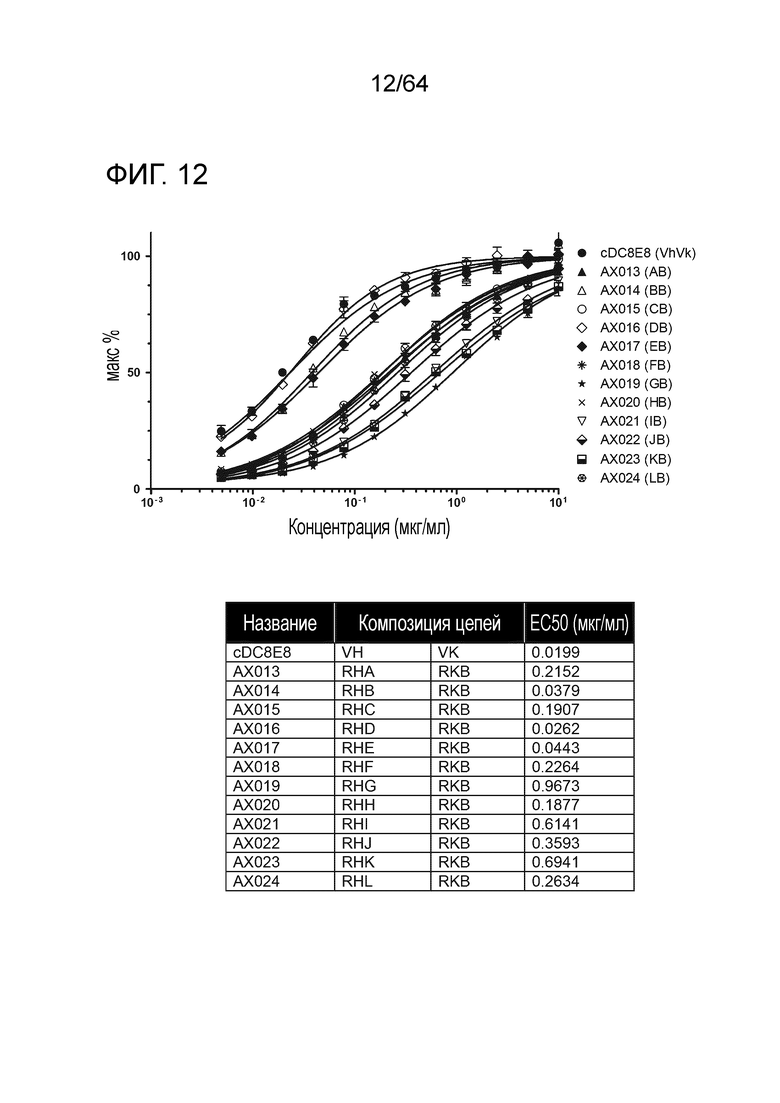



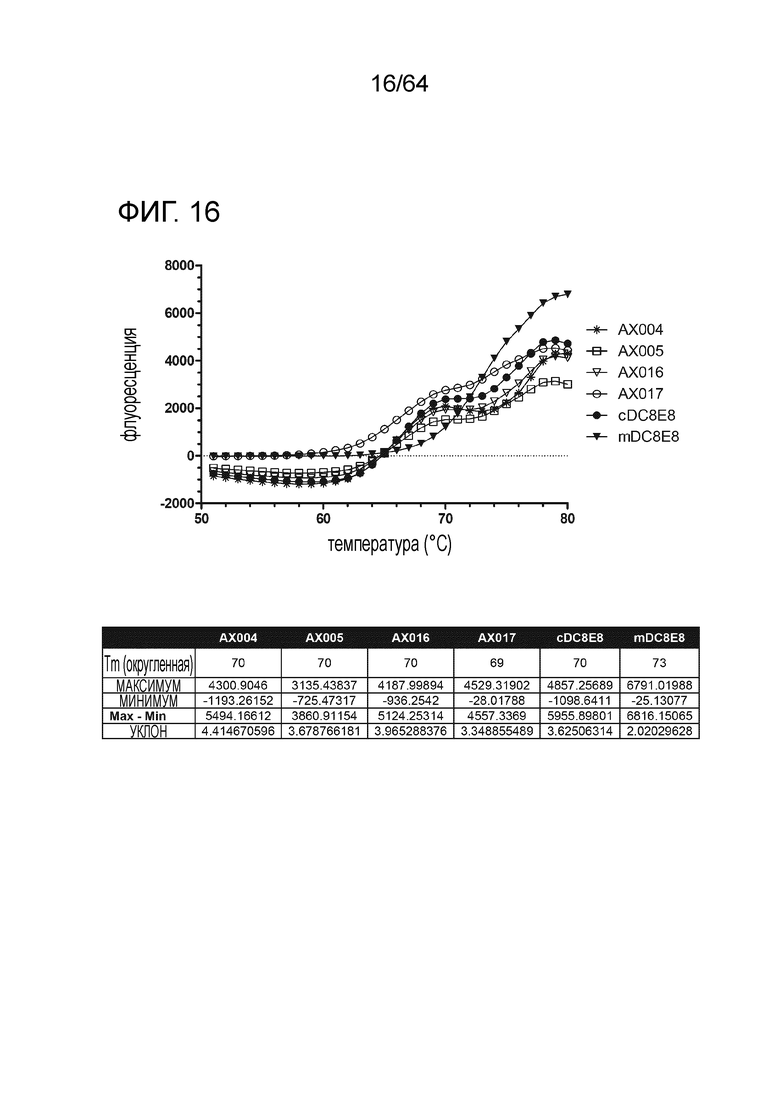
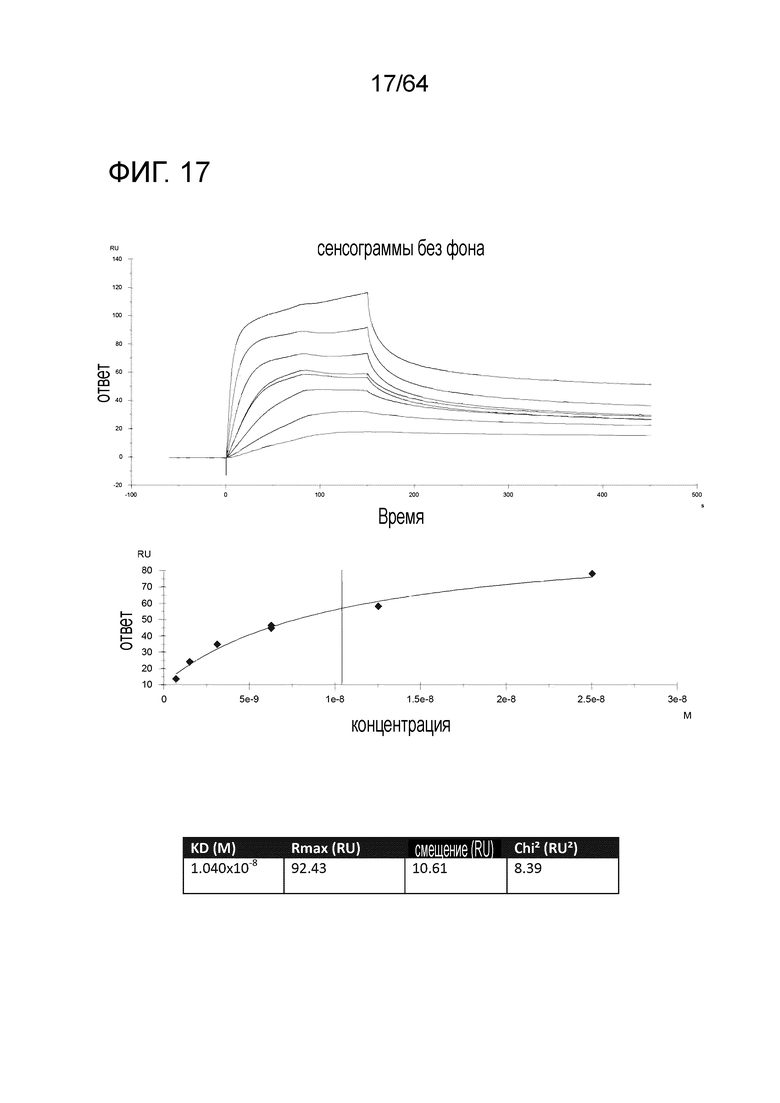

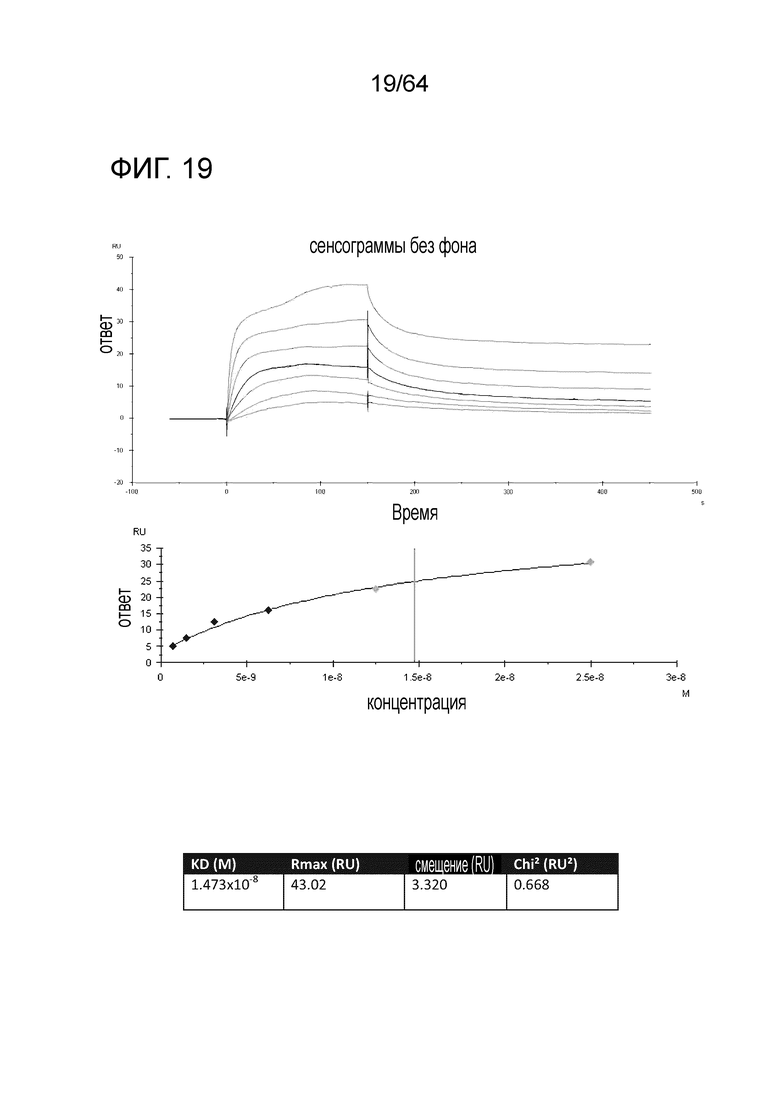

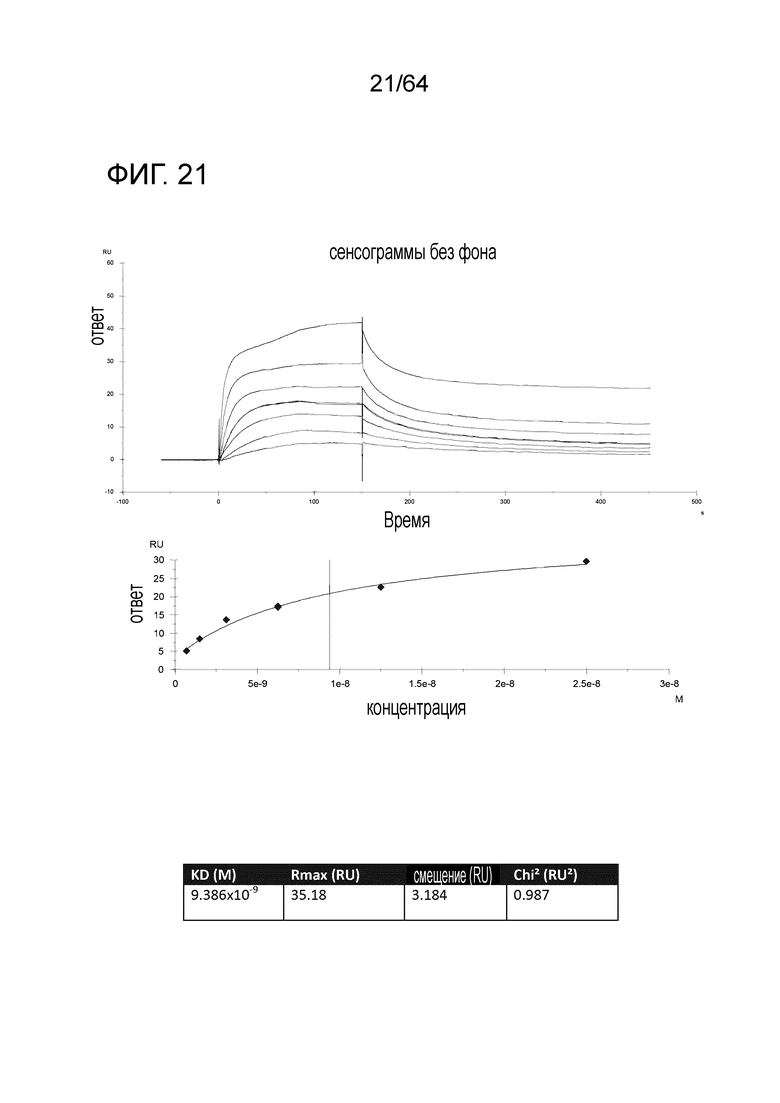

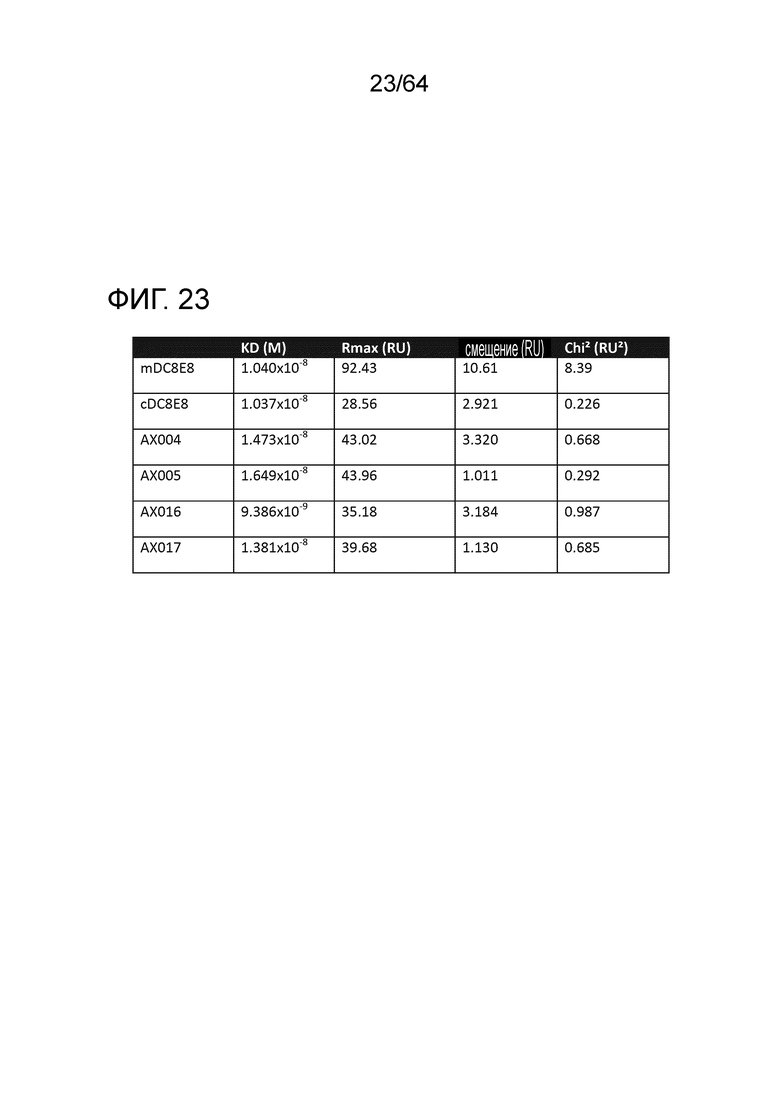

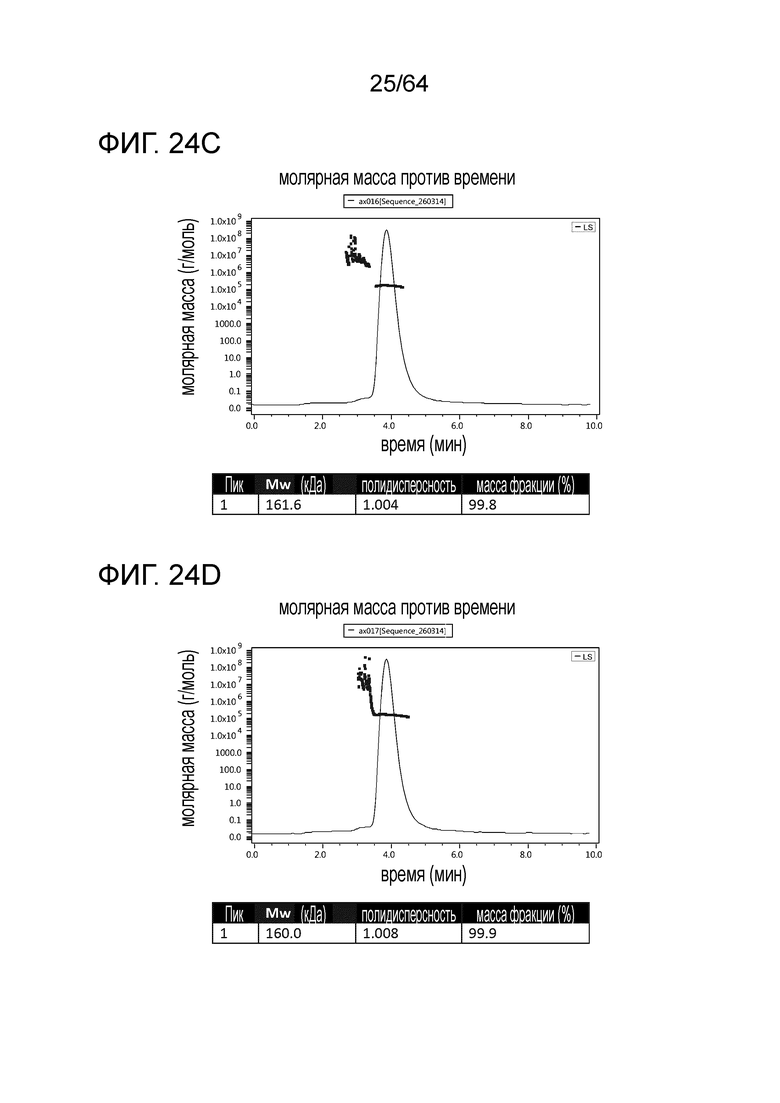
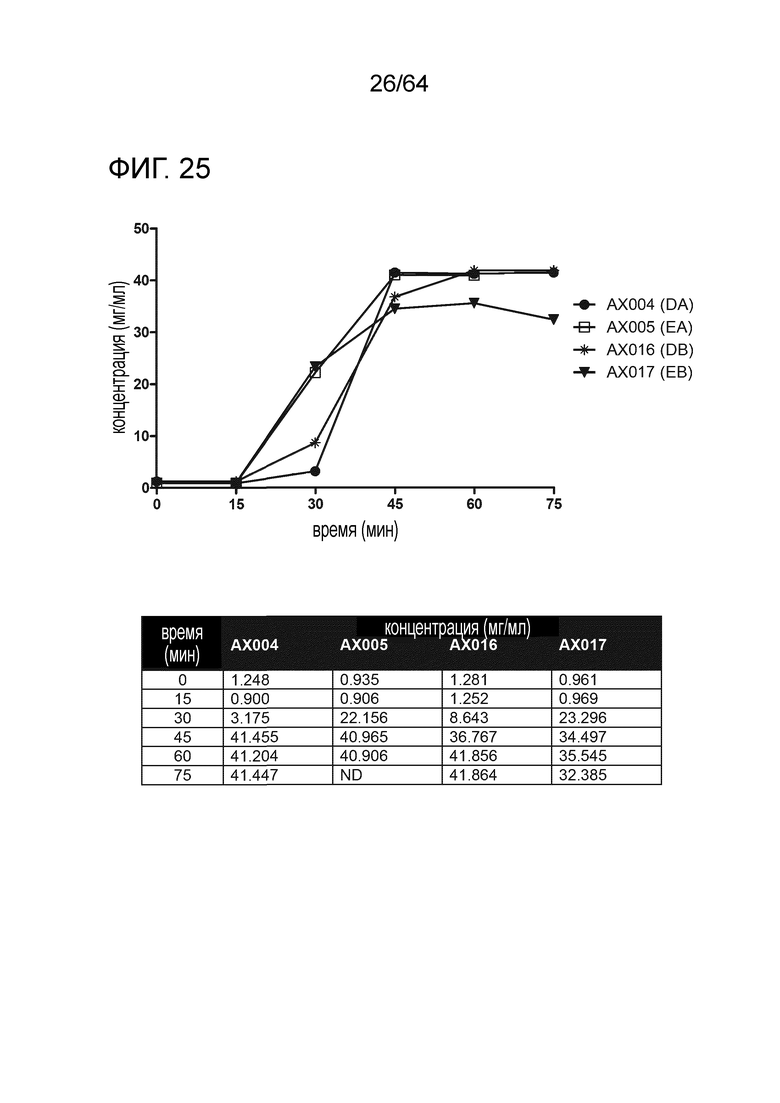
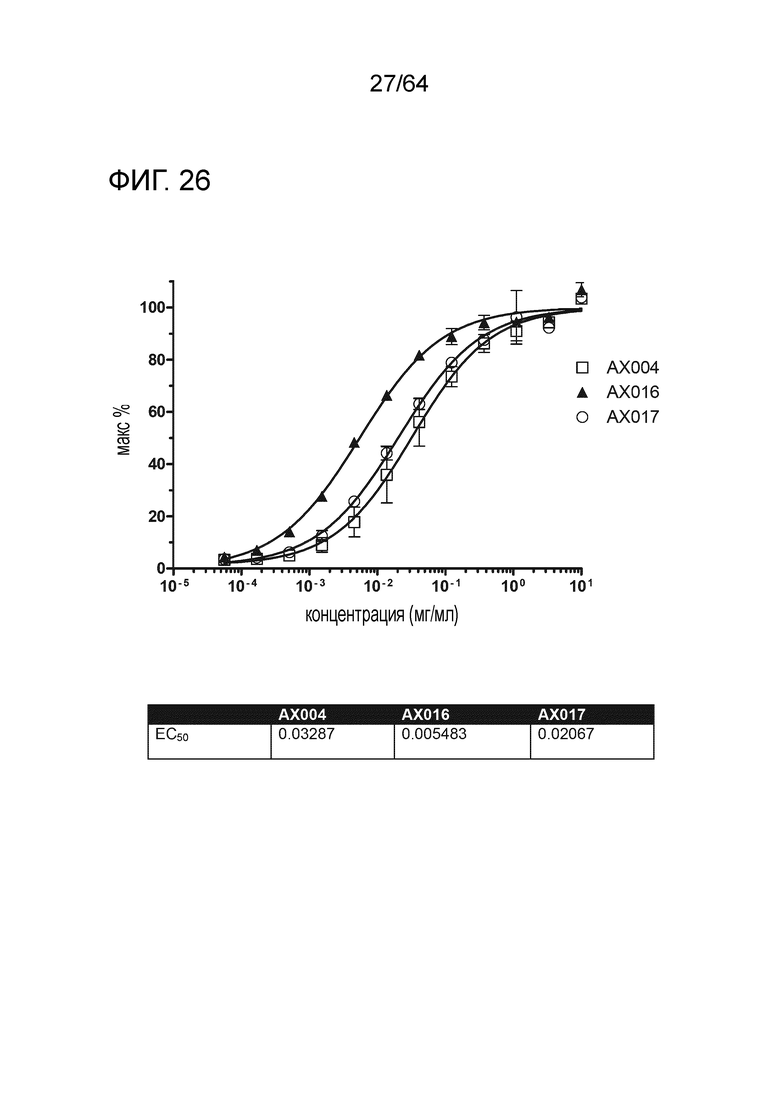


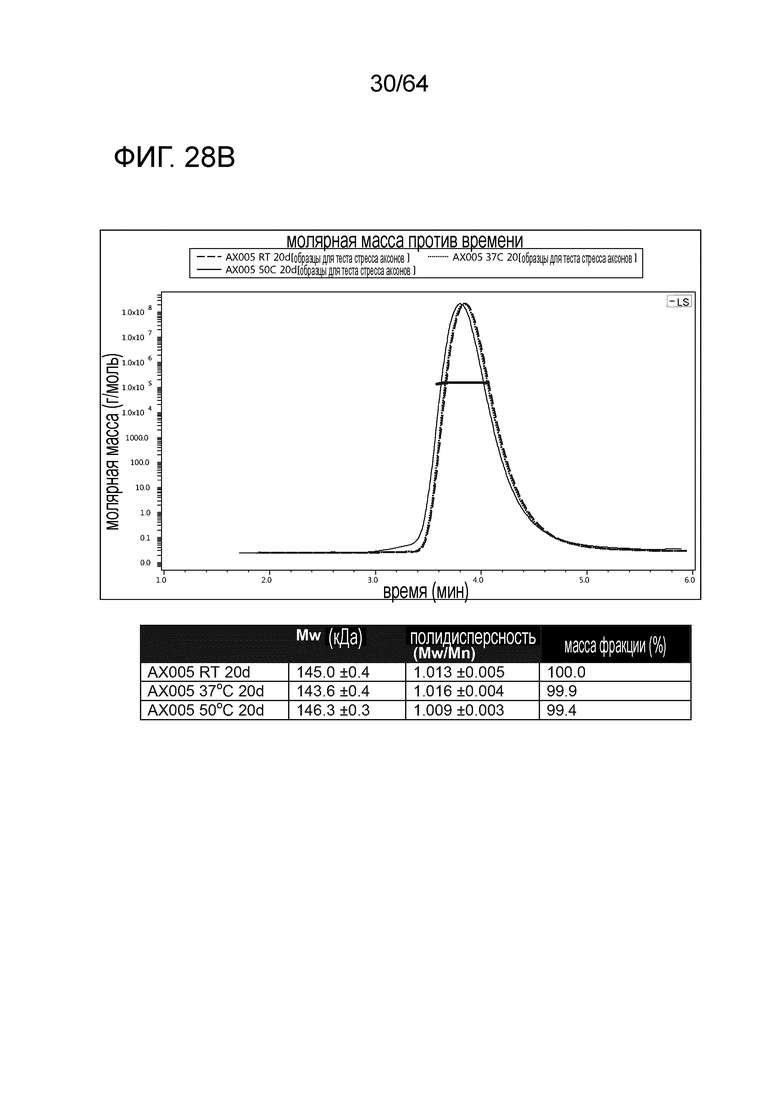
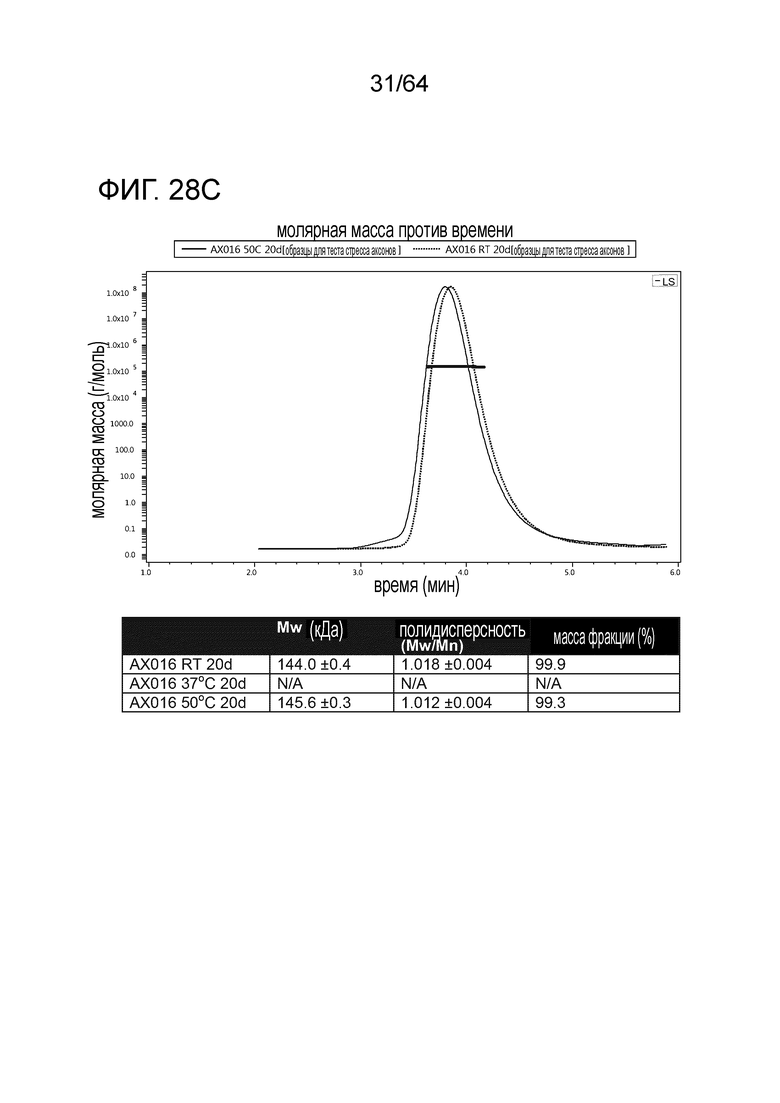
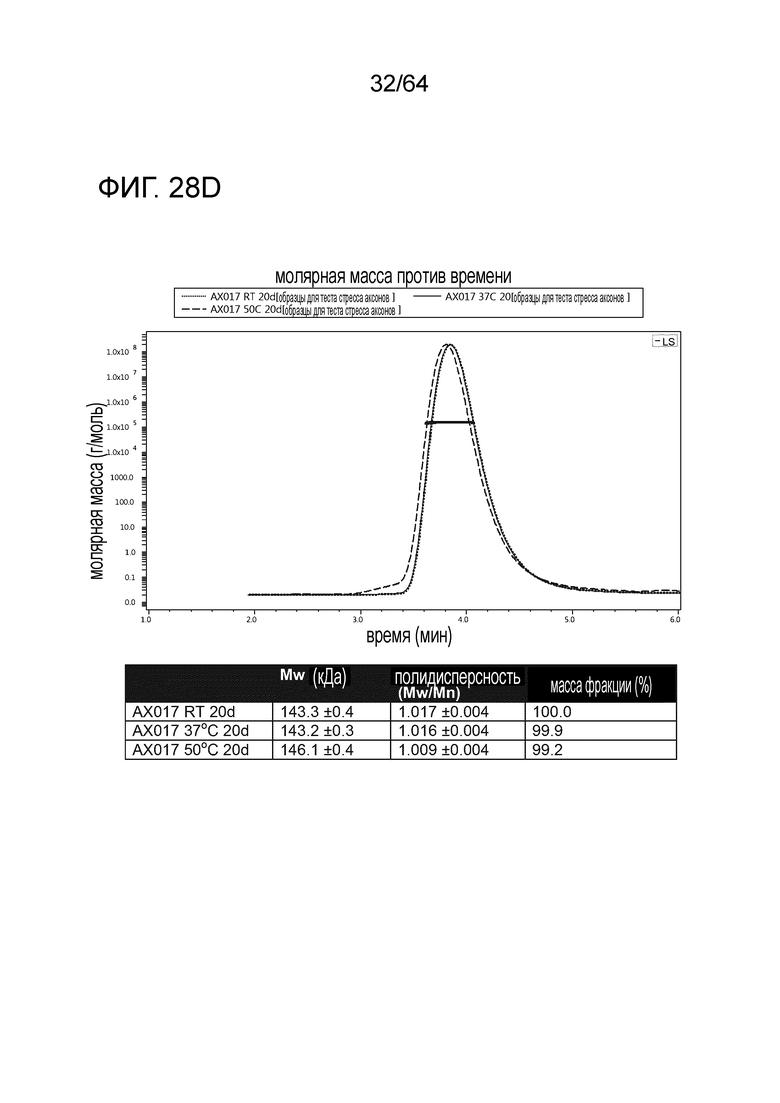



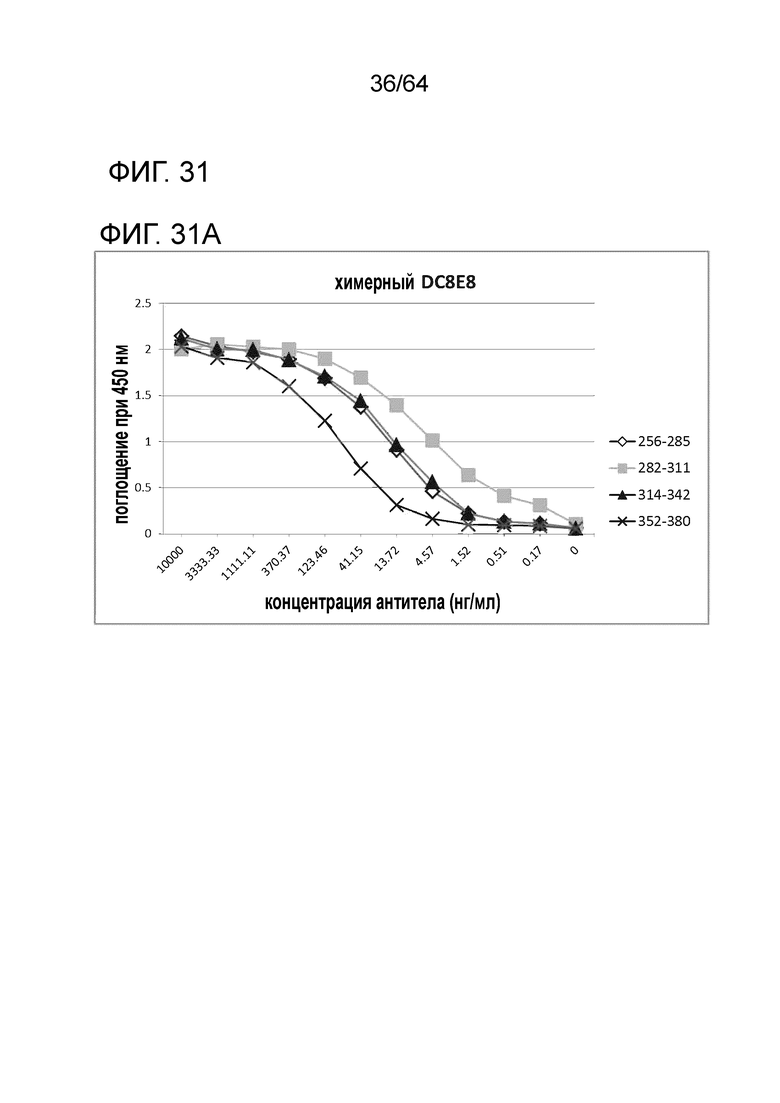
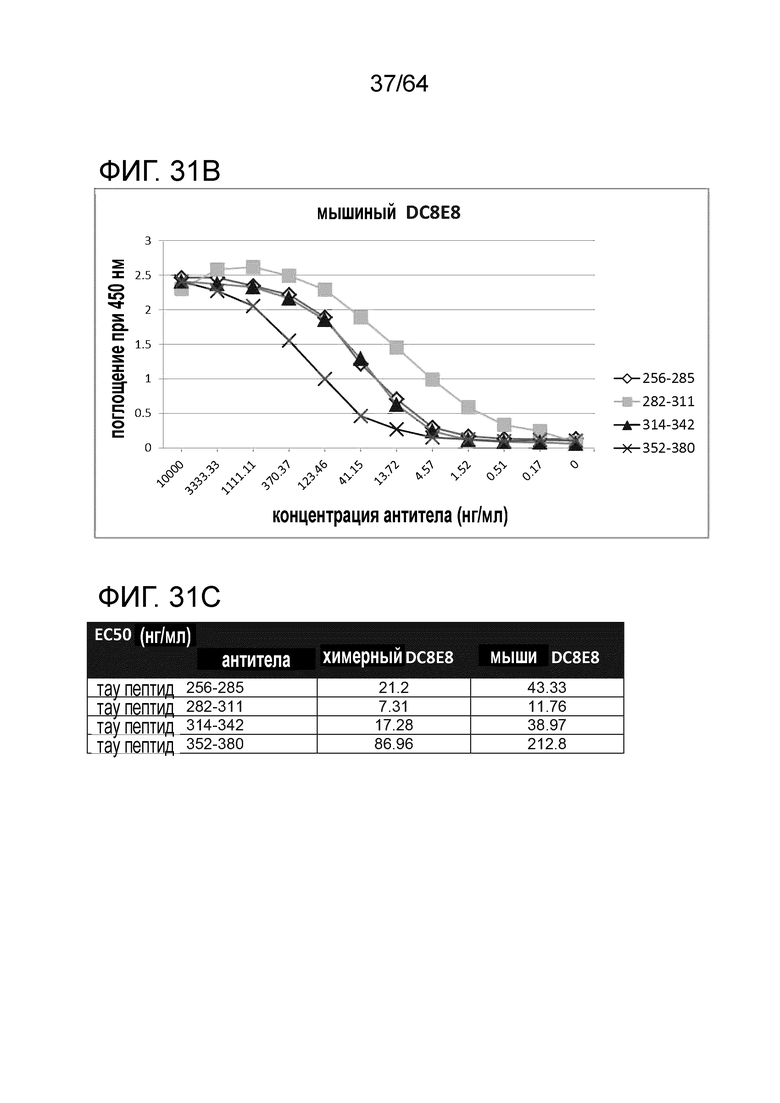
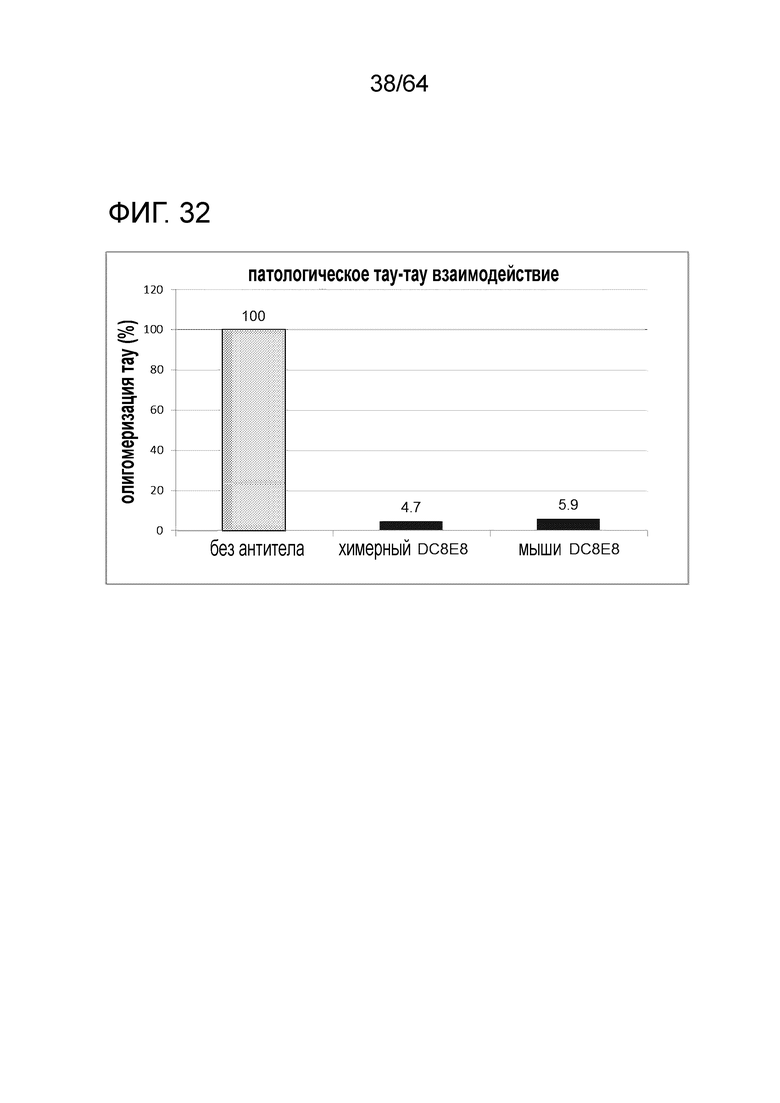
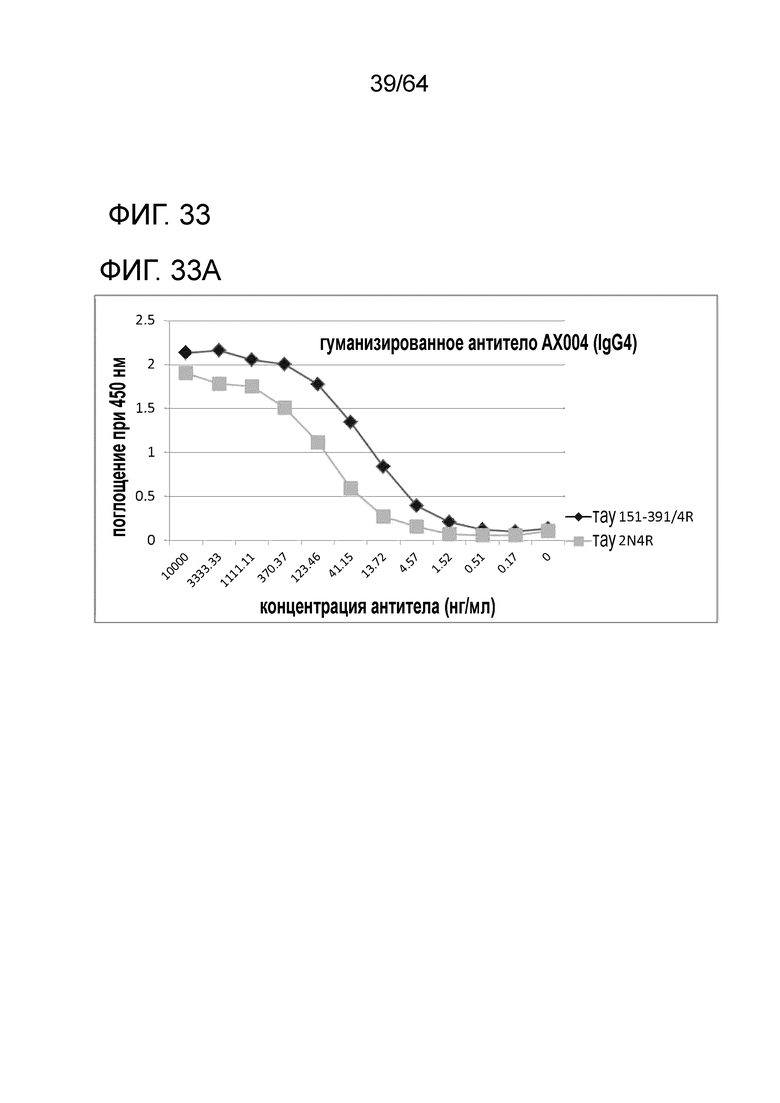
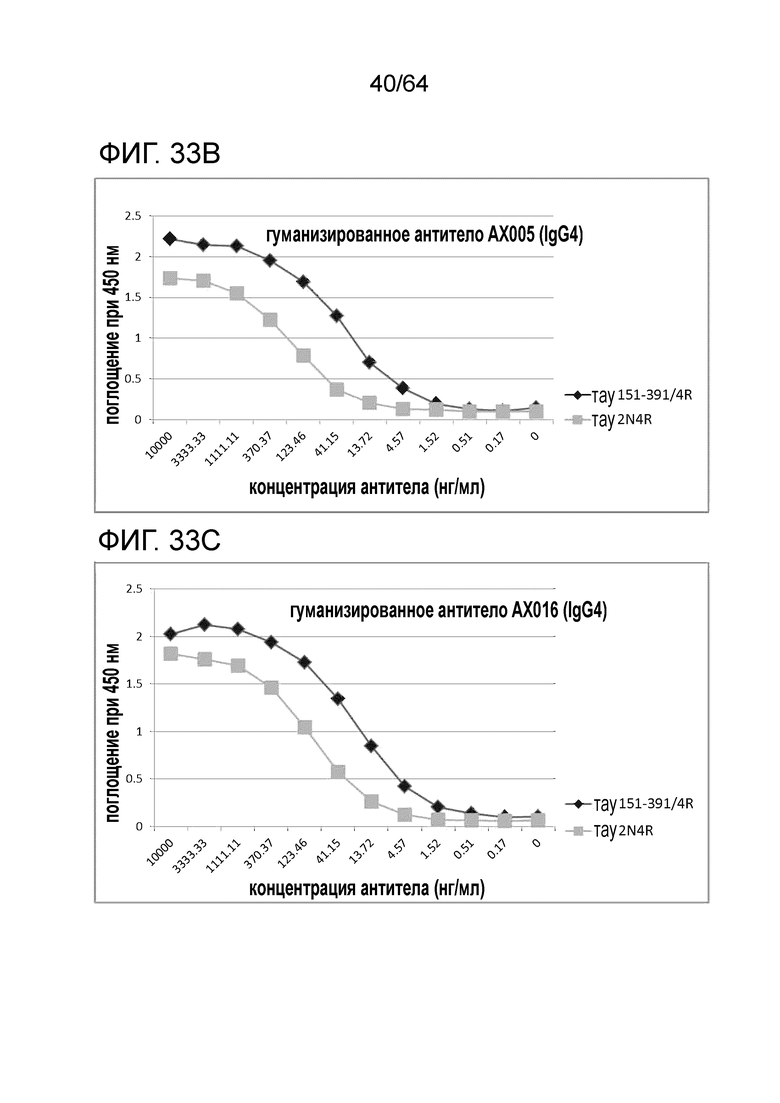


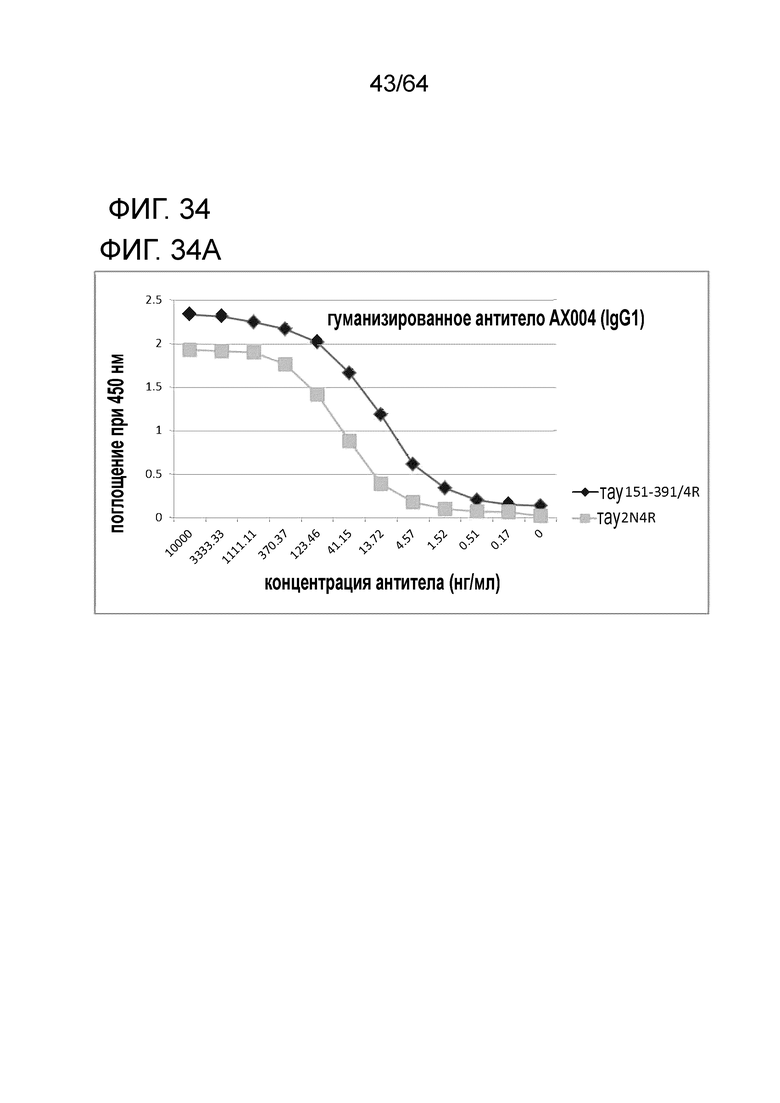
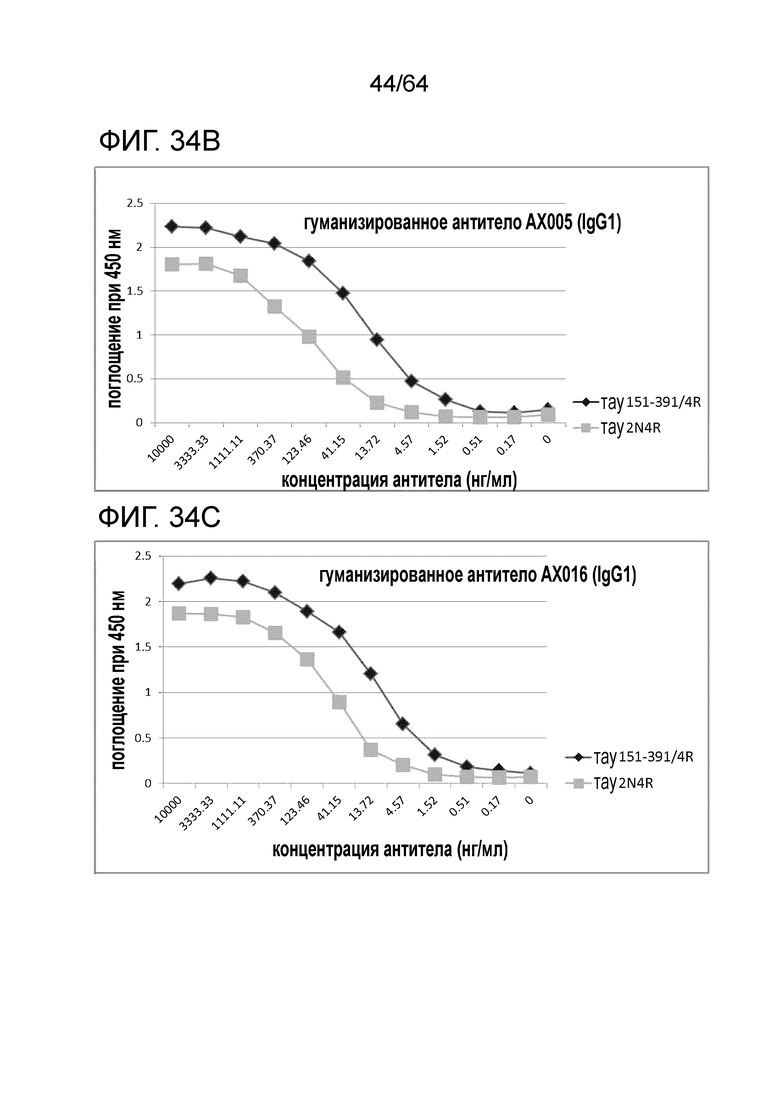
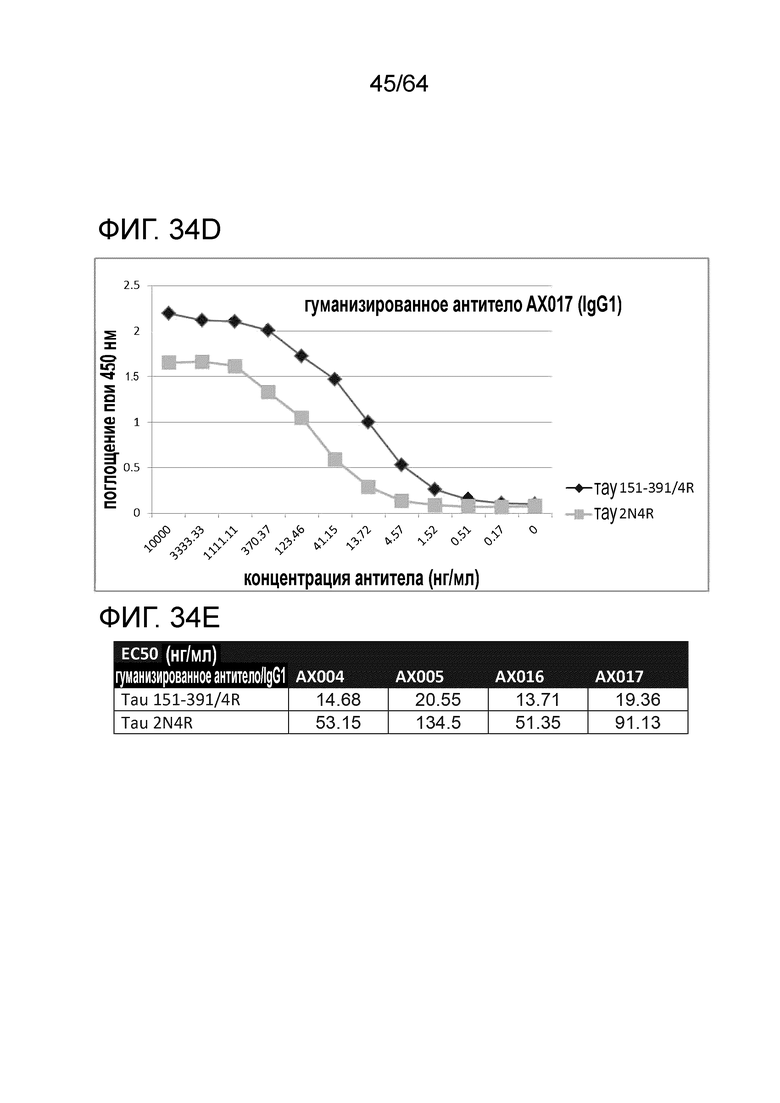
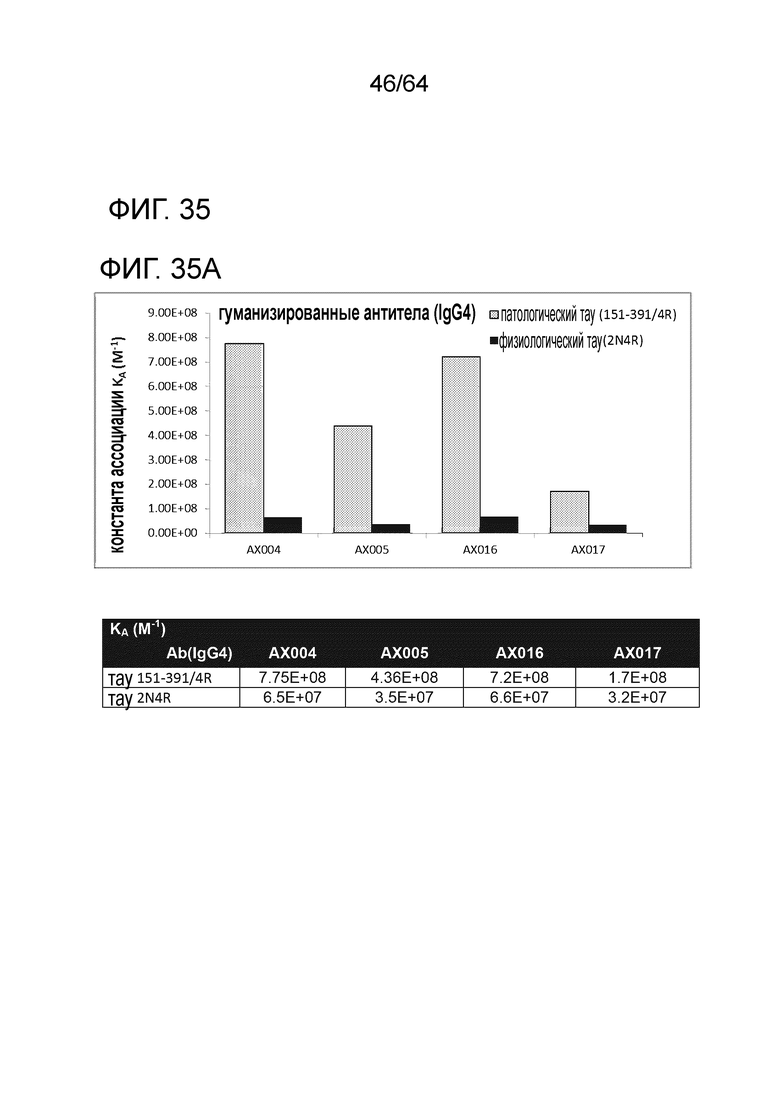

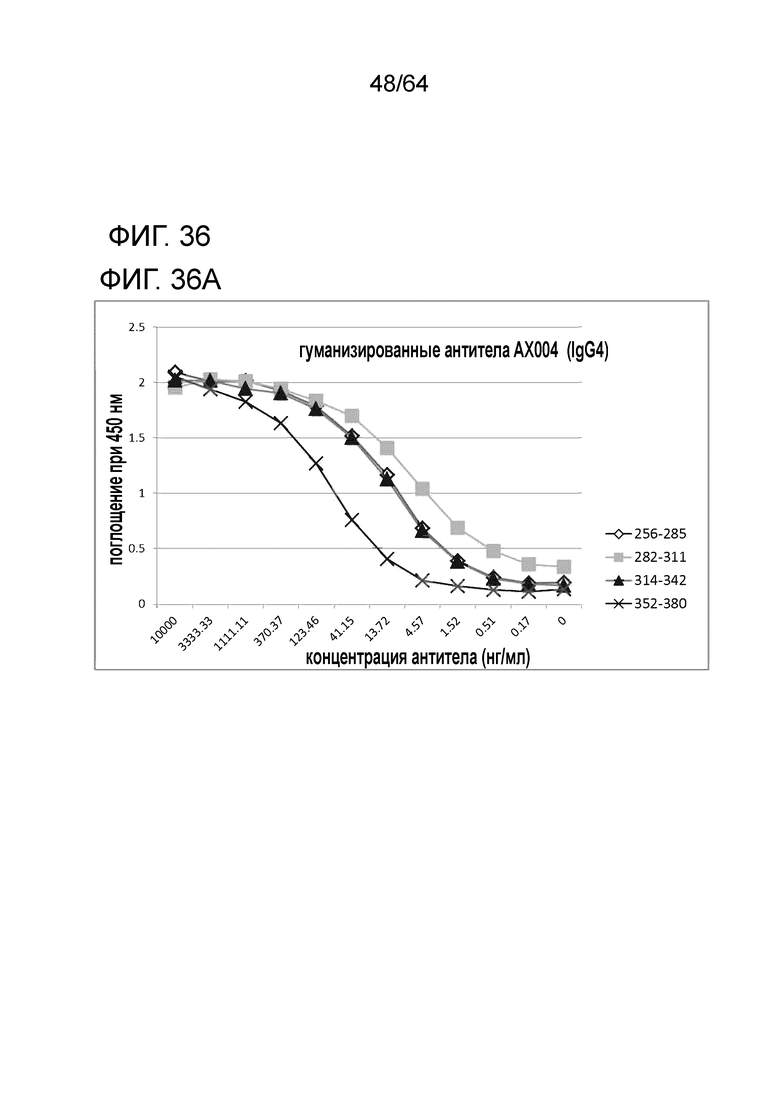

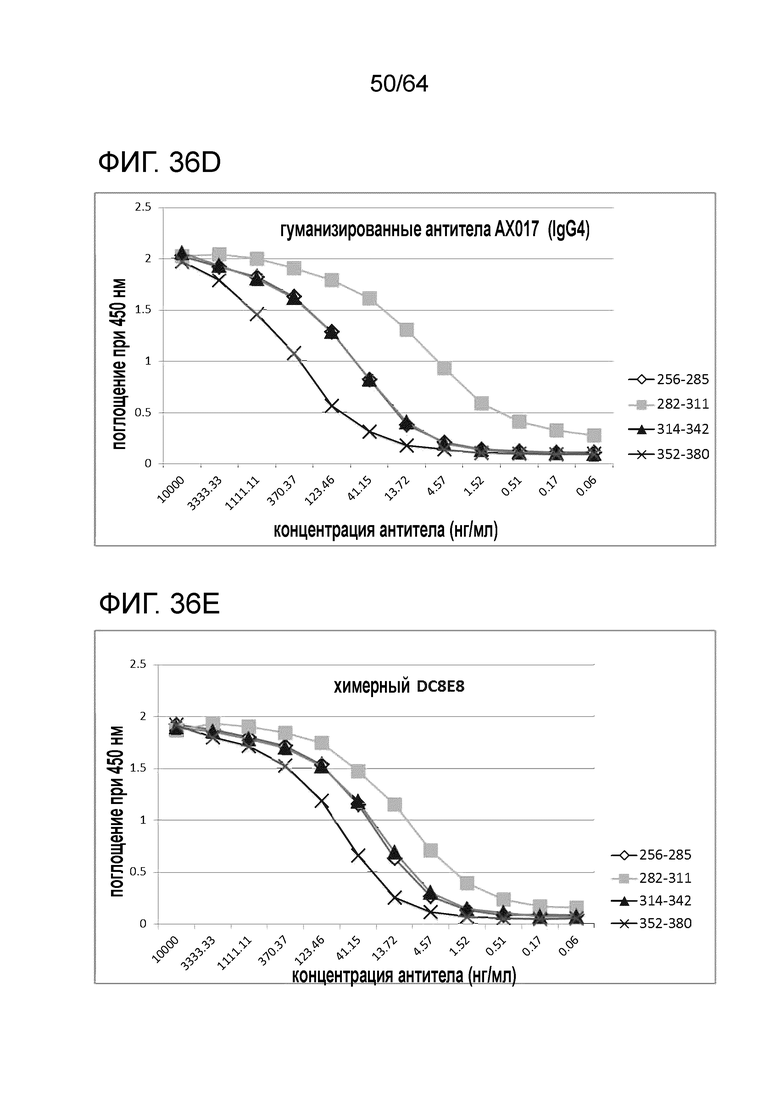
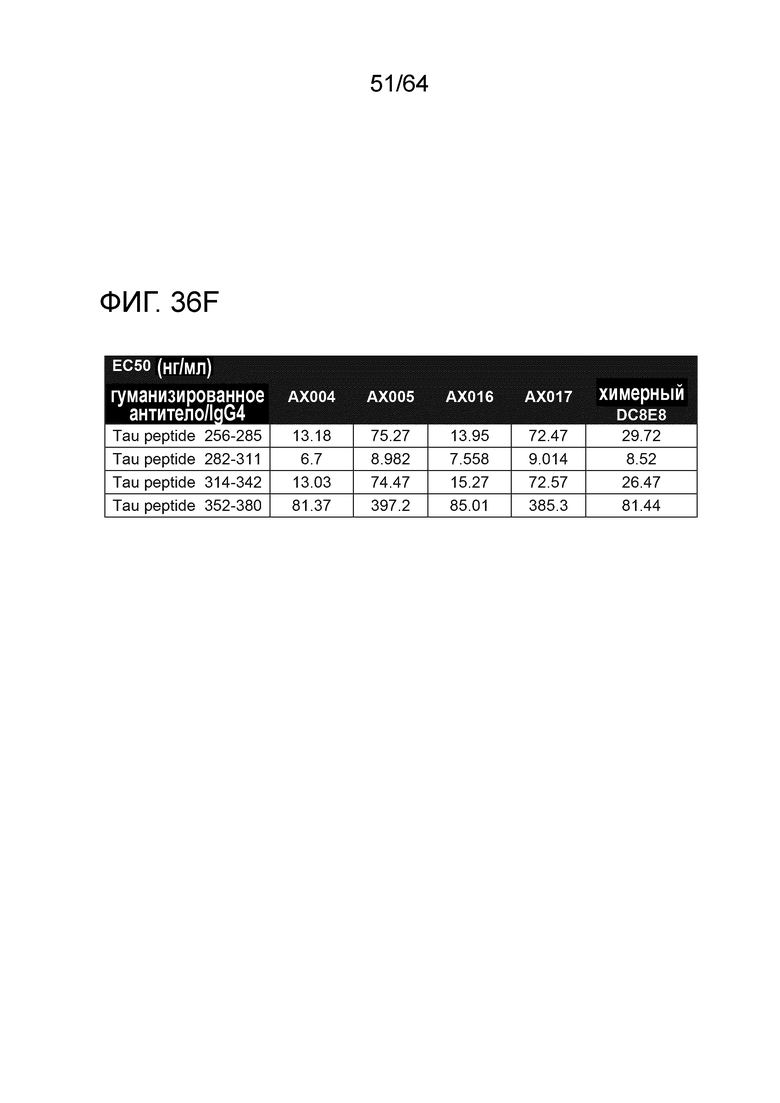


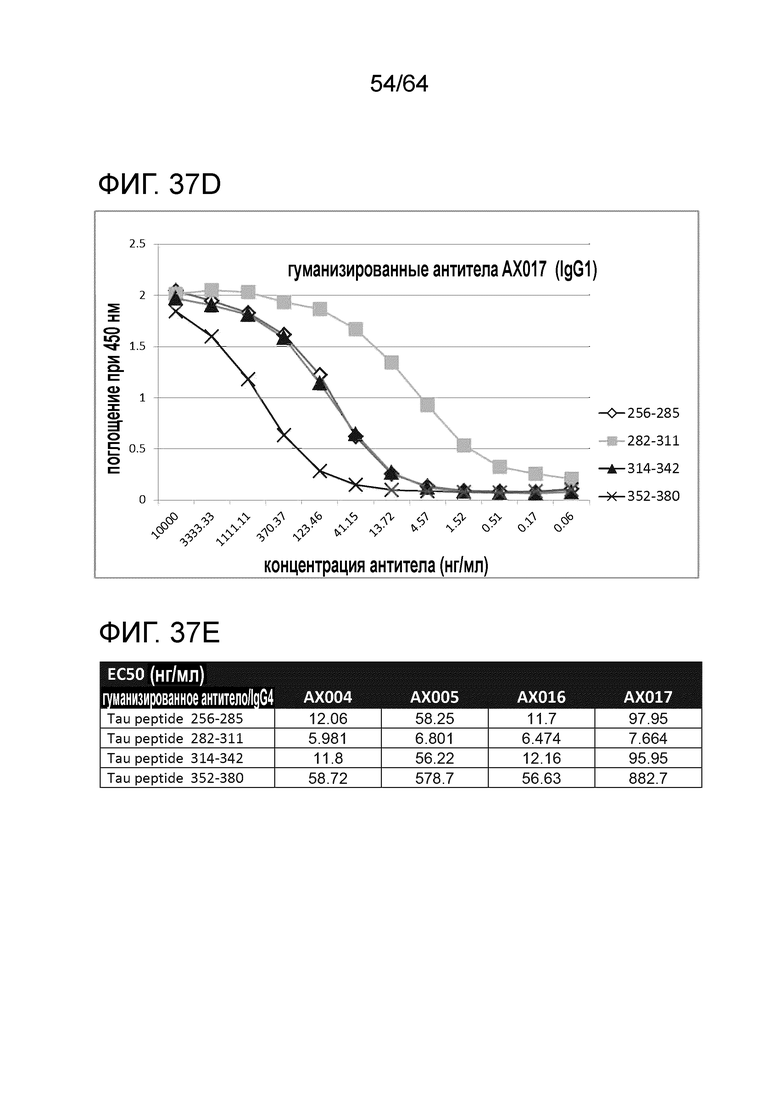
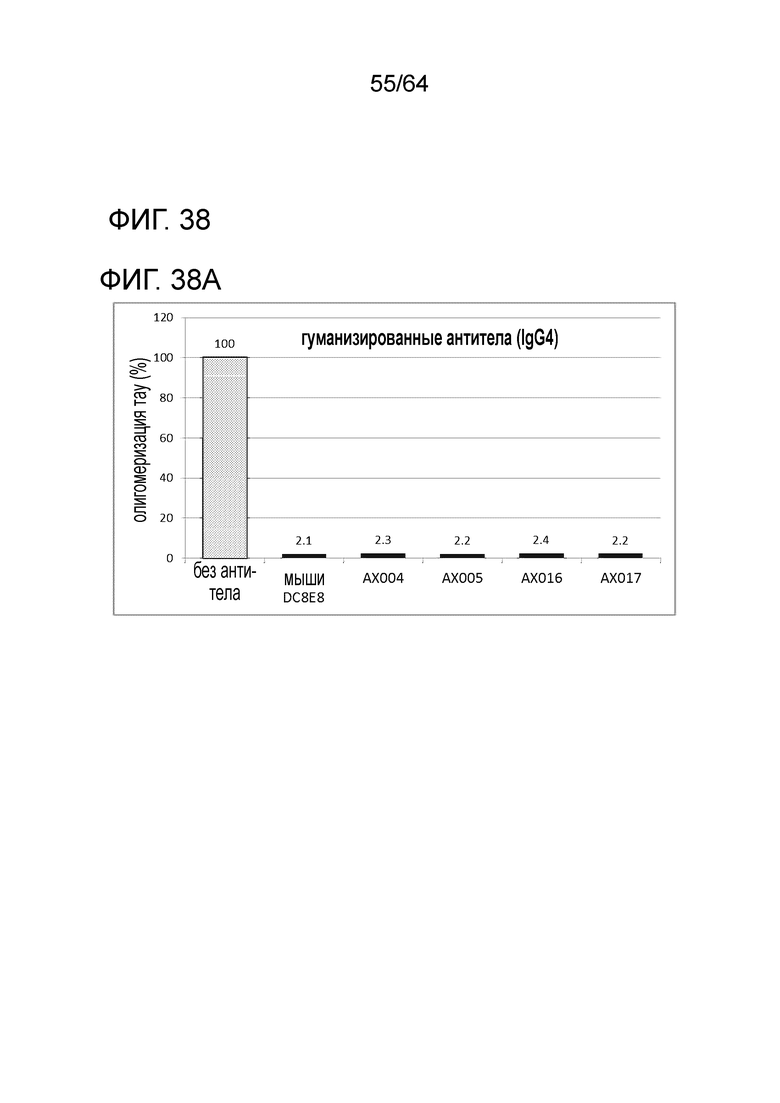


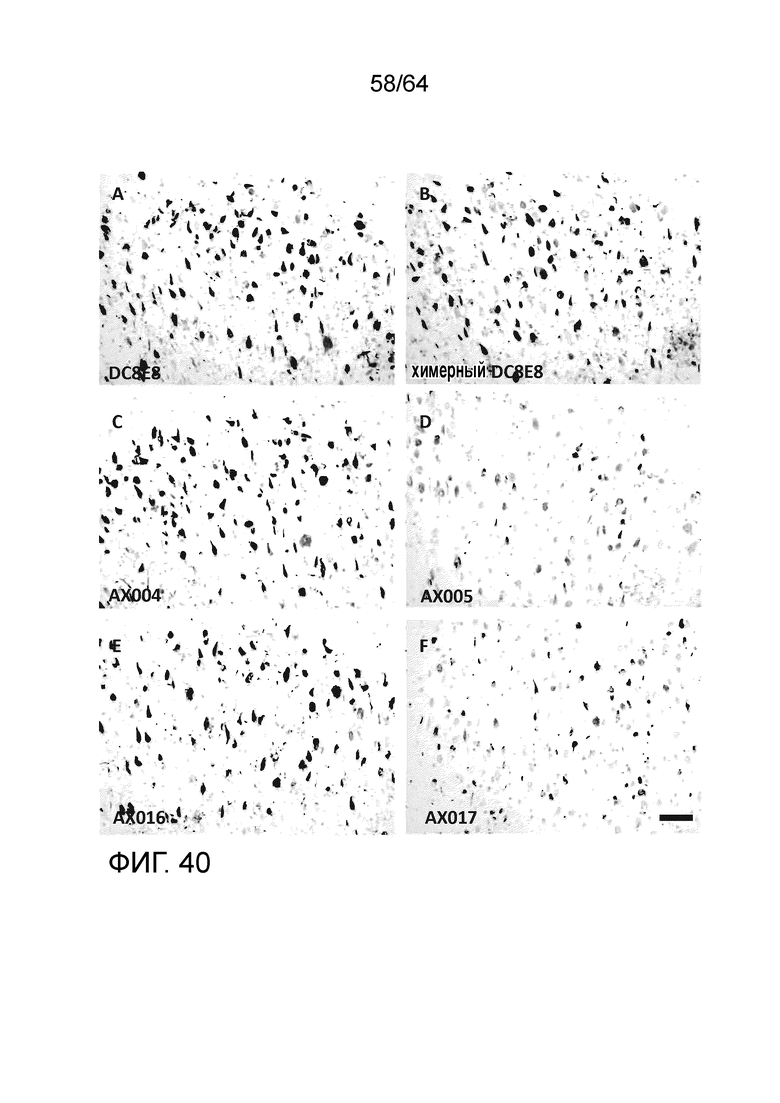
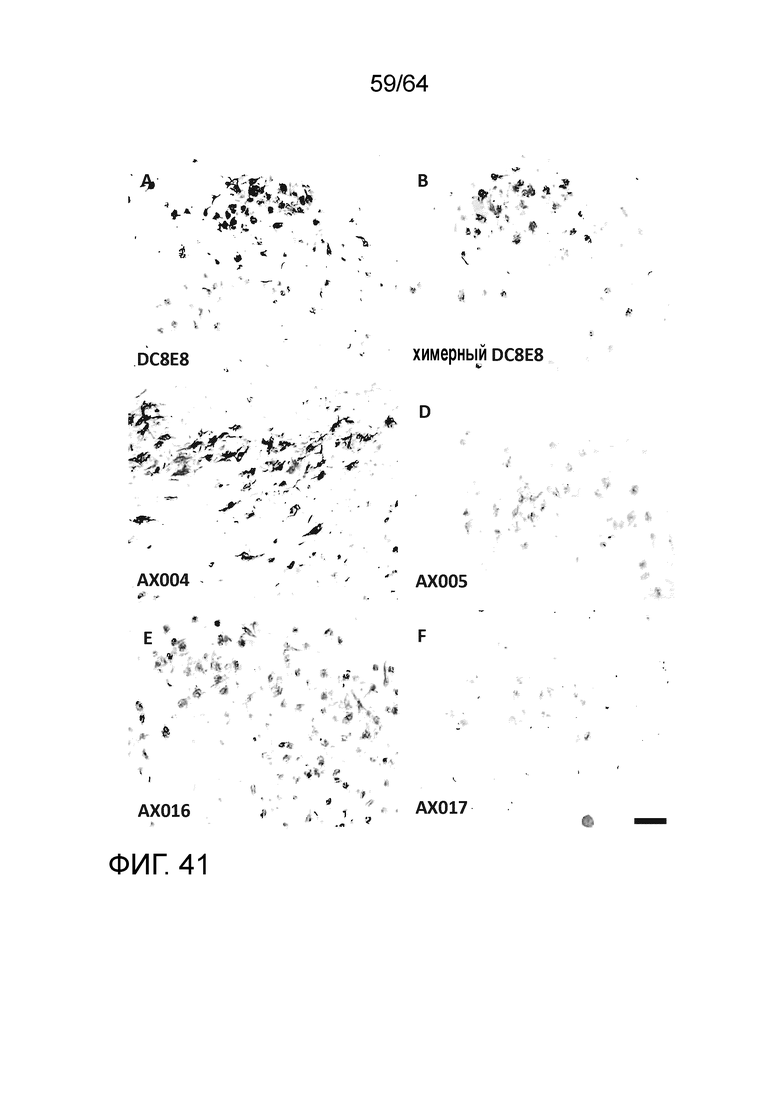
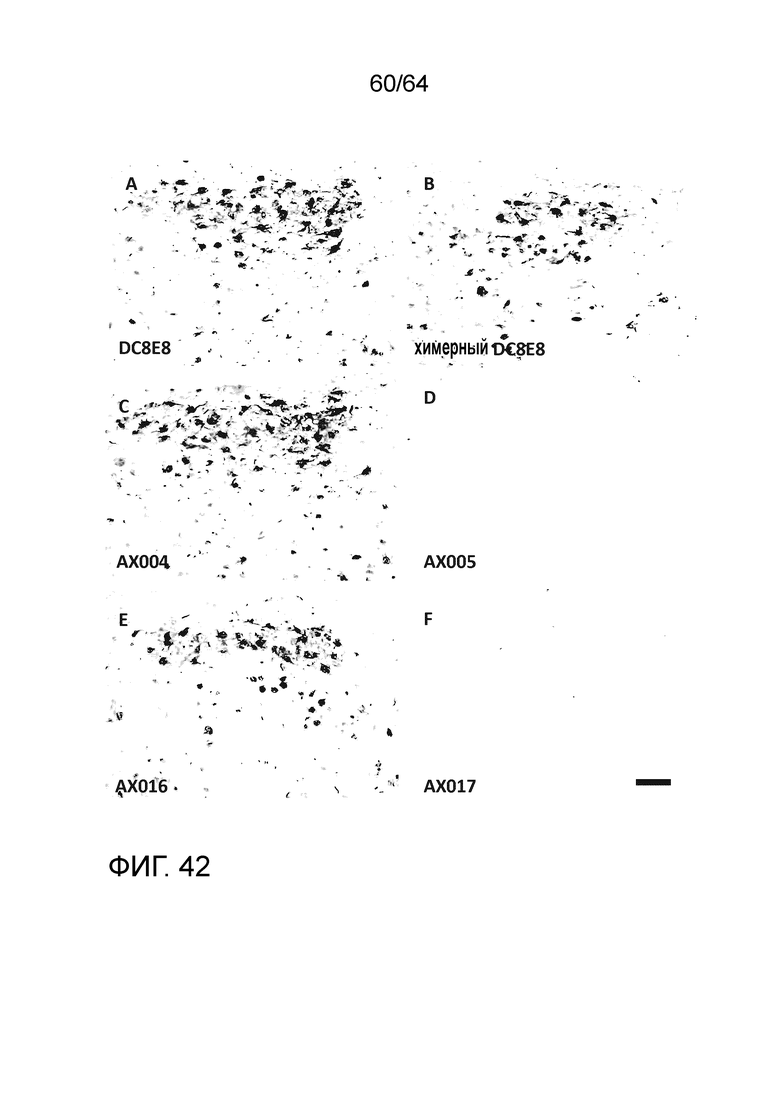
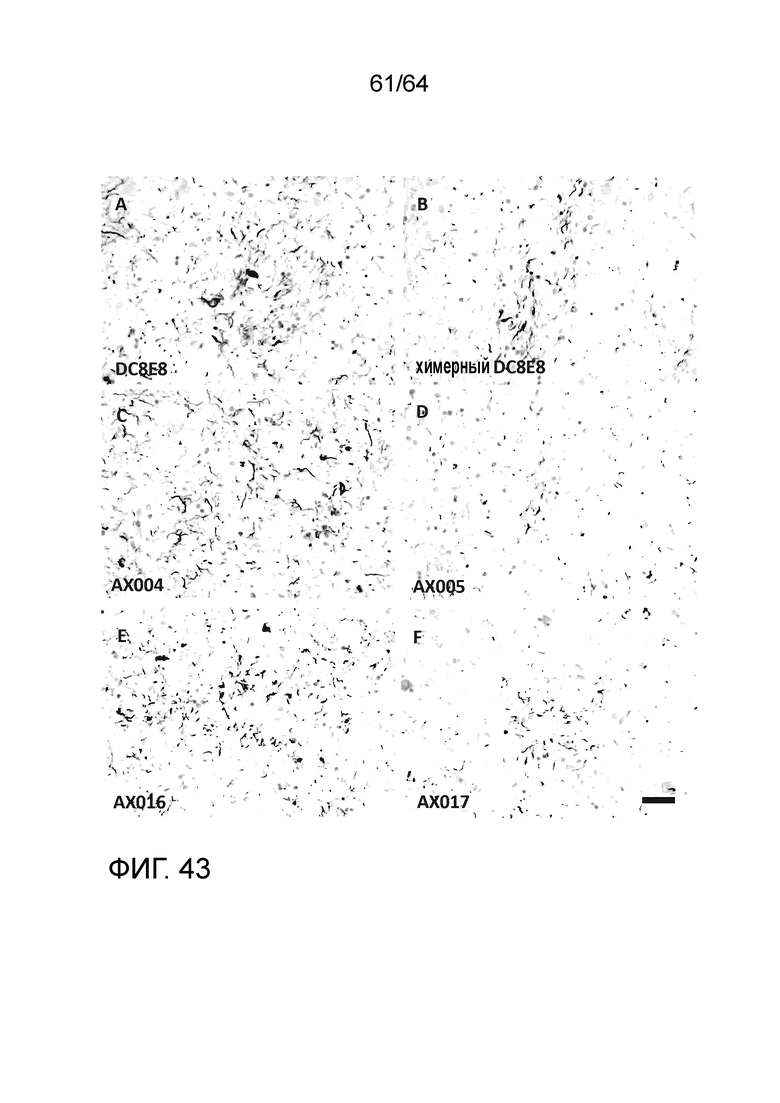



Изобретение относится к области биохимии, в частности к гуманизированному антителу против тау-белка или его тау-связывающему фрагменту, фармацевтической композиции, иммуноконъюгату, а также диагностическому реагенту, его содержащему. Также раскрыта молекула нуклеиновой кислоты, кодирующая вышеуказанное антитело или его фрагмент, а также вектор и клетка-хозяин, ее содержащие. Изобретение также относится к способу получения гуманизированного антитела против тау-белка или тау-связывающего фрагмента, предусматривающему использование вышеуказанной клетки. Изобретение позволяет эффективно осуществлять профилактику или лечение таутопатии. 14 н. и 14 з.п. ф-лы, 46 ил., 10 табл., 7 пр.
1. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или его тау-связывающий фрагмент специфически связывается с тау-белком и содержит:
(а) вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2 и 3 соответственно, и каркасную область тяжелой цепи с SEQ ID NO:71,
где SEQ ID NO:71 замещена в одном или нескольких положениях, выбранных из аминокислотных остатков 9, 21, 27, 28, 30, 38, 48, 67, 68, 70 и 95 (согласно нумерации Кэбат), и где:
положение 9 занято A или P;
положение 21 занято P или S;
положение 27 занято G или Y;
положение 28 занято I или T;
положение 30 занято S или T;
положение 38 занято K или R;
положение 48 занято I или M;
положение 67 занято K или R;
положение 68 занято A или V;
положение 70 занято I или L; и
положение 95 занято F или Y; и
(b) вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5 и 6, соответственно, и каркасную область легкой цепи с SEQ ID NO:65,
где SEQ ID NO:65 необязательно замещена S в положении 5 (согласно нумерации Кэбат); и
(c) константные области тяжелой цепи и легкой цепи, каждая из иммуноглобулина человека.
2. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.1,
где в каркасной области тяжелой цепи положение 9 занято P,
положение 21 занято P,
положение 27 занято Y,
положение 28 занято I,
положение 30 занято T,
положение 38 занято K,
положение 48 занято I,
положение 67 занято K,
положение 68 занято A,
положение 70 занято L и/или
положение 95 занято F (согласно нумерации Кэбат).
3. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.1,
где в каркасной области тяжелой цепи положение 9 занято А,
положение 21 занято S,
положение 27 занято Y,
положение 28 занято T,
положение 30 занято S,
положение 38 занято R,
положение 48 занято M,
положение 67 занято R,
положение 68 занято V,
положение 70 занято I и/или
положение 95 занято Y (согласно нумерации Кэбат).
4. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.1 или 2, где в каркасной области легкой цепи положение 5 занято S (согласно нумерации Кэбат).
5. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.1,
где последовательность вариабельной области тяжелой цепи содержит любую последовательность из SEQ ID NO:14-25; и
последовательность вариабельной области легкой цепи содержит SEQ ID NO:26.
6. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.1,
где последовательность вариабельной области тяжелой цепи содержит любую последовательность из SEQ ID NO:14-25; и
последовательность вариабельной области легкой цепи содержит SEQ ID NO:27.
7. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-6, где антитело относится к изотипу IgG1 или изотипу IgG4.
8. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент, где указанное антитело или его тау-связывающий фрагмент специфически связывается с тау-белком и содержит вариабельную область тяжелой цепи, которая содержит SEQ ID NO:16, и вариабельную область легкой цепи, которая содержит SEQ ID NO:26, и антитело относится к изотипу IgG1 или изотипу IgG4.
9. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент, где указанное гуманизированное антитело против тау-белка или его тау-связывающий фрагмент специфически связывается с тау-белком и содержит:
a) вариабельную область тяжелой цепи, содержащую CDR-H1, CDR-H2 и CDR-H3 с SEQ ID NO:1, 2 и 3 соответственно, и каркасную область тяжелой цепи из SEQ ID NO:71;
b) вариабельную область легкой цепи, содержащую CDR-L1, CDR-L2 и CDR-L3 с SEQ ID NO:4, 5 и 6, соответственно, и каркасную область легкой цепи из SEQ ID NO:65; и
c) константные области тяжелой цепи и легкой цепи, каждая из которых из иммуноглобулина человека.
10. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент, где указанное гуманизированное антитело против тау-белка или его тау-связывающий фрагмент специфически связывается с тау-белком и содержит:
a) тяжелую цепь, содержащую любую аминокислотную последовательность SEQ ID NO:28-40 или 43-55; и
b) легкую цепь, содержащую любую аминокислотную последовательность SEQ ID NO:57 или 58.
11. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.10, где
тяжелая цепь содержит аминокислотную последовательность SEQ ID NO:31, и
легкая цепь содержит аминокислотную последовательность SEQ ID NO:57.
12. Гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по п.10, где
тяжелая цепь содержит аминокислотную последовательность SEQ ID NO:46, и
легкая цепь содержит аминокислотную последовательность SEQ ID NO:57.
13. Гуманизированное антитело или его тау-связывающий фрагмент по любому из пп.1-12, где указанное гуманизированное антитело против тау-белка или его тау-связывающий фрагмент связывается с одним или несколькими эпитопами, выбранными из HQPGGG (SEQ ID NO:148), HVPGGG (SEQ ID NO:149) и HKPGGG (SEQ ID NO:150).
14. Фармацевтическая композиция для профилактики или лечения таутопатии, где фармацевтическая композиция содержит эффективное количество гуманизированного антитела против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13 и фармацевтически приемлемый носитель, разбавитель, вспомогательное вещество и/или стабилизатор.
15. Фармацевтическая композиция по п.14, где таутопатия представляет собой болезнь Альцгеймера.
16. Фармацевтическая композиция по п.14, которая дополнительно содержит второе терапевтическое средство.
17. Фармацевтическая композиция по п.16, где второе терапевтическое средство и гуманизированное антитело против тау-белка или его тау-связывающий фрагмент химически конъюгированы.
18. Фармацевтическая композиция по п.16, где второе терапевтическое средство используется для профилактики или лечения болезни Альцгеймера.
19. Фармацевтическая композиция по любому из пп.16-18, где второе терапевтическое средство может быть выбрано из одного или нескольких средств: тау-пептидов, бета-амилоидных пептидов, N-концевых бета-амилоидных пептидов, мутированного дифтерийного токсина; других антител против тау-белка, антител против бета-амилоида, бапинезумаба, соланезумаба, гантенерумаба, кренезумаба, иммуноглобулина IVIG, других иммунологических лекарственных средств, нацеливающихся на олигомеры A-бета, соединений, предотвращающих гиперфосфорилирование тау-белка, активных и пассивных иммунологических лекарственных средств, нацеливающихся на тау-агрегаты, ингибиторов агрегации бета-амилоида, трамипросата, ингибиторов гамма-секретазы, семагацестата, модуляторов гамма-секретазы, таренфлурбила, ингибиторов ацетилхолинэстеразы, донепезила, ривастигмина, галантамина, такрина, пищевых добавок, антагонистов рецептора N-метил-D-аспартата (NMDA), мемантина, ингибиторов восстановления ДНК, пирензепина или его метаболита, хелаторов переходных металлов, факторов роста, гормонов, нестероидных противовоспалительных препаратов (NSAID), антиоксидантов, агентов, уменьшающих уровень липидов, селективных ингибиторов фосфодиэстеразы, ингибиторов агрегации тау-белка, ингибиторов протеинкиназы, лекарственных средств ингибиторов лекарств митохондриальной дисфункции, нейротрофинов, ингибиторов белков теплового шока, ингибиторов липопротеин-связанной фосфолипазы A2, антиапоптотического соединения, хелатора металла, ингибитора репарации ДНК, 3-амино-1-пропансульфоновой кислоты (3APS), 1,3-пропандисульфоната (1,3PDS), активатора секретазы, ингибитора бета-секретазы, ингибитора гамма-секретазы, бета-амилоидного пептида, бета-амилоидного антитела, нейротрансмиттера, разрушителя бета-структуры, противовоспалительной молекулы, ингибиторов BACE, мускариновых антагонистов, ингибиторов холинэстеразы, ингибиторов гамма-секретазы, модуляторов гамма-секретазы, ингибиторов HMG-CoA-редуктазы, нестероидных противовоспалительных средств, антагонистов рецептора N-метил-D-аспартата, антител против амилоида, витамина Е, агонистов никотинацетилхолинового рецептора, обратных агонистов рецептора CB1, антагонистов рецептора CB1, антибиотика, стимуляторов секреции гормона роста, антагонистов гистамина Н3, агонистов АМРА, ингибиторов PDE4, обратных агонистов GABAA, ингибиторов амилоидной агрегации, ингибиторов гликогенсинтаза-киназа бета, промоторов активности альфа секретазы, ингибиторов PDE-10, ингибиторов абсорбции холестерина и их любых фармацевтически приемлемых солей.
20. Диагностический реагент для диагностики таутопатии, где диагностический реагент содержит гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13, и носитель, разбавитель, вспомогательное вещество и/или стабилизатор.
21. Иммуноконъюгат для профилактики или лечения таутопатии, где иммуноконъюгат имеет формулу (A)-(L)-(C), где:
(A) представляет собой гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13;
(L) представляет собой линкер; и
(C) представляет собой терапевтический агент; и
где указанный линкер (L) соединяет (A) и (C).
22. Иммуноконъюгат для визуализации таутопатии, где иммуноконъюгат имеет формулу (A)-(L)-(C), где:
(A) представляет собой гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13;
(L) представляет собой линкер; и
(C) представляет собой агент визуализации; и
где указанный линкер (L) соединяет (A) и (C).
23. Иммуноконъюгат для детекции таутопатии, где иммуноконъюгат имеет формулу (A)-(L)-(C), где:
(A) представляет собой гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13;
(L) представляет собой линкер; и
(C) представляет собой агент детекции; и
где указанный линкер (L) соединяет (A) и (C).
24. Иммуноконъюгат для диагностики таутопатии, где иммуноконъюгат имеет формулу (A)-(L)-(C), где:
(A) представляет собой гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13;
(L) представляет собой линкер; и
(C) представляет собой агент диагностики; и
где указанный линкер (L) соединяет (A) и (C).
25. Молекула нуклеиновой кислоты, кодирующая гуманизированное антитело против тау-белка или его тау-связывающий фрагмент по любому из пп.1-13.
26. Вектор экспрессии, содержащий молекулу нуклеиновой кислоты по п.25.
27. Клетка-хозяин для продукции гуманизированного антитела против тау-белка или его тау-связывающего фрагмента по любому из пп.1-13, содержащая вектор экспрессии по п.26.
28. Способ получения гуманизированного антитела против тау-белка или тау-связывающего фрагмента, которое специфически связывается с тау-белком, включающий культивирование клетки-хозяина по п.27 и, таким образом, экспрессию нуклеиновой кислоты и продукцию гуманизированного антитела против тау-белка или его тау-связывающего фрагмента.
| WO2013041962 A1, 28.03.2013 | |||
| YAGHOUB SAFDARI et al., Antibody humanization methods - a review and update, Biotechnology and Genetic Engineering Reviews, 2013, Vol | |||
| Солесос | 1922 |
|
SU29A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| WO2014100600 A2, 26.06.2014 | |||
| WO2012049570 A1, 19.04.2012 | |||
| RU2011152816 A, 20.07.2013. | |||
Авторы
Даты
2020-08-24—Публикация
2015-11-18—Подача