Область техники, к которой относится изобретение
Данное изобретение относится к композициям для применения в профилактике и/или лечении запора, улучшении консистенции/частоты стула и/или профилактике или лечении метеоризма, вздутия живота, колик или кишечного дискомфорта у младенцев или детей младшего возраста.
Уровень техники
Материнское молоко рекомендовано всем младенцам. Однако в некоторых случаях грудное вскармливание является недостаточным или неблагоприятным по медицинским показаниям, или мать отказывается от грудного вскармливания. Для этих ситуаций были разработаны детские смеси. Также были разработаны обогатители для обогащения материнского молока или детской смеси определенными ингредиентами. Младенцы и дети младшего возраста могут страдать запором или твердым стулом, в частности, из-за недоразвития кишечника, его недостаточной активности для данного младшего возраста и отсутствия разнообразия в составе питания. Поэтому пребиотики благодаря их полезным эффектам часто включают в детские смеси, обогатители или любые другие искусственные питательные композиции и питательные добавки.
Пребиотики являются неперевариваемыми углеводами, которые способствуют здоровью их потребителей. Как правило, они представляют собой соединения, которые проходят через верхний отдел желудочно-кишечного тракта в непереваренном виде и за счет своего действия в качестве субстрата для благоприятных бактерий, таких как бифидобактерии, которые заселяют толстый кишечник, стимулируют их рост и/или активность. Эти соединения формируют основу стула.
Однако некоторые виды клетчатки, включая полезные пребиотики инулин и олигофруктозу, выделяют газы, обогащающие здоровые бактерии, которые живут в нижнем отделе кишечника. Это может привести к метеоризму, вздутию живота, коликам и/или кишечному дискомфорту у человека. Эти сопутствующие явления могут вызвать особые проблемы у младенцев и детей младшего возраста и могут привести к периодам плача, затруднениям при вскармливании, раздражительности, боли, особенно боли в животе, спазмам в животе, нарушениям сна.
Олигосахариды грудного молока (ОГМ) являются в совокупности третьим по величине компонентом (по содержанию в сухом веществе) в грудном молоке после лактозы и жира. ОГМ обычно состоят из лактозы на восстанавливающем конце с углеводным ядром, которое часто содержит фукозу или сиаловую кислоту на невосстанавливающем конце. В грудном молоке выделено и охарактеризовано более сотни олигосахаридов молока.
Для различных целей разработано несколько композиций с использованием ингредиентов ОГМ, таких как фукозилированные олигосахариды, лакто-N-тетраоза, лакто-N-неотетраоза и/или сиалилированные олигосахариды.
Например, в публикации WO2005055944 медицинского центра детской больницы Цинциннати описана фармацевтическая композиция, содержащая молекулу, содержащую фукозную группу, соединенную с галактозной группой альфа-2 связью, альфа-3 связью или альфа-4 связью, и фармацевтически приемлемый носитель. Описаны различные молекулы, такие как 2’-фукозиллактоза. Эта заявка носит достаточно общий характер, поскольку описывает предотвращение или лечение нескольких инфекций, включая респираторные или кишечные инфекции, в большой целевой группе пациентов (младенцы, дети или взрослые). Дополнительно, данный документ позволяет предположить, что за счет обеспечения средних или больших количеств 2FL снижается распространенность Campylobacter diarrhea.
WO9956754 компании Abbott относится к композициям, содержащим по меньшей мере один остаток фукозы в альфа-1-2 связи, например 2FL, и к их применению. В частности, такие композиции могут применяться в лечении и профилактике желудочно-кишечных инфекций, вызывающих, например, диарею и энтероколит.
В WO2004002495 описано содержащее олигосахариды вещество или рецептор, связывающийся с диареегенными Escherichia coli и/или зоонотическими видами Helicobacter, и его применение, например, в фармацевтических, питательных и других композициях для профилактики и лечения диареи, геморрагического колита или гемолитико-уремического синдрома.
WO2012092156 относится к питательной композиции, содержащей ОГМ, но предназначенной для широкого перечня полезных для здоровья эффектов, в том числе переносимости кормления и, в частности, уменьшения диареи и жидкого стула (т. е. противоположности запора), а также уменьшения сопутствующего газообразования и колик.
Действительно, как показано в публикации Simone Albrecht et al. Oligosaccharides in feces of breast- and formula-fed babies, 2005, пребиотические углеводы (например, ОГМ, галактоолигосахариды (ГОС)) оказывают влияние на развитие кишечника новорожденных. Однако эти действия специфичны для определенных типов клетчатки (ОГМ и ГОС различаются по структуре). Например, показано, что ОГМ способствует заселению кишечника защитными бактериями у новорожденных младенцев (Riccardo Locascio et al., 2007, ссылочный документ 2 данной публикации), а также создает защиту от диареи (Newburg et al., 2004, ссылочный документ 5 данной публикации).
Таким образом, ни в одной из предшествующих работ не уделяется внимание профилактике и/или лечению запора и/или улучшению консистенции/частоты стула при отсутствии упоминаемых выше сопутствующих проблем, связанных с метеоризмом, вздутием живота, коликами и/или кишечным дискомфортом, которые могут быть особенно болезненными у младенцев и детей младшего возраста.
Существует явная необходимость в разработке приемлемых способов уменьшения распространенности этих состояний/проблем со здоровьем у младенцев и детей младшего возраста, и в особенности необходима разработка питательных композиций, таких как детские смеси, которые могут обеспечить более мягкий стул, не усиливая метеоризм, вздутие живота, колики и/или кишечный дискомфорт.
Также существует необходимость обеспечить такую пользу для здоровья способом, который особенно подходит для молодых субъектов (младенцев и детей младшего возраста), при этом способ не должен включать в себя классическое фармацевтическое вмешательство, поскольку эти младенцы или дети младшего возраста особенно уязвимы.
Существует необходимость в обеспечении такой пользы для здоровья этих младенцев или детей младшего возраста с помощью способа, который не вызывает побочных эффектов и/или который является легко осуществимым и приемлемым для родителей или медицинских работников.
Также существует необходимость обеспечить такую пользу способом, который позволит сохранить разумную и доступную для большинства стоимость такого обеспечения.
Раскрытие изобретения
Авторы настоящего изобретения обнаружили, что композицию, содержащую по меньшей мере один фукозилированный олигосахарид, можно преимущественно применять для улучшения консистенции стула у младенца или ребенка младшего возраста, особенно за счет уменьшения твердости стула.
Соответственно, в данном изобретении предложена питательная композиция, содержащая по меньшей мере один фукозилированный олигосахарид, для применения в профилактике и/или лечении запора, в улучшении консистенции/частоты стула, в профилактике и/или лечении метеоризма, вздутия живота, колик и/или кишечного дискомфорта у младенца или ребенка младшего возраста.
В некоторых вариантах осуществления питательная композиция содержит по меньшей мере пробиотический микроорганизм, в частности пробиотические бактерии, которые могут относиться к следующим родам: Lactobacillus spp., Streptococcus spp., Enterococcus spp. или Bifidobacterium spp. В некоторых предпочтительных вариантах осуществления пробиотические бактерии относятся к штамму Lactobacillus.
В особенно преимущественном варианте осуществления питательная композиция содержит 2’-фукозиллактозу (2-FL) в количестве 0,2–3 г/л питательной композиции.
Краткое описание фигур
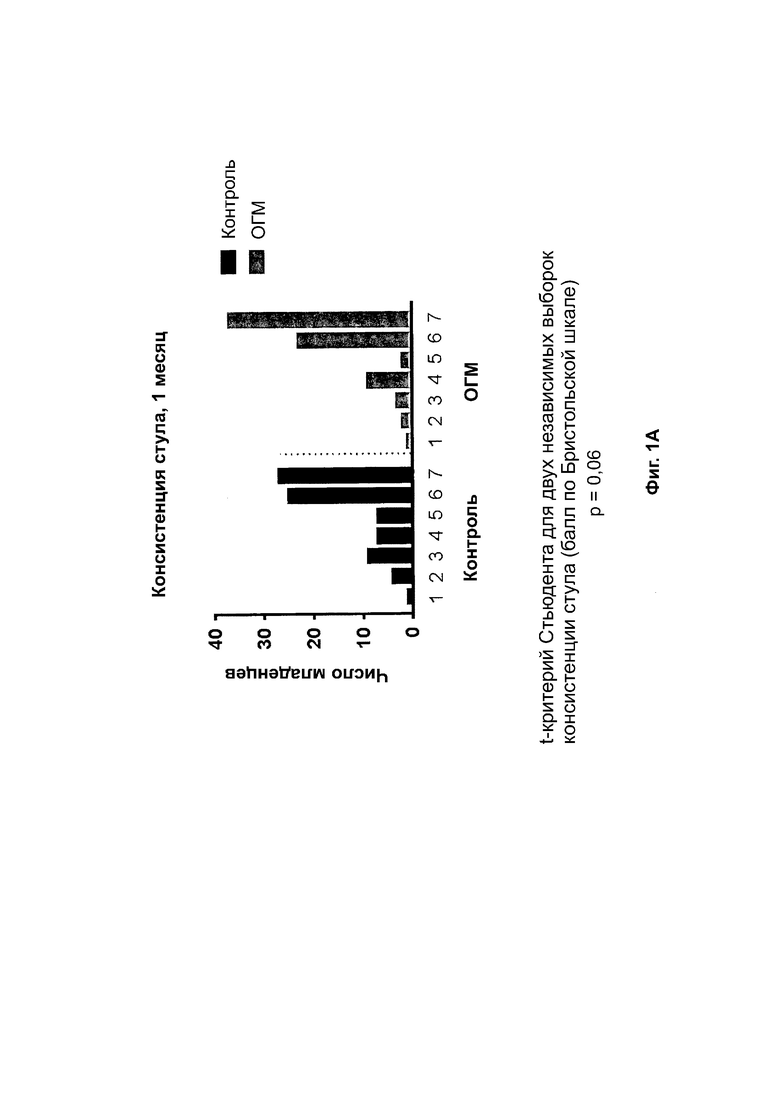
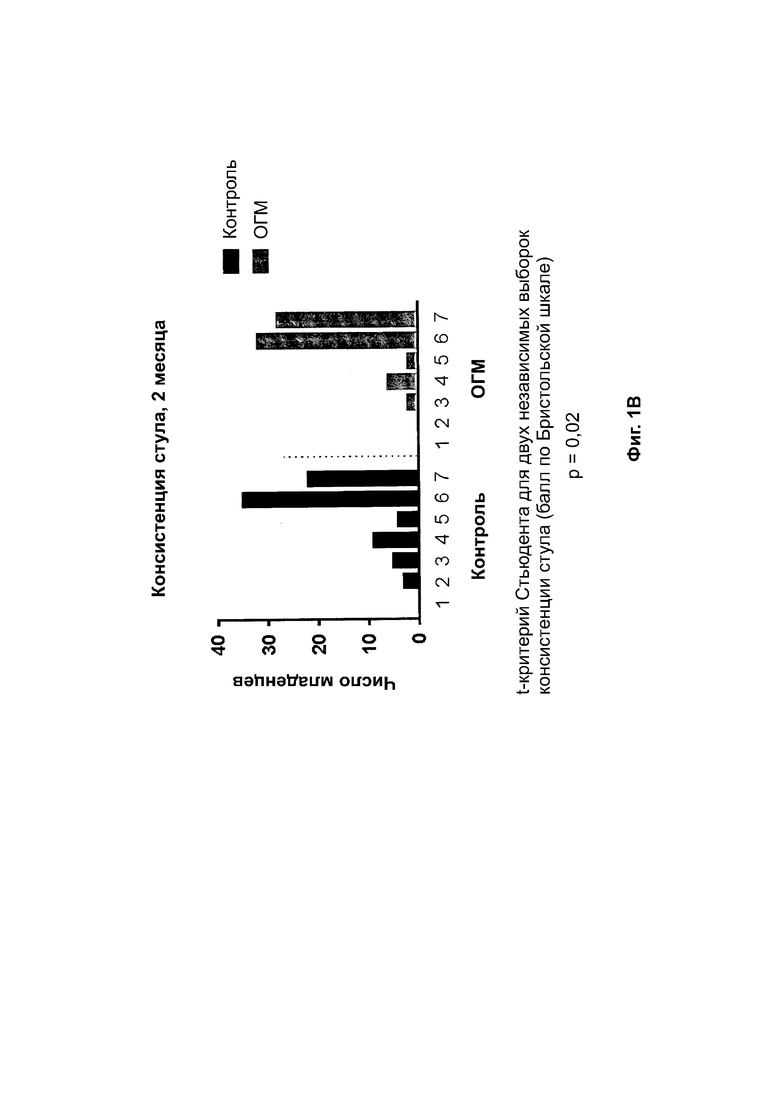
На фиг. 1 представлена консистенция стула в возрасте 1 месяца (фиг. 1A) и в возрасте 2 месяцев (фиг. 1B) у младенцев, вскармливаемых классической начальной детской смесью или классической начальной детской смесью, содержащей ОГМ, т. е. 2’-фукозиллактозу, в количестве 1,24 г/л и лакто-N-неотетраозу в количестве 0,63 г/л. Числами указана консистенция стула по Бристольской шкале: 1 — отдельные твердые комки, похожие на орехи (проходят с трудом); приводит к медленному транзиту; 2 — колбасовидный, но комковатый; 3 — колбасовидный, но с трещинами на поверхности; 4 — колбасовидный или змеевидный, гладкий и мягкий; 5 — мягкие комки с четкими краями (проходят легко); 6 — пушистые комочки с рваными краями, пористый стул; 7 — водянистый, без твердых кусочков.
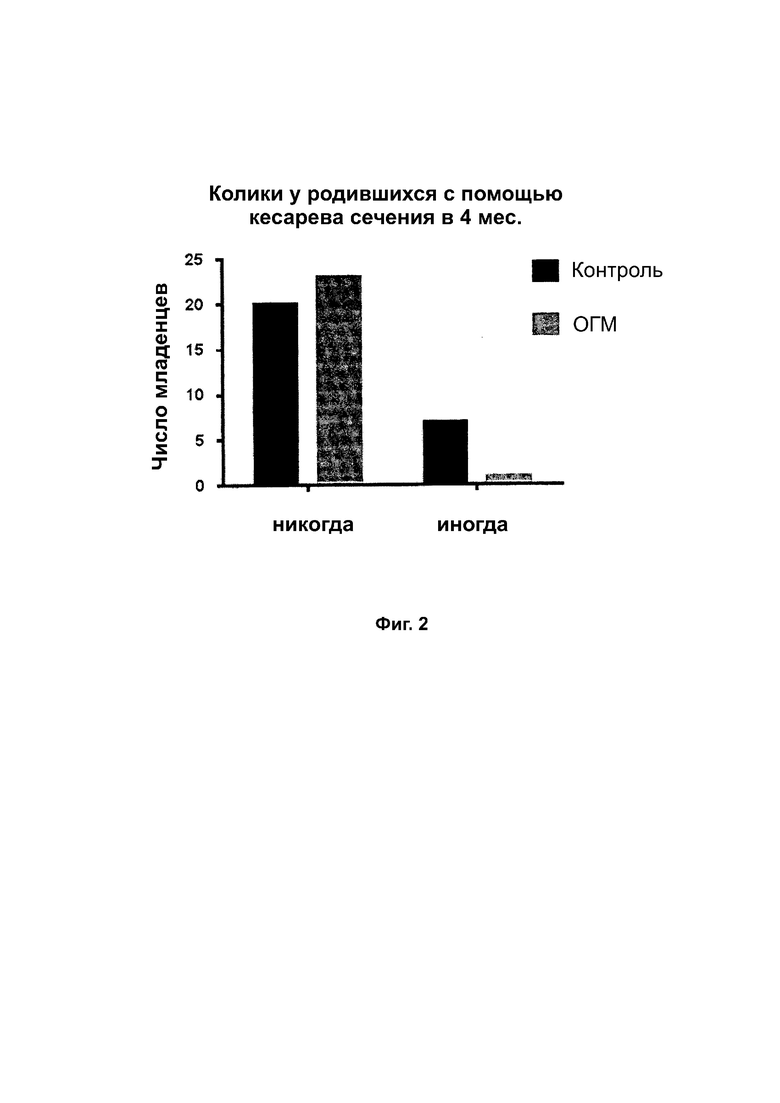
На фиг. 2 представлено число младенцев, родившихся с помощью кесарева сечения, которые, по сообщениям родителей, «никогда не испытывали» или «иногда испытывали» колики в возрасте 4 месяцев. Анализ линейных ассоциаций для лечения и колик по визиту и способу доставки с использованием критерия Кохрана — Мантеля — Гензеля для ассоциаций показал значимое различие в группе кесарева сечения в возрасте 4 месяцев.
Осуществление изобретения
Для целей настоящего документа следующие термины имеют приведенные ниже определения.
Термин «младенец» означает ребенка в возрасте до 12 месяцев.
Выражение «ребенок младшего возраста» означает ребенка в возрасте от одного до трех лет (также называется ребенком, начинающим ходить).
«Младенец или ребенок младшего возраста, рожденный с помощью кесарева сечения» означает младенца или ребенка младшего возраста, рожденного путем кесарева сечения. Это означает, что младенец или ребенок младшего возраста был рожден не посредством вагинальных родов.
Выражение «младенец или ребенок младшего возраста, рожденный посредством вагинальных родов» означает младенца или ребенка младшего возраста, который был рожден посредством вагинальных родов, а не путем кесарева сечения.
«Недоношенный» или «преждевременно родившийся» означает младенца или ребенка младшего возраста, который родился раньше срока. По существу, этот термин относится к младенцу или ребенку младшего возраста, рожденному до 36-й недели беременности.
Выражение «питательная композиция» означает композицию, которой питается субъект. Эта питательная композиция обычно предназначена для перорального или внутривенного применения и обычно включает в себя источник липидов или жиров и источник белков.
В конкретном варианте осуществления композиция настоящего изобретения представляет собой гипоаллергенную питательную композицию. Выражение «гипоаллергенная питательная композиция» означает питательную композицию, для которой вероятность того, что она вызовет аллергические реакции, является малой.
В конкретном варианте осуществления композиция настоящего изобретения представляет собой искусственную питательную композицию. Выражение «искусственная питательная композиция» означает смесь, полученную с помощью химических и/или биологических средств, которые могут быть химически идентичны смеси природного происхождения, присутствующей в молоке млекопитающих (т. е. искусственная композиция не является грудным молоком).
Выражение «детская смесь» при использовании в настоящем документе относится к продукту питания, специально предназначенному для применения в пищу младенцами в течение первых месяцев жизни, который сам по себе удовлетворяет потребности в питании этой категории лиц (статья 2(c) Директивы Европейской комиссии 91/321/EEC 2006/141/EC от 22 декабря 2006 г. о детских смесях и смесях для прикармливаемых детей). Оно также относится к питательной композиции, предназначенной для младенцев, как определено в Codex Alimentarius (Codex STAN 72–1981) и стандарте «Специальные продукты для младенцев» (включая статью «Продукты питания для специальных медицинских целей»). Выражение «детская смесь» охватывает как «начальную детскую смесь», так и «смесь последующего уровня» или «смесь для прикармливаемых детей».
Смесь последующего уровня или смесь для прикармливаемых детей дают начиная с 6-го месяца. Она составляет главный жидкий элемент в постепенно увеличивающемся разнообразии рациона для лиц данной категории.
Выражение «детское питание» означает продукт питания, специально предназначенный для применения в пищу младенцами или детьми младшего возраста в течение первых лет жизни.
Выражение «детская композиция на зерновой основе» означает продукт питания, специально предназначенный для применения в пищу младенцами или детьми младшего возраста в течение первых лет жизни.
Термин «обогатитель» относится к жидким или сухим питательным композициям, подходящим для смешивания с грудным молоком или детской смесью.
Выражение «период отлучения от груди» означает период, в течение которого в рационе младенца или ребенка младшего возраста материнское молоко замещают другой пищей.
Выражения «дни/недели/месяцы/годы жизни» и «дни/недели/месяцы/годы после рождения» могут использоваться взаимозаменяемо.
Выражение «профилактика и/или лечение запора и/или улучшение консистенции/частоты стула» охватывает одно или несколько из следующего:
- профилактика запора;
- лечение запора;
- улучшение консистенции стула;
- улучшение частоты стула.
Выражение «профилактика и/или лечение метеоризма, вздутия живота, колик и/или кишечного дискомфорта» охватывает одно или несколько из следующего:
- профилактика метеоризма;
- лечение метеоризма;
- профилактика вздутия живота;
- лечение вздутия живота;
- профилактика колик;
- лечение колик;
- профилактика кишечного дискомфорта;
- лечение кишечного дискомфорта.
Выражения «в профилактике запора/метеоризма/вздутия живота/колик/кишечного дискомфорта», «осуществлять профилактику запора/метеоризма/вздутия живота/колик/кишечного дискомфорта», «при профилактике запора/метеоризма/вздутия живота/колик/кишечного дискомфорта» и «для профилактики запора/метеоризма/вздутия живота/колик/кишечного дискомфорта» могут использоваться взаимозаменяемо.
Эти выражения означают избегание возникновения этих состояний/проблем здоровья (запора/метеоризма/вздутия живота/колик/кишечного дискомфорта) и/или снижение распространенности указанных состояний/проблем здоровья (снижение частоты, т. е. числа этих состояний/проблем здоровья). В некоторых вариантах осуществления изобретения эти состояния/проблемы здоровья возникают в процессе лечения (т. е. в процессе введения композиции настоящего изобретения, либо сразу после начала ее введения, либо через некоторое время, например через несколько дней или недель после начала). Они также могут охватывать профилактику этих состояний/проблем здоровья в дальнейшей жизни. Термин «в дальнейшей жизни» охватывает влияние после прекращения вмешательства или лечения. Влияние «в дальнейшей жизни» может длиться от 1 недели до нескольких месяцев, например от 2 до 4 недель, от 2 до 6 недель, от 2 до 8 недель, от 1 до 6 месяцев или от 2 до 12 месяцев.
Выражения «в лечении запора/метеоризма/вздутия живота/колик/кишечного дискомфорта», «лечить запор/метеоризм/вздутие живота/колики/кишечный дискомфорт», «при лечении запора/метеоризма/вздутия живота/колик/кишечного дискомфорта» и «для лечения запора/метеоризма/вздутия живота/колик/кишечного дискомфорта» могут использоваться взаимозаменяемо.
Следует понимать, что они включают в себя уменьшение продолжительности этих состояний/проблем здоровья (запора/метеоризма/вздутия живота/колик/кишечного дискомфорта) (например, числа дней/недель/лет, в течение которых младенцы или дети младшего возраста будут страдать этими состояниями/проблемами здоровья), уменьшение выраженности (или уровня) этих состояний/проблем здоровья (например, последствий и/или серьезности этих состояний/проблем здоровья). Эти выражения также охватывают облегчение симптомов или последствий, таких как блокирование стула, периоды плача, затруднения при вскармливании, раздражительность, боль, особенно боль в животе, спазмы в животе, нарушение сна и любые их комбинации, и/или уменьшение осложнений состояния здоровья младенца или ребенка младшего возраста, вызванных этими состояниями/проблемами здоровья, таких как анальная трещина, ректальное кровотечение, необходимость в хирургическом вмешательстве, применение медикаментозной терапии, применение размягчителей стула, и/или уменьшение боли, и/или уменьшение утомляемости, и/или облегчение засыпания, и/или стабилизацию активности младенцев или детей младшего возраста, страдающих этими состояниями/проблемами здоровья.
Выражения «отсутствие или ограниченный уровень» и «отсутствие особых проблем» метеоризма, вздутия живота, колик и/или кишечного дискомфорта могут использоваться взаимозаменяемо. В контексте настоящего изобретения необходимо понимать, что младенцы или дети младшего возраста, которых вскармливают композицией настоящего изобретения, не будут страдать метеоризмом, вздутием живота, коликами и/или кишечным дискомфортом, либо уровень метеоризма, вздутия живота, колик и/или кишечного дискомфорта будет низким, либо у них будет меньше (например, по меньшей мере на 1% меньше или по меньшей мере на 2% меньше, или по меньшей мере на 5% меньше, или по меньшей мере на 10% меньше, или по меньшей мере на 20% меньше, или по меньшей мере на 50% меньше…) эпизодов метеоризма, вздутия живота, колик и/или кишечного дискомфорта по сравнению с младенцами или детьми младшего возраста, которых вскармливают стандартной композицией (т. е. такой же композицией, но не содержащей фукозилированных олигосахаридов). Выражения «ограниченный уровень» и «пониженный уровень» могут использоваться взаимозаменяемо. Они могут относиться к частоте и/или распространенности и/или выраженности.
Термины «кишечный», «КИШЕЧНИК» и «желудочно-кишечный» могут использоваться взаимозаменяемо.
Выражение «кишечный дискомфорт» включает в себя боль и/или спазмы в животе.
Выражения «в улучшении консистенции/частоты стула», «в улучшении консистенции и/или частоты стула» и «в улучшении консистенции стула и/или частоты стула» могут использоваться взаимозаменяемо. Они охватывают улучшение консистенции стула, улучшение частоты стула и/или обоих показателей. Выражение «улучшение консистенции стула» означает, что стул младенца или ребенка младшего возраста, которого вскармливают питательной композицией согласно изобретению, имеет более мягкую консистенцию, чем стул младенца или ребенка младшего возраста, которого не вскармливают питательной композицией согласно изобретению. Выражение «улучшение консистенции стула» может, в частности, охватывать или означать «уменьшение твердости стула», «размягчение стула» и/или «обеспечение более мягкого стула», например уменьшение количества твердых комков, похожих на орехи, которые с трудом проходят.
Выражение «улучшение частоты стула» означает, что стул у младенца или ребенка младшего возраста станет более частым, т.е. транзит станет регулируемым и/или ускорится. Это выражение, таким образом, может также охватывать или означать «улучшение/повышение скорости транзита» или «регулирование транзита». Улучшение консистенции/частоты стула может, в частности, позволить избежать боли, особенно боли в животе, спазмов в животе, а также дополнительных осложнений, таких как анальная трещина, ректальное кровотечение, необходимость в хирургическом вмешательстве, применение медикаментозной терапии, применение размягчителей стула.
Под «материнским молоком» следует понимать грудное молоко или молозиво матери.
«Олигосахарид» представляет собой сахаридный полимер, содержащий небольшое число (как правило, от трех до десяти) простых сахаров (моносахаридов).
Термин «ОГМ» относится к олигосахариду (-ам) грудного молока. Эти углеводы обладают высокой устойчивостью к ферментативному гидролизу, что указывает на то, что они могут проявлять основные функции, непосредственно не связанные с их калорийной ценностью. В первую очередь было показано, что они играют жизненно важную роль в раннем развитии младенцев и детей младшего возраста, например в развитии иммунной системы. В грудном молоке обнаружено много различных видов ОГМ. Каждый отдельный олигосахарид основан на комбинации глюкозы, галактозы, сиаловой кислоты (N-ацетилнейраминовой кислоты), фукозы и/или N-ацетилглюкозамина с образованием многочисленных и разнообразных связей между ними. Таким образом, это обусловливает присутствие огромного числа различных олигосахаридов в грудном молоке — на данный момент было выявлено более 130 таких структур. Почти все они имеют фрагмент лактозы на своем восстанавливающем конце, в то время как сиаловая кислота и/или фукоза (при наличии) занимают концевые положения на невосстанавливающих концах. ОГМ могут быть кислотными (например, содержащий заряженную сиаловую кислоту олигосахарид) или нейтральными (например, фукозилированный олигосахарид).
«Фукозилированный олигосахарид» представляет собой олигосахарид, имеющий остаток фукозы. Он имеет нейтральный характер. Некоторыми примерами являются 2-FL (2’-фукозиллактоза), 3-FL (3-фукозиллактоза), дифукозиллактоза, лакто-N-фукопентаоза (например, лакто-N-фукопентаоза I, лакто-N-фукопентаоза II, лакто-N-фукопентаоза III, лакто-N-фукопентаоза V), лакто-N-фукогексаоза, лакто-N-дифукогексаоза I, фукозиллакто-N-гексаоза, фукозиллакто-N-неогексаоза, дифукозиллакто-N-гексаоза I, дифукозиллакто-N-неогексаоза II и любая их комбинация.
Выражения «фукозилированные олигосахариды, содержащие 2’-фукозил-эпитоп» и «2-фукозилированные олигосахариды» охватывают фукозилированные олигосахариды с определенной гомологией формы, поскольку они содержат 2’-фукозил-эпитоп, следовательно, можно ожидать некоторую гомологию функции.
Выражение «N-ацетилированный (-ые) олигосахарид (-ы)» подразумевает как «N-ацетиллактозамин», так и «олигосахарид (-ы), содержащий (-ие) N-ацетиллактозамин». Они являются нейтральными олигосахаридами, имеющими остаток N-ацетиллактозамина. Подходящими примерами являются LNT (лакто-N-тетраоза), пара-лакто-N-неогексаоза (пара-LNnH), LNnT (лакто-N-неотетраоза) или любая их комбинация. Другими примерами являются лакто-N-гексаоза, лакто-N-неогексаоза, пара-лакто-N-гексаоза, пара-лакто-N-неогексаоза, лакто-N-октаоза, лакто-N- неооктаоза, изолакто-N-октаоза, пара-лакто-N-октаоза и лакто-N-декаоза.
«Предшественник ОГМ» представляет собой ключевое соединение, которое включается в выработку ОГМ, такое как сиаловая кислота и/или фукоза.
«Сиалилированный олигосахарид» представляет собой олигосахарид, содержащий заряженную сиаловую кислоту, т. е. олигосахарид, имеющий остаток сиаловой кислоты. Он имеет кислотный характер. Некоторыми примерами являются 3-SL (3’-сиалиллактоза) и 6-SL (6’-сиалиллактоза).
Питательная композиция настоящего изобретения может быть представлена в твердом (например, порошок) или жидком виде. Количество различных ингредиентов (например, олигосахаридов) может быть выражено в г/100 г композиции в расчете на массу сухого вещества, если композиция находится в твердой, например в порошкообразной, форме или в виде концентрации в г/л композиции, когда она относится к форме жидкости (последнее также охватывает жидкую композицию, которую можно получить из порошка после восстановления в жидкости, такой как молоко, вода и т. п., например восстановленную детскую смесь или смесь для прикармливаемых детей/смесь последующего уровня, или детский продукт на зерновой основе, или любую другую рецептуру, предназначенную для детского питания).
Термин «пребиотик» означает неперевариваемые углеводы, которые благоприятно влияют на организм хозяина, выборочно стимулируя рост и/или активность полезных для здоровья бактерий, например бифидобактерий, в толстом кишечнике человека (Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr. 1995;125:1401–12).
Термин «пробиотик» означает препараты из клеток микроорганизмов или компоненты клеток микроорганизмов, которые оказывают благоприятное воздействие на здоровье или состояние организма-хозяина (Salminen S, Ouwehand A. Benno Y. et al. Probiotics: how should they be defined Trends Food Sci. Technol. 1999:10 107–10). Клетки микроорганизмов обычно являются бактериями или дрожжами.
Под термином «КОЕ» следует понимать колониеобразующую единицу.
Если не указано иное, все приводимые процентные соотношения даются в массовых процентах.
Кроме того, в контексте изобретения термины «содержащий» или «содержит» не исключают других возможных элементов. Композиция настоящего изобретения, включая многие варианты осуществления, описанные в настоящем документе, может содержать существенные элементы и признаки изобретения, описанные в настоящем документе, а также любые дополнительные или используемые по выбору ингредиенты, компоненты или признаки изобретения, описанные в настоящем документе, или иные в зависимости от потребностей, состоять или, по существу, состоять из них.
Любую ссылку на документы предшествующего уровня техники в данном описании не следует рассматривать как признание того, что такой предшествующий уровень техники является широко известным или составляет часть общеизвестных знаний в области.
Далее изобретение будет описано более подробно. Следует отметить, что различные аспекты, признаки, примеры и варианты осуществления, описанные в настоящей заявке, могут быть совместимыми и/или комбинироваться друг с другом.
Таким образом, первым объектом настоящего изобретения является питательная композиция, содержащая по меньшей мере один фукозилированный олигосахарид, для применения в профилактике и/или лечении запора и/или в улучшении консистенции/частоты стула у младенца или ребенка младшего возраста.
В то же время питательная композиция может обеспечить отсутствие или ограниченный уровень метеоризма, вздутия живота, колик и/или кишечного дискомфорта у указанного младенца или ребенка младшего возраста.
Другим объектом настоящего изобретения является питательная композиция, содержащая по меньшей мере один фукозилированный олигосахарид, для применения в профилактике и/или лечении метеоризма, вздутия живота, колик и/или кишечного дискомфорта у младенца или ребенка младшего возраста, и при этом фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,8–1,5 г/л композиции и/или в общем количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества.
Не желая ограничиваться какой-либо теорией, авторы настоящего изобретения считают, что фукозилированный (-ые) олигосахарид (-ы) является (-ются) ключевым ингредиентом, который, как неожиданно обнаружено, обеспечивает упомянутые выше полезные для здоровья эффекты.
Не желая ограничиваться какой-либо теорией, авторы настоящего изобретения также считают, что наблюдаемый эффект опосредован изменением экосистемы кишечника, что, таким образом, косвенно влияет на консистенцию/частоту стула, перистальтику кишечника и в конечном счете кишечный дискомфорт.
В некоторых предпочтительных вариантах осуществления изобретения питательная композиция содержит по меньшей мере один пробиотический микроорганизм, предпочтительно по меньшей мере один пробиотический штамм. Не желая ограничиваться какой-либо теорией, авторы настоящего изобретения считают, что фукозилированный (-ые) олигосахарид (-ы) и пробиотический (-ие) микроорганизм (-ы) могут обладать синергическим действием, дополнительно обеспечивая упомянутые выше полезные для здоровья эффекты.
Композиция настоящего изобретения содержит по меньшей мере один фукозилированный олигосахарид. В ней может присутствовать один или несколько типов фукозилированных олигосахаридов. Фукозилированный (-ые) олигосахарид (-ы) можно выбирать из перечня, содержащего 2’-фукозиллактозу, 3’-фукозиллактозу, дифукозиллактозу, лакто-N-фукопентаозу (например, лакто-N-фукопентаозу I, лакто-N-фукопентаозу II, лакто-N-фукопентаозу III, лакто-N-фукопентаозу V), лакто-N-фукогексаозу, лакто-N-дифукогексаозу I, фукозиллакто-N-гексаозу, фукозиллакто-N-неогексаозу (например, фукозиллакто-N-неогексаозу I, фукозиллакто-N-неогексаозу II), дифукозиллакто-N-гексаозу I, дифуколакто-N-неогексаозу, дифукозиллакто-N-неогексаозу I, дифукозиллакто-N-неогексаозу II, фукозил-пара-лакто-N-гексаозу, три-фуко-пара-лакто-N-гексаозу I и любую их комбинацию.
В некоторых конкретных вариантах осуществления фукозилированный олигосахарид содержит 2’-фукозил-эпитоп. Он может быть, например, выбран из перечня, содержащего 2’-фукозиллактозу, дифукозиллактозу, лакто-N-фукопентаозу, лакто-N-фукогексаозу, лакто-N-дифукогексаозу, фукозиллакто-N-гексаозу, фукозиллакто-N-неогексаозу, дифукозиллакто-N-гексаозу дифуколакто-N-неогексаозу, дифукозиллакто-N-неогексаозу, фукозил-пара-лакто-N-гексаозу и любую их комбинацию.
В предпочтительном варианте осуществления питательная композиция в соответствии с изобретением содержит 2’-фукозиллактозу (или 2FL, или 2’FL, или 2-FL, или 2’-FL). В конкретном варианте осуществления другие типы фукозилированных олигосахаридов, кроме 2’-фукозиллактозы, отсутствуют, т. е. питательная композиция изобретения содержит в качестве фукозилированного олигосахарида только 2’-фукозиллактозу.
Фукозилированный (-ые) олигосахарид (-ы) может (могут) быть выделен (-ы) из природного источника, такого как молоко животных, методами хроматографии или фильтрации. В альтернативном варианте осуществления он может быть получен с помощью биотехнологических средств с использованием специфических фукозилтрансфераз и/или фукозидаз либо посредством применения метода ферментации на основе ферментов (рекомбинантных или природных ферментов), либо метода микробиологической ферментации. В последнем случае либо микроорганизмы могут экспрессировать свои природные ферменты и субстраты, либо возможно создание микроорганизмов, вырабатывающих соответствующие субстраты и ферменты. Можно использовать культуры из микроорганизмов одного вида и/или смешанные культуры. Образование фукозилированных олигосахаридов может быть инициировано акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP = 1 и далее. В альтернативном варианте осуществления фукозилированные олигосахариды можно получить с помощью химического синтеза из лактозы и свободной фукозы. Фукозилированные олигосахариды также доступны в продаже, например, производства компании Kyowa Hakko Kogyo, Япония.
Фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в соответствии с настоящим изобретением в общем количестве 0,2–3 г/л, например 0,5–2 г/л или 0,75–1,65 г/л композиции. В некоторых вариантах осуществления фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в общем количестве 0,8–1,5 г/л композиции, например 0,85–1,3 г/л или 0,9–1,25 г/л, или 0,9–1,1 г/л, или 1–1,25 г/л, или 1,05–1,25 г/л композиции. В конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 1 г/л композиции. В другом конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 1,24 г/л композиции.
Фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в общем количестве 0,13–2,1 г/100 г, например 0,34–1,4 г/100 г или 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества. Фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в общем количестве 0,55–1,05 г/100 г композиции, например 0,59–0,9 г/100 г, или 0,62–0,87 г/100 г, или 0,62–0,77 г/100 г, или 0,69–0,87 г/100 г, или 0,73–0,87 г/100 г композиции. В конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,69 г/100 г композиции. В другом конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,86 г/100 г композиции.
Питательная композиция в соответствии с настоящим изобретением может также содержать по меньшей мере другой (-ие) олигосахарид (-ы) (т. е. отличающийся (-иеся) от фукозилированного (-ых) олигосахарида (-ов), обязательно присутствующего (-их) в композиции) и/или по меньшей мере клетчатку (виды клетчатки) и/или по меньшей мере ее предшественник (-и). Другой олигосахарид и/или клетчатку и/или ее предшественник можно выбирать из перечня, содержащего галактоолигосахариды (ГОС), фруктоолигосахариды (ФОС), инулин, ксилоолигосахариды (КОС), полидекстрозу, N-ацетилированные олигосахариды, сиалилированные олигосахариды, сиаловую кислоту, фукозу и любую их комбинацию. Они могут присутствовать в количестве от 0 до 10 мас.% композиции.
Подходящие доступные на рынке продукты, которые можно применять дополнительно к олигосахаридам, содержащимся в смеси олигосахаридов, для получения питательных композиций в соответствии с изобретением, включают в себя комбинации ФОС с инулином, такие как продукты, продаваемые компанией BENEO под товарным знаком Orafti, или полидекстрозу, продаваемую компанией Tate & Lyle под товарным знаком STA-LITE®.
В некоторых конкретных вариантах осуществления питательная композиция настоящего изобретения может также содержать по меньшей мере один N-ацетилированный олигосахарид. В ней может присутствовать один или несколько N-ацетилированных олигосахаридов. N-ацетилированный (-ые) олигосахарид (-ы) может (могут) представлять собой, например, лакто-N-тетраозу (LNT), лакто-N-неотетраозу (LNnT) или любую их комбинацию. В некоторых конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой лакто-N-неотетраозу (LNnT), пара-лакто-N-неогексаозу (пара-LNnH) или любую их комбинацию. В некоторых конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой LNnT. В некоторых конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой LNT. В некоторых других конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой смесь LNT и LNnT. В некоторых конкретных вариантах осуществления композиция содержит как LNT, так и LNnT в соотношении LNT : LNnT между 5 : 1 и 1 : 2 или от 2 : 1 до 1 : 1, или от 2 : 1,2 до 2 : 1,6.
N-ацетилированный (-ые) олигосахарид (-ы) можно синтезировать химическим путем с помощью ферментативного переноса сахаридных единиц с донорных фрагментов на акцепторные фрагменты с использованием гликозилтрансфераз, как описано, например, в патентах США № 5,288,637 и WO 96/10086. В альтернативном варианте осуществления LNT и LNnT можно получить путем химического преобразования кетогексоз (например, фруктозы), либо свободных, либо связанных с олигосахаридом (например, лактулозы), в N-ацетилгексозамин или N-ацетилгексозамин-содержащий олигосахарид, как описано в работе Wrodnigg, T.M.; Stutz, A.E. (1999) Angew. Chem. Int. Ed. 38:827–828. N-ацетиллактозамин, полученный таким образом, можно впоследствии переносить в качестве акцепторного фрагмента на лактозу.
N-ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в соответствии с настоящим изобретением в общем количестве 0,1– 2 г/л, например 0,3–1 г/л или 0,45–0,85 г/л композиции.
В некоторых вариантах осуществления N-ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в общем количестве 0,5–0,8 г/л композиции, например 0,5–0,75 г/л или 0,5–0,7 г/л композиции. В конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,5 г/л композиции. В другом конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,63 г/л композиции.
N-ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в общем количестве 0,06–1,4 г/100 г, например 0,2–0,7 г/100 г или 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества. N-ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в общем количестве 0,35–0,56 г/100 г композиции, например 0,35–0,52 г/100 г или 0,35–0,49 г/100 г. В конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,35 г/100 г композиции. В другом конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (ы) присутствует (-ют) в общем количестве 0,44 г/100 г композиции.
В некоторых вариантах осуществления питательная композиция содержит как 2’-фукозиллактозу (2-FL), так и лакто-N-неотетраозу (LNnT). В другом конкретном варианте осуществления питательная композиция настоящего изобретения содержит смесь олигосахаридов, состоящую из 2’-фукозиллактозы (2-FL) и лакто-N-неотетраозы (LNnT). Иными словами, питательная композиция изобретения содержит только 2’-фукозиллактозу (2-FL) в качестве фукозилированного олигосахарида и только лакто-N-неотетраозу (LNnT) в качестве N-ацетилированного олигосахарида.
Питательная композиция может содержать фукозилированный (-ые) олигосахарид (-ы) и N-ацетилированный (-ые) олигосахарид (-ы) в соотношении фукозилированный (-ые) олигосахарид (-ы) : N-ацетилированный (-ые) олигосахарид (-ы) от 2 : 0,065 до 2 : 20, например от 2 : 0,3 до 2 : 4, например от 2 : 0,54 до 2 : 2,26 или 2 : 0,76 – 2 : 1,8, или 2 : 0,8 – 2 : 1,4. В особенно преимущественном варианте осуществления это соотношение составляет 2 : 1 или около 2 : 1.
В некоторых других конкретных вариантах осуществления питательная композиция в соответствии с изобретением вообще не содержит N-ацетилированных олигосахаридов.
В конкретном варианте осуществления композиция в соответствии с изобретением может содержать сиалилированный (-ые) олигосахарид (-ы). В ней может присутствовать один или несколько сиалилированных олигосахаридов.
Сиалилированный (-ые) олигосахарид (-ы) может (могут) быть выбран (-ы) из группы, содержащей 3’-сиалиллактозу (3-SL), 6’-сиалиллактозу (6-SL) и любую их комбинацию. В некоторых вариантах осуществления изобретения композиция содержит 3-SL и 6-SL. В некоторых конкретных вариантах осуществления соотношение 3'-сиалиллактозы (3-SL) и 6'-сиалиллактозы (6-SL) может находиться в диапазоне между 5 : 1 и 1 : 10 или от 3 : 1 до 1 : 1, или от 1 : 1 до 1 : 10.
В некоторых конкретных вариантах осуществления сиалилированный олигосахарид композиции представляет собой 6'-сиалиллактозу (6-SL).
Сиалилированный (-ые) олигосахарид (-ы) может (могут) быть выделен (-ы) из природного источника, такого как молоко животных, методами хроматографии или фильтрации. В альтернативном варианте осуществления их можно получить с помощью биотехнологических средств с использованием специфических сиалилтрансфераз или сиалидаз, нейраминидаз посредством метода ферментации на основе ферментов (рекомбинантных или природных ферментов), путем химического синтеза или метода микробиологической ферментации. В последнем случае либо микроорганизмы могут экспрессировать свои природные ферменты и субстраты, либо могут быть созданы микроорганизмы, вырабатывающие соответствующие субстраты и ферменты. Можно применять культуры микроорганизмов одного вида или смешанные культуры. Образование сиалилолигосахаридов может быть инициировано акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP = 1 и далее. В альтернативном варианте осуществления сиалиллактозы можно получить путем химического синтеза из лактозы и свободной N’-ацетилнейраминовой кислоты (сиаловой кислоты). Сиалиллактозы также имеются в продаже, например, производства компании Kyowa Hakko Kogyo, Япония.
В конкретных примерах композиция может содержать от 0,05 до 5 г/л сиалилированного (-ых) олигосахарида (-ов) или от 0,1 до 4 г/л, или от 0,3 до 2 г/л, или от 0,4 до 1,5 г/л, или от 0,4 до 1 г/л, например 0,5 или 0,9 г/л сиалилированного (-ых) олигосахарида (-ов). В некоторых конкретных вариантах осуществления композиция может содержать от 0,8 до 1,7 г/л сиалилированного (-ых) олигосахарида (-ов).
Композиция в соответствии с изобретением может содержать от 0,03 до 3,5 г сиалилированного (-ых) олигосахарида (-ов) на 100 г композиции в расчете на массу сухого вещества, например от 0,1 до 2 г или от 0,2 до 1 г, или от 0,3 до 0,6 г сиалилированного (-ых) олигосахарида (-ов) на 100 г композиции в расчете на массу сухого вещества.
В некоторых конкретных вариантах осуществления настоящего изобретения питательная композиция содержит сиалилированный (-ые) олигосахарид (-ы) в количестве менее 0,1 г/100 г композиции в расчете на массу сухого вещества.
В некоторых конкретных вариантах осуществления настоящего изобретения питательная композиция вообще не содержит сиалилированных олигосахаридов.
В некоторых других конкретных вариантах осуществления настоящего изобретения питательная композиция вообще не содержит галактоолигосахаридов (ГОС).
В конкретном варианте осуществления питательная композиция может также содержать по меньшей мере один BMO (олигосахарид из коровьего молока). В другом конкретном варианте осуществления питательная композиция вообще не содержит олигосахаридов из коровьего молока.
Композиция в соответствии с настоящим изобретением может также необязательно содержать по меньшей мере один предшественник олигосахарида. В ней может присутствовать один или несколько предшественников олигосахарида. Например, предшественником олигосахарида грудного молока является сиаловая кислота, фукоза или их смесь. В некоторых конкретных вариантах осуществления композиция содержит сиаловую кислоту.
В конкретных примерах композиция содержит от 0 до 3 г/л предшественника (-ов) олигосахарида или от 0 до 2 г/л, или от 0 до 1 г/л, или от 0 до 0,7 г/л, или от 0 до 0,5 г/л, или от 0 до 0,3 г/л, или от 0 до 0,2 г/л предшественника (-ов) олигосахарида.
Композиция в соответствии с изобретением может содержать от 0 до 2,1 г предшественника (-ов) олигосахарида на 100 г композиции в расчете на массу сухого вещества, например от 0 до 1,5 г или от 0 до 0,8 г, или от 0 до 0,15 г предшественника (ов) олигосахарида на 100 г композиции в расчете на массу сухого вещества.
В предпочтительном варианте осуществления питательная композиция настоящего изобретения может дополнительно содержать по меньшей мере один пробиотический микроорганизм, такой как пробиотический бактериальный штамм.
Наиболее часто используемые пробиотические микроорганизмы представляют собой главным образом бактерии и дрожжи следующих родов: Lactobacillus spp., Streptococcus spp., Enterococcus spp., Bifidobacterium spp. и Saccharomyces spp.
В некоторых конкретных вариантах осуществления пробиотик представляет собой пробиотический бактериальный штамм. В некоторых конкретных вариантах осуществления он представляет собой, в частности, штамм Lactobacilli. В предпочтительном варианте осуществления питательная композиция содержит по меньшей мере один штамм Lactobacillus.
Подходящие пробиотические бактериальные штаммы включают Lactobacillus rhamnosus, ATCC 53103, от компании Valio Oy, Финляндия, под торговой маркой LGG; Lactobacillus rhamnosus, CGMCC 1.3724, Lactobacillus paracasei, CNCM I-2116, Lactobacillus johnsonii, CNCM I-1225, Streptococcus salivarius, DSM 13084, продаваемые компанией BLIS Technologies Limited, Новая Зеландия, под названием KI2; Bifidobacterium lactis, CNCM 1-3446, продаваемый в числе прочих компанией Christian Hansen, Дания, под торговой маркой Bb 12; Bifidobacterium longum, ATCC BAA-999, продаваемый компанией Morinaga Milk Industry Co. Ltd., Япония, под торговой маркой BB536; Bifidobacterium breve, продаваемый компанией Danisco под торговой маркой Bb-03; Bifidobacterium breve, продаваемый компанией Morinaga под торговой маркой M-16V; Bifidobacterium infantis, продаваемый компанией Procter & Gamble Co. под торговой маркой Bifantis; и Bifidobacterium breve, продаваемый компанией Institut Rosell (г. Лаллеманд) под торговой маркой R0070.
Питательная композиция в соответствии с изобретением может содержать от 103 до 1012 КОЕ пробиотического штамма, более предпочтительно от 107 до 1012 КОЕ, например от 108 до 1010 КОЕ пробиотического штамма на грамм композиции в пересчете на массу сухого вещества.
В одном варианте осуществления пробиотики являются жизнеспособными. В другом варианте осуществления пробиотики являются неразмножающимися или инактивированными. В некоторых других вариантах осуществления могут использоваться жизнеспособные пробиотики и инактивированные пробиотики.
Питательная композиция изобретения может дополнительно содержать по меньшей мере один фаг (бактериофаг) или смесь фагов, предпочтительно направленных против патогенных микроорганизмов родов Streptococci, Haemophilus, Moraxella и Staphylococci.
Питательная композиция в соответствии с изобретением может представлять собой, например, детскую смесь, начальную детскую смесь, смесь для прикармливаемых детей или смесь последующего уровня, детское питание, детскую композицию на зерновой основе, обогатитель, такой как обогатитель грудного молока, или добавку. В некоторых вариантах осуществления композиция изобретения представляет собой детскую смесь, обогатитель или добавку, предназначенные для первых 4 или 6 месяцев жизни. В предпочтительном варианте осуществления питательная композиция изобретения представляет собой детскую смесь.
В некоторых других вариантах осуществления питательная композиция настоящего изобретения представляет собой обогатитель. Обогатитель может представлять собой обогатитель грудного молока (например, обогатитель человеческого грудного молока) или обогатитель смеси, такой как обогатитель детской смеси или обогатитель смеси для прикармливаемых детей/смеси последующего уровня.
Когда питательная композиция является добавкой, ее можно предоставлять в виде стандартных доз.
Питательная композиция настоящего изобретения может быть представлена в твердой (например, порошок), жидкой или желеобразной форме.
Питательная композиция в соответствии с изобретением, по существу, содержит источник белков. Белок может содержаться в количестве от 1,6 до 3 г на 100 ккал. В некоторых вариантах осуществления, в частности, когда композиция предназначена для преждевременно родившихся младенцев, количество белка может составлять от 2,4 до 4 г/100 ккал или более 3,6 г/100 ккал. В некоторых других вариантах осуществления количество белка может быть ниже 2,0 г на 100 ккал, например от 1,8 до 2 г/100 ккал, или в количестве ниже 1,8 г на 100 ккал.
Тип белка не считается критическим для настоящего изобретения при условии, что соблюдены минимальные требования по содержанию незаменимых аминокислот и обеспечивается удовлетворительной рост. Таким образом, можно использовать источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается белков молочной сыворотки, источник белка может быть основан на кислой сыворотке или сладкой сыворотке, или их смесях, и может включать альфа-лактальбумин и бета-лактоглобулин в любых желаемых соотношениях.
В некоторых преимущественных вариантах осуществления в источнике белка преобладает молочная сыворотка (т. е. более 50% белков происходят из белков молочной сыворотки, например 60% или 70%).
Белки могут быть нативными или гидролизованными или могут представлять собой смесь нативных и гидролизованных белков. Под термином «нативный» подразумевается, что основная часть белков нативна, т. е. их молекулярная структура не изменена, например не изменено по меньшей мере 80% белков, например не изменено по меньшей мере 85% белков, предпочтительно не изменено по меньшей мере 90% белков, еще более предпочтительно не изменено по меньшей мере 95% белков, например не изменено по меньшей мере 98% белков. В конкретном варианте осуществления не изменено 100% белков.
Термин «гидролизованный» в контексте настоящего изобретения означает белок, который был гидролизован или расщеплен на составляющие его аминокислоты.
Белки могут быть полностью или частично гидролизованными. Может быть желательно вводить частично гидролизованные белки (степень гидролиза от 2 до 20%), например, младенцам или детям младшего возраста, предположительно подверженным риску развития аллергии на коровье молоко. При необходимости использования гидролизованных белков процесс гидролиза может проводиться по желанию и так, как известно в данной области. Например, гидролизаты белка молочной сыворотки можно получить ферментативным гидролизом фракции молочной сыворотки в одну или более стадий. Если фракция молочной сыворотки, которая используется в качестве исходного материала, по существу, не содержит лактозы, то установлено, что в процессе гидролиза блокировка лизина белка проявляется в гораздо меньшей степени. Это позволяет снизить степень блокады лизина с приблизительно 15 мас.% общего лизина до менее приблизительно 10 мас.% лизина; например приблизительно 7 мас.% лизина, что значительно улучшает питательное качество источника белка.
В одном варианте осуществления изобретения гидролизовано по меньшей мере 70% белков, гидролизовано предпочтительно по меньшей мере 80% белков, например гидролизовано по меньшей мере 85% белков, еще более предпочтительно гидролизовано по меньшей мере 90% белков, например гидролизовано по меньшей мере 95% белков, в частности гидролизовано по меньшей мере 98% белков. В конкретном варианте осуществления гидролизовано 100% белков.
В одном конкретном варианте осуществления белки питательной композиции гидролизованы, полностью гидролизованы или частично гидролизованы. Степень гидролиза (DH) белка может составлять от 8 до 40, либо от 20 до 60, либо от 20 до 80, либо более 10, 20, 40, 60, 80 или 90.
В другом конкретном варианте осуществления питательная композиция в соответствии с изобретением представляет собой гипоаллергенную композицию. В другом конкретном варианте осуществления композиция в соответствии с изобретением представляет собой гипоаллергенную питательную композицию.
Питательная композиция в соответствии с настоящим изобретением, по существу, содержит источник углеводов. Это особенно предпочтительно в том случае, когда питательная композиция изобретения представляет собой детскую смесь. В этом случае можно применять любой источник углеводов, традиционно находящийся в детских смесях, такой как лактоза, сукроза, сахароза, мальтодекстрин, крахмал и их смеси, хотя одним из предпочтительных источников углеводов является лактоза.
Питательная композиция в соответствии с настоящим изобретением обычно содержит источник липидов. Это особенно важно, если питательная композиция изобретения представляет собой детскую смесь. В этом случае источником липидов может быть любой липид или жир, который подходит для применения в детских смесях. Некоторые подходящие источники жира включают пальмовое масло, подсолнечное масло с высоким содержанием олеиновой кислоты и сафлоровое масло с высоким содержанием олеиновой кислоты. Также можно добавлять незаменимые жирные кислоты — линоленовую кислоту и α-линоленовую кислоту, а также небольшие количества масел, содержащих большие количества арахидоновой кислоты и докозагексаеновой кислоты в готовом виде, например рыбьи жиры или микробные масла. Соотношение жирных кислот n-6 и n-3 в источнике жиров может составлять от приблизительно 5 : 1 до приблизительно 15 : 1; например от приблизительно 8 : 1 до приблизительно 10 : 1.
Питательная композиция изобретения может также содержать все витамины и минералы, которые считаются обязательными в повседневном пищевом рационе, в значимых с точки зрения питания количествах. Для некоторых витаминов и минеральных веществ установлены минимальные требования. Примеры минеральных веществ, витаминов и других питательных веществ, необязательно присутствующих в композиции изобретения, включают витамин А, витамин В1, витамин В2, витамин В6, витамин В12, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту, инозит, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлор, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно добавляют в форме соли. Присутствие и количества конкретных минеральных веществ и других витаминов будут варьироваться в зависимости от предполагаемой популяции.
При необходимости питательная композиция изобретения может содержать эмульгаторы и стабилизаторы, такие как соя, лецитин, сложноэфирные моно- и диглицериды лимонной кислоты и т. п.
Питательная композиция изобретения может также содержать другие вещества, которые могут оказывать благоприятное воздействие, такие как лактоферрин, нуклеотиды, нуклеозиды и т. п.
Питательная композиция изобретения может также содержать каротиноид (-ы). В некоторых конкретных вариантах осуществления изобретения питательная композиция изобретения вообще не содержит каротиноид.
Питательную композицию в соответствии с изобретением можно получить любым подходящим способом. Далее композиция будет описана на примере.
Например, смесь, такую как детская смесь, можно получать путем смешивания источника белков, источника углеводов и источника жиров в соответствующих пропорциях. На данном этапе можно включать эмульгаторы в случае их использования. На данном этапе можно добавлять витамины и минералы, но обычно их добавляют позднее для предотвращения термического разложения. Перед перемешиванием в источнике жира можно растворять любые липофильные витамины, эмульгаторы и т. п. Затем можно примешивать воду, предпочтительно воду, очищенную обратным осмосом, с образованием жидкой смеси. Температура воды для удобства находится в диапазоне от приблизительно 50 °C до приблизительно 80 °C, чтобы облегчить диспергирование ингредиентов. Для образования жидкой смеси можно использовать доступные в продаже разжижители.
На этом этапе можно добавлять фукозилированный (-ые) олигосахарид (-ы), особенно если конечный продукт должен иметь жидкую форму. Если конечный продукт должен представлять собой порошок, при необходимости их также можно добавить на данном этапе.
Затем жидкую смесь гомогенизируют, например, в две стадии.
Затем жидкую смесь можно термически обрабатывать для снижения бактериальной нагрузки путем быстрого нагрева жидкой смеси, например до температуры в диапазоне от приблизительно 80°C до приблизительно 150°C, в течение периода времени, например от приблизительно 5 секунд до приблизительно 5 минут. Это можно осуществлять путем нагнетания пара, с помощью автоклава или теплообменника, например пластинчатого теплообменника.
Затем жидкую смесь можно охлаждать до температуры от приблизительно 60 °C до приблизительно 85 °C, например путем мгновенного охлаждения. Затем жидкую смесь можно снова гомогенизировать, например, двухэтапно: под давлением в диапазоне от приблизительно 10 МПа до приблизительно 30 МПа на первом этапе и от приблизительно 2 МПа до приблизительно 10 МПа на втором этапе. Затем гомогенизированную смесь можно дополнительно охлаждать для добавления любых термочувствительных компонентов, таких как витамины и минералы. На данном этапе для удобства регулируют рН и содержание твердых веществ в гомогенизированной смеси.
Если конечный продукт должен представлять собой порошок, гомогенизированную смесь переносят в подходящий сушильный аппарат, такой как распылительная сушилка или сублимационная сушилка, и превращают в порошок. Влагосодержание порошка должно составлять менее приблизительно 5 мас.%. Также на этом этапе или альтернативно можно добавить фукозилированный (-ые) олигосахарид (-ы) путем сухого смешивания или путем перемешивания их в форме сиропа из кристаллов, вместе с пробиотическим (-ими) штаммом (-ами) (при использовании), и смесь подвергают распылительной сушке или сублимационной сушке.
Если предпочтительна жидкая композиция, гомогенизированную смесь можно стерилизовать, а затем асептически разливать в подходящие контейнеры или можно сначала разливать в контейнеры, а затем стерилизовать в автоклаве.
В другом варианте осуществления композиция изобретения может представлять собой добавку.
Добавка может быть, например, в форме таблеток, капсул, пастилок или жидкости. Добавка может дополнительно содержать защитные гидроколлоиды (такие как камеди, белки, модифицированные крахмалы), связующие вещества, пленкообразующие агенты, инкапсулирующие агенты/материалы, материалы стенок/оболочек, матричные соединения, покрытия, эмульгаторы, поверхностно-активные агенты, солюбилизирующие агенты (масла, жиры, воски, лецитины и т. п.), адсорбенты, носители, наполнители, вспомогательные соединения, диспергирующие агенты, увлажняющие агенты, технологические добавки (растворители), антислеживающие агенты, маскирующие вкус агенты, утяжеляющие агенты, желирующие агенты и гелеобразующие агенты. Добавка может также содержать традиционные фармацевтические добавки и адъюванты, эксципиенты и разбавители, включая, без ограничений, воду, желатин любого происхождения, растительные камеди, лигнинсульфонат, тальк, сахара, крахмал, гуммиарабик, растительные масла, полиалкиленгликоли, ароматизирующие агенты, консерванты, стабилизаторы, эмульгирующие агенты, буферы, смазывающие вещества, красители, увлажняющие агенты, наполнители и т. п.
Кроме того, добавка может содержать органический или неорганический материал-носитель, подходящий для перорального или парентерального введения, а также витамины, минералы, микроэлементы и другие питательные микроэлементы в соответствии с рекомендациями государственных органов, такими как рекомендуемые нормы потребления (RDA) США.
Питательная композиция в соответствии с изобретением предназначена для применения у младенцев или детей младшего возраста. Младенцы или дети младшего возраста могли родиться доношенными или недоношенными. В конкретном варианте осуществления питательная композиция изобретения предназначена для применения у младенцев или детей младшего возраста, которые также являются недоношенными. В конкретном варианте осуществления питательная композиция изобретения предназначена для применения у недоношенных младенцев.
Питательную композицию настоящего изобретения можно также применять у младенца или ребенка младшего возраста, который родился с помощью кесарева сечения или посредством вагинальных родов.
В некоторых вариантах осуществления композиция в соответствии с изобретением может быть предназначена для применения до и/или во время периода отлучения от груди.
Возраст для требующей введения (вскармливания или питания) питательной композиции, а также продолжительность такого введения может зависеть от потребностей. Питательную композицию настоящего изобретения можно применять в целях профилактики или лечения:
- в профилактике и/или лечении запора у младенца или ребенка младшего возраста;
- в улучшении консистенции стула у младенца или ребенка младшего возраста, например в уменьшении твердости стула у указанного младенца или ребенка младшего возраста;
- в улучшении частоты стула у младенца или ребенка младшего возраста, например в регулировании/ускорении транзита у указанного младенца или ребенка младшего возраста;
- в профилактике и/или лечении метеоризма, вздутия живота, колик и/или кишечного дискомфорта у младенца или ребенка младшего возраста.
В некоторых вариантах осуществления питательную композицию применяют в целях профилактики. Питательную композицию можно давать, например, сразу после рождения младенцев. Композицию изобретения также можно давать в течение первой недели жизни младенца или в течение первых 2 недель жизни, или в течение первых 3 недель жизни, или в течение первого месяца жизни, или в течение первых 2 месяцев жизни, или в течение первых 3 месяцев жизни, или в течение первых 4 месяцев жизни, или в течение первых 6 месяцев жизни, или в течение первых 8 месяцев жизни, или в течение первых 10 месяцев жизни, или в течение первого года жизни, или в течение первых двух лет жизни, или даже дольше. В некоторых особенно преимущественных вариантах осуществления изобретения питательную композицию дают (или вводят) младенцу в течение первых 4 или 6 месяцев после рождения указанного младенца.
В некоторых других вариантах осуществления питательную композицию изобретения дают несколько дней (например, 1, 2, 3, 5, 10, 15, 20...) или несколько недель (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10...), или несколько месяцев (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10...) после рождения. В первую очередь это может быть актуально, но не обязательно, в том случае, когда младенец родился преждевременно.
В одном варианте осуществления композицию изобретения дают младенцу или ребенку младшего возраста в качестве композиции, дополнительной к материнскому молоку. В некоторых вариантах осуществления младенец или ребенок младшего возраста получает материнское молоко в течение по меньшей мере первых 2 недель, первых 1, 2, 4 или 6 месяцев. В одном варианте осуществления питательную композицию изобретения дают младенцу или ребенку младшего возраста после такого периода питания материнским молоком или дают во время такого периода питания материнским молоком. В другом варианте осуществления изобретения композицию дают младенцу или ребенку младшего возраста в качестве единственной или основной питательной композиции в течение по меньшей мере одного периода времени, например после 1, 2 или 4-го месяца жизни, в течение по меньшей мере 1, 2, 4 или 6 месяцев.
В одном варианте осуществления питательная композиция изобретения является полной питательной композицией (удовлетворяющей все или большинство питательных потребностей субъекта). В другом варианте осуществления питательная композиция является добавкой или обогатителем, предназначенным, например, для дополнения грудного молока или дополнения детской смеси или смеси для прикармливаемых детей.
В некоторых других вариантах осуществления питательную композицию изобретения дают в целях лечения, например при применении композиции для лечения запора. В этих случаях питательную композицию изобретения можно давать в зависимости от потребностей в течение нескольких дней (1, 2, 3, 4, 5, 6...) или в течение нескольких недель (1, 2, 3, 4, 5, 6, 7, 8 или даже более), или в течение нескольких месяцев (1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или даже более). Ее можно давать сразу, как только появились симптомы или как только диагностированы эти заболевания/состояния. Ее можно давать до исчезновения симптомов заболеваний/состояний, которые лечат, или в течение нескольких дней/недель/месяцев после указанного исчезновения.
В некоторых вариантах осуществления полезные для здоровья эффекты/действия наблюдают в течение первых нескольких недель или месяцев жизни и/или в течение первых нескольких недель или месяцев после введения питательной композиции, например в течение первой недели, первых 2 недель, первого месяца, первых 2 месяцев, первых 4 месяцев или первых 6 месяцев. Действия в течение более длительного срока могут быть менее значительными. В некоторых вариантах осуществления питательная композиция в соответствии с настоящим изобретением предназначена для применения в улучшении консистенции/частоты стула у младенца в течение первого месяца или первых 2 месяцев жизни и/или после введения питательной композиции. В некоторых других вариантах осуществления питательная композиция в соответствии с настоящим изобретением предназначена для применения в профилактике и/или лечении колик у младенцев в течение первого месяца, первых 2 месяцев или первых 4 месяцев жизни и/или после введения питательной композиции, особенно у младенцев, родившихся с помощью кесарева сечения.
Авторы настоящего изобретения обнаружили, что конкретная питательная композиция в соответствии с изобретением особенно эффективно уменьшает твердость стула у младенцев или детей младшего возраста. Питательная композиция была также особенно эффективна в отношении метеоризма, вздутия живота, колик и кишечного дискомфорта, поскольку они не наблюдались или наблюдались на ограниченном уровне у указанного младенца или ребенка младшего возраста.
В конкретном аспекте настоящее изобретение также относится к питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид, для применения в уменьшении твердости стула у младенца или ребенка младшего возраста, в частности без (т. е. в отсутствие или с ограниченным уровнем) сопутствующего метеоризма, вздутия живота, колик или кишечного дискомфорта.
Другие объекты
Другим объектом настоящего изобретения является применение по меньшей мере одного фукозилированного олигосахарида в приготовлении питательной композиции для профилактики и/или лечения запора и/или для улучшения консистенции/частоты стула у младенца или ребенка младшего возраста.
Другим объектом настоящего изобретения является применение по меньшей мере одного фукозилированного олигосахарида в приготовлении питательной композиции для профилактики и/или лечения метеоризма, вздутия живота, колик и/или кишечного дискомфорта у младенца или ребенка младшего возраста, причем фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,8–1,5 г/л композиции и/или в общем количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества.
Другим объектом настоящего изобретения является применение по меньшей мере одного фукозилированного олигосахарида для улучшения консистенции/частоты стула у младенца или ребенка младшего возраста.
Другим объектом настоящего изобретения является применение по меньшей мере одного фукозилированного олигосахарида для уменьшения метеоризма, для уменьшения вздутия живота, для уменьшения колик и/или для облегчения кишечного дискомфорта у младенца или ребенка младшего возраста, причем фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,8–1,5 г/л композиции и/или в общем количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества.
Упомянутые выше варианты осуществления и примеры (например, относящиеся к типам и количествам олигосахарида, питательной композиции, введению, целевой популяции...) также применимы к этим объектам (т.е. к вариантам их применения).
Другим объектом настоящего изобретения является фармацевтическая композиция, содержащая по меньшей мере один фукозилированный олигосахарид, для профилактики и/или лечения запора и/или для улучшения консистенции/частоты стула, и/или для профилактики и/или лечения метеоризма, вздутия живота, колик и/или кишечного дискомфорта у младенца или ребенка младшего возраста.
Упомянутые выше варианты осуществления и примеры (например, относящиеся к типам и количествам олигосахарида, введению, целевой популяции...) также применимы к этому объекту (т. е. к фармацевтической композиции).
Другой объект настоящего изобретения относится к способу профилактики и/или лечения запора и/или улучшения консистенции/частоты стула у младенца или ребенка младшего возраста, включающему введение указанному младенцу или ребенку младшего возраста питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид.
Другим объектом настоящего изобретения является способ профилактики и/или лечения метеоризма, вздутия живота, колик и/или кишечного дискомфорта у младенца или ребенка младшего возраста, включающий введение указанному младенцу или ребенку младшего возраста питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид, причем фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,8–1,5 г/л композиции и/или в общем количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества.
Различные варианты осуществления, подробные описания и примеры, описанные выше в спецификации (например, относящиеся к типам и количествам олигосахарида, питательной композиции, введению, целевой популяции...), также применимы к этим объектам (т.е. к способам).
Примеры
Следующие примеры показывают некоторые конкретные варианты осуществления композиции для применения в соответствии с настоящим изобретением. Примеры приведены исключительно в целях иллюстрации, и их не следует истолковывать как ограничивающие настоящее изобретение.
Пример 1
Ниже в таблице 1 приведен пример состава питательной композиции (например, детской смеси) в соответствии с настоящим изобретением. Эта композиция приведена только в качестве иллюстрации.
Таблица 1. Пример состава питательной композиции (например, детской смеси) в соответствии с настоящим изобретением
Пример 2
Описание исследования
Было проведено контролируемое, односторонне слепое, рандомизированное, многоцентровое, интервенционное клиническое исследование в 2 группах параллельно. Младенцев набирали в исследование и рандомизировали в одну из 2 исследуемых групп в пределах 14 дней после рождения. Исследуемые группы состояли из классической начальной детской смеси, не содержащей ОГМ [контроль], или той же классической начальной детской смеси с добавлением 2 ОГМ [ОГМ]. Композиция исследуемой детской смеси с добавлением или без добавления ОГМ была эквивалентна композиции, представленной в таблице 1, за исключением того, что:
- контрольная детская смесь не содержала олигосахаридов/ОГМ (т. е. не содержала 2’-фукозиллактозу и не содержала лакто-N-неотетраозу);
- исследуемая детская смесь с ОГМ содержала 2’-фукозиллактозу, но в количестве 1,24 г/л (соответствующем количеству 0,86 г/100 г порошка до восстановления; при восстановлении добавляли 129,18 г порошка на 900 мл), и лакто-N-неотетраозу, но в количестве 0,63 г/л (соответствующем 0,44 г/100 г порошка до восстановления; при восстановлении добавляли 129,18 г порошка на 900 мл).
Введение смесей для докорма после отъема от груди начинали с 4 месяцев.
Исследование состояло из периода введения одного из двух видов композиции в течение 6 месяцев ± 7 дней и периода последующего наблюдения без введения композиции в течение 6 месяцев.
Результаты
Авторы изобретения неожиданно наблюдали, что у младенцев из группы ОГМ (т. е. тех, которых вскармливали классической детской смесью с добавлением 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы) стул был менее твердым, как в возрасте 1 месяца (фиг. 1A), так и в возрасте 2 месяцев (фиг. 1B). В то же время об особых проблемах, связанных с метеоризмом, вздутием живота, коликами и кишечным дискомфортом, у указанного младенца или ребенка младшего возраста не сообщали.
В частности, у младенцев, родившихся с помощью кесарева сечения, которых вскармливали ОГМ, также наблюдался значимо пониженный уровень колик в возрасте 4 месяцев, см. фиг. 2.
Таким образом, композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, обладает высокой эффективностью для применения у младенцев в улучшении консистенции стула и, следовательно, в улучшении частоты стула, в профилактике и/или лечении запора, но также в профилактике и/или лечении метеоризма, вздутия живота, колик и/или кишечного дискомфорта у указанных младенцев.
В свете результатов, полученных в примере 3, но без желания ограничиться какой-либо теорией, считают, что фукозилированный олигосахарид является ключевым ингредиентом указанной смеси олигосахаридов, позволяющей получить такие эффекты. Таким образом, композиция, содержащая по меньшей мере один фукозилированный олигосахарид, должна обладать высокой эффективностью для применения у младенцев в улучшении консистенции стула, в улучшении частоты стула, в профилактике и/или лечении запора, но также в профилактике и/или лечении метеоризма, вздутия живота, колик и/или кишечного дискомфорта у указанных младенцев.
Пример 3
Описание исследования
Популяция исследования состоит из здоровых доношенных младенцев (как мальчиков, так и девочек), которые на момент включения в исследование находятся в постнатальном возрасте от 0 до 14 дней (дата рождения = день 0). Оценивают следующие показатели: характер стула (частоту и консистенцию стула), состав и разнообразие микробиоты кала (в том числе потенциально полезные и потенциально патогенные бактерии и вирусы), маркеры кала, показывающие состояние здоровья кишечника, ЖК толерантность, включающую ЖК симптомы и виды поведения, связанные с ЖК трактом.
• Характер стула, в том числе частота стула и консистенция стула
- Данные, собранные в дни 1, 30, 60, 90, 120 и 180 исследования.
- Консистенцию стула указывают в виде средней консистенции стула в течение 3-дневной регистрации ЖК симптомов и поведения с использованием опубликованной валидированной 5-балльной шкалы стула, разработанной для младенцев ≤ 1 года (1 = водянистый, 2 = жидкий, 3 = неоформленный мягкий, 4 = оформленный, 5 = твердый), а также указывают в виде процента стула в каждой из 5 категорий консистенции стула.
• ЖК толерантность, включая ЖК симптомы и связанные с ЖК трактом виды поведения
- Данные, собранные в дни 1, 30, 60, 90, 120 и 180 исследования.
- ЖК симптомы указывают в виде частоты срыгивания/рвоты и метеоризма в течение 3-дневной регистрации ЖК симптомов и поведения.
- Связанные с ЖК трактом виды поведения указывают в виде средней продолжительности плача и беспокойства (мин), а также сна (мин), и частоты эпизодов продолжительного плача (определяемого как плач в течение более 2,25 часа или 140 минут в день [52, 53]) на основании записей 3-дневной регистрации ЖК симптомов и поведения.
• Состав и разнообразие микробиоты кала
- Образец кала, собранный в дни 1, 120 и 180 исследования.
- Состав и разнообразие микробиоты кала (в том числе уровни потенциально полезных и потенциально патогенных бактерий и вирусов) оценивают с использованием метагеномного секвенирования методом дробовика для выборки всех генов во всех организмах и высокопроизводительного секвенирования 16S-рибосомальных генов для обеспечения меры таксономического состава и разнообразия, при этом количественные изменения специфичных бактериальных и вирусных мишеней, включая виды патогенных бактерий и вирусов, оценивают с использованием количественной полимеразной цепной реакции (кПЦР). Мишени кПЦР могут включать Lactobacillus reuteri, Campylobacter jejuni, энтеропатогенные виды Escherichia coli (EPEC), Clostridium difficile, Clostridium perfringens, Klebsiella pneumoniae. Для нормализации данных также рассчитывают массу сухого кала.
• Маркеры кала, показывающие состояние здоровья кишечника
- Образец кала, собранный в дни 1, 120 и 180 исследования.
- Маркеры кала, показывающие состояние здоровья кишечника, включают секреторный IgA [в общей сумме], B-дефензин-2 человека, миелопероксидазу и лактоферрин.
• Частота новых случаев сообщаемых нежелательных явлений (НЯ) (включая распространенные заболевания, представляющие интерес, определяемые с использованием стандартизованных критериев НЯ) и сообщаемого применения сопутствующих лекарственных средств или нефармакологических методов лечения, представляющих интерес.
- Данные, собранные со дня 1 исследования до телефонной связи через 2 недели после окончания исследования в день 194 исследования. Примечание: медицинская запись о состоянии здоровья младенца — это рабочий журнал, заполняемый родителями в ходе исследования в любой момент заболевания ребенка, приема лекарственного средства или посещений врача по любой причине. Этот рабочий журнал используется в качестве средства, помогающего заполнять формы уведомления о нежелательных явлениях (используемые для повышения точности кодирования конкретных нежелательных явлений, представляющих интерес), и в конечном счете для сообщения о нежелательных явлениях, а также записей о лекарственных средствах и нефармакологических методах лечения.
- Сообщаемые НЯ и серьезные нежелательные явления (СНЯ), включая тип, частоту новых случаев, выраженность, серьезность и связь с кормлением.
- Сводные данные учета впервые выявленных случаев, а также кумулятивной частоты и продолжительности новых случаев (рассчитанной, как описано ниже) будут представлены со дня 1 до дня 120 исследования, со дня 1 до дня 180 исследования и со дня 1 до дня 194 исследования.
Схема дозирования
Рандомизированная, двойная слепая, контролируемая схема интервенционного клинического исследования наиболее целесообразна для оценки роста, безопасности и эффективности экспериментальной смеси (EF) с добавлением 2’-FL по сравнению с контрольной смесью (CF).
Было представлено 3 группы:
• Группа CF: здоровые доношенные младенцы, которых вскармливали только смесью. Смесь представляла собой CF = смесь Lactogen, разработанная компанией Nestle SA.
• Группа EF: здоровые доношенные младенцы, которых вскармливали только смесью. Смесь представляла собой EF = смесь Lactogen, разработанная компанией Nestle SA, с добавлением 2’-FL в дозе 1 г/л.
• Группа BF: здоровые доношенные младенцы, находящиеся только на грудном вскармливании.
Смесь Lactogen включает в себя пробиотический штамм Lactobacillus в количестве 106 КОЕ/г указанной смеси (в расчете на массу сухого вещества).
Результаты
Исследуемые показатели для группы EF являются лучшими, чем для группы CF, и результаты склонны к приближению к результатам, полученным для группы BF.
Изобретение относится к питательной композиции для младенца или ребенка младшего возраста. Искусственная питательная композиция содержит по меньшей мере один фукозилированный олигосахарид, который представляет собой 2’-фукозиллактозу (2’FL), и по меньшей мере один пробиотический микроорганизм для применения в профилактике и/или лечении запора и/или в уменьшении твердости стула и/или в повышении скорости транзита у младенца или ребенка младшего возраста. Причём фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,8–1,5 г/л композиции или в общем количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества, а пробиотический микроорганизм присутствует в количестве от 103 до 1012 КОЕ/г указанной композиции (в расчете на массу сухого вещества). При этом младенец представляет собой ребёнка в возрасте до 12 месяцев, а ребёнок младшего возраста является ребёнком в возрасте от одного года до трёх лет. 6 з.п. ф-лы, 3 ил., 1 табл., 3 пр.
1. Искусственная питательная композиция, содержащая по меньшей мере один фукозилированный олигосахарид, который представляет собой 2’-фукозиллактозу (2’FL), и по меньшей мере один пробиотический микроорганизм, для применения в профилактике и/или лечении запора и/или в уменьшении твердости стула и/или в повышении скорости транзита у младенца или ребенка младшего возраста,
причём фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 0,8–1,5 г/л композиции или в общем количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества,
причём пробиотический микроорганизм присутствует в количестве от 103 до 1012 КОЕ/г указанной композиции (в расчете на массу сухого вещества), и
при этом младенец представляет собой ребёнка в возрасте до 12 месяцев, а ребёнок младшего возраста является ребёнком в возрасте от одного года до трёх лет.
2. Искусственная питательная композиция по п. 1, в которой фукозилированный олигосахарид выбирают также из перечня, состоящего из 3'-фукозиллактозы, дифукозиллактозы, лакто-N-фукопентаозы I, лакто-N-фукопентаозы II, лакто-N-фукопентаозы III, лакто-N-фукопентаозы V, лакто-N-фукогексаозы, лакто-N-дифукогексаозы I, фукозиллакто-N-гексаозы, фукозиллакто-N-неогексаозы I, фукозиллакто-N-неогексаозы II, дифукозиллакто-N-гексаозы I, дифукозиллакто-N-неогексаозы I, дифукозиллакто-N-неогексаозы II, фукозил-пара-лакто-N-гексаозы и любой их комбинации.
3. Искусственная питательная композиция по любому из предшествующих пунктов, в которой фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в общем количестве 1–1,25 г/л композиции или в общем количестве 0,69–0,87 г/100 г композиции в расчете на массу сухого вещества.
4. Искусственная питательная композиция по любому из предшествующих пунктов, содержащая по меньшей мере другой (-ие) олигосахарид (-ы), и/или клетчатку, и/или их предшественник (-и), которые выбирают из перечня, содержащего галактоолигосахариды (ГОС), фруктоолигосахариды (ФОС), ксилоолигосахариды (КОС), инулин, полидекстрозу, N-ацетилированные олигосахариды, сиалилированные олигосахариды, сиаловую кислоту, фукозу и любую их комбинацию.
5. Искусственная питательная композиция по п. 1, в которой пробиотический микроорганизм выбирают из перечня, состоящего из Lactobacillus spp., Streptococcus spp., Enterococcus spp., Bifidobacterium spp. и Saccharomyces spp.
6. Искусственная питательная композиция по любому из пп. 1-5, в которой пробиотический микроорганизм представляет собой штамм Lactobacillus.
7. Искусственная питательная композиция по любому из предшествующих пунктов, которая представляет собой детскую смесь, начальную детскую смесь, детскую смесь для прикармливаемых детей, детское питание, детскую композицию на зерновой основе, обогатитель или добавку.
| US 20120172319 A1, 05.07.2012 | |||
| US 20130251844 A1, 26.09.2013 | |||
| US 20130236423 A1, 12.09.2013 | |||
| US 20090305996 A1, 10.12.2009 | |||
| US 20110207659 A1, 25.08.2011. |
Авторы
Даты
2020-08-28—Публикация
2016-03-04—Подача