Область техники, к которой относится изобретение
Настоящее изобретение относится к композициям для применения в профилактике и/или лечении инфекций и/или воспаления нижних дыхательных путей и/или уха, например бронхита или отита, у младенцев или детей младшего возраста.
Уровень техники
Инфекции и/или воспаления дыхательных путей очень часто встречаются, особенно у младенцев и детей младшего возраста по причине их физической слабости и незрелости элементов иммунной защиты (например, их дыхательные пути еще в недостаточной мере способны противостоять таким инфекциям и/или воспалениям). Например, в первый год жизни у младенца часто будет наблюдаться от трех до шести таких инфекций. Такие инфекции и/или воспаления могут иметь бактериальное происхождение, вирусное происхождение или быть результатом воздействия окружающей среды.
Инфекции дыхательных путей могут поражать различные отделы дыхательных путей младенцев и детей младшего возраста. Возможные инфекции верхних дыхательных путей (также называемые инфекциями ВДП или ИВДП) могут представлять собой заболевания, вызванные острой инфекцией, поражающей верхние дыхательные пути: нос, придаточные пазухи носа, глотку и/или гортань. Наиболее распространенными примерами инфекций ВДП являются ринит, риносинусит, назофарингит, фарингит, эпиглоттит, ларингит, тонзиллит, ларинготрахеит, трахеит или их комбинации. ИВДП часто бывают вызваны вирусами. У пациентов с ИВДП было выявлено более 200 различных вирусов. Наиболее распространенный вирус называется риновирусом. Другие вирусы включают коронавирус, вирус парагриппа, аденовирус, энтеровирус и респираторно-синцитиальный вирус.
Другой тип инфекций дыхательных путей называют инфекциями нижних дыхательных путей (также называемыми инфекциями НДП или ИНДП). Это заболевания, вызванные острой инфекцией, затрагивающей нижние дыхательные пути (то есть нижние воздушные пути): трахею, бронхи, бронхиолы и/или легкие. Примеры инфекций нижних дыхательных путей включают пневмонию, бронхит, бронхиолит.
ИНДП иногда может предшествовать обычная вирусная ИВДП.
Инфекции НДП могут быть вызваны бактериями или вирусами. Некоторыми примерами бактерий, вызывающих такие инфекции, являются Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Staphylococcus aureus, Klebsiella pneumoniae, энтеробактерии, например Escherichia coli, анаэробы. Некоторыми примерами вирусов, вызывающих такие инфекции, являются вирус гриппа А, респираторно-синцитиальный вирус (РСВ), метапневмовирус человека (МПВ), вирус ветряной оспы.
Основными симптомами инфекций НДП являются стерторозное дыхание, трудности кормления, повышенная возбудимость, плохой сон, кашель и/или тахипноэ. Инфекции НДП также могут сопровождаться лихорадкой.
В прошлом большинство инфекций НДП приводили к смертельному исходу, но благодаря современным исследованиям и лекарственным препаратам в настоящее время они поддаются лечению. В случае бактериальных инфекций назначают антибиотики, тогда как вирусные инфекции лечить сложнее, но тем не менее они излечимы. В случае инфекций нижних дыхательных путей антибиотики часто рассматриваются как терапия первого ряда; однако они не показаны при вирусных инфекциях. Существуют также проблемы, связанные с растущей резистентностью бактерий к лечению антибиотиками.
Причиной воспалений нижних дыхательных путей, например воспалений легких, также могут стать некоторые экологические факторы, такие как вдыхание дыма, химических веществ, загрязнение воздуха (например, частицами ископаемого топлива (дизельного топлива, угля)) и песчаные бури.
Инфекции и/или воспаления уха также часто встречаются у младенцев и детей младшего возраста. Они могут иметь бактериальное или вирусное происхождение. Некоторые примеры инфекций и/или воспалений уха включают инфекции уха, воспаления уха, отит, отит среднего уха, острый отит среднего уха, отит наружного уха, мастоидит, лабиринтит. Отитом наружного уха называют воспаление наружного уха, мастоидитом называют воспаление сосцевидного отростка, а лабиринтитом называют воспаление внутреннего уха. Наиболее распространенным примером инфекций и/или воспалений уха является отит, например отит среднего уха, который представляет собой воспаление среднего уха. Отит среднего уха может включать: острый отит среднего уха, экссудативный отит среднего уха, не поддающийся лечению острый отит среднего уха, рецидивирующий острый отит среднего уха, отит среднего уха с осложнениями или хронический гнойный отит среднего уха.
Отиту среднего уха могут также предшествовать ИВДП и/или ИНДП (так что младенец или ребенок младшего возраста может страдать от инфекции/воспаления нижних дыхательных путей и уха одновременно). Главным симптомом отита среднего уха является боль в ухе, но он может также сопровождаться повышенной температурой и/или повышенной возбудимостью. Он представляет собой инфекцию среднего уха, в ходе которой евстахиева труба, соединяющая полость среднего уха с окружающей средой через рот, воспаляется, а затем блокируется, удерживая бактерии в среднем ухе. Полость среднего уха также воспаляется с накоплением жидкости, что приводит к росту давления, которое воспринимается пациентом как боль, из-за невозможности выравнивания давления между средним ухом и окружающей средой через евстахиеву трубу, как у здоровых людей. В тяжелых случаях возможен разрыв барабанной перепонки под давлением, в результате чего инфицированная жидкость попадает во внутреннее ухо. Это потенциально опасная ситуация, которая при отсутствии лечения может приводить к необратимому ухудшению слуха. У 50% детей отмечался по меньшей мере один случай острого отита среднего уха в первый год жизни (то есть в младенчестве), а у 35% детей в возрасте от одного года до трех лет (то есть в младшем возрасте) наблюдались рецидивы острого отита среднего уха. Это, в свою очередь, может приводить к развитию состояния, называемого экссудативным отитом, при котором в промежуток между приступами инфекции жидкость не удаляется из среднего уха полностью. В случае стабилизации подобного состояния может потребоваться хирургическое вмешательство.
Острый отит среднего уха, по-видимому, главным образом связан с деятельностью патогенных бактерий, которые обычно присутствуют в природной микробиоте носоглоточной полости. С количественной точки зрения наиболее значимыми патогенами являются Streptococcus pneumoniae (35% случаев), нетипируемые Haemophilus influenzae (30% случаев) и Moraxella catarrhalis (10% случаев). По этой причине острый отит среднего уха, как правило, лечат введением антибиотиков, в особенности у младенцев. В самом деле, антибиотики чаще назначают для лечения отита среднего уха, чем для любого другого заболевания у младенцев. Это также неизбежно привело к развитию устойчивости к часто назначаемым антибиотикам у бактериальных штаммов, связанных с отитом среднего уха. Например, принято считать, что по меньшей мере 20% штаммов S. pneumoniae устойчивы к пенициллинам и цефалоспоринам. Аналогичным образом, по меньшей мере у 30% штаммов H. influenzae и у большинства штаммов M. catarrhalis сформировалась устойчивость к антибиотикам. Подобная частота назначения антибиотиков по меньшей мере частично вызвана болями, которые наблюдаются у младенцев и детей младшего возраста, страдающих отитом среднего уха и реагирующих на такие боли продолжительным плачем, который родители и другие опекуны всеми силами стараются успокоить. Отит может также вызываться вирусами, например РСВ и риновирусом, вызывающим обычную простуду. В этом случае лечение антибиотиками будет неэффективным.
Таким образом, существует очевидная потребность в альтернативных способах снижения частоты возникновения таких болезненных и потенциально серьезных заболеваний у младенцев и детей младшего возраста.
Предпринималось множество попыток разработать альтернативные подходы для профилактики/лечения инфекций и/или воспалений нижних дыхательных путей и уха. В частности, проводятся исследования применения пробиотиков. Пробиотики считаются препаратами на основе жизнеспособных микроорганизмов, которые укрепляют здоровье индивида путем сохранения естественной микрофлоры в кишечнике. Предполагается, что пробиотики прикрепляются к слизистой оболочке кишечника, колонизируют кишечник и таким же путем предотвращают прикрепление к нему вредных микроорганизмов. Важнейшее условие их действия заключается в том, что они должны достичь слизистой оболочки кишечника в надлежащей и жизнеспособной форме и не должны разрушиться в верхнем отделе желудочно-кишечного тракта, в частности, под влиянием низкого рН, преобладающего в желудке.
Например, в документе WO2008042101 компании Danisco предлагаются способы снижения частоты заболеваний органов дыхания у детей, включающие: обеспечение культуры L. acidophilus; выявление ребенка, подверженного риску развития заболевания органов дыхания; и введение культуры L. acidophilus подверженному риску ребенку в таких условиях, что риск развития заболевания органов дыхания снижается. Однако добавление живых пробиотических бактерий в продукты так, чтобы они оставались жизнеспособными до потребления, является нетривиальной задачей. В частности, это трудно осуществить для продуктов с длительным сроком хранения и может потребовать дополнительных технических усилий.
Настоящее изобретение нацелено на детей, предпочтительно в возрасте от 3 до 5 лет.
Изучаются и другие возможности, отличные от пробиотиков, такие как применение олигосахаридов, в частности олигосахаридов человеческого грудного молока. Олигосахариды грудного молока (ОГМ) являются в совокупности третьим по величине компонентом (по содержанию в сухом веществе) в грудном молоке после лактозы и жира. ОГМ обычно состоят из лактозы на восстанавливающем конце с углеводным ядром, которое часто содержит фукозу или сиаловую кислоту на невосстанавливающем конце. Из грудного молока выделено и охарактеризовано более ста молочных олигосахаридов.
Материнское молоко рекомендовано всем младенцам. Однако в некоторых случаях грудное вскармливание является недостаточным или неуспешным по медицинским причинам, или мать отказывается от грудного вскармливания. Для этих ситуаций были разработаны детские смеси. Также были разработаны обогатители для обогащения материнского молока или детской смеси определенными ингредиентами.
Так, для различных целей разработано несколько композиций с использованием ингредиентов ОГМ, таких как фукозилированные олигосахариды, лакто-N-тетраоза, лакто-N-неотетраоза и/или сиалилированные олигосахариды.
Например, в патенте WO2005055944 организации Children’s hospital medical center описана фармацевтическая композиция, содержащая молекулу, которая содержит фукозную группу, соединенную с галактозной группой альфа-2 связью, альфа-3 связью или альфа-4 связью, и фармацевтически приемлемый носитель. Описаны различные молекулы, такие как 2'-фукозиллактоза. Эта заявка носит достаточно общий характер, поскольку возможны профилактика или лечение нескольких инфекций, включая респираторные или кишечные инфекции, в большой целевой группе пациентов (младенцы, дети или взрослые).
Заявка WO2012092158, поданная компанией Abbott, относится к детской смеси, содержащей смесь сиалилированных олигосахаридов в определенных количествах для модуляции воспаления, вызванного респираторными вирусами.
В заявках WO2009/059996 и WO2012/076323, поданных Nestec SA, описаны композиции со смесью ОГМ, в обязательном порядке содержащие сиалилированные олигосахариды как компоненты, необходимые для профилактики вторичных инфекций или острых респираторных инфекций (ОРИ).
Дополнительные исследования были сосредоточены на различных ассоциациях ОГМ с пробиотическим штаммом или с другими специфическими компонентами.
Например, документ WO2009/077352 компании Nestec SA относится к композиции, приемлемой для профилактики оппортунистических инфекций и содержащей особое синергетическое сочетание пробиотика Bifidobacterium с фукозилированным олигосахаридом. В числе оппортунистических инфекций, подлежащих профилактике, приводятся инфекции дыхательных путей. Настоящее изобретение, в частности, нацелено на индивидов с ослабленным иммунитетом, таких как недоношенные младенцы, дети старшего возраста или взрослые с не полностью эффективной иммунной системой вследствие имеющегося патологического состояния или заболевания (например, ВИЧ) или вследствие терапии по поводу имеющегося патологического состояния, например болезни Крона или ревматоидного артрита, или химиотерапии для лечения рака).
Олигосахариды в целом известны своей защитной ролью при воздействии на желудочно-кишечный тракт, дыхательные или мочевыводящие пути, см., например, работу Wataru et al., 2003, и WO9843494. Вместе с тем в большинстве таких исследований различные ОГМ описываются без увязки конкретного вида олигосахаридов или их синергетического сочетания с конкретной пользой для организма. В них также описываются различные примеры концентраций и отмечается лишь общее полезное воздействие (то есть без акцента на нижние дыхательные пути и ухо).
Патент WO2012/092154 компании Abbott относится к способам применения ОГМ для улучшения состояния дыхательных путей у младенцев, детей, начинающих ходить, и детей других возрастов. Однако в этой заявке представлен обширный перечень ОГМ, а также несколько комбинаций различных ОГМ. Заявлено, что композиция демонстрирует эффективность только тогда, когда ОГМ присутствуют вместе с каротиноидом.
В заявке WO2012092155 описаны композиции, содержащие ОГМ в обязательном порядке с другим видом пребиотика, который выбирают из перечня ГОС или ФОС, и призванные благоприятно воздействовать на желудочно-кишечный тракт.
Ряд других исследований также относится к лечению/профилактике патогенных инфекций ВДП, которые отличаются от НДП, поскольку они воздействуют на другие ткани/органы тела или затрагивают их, как уже отмечалось выше. Например, патент WO2009/112361 компании Nestec SA относится к другой композиции, приемлемой для профилактики оппортунистических инфекций и содержащей особое синергетическое сочетание N-ацетиллактозамина и/или олигосахарида, содержащего N-ацетиллактозамин, с пробиотиком Lactobacillus sp. В качестве примера приводятся несколько патологических состояний, таких как вызванные патогенными микроорганизмами инфекции верхних дыхательных путей.
Таким образом, ни одна из предыдущих работ не описывает профилактику и/или лечение инфекций/воспалений нижних дыхательных путей и уха у младенцев или детей младшего возраста, тогда как именно они подвержены более высоким рискам развития таких инфекций/воспалений, чем в среднем.
Существует очевидная потребность в разработке приемлемых способов снижения частоты таких заболеваний у младенцев и детей младшего возраста.
Также существует потребность обеспечить такие полезные для здоровья эффекты способом, который особенно приемлем для молодых субъектов (младенцев и детей младшего возраста), при этом способ не должен включать в себя классическое фармацевтическое вмешательство, поскольку эти младенцы или дети младшего возраста особенно уязвимы.
Существует потребность в обеспечении таких полезных для здоровья этих младенцев и детей младшего возраста эффектов с помощью способа, который не вызывает побочных эффектов и/или который легко осуществлять и который приемлем для родителей или медицинских работников.
Также существует потребность обеспечивать такие полезные эффекты способом, который позволит сохранять разумную и доступную для большинства стоимость такого обеспечения.
Таким образом, существует очевидная потребность в разработке альтернативных способов, отличных от классического фармацевтического вмешательства, например применения антибиотиков, по меньшей мере по причине перечисленных выше проблем формирования устойчивости.
Существует также потребность в разработке альтернативного подхода к лечению, который может быть эффективным для широкого диапазона источников, то есть не зависеть от причин инфекций и/или воспалений (например, бактериальное, вирусное или экологическое происхождение).
Раскрытие изобретения
Авторы настоящего изобретения обнаружили, что композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, оба в определенных количествах, может преимущественно применяться в качестве средства от инфекций и/или воспалений нижних дыхательных путей, например бронхита, а также инфекций и/или воспалений уха, например отита, у младенца или ребенка младшего возраста. Без ограничений, накладываемых теорией, считается, что такой (-ие) олигосахарид (-ы) проявляет (-ют) синергическое воздействие в случае таких специфических заболеваний.
Соответственно, по этой причине в настоящем изобретении обеспечивается питательная композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для применения в профилактике и/или лечении инфекций и/или воспалений нижних дыхательных путей и/или уха у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
В особенно преимущественном варианте осуществления питательная композиция содержит 2’-фукозиллактозу (2-FL) и лакто-N-неотетраозу (LNnT), и в частности 2’-фукозиллактозу (2-FL) в количестве 1–1,5 г/л питательной композиции и LNnT в количестве 0,5–0,7 г/л питательной композиции.
Авторы настоящего изобретения также обнаружили, что конкретная питательная композиция в соответствии с изобретением отличается особой эффективностью при снижении температуры и применении (то есть введении) антибиотиков и применении жаропонижающих средств для лечения младенца или ребенка младшего возраста.
Краткое описание фигур
На фиг. 1 представлено число младенцев по меньшей мере с одним случаем бронхита, при этом упомянутые младенцы получали либо стандартную детскую смесь (контрольная группа), либо стандартную смесь с добавкой 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы (группа ОГМ). Среди младенцев, рожденных с помощью кесарева сечения, OR = 0,15, p = 0,02; среди младенцев, рожденных посредством вагинальных родов, OR = 0,42, p = 0,095; среди всех младенцев OR = 0,3, p = 0,004. В контрольной группе n = 87, а группе ОГМ n = 88.
Фиг. 1А: частичные результаты (не были получены данные обо всех младенцах) в течение первых 12 месяцев после рождения.
Фиг. 1В: полные результаты (были получены данные обо всех младенцах) за 0–4, 0–6 и 0–12 месяцев после рождения.
На фиг. 2 представлено число младенцев по меньшей мере с одним случаем инфекции/воспаления уха в течение первых 12 месяцев после рождения, при этом упомянутые младенцы получали либо стандартную детскую смесь (контрольная группа), либо стандартную смесь с добавкой 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы (группа ОГМ). Среди всех младенцев OR = 0,3, p = 0,06. В контрольной группе n = 87, а группе ОГМ n = 88.
Фиг. 2А: частичные результаты (не были получены данные обо всех младенцах) в течение первых 12 месяцев после рождения.
Фиг. 2В: полные результаты (были получены данные обо всех младенцах) за 0–4, 0–6 и 0–12 месяцев после рождения.
На фиг. 3 представлено число младенцев, которым вводили антибиотики по меньшей мере один раз в течение первых 12 месяцев после рождения, при этом упомянутые младенцы получали либо стандартную детскую смесь (контрольная группа), либо стандартную смесь с добавкой 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы (группа ОГМ). Среди младенцев, рожденных с помощью кесарева сечения, OR = 0,5, p = 0,2; среди младенцев, рожденных посредством вагинальных родов, OR = 0,45, p = 0,068; среди всех младенцев OR = 0,47, p = 0,025. В контрольной группе n = 87, а в группе ОГМ n = 88.
Фиг. 3А: частичные результаты (не были получены данные обо всех младенцах) в течение первых 12 месяцев после рождения.
Фиг. 3В: полные результаты (были получены данные обо всех младенцах) за 0–4, 0–6 и 0–12 месяцев после рождения.
На фиг. 4 представлено число младенцев по меньшей мере с одним случаем повышенной температуры в течение первых 12 месяцев после рождения, при этом упомянутые младенцы получали либо стандартную детскую смесь (контрольная группа), либо стандартную смесь с добавкой 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы (группа ОГМ). Среди младенцев, рожденных с помощью кесарева сечения, OR = 0,3, p = 0,6; среди младенцев, рожденных посредством вагинальных родов, OR = 0,4, p = 0,15; среди всех младенцев OR = 0,4, p = 0,08. В контрольной группе n = 87, а в группе ОГМ n = 88.
Фиг. 4А: частичные результаты (не были получены данные обо всех младенцах) в течение первых 12 месяцев после рождения.
Фиг. 4В: полные результаты (были получены данные обо всех младенцах) за 0–4, 0–6 и 0–12 месяцев после рождения.
На фиг. 5 представлено общее число событий на группу с бронхитом в течение 0–6 месяцев после рождения (фиг. 5А), группу с инфекциями/воспалениями уха в течение 0–12 месяцев после рождения (фиг. 5В), группу с применением антибиотиков в течение 0–6 месяцев после рождения (фиг. 5С) и группу с применением жаропонижающих средств в течение 0–6 месяцев после рождения (фиг. 5D) у младенцев, которые получали либо стандартную детскую смесь (контрольная группа), либо стандартную смесь с добавкой 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы (группа ОГМ) (частичные результаты — не были получены данные по всем младенцам). Антибиотики включают все назначенные лекарственные препараты, обладающие способностью ингибировать рост микроорганизмов или уничтожать их. Жаропонижающие средства включают все назначенные лекарственные препараты, обладающие способностью и предназначенные для понижения температуры.
На фиг. 6 представлено общее число событий на группу с бронхитом (фиг. 6А), группу с инфекциями/воспалениями уха (фиг. 6В), группу с применением антибиотиков (фиг. 6С) и группу с применением жаропонижающих средств (фиг. 6D) в течение 0–12 месяцев после рождения у младенцев, которые получали либо стандартную детскую смесь (контрольная группа), либо стандартную смесь с добавкой 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы (группа ОГМ). Полные результаты (получены данные для всех младенцев). Символ # означает номер.
Осуществление изобретения
В контексте настоящего документа следующие термины имеют приведенные ниже определения.
Термин «младенец» означает ребенка в возрасте до 12 месяцев.
Выражение «ребенок младшего возраста» означает ребенка в возрасте от одного до трех лет (также называется ребенком, начинающим ходить).
«Младенец или ребенок младшего возраста, рожденный с помощью кесарева сечения» означает младенца или ребенка младшего возраста, рожденного с помощью кесарева сечения. Это означает, что младенец или ребенок младшего возраста был рожден не посредством вагинальных родов.
«Младенец или ребенок младшего возраста, рожденный посредством вагинальных родов» означает младенца или ребенка младшего возраста, который был рожден посредством вагинальных родов, а не с помощью кесарева сечения.
«Недоношенный» или «преждевременно родившийся» означает младенца или ребенка младшего возраста, который родился раньше срока. Как правило, этот термин относится к младенцу или ребенку младшего возраста, рожденному до 36 недели беременности.
Выражение «питательная композиция» означает композицию, которой питается субъект. Данная питательная композиция обычно предназначена для перорального или внутривенного применения и обычно включает в себя источник липидов или жира и источник белка.
В конкретном варианте осуществления композиция настоящего изобретения представляет собой гипоаллергенную питательную композицию. Выражение «гипоаллергенная питательная композиция» означает питательную композицию, для которой вероятность того, что она вызовет аллергические реакции, является малой.
В конкретном варианте осуществления композиция настоящего изобретения представляет собой «искусственную питательную композицию». Выражение «искусственная питательная композиция» означает смесь, полученную с помощью химических и/или биологических средств, которые могут быть химически идентичны смеси природного происхождения, присутствующей в молоке млекопитающих (т.е. синтетическая композиция не является грудным молоком).
Выражение «детская смесь» в контексте настоящего документа относится к продукту питания, специально предназначенному для применения в пищу младенцами в течение первых месяцев жизни, который сам по себе удовлетворяет потребности в питании этой категории лиц (статья 2(c) Директивы Европейской комиссии 91/321/EEC 2006/141/EC от 22 декабря 2006 г. о детских смесях первого уровня и смесях для прикармливаемых детей). Оно также относится к питательной композиции, предназначенной для младенцев, как определено в Codex Alimentarius (Codex STAN 72-1981) и стандарте «Специальные продукты для младенцев» (включая статью «Продукты для специальных медицинских целей»). Выражение «детская смесь» включает в себя понятия как «начальная детская смесь», так и «смесь для прикармливаемых детей».
«Смесь для прикармливаемых детей» дают, начиная с 6-го месяца. Она представляет собой главный жидкий элемент в постепенно увеличивающемся разнообразии рациона для лиц данной категории.
Выражение «детское питание» означает продукт питания, специально предназначенный для применения в пищу младенцами или детьми младшего возраста в течение первых лет жизни.
Выражение «детская композиция на зерновой основе» означает продукт питания, специально предназначенный для применения в пищу младенцами или детьми младшего возраста в течение первых лет жизни.
Термин «обогатитель» относится к жидким или твердым питательным композициям, приемлемым для смешивания с грудным молоком или детской смесью.
Выражение «период отлучения от груди» означает период, в течение которого в рационе младенца или ребенка младшего возраста материнское молоко замещают другим продуктом.
Выражения «в возрасте дней/недель/месяцев/лет» и «дней/недель/месяцев/лет после рождения» могут использоваться как взаимозаменяемые.
Выражение «профилактика и/или лечение инфекций и/или воспалений нижних дыхательных путей и/или уха» включает одну или несколько из перечисленных ниже позиций:
- профилактика инфекций нижних дыхательных путей;
- профилактика инфекций уха;
- профилактика воспалений нижних дыхательных путей;
- профилактика воспалений уха;
- лечение инфекций нижних дыхательных путей;
- лечение инфекций уха;
- лечение воспалений нижних дыхательных путей;
- лечение воспалений уха.
Выражения «инфекции нижних дыхательных путей», «инфекции НДП» и «ИНДП» могут использоваться как взаимозаменяемые. Это заболевания, вызванные острой инфекцией, затрагивающей нижние дыхательные пути (то есть нижние воздушные пути): трахею, бронхи, бронхиолы и/или легкие. Примерами инфекций НДП являются пневмония, бронхит, бронхиолит или их сочетания. Как подробно указывалось выше, инфекции НДП могут иметь бактериальное происхождение, вирусное происхождение или быть результатом воздействия окружающей среды.
Выражения «инфекции и/или воспаления уха» и «ушные инфекции и/или воспаления» могут использоваться как взаимозаменяемые. Они включают инфекции уха, воспаления уха, отит, отит среднего уха, острый отит среднего уха, отит наружного уха, мастоидит, лабиринтит. Как подробно указывалось выше, такие инфекции и/или воспаления могут иметь бактериальное происхождение, вирусное происхождение или быть результатом воздействия окружающей среды.
Выражения «в профилактике инфекций и/или воспалений», «для профилактики инфекций и/или воспалений», «в ходе профилактики инфекций и/или воспалений» и «в целях профилактики инфекций и/или воспалений» могут использоваться как взаимозаменяемые.
Такие выражения подразумевают противодействие возникновению инфекций и/или воспалений НДП/уха и/или снижение частоты возникновения упомянутых инфекций и/или воспалений (снижение частоты, то есть числа инфекций и/или воспалений НДП/уха). В некоторых вариантах осуществления профилактика инфекций и/или воспалений НДП/уха происходит в ходе лечения (то есть в ходе введения композиции настоящего изобретения либо непосредственно после начала введения, либо через некоторое время после начала, например несколько дней или недель). Она также может включать профилактику инфекций и/или воспалений НДП/уха в дальнейшей жизни. Термин «в дальнейшей жизни» включает эффект после прекращения вмешательства или лечения. Эффект «в дальнейшей жизни» может длиться от 1 недели до нескольких месяцев, например от 2 до 4 недель, от 2 до 6 недель, от 2 до 8 недель, от 1 до 6 месяцев или от 2 до 12 месяцев.
Выражения «в лечении инфекций и/или воспалений», «для лечения инфекций и/или воспалений», «в ходе лечения инфекций и/или воспалений» и «для лечения инфекций и/или воспалений» могут использоваться как взаимозаменяемые.
Их следует понимать как включающие снижение продолжительности инфекций и/или воспалений НДП/уха (число дней/недель/лет, в течение которых младенцы или дети младшего возраста будут страдать от инфекций и/или воспалений НДП/уха), степени тяжести инфекций и/или воспалений НДП/уха (последствий и/или серьезности инфекций и/или воспалений НДП/уха). Эти выражения также включают облегчение симптомов, таких как стерторозное дыхание, трудности кормления, повышенная возбудимость, плохой сон, кашель, тахипноэ, боль в ушах, повышенная температура и их комбинации, и/или уменьшение осложнений, вызванных инфекциями и/или воспалениями НДП/уха, для здоровья младенца или ребенка младшего возраста, таких как астма, проблемы экссудативного отита, необходимость хирургического вмешательства, и/или уменьшение боли, и/или уменьшение усталости, и/или облегчение сна, и/или стабилизацию активности младенцев или детей младшего возраста, страдающих от инфекций и/или воспалений НДП/уха.
Под «материнским молоком» следует понимать грудное молоко или молозиво матери.
«Олигосахарид» представляет собой полимер сахарида, содержащий небольшое число (как правило, от трех до десяти) простых сахаров (моносахаридов).
Термин «ОГМ» относится к олигосахариду (-ам) грудного молока. Эти углеводы обладают высокой устойчивостью к ферментативному гидролизу, что указывает на то, что они могут проявлять основные функции, непосредственно не относящиеся к их калорийной ценности. В первую очередь было показано, что они играют жизненно важную роль в раннем развитии младенцев и детей младшего возраста, например в развитии иммунной системы. В грудном молоке обнаружено много различных видов ОГМ. Каждый отдельный олигосахарид основан на комбинации глюкозы, галактозы, сиаловой кислоты (N-ацетилнейраминовой кислоты), фукозы и/или N-ацетилглюкозамина с образованием многочисленных и разнообразных связей между ними, что обусловливает присутствие огромного числа различных олигосахаридов в грудном молоке — на данный момент было выявлено более 130 таких структур. Почти все они имеют лактозную группу на своем восстанавливающем конце, в то время как сиаловая кислота и/или фукоза (при наличии) занимают концевые положения на невосстанавливающих концах. ОГМ может быть кислотным (например, олигосахарид, содержащий заряженную сиаловую кислоту) или нейтральным (например, фукозилированный олигосахарид).
«Фукозилированный олигосахарид» представляет собой олигосахарид, имеющий остаток фукозы. Он имеет нейтральный характер. Некоторыми примерами являются 2-FL (2’-фукозиллактоза), 3-FL (3-фукозиллактоза), дифукозиллактоза, лакто-N-фукопентаоза (например, лакто-N-фукопентаоза I, лакто-N-фукопентаоза II, лакто-N-фукопентаоза III, лакто-N-фукопентаоза V), лакто-N-фукогексаоза, лакто-N-дифукогексаоза I, фукозиллакто-N-гексаоза, фукозиллакто-N-неогексаоза, дифукозиллакто-N-гексаоза I, дифукозиллакто-N-неогексаоза II и любая их комбинация. Хотя авторы не желают ограничиваться какой-либо теорией, считается, что фукозил-эпитоп фукозилированных олигосахаридов может выступать в качестве «ловушки» на поверхности слизистой оболочки. Посредством конкурентного эффекта он может предотвращать и/или ограничивать действие патогенов, вызывающих инфекции (вирусного или бактериального происхождения), или секретируемых ими компонентов (например, токсинов), в первую очередь исключая их связывание с природными лигандами, и, безотносительно к какой-либо теории, считается, что за счет этого будет снижаться риск возникновения инфекций/воспалений, и в частности риск возникновения инфекций и/или воспалений НДП/уха. Дополнительно принято считать, что фукозилированные олигосахариды стимулируют рост и метаболическую активность специфических симбиотических микробов, снижающих воспалительную реакцию и создающих неблагоприятную среду для патогенов, тем самым обеспечивая колонизационную резистентность.
Выражения «фукозилированные олигосахариды, содержащие 2’-фукозил-эпитоп» и «2-фукозилированные олигосахариды» включают фукозилированные олигосахариды с определенной гомологией формы, поскольку они содержат 2’-фукозил-эпитоп, следовательно, можно ожидать определенную гомологию функции. Хотя авторы не желают ограничиваться какой-либо теорией, считается, что 2'-фукозил-эпитоп этих фукозилированных олигосахаридов особо характерен для патогенов (или секретируемых ими компонентов), вызывающих инфекции НДП и/или уха.
Выражение «N-ацетилированный (-ые) олигосахарид (-ы)» включает как «N-ацетиллактозамин», так и «олигосахарид (-ы), содержащий (-ие) N-ацетиллактозамин». Они являются нейтральными олигосахаридами, имеющими остаток N-ацетиллактозамина. Приемлемыми примерами являются LNT (лакто-N-тетраоза), пара-лакто-N-неогексаоза (пара-LNnH), LNnT (лакто-N-неотетраоза) и любые их комбинации. Другими примерами являются лакто-N-гексаоза, лакто-N-неогексаоза, пара-лакто-N-гексаоза, пара-лакто-N-неогексаоза, лакто-N-октаоза, лакто-N-неооктаоза, изо-лакто-N-октаоза, пара-лакто-N-октаоза и лакто-N-декаоза.
Выражения «по меньшей мере один фукозилированный олигосахарид» и «по меньшей мере один N-ацетилированный олигосахарид» означают «по меньшей мере один тип фукозилированного олигосахарида» и «по меньшей мере один тип N-ацетилированного олигосахарида».
«Предшественник ОГМ» представляет собой ключевое соединение, которое включается в выработку ОГМ, такое как сиаловая кислота и/или фукоза.
«Сиалилированный олигосахарид» представляет собой олигосахарид, содержащий заряженную сиаловую кислоту, то есть олигосахарид, имеющий остаток сиаловой кислоты. Он имеет кислотный характер. Некоторыми примерами являются 3-SL (3’-сиалиллактоза) и 6-SL (6’-сиалиллактоза).
Питательная композиция настоящего изобретения может быть представлена в твердой форме (например, в порошке) или в жидком виде. Количество различных ингредиентов (например, олигосахаридов) может выражаться в г/100 г композиции в расчете на массу сухого вещества, если она представлена в твердой форме, например в порошке, или как концентрация в г/л композиции, если она относится к жидкой форме (последний случай также включает жидкую композицию, которую можно получать из порошка после растворения в жидкости, например в молоке, воде ..., например растворенные детские смеси, или смеси для прикармливаемых детей, или зерновой продукт для детского питания, или любая другая рецептура, предназначенная для питания младенцев).
Термин «пребиотик» означает неперевариваемые углеводы, которые благоприятно влияют на организм-хозяина, выборочно стимулируя рост и/или активность полезных для здоровья бактерий, например бифидобактерий, в толстом кишечнике человека (Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr. 1995; 125:1401–12).
Термин «пробиотик» означает препараты из клеток микроорганизмов или компоненты клеток микроорганизмов, которые оказывают благоприятное воздействие на здоровье или самочувствие организма-хозяина. (Salminen S, Ouwehand A. Benno Y. et al. "Probiotics: how should they be defined" Trends Food Sci. Technol. 1999:10, 107–10). Клетки микроорганизмов обычно являются бактериями или дрожжами.
Под термином «КОЕ» следует понимать колониеобразующую единицу.
Если не указано иное, все приводимые процентные соотношения представляют собой мас.%.
Дополнительно в контексте изобретения термины «содержащий» или «содержит» не исключают других возможных элементов. Композиция настоящего изобретения, включая многие варианты осуществления, описанные в настоящем документе, может содержать существенные элементы и признаки изобретения, описанные в настоящем документе, а также любые дополнительные или необязательные ингредиенты, компоненты или признаки изобретения, описанные в настоящем документе, или иные в зависимости от потребностей, состоять или, по существу, состоять из них.
Любую ссылку на документы предшествующего уровня техники в данном описании не следует рассматривать как признание того, что такой предшествующий уровень техники является широко известным или составляет часть общеизвестных знаний в области.
Далее изобретение будет описано более подробно. Следует отметить, что различные аспекты, признаки, примеры и варианты осуществления, описанные в настоящей заявке, могут быть совместимыми и/или комбинироваться друг с другом.
Поэтому первой целью настоящего изобретения является питательная композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для применения в профилактике и/или лечении инфекций и/или воспалений нижних дыхательных путей и/или уха у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
Композиция настоящего изобретения содержит по меньшей мере один фукозилированный олигосахарид. В ней может присутствовать один или несколько типов фукозилированного (-ых) олигосахарида (-ов). Фукозилированный (-е) олигосахарид (-ы) можно фактически выбирать из перечня, содержащего 2’-фукозиллактозу, 3’-фукозиллактозу, дифукозиллактозу, лакто-N-фукопентаозу (например, лакто-N-фукопентаозу I, лакто-N-фукопентаозу II, лакто-N-фукопентаозу III, лакто-N-фукопентаозу V), лакто-N-фукогексаозу, лакто-N-дифукогексаозу I, фукозиллакто-N-гексаозу, фукозиллакто-N-неогексаозу (например, фукозиллакто-N-неогексаозу I, фукозиллакто-N-неогексаозу II), дифукозиллакто-N-гексаозу I, дифуко-лакто-N-неогексаозу, дифукозиллакто-N-неогексаозу I, дифукозиллакто-N-неогексаозу II, фукозил-пара-лакто-N-гексаозу, три-фуко-пара-лакто-N-гексаозу I и любую их комбинацию.
В некоторых конкретных вариантах осуществления фукозилированный олигосахарид содержит 2’-фукозил-эпитоп. Он может быть, например, выбран из перечня, содержащего 2’-фукозиллактозу, дифукозиллактозу, лакто-N-фукопентаозу, лакто-N-фукогексаозу, лакто-N-дифукогексаозу, фукозиллакто-N-гексаозу, фукозиллакто-N-неогексаозу, дифукозиллакто-N-гексаозу дифуко-лакто-N-неогексаозу, дифукозиллакто-N-неогексаозу, фукозил-пара-лакто-N-гексаозу и любую их комбинацию.
В предпочтительном варианте осуществления питательная композиция в соответствии с изобретением содержит 2’-фукозиллактозу (или 2FL, или 2’FL, или 2-FL, или 2’-FL). В конкретном варианте осуществления не используется никакой другой тип фукозилированного олигосахарида, кроме 2’-фукозиллактозы, то есть питательная композиция настоящего изобретения содержит только 2’-фукозиллактозу в качестве фукозилированного олигосахарида.
Фукозилированный (-ые) олигосахарид (-ы) может (могут) быть выделен (-ы) из природного источника, такого как молоко животных, методами хроматографии или фильтрации. В альтернативном варианте осуществления он может быть получен с помощью биотехнологических средств с использованием специфических фукозилтрансфераз и/или фукозидаз либо посредством применения метода ферментации на основе ферментов (рекомбинантных или природных ферментов), либо метода микробиологической ферментации. В последнем случае либо микроорганизмы могут экспрессировать свои природные ферменты и субстраты, либо возможно создание микроорганизмов, вырабатывающих соответствующие субстраты и ферменты. Можно применять культуры из микроорганизмов одного вида и/или смешанные культуры. Образование фукозилированного олигосахарида может быть инициировано акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP = 1 и далее. В альтернативном варианте осуществления фукозилированные олигосахариды можно получать с помощью химического синтеза из лактозы и свободной фукозы. Фукозилированные олигосахариды также доступны в продаже, например производства компании Kyowa Hakko Kogyo, Япония.
Композиция настоящего изобретения также содержит по меньшей мере один N-ацетилированный олигосахарид. В ней может присутствовать один или несколько типов N-ацетилированного (-ых) олигосахарида (-ов). N-ацетилированный (-ые) олигосахарид (-ы) может (могут) представлять собой, например, лакто-N-тетраозу (LNT), лакто-N-неотетраозу (LNnT) или любую их комбинацию. В некоторых конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой лакто-N-неотетраозу (LNnT), пара-лакто-N-неогексаозу (пара-LNnH) или любую их комбинацию. В некоторых конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой LNnT. В некоторых конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой LNT. В некоторых других конкретных вариантах осуществления N-ацетилированный олигосахарид представляет собой смесь LNT и LNnT. В некоторых конкретных вариантах осуществления композиция содержит как LNT, так и LNnT в соотношении LNT : LNnT между 5 : 1 и 1 : 2 или от 2 : 1 до 1 : 1, или от 2 : 1,2 до 2 : 1,6.
В предпочтительном варианте осуществления питательная композиция в соответствии с изобретением содержит лакто-N-неотетраозу (LNnT). В конкретном варианте осуществления не используется никакой другой тип N-ацетилированного олигосахарида, кроме лакто-N-неотетраозы (LNnT), то есть питательная композиция изобретения содержит только лакто-N-неотетраозу (LNnT) в качестве N-ацетилированного олигосахарида.
N-ацетилированный (-ые) олигосахарид (-ы) можно синтезировать химическим путем с помощью ферментативного переноса сахаридных единиц с донорных фрагментов на акцепторные фрагменты с использованием гликозилтрансфераз, как описано, например, в патенте США № 5,288,637 и публикации WO 96/10086. В альтернативном варианте осуществления LNT и LNnT могут быть приготовлены путем химического преобразования кетогексоз (например, фруктозы), либо свободных, либо связанных с олигосахаридом (например, лактулозой), в N-ацетилгексозамин или N-ацетилгексозамин-содержащий олигосахарид, как описано в работе Wrodnigg, T.M.; Stutz, A.E. (1999) Angew. Chem. Int. Ed. 38:827–828. N-ацетиллактозамин, полученный таким образом, можно впоследствии переносить в качестве акцепторного фрагмента на лактозу.
В наиболее преимущественном варианте осуществления настоящего изобретения питательная композиция содержит 2’-фукозиллактозу (2FL) и лакто-N-неотетраозу (LNnT).
В другом конкретном варианте осуществления питательная композиция настоящего изобретения содержит смесь олигосахаридов, которая состоит из 2’-фукозиллактозы (2FL) и лакто-N-неотетраозы (LNnT). Иными словами, питательная композиция изобретения содержит только 2’-фукозиллактозу (2FL) в качестве фукозилированного олигосахарида и только лакто-N-неотетраозу (LNnT) в качестве N-ацетилированного олигосахарида.
В настоящем изобретении фукозилированный (-ые) олигосахарид (-ы) и N-ацетилированный (-ые) олигосахарид (-ы) присутствуют в питательной композиции в некоторых определенных количествах. Термин «количество», если не указано иное, относится к суммарному количеству каждого из таких 2 компонентов в питательной композиции. Поэтому он не относится к индивидуальному количеству, кроме случаев, когда речь идет о единственном типе таких компонентов (в этом случае как суммарное, так и индивидуальное количество будут одинаковыми). В качестве иллюстрирующего примера, если в композиции используется только один фукозилированный олигосахарид (то есть только один его тип) (например, 2FL), его индивидуальное количество (а потому и суммарное количество фукозилированных олигосахаридов) будет находиться в диапазоне 0,75–1,65 г/л. В случае нескольких фукозилированных олигосахаридов (то есть нескольких типов) их индивидуальное количество будет меньше (например, в случае 2 различных типов фукозилированных олигосахаридов, например 2FL + 3FL, каждый из них может присутствовать в индивидуальном количестве 0,5 г/л), но суммарное количество фукозилированных олигосахаридов будет находиться в диапазоне 0,75–1,65 г/л.
Фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в соответствии с настоящим изобретением в суммарном количестве 0,75–1,65 г/л композиции. В некоторых вариантах осуществления фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в суммарном количестве 0,8–1,5 г/л композиции, например 0,85–1,3 г/л или 0,9–1,25 г/л или 0,9–1,1 г/л или 1–1,25 г/л или 1,05–1,25 г/л композиции. В конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 1 г/л композиции. В другом варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 1,24 г/л композиции.
Фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества. Фукозилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в суммарном количестве 0,55–1,05 г/100 г композиции, например 0,59–0,9 г/100 г, или 0,62–0,87 г/100 г, или 0,62–0,77 г/100 г, или 0,69–0,87 г/100 г, или 0,73–0,87 г/100 г композиции. В конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,69 г/100 г композиции. В другом конкретном варианте осуществления фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,86 г/100 г композиции.
N-Ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в соответствии с настоящим изобретением в суммарном количестве 0,45–0,85 г/л композиции.
В некоторых вариантах осуществления N-ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в суммарном количестве 0,5–0,8 г/л композиции, например 0,5–0,75 г/л или 0,5–0,7 г/л композиции. В конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,5 г/л композиции. В другом конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,63 г/л композиции.
N-Ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в питательной композиции в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества. N-ацетилированный (-ые) олигосахарид (-ы) может (могут) присутствовать в суммарном количестве 0,35–0,56 г/100 г композиции, например 0,35–0,52 г/100 г или 0,35–0,49 г/100 г. В конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,35 г/100 г композиции. В другом конкретном варианте осуществления N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,44 г/100 г композиции.
Поэтому в одном варианте осуществления настоящего изобретения питательная композиция содержит по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, причем:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,8–1,5 г/л композиции и/или в суммарном количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества; и/или
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,5–0,8 г/л композиции и/или в суммарном количестве 0,35–0,56 г/100 г композиции в расчете на массу сухого вещества.
В другом конкретном варианте осуществления питательная композиция настоящего изобретения содержит по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, причем:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,85–1,3 г/л композиции и/или в суммарном количестве 0,59–0,9 г/100 г композиции в расчете на массу сухого вещества; и/или
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,5–0,75 г/л композиции и/или в суммарном количестве 0,35–0,52 г/100 г композиции в расчете на массу сухого вещества.
В другом конкретном варианте осуществления питательная композиция настоящего изобретения содержит по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, причем:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 1–1,25 г/л композиции и/или в суммарном количестве 0,69–0,87 г/100 г композиции в расчете на массу сухого вещества; и/или
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,5–0,7 г/л композиции и/или в суммарном количестве 0,35–0,49 г/100 г композиции в расчете на массу сухого вещества.
В другом конкретном варианте осуществления питательная композиция настоящего изобретения содержит по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, причем:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 1,05–1,25 г/л композиции и/или в суммарном количестве 0,73–0,87 г/100 г композиции в расчете на массу сухого вещества; и/или
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,5–0,7 г/л композиции и/или в суммарном количестве 0,35–0,49 г/100 г композиции в расчете на массу сухого вещества.
В конкретном варианте осуществления питательная композиция в соответствии с настоящим изобретением содержит по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, причем:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 1 г/л композиции и/или в суммарном количестве 0,69 г/100 г композиции в расчете на массу сухого вещества; и/или
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,5 г/л композиции и/или в суммарном количестве 0,35 г/100 г композиции в расчете на массу сухого вещества.
В другом конкретном варианте осуществления питательная композиция в соответствии с настоящим изобретением содержит по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, причем:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 1,24 г/л композиции и/или в суммарном количестве 0,86 г/100 г композиции в расчете на массу сухого вещества; и/или
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,63 г/л композиции и/или в суммарном количестве 0,44 г/100 г композиции в расчете на массу сухого вещества.
Фукозилированный (-ые) олигосахарид (-ы) и N-ацетилированный (-ые) олигосахарид (-ы) в составе питательной композиции в соответствии с изобретением, как правило, присутствуют в соотношении фукозилированный (-ые) олигосахарид (-ы) : N-ацетилированный (-ые) олигосахарид (-ы) от 2 : 0,54 до 2 : 2,26, например 2 : 0,76 – 2 : 1,8 или 2 : 0,8 – 2 : 1,4. В особенно преимущественном варианте осуществления такое соотношение составляет 2 : 1 или примерно 2 : 1.
Питательная композиция в соответствии с настоящим изобретением может также содержать по меньшей мере другой (-ие) олигосахарид (-ы) (то есть отличные от фукозилированного (-ых) олигосахарида (-ов) и N-ацетилированного (-ых) олигосахарида (-ов), которые в обязательном порядке присутствуют в композиции) и/или по меньшей мере клетчатку и/или по меньшей мере ее предшественник (-и). Другой олигосахарид и/или клетчатка и/или ее предшественник могут быть выбраны из перечня, содержащего галактоолигосахариды (GOS), фруктоолигосахариды (FOS), инулин, ксилоолигосахариды
(XOS), полидекстрозу, сиалилированные олигосахариды, сиаловую кислоту, фукозу и любую их комбинацию. Они могут присутствовать в количестве от 0 до 10 мас.% композиции. В конкретном варианте осуществления питательная композиция может также содержать по меньшей мере один олигосахарид коровьего молока (BMO).
Приемлемые доступные на рынке продукты, которые можно применять дополнительно к олигосахаридам, содержащимся в смеси олигосахаридов для получения питательных композиций в соответствии с изобретением, включают комбинации FOS с инулином, такие как продукты, продаваемые компанией BENEO под товарным знаком Orafti, или полидекстрозу, продаваемую компанией Tate & Lyle под товарным знаком STA-LITE®.
В конкретном варианте осуществления композиция в соответствии с изобретением может содержать сиалилированный (-ые) олигосахарид (-ы). В ней может присутствовать один или несколько сиалилированных олигосахаридов.
Сиалилированный (-ые) олигосахарид (-ы) может (могут) быть выбран (-ы) из группы, содержащей 3’-сиалиллактозу (3-SL), 6’-сиалиллактозу (6-SL) и любую их комбинацию. В некоторых вариантах осуществления изобретения композиция содержит 3-SL и 6-SL. В некоторых конкретных вариантах осуществления соотношение 3'-сиалиллактозы (3-SL) и 6'-сиалиллактозы (6-SL) может находиться в диапазоне между 5 : 1 и 1 : 10 или от 3 : 1 до 1 : 1, или от 1 : 1 до 1 : 10.
В некоторых конкретных вариантах осуществления сиалилированный олигосахарид композиции представляет собой 6'-сиалиллактозу (6-SL).
Сиалилированный (-ые) олигосахарид (-ы) может (могут) быть выделен (-ы) из природного источника, такого как молоко животных, методами хроматографии или фильтрации. В альтернативном варианте осуществления их можно получать с помощью биотехнологических средств с использованием специфических сиалилтрансфераз или сиалидаз, нейраминидаз, посредством метода ферментации на основе ферментов (рекомбинантных или природных ферментов), путем химического синтеза или метода микробиологической ферментации. В последнем случае либо микроорганизмы могут экспрессировать свои природные ферменты и субстраты, либо могут быть созданы микроорганизмы, вырабатывающие соответствующие субстраты и ферменты. Можно применять культуры микроорганизмов одного вида или смешанные культуры. Образование сиалилолигосахарида может быть инициировано акцепторными субстратами, начиная с любой степени полимеризации (DP) от DP = 1 и далее. В альтернативном варианте осуществления сиалиллактозы можно получать путем химического синтеза из лактозы и свободной N’-ацетилнейраминовой кислоты (сиаловой
кислоты). Сиалиллактозы также имеются в продаже, например производства компании Kyowa Hakko Kogyo, Япония.
В конкретных примерах композиция может содержать от 0,05 до 5 г/л сиалилированного (-ых) олигосахарида (-ов), или от 0,1 до 4 г/л, или от 0,3 до 2 г/л, или от 0,4 до 1,5 г/л, или от 0,4 до 1 г/л, например 0,5 или 0,9 г/л сиалилированного (-ых) олигосахарида (-ов). В некоторых конкретных вариантах осуществления композиция может содержать от 0,8 до 1,7 г/л сиалилированного (-ых) олигосахарида (-ов).
Композиция в соответствии с изобретением может содержать от 0,03 до 3,5 г сиалилированного (-ых) олигосахарида (-ов) на 100 г композиции в расчете на массу сухого вещества, например от 0,1 до 2 г или от 0,2 до 1 г, или от 0,3 до 0,6 г сиалилированного (-ых) олигосахарида (-ов) на 100 г композиции в расчете на массу сухого вещества.
В некоторых конкретных вариантах осуществления настоящего изобретения питательная композиция содержит сиалилированный (-ые) олигосахарид (-ы) в количестве меньше 0,1 г/100 г композиции в расчете на массу сухого вещества.
В некоторых конкретных вариантах осуществления настоящего изобретения питательная композиция не содержит сиалилированный (-ые) олигосахарид (-ы).
Композиция в соответствии с настоящим изобретением может также необязательно содержать по меньшей мере один предшественник олигосахарида. В ней может присутствовать один или несколько предшественников олигосахарида. Например, предшественником олигосахарида грудного молока является сиаловая кислота, фукоза или их смесь. В некоторых конкретных вариантах осуществления композиция содержит сиаловую кислоту.
В конкретных примерах композиция содержит от 0 до 3 г/л предшественника (-ов) олигосахарида, или от 0 до 2 г/л, или от 0 до 1 г/л, или от 0 до 0,7 г/л, или от 0 до 0,5 г/л, или от 0 до 0,3 г/л, или от 0 до 0,2 г/л предшественника (-ов) олигосахарида.
Композиция в соответствии с изобретением может содержать от 0 до 2,1 г предшественника (-ов) олигосахарида на 100 г композиции в расчете на массу сухого вещества, например от 0 до 1,5 г, или от 0 до 0,8 г, или от 0 до 0,15 г предшественника (-ов) олигосахарида на 100 г композиции в расчете на массу сухого вещества.
Питательная композиция настоящего изобретения может дополнительно содержать по меньшей мере один пробиотик (или пробиотический штамм), такой как пробиотический бактериальный штамм.
Наиболее часто применяемыми пробиотическими микроорганизмами являются главным образом бактерии и дрожжи следующих родов: Lactobacillus spp., Streptococcus spp., Enterococcus spp., Bifidobacterium spp. и Saccharomyces spp.
В некоторых конкретных вариантах осуществления пробиотик представляет собой пробиотический бактериальный штамм. В некоторых конкретных вариантах осуществления он представляют собой, в частности, Bifidobacteria и/или Lactobacilli.
Приемлемые пробиотические бактериальные штаммы включают Lactobacillus rhamnosus ATCC 53103, доступный для приобретения у компании Valio Oy, Финляндия, под товарным знаком LGG; Lactobacillus rhamnosus CGMCC 1.3724, Lactobacillus paracasei CNCM I-2116, Lactobacillus johnsonii CNCM I-1225, Streptococcus salivarius DSM 13084, продаваемые компанией BLIS Technologies Limited, Новая Зеландия, под названием KI2; Bifidobacterium lactis CNCM 1-3446, продаваемый в числе прочих компанией Christian Hansen, Дания, под товарным знаком Bb 12; Bifidobacterium longum ATCC BAA-999, продаваемый компанией Morinaga Milk Industry Co. Ltd., Япония, под товарным знаком BB536; Bifidobacterium breve, продаваемый компанией Danisco под товарным знаком Bb-03; Bifidobacterium breve, продаваемый компанией Morinaga под товарным знаком M-16V; Bifidobacterium infantis, продаваемый компанией Procter & GambIe Co. под товарным знаком Bifantis; и Bifidobacterium breve, продаваемый компанией Institut Rosell (Lallemand) под товарным знаком R0070.
Питательная композиция в соответствии с изобретением может содержать от 10e3 до 10e12 КОЕ пробиотического штамма, более предпочтительно от 10e7 до 10e12 КОЕ, например от 10e8 до 10e10 КОЕ пробиотического штамма на грамм композиции в расчете на массу сухого вещества.
В одном варианте осуществления пробиотики являются жизнеспособными. В другом варианте осуществления изобретения пробиотики являются неразмножающимися, или инактивированными. В некоторых других вариантах осуществления могут использоваться как жизнеспособные пробиотики, так и инактивированные пробиотики.
Питательная композиция изобретения может дополнительно содержать по меньшей мере один фаг (бактериофаг) или смесь фагов, предпочтительно направленных против патогенных микроорганизмов Streptococci, Haemophilus, Moraxella и Staphylococci.
Питательная композиция в соответствии с изобретением может представлять собой, например, детскую смесь, начальную детскую смесь, смесь для прикармливаемых детей, детское питание, детскую композицию на зерновой основе, обогатитель, такой как обогатитель грудного молока, или добавку. В некоторых конкретных вариантах осуществления композиция изобретения представляет собой детскую смесь, обогатитель или добавку, которые могут предназначаться для первых 4 или 6 месяцев жизни. В предпочтительном варианте осуществления питательная композиция изобретения представляет собой детскую смесь.
В некоторых других вариантах осуществления питательная композиция настоящего изобретения представляет собой обогатитель. Обогатитель может представлять собой обогатитель грудного молока (например, обогатитель человеческого грудного молока) или обогатитель смеси, такой как обогатитель детской смеси или обогатитель смеси для прикармливаемых детей.
Когда питательная композиция является добавкой, ее можно обеспечивать в форме стандартных доз.
Питательная композиция настоящего изобретения может быть представлена в твердой (например, порошок), жидкой или желеобразной форме.
Питательная композиция в соответствии с изобретением, по существу, содержит источник белка. Белок может содержаться в количестве от 1,6 до 3 г на 100 ккал. В некоторых вариантах осуществления, в частности, когда композиция предназначена для преждевременно родившихся младенцев, такое количество может составлять от 2,4 до 4 г/100 ккал или более 3,6 г/100 ккал. В некоторых других вариантах осуществления количество белка может быть ниже 2,0 г на 100 ккал, например от 1,8 до 2 г/100 ккал, или в количестве ниже 1,8 г на 100 ккал.
Тип белка не считается критическим для настоящего изобретения при условии, что соблюдены минимальные требования по содержанию незаменимых аминокислот и обеспечивается удовлетворительной рост. Таким образом, можно применять источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается белков молочной сыворотки, источник белка может быть основан на кислой сыворотке или сладкой молочной сыворотке или их смесях и может включать альфа-лактальбумин и бета-лактальбумин в любых желаемых соотношениях.
В некоторых преимущественных вариантах осуществления в источнике белка преобладает молочная сыворотка (то есть более 50% белков происходят из белков молочной сыворотки, например 60% или 70%).
Белки могут быть интактными или гидролизованными или могут представлять собой смесь интактных и гидролизованных белков. Под термином «интактный» подразумевается, что основная часть белков интактна, то есть их молекулярная структура не изменена, например не изменено по меньшей мере 80% белков, например не изменено по меньшей мере 85% белков, предпочтительно не изменено по меньшей мере 90% белков, еще более предпочтительно не изменено по меньшей мере 95% белков, например не изменено по меньшей мере 98% белков. В конкретном варианте осуществления 100% белков не изменено.
Термин «гидролизованный» в контексте настоящего изобретения означает белок, который был гидролизован или расщеплен на составляющие его аминокислоты.
Белки могут быть полностью или частично гидролизованными. Может быть желательным вводить частично гидролизованные белки (степень гидролиза от 2 до 20%), например, младенцам или детям младшего возраста, предположительно подверженным риску развития аллергии на коровье молоко. При необходимости использования гидролизованных белков процесс гидролиза может проводиться по желанию и так, как известно в данной области. Например, гидролизаты белка молочной сыворотки можно приготовить ферментативным гидролизом фракции молочной сыворотки в одну или более стадий. Если фракция молочной сыворотки, которая используется в качестве исходного материала, по существу, не содержит лактозы, то установлено, что в процессе гидролиза блокировка лизина белка проявляется в гораздо меньшей степени. Это позволяет снижать степень блокировки лизина с приблизительно 15 мас.% общего лизина до менее приблизительно 10 мас.% лизина; например приблизительно 7 мас.% лизина, что значительно улучшает питательное качество источника белка.
В варианте осуществления изобретения по меньшей мере 70% белков гидролизовано, предпочтительно по меньшей мере 80% белков гидролизовано, например по меньшей мере 85% белков гидролизовано, более предпочтительно по меньшей мере 90% белков гидролизовано, например по меньшей мере 95% белков гидролизовано, в частности по меньшей мере 98% белков гидролизовано. В конкретном варианте осуществления 100% белков гидролизовано.
В одном конкретном варианте осуществления белки питательной композиции гидролизованы, полностью гидролизованы или частично гидролизованы. Степень гидролиза (DH) белка может составлять от 8 до 40, или от 20 до 60, или от 20 до 80, или более 10, 20, 40, 60, 80 или 90.
В конкретном варианте осуществления питательная композиция в соответствии с изобретением представляет собой гипоаллергенную композицию. В другом конкретном варианте осуществления композиция в соответствии с изобретением представляет собой гипоаллергенную питательную композицию.
Питательная композиция в соответствии с настоящим изобретением, по существу, содержит источник углеводов. Это особенно предпочтительно в том случае, когда питательная композиция изобретения представляет собой детскую смесь. В этом случае можно применять любой источник углеводов, традиционно находящийся в детских смесях, такой как лактоза, сукроза, сахароза, мальтодекстрин, крахмал и их смеси, хотя одним из предпочтительных источников углеводов является лактоза.
Питательная композиция в соответствии с настоящим изобретением обычно содержит источник липидов. Это особенно важно, если питательная композиция изобретения представляет собой детскую смесь. В этом случае источником липидов может быть любой липид или жир, который приемлем для применения в детских смесях. Некоторые приемлемые источники жира включают пальмовое масло, подсолнечное масло с высоким содержанием олеиновой кислоты и сафлоровое масло с высоким содержанием олеиновой кислоты. Также можно добавлять незаменимые жирные кислоты — линоленовую кислоту и α-линоленовую кислоту, а также небольшие количества масел, содержащих большие количества арахидоновой кислоты и докозагексаеновой кислоты в готовом виде, например рыбьи жиры или микробные масла. Соотношение n-6 и n-3 жирных кислот в источнике жира может составлять от приблизительно 5 : 1 до приблизительно 15 : 1; например от приблизительно 8 : 1 до приблизительно 10 : 1.
Питательная композиция изобретения может также содержать все витамины и минералы, которые считаются обязательными в повседневном пищевом рационе, в значимых с точки зрения питания количествах. Для некоторых витаминов и минеральных веществ установлены минимальные требования. Примеры минеральных веществ, витаминов и других питательных веществ, необязательно присутствующих в композиции изобретения, включают витамин А, витамин В1, витамин В2, витамин В6, витамин В12, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту, инозитол, ниацин, биотин, пантотеновую кислоту, холин, кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлор, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно добавляют в форме соли. Присутствие и количества конкретных минеральных веществ и других витаминов будут варьироваться в зависимости от целевой популяции.
При необходимости питательная композиция изобретения может содержать эмульгаторы и стабилизаторы, такие как соя, лецитин, сложноэфирные моно- и диглицериды лимонной кислоты и т.п.
Питательная композиция изобретения может также содержать другие вещества, которые могут оказывать благоприятное воздействие, такие как лактоферрин, нуклеотиды, нуклеозиды и т.п.
Питательная композиция изобретения также может содержать каротиноид (-ы). В некоторых конкретных вариантах осуществления изобретения питательная композиция изобретения не содержит каротиноидов.
Питательную композицию в соответствии с изобретением можно готовить любым приемлемым способом. Далее композиция будет описана на примере.
Например, смесь, такую как детская смесь, можно получать путем смешивания источника белка, источника углеводов и источника жира в соответствующих пропорциях. На данном этапе можно включать эмульгаторы в случае их применения. На данном этапе можно добавлять витамины и минералы, но обычно их добавляют позднее для предотвращения термического разложения. Перед перемешиванием в источнике жира можно растворять любые липофильные витамины, эмульгаторы и т.п. Затем можно примешивать воду, предпочтительно воду, очищенную обратным осмосом, с образованием жидкой смеси. Температура воды для удобства находится в диапазоне от приблизительно 50°C до приблизительно 80°C, чтобы облегчать диспергирование ингредиентов. Для образования жидкой смеси можно применять доступные в продаже разжижители.
На данной стадии можно добавлять фукозилированный (-ые) олигосахарид (-ы) и N-ацетилированный (-ые) олигосахарид (-ы), в особенности если конечный продукт должен иметь жидкую форму. Если конечный продукт должен представлять собой порошок, при необходимости их также можно добавлять на данном этапе.
Затем жидкую смесь гомогенизируют, например, в два этапа.
Затем жидкую смесь можно термически обрабатывать для снижения бактериальной нагрузки путем быстрого нагрева жидкой смеси, например, до температуры в диапазоне от приблизительно 80°C до приблизительно 150°C, в течение периода времени, например, от приблизительно 5 секунд до приблизительно 5 минут. Это можно осуществлять путем нагнетания пара или с помощью автоклава или теплообменника, например пластинчатого теплообменника.
Затем жидкую смесь можно охлаждать до температуры от приблизительно 60°C до приблизительно 85°C, например, путем мгновенного охлаждения. Затем жидкую смесь можно снова гомогенизировать, например, в две стадии: под давлением в диапазоне от приблизительно 10 МПа до приблизительно 30 МПа на первой стадии и от приблизительно 2 МПа до приблизительно 10 МПа на второй стадии. Затем гомогенизированную смесь можно дополнительно охлаждать для добавления любых термочувствительных компонентов, например витаминов и минералов. На данном этапе для удобства регулируют рН и содержание твердых веществ в гомогенизированной смеси.
Если конечный продукт должен представлять собой порошок, гомогенизированную смесь переносят в приемлемый сушильный аппарат, такой как распылительная сушилка или сублимационная сушилка, и превращают в порошок. Влагосодержание порошка должно составлять менее приблизительно 5 мас.%. Альтернативно на данном этапе также можно добавлять фукозилированный (-ые) олигосахарид (-ы) и N-ацетилированный (-ые) олигосахарид (-ы) путем сухого смешивания или путем перемешивания их в форме сиропа из кристаллов вместе с пробиотическим (-ими) штаммом (-ами) (при использовании), и смесь подвергают распылительной сушке или сублимационной сушке.
Если предпочтительна жидкая композиция, гомогенизированную смесь можно стерилизовать, а затем асептически разливать в приемлемые контейнеры или можно сначала разливать в контейнеры, а затем стерилизовать в автоклаве.
В другом варианте осуществления, композиция изобретения может представлять собой добавку.
Добавка может быть, например, в форме таблеток, капсул, пастилок или жидкости. Добавка может дополнительно содержать защитные гидроколлоиды (например, камеди, белки, модифицированные крахмалы), связующие вещества, пленкообразующие агенты, инкапсулирующие агенты/материалы, материалы стенок/оболочек, матричные соединения, покрытия, эмульгаторы, поверхностно-активные агенты, солюбилизирующие агенты (масла, жиры, воски, лецитины и т.п.), адсорбенты, носители, наполнители, вспомогательные соединения, диспергирующие агенты, увлажняющие агенты, технологические добавки (растворители), антислеживающие агенты, маскирующие вкус агенты, утяжеляющие агенты, желирующие агенты и гелеобразующие агенты. Добавка может также содержать традиционные фармацевтические добавки и адъюванты, эксципиенты и разбавители, включая, без ограничений, воду, желатин любого происхождения, растительные камеди, лигнинсульфонат, тальк, сахара, крахмал, гуммиарабик, растительные масла, полиалкиленгликоли, ароматизирующие агенты, консерванты, стабилизаторы, эмульгирующие агенты, буферы, смазывающие вещества, красители, увлажняющие агенты, наполнители и т.п.
Дополнительно добавка может содержать органический или неорганический материал-носитель, приемлемый для перорального или парентерального введения, а также витамины, минеральные микроэлементы и другие микроэлементы в соответствии с рекомендациями государственных органов, такими как рекомендуемые нормы потребления (RDA) США.
Питательная композиция в соответствии с изобретением подходит для применения у младенцев или детей младшего возраста. Младенцы или дети младшего возраста могут рождаться в срок или недоношенными. В конкретном варианте осуществления питательная композиция изобретения предназначена для применения у младенцев или детей младшего возраста, которые были рождены недоношенными. В конкретном варианте осуществления питательная композиция изобретения предназначена для применения у недоношенных младенцев.
Питательная композиция настоящего изобретения может также применяться у младенцев или детей младшего возраста, рожденных с помощью кесарева сечения или посредством вагинальных родов. В самом деле, как показано в экспериментальной части, авторы настоящего изобретения смогли продемонстрировать хорошие результаты при введении питательной композиции настоящего изобретения для каждой из упомянутых популяций.
В некоторых вариантах осуществления композиция в соответствии с изобретением может быть предназначена для применения до и/или во время периода отлучения от груди.
Возраст для введения (применения или скармливания) питательной композиции, а также продолжительность такого введения зависит от потребностей. Питательную композицию настоящего изобретения можно применять для целей профилактики или лечения:
- в профилактике и/или лечении инфекций и/или воспалений нижних дыхательных путей и/или уха у младенца или ребенка младшего возраста;
- для снижения температуры у младенца или ребенка младшего возраста;
- для сокращения применения антибиотиков у младенца или ребенка младшего возраста;
- для сокращения применения жаропонижающих средств у младенца или ребенка младшего возраста; и/или
- в профилактике и/или лечении заболеваний/состояний с повышенной температурой и/или требующих введения антибиотиков или жаропонижающих средств младенцу или ребенку младшего возраста.
В некоторых вариантах осуществления питательная композиция применяется в целях профилактики. Питательную композицию можно, например, давать младенцам сразу же после рождения. Композицию изобретения также можно давать в течение первой недели жизни младенца или в течение первых 2 недель жизни, или в течение первых 3 недель жизни, или в течение первого месяца жизни, или в течение первых 2 месяцев жизни, или в течение первых 3 месяцев жизни, или в течение первых 4 месяцев жизни, или в течение первых 6 месяцев жизни, или в течение первых 8 месяцев жизни, или в течение первых 10 месяцев жизни, или в течение первого года жизни, или в течение первых двух лет жизни, или даже дольше. В ряде конкретных преимущественных вариантов осуществления изобретения питательную композицию дают (или вводят) младенцу в период первых от 4 до 6 месяцев после рождения упомянутого младенца.
В некоторых других вариантах осуществления питательную композицию изобретения дают несколько дней (например, 1, 2, 3, 5, 10, 15, 20...) или несколько недель (например, 1, 2, 3, 4, 5, 6 ,7, 8, 9, 10...), или несколько месяцев (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10...) после рождения. В первую очередь это может быть актуально, но не обязательно, в том случае, когда младенец родился преждевременно.
В одном варианте осуществления композицию изобретения дают младенцу или ребенку младшего возраста в качестве композиции, дополнительной к материнскому молоку. В некоторых вариантах осуществления изобретения младенец или ребенок младшего возраста получает материнское молоко в течение по меньшей мере первых 2 недель, первых 1, 2, 4 или 6 месяцев. В одном варианте осуществления питательную композицию изобретения дают младенцу или ребенку младшего возраста после такого периода питания материнским молоком или дают во время такого периода питания материнским молоком. В другом варианте осуществления композицию дают младенцу или ребенку младшего возраста в качестве единственной или основной питательной композиции в течение по меньшей мере одного периода времени, например после 1-го, 2-го или 4-го месяца жизни, в течение по меньшей мере 1, 2, 4 или 6 месяцев.
В одном варианте осуществления питательная композиция изобретения является полной питательной композицией (удовлетворяющей все или большинство питательных потребностей субъекта). В другом варианте осуществления питательная композиция представляет собой добавку или обогатитель, предназначенные, например, для дополнения грудного молока или для дополнения детской смеси или смеси для прикармливаемых детей.
В некоторых других вариантах осуществления питательную композицию изобретения дают в лечебных целях. Чаще всего это наблюдается в случаях применения композиции для лечения инфекций и/или воспалений нижних дыхательных путей и/или уха.
В таких случаях питательную композицию изобретения можно давать в течение нескольких дней (1, 2, 3, 4, 5, 6...), или в течение нескольких недель (1, 2, 3, 4, 5, 6, 7, 8 или даже более), или в течение нескольких месяцев (1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или даже более) в зависимости от потребностей. Ее можно давать сразу после проявления симптомов или после постановки диагноза таких заболеваний/состояний. Ее можно продолжать давать до момента исчезновения симптомов заболеваний/состояний, против которых направлено лечение, или через несколько дней/недель/месяцев после упомянутого исчезновения.
Питательная композиция в соответствии с изобретением может применяться в профилактике и/или лечении инфекций и/или воспалений нижних дыхательных путей и/или уха. Как подробно указывалось выше, инфекции и/или воспаления нижних дыхательных путей и/или уха могут иметь бактериальное происхождение, вирусное происхождение или быть результатом воздействия окружающей среды. В некоторых вариантах осуществления такие инфекции и/или воспаления имеют бактериальное происхождение. В некоторых других вариантах осуществления они имеют вирусное происхождение.
Примерами инфекций и/или воспалений нижних дыхательных путей могут являться пневмония, бронхит и/или бронхиолит. Они могут быть локализованы по меньшей мере в одном из следующих отделов нижних дыхательных путей: в трахее, бронхах, бронхиолах и/или легких. В конкретном примере питательная композиция в соответствии с изобретением применяется в профилактике и/или лечении бронхита.
Инфекциями и/или воспалениями уха могут являться инфекции уха, воспаления уха, отит, отит среднего уха, острый отит среднего уха. Они могут быть локализованы в среднем ухе. В конкретном примере питательная композиция в соответствии с изобретением применяется в профилактике и/или лечении отита или отита среднего уха.
Авторы настоящего изобретения также обнаружили, что конкретная питательная композиция в соответствии с изобретением отличается особой эффективностью в снижении температуры и сокращении применения (то есть введения) антибиотиков и жаропонижающих средств младенцу или ребенку младшего возраста.
Питательная композиция в соответствии с изобретением может также применяться для снижения температуры и/или сокращения применения антибиотиков и жаропонижающих средств у младенца или ребенка младшего возраста дополнительно к профилактике и/или лечению инфекций и/или воспалений нижних дыхательных путей и/или уха.
В конкретном аспекте настоящее изобретение также относится к питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для применения в снижении температуры, и/или сокращении введения антибиотиков, и/или сокращении применения жаропонижающих средств у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
Ранее отмечавшиеся варианты осуществления и примеры (например, относящиеся к типам и количествам олигосахарида, питательной композиции, введению, целевой популяции ...) также применимы к настоящему аспекту.
В другом конкретном аспекте настоящее изобретение также относится к питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для применения в профилактике и/или лечении заболеваний/состояний (например, инфекций, воспалений...), связанных с повышением температуры и/или введением антибиотиков или жаропонижающих средств младенцу или ребенку младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
Ранее отмечавшиеся варианты осуществления и примеры (например, относящиеся к типам и количествам олигосахарида, питательной композиции, введению, целевой популяции ...) также применимы к настоящему аспекту.
Другие цели
Другой целью настоящего изобретения является применение по меньшей мере одного фукозилированного олигосахарида и по меньшей мере одного N-ацетилированного олигосахарида для приготовления питательной композиции для профилактики и/или лечения инфекций и/или воспалений нижних дыхательных путей и/или уха у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л питательной композиции и/или в суммарном количестве 0,52–1,15 г/100 г питательной композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л питательной композиции и/или в суммарном количестве 0,31–0,59 г/100 г питательной композиции в расчете на массу сухого вещества.
Другой целью настоящего изобретения является применение по меньшей мере одного фукозилированного олигосахарида и по меньшей мере одного N-ацетилированного олигосахарида для приготовления питательной композиции для снижения температуры, и/или сокращения введения антибиотиков, и/или сокращения введения жаропонижающих средств, и/или профилактики и/или лечения заболеваний/состояний (например, инфекций, воспалений...), связанных с повышением температуры и/или введением антибиотиков или жаропонижающих средств младенцу или ребенку младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
Другая цель настоящего изобретения относится к применению питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для снижения температуры и/или сокращения введения антибиотиков или жаропонижающих средств у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
Ранее отмечавшиеся варианты осуществления и примеры (например, относящиеся к типам и количествам олигосахарида, питательной композиции, применению, целевой популяции ...) также применимы к перечисленным целям (то есть аспектам применения).
Другой целью настоящего изобретения является фармацевтическая композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид для профилактики и/или лечения инфекций и/или воспалений нижних дыхательных путей и/или уха у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л питательной композиции и/или в суммарном количестве 0,52–1,15 г/100 г питательной композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л питательной композиции и/или в суммарном количестве 0,31–0,59 г/100 г питательной композиции в расчете на массу сухого вещества.
Другой целью настоящего изобретения является фармацевтическая композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для применения в снижении температуры, и/или сокращении введения антибиотиков, и/или сокращении введения жаропонижающих средств у младенца или ребенка младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
В другом конкретном аспекте настоящее изобретение также относится к фармацевтической композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для применения в профилактике и/или лечении заболеваний/состояний (например, инфекций, воспалений...), связанных с повышением температуры и/или введением антибиотиков и/или введением жаропонижающих средств младенцу или ребенку младшего возраста, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
Ранее отмечавшиеся варианты осуществления и примеры (например, относящиеся к типам и количествам олигосахарида, питательной композиции, введению, целевой популяции ...) также применимы к перечисленным целям (то есть к фармацевтической композиции).
Другая цель настоящего изобретения относится к способу профилактики и/или лечения инфекций и/или воспалений нижних дыхательных путей и/или уха у младенца или ребенка младшего возраста, причем упомянутый способ включает введение упомянутому младенцу или ребенку младшего возраста питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л питательной композиции и/или в суммарном количестве 0,52–1,15 г/100 г питательной композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л питательной композиции и/или в суммарном количестве 0,31–0,59 г/100 г питательной композиции в расчете на массу сухого вещества.
Другой целью настоящего изобретения является способ снижения температуры и/или сокращения введения антибиотиков, и/или сокращения введения жаропонижающих средств, и/или профилактики и/или лечения заболеваний/состояний (например, инфекций, воспалений...), связанных с повышением температуры и/или введением антибиотиков у младенца или ребенка младшего возраста, причем упомянутый способ включает введение упомянутому младенцу или ребенку младшего возраста питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, в которой:
- фукозилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,75–1,65 г/л питательной композиции и/или в суммарном количестве 0,52–1,15 г/100 г питательной композиции в расчете на массу сухого вещества; и
- N-ацетилированный (-ые) олигосахарид (-ы) присутствует (-ют) в суммарном количестве 0,45–0,85 г/л питательной композиции и/или в суммарном количестве 0,31–0,59 г/100 г питательной композиции в расчете на массу сухого вещества.
Различные варианты осуществления, подробности и примеры, ранее описанные в спецификации (например, относящиеся к типам и количествам олигосахарида, питательной композиции, введению, целевой популяции ...), также применимы к перечисленным целям (то есть к способам).
Примеры
Следующие примеры демонстрируют некоторые конкретные варианты осуществления композиции для применения в соответствии с настоящим изобретением. Примеры приводятся исключительно в целях иллюстрации и не должны рассматриваться в качестве ограничений настоящего изобретения.
Пример 1
Ниже в таблице 1 приведен пример состава питательной композиции (например, детской смеси) в соответствии с настоящим изобретением. Эта композиция приводится исключительно в качестве иллюстрации.
Таблица 1. Пример состава питательной композиции (например, детской смеси) в соответствии с настоящим изобретением
Пример 2
Описание исследования
Проводилось контролируемое, слепое, рандомизированное, многоцентровое, интервенционное клиническое исследование для 2 параллельных групп. Младенцев отбирали и рандомизировали в одну из 2 исследовательских групп в течение 14 дней после рождения. Исследовательские группы предусматривали использование классической начальной детской смеси без ОГМ [контроль] или этой же классической начальной детской смеси с добавкой 2 ОГМ [ОГМ].
Композиция испытываемой детской смеси с добавкой или без добавки ОГМ была идентична композиции, приведенной в таблице 1, за исключением того, что:
- контрольная детская смесь не содержала олигосахаридов/ОГМ (то есть не содержала 2’-фукозиллактозы и лакто-N-неотетраозы);
- испытываемая детская смесь с ОГМ содержала 2’-фукозиллактозу, но в количестве 1,24 г/л (что соответствовало количеству 0,86 г/100 г порошка до растворения; для растворения использовали 129,18 г порошка/900 мл), а также лакто-N-неотетраозу, но в количестве 0,63 г/л (что соответствовало 0,44 г/100 г порошка до растворения; для растворения использовали 129,18 г порошка/900 мл).
Введение питания для отлучения от груди начинали с возраста 4 месяца.
Исследование включало период лечения 6 месяцев ± 7 дней с применением одного из двух вариантов лечения с последующим периодом наблюдения 6 месяцев без лечения.
Результаты
Авторы изобретения неожиданно обнаружили, что младенцы из группы ОГМ (то есть получавшие классическую смесь с добавками 1,24 г/л 2’-фукозиллактозы и 0,63 г/л лакто-N-неотетраозы) меньше заболевали бронхитом (фиг. 1). Приводится число младенцев с по меньшей мере одним случаем бронхита.
Авторы изобретения также неожиданно обнаружили, что младенцы из группы ОГМ, как правило, меньше страдали от инфекций/воспалений уха (фиг. 2). Приводится число младенцев с по меньшей мере одним случаем инфекций/воспалений уха. К регистрируемым примерам инфекций и/или воспалений уха относятся любые инфекции уха, воспаления уха, отит, отит среднего уха, острый отит среднего уха, отит наружного уха, мастоидит или лабиринтит, диагностированные врачом или медицинским работником.
Авторы изобретения также неожиданно обнаружили, что младенцам из группы ОГМ требовалось меньше антибиотиков (фиг. 3), и температура у них была ниже (фиг. 4).
Эти эффекты наблюдались независимо от способа введения.
Оценка числа случаев на группу подтверждает описанные выше результаты (фиг. 5 и 6). В частности, у младенцев, которые получали испытательную смесь с ОГМ, отмечалось меньше случаев (i) бронхита (фиг. 5A и 6A), (ii) инфекций/воспалений уха (фиг. 5B и 6B), (iii) применения антибиотиков (фиг. 5C и 6C) и (iv) применения жаропонижающих средств (фиг. 5D и 6D).
Все перечисленные результаты наблюдались в течение всего периода проведения эксперимента (12-месячный период), например от 0 до 4 месяцев, от 0 до 6 месяцев и от 0 до 12 месяцев.
Таким образом, композиция, содержащая по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид в заявленных количествах, является весьма эффективной для младенцев для применения в профилактике и/или лечении инфекций и/или воспалений нижних дыхательных путей и уха, а также для снижения температуры и сокращения введения антибиотиков и жаропонижающих средств у упомянутых младенцев.
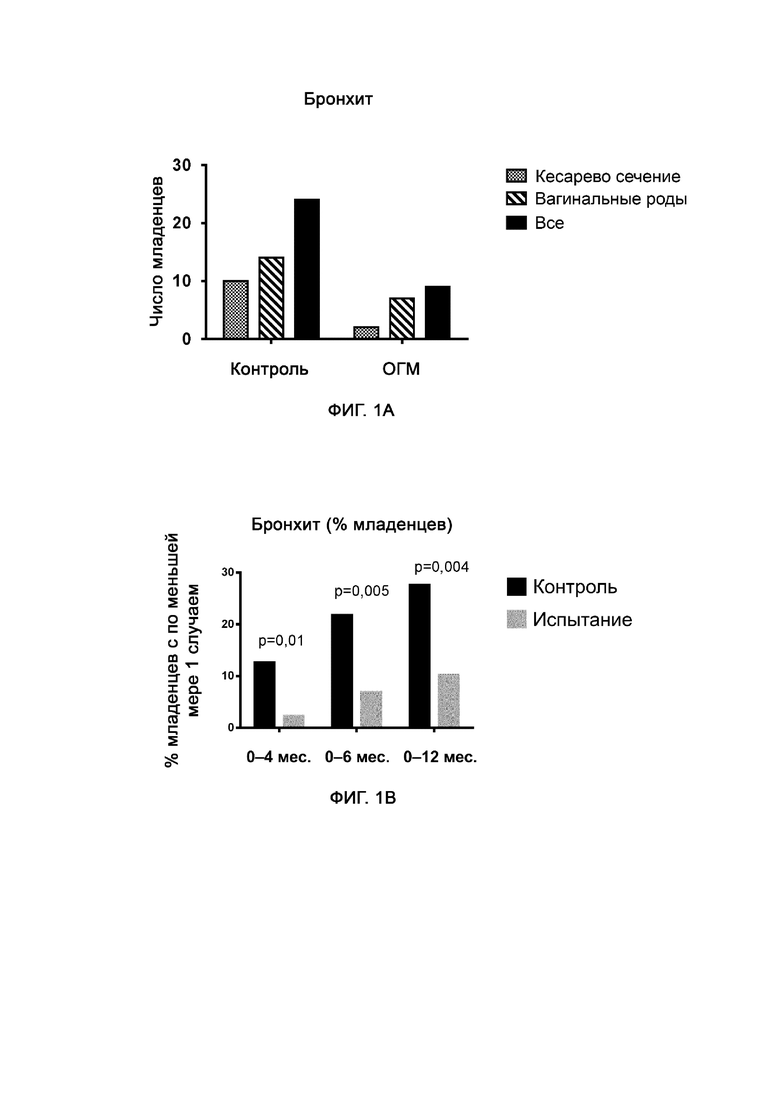


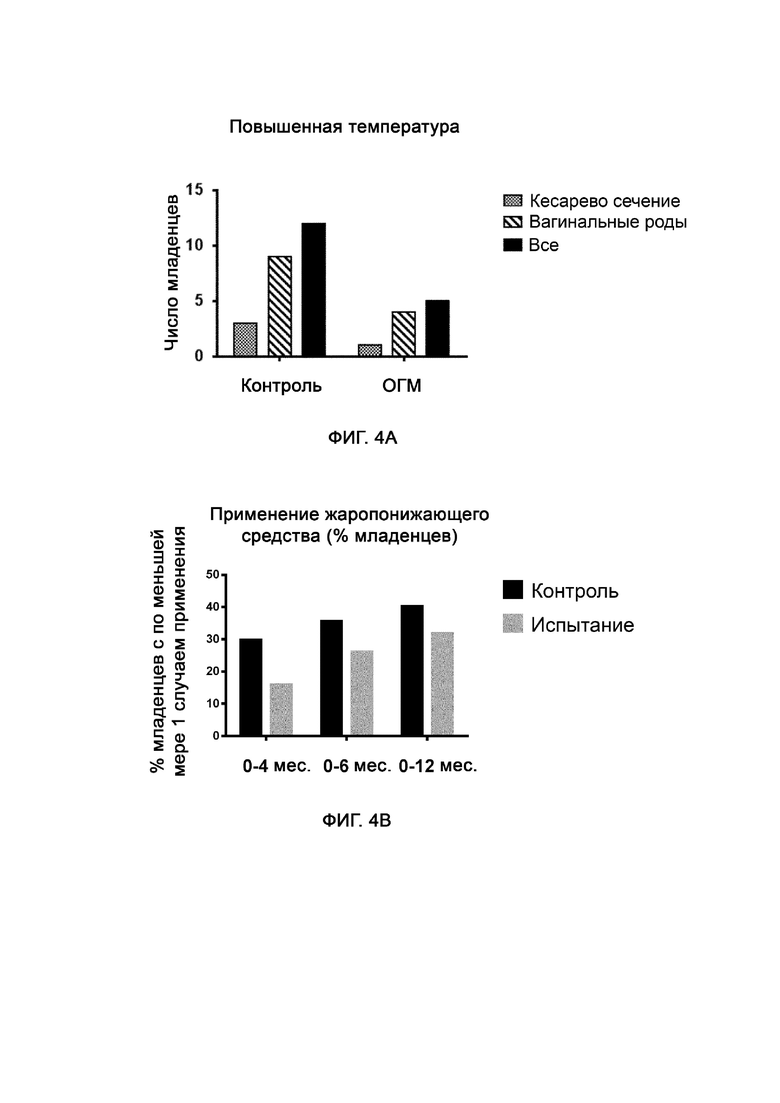
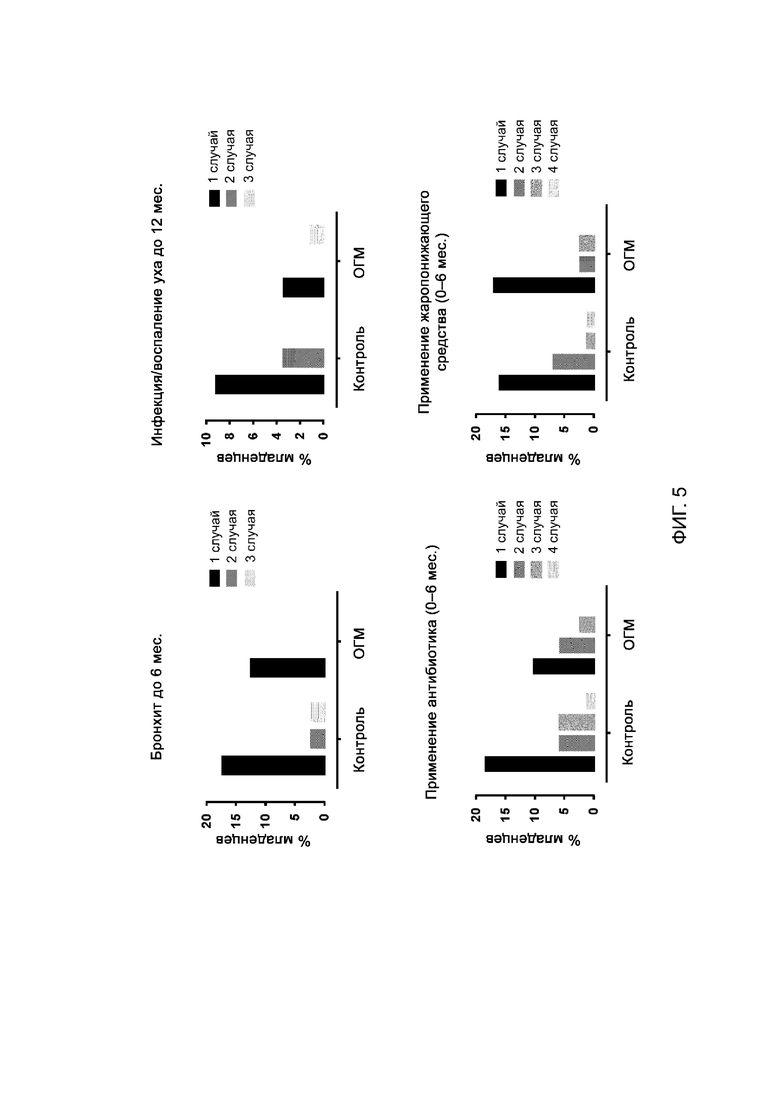
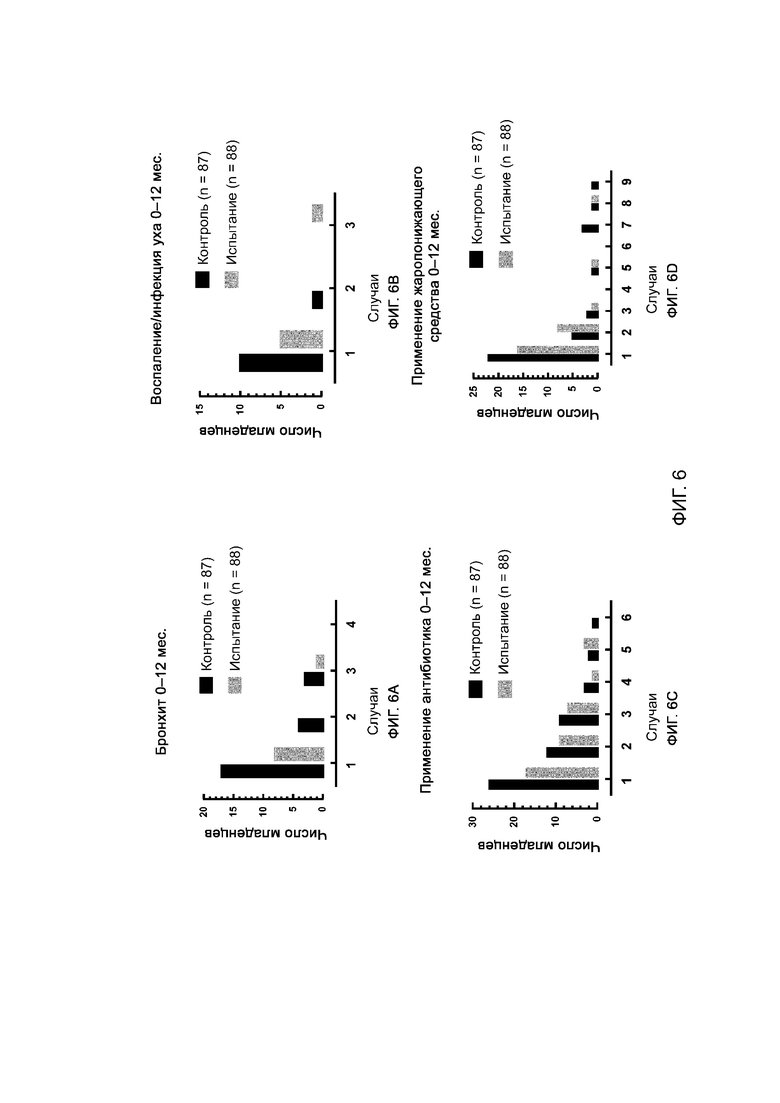
Настоящее изобретение относится к области медицины, а именно к применению питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для снижения температуры и/или сокращения введения антибиотиков и/или жаропонижающих средств младенцу или ребенку младшего возраста, в которой фукозилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и N-ацетилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества. Настоящее изобретение обеспечивает синергетическое воздействие по меньшей мере одного фукозилированного олигосахарида и по меньшей мере одного N-ацетилированного олигосахарида в случае их применения для снижения температуры и/или сокращения введения антибиотиков и/или жаропонижающих средств младенцу или ребенку младшего возраста. 12 з.п. ф-лы, 6 ил., 1 табл., 2 пр.
1. Применение питательной композиции, содержащей по меньшей мере один фукозилированный олигосахарид и по меньшей мере один N-ацетилированный олигосахарид, для снижения температуры и/или сокращения введения антибиотиков и/или жаропонижающих средств младенцу или ребенку младшего возраста, в которой
- фукозилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,75–1,65 г/л композиции и/или в суммарном количестве 0,52–1,15 г/100 г композиции в расчете на массу сухого вещества; и
- N-ацетилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,45–0,85 г/л композиции и/или в суммарном количестве 0,31–0,59 г/100 г композиции в расчете на массу сухого вещества.
2. Применение по п. 1, где фукозилированный олигосахарид выбирают из перечня, состоящего из 2’-фукозиллактозы, 3’-фукозиллактозы, дифукозиллактозы, лакто-N-фукопентаозы I, лакто-N-фукопентаозы II, лакто-N-фукопентаозы III, лакто-N-фукопентаозы V, лакто-N-фукогексаозы, лакто-N-дифукогексаозы I, фукозиллакто-N-гексаозы, фукозиллакто-N-неогексаозы I, фукозиллакто-N-неогексаозы II, дифукозиллакто-N-гексаозы I, дифукозиллакто-N-неогексаозы I, дифукозиллакто-N-неогексаозы II, фукозил-пара-лакто-N-гексаозы и любой их комбинации.
3. Применение по любому из предшествующих пунктов, где фукозилированный олигосахарид содержит 2'-фукозил-эпитоп.
4. Применение по любому из предшествующих пунктов, где фукозилированный олигосахарид представляет собой 2’-фукозиллактозу (2’FL).
5. Применение по любому из предшествующих пунктов, где N-ацетилированный олигосахарид представляет собой лакто-N-тетраозу (LNT), лакто-N-неотетраозу (LNnT) или любую их комбинацию.
6. Применение по любому из предшествующих пунктов, где N-ацетилированный олигосахарид представляет собой лакто-N-неотетраозу (LNnT), пара-лакто-N-неогексаозу (пара-LNnH) или любую их комбинацию, причем N-ацетилированный олигосахарид предпочтительно представляет собой лакто-N-неотетраозу (LNnT).
7. Применение по любому из предшествующих пунктов, где питательная композиция содержит 2’-фукозиллактозу и лакто-N-неотетраозу (LNnT) или содержит смесь олигосахаридов, состоящую из 2’-фукозиллактозы (2’FL) и лакто-N-неотетраозы (LNnT).
8. Применение по любому из предшествующих пунктов, где
фукозилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,8–1,5 г/л композиции и/или в суммарном количестве 0,55–1,05 г/100 г композиции в расчете на массу сухого вещества; и/или
N-ацетилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,5–0,8 г/л композиции и/или в суммарном количестве 0,35–0,56 г/100 г композиции в расчете на массу сухого вещества.
9. Применение по любому из предшествующих пунктов, где
фукозилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,85–1,3 г/л композиции и/или в суммарном количестве 0,59–0,9 г/100 г композиции в расчете на массу сухого вещества; и/или
N-ацетилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,5–0,75 г/л композиции и/или в суммарном количестве 0,35–0,52 г/100 г композиции в расчете на массу сухого вещества.
10. Применение по любому из предшествующих пунктов, где
фукозилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 1–1,25 г/л композиции и/или в суммарном количестве 0,69–0,87 г/100 г композиции в расчете на массу сухого вещества; и/или
N-ацетилированный(-ые) олигосахарид(-ы) присутствует(-ют) в суммарном количестве 0,5–0,7 г/л композиции и/или в суммарном количестве 0,35–0,49 г/100 г композиции в расчете на массу сухого вещества.
11. Применение по любому из предшествующих пунктов, где питательная композиция содержит по меньшей мере другой(-ие) олигосахарид(-ы) и/или клетчатку, и/или ее предшественник(-и), которые выбирают из перечня, содержащего галактоолигосахариды (GOS), фруктоолигосахариды (FOS), ксилоолигосахариды (XOS), инулин, полидекстрозу, сиалилированные олигосахариды, сиаловую кислоту, фукозу и любые их комбинации.
12. Применение по любому из предшествующих пунктов, где питательная композиция дополнительно содержит по меньшей мере один пробиотик в количестве от 103 до 1012 КОЕ/г указанной композиции (масса сухого вещества).
13. Применение по любому из предшествующих пунктов, где питательная композиция представляет собой детскую смесь, начальную детскую смесь, детскую смесь для прикармливаемых детей, детское питание, детскую композицию на зерновой основе, обогатитель или добавку.
| US 2015031645 A1, 29.01.2015 | |||
| US 20120172319 A1, 05.07.2012. |
Авторы
Даты
2020-04-27—Публикация
2016-03-04—Подача