Изобретение относится к области медицины и может быть использовано при лечении женщин, имевших многократные неудачные попытки экстракорпорального оплодотворения.
Статистические данные по женскому бесплодию свидетельствуют о значительном росте данной патологии за последнее 10-летие. Среди причин часто называют хронические заболевания женской репродуктивной системы. Лидирующие позиции занимают эндометриоз и воспалительные заболевания малого таза.
Хронический эндометрит (ХЭ) в современных условиях трактуется как субклиническое воспалительное заболевание, сопровождающееся нарушением репродуктивной функции. Бесплодие, невынашивание беременности, эктопическая беременность, неудачи при проведении программ вспомогательных репродуктивных технологий и другие нарушения репродукции типичны для данной патологии.
Доказано, что при ХЭ существенно нарушаются межклеточные взаимодействия, повреждается внеклеточный матрикс, нарушаются процессы клеточной выживаемости, поддержания тканевой архитектоники, экспрессии и функционирования стероидных рецепторов. Все это приводит к выраженным изменениям функциональных параметров эндометрия, дегенеративным и трофическим расстройствам (гипоплазия, формирование "тонкого эндометрия") и, в итоге, к нарушению рецептивности эндометрия, т.е. его способности к эффективной имплантации эмбриона, и к бесплодию.
Известно, что низкая рецептивность эндометрия является причиной подавляющего числа неудач при имплантации эмбриона, в том числе при проведении программ экстракорпорального оплодотворения (ЭКО), и одной из главных причин женского бесплодия.
Согласно данным современной молекулярной медицины, к числу ключевых регуляторов процессов рецептивности эндометрия, предопределяющих фертильность, принадлежат гены и кодируемые ими белки НОХА10 и НОХА11 [Hsieh-Li Н. М, Witte D. P., Weinstein М., Branford W., Li Н., Small К. et al. Ноха 11 structure, extensive antisense transcription, and function in male and female fertility. Development. 1995; 121(5): 1373-85; Kwon H.E., Taylor H.S. The role of HOX genes in human implantation. In Annals of the New York Academy of Sciences. 2004; 1034: 1-18].
HOXA10 и НОХА11 экспрессируются в клетках эндометрия в различных сегментах матки, причем данный процесс является гормонозависимым и активируется под действием прогестерона и эстрогенов в секреторной фазе менструального цикла, достигая максимума в период "окна имплантации" [Taylor H.S. The role of HOX genes in human implantation. Hum Reprod Update. 2000; 6(1): 75-9]. HOXA10 регулирует экспрессию маркеров рецептивности эндометрия: белка клеточной адгезии интегрина β3 [Daftary G.S., Troy P.J., Bagot С.N., Young S.L., H.S. Taylor. Direct regulation of beta3-integrin subunit gene expression by HOXA10 in endometrial cells. Mol. Endocrinol. 2002; 16: 571-579], белка, связывающего инсулиноподобный фактор белка IGFBP-1 [Kim J.J., Taylor H.S.,. Akbas G.E, Foucher I., Trembleau A., Jaffe R.C. et al. Regulation of insulin-like growth factor binding protein-1 promoter activity by FKHR and HOXA10 in primate endometrial cells. Biol. Reprod. 2003; 68: 24-30].
Показано, что у больных эндометриозом экспрессия генов НОХА10 и НОХА11 в эндометрии снижена по причине их аномального гиперметилирования в регуляторном (промоторном) участке. При этом снижается содержание и других клеточных компонентов и белков-медиаторов рецептивности эндометрия, регулируемых генами НОХ, таких как эндометриальные пиноподии, интегрин αvβ3, белок IGFBP-1 [Cakmak Н., Taylor H.S. Molecular mechanisms of treatment resistance in endometriosis: the role of progesterone-hox gene interactions. Semin Reprod Med. 2010 28(1): 69-74].
Известно, что снижение уровня содержания белка в ткани может быть вызвано как генетическими причинами (мутацией или полиморфизмом кодирующего его гена), так и эпигенетическими отклонениями, например, метилированием промоторной области гена. Такое метилирование происходит по цитозиновому остатку под действием фермента ДНК-метилтрансферазы в строго определенных участках гена, так называемых динуклеотидных островках CpG, которые содержатся в промоторной области подавляющего большинства генов. Промоторное метилирование приводит к снижению экспрессии гена, вплоть до его полной инактивации ("эпигенетического молчания") и является одним из ключевых механизмов эпигенетической регуляции [Zhang X, Hu М, Lyu X, Li С, Thannickal VJ, Sanders YY, DNA methylation regulated gene expression in organ fibrosis. Biochim Biophys Acta Mol Basis Dis. 2017; 1863(9):2389-2397.].
Было показано, что гены НОХА гиперметилированы и, как следствие, неактивны у 70-100% бесплодных женщин с эндометриозом и миомой, а также у 56% женщин с необъяснимым бесплодием [Cakmak Н., Taylor H.S. Implantation failure: molecular mechanisms and clinical treatment. Hum Reprod Update. 2011 17(2): 242-53; Cakmak H., Taylor H.S. Molecular mechanisms of treatment resistance in endometriosis: the role of progesterone-hox gene interactions. Semin Reprod Med. 2010; 28(1): 69-74]. В то же время метилирование генов НОХА10 и НОХА11 в образцах ткани, взятых у здоровых доноров, отсутствовало [Wu Y., Halverson G., Basir Z., Strawn E., Yan P., Guo S.-W. Aberrant methylation at HOXA10 may be responsible for its aberrant expression in the endometrium of patients with endometriosis. Am. J. Obstet. Gynecol. 2005; 193(2): 371-80]. Эти данные позволили, во-первых, говорить об эпигенетической составляющей патогенеза данных заболеваний, а, во-вторых, о ДНК-метилировании как о потенциальном диагностическом маркере состояния бесплодия, возникающего при указанных патологиях [Сухих Г.Т., Осипьянц А.И., Мальцева Л.И., Смолина Г.Р., Полозников А.А., Муйжнек Е.Л., Киселев В.И. Аномальное гиперметилирование генов НОХА10 и НОХА11 при бесплодии, ассоциированном с хроническим эндометритом, Акушерство и гинекология, 2015, №12, стр. 69-74]. В отличие от мутаций, нарушающих структуру гена, эпигенетические модификации, в частности, метилирование промоторных участков гена, являются обратимыми. Этот факт позволяет рассматривать возможность восстановления активности генов, чья экспрессия нарушена в результате метилирования [Omar Castillo-Aguilera, Patrick Depreux, Ludovic Halby, Paola B. Arimondo, Laurence Goossens, DNA Methylation Targeting: The DNMT/HMT Crosstalk Challenge. Biomolecules 2017, 7, 3].
В литературе имеются указания на восстановление активности генов путем воздействия на клетки-мишени веществами, ингибирующими внутриклеточную ДНК-метилтрансферазу [Neeraj К. Saxena, Dipali Sharma, Epigenetic Reactivation of Estrogen Receptor: Promising Tools for Restoring Response to Endocrine Therapy. Mol Cell Pharmacol. 2010 2(5): 191-202; Won Jun Lee, Joong-Youn Shim, Bao Ting Zhu, Mechanisms for the Inhibition of DNA Methyltransferases by Tea Catechins and Bioflavonoids. Mol Pharmacol 2005 68:1018-1030].
В результате такого воздействия на делящиеся клетки происходит снижение уровня метилирования генов и восстановление их функциональной активности. Индол-3-карбинол (I3С) способен проявлять эпигенетическую деметилирующую активность. На модели опухолевых клеток поджелудочной железы методом RT-PCR-анализа, позволяющим определить уровень ДНК-метилирования, было показано, что I3С дозозависимым образом деметилировал (удалял метильную группу) из промоторной области гена р16 INK4а и, как следствие, реактивировал его [Lyn-Cook B.D., Mohammed S.I., Davis С. et al. (2010) Gender differences in gemcitabine (Gemzar) efficacy in cancer cells: effect of indole-3-carbinol. Anticancer Res., 30(12), 490704913]. Ранее нами был разработан препарат на основе индол-3-карбинола обладающий деметилирующей активностью (RU 2601893 С1, опуб. 10.11.2016)
Для эпигаллокатехин-3-галлата (EGCG) также установлен деметилирующий эффект, обусловленный ингибированием активности ДНК-метилтранфераз [Ruchi Aggarwal, Meenakshi Jha, Anju Shrivastava, Abhimanyu Kumar Jha, Natural Compounds: Role in Reversal of Epigenetic Changes, Biochemistry (Moscow) 2015 Vol. 80, No. 8, pp. 972-989].
Важно отметить, что индол-3-карбинол и эпигаллокатехин-3-галлат обладают противовоспалительным эффектом, ингибируя образование инфламмасом, внутриклеточных структур, запускающих хронический воспалительный процесс. Известно, что воспаление является сильным стимулом инициирующим эпигенетические модификации и, в частности, метилирование [ AM, Mendoza-Rodriguez MG, Urrutia-Cabrera D, Dommguez-Robles MC,
AM, Mendoza-Rodriguez MG, Urrutia-Cabrera D, Dommguez-Robles MC,  EA, Ayala-Sumuano JT, Meza IL-1β induced methylation of the estrogen receptor ERα gene correlates with EMT and chemoresistance in breast cancer cells. Biochemical and Biophysical Research Communications (2017) 490(3)].
EA, Ayala-Sumuano JT, Meza IL-1β induced methylation of the estrogen receptor ERα gene correlates with EMT and chemoresistance in breast cancer cells. Biochemical and Biophysical Research Communications (2017) 490(3)].
Современные протоколы ЭКО не учитывают эпигенетический фактор бесплодия. Самые последние исследования по лечению хронического эндометрита, как фактора бесплодия даже не упоминают эпигенетические причины этого состояния [К.Г. Серебренникова, И.И. Бабиченко, Н.А. Арутюнян, С.Н. Кацалап, А.С. Акатьева, Новое в диагностике и терапии хронического эндометрита при бесплодии, Gynecology. 2019; 21 (1): 14-18]. За прототип принят описанный в данной работе способ восстановления репродуктивной функции у женщин с неудачными попытками экстракорпорального оплодотворения, заключающийся в лечении хронического эндометрита методом внутривенной фотодинамической терапии в сочетании с гормональной терапией с применением 17β-экстрадиола трандермально по 2 мг 1 раз в сутки с 5 по 28 день месячного цикла. Эффективность имплантации эмбриона после такого лечения не превышает 40%.
Технической проблемой данного изобретения является разработка диагностического алгоритма и эпигенетической лекарственной коррекции гена, ответственного за рецептивность эндометрия НОХА 10 у женщин, страдающих бесплодием.
Техническая проблема решается способом восстановления репродуктивной функции у женщины с многократными неудачными попытками экстракорпорального оплодотворения (ЭКО), страдающей бесплодием на фоне хронического эндометрита, включающим проведение женщине исследования уровня метилирования гена рецептивности эндометрия НОХА10, при высоком уровне метилирования указанного гена проводят терапию по схеме: индол-3-карбинол 300-500 мг в сутки 2 раза в день и эпигаллокатехин-3-галлат 400-600 мг в сутки 2 раза в день в течение 3 месяцев, после чего проводят повторное исследование уровня метилирования указанного гена, в случае отсутствия метильных групп в указанном гене женщине назначают подготовку к ЭКО, а в случае сохранения уровня метилирования указанного гена женщине назначают повторную терапию по указанной схеме в течение еще 3 месяцев.
Технический результат, достигаемый изобретением, заключается в повышении эффективности имплантации эмбриона после лечения предложенным способом.
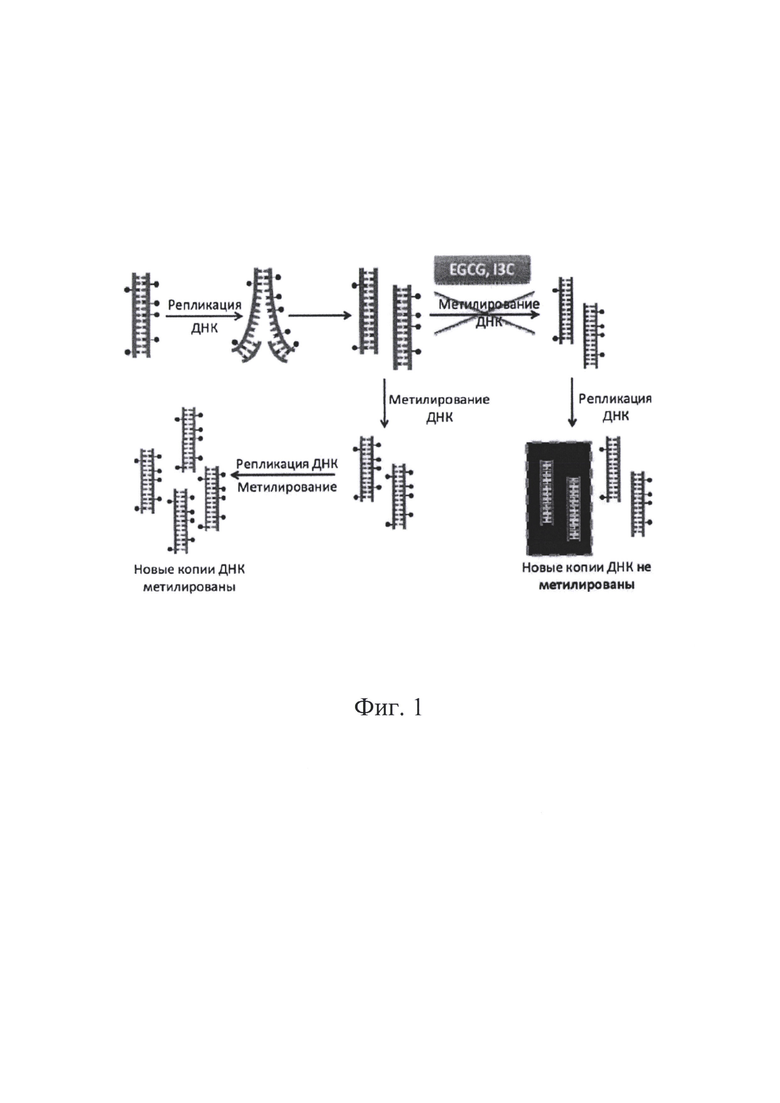
На фиг. 1 представлена схема репликации ДНК при метилировании гена НОХА10 и при проведении терапии препаратами индол-3-карбинол и эпигаллокатехин-3-галлат.
На фиг. 2 показаны результаты исследования уровня метилирования генов рецептивности эндометрия НОХА10 у группы женщин, страдающих бесплодием на фоне хронического эндометрита.
На фиг. 3 показаны результаты исследования уровня метилирования генов рецептивности эндометрия НОХА10 у женщин после проведенной эпигенетической терапии.
Результативность данного подхода может быть проиллюстрирована следующими примерами.
Пример 1
Исследование образцов эндометрия у женщин, страдающих бесплодием на предмет метилирования гена НОХА10
Образцы ткани. Биоптаты эутопического эндометрия были получены у 16 пациенток в возрасте от 28 до 40 лет, страдающих бесплодием на фоне хронического эндометрита, в ходе диагностической контрольной гистероскопии и лечебно-диагностического выскабливания полости матки. Полученные образцы ткани были трижды промыты буфером PBS (натрий-фосфатный буфер) и заморожены при температуре -20°С перед отправкой на исследование.
Выделение ДНК. Полученные образцы эндометрия измельчали хирургическим скальпелем и гомогенизировали в гомогенизаторе FastPrep®-24 (MP Biomedicals, США) с добавлением матрикса D. Из полученных образцов выделяли ДНК с использованием и по протоколу набора ReliaPrep™ gDNA Tissue Miniprep System (Promega, США). Концентрацию ДНК определяли флуориметрически с использованием стандартного набора Qubit dsDNA HS Assay Kit на флуориметре Qubit 2.0 (Life Technologies, США).
Бисульфитная конверсия. 150 нг полученной ДНК подвергали бисульфитной конверсии (переводу неметилированных остатков цитозина в тимин при сохранении метилированных остатков цитозина в неизмененном виде) с использованием набора MethylEdge™ Bisulfite Conversion System (Promega, США). Концентрацию конвертированной ДНК определяли фотометрически в планшете ц-drop (BMG Labtech, Германия) с использованием мультидетектора CLARIOstar (BMG Labtech, Германия).
Проведение ПЦР. 20 нг бисульфит-конвертированной ДНК отбирали для последующей ПЦР-амплификации с использованием полимеразной смеси GoTaq™ Hot Start Green Master Mix (Promega, США) и следующих праймеров:
HOXA10F
5' -TATGATATTGTTGTGGGATAATTTG-3'
HOXA10R
5 '-CATAAACACCCCACTTATTAACTAC-3'
HOXA11F
5' - ATTAGTATTTTTTTGTTAAGGATGGG-3'
HOXA11R
5 '-CCTACAAACAATCTCTATACAC-3'
Наличие и размер (длину) ПЦР-продуктов определяли посредством электрофореза в 2,5% агарозном геле с маркерами молекулярного веса 100 bp Molecular Ruler (Bio-Rad, США). Полученные ПЦР-продукты выделяли из геля с использованием набора PureLink Quick Gel Extraction Kit (Invitrogen, США).
Секвенирование. Секвенирование проводилось по стандартному протоколу с использованием прямых праймеров и набора реактивов ABI PRISM® BigDye™ Terminator v. 3.1. Анализ продуктов реакции проводили на автоматическом секвенаторе Applied Biosystems 3730 DNA Analyzer (Applied Biosystems, США).
Статистический анализ. Статистический анализ результатов секвенирования проводили с использование программного обеспечения DNA Sequencing Analysis Software версии 5.1 (Applied Biosystems, США) и BiQ Analyzer (biq-analyzer.bioinf.mpi-inf.mpg.de). Уровень ДНК-метилирования оценивали качественно (наличие/отсутствие).
Полученные результаты представлены в виде таблицы на фиг.2, где темным цветом отмечены участки метилирования генов. Из таблицы следует, что из 16 исследуемых образцов эндометрия в 7 образцах не выявлено метилирование промотора гена HOX10 (высоким уровнем метилирования гена НОХА10 считалось две и более метальных групп). Вероятно, бесплодие у этих женщин обусловлено факторами, не связанными с эпигенетическими изменениями гена рецептивности. В 9 случаях обнаружен высокий уровень метилирования, что явилось основанием для назначения им эпигенетической терапии.
Пример 2
Проведение эпигенетической терапии препаратами на основе индол-3-карбинола и эпигаллокатехин-3-галлат у женщин с гиперметилированным геном HОХА10
Для проведения терапии были отобраны 9 женщин с высоким уровнем метилирования гена НОХА10.
При высоком уровне метилирования гена НОХА10 (две и более метильных групп) в рамках прегравидарной подготовки, проводится предварительная эпигенетическая терапия по следующей схеме: индол-3-карбинол 300 мг в сутки женщинам с весом до 70 кг и 500 мг в сутки женщинам с весом свыше 70 кг дробно - 2 раза в день + эпигаллокатехин-3-галлат 400 мг в сутки женщинам с весом до 70 кг и 600 мг в сутки женщинам с весом свыше 70 кг дробно - 2 раза в день) в течение 3-6 месяцев. После 3-месячного приема препаратов производился повторный анализ на метилирование генов. В случае отсутствия метальных групп в исследуемых генах, женщинам назначали стандартный протокол для подготовки к ЭКО. Результаты анализов метилирования генов после терапии представлены в таблице на фиг. 3. При сохранении уровня метилирования исследуемых генов, терапия была продолжена еще в течении 3 месяцев.
Пример 3
Эффективность ЭКО у женщин после проведенной эпигенетической терапии
У 9 женщин с диагнозом бесплодие и высоким уровнем метилирования гена НОХ10, прошедших две и более неудачных попыток ЭКО, после проведения эпигенетической терапии и подтверждения деметилирования гена НОХ10 была проведена очередная процедура ЭКО в соответствии с международными протоколами. В 7 случаях достигнута беременность и рождены здоровые дети.


Изобретение относится к медицине, а именно к репродуктологии, и может быть использовано при лечении женщин, имевших многократные неудачные попытки экстракорпорального оплодотворения. Способ включает проведение женщине, страдающей бесплодием на фоне хроническог эндометрита, исследования уровня метилирования гена рецептивности эндометрия НОХА10, при высоком уровне метилирования указанного гена проводят терапию по схеме: индол-3-карбинол 300-500 мг в сутки 2 раза в день и эпигаллокатехин-3-галлат 400-600 мг в сутки 2 раза в день в течение 3 месяцев. После этого проводят повторное исследование уровня метилирования указанного гена, в случае отсутствия метильных групп в указанном гене женщине назначают подготовку к ЭКО, а в случае сохранения уровня метилирования указанного гена женщине назначают повторную терапию по указанной схеме в течение еще 3 месяцев. Использование изобретения позволяет повысить эффективность имплантации эмбриона за счет эпигенетической лекарственной коррекции гена, ответственного за рецептивность эндометрия НОХА10. 3 пр., 3 ил.
Способ восстановления репродуктивной функции у женщины с неудачными попытками экстракорпорального оплодотворения (ЭКО), страдающей бесплодием на фоне хронического эндометрита, включающий проведение женщине исследования уровня метилирования гена рецептивности эндометрия НОХА10, при высоком уровне метилирования указанного гена проводят терапию по схеме: индол-3-карбинол 300-500 мг в сутки 2 раза в день и эпигаллокатехин-3-галлат 400-600 мг в сутки 2 раза в день в течение 3 месяцев, после чего проводят повторное исследование уровня метилирования указанного гена, в случае отсутствия метильных групп в указанном гене женщине назначают подготовку к ЭКО, а в случае сохранения уровня метилирования указанного гена женщине назначают повторную терапию по указанной схеме в течение еще 3 месяцев.
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ИНДОЛ-3-КАРБИНОЛА С ПОВЫШЕННОЙ ЭПИГЕНЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2601893C1 |
| СПОСОБ ЛЕЧЕНИЯ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ У ДЕВОЧЕК-ПОДРОСТКОВ НЕГОРМОНАЛЬНЫМИ ПРЕПАРАТАМИ | 2014 |
|
RU2563181C1 |
| WO 2004022544 A1, 18.03.2004 | |||
| ТАЮКИНА И.П | |||
| и др | |||
| Морфофункциональное состояние эндометрия и экспрессия рецепторов половых стероидных гормонов у пациенток с бесплодием//Сибирский медицинский журнал, 2010, Т.25, N 4, Выпуск 2, С | |||
| Прибор, автоматически записывающий пройденный путь | 1920 |
|
SU110A1 |
Авторы
Даты
2020-09-28—Публикация
2019-10-25—Подача