ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка, согласно Своду законов США, раздел 35, §119(e), заявляет приоритет по дате подачи предварительной заявки на патент США № 62/186254, поданной 29 июня 2015 года, и предварительной заявки на патент США № 62/338245, поданной 18 мая 2016 года. Полное содержание каждой из указанных выше заявок включено в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение в целом относится к конъюгатам сконструированных антител с цистеиновыми заменами. Данное изобретение также относится к способам применения таких конъюгатов для лечения заболеваний, таких как рак.
УРОВЕНЬ ТЕХНИКИ
Конъюгаты антитела с цитотоксическим агентом (или «конъюгаты антитела с лекарственным препаратом (ADC)») и конъюгаты клеточносвязывающего агента с лекарственным препаратом зарождаются как эффективный класс противоопухолевых средств, обладающих эффективностью против ряда раковых заболеваний. Конъюгаты клеточносвязывающего агента с лекарственным препаратом (такие как ADC) обычно состоят из трех различных элементов: клеточносвязывающего агента (например, антитела); линкера; и цитотоксического фрагмента. Обычно фрагмент цитотоксического лекарственного средства ковалентно связан с лизиновыми остатками антитела с образованием конъюгатов, которые представляют собой гетерогенные смеси ADC, содержащие различные количества лекарственных препаратов, присоединенных в различных положениях молекулы антитела.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В данном изобретении предложены конъюгаты сайт-специфического антитела с цитотоксическим агентом, при этом цитотоксический агент ковалентно связан с одним или более остатками цистеина антитела. В частности, остаток цистеина находится в положении 442 тяжелой цепи (цепей) в соответствии с нумерацией EU/OU. Конъюгаты сайт-специфического антитела с цитотоксическим агентом по данному изобретению обладают неожиданно улучшенной переносимостью с сохранением аналогичной активности, что приводит к более высокому терапевтическому индексу (отношению максимально переносимой дозы к минимальной эффективной дозе) по сравнению с лизин-связанными конъюгатами (тезисы доклада № 645, ежегодное собрание AACR, 18-22 апреля, 2015 года).
Таким образом, в одном из аспектов данного изобретения предложен конъюгат антитела с цитотоксическим агентом, представленный следующей формулой:
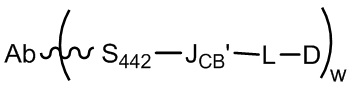
или его фармацевтически приемлемая соль, где:
Ab представляет собой антитело, содержащее остаток цистеина в положении 442 тяжелой цепи антитела (нумерация EU/OU), и ковалентно связанное со связывающим фрагментом JCB’ через тиольную группу S442 остатка цистеина;
D представляет собой цитотоксический агент, ковалентно связанный с линкером L, который ковалентно связан с JCB’; и
w равен 1 или 2.
В некоторых вариантах реализации изобретения w равен 2. В альтернативном варианте w равен 1.
В некоторых вариантах реализации изобретения остаток цистеина в положении 442 рекомбинантно вводят в указанное Ab.
В некоторых вариантах реализации изобретения JCB’ представляет собой 
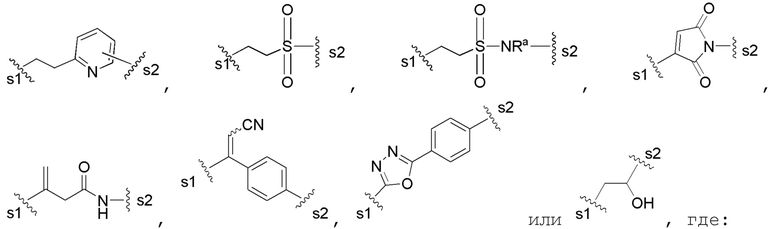
s1 представляет собой место ковалентной связи с остатком цистеина, а s2 представляет собой место ковалентной связи с группой L; и
Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил, предпочтительно каждый из Ra, Rb, Rc и Re представляют собой H.
В некоторых вариантах реализации изобретения JCB’ представляет собой  .
.
В некоторых вариантах реализации изобретения -L- представлен следующей структурной формулой:

где:
s3 представляет собой место ковалентной связи с JCB’, а s4 представляет собой место0 ковалентной связи с D;
E представляет собой -(CR10R11)q-, циклоалкил или циклоалкилалкил;
Z отсутствует, представляет собой -SO2NR9-, -NR9SO2-, -C(=O)-NR9-, -NR9-C(=O)-, -C(=O)-O-, -O-C(=O)-, -C(=O)-NR9-(CH2CH2O)p-, -NR9-C(=O)-(CH2CH2O)p-, -(OCH2CH2)p-C(=O)NR9- или -(OCH2CH2)p-NR9-C(=O)-;
p представляет собой целое число от 1 до 24;
Q представляет собой H, заряженный заместитель или ионизируемую группу;
R9, R10, R11, R12 и R13, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и
q и r, для каждого случая, независимо представляют собой целое число от 0 до 10.
В некоторых вариантах реализации изобретения E представляет собой -(CR10R11)q-.
В некоторых вариантах реализации изобретения E представляет собой  .
.
В некоторых вариантах реализации изобретения Z представляет собой -C(=O)-NR9- или -NR9-C(=O)-; в некоторых вариантах реализации изобретения Z представляет собой R9 представляет собой -H.
В некоторых вариантах реализации изобретения Q представляет собой:
i) H;
ii) -SO3H, -Z’-SO3H, -OPO3H2, -Z’-OPO3H2, -PO3H2, -Z’-PO3H2, -CO2H, -Z’-CO2H, -NR11R12 или -Z’-NR14R15, или их фармацевтически приемлемую соль; или
iii) -N+R14R15R16X- или -Z’-N+R14R15R16X-;
Z’ представляет собой необязательно замещенный алкилен, необязательно замещенный циклоалкилен или необязательно замещенный фенилен; предпочтительно Z’ представляет собой необязательно замещенный алкилен;
каждый из R14, R15 и R16 независимо представляет собой необязательно замещенный алкил; и
X- представляет собой фармацевтически приемлемый анион.
В некоторых вариантах реализации изобретения Q представляет собой H или -SO3M, где M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения все R9, R10, R11, R12, и R13 представляют собой H; а каждый из q и r независимо представляет собой целое число от 1 до 6.
В некоторых вариантах реализации изобретения -JCB’-L- представлен любой из следующих структурных формул:
 и
и
 ,
,
где M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения -L- представлен следующей структурной формулой:
 ,
,
где:
s3 представляет собой место ковалентной связи с JCB’, а s4 представляет собой место ковалентной связи с D;
R19-R22, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
каждый из m и n независимо представляет собой целое число от 0 до 10;
Rh представляет собой H или необязательно замещенный алкил;
P представляет собой необязательно замещенный алкилен, -(CH2-CH2-O)j- (где атом кислорода связан с группой –(C=O)-, связанной с P), аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков; и
j представляет собой целое число от 1 до 24.
В некоторых вариантах реализации изобретения каждый из R19, R20, R21 и R22 представляет собой H; и каждый из m и n независимо представляет собой целое число от 1 до 6.
В некоторых вариантах реализации изобретения P представляет собой аминокислотный остаток или пептид, содержащий от 2 до 10 аминокислотных остатков; предпочтительно P представляет собой пептид, содержащий от 2 до 5 аминокислотных остатков.
В некоторых вариантах реализации изобретения каждый аминокислотный остаток представляет собой остаток аминокислоты, независимо выбранной из: природной аминокислоты, синтетической аминокислоты, аналога аминокислоты и миметика аминокислоты, который действует таким же образом, как природные аминокислоты.
В некоторых вариантах реализации изобретения каждый аминокислотный остаток представляет собой остаток аминокислоты, независимо выбранной из группы, состоящей из: гистидина, аланина, изолейцина, аргинина, лейцина, аспарагина, лизина, аспарагиновой кислоты, метионина, цистеина, фенилаланина, глутаминовой кислоты, треонина, глутамина, триптофана, глицина, валина, пролина, серина, тирозина, N-метил-гистидина, N-метил-аланина, N-метил-изолейцина, N-метил-аргинина, N-метил-лейцина, N-метил-аспарагина, N-метил-лизина, N-метил-аспарагиновой кислоты, N-метил-метионина, N-метил-цистеина, N-метил-фенилаланина, N-метил-глутаминовой кислоты, N-метил-треонина, N-метил-глутамина, N-метил-триптофана, N-метил-глицина, N-метил-валина, N-метил-пролина, N-метил-серина, N-метил-тирозина, гидроксипролина, γ-карбоксиглутамата, селеноцистеина, O-фосфосерина, гомосерина, норлейцина, метионинсульфоксида, метилметионинсульфония, цитруллина, орнитина, цистеинсульфоновой кислоты, цистеинсульфиновой кислоты, 3-аминоаланина, 3-диметиламиноаланина, 2-амино-4-(диметиламино)бутановой кислоты, 2,4-диаминобутановой кислоты, 2-амино-6-(диметиламино)капроновой кислоты, 2-амино-5-(диметиламино)валериановой кислоты и β-аланина, каждый независимо в виде L- или D-изомера. Предпочтительно каждый аминокислотный остаток представляет собой остаток независимо выбранного глицина или аланина.
В некоторых вариантах реализации изобретения P представляет собой пептид, расщепляемый протеазой.
В некоторых вариантах реализации изобретения Р выбран из группы, состоящей из: Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID №: 14), β-Ala-Leu-Ala-Leu (SEQ ID №: 15), Gly-Phe-Leu-Gly (SEQ ID №: 16), Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala и D-Ala-D-Ala, Gly-Gly-Gly, Ala-Ala-Ala, D-Ala-Ala-Ala, Ala-D-Ala-Ala, Ala-Ala-D-Ala, Ala-Val-Cit, Ala-Val-Ala и β-Ala-Gly-Gly-Gly. Например, P может представлять собой Gly-Gly-Gly, Ala-Ala-Ala, D-Ala-Ala-Ala, Ala-D-Ala-Ala, Ala-Val-Ala или β-Ala-Gly-Gly-Gly.
В некоторых вариантах реализации изобретения -JCB’-L- представлен следующей структурной формулой:
 .
.
В некоторых вариантах реализации изобретения -L- представлен следующей структурной формулой:
 ,
,
где:
s3 представляет собой место ковалентной связи с JCB’, а s4 представляет собой место ковалентной связи с D;
R23 и R24, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
m’ представляет собой целое число от 0 до 10; и
Rh’ представляет собой H или необязательно замещенный алкил.
В некоторых вариантах реализации изобретения оба R23 и R24 представляют собой H; и m’ представляет собой целое число от 1 до 6.
В некоторых вариантах реализации изобретения Rh’ представляет собой H.
В некоторых вариантах реализации изобретения -JCB’-L- представлен следующей структурной формулой:
 .
.
В некоторых вариантах реализации изобретения D представляет собой соединение бензодиазепина, такое как соединение индолинбензодиазепина.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:

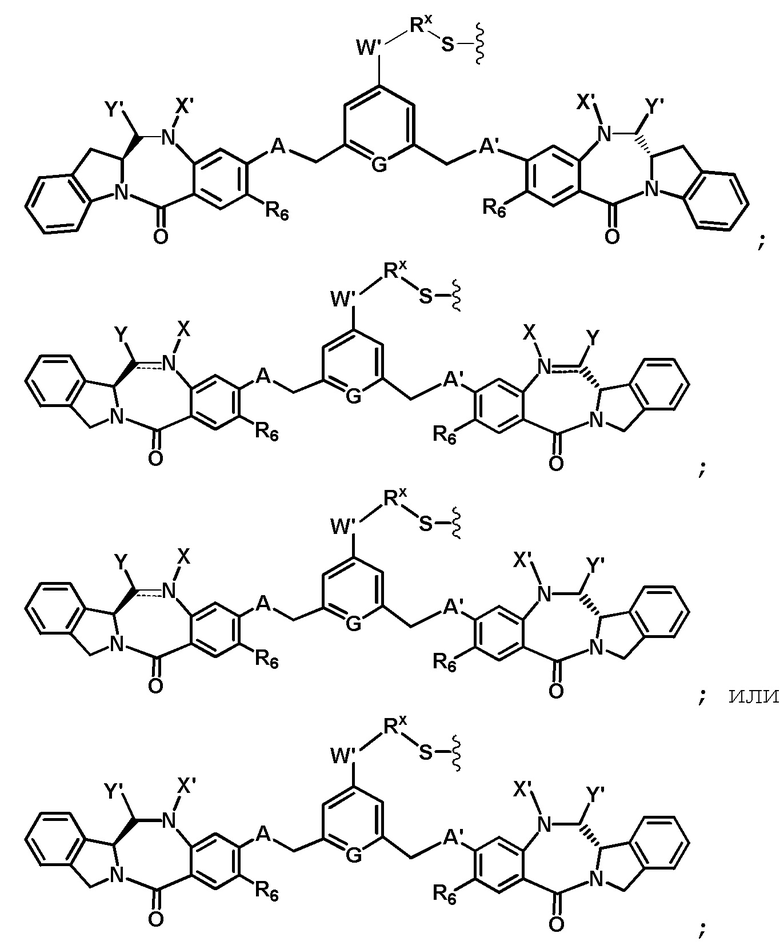
или его фармацевтически приемлемая соль, где:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X выбран из -H или аминозащитной группы; и Y выбран из -OR, -OCOR’, -SR, -NR’R”, -SO3M, -SO2M или -OSO3M, где М представляет собой -Н или катион;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X выбран из -H или аминозащитной группы; и Y выбран из -OR, -OCOR’, -SR, -NR’R”, -SO3M, -SO2M или -OSO3M, где М представляет собой -Н или катион;
R представляет собой -H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода или ПЭГ-группу -(CH2CH2O)n-Rc, где n представляет собой целое число от 1 до 24 и Rc представляет собой линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода;
каждый из R’ и R” независимо выбран из -H, -OH, -OR, -NRRg’, -COR, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, выбранных из O, S, N и P, ПЭГ-группы -(CH2CH2O)n-Rc, и Rg’ представляет собой -H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или ПЭГ-группу -(CH2CH2O)n-Rc;
X’ выбран из группы, состоящей из -H, -OH, замещенного или незамещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, фенила и аминозащитной группы;
Y’ выбран из группы, состоящей из -H, оксогруппы (т.е. Y’ вместе с атомом углерода, к которому он присоединен, образуют –C(=O)-группу), замещенного или незамещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода;
A и A’ выбраны из -O- и -S-;
W’ отсутствует или выбран из -O-, -N(Re)-, -N(Re)-C(=O)-, -N(C(=O)Re)-, -S- или -CH2-S-, -CH2NRe-;
Rx отсутствует или выбран из линейного, разветвленного или циклического алкила, содержащего от 1 до 10 атомов углерода;
Re представляет собой -H, линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или -(CH2-CH2-O)n-Rk, где Rk представляет собой -H, линейный, разветвленный или циклический алкил, содержащий 1 до 6 атомов углерода, необязательно содержащий вторичную аминогруппу (например, -NHR101) или третичную аминогруппу (-NR101R102), или 5- или 6-членный азотсодержащий гетероцикл, где каждый из R101 и R102 независимо представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
G выбран из -CH- или -N-; и
R6 представляет собой -H, -R, -OR, -SR, -NR’R’’, -NO2 или галоген.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:
 .
.
В некоторых вариантах реализации изобретения:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -OH или -SO3M;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -OH или -SO3M;
М представляет собой -Н или фармацевтически приемлемый катион;
оба X’ и Y’ представляют собой -H;
оба A и A’ представляют собой -O-;
R6 представляет собой -OMe; и
Rx представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:
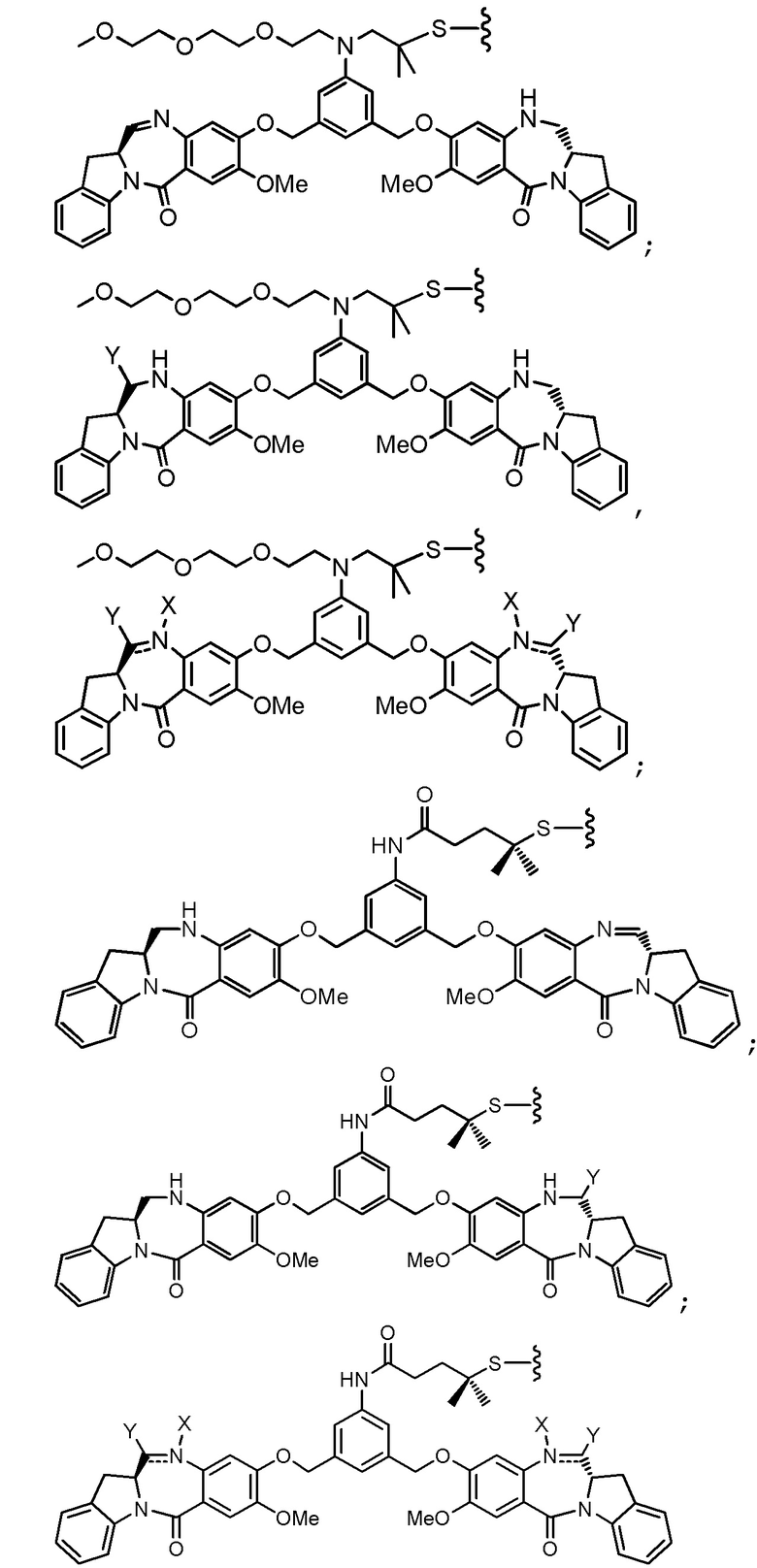
или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения Y представляет собой -SO3M и M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль, где:
один из L’, L’’ и L’’’ представлен следующей формулой:
-Z1-P1-Z2-Rx1-C(=O)- (A’) или
-N(Re)-Rx1-C(=O)- (D’);
и каждый из двух других независимо выбран из -H, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, галогена, гуанидиния [-NH(C=NH)NH2], -OR, -NR’R’’, -NO2, -NR’COR’’, -SR, -SOR’, -SO2R’, -SO3H, -OSO3H, -SO2NR’R’’, циано, азидо, -COR’, -OCOR’ и -OCONR’R’’;
один из Z1 и Z2 представляет собой -C(=O)-, а другой представляет собой -NR5-;
P1 представляет собой аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков;
Rx1 представляет собой необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
Re представляет собой -H, линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или -(CH2-CH2-O)n-Rk, где Rk представляет собой -H, линейный, разветвленный или циклический алкил, содержащий 1 до 6 атомов углерода, необязательно содержащий вторичную аминогруппу (например, -NHR101) или третичную аминогруппу (-NR101R102), или 5- или 6-членный азотсодержащий гетероцикл, где каждый из R101 и R102 независимо представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, и если она представляет собой одинарную связь, то X1 представляет собой -H или аминозащитный фрагмент; и Y1 представляет собой уходящую группу, выбранную из -OR, -OCOR’, -OCOOR’, -OCONR’R’’, -NR’R’’, -NR’COR’’, -NR’NR’R’’, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, гуанидиния, представленного -NR’(C=NH)NR’R’’, аминокислоты или пептида, представленного -NRCOP’, -SR, -SOR’, галогена, циано, азидо, -OSO3H (или его соли), сульфита (-SO3H или -SO2H, или их соли), метабисульфита (H2S2O5 или его соли), моно-, ди-, три- и тетратиофосфата (PO3SH3, PO2S2H2, POS3H2, PS4H2 или их соли), сложного тиофосфатного эфира (RiO)2PS(ORi), RiS-, RiSO, RiSO2, RiSO3, тиосульфата (HS2O3 или его соли), дитионита (HS2O4 или его соли) фосфородитиоата (P(=S)(ORk’)(S)(OH) или его соли), гидроксамовой кислоты (Rk’C(=O)NOH или ее соли) и формальдегидсульфоксилата (HOCH2SO2- или его соли) или их смеси, где Ri представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H и -PO3H; Ri также может быть необязательно замещен заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; Rk’ представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, и если она представляет собой одинарную связь, то X1 представляет собой -H или аминозащитный фрагмент; и Y1 представляет собой уходящую группу, выбранную из -OR, -OCOR’, -OCOOR’, -OCONR’R’’, -NR’R’’, -NR’COR’’, -NR’NR’R’’, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, гуанидиния, представленного -NR’(C=NH)NR’R’’, аминокислоты или пептида, представленного -NRCOP’, -SR, -SOR’, галогена, циано, азидо, -OSO3H (или его соли), сульфита (-SO3H или -SO2H, или их соли), метабисульфита (H2S2O5 или его соли), моно-, ди-, три- и тетратиофосфата (PO3SH3, PO2S2H2, POS3H2, PS4H2 или их соли), сложного тиофосфатного эфира (RiO)2PS(ORi), RiS-, RiSO, RiSO2, RiSO3, тиосульфата (HS2O3 или его соли), дитионита (HS2O4 или его соли) фосфородитиоата (P(=S)(ORk’)(S)(OH) или его соли), гидроксамовой кислоты (Rk’C(=O)NOH или ее соли) и формальдегидсульфоксилата (HOCH2SO2- или его соли) или их смеси, где Ri представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H и -PO3H; Ri также может быть необязательно замещен заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; Rk’ представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил;
P’ представляет собой аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков,
R, для каждого случая, независимо выбран из группы, состоящей из -H, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, или необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из O, S, N и P;
каждый из R’ и R’’ независимо выбран из -H, -OH, -OR, -NHR, -NR2, -COR, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc и необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из O, S, N и P;
Rc представляет собой -H или необязательно замещенный линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода;
n представляет собой целое число от 1 до 24;
X1’ выбран из -Н, аминозащитной группы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, и необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из О, S, N и Р;
Y1’ выбран из -H, оксогруппы (т.е. Y1’ вместе с атомом углерода, к которому он присоединен, образуют –C(=O)-группу), необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, необязательно замещенного 6-18-членного арила, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов;
каждый из R1, R2, R3, R4, R1’, R2’, R3’ и R4’ независимо выбран из группы, состоящей из -Н, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, галогена, гуанидиния [-NH(C=NH)NH2], -OR, -NR’R’’, -NO2, -NCO, -NR’COR’’, -SR, -SOR’, -SO2R’, -SO3-H, -OSO3H, -SO2NR’R’’, циано, азидо, -COR’, -OCOR’ и -OCONR’R’’;
R6 представляет собой -H, -R, -OR, -SR, -NR’R’’, -NO2 или галоген;
G представляет собой -CH- или –N-;
A и A’ являются одинаковыми или различными и независимо выбраны из -O-, оксо (-C(=O)-), -CRR’O-, -CRR’-, -S-, -CRR’S-, -NR5 и -CRR’N(R5)-; и
R5 для каждого случая независимо представляет собой -H или необязательно замещенный линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль.
В некоторых вариантах реализации изобретения один из L’, L” и L’” представлен формулой (A’) или (D’), а другие представляют собой -H, линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода, галоген, -OH, (C1-C6)алкокси или -NO2.
В некоторых вариантах реализации изобретения L’ представлен формулой (A’); и оба L” и L’” представляют собой -H.
В некоторых вариантах реализации изобретения L’ представлен формулой (D’); и оба L” и L’” представляют собой -H.
В некоторых вариантах реализации изобретения Rx1 представляет собой линейный, разветвленный или циклический алкил, содержащий от 1 до 6 атомов углерода, необязательно замещенный галогеном, -OH, -SO3H, (C1-C3)алкилом, (C1-C3)алкокси, гало(C1-C3)алкилом или заряженным заместителем, или ионизируемой группой Q.
В некоторых вариантах реализации изобретения L’ представлен следующей формулой:
-NR5-P1-C(=O)-(CRaRb)s-C(=O)- (B1’);
-NR5-P1-C(=O)-Cy-(CRaRb)s1’-C(=O)- (B2’);
-C(=O)-P1-NR5-(CRaRb)s-C(=O)- (C1’) или
-C(=O)-P1-NR5-Cy-(CRaRb)s1’-C(=O)- (C2’)
где:
каждый из Ra и Rb, для каждого случая, независимо представляет собой -H, (C1-C3)алкил или заряженный заместитель, или ионизируемую группу Q;
s представляет собой целое число от 1 до 6;
s1’ представляет собой 0 или целое число от 1 до 6; и
Cy представляет собой циклический алкил, содержащий 5 или 6 кольцевых атомов углерода, необязательно замещенный галогеном, -OH, (C1-C3)алкилом, (C1-C3)алкокси или гало(C1-C3)алкилом.
В некоторых вариантах реализации изобретения оба Ra и Rb представляют собой H; Cy в формулах (B2’) и (C2’) представляет собой циклогексан; и R5 представляет собой H или Me.
В некоторых вариантах реализации изобретения s1’ равен 0 или 1.
В некоторых вариантах реализации изобретения заряженный заместитель или ионизируемая группа Q представляет собой i) -SO3H, -Z’-SO3H, -OPO3H2, -Z’-OPO3H2, -PO3H2, -Z’-PO3H2, -CO2H, -Z’-CO2H, -NR11R12 или -Z’-NR11R12, или их фармацевтически приемлемую соль; или ii) -N+R14R15R16X- или -Z’-N+R14R15R16X-; Z’ представляет собой необязательно замещенный алкилен, необязательно замещенный циклоалкилен или необязательно замещенный фенилен; каждый из R14-R16 независимо представляет собой необязательно замещенный алкил; и X- представляет собой фармацевтически приемлемый анион.
В некоторых вариантах реализации изобретения Q представляет собой -SO3H или его фармацевтически приемлемую соль.
В некоторых вариантах реализации изобретения P1 представляет собой пептид, содержащий от 2 до 10 аминокислотных остатков. Например, P1 может представлять собой пептид, содержащий от 2 до 5 аминокислотных остатков, таких как Gly-Gly-Gly, Ala-Val, Val-Ala, Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu, β-Ala-Leu-Ala-Leu, Gly-Phe-Leu-Gly, Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala, D-Ala-D-Ala, Ala-Met или Met-Ala. В некоторых вариантах реализации изобретения P1 представляет собой Gly-Gly-Gly, Ala-Val, Ala-Ala, Ala-D-Ala, D-Ala-Ala или D-Ala-D-Ala.
В некоторых вариантах реализации изобретения двойная линия  между N и C представляет собой двойную связь.
между N и C представляет собой двойную связь.
В некоторых вариантах реализации изобретения двойная линия  между N и C представляет собой одинарную связь, X1 представляет собой –H или аминозащитную группу; и Y1 выбран из -OR, -OCOR’, -SR, -NR’R”, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, -SO3M, -SO2M и -OSO3M, где M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь, X1 представляет собой –H или аминозащитную группу; и Y1 выбран из -OR, -OCOR’, -SR, -NR’R”, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, -SO3M, -SO2M и -OSO3M, где M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения Y1 выбран из -SO3M, -OH, -OMe, -OEt или -NHOH.
В некоторых вариантах реализации изобретения Y1 представляет собой -SO3M или -OH, где M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения X1’ выбран из группы, состоящей из -H, -OH, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, и фенила.
В некоторых вариантах реализации изобретения X1’ представляет собой -H, -OH, (C1-C3)алкил, гало(C1-C3)алкил или фенил. Предпочтительно X1’ представляет собой -H, -OH или -Me. В некоторых вариантах реализации изобретения X1’ представляет собой -H.
В некоторых вариантах реализации изобретения Y1’ выбран из группы, состоящей из -H, оксогруппы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода. В некоторых вариантах реализации изобретения Y1’ представляет собой -H, оксогруппу, (C1-C3)алкил или гало(C1-C3)алкил. В некоторых вариантах реализации изобретения Y1’ представляет собой -H или оксо. В некоторых вариантах реализации изобретения Y1’ представляет собой -H.
В некоторых вариантах реализации изобретения A и A’ являются одинаковыми или различными и выбраны из -O-, -S-, -NR5- и оксо -(C=O)-. В некоторых вариантах реализации изобретения A и A’ являются одинаковыми или различными и выбраны из -O- и -S-. В некоторых вариантах реализации изобретения A и A’ представляют собой -O-.
В некоторых вариантах реализации изобретения R6 представляет собой -OMe.
В некоторых вариантах реализации изобретения R1, R2, R3, R4, R1’, R2’, R3’ и R4’ независимо представляют собой -H, галоген, -NO2, -OH, (C1-C3)алкил, гало(C1-C3)алкил или (C1-C3) алкокси. В некоторых вариантах реализации изобретения все R1, R2, R3, R4, R1’, R2’, R3’ и R4’ представляют собой -H.
В некоторых вариантах реализации изобретения каждый из R, R’, R” и R5 независимо представляет собой -H или (C1-C3)алкил.
В некоторых вариантах реализации изобретения:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H; и если она представляет собой одинарную связь, то X1 представляет собой –H и Y1 представляет собой -OH или -SO3M;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H; и если она представляет собой одинарную связь, то X1 представляет собой –H и Y1 представляет собой -OH или -SO3M;
все R1, R2, R3, R4, R1’, R2’, R3’ и R4’ представляют собой -H;
R6 представляет собой -OMe;
оба X1’ и Y1’ представляют собой -H;
A и A’ представляют собой -O-; и
M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:


где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион; M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион; M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения конъюгат представлен следующей структурной формулой:
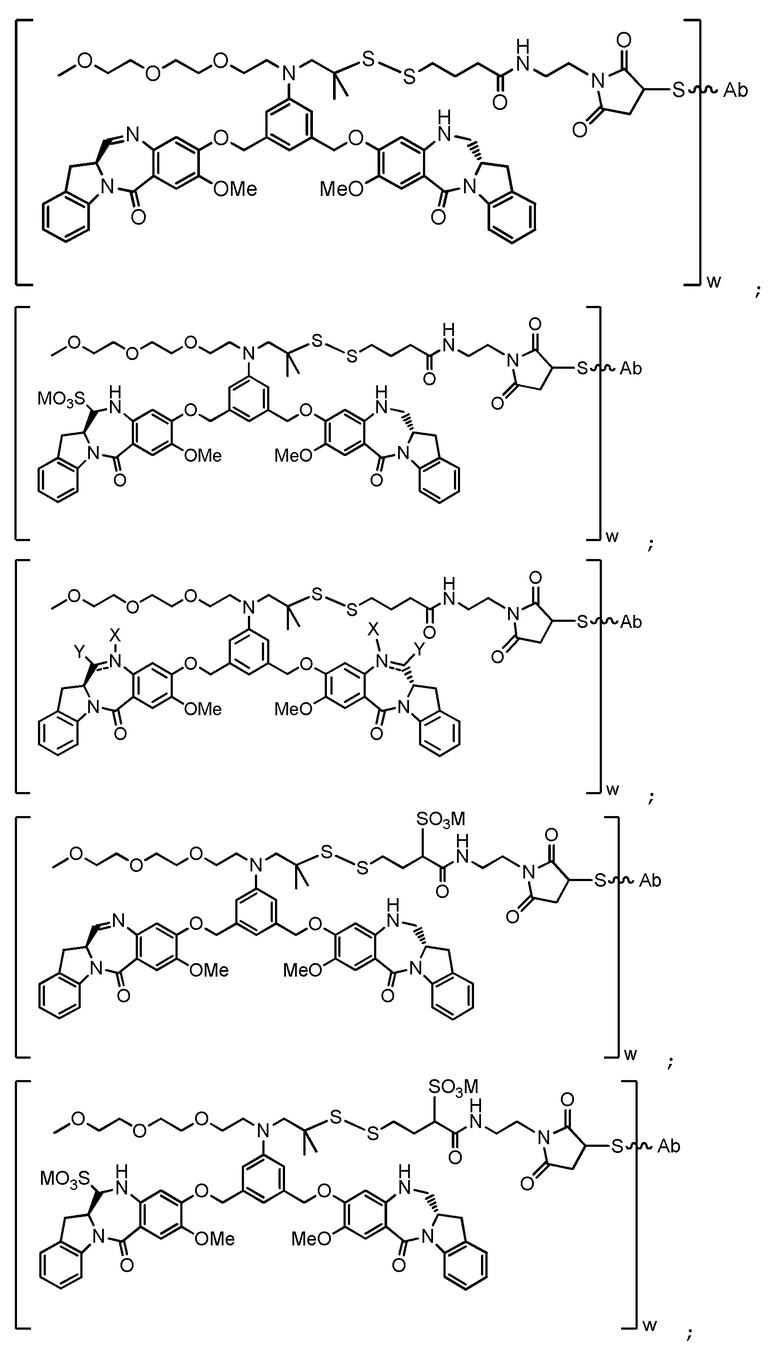



или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения M, если присутствует, представляет собой H+, Na+ или K+.
В другом аспекте данного изобретения предложено соединение, представленное следующей структурной формулой:
D-L-JCB,
или его фармацевтически приемлемая соль, где:
D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль, где:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X выбран из -H или аминозащитной группы; и Y выбран из -OR, -OCOR’, -SR, -NR’R”, -SO3M, -SO2M или -OSO3M, где М представляет собой -Н или катион;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X выбран из -H или аминозащитной группы; и Y выбран из -OR, -OCOR’, -SR, -NR’R”, -SO3M, -SO2M или -OSO3M, где М представляет собой -Н или катион;
R представляет собой -H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода или ПЭГ-группу -(CH2CH2O)n-Rc, где n представляет собой целое число от 1 до 24 и Rc представляет собой линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода;
каждый из R’ и R” независимо выбран из -H, -OH, -OR, -NRRg’, -COR, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, выбранных из O, S, N и P, ПЭГ-группы -(CH2CH2O)n-Rc, и Rg’ представляет собой -H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или ПЭГ-группу -(CH2CH2O)n-Rc;
X’ выбран из группы, состоящей из -H, -OH, замещенного или незамещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, фенила и аминозащитной группы;
Y’ выбран из группы, состоящей из -H, оксогруппы, замещенного или незамещенного линейного, разветвленного или циклического алкил, алкенила или алкинила, содержащего от 1 до 10 атомов углерода;
A и A’ выбраны из -O- и -S-;
W’ отсутствует или выбран из -O-, -N(Re)-, -N(Re)-C(=O)-, -N(C(=O)Re)-, -S- или -CH2-S-, -CH2NRe-;
Rx отсутствует или выбран из линейного, разветвленного или циклического алкила, содержащего от 1 до 10 атомов углерода;
Re представляет собой -H, линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или -(CH2-CH2-O)n-Rk, где Rk представляет собой -H, линейный, разветвленный или циклический алкил, содержащий 1 до 6 атомов углерода, необязательно содержащий вторичную аминогруппу (например, -NHR101) или третичную аминогруппу (-NR101R102), или 5- или 6-членный азотсодержащий гетероцикл, где каждый из R101 и R102 независимо представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
G выбран из -CH- или -N-;
R6 представляет собой -H, -R, -OR, -SR, -NR’R’’, -NO2 или галоген;
-L- представлен следующей структурной формулой:
 ,
,
где:
s3 представляет собой место ковалентной связи с JCB, а s4 представляет собой место ковалентной связи с D;
E представляет собой -(CR10R11)q-, циклоалкил или циклоалкилалкил;
Z отсутствует, представляет собой -SO2NR9-, -NR9SO2-, -C(=O)-NR9-, -NR9-C(=O)-, -C(=O)-O-, -O-C(=O)-, -C(=O)-NR9-(CH2CH2O)p-, -NR9-C(=O)-(CH2CH2O)p-, -(OCH2CH2)p-C(=O)NR9- или -(OCH2CH2)p-NR9-C(=O)-;
p представляет собой целое число от 1 до 1000;
Q представляет собой H, заряженный заместитель или ионизируемую группу;
R9, R10, R11, R12 и R13, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
q и r, для каждого случая, независимо представляют собой целое число от 0 до 10; и
JCB представляет собой 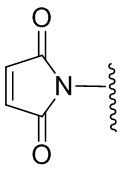 , X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,
, X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,  ,
,  ,
, ,
, ,
,  ,
,  ,
,  или
или  .
.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:
 ,
,
или его фармацевтически приемлемая соль.
В некоторых вариантах реализации изобретения каждый из Ra, Rb, Rc и Re представляет собой H.
В некоторых вариантах реализации изобретения JCB представляет собой  .
.
В некоторых вариантах реализации изобретения:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H; Y представляет собой -OH или -SO3M;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H; Y представляет собой -OH или -SO3M;
M представляет собой -H или фармацевтически приемлемый катион (например, Na+);
оба X’ и Y’ представляют собой -H;
оба A и A’ представляют собой -O-;
R6 представляет собой -OMe; и
Rx представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль.
В некоторых вариантах реализации изобретения Y представляет собой –SO3M; и M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения E представляет собой -(CR10R11)q-.
В некоторых вариантах реализации изобретения E представляет собой 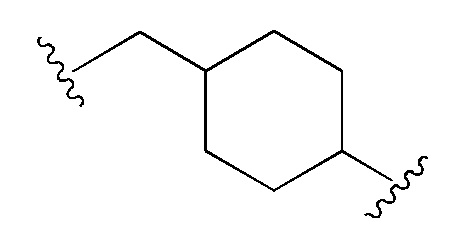 .
.
В некоторых вариантах реализации изобретения Z представляет собой -C(=O)-NR9- или -NR9-C(=O)-. В некоторых вариантах реализации изобретения R9 представляет собой -H.
В некоторых вариантах реализации изобретения Q представляет собой:
i) H;
ii) -SO3H, -Z’-SO3H, -OPO3H2, -Z’-OPO3H2, -PO3H2, -Z’-PO3H2, -CO2H, -Z’-CO2H, -NR11R12 или -Z’-NR14R15, или их фармацевтически приемлемую соль; или
iii) -N+R14R15R16X- или -Z’-N+R14R15R16X-;
Z’ представляет собой необязательно замещенный алкилен, необязательно замещенный циклоалкилен или необязательно замещенный фенилен;
каждый из R14, R15 и R16 независимо представляет собой необязательно замещенный алкил; и
X- представляет собой фармацевтически приемлемый анион.
В некоторых вариантах реализации изобретения Z’ представляет собой необязательно замещенный алкилен.
В некоторых вариантах реализации изобретения Q представляет собой H или -SO3M, где M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения все R9, R10, R11, R12 и R13 представляют собой H; а каждый из q и r независимо представляет собой целое число от 1 до 6.
В некоторых вариантах реализации изобретения –L-JCB представлен следующей структурной формулой:
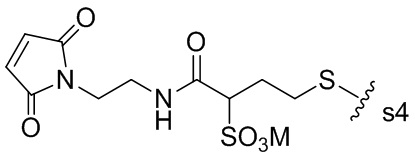 ; или
; или
 .
.
где M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения соединение представлено следующей структурной формулой:
 ;
;

или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
В другом аспекте данного изобретения предложено соединение, представленное следующей структурной формулой:
D-L-JCB,
или его фармацевтически приемлемая соль, где:
D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль, где:
один из L’, L’’ и L’’’ представлен следующей формулой:
-Z1-P1-Z2-Rx1-C(=O)- (A’) или
-N(Re)-Rx1-C(=O)- (D’);
и каждый из двух других независимо выбран из -H, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, галогена, гуанидиния [-NH(C=NH)NH2], -OR, -NR’R’’, -NO2, -NR’COR’’, -SR, -SOR’, -SO2R’, -SO3H, -OSO3H, -SO2NR’R’’, циано, азидо, -COR’, -OCOR’ и -OCONR’R’’;
один из Z1 и Z2 представляет собой –C(=O)-, а другой представляет собой –NR5-;
P1 представляет собой аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков;
Rx1 представляет собой необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
Re представляет собой -H, линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или -(CH2-CH2-O)n-Rk, где Rk представляет собой -H, линейный, разветвленный или циклический алкил, содержащий 1 до 6 атомов углерода, необязательно содержащий вторичную аминогруппу (например, -NHR101) или третичную аминогруппу (-NR101R102), или 5- или 6-членный азотсодержащий гетероцикл, где каждый из R101 и R102 независимо представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, и если она представляет собой одинарную связь, то X1 представляет собой -Н или аминозащитный фрагмент; и Y1 представляет собой уходящую группу, выбранную из -OR, -OCOR’, -OCOOR’, -OCONR’R’’, -NR’R’’, -NR’COR’’, -NR’NR’R’’, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, гуанидиния, представленного -NR’(C=NH)NR’R’’, аминокислоты или пептида, представленного -NRCOP’, -SR, -SOR’, галогена, циано, азидо, -OSO3H (или его соли), сульфита (-SO3H или -SO2H, или их соли), метабисульфита (H2S2O5 или его соли), моно-, ди-, три- и тетратиофосфата (PO3SH3, PO2S2H2, POS3H2, PS4H2 или их соли), сложного тиофосфатного эфира (RiO)2PS(ORi), RiS-, RiSO, RiSO2, RiSO3, тиосульфата (HS2O3 или его соли), дитионита (HS2O4 или его соли) фосфородитиоата (P(=S)(ORk’)(S)(OH) или его соли), гидроксамовой кислоты (Rk’C(=O)NOH или ее соли) и формальдегидсульфоксилата (HOCH2SO2- или его соли) или их смеси, где Ri представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H, и -PO3H; Ri также может быть необязательно замещен заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; Rk’ представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, и если она представляет собой одинарную связь, то X1 представляет собой -Н или аминозащитный фрагмент; и Y1 представляет собой уходящую группу, выбранную из -OR, -OCOR’, -OCOOR’, -OCONR’R’’, -NR’R’’, -NR’COR’’, -NR’NR’R’’, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, гуанидиния, представленного -NR’(C=NH)NR’R’’, аминокислоты или пептида, представленного -NRCOP’, -SR, -SOR’, галогена, циано, азидо, -OSO3H (или его соли), сульфита (-SO3H или -SO2H, или их соли), метабисульфита (H2S2O5 или его соли), моно-, ди-, три- и тетратиофосфата (PO3SH3, PO2S2H2, POS3H2, PS4H2 или их соли), сложного тиофосфатного эфира (RiO)2PS(ORi), RiS-, RiSO, RiSO2, RiSO3, тиосульфата (HS2O3 или его соли), дитионита (HS2O4 или его соли) фосфородитиоата (P(=S)(ORk’)(S)(OH) или его соли), гидроксамовой кислоты (Rk’C(=O)NOH или ее соли) и формальдегидсульфоксилата (HOCH2SO2- или его соли) или их смеси, где Ri представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H, и -PO3H; Ri также может быть необязательно замещен заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; Rk’ представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил;
P’ представляет собой аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков,
R, для каждого случая, независимо выбран из группы, состоящей из -H, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, или необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из O, S, N и P;
каждый из R’ и R’’ независимо выбран из -H, -OH, -OR, -NHR, -NR2, -COR, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc и необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из O, S, N и P;
Rc представляет собой -H или необязательно замещенный линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода;
n представляет собой целое число от 1 до 24;
X1’ выбран из -Н, аминозащитной группы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, и необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из О, S, N и Р;
Y1’ выбран из -H, оксогруппы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, необязательно замещенного 6-18-членного арила, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов;
каждый из R1, R2, R3, R4, R1’, R2’, R3’ и R4’ независимо выбран из группы, состоящей из -Н, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, галогена, гуанидиния [-NH(C=NH)NH2], -OR, -NR’R’’, -NO2, -NCO, -NR’COR’’, -SR, -SOR’, -SO2R’, -SO3-H, -OSO3H, -SO2NR’R’’, циано, азидо, -COR’, -OCOR’ и -OCONR’R’’;
R6 представляет собой -H, -R, -OR, -SR, -NR’R’’, -NO2 или галоген;
G представляет собой -CH- или -N-;
A и A’ являются одинаковыми или различными и независимо выбраны из -O-, оксо (-C(=O)-), -CRR’O-, -CRR’-, -S-, -CRR’S-, -NR5 и -CRR’N(R5)-; и
R5 для каждого случая независимо представляет собой -H или необязательно замещенный линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода;
-L- представлен следующей структурной формулой:
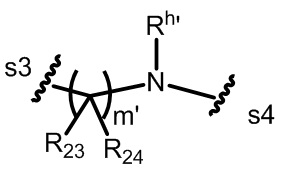 ,
,
где:
s3 представляет собой место ковалентной связи с JCB’, а s4 представляет собой место ковалентной связи с D;
R23 и R24, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
m’ представляет собой целое число от 0 до 10;
Rh’ представляет собой H или необязательно замещенный алкил; и
JCB представляет собой  , X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,
, X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,  ,
,  ,
,  ,
,  ,
,  ,
, 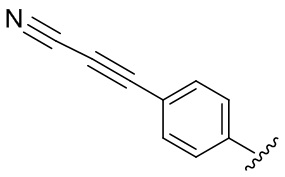 ,
,  или
или  .
.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:
 ,
,
или его фармацевтически приемлемая соль.
В некоторых вариантах реализации изобретения каждый из Ra, Rb, Rc и Re представляет собой H.
В некоторых вариантах реализации изобретения JCB представляет собой  .
.
В некоторых вариантах реализации изобретения один из L’, L” и L’” представлен формулой (A’) или (D’), а другие представляют собой -H, линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода, галоген, -OH, (C1-C6)алкокси или -NO2.
В некоторых вариантах реализации изобретения L’ представлен формулой (A’); и оба L” и L’” представляют собой -H.
В некоторых вариантах реализации изобретения L’ представлен формулой (D’); и оба L” и L’” представляют собой -H.
В некоторых вариантах реализации изобретения Rx1 представляет собой линейный, разветвленный или циклический алкил, содержащий от 1 до 6 атомов углерода, необязательно замещенный галогеном, -OH, -SO3H, (C1-C3)алкилом, (C1-C3)алкокси, гало(C1-C3)алкилом или заряженным заместителем, или ионизируемой группой Q.
В некоторых вариантах реализации изобретения L’ представлен следующей формулой:
-NR5-P1-C(=O)-(CRaRb)s-C(=O)- (B1’);
-NR5-P1-C(=O)-Cy-(CRaRb)s1’-C(=O)- (B2’);
-C(=O)-P1-NR5-(CRaRb)s-C(=O)- (C1’) или
-C(=O)-P1-NR5-Cy-(CRaRb)s1’-C(=O)- (C2’)
где:
каждый из Ra и Rb, для каждого случая, независимо представляет собой –H, (C1-C3)алкил или заряженный заместитель, или ионизируемую группу Q;
s представляет собой целое число от 1 до 6;
s1’ представляет собой 0 или целое число от 1 до 6; и
Cy представляет собой циклический алкил, содержащий 5 или 6 кольцевых атомов углерода, необязательно замещенный галогеном, -OH, (C1-C3)алкилом, (C1-C3)алкокси или гало(C1-C3)алкилом.
В некоторых вариантах реализации изобретения оба Ra и Rb представляют собой H; Cy для формул (B2’) и (C2’) представляет собой циклогексан; и R5 представляет собой H или Me.
В некоторых вариантах реализации изобретения s1’ равен 0 или 1.
В некоторых вариантах реализации изобретения заряженный заместитель или ионизируемая группа Q представляет собой i) -SO3H, -Z’-SO3H, -OPO3H2, -Z’-OPO3H2, -PO3H2, -Z’-PO3H2, -CO2H, -Z’-CO2H, -NR11R12 или -Z’-NR11R12, или их фармацевтически приемлемую соль; или ii) -N+R14R15R16X- или -Z’-N+R14R15R16X-; Z’ представляет собой необязательно замещенный алкилен, необязательно замещенный циклоалкилен или необязательно замещенный фенилен; каждый из R14-R16 независимо представляет собой необязательно замещенный алкил; и X- представляет собой фармацевтически приемлемый анион.
В некоторых вариантах реализации изобретения Q представляет собой SO3H или его фармацевтически приемлемую соль.
В некоторых вариантах реализации изобретения P1 представляет собой пептид, содержащий от 2 до 10 аминокислотных остатков. Например, P1 может представлять собой пептид, содержащий от 2 до 5 аминокислотных остатков, таких как Gly-Gly-Gly, Ala-Val, Val-Ala, Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID №: 14), β-Ala-Leu-Ala-Leu (SEQ ID №: 15), Gly-Phe-Leu-Gly (SEQ ID №: 16), Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala, D-Ala-D-Ala, Ala-Met и Met-Ala. В некоторых вариантах реализации изобретения P1 представляет собой Gly-Gly-Gly, Ala-Val, Ala-Ala, Ala-D-Ala, D-Ala-Ala и D-Ala-D-Ala.
В некоторых вариантах реализации изобретения двойная линия  между N и C представляет собой двойную связь.
между N и C представляет собой двойную связь.
В некоторых вариантах реализации изобретения двойная линия  между N и C представляет собой одинарную связь, X1 представляет собой -H или аминозащитную группу; и Y1 выбран из -OR, -OCOR’, -SR, -NR’R”, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, -SO3M, -SO2M и -OSO3M, где M представляет собой H+ или фармацевтически приемлемый катион. В некоторых вариантах реализации изобретения Y1 выбран из -SO3M, -OH, -OMe, -OEt или -NHOH. В некоторых вариантах реализации изобретения Y1 представляет собой -SO3M или -OH, а M представляет собой H+, Na+ или K+.
между N и C представляет собой одинарную связь, X1 представляет собой -H или аминозащитную группу; и Y1 выбран из -OR, -OCOR’, -SR, -NR’R”, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла, -SO3M, -SO2M и -OSO3M, где M представляет собой H+ или фармацевтически приемлемый катион. В некоторых вариантах реализации изобретения Y1 выбран из -SO3M, -OH, -OMe, -OEt или -NHOH. В некоторых вариантах реализации изобретения Y1 представляет собой -SO3M или -OH, а M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения X1’ выбран из группы, состоящей из -H, -OH, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, и фенила. В некоторых вариантах реализации изобретения X1’ представляет собой -H, -OH, (C1-C3)алкил, гало(C1-C3)алкил или фенил. В некоторых вариантах реализации изобретения X1’ представляет собой -H, -OH или -Me. В некоторых вариантах реализации изобретения X1’ представляет собой -H.
В некоторых вариантах реализации изобретения Y1’ выбран из группы, состоящей из -H, оксогруппы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода. В некоторых вариантах реализации изобретения Y1’ представляет собой -H, оксогруппу, (C1-C3)алкил или гало(C1-C3)алкил. В некоторых вариантах реализации изобретения Y1’ представляет собой -H или оксо. В некоторых вариантах реализации изобретения Y1’ представляет собой -H.
В некоторых вариантах реализации изобретения A и A’ являются одинаковыми или различными и выбраны из -O-, -S-, -NR5- и оксо -(C=O)-. В некоторых вариантах реализации изобретения A и A’ являются одинаковыми или различными и выбраны из -O- и -S-. В некоторых вариантах реализации изобретения A и A’ представляют собой -O-.
В некоторых вариантах реализации изобретения R6 представляет собой -OMe.
В некоторых вариантах реализации изобретения R1, R2, R3, R4, R1’, R2’, R3’ и R4’ независимо представляют собой –H, галоген, -NO2, -OH, (C1-C3)алкил, гало(C1-C3)алкил или (C1-C3)алкокси. В некоторых вариантах реализации изобретения все R1, R2, R3, R4, R1’, R2’, R3’ и R4’ представляют собой -H.
В некоторых вариантах реализации изобретения каждый из R, R’, R” и R5 независимо представляет собой –H или (C1-C3)алкил.
В некоторых вариантах реализации изобретения:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой –H, и если она представляет собой одинарную связь, то X1 представляет собой –H, Y представляет собой –OH или –SO3M;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой –H, и если она представляет собой одинарную связь, то X1 представляет собой –H, Y представляет собой –OH или –SO3M;
все R1, R2, R3, R4, R1’, R2’, R3’ и R4’ представляют собой -H;
R6 представляет собой -OMe;
оба X1’ и Y1’ представляют собой -H;
A и A’ представляют собой -O-; и
M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения D представлен следующей структурной формулой:
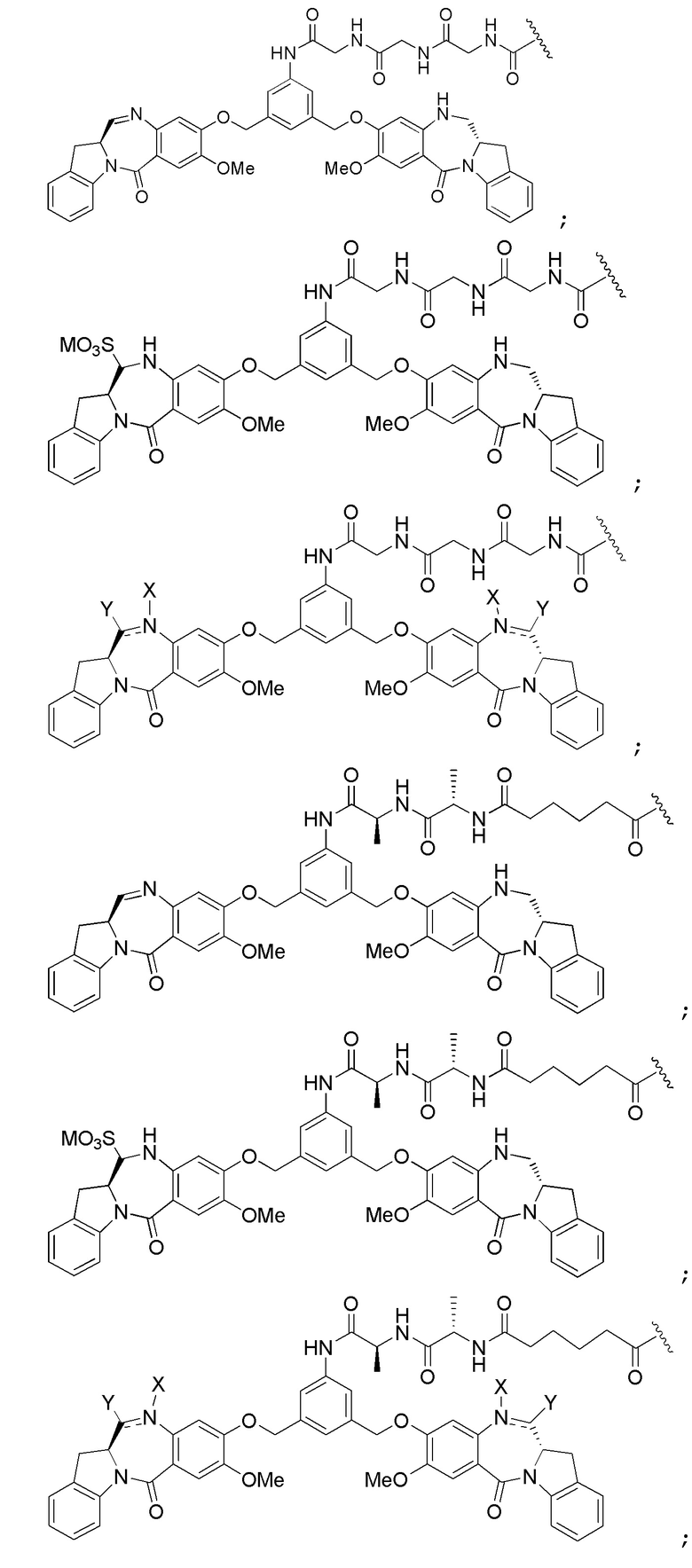

или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения оба R23 и R24 представляют собой H; и m’ представляет собой целое число от 1 до 6. В некоторых вариантах реализации изобретения Rh’ представляет собой H.
В некоторых вариантах реализации изобретения -L-JCB представлен следующей структурной формулой:
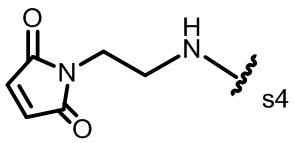 .
.
В некоторых вариантах реализации изобретения соединение представлено следующей структурной формулой:

где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
В некоторых вариантах реализации изобретения M представляет собой H+, Na+ или K+.
В другом аспекте данного изобретения предложена фармацевтическая композиция, содержащая конъюгат по данному изобретению и фармацевтически приемлемый носитель.
В другом аспекте данного изобретения предложен способ ингибирования аномального роста клеток или лечения пролиферативного нарушения, аутоиммунного нарушения, деструктивного поражения костей, инфекционного заболевания, вирусного заболевания, фиброзного заболевания, нейродегенеративного расстройства, панкреатита или заболевания почек у млекопитающего, включающий введение млекопитающему терапевтически эффективного количества конъюгата по данному изобретению и необязательно второго терапевтического агента.
В некоторых вариантах реализации изобретения данный способ ингибирует аномальный рост клеток или лечит пролиферативное нарушение. В некоторых вариантах реализации изобретения пролиферативное нарушение представляет собой рак, такой как гемобластоз или солидная опухоль. Типовой гемобластоз включает лейкоз и лимфому. Лейкоз может представлять собой острый миелоидный лейкоз (ОМЛ), острый лимфобластный лейкоз (ОЛЛ), такой как острый В-клеточный лимфобластный лейкоз (В-ОЛЛ), хронический миелогенный лейкоз (ХМЛ) или хронический лимфоцитарный лейкоз (ХЛЛ). Солидная опухоль может представлять собой меланому, рак легких (например, немелкоклеточный рак легкого), рак яичников, рак эндометрия, рак брюшины, рак поджелудочной железы, рак молочной железы, рак предстательной железы или рак шейки матки.
Следует понимать, что любой из вариантов реализации изобретения, описанных в данном документе, включая варианты реализации изобретения, описанные только в соответствии с одним аспектом данного изобретения, но не с другими аспектами, и включая варианты реализации, представленные только в Примерах, можно комбинировать с любым одним или более другими вариантами реализации, если это явным образом не опровергнуто или не является неприемлемым.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1А показывает ЖХ-МС дегликозилированного конъюгата huMOV19-C442-Mal-CX1-1-DM1, который, как было установлено, содержит в среднем 2 моль DM1/моль антитела согласно UV-Vis-спектроскопии; 99,3% мономера согласно SEC; и не содержит детектируемого неконъюгированного DM1 согласно ВЭЖХ на колонке HISEP.
Фиг. 1Б показывает ЖХ-МС дегликозилированного конъюгата huMOV19-C442-Mal-SPDB-DM4, который, как было установлено, содержит в среднем 2 моль DM4/моль антитела согласно UV-Vis-спектроскопии; 99,5% мономера согласно SEC; и 0,8% неконъюгированного DM4 согласно ВЭЖХ на колонке HISEP.
Фиг. 1В показывает ЖХ-МС дегликозилированного конъюгата huMOV19-C442-D5, который, как было установлено, содержит в среднем 2 моль D5/моль антитела согласно UV-Vis-спектроскопии; 94,6% мономера согласно SEC; и 0,8% неконъюгированного D5 согласно SEC/обращенно-фазовой ВЭЖХ.
Фиг. 1Г показывает ЖХ-МС дегликозилированного конъюгата huMOV19-C442-D4, который, как было установлено, содержит в среднем 2 моль D4/моль антитела согласно UV-Vis-спектроскопии; и 93,6% мономера согласно SEC.
Фиг. 1Д показывает ЖХ-МС дегликозилированного конъюгата huCD123-6Gv1.1S2-C442-D7, который, как было установлено, содержит в среднем 2 моль D7/моль антитела согласно UV-Vis-спектроскопии; 97,2% мономера согласно SEC; и 1,9% неконъюгированного D7 согласно SEC/обращенно-фазовой ВЭЖХ.
Фиг. 1Е показывает ЖХ-МС дегликозилированного конъюгата huCD123-6Gv4.7-C442-D5, который, как было установлено, содержит в среднем 2 моль D5/моль антитела согласно UV-Vis-спектроскопии и 94,8% мономера согласно SEC.
Фиг. 1Ж показывает ЖХ-МС дегликозилированного конъюгата huCD123-6Gv4.7-C442-D4, который, как было установлено, содержит в среднем 1,8 моль D4/моль антитела согласно UV-Vis-спектроскопии; и 97,4% мономера согласно SEC.
Фиг. 2 показывает, что Cys-связанные конъюгаты по меньшей мере так же активны, как Lys-связанные конъюгаты среди нескольких клеточных линий-мишеней (например, клеточной линии EOL-1 ОМЛ, клеточной линии KOPN-8 В-ОЛЛ и клеточной линии MOLM-1 ХМЛ), экспрессирующих антиген, распознаваемый антителом конъюгатов (т.е. CD123). Кривые данных, связывающие незакрашенные квадраты и незакрашенные кружки, представляют собой контрольные образцы с избытком неконъюгированных конкурирующих антител (т.е. chCD123-6), для кривых, связывающих закрашенные квадраты и закрашенные кружки, соответственно.
Фиг. 3А, 3Б и 3В показывают, что Cys-связанные конъюгаты по меньшей мере так же активны, как Lys-связанные конъюгаты среди нескольких клеточных линий-мишеней (например, клеток KB, клеток T47D и клеток KB, соответственно), экспрессирующих антиген (т.е. FRα), распознаваемый антителом конъюгатов (т.е. M9346A или Mov19). Кривые данных, обозначенные «+B», представляют собой соответствующие контрольные образцы с избытком неконъюгированных конкурирующих антител (т.е. неконъюгированного антитела M9346A).
Фиг. 4А и 4Б показывают, что Cys-связанный конъюгат huMOV19-C442-D5 и Lys-связанный конъюгат huMOV19-D2 обладают почти одинаковой неспецифической киллинговой активностью в 300,19 клетках.
Фиг. 5 показывает, что Cys-связанный конъюгат huMOV19-C442-D5 и Lys-связанные конъюгаты huMOV19-D2 обладают одинаковой активностью в моделях ксенотрансплантата NCI-H2110 НМРЛ, независимо от типа конъюгации (например, Lys-связь в сравнении с Cys-связью). Всем мышам вводили одну в/в инъекцию соответствующих ADC в указанной дозе по достижении ксенотрансплантатной опухолью размера около 100 мм3.
Фиг. 6 показывает фармакокинетику ADC huMOV19-C442-D5 у мышей CD1 в течение 28 дней.
Фиг. 7А показывает индивидуальное процентное изменение массы тела самок мышей CD-1, обработанных с помощью 200 мкг/кг сайт-специфического CysMab huMOV19-C442-D5. Фиг. 7Б показывает индивидуальное процентное изменение массы тела самок мышей CD-1, обработанных с помощью 250 мкг/кг сайт-специфического CysMab huMOV19-C442-D5. Фиг. 7В показывает индивидуальное процентное изменение массы тела самок мышей CD-1, обработанных с помощью 100 мкг/кг Lys-связанного huMOV19-D2. Фиг. 7Г показывает индивидуальное процентное изменение массы тела самок мышей CD-1, обработанных с помощью контроля растворителя, или 175, 200 или 250 мкг/кг сайт-специфического конъюгата huMOV19-C442-D5.
Фиг. 8 показывает, что конъюгация антитела huCD123-6Gv4.7 через Cys-связь с соединениями D4 и D5 лишь умеренно влияла на аффинность связывания конъюгатов.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Далее будет приведено детальное описание определенных вариантов реализации изобретения, примеры которых проиллюстрированы при помощи прилагаемых структур и формул. Хотя данное изобретение будет описано в отношении перечисленных вариантов реализации, следует понимать, что они не предназначены для ограничения изобретения такими вариантами реализации. Наоборот, предполагается, что данное изобретение включает все альтернативные варианты, модификации и эквивалентные варианты, которые могут быть включены в объем данного изобретения, определяемый формулой изобретения. Специалисту в данной области техники будут понятны многие способы и материалы, аналогичные или эквивалентные тем, что описаны в данной заявке, которые можно применять для реализации данного изобретения.
Следует понимать, что любой из вариантов реализации, описанных в данном документе, включая описанные в различных аспектах данного изобретения (например, соединения, молекулы соединения-линкера, конъюгаты, композиции, способы получения и применения) и различных частях данного описания (включая варианты реализации, описанные только в Примерах), можно комбинировать с одним или более другими вариантами реализации данного изобретения, если это явным образом не опровергнуто или не является неприемлемым. Комбинации вариантов реализации не ограничены конкретными комбинациями, заявленными в многочисленных зависимых пунктах формулы изобретения.
ОПРЕДЕЛЕНИЯ
В контексте данного документа термин «алкил» или «линейный, или разветвленный алкил» относится к насыщенному линейному или разветвленному одновалентному углеводородному радикалу, содержащему от одного до двадцати атомов углерода. Примеры алкила включают, но не ограничиваются ими, метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-метил-1-пропил, -CH2CH(CH3)2, 2-бутил, 2-метил-2-пропил, 1-пентил, 2-пентил, 3-пентил, 2-метил-2-бутил, 3-метил-2-бутил, 3-метил-1-бутил, 2-метил-1-бутил, 1-гексил, 2-гексил, 3-гексил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 3-метил-3-пентил, 2-метил-3-пентил, 2,3-диметил-2-бутил, 3,3-диметил-2-бутил, 1-гептил, 1-октил и т.п. Предпочтительно алкил содержит от одного до десяти атомов углерода. Более предпочтительно алкил содержит от одного до четырех атомов углерода.
Термин «алкенил» или «линейный или разветвленный алкенил» относится к линейному или разветвленному одновалентному углеводородному радикалу, содержащему от двух до двадцати атомов углерода и по меньшей мере один центр ненасыщенности, т.е. двойную связь углерод-углерод, где указанный алкениловый радикал включает радикалы, имеющие «цис» и «транс» ориентации, или в альтернативном варианте «E» и «Z» ориентации. Примеры включают, но не ограничиваются ими, этилен или винил (-CH=CH2), аллил (-CH2CH=CH2) и т.п. Предпочтительно алкенил содержит от двух до десяти атомов углерода. Более предпочтительно алкенил содержит от двух до четырех атомов углерода.
Термин «алкинил» или «линейный или разветвленный алкинил» относится к линейному или разветвленному одновалентному углеводородному радикалу, содержащему от двух до двадцати атомов углерода и по меньшей мере один центр ненасыщенности, т.е. тройную связь углерод-углерод. Примеры включают, но не ограничиваются ими, этинил, пропинил, 1-бутинил, 2-бутинил, 1-пентинил, 2-пентинил, 3-пентинил, гексинил и т.п. Предпочтительно алкинил содержит от двух до десяти атомов углерода. Более предпочтительно алкинил содержит от двух до четырех атомов углерода.
Термины «циклический алкил» и «циклоалкил» могут использоваться взаимозаменяемо. Они относятся к одновалентному насыщенному карбоциклическому кольцевому радикалу. Предпочтительно циклический алкил представляет собой 3-7-членный моноциклический кольцевой радикал. Более предпочтительно циклический алкил представляет собой циклогексил.
Термин «циклоалкилалкил» относится к описанной выше алкильной группе, которая замещена циклоалкильной группой.
Термин «циклический алкенил» относится к карбоциклическому кольцевому радикалу, содержащему по меньшей мере одну двойную связь в кольцевой структуре.
Термин «циклический алкинил» относится к карбоциклическому кольцевому радикалу, содержащему по меньшей мере одну тройную связь в кольцевой структуре.
Термин «арил» означает одновалентный ароматический углеводородный радикал, содержащий 6-18 атомов углерода, полученный посредством удаления одного атома водорода от одного атома углерода исходной ароматической кольцевой системы. Некоторые арильные группы представлены в типовых структурах как «Ar». Арил включает бициклические радикалы, содержащие ароматическое кольцо, конденсированное с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим, или гетероциклическим кольцом. Типовые арильные группы включают, но не ограничиваются ими, радикалы, полученные из бензола (фенил), замещенных бензолов, нафталина, антрацена, инденила, инданила, 1,2-дигидронафталина, 1,2,3,4-тетрагидронафтила и т.п. Предпочтительно арил представляет собой фенильную группу.
Термины «гетероцикл», «гетероциклил» и «гетероциклическое кольцо» используются в данном документе взаимозаменяемо и относятся к насыщенному или частично ненасыщенному (т.е. содержащему одну или более двойных и/или тройных связей в кольце) карбоциклическому радикалу, содержащему от 3 до 18 кольцевых атомов, в котором по меньшей мере один кольцевой атом представляет собой гетероатом, выбранный из азота, кислорода, фосфора и серы, а остальные кольцевые атомы представляют собой C, при этом один или более кольцевых атомов необязательно независимо замещены одним или более заместителями, описанными ниже. Гетероцикл может представлять собой моноцикл, содержащий от 3 до 7 кольцевых членов (от 2 до 6 атомов углерода и от 1 до 4 гетероатомов, выбранных из N, O, P и S), или бицикл, содержащий от 7 до 10 кольцевых членов (от 4 до 9 атомов углерода и от 1 до 6 гетероатомов, выбранных из N, O, P и S), например, бицикло [4,5], [5,5], [5,6] или [6,6] систему. Гетероциклы описаны в публикации Paquette, Leo A.; «Principles of Modern Heterocyclic Chemistry» (W. A. Benjamin, New York, 1968), в частности в главах 1, 3, 4, 6, 7 и 9; «The Chemistry of Heterocyclic Compounds, A series of Monographs» (John Wiley & Sons, New York, с 1950 года до данного времени), в частности в томах 13, 14, 16, 19 и 28; и J. Am. Chem. Soc. (1960) 82:5566. Термин «гетероциклил» также включает радикалы, где гетероциклические радикалы конденсированы с насыщенным, частично ненасыщенным кольцом или ароматическим карбоциклическим, или гетероциклическим кольцом. Примеры гетероциклических колец включают, но не ограничиваются ими, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидино, морфолино, тиоморфолино, тиоксанил, пиперазинил, гомопиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 2-пирролинил, 3-пирролинил, индолинил, 2H-пиранил, 4H-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил и азабицикло[2.2.2]гексанил. В объем данного определения также включены спиро-фрагменты. Примеры гетероциклической группы, в которой кольцевые атомы замещены оксо-фрагментами (=O), представляют собой пиримидинонил и 1,1-диоксотиоморфолинил.
В контексте данного документа термин «5- или 6-членный азотсодержащий гетероцикл» относится к гетероциклу, содержащему 5 или 6 кольцевых атомов по меньшей мере с одним кольцевым атомом азота. Он может необязательно дополнительно содержать от 1 до 3 гетероатомов, выбранных из O, N и S.
Термин «гетероарил» относится к одновалентному ароматическому радикалу из 5- или 6-членных колец и включает системы конденсированных колец (по меньшей мере одно из которых является ароматическим) из 5-18 атомов, содержащие один или более гетероатомов, независимо выбранных из азота, кислорода и серы. Примерами гетероарильных групп являются пиридинил (включая, например, 2-гидроксипиридинил), имидазолил, имидазопиридинил, пиримидинил (включая, например, 4-гидроксипиримидинил), пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, циннолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, триазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил.
Гетероциклические или гетероарильные группы могут быть присоединены через атом углерода (углерод-связанные) или азота (азот-связанные), если это возможно. В качестве примера, а не ограничения, гетероциклы или гетероарилы, связанные через атом углерода, присоединены в положении 2, 3, 4, 5 или 6 пиридина, положении 3, 4, 5 или 6 пиридазина, положении 2, 4, 5 или 6 пиримидина, положении 2, 3, 5 или 6 пиразина, положении 2, 3, 4 или 5 фурана, тетрагидрофурана, тиофурана, тиофена, пиррола или тетрагидропиррола, положении 2, 4 или 5 оксазола, имидазола или тиазола, положении 3, 4 или 5 изоксазола, пиразола или изотиазола, положении 2 или 3 азиридина, положении 2, 3 или 4 азетидина, положении 2, 3, 4, 5, 6, 7 или 8 хинолина или положении 1, 3, 4, 5, 6, 7 или 8 изохинолина.
В качестве примера, а не ограничения, гетероциклы или гетероарилы, связанные через атом азота, присоединены в положении 1 азиридина, азетидина, пиррола, пирролидина, 2-пирролина, 3-пирролина, имидазола, имидазолидина, 2-имидазолина, 3-имидазолина, пиразола, пиразолина, 2-пиразолина, 3-пиразолина, пиперидина, пиперазина, индола, индолина, 1H-индазола, положении 2 изоиндола или изоиндолина, положении 4 морфолина и положении 9 карбазола или O-карболина.
Гетероатомы, присутствующие в гетероариле или гетероциклиле, включают окисленные формы, такие как NO, SO и SO2.
Термин «гало» или «галоген» относится к F, Cl, Br или I.
В контексте данного документа термин «галогеналкил» относится к алкилу, как определено в данном документе, который замещен одной или более галогеновыми группами, как определено в данном документе. Галогеналкил может представлять собой моногалогеналкил, дигалогеналкил или полигалогеналкил. Моногалогеналкил может иметь один заместитель фтора, хлора, брома или йода. Дигалогеналкил или полигалогеналкил могут быть замещены двумя или более одинаковыми атомами галогена или комбинацией различных галогеновых групп. Примеры галогеналкила включают, но не ограничиваются ими, фторметил, дифторметил, трифторметил, хлорметил, дихлорметил, трихлорметил, пентафторэтил, гептафторпропил, дифторхлорметил, дихлорфторметил, дифторэтил, дифторпропил, дихлорэтил и дихлорпропил.
Термин «алкокси» в контексте данного документа относится к алкил-O-, где алкил является таким, как определено в данном документе выше. Примеры алкокси включают, не ограничиваясь ими, метокси, этокси, пропокси, 2-пропокси, бутокси, трет-бутокси, пентилокси, гексилокси и т.п.
Алкил, галогеналкил, алкокси, алкенил, алкинил, циклический алкил, циклический алкенил, циклический алкинил, карбоциклил, арил, гетероциклил и гетероарил, описанные выше, могут быть необязательно замещены одним или более (например, 2, 3, 4, 5, 6 или более) заместителями.
Если заместитель описан как «замещенный», то неводородный заместитель занимает место водородного заместителя у атома углерода, кислорода, серы или азота данного заместителя. Так, например, замещенный алкильный заместитель представляет собой алкильный заместитель, в котором по меньшей мере один неводородный заместитель занимает место водородного заместителя в данном алкильном заместителе. Для наглядности, монофторалкил представляет собой алкил, замещенный фтор-заместителем, а дифторалкил представляет собой алкил, замещенный двумя фтор-заместителями. Следует понимать, что если заместитель имеет более одного замещения, то неводородные заместители могут быть одинаковыми или различными (если не указано иное).
Если заместитель описан как «необязательно замещенный», то заместитель может быть либо (1) незамещенным, либо (2) замещенным. Если атом углерода заместителя описан как необязательно замещенный одним или более из списка заместителей, то один или более атомов водорода у данного атома углерода (при их наличии) могут быть по отдельности и/или вместе замещены независимо выбранным необязательным заместителем. Если атом азота заместителя описан как необязательно замещенный одним или более из списка заместителей, то один или более атомов водорода у данного атома азота (при их наличии) могут быть замещены независимо выбранным необязательным заместителем. Один типовой заместитель может быть изображен как -NR’R’’, где R’ и R’’ вместе с атомом азота, к которому они присоединены, могут образовывать гетероциклическое кольцо. Гетероциклическое кольцо, образованное из R’ и R’’ вместе с атомом азота, к которому они присоединены, может быть частично или полностью насыщенным. В одном варианте реализации изобретения гетероциклическое кольцо состоит из 3-7 атомов. В другом варианте реализации изобретения гетероциклическое кольцо выбрано из группы, состоящей из пирролила, имидазолила, пиразолила, триазолила, тетразолила, изоксазолила, пиридила и тиазолила.
В данном описании термины «заместитель», «радикал» и «группа» используются взаимозаменяемо.
Если группа заместителей обобщенно описана как необязательно замещенная одним или более из списка заместителей, то указанная группа может включать: (1) незамещаемые заместители, (2) замещаемые заместители, которые не замещены необязательными заместителями, и/или (3) замещаемые заместители, которые замещены одним или более необязательными заместителями.
Если заместитель описан как необязательно замещенный неводородными заместителями до определенного количества, то указанный заместитель может быть либо (1) незамещенным; либо (2) замещенным неводородными заместителями до определенного количества или до максимального количества замещаемых положений в данном заместителе, в зависимости от того, что меньше. Так, например, если заместитель описан как гетероарил, необязательно замещенный не более 3 неводородными заместителями, то любой гетероарил, содержащий менее 3 замещаемых положений, может быть необязательно замещен только таким количеством неводородных заместителей, которое равно количеству замещаемых положений в данном гетероариле. Такие заместители, в неограничивающих примерах, могут быть выбраны из линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, арила, гетероарила, гетероциклила, галогена, гуанидиния [-NH(C=NH)NH2], -OR100, NR101R102, -NO2, -NR101COR102, -SR100, сульфоксида, представленного -SOR101, сульфона, представленного -SO2R101, сульфоната -SO3M, сульфата -OSO3M, сульфонамида, представленного -SO2NR101R102, циано, азидо, -COR101, -OCOR101, -OCONR101R102 и полиэтиленгликолевого звена (-OCH2CH2)nR101, где М представляет собой Н или катион (такой как Na+ или K+); каждый из R101, R102 и R103 независимо выбран из H, линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена (-OCH2CH2)n-R104, где n представляет собой целое число от 1 до 24, арила, содержащего от 6 до 10 атомов углерода, гетероциклического кольца, содержащего от 3 до 10 атомов углерода, и гетероарила, содержащего от 5 до 10 атомов углерода; и R104 представляет собой Н или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, где алкил, алкенил, алкинил, арил, гетероарил и гетероциклил в группах, представленных R100, R101, R102, R103 и R104, необязательно замещены одним или более (например, 2, 3, 4, 5, 6 или более) заместителями, независимо выбранными из галогена, -OH, -CN, -NO2 и незамещенного линейного или разветвленного алкила, содержащего от 1 до 4 атомов углерода. Предпочтительно заместители для необязательно замещенного алкила, алкенила, алкинила, циклического алкила, циклического алкенила, циклического алкинила, карбоциклила, арила, гетероциклила и гетероарила, описанных выше, включают галоген, -CN, -NR102R103, -CF3, -OR101, арил, гетероарил, гетероциклил, -SR101, -SOR101, -SO2R101 и -SO3M.
Количество атомов углерода в группе указано в данном документе приставкой «Cx-xx» или «Cx-Cxx», где x и xx представляют собой целые числа. Например, «C1-4алкил» или «C1-C4 алкил» представляет собой алкильную группу, содержащую от 1 до 4 атомов углерода.
Термины «соединение» или «цитотоксическое соединение», «цитотоксический димер» и «цитотоксическое димерное соединение» используются взаимозаменяемо. Они предполагают включение соединений, для которых в данном изобретении описаны структура или формула, или любое их производное; или структура или формула, или любое их производное включены посредством ссылки. Данный термин также включает стереоизомеры, геометрические изомеры, таутомеры, сольваты, метаболиты, соли (например, фармацевтически приемлемые соли), а также пролекарства и пролекарственные соли соединений всех формул, описанных в данном изобретении. Данный термин также включает любые сольваты, гидраты и полиморфы любых вышеуказанных форм. Конкретное упоминание «стереоизомеров», «геометрических изомеров», «таутомеров», «сольватов», «метаболитов», «солей», «пролекарств», «солей пролекарств», «конъюгатов», «солей конъюгатов», «сольватов», «гидратов» или «полиморфов» в некоторых аспектах данного изобретения, описанного в данной заявке, не следует толковать как намеренное исключение этих форм в других аспектах данного изобретения, в которых термин «соединение» используется без указания этих других форм.
Термин «конъюгат» в контексте данного документа относится к соединению, описанному в данном документе, или его производному, которое связано с клеточносвязывающим агентом.
Термин «связываемый с клеточносвязывающим средством» в контексте данного документа относится к соединениям, описанным в данном документе, или их производным, содержащим по меньшей мере одну связывающую группу или ее предшественник, подходящий для связывания этих соединений или их производных с клеточносвязывающим агентом.
Термин «предшественник» данной группы относится к любой группе, которая может образовывать эту группу посредством снятия защиты, химической модификации или реакции связывания.
Термин «хиральный» относится к молекулам, которые при наложении обладают свойством не совпадать со своим зеркальным отображением, тогда как термин «ахиральный» относится к молекулам, которые при наложении совпадают со своим зеркальным отображением.
Термин «стереоизомер» относится к соединениям, которые имеют одинаковый химический состав и связность, но различные ориентации атомов в пространстве, которые не могут быть взаимопревращены при вращении вокруг одинарных связей.
Термин «диастереомер» относится к стереоизомеру с двумя или более центрами хиральности, молекулы которого не являются зеркальными отображениями друг друга. Диастереомеры имеют различные физические свойства, например, температуры плавления, температуры кипения, спектральные свойства и реакционную способность. Смеси диастереомеров можно разделить с помощью аналитических методик с высоким разрешением, таких как кристаллизация, электрофорез и хроматография.
Термин «энантиомеры» относится к двум стереоизомерам соединения, которые при наложении не совпадают с зеркальными отображениями друг друга.
Стереохимические определения и условные обозначения, используемые в данном документе, как правило, соответствуют S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, Нью-Йорк; и Eliel, E. and Wilen, S., «Stereochemistry of Organic Compounds», John Wiley & Sons, Inc., Нью-Йорк, 1994. Соединения по данному изобретению могут содержать асимметрические или хиральные центры и, таким образом, существовать в различных стереоизомерных формах. Подразумевается, что все стереоизомерные формы соединений по данному изобретению, включая, но не ограничиваясь ими, диастереомеры, энантиомеры и атропизомеры, а также их смеси, такие как рацемические смеси, образуют часть данного изобретения. Многие органические соединения существуют в оптически активных формах, т.е. они обладают способностью вращать плоскость плоскополяризованного света. В описании оптически активного соединения приставки D и L или R и S используются для обозначения абсолютной конфигурации молекулы относительно ее хирального центра (центров). Приставки d и l или (+) и (-) используются для обозначения знака вращения плоскополяризованного света соединением, при этом (-) или 1 означают, что соединение является левовращающим. Соединение с приставкой (+) или d является правовращающим. Для данной химической структуры эти стереоизомеры являются одинаковыми за исключением того, что они представляют собой зеркальные отражения друг друга. Отдельный стереоизомер может упоминаться также как энантиомер, а смесь таких изомеров часто называют энантиомерной смесью. Смесь энантиомеров 50:50, которую называют рацемической смесью или рацематом, может образовываться в случае, если химическая реакция или процесс были нестереоселективными или нестереоспецифическими. Термины «рацемическая смесь» и «рацемат» относятся к эквимолярной смеси двух типов энантиомеров, не обладающей оптической активностью.
Термин «таутомер» или «таутомерная форма» относится к структурным изомерам различных энергий, которые могут быть взаимопревращены за счет низкоэнергетичного барьера. Например, протонные таутомеры (также известные как прототропные таутомеры) включают взаимопревращения за счет миграции протона, такие как кето-енольная и имин-енаминная изомеризация. Валентные таутомеры включают взаимопревращения за счет перегруппировки некоторых связывающих электронов.
Одна из предпочтительных форм пролекарства по данному изобретению включает соединения (с линкерными группами или без них) и конъюгаты по данному изобретению, содержащие аддукт, образованный между иминной связью данных соединений / конъюгатов и способным взаимодействовать с иминами реагентом. Другая предпочтительная форма пролекарства по данному изобретению включает соединения, такие как соединения формул (I) - (IV), где если двойная линия  между N и C представляет собой одинарную связь, то X представляет собой H или аминозащитную группу, и данное соединение становится пролекарством. Пролекарство по данному изобретению может содержать одну или обе формы пролекарств, описанных в данном документе (например, может содержать аддукт, образованный между иминной связью данных соединений / конъюгатов и способным взаимодействовать с иминами реагентом, и/или содержать уходящую группу Y, если X представляет собой -H).
между N и C представляет собой одинарную связь, то X представляет собой H или аминозащитную группу, и данное соединение становится пролекарством. Пролекарство по данному изобретению может содержать одну или обе формы пролекарств, описанных в данном документе (например, может содержать аддукт, образованный между иминной связью данных соединений / конъюгатов и способным взаимодействовать с иминами реагентом, и/или содержать уходящую группу Y, если X представляет собой -H).
Термин «способный взаимодействовать с иминами реагент» относится к реагенту, способному взаимодействовать с иминогруппой. Примеры способного взаимодействовать с иминами реагента включают, но не ограничиваются ими, сульфиты (H2SO3, H2SO2 или соль HSO3-, SO32- или HSO2-, образованную катионом), метабисульфит (H2S2O5 или соль S2O52-, образованную катионом), моно-, ди-, три- и тетратиофосфаты (PO3SH3, PO2S2H3, POS3H3, PS4H3 или соль PO3S3-, PO2S23-, POS33- или PS43-, образованную катионом), тиофосфатные сложные эфиры ((RiO)2PS(ORi), RiSH, RiSOH, RiSO2H, RiSO3H), различные амины (гидроксиламин (например, NH2OH), гидразин (например, NH2NH2), NH2O-Ri, Ri’NH-Ri, NH2-Ri), NH2-CO-NH2, NH2-C(=S)-NH2, тиосульфат (H2S2O3 или соль S2O32-, образованную катионом), дитионит (H2S2O4 или соль S2O42-, образованную катионом), фосфордитиоат (P(=S)(ORk)(SH)(OH) или его соль, образованную катионом), гидроксамовую кислоту (RkC(=O)NHOH или соль, образованную катионом), гидразид (RkCONHNH2), формальдегидсульфоксилат (HOCH2SO2H или соль HOCH2SO2-, образованную катионом, такую как HOCH2SO2-Na+), гликозилированный нуклеотид (такой как ГДФ-манноза), флударабин или их смесь, где каждый из Ri и Ri’ независимо представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H и -PO3H; Ri и Ri’ необязательно могут быть дополнительно замещены заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; и Rk представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил (предпочтительно Rk представляет собой линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, более предпочтительно Rk представляет собой метил, этил или пропил). Предпочтительно катион представляет собой одновалентный катион, такой как Na+ или K+. Предпочтительно способный взаимодействовать с иминами реагент выбран из сульфитов, гидроксиламина, мочевины и гидразина. Более предпочтительно способный взаимодействовать с иминами реагент представляет собой NaHSO3 или KHSO3.
В контексте данного документа соединение «бензодиазепина» представляет собой соединение, имеющее бензодиазепиновую структуру. Бензодиазепиновое ядро может быть замещено и/или сконденсировано с одной или более кольцевыми структурами. Оно также включает соединение, имеющее два бензодиазепиновых ядра, соединенных линкером. Иминная функциональная группа (-C=N-) как часть бензодиазепинового ядра может быть восстановлена.
В контексте данного документа соединение «индолинбензодиазепина» (IBD) представляет собой соединение, имеющее индолинбензодиазепиновую структуру. Индолинбензодиазепин может быть замещен. Он также включает соединение, имеющее два индолинбензодиазепиновых ядра, соединенных линкером. Иминная функциональная группа (-C=N-) как часть индолинбензодиазепинового ядра может быть восстановлена.
Выражение «фармацевтически приемлемая соль» в контексте данного документа относится к фармацевтически приемлемым органическим или неорганическим солям соединения по данному изобретению. Типовые соли включают, но не ограничиваются ими, сульфатные, цитратные, ацетатные, оксалатные, хлоридные, бромидные, йодидные, нитратные, бисульфатные, фосфатные, кислые фосфатные, изоникотинатные, лактатные, салицилатные, кислые цитратные, тартратные, олеатные, таннатные, пантотенатные, битартратные, аскорбатные, сукцинатные, малеатные, гентизинатные, фумаратные, глуконатные, глюкуронатные, сахаратные, формиатные, бензоатные, глутаматные, метансульфонатные «мезилатные», этансульфонатные, бензолсульфонатные, п-толуолсульфонатные, памоатные (т.е. 1,1’-метилен-бис-(2-гидрокси-3-нафтоатные)) соли, соли щелочных металлов (например, натрия и калия), соли щелочноземельных металлов (например, магния) и соли аммония. Фармацевтически приемлемые соли могут содержать включение другой молекулы, такой как ацетат-ион, сукцинат-ион или другой противоион. Противоионом может быть любой органический или неорганический фрагмент, который стабилизирует заряд исходного соединения. Кроме того, фармацевтически приемлемая соль может содержать в своей структуре более одного заряженного атома. В случаях, где несколько заряженных атомов являются частью фармацевтически приемлемой соли, она может содержать несколько противоионов. Таким образом, фармацевтически приемлемая соль может содержать один или более заряженных атомов и/или один или более противоионов.
Если соединение по данному изобретению представляет собой основание, то необходимая фармацевтически приемлемая соль может быть получена любым подходящим способом, доступным в данной области техники, например, обработкой указанного свободного основания неорганической кислотой, такой как соляная кислота, бромистоводородная кислота, серная кислота, азотная кислота, метансульфоновая кислота, фосфорная кислота и т.п., или органической кислотой, такой как уксусная кислота, малеиновая кислота, янтарная кислота, миндальная кислота, фумаровая кислота, малоновая кислота, пировиноградная кислота, щавелевая кислота, гликолевая кислота, салициловая кислота, пиранозидильная кислота, такая как глюкуроновая кислота или галактуроновая кислота, альфа-гидроксикислота, такая как лимонная кислота или винная кислота, аминокислота, такая как аспарагиновая кислота или глутаминовая кислота, ароматическая кислота, такая как бензойная кислота или коричная кислота, сульфоновая кислота, такая как п-толуолсульфоновая кислота или этансульфоновая кислота, или т.п.
Если соединение по данному изобретению представляет собой кислоту, то необходимая фармацевтически приемлемая соль может быть получена любым подходящим способом, например, обработкой указанной свободной кислоты неорганическим или органическим основанием, таким как амин (первичный, вторичный или третичный), гидроксид щелочного металла или гидроксид щелочноземельного металла, или т.п. Иллюстративные примеры подходящих солей включают, но не ограничиваются ими, органические соли, полученные из аминокислот, таких как глицин и аргинин, аммиака, первичных, вторичных и третичных аминов, и циклических аминов, таких как пиперидин, морфолин и пиперазин, и неорганические соли, полученные из натрия, кальция, калия, магния, марганца, железа, меди, цинка, алюминия и лития.
В контексте данного документа термин «сольват» означает соединение, которое дополнительно содержит стехиометрическое или нестехиометрическое количество растворителя, такого как вода, изопропанол, ацетон, этанол, метанол, ДМСО, этилацетат, уксусная кислота, а также этаноламин, дихлорметан, 2-пропанол или т.п., связанного нековалентными силами межмолекулярного взаимодействия. Сольваты или гидраты соединений легко получают добавлением по меньшей мере одного молярного эквивалента гидроксильного растворителя, такого как метанол, этанол, 1-пропанол, 2-пропанол или вода, к указанному соединению, что приводит к сольватации или гидратации иминного фрагмента.
Термины «аномальный рост клеток» и «пролиферативное нарушение» используются в данной заявке взаимозаменяемо. «Аномальный рост клеток», в контексте данного документа, если не указано иное, относится к росту клеток, который не зависит от нормальных регуляторных механизмов (например, потери контактного торможения). Он включает, например, аномальный рост: (1) опухолевых клеток (опухолей), которые разрастаются посредством экспрессии мутантной тирозинкиназы или сверхэкспрессии рецепторной тирозинкиназы; (2) доброкачественных и злокачественных клеток других пролиферативных заболеваний, в которых происходит аберрантная активация тирозинкиназы; (3) любых опухолей, которые разрастаются за счет рецепторных тирозинкиназ; (4) любых опухолей, которые разрастаются вследствие аберрантной активации серин/треонинкиназы; и (5) доброкачественных и злокачественных клеток других пролиферативных заболеваний, в которых происходит аберрантная активация серин/треонинкиназы.
Термины «рак» и «раковый» относятся или описывают физиологическое состояние у млекопитающих, которое, как правило, характеризуется нерегулируемым ростом клеток. «Опухоль» содержит одну или более раковых клеток и/или доброкачественных или предраковых клеток.
«Терапевтический агент» включает биологический агент, такой как антитело, пептид, белок, фермент, или химиотерапевтический агент. Терапевтический агент также включает иммуноконъюгаты клеточносвязывающих агентов (CBA) и химических соединений, таких как конъюгаты антитела с лекарственным препаратом (ADC). Лекарственный препарат в конъюгатах может представлять собой цитотоксический агент, такой как описанный в данном документе.
«Химиотерапевтический агент» представляет собой химическое соединение, применимое в лечении рака.
«Метаболит» или «катаболит» представляет собой продукт, полученный посредством метаболизма или катаболизма определенного соединения, его производного или его конъюгата, или его соли в организме. Метаболиты соединения, его производного или его конъюгата могут быть идентифицированы с помощью стандартных методов, известных в данной области техники, и их активность определяют с помощью испытаний, таких как испытания, описанные в данном документе. Такие продукты могут быть образованы, например, в результате окисления, гидроксилирования, восстановления, гидролиза, амидирования, дезамидирования, этерификации, деэтерификации, ферментативного расщепления и т.п. введенного соединения. Соответственно, данное изобретение включает метаболиты соединений, их производных или их конъюгатов по данному изобретению, включая соединения, их производные или их конъюгаты, полученные способом, включающим приведение в контакт соединения, его производного или его конъюгата по данному изобретению с организмом млекопитающего в течение периода времени, достаточного для получения его метаболического продукта.
Выражение «фармацевтически приемлемый» означает, что вещество или композиция должны быть совместимы химически и/или токсикологически с другими ингредиентами, содержащимися в лекарственной форме, и/или с млекопитающим, которое получает лечение ими.
Термин «защитная группа» или «защитный фрагмент» относится к заместителю, который обычно используют для блокирования или защиты конкретной функциональной группы при взаимодействии других функциональных групп соединения, его производного или его конъюгата. Например, «аминозащитная группа» или «аминозащитный фрагмент» представляет собой заместитель, присоединенный к аминогруппе, который блокирует или защищает функциональную аминогруппу в соединении. Такие группы хорошо известны в данной области техники (см., например, P. Wuts and T. Greene, 2007, Protective Groups in Organic Synthesis, глава 7, J. Wiley & Sons, Нью-Джерси), и их примерами являются карбаматы, такие как метил- и этилкарбамат, FMOC, замещенные этилкарбаматы, карбаматы, расщепленные посредством 1,6-β-элиминирования (также называемые «саморасщепляющимися»), мочевины, амиды, пептиды, алкильные и арильные производные. Подходящие аминозащитные группы включают ацетил, трифторацетил, трет-бутоксикарбонил (BOC), бензилоксикарбонил (CBZ) и 9-флуоренилметиленоксикарбонил (Fmoc). Общее описание защитных групп и их применение см. в публикации P. G.M. Wuts & T. W. Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, Нью-Йорк, 2007.
Термин «уходящая группа» относится к группе заряженного или незаряженного фрагмента, которая отщепляется во время замещения или вытеснения. Такие уходящие группы хорошо известны в данной области техники и включают, но не ограничиваются ими, галогены, сложные эфиры, алкокси, гидроксил, тозилаты, трифлаты, мезилаты, нитрилы, азид, карбамат, дисульфиды, сложные тиоэфиры, простые тиоэфиры и соединения диазония.
Термин «бифункциональный сшивающий агент», «бифункциональный линкер» или «сшивающие агенты» относится к модифицирующим агентам, обладающим двумя реакционноспособными группами; одна из которых способна взаимодействовать с клеточносвязывающим агентом, а другая взаимодействует с цитотоксическим соединением, связывая два указанных фрагмента друг с другом. Такие бифункциональные сшивающие агенты хорошо известны в данной области техники (см., например, публикацию Isalm and Dent in Bioconjugation, глава 5, с. 218-363, Groves Dictionaries Inc., Нью-Йорк, 1999). Например, бифункциональные сшивающие агенты, которые обеспечивают связь посредством простой тиоэфирной связи, включают N-сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (SMCC) для введения малеимидных групп, или N-сукцинимидил-4-(йодацетил)аминобензоат (SIAB) для введения йодацетильных групп. Другие бифункциональные сшивающие агенты, которые могут обеспечивать введение малеимидных групп или галогенацетильных групп в клеточносвязывающий агент, хорошо известны в данной области техники (см. заявки на патент США 2008/0050310, 20050169933 от Pierce Biotechnology Inc., п/я 117, Рокленд, штат Иллинойс 61105, США) и включают, без ограничения ими, бис-малеимидополиэтиленгликоль (BMPEO), BM(PEO)2, BM(PEO)3, N-(β-малеимидопропилокси)сукцинимидный эфир (BMPS), N-сукцинимидильный эфир γ-малеимидомасляной кислоты (GMBS), N-гидроксисукцинимидный эфир ε-малеимидокапроновой кислоты (EMCS), NHS 5-малеимидовалериановой кислоты, HBVS, N-сукцинимидил-4-(N-малеимидометил)-циклогексан-1-карбокси-(6-амидокапроат), который представляет собой «длинноцепочечный» аналог SMCC (LC-SMCC), м-малеимидобензоил-N-гидроксисукцинимидный эфир (MBS), гидразид или соль HCl и 4-(4-N-малеимидофенил)-масляной кислоты (MPBH), N-сукцинимидил-3-(бромацетамидо)пропионат (SBAP), N-сукцинимидилиодацетат (SIA), N-сукцинимидильный эфир κ-малеимидоундекановой кислоты (KMUA), N-сукцинимидил-4-(п-малеимидофенил)-бутират (SMPB), сукцинимидил-6-(β-малеимидопропионамидо)гексаноат (SMPH), сукцинимидил-(4-винилсульфонил)бензоат (SVSB), дитиобис-малеимидоэтан (DTME), 1,4-бис-малеимидобутан (BMB), 1,4-бис-малеимидил-2,3-дигидроксибутан (BMDB), бис-малеимидогексан (BMH), бис-малеимидоэтан (BMOE), сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC), сульфосукцинимидил-(4-иодацетил)аминобензоат (сульфо-SIAB), м-малеимидобензоил-N-гидроксисульфосукцинимидный эфир (сульфо-MBS), N-(γ-малеимидобутирилокси)сульфосукцинимидный эфир (сульфо-GMBS), N-(ε-малеимидокапроилокси)сульфосукцинимидный эфир (сульфо-EMCS), N-(κ-малеимидоундеканоилокси)сульфосукцинимидный эфир (сульфо-KMUS) и сульфосукцинимидил-4-(п-малеимидофенил)бутират (сульфо-SMPB).
Гетеробифункциональные сшивающие агенты представляют собой бифункциональные сшивающие агенты, имеющие две различные реакционноспособные группы. Гетеробифункциональные сшивающие агенты, содержащие как амино-реакционноспособную N-гидроксисукцинимидную группу (группу NHS), так и карбонил-реакционноспособную гидразиновую группу, могут применяться для связывания цитотоксических соединений, описанных в данном документе, с клеточносвязывающим агентом (например, антителом). Примеры таких коммерчески доступных гетеробифункциональных сшивающих агентов включают сукцинимидил-6-гидразиноникотинамид-ацетон-гидразон (SANH), сукцинимидил-4-гидразидтерефталата гидрохлорид (SHTH) и сукцинимидилгидразиния никотината гидрохлорид (SHNH). Конъюгаты, содержащие кислотонеустойчивую связь, также могут быть получены с применением содержащего гидразин производного бензодиазепина по данному изобретению. Примеры бифункциональных сшивающих агентов, которые могут применяться, включают сукцинимидил-п-формилбензоат (SFB) и сукцинимидил-п-формилфеноксиацетат (SFPA).
Бифункциональные сшивающие агенты, которые могут обеспечивать связь клеточносвязывающего агента с цитотоксическими соединениями посредством дисульфидных связей, известны в данной области техники и включают N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP), N-сукцинимидил-4-(2-пиридилдитио)пентаноат (SPP), N-сукцинимидил-4-(2-пиридилдитио)бутаноат (SPDB), N-сукцинимидил-4-(2-пиридилдитио)-2-сульфобутаноат (сульфо-SPDB) для введения дитиопиридильных групп. Другие бифункциональные сшивающие агенты, которые могут применяться для введения дисульфидных групп, известны в данной области техники и описаны в патентах США 6913748, 6716821 и в публикациях патентов США 20090274713 и 20100129314, все из которых включены в данный документ посредством ссылки. В альтернативном варианте также могут применяться сшивающие агенты, которые обеспечивают введение тиольных групп, такие как 2-иминотиолан, гомоцистеин тиолактон или S-ацетилянтарный ангидрид.
Термины «линкер», «линкерный фрагмент» или «связывающая группа» в контексте данного документа относятся к фрагменту, который соединяет две группы, такие как клеточносвязывающий агент и цитотоксическое соединение, друг с другом. Как правило, линкер является по сути инертным в условиях, в которых он связывает две указанные группы. Бифункциональный сшивающий агент может содержать две реакционноспособные группы, по одной на каждом конце линкерного фрагмента, так чтобы одна реакционноспособная группа могла сначала взаимодействовать с цитотоксическим соединением с получением соединения, содержащего линкерный фрагмент и вторую реакционноспособную группу, которая впоследствии может взаимодействовать с клеточносвязывающим агентом. В альтернативном варианте один конец бифункционального сшивающего агента может сначала взаимодействовать с клеточносвязывающим агентом с получением клеточносвязывающего агента, содержащего линкерный фрагмент и вторую реакционноспособную группу, которая впоследствии может взаимодействовать с цитотоксическим соединением. Линкерный фрагмент может содержать химическую связь, которая обеспечивает возможность высвобождения цитотоксического фрагмента в определенном месте. Подходящие химические связи хорошо известны в данной области техники и включают дисульфидные связи, простые тиоэфирные связи, кислотонеустойчивые связи, фотолабильные связи, пептидаза-неустойчивые связи и эстераза-неустойчивые связи (см., например, патенты США №№ 5208020; 5475092; 6441163; 6716821; 6913748; 7276497; 7276499; 7368565; 7388026 и 7414073). Предпочтительными являются дисульфидные связи, простые тиоэфирные и пептидаза-неустойчивые связи. Другие линкеры, которые могут применяться в данном изобретении, включают нерасщепляемые линкеры, такие как линкеры, подробно описанные в публикации патента США № 20050169933, или заряженные линкеры, или гидрофильные линкеры, описанные в US 2009/0274713, US 2010/01293140 и WO 2009/134976, каждый из которых специально включен в данный документ посредством ссылки.
В одном варианте реализации изобретения связывающая группа с реакционноспособной группой, присоединенной на одном конце, такой как реакционноспособный сложный эфир, выбрана из следующего:
-O(CR20R21)m(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-O(CR20R21)m(CR26=CR27)m’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-O(CR20R21)m(алкинил)n’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-O(CR20R21)m(пиперазино)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-O(CR20R21)m(пирроло)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-O(CR20R21)mA”m”(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-S(CR20R21)m(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-S(CR20R21)m(CR26=CR27)m’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-S(CR20R21)m(алкинил)n’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-S(CR20R21)m(пиперазино)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-S(CR20R21)m(пирроло)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-S(CR20R21)mA”m”(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-NR33(C=O)p”(CR20R21)m(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-NR33(C=O)p”(CR20R21)m(CR26=CR27)m’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-NR33(C=O)p”(CR20R21)m(алкинил)n’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q-(CO)tX’’,
-NR33(C=O)p”(CR20R21)m(пиперазино)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q (CO)tX’’,
-NR33(C=O)p”(CR20R21)m(пирроло)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q-(CO)tX’’,
-NR33(C=O)p”(CR20R21)mA”m”(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)m(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)m(CR26=CR27)m’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)m(алкинил)n’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)m(пиперазино)t’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)mA”m”(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)m(CR29=N-NR30)n”(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q(CO)tX’’,
-(CR20R21)m(CR29=N-NR30)n”(CR26=CR27)m’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’
(CR24R25)q(CO)tX’’,
-(CR20R21)m(CR29=N-NR30)n”( алкинил)n’(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’
(CR24R25)q-(CO)tX’’,
-(CR20R21)m(CR29=N-NR30)n”A”m”(CR22R23)n(OCH2CH2)p(CR40R41)p”Y’’(CR24R25)q
(CO)tX’’,
где:
m, n, p, q, m’, n’, t’ представляют собой целые числа от 1 до 10 или необязательно равны 0;
t, m”, n” и p” равны 0 или 1;
X” выбран из OR36, SR37, NR38R39, где R36, R37, R38, R39 представляют собой H или линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 20 атомов углерода, и, или, полиэтиленгликолевое звено -(OCH2CH2)n, R37 необязательно представляет собой тиольную защитную группу, если t = 1, то COX’’ образует реакционноспособный сложный эфир, выбранный из N-гидроксисукцинимидных эфиров, N-гидроксифталимидных эфиров, N-гидроксисульфосукцинимидных эфиров, пара-нитрофениловых эфиров, динитрофениловых эфиров, пентафторфениловых эфиров и их производных, при этом указанные производные облегчают образование амидной связи;
Y’’ отсутствует или выбран из O, S, S-S или NR32, где R32 имеет такое же определение, как указано выше для R; или
если Y” не представляет собой S-S и t = 0, то X” выбран из малеимидной группы, галогенацетильной группы или SR37, где R37 имеет такое же определение, как указано выше;
A” представляет собой остаток аминокислоты или полипептида, содержащий от 2 до 20 аминокислотных звеньев;
R20, R21, R22, R23, R24, R25, R26 и R27 являются одинаковыми или различными и представляют собой -H или линейный или разветвленный алкил, содержащий от 1 до 5 атомов углерода;
R29 и R30 являются одинаковыми или различными и представляют собой -H или алкил, содержащий от 1 до 5 атомов углерода;
R33 представляет собой -H или линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 12 атомов углерода, полиэтиленгликолевое звено R-(OCH2CH2)n-, или R33 представляет собой -COR34, -CSR34, -SOR34 или -SO2R34, где R34 представляет собой H или линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 20 атомов углерода, или полиэтиленгликолевое звено -(OCH2CH2)n; и
один из R40 и R41 необязательно представляет собой отрицательно или положительно заряженную функциональную группу, а другой представляет собой Н или алкил, алкенил, алкинил, содержащий от 1 до 4 атомов углерода.
Любая из указанных выше связывающих групп может присутствовать в любом из соединений, соединений лекарственного препарата с линкером или конъюгатов по данному изобретению, включая замену связывающих групп любой из формул, описанных в данном документе.
Термин «аминокислота» относится к природным аминокислотам или не встречающейся в природе аминокислоте. В одном варианте реализации изобретения аминокислота представлена NH2-C(Raa’Raa)-C(=O)OH, где каждый из Raa и Raa’ независимо представляет собой H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероарил или гетероциклил, или Raa и N-концевой атом азота могут вместе образовывать гетероциклическое кольцо (например, как в пролине). Термин «аминокислотный остаток» относится к соответствующему остатку при удалении одного атома водорода из аминного и/или карбоксильного конца аминокислоты, такому как -NH-C(Raa’Raa)-C(=O)O-.
Термин «катион» относится к иону с положительным зарядом. Катион может быть одновалентным (например, Na+, K+ и т.д.), двухвалентным (например, Ca2+, Mg2+ и т.д.) или поливалентным (например, Al3+ и т.д.). Предпочтительно катион является одновалентным.
Термин «терапевтически эффективное количество» означает количество активного соединения или конъюгата, которое вызывает необходимую биологическую реакцию у субъекта. Такая реакция включает облегчение симптомов заболевания или расстройства, подлежащего лечению, предотвращение, ингибирование или задержку рецидива симптома заболевания или самого заболевания, увеличение продолжительности жизни субъекта по сравнению с отсутствием лечения, или предотвращение, ингибирование или задержку прогрессирования симптома заболевания или самого заболевания. Определение эффективного количества находится в пределах возможностей специалистов в данной области техники, особенно в свете подробного описания, представленного в данном документе. Токсичность и терапевтическая эффективность соединения или конъюгата могут быть определены стандартными фармацевтическими способами в клеточных культурах и на подопытных животных. Эффективное количество соединения или конъюгата по данному изобретению или другого терапевтического агента, подлежащего введению субъекту, зависит от стадии, категории и состояния множественной миеломы и характеристик субъекта, таких как общее состояние здоровья, возраст, пол, масса тела и переносимость лекарственных средств. Эффективное количество соединения или конъюгата по данному изобретению или другого терапевтического агента, подлежащего введению, зависит также от способа введения и лекарственной формы. Величина дозы и интервал могут быть подобраны индивидуально для обеспечения уровней активного соединения в плазме, которые достаточны для поддержания необходимого терапевтического эффекта.
Термин «сконструированное антитело с цистеиновыми заменами» включает антитело, содержащее по меньшей мере один Cys, который обычно не присутствует в данном остатке легкой цепи или тяжелой цепи антитела. Такой Cys, который также может называться «сконструированный Cys», может быть введен, например, с помощью стандартной рекомбинантной технологии (например, посредством замены кодирующей последовательности для остатка не-Cys в остатке-мишени кодирующей последовательностью для Cys). В некоторых вариантах реализации изобретения сконструированное антитело с Cys-заменами по данному изобретению содержит сконструированный Cys в тяжелой цепи. В некоторых вариантах реализации изобретения сконструированный Cys находится в домене CH3 тяжелой цепи или вблизи него. В некоторых вариантах реализации изобретения сконструированный Cys представляет собой остаток 442 тяжелой цепи (нумерация EU/OU).
В контексте данного документа все аминокислотные остатки антитела, описанные в данном документе, нумеруются в соответствии с EU-индексом, Kabat et al., Sequences of Proteins of Immunological Interest, 5ое изд., публикация NIH № 91-3242, 1991 (нумерация EU/OU, полное содержание включены в данный документ посредством ссылки). Известные изотипы обозначают как G1, G2, G4 и т.д.
Некоторые примеры, представленные ниже, относятся к различным гуманизированным антителам к CD123, номенклатура таких антител вкратце описана в данном документе. Антитела одного класса huCD123-6 являются гуманизированными посредством прививания 6 CDR из тяжелых и легких цепей мышиного анти-CD123 антитела muCD123-6. В этих антителах буква «G» указана сразу после обозначения клона (т.е. huCD123-6), которое, в свою очередь, следует за номером версии, который обозначает происхождение последовательностей вариабельных областей легкой цепи и тяжелой цепи человека. Таким образом, huCD123-6Gv4.6 относится к гуманизированному антителу CD123, полученному посредством прививания («G») 6 CDR областей из соответствующего антитела muCDR123-6 на вариабельную область Gv4 легкой цепи и на вариабельную область Gv6 тяжелой цепи человека. Аналогичным образом, Gv4.7 содержит вариабельную область Gv4 легкой цепи и вариабельную область Gv7 тяжелой цепи человека.
Антитела другого класса huCD123-6 гуманизируются посредством изменения поверхности. Антитело с измененной поверхностью, которое имеет последовательность huCD123-6rhv1.1 тяжелой цепи с измененной поверхностью и последовательность huCD123-6rlv1.0 легкой цепи с измененной поверхностью, представляет собой huCD123-6Rv1.1.
Если любое из антител к CD123 содержит сконструированный остаток Cys, как описано выше, то данное антитело может содержать обозначение CysMab или C442, например huCD123-6Gv4.7-C442. Остаток C442 может быть конъюгирован с цитотоксическим лекарственным средством/агентом через свободную тиольную группу остатка C442, например, посредством взаимодействия с тиол-реакционноспособным агентом цитотоксического лекарственного средства (например, малеимидную группу). Типичный список таких цитотоксических лекарственных средств с тиол-реакционноспособными группами - D4-D7 - и их синтез описаны в Примере 1 и приведены в таблице ниже. Дополнительные родственные соединения D1, D2, DGN462 и D3, которые имеют те же структуры, что и D4, D5, D6 и D7, соответственно, но не имеют тиол-реакционноспособной группы, также приведены ниже. D1-D3 и DGN462 не могут связываться с C442 из-за отсутствия малеимидо-тиольной реакционноспособной группы.



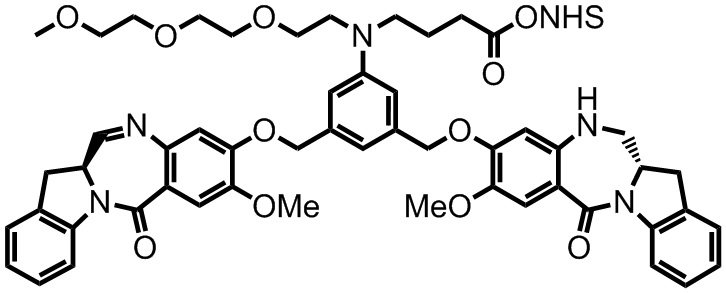





Конъюгаты между антителами по данному изобретению с D4-D7 через свободную тиольную группу просто повторяют название антитела и связанного с ним цитотоксического лекарственного средства. Например, huCD123-6Gv4.7-C442-D5 представляет собой конъюгат соединения D5 и huCD123-6Gv4.7 через тиольную группу C442, а huMov19-C442-D5 представляет собой конъюгат соединения D5 и антитела huMov19 через тиольную группу C442. В некоторых вариантах реализации изобретения соединениям, таким как D1, требуется дополнительный линкер (например, линкер сульфо-SPDB или sSPDB), подлежащий конъюгации с антителом, например, с аминогруппами боковой цепи Lys. Ниже приведена структура Lys-связанного конъюгата huCD123-6Gv4.7-сульфо-SPDB-D1 (или huCD123-6Gv4.7-сульфо-SPDB-D1).

Следует отметить, что некоторые антитела CD123 имеют «S2» и/или «S3» в названии таких антител или их иммуноконъюгатов, которые не следует путать с обозначениями «s2» или «s3» в химических формулах, которые представляют собой места присоединения или образования ковалентной связи.
КОНЪЮГАТЫ И СОЕДИНЕНИЯ ПО ДАННОМУ ИЗОБРЕТЕНИЮ
В первом аспекте данного изобретения предложены конъюгаты клеточносвязывающего агента с цитотоксическим агентом, в которых клеточносвязывающий агент (CBA) ковалентно связан с цитотоксическим агентом через тиольную (-SH) группу, расположенную в CBA. В некоторых вариантах реализации изобретения свободная тиольная группа находится на сконструированном остатке Cys в области CH3 тяжелой цепи антитела, в положении 442 этой тяжелой цепи по системе нумерации EU/OU (или сокращенно С442).
Таким образом, в одном варианте реализации изобретения конъюгат антитела с цитотоксическим агентом по данному изобретению содержит антитело, содержащее остаток цистеина (например, в положении 442 тяжелой цепи по системе нумерации EU/OU), и цитотоксический агент, при этом антитело ковалентно связано с цитотоксическим агентом через остаток цистеина (например, C442). Данный конъюгат представлен следующей формулой:
 (I),
(I),
где:
Ab представляет собой антитело, содержащее остаток цистеина в положении 442 (нумерация EU/OU) тяжелой цепи;
S442 представляет тиольную группу из остатка цистеина в положении 442 тяжелой цепи антитела, которая ковалентно связана с группой JCB’;
JCB’ представляет собой связывающий фрагмент, соединяющий остаток цистеина с группой L;
L представляет собой линкер, соединяющий цитотоксический агент и фрагмент JCB’;
D представляет собой цитотоксический агент, ковалентно связанный с группой L; и
w равен 1 или 2.
В одном варианте реализации изобретения остаток цистеина в положении 442 рекомбинантно вводят в указанное Ab.
Во втором аспекте данного изобретения предложено соединение цитотоксического агента с линкером, которое способно взаимодействовать с антителами по данному изобретению, содержащими свободный остаток цистеина, с образованием конъюгатов по данному изобретению.
В одном варианте реализации изобретения соединение цитотоксического агента с линкером по данному изобретению представлено следующей структурной формулой:
D-L-JCB (II),
где:
JCB представляет собой связывающую группу, способную образовывать ковалентную связь с описанным в данном документе антителом;
L представляет собой линкер, соединяющий цитотоксический агент, представленный D и группой JCB; и
D представляет собой цитотоксический агент, ковалентно связанный с группой L.
В одном варианте реализации изобретения JCB представляет собой тиол-реакционноспособную группу.
Ниже описаны некоторые варианты изобретения и конкретные варианты реализации изобретения для первого и второго аспектов данного изобретения.
В 1ом варианте реализации, для конъюгатов формулы (I) в первом аспекте данного изобретения, JCB’ представляет собой  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ,
,
где s1 представляет собой место ковалентной связи с остатком цистеина антитела, а s2 представляет собой место ковалентной связи с группой L; и Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (I). В конкретном варианте реализации изобретения Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или C1-3алкил. В другом конкретном варианте реализации изобретения все Ra, Rb, Rc и Re представляют собой H.
Кроме того, в 1ом варианте реализации, для соединений формулы (II) во втором аспекте изобретения, JCB представляет собой  , X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,
, X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,  ,
,  ,
,  ,
,  ,
,  ,
, 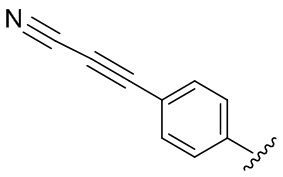 ,
,  или
или  ; Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (II).
; Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (II).
Во 2ом варианте реализации, для конъюгатов формулы (I) в первом аспекте данного изобретения, JCB’ представляет собой  ,
,  ,
,  ,
,  ,
,  или
или  , где s1 представляет собой место ковалентной связи с остатком цистеина антитела, а s2 представляет собой место ковалентной связи с группой L; и Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (I) в 1ом варианте реализации изобретения. В конкретном варианте реализации изобретения Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или C1-3алкил. В другом конкретном варианте реализации изобретения все Ra, Rb, Rc и Re представляют собой H.
, где s1 представляет собой место ковалентной связи с остатком цистеина антитела, а s2 представляет собой место ковалентной связи с группой L; и Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (I) в 1ом варианте реализации изобретения. В конкретном варианте реализации изобретения Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или C1-3алкил. В другом конкретном варианте реализации изобретения все Ra, Rb, Rc и Re представляют собой H.
Кроме того, во 2ом варианте реализации, для соединений формулы (II) по второму аспекту изобретения, JCB представляет собой  , X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,
, X’-CRbRc-C(=O)-, X’-CRbRc-C(=O)-NRe-,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ; Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (II) в 1ом варианте реализации изобретения.
; Ra, Rb, Rc и Re, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и остальные переменные являются такими, как описано выше для формулы (II) в 1ом варианте реализации изобретения.
В 3ем варианте реализации, для конъюгатов формулы (I) в первом аспекте данного изобретения, JCB’ представляет собой  ; и остальные переменные являются такими, как описано выше для формулы (I).
; и остальные переменные являются такими, как описано выше для формулы (I).
Кроме того, в 3ем варианте реализации, для соединений формулы (II) во втором аспекте изобретения, JCB’ представляет собой  ; и остальные переменные являются такими, как описано выше для формулы (II).
; и остальные переменные являются такими, как описано выше для формулы (II).
В 4ом варианте реализации, для конъюгатов формулы (I) первого аспекта изобретения и соединений формулы (II) второго аспекта данного изобретения, –L- представлен следующей структурной формулой:
 (L1),
(L1),
где:
s3 представляет собой место ковалентной связи с группой JCB’, а s4 представляет собой место ковалентной связи с группой D;
E представляет собой –(CR10R11)q-, циклоалкил или циклоалкилалкил;
Z отсутствует, представляет собой -SO2NR9-, -NR9SO2-, -C(=O)-NR9-, -NR9-C(=O)-, -C(=O)-O-, -O-C(=O)-, -C(=O)-NR9-(CH2CH2O)p-, -NR9-C(=O)-(CH2CH2O)p-, -(OCH2CH2)p-C(=O)NR9- или -(OCH2CH2)p-NR9-C(=O)-;
p представляет собой целое число от 1 до 24;
Q представляет собой H, заряженный заместитель или ионизируемую группу;
R9, R10, R11, R12 и R13, для каждого случая, независимо представляют собой H или необязательно замещенный алкил; и
q и r, для каждого случая, независимо представляют собой целое число от 0 до 10.
Остальные переменные в формуле (I) или формуле (II) являются такими, как описано выше в первом варианте реализации, 1ом, 2ом или 3ем варианте реализации или в более конкретных вариантах реализации изобретения, описанных в них.
В конкретном варианте реализации изобретения q и r независимо представляют собой целое число от 1 до 6, более конкретно – от 1 до 3.
В другом конкретном варианте реализации изобретения R9, R10, R11, R12 и R13, для каждого случая, независимо представляют собой H или C1-3алкил. Более конкретно все R9, R10, R11, R12 и R13 представляют собой H.
В другом конкретном варианте реализации изобретения p представляет собой целое число от 2 до 14. Более конкретно p представляет собой целое число от 2 до 8, от 2 до 6 или от 2 до 4.
В конкретном варианте реализации изобретения E представляет собой –(CR10R11)q-; и остальные переменные в формуле (L1) являются такими, как описано выше в 4ом варианте реализации изобретения.
В другом конкретном варианте реализации изобретения E представляет собой  ; и остальные переменные в формуле (L1) являются такими, как описано выше в 4ом варианте реализации изобретения.
; и остальные переменные в формуле (L1) являются такими, как описано выше в 4ом варианте реализации изобретения.
В еще одном конкретном варианте реализации изобретения Z представляет собой -C(=O)-NR9- или -NR9-C(=O)-; и остальные переменные в формуле (L1) являются такими, как описано выше в 4ом варианте реализации или в более конкретных вариантах реализации изобретения, описанных выше. Еще более конкретно R9 представляет собой H или Me. В альтернативном варианте, R9 представляет собой H.
В еще одном конкретном варианте реализации изобретения Q представляет собой i) H; ii) -SO3H, -Z’-SO3H, -OPO3H2, -Z’-OPO3H2, -PO3H2, -Z’-PO3H2, -CO2H, -Z’-CO2H, -NR14R15 или -Z’-NR14R15, или их фармацевтически приемлемую соль; или iii) -N+R14R15R16X- или -Z’-N+R14R15R16X-; Z’ представляет собой необязательно замещенный алкилен, необязательно замещенный циклоалкилен или необязательно замещенный фенилен; каждый из R14-R16 независимо представляет собой необязательно замещенный алкил; и X- представляет собой фармацевтически приемлемый анион; и остальные переменные в формуле (L1) являются такими, как описано выше в 4ом конкретном варианте реализации или в более конкретных вариантах реализации изобретения, описанных выше. В одном варианте реализации изобретения Z’ представляет собой необязательно замещенный алкилен. В еще одном варианте реализации изобретения Z’ представляет собой C1-3алкилен (например, -CH2); и каждый из R14-R16 независимо представляет собой C1-4алкил.
В еще одном конкретном варианте реализации изобретения Q представляет собой H или -SO3M, где М представляет собой фармацевтически приемлемый катион (например, H+, Na+ или K+); и остальные переменные в формуле (L1) являются такими, как описано выше в 4ом варианте реализации или в более конкретных вариантах реализации изобретения, описанных выше.
В 5ом варианте реализации, для конъюгатов формулы (I) первого аспекта данного изобретения, -JCB’-L- представлен любой из следующих структурных формул:
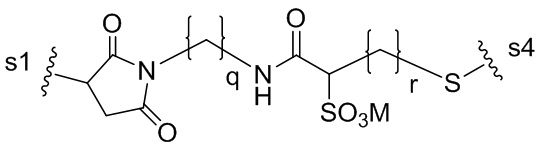 (L1a); или
(L1a); или
 (L1b),
(L1b),
где каждый из q и r независимо представляет собой целое число от 1 до 6; М представляет собой фармацевтически приемлемый катион; и остальные переменные являются такими, как описано выше для формулы (I). Более конкретно каждый из q и r независимо представляет собой целое число от 1 до 3. В другом более конкретном варианте реализации изобретения M представляет собой H+, Na+ или K+.
Кроме того, в 5ом варианте реализации, для соединений формулы (II) во втором аспекте данного изобретения, JCB-L- представлен любой из следующих структурных формул:
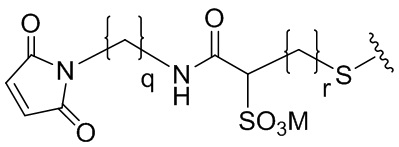 (L1a’); или
(L1a’); или
 (L1b’),
(L1b’),
где каждый из q и r независимо представляет собой целое число от 1 до 6; М представляет собой фармацевтически приемлемый катион; и остальные переменные являются такими, как описано выше для формулы (II). Более конкретно каждый из q и r независимо представляет собой целое число от 1 до 3. В другом более конкретном варианте реализации изобретения M представляет собой H+, Na+ или K+.
В 6ом варианте реализации, для конъюгатов формулы (I) в первом аспекте, –JCB’-L- представлен любой из следующих структурных формул:
 ; или
; или
 ,
,
где М представляет собой фармацевтически приемлемый катион, а остальные переменные являются такими, как описано выше для формулы (I). Более конкретно M представляет собой H+, Na+ или K+.
Кроме того, в 6ом варианте реализации, для соединений формулы (I) во втором аспекте, JCB-L- представлен любой из следующих структурных формул:
 ; или
; или
 ,
,
где М представляет собой фармацевтически приемлемый катион, а остальные переменные являются такими, как описано выше для формулы (II). Более конкретно M представляет собой H+, Na+ или K+.
В 7ом конкретном варианте реализации, для конъюгатов формулы (I) в первом аспекте и соединений формулы (II) во втором аспекте, -L- представлен следующей структурной формулой:
 (L2),
(L2),
где:
s3 представляет собой место ковалентной связи с группой JCB’, а s4 представляет собой место ковалентной связи с группой D;
R19-R22, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
каждый из m и n независимо представляет собой целое число от 0 до 10;
Rh представляет собой H или необязательно замещенный алкил;
P представляет собой необязательно замещенный алкилен, -(CH2-CH2-O)j-, -(O-CH2-CH2)j-, аминокислотный остаток или пептид, содержащий 2-20 аминокислотных остатков; и
j представляет собой целое число от 1 до 24;
и остальные переменные являются такими, как описано выше для формулы (I) или формулы (II), 1го, 2го или 3го варианта реализации или любых более конкретных вариантов реализации изобретения, описанных в них.
В 8ом варианте реализации, для формулы (L2), каждый из R19, R20, R21 и R22 представляет собой H или C1-3алкил; алкил; каждый из m и n независимо представляет собой целое число от 1 до 6; и остальные переменные являются такими, как описано выше в 7ом варианте реализации изобретения. Более конкретно все R19, R20, R21 и R22 представляют собой H. Еще более конкретно все R19, R20, R21 и R22 представляют собой H; и каждый из m и n независимо представляет собой целое число от 1 до 3.
В 9ом конкретном варианте реализации, для формулы (L2), P представляет собой аминокислотный остаток или пептид, содержащий от 2 до 10 аминокислотных остатков; и остальные переменные являются такими, как описано выше в 7ом или 8ом варианте реализации изобретения. Более конкретно P представляет собой пептид, содержащий от 2 до 5 аминокислотных остатков.
В одном варианте реализации изобретения каждый аминокислотный остаток представляет собой остаток аминокислоты, независимо выбранной из: природной аминокислоты, синтетической аминокислоты, аналога аминокислоты и миметика аминокислоты, который действует таким же образом, как природные аминокислоты.
В другом варианте реализации изобретения каждый аминокислотный остаток представляет собой остаток аминокислоты, независимо выбранной из группы, состоящей из: гистидина, аланина, изолейцина, аргинина, лейцина, аспарагина, лизина, аспарагиновой кислоты, метионина, цистеина, фенилаланина, глутаминовой кислоты, треонина, глутамина, триптофана, глицина, валина, пролина, серина, тирозина, N-метил-гистидина, N-метил-аланина, N-метил-изолейцина, N-метил-аргинина, N-метил-лейцина, N-метил-аспарагина, N-метил-лизина, N-метил-аспарагиновой кислоты, N-метил-метионина, N-метил-цистеина, N-метил-фенилаланина, N-метил-глутаминовой кислоты, N-метил-треонина, N-метил-глутамина, N-метил-триптофана, N-метил-глицина, N-метил-валина, N-метил-пролина, N-метил-серина, N-метил-тирозина, гидроксипролина, γ-карбоксиглутамата, селеноцистеина, O-фосфосерина, гомосерина, норлейцина, метионинсульфоксида, метилметионинсульфония, цитруллина, орнитина, цистеинсульфоновой кислоты, цистеинсульфиновой кислоты, 3-аминоаланина, 3-диметиламиноаланина, 2-амино-4-(диметиламино)бутановой кислоты, 2,4-диаминобутановой кислоты, 2-амино-6-(диметиламино)капроновой кислоты, 2-амино-5-(диметиламино)валериановой кислоты и β-аланина, каждый независимо в виде L- или D-изомера. Более конкретно каждый аминокислотный остаток представляет собой остаток независимо выбранного глицина или аланина.
В другом варианте реализации изобретения P представляет собой пептид, расщепляемый протеазой. Более конкретно P представляет собой пептид, расщепляемый протеазой, экспрессируемой в опухолевой ткани. В альтернативном варианте, P представляет собой пептид, расщепляемый лизосомальной протеазой.
В еще одном варианте реализации изобретения Р выбран из группы, состоящей из: Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID №: 14), β-Ala-Leu-Ala-Leu (SEQ ID №: 15), Gly-Phe-Leu-Gly (SEQ ID №: 16), Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala и D-Ala-D-Ala, Gly-Gly-Gly, Ala-Ala-Ala, D-Ala-Ala-Ala, Ala-D-Ala-Ala, Ala-Ala-D-Ala, Ala-Val-Cit, Ala-Val-Ala и β-Ala-Gly-Gly-Gly. Более конкретно P представляет собой Gly-Gly-Gly, Ala-Ala-Ala, D-Ala-Ala-Ala, Ala-D-Ala-Ala, Ala-Val-Ala или β-Ala-Gly-Gly-Gly.
В 10ом варианте реализации, для конъюгатов формулы (I) в первом аспекте, -JCB’–L- представлен следующей структурной формулой:
 ,
,
и остальные переменные являются такими, как описано выше для формулы (I).
Кроме того, в 10ом варианте реализации, для соединений формулы (II) во втором аспекте, JCB–L- представлен следующей структурной формулой:
 ,
,
и остальные переменные являются такими, как описано выше для формулы (II).
В 11ом варианте реализации, для конъюгатов формулы (I) и соединений формулы (II), -L- представлен следующей структурной формулой:
 (L3),`
(L3),`
где:
s3 представляет собой место ковалентной связи с JCB’, а s4 представляет собой место ковалентной связи с D;
R23 и R24, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
m’ представляет собой целое число от 0 до 10; и
Rh’ представляет собой H или необязательно замещенный алкил;
и остальные переменные являются такими, как описано выше для формулы (I) или формулы (II), 1го, 2го или 3го варианта реализации или любых конкретных вариантов реализации изобретения, описанных в них.
В конкретном варианте реализации изобретения m’ представляет собой целое число от 1 до 6. Еще более конкретно m’ представляет собой целое число от 1 до 3.
В другом конкретном варианте реализации изобретения R23 и R24, для каждого случая, независимо представляют собой H или C1-3алкил. Еще более конкретно оба R23 и R24 представляют собой H.
В другом конкретном варианте реализации изобретения Rh’ представляет собой H или C1-3алкил. Более конкретно Rh’ представляет собой H.
В другом конкретном варианте реализации изобретения оба R23 и R24 представляют собой H; m’ представляет собой целое число от 1 до 6. Еще более конкретно m’ представляет собой целое число от 1 до 3.
В 12ом варианте реализации, для конъюгатов формулы (I) в первом аспекте, -JCB’-L- представлен следующей структурной формулой:
 ;
;
и остальные переменные являются такими, как описано выше для формулы (I).
Кроме того, в 12ом варианте реализации, для соединений формулы (II) во втором аспекте, JCB-L- представлен следующей структурной формулой:
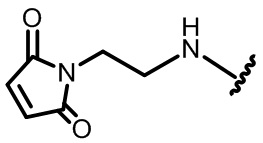 ;
;
и остальные переменные являются такими, как описано выше для формулы (II).
В другом варианте реализации изобретения, для конъюгатов формулы (I) или соединений формулы (II), цитотоксический агент, представленный D, представляет собой майтанзиноид; и оставшиеся переменные являются такими, как описано для формулы (I) или (II), любого из описанных выше 1го – 12го вариантов реализации или любых более конкретных вариантов реализации изобретения, описанных в них.
В другом варианте реализации изобретения, для конъюгатов формулы (I) или соединений формулы (II), цитотоксический агент, представленный D, представляет собой бензодиазепин; и оставшиеся переменные являются такими, как описано для формулы (I) или (II), любого из описанных выше 1го – 12го вариантов реализации или любых более конкретных вариантов реализации изобретения, описанных них.
В 13ом варианте реализации, для конъюгатов формулы (I) или соединений формулы (II), D представляет собой майтанзиноид, представленный следующей структурной формулой:
 (M1);
(M1);
где:
RM, RM’ и RM”, для каждого случая, независимо представляют собой H или необязательно замещенный алкил;
R1’, R2’, R3’ и R4’, для каждого случая, независимо представляют собой Н, необязательно замещенный алкил, необязательно замещенный алкенил, необязательно замещенный циклоалкил, необязательно замещенный гетероциклил, необязательно замещенный арил или необязательно замещенный гетероарил; и
i представляет собой целое число от 0 до 15;
и остальные переменные являются такими, как описано выше для формулы (I) или (II), любого из описанных выше 1го -10го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них.
Более конкретно D представлен следующей структурной формулой:
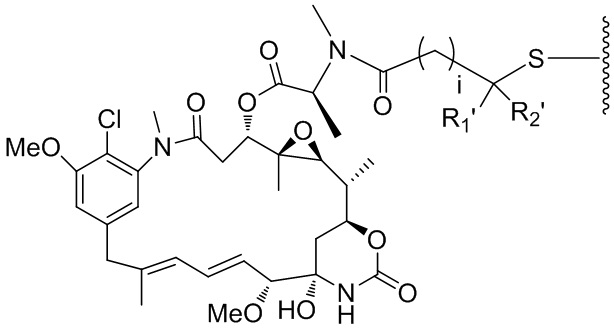 (M2),
(M2),
где i равен 1 или 2; и каждый из R1’ и R2’ независимо представляет собой H или C1-3алкил; и остальные переменные являются такими, как описано в 13ом варианте реализации изобретения.
В 14ом конкретном варианте реализации, для конъюгатов формулы (I) или соединений формулы (II), D представляет собой майтанзиноид, представленный следующей структурной формулой:
 (M3); или
(M3); или  (M4),
(M4),
и остальные переменные являются такими, как описано выше для формулы (I) или (II), любого из описанных выше 1го -10го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них.
В 15ом варианте реализации, для конъюгатов формулы (I) или соединений формулы (II), D представлен следующей структурной формулой:


или его фармацевтически приемлемая соль, где:
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X выбран из -H или аминозащитной группы (предпочтительно Х представляет собой -H); и Y выбран из -OR, -OCOR’, -SR, -NR’R”, -SO3M, -SO2M или -OSO3M, где М представляет собой -H или катион (такой как Na+ или K+);
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X выбран из -H или аминозащитной группы (предпочтительно Х представляет собой -H); и Y выбран из -OR, -OCOR’, -SR, -NR’R”, -SO3M, -SO2M или -OSO3M, где М представляет собой -H или катион (такой как Na+ или K+);
R представляет собой -H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода или ПЭГ-группу -(CH2CH2O)n-Rc, где n представляет собой целое число от 1 до 24 и Rc представляет собой линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода;
каждый из R’ и R” независимо выбран из -H, -OH, -OR, -NRRg’, -COR, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, выбранных из O, S, N и P, ПЭГ-группы -(CH2CH2O)n-Rc, и Rg’ представляет собой -H, необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или ПЭГ-группу -(CH2CH2O)n-Rc;
X’ выбран из группы, состоящей из -H, -OH, замещенного или незамещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, фенила и аминозащитной группы;
Y’ выбран из группы, состоящей из -H, оксогруппы, замещенного или незамещенного линейного, разветвленного или циклического алкил, алкенила или алкинила, содержащего от 1 до 10 атомов углерода;
A и A’ выбраны из -O- и -S-;
W’ отсутствует или выбран из -O-, -N(Re)-, -N(Re)-C(=O)-, -N(C(=O)Re)-, -S- или -CH2-S-, -CH2NRe-;
Rx отсутствует или выбран из линейного, разветвленного или циклического алкила, содержащего от 1 до 10 атомов углерода;
Re представляет собой -H, линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или -(CH2-CH2-O)n-Rk, где Rk представляет собой -H, линейный, разветвленный или циклический алкил, содержащий 1 до 6 атомов углерода, необязательно содержащий вторичную аминогруппу (например, -NHR101) или третичную аминогруппу (-NR101R102), или 5- или 6-членный азотсодержащий гетероцикл, такой как пиперидин или морфолин, где каждый из R101 и R102 независимо представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
G выбран из -CH- или -N-; и
R6 представляет собой -H, -R, -OR, -SR, -NR’R’’, -NO2 или галоген;
и остальные переменные являются такими, как описано выше для формулы (I) или (II), любого из 1го – 10го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них.
В конкретном варианте реализации изобретения D представлен приведенной выше формулой (IBD1), или его фармацевтически приемлемая соль.
В другом конкретном варианте реализации изобретения, для формул (IBD1)-(IBD6):
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -OH или -SO3M;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -OH или -SO3M;
M представляет собой -H или фармацевтически приемлемый катион (например, Na+);
оба X’ и Y’ представляют собой -H;
оба A и A’ представляют собой -O-;
R6 представляет собой -OMe; и
Rx представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода.
В 16ом варианте реализации, для конъюгатов формулы (I) или соединений формулы (II), D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -OH или -SO3M; и остальные переменные являются такими, как описано выше для формулы (I) или (II), любого из 1го – 10го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -OH или -SO3M; и остальные переменные являются такими, как описано выше для формулы (I) или (II), любого из 1го – 10го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них.
В конкретном варианте реализации изобретения, для приведенных выше формул (IBD7)-(IBD10), а также (IBD7a) и (IBD9a), Y представляет собой –SO3M и M представляет собой H+, Na+ или K+.
В 17ом варианте реализации, для конъюгатов формулы (I) или соединений формулы (II), D представлен следующей структурной формулой:

или его фармацевтически приемлемая соль, где:
один из L’, L’’ и L’’’ представлен следующей формулой:
-Z1-P1-Z2-Rx1-C(=O)- (A’) или
-N(Re)-Rx1-C(=O)- (D’);
и каждый из двух других независимо выбран из -H, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, галогена, гуанидиния [-NH(C=NH)NH2], -OR, -NR’R’’, -NO2, -NR’COR’’, -SR, -SOR’, -SO2R’, -SO3H, -OSO3H, -SO2NR’R’’, циано, азидо, -COR’, -OCOR’ и -OCONR’R’’;
один из Z1 и Z2 представляет собой -C(=O)-, а другой представляет собой -NR5-;
P1 представляет собой аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков;
Rx1 представляет собой необязательно замещенный линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
Re представляет собой -H, линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, или -(CH2-CH2-O)n-Rk, где Rk представляет собой -H, линейный, разветвленный или циклический алкил, содержащий 1 до 6 атомов углерода, необязательно содержащий вторичную аминогруппу (например, -NHR101) или третичную аминогруппу (-NR101R102), или 5- или 6-членный азотсодержащий гетероцикл, такой как пиперидин или морфолин, где каждый из R101 и R102 независимо представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода;
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, и если она представляет собой одинарную связь, то X1 представляет собой –H или аминозащитный фрагмент; и Y1 представляет собой уходящую группу, выбранную из -OR, -OCOR’, -OCOOR’, -OCONR’R’’, -NR’R’’, -NR’COR’’, -NR’NR’R’’, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла (например, пиперидина, тетрагидропиррола, пиразола, морфолина и т.д., присоединенного через атом азота), гуанидиния, представленного -NR’(C=NH)NR’R’’, аминокислоты или пептида, представленного -NRCOP’, -SR, -SOR’, галогена, циано, азидо, -OSO3H (или его соли), сульфита (-SO3H или -SO2H, или их соли), метабисульфита (H2S2O5 или его соли), моно-, ди-, три- и тетратиофосфата (PO3SH3, PO2S2H2, POS3H2, PS4H2 или их соли), сложного тиофосфатного эфира (RiO)2PS(ORi), RiS-, RiSO, RiSO2, RiSO3, тиосульфата (HS2O3 или его соли), дитионита (HS2O4 или его соли) фосфородитиоата (P(=S)(ORk’)(S)(OH) или его соли), гидроксамовой кислоты (Rk’C(=O)NOH или ее соли) и формальдегидсульфоксилата (HOCH2SO2- или его соли) или их смеси, где Ri представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H и -PO3H; Ri также может быть необязательно замещен заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; Rk’ представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H или линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода, и если она представляет собой одинарную связь, то X1 представляет собой –H или аминозащитный фрагмент; и Y1 представляет собой уходящую группу, выбранную из -OR, -OCOR’, -OCOOR’, -OCONR’R’’, -NR’R’’, -NR’COR’’, -NR’NR’R’’, необязательно замещенного 5- или 6-членного азотсодержащего гетероцикла (например, пиперидина, тетрагидропиррола, пиразола, морфолина и т.д., присоединенного через атом азота), гуанидиния, представленного -NR’(C=NH)NR’R’’, аминокислоты или пептида, представленного -NRCOP’, -SR, -SOR’, галогена, циано, азидо, -OSO3H (или его соли), сульфита (-SO3H или -SO2H, или их соли), метабисульфита (H2S2O5 или его соли), моно-, ди-, три- и тетратиофосфата (PO3SH3, PO2S2H2, POS3H2, PS4H2 или их соли), сложного тиофосфатного эфира (RiO)2PS(ORi), RiS-, RiSO, RiSO2, RiSO3, тиосульфата (HS2O3 или его соли), дитионита (HS2O4 или его соли) фосфородитиоата (P(=S)(ORk’)(S)(OH) или его соли), гидроксамовой кислоты (Rk’C(=O)NOH или ее соли) и формальдегидсульфоксилата (HOCH2SO2- или его соли) или их смеси, где Ri представляет собой линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода, и замещен по меньшей мере одним заместителем, выбранным из -N(Rj)2, -CO2H, -SO3H и -PO3H; Ri также может быть необязательно замещен заместителем для алкила, описанным в данном документе; Rj представляет собой линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода; Rk’ представляет собой линейный, разветвленный или циклический алкил, алкенил или алкинил, содержащий от 1 до 10 атомов углерода, арил, гетероциклил или гетероарил;
P’ представляет собой аминокислотный остаток или пептид, содержащий от 2 до 20 аминокислотных остатков,
R, для каждого случая, независимо выбран из группы, состоящей из -H, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, или необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из O, S, N и P;
каждый из R’ и R’’ независимо выбран из -H, -OH, -OR, -NHR, -NR2, -COR, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc и необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из O, S, N и P;
Rc представляет собой -H или необязательно замещенный линейный или разветвленный алкил, содержащий от 1 до 4 атомов углерода;
n представляет собой целое число от 1 до 24;
X1’ выбран из -Н, аминозащитной группы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, необязательно замещенного арила, содержащего от 6 до 18 атомов углерода, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, и необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов, независимо выбранных из О, S, N и Р;
Y1’ выбран из -H, оксогруппы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, необязательно замещенного 6-18-членного арила, необязательно замещенного 5-18-членного гетероарильного кольца, содержащего один или более гетероатомов, независимо выбранных из азота, кислорода и серы, необязательно замещенного 3-18-членного гетероциклического кольца, содержащего от 1 до 6 гетероатомов;
каждый из R1, R2, R3, R4, R1’, R2’, R3’ и R4’ независимо выбран из группы, состоящей из -Н, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, полиэтиленгликолевого звена -(CH2CH2O)n-Rc, галогена, гуанидиния [-NH(C=NH)NH2], -OR, -NR’R’’, -NO2, -NCO, -NR’COR’’, -SR, -SOR’, -SO2R’, -SO3-H, -OSO3H, -SO2NR’R’’, циано, азидо, -COR’, -OCOR’ и -OCONR’R’’;
R6 представляет собой -H, -R, -OR, -SR, -NR’R’’, -NO2 или галоген;
G представляет собой -CH- или –N-;
A и A’ являются одинаковыми или различными и независимо выбраны из -O-, оксо (-C(=O)-), -CRR’O-, -CRR’-, -S-, -CRR’S-, -NR5 и -CRR’N(R5)-; и
R5 для каждого случая независимо представляет собой -H или необязательно замещенный линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода;
и остальные переменные являются такими, как описано для формулы (I) или (II), 1го, 2го, 3го, 11го или 12го конкретного варианта реализации или любых более конкретных вариантов реализации изобретения, описанных в них.
В более конкретном варианте реализации изобретения D представлен формулой (IBD11)
В другом более конкретном варианте реализации изобретения, для формул (IBD11)-(IBD16), один из L’, L” и L’” представлен формулой (A’) или (D’), а другие представляют собой -H, линейный или разветвленный алкил, содержащий от 1 до 6 атомов углерода, галоген, -OH, (C1-C6)алкокси или -NO2.
В другом более конкретном варианте реализации изобретения, для формул (IBD11)-(IBD16), L’ представлен формулой (A’); и оба L” и L”’ представляют собой -H.
В другом более конкретном варианте реализации изобретения, для формул (IBD11)-(IBD16), L’ представлен формулой (D’); и оба L” и L”’ представляют собой –H.
В другом более конкретном варианте реализации изобретения, для формул (IBD11)-(IBD16), Rx1 представляет собой линейный, разветвленный или циклический алкил, содержащий от 1 до 6 атомов углерода, необязательно замещенный галогеном, -OH, -SO3H, (C1-C3)алкилом, (C1-C3)алкокси, гало(C1-C3)алкилом или заряженным заместителем, или ионизируемой группой Q.
В 18ом конкретном варианте реализации, для формул (IBD11)-(IBD16), L’ представлен следующей формулой:
-NR5-P1-C(=O)-(CRaRb)s-C(=O)- (B1’);
-NR5-P1-C(=O)-Cy-(CRaRb)s1’-C(=O)- (B2’);
-C(=O)-P1-NR5-(CRaRb)s-C(=O)- (C1’) или
-C(=O)-P1-NR5-Cy-(CRaRb)s1’-C(=O)- (C2’)
где:
каждый из Ra и Rb, для каждого случая, независимо представляет собой -H, (C1-C3) алкил или заряженный заместитель, или ионизируемую группу Q;
s представляет собой целое число от 1 до 6;
s1’ представляет собой 0 или целое число от 1 до 6; и
Cy представляет собой циклический алкил, содержащий 5 или 6 кольцевых атомов углерода, необязательно замещенный галогеном, -OH, (C1-C3)алкилом, (C1-C3)алкокси или гало(C1-C3)алкилом;
и остальные переменные являются такими, как описано выше в 17ом конкретном варианте реализации или в более конкретных вариантах реализации изобретения, описанных в нем.
В более конкретном варианте реализации изобретения оба Ra и Rb представляют собой H; Cy в формулах (B2’) и (C2’) представляет собой циклогексан; и R5 представляет собой H или Me. Еще более конкретно s1’ равен 0 или 1.
В 19ом варианте реализации, для формул (IBD11)-(IBD16), P1 представляет собой пептид, содержащий от 2 до 10 аминокислотных остатков; и остальные переменные являются такими, как описано в 17ом или 18ом конкретном варианте реализации изобретения.
В конкретном варианте реализации изобретения P1 представляет собой пептид, содержащий от 2 до 5 аминокислотных остатков.
В другом конкретном варианте реализации изобретения P1 представляет собой Gly-Gly-Gly, Ala-Val, Val-Ala, Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID №: 14), β-Ala-Leu-Ala-Leu (SEQ ID №: 15), Gly-Phe-Leu-Gly (SEQ ID №: 16), Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala, D-Ala-D-Ala, Ala-Met или Met-Ala. Еще более конкретно P представляет собой Gly-Gly-Gly, Ala-Val, Ala-Ala, Ala-D-Ala, D-Ala-Ala или D-Ala-D-Ala.
В 20ом варианте реализации, для формул (IBD11)-(IBD16), двойная линия  между N и C представляет собой двойную связь; и остальные переменные являются такими, как описано выше в 17ом, 18ом или 19ом варианте реализации изобретения.
между N и C представляет собой двойную связь; и остальные переменные являются такими, как описано выше в 17ом, 18ом или 19ом варианте реализации изобретения.
В 21ом варианте реализации, для формул (IBD11)-(IBD16), двойная линия  между N и C представляет собой одинарную связь, X1 представляет собой –H или аминозащитную группу; и Y1 представляет собой -OR, -OCOR’, -SR, -NR’R”, необязательно замещенный 5- или 6-членный азотсодержащий гетероцикл, -SO3M, -SO2M или -OSO3M, где M представляет собой H+ или фармацевтически приемлемый катион; и остальные переменные являются такими, как описано выше в 17ом, 18ом или 19ом варианте реализации изобретения. В частности, Y1 выбран из -SO3M, -OH, -OMe, -OEt или -NHOH. Более конкретно Y1 представляет собой -SO3M или -OH, где M представляет собой H+, Na+ или K+.
между N и C представляет собой одинарную связь, X1 представляет собой –H или аминозащитную группу; и Y1 представляет собой -OR, -OCOR’, -SR, -NR’R”, необязательно замещенный 5- или 6-членный азотсодержащий гетероцикл, -SO3M, -SO2M или -OSO3M, где M представляет собой H+ или фармацевтически приемлемый катион; и остальные переменные являются такими, как описано выше в 17ом, 18ом или 19ом варианте реализации изобретения. В частности, Y1 выбран из -SO3M, -OH, -OMe, -OEt или -NHOH. Более конкретно Y1 представляет собой -SO3M или -OH, где M представляет собой H+, Na+ или K+.
В некоторых вариантах реализации изобретения, для формул (IBD11)-(IBD16), X1’ выбран из группы, состоящей из -H, -OH, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода, и фенила; и остальные переменные являются такими, как описано выше в 17ом, 18ом, 19ом, 20ом или 21ом варианте реализации изобретения. Более конкретно X1’ представляет собой -H, -OH, (C1-C3)алкил, гало(C1-C3)алкил или фенил. В другом более конкретном варианте реализации изобретения X1’ представляет собой -H, -OH или -Me. Еще более конкретно X1’ представляет собой -H.
В некоторых вариантах реализации изобретения, для формул (IBD11)-(IBD16), Y1’ выбран из группы, состоящей из -H, оксогруппы, необязательно замещенного линейного, разветвленного или циклического алкила, алкенила или алкинила, содержащего от 1 до 10 атомов углерода; и остальные переменные являются такими, как описано выше в 17ом, 18ом, 19ом, 20ом или 21ом варианте реализации изобретения. Более конкретно Y1’ представляет собой -H, оксогруппу, (C1-C3)алкил или гало(C1-C3)алкил. В другом более конкретном варианте реализации изобретения Y1’ представляет собой -H или оксо. Еще более конкретно Y1’ представляет собой –H.
В некоторых вариантах реализации изобретения, для формул (IBD11)-(IBD16), A и A’ являются одинаковыми или различными и представляют собой -O-, -S-, -NR5- или оксо -(C=O)-; и остальные переменные являются такими, как описано выше в 17ом, 18ом, 19ом, 20ом или 21ом варианте реализации изобретения. Более конкретно A и A’ являются одинаковыми или различными и представляют собой -O- или -S-. Еще более конкретно A и A’ представляют собой -O-.
В некоторых вариантах реализации изобретения, для формул (IBD11)-(IBD16), R6 представляет собой -OMe; и остальные переменные являются такими, как описано выше в 17ом, 18ом, 19ом, 20ом или 21ом варианте реализации изобретения.
В некоторых вариантах реализации изобретения, для формул (IBD11)-(IBD16), каждый из R1, R2, R3, R4, R1’, R2’, R3’ и R4’ независимо представляет собой -H, галоген, -NO2, -OH, (C1-C3)алкил, гало(C1-C3)алкил или (C1-C3)алкокси; и остальные переменные являются такими, как описано. Более конкретно все R1, R2, R3, R4, R1’, R2’, R3’ и R4’ представляют собой -H.
В некоторых вариантах реализации изобретения, для формул (IBD11)-(IBD16), каждый из R, R’, R” и R5 независимо представляет собой -H или (C1-C3)алкил; и остальные переменные являются такими, как описано выше в 17ом, 18ом, 19ом, 20ом или 21ом варианте реализации изобретения.
В 22ом варианте реализации изобретения, для формул (IBD11)-(IBD16):
двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H; и если она представляет собой одинарную связь, то X1 представляет собой -H и Y1 представляет собой -OH или -SO3M;
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X1 отсутствует и Y1 представляет собой -H; и если она представляет собой одинарную связь, то X1 представляет собой -H и Y1 представляет собой -OH или -SO3M;
все R1, R2, R3, R4, R1’, R2’, R3’ и R4’ представляют собой -H;
R6 представляет собой -OMe;
оба X1’ и Y1’ представляют собой -H;
A и A’ представляют собой -O-; и
M представляет собой H+, Na+ или K+; и остальные переменные являются такими, как описано выше в 17ом, 18ом, 19ом, 20ом или 21ом конкретном варианте реализации изобретения. Более конкретно каждый из R, R’, R” и R5 независимо представляет собой –H или (C1-C3)алкил. Еще более конкретно все R, R’, R” и R5 представляют собой -H.
В 23ем варианте реализации, для конъюгатов формулы (I) или соединений формулы (II), D представлен следующей структурной формулой:
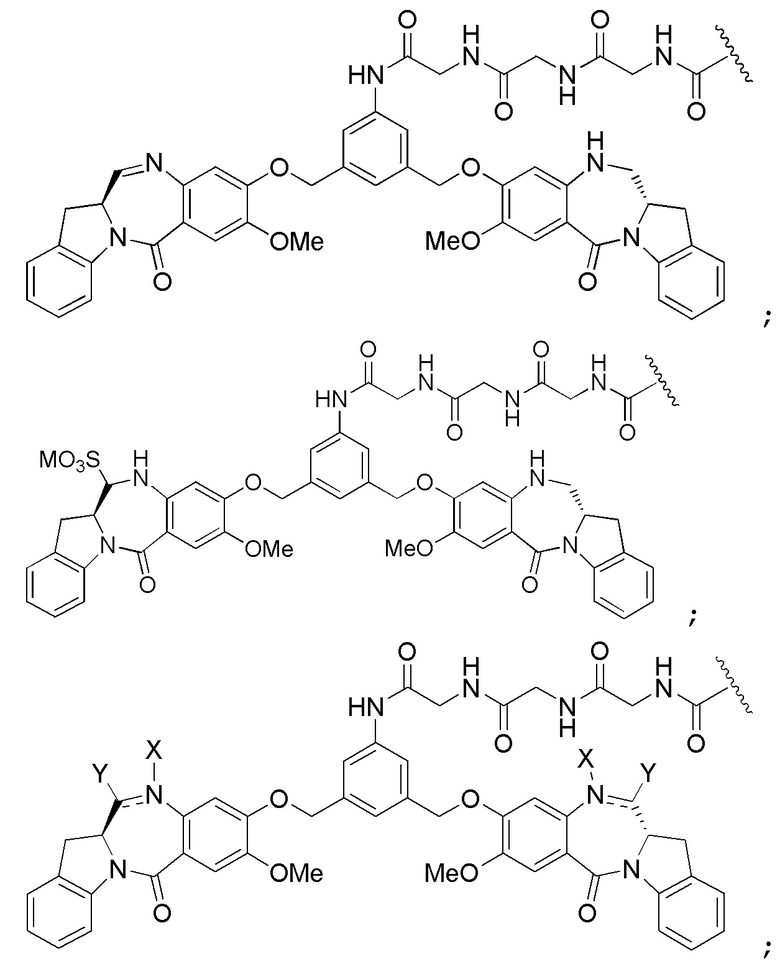
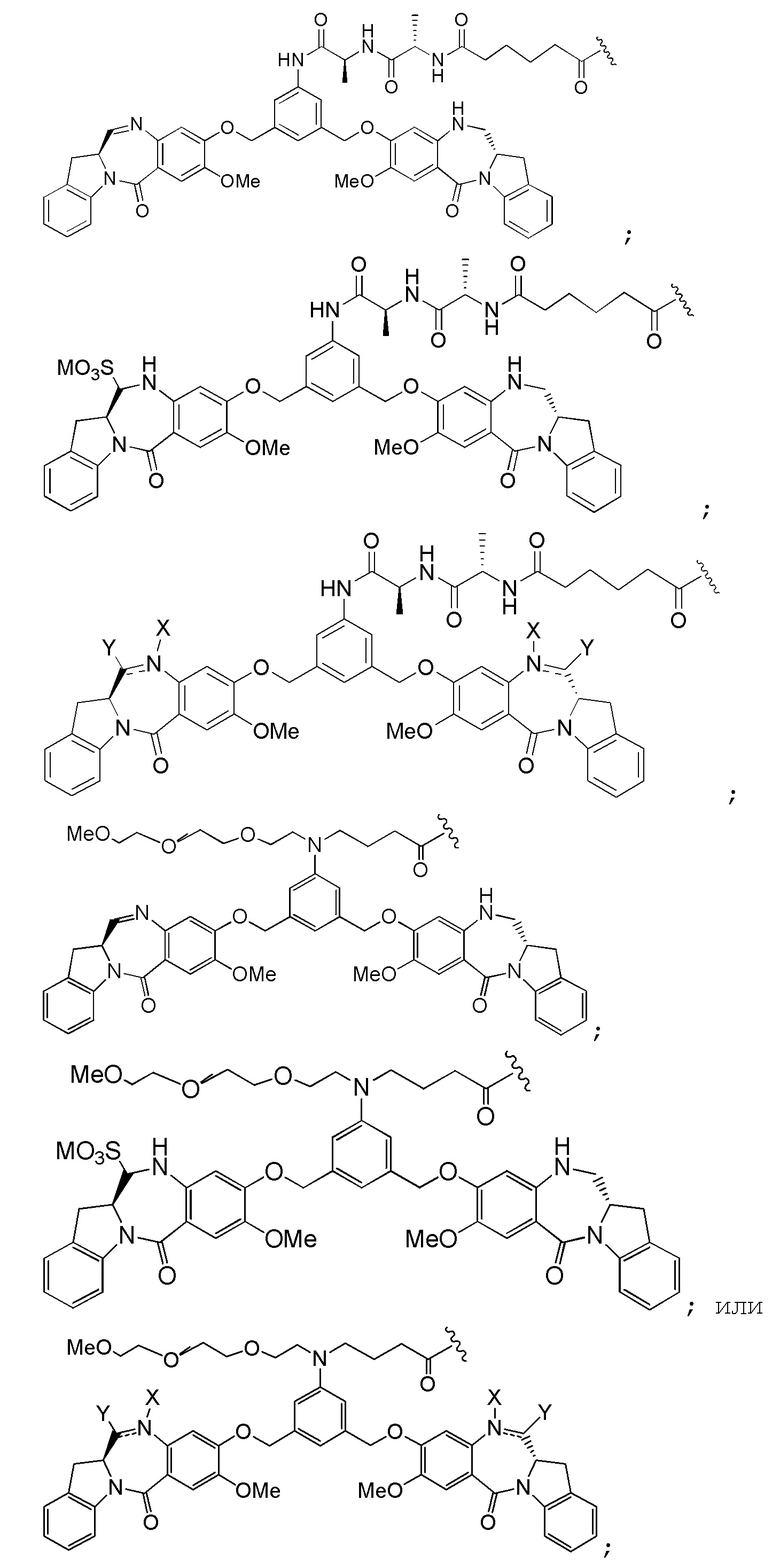
где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; M представляет собой H+ или фармацевтически приемлемый катион; и остальные переменные являются такими, как описано выше в 17ом варианте реализации изобретения.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; M представляет собой H+ или фармацевтически приемлемый катион; и остальные переменные являются такими, как описано выше в 17ом варианте реализации изобретения.
В 24ом варианте реализации, для конъюгатов формулы (I), конъюгат представлен следующей структурной формулой:




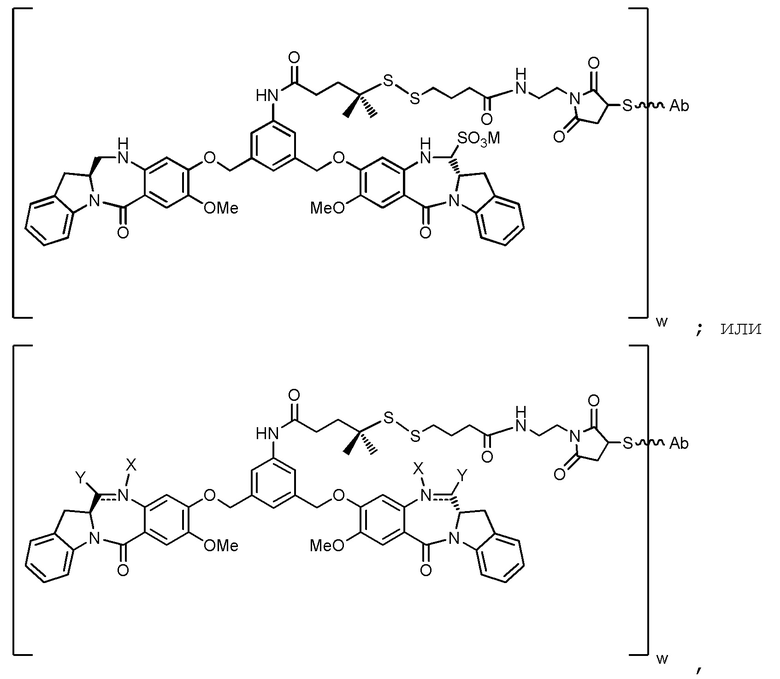
или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион. Более конкретно M представляет собой H+, Na+ или K+.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион. Более конкретно M представляет собой H+, Na+ или K+.
Кроме того, в 24ом варианте реализации, для соединений формулы (II), соединение представлено следующей структурной формулой:


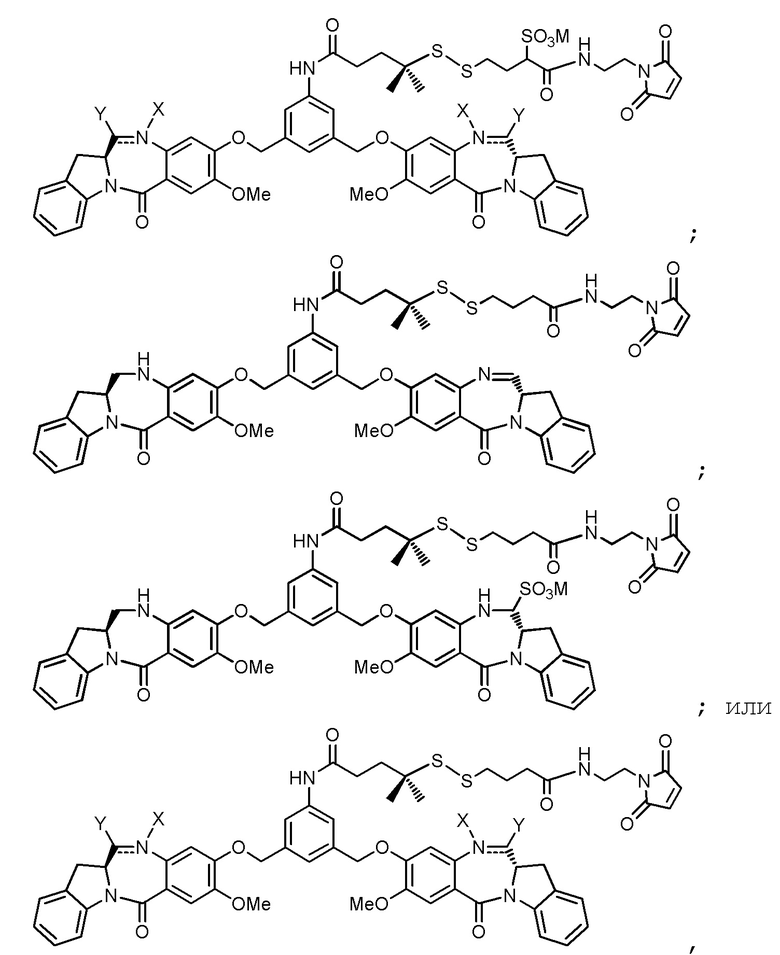
или его фармацевтически приемлемая соль, где двойная линия  между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
между N и C представляет собой одинарную связь или двойную связь, при условии, что если она представляет собой двойную связь, то X отсутствует и Y представляет собой -H, и если она представляет собой одинарную связь, то X представляет собой -H и Y представляет собой -SO3M; и M представляет собой H+ или фармацевтически приемлемый катион.
В 25ом варианте реализации, для конъюгатов, описанных в первом варианте реализации или в любом из 1го-24го вариантов реализации изобретения, w равен 2. В альтернативном варианте w равен 1.
В некоторых вариантах реализации изобретения заряженный заместитель или ионизируемая группа Q, описанная в любых приведенных выше вариантах реализации, представляет собой i) -SO3H, -Z’-SO3H, -OPO3H2, -Z’-OPO3H2, -PO3H2, -Z’-PO3H2, -CO2H, -Z’-CO2H, -NR11R12 или -Z’-NR11R12, или их фармацевтически приемлемую соль; или ii) -N+R14R15R16X- или -Z’-N+R14R15R16X-; Z’ представляет собой необязательно замещенный алкилен, необязательно замещенный циклоалкилен или необязательно замещенный фенилен; каждый из R14-R16 независимо представляет собой необязательно замещенный алкил; и X- представляет собой фармацевтически приемлемый анион. Более конкретно Q представляет собой –SO3H или его фармацевтически приемлемую соль.
В некоторых вариантах реализации изобретения антитело в конъюгатах по данному изобретению представляет собой антитело, содержащее сконструированный остаток цистеина (например, в положении 442 тяжелой цепи (цепей) по системе нумерации EU/OU). Сконструированный остаток Cys может быть расположен на одной или обеих тяжелых цепях антитела или на одной или обеих легких цепях антитела, или его антигенсвязывающей части, или их комбинации. В одном варианте реализации изобретения остаток Cys находится в положении 442 тяжелой цепи (цепей) антитела по системе нумерации EU/OU. В некоторых вариантах реализации изобретения антитело представляет собой сконструированное антитело с цистеиновыми заменами, как описано в данном документе.
В некоторых вариантах реализации изобретения антитело по данному изобретению представляет собой моноклональное антитело, химерное антитело, гуманизированное антитело, антитело с измененной поверхностью или антитело человека.
В других вариантах реализации изобретения клеточносвязывающий агент представляет собой антитело, одноцепочечное антитело, фрагмент антитела, который специфически связывается с клеткой-мишенью, моноклональное антитело, одноцепочечное моноклональное антитело, фрагмент моноклонального антитела (или «антигенсвязывающую часть»), который специфически связывается с клеткой-мишенью, химерное антитело, фрагмент химерного антитела (или «антигенсвязывающую часть»), который специфически связывается с клеткой-мишенью, доменное антитело (например, sdAb) или фрагмент доменного антитела, который специфически связывается с клеткой-мишенью.
В некоторых вариантах реализации изобретения клеточносвязывающий агент представляет собой гуманизированное антитело, гуманизированное одноцепочечное антитело или фрагмент гуманизированного антитела (или «антигенсвязывающую часть»). В конкретном варианте реализации изобретения гуманизированное антитело представляет собой huMy9-6 или другое родственное антитело, описанное в патентах США №№ 7342110 и 7557189. В другом конкретном варианте реализации изобретения гуманизированное антитело представляет собой антитело к рецептору фолиевой кислоты, описанное в патенте США № 8557966. В еще одном варианте реализации изобретения гуманизированное антитело представляет собой антитело к CD123, описанное в предварительной заявке на патент США № 62/186161, поданной 29 июня 2015 года, озаглавленной «ANTI-CD123 ANTIBODIES AND CONJUGATES AND DERIVATIVES THEREOF» («АНТИТЕЛА К CD123, А ТАКЖЕ ИХ КОНЪЮГАТЫ И ПРОИЗВОДНЫЕ»). Принципы всех этих заявок включены в данный документ в полном объеме посредством ссылки.
В некоторых вариантах реализации изобретения клеточносвязывающий агент представляет собой антитело с измененной поверхностью, одноцепочечное антитело с измененной поверхностью, фрагмент антитела с измененной поверхностью (или «антигенсвязывающую часть») или биспецифическое антитело.
В еще одном аспекте данного изобретения предложено рекомбинантное антитело, содержащее зрелую процессированную последовательность тяжелой цепи, легкой цепи или их антигенсвязывающей части, полученную из тяжелой цепи (HC), легкой цепи (LC) любого рассматриваемого рекомбинантного антитела или его антигенсвязывающей части, описанной в данном документе.
Например, рекомбинантное антитело может представлять собой или может содержать scFv-Fc, Fcab, mAb2, иммунофармацевтическое средство на основе модульного белка малого размера (SMIP), Genmab / Unibody или Duobody, миниантитело, IgGΔCH2, DVD-Ig, проантитело, интраантитело или полиспецифическое антитело.
DuoBody® представляет собой биспецифический модифицированний гетеродимер антитела IgG1. Шарнирная область IgG1, как правило, содержит (i) стабильную шарнирную область, которая содержит последовательность CPPC и является непермиссивной для обмена фрагментами Fab in vivo, и (ii) IgG4-подобный домен CH3, который модифицирован так, чтобы содержать остатки F405L и K409R, которые обеспечивают ее пермиссивность к обмену фрагментами Fab in vivo. (см., например, WO2008119353 и WO2011131746).
В некоторых вариантах реализации изобретения рекомбинантное антитело может содержать 1, 2, 3 или 4 зрелые процессированные последовательности тяжелой цепи, легкой цепи или их антигенсвязывающей части, каждая из которых получена из тяжелой цепи (HC), легкой цепи (LC) любого рассматриваемого рекомбинантного антитела или его антигенсвязывающей части, описанной в данном документе.
В некоторых вариантах реализации изобретения рекомбинантное антитело может представлять собой гетеродимерное антитело, содержащее первый полипептид тяжелой цепи и второй полипептид тяжелой цепи, где Fc-область первого полипептида тяжелой цепи и Fc-область второго полипептида тяжелой цепи встречаются в области контакта, и область контакта Fc-области второго полипептида тяжелой цепи содержит выступ, который может быть вмещен во впадину в области контакта Fc-области первого полипептида тяжелой цепи. В некоторых вариантах реализации изобретения для ускорения специфического спаривания тяжелых цепей в биспецифическом антителе технология «выступ-во-впадину» может быть дополнительно улучшена на основе, например, технологии CrossMab от Genentech / Roche, например, посредством замены константных областей CH1 и каппа для дополнительного уменьшения или устранения ошибочного спаривания легкой цепи.
В альтернативном варианте, подобные результаты могут быть достигнуты с применением гетеродимеров LC, например, технологии на платформе легкой цепи гетеродимерного IgG1 Azymetric™ от Zymeworks, которая полностью дополняет несколько других биологических подходов, включая обычные форматы легкой цепи, доменного антитела и одиночной цепи, при разработке полностью биспецифических антител.
В некоторых вариантах реализации изобретения Fc-область второго полипептида тяжелой цепи изменена относительно матричного/исходного полипептида для кодирования указанного выступа или Fc-область первого полипептида тяжелой цепи изменена относительно матричного/исходного полипептида для кодирования указанной впадины, или имеют место оба варианта.
В некоторых вариантах реализации изобретения каждый из выступа и впадины содержит природный аминокислотный остаток.
В некоторых вариантах реализации изобретения Fc-область второго полипептида тяжелой цепи, содержащую выступ, получают заменой исходного остатка из области контакта матричного/исходного полипептида на импортируемый остаток, имеющий больший объем боковой цепи, чем исходный остаток.
В некоторых вариантах реализации изобретения Fc-область второго полипептида тяжелой цепи, содержащую выступ, получают способом, включающим этап, на котором нуклеиновые кислоты, кодирующие исходный остаток из области контакта указанного полипептида, заменяют на нуклеиновые кислоты, кодирующие импортируемый остаток, имеющий больший объем боковой цепи, чем исходный остаток.
В некоторых вариантах реализации изобретения антитело включает биспецифические, мультиспецифические и моноспецифические варианты антител, которые содержат антигенсвязывающие области и константный домен тяжелой цепи, при этом константный домен тяжелой цепи модифицирован, чтобы содержать Cys в положении 442 в соответствии с нумерацией EU/OU.
В некоторых вариантах реализации изобретения антитело может связываться с лигандом на клетке-мишени, таким как лиганд клеточной поверхности, включая рецепторы клеточной поверхности.
Конкретные типовые антигены или лиганды могут включать ренин; гормон роста (например, человеческий гормон роста и бычий гормон роста); фактор, высвобождающий гормон роста; паратиреоидный гормон; тиреотропный гормон; липопротеин; альфа-1-антитрипсин; А-цепь инсулина; В-цепь инсулина; проинсулин; фолликулостимулирующий гормон; кальцитонин; лютеинизирующий гормон; глюкагон; фактор свертывания крови (например, фактор vmc, фактор IX, тканевый фактор и фактор фон Виллебранда), противосвертывающий фактор (например, протеин C); предсердный натрийуретический фактор; сурфактант легких; активатор плазминогена (например, урокиназный, мочевой или тканевый активатор плазминогена человека); бомбезин; тромбин; гемопоэтический фактор роста; фактор некроза опухоли-альфа и -бета; энкефалиназу; RANTES (т.е. хемокин, экспрессируемый и секретируемый T-клетками при активации); макрофагальный воспалительный белок человека-1-альфа; сывороточный альбумин (сывороточный альбумин человека); ингибирующее вещество Мюллера; A-цепь релаксина; B-цепь релаксина; прорелаксин; гонадотропин-ассоциированный пептид мыши; микробный белок (бета-лактамазу); ДНКазу; IgE; ассоциированный с цитотоксическими T-лимфоцитами антиген (например, CTLA-4); ингибин; активин; фактор роста эндотелия сосудов; рецептор гормонов или факторов роста; протеин A или D; ревматоидный фактор; нейротрофический фактор (например, костный нейтротрофический фактор, нейтротрофин-3, -4, -5 или -6), фактор роста нервов (например, NGF-β); тромбоцитарный фактор роста; фактор роста фибробластов (например, aFGF и bFGF); рецептор 2 фактора роста фибробластов; эпидермальный фактор роста; трансформирующий фактор роста (например, TGF-альфа, TGF-β1, TGF-β2, TGF-β3, TGF-β4 и TGF-β5); инсулиноподобный фактор роста-I и -II; дез(1-3)-IGF-I (IGF-I головного мозга); белок, связывающий инсулиноподобный фактор роста; меланотрансферрин; EpCAM; GD3; FLT3; PSMA; PSCA; MUC1; MUC16; STEAP; CEA; TENB2; рецептор EphA; рецептор EphB; рецептор фолиевой кислоты; FOLR1; мезотелин; крипто; альфаvбета6; интегрины; VEGF; VEGFR; EGFR; рецептор трансферрина; IRTA1; IRTA2; IRTA3; IRTA4; IRTA5; белки CD (например, CD2, CD3, CD4, CD5, CD6, CD8, CD11, CD14, CD19, CD20, CD21, CD22, CD25, CD26, CD28, CD30, CD33, CD36, CD37, CD38, CD40, CD44, CD52, CD55, CD56, CD59, CD70, CD79, CD80, CD81, CD103, CD105, CD123, CD134, CD137, CD138 и CD152), один или более опухолеассоциированных антигенов или рецепторов клеточной поверхности (см. публикацию США № 2008/0171040 или публикацию США № 2008/0305044, в полном объеме включенные в данный документ посредством ссылки); эритропоэтин; остеоиндуктивный фактор, иммунотоксин; костный морфогенетический белок, интерферон (например, интерферон-альфа, -бета и -гамма); колониестимулирующий фактор (например, M-CSF, GM-CSF и G-CSF); интерлейкины (например, IL-1-IL-10); супероксиддисмутазу; T-клеточный рецептор; поверхностный мембранный белок; фактор ускорения распада; вирусный антиген (например, часть оболочки ВИЧ); транспортный белок, хоминг-рецептор; адрессин; регуляторный белок; интегрин (например, CD11a, CD11b, CD11c, CD18, ICAM, VLA-4 и VCAM); опухолеассоциированный антиген (например, рецептор HER2, HER3 и HER4); эндоглин; c-Met; c-kit; 1GF1R; PSGR; NGEP; PSMA; PSCA; TMEFF2; LGR5; B7H4; и фрагменты любых вышеперечисленных полипептидов.
В одном варианте реализации изобретения клеточносвязывающий агент представляет собой антитело к рецептору фолиевой кислоты. Более конкретно антитело к рецептору фолиевой кислоты представляет собой гуманизированное антитело, которое специфически связывает рецептор фолиевой кислоты 1 человека, при этом данное антитело содержит: (а) CDR1 тяжелой цепи, содержащий GYFMN (SEQ ID №: 1); CDR2 тяжелой цепи, содержащий RIHPYDGDTFYNQXaa1FXaa2Xaa3 (SEQ ID №: 2); и CDR3 тяжелой цепи, содержащий YDGSRAMDY (SEQ ID №: 3); и (б) CDR1 легкой цепи, содержащий KASQSVSFAGTSLMH (SEQ ID №: 4); CDR2 легкой цепи, содержащий RASNLEA (SEQ ID №: 5); и CDR3 легкой цепи, содержащий QQSREYPYT (SEQ ID №: 6); где Xaa1 выбран из K, Q, H и R; Xaa2 выбран из Q, H, N и R; и Xaa3 выбран из G, E, T, S, A и V. Предпочтительно последовательность CDR2 тяжелой цепи содержит RIHPYDGDTFYNQKFQG (SEQ ID №: 7).
В другом варианте реализации изобретения антитело к рецептору фолиевой кислоты представляет собой гуманизированное антитело или его антигенсвязывающий фрагмент, который специфически связывает рецептор фолиевой кислоты 1 человека, содержащий тяжелую цепь, имеющую аминокислотную последовательность QVQLVQSGAEVVKPGASVKISCKASGYTFTGYFMNWVKQSPGQSLEWIGRIHPYDGDTFYNQKFQGKATLTVDKSSNTAHMELLSLTSEDFAVYYCTRYDGSRAMDYWGQGTTVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSRDELTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLCLSPG (SEQ ID №: 8).
В другом варианте реализации изобретения антитело к рецептору фолиевой кислоты представляет собой гуманизированное антитело или его антигенсвязывающий фрагмент, который специфически связывает рецептор фолиевой кислоты 1 человека, содержащий легкую цепь, имеющую аминокислотную последовательность DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLNISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID №: 9); или DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLTISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC (SEQ ID №: 10).
В другом варианте реализации изобретения антитело к рецептору фолиевой кислоты представляет собой гуманизированное антитело или его антигенсвязывающий фрагмент, который специфически связывает рецептор фолиевой кислоты 1 человека, содержащий тяжелую цепь, имеющую аминокислотную последовательность SEQ ID №: 8, и легкую цепь, имеющую аминокислотную последовательность SEQ ID №: 9 или SEQ ID №: 10. Предпочтительно данное антитело содержит тяжелую цепь, имеющую аминокислотную последовательность SEQ ID №: 8, и легкую цепь, имеющую аминокислотную последовательность SEQ ID №: 10 (huMov19).
В другом варианте реализации изобретения антитело к рецептору фолиевой кислоты представляет собой гуманизированное антитело или его антигенсвязывающий фрагмент, содержащий сконструированный остаток Cys (например, C442) и вариабельный домен тяжелой цепи, по меньшей мере на около 90%, 95%, 99% или на 100% идентичный относительно QVQLVQSGAEVVKPGASVKISCKASGYTFTGYFMNWVKQSPGQSLEWIGRIHPYDGDTFYNQKFQGKATLTVDKSSNTAHMELLSLTSEDFAVYYCTRYDGSRAMDYWGQGTTVTVSS (SEQ ID №: 11), и вариабельный домен легкой цепи, по меньшей мере на около 90%, 95%, 99% или на 100% идентичный относительно DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLNISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKR (SEQ ID №: 12); или DIVLTQSPLSLAVSLGQPAIISCKASQSVSFAGTSLMHWYHQKPGQQPRLLIYRASNLEAGVPDRFSGSGSKTDFTLTISPVEAEDAATYYCQQSREYPYTFGGGTKLEIKR (SEQ ID №: 13).
В конкретном варианте реализации изобретения гуманизированное антитело представляет собой huMy9-6 или другое родственное антитело, которое описано в патентах США №№ 7342110 и 7557189. В другом конкретном варианте реализации изобретения гуманизированное антитело представляет собой антитело к рецептору фолиевой кислоты (например, huMov19), описанное в патенте США № 8577966. В некоторых вариантах реализации изобретения гуманизированное антитело представляет собой антитело к CD37 (например, к CD37-3), описанное в патенте США № 8765917. В некоторых вариантах реализации изобретения гуманизированное антитело представляет собой антитело к EGFR, описанное в патенте США № 8790649. В другом варианте реализации изобретения антитело представляет собой антитело к EGFR. В одном варианте реализации изобретения антитело к EGFR представляет собой антитело-не антагонист, включая, например, антитела, описанные в WO2012058592, включенной в данный документ посредством ссылки. В другом варианте реализации изобретения антитело к EGFR представляет собой нефункциональное антитело, например, гуманизированное ML66. Более конкретно антитело к EGFR представляет собой huML66.
В одном варианте реализации изобретения антитело представляет собой антитело к CD123, такое как гуманизированное антитело huCD123, описанное в предварительной заявке на патент США № 62/186161, поданной 29 июня 2015 года, озаглавленной «ANTI-CD123 ANTIBODIES AND CONJUGATES AND DERIVATIVES THEREOF» (полное содержание которой, включая все последовательности и графические материалы, включены в данный документ).
СПОСОБ ПОЛУЧЕНИЯ КОНЪЮГАТОВ ПО ДАННОМУ ИЗОБРЕТЕНИЮ
Иммуноконъюгаты, описанные выше (например, иммуноконъюгаты формулы (I) или иммуноконъюгаты любого из 1го-25го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них), могут быть получены посредством приведения в контакт антитела, содержащего один или более свободных цистеинов, с соединением, имеющим тиол-реакционноспособную группу, описанным в данном документе.
В одном варианте реализации изобретения соединение, имеющее тиол-реакционноспособную группу, представлено формулой (II) или соединениями любого из 1го-25го вариантов реализации или любых конкретных вариантов реализации изобретения, описанных в них.
В некоторых вариантах реализации изобретения органические растворители применяют в реакции CBA и соединения, имеющего тиол-реакционноспособную группу, для солюбилизации данного соединения. Типовые органические растворители включают, но не ограничиваются ими, диметилацетамид (ДМА), пропиленгликоль и т.д. В одном варианте реализации изобретения реакцию CBA и соединения проводят в присутствии ДМА и пропиленгликоля.
КОМПОЗИЦИИ И СПОСОБЫ ПРИМЕНЕНИЯ
Данное изобретение включает композицию (например, фармацевтическую композицию), содержащую новые соединения бензодиазепина, описанные в данном документе (например, индолинбензодиазепин или оксазолидинбензодиазепин), их производные или их конъюгаты (и/или их сольваты, гидраты и/или соли), и носитель (фармацевтически приемлемый носитель). Данное изобретение также включает композицию (например, фармацевтическую композицию), содержащую новые соединения бензодиазепина, описанные в данном документе, их производные или их конъюгаты (и/или их сольваты, гидраты и/или соли), и носитель (фармацевтически приемлемый носитель), дополнительно содержащую второй терапевтический агент. Композиции по данному изобретению пригодны для ингибирования аномального роста клеток или лечения пролиферативного нарушения у млекопитающего (например, человека). Данное изобретение включает способ ингибирования аномального роста клеток или лечения пролиферативного нарушения у млекопитающего (например, человека), включающий введение указанному млекопитающему терапевтически эффективного количества терапевтического агента или композиции, например, новых соединений бензодиазепина, описанных в данном документе (например, индолинбензодиазепина или оксазолидинбензодиазепина), их производных или их конъюгатов (и/или их сольватов и солей), или их композиции, отдельно или в комбинации со вторым терапевтическим агентом.
В одном варианте реализации изобретения пролиферативное нарушение представляет собой рак. Рак может включать гемобластоз или солидную опухоль. Более конкретно рак представляет собой лейкоз (например, острый миелоидный лейкоз (ОМЛ), острый лимфобластный лейкоз (ОЛЛ), такой как острый В-клеточный лимфобластный лейкоз (В-ОЛЛ), хронический миелогенный лейкоз (ХМЛ), хронический лимфоцитарный лейкоз (ХЛЛ)) или лимфому, меланому, рак легкого (например, немелкоклеточный рак легкого), рак яичников, рак эндометрия, рак брюшины, рак поджелудочной железы, рак молочной железы, рак предстательной железы и рак шейки матки.
В данном изобретении также предложены способы лечения, включающие введение субъекту, нуждающемуся в лечении, эффективного количества любого из конъюгатов, описанных выше.
Аналогичным образом, в данном изобретении предложен способ индуцирования гибели клеток в выбранных клеточных популяциях, включающий приведение в контакт клеток-мишеней или ткани, содержащей клетки-мишени, с эффективным количеством цитотоксического агента, содержащего любой из конъюгатов цитотоксического соединения с клеточносвязывающим агентом (например, димера индолинбензодиазепина или оксазолидинбензодиазепина, связанного с клеточносвязывающим агентом) по данному изобретению, его соли или сольвата. Клетки-мишени представляют собой клетки, с которыми может связываться клеточносвязывающий агент.
При необходимости вместе с указанным конъюгатом могут быть введены другие активные агенты, такие как другие противоопухолевые агенты.
Подходящие фармацевтически приемлемые носители, разбавители и вспомогательные вещества хорошо известны и могут быть определены специалистами в данной области техники в зависимости от требований клинической ситуации. Примеры подходящих носителей, разбавителей и/или вспомогательных веществ включают: (1) фосфатно-солевой буферный раствор Дульбекко, pH около 7,4, содержащий или не содержащий от около 1 мг/мл до около 25 мг/мл сывороточного альбумина человека, (2) 0,9% солевой раствор (0,9% мас./об. NaCl) и (3) 5% (мас./об.) раствор декстрозы; и могут включать также антиоксидант, такой как триптамин, и стабилизирующий агент, такой как Твин 20.
Способ индуцирования гибели клеток в выбранных клеточных популяциях может быть осуществлен in vitro, in vivo или ex vivo.
Примеры применений in vitro включают обработку аутологичного костного мозга до его трансплантации тому же пациенту для уничтожения пораженных или злокачественных клеток; обработку костного мозга до его трансплантации для уничтожения компетентных T-клеток и предотвращения реакции «трансплантат против хозяина» (GVHD); обработку клеточных культур для уничтожения всех клеток, кроме требуемых вариантов, которые не экспрессируют антиген-мишень; или для уничтожения вариантов, которые экспрессируют нежелательный антиген. Условия неклинического применения in vitro могут быть легко определены специалистами в данной области техники.
Примерами клинического применения ex vivo являются удаление опухолевых клеток или лимфоидных клеток из костного мозга до аутологичной трансплантации при лечении рака или при лечении аутоиммунного заболевания, или удаление T-клеток и других лимфоидных клеток из аутологичного или аллогенного костного мозга или ткани до трансплантации для предупреждения GVHD. Обработка может быть осуществлена следующим образом. Костный мозг берут у пациента или другого индивидуума и затем инкубируют в среде, содержащей сыворотку, в которую добавлен цитотоксический агент по данному изобретению в концентрации, составляющей от около 10 мкМ до 1 пМ, в течение от около 30 минут до около 48 часов при температуре около 37 oC. Точные условия концентрации и время инкубации, т.е. доза, могут быть легко определены специалистами в данной области техники. После инкубации клетки костного мозга промывают средой, содержащей сыворотку, и возвращают пациенту внутривенно в соответствии с известными способами. В тех обстоятельствах, в которых пациент получает другое лечение, такое как курс аблативной химиотерапии или облучение всего тела, от момента сбора костного мозга до момента реинфузии обработанных клеток, обработанные клетки костного мозга хранят в замороженном состоянии в жидком азоте, используя стандартное медицинское оборудование.
Для клинического применения in vivo цитотоксический агент по данному изобретению обеспечивают в виде раствора или лиофилизированного порошка, которые проверяют на стерильность и содержание эндотоксинов. Конкретные клинические протоколы в отношении способа введения, вспомогательных веществ, разбавителей, доз, времени и т.д. могут быть определены специалистами в данной области техники в зависимости от требований клинической ситуации.
Примеры медицинских состояний, которые можно лечить в соответствии со способами индуцирования гибели клеток in vivo или ex vivo в выбранных клеточных популяциях, включают злокачественное заболевание любого типа, включая, например, рак; аутоиммунные заболевания, такие как системная красная волчанка, ревматоидный артрит и рассеянный склероз; отторжение трансплантата, такое как отторжение трансплантата почек, отторжение трансплантата печени, отторжение трансплантата легких, отторжение трансплантата сердца и отторжение трансплантата костного мозга; реакцию «трансплантат против хозяина»; вирусные инфекции, такие как инфекция ЦМВ, инфекция ВИЧ, СПИД и т.д.; и паразитарные инфекции, такие как лямблиоз, амебиаз, шистосомоз и другие, известные специалистам в данной области техники.
Конкретные клинические протоколы в отношении способа введения, вспомогательных веществ, разбавителей, доз, времени и т.д. могут быть определены специалистами в данной области техники в зависимости от требований клинической ситуации.
Противораковые терапии и их дозы, способы введения и рекомендуемое применение известны в данной области техники и описаны в таких литературных источниках как Physician's Desk Reference (PDR). В PDR описаны дозы агентов, которые применяют при лечении различных раковых заболеваний. Схема применения и дозы этих вышеупомянутых химиотерапевтических лекарственных средств, которые являются терапевтически эффективными, зависят от конкретного типа рака, подлежащего лечению, тяжести заболевания и других факторов, известных опытным врачам, и могут быть определены данным врачом. Содержание PDR специально включено в данный документ посредством ссылки в полном объеме. Специалисты в данной области техники могут обратиться к PDR, используя один или более из следующих параметров, для определения схемы применения и доз химиотерапевтических агентов и конъюгатов, которые могут применяться в соответствии с принципами данного изобретения. Эти параметры включают:
• Подробный указатель
• По производителю
• Продукты (по названию компании или товарному знаку лекарственного средства)
• Указатель категории
• Непатентованный/химический указатель (общепринятые названия лекарственных средств, не относящиеся к товарным знакам)
• Цветные изображения медикаментов
• Информацию о продукте, соответствующую маркировке FDA
• Химическую информацию
• Функцию/действие
• Показания и противопоказания
• Пробные испытания, побочные эффекты, предостережения
ПРИМЕРЫ
Пример 1 Подготовка реагентов линкер-эффектор для конъюгации антител
Следующие растворители, реагенты, защитные группы, фрагменты и другие обозначения могут указываться в виде сокращений в скобках:
ванная вода
карбодиимид
хроматография
кт
около 25 ºC)
фуран
или ОФ-ВЭЖХ
А. Синтез N-(2-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)этил)-11-(3-((((S)-8-метокси-6-оксо-11,12,12a,13-тетрагидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол-9-ил)окси)метил)-5-((((S)-8-метокси-6-оксо-12а,13-дигидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол-9-ил)окси)метил)фенил)-13,13-диметил-2,5,8-триокса-14,15-дитиа-11-азанонадекан-19-амида, соединения D6

К раствору свободного тиола 6a (40 мг, 0,042 ммоль) и NHS 4-(2-пиридилдитио)бутаната (35 мг, 80% чистоты, 0,085 ммоль) в безводном дихлорметане (0,5 мл) добавляли безводный диизопропилэтиламин (0,015 мл, 0,085 ммоль) и перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь гасили насыщенным раствором хлорида аммония и разбавляли дихлорметаном. Полученную смесь отделяли в делительной воронке. Органический слой промывали насыщенным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и отгоняли при пониженном давлении. Остаток очищали посредством полупрепаративной обращенно-фазовой ВЭЖХ (колонка С18, CH3CN/H2O). Фракции, содержащие чистый продукт, объединяли, замораживали и лиофилизировали с получением необходимого эфира NHS, 6b (29,7 мг, выход 60%). ЖХМС = 9,1 мин (15-минутный способ). МС (m/z): 1157,3 (M + 1)+.

К раствору эфира NHS, 6b (12,3 мг, 0,011 ммоль) и N-(2-аминоэтил)малеимида гидрохлорида (2,0 мг, 0,011 ммоль) в безводном дихлорметане (0,3 мл) добавляли DIPEA (0,0022 мл, 0,013 ммоль). Смесь перемешивали при комнатной температуре в течение 3 часов, затем ее отгоняли при пониженном давлении. Остаток очищали посредством полупрепаративной обращенно-фазовой ВЭЖХ (колонка С18, CH3CN/H2O). Фракции, содержащие чистый продукт, объединяли, замораживали и лиофилизировали с получением необходимого малеимида, соединения D6 (10 мг, выход 80%). ЖХМС = 8,3 мин (15-минутный способ). МС (m/z): 1181,8 (M + 1)+.
Б. Синтез N1-(2-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)этил)-N6-((S)-1-(((S)-1-((3-((((S)-8-метокси-6-оксо-11,12,12a,13-тетрагидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол 9-ил)окси)метил)-5-((((S)-8-метокси-6-оксо-12а,13-дигидро-6Н-бензо[5,6][1,4]диазепино[1,2-а)индол-9-ил)окси)метил)фенил)амино)-1-оксопропан-2-ил)амино)-1-оксопропан-2-ил)адипамида, соединения D5

Эфир NHS 5a (8,2 мг, 7,6 мкмоль) и 1-(2-аминоэтил)-1H-пиррол-2,5-диона гидрохлорид (2,2 мг, 0,011 ммоль) растворяли в безводном дихлорметане (305 мкл) при комнатной температуре. Добавляли DIPEA (2,66 мкл, 0,015 ммоль) и перемешивали реакционную смесь в течение 3,5 часов. Реакционную смесь концентрировали и очищали посредством ОФ-ВЭЖХ (колонка C18, CH3CN/H2O, градиент, от 35% до 55%). Необходимые фракции продукта замораживали и лиофилизировали с получением малеимида, соединения D5 в виде твердого белого порошка (5,3 мг, выход 58%). ЖХМС = 5,11 мин (8-минутный способ). МС (m/z): 1100,6 (M + 1)+.
В. Синтез 1-((2-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)этил)амино)-4-((5-((3-((((S)-8-метокси-6-оксо-11,12,12a,13-тетрагидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол-9-ил)окси)метил)-5-((((S)-8-метокси-6-оксо-12а,13-дигидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол-9-ил)окси)метил)фенил)амино)-2-метил-5-оксопентан-2-ил)дисульфанил)-1-оксобутан-2-сульфоновой кислоты, соединения D4

К суспензии свободного тиола, 4a (88 мг, 0,105 ммоль) и 1-((2,5-диоксопирролидин-1-ил)окси)-1-оксо-4-(пиридин-2-илдисульфанил)бутан-2-сульфоновой кислоты (64,0 мг, 0,158 ммоль) в безводном дихлорметане (2,10 мл) добавляли DIPEA (55,0 мкл, 0,315 ммоль) в атмосфере азота при комнатной температуре. Смесь перемешивали в течение 16 часов и затем добавляли 1-(2-аминоэтил)-1H-пиррол-2,5-диона гидрохлорид (55,6 мг, 0,315 ммоль), безводный дихлорметан (1,0 мл) и DIPEA (0,055 мл, 0,315 ммоль). Смесь перемешивали в течение еще 5 часов при комнатной температуре, после чего реакционную смесь концентрировали в вакууме. Полученный остаток очищали посредством ОФ-ВЭЖХ (C18, CH3CN/H2O). Фракции, содержащие необходимый продукт, замораживали и лиофилизировали с получением малеимида, соединения D4 (20 мг, выход 16%) в виде белого твердого вещества. ЖХМС = 4,92 мин (8-минутный способ). МС (m/z): 1158,6 (M + 1)+.
Г. Синтез N-(2-(2,5-диоксо-2,5-дигидро-1Н-пиррол-1-ил)этил)-11-(3-((((S)-8-метокси-6-оксо-11,12,12a,13-тетрагидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол-9-ил)окси)метил)-5-((((S)-8-метокси-6-оксо-12а,13-дигидро-6Н-бензо[5,6][1,4]диазепино[1,2-а]индол-9-ил)окси)метил)фенил)-2,5,8-триокса-11-азапентадекан-15-амида, соединения D7

К раствору эфира NHS, 7a (5 мг, 4,82 мкмоль) и 1-(2-аминоэтил)-1H-пиррол-2,5-диона гидрохлорида (1,7 мг, 9,64 мкмоль) в безводном дихлорметане (200 мкл) добавляли DIPEA (1,512 мкл, 8,68 мкмоль) в атмосфере азота. Смесь перемешивали при комнатной температуре в течение 4 часов и затем концентрировали в вакууме. Полученный остаток очищали посредством ОФ-ВЭЖХ (C18, CH3CN/H2O). Фракции, содержащие необходимый продукт, замораживали и лиофилизировали с получением малеимида, соединения D7 (3,5 мг, выход 68%). ЖХМС = 4,61 мин (15-минутный способ). МС (m/z): 1062,8 (M + 1)+.
Пример 2 Конъюгирование антител с типовыми реагентами линкер-эффектор
Реагенты антител
Экспрессионный вектор, кодирующий тяжелую цепь ранее описанного гуманизированного антитела MOV19 (huMOV19, патент США № 8557966, включенный посредством ссылки), подвергали мутагенезу так, чтобы экспрессируемый белок содержал остаток цистеина в положении 442 по системе нумерации EU/OU в домене CH3 тяжелой цепи, с использованием стандартных способов молекулярного клонирования. Вариант IgG1 huMOV19-HC-C442 (или сокращенно huMOV19-C442) экспрессировали и очищали от клеток млекопитающих с помощью установленных способов для IgG1-антител человека. Аналогичные способы применяли для клонирования, экспрессии и очистки нескольких вариантов антитела huCD123-6G, содержащих такую же мутацию цистеина 442 (например, huCD123-6Gv1.1-C442 и huCD123-6Gv4.7-C442). Эти антитела huCD123-6 подробно описаны в предварительной заявке на патент США № 62/186161, поданной 29 июня 2015 года, озаглавленной «ANTI-CD123 ANTIBODIES AND CONJUGATES AND DERIVATIVES THEREOF», полное содержание которой, включая все белки и нуклеотидные последовательности, а также графические материалы, включены в данный документ посредством ссылки.
А. huMOV19-C442-Mal-CX1-1-DM1
Антитело huMOV19-C442, содержащее два неспаренных остатка цистеина (в положении C442 области CH3 тяжелой цепи) в восстановленном состоянии, получали с помощью стандартных методов химии белков. К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N-диметилацетамид (ДМА) и 8 молярных эквивалентов Mal-CX1-1-DM1 (см. WO 2014/134486) в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 10% об./об. ДМА в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на ночь при 25 °С.

При образовании ковалентной связи между свободной тиольной группой остатков C442 и малеимидной (Mal) группой Mal-CX1-1-DM1, показанной выше, конъюгат очищали в рецептурном буфере, содержащем 10 мМ сукцината, 250 мМ глицина, 0,5% сахарозы, 0,01% Твин-20, pH 5.5, с применением обессоливающих колонок Sephadex G25, концентрировали посредством ультрафильтрации через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,25 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что данный конъюгат содержит в среднем 2 моль DM1/моль антитела согласно UV-Vis-спектроскопии; 99,3% мономера согласно SEC; и не содержит детектируемого неконъюгированного DM1 согласно ВЭЖХ на колонке HISEP. ЖХ-МС дегликозилированного конъюгата показана на Фиг. 1А.
Б. huMOV19-C442-Mal-SPDB-DM4
Антитело huMOV19, содержащее два неспаренных остатка цистеина (в положении C442 области CH3 тяжелой цепи) в восстановленном состоянии, получали с помощью стандартных методов. К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N-диметилацетамид (ДМА) и 6 молярных эквивалентов Mal-SPDB-DM4 (см. WO 2014/134483) в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 10% об./об. ДМА в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на ночь при 25 °С.

Конъюгат очищали в рецептурном буфере, содержащем 10 мМ сукцината, 250 мМ глицина, 0,5% сахарозы, 0,01% Твин-20, pH 5,5 с применением обессоливающих колонок Sephadex G25, концентрировали ультрафильтрацией через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,22 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что данный конъюгат содержит 2 моль DM4/моль антитела согласно UV-Vis-спектроскопии; 99,5% мономера согласно SEC; и 0,8% неконъюгированного DM4 согласно ВЭЖХ на колонке HISEP. ЖХ-МС дегликозилированного конъюгата показана на Фиг. 1Б.
В. huMOV19-C442-D5
Антитело huMOV19, содержащее два неспаренных остатка цистеина (в положении C442 области CH3 тяжелой цепи) в восстановленном состоянии, получали с помощью стандартных методов. К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N-диметилацетамид (ДМА), пропиленгликоль и 8 молярных эквивалентов соединения D5 в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 2% об./об. ДМА и 38% об./об. пропиленгликоля в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на 24 часа при 25 °С.
Конъюгат очищали в рецептурном буфере, содержащем 20 мМ гистидина, 50 мМ хлорида натрия, 8,5% сахарозы, 0,01% Твин-20, 50 мкМ бисульфита натрия, pH 6,2 с применением обессоливающих колонок Sephadex G25, концентрировали ультрафильтрацией через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,22 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что конъюгат содержит в среднем 2 моль D5/моль антитела согласно UV-Vis-спектроскопии; 94,6% мономера согласно SEC; и 0,8% неконъюгированного D5 согласно SEC/обращенно-фазовой ВЭЖХ. ЖХ-МС дегликозилированного конъюгата показана на Фиг. 1В.
Г. huMOV19-C442-D4
Антитело huMOV19, содержащее два неспаренных остатка цистеина (в положении C442 области CH3 тяжелой цепи) в восстановленном состоянии, получали с помощью стандартных методов. К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N- диметилацетамид (ДМА), пропиленгликоль и 6 молярных эквивалентов D4 в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 2% об./об. ДМА и 38% об./об. пропиленгликоля в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на 24 часа при 25 °С.
Конъюгат очищали в рецептурном буфере, содержащем 20 мМ гистидина, 50 мМ хлорида натрия, 8,5% сахарозы, 0,01% Твин-20, 50 мкМ бисульфита натрия, pH 6,2 с применением обессоливающих колонок Sephadex G25, концентрировали ультрафильтрацией через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,22 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что конъюгат содержит в среднем 2 моль D4/моль антитела согласно UV-Vis-спектроскопии; 92,1% мономера согласно SEC; и 0,3% неконъюгированного D4 согласно SEC/обращенно-фазовой ВЭЖХ. ЖХ-МС дегликозилированного антитела показана на Фиг. 1Г.
Д. huCD123-6Gv1.1S2-C442-D7
Антитело huCD123, содержащее два неспаренных остатка цистеина (в положении C442 области CH3 тяжелой цепи) в восстановленном состоянии (и сконструированный N-концевой Ser на тяжелой цепи), получали с помощью стандартных методов. К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N-диметилацетамид (ДМА), пропиленгликоль и 10 молярных эквивалентов соединения D7 в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 2% об./об. ДМА и 38% об./об. пропиленгликоля в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на 24 часа при 25 °С.
Конъюгат очищали в рецептурном буфере, содержащем 20 мМ гистидина, 50 мМ хлорида натрия, 8,5% сахарозы, 0,01% Твин-20, 50 мкМ бисульфита натрия, pH 6,2 с применением обессоливающих колонок Sephadex G25, концентрировали ультрафильтрацией через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,22 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что конъюгат содержит 2 моль D7/моль антитела согласно UV-Vis-спектроскопии; 97,2% мономера согласно SEC; и 1,9% неконъюгированного D7 согласно SEC/обращенно-фазовой ВЭЖХ. ЖХ-МС дегликозилированного конъюгата показана на Фиг. 1Д.
Е. huCD123-6Gv4.7-C442-D5/huCD123-6Gv4.6-C442-D5
Антитело huCD123 (huCD123-6Gv4.7-C442 или huCD123-6Gv4.6-C442), содержащее два неспаренных остатка цистеина в восстановленном состоянии, получали с помощью стандартных методов. Оба антитела huCD123 имеют сконструированный остаток Cys в положении 442 по системе нумерации EU/OU в области CH3 тяжелой цепи и отличаются только во 2ом остатке из N-конца цепи тяжелой цепи (т.е. Val для huCD123-6Gv4.7-C442 и Phe для huCD123-6Gv4.6-C442).
К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N-диметилацетамид (ДМА), пропиленгликоль и 10 молярных эквивалентов соединения D5 в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 2% об./об. ДМА и 38% об./об. пропиленгликоля в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на 24 часа при 25 °С.
Конъюгат очищали в рецептурном буфере, содержащем 20 мМ гистидина, 50 мМ хлорида натрия, 8,5% сахарозы, 0,01% Твин-20, 50 мкМ бисульфита натрия, pH 6,2 с применением обессоливающих колонок Sephadex G25, концентрировали ультрафильтрацией через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,22 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что конъюгат содержит в среднем 2 моль D5/моль антитела согласно UV-Vis-спектроскопии; и 94,8% мономера согласно SEC. ЖХ-МС дегликозилированного конъюгата показана на Фиг. 1Е.
Ж. huCD123-6Gv4.7-C442-D4/huCD123-6Gv4.6-C442-D4
Антитело huCD123, содержащее два неспаренных цистеиновых остатка (huCD123-6Gv4.7-C442 и huCD123-6Gv4.6-C442, см. выше) в восстановленном состоянии, получали с помощью стандартных методов.
К раствору этого промежуточного продукта в фосфатно-солевом буферном растворе (ФСБ), 5 мМ N,N,N’,N’-этилендиаминтетрауксусной кислоты (ЭДТА), pH 6,0, добавляли N,N-диметилацетамид (ДМА), пропиленгликоль и 5 молярных эквивалентов соединения D4 в качестве исходного раствора в ДМА с получением реакционной смеси с конечным составом раствора, содержащим 2% об./об. ДМА и 38% об./об. пропиленгликоля в ФСБ, 5 мМ ЭДТА, рН 6,0. Реакционную смесь оставляли на 6 часов при 25 °С.
Конъюгат очищали в рецептурном буфере, содержащем 20 мМ гистидина, 50 мМ хлорида натрия, 8,5% сахарозы, 0,01% Твин-20, 50 мкМ бисульфита натрия, pH 6,2 с применением обессоливающих колонок Sephadex G25, концентрировали ультрафильтрацией через мембрану с отсечкой по молекулярной массе 10 кДа и фильтровали через шприцевой фильтр с диаметром пор 0,22 мкм. Затем конъюгат диализовали против того же буфера с применением мембраны с отсечкой по молекулярной массе 10 кДа.
Было установлено, что конъюгат содержит 1,8 моль D4/моль антитела согласно UV-Vis-спектроскопии; и 97,4% мономера согласно SEC. ЖХ-МС дегликозилированного конъюгата показана на Фиг. 1Ж.
Фиг. 8 показывает, что конъюгация антитела huCD123-6Gv4.7 через Cys-связь с соединениями D4 и D5 лишь умеренно влияла на аффинность связывания конъюгатов.
Пример 3 Активность huCD123-6Rv1.1-C442-D5 in vitro в CD123-экспрессирующих клетках
Способность huCD123-6Rv1.1-C442-D5 уничтожать клетки, которые экспрессируют CD123 на своей клеточной поверхности, сравнивали с данной способностью лизин-связанного конъюгата, содержащего такое же антитело и полезную нагрузку (huCD123-6Rv1.1-D2), с применением анализов цитотоксичности in vitro.
Для химерного антитела к CD123 (chCD123) подтвержденные аминокислотные последовательности вариабельной области для мышиных CD123-антител оптимизировали по кодонам, синтезировали и клонировали в рамке считывания с константными областями антитела человека с помощью Blue Heron Biotechnology для создания химерных версий CD123-антител с использованием константных последовательностей IgG1 и каппа человека для тяжелых и легких цепей, соответственно.
Клеточные линии культивировали в культуральной среде в соответствии с рекомендациями поставщика клеток (ATCC или DSMZ). Клетки, от 2000 до 10000 в 100 мкл культуральной среды, добавляли в каждую лунку плоскодонных 96-луночных планшетов. Для блокирования Fc-рецепторов на клеточной поверхности в культуральную среду добавляли 100 нМ антитела chKTI (антитела того же изотипа). Конъюгаты разводили в культуральной среде с использованием 3-кратных серий разведений, и добавляли 100 мкл на лунку. Для определения вклада CD123-независимой цитотоксичности в некоторые лунки перед испытанием конъюгатов добавляли антитело, блокирующее CD123 – 100 нМ антитела chCD123-6. Лунки отрицательного контроля, содержащие клетки и среду, но не содержащие конъюгатов, а также лунки, содержащие только среду, включали в каждый аналитический планшет. Анализы проводили в трех повторностях для каждой точки данных. Планшеты инкубировали при 37 °С в увлажненном инкубаторе с 6% CO2 в течение 4-7 дней. Затем определяли относительное количество жизнеспособных клеток в каждой лунке с применением Cell Counting Kit-8 (набор 8 для подсчета клеток) на основе WST-8 (Dojindo Molecular Technologies, Inc., Роквилл, штат Мэриленд). Видимую выжившую фракцию клеток в каждой лунке рассчитывали, проводя первоначальную поправку на фоновое поглощение среды, а затем деля каждое значение на среднее значение в контрольных лунках (необработанных клетках). Выжившую фракцию клеток наносили на полулогарифмический график зависимости от концентрации конъюгата.
Эти данные показали, что конъюгат huCD123-6Rv1.1-C442-D5 был по меньшей мере настолько же активным, как лизин-связанный конъюгат huCD123-6Rv1.1-D2 в нескольких клеточных линиях. Некоторые примеры анализа цитотоксичности, проведенные с использованием клеточной линии EOL-1 ОМЛ, клеточной линии KOPN-8 В-ОЛЛ и клеточной линии MOLM-1 ХМЛ, представлены на Фиг. 2.
Оба конъюгата обеспечивали киллинг клеток дозозависимым образом, причем значения IC50 составляли около 0,002 нМ, 0,005 нМ и 0,02 нМ для клеток EOL-1, клеток KOPN-8 и клеток MOLM-1, соответственно. Киллинг был CD123-зависимым, поскольку конъюгаты были по меньшей мере в 100 раз менее токсичными в отношении клеток при блокировании антигена CD123 с помощью неконъюгированного антитела chCD123-6.
Пример 3а Активность huCD123-6Rv1.1-C442-D5’ in vitro в CD123-экспрессирующих клетках
Конъюгат huCD123 соединения D5’, кросс-линкер ДНК, получали в соответствии с аналогичными способами, описанными в Примере 2. Активность полученного конъюгата in vitro испытывали в отношении различных клеток-предшественников ОМЛ. Медианное значение IC50 находится в пикомолярном диапазоне.
Пример 4. Активность конъюгатов huMOV19-C442 in vitro в клеточных линиях FRα+
Способность huMOV19-C442-D5 и huMOV19-C442-D4 уничтожать клетки, которые экспрессируют рецептор фолиевой кислоты альфа (FRα) на своей клеточной поверхности, сравнивали с данной способностью лизин-связанного конъюгата, содержащего такое же антитело и полезную нагрузку (huMOV19-D2 и huMOV19-сульфо-SPDB-D1), с применением анализов цитотоксичности in vitro. Клеточные линии культивировали в культуральной среде в соответствии с рекомендациями поставщика клеток (ATCC или DSMZ). В каждую лунку плоскодонного 96-луночного планшета добавляли 1000-2000 клеток в 100 мкл культуральной среды. Конъюгаты разводили в культуральной среде с использованием 3-кратных серий разведений, и добавляли 100 мкл на лунку. Для определения вклада FRα-независимой цитотоксичности клетки в некоторых лунках предварительно инкубировали с 2 мкМ антитела huMOV19 перед добавлением конъюгатов («блокированных» или «+B»). Контрольные лунки, содержащие клетки и среду, но не содержащие конъюгатов, а также лунки, содержащие только среду, включали в каждый аналитический планшет. Анализы проводили в трех повторностях для каждой точки данных. Планшеты инкубировали при 37 °C в увлажненном инкубаторе с 6% CO2 в течение 5-6 дней. Затем определяли относительное количество жизнеспособных клеток в каждой лунке с применением либо аламарового синего (Alamar Blue) в соответствии с протоколом производителя (Life Technologies), либо Cell Counting Kit-8 на основе WST-8 (Dojindo Molecular Technologies, Inc., Роквилл, штат Мэриленд). Видимую выжившую фракцию клеток в каждой лунке рассчитывали, проводя первоначальную поправку на фоновое поглощение среды, а затем деля каждое значение на среднее значение в контрольных лунках (необработанных клетках). Выжившую фракцию клеток наносили на полулогарифмический график зависимости от концентрации конъюгата.
Cys-связанный конъюгат huMOV19-C442-D5 был по меньшей мере настолько же активным, как Lys-связанный конъюгат huMOV19-D2 в нескольких клеточных линиях. Два примера анализа цитотоксичности, проведенные с применением линии клеток KB карциномы шейки матки и линии клеток T47D метастатического рака молочной железы, показаны на Фиг. 3А и 3Б. Оба конъюгата обеспечивали киллинг клеток дозозависимым образом, причем значения IC50 составляли около 0,007-0,01 нМ для KB и 0,01-0,02 нМ для T47D (в расчете на моль антитела). Киллинг был FR-зависимым, поскольку конъюгаты были по меньшей мере в 100 раз менее токсичными в отношении клеток при блокировании антигена FRα с помощью неконъюгированного антитела huMOV19.
Аналогичным образом, конъюгат huMOV19-C442-D4 испытывали на клетках KB и установили, что он по меньшей мере настолько же активен, как лизин-связанный конъюгат huMOV19-сульфо-SPDB-D1. Типовые данные анализа цитотоксичности показаны на Фиг. 3В. Оба конъюгата обеспечивали киллинг клеток дозозависимым образом, причем значения IC50 составляли около 0,009-0,01 нМ. Киллинг был FRα-зависимым, поскольку конъюгаты были по меньшей мере в 100 раз менее токсичными в отношении клеток при блокировании антигена FRα с помощью неконъюгированного антитела huMOV19.
Пример 5. Неспецифическая активность
Около 50 мкл/лунку каждого конъюгата (либо Cys-связанного конъюгата huMOV19-C442-D5, либо Lys-связанного конъюгата huMOV19-D2) разводили в среде RPMI-1640 (Life Technologies) с добавлением термоинактивированной 10% ФБС (Life Technologies), 0,1 мг/мл гентамицина (Life Technologies) и βME (Life Technologies) в 96-луночном планшете (Falcon, круглодонный) в концентрациях, составляющих 1 × 10-10 М и 4 × 10-10 М, в шести повторностях. 300,19 клеток (мыши), как экспрессирующих рекомбинантный экспрессионный вектор FOLR1(FR1#14), так и не имеющих его (исходного), подсчитывали на гемоцитометре. 50 мкл/мл 1000 FR1#14 клеток/лунку добавляли в лунки, содержащие конъюгат или только среду, 50 мкл/мл 2000 исходных клеток/лунку добавляли в лунки, содержащие конъюгат или только среду, а также добавляли вместе и FR1#14, и исходные клетки в лунки, содержащие конъюгат или только среду. Все планшеты инкубировали в инкубаторе при 37 oC с 5% CO2 в течение 4 дней. Общий объем составлял 150 мкл/лунку. После инкубации анализировали жизнеспособность клеток, добавляя 75 мкл/лунку Cell Titer Glo (Promega) и оставляя для развития окраски в течение 30 минут. На люминометре считывали люминесценцию, и из всех значений вычитали фоновое значение, полученное в лунках, содержащих только среду. Столбчатую диаграмму среднего значения для каждой экспериментальной группы клеток строили с помощью Graph Pad Prism.
Как показано на Фиг. 4А и 4Б, и Cys-связанный конъюгат huMOV19-C442-D5, и Lys-связанный конъюгат huMOV19-D2 показывают сильный неспецифический киллинг ближайших антиген-отрицательных клеток.
Пример 6. Эффективность huMOV19-C442-D5 in vivo в модели ксенотрансплантата NCI-H2110 мыши
Противоопухолевую активность huMOV19-C442-D5 оценивали в установленной подкожной модели ксенотрансплантата немелкоклеточного рака легкого (НМРЛ).
Мышей SCID (24 животных) инокулировали клетками NCI-H2110 НМРЛ человека (1 × 107 клеток/животное), вводимыми подкожно в правый бок мышей. Когда опухоли достигали размера около 100 мм3 (через 6 дней после инокуляции опухолевых клеток), мышей в случайном порядке делили на группы лечения по 6 животных в зависимости от объема опухоли и обрабатывали одной внутривенной инъекцией либо huMOV19-D2, либо huMOV19-C442-D5, двумя дозами каждого, в соответствии со следующей таблицей.
1. Контроль растворителя
2. huMOV19-D2 (Lys-связанный) 2,7 мкг/кг в/в, однократно
3. huMOV19-D2 (Lys-связанный) 8,9 мкг/кг в/в, однократно
4. huMOV19-C442-D5 2,6 мкг/кг в/в, однократно
5. huMOV19-C442-D5 8,7 мкг/кг в/в, однократно
Дозы приведены, исходя из концентрации D2 или D5. При более высоких дозах все ADC были одинаково высокоактивны в отношении ксенотрансплантатов NCI-H2110 (средний T/C = 1-2%, 22 день) с полными регрессиями у 6/6 животных. При более низких дозах оба ADC были одинаково активны, при этом huMOV19-D2 в среднем приводил к T/C = 32% (22 день) и huMOV19-C442-D5 в среднем приводил к T/C = 39% (22 день).
См. результаты, приведенные в таблице ниже. См. также Фиг. 5.
(22 день)
Результаты показывают, что все испытуемые конъюгаты одинаково активны в моделях ксенотрансплантата НМРЛ NCI-H2110, независимо от типа конъюгации или места конъюгации.
Пример 7. Фармакокинетика huMOV19-C442-D5 у мышей
Фармакокинетику huMOV19-C442-D5 оценивали у самок мышей CD1. Самки мышей CD1 в возрасте около 7 недель (9 животных) получали однократную внутривенную инъекцию 2,5 мг/кг huMOV19-C442-D5. Затем производили забор крови из ретро-орбитального синуса в следующие моменты времени: 2 и 30 минут; 2, 4 и 8 часов; 1, 2, 3, 5, 7, 10, 14, 21 и 28 дней. Пробы поочередно брали у n = 3 животных в каждый момент времени и не брали пробы у животных более двух раз за 24 часа. Пробы крови центрифугировали и плазму декантировали в полипропиленовые пробирки, а затем хранили при -80 ºC до анализа.
Концентрации антитела huMOV19 в плазме определяли с помощью ELISA-анализа с применением планшетов, покрытых козьими антителами к IgG человека для иммобилизации, и фрагментами Fc к IgG человека, связанными с пероксидазой хрена для детектирования. Предел количественного определения для анализа составлял 1,6 нг/мл. Концентрации D5, связанного с IgG человека, в плазме определяли с помощью ELISA-анализа с применением планшетов, покрытых антителом к соединению индолинбензодиазепина, и детектировали с применением того же реагента на основе фрагмента Fc к IgG человека/пероксидазы хрена, что и для указанного выше анализа антител. LOQ для этого анализа составлял 1,0 нг/мл. Средняя концентрация в плазме из каждой из трех отдельных взятых у животных проб сообщается для каждого момента времени.
Как показано на Фиг. 6, конъюгат имеет такой же фармакокинетический профиль, как и неконъюгированное антитело.
Пример 8 Острая переносимость huMOV19-C442-D5 с однократным введением у самок мышей CD-1
Самок мышей CD-1 в возрасте 6 недель приобретали у компании Charles River Laboratories. Мышей содержали в течение периода акклиматизации, составляющего по меньшей мере 7 дней, с момента прибытия до начала исследования. Эксперименты по опытной переносимости проводили с использованием 2 мышей на группу, при дозах huMOV19-C442-D5, составляющих 175 мкг/кг (Фиг. 7А) или 218 мкг/кг (Фиг. 7Б), исходя из концентрации D5, для определения соответствующих доз для исследования полной МПД.
Для исследования МПД, животных распределяли по группам (n=8), исходя из массы тела. Мышам однократно в/в вводили контроль растворителя (0,1 мл/мышь) или huMOV19-C442-D5 в дозе, составляющей 153, 175 или 218 мкг/кг, в пересчете на концентрацию D5. Введение лекарственных средств проводили внутривенно с помощью 1,0 мл шприца, оснащенного ½-дюймовой иглой 27-го калибра. Массу тела измеряли ежедневно в течение по меньшей мере одной недели, а затем по меньшей мере два раза в неделю на протяжении оставшейся части эксперимента. Массы тела (МТ) мышей выражали как процентное изменение массы тела от массы тела перед обработкой следующим образом:
% изменение МТ = [(МТ до/МТ после) – 1] × 100
где «МТ после» представляет собой массу после обработки, а «МТ до» представляет собой начальную массу тела до обработки.
Процентную потерю массы тела (ПМТ) на максимально низком уровне выражали как среднее изменение массы тела после обработки. Если в любой момент исследования (1) масса тела падала более чем на 20% от исходной, животных умерщвляли. Мышей также умерщвляли, если (2) одна или обе задние лапы были парализованы или если (3) животное было слишком больным, чтобы суметь добраться до пищи и воды.
Нижеследующая таблица представляет собой сводные данные по группам лечения в рамках исследования МПД, дозированию/режиму дозирования и процентной потере массы тела на максимально низком уровне у самок мышей CD-1, внутривенно получавших huMOV19-C442-D5.

| название | год | авторы | номер документа |
|---|---|---|---|
| КОНЪЮГАТЫ СКОНСТРУИРОВАННЫХ АНТИТЕЛ С ЦИСТЕИНОВЫМИ ЗАМЕНАМИ | 2016 |
|
RU2834224C1 |
| АНТИ-CD123 АНТИТЕЛА И ИХ КОНЪЮГАТЫ И ПРОИЗВОДНЫЕ | 2016 |
|
RU2739612C2 |
| ПРОИЗВОДНЫЕ МАЙТАНЗИНОИДА С САМОРАСЩЕПЛЯЮЩИМИСЯ ПЕПТИДНЫМИ ЛИНКЕРАМИ И ИХ КОНЪЮГАТЫ | 2018 |
|
RU2765098C2 |
| ПТГ-СОЕДИНЕНИЯ С НИЗКИМИ СООТНОШЕНИЯМИ ПИКА И МИНИМУМА | 2017 |
|
RU2766959C2 |
| РЕЖИМ ДОЗИРОВАНИЯ СОЕДИНЕНИЯ PTH КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ | 2017 |
|
RU2777357C2 |
| ЖИДКИЕ ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ КОНЪЮГАТОВ PTH | 2020 |
|
RU2817015C2 |
| КОМБИНАТОРНАЯ ТЕРАПИЯ С АГОНИСТАМИ CNP КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ | 2017 |
|
RU2768747C2 |
| КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ РАКА С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ, СВЯЗЫВАЮЩИХСЯ С КОМПОНЕНТОМ СИГНАЛЬНОГО ПУТИ PD-1, И ИНГИБИТОРОВ MEK | 2015 |
|
RU2733735C2 |
| CNP ПРОЛЕКАРСТВА | 2016 |
|
RU2824988C1 |
| Лечение гипопаратиреоидизма | 2021 |
|
RU2827712C1 |



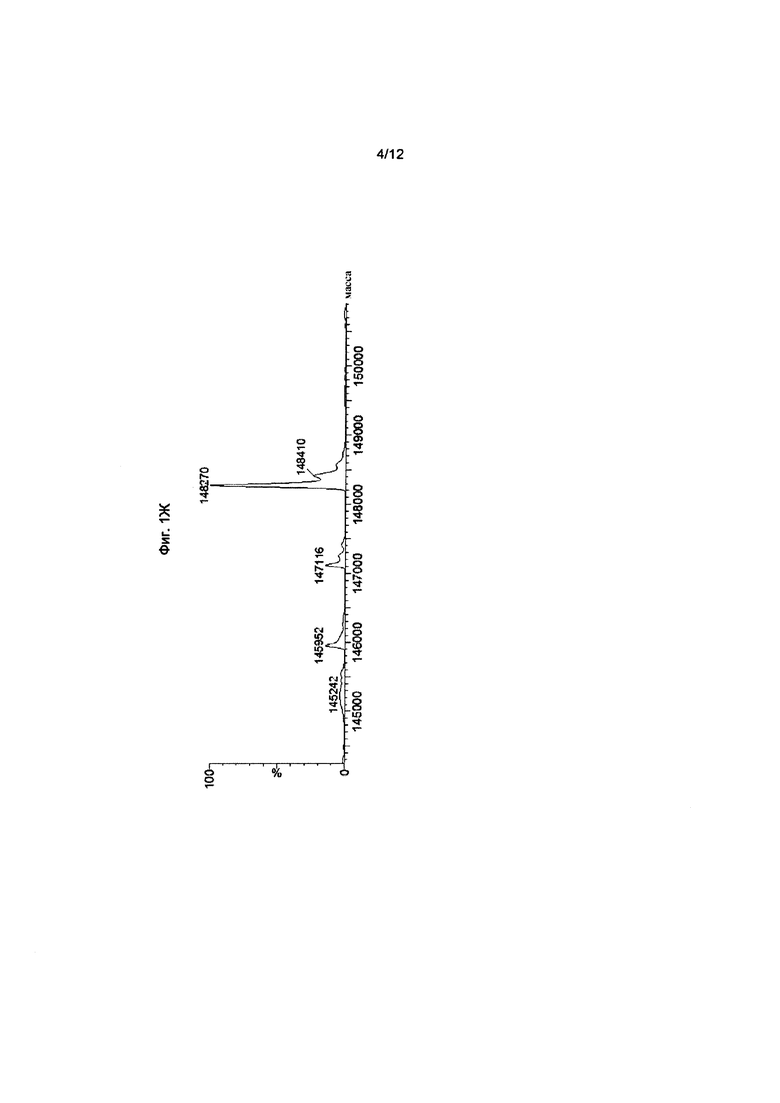


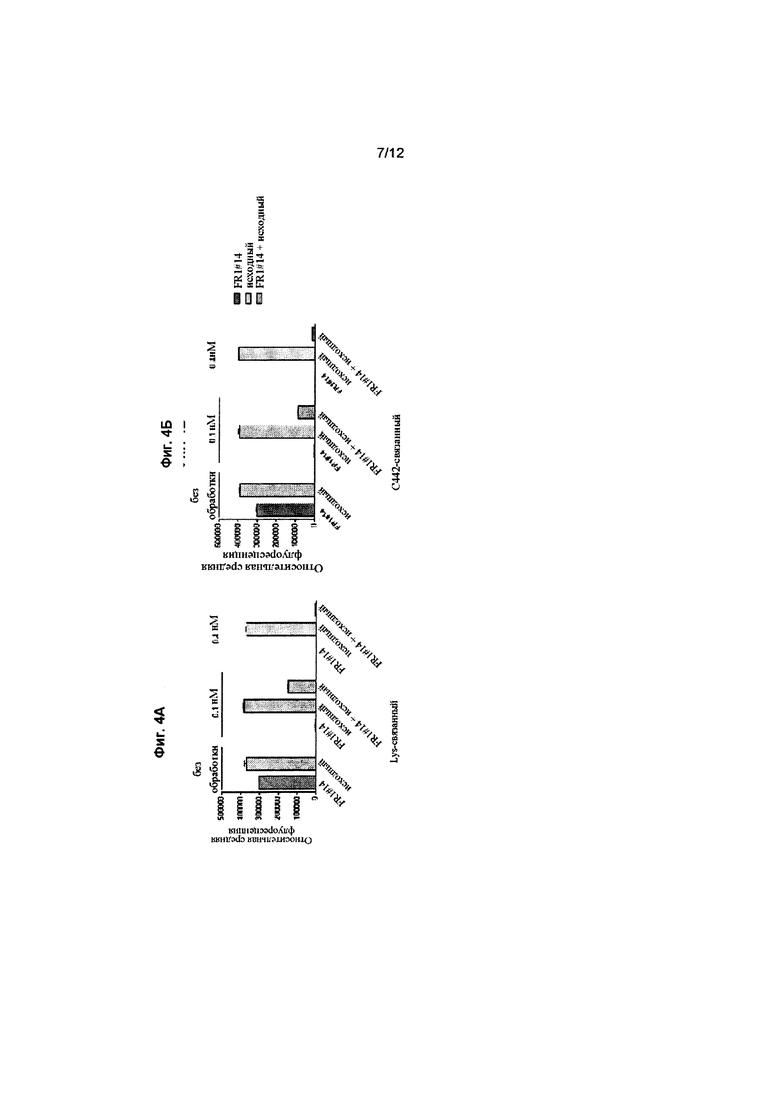





Изобретение относится к новым конъюгатам клеточносвязывающего агента с цитотоксическим агентом, в которых клеточносвязывающий агент (CBA) ковалентно связан с цитотоксическим агентом через сконструированный Cys, такой как сконструированный Cys в домене CH3 тяжелой цепи, в положении, соответствующем положению 442 (или C442) по системе нумерации EU/OU в CBA антитела. В данном изобретении также предложены способы получения конъюгатов по данному изобретению. Дополнительно предложены фармацевтическая композиция и способы, пригодные для ингибирования аномального роста клеток или лечения пролиферативного нарушения у млекопитающего с применением конъюгатов по данному изобретению. 5 н. и 28 з.п. ф-лы, 8 ил., 3 табл., 7 пр.
1. Конъюгат антитела с цитотоксическим средством, представленный следующей формулой:
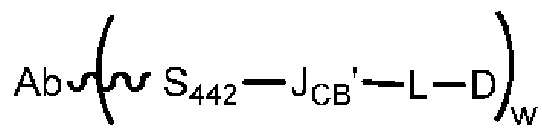 ,
,
или его фармацевтически приемлемая соль, где:
(i) Ab представляет собой антитело, содержащее остаток цистеина в положении 442 тяжелой цепи антитела в соответствии с нумерацией EU/OU и ковалентно связанное со связывающим фрагментом JCB' через тиольную группу S442 остатка цистеина;
(ii) JCB' представляет собой  ,
,
(iii) -L- представлен следующей структурной формулой:
 ,
,
где:
s3 представляет собой место ковалентной связи с JCB', а s4 представляет собой место ковалентной связи с D;
R23 и R24 представляют собой Н;
m' представляет собой целое число от 1 до 6; и
Rh' представляет собой Н;
(iv) D представляет собой цитотоксический агент, ковалентно связанный с линкером L, который ковалентно связан с JCB', где D представлен следующей формулой:
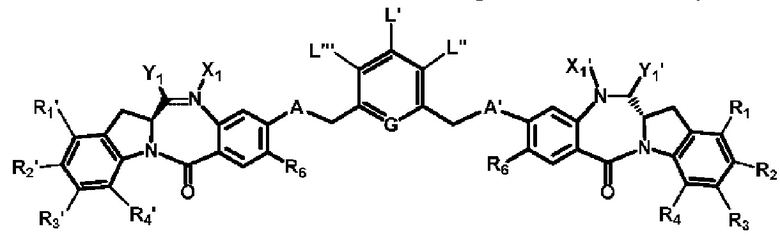
где:
оба L'' и L''' представляют собой Н и L' представлен следующей формулой:
 ,
,
R5 представляет собой Н или линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода;
P1 представляет собой пептид, содержащий от 2 до 10 аминокислотных остатков;
каждый из Ra и Rb, для каждого случая, независимо представляет собой -Н, (С1-С3)алкил или группу Q, которая представляет собой -SO3H или ее фармацевтически приемлемую соль;
s представляет собой целое число от 1 до 6;
G представляет собой -СН-;
двойная линия  между N и С представляет собой одинарную или двойную связь при условии, что, если она представляет собой двойную связь, X1 отсутствует и Y1 представляет собой Н; а когда она представляет собой одинарную связь, X1 представляет собой -Н и Y1 представляет собой -ОН или -SO3M;
между N и С представляет собой одинарную или двойную связь при условии, что, если она представляет собой двойную связь, X1 отсутствует и Y1 представляет собой Н; а когда она представляет собой одинарную связь, X1 представляет собой -Н и Y1 представляет собой -ОН или -SO3M;
R1, R2, R3, R4, R1', R2', R3' и R4' все представляют собой -Н;
R6 представляет собой -ОМе;
X1' и Y1' оба представляют собой -Н;
А и А' представляют собой -O-; и
М представляет собой Н+, Na+ или K+; и
(v) w равен 1 или 2.
2. Конъюгат по п. 1, отличающийся тем, что остаток цистеина в положении 442 рекомбинантно вводят в указанное Ab.
3. Конъюгат по п. 1 или 2, отличающийся тем, что -JCB'-L- представлен следующей структурной формулой:

4. Конъюгат по любому из пп. 1-3, отличающийся тем, что оба Ra и Rb представляют собой Н и R5 представляет собой Н или Me.
5. Конъюгат по любому из пп. 1-4, отличающийся тем, что P1 представляет собой пептид, содержащий от 2 до 5 аминокислотных остатков.
6. Конъюгат по п. 5, отличающийся тем, что P1 представляет собой Gly-Gly-Gly, Ala-Val, Val-Ala, Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID NO: 14), β-Ala-Leu-Ala-Leu (SEQ ID NO: 15), Gly-Phe-Leu-Gly (SEQ ID NO: 16), Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala, D-Ala-D-Ala, Ala-Met или Met-Ala.
7. Конъюгат по п. 6, отличающийся тем, что P1 представляет собой Gly-Gly-Gly, Ala-Val, Ala-Ala, Ala-D-Ala, D-Ala-Ala или D-Ala-D-Ala.
8. Конъюгат по любому из пп. 1-7, отличающийся тем, что двойная линия  между N и С представляет собой двойную связь.
между N и С представляет собой двойную связь.
9. Конъюгат по любому из пп. 1-7, отличающийся тем, что двойная линия  между N и С представляет собой одинарную связь, X1 представляет собой -Н; Y1 представляет собой -SO3M, где М представляет собой Н+, Na+ или K+.
между N и С представляет собой одинарную связь, X1 представляет собой -Н; Y1 представляет собой -SO3M, где М представляет собой Н+, Na+ или K+.
10. Конъюгат по п. 1, отличающийся тем, что D представлен следующей структурной формулой:

11. Конъюгат по п. 1, отличающийся тем, что данный конъюгат представлен следующей структурной формулой:

или его фармацевтически приемлемая соль, где Ab представляет собой антитело.
12. Конъюгат по любому из пп. 1-11, отличающийся тем, что w равен 2.
13. Соединение, представленное следующей структурной формулой:
D-L-JCB,
или его фармацевтически приемлемая соль, где:
D представлен следующей структурной формулой:
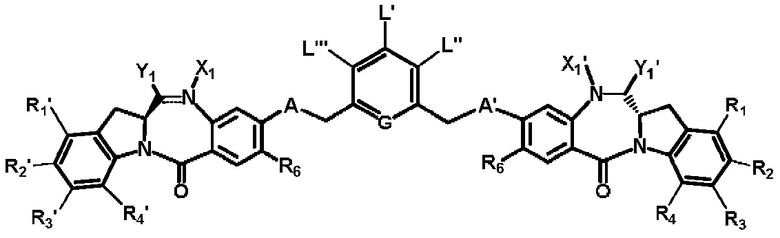 ,
,
или его фармацевтически приемлемая соль, где:
L'' и L''' представляют собой Н и L' представлен следующей формулой:

где:
каждый из Ra и Rb, для каждого случая, независимо представляет собой -Н, (С1-С3)алкил или группу Q, которая представляет собой -SO3H или ее фармацевтически приемлемую соль;
s представляет собой целое число от 1 до 6;
P1 представляет собой пептид, содержащий от 2 до 10 аминокислотных остатков;
R5 представляет собой Н или линейный или разветвленный алкил, содержащий от 1 до 10 атомов углерода;
G представляет собой -СН-;
двойная линия  между N и С представляет собой одинарную или двойную связь при условии, что, если она представляет собой двойную связь, X1 отсутствует и Y1 представляет собой Н; а когда она представляет собой одинарную связь, X1 представляет собой -Н и Y1 представляет собой -ОН или -SO3M;
между N и С представляет собой одинарную или двойную связь при условии, что, если она представляет собой двойную связь, X1 отсутствует и Y1 представляет собой Н; а когда она представляет собой одинарную связь, X1 представляет собой -Н и Y1 представляет собой -ОН или -SO3M;
R1, R2, R3, R4, R1', R2', R3' и R4' все представляют собой -Н;
R6 представляет собой -ОМе;
X1' и Y1' оба представляют собой -Н;
А и А' представляют собой -О-; и
М представляет собой Н+, Na+ или K+;
-L- представлен следующей структурной формулой:

где:
s3 представляет собой место ковалентной связи с JCB', а s4 представляет собой место ковалентной связи с D;
R23 и R24 независимо представляют собой Н;
m' представляет собой целое число от 1 до 6;
Rh' представляет собой Н; и
JCB представляет собой  .
.
14. Соединение по п. 13, отличающееся тем, что оба Ra и Rb представляют собой Н и R5 представляет собой Н или Me.
15. Соединение по п. 13 или 14, отличающееся тем, что P1 представляет собой пептид, содержащий от 2 до 5 аминокислотных остатков.
16. Соединение по п. 13 или 14, отличающееся тем, что P1 выбран из Gly-Gly-Gly, Ala-Val, Val-Ala, Val-Cit, Val-Lys, Phe-Lys, Lys-Lys, Ala-Lys, Phe-Cit, Leu-Cit, Ile-Cit, Trp, Cit, Phe-Ala, Phe-N9-тозил-Arg, Phe-N9-нитро-Arg, Phe-Phe-Lys, D-Phe-Phe-Lys, Gly-Phe-Lys, Leu-Ala-Leu, Ile-Ala-Leu, Val-Ala-Val, Ala-Leu-Ala-Leu (SEQ ID NO: 14), β-Ala-Leu-Ala-Leu (SEQ ID NO: 15), Gly-Phe-Leu-Gly (SEQ ID NO: 16), Val-Arg, Arg-Val, Arg-Arg, Val-D-Cit, Val-D-Lys, Val-D-Arg, D-Val-Cit, D-Val-Lys, D-Val-Arg, D-Val-D-Cit, D-Val-D-Lys, D-Val-D-Arg, D-Arg-D-Arg, Ala-Ala, Ala-D-Ala, D-Ala-Ala, D-Ala-D-Ala, Ala-Met и Met-Ala.
17. Соединение по п. 16, отличающееся тем, что P1 представляет собой Gly-Gly-Gly, Ala-Val, Ala-Ala, Ala-D-Ala, D-Ala-Ala и D-Ala-D-Ala.
18. Соединение по любому из пп. 13-17, отличающееся тем, что двойная линия  между N и С представляет собой двойную связь.
между N и С представляет собой двойную связь.
19. Соединение по любому из пп. 13-17, отличающееся тем, что двойная линия  между N и С представляет собой одинарную связь, X1 представляет собой -Н и Y1 представляет собой -SO3M.
между N и С представляет собой одинарную связь, X1 представляет собой -Н и Y1 представляет собой -SO3M.
20. Соединение по п. 13, отличающееся тем, что D представлен следующей структурной формулой:
 или
или
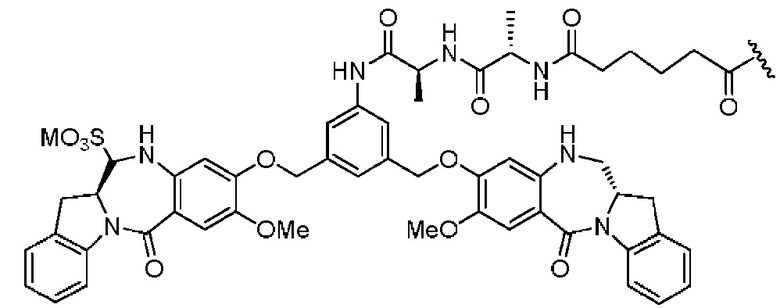
21. Соединение по любому из пп. 13-20, отличающееся тем, что -L-JCB представлен следующей структурной формулой:

22. Соединение по п. 13, отличающееся тем, что данное соединение представлено следующей структурной формулой:
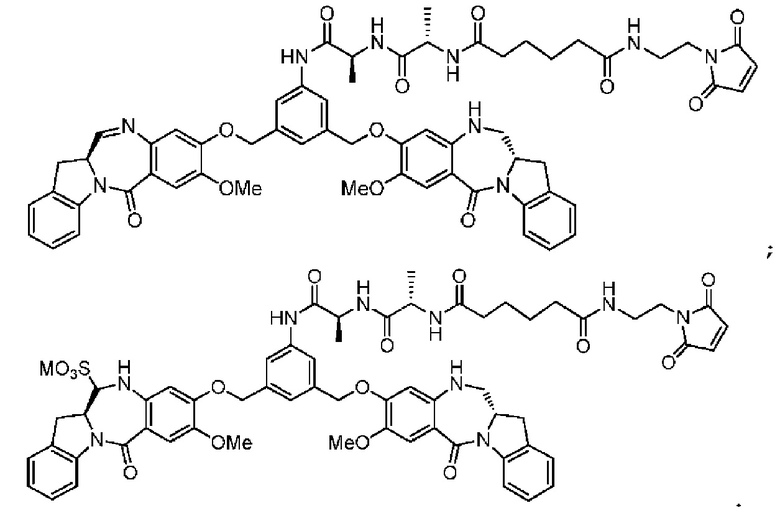
23. Фармацевтическая композиция для лечения рака, содержащая терапевтически эффективное количество конъюгата по любому из пп. 1-12 и фармацевтически приемлемый носитель.
24. Способ лечения рака у млекопитающего, включающий введение указанному млекопитающему терапевтически эффективного количества конъюгата по любому из пп. 1-12.
25. Способ по п. 24, отличающийся тем, что рак представляет собой гемобластоз или солидную опухоль.
26. Способ по п. 25, отличающийся тем, что гемобластоз представляет собой лейкоз или лимфому.
27. Способ по п. 25, отличающийся тем, что солидная опухоль представляет собой меланому, рак легких, немелкоклеточный рак легкого, рак яичников, рак эндометрия, рак брюшины, рак поджелудочной железы, рак молочной железы, рак предстательной железы или рак шейки матки.
28. Способ по п. 26, отличающийся тем, что гемобластоз представляет собой острый миелоидный лейкоз (ОМЛ), острый лимфобластный лейкоз (ОЛЛ), острый В-клеточный лимфобластный лейкоз (В-ОЛЛ), хронический миелоидный лейкоз (ХМЛ) или хронический лимфоцитарный лейкоз (ХЛЛ).
29. Применение конъюгата по любому из пп. 1-12 для лечения рака.
30. Применение по п. 29, отличающееся тем, что рак представляет собой гемобластоз или солидную опухоль.
31. Применение по п. 30, отличающееся тем, что гемобластоз представляет собой лейкоз или лимфому.
32. Применение по п. 31, отличающееся тем, что гемобластоз представляет собой острый миелоидный лейкоз (ОМЛ), острый лимфобластный лейкоз (ОЛЛ), острый В-клеточный лимфобластный лейкоз (В-ОЛЛ), хронический миелоидный лейкоз (ХМЛ) или хронический лимфоцитарный лейкоз (ХЛЛ).
33. Применение по п. 30, отличающееся тем, что солидная опухоль представляет собой меланому, рак легких, немелкоклеточный рак легкого, рак яичников, рак эндометрия, рак брюшины, рак поджелудочной железы, рак молочной железы, рак предстательной железы или рак шейки матки.
| WO 1996014339 A1, 17.05.1996 | |||
| RU 2013141829 A, 27.03.2015 | |||
| RU 2011136686 A, 20.03.2013 | |||
| Stimmel, J | |||
| B | |||
| et al | |||
| "Site-specific Conjugation on Serine → Cysteine Variant Monoclonal Antibodies | |||
| Journal of Biological Chemistry", 2000, 275(39), 30445-30450 | |||
| RU 2017101662 A, 23.07.2018. |
Авторы
Даты
2020-10-06—Публикация
2016-06-28—Подача