Настоящее изобретение относится к фармацевтической композиции, содержащей ПТГ соединение, где после подкожного введения фармакокинетический профиль ПТГ соединения проявляет соотношение пика и минимума менее 4 в течение одного интервала инъекции.
Гипопаратиреоидизм является редким эндокринным нарушением метаболизма кальция и фосфата, которое чаще всего возникает в результате повреждения или удаления паращитовидной железы во время операции на щитовидной железе. Гипопаратиреоидизм отличается от эндокринных расстройств тем, что до недавнего времени его не лечили замещением отсутствующего гормона, паратиреоидного гормона или ПТГ. Традиционная терапия гипопаратиреоидизма включает большие дозы витамина D и пероральные добавки кальция, которые, хотя часто и эффективны, связаны с заметными колебаниями в крови Ca2+, приводящими к гиперкальциемии и гипокальциемии, избыточному выделению кальция с мочой и нефрокальцинозу.
Кальций является наиболее распространенным минералом в организме человека, и его жесткая регуляция необходима для многих важных биологических функций, таких как, например, минерализация костей, сокращение мышц, нервная проводимость, выделение гормонов и свертывание крови. Особенно важно поддерживать концентрацию кальция настолько стабильной, насколько это возможно, из-за высокой чувствительности различных клеточных систем или органов, включая центральную нервную систему, мышцы и экзо/эндокринных желез, к небольшим изменениям в Ca2+. ПТГ является основным регулятором гомеостаза кальция.
Неадекватно низкий уровень ПТГ по отношению к концентрации Ca2+ в сыворотке, характерный для гипопаратиреоидизма, приводит к уменьшенной почечной канальцевой реабсорбции Ca2+ и одновременно к увеличенной почечной канальцевой реабсорбции фосфата. Таким образом, основными биохимическими нарушениями гипопаратиреоидизма являются гипокальциемия и гиперфосфатемия. Клинические признаки заболевания включают симптомы гипокальциемии, например, периоральное онемение, парестезия и мышечные спазмы запястья / стопы. Горловой спазм, тетания и судороги являются серьезными и потенциально опасными для жизни осложнениями. Гиперфосфатемия и повышенный кальций-фосфатный продукт способствуют эктопическому отложению нерастворимых комплексов фосфата кальция в мягких тканях, включая сосудистую сеть, мозг, почки и другие органы.
Стандартной терапией гипопаратиреоидизма является пероральное введение добавк кальция и витамина D. Целями терапии являются: а) улучшение симптомов гипокальциемии; b) поддержание уровня кальция в сыворотке крови натощак в пределах или немного ниже нормы; с) поддержание уровня фосфора в сыворотке натощак в пределах нормального диапазона или только слегка повышенным; d) избегать или минимизировать гиперкальциурию; е) поддерживать содержание фосфатно-кальциевого продукта на уровне значительно ниже верхнего предела нормы; f) избегать эктопической кальцификации почек (камни и нефрокальциноз) и других мягких тканей.
Несколько проблем возникает при длительном применении кальция и активного витамина D в больших дозах, особенно в отношении гиперкальциурии, камней в почках, нефрокальциноза и эктопической кальцификации мягких тканей. Кроме того, традиционная терапия кальцием и активным витамином D не уменьшает жалоб на качество жизни и не устраняет аномалии ремоделирования костной ткани, характерные для этого заболевания. Кратко, существует высокая потребность в улучшенных методах лечения гипопаратиреоидизма.
В 2015, Natpara, ПТГ(1-84) был одобрен для подкожных инъекций один раз в день ежедневно в качестве дополнения к витамину D и кальцию у пациентов с гипопаратиреоидизмом. Natpara, ПТГ (1-84), был одобрен для контроля гипокальциемии на основе основного исследования, продемонстрировавшего, что 42 процента участников, принимавших ПТГ (1-84), достигли нормальных уровней кальция в крови при сниженных дозах добавок кальция и активных форм витамина D, по сравнению с 3 процентами участников, получавших плацебо. После периода времени, в течение которого после инъекции контролировался уровень сывороточного кальция, у 71 процента пациентов, получавших ПТГ (1-84), развивалась гиперкальциемия при одном или более измерениях в течение 24-часового периода. ПТГ (1-84) снижал экскрецию кальция с мочой через 2-8 часов после инъекции, но в течение 24-часового периода экскреция кальция с мочой не изменялась. Точно так же экскреция фосфата с мочой увеличивалась только в течение первых 8 часов после инъекции ПТГ (1-84).
Хотя это представляет собой важный прогресс в лечении этого заболевания, Natpara не продемонстрировал способность снижать частоту случаев гиперкальциемии (повышенный уровень кальция в сыворотке крови), гипокальциемии (низкий уровень кальция в сыворотке крови) или гиперкальциурии (повышенный уровень кальция в моче) по сравнению с традиционной терапией у подлежащих лечению пациентов.
Таким образом, существует высокая потребность в улучшенных методах лечения гипопаратиреоидизма на основе ПТГ.
ПТГ (1-34), или терипаратид, был одобрен FDA в 2002 году для лечения остеопороза. Несмотря на то, что он не был одобрен для этого показания, ПТГ (1-34) исторически использовался для лечения гипопаратиреоидизма у пациентов, получавших инъекции дважды или трижды в день. Чтобы способствовать более физиологическим уровням ПТГ, были проведены клинические исследования с ПТГ (1-34), вводимым с помощью насосной системы упаковки, по сравнению с инъекциями дважды в день. Через 6 месяцев доставка с помощью насосной системы упаковки обеспечила нормальный, стабильный уровень кальция с минимальными колебаниями и предотвратила повышение уровня кальция в сыворотке и моче, которое проявляется вскоре после инъекции ПТГ. Заметное снижение экскреции кальция с мочой, когда ПТГ (1-34) вводится с помощью насосной системы упаковки, может указывать на то, что ПТГ должен постоянно подвергаться почечным канальцам для эффекта хранения кальция в почках. Доставка с помощью насосной системы упаковки ПТГ (1-34) позволила одновременно нормализовать маркеры костного ремоделирования, сывороточный кальций и экскрецию кальция с мочой. Эти результаты были достигнуты при более низкой суточной дозе ПТГ (1-34) и сниженной потребности в добавках магния по сравнению с режимом инъекции ПТГ (1-34) дважды в день.
Однако непрерывная помповая терапия неудобна и сложна для пациентов, и задачей настоящего изобретения является создание более удобного терапевтического варианта обеспечения непрерывного воздействия ПТГ.
Долгосрочное болюсное введение ПТГ связано с прогрессирующей потерей кортикального слоя кости из-за усиления метаболизма костной ткани. В течение 6 лет наблюдения за пациентами, получавшими ПТГ (1-84) (Rubin, JCEM 2016), маркеры костного ремоделирования оставались более высокими, чем значения до лечения, достигая пика в первые годы после начала ПТГ (1-84) и снижаясь после этого, но оставаясь значительно выше, чем базовые значения к 6 году. Минеральная плотность костной ткани (BMD) согласно двойной рентгеновской абсорбциометрии (DXA) соответствовала известным сайт-специфическим эффектам ПТГ, а именно увеличению поясничного отдела позвоночника в дистальном радиусе 1/3 (радиус i / 3). Наблюдаемое уменьшение в радиусе i / 3 согласуется с известными эффектами периодического ПТГ для увеличения кортикальной пористости и внутрикостной резорбции.
Задача настоящего изобретения состоит в том, чтобы обеспечить способ периодического введения ПТГ с более низким повышением маркеров костного ремоделирования, чем применяемые в настоящее время методы лечения ПТГ. Предпочтительно «периодически» означает с ежедневными интервалами или, альтернативно или более предпочтительно, с недельными интервалами.
В программе доклинического развития как Forteo, ПТГ (1-34), так и Natpara, ПТГ (1-84), дозозависимое увеличение частоты остеосаркомы наблюдалось у крыс, получавших ежедневные инъекции соединения ПТГ. В исследовании Natpara дозирование крыс с высокой дозой было прекращено из-за чрезмерной смертности в этой группе, главным образом от метастатической остеосаркомы.
Таким образом, задача настоящего изобретения состоит в обеспечении периодической заместительной терапии ПТГ, которая обеспечивает контроль симптомов при более низкой вводимой дозе. Предпочтительно «периодически» означает с ежедневными интервалами или, альтернативно или более предпочтительно, с недельными интервалами.
Таким образом, существует потребность в более удобном и безопасном лечении гипопаратиреоидизма с уменьшенными побочными эффектами.
Поэтому задача согласно настоящему изобретению состоит в по меньшей мере частичном преодолении описанных выше недостатков.
Эта задача решается с помощью фармацевтической композиции, содержащей ПТГ соединение, где после введения, предпочтительно подкожного введения, фармакокинетический профиль ПТГ соединения проявляет соотношение пика и минимума менее 4 в течение одного интервала инъекции.
Неожиданно было обнаружено, что такое соединение ПТГ способно обеспечить стабильный профиль ПТГ в плазме, который обеспечивает физиологические уровни кальция в сыворотке и в моче или даже пониженные уровни кальция в моче, сопоставимые с измеренными у здоровых субъектов.
В контексте настоящего изобретения применяемые термины имеют следующие значения.
Как применяется в настоящей заявке термин «интервал инъекции» относится к времени между двумя последовательными введениями фармацевтической композиции согласно настоящему изобретению.
Как применяется в настоящей заявке, термин «стабильное состояние» относится к состоянию, достигаемому после множества постоянных доз, как например, после 3, 4, 5, 6, 7 или более постоянных доз лекарственного средства, вводимого пациенту с постоянными временными интервалами между двумя последовательными введениями, причем это состояние характеризуется тем, что уровни в плазме соединения ПТГ, если соединение ПТГ не высвобождает ПТГ, т.е. представляет собой стабильное соединение ПТГ, или высвобожденного ПТГ, если соединение ПТГ является соединением ПТГ контролируемого высвобождения, в начале и в конце интервала изменяются не более чем на 10%, предпочтительно не более чем на 7,5%, даже более предпочтительно не более чем на 5%, даже более предпочтительно не более чем на 4% и наиболее предпочтительно не более чем на 3%. Термин «начало интервала» относится к моменту времени, в который вводится доза, а термин «конец интервала» относится к моменту времени, в который вводится следующая доза.
Как применяется в настоящей заявке, термин “соотношение пика и минимума” относится к соотношению между самой высокой концентрацией в плазме и самой низкой концентрацией в плазме соединения ПТГ в стационарном состоянии, если соединение ПТГ не высвобождает ПТГ, то есть представляет собой стабильное соединение ПТГ, или высвобожденного ПТГ, если соединение ПТГ является соединением ПТГ контролируемого высвобождением, в течение периода времени между двумя последовательными введениями отличному от человека примату, предпочтительно, предпочтительной яванской макаке. Однако, поскольку существует хорошая корреляция между свободным ПТГ и общим ПТГ (т.е. сумма ПТГ, все еще содержащегося в соединение ПТГ, и высвобожденного ПТГ), то общий ПТГ обеспечивает достаточно хорошее приближение. Период времени между двумя последовательными введениями также называют «интервалом инъекции», «интервалом введения» или «интервалом».
Как применяется в настоящей заявке, термин “ПТГ соединение контролируемого высвобождения” относится к любому соединению, конъюгату, кристаллу или смеси, которая содержит по меньшей мере одну ПТГ молекулу или ПТГ составляющую, и из которой по меньшей мере одна ПТГ молекула или ПТГ составляющая высвобождается с периодом полувысвобождения по меньшей мере 12 часов.
Как применяется в настоящей заявке, термины “период полувысвобождения” и “период полувыведения” относятся ко времени, требуемому в физиологических условиях (то есть, в водном буфере, pH 7.4, 37°C), до тех пор, пока половина всего ПТГ или составляющих ПТГ, соответственно, содержащихся в соединении ПТГ контролируемого высвобождения, не будет высвобождена из указанного соединения ПТГ контролируемого высвобождения.
Как применяется в настоящей заявке, термин “стабильное ПТГ соединение” относится к любому ковалентному конъюгату по меньшей мере одной ПТГ составляющей с другой составляющей, где по меньшей мере одна ПТГ составляющая соединена с указанной другой составляющей через стабильную связь.
Как применяется в настоящей заявке, термин “ПТГ” относится ко всем полипептидам ПТГ, предпочтительно видов млекопитающих, более предпочтительно человека и видов млекопитающих, более предпочтительно человека и видов мышиные, а также их вариантам, аналогам, ортологам, гомологам и производным и фрагментам, которые характеризуются увеличением сывороточного кальция и экскреции фосфора почками, и уменьшением сывороточного фосфора и экскреции кальция почками. Термин “ПТГ” также относится ко всем ПТГ-родственным полипептидам (ПТГrP), как например полипептид согласно SEQ ID NO:121, который связывается с и активирует общий рецептор ПТГ/ПТГrP1. Предпочтительно, термин “ПТГ” относится к полипептиду ПТГ согласно SEQ ID NO:51 а также к его вариантам, гомологам и производным, проявляющим по существу такую же биологическую активность, т.е. увеличивающим сывороточный кальций и экскрецию фосфора почками, и уменьшающим сывороточный фосфор и экскрецию кальция почками.
Предпочтительно, термин “ПТГ” относится к следующим полипептидным последовательностям:
SEQ ID NO:1 (ПТГ 1-84)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKAKSQ
SEQ ID NO:2 (ПТГ 1-83)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKAKS
SEQ ID NO:3 (ПТГ 1-82)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKAK
SEQ ID NO:4 (ПТГ 1-81)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKA
SEQ ID NO:5 (ПТГ 1-80)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTK
SEQ ID NO:6 (ПТГ 1-79)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLT
SEQ ID NO:7 (ПТГ 1-78)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVL
SEQ ID NO:8 (ПТГ 1-77)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNV
SEQ ID NO:9 (ПТГ 1-76)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVN
SEQ ID NO:10 (ПТГ 1-75)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADV
SEQ ID NO:11 (ПТГ 1-74)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKAD
SEQ ID NO:12 (ПТГ 1-73)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKA
SEQ ID NO:13 (ПТГ 1-72)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADK
SEQ ID NO:14 (ПТГ 1-71)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEAD
SEQ ID NO:15 (ПТГ 1-70)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEA
SEQ ID NO:16 (ПТГ 1-69)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGE
SEQ ID NO:17 (ПТГ 1-68)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLG
SEQ ID NO:18 (ПТГ 1-67)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSL
SEQ ID NO:19 (ПТГ 1-66)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKS
SEQ ID NO:20 (ПТГ 1-65)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEK
SEQ ID NO:21 (ПТГ 1-64)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHE
SEQ ID NO:22 (ПТГ 1-63)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESH
SEQ ID NO:23 (ПТГ 1-62)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVES
SEQ ID NO:24 (ПТГ 1-61)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVE
SEQ ID NO:25 (ПТГ 1-60)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLV
SEQ ID NO:26 (ПТГ 1-59)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVL
SEQ ID NO:27 (ПТГ 1-58)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNV
SEQ ID NO:28 (ПТГ 1-57)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDN
SEQ ID NO:29 (ПТГ 1-56)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKED
SEQ ID NO:30 (ПТГ 1-55)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKE
SEQ ID NO:31 (ПТГ 1-54)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKK
SEQ ID NO:32 (ПТГ 1-53)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRK
SEQ ID NO:33 (ПТГ 1-52)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPR
SEQ ID NO:34 (ПТГ 1-51)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRP
SEQ ID NO:35 (ПТГ 1-50)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQR
SEQ ID NO:36 (ПТГ 1-49)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQ
SEQ ID NO:37 (ПТГ 1-48)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGS
SEQ ID NO:38 (ПТГ 1-47)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAG
SEQ ID NO:39 (ПТГ 1-46)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDA
SEQ ID NO:40 (ПТГ 1-45)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRD
SEQ ID NO:41 (ПТГ 1-44)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPR
SEQ ID NO:42 (ПТГ 1-43)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAP
SEQ ID NO:43 (ПТГ 1-42)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLA
SEQ ID NO:44 (ПТГ 1-41)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPL
SEQ ID NO:45 (ПТГ 1-40)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAP
SEQ ID NO:46 (ПТГ 1-39)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGA
SEQ ID NO:47 (ПТГ 1-38)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALG
SEQ ID NO:48 (ПТГ 1-37)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVAL
SEQ ID NO:49 (ПТГ 1-36)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVA
SEQ ID NO:50 (ПТГ 1-35)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFV
SEQ ID NO:51 (ПТГ 1-34)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNF
SEQ ID NO:52 (ПТГ 1-33)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHN
SEQ ID NO:53 (ПТГ 1-32)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVH
SEQ ID NO:54 (ПТГ 1-31)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDV
SEQ ID NO:55 (ПТГ 1-30)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQD
SEQ ID NO:56 (ПТГ 1-29)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQ
SEQ ID NO:57 (ПТГ 1-28)
SVSEIQLMHNLGKHLNSMERVEWLRKKL
SEQ ID NO:58 (ПТГ 1-27)
SVSEIQLMHNLGKHLNSMERVEWLRKK
SEQ ID NO:59 (ПТГ 1-26)
SVSEIQLMHNLGKHLNSMERVEWLRK
SEQ ID NO:60 (ПТГ 1-25)
SVSEIQLMHNLGKHLNSMERVEWLR
SEQ ID NO:61 (амидированный ПТГ 1-84)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKAKSQ; где C-конец амидирован
SEQ ID NO:62 (амидированный ПТГ 1-83)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKAKS; где C-конец амидирован
SEQ ID NO:63 (амидированный ПТГ 1-82)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKAK; где C-конец амидирован
SEQ ID NO:64 (амидированный ПТГ 1-81)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTKA; где C-конец амидирован
SEQ ID NO:65 (амидированный ПТГ 1-80)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLTK; где C-конец амидирован
SEQ ID NO:66 (амидированный ПТГ 1-79)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVLT; где C-конец амидирован
SEQ ID NO:67 (амидированный ПТГ 1-78)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNVL; где C-конец амидирован
SEQ ID NO:68 (амидированный ПТГ 1-77)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVNV; где C-конец амидирован
SEQ ID NO:69 (амидированный ПТГ 1-76)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADVN; где C-конец амидирован
SEQ ID NO:70 (амидированный ПТГ 1-75)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKADV; где C-конец амидирован
SEQ ID NO:71 (амидированный ПТГ 1-74)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKAD; где C-конец амидирован
SEQ ID NO:72 (амидированный ПТГ 1-73)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADKA; где C-конец амидирован
SEQ ID NO:73 (амидированный ПТГ 1-72)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEADK; где C-конец амидирован
SEQ ID NO:74 (амидированный ПТГ 1-71)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEAD; где C-конец амидирован
SEQ ID NO:75 (амидированный ПТГ 1-70)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGEA; где C-конец амидирован
SEQ ID NO:76 (амидированный ПТГ 1-69)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLGE; где C-конец амидирован
SEQ ID NO:77 (амидированный ПТГ 1-68)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSLG; где C-конец амидирован
SEQ ID NO:78 (амидированный ПТГ 1-67)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKSL; где C-конец амидирован
SEQ ID NO:79 (амидированный ПТГ 1-66)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEKS; где C-конец амидирован
SEQ ID NO:80 (амидированный ПТГ 1-65)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHEK; где C-конец амидирован
SEQ ID NO:81 (амидированный ПТГ 1-64)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESHE; где C-конец амидирован
SEQ ID NO:82 (амидированный ПТГ 1-63)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVESH; где C-конец амидирован
SEQ ID NO:83 (амидированный ПТГ 1-62)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVES; где C-конец амидирован
SEQ ID NO:84 (амидированный ПТГ 1-61)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLVE; где C-конец амидирован
SEQ ID NO:85 (амидированный ПТГ 1-60)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVLV; где C-конец амидирован
SEQ ID NO:86 (амидированный ПТГ 1-59)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNVL; где C-конец амидирован
SEQ ID NO:87 (амидированный ПТГ 1-58)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDNV; где C-конец амидирован
SEQ ID NO:88 (амидированный ПТГ 1-57)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKEDN; где C-конец амидирован
SEQ ID NO:89 (амидированный ПТГ 1-56)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKED; где C-конец амидирован
SEQ ID NO:90 (амидированный ПТГ 1-55)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKKE; где C-конец амидирован
SEQ ID NO:91 (амидированный ПТГ 1-54)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRKK; где C-конец амидирован
SEQ ID NO:92 (амидированный ПТГ 1-53)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPRK; где C-конец амидирован
SEQ ID NO:93 (амидированный ПТГ 1-52)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRPR; где C-конец амидирован
SEQ ID NO:94 (амидированный ПТГ 1-51)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQRP; где C-конец амидирован
SEQ ID NO:95 (амидированный ПТГ 1-50)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQR; где C-конец амидирован
SEQ ID NO:96 (амидированный ПТГ 1-49)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGSQ; где C-конец амидирован
SEQ ID NO:97 (амидированный ПТГ 1-48)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAGS; где C-конец амидирован
SEQ ID NO:98 (амидированный ПТГ 1-47)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDAG; где C-конец амидирован
SEQ ID NO:99 (амидированный ПТГ 1-46)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRDA; где C-конец амидирован
SEQ ID NO:100 (амидированный ПТГ 1-45)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPRD; где C-конец амидирован
SEQ ID NO:101 (амидированный ПТГ 1-44)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAPR; где C-конец амидирован
SEQ ID NO:102 (амидированный ПТГ 1-43)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLAP; где C-конец амидирован
SEQ ID NO:103 (амидированный ПТГ 1-42)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPLA; где C-конец амидирован
SEQ ID NO:104 (амидированный ПТГ 1-41)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAPL; где C-конец амидирован
SEQ ID NO:105 (амидированный ПТГ 1-40)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGAP; где C-конец амидирован
SEQ ID NO:106 (амидированный ПТГ 1-39)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALGA; где C-конец амидирован
SEQ ID NO:107 (амидированный ПТГ 1-38)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVALG; где C-конец амидирован
SEQ ID NO:108 (амидированный ПТГ 1-37)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVAL; где C-конец амидирован
SEQ ID NO:109 (амидированный ПТГ 1-36)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFVA; где C-конец амидирован
SEQ ID NO:110 (амидированный ПТГ 1-35)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNFV; где C-конец амидирован
SEQ ID NO:111 (амидированный ПТГ 1-34)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHNF; где C-конец амидирован
SEQ ID NO:112 (амидированный ПТГ 1-33)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVHN; где C-конец амидирован
SEQ ID NO:113 (амидированный ПТГ 1-32)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDVH; где C-конец амидирован
SEQ ID NO:114 (амидированный ПТГ 1-31)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQDV; где C-конец амидирован
SEQ ID NO:115 (амидированный ПТГ 1-30)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQD; где C-конец амидирован
SEQ ID NO:116 (амидированный ПТГ 1-29)
SVSEIQLMHNLGKHLNSMERVEWLRKKLQ; где C-конец амидирован
SEQ ID NO:117 (амидированный ПТГ 1-28)
SVSEIQLMHNLGKHLNSMERVEWLRKKL; где C-конец амидирован
SEQ ID NO:118 (амидированный ПТГ 1-27)
SVSEIQLMHNLGKHLNSMERVEWLRKK; где C-конец амидирован
SEQ ID NO:119 (амидированный ПТГ 1-26)
SVSEIQLMHNLGKHLNSMERVEWLRK; где C-конец амидирован
SEQ ID NO:120 (амидированный ПТГ 1-25)
SVSEIQLMHNLGKHLNSMERVEWLR; где C-конец амидирован
SEQ ID NO:121 (ПТГrP)
AVSEHQLLHDKGKSIQDLRRRFFLHHLIAEIHTAEIRATSEVSPNSKPSPNTKNHPVRFGSDDEGRYLTQETNKVETYKEQPLKTPGKKKKGKPGKRKEQEKKKRRTRSAWLDSGVTGSGLEGDHLSDTSTTSLELDSRRH
Более предпочтительно, термин “ПТГ” относится к последовательности SEQ ID:NO 47, 48, 49, 50, 51, 52, 53, 54, 55, 107, 108, 109, 110, 111, 112, 113, 114 и 115. Даже более предпочтительно, термин “ПТГ” относится к последовательности SEQ ID:NO 50, 51, 52, 110, 111 и 112. В особенно предпочтительном варианте выполнения настоящего изобретения термин “ПТГ” относится к последовательности SEQ ID NO:51.
Как применяется в настоящей заявке, термин “вариант полипептида ПТГ ” относится к полипептиду из того же самого вида, который отличается от ссылочного полипептида ПТГ или ПТГrP. Предпочтительно, таким ссылочным полипептидом является ПТГ полипептидная последовательность SEQ ID NO:51. В общем, различия ограничены таким образом, что аминокислотные последовательности ссылочного полипептида и варианта в общем очень подобны и, во многих областях, идентичны. Предпочтительно, варианты полипептида ПТГ на по меньшей мере 70%, 80%, 90%, или 95% идентичны ссылочному полипептиду ПТГ или ПТГrP, предпочтительно полипептиду ПТГ с SEQ ID NO:51. Под полипептидном, имеющим аминокислотную последовательность на по меньшей мере, например, 95% “идентичную” рассматриваемой аминокислотной последовательности понимается, что аминокислотная последовательность данного полипептида идентична рассматриваемой последовательности, за исключением того, что данная полипептидная последовательность может включать вплоть до пяти аминокислотных изменений на каждые 100 аминокислот рассматриваемой аминокислотной последовательности. Эти замены в ссылочной последовательности могут происходить при амино (N-концевое) или карбокси концевых (C-концевое) положениях ссылочной аминокислотной последовательности или в любом мести между этими концевыми положениями, распределяясь либо по отдельности среди остатков в ссылочной последовательности, либо в виде одной или более соприкасающихся групп в ссылочной последовательности. Рассматриваемая последовательность может быть либо полностью аминокислотной последовательностью ссылочной последовательности, либо любым фрагментом, уточненным как описано в настоящей заявке. Предпочтительно, рассматриваемой последовательностью является последовательность SEQ ID NO:51.
Такие варианты полипептида ПТГ могут быть вариантами, встречающимися в природе, как например встречающиеся в природе аллельные варианты, кодируемые одной из нескольких альтернативных форм ПТГ или ПТГrP, занимающих данный локус на хромосоме или организме, или изоформы, кодируемые встречающимися в природе вариантами сплайсинга, происходящими из одного первичного транскрипта. Альтернативно вариант полипептида ПТГ может быть вариантом, который, как известно, не встречается в природе, и который может быть получен методиками мутагенеза, известными в данной области техники.
В данной области известно, что одна или более аминокислот могут быть удалены с N-конца или С-конца биоактивного полипептида без существенной потери биологической функции. Такие N- и/или С-концевые делеции также охватываются термином вариант полипептида ПТГ.
Специалистам в данной области техники также известно, что некоторые аминокислотные последовательности полипептидов ПТГ или ПТГrP могут быть изменены без значительного влияния структуры или функции полипептида. Такие мутанты включают делеции, вставки, инверсии, повторы и замены, выбранные в соответствии с общими правилами, известными в данной области техники, чтобы иметь небольшой эффект на активность. Например, указания относительно того, как сделать фенотипически молчащие аминокислота замены, приведены в Bowie et al. (1990), Science 247:1306-1310, который полностью включен в настоящее описание посредством ссылки, где авторы указывают, что существуют два основных подхода к изучению толерантности аминокислотной последовательности к изменению.
Термин полипептид ПТГ также охватывает все полипептиды ПТГ и ПТГrP, кодируемые аналогами, ортологами и/или видовыми гомологами ПТГ и ПТГrP. Специалистам в данной области техники также понятно, что аналоги ПТГrP и ПТГrP связываются с активированием общего рецептора ПТГ/ПТГrP1, поэтому термин ПТГ полипептид также охватывает все аналоги ПТГrP. Как применяется в настоящей заявке, термин “ПТГ аналог” относится к ПТГ и ПТГrP различных и не связанных между собой организмов, которые выполняют одни и те же функции в каждом организме, но которые не происходят из родовой структуры, которую имели предки организмов. Вместо этого аналогичные ПТГ и ПТГrP возникали отдельно, а затем эволюционировали для выполнения одних и тех же или подобных функций. Другими словами, аналогичные полипептиды ПТГ и ПТГrP представляют собой полипептиды с совершенно различными аминокислотными последовательностями, но которые имеют одну и ту же биологическую активность, а именно увеличение сывороточного кальция и экскреции фосфора почками, и уменьшение сывороточного фосфора и экскреции кальция почками.
Как применяется в настоящей заявке термин “отртолог ПТГ” относится к ПТГ и ПТГrP двух различных видов, последовательности которых связаны друг с другом через общий гомологичный ПТГ в родоначальном виде, но которые в ходе эволюции стали отличными друг от друга.
Как применяется в настоящей заявке, термин “гомолог ПТГ” относится к ПТГ и ПТГrP различных организмов, которые осуществляют одну и ту же функцию в каждом организме и которые происходят из родоначальной структуры, которую в общем имели предки организмов. Другими словами, гомологичные ПТГ полипептиды представляют собой полипептиды с совершенно подобными аминокислотными последовательностями, которые имеют одну и ту же биологическую активность, а именно увеличение сывороточного кальция и экскреции фосфора почками, и уменьшение сывороточного фосфора и экскреции кальция почками. Предпочтительно, гомологи полипептида ПТГ могут определяться как полипептиды, имеющие идентичность по меньшей мере 40%, 50%, 60%, 70%, 80%, 90% или 95% со ссылочным полипептидом ПТГ или ПТГrP, предпочтительно ПТГ полипептидом с SEQ ID NO:51.
Таким образом, полипептидом ПТГ в соответствии с настоящим изобретением может быть, например: (i) полипептид, в котором по меньшей мере один из аминокислотных остатков имеет в качестве заместителя консервативный или неконсервированный аминокислотный остаток, предпочтительно консервативный аминокислотный остаток, и такой замещенный аминокислотный остаток может или не может быть кодирован генетическим кодом; и/или (ii) полипептид, в котором по меньшей мере один из аминокислотных остатков включает группу заместителя; и/или (iii) полипептид, где полипептид ПТГ слит с другим соединением, как например соединение для увеличения периода полувысвобождения полипептида (например, полиэтилэтенгликоль); и/или (iv) полипептид, в котором дополнительные аминокислоты слиты с полипептидом ПТГ, как например, полипептидная или лидерная или секреторная последовательность области слияния IgG Fc или последовательность, которая используется для очистки вышеуказанной формы полипептида, или последовательность белка-предшественника.
Как применяется в настоящей заявке, термин “фрагмент полипептида ПТГ” относится к любому пептиду, содержащему последовательный промежуток части аминокислотной последовательности ПТГ или ПТГrP полипептида, предпочтительно полипептида последовательности SEQ ID NO:51.
Более конкретно, фрагмент полипептида ПТГ содержит по меньшей мере 6, как например по меньшей мере 8, по меньшей мере 10 или по меньшей мере 17 последовательных аминокислот ПТГ или ПТГrP полипептида, более предпочтительно полипептида последовательности SEQ ID NO:51. Фрагмент полипептида ПТГ может быть дополнительно описан как подвид ПТГ или ПТГrP полипептидов, содержащих по меньшей мере 6 аминокислот, где “по меньшей мере 6” определяется как целое число между 6 и целым числом, обозначающим C-концевую аминокислоту ПТГ или ПТГrP полипептида, предпочтительно полипептида последовательности SEQ ID No:51. Также включены виды фрагментов полипептида ПТГ или ПТГrP из по меньшей мере 6 аминокислот в длину, как описано выше, которые дополнительно уточнены с точки зрения их N-концевых и C- концевых положений. Также термином “фрагмент полипептида ПТГ” охватываются в качестве отдельных видов все фрагменты полипептида ПТГ или ПТГrP из по меньшей мере 6 аминокислот в длину, как описано выше, которые могут быть в частности уточнены их N-концевым и C-концевым положением. То есть, каждая комбинация N-концевого и C-концевого положения, которые составляющая из по меньшей мере 6 последовательных аминокислотных остатков в длину может занимать, на любой данной аминокислотной последовательности ПТГ или ПТГrP полипептида, предпочтительно ПТГ полипептида последовательности SEQ ID:NO51, включена в настоящее изобретение.
Термин “ПТГ” также включает поли(аминокислотные) конъюгаты, которые имеют последовательность, как описано выше, но имеющие основную цепь, содержит как амидные, так и неамидные связи, как например сложноэфирные связи, как например депсипептиды. Депсипептиды представляют собой цепи аминокислотных остатков, в которых основная цепь содержит как амидные (пептидные), так и сложноэфирные связи. Соответственно, термин “боковая цепь”, как применяется в настоящей заявке, относится либо к составляющей, присоединенной к альфа-атому углерода аминокислотной составляющей, если аминокислотная составляющая соединена через аминные связи, как например в полипептидах, либо к любой составляющей, содержащей атом углерода, присоединенной к основной цепи поли(аминокислотного) конъюгата, как например в случае депсипептидов. Предпочтительно, термин “ПТГ” относится к полипептидам, имеющим основную цепь, образованную через амидные (пептидные) связи.
Поскольку термин ПТГ включает вышеописанные варианты, аналоги, ортологи, гомологи, производные и фрагменты ПТГ и ПТГrP, все ссылки на конкретные положения в ссылочной последовательности также включают эквивалентные положения в вариантах, аналогах, ортологах, гомологах, производных и фрагментах ПТГ или ПТГrP составляющей, даже если специально не указано.
Как применяется в настоящей заявке, термин “мицелла” означает агрегат амфифильных молекул, диспергированных в жидком коллоиде. В водном растворе типичная мицелла образует агрегат с гидрофильной частью молекул поверхностно-активного вещества, обращенной к окружающему растворителю, и гидрофобной частью молекулы поверхностно-активного вещества, обращенной внутрь, также называемый «мицеллой нормальной фазы». «Мицеллы Invers» имеют гидрофильную часть, обращенную внутрь, и гидрофобную часть, обращенную к окружающему растворителю.
Как применяется в настоящей заявке, термин “липосома” относится к везикуле, предпочтительно сферической везикуле, имеющей по меньшей мере один липидный бислой. Предпочтительно, липосомы содержат фосфолипиды, даже более предпочтительно фосфатидилхолин. Термин «липосома» относится к различным структурам и размерам, например, к многослойным липосомальным везикулам (MLV), имеющим более одного концентрического липидного бислоя со средним диаметром от 100 до 1000 нм, к небольшие однослойным липосомальным везикулам (SUV), имеющим один липидный бислой и средний диаметр от 25 до 100 нм, к большим однослойным липосомальным везикулам (LUV), имеющим один липидный бислой, и средний диаметр около 1000 мкм, и гигантским однослойным везикулам (GUV), имеющим один липидный бислой и средний диаметр от 1 до 100 мкм. Термин «липосома» также включает эластичные везикулы, такие как, например, трансферосомы и этосомы.
Как применяется в настоящей заявке, термин “аквасома” относится к сферическим наночастицам диаметром от 60 до 300 нм, которые содержат по меньшей мере три слоя самоорганизующейся структуры, а именно твердофазное нанокристаллическое ядро, покрытое олигомерной пленкой, на которой молекулы лекарственного средства адсорбируются с модификацией лекарственного средства или без нее.
Как применяется в настоящей заявке, термин “этосома” относится к липидным везикулам, содержащим фосфолипиды и этанол и/или изопропанол в относительно высокой концентрации и воду, имеющим размер в интервале от десятков нанометров до микрометров.
Как применяется в настоящей заявке, термин “LeciPlex” относится к положительно заряженной везикулярной системе на основе фосфолипидов, которая содержит соевый PC, катионный агент и биосовместимый растворитель, такой как ПЭГ 300, ПЭГ 400, моноэтиловый простой эфир диэтиленгликоля, простой эфир полиэтиленгликоля и тетрагидрофурфурилового спирта или 2-пирролидон или N-метил-2 -пирролидон.
Как применяется в настоящей заявке, термин “ниосома” относится к однослойным или многослойным везикулам, содержащим неионные поверхностно-активные вещества.
Как применяется в настоящей заявке, термин “фармакосома” относится к ультрадисперсным везикулярным, мицеллярным или гексагональным агрегатам из липидов, ковалентно связанных с биологически активными составляющими.
Как применяется в настоящей заявке, термин “прониосома” относится к сухим композициям покрытого поверхностно-активным веществом носителя, который при регидратации и умеренном перемешивании дает ниосомы.
Как применяется в настоящей заявке, термин “полимерсома” относится к искусственной сферической везикуле, содержащей мембрану, образованную из амфифильных синтетических блок-сополимеров, и может необязательно содержать водный раствор в своем ядре. Полимерсома имеет диаметр в интервале от 50 нм до 5 мкм и более. Термин также включает синтосомы, которые представляют собой полимерсомы, сконструированные так, чтобы они содержали каналы, которые позволяют определенным химическим веществам проходить через мембрану в везикулу или из нее.
Как применяется в настоящей заявке, термин “сфингосома” относится к концентрической бислойной везикуле, в котором водный объем полностью окружен мембранным липидным бислоем, в основном состоящим из природного или синтетического сфинголипида.
Как применяется в настоящей заявке, термин «трансферосома» относится к ультрагибким липидным везикулам, содержащим водное ядро, которое образовано из смеси обычных полярных и подходящих липидов, активированных по краям, которые облегчают образование сильно искривленных бислоев, которые делают трансферосому весьма деформируемой.
Как применяется в настоящей заявке, термин “уфасома” относится к везикуле, содержащей ненасыщенные жирные кислоты.
Как применяется в настоящей заявке, термин “полипептид” относится к пептиду, содержащему до и включая 50 аминокислотных мономеров.
Как применяется в настоящей заявке, термин “белок” относится к пептиду из более 50 аминокислотных остатков. Предпочтительно белок содержит самое большее 20000 аминокислотных остатков, как например самое большее 15000 аминокислотных остатков, как например самое большее 10000 аминокислотных остатков, как например самое большее 5000 аминокислотных остатков, как например самое большее 4000 аминокислотных остатков, как например самое большее 3000 аминокислотных остатков, как например самое большее 2000 аминокислотных остатков, как например самое большее 1000 аминокислотных остатков.
Как применяется в настоящей заявке, термин “физиологические состояния” относятся к водному буферу при pH 7.4, 37°C.
Как применяется в настоящей заявке термин “фармацевтическая композиция” относится к композиции, содержащей один или более активных ингредиентов, таких как, например, по меньшей мере одно ПТГ соединение контролируемого высвобождения, и один или более эксципиентов, а также любой продукт, который, прямо или косвенно, является результатом комбинации, комплексообразования или агрегация любых двух или более ингредиентов композиции, или диссоциации одного или более ингредиентов, или других типов реакций или взаимодействий одного или более ингредиентов. Соответственно, фармацевтическая композиция согласно настоящему изобретению охватывает любую композицию, полученную путем смешивания одного или более ПТГ соединений контролируемого высвобождения и фармацевтически приемлемого эксципиента.
Как применяется в настоящей заявке термин “жидкая композиция” относится к смеси, содержащей растворимое в воде ПТГ соединение, предпочтительно растворимое в воде ПТГ соединение контролируемого высвобождения, и один или более растворителей, как например воду.
Термин “композиция в виде суспензии” относится к смеси, содержащей нерастворимое в воде ПТГ соединение, предпочтительно нерастворимое в воде ПТГ соединение контролируемого высвобождения, и один или более растворителей, как например воду.
Как применяется в настоящей заявке, термин “сухая композиция” означает, что фармацевтическая композиция обеспечивается в сухой форме. Подходящими способами сушки является распылительная сушка и лиофилизация, т.е. сушка замораживанием. Такая сухая композиция пролекарства имеет остаточное содержание воды, равное максимум 10 %, предпочтительно менее 5% и более предпочтительно менее 2%, как определено по методу Карла Фишера. Предпочтительно, фармацевтическая композиция согласно настоящему изобретению высушивается посредством лиофилизации.
Термин “лекарственное средство”, как применяется в настоящей заявке, относится к веществу, такому как ПТГ, применяемому для лечения, облегчения, профилактики или диагностике заболевания или, в противном случае, для улучшения физического или умственного здоровья. Если лекарственное средство конъюгирована с другой составляющей, составляющая полученного продукта, которая происходит из лекарственного средства, обозначается как “биологически активная составляющая”.
Как применяется в настоящей заявке термин “пролекарство” относится к конъюгату, содержащему биологически активную составляющую, обратимо и ковалентно соединенную со специализированной защитной группой через обратимую линкерную составляющую, также упоминаемую как “обратимая линкерная составляющая пролекарства”, которая содержит обратимую связь с биологически активной составляющей, и где специализированная защитная группа изменяет или уменьшает нежелательные свойства в родоначальной молекуле. Это также включает усиления желательных свойств лекарственного средства и подавление нежелательных свойств. Специализированная нетоксичная защитная группа обозначается как “носитель”. Пролекарство высвобождает обратимо и ковалентно связанную биологически активную составляющую в форме соответствующего ей лекарственного средства. Другими словами, пролекарство представляет собой конъюгат, содержащий биологически активную составляющую, которая обратимо и ковалентно конъюгирована с составляющей-носителем через обратимую линкерную составляющую пролекарства, где ковалентное или обратимое конъюгирование носителя с обратимой линкерной составляющей пролекарства является либо непосредственным, либо через спейсер. Такой конъюгат высвобождает прежде конъюгированную биологически активную составляющую в форме свободного лекарственного средства.
Как применяется в настоящей заявке, термин “обратимая линкерная составляющая пролекарства представляет собой спейсерную составляющую, которая соединяет биологически активную составляющую, такую как составляющая ПТГ, с составляющей носителя, либо непосредственно, либо через дополнительную спейсерную составляющую, и где связь между обратимой линкерной составляющей пролекарства и биологически активной составляющей является обратимой. Предпочтительно связь между составляющей носителя и обратимой линкерной составляющей пролекарства является стабильной.
Термины “биодеградируемая связь” или “обратимая связь” означает связь, которая является гидролитически разрушаемой, т.е. расщепляемой, в отсутствии ферментов при физиологических условиях (водный буфер при pH 7.4, 37°C) с периодом полувысвобождения в интервале от одного часа до трех месяцев, предпочтительно от одного часа до двух месяцев, даже более предпочтительно от одного часа до одного месяца, даже более предпочтительно от одного часа до трех недель, наиболее предпочтительно от одного часа до двух недель. Соответственно, стабильная связь представляет собой связь, имеющую период полувысвобождения при физиологических условиях (водный буфер при pH 7.4, 37°C), равный более чем три месяца.
Как применяется в настоящей заявке, термин “бесследный линкер пролекарства” означает обратимый линкер пролекарства, т.e. линкерную составляющую, обратимо и ковалентно соединяющую биологически активную составляющую с носителем, который при расщеплении высвобождает лекарственное средство в его свободной форме. Как применяется в настоящей заявке, термин “свободная форма” лекарственного средства означает лекарственное средство в его немодифицированной, фармакологически активной форме.
Как применяется в настоящей заявке, термин "эксципиент" относится к разбавителю, вспомогательному средству или носителю, совместно с которым вводится терапевтическое средство, как например лекарственное средство или пролекарство. Такой фармацевтический эксципиент может представлять собой стерильную жидкость, такую как вода и масла, включая жидкости нефтяного, животного, растительного или синтетического происхождения, включая, но без ограничения к этому, арахисовое масло, соевое масло, минеральное масло, сезамовое масло и тому подобное. Вода является предпочтительным эксципиентом, когда фармацевтическая композиция вводится перорально. Соляной раствор и водный раствор декстрозы являются предпочтительными наполнителями, когда фармацевтическая композиция вводится внутривенно. Соляные растворы и водные растворы декстрозы и глицерина предпочтительно применяются в качестве жидких эксципиентов для инъецируемых растворов. Подходящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, маннит, трегалозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, глицерин моностеарат, тальк, хлорид натрия, сухое молоко, глицерин, пропиленгликоль, воду, этанол и тому подобное. Композиция при желании может содержать также небольшие количества увлажняющих или эмульгирующих средств, рН-буферных средств, таких как, например, ацетат, сукцинат, трис, карбонат, фосфат, HEPES (4-(2-гидроксиэтил)-1-пиперазинэтансульфокислота, MES (2-(N-морфолин)этансульфокислота) или может содержать детергенты, такие как Tween, полоксамеры, полоксамины, CHAPS, Igepal, или аминокислоты, такие как, например, глицин, лизин или гистидин. Такие фармацевтические композиции могут иметь форму растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, препаратов с замедленным высвобождением и тому подобное. Фармацевтическая композиция может иметь вид суппозитория, с традиционными связующими средствами и эксципиентами, такими как триглицериды. Препарат для перорального введения может содержать стандартные эксципиенты, такие как фармацевтические марки маннита, лактозы, крахмала, стеарата магния, сахарина натрия, целлюлозы, карбоната магния и т.д. Такие композиции содержат терапевтически эффективное количество лекарственного средства или биологически активной составляющей, вместе с подходящим количеством эксципиента, так чтобы получилась форма, подходящая для введения пациенту. Композиция должна соответствовать способу введения.
Как применяется в настоящей заявке, термин “реагент” означает химическое соединение, которое содержит по меньшей мере одну функциональную группу для реакции с функциональной группой другого химического соединения или лекарственного средства. Понятно, что лекарственное средство, содержащее функциональную группу (как например первичный или вторичный амин или гидроксильная функциональная группа) также представляет собой реагент.
Как применяется в настоящей заявке, термин “составляющая” означает часть молекулы, в которой отсутствует один или более атомов по сравнению с соответствующим реагентов. Если, например, реагент формулы “H-X-H” реагирует с другим реагентом и становится частью продукта реакции, соответствующая составляющая продукта реакции имеет структуру “H-X-“ или “-X- “, где каждый “-“обозначает присоединение к другой составляющей. Соответственно, биологически активная составляющая высвобождается из пролекарства в качестве лекарственного средства.
Понятно, что если обеспечивается последовательность или химическая структура группы атомов, где группа атомов присоединяется к двум составляющим или прерывает составляющую, указанная последовательность или структура может быть присоединена к двум составляющим в любой ориентации, если иного не указано. Например, составляющая “-C(O)N(R1)-“ может быть присоединена к двум составляющим или прерывать составляющую либо как “-C(O)N(R1)-“, либо как “-N(R1)C(O)-“. Подобным образом, составляющая

может быть присоединена к двум составляющим или может прерывать составляющую либо как  , либо как
, либо как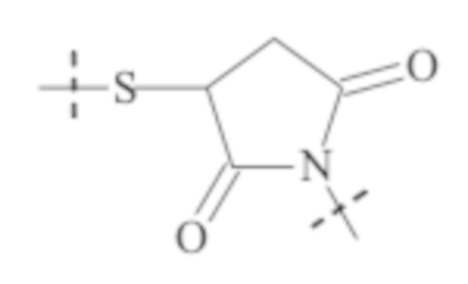 .
.
Как применяется в настоящей заявке, термин “функциональная группа” означает группу атомов, которая может реагировать с другими группами атомов. Функциональные группы включают, но без ограничения к этому, следующие группы: карбоновая кислота (-(C=O)OH), первичный и вторичный амин (-NH2, -NH-), малеимид, тиол (-SH), сульфоновая кислота (-(O=S=O)OH), карбонат, карбамат (-O(C=O)N<), гидроксил (-OH), альдегид (-(C=O)H), кетон (-(C=O)-), гидразин (>N-N<), изоцианат, изотиоцианат, фосфорная кислота (-O(P=O)OHOH), фосфоновая кислота (-O(P=O)OHH), галоацетил, алкилгалогенид, акрилоил, арилфторид, гидроксиламин, дисульфид, сульфонамиды, серная кислота, винилсульфон, винилкетон, диазоалкан, оксиран и азиридин.
В случае, если ПТГ соединение, предпочтительно ПТГ соединение контролируемого высвобождения, согласно настоящему изобретению содержат одну или более кислотных или основных групп, настоящее изобретение включает также их соответствующие фармацевтически или токсикологически приемлемые соли, в частности их фармацевтически применимые соли. Таким образом, ПТГ соединение, предпочтительно ПТГ соединение контролируемого высвобождения, согласно настоящему изобретению, содержащие кислотные группы, могут применяться по настоящему изобретению, например, в виде солей щелочных металлов, солей щелочноземельных металлов или аммониевых солей. Более конкретные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния или соли аммония или с органическими аминами, такими как, например, этиламин, этаноламин, триэтаноламин или аминокислоты. ПТГ соединение, предпочтительно ПТГ соединение контролируемого высвобождения, согласно настоящему изобретению, содержащие одну или более основных групп, т.е. групп, которые могут быть протонированы, могут присутствовать и использоваться согласно настоящему изобретению в форме их аддитивных солей с неорганическими или органическими кислотами. Примеры подходящих кислот включают хлорид водорода, бромид водорода, фосфорную кислоту, серную кислоту, азотную кислоту, метансульфокислоту, п-толуолсульфокислоту, нафталинсульфокислоту, щавелевую кислоту, уксусную кислоту, винную кислоту, молочную кислоту, салициловую кислоту, бензойную кислоту, муравьиную кислоту, пропионовую кислоту, пивалоиловую кислоту, диэтилуксусную кислоту, малоновую кислоту, янтарную кислоту, пимелиновую кислоту, фумаровую кислоту, малеиновую кислоту, яблочную кислоту, сульфаминовую кислоту, фенилпропионовую кислоту, глюконовую кислоту, аскорбиновую кислоту, изоникотиновую кислоту, лимонную кислоту, адипиновую кислоту и другие кислоты, известные квалифицированным специалистам в данной области. Специалистам в данной области техники известно превращение основной группы в катион, такие как алкилирование аминной группы с получением положительно заряженной аммониевой группы и соответствующего противоиона соли. Если ПТГ соединение, предпочтительно ПТГ соединение контролируемого высвобождения, согласно настоящему изобретению одновременно содержат кислотные и основные группы, настоящее изобретение также включает, в дополнение к упомянутым солевым формам, внутренние соли или бетаины (цвиттерионы). Соответствующие соли могут быть получены обычными методами, известными квалифицированным специалистам в данной области, например путем контакта этих соединений с органической или неорганической кислотой или основанием в растворителе или диспергирующем средстве, или путем анионного обмена или катионного обмена с другими солями. Настоящее изобретение также включает все соли соединений согласно настоящему изобретению, которые, вследствие низкой физиологической совместимости не пригодны непосредственно для применения в фармацевтических продуктах, но которые могут использоваться, например, как промежуточные соединения для химических реакций или для получения фармацевтически приемлемых солей.
Термин "фармацевтически приемлемый" означает вещество, которое не наносит вред при введении пациенту и предпочтительно одобрено надзорным органом, таким как ЕМЕА (Европа) и/или FDA (США) и/или любым другим национальным надзорным органом для применения в отношении животных, предпочтительно человека.
Как применяется в настоящей заявке термин “около” в комбинации с числовым значением применяется для указания на диапазон в интервале и включая числовое значение плюс и минус не более 10% от указанного числового значения, более предпочтительно не более 8% от указанного значения, даже более предпочтительно не более 5% от указанного значения и наиболее предпочтительно не более 2% от указанного значения. Например, фраза “около 200” применяется для обозначения диапазона в интервале и включая 200 +/- 10%, т.е. в интервале и включая 180 - 220; предпочтительно 200 +/- 8%, т.е. в интервале и включая 184 - 216; даже более предпочтительно в интервале и включая 200 +/-5%, т.е. в интервале и включая 190 - 210; и наиболее предпочтительно 200 +/- 2%, т.е. в интервале и включая 196 - 204. Понятно, что процент, приведенный как “около 20%” не означает “20% +/- 10%”, т.е. в интервале и включая 10 - 30%, но “около 20%” означает в интервале и включая 18 - 22%, т.е. плюс и минус 10% от числового значения, которое равно 20.
Как применяется в настоящей заявке, термин «полимер» означает молекулу, содержащую повторяющиеся структурные единицы, т.е. мономеры, связанные химическими связями линейным, кольцевым, разветвленным, сшитым или дендримерным образом или их комбинацией, которая может быть синтетического или биологического происхождения или комбинацией обоих. Понятно, что полимер может также содержать одну или более других химических групп и/или составляющих, таких как, например, одна или более функциональные группы. Предпочтительно, растворимый полимер имеет молекулярную массу, равную по меньшей мере 0.5 кДа, например, молекулярную массу, равную по меньшей мере 1 кДа, молекулярную массу, равную по меньшей мере 2 кДа, молекулярную массу, равную по меньшей мере 3 кДа, или молекулярную массу, равную по меньшей мере 5 кДа. Если полимер является растворимым, он предпочтительно имеет молекулярную массу, равную самое большее 1000 кДа, как например самое большее 750 кДа, как например самое большее 500 кДа, как например самое большее 300 кДа, как например самое большее 200 кДа, как например самое большее 100 кДа. Понятно, что для нерастворимых полимеров, как например гидрогели, нет значимых диапазонов молекулярной массы. Понятно также, что белок представляет собой полимер, в котором аминокислоты являются повторяющимися структурными звеньями, даже не смотря на то, что боковые цепи каждой аминокислоты могут быть различными.
Как применяется в настоящей заявке, термин “полимерный” означает реагент или составляющую, содержащую один или более полимеров или полимерных составляющих. Полимерный реагент или составляющая может необязательно также содержать одну или более других составляющих, которые предпочтительно выбирают из группы, состоящей из:
C1-50 алкила, C2-50 алкенила, C2-50 алкинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, фенила, нафтила, инденила, инданила и тетралинила; и
связей, выбранных из группы, содержащей
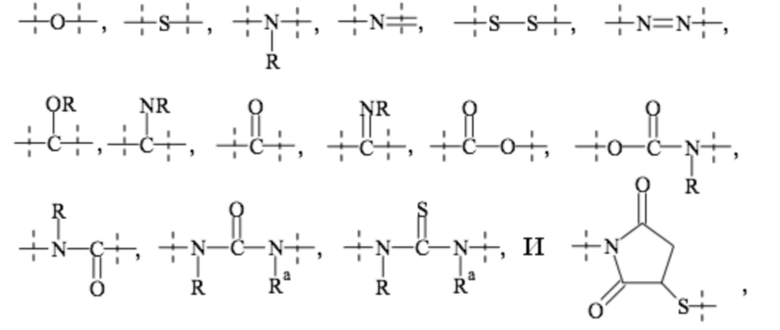
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента, и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -H, метила, этила, пропила, бутила, пентила и гексила.
Специалист в данной области понимает, что продукты полимеризации, полученные из реакции полимеризации, не все имеют одинаковую молекулярную массу, а скорее имеют молекулярно-массовое распределение. Следовательно, диапазоны молекулярных масс, молекулярные массы, диапазоны количества мономеров в полимере и количества мономеров в полимере, как применяется в настоящей заявке, относятся к среднечисловой молекулярной массе и среднему числу мономеров, т.е. к среднему арифметическому молекулярной массы полимера или полимерного фрагмента и среднему арифметическому числа мономеров полимера или полимерного фрагмента.
Соответственно, в полимерной составляющей, содержащей “x” мономерных единиц, любое целое число, приведенное для “x”, поэтому соответствует арифметическому среднему числу мономеров. Любой диапазон целых чисел, приведенный для “x”, обеспечивает диапазон целых чисел, в котором лежит арифметическое среднее число мономеров. Целое число для “x”, приведенное как “около x”, означает, что арифметические средние числа мономеров лежат в диапазоне целых чисел x +/- 10%, предпочтительно x +/- 8%, более предпочтительно x +/- 5% и наиболее предпочтительно x +/- 2%.
Как применяется в настоящей заявке, термин “среднечисловая молекулярная масса” означает обычное среднее арифметическое молекулярных масс отдельных полимеров.
Как применяется в настоящей заявке, термин “растворимый в воде” со ссылкой на носитель означает, что когда такой носитель является частью ПТГ соединения, предпочтительно ПТГ соединения контролируемого высвобождения, согласно настоящему изобретению по меньшей мере 1 г ПТГ соединения, предпочтительно ПТГ соединения контролируемого высвобождения, содержащего такой растворимый в воде носитель, может быть растворено в одном литре воды при 20°C с образованием гомогенного раствора. Соответственно, термин “нерастворимый в воде” со ссылкой на носитель означает, что когда такой носитель является частью ПТГ соединения, предпочтительно ПТГ соединения контролируемого высвобождения, согласно настоящему изобретению менее 1 г ПТГ соединения, предпочтительно ПТГ соединения контролируемого высвобождения, содержащего такой растворимый в воде носитель, может быть растворено в одном литре воды при 20°C с образованием гомогенного раствора.
Как применяется в настоящей заявке, термин “растворимый в воде” со ссылкой на ПТГ соединение означает, что по меньшей мере 1 г ПТГ соединения может быть растворено в одном литре воды при 20°C с образованием гомогенного раствора. Соответственно, термин “нерастворимый в воде” со ссылкой на ПТГ соединение означает, что менее 1 г ПТГ соединения может быть растворено в одном литре воды при 20°C с образованием гомогенного раствора.
Как применяется в настоящей заявке, термин “гидрогель” означает гидрофильную или амфифильную полимерную сеть, состоящую из гомополимеров или coполимеров, которая является не растворимой из-за присутствия ковалентных химических поперечных связей. Поперечные связи образуют структуру сети и физическую целостность.
Как применяется в настоящей заявке термин «термогелевое» означает соединение, которое представляет собой жидкость или раствор с низкой вязкостью, имеющий вязкость менее 500 сПз при 25°C при скорости сдвига около 0,1/с при низкой температуре, причем низкая температура находится в интервале от около 0°C до около 10°C, но которое представляет собой соединение с более высокой вязкостью менее 10000 сПз при 25°C со скоростью сдвига около 0,1/с при более высокой температуре, причем более высокая температура находится в интервале от около 30°C до около 40°C, например, при температуре около 37°C.
Как применяется в настоящей заявке, термин “на основе ПЭГ” в отношении составляющей или реагента означает, что указанная составляющая или реагент содержит ПЭГ. Предпочтительно, составляющая или реагент на основе ПЭГ содержит по меньшей мере 10% (мас./мас.) ПЭГ, как например по меньшей мере 20% (мас./мас.) ПЭГ, как например по меньшей мере 30% (мас./мас.) ПЭГ, как например по меньшей мере 40% (мас./мас.) ПЭГ, как например по меньшей мере 50% (мас./мас.), как например по меньшей мере 60 (мас./мас.) ПЭГ, как например по меньшей мере 70% (мас./мас.) ПЭГ, как например по меньшей мере 80% (мас./мас.) ПЭГ, как например по меньшей мере 90% (мас./мас.) ПЭГ, как например по меньшей мере 95%. Оставшиеся массовые проценты составляющей или реагента на основе ПЭГ составляют другие составляющие, предпочтительно выбранные из следующих составляющих и связей:
C1-50 алкил, C2-50 алкенил, C2-50 алкинил, C3-10 циклоалкил, 3-10-ти членный гетероциклил, 8-11-ти членный гетеробициклил, фенил, нафтил, инденил, инданил и тетралинил; и
связей, выбранных из группы, содержащей

где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента, и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -H, метила, этила, пропила, бутила, пентила и гексила.
Как применяется в настоящей заявке, термин “на основе ПЭГ, содержащий по меньшей мере X% ПЭГ” в отношении составляющей или реагента означает, что указанная составляющая или реагент содержит по меньшей мере X% (мас./мас.) единиц этиленгликоля (-CH2CH2O-), где единицы этиленгликоля могут быть расположены блочным, чередующимся образом или могут быть расположены случайным образом в составляющей или реагента, и предпочтительно все единицы этиленгликоля указанной составляющей или реагента присутствуют в одном блоке; оставшиеся массовые проценты составляющей или реагента на основе ПЭГ составляют другие составляющие, предпочтительно выбранные из следующих составляющих и связей:
C1-50 алкил, C2-50 алкенил, C2-50 алкинил, C3-10 циклоалкил, 3-10-ти членный гетероциклил, 8-11-ти членный гетеробициклил, фенил, нафтил, инденил, инданил и тетралинил; и
связей, выбранных из группы, содержащей
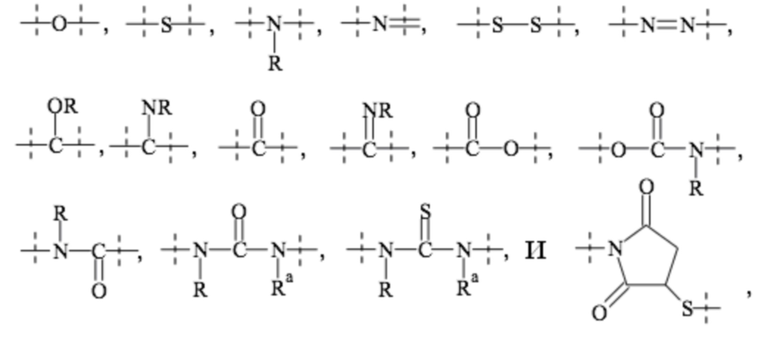
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента, и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -H, метила, этила, пропила, бутила, пентила и гексила.
Термин “на основе гиалуроновой кислоты, содержащая по меньшей мере X% гиалуроновая кислота” применяется соответствующим образом.
Термин “спейсерная составляющая”, как применяется в настоящей заявке, относится к любой составляющей, которая является подходящей для соединения двух других составляющих. Предпочтительно, спейсер выбран из группы, состоящей из -T-, C1-50 алкил, C2-50 алкенила, и C2-50 алкинила; где -T-, C1-50 алкил, C2-50 алкенил, и C2-50 алкинил необязательно замещены одним или более -Ry2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил, и C2-50 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)-, и -OC(O)N(Ry3)-;
каждый T независимо выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, 8-30-ти членного карбополициклила, и 8-30-ти членного гетерополициклила; где каждый T независимо необязательно замещен одним или более -Ry2, которые являются одинаковыми или различными;
каждый -Ry2 независимо выбран из группы, состоящей из галогена, -CN, оксо (=O), -COORy5, -ORy5, -C(O)Ry5, -C(O)N(Ry5Ry5a), -S(O)2N(Ry5Ry5a), -S(O)N(Ry5Ry5a), -S(O)2Ry5, -S(O)Ry5, -N(Ry5)S(O)2N(Ry5aRy5b), -SRy5, -N(Ry5Ry5a), -NO2, -OC(O)Ry5, N(Ry5)C(O)Ry5a, N(Ry5)S(O)2Ry5a, N(Ry5)S(O)Ry5a, N(Ry5)C(O)ORy5a, N(Ry5)C(O)N(Ry5aRy5b), OC(O)N(Ry5Ry5a), и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо выбран из группы, состоящей из H, и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными.
Термин “замещенный”, как применяется в настоящей заявке, означает, что один или более атомов водорода молекулы или составляющей замещены другим атомом или группой атомов, которые обозначаются как “заместитель”.
Предпочтительно, одни или более дополнительные необязательные заместители независимо друг от друга выбирают из группы, состоящей из галогена, -CN, -COORx1, -ORx1, -C(O)Rx1, -C(O)N(Rx1Rx1a), -S(O)2N(Rx1Rx1a), -S(O)N(Rx1Rx1a), -S(O)2Rx1, -S(O)Rx1, -N(Rx1)S(O)2N(Rx1aRx1b), -SRx1, -N(Rx1Rx1a), -NO2, -OC(O)Rx1, -N(Rx1)C(O)Rx1a, -N(Rx1)S(O)2Rx1a, -N(Rx1)S(O)Rx1a, -N(Rx1)C(O)ORx1a, -N(Rx1)C(O)N(Rx1aRx1b), -OC(O)N(Rx1Rx1a), -T0, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T0, C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более -Rx2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T0-, -C(O)O-, -O-, -C(O)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-, -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
-Rx1, -Rx1a, -Rx1b независимо друг от друга выбирают из группы, состоящей из -H, -T0, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T0, C1-50 алкил, C2-50 алкенил, и C2-50 алкинил необязательно замещены одним или более заместителями -Rx2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -T0-, -C(O)O-, -O-, -C(O)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-; -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
каждый T0 независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила и 8-11-ти членного гетеробициклила; где каждый T0 независимо необязательно замещен одним или более заместителями -Rx2, которые являются одинаковыми или различными;
каждый -Rx2 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COORx4, -ORx4, -C(O)Rx4, -C(O)N(Rx4Rx4a), -S(O)2N(Rx4Rx4a), -S(O)N(Rx4Rx4a), -S(O)2Rx4, -S(O)Rx4, -N(Rx4)S(O)2N(Rx4aRx4b), -SRx4, -N(Rx4Rx4a), -NO2, -OC(O)Rx4, -N(Rx4)C(O)Rx4a, -N(Rx4)S(O)2Rx4a, -N(Rx4)S(O)Rx4a, -N(Rx4)C(O)ORx4a, -N(Rx4)C(O)N(Rx4aRx4b), -OC(O)N(Rx4Rx4a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -Rx3, -Rx3a, -Rx4, -Rx4a, -Rx4b независимо выбирают из группы, состоящей из -H и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными.
Более предпочтительно, один или более дополнительных необязательных заместителей независимо друг от друга выбраны из группы, состоящей из галогена, -CN, -COORx1, -ORx1, -C(O)Rx1, -C(O)N(Rx1Rx1a), -S(O)2N(Rx1Rx1a), -S(O)N(Rx1Rx1a), -S(O)2Rx1, -S(O)Rx1, -N(Rx1)S(O)2N(Rx1aRx1b), -SRx1, -N(Rx1Rx1a), -NO2, -OC(O)Rx1, -N(Rx1)C(O)Rx1a, -N(Rx1)S(O)2Rx1a, -N(Rx1)S(O)Rx1a, -N(Rx1)C(O)ORx1a, -N(Rx1)C(O)N(Rx1aRx1b), -OC(O)N(Rx1Rx1a), -T0, C1-10 алкила, C2-10 алкенила и C2-10 алкинила; где -T0, C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно замещены одним или более -Rx2, которые являются одинаковыми или различными, и где C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T0-, -C(O)O-, -O-, -C(O)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-, -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-, -S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)- и -OC(O)N(Rx3)-;
каждый -Rx1, -Rx1a, -Rx1b, -Rx3, -Rx3a независимо выбран из группы, состоящей из H, галогена, C1-6 алкила, C2-6 алкенила и C2-6 алкинила;
каждый T0 независимо выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, и 8- 11-ти членного гетеробициклила; где каждый T0 независимо необязательно замещен одним или более -Rx2, которые являются одинаковыми или различными;
каждый -Rx2 независимо выбран из группы, состоящей из галогена, -CN, оксо (=O), -COORx4, -ORx4, -C(O)Rx4, -C(O)N(Rx4Rx4a), -S(O)2N(Rx4Rx4a), -S(O)N(Rx4Rx4a), -S(O)2Rx4, -S(O)Rx4, -N(Rx4)S(O)2N(Rx4aRx4b), -SRx4, -N(Rx4Rx4a), -NO2, -OC(O)Rx4, -N(Rx4)C(O)Rx4a, -N(Rx4)S(O)2Rx4a, -N(Rx4)S(O)Rx4a, -N(Rx4)C(O)ORx4a, -N(Rx4)C(O)N(Rx4aRx4b), -OC(O)N(Rx4Rx4a), и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными;
каждый -Rx4, -Rx4a, -Rx4b независимо выбран из группы, состоящей из H, галогена, C1-6 алкила, C2-6 алкенила и C2-6 алкинила;
Даже более предпочтительно, один или более дополнительных необязательных заместителей независимо друг от друга выбраны из группы, состоящей из галогена, -CN, -COORx1, -ORx1, -C(O)Rx1, -C(O)N(Rx1Rx1a), -S(O)2N(Rx1Rx1a), -S(O)N(Rx1Rx1a), -S(O)2Rx1, -S(O)Rx1, -N(Rx1)S(O)2N(Rx1aRx1b), -SRx1, -N(Rx1Rx1a), -NO2, -OC(O)Rx1, -N(Rx1)C(O)Rx1a, -N(Rx1)S(O)2Rx1a, -N(Rx1)S(O)Rx1a, -N(Rx1)C(O)ORx1a, -N(Rx1)C(O)N(Rx1aRx1b), -OC(O)N(Rx1Rx1a), -T0, C1-6 алкила, C2-6 алкенила и C2-6 алкинила; где -T0, C1-6 алкил, C2-6 алкенил и C2-6 алкинил необязательно замещены одним или более -Rx2, которые являются одинаковыми или различными, и где C1-6 алкил, C2-6 алкенил и C2-6 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T0-, -C(O)O-, -O-, -C(O)-, -C(O)N(Rx3)-, -S(O)2N(Rx3)-, -S(O)N(Rx3)-, -S(O)2-, -S(O)-, -N(Rx3)S(O)2N(Rx3a)-,-S-, -N(Rx3)-, -OC(ORx3)(Rx3a)-, -N(Rx3)C(O)N(Rx3a)-, и -OC(O)N(Rx3)-;
каждый -Rx1, -Rx1a, -Rx1b, -Rx2, -Rx3, -Rx3a независимо выбран из группы, состоящей из H, галогена, C1-6 алкила, C2-6 алкенила и C2-6 алкинила;
каждый T0 независимо выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, и 8-11-ти членного гетеробициклила; где каждый T0 независимо необязательно замещен одним или более -Rx2, которые являются одинаковыми или различными.
Предпочтительно, максимум 6 -H атомов необязательно замещенной молекулы независимо замещены заместителем, например, 5 -H атомов независимо замещены заместителем, 4 -H атома независимо замещены заместителем, 3 -H атома независимо замещены заместителем, 2 -H атома независимо замещены заместителем, или 1 -H атом замещен заместителем.
Термин “прерванный” означает, что фрагмент вставлен между двумя атомами углерода или - если вставка находится на одном из концов составляющей - между атомом углерода или гетероатомом и атомом водорода, предпочтительно между атомом углерода и атомом водорода.
Как применяется в настоящей заявке, термин “C1-4 алкил” сам по себе или в комбинации означает неразветвленную или разветвленную алкильную составляющую, имеющую от 1 до 4 атомов углерода. Если присутствует на конце молекулы, примерами неразветвленного или разветвленного C1-4 алкила являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор.-бутил и трет.-бутил. Когда две составляющие молекулы связаны C1-4 алкилом, примерами таких C1-4 алкильных групп являются -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-. Каждый водород C1-4 алкильного углерода может необязательно быть замещен заместителем, как определено выше. Необязательно, C1-4 алкил может быть прерван одной или более составляющими, как определено далее.
Как применяется в настоящей заявке, термин “C1-6 алкил” сам по себе или в комбинации означает неразветвленную или разветвленную алкильную составляющую, имеющую от 1 до 6 атомов углерода. Если присутствует на конце молекулы, примерами неразветвленных или разветвленных C1-6 алкильных групп являются метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор.-бутил, трет-бутил, н-пентил, 2-метилбутил, 2,2-диметилпропил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил, 2,3-диметилбутил и 3,3-диметилпропил. Когда две составляющие молекулы связаны C1-6 алкильной группой, примерами таких C1-6 алкильных групп являются -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)- и C(CH3)2-. Каждый атом водорода при C1-6 атоме углерода может необязательно быть замещен заместителем, как определено выше. Необязательно, C1-6 алкил может быть прерван одной или более составляющими, как определено далее.
Соответственно, “C1-10 алкил”, “C1-20 алкил” или “C1-50 алкил” означает алкильную цепь, имеющую от 1 до 10, от 1 до 20 или от 1 до 50 атомов углерода, соответственно, где каждый атом водорода при C1-10, C1-20 или C1-50 атоме углерода может необязательно быть замещен заместителем, как определено выше. Необязательно, C1-10 или C1-50 алкил может быть прерван одной или более составляющими, как определено далее.
Как применяется в настоящей заявке, термин “C2-6 алкенил” сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну двойную связь углерод-углерод, имеющую от 2 до 6 атомов углерода. Если присутствует на конце молекулы, примерами являются CH=CH2, -CH=CH-CH3, -CH2-CH=CH2, -CH=CHCH2-CH3 и -CH=CH-CH=CH2. Когда две составляющие молекулы связаны C2-6 алкенильной группой, тогда примером такого C2-6 алкенила является -CH=CH-. Каждый атом водорода C2-6 алкенильной составляющей может необязательно быть замещен заместителем, как определено выше. Необязательно, C2-6 алкенил может быть прерван одной или более составляющими, как определено далее.
Соответственно, термин “C2-10 алкенил”, “C2-20 алкенил” или “C2-50 алкенил” сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну двойную связь углерод-углерод, имеющую от 2 до 10, от 2 до 20 или от 2 до 50 атомов углерода. Каждый атом водорода C2-10 алкенильной, C2-20 алкенильной или C2-50 алкенильной группы может необязательно быть замещен заместителем, как определено выше. Необязательно, C2-10 алкенил, C2-20 алкенил или C2-50 алкенил может быть прерван одной или более составляющими, как определено далее.
Как применяется в настоящей заявке, термин “C2-6 алкинил” сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну тройную связь углерод-углерод, имеющую от 2 до 6 атомов углерода. Если присутствует на конце молекулы, примерами являются -C≡CН, -CH2-C≡СH, CH2-CH2-C≡CH и CH2-C≡C-CH3. Когда две составляющие молекулы связаны алкинильной группой, тогда примером является -C≡C-. Каждый атом водорода C2-6 алкинильной группы может необязательно быть замещен заместителем, как определено выше. Необязательно, могут присутствовать одна или более двойных связей. Необязательно, C2-6 алкинил может быть прерван одной или более составляющими, как определено далее.
Соответственно, как применяется в настоящей заявке, термин “C2-10 алкинил”, “C2-20 алкинил” и “C2-50 алкинил” сам по себе или в комбинации означает неразветвленную или разветвленную углеводородную составляющую, содержащую по меньшей мере одну тройную связь углерод-углерод, имеющую от 2 до 10, от 2 до 20 или от 2 до 50 атомов углерода, соответственно. Каждый атом водорода C2-10 алкинильной, C2-20 алкинильной или C2-50 алкинильной группы может необязательно быть замещен заместителем, как определено выше. Необязательно, могут присутствовать одна или более двойных связей. Необязательно, C2-10 алкинил, C2-20 алкинил или C2-50 алкинил может быть прерван одной или более составляющими, как определено далее.
Как упомянуто выше, C1-4 алкил, C1-6 алкил, C1-10 алкил, C1-20 алкил, C1-50 алкил, C2-6 алкенил, C2-10 алкенил, C2-20 алкенил, C2-50 алкенил, C2-6 алкинил, C2-10 алкинил, C2-20 алкенил или C2-50 алкинил может необязательно быть прерван одной или более составляющими, которые предпочтительно выбирают из группы, состоящей из
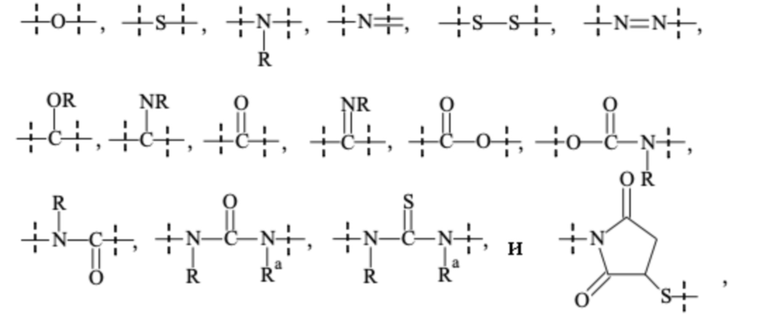
где
пунктирные линии обозначают присоединение к оставшейся части составляющей или реагента,; и
-R и Ra независимо друг от друга выбирают из группы, состоящей из -H, метила, этила, пропила, бутила, пентила и гексила.
Как применяется в настоящей заявке, термин "C3-10 циклоалкил" означает циклическую алкильную цепь, имеющую от 3 до 10 атомов углерода, которая может быть насыщенной или ненасыщенной, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил, циклооктил, циклононил или циклодецил. Каждый атом водорода C3-10 циклоалкильного углерода может быть замещен заместителем, как определено выше. Термин "C3-10 циклоалкил" также включает мостиковые бициклы, такие как норборнан или норборнен.
Термин “8-30-членный карбополициклил” или “8-30-ти членный карбополицикл” означает циклическую составляющую из двух или более колец с 8 - 30 кольцевыми атомами, где два соседних кольца разделяют по мере один кольцевой атом, и которая может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным). Предпочтительно 8-30-членный карбополициклил означает циклическую составляющую из двух, трех, четырех или пяти колец, более предпочтительно двух, трех или четырех колец.
Как применяется в настоящей заявке, термин "3-10-ти членный гетероциклил" или "3-10-ти членный гетероцикл" означает кольцо с 3, 4, 5, 6, 7, 8, 9 или 10 кольцевыми атомами, которое может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным), где по меньшей мере от одного кольцевого атома до четырех кольцевых атомов замещены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остатком молекулы через атом углерода или азота. Примеры 3-10-ти членных гетероциклов включают, но без ограничения к этому, азиридин, оксиран, тиран, азирин, оксирен, тиирен, азетидин, оксетан, тиетан, фуран, тиофен, пиррол, пирролин, имидазол, имидазолин, пиразол, пиразолин, оксазол, оксазолин, изоксазол, изоксазолин, тиазол, тиазолин, изотиазол, изотиазолин, тиадиазол, тиадиазолин, тетрагидрофуран, тетрагидротиофен, пирролидин, имидазолидин, пиразолидин, оксазолидин, изоксазолидин, тиазолидин, изотиазолидин, тиадиазолидин, сульфолан, пиран, дигидропиран, тетрагидропиран, имидазолидин, пиридин, пиридазин, пиразин, пиримидин, пиперазин, пиперидин, морфолин, тетразол, триазол, триазолидин, тетразолидин, диазепан, азепин или гомопиперазин. Каждый атом водорода 3-10-ти членного гетероциклила или 3-10-ти членной гетероциклической группы может быть замещен заместителем, как определено далее.
Как применяется в настоящей заявке, термин "8-11-ти членный гетеробициклил" или "8-11-ти членный гетеробицикл" означает гетероциклическую составляющую из двух колец с 8 - 11 кольцевыми атомами, где по меньшей мере один кольцевой атом разделен между двумя кольцами, и которая содержит до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным), где по меньшей мере от одного кольцевого атома до шести кольцевых атомов замещены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остатком молекулы через атом углерода или азота. Примерами 8-11-ти членного гетеробицикла являются индол, индолин, бензофуран, бензотиофен, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензимидазол, бензимидазолин, хинолин, хиназолин, дигидрохиназолин, хинолин, дигидрохинолин, тетрагидрохинолин, декагидрохинолин, изохинолин, декагидроизохинолин, тетрагидроизохинолин, дигидроизохинолин, бензазепин, пурин или птеридин. Термин 8-11-ти членный гетеробицикл также включает спиро-структуры из двух циклов, такие как 1,4-диокса-8-азаспиро[4.5]декан или мостиковые гетероциклы, такие как 8-аза-бицикло[3.2.1]октан. Каждый атом водорода 8-11-ти членного гетеробициклила или 8-11-ти членного гетеробицикла может быть замещен заместителем, как определено далее.
Подобным образом, термин “8-30-ти членный гетерополициклил” или “8-30-членный гетерополицикл” означает гетероциклическую составляющую из более чем двух колец с 8 - 30 кольцевыми атомами, предпочтительно тремя, четырьмя или пятью кольцами, где два соседних кольца разделяют по мере один кольцевой атом, и которая может содержать до максимального числа двойных связей (ароматическое или неароматическое кольцо, которое является полностью насыщенным, частично ненасыщенным или ненасыщенным), где по меньшей мере от одного кольцевого атома до 10 кольцевых атомов замещены гетероатомом, выбранным из группы, состоящей из серы (включая -S(O)-, -S(O)2-), кислорода и азота (включая =N(O)-), и где кольцо связано с остатком молекулы через атом углерода или азота.
Понятно, что фраза “пара Rx/Ry, соединяется вместе с атомом, к которому они присоединены, с образованием C3-10 циклоалкила или 3-10-ти членного гетероциклила” в отношении составляющей структуры
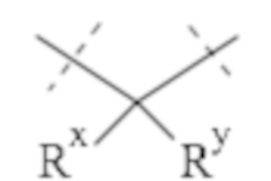
означает, что Rx и Ry образуют следующую структуру:
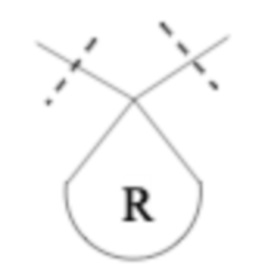 ,
,
где R представляет собой C3-10 циклоалкил или 3-10-ти членный гетероциклил.
Также понятно, что фраза “пара Rx/Ry, соединяется вместе с атомом, к которому они присоединены, с образованием кольца A” в отношении составляющей структуры

означает, что Rx и Ry образуют следующую структуру:
 .
.
Как применяется в настоящей заявке, "галоген" означает фтор, хлор, бром или иод. В общем предпочтительно, что галогеном является фтор или хлор.
В общем, термин “содержит” или “содержащий” также охватывает “состоит из” или “состоящий из”.
Предпочтительно, ПТГ соединение содержит ПТГ молекулу или ПТГ составляющую, имеющую последовательность SEQ ID NO:47, SEQ ID NO:48, SEQ ID NO:49, SEQ ID NO:50, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:55, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, SEQ ID NO:110, SEQ ID NO:111, SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114 или SEQ ID NO:115. Более предпочтительно ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:50, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:110, SEQ ID NO:111 или SEQ ID NO:112.
В одном варианте выполнения настоящего изобретения ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:50.
В другом варианте выполнения настоящего изобретения ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:52.
В другом варианте выполнения настоящего изобретения ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:110.
В другом варианте выполнения настоящего изобретения ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:111.
В другом варианте выполнения настоящего изобретения ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:112.
Наиболее предпочтительно ПТГ молекула или ПТГ составляющая имеет последовательность SEQ ID NO:51.
Введение ПТГ соединения предпочтительно представляет собой подкожное введение. В другом варианте выполнения настоящего изобретения введение ПТГ соединения представляет собой внутривенное введение. В другом предпочтительном варианте выполнения настоящего изобретения введение ПТГ соединения представляет собой внутримышечное введение.
Период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, т.e. интервал введения, составляет предпочтительно по меньшей мере 24 часов, как например 24 часов, 36 часов, 48 часов, 60 часов, 72 часов, каждые 84 часов, 96 часов, 108 часов, 120 часов, 132 часов, 144 часов, 156 часов, одна неделя, две недели, три недели или четыре недели.
В одном варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет 24 часов.
В другом варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет 48 часов.
В другом варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет 72 часов.
В другом варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет 96 часов.
В другом варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет 120 часов.
В другом варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет 144 часов.
В другом варианте выполнения настоящего изобретения период времени между двумя последовательными введениями, предпочтительно между двумя последовательными подкожными введениями, составляет одну неделю.
Соотношение пика и минимума, измеренное для каждого интервала введения, составляет менее 4, предпочтительно менее 3.8, более предпочтительно менее 3.6, даже более предпочтительно менее 3.4, даже более предпочтительно менее 3.2, даже более предпочтительно менее 3, даже более предпочтительно менее 2.8, даже более предпочтительно менее 2.6, даже более предпочтительно менее 2.4, даже более предпочтительно менее 2.2 и наиболее предпочтительно менее 2.
Предпочтительно подкожное введение осуществляют посредством подкожной инъекции. Предпочтительно, указанная подкожная инъекция осуществляется с помощью шприца-ручки.
В одном варианте выполнения настоящего изобретения ПТГ соединение представляет собой стабильное ПТГ соединение.
В одном варианте выполнения настоящего изобретения ПТГ соединение представляет собой стабильное ПТГ соединение, в котором по меньшей мере одна ПТГ составляющая ковалентно конъюгирована через стабильную связь с полимерной составляющей, либо напрямую, либо через спейсерную составляющую.
Предпочтительно, в таких стабильных ПТГ соединениях ПТГ составляющая ковалентно конъюгирована через стабильную связь с растворимой в воде полимерной составляющей, либо напрямую, либо через спейсерную составляющую.
Предпочтительно, такая полимерная составляющая выбрана из группы, состоящей из 2-метакрилоил-оксиэтила фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометилцеллюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
Даже более предпочтительно, полимерная составляющая представляет собой составляющую на основе ПЭГ.
В другом варианте выполнения настоящего изобретения по меньшей мере одна ПТГ составляющая ковалентно конъюгирована через стабильную связь с альбумин-связывающей составляющей. Предпочтительно, указанная альбумин-связывающая составляющая представляет собой C8--24 алкильную составляющую или производную жирной кислоты. Предпочтительными производными жирной кислоты являются те, которые раскрываются в WO 2005/027978 A2 и WO 2014/060512 A1, которые включены в настоящую заявку посредством ссылки.
В другом варианте выполнения настоящего изобретения стабильное ПТГ соединение представляет собой слитый белок, т.e. ПТГ составляющую, стабильно и ковалентно связанную с другой пептидной или белковой составляющей через пептидную связь.
В предпочтительном варианте выполнения настоящего изобретения ПТГ соединение представляет собой ПТГ соединение контролируемого высвобождения.
В одном варианте выполнения настоящего изобретения ПТГ соединение контролируемого высвобождения является нерастворимым в воде.
Предпочтительно, нерастворимое в воде ПТГ соединение контролируемого высвобождения выбрано из группы, состоящей из кристаллов, наночастиц, микрочастиц, наносфер и микросфер.
В одном варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой кристалл, содержащий по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой наночастицу, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой микрочастицу, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой наносферу, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой микросферу, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В одном варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой везикулу, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую. Предпочтительно, такая везикула, содержащая по меньшей мере одну ПТГ молекулу или ПТГ составляющую, представляет собой мицеллу, липосому или полимерсому.
В одном варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой мицеллу, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой липосому, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую. Предпочтительно, такая липосома выбрана из группы, состоящей из аквасом; неионных поверхностно-активных везикул, как например ниосомы и прониосомы; катионные липосомы, такие как LeciPlex; трансферсомы; этосомы; уфасомы; сфингосомы; и фармакосомы.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой полимерсому, содержащую по меньшей мере одну ПТГ молекулу или ПТГ составляющую.
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения содержит по меньшей мере одну ПТГ молекулу, нековалентно внедренную в нерастворимый в воде полимер. Предпочтительно, такой нерастворимый в воде полимер содержит полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтила фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометилцеллюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
В предпочтительном варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения содержит по меньшей мере одну ПТГ молекулу, нековалентно внедренную в поли(сополимер молочных и гликолевых кислот) (PLGA).
В другом варианте выполнения настоящего изобретения нерастворимое в воде ПТГ соединение контролируемого высвобождения содержит по меньшей мере одну ПТГ составляющую, ковалентно и обратимо конъюгированную с нерастворимым в воде полимером. Предпочтительно такой нерастворимый в воде полимер содержит полимер содержит полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтила фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометилцеллюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
В одном варианте выполнения настоящего изобретения такое нерастворимое в воде ПТГ соединение контролируемого высвобождения представляет собой соединение, содержащее конъюгат D-L, где
-D представляет собой ПТГ составляющую; и
-L содержит обратимую линкерную составляющую пролекарства -L1-, где составляющая -L1- соединена с ПТГ составляющей -D через функциональную группу ПТГ;
где -L1- замещена -L2-Z' и необязательно дополнительно замещена; где
-L2- представляет собой простую химическую связь или спейсерную составляющую; и
-Z' представляет собой нерастворимую в воде составляющую носителя.
Понятно, что множество составляющих -L2-L1-D соединено с нерастворимым в воде носителем -Z' , и что такие ПТГ соединения контролируемого высвобождения представляют собой ПТГ пролекарства, более конкретно связанные с носителем ПТГ пролекарства.
Предпочтительные варианты для -D, -L1-, -L2- и -Z' описаны ниже.
В предпочтительном варианте выполнения настоящего изобретения ПТГ соединение контролируемого высвобождения является растворимым в воде.
В предпочтительном варианте выполнения настоящего изобретения такое растворимое в воде ПТГ соединение контролируемого высвобождения представляет собой соединение формулы (Ia) или (Ib) или его фармацевтически приемлемую соль
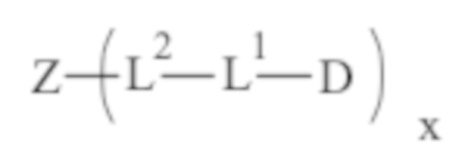 (Ia)
(Ia)
 (Ib),
(Ib),
где
-D представляет собой ПТГ составляющую;
-L1- представляет собой обратимую линкерную составляющую пролекарства, соединенную с ПТГ составляющей -D через функциональную группу ПТГ;
-L2- представляет собой простую химическую связь или спейсерную составляющую;
-Z представляет собой растворимую в воде составляющую носителя;
x представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16; и
y представляет собой целое число, выбранное из группы, состоящей из 1, 2, 3, 4 и 5.
Понятно, что соединения формулы (Ia) и (Ib) представляют собой ПТГ пролекарства, более конкретно растворимые в воде ПТГ пролекарства.
Предпочтительно, -D имеет последовательность SEQ ID NO:47, SEQ ID NO:48, SEQ ID NO:49, SEQ ID NO:50, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:55, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, SEQ ID NO:110, SEQ ID NO:111, SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114 или SEQ ID NO:115. Более предпочтительно -D имеет последовательность SEQ ID NO:50, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:110, SEQ ID NO:111 или SEQ ID NO:112.
В одном варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:50.
В другом варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:52.
В другом варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:110.
В другом варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:111.
В другом варианте выполнения настоящего изобретения -D имеет последовательность SEQ ID NO:112.
Наиболее предпочтительно -D имеет последовательность SEQ ID NO:51.
Составляющая -L1- либо конъюгирована с функциональной группой боковой цепи остатка аминокислоты -D, с N-концевой аминовой функциональной группой или с C-концевой карбоксильной функциональной группой -D, либо с атомом азота основной полипептидной цепи -D. Присоединение либо к N-концу, либо к C-концу может быть либо непосредственно через соответствующую аминовую или карбоксильную функциональную группу, соответственно, либо не напрямую, когда спейсерная составляющая сначала конъюгируется с аминовой или карбоксильной функциональной группой, с которой коъюгирована спейсерная составляющая -L1.
Предпочтительно, аминокислотный остаток ПТГ, с которым -L1- конъюгирована, содержит функциональную группу, выбранную из группы, состоящей из карбоновой кислоты, первичного и вторичного амина, малеимида, тиола, сульфоновой кислоты, карбоната, карбамата, гидроксила, альдегида, кетона, гидразина, изоцианата, изотиоцианата, фосфорной кислоты, фосфоновой кислоты, галоацетила, алкилгалогенида, акрилоила, арилфторида, гидроксиламина, сульфата, дисульфида, винилсульфона, винилкетона, диазоалкана, оксирана, гуанидина и азиридина. Даже более предпочтительно аминокислотный остаток ПТГ, с которым -L1- конъюгирована, содержит функциональную группу, выбранную из группы, состоящей из гидроксила, первичного и вторичного амина и гуанидина. Даже более предпочтительно аминокислотный остаток ПТГ, с которым -L1- конъюгирована, содержит функциональную группу первичного или вторичного амина. Наиболее предпочтительно аминокислотный остаток ПТГ, с которым -L1- конъюгирована, содержит функциональную группу первичного амина.
Если составляющая -L1- конъюгирована с функциональной группой боковой цепи аминокислотного остатка ПТГ указанный аминокислотный остаток выбран из группы, состоящей из протеогенных аминокислотных остатков и непротеогенных аминокислотных остатков.
В одном варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи непротеогенного аминокислотного остатка ПТГ. Понятно, что такая непротеогенная аминокислота не обнаруживается в последовательности природного ПТГ или его фрагментов, и что она может присутствовать только в вариантах и производных ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи остатка протеогенной кислоты в ПТГ. Предпочтительно, указанная аминокислота выбрана из группы, состоящей из состоящей из гистидина, лизина, триптофана, серина, треонина, тирозина, аспарагиновой кислоты, глутаминовой кислоты и аргинина. Даже более предпочтительно указанная аминокислота выбрана из группы, состоящей из состоящей из лизина, аспарагиновой кислоты, аргинина и серина. Даже более предпочтительно указанная аминокислота выбрана из группы, состоящей из состоящей из лизина, аргинина и серина.
В одном варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи гистидина ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи лизина ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи триптофана ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи серина ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи треонина ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи тирозина ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи аспарагиновой кислоты ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи глутаминовой кислоты ПТГ.
В другом варианте выполнения настоящего изобретения -L1- конъюгирована с функциональной группой боковой цепи аргинина ПТГ.
Понятно, что не каждая составляющая ПТГ может содержать все эти аминокислотные остатки.
В предпочтительном варианте выполнения настоящего изобретения -L1- конъюгирована с N-концевой аминовой функциональной группой ПТГ, либо непосредственно через соответствующую аминовую функциональную группу, либо не напрямую, когда спейсерная составляющая сначала конъюгирована с аминовой функциональной группой, с которой конъюгирована спейсерная составляющая -L1-. Даже более предпочтительно, -L1- напрямую конъюгирована с N-концевой аминовой функциональной группой ПТГ.
В равно предпочтительном варианте выполнения настоящего изобретения - -L1- конъюгирована с С-концевой функциональной группой ПТГ либо непосредственно через соответствующую карбоксильную функциональную группу, либо не напрямую, когда спейсерная составляющая сначала конъюгирована с карбоксильной функциональной группой, с которой конъюгирована спейсерная составляющая -L1-.
Наиболее предпочтительно L1- непосредственно конъюгировна с N-концевой аминовой функциональной группой ПТГ.
Составляющая -L1- может быть соединена с -D через любой тип связи, при условии, что она является обратимой. Предпочтительно, -L1- соединена с -D через связь, выбранную из группы, состоящей из амида, сложного эфира, карбамата, ацеталя, аминаля, имина, оксима, гидразона, дисульфида и ацилгуанидина. Даже более предпочтительно -L1- соединена с -D через связь, выбранную из группы, состоящей из амида, сложного эфира, карбамата и ацилгуанидина. Понятно, что некоторые из этих связей сами по себе не являются обратимыми, но в настоящем изобретении соседние группы, содержащиеся в L1, делают эти связи обратимыми.
В одном варианте выполнения настоящего изобретения -L1- соединена с -D через простоэфирную связь.
В другом варианте выполнения настоящего изобретения -L1- соединена с -D через карбаматную связь.
В другом варианте выполнения настоящего изобретения -L1- соединена с -D через ацилгуанидиновую связь.
В предпочтительном варианте выполнения настоящего изобретения-L1- соединена с -D через амидную связь.
Составляющая -L1- представляет собой обратимый линкер пролекарства, из которого лекарственное средство, т.е. ПТГ, высвобождается в его свободной форме, т.е. представляет собой бесследный линкер пролекарства. Подходящие пролекарственные линкеры известны в данной области техники, как например обратимые линкерные составляющие пролекарства, раскрываются в WO 2005/099768 A2, WO 2006/136586 A2, WO 2011/089216 A1 и WO 2013/024053 A1, которые включены в настоящую заявку посредством ссылки.
В другом варианте выполнения настоящего изобретения -L1- представляет собой обратимый пролекарственный линкер, как описано в WO 2011/012722 A1, WO 2011/089214 A1, WO 2011/089215 A1, WO 2013/024052 A1 и WO 2013/160340 A1, которые включены в настоящую заявку посредством ссылки.
Особенно предпочтительная составляющая -L1- раскрывается в WO 2009/095479 A2. Соответственно, в предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (II):
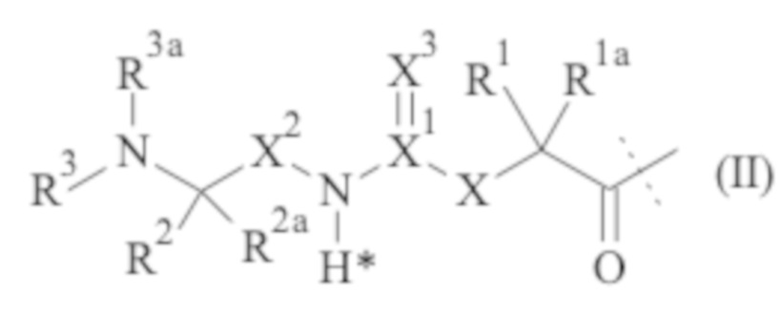 ,
,
где пунктирная линия обозначает присоединение к атому азота, гидроксилу или тиолу составляющей -D, которая представляет собой ПТГ составляющую;
-X- выбран из группы, состоящей из -C(R4R4a)-; -N(R4)-; -O-; -C(R4R4a)-C(R5R5a)-; -C(R5R5a)-C(R4R4a)-; -C(R4R4a)-N(R6)-; -N(R6)-C(R4R4a)-; -C(R4R4a)-O-; -O-C(R4R4a)-; и -C(R7R7a)-;
X1 выбран из группы, состоящей из C; и S(O);
-X2- выбран из группы, состоящей из -C(R8R8a)-; и-C(R8R8a)-C(R9R9a)-;
=X3 выбран из группы, состоящей из =O; =S; и =N-CN;
-R1, -R1a, -R2, -R2a, -R4, -R4a, -R5, -R5a, -R6, -R8, -R8a, -R9, и -R9a независимо выбраны из группы, состоящей из -H; и C1-6 алкила;
-R3, и -R3a независимо выбраны из группы, состоящей из -H; и C1-6 алкила, при условии, что в случае, если один из -R3, -R3a или оба отличны от водорода, они соединены с N, к которому они присоединены через SP3-гибридизованный атом углерода;
-R7 выбран из группы, состоящей из-N(R10R10a); и -NR10-(C=O)-R11;
-R7a, -R10, -R10a, и -R11 независимо друг от друга выбраны из группы, состоящей из -H; и C1-6 алкила;
необязательно, одна или более из пар -R1a/-R4a, -R1a/-R5a, -R1a/-R7a, -R4a/-R5a, и -R8a/-R9a образуют химическую связь;
необязательно, одна или более из пар -R1/-R1a, -R2/-R2a, -R4/-R4a, -R5/-R5a, -R8/-R8a,
и -R9/-R9a соединяются вместе с атомом, к которому они присоединены, с образованием C3-10 циклоалкила; или 3-10-ти членного гетероциклила;
необязательно, одна или более из пар -R1/-R4, -R1/-R5, -R1/-R6, -R1/-R7a, -R4/-R5, -R4/-R6, -R8/-R9, и -R2/-R3 соединяются вместе с атомами, к которым они присоединены, с образованием кольца A;
необязательно, R3/R3a соединяются вместе с атомом азота, к которому они присоединены, с образованием 3-10-ти членного гетероцикла;
A выбирают из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; C3-10 циклоалкила; 3-10-ти членного гетероциклила; и 8-11-ти членного гетеробициклила; и
где -L1- имеет в качестве заместителя -L2-Z или -L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (II), не замещен -L2-Z или -L2-Z' или заместителем;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Предпочтительно -L1- формулы (II) имеет в качестве заместителя одну составляющую -L2-Z или -L2-Z'.
В одном варианте выполнения настоящего изобретения -L1- формулы (II) дополнительно не замещена.
Понятно, что если -R3/-R3a формулы (II) соединяются вместе с атомом азота, к которому они присоединены, с образованием 3-10-ти членного гетероцикла, только такие 3-10-ти членные гетероциклы могут быть образованы, в которых атомы, непосредственно соединенные с атомом азота, представляют собой SP3-гибридизованные атомы углерода. Другими словами, такой 3-10-ти членный гетероцикл, образованный -R3/-R3a вместе с атомом азота, с которыми они соединены, имеет следующую структуру:
 ,
,
где
пунктирная линия обозначает присоединение к остатку -L1-;
кольцо содержит от 3 до 10 атомов, включая по меньшей мере один атом азота; и
R# и R## представляют собой SP3-гибридизованный атом углерода.
Также понятно, что 3-10-ти членный гетероцикл может быть дополнительно замещен.
Примерными вариантами выполнения подходящих 3-10-ти членных гетероциклов, образованных -R3/-R3a формулы (II) вместе с атомом азота, к которому они присоединены, являются следующие:

где
пунктирная линия обозначает присоединение к остатку молекулы; и
-R выбирают из группы, состоящей из -H и C1-6 алкила.
-L1- формулы (II) может необязательно быть дополнительно замещенной. В общем, любой заместитель может применяться, до тех пор, пока принцип расщепления не затронут, т.е. водород, помеченный звездочкой в формуле (II), не заменен, а азот составляющей

формулы (II) остается частью первичного, вторичного или третичного амина, т.е. -R3 и R3a независимо друг от друга представляют собой -H или соединены с -N< через SP3-гибридизованный атом углерода.
В одном варианте выполнения настоящего изобретения -R1 или R1a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R2 или R2a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R3 или R3a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R4 формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R5 или R5a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R6 формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R7 или R7a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R8 или R8a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R9 или R9a формулы (II) имеет в качестве заместителя -L2-Z или L2-Z'. В другом варианте выполнения настоящего изобретения -R10 имеет в качестве заместителя -L2-Z или -L2-Z'. В другом варианте выполнения настоящего изобретения -R11 имеет в качестве заместителя -L2-Z или -L2-Z'. Предпочтительно, -R3 формулы (II) имеет в качестве заместителя -L2-Z или -L2-Z'.
Предпочтительно, -X- формулы (II) выбран из группы, состоящей из -C(R4R4a)-, -N(R4)- и -C(R7R7a)-.
В одном варианте выполнения настоящего изобретения -X- формулы (II) представляет собой -C(R4R4a)-.
В одном предпочтительном варианте выполнения настоящего изобретения- X - формулы (II) представляет собой -C(R7R7a)-.
Предпочтительно, -R7 формулы (II) представляет собой -NR10-(C=O)-R11.
Предпочтительно, -R7a формулы (II) выбран из H, метила и этила. Наиболее предпочтительно -R7a формулы (II) представляет собой -H.
Предпочтительно, -R10 выбран из H, метила и этила. Наиболее предпочтительно -R10 представляет собой метил.
Предпочтительно, -R11 выбран из H, метила и этила. Наиболее предпочтительно -R11 представляет собой -H.
Предпочтительно, -R11 замещен -L2-Z или -L2-Z'.
В другом предпочтительном варианте выполнения настоящего изобретения -X- формулы (II) представляет собой -N(R4)-.
Предпочтительно, -R4 выбран из группы, состоящей из H, метила и этила. Предпочтительно, -R4 представляет собой -H.
Предпочтительно, X1 формулы (II) представляет собой C.
Предпочтительно, =X3 формулы (II) представляет собой =O.
Предпочтительно, -X2- формулы (II) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и -R8a формулы (II) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и -R8a формулы (II) представляет собой -H. Даже более предпочтительно как -R8 , так и -R8a формулы (II) представляет собой -H.
Предпочтительно, -R1 и -R1a формулы (II) независимо выбраны из группы, состоящей из H, метила и этила.
В одном предпочтительном варианте выполнения настоящего изобретения по меньшей мере один из -R1 и -R1a формулы (II) представляет собой -H, более предпочтительно оба -R1 и -R1a формулы (II) представляют собой H.
В другом предпочтительном варианте выполнения настоящего изобретения по меньшей мере один из -R1 и -R1a формулы (II) представляет собой метил, более предпочтительно оба -R1 и R1a формулы (II) представляют собой метил.
Предпочтительно, -R2 и R2a формулы (II) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (II) представляет собой -H. Даже более предпочтительно оба -R2 и R2a формулы (II) представляют собой H.
Предпочтительно, -R3 и R3a формулы (II) независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила.
В одном предпочтительном варианте выполнения настоящего изобретения по меньшей мере один из -R3 и -R3a формулы (II) представляет собой метил, более предпочтительно -R3 формулы (II) представляет собой метил и R3a формулы (II) представляет собой -H.
В другом предпочтительном варианте выполнения настоящего изобретения -R3 и -R3a формулы (II) оба представляют собой -H.
Предпочтительно, -D соединена с -L1- через атом азота посредством образования амидной связи.
В одном предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (IIa-i):
 (IIa-i),
(IIa-i),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
-R1, -R1a, -R2, -R2a, -R3, -R3a, -R7, -R7a и -X2- имеют значения, как определено в формуле (II); и
где -L1- замещена -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIa-i) не замещен -L2-Z или -L2-Z' или заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIa-i) или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно -L1- формулы (IIa-i) замещена одной составляющей -L2-Z или -L2-Z'.
Предпочтительно составляющая -L1- формулы (IIa-i) дополнительно не замещена.
Предпочтительно, -R1 и R1a формулы (IIa-i) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно, по меньшей мере один из -R1 и -R1a формулы (IIa-i) представляет собой -H. Даже более предпочтительно оба -R1 и -R1a формулы (IIa-i) представляют собой -H.
Предпочтительно, -R7 формулы (IIa-i) представляет собой -NR10-(C=O)-R11.
Предпочтительно, -R7a формулы (II-i) выбран из H, метила и этила. Наиболее предпочтительно -R7a формулы (II-i) представляет собой -H.
Предпочтительно, -R10 формулы (IIa-i) выбран из H, метила и этила. Наиболее предпочтительно -R10 формулы (IIa-i) представляет собой метил.
Предпочтительно, -R11 формулы (IIa-i) выбран из H, метила и этила. Наиболее предпочтительно -R11 формулы (IIa-i) представляет собой -H.
Предпочтительно, -R11 формулы (IIa-i) замещен -L2-Z или L2-Z'.
Предпочтительно, -X2- формулы (IIa-i) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и -R8a формулы (IIa-i) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и -R8a формулы (IIa-i) представляет собой -H. Даже более предпочтительно оба -R8 и -R8a формулы (IIa-i) представляют собой -H.
Предпочтительно, -R2 и -R2a формулы (IIa-i) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и -R2a формулы (IIa-i) представляет собой -H. Даже более предпочтительно оба -R2 и -R2a формулы (IIa-i) представляют собой -H.
Предпочтительно, -R3 и -R3a формулы (IIa-i) независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и -R3a формулы (IIa-i) представляет собой метил.
Предпочтительно, -R3 формулы (IIa-i) представляет собой -H, и -R3a формулы (IIa-i) представляет собой метил.
Более предпочтительно составляющая -L1- имеет формулу (IIa-ii):
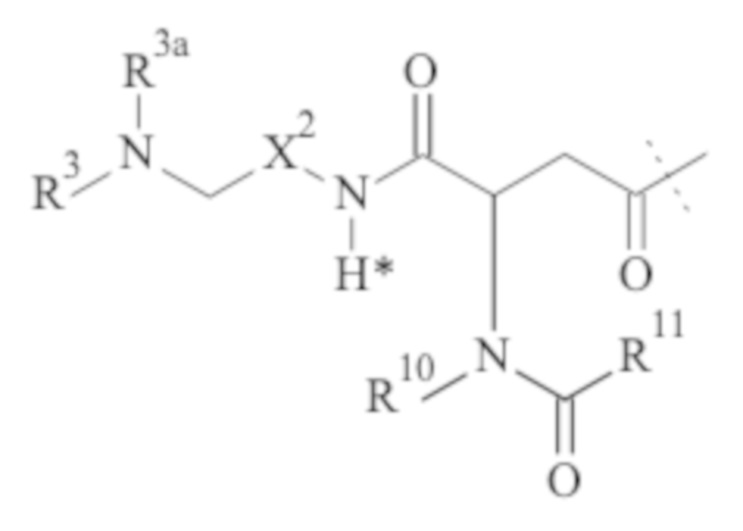 (IIa-ii),
(IIa-ii),
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
-R2, -R2a, -R10, -R11 и -X2- имеют значения, как определено в формуле (II); и
где -L1- замещена -L2-Z или L2-Z' и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIa-ii) не замещен -L2-Z или -L2-Z' или заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIa-ii) или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно -L1- формулы (IIa-ii) замещена одной составляющей -L2-Z или -L2-Z'.
Предпочтительно составляющая -L1- формулы (IIa-ii) дополнительно не замещена.
Предпочтительно, -X2- формулы (IIa-ii) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и -R8a формулы (IIa-ii) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIa-ii) представляет собой -H. Даже более предпочтительно оба -R8 и R8a формулы (IIa-ii) представляют собой -H.
Предпочтительно, -R3 и R3a формулы (IIa-ii) независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIa-ii) представляет собой метил.
Предпочтительно, -R3 формулы (IIa-ii) представляет собой -H, и R3a формулы (IIa-ii) представляет собой метил.
Предпочтительно, -R10 формулы (IIa-ii) выбран из H, метила и этила. Наиболее предпочтительно -R10 формулы (IIa-ii) представляет собой метил.
Предпочтительно, -R11 формулы (IIa-ii) выбран из H, метила и этила. Наиболее предпочтительно -R11 формулы (IIa-ii) представляет собой -H.
Предпочтительно, -R11 формулы (IIa-ii) замещен -L2-Z или L2-Z'.
В еще более предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (IIa-ii'):
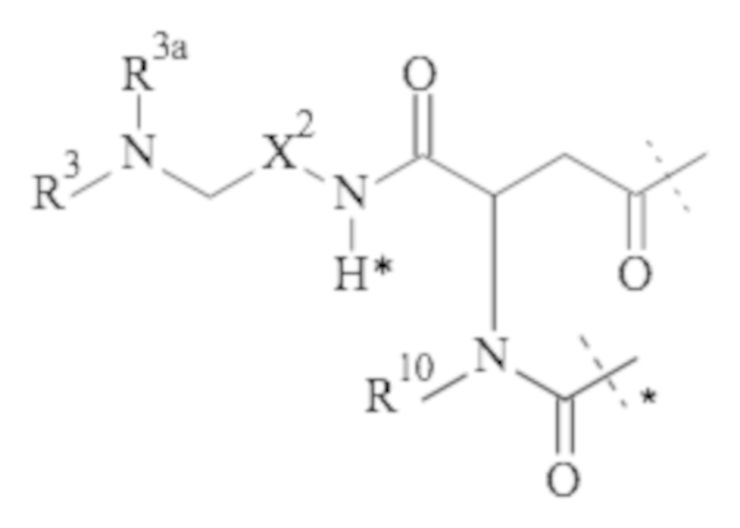 (IIa-ii'),
(IIa-ii'),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
пунктирная линия, отмеченная звездочкой, означает присоединение к -L2-;
-R3, -R3a, -R10 и X2- имеют значения, как определено в формуле (II); и
где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIa-ii') не замещен заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIa-ii') или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно составляющая -L1- формулы (IIa-ii') дополнительно не замещена.
Предпочтительно, -X2- формулы (IIa-ii') представляет собой -C(R8R8a)-.
Предпочтительно -R8 и R8a формулы (IIa-ii') независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIa-ii') представляет собой -H. Даже более предпочтительно оба -R8 и R8a формулы (IIa-ii') представляют собой -H.
Предпочтительно, -R3 и R3a формулы (IIa-ii') независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIa-ii') представляет собой метил.
Предпочтительно, -R3 формулы (IIa-ii') представляет собой -H, и R3a формулы (IIa-ii') представляет собой метил.
Предпочтительно, -R10 формулы (IIa-ii') выбран из H, метила и этила. Наиболее предпочтительно -R10 формулы (IIa-ii') представляет собой метил.
Даже более предпочтительно составляющая -L1- имеет формулу (IIa-iii):
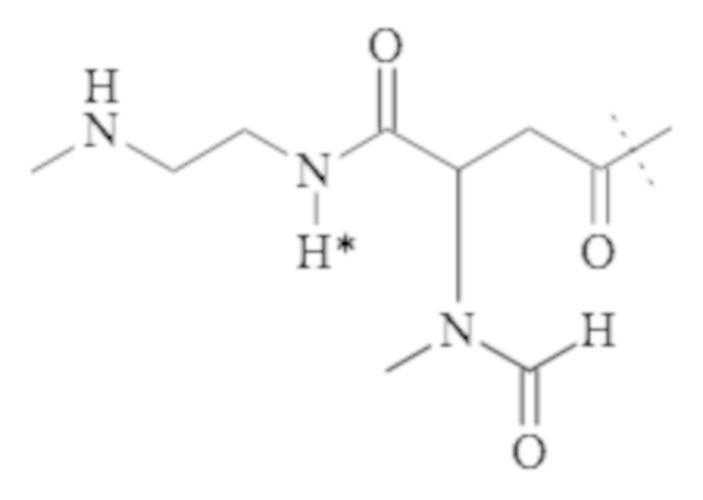 (IIa-iii),
(IIa-iii),
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи; и
где -L1- замещена -L2-Z или -L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIa-iii) не замещен -L2-Z или -L2-Z' или заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIa-iii) или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно -L1- формулы (IIa-iii) замещена одной составляющей -L2-Z или -L2-Z'.
Предпочтительно составляющая -L1- формулы (IIa-iii) дополнительно не замещена.
Наиболее предпочтительно составляющая -L1- имеет формулу (IIa-iii'):
 (IIa-iii'),
(IIa-iii'),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
пунктирная линия, отмеченная звездочкой, означает присоединение к -L2-;
-R2, -R2a, -R3, -R3a и X2- имеют значения, как определено в формуле (II); и
где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIa-iii') не замещен заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIa-iii') или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно составляющая -L1- формулы (IIa-iii') дополнительно не замещена.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (IIb-i)
 (IIb-i),
(IIb-i),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
-R1, -R1a, -R2, -R2a, -R3, -R3a, -R4 и X2- имеют значения, как определено в формуле (II); и
где -L1- замещена -L2-Z или -L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIb-i) не замещен -L2-Z или -L2-Z' или заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIb-i) или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно -L1- формулы (IIb-i) замещена одной составляющей -L2-Z или -L2-Z'.
Предпочтительно составляющая -L1- формулы (IIb-i) дополнительно не замещена.
Предпочтительно, -R1 и R1a формулы (IIb-i) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно, по меньшей мере один из -R1 и R1a формулы (IIb-i) представляет собой метил. Даже более предпочтительно оба -R1 и R1a формулы (IIb-i) представляют собой -метил.
Предпочтительно, -R4 формулы (IIb-i) выбран из группы, состоящей из H, метила и этила. Более предпочтительно, -R4 формулы (IIb-i) представляет собой -H.
Предпочтительно, -X2- формулы (IIb-i) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и R8a формулы (IIb-i) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIb-i) представляет собой -H. Даже более предпочтительно оба -R8 и R8a формулы (IIb-i) представляют собой -H.
Предпочтительно, -R2 и R2a формулы (IIb-i) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (IIb-i) представляет собой -H. Даже более предпочтительно оба -R2 и R2a формулы (IIb-i) представляют собой -H.
Предпочтительно, -R3 и R3a формулы (IIb-i) независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIb-i) представляет собой -H. Даже более предпочтительно оба -R3 и R3a формулы (IIb-i) представляют собой -H.
Более предпочтительно составляющая -L1- имеет формулу (IIb-ii):
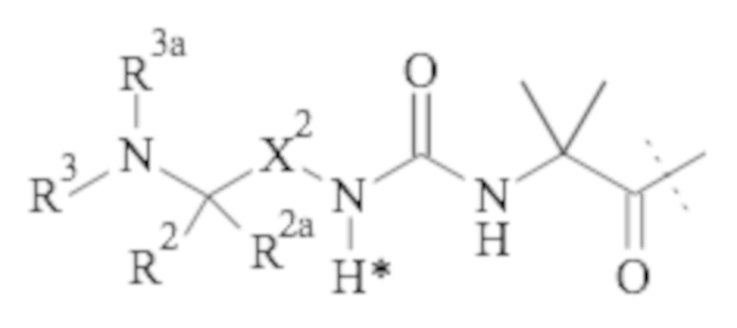 (IIb-ii),
(IIb-ii),
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
-R2, -R2a, -R3, -R3a и X2- имеют значения, как определено в формуле (II); и
где -L1- замещена -L2-Z или -L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIb-ii) не замещен -L2-Z или -L2-Z' или заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIb-ii) или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно -L1- формулы (IIb-ii) замещена одной составляющей -L2-Z или -L2-Z'.
Предпочтительно составляющая -L1- формулы (IIb-ii) дополнительно не замещена.
Предпочтительно, -X2- формулы (IIb-ii) представляет собой -C(R8R8a)-.
Предпочтительно -R8 и R8a формулы (IIb-ii) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и R8a формулы (IIb-ii) представляет собой -H. Даже более предпочтительно оба -R8 и R8a формулы (IIb-ii) представляют собой -H.
Предпочтительно, -R2 и R2a формулы (IIb-ii) независимо выбраны из группы, состоящей из H, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и R2a формулы (IIb-ii) представляет собой -H. Даже более предпочтительно оба -R2 и R2a формулы (IIb-ii) представляют собой -H.
Предпочтительно, -R3 и R3a формулы (IIb-ii) независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Даже более предпочтительно по меньшей мере один из -R3 и R3a формулы (IIb-ii) представляет собой -H. Даже более предпочтительно оба -R3 и R3a формулы (IIb-ii) представляют собой -H.
Даже более предпочтительно составляющая -L1- имеет формулу (IIb-ii'):
 (IIb-ii'),
(IIb-ii'),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
-R2, -R2a, -R3, -R3a и X2- имеют значения, как определено в формуле (II); и
где -L1- замещена -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIb-ii') не замещен -L2-Z или -L2-Z' или заместителем.
Понятно, что в случае, если -R3a формулы (IIb-ii') отличен от -H, он соединен с N, к которому он присоединен через sp3-гибридизованный атом углерода.
Предпочтительно составляющая -L1- формулы (IIb-ii') дополнительно не замещена.
Предпочтительно, -X2- формулы (IIb-ii') представляет собой -C(R8R8a)-.
Предпочтительно -R8 и -R8a формулы (IIb-ii') независимо выбраны из группы, состоящей из -H, метила и этила. Более предпочтительно по меньшей мере один из -R8 и -R8a формулы (IIb-ii') представляет собой -H. Даже более предпочтительно оба -R8 и -R8a формулы (IIb-ii') представляют собой -H.
Предпочтительно, -R2 и -R2a формулы (IIb-ii') независимо выбраны из группы, состоящей из -H, метила и этила. Более предпочтительно, по меньшей мере один из -R2 и -R2a формулы (IIb-ii') представляет собой -H. Даже более предпочтительно оба -R2 и -R2a формулы (IIb-ii') представляют собой H.
Предпочтительно, -R3a формулы (IIb-ii') выбран из группы, состоящей из -H, метила, этила, пропила и бутила. В одном варианте выполнения настоящего изобретения -R3a формулы (IIb-ii') представляет собой -H.
Даже более предпочтительно составляющая -L1- имеет формулу (IIb-iii):
 (IIb-iii),
(IIb-iii),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи; и
где -L1- замещена -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена, при условии, что водород, отмеченный звездочкой в формуле (IIb-iii) не замещен -L2-Z или L2-Z' или заместителем.
Понятно, что в случае, когда один из -R3, -R3a формулы (IIb-iii) или оба отличны от -H, они соединены с N, к которому они присоединены через sp3-гибридизованный атом углерода.
Предпочтительно -L1- формулы (IIb-iii) замещена одной составляющей -L2-Z или L2-Z'.
Предпочтительно составляющая -L1- формулы (IIb-iii) дополнительно не замещена.
Наиболее предпочтительно составляющая -L1- имеет формулу (IIb-iii'):
 (IIb-iii'),
(IIb-iii'),
где
где пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
пунктирная линия, отмеченная звездочкой, обозначает присоединение -L2-Z или -L2-Z'; и
где -L1- необязательно дополнительно замещена, при условии, что атом водорода, отмеченный звездочкой, в формуле (IIb-iii') не замещен заместителем.
Понятно, что азот, соседний с пунктирной линией, отмеченной звездочкой, в формуле (IIb-iii') присоединен к -L2- через sp3-гибридизованный атом углерода.
Предпочтительно составляющая -L1- формулы (IIb-iii') дополнительно не замещена.
Другая предпочтительная составляющая-L1- раскрывается в WO2016/020373A1. Соответственно, в другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1- имеет формулу (III):
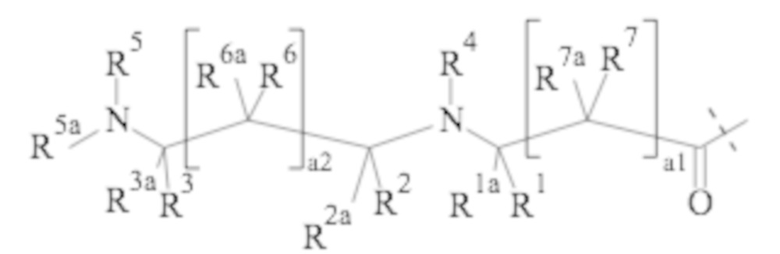 (III),
(III),
где
пунктирная линия показывает присоединение к первичному или вторичному амину или гидроксилу составляющей D путем образования амидной или сложноэфирной связи, соответственно;
-R1, -R1a, -R2, -R2a, -R3 и R3a независимо друг от друга выбирают из группы, состоящей из -H, -C(R8R8aR8b), -C(=O)R8, -C≡N, -C(=NR8)R8a, -CR8(=CR8aR8b), -C≡CR8 и T;
-R4, -R5 и R5a независимо друг от друга выбирают из группы, состоящей из -H, -C(R9R9aR9b) и T;
a1 и a2 независимо друг от друга представляют собой 0 или 1;
каждый -R6, -R6a, -R7, -R7a, -R8, -R8a, -R8b, -R9, -R9a, и -R9b независимо друг от друга выбирают из группы, состоящей из -H, галогена, -CN, -COOR10, -OR10, -C(O)R10, -C(O)N(R10R10a), -S(O)2N(R10R10a), -S(O)N(R10R10a), -S(O)2R10, -S(O)R10, -N(R10)S(O)2N(R10aR10b), -SR10, -N(R10R10a), -NO2, -OC(O)R10, -N(R10)C(O)R10a, -N(R10)S(O)2R10a, -N(R10)S(O)R10a, -N(R10)C(O)OR10a, -N(R10)C(O)N(R10aR10b), -OC(O)N(R10R10a), -T, C1-20 алкила, C2-20 алкенила и C2-20 алкинила; где -T, C1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно замещены одним или более заместителями -R11, которые являются одинаковыми или различными, и где C1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(R12)-, -S(O)2N(R12)-, -S(O)N(R12)-, -S(O)2-, -S(O)-, -N(R12)S(O)2N(R12a)-, -S-, -N(R12)-, -OC(OR12)(R12a)-, -N(R12)C(O)N(R12a)- и -OC(O)N(R12)-;
каждый -R10, -R10a, и -R10b независимо выбирают из группы, состоящей из -H, -T, C1-20 алкила, C2-20 алкенила и C2-20 алкинила; где -T, C1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно замещены одним или более заместителями -R11, которые являются одинаковыми или различными, и где C1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(R12)-, -S(O)2N(R12)-, -S(O)N(R12)-, -S(O)2-, -S(O)-, -N(R12)S(O)2N(R12a)-, -S-, -N(R12)-, -OC(OR12)(R12a)-, -N(R12)C(O)N(R12a)- и -OC(O)N(R12)-;
каждый T независимо друг от друга выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила и 8-11-ти членного гетеробициклила; где каждый T независимо необязательно замещен одним или более заместителями -R11, которые являются одинаковыми или различными;
каждый -R11 независимо друг от друга выбирают из галогена, -CN, оксо (=O), -COOR13, -OR13, -C(O)R13, -C(O)N(R13R13a), -S(O)2N(R13R13a), -S(O)N(R13R13a), -S(O)2R13, -S(O)R13, -N(R13)S(O)2N(R13aR13b), -SR13, -N(R13R13a), -NO2, -OC(O)R13, -N(R13)C(O)R13a, -N(R13)S(O)2R13a, -N(R13)S(O)R13a, -N(R13)C(O)OR13a, -N(R13)C(O)N(R13aR13b), -OC(O)N(R13R13a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R12, -R12a, -R13, -R13a, и -R13b независимо выбирают из группы, состоящей из -H и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
необязательно, одна или более из пар -R1/-R1a, -R2/-R2a, -R3/-R3a, -R6/-R6a, и -R7/-R7a соединяются вместе с атомом, к которому они присоединены, с образованием C3-10 циклоалкила или 3-10-ти членного гетероциклила;
необязательно, одна или более из пар -R1/-R2, -R1/-R3, -R1/-R4, -R1/-R5, -R1/-R6, -R1/-R7, -R2/-R3, -R2/-R4, -R2/-R5, -R2/-R6, -R2/-R7, -R3/-R4, -R3/-R5, -R3/-R6, -R3/-R7, -R4/-R5, -R4/-R6, -R4/-R7, -R5/-R6, -R5/-R7, и -R6/-R7 соединяются вместе с атомами, к которым они присоединены, с образованием кольца A;
A выбирают из группы, состоящей из фенила; нафтила; инденила; инданила; тетралинила; C3-10 циклоалкила; 3-10-ти членного гетероциклила; и 8-11-ти членного гетеробициклила;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Необязательные другие заместители составляющей -L1- формулы (III) предпочтительно являются такими, как описано выше.
Предпочтительно -L1- формулы (III) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
В одном варианте выполнения настоящего изобретения -L1- формулы (III) дополнительно не замещена.
Дополнительные предпочтительные варианты выполнения для -L1- раскрываются в EP1536334B1, WO2009/009712A1, WO2008/034122A1, WO2009/143412A2, WO2011/082368A2 и US8618124B2, которые включены в настоящую заявку посредством ссылки в полном объеме.
Дополнительные предпочтительные варианты выполнения для -L1- раскрываются в US8946405B2 и US8754190B2, которые включены в настоящую заявку посредством ссылки в полном объеме. Соответственно, предпочтительная составляющая -L1- имеет формулу (IV):
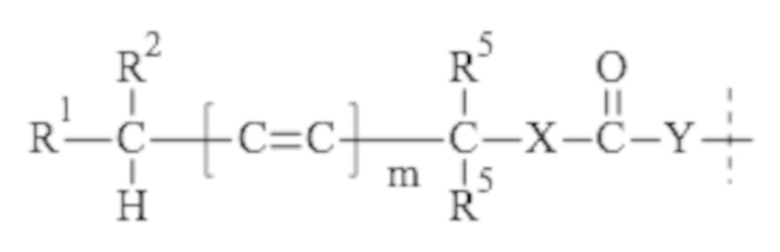 (IV),
(IV),
где
пунктирная линия показывает присоединение к -D, которая представляет собой ПТГ составляющую, и где присоединение осуществляется через функциональную группу составляющей -D, выбранную из группы, состоящей из -OH, -SH и NH2;
m равно 0 или 1;
по меньшей мере один или оба из -R1 и R2 выбирается/независимо друг от друга выбирают из группы, состоящей из -CN, -NO2, необязательно замещенного арила, необязательно замещенного гетероарила, необязательно замещенного алкенила, необязательно замещенного алкинила, -C(O)R3, -S(O)R3, -S(O)2R3 и -SR4,
один и только один из -R1 и R2 выбирают из группы, состоящей из -H, необязательно замещенного алкила, необязательно замещенного арилалкила и необязательно замещенного гетероарилалкила;
-R3 выбирают из группы, состоящей из -H, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила, необязательно замещенного гетероарилалкила, -OR9 и N(R9)2;
-R4 выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероарилалкила;
каждый -R5 независимо выбирают из группы, состоящей из -H, необязательно замещенного алкила, необязательно замещенного алкенилалкила, необязательно замещенного алкинилалкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероарилалкила;
-R9 выбирают из группы, состоящей из -H и необязательно замещенного алкила;
-Y- отсутствует, и -X- представляет собой -O- или S-; или
-Y- представляет собой -N(Q)CH2-, и X- представляет собой -O-;
Q выбирают из группы, состоящей из необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного арилалкила, необязательно замещенного гетероарила и необязательно замещенного гетероарилалкила;
необязательно, -R1 и R2 могут соединяться с образованием 3-8-членного кольца; и
необязательно, оба -R9 вместе с атомом азота, к которому они присоединены, образуют гетероциклическое кольцо;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Только в контексте формулы (IV) применяемые термины имеют следующие значения:
Термин “алкил”, как применяется в настоящей заявке, включает линейные, разветвленные или циклические насыщенные углеводородные группы, имеющие от 1 до 8 атомов углерода, или в некоторых вариантах выполнения настоящего изобретения от 1 до 6 или от 1 до 4 атомов углерода.
Термин “алкокси” включает алкильные группы, связанные с кислородом, включая метокси, этокси, изопропокси, циклопропокси, циклобутокси и подобное.
Термин “алкенил” включает неароматические ненасыщенные углеводороды с двойными связями углерод-углерод.
Термин “алкинил” включает неароматические ненасыщенные углеводороды с тройными связями углерод-углерод.
Термин “арил” включает ароматические углеводородные группы, имеющие от 6 до 18 атомов углерода, предпочтительно от 6 до 10 атомов углерода, включая группы, такие как фенил, нафтил и антраценил. Термин “гетероарил” включает ароматические кольца, содержащие от 3 до 15 атомов углерода, содержащие по меньшей мере один N, O или S атом, предпочтительно от 3 до 7 атомов углерода, содержащие по меньшей мере один N, O или S атом, включая группы, такие как пирролил, пиридил, пиримидинил, имидазолил, оксазолил, изооксазолил, тиазолил, изотиазолил, хинолил, индолил, инденил и подобное.
В некоторых случаях, алкенильные, алкинильные, арильные или гетероарильные составляющие могут быть соединены с оставшейся частью молекулы через алкиленовую связь. При этих обстоятельствах заместитель будет называться алкенилалкил, алкинилалкил, арилалкил или гетероарилалкил, что указывает на то, что алкиленовая составляющая находится между алкенилом, алкинилом, арилом или гетероарилом и молекулой, с которой связан алкенил, алкинил, арил или гетероарил.
Термин “галоген” включает бром, фтор, хлор и иод.
Термин “гетероциклическое кольцо” относится к 4 - 8-членному ароматическому или неароматическому кольцу, содержащему от 3 до 7 атомов углерода и по меньшей мере один N, O, или S атом. Примерами являются пиперидинил, пиперазинил, тетрагидропиранил, пирролидин и тетрагидрофуранил, а также примерные группы, приведенные вые для термина “гетероарил”.
Когда кольцевая система необязательно замещена, подходящие заместители выбирают из группы, состоящей из алкила, алкенила, алкинила или дополнительного кольца, где каждый необязательно дополнительно замещен. Необязательные заместители в любой группе, включая вышеуказанные, включают гало, нитро, циано, OR, -SR, -NR2, -OCOR, -NRCOR, -COOR, -CONR2, -SOR, -SO2R, -SONR2, -SO2NR2, где каждый R независимо представляет собой алкил, алкенил, алкинил, арил или гетероарил, или две R группы, взятые вместе с атомами, к которым они присоединены, образуют кольцо.
Предпочтительно -L1- формулы (IV) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
Дополнительный предпочтительный вариант -L1- раскрывается в WO2013/036857A1, который включен в настоящую заявку в полном объеме посредством ссылки. Соответственно, предпочтительная составляющая -L1- имеет формулу (V):
 (V),
(V),
где
пунктирная линия показывает присоединение к -D, которая представляет собой
ПТГ составляющую, и где присоединение осуществляется через аминную функциональную группу составляющей -D;
-R1 выбирают из группы, состоящей из необязательно замещенного C1-C6 линейного, разветвленного, или циклического алкила; необязательно замещенного арила; необязательно замещенного гетероарила; алкокси; и NR52;
-R2 выбирают из группы, состоящей из -H; необязательно замещенного C1-C6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила;
-R3 выбирают из группы, состоящей из -H; необязательно замещенного C1-C6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила;
-R4 выбирают из группы, состоящей из -H; необязательно замещенного C1-C6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила;
каждый -R5 независимо друг от друга выбирают из группы, состоящей из -H; необязательно замещенного C1-C6 алкила; необязательно замещенного арила; и необязательно замещенного гетероарила; или взятые вместе два -R5 могут представлять собой циклоалкил или циклогетероалкил;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Только в контексте формулы (V) применяемые термины имеют следующие значения:
“Алкил”, “алкенил” и “алкинил” включают линейные, разветвленные или циклические углеводородные группы, имеющие от 1 до 8 атомов углерода или 1-6 атомов углерода или 1-4 атомов углерода, где алкилом является насыщенный углеводород, алкенил включает одну или более двойных связей углерод-углерод, и алкинил включает одну или более тройных связей углерод-углерод. Если иного не указано, они содержат 1-6 атомов углерода.
“Арил” включает ароматические углеводородные группы, имеющие от 6 до 18 атомов углерода, предпочтительно 6-10 атомов углерода, включая группы, такие как фенил, нафтил и антрацен. “Гетероарил” включает ароматические кольца, содержащие 3-15 атомов углерода, содержащие по меньшей мере один N, O или S атом, предпочтительно 3-7 атомов углерода, содержащие по меньшей мере один N, O или S атом, включая группы, такие как пирролил, пиридил, пиримидинил, имидазолил, оксазолил, изооксазолил, тиазолил, изотиазолил, хинолил, индолил, инденил и подобное.
Термин “замещенный” означает алкильную, алкенильную, алкинильную, арильную или гетероарильную группу, включающую одну или более групп заместителей вместо одного или более атомов водорода. Заместители могут в общем быть выбраны из галогена, включая F, Cl, Br и I; низшего алкила, включая линейный, разветвленный и циклический; низшего галоалкила, включая фторалкил, хлоралкил, бромалкил и иодалкил; ОН; низшего алкокси, включая линейные, разветвленные и циклические; SH; низшего алкилтио, включая линейный, разветвленный и циклический; амино, алкиламино, диалкиламино, силила, включая алкилсилил, алкоксисилил и арилсилил; нитро; циано; карбонила; карбоновой кислоты, сложного эфира карбоновой кислоты, карбоксильного амида, аминокарбонила; аминоацила; карбамата; мочевины; тиокарбамата; тиомочевины; кетона; сульфона; сульфонамида; арила, включая фенил, нафтил и антраценил; гетероарила, включая 5-ти членные гетероарилы, включая пиррол, имидазол, фуран, тиофен, оксазол, тиазол, изоксазол, изотиазол, тиадиазол, триазол, оксадиазол и тетразол, 6-ти членные гетероарилы, включая пиридин, пиримидин, пиразин, и конденсированные гетероарилы, включая бензофуран, бензотиофен, бензоксазол, бензимидазол, индол, бензотиазол, бензизоксазол и бензизотиазол.
Предпочтительно -L1- формулы (V) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
Другой предпочтительный вариант -L1- раскрывается в US7585837B2, который включен в настоящую заявку в полном объеме посредством ссылки. Соответственно, предпочтительная составляющая -L1- имеет формулу (VI):
 (VI),
(VI),
где
пунктирная линия показывает присоединение к -D, которая представляет собой ПТГ составляющую, и где присоединение осуществляется через аминную функциональную группу составляющей -D;
R1 и R2 независимо выбирают из группы, состоящей из водорода, алкила, алкокси, алкоксиалкила, арила, алкарила, аралкила, галогена, нитро, -SO3Н, -SO2NHR5, амино, аммония, карбоксила, PO3H2 и OPO3H2;
R3, R4 и R5 независимо выбирают из группы, состоящей из водорода, алкила и арила;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Подходящими заместителями для формулы (VI) являются составляющие алкил (как например C1-6 алкил), алкенил (как например C2-6 алкенил), алкинил (как например C2-6 алкинил), арил (как например фенил), гетероалкил, гетероалкенил, гетероалкинил, гетероарил (как например ароматический 4 - 7 членный гетероцикл) или галоген.
Только в контексте формулы (VI) применяемые термины имеют следующие значения:
Термины “алкил”, “алкокси”, “алкоксиалкил”, “арил”, “алкарил” и “аралкил” означают алкильные радикалы, содержащие 1-8, предпочтительно 1-4 атомов углерода, например, метил, этил, пропил, изопропил и бутил, и арильные радикалы, содержащие 6-10 атомов углерода, например, фенил и нафтил. Термин “галоген” включает бром, фтор, хлор и иод.
Предпочтительно -L1- формулы (VI) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
Другой предпочтительный вариант -L1- раскрывается в WO2002/089789A1, который включен в настоящую заявку в полном объеме посредством ссылки. Соответственно, предпочтительная составляющая -L1- имеет формулу (VII):
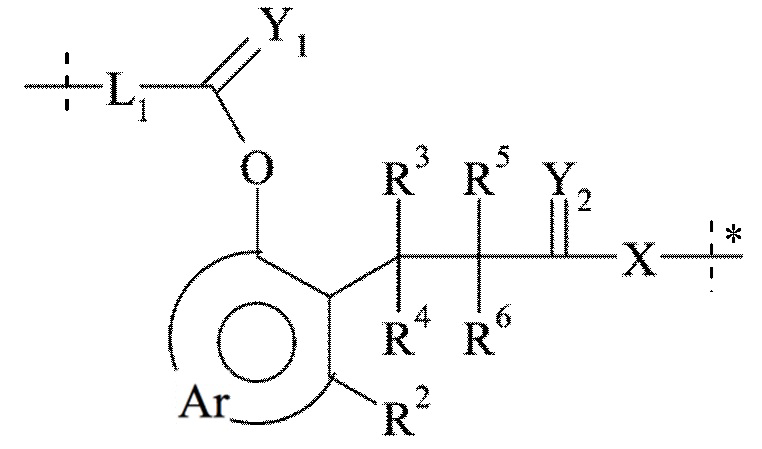 (VII),
(VII),
где
пунктирная линия показывает присоединение к -D, которая представляет собой ПТГ составляющую, и где присоединение осуществляется через аминную функциональную группу составляющей -D;
L1 представляет собой бифункциональную связывающую группу,
Y1 и Y2 независимо представляют собой O, S или NR7;
R2, R3, R4, R5, R6 и R7 независимо выбирают из группы, состоящей из водорода, C1-6 алкилов, C3-12 разветвленных алкилов, C3-8 циклоалкилов, C1-6 замещенных алкилов, C3-8 замещенных циклоалкилов, арилов, замещенных арилов, аралкилов, C1-6 гетероалкилов, замещенных C1-6 гетероалкилов, C1-6 алкокси, фенокси и C1-6 гетероалкокси;
Ar представляет собой составляющую, которая при включении в формулу (VII), образует мультизамещенный ароматический углеводород или мульти-замещенную гетероциклическую группу;
X представляет собой химическую связь или составляющую, которая активно переносится в клетку-мишень, гидрофобную составляющую или их комбинацию,
y равно 0 или 1;
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Только в контексте формулы (VII) применяемые термины имеют следующие значения:
Термин “алкил”, как следует понимать, включает, например, неразветвленные, разветвленные, замещенные C1-12 алкилы, включая алкокси, C3-8 циклоалкилы или замещенные циклоалкилы, и т.д.
Термин “замещение”, как следует понимать, включает добавление или замещение одного или более атомов, содержащихся в функциональной группе, или соединения с одним или более отличными атомами.
Замещенные алкилы включают карбоксиалкилы, аминоалкилы, диалкиламины, гидроксиалкилы и меркаптоалкилы; замещенные циклоалкилы включают составляющие, как например 4-хлорциклогексил; арилы включают составляющие, как например нафтил; замещенные арилы включают составляющие, как например 3-бром-фенил; аралкилы включают составляющие, как например толуил; гетероалкилы включают составляющие, как например этилтиофен; замещенный гетероалкилы включают составляющие, как например 3-метокситиофен; алкокси включает составляющие, как например метокси; и фенокси включает составляющие, как например 3-нитрофенокси. Гало-, как необходимо понимать, включает фтор, хлор, иод и бром.
Предпочтительно -L1- формулы (VII) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
В другом предпочтительном варианте выполнения настоящего изобретения -L1- содержит подструктуру формулы (VIII)
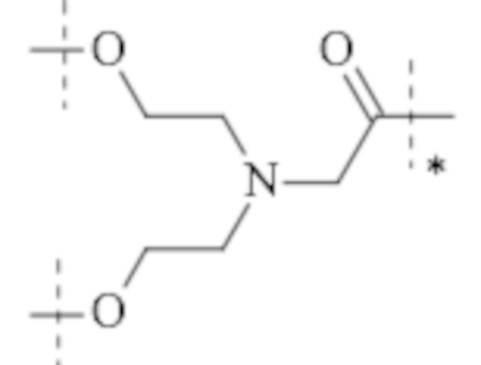 (VIII),
(VIII),
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к атому азота составляющей- D, которая представляет собой ПТГ составляющую, путем образования амидной связи;
непомеченные пунктирные линии показывают присоединение к оставшейся части -L1-; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Предпочтительно -L1- формулы (VIII) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
В одном варианте выполнения настоящего изобретения -L1- формулы (VIII) дополнительно не замещена.
В другом предпочтительном варианте выполнения настоящего изобретения -L1- содержит подструктуру формулы (IX)
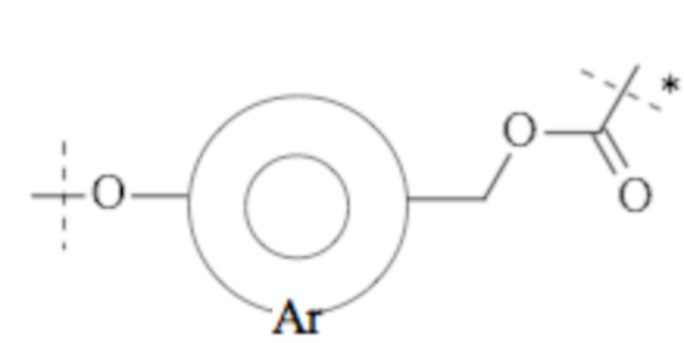 (IX),
(IX),
где
пунктирная линия, отмеченная звездочкой, обозначает присоединение к атому азота составляющей- D, которая представляет собой ПТГ составляющую, путем образования карбаматной связи;
непомеченные пунктирные линии показывают присоединение к оставшейся части -L1-; и
где -L1- имеет в качестве заместителя -L2-Z или L2-Z', и где -L1- необязательно дополнительно замещена;
где
-L2- представляет собой простую химическую связь или спейсер;
-Z представляет собой растворимый в воде носитель; и
-Z' представляет собой нерастворимый в воде носитель.
Предпочтительно -L1- формулы (IX) имеет в качестве заместителя одну составляющую -L2-Z или L2-Z'.
В одном варианте выполнения настоящего изобретения -L1- формулы (IX) дополнительно не замещена.
В пролекарствах согласно настоящему изобретению -L2- представляет собой химическую cвязь или спейсерную составляющую.
В одном варианте выполнения настоящего изобретения -L2- представляет собой химическую cвязь.
В другом варианте выполнения настоящего изобретения -L2- представляет собой спейсерную составляющую.
Когда -L2- отлична от простой химической связи, -L2- предпочтительно выбрана из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry1)-, -S(O)2N(Ry1)-, -S(O)N(Ry1)-, -S(O)2-, -S(O)-, -N(Ry1)S(O)2N(Ry1a)-, -S-, -N(Ry1)-, -OC(ORy1)(Ry1a)-, -N(Ry1)C(O)N(Ry1a)-, -OC(O)N(Ry1)-, C1-50 алкила, C2-50 алкенила и C2-50 алкинил; где -T-, C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более -Ry2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)-, и OC(O)N(Ry3)-;
-Ry1 и Ry1a независимо друг от друга выбраны из группы, состоящей из H, -T, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T, C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более -Ry2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry4)-, -S(O)2N(Ry4)-, -S(O)N(Ry4)-, -S(O)2-, -S(O)-, -N(Ry4)S(O)2N(Ry4a)-, -S-, -N(Ry4)-, -OC(ORy4)(Ry4a)-, -N(Ry4)C(O)N(Ry4a)-, и OC(O)N(Ry4)-;
каждый T независимо выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, 8-30-ти членного карбополициклила, и 8-30-ти членного гетерополициклила; где каждый T независимо необязательно замещен одним или более -Ry2, которые являются одинаковыми или различными;
каждый -Ry2 независимо выбран из группы, состоящей из галогена, -CN, оксо (=O), -COORy5, -ORy5, -C(O)Ry5, -C(O)N(Ry5Ry5a), -S(O)2N(Ry5Ry5a), -S(O)N(Ry5Ry5a), -S(O)2Ry5, -S(O)Ry5, -N(Ry5)S(O)2N(Ry5aRy5b), -SRy5, -N(Ry5Ry5a), -NO2, -OC(O)Ry5, -N(Ry5)C(O)Ry5a, -N(Ry5)S(O)2Ry5a, -N(Ry5)S(O)Ry5a, -N(Ry5)C(O)ORy5a, -N(Ry5)C(O)N(Ry5aRy5b), -OC(O)N(Ry5Ry5a), и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо выбран из группы, состоящей из - H, и C 1-6 алкила, где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными.
Когда -L2- отлична от простой химической связи, -L2- даже более предпочтительно выбрана из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry1)-, -S(O)2N(Ry1)-, -S(O)N(Ry1)-, -S(O)2-, -S(O)-, -N(Ry1)S(O)2N(Ry1a)-, -S-, -N(Ry1)-, -OC(ORy1)(Ry1a)-, -N(Ry1)C(O)N(Ry1a)-, -OC(O)N(Ry1)-, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T-, C1-20 алкил, C2-20 алкенил, и C2-20 алкинил необязательно замещены одним или более -Ry2, которые являются одинаковыми или различными, и где C1-20 алкил, C2-20 алкенил и C2-20 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)-, и OC(O)N(Ry3)-;
-Ry1 и Ry1a независимо друг от друга выбраны из группы, состоящей из H, -T, C1-10 алкила, C2-10 алкенила и C2-10 алкинила; где -T, C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно замещены одним или более -Ry2, которые являются одинаковыми или различными, и где C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry4)-, -S(O)2N(Ry4)-, -S(O)N(Ry4)-, -S(O)2-, -S(O)-, -N(Ry4)S(O)2N(Ry4a)-, -S-, -N(Ry4)-, -OC(ORy4)(Ry4a)-, -N(Ry4)C(O)N(Ry4a)-, и OC(O)N(Ry4)-;
каждый T независимо выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, 8-30-ти членного карбополициклила, и 8-30-ти членного гетерополициклила; где каждый T независимо необязательно замещен одним или более -Ry2, которые являются одинаковыми или различными;
-Ry2 выбран из группы, состоящей из галогена, -CN, оксо (=O), -COORy5, -ORy5, -C(O)Ry5, -C(O)N(Ry5Ry5a), -S(O)2N(Ry5Ry5a), -S(O)N(Ry5Ry5a), -S(O)2Ry5, -S(O)Ry5, -N(Ry5)S(O)2N(Ry5aRy5b), -SRy5, -N(Ry5Ry5a), -NO2, -OC(O)Ry5, -N(Ry5)C(O)Ry5a, -N(Ry5)S(O)2Ry5a, -N(Ry5)S(O)Ry5a, -N(Ry5)C(O)ORy5a, -N(Ry5)C(O)N(Ry5aRy5b), -OC(O)N(Ry5Ry5a), и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо от каждого другого выбран из группы, состоящей из H, и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными.
Когда -L2- отлична от простой химической связи, -L2- даже более предпочтительно выбрана из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry1)-, -S(O)2N(Ry1)-, -S(O)N(Ry1)-, -S(O)2-, -S(O)-, -N(Ry1)S(O)2N(Ry1a)-, -S-, -N(Ry1)-, -OC(ORy1)(Ry1a)-, -N(Ry1)C(O)N(Ry1a)-, -OC(O)N(Ry1)-, C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где -T-, C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более -Ry2, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерываются одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(Ry3)-, -S(O)2N(Ry3)-, -S(O)N(Ry3)-, -S(O)2-, -S(O)-, -N(Ry3)S(O)2N(Ry3a)-, -S-, -N(Ry3)-, -OC(ORy3)(Ry3a)-, -N(Ry3)C(O)N(Ry3a)-, и OC(O)N(Ry3)-;
-Ry1 и Ry1a независимо выбраны из группы, состоящей из H, -T, C1-10 алкила, C2-10 алкенила и C2-10 алкинила;
каждый T независимо выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, 8-30-ти членного карбополициклила, и 8-30-ти членного гетерополициклила;
каждый -Ry2 независимо выбран из группы, состоящей из галогена и C1-6 алкила; и
каждый -Ry3, -Ry3a, -Ry4, -Ry4a, -Ry5, -Ry5a и Ry5b независимо от каждого другого выбран из группы, состоящей из H, и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более галогенами, которые являются одинаковыми или различными.
Даже более предпочтительно, -L2- представляет собой C1-20 алкильную цепь, которая необязательно прерывается одной или более группами, независимо выбранными из -O-, -T- и -C(O)N(Ry1)-; и где C1-20 алкильная цепь необязательно замещена одной или более группами, независимо выбранными из -OH, -T и C(O)N(Ry6Ry6a); где -Ry1, -Ry6, -Ry6a независимо выбраны из группы, состоящей из H и C1-4 алкила, и где T выбран из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, 8-30-ти членного карбополициклила, и 8-30-ти членного гетерополициклила.
Предпочтительно, -L2- имеет молекулярную массу в интервале от 14 г/моль до 750 г/моль.
Предпочтительно, -L2- содержит составляющую, выбранную из
 ,
,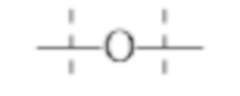 ,
, 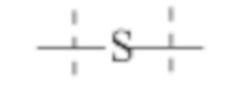 ,
,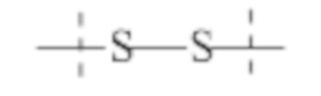 ,
,  ,
,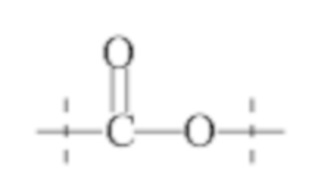 ,
,  ,
, 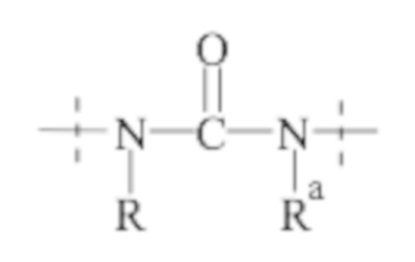 ,
,  ,
, 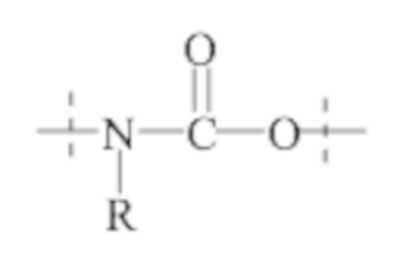 ,
,  ,
,  ,
, 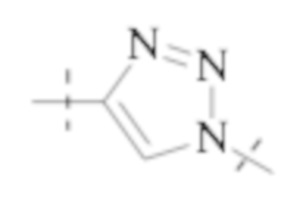 ,
, 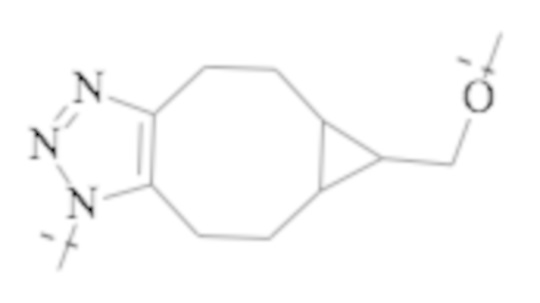 ,
, 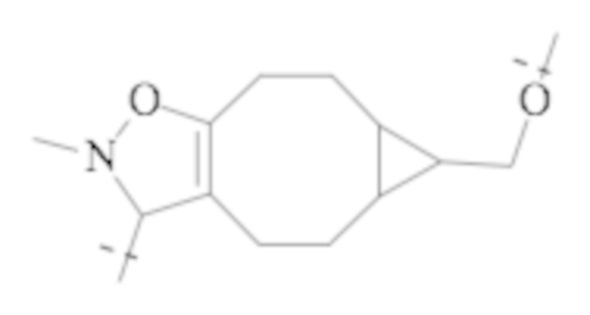 ,
,  ,
,  ,
,  ,
,  ,
,
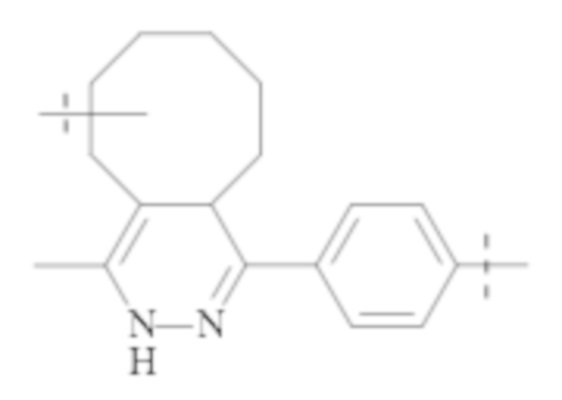 ,
,  , и
, и 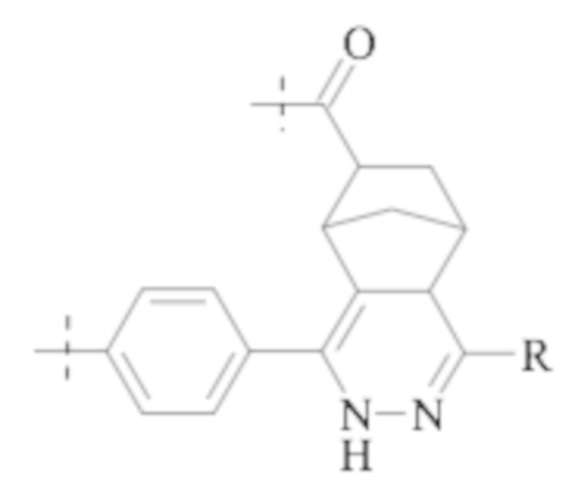 ;
;
где
пунктирная линия обозначает присоединение к остальной части -L2-, -L1-, -Z и/или -Z', соответственно; и
-R и Ra независимо друг от друга выбраны из группы, состоящей из H, метила, этила, пропила, бутила, пентила и гексила.
В одном предпочтительном варианте выполнения настоящего изобретения- L2- имеет длину цепи от 1 до 20 атомов.
Как применяется в настоящей заявке термин “длина цепи” в отношении составляющей -L2- относится к числу атомов -L2-, присутствующих в самом коротком соединении между -L1- и Z.
Предпочтительно, -L2- имеет формулу (i)
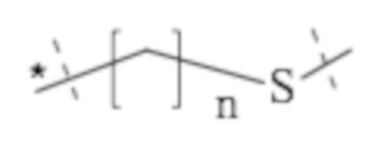 (i),
(i),
где
пунктирная линия, отмеченная звездочкой, означает присоединение к -L1-;
неотмеченная пунктирная линия обозначает присоединение к -Z или Z';
n выбран из группы, состоящей из 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17 и 18; и
где составляющая формулы (i) необязательно дополнительно замещена.
Предпочтительно, n формулы (i) выбран из группы, состоящей из 3, 4, 5, 6, 7, 8, и 9. Даже более предпочтительно n формулы (i) равно 4, 5, 6, или 7. В одном варианте выполнения настоящего изобретения n формулы (i) равно 4. В другом варианте выполнения настоящего изобретения n формулы (i) равно 5. В другом варианте выполнения настоящего изобретения n формулы (i) равно 6.
В одном предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- выбрана из группы, состоящей из 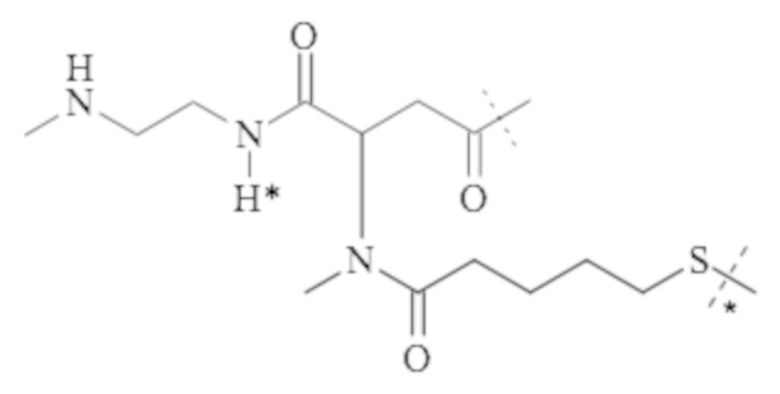 (IIca-i),
(IIca-i),
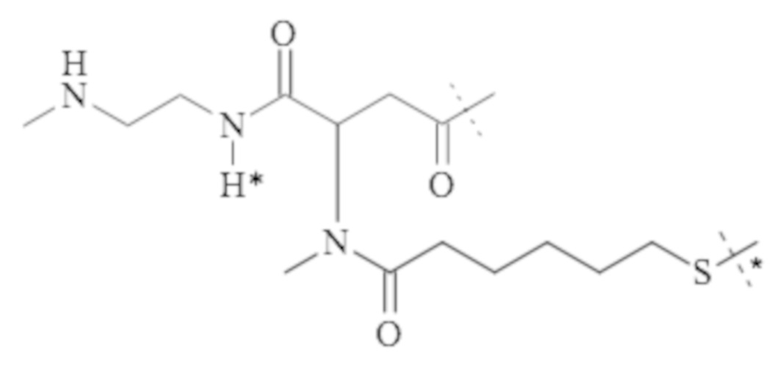 (IIca-ii) и
(IIca-ii) и
 (IIca-iii);
(IIca-iii);
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, означает присоединение к -Z или -Z'.
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- выбрана из группы, состоящей из
 (IIcb-i),
(IIcb-i),
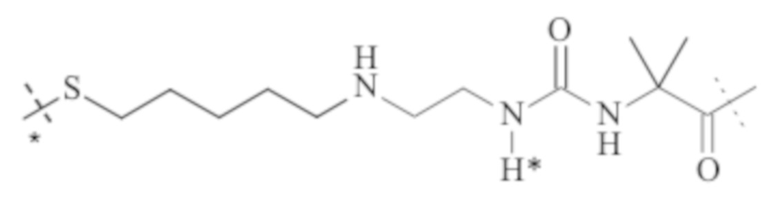 (IIcb-ii) и
(IIcb-ii) и
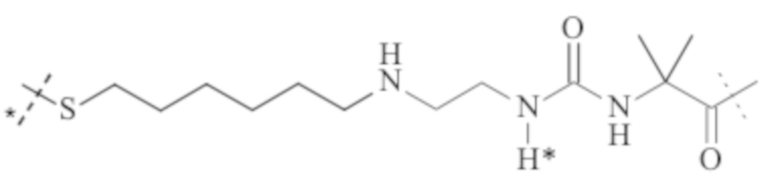 (IIcb-iii);
(IIcb-iii);
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей D, которая представляет собой ПТГ составляющую, путем образования амидной связи; и
пунктирная линия, отмеченная звездочкой, означает присоединение к -Z или -Z'.
В предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- имеет формулу (IIca-ii).
В другом предпочтительном варианте выполнения настоящего изобретения составляющая -L1-L2- имеет формулу (IIcb-ii).
Предпочтительно, ПТГ соединение контролируемого высвобождения согласно настоящему изобретению имеет формулу (Ia) с x = 1.
Носитель -Z содержит C8-24 алкил или полимер. Предпочтительно, -Z содержит полимер, предпочтительно полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтила фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометилцеллюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
Предпочтительно, -Z имеет молекулярную массу в интервале от 5 до 200 кДа. Даже более предпочтительно, -Z имеет молекулярную массу в интервале от 8 до 100 кДа, даже более предпочтительно в интервале от 10 до 80 кДа, даже более предпочтительно от 12 до 60, даже более предпочтительно от 15 до 40, и наиболее предпочтительно -Z имеет молекулярную массу около 20 кДа. В другом в равной степени предпочтительном варианте выполнения настоящего изобретения -Z имеет молекулярную массу около 40 кДа.
В одном варианте выполнения настоящего изобретения такой растворимый в воде носитель -Z содержит белок. Предпочтительные белки выбирают из группы, состоящей из карбоксил-концевого полипептида хорионического гонадотропина, как описано в US 2012/0035101 A1, которые включены в настоящую заявку посредством ссылки; альбумина; XTEN, как описано в WO 2011123813 A2, которая включена в настоящую заявку посредством ссылки; последовательностей пролиновых/аланиновых случайных спиралей, как описано в WO 2011/144756 A1, который включен в настоящую заявку посредством ссылки; последовательностей пролина/аланина/серина, как описано в WO 2008/155134 A1 и WO 2013/024049 A1, которые включены в настоящую заявку посредством ссылками; с Fc слитых белков.
В одном варианте выполнения настоящего изобретения -Z представляет собой полисаркозин.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит поли(N-метилглицин).
В особенно предпочтительном варианте выполнения настоящего изобретения -Z содержит составляющую белка со структурой случайной спирали.
В одном предпочтительном варианте выполнения настоящего изобретения -Z содержит одну составляющую белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит две составляющие белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит три составляющие белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит четыре составляющие белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит пять составляющих белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит шесть составляющих белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит семь составляющих белка со структурой случайной спирали.
В другом предпочтительном варианте выполнения настоящего изобретения -Z содержит восемь составляющих белка со структурой случайной спирали.
Предпочтительно составляющая белка со структурой случайной спирали содержит по меньшей мере 25 аминокислотных остатков и самое большее 2000 аминокислот. Даже более предпочтительно составляющая белка со структурой случайной спирали содержит по меньшей мере 30 аминокислотных остатков и самое большее 1500 аминокислотных остатков. Даже более предпочтительно составляющая белка со структурой случайной спирали содержит по меньшей мере 50 аминокислотных остатков и самое большее 500 аминокислотных остатков.
В предпочтительном варианте выполнения настоящего изобретения, -Z содержит составляющую белка со структурой случайной спирали, где по меньшей мере 80%, предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, даже более предпочтительно по меньшей мере 95%, даже более предпочтительно по меньшей мере 98% и наиболее предпочтительно по меньшей мере 99% от общего числа аминокислот, образующих указанную составляющую белка со структурой случайной спирали, выбраны из аланина и пролина. Даже более предпочтительно, по меньшей мере 10%, но менее 75%, предпочтительно менее 65%, от общего числа аминокислотных остатков составляющей белка со структурой случайной спирали представляют собой пролиновые остатки. Предпочтительно, составляющая белка со структурой случайной спирали является такой, как описано в WO 2011/144756 A1, которая включена в настоящую заявку в полном объеме посредством ссылки. Даже более предпочтительно Z содержит по меньшей мере одну составляющую, выбранную из группы, состоящей из SEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:7, SEQ ID NO:8, SEQ ID NO:9, SEQ ID NO:10, SEQ ID NO:11, SEQ ID NO:12, SEQ ID NO:13, SEQ ID NO:14, SEQ ID NO:15, SEQ ID NO:16, SEQ ID NO:17, SEQ ID NO:51 и SEQ ID NO:61, как раскрывается в WO2011/144756, которая включена в настоящую заявку посредством ссылки. Составляющая, содержащая такой белок со структурой случайной спирали, содержащая аланин и пролин, которые упоминаются как “PA” или “PA составляющая”.
Соответственно, -Z содержит PA составляющую.
В равной мере предпочтительном варианте выполнения настоящего изобретения, -Z содержит составляющая белка со структурой случайной спирали, в которой по меньшей мере 80%, предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, даже более предпочтительно по меньшей мере 95%, даже более предпочтительно по меньшей мере 98% и наиболее предпочтительно по меньшей мере 99% от общего числа аминокислот, образующих указанную составляющую белка со структурой случайной спирали, выбраны из аланина, серина и пролина. Даже более предпочтительно, по меньшей мере 4%, но менее 40% от общего числа аминокислотных остатков составляющей белка со структурой случайной спирали представляют собой пролиновые остатки. Предпочтительно, составляющая белка со структурой случайной спирали описана в WO 2008/155134 A1, которая включена в настоящую заявку в полном объеме посредством ссылки. Даже более предпочтительно Z содержит по меньшей мере одну составляющую, выбранную из группы, состоящей из SEQ ID NO:2, SEQ ID NO:4, SEQ ID NO:6, SEQ ID NO:8, SEQ ID NO:10, SEQ ID NO:12, SEQ ID NO:14, SEQ ID NO:16, SEQ ID NO:18, SEQ ID NO:20, SEQ ID NO:22, SEQ ID NO:24, SEQ ID NO:26, SEQ ID NO:28, SEQ ID NO:30, SEQ ID NO:32, SEQ ID NO:34, SEQ ID NO:36, SEQ ID NO:40, SEQ ID NO:42, SEQ ID NO:44, SEQ ID NO:46, SEQ ID NO:50, SEQ ID NO:52, SEQ ID NO:54 и SEQ ID NO:56, как описано в WO 2008/155134 A1, которая включена в настоящую заявку посредством ссылки. Составляющая, содержащая белок со структурой случайной спирали, содержащий аланин, серин и пролин, упоминаются как “PAS” или “PAS составляющая”.
Соответственно, -Z содержит PAS составляющую.
В равной мере предпочтительном варианте выполнения настоящего изобретения, -Z содержит составляющую белка со структурой случайной спирали, в которой по меньшей мере 80%, предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, даже более предпочтительно по меньшей мере 95%, даже более предпочтительно по меньшей мере 98% и наиболее предпочтительно по меньшей мере 99% от общего числа аминокислот, образующих указанную составляющую белка со структурой обратной спирали, выбраны аланина, глицина и пролина. Составляющая, содержащая белок со структурой случайной спирали, содержащий аланин, глицин и пролин, упоминается как “PAG” или “PAG составляющая”.
Соответственно, -Z содержит PAG составляющую.
В равной мере предпочтительном варианте выполнения настоящего изобретения, -Z содержит составляющая белка со структурой случайной спирали, в которой по меньшей мере 80%, предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, даже более предпочтительно по меньшей мере 95%, даже более предпочтительно по меньшей мере 98% и наиболее предпочтительно по меньшей мере 99% от общего числа аминокислот, образующих указанную составляющую белка со структурой обратной спирали, выбирают из пролина и глицина. Составляющая, содержащая белок со структурой случайной спирали, содержащий пролин и глицин, упоминается как “PG” или “PG составляющая”.
Предпочтительно, такая PG составляющая содержит составляющую формулы (a-0)
[(Gly)p-Pro-(Gly)q]r (a-0);
где
p выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5;
q выбран из группы, состоящей из 0, 1, 2, 3, 4 и 5;
r представляет собой целое число в интервале и включительно от 10 до 1000;
при условии, что по меньшей мере один из p и q равен по меньшей мере 1;
Предпочтительно, p формулы (a-0) выбран из группы, состоящей из 1, 2 и 3.
Предпочтительно, q формулы (a-0) выбран из 0, 1 и 2.
Даже более предпочтительно PG составляющая содержит последовательность SEQ ID:NO 122: GGPGGPGPGGPGGPGPGGPG
Даже более предпочтительно, PG составляющая содержит последовательность SEQ ID:NO 97 формулы (a-0-a)
(GGPGGPGPGGPGGPGPGGPG)v (a-0-a),
где
v представляет собой целое число в интервале и включительно от 1 до 50.
Понятно, что последовательность формулы (a-0-a) содержит v повторений последовательности SEQ ID NO:122.
Соответственно, -Z содержит PG составляющую.
В равной мере предпочтительном варианте выполнения настоящего изобретения, -Z содержит составляющая белка со структурой случайной спирали, в которой по меньшей мере 80%, предпочтительно по меньшей мере 85%, даже более предпочтительно по меньшей мере 90%, даже более предпочтительно по меньшей мере 95%, даже более предпочтительно по меньшей мере 98% и наиболее предпочтительно по меньшей мере 99% от общего числа аминокислот, образующих указанный белок со структурой обратной спирали, выбраны из аланина, глицина, серина, треонина, глутамата и пролина. Предпочтительно, составляющая белка со структурой случайной спирали является такой, как описано в WO 2010/091122 A1, который включен в настоящую заявку посредством ссылки. Даже более предпочтительно -Z содержит по меньшей мере одну составляющую, выбранную из группы, состоящей из SEQ ID NO:182, SEQ ID NO:183, SEQ ID NO:184; SEQ ID NO:185, SEQ ID NO:186, SEQ ID NO:187, SEQ ID NO:188, SEQ ID NO:189, SEQ ID NO:190, SEQ ID NO:191, SEQ ID NO:192, SEQ ID NO:193, SEQ ID NO:194, SEQ ID NO:195, SEQ ID NO:196, SEQ ID NO:197, SEQ ID NO:198, SEQ ID NO:199, SEQ ID NO:200, SEQ ID NO:201, SEQ ID NO:202, SEQ ID NO:203, SEQ ID NO:204, SEQ ID NO:205, SEQ ID NO:206, SEQ ID NO:207, SEQ ID NO:208, SEQ ID NO:209, SEQ ID NO:210, SEQ ID NO:211, SEQ ID NO:212, SEQ ID NO:213, SEQ ID NO:214, SEQ ID NO:215, SEQ ID NO:216, SEQ ID NO:217, SEQ ID NO:218, SEQ ID NO:219, SEQ ID NO:220, SEQ ID NO:221, SEQ ID NO:759, SEQ ID NO:760, SEQ ID NO:761, SEQ ID NO:762, SEQ ID NO:763, SEQ ID NO:764, SEQ ID NO:765, SEQ ID NO:766, SEQ ID NO:767, SEQ ID NO:768, SEQ ID NO:769, SEQ ID NO:770, SEQ ID NO:771, SEQ ID NO:772, SEQ ID NO:773, SEQ ID NO:774, SEQ ID NO:775, SEQ ID NO:776, SEQ ID NO:777, SEQ ID NO:778, SEQ ID NO:779, SEQ ID NO:1715, SEQ ID NO:1716, SEQ ID NO:1718, SEQ ID NO:1719, SEQ ID NO:1720, SEQ ID NO:1721 и SEQ ID NO:1722, как описано в WO2010/091122A1, которая включена в настоящую заявку посредством ссылки. Составляющая, содержащая белок со структурой случайной спирали, содержащий аланин, глицин, серин, треонин, глутамат и пролин, упоминается как “XTEN” или “XTEN составляющая” наряду с ее обозначением в WO 2010/091122 A1.
Соответственно, -Z содержит XTEN составляющую.
В другом предпочтительном варианте выполнения настоящего изобретения, Z содержит производное жирной кислоты. Предпочтительными производными жирной кислоты являются описанные в WO 2005/027978 A2 и WO 2014/060512 A1, которые включены в настоящую заявку посредством ссылки.
В другом предпочтительном варианте выполнения настоящего изобретения Z представляет собой полимер на основе гиалуроновой кислоты.
В одном варианте выполнения настоящего изобретения Z представляет собой носитель, как раскрывается в WO 2012/02047 A1, который включен в настоящую заявку посредством ссылки.
В другом варианте выполнения настоящего изобретения Z представляет собой носитель, как раскрывается в WO 2013/024048 A1, который включен в настоящую заявку посредством ссылки.
В другом предпочтительном варианте выполнения настоящего изобретения -Z представляет собой полимер на основе ПЭГ, такой как линейный, разветвленный или полимер на основе ПЭГ с множеством ветвей.
В одном варианте выполнения настоящего изобретения -Z представляет собой линейный полимер на основе ПЭГ.
В другом варианте выполнения настоящего изобретения -Z представляет собой полимер на основе ПЭГ с множеством ветвей. Предпочтительно, -Z представляет собой полимер на основе ПЭГ с множеством ветвей, имеющий по меньшей мере 4 ветви на основе ПЭГ.
Предпочтительно, такой полимер на основе ПЭГ с множеством ветвей -Z соединен с множеством составляющих- L2-L1-D, где каждая составляющая -L2-L1-D предпочтительно соединена с концом ветви, предпочтительно с концом ветви. Предпочтительно такой полимер на основе ПЭГ с множеством ветвей -Z соединен с 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 или 16 составляющими -L2-L1-D. Даже более предпочтительно такой полимер на основе ПЭГ с множеством ветвей -Z соединен с 2, 3, 4, 6 или 8 составляющими -L2-L1- D. Даже более предпочтительно такой полимер на основе ПЭГ с множеством ветвей -Z соединен с 2, 4 или 6 составляющими -L2-L1-D, даже более предпочтительно такой полимер на основе ПЭГ с множеством ветвей -Z соединен с 4 или 6 составляющими -L2-L1-D, и наиболее предпочтительно такой полимер на основе ПЭГ с множеством ветвей -Z соединена с 4 составляющими -L2-L1-D.
Предпочтительно таким полимером Z на основе ПЭГ с множеством ветвей является ПЭГ производное с множеством ветвей, как например подробно описано для продуктов, перечисленных в JenKem Technology, USA (доступно по ссылке http://www.jenkemusa.com/Pages/PEGProducts.aspx на 18 декабря 2014), как например ПЭГ производная с 4-мя ветвями, в частности ПЭГ производная с 4-мя ветвями, содержащая ядро из пентаэритрита, ПЭГ производная с восемью ветвями, содержащая ядро из гексаглицерина, и ПЭГ производная с восемью ветвями, содержащая ядро из трипентаэритрита. Более предпочтительно, растворимый в воде носителем -Z на основе ПЭГ содержит составляющую, выбранную из:
ПЭГ-амин с 4-мя ветвями, содержащий ядро из пентаэритрита:
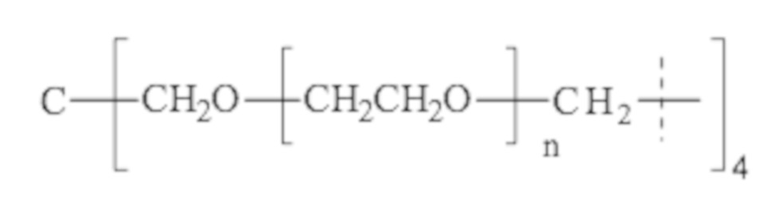
с n в интервале от 20 до 500;
ПЭГ-амин с восемью ветвями, содержащий ядро из гексаглицерина:

с n в интервале от 20 до 500; и
R = структура ядра из гексаглицерина или трипентаэритрита; и
ПЭГ-амин с шестью ветвями, содержащий ядро из сорбита или дипентаэритрита:
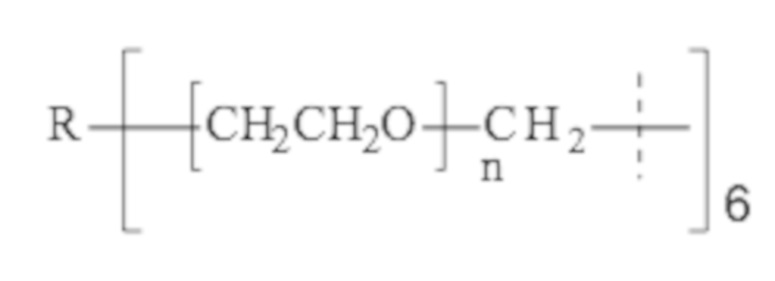
с n в интервале от 20 до 500; и
R = содержащий ядро из сорбита или дипентаэритрита;
и где пунктирные линии обозначают присоединение к остальной части ПТГ пролекарства.
В предпочтительном варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер на основе ПЭГ. В одном варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер на основе ПЭГ, имеющий одну, две, три, четыре, пять или шесть точек разветвления. Предпочтительно, -Z представляет собой разветвленный полимер на основе ПЭГ, имеющий одну, две или три точки разветвления. В одном варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер на основе ПЭГ, имеющий одну точку разветвления. В другом варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер на основе ПЭГ, имеющий две точки разветвления. В другом варианте выполнения настоящего изобретения -Z представляет собой разветвленный полимер на основе ПЭГ, имеющий три точки разветвления.
Точку разветвления предпочтительно выбирают из группы, состоящей из -N<, -CH< и >C<.
Предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу, равную по меньшей мере 10 кДа.
В одном варианте выполнения настоящего изобретения такая разветвленная составляющая -Z имеет молекулярную массу в интервале и включая 10 кДа - 500 кДа, более предпочтительно в интервале и включая 10 кДа - 250 кДа, даже более предпочтительно в интервале и включая 10 кДа - 150 кДа, даже более предпочтительно в интервале и включая 12 кДа - 100 кДа и наиболее предпочтительно в интервале и включая 15 кДа - 80 кДа.
Предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу в интервале и включая 10 кДа - 80 кДа. В одном варианте выполнения настоящего изобретения молекулярная масса равна около 10 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 20 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 30 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 40 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 50 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 60 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 70 кДа. В другом варианте выполнения настоящего изобретения молекулярная масса такой разветвленной составляющей -Z равна около 80 кДа. Наиболее предпочтительно, такая разветвленная составляющая -Z имеет молекулярную массу, равную около 40 кДа.
Предпочтительно, -Z или Z' содержит составляющую
 .
.
В равно предпочтительном варианте выполнения настоящего изобретения- Z содержит амидную связь.
Предпочтительно -Z содержит составляющую формулы (a)
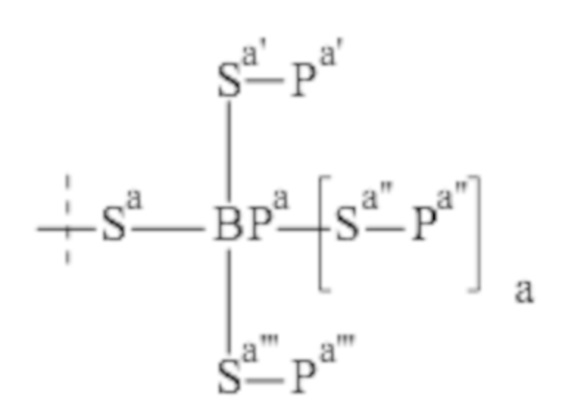 (a),
(a),
где
пунктирная линия показывает присоединение к -L2- или к оставшейся части -Z;
BPa представляет собой точку разветвления, выбранную из группы, состоящей из -N<, -CR< и >C<;
-R выбирают из группы, состоящей из -H и C1-6 алкила;
a равно 0, если BPa представляет собой -N< или CR<, и n равно 1, если BPa представляет собой >C<;
-Sa-, -Sa'-, -Sa''- и Sa'''- независимо друг от друга представляют собой химическую связь или выбирают из группы, состоящей из C1-50 алкила, C2-50 алкенила и C2-50 алкинила; где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно замещены одним или более заместителями -R1, которые являются одинаковыми или различными, и где C1-50 алкил, C2-50 алкенил и C2-50 алкинил необязательно прерваны одной или более группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(R2)-, -S(O)2N(R2)-, -S(O)N(R2)-, -S(O)2-, -S(O)-, -N(R2)S(O)2N(R2a)-, -S-, -N(R2)-, -OC(OR2)(R2a)-, -N(R2)C(O)N(R2a)- и -OC(O)N(R2)-;
каждый -T- независимо выбирают из группы, состоящей из фенила, нафтила, инденила, инданила, тетралинила, C3-10 циклоалкила, 3-10-ти членного гетероциклила, 8-11-ти членного гетеробициклила, 8-30-членного карбополициклила и 8-30-членного гетерополициклила; где каждый -T- независимо необязательно замещен одним или более заместителями -R1, которые являются одинаковыми или различными;
каждый -R1 независимо выбирают из группы, состоящей из галогена, -CN, оксо (=O), -COOR3, -OR3, -C(O)R3, -C(O)N(R3R3a), -S(O)2N(R3R3a), -S(O)N(R3R3a), -S(O)2R3, -S(O)R3, -N(R3)S(O)2N(R3aR3b), -SR3, -N(R3R3a), -NO2, -OC(O)R3, -N(R3)C(O)R3a, -N(R3)S(O)2R3a, -N(R3)S(O)R3a, -N(R3)C(O)OR3a, -N(R3)C(O)N(R3aR3b), -OC(O)N(R3R3a) и C1-6 алкила; где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными;
каждый -R2, -R2a, -R3, -R3a и R3b независимо выбирают из группы, состоящей из -H и C1-6 алкила, где C1-6 алкил необязательно замещен одним или более заместителями галоген, которые являются одинаковыми или различными; и
-Pa', -Pa'' и Pa''' независимо представляют собой полимерную составляющую.
В одном варианте выполнения настоящего изобретения BPa формулы (a) представляет собой -N<.
В другом варианте выполнения настоящего изобретения BPa формулы (a) представляет собой >C<.
В предпочтительном варианте выполнения настоящего изобретения BPa формулы (a) представляет собой -CR<. Предпочтительно, -R представляет собой -H. Соответственно, a формулы (a) равно 0.
В одном варианте выполнения настоящего изобретения -Sa- формулы (a) представляет собой химическую cвязь.
В другом варианте выполнения настоящего изобретения -Sa- формулы (a) выбрана из группы, состоящей из C1-10 алкила, C2-10 алкенила и C2-10 алкинила, где C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -T-, -C(O)O-, -O-, -C(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-, -S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)(R4a)-, -N(R4)C(O)N(R4a)-, и OC(O)N(R4)-; где -T- представляет собой 3-10-ти членный гетероциклил; и R4 и R4a независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила.
Предпочтительно -Sa- формулы (a) выбран из группы, состоящей из C1-10 алкила, который прерывается одной или более химическими группами, выбранными из группы, состоящей из -T-, -C(O)N(R4)- и O-.
В одном варианте выполнения настоящего изобретения -Sa'- формулы (a) представляет собой химическую cвязь.
В другом варианте выполнения настоящего изобретения -Sa'- формулы (a) выбрана из группы, состоящей из C1-10 алкила, C2-10 алкенила и C2-10 алкинила, где C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -C(O)O-, -O-, -C(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-, -S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)(R4a)-, -N(R4)C(O)N(R4a)-, и OC(O)N(R4)-; где -R4 и R4a независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Предпочтительно -Sa'- формулы (a) выбран из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -O-, -C(O)- и C(O)N(R4)-.
В одном варианте выполнения настоящего изобретения -Sa''- формулы (a) представляет собой химическую cвязь.
В другом варианте выполнения настоящего изобретения -Sa''- формулы (a) выбран из группы, состоящей из C1-10 алкила, C2-10 алкенила и C2-10 алкинила, где C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -C(O)O-, -O-, -C(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-,-S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)(R4a)-, -N(R4)C(O)N(R4a)-, и OC(O)N(R4)-; где -R4 и R4a независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Предпочтительно -Sa''- формулы (a) выбран из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -O-, -C(O)- и C(O)N(R4)-.
В одном варианте выполнения настоящего изобретения -Sa'''- формулы (a) представляет собой химическую cвязь.
В другом варианте выполнения настоящего изобретения -Sa'''- формулы (a) выбран из группы, состоящей из C1-10 алкила, C2-10 алкенила и C2-10 алкинила, где C1-10 алкил, C2-10 алкенил и C2-10 алкинил необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -C(O)O-, -O-, -C(O)-, -C(O)N(R4)-, -S(O)2N(R4)-, -S(O)N(R4)-,-S(O)2-, -S(O)-, -N(R4)S(O)2N(R4a)-, -S-, -N(R4)-, -OC(OR4)(R4a)-, -N(R4)C(O)N(R4a)-, и OC(O)N(R4)-; где -R4 и R4a независимо выбраны из группы, состоящей из H, метила, этила, пропила и бутила. Предпочтительно -Sa'''- формулы (a) выбран из группы, состоящей из метила, этила, пропила, бутила, которые необязательно прерываются одной или более химическими группами, выбранными из группы, состоящей из -O-, -C(O)- и C(O)N(R4)-.
Предпочтительно, -Pa', -Pa'' и Pa''' формулы (a) независимо содержат полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтилфосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометил целлюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
Более предпочтительно, -Pa', -Pa'' и Pa''' формулы (a) независимо содержат составляющую на основе ПЭГ. Даже более предпочтительно, -Pa', -Pa'' и Pa''' формулы (a) независимо содержат составляющую на основе ПЭГ, содержащую по меньшей мере 20% ПЭГ, даже более предпочтительно по меньшей мере 30%, даже более предпочтительно по меньшей мере 40% ПЭГ, даже более предпочтительно по меньшей мере 50% ПЭГ, даже более предпочтительно по меньшей мере 60% ПЭГ, даже более предпочтительно по меньшей мере 70% ПЭГ, даже более предпочтительно по меньшей мере 80% ПЭГ и наиболее предпочтительно по меньшей мере 90% ПЭГ.
Предпочтительно, -Pa', -Pa'' и Pa''' формулы (a) независимо имеют молекулярную массу в интервале и включая 5 кДа - 50 кДа, более предпочтительно имеют молекулярную массу в интервале и включая 5 кДа - 40 кДа, даже более предпочтительно в интервале и включая 7.5 кДа - 35 кДа, даже более предпочтительно в интервале от и 7.5 - 30 кДа, даже более предпочтительно в интервале и включая 10 - 30 кДа.
В одном варианте выполнения настоящего изобретения -Pa', -Pa'' и Pa''' формулы (a) имеют молекулярную массу, равную около 5 кДа.
В другом варианте выполнения настоящего изобретения -Pa', -Pa'' и Pa''' формулы (a) имеют молекулярную массу, равную около 7.5 кДа.
В другом варианте выполнения настоящего изобретения -Pa', -Pa'' и Pa''' формулы (a) имеют молекулярную массу, равную около 10 кДа.
В другом варианте выполнения настоящего изобретения -Pa', -Pa'' и Pa''' формулы (a) имеют молекулярную массу, равную около 12.5 кДа.
В другом варианте выполнения настоящего изобретения -Pa', -Pa'' и Pa''' формулы (a) имеют молекулярную массу, равную около 15 кДа.
В другом варианте выполнения настоящего изобретения -Pa', -Pa'' и Pa''' формулы (a) имеют молекулярную массу, равную около 20 кДа.
В одном варианте выполнения настоящего изобретения -Z содержит одну составляющую формулы (a).
В другом варианте выполнения настоящего изобретения -Z содержит две составляющие формулы (a).
В другом варианте выполнения настоящего изобретения -Z содержит три составляющие формулы (a).
Предпочтительно, -Z представляет собой составляющую формулы (a).
Более предпочтительно, -Z содержит составляющую формулы (b)
 (b),
(b),
где
пунктирная линия показывает присоединение к -L2- или к оставшейся части -Z; и
m и p независимо друг от друга представляют собой целое число в интервале и включительно от 150 до 1000; предпочтительно целое число в интервале и включительно от 150 до 500; более предпочтительно целое число в интервале и включительно от 200 до 500; и наиболее предпочтительно целое число в интервале и включительно от 400 до 500.
Предпочтительно, m и p формулы (b) представляют собой одно и то же целое число.
Наиболее предпочтительно m и p формулы (b) равны около 450.
Предпочтительно, -Z представляет собой составляющую формулы (b).
Носитель -Z' представляет собой не растворимый в воде полимер, даже более предпочтительно гидрогель. Предпочтительно, такой гидрогель содержит полимер, выбранный из группы, состоящей из 2-метакрилоил-оксиэтил фосфоилхолинов, поли(акриловых кислот), поли(акрилатов), поли(акриламидов), поли(алкилокси) полимеров, поли(амидов), поли(амидоаминов), поли(аминокислот), поли(ангидридов), поли(аспартамидов), поли(масляных кислот), поли(гликолевых кислот), полибутилентерефталатов, поли(капролактонов), поли(карбонатов), поли(цианоакрилатов), поли(диметилакриламидов), поли(сложных эфиров), поли(этиленов), поли(этиленгликолей), поли(этиленоксидов), поли(этилфосфатов), поли(этилоксазолинов), поли(гликолевых кислот), поли(гидроксиэтилакрилатов), поли(гидроксиэтил-оксазолинов), поли(гидроксиметакрилатов), поли(гидроксипропилметакриламидов), поли(гидроксипропил метакрилатов), поли(гидроксипропилоксазолинов), поли(иминокарбонатов), поли(молочных кислот), поли(сополимеров молочных и гликолевых кислот), поли(метакриламидов), поли(метакрилатов), поли(метилоксазолинов), поли(органофосфазенов), поли(ортосложных эфиров), поли(оксазолинов), поли(пропиленгликолей), поли(силоксанов), поли(уретанов), поли(виниловых спиртов), поли(виниламинов), поли(винилметиловых простых эфиров), поли(винилпирролидонов), силиконов, целлюлоз, карбометил целлюлоз, гидроксипропил метилцеллюлоз, хитинов, хитозанов, декстранов, декстринов, желатинов, гиалуроновых кислот и производных, функционализированных гиалуроновых кислот, маннанов, пектинов, рамногалактуронанов, крахмалов, гидроксиалкил крахмалов, гидроксиэтил крахмалов и других полимеров на основе углеводов, ксиланов и их сополимеров.
Если носитель -Z' представляет собой гидрогель, это предпочтительно гидрогель, содержащий ПЭГ или гиалуроновую кислоту. Наиболее предпочтительно такой гидрогель содержит ПЭГ.
Даже более предпочтительно, носитель -Z' представляет собой гидрогель, как раскрывается в WO 2006/003014 A2, WO 2011/012715 A1 или WO 2014/056926 A1, которые включены в настоящую заявку посредством ссылки в полном объеме.
В другом варианте выполнения настоящего изобретения -Z' представляет собой полимерную сеть, образованную посредством физической агрегации полимерных цепей, причем физическая агрегация предпочтительно вызвана водородными связями, кристаллизацией, спирализацией или комплексообразованием. В одном варианте выполнения настоящего изобретения такая полимерная сеть представляет собой термогелевый полимер.
Если ПТГ соединение контролируемого высвобождения согласно настоящему изобретению представляет собой пролекарство, его общая масса предпочтительно составляет по меньшей мере 10 кДа, как например по меньшей мере 12 кДа, как например по меньшей мере 15 кДа, как например по меньшей мере 20 кДа или как например по меньшей мере 30 кДа. Если ПТГ соединение контролируемого высвобождения представляет собой растворимое в воде пролекарство, его общая масса предпочтительно составляет самое большее 250 кДа, как например самое большее 200 кДа, 180 кДа, 150 кДа или 100 кДа. Понятно, что никакой значимый верхний предел молекулярной массы не может быть обеспечен в случае, если ПТГ соединение контролируемого высвобождения является нерастворимым в воде.
В одном предпочтительном варианте выполнения настоящего изобретения ПТГ соединение контролируемого высвобождения имеет формулу (IIe-i):
 (IIe-i),
(IIe-i),
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой ПТГ составляющую, посредством образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей

где
m и p независимо представляют собой целое число в интервале и включая 400 - 500.
Предпочтительно, -D присоединена к ПТГ пролекарству формулы (IIe-i) через N-концевую аминовую функциональную группу составляющей ПТГ.
В другом предпочтительном варианте выполнения настоящего изобретения пролекарство ПТГ согласно настоящему изобретению имеет формулу (IIf-i):
 (IIf-i),
(IIf-i),
где
неотмеченная пунктирная линия обозначает присоединение к атому азота составляющей -D, которая представляет собой ПТГ составляющую, посредством образования амидной связи; и
пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей

где
m и p независимо представляют собой целое число в интервале и включая 400 - 500.
Предпочтительно, -D присоединена к ПТГ пролекарству формулы (IIf-i) через N-концевую аминовую функциональную группу составляющей ПТГ.
В предпочтительном варианте выполнения настоящего изобретения остаточная активность ПТГ пролекарства составляет менее 10%, более предпочтительно менее 1%, даже более предпочтительно менее 0.1%, даже более предпочтительно менее 0.01%, даже более предпочтительно менее 0.001% и наиболее предпочтительно менее 0.0001%.
Как применяется в настоящей заявке термин “остаточная активность” относится к активности, проявляемой пролекарством ПТГ, где ПТГ составляющая связана с носителем, относительно активности, проявляемой соответствующим свободным ПТГ. В этом контексте термин «активность» относится к связыванию с доменом активации рецептора ПТГ/ПТГrP1, приводящий к активации аденилатциклазы с образованием cAMP, фосфолипазы C с образованием внутриклеточного кальция или остеобластной экспрессии RANKL (которая связывается с RANK (активатор рецептора ядерного фактора kB) на остеокластах. Понятно, что измерение остаточной активности ПТГ пролекарства согласно настоящему изобретению требует времени, в ходе которого определенное количество ПТГ будет высвобождено из пролекарства ПТГ согласно настоящему изобретению, и что такой высвобожденный ПТГ исказит результаты, измеренные для пролекарства ПТГ. Таким образом, на практике принято проводить испытание остаточной активности пролекарства с конъюгатом, в котором лекарственная составляющая, в данном случае ПТГ, является необратимой, т.е. стабильно связанной с носителем, который насколько это возможно, напоминает структуру пролекарства ПТГ, для которого должна быть измерена остаточная активность.
Предпочтительно, фармацевтическая композиция согласно настоящему изобретению имеет значение pH в интервале и включая pH 3 - pH 8. Более предпочтительно, фармацевтическая композиция имеет значение pH в интервале и включая pH 4 - pH 6. Наиболее предпочтительно, фармацевтическая композиция имеет значение pH в интервале и включая pH 4 - pH 5.
В одном варианте выполнения настоящего изобретения фармацевтическая композиция согласно настоящему изобретению представляет собой жидкую композицию или композицию в форме суспензии. Понятно, что фармацевтическая композиция представляет собой композицию в форме суспензии, если ПТГ соединение контролируемого высвобождения согласно настоящему изобретению является нерастворимым в воде.
В другом варианте выполнения настоящего изобретения фармацевтическая композиция согласно настоящему изобретению представляет собой сухую композицию, которую восстанавливают перед введением пациенту.
Такая жидкая фармацевтическая композиция, фармацевтическая композиция в виде суспензии, сухая или восстановленная фармацевтическая композиция содержит по меньшей мере один эксципиент. Эксципиенты, применяемые в парентеральных композициях, могут быть разделены на категории следующим образом, например, буферные средства, модификаторы изотоничности, консерванты, стабилизаторы, антиадсорбционные средства, средства защиты от окисления, загустители/вещества, увеличивающие вязкость, или другие вспомогательные средства. Однако, в некоторых случаях, один эксципиент может иметь двойные или тройные функции. Предпочтительно, по меньшей мере один эксципиент, содержащийся в фармацевтической композиции согласно настоящему изобретению выбирают из группы, состоящей из следующего:
(i) Буферные средства: физиологически допустимые буферы для поддержания значения pH в желаемом диапазоне, такие как фосфат натрия, бикарбонат, сукцинат, гистидин, цитрат и ацетат, сульфат, нитрат, хлорид, пируват; нейтролизаторы кислот, такие как Mg(OH)2 или ZnCO3 также могут применяться;
(ii) Модификаторы изотоничности: чтобы минимизировать боль, которая может стать результатом повреждения клеток в ходе разности осмотического давления при инъекции веществ замедленного всасывания; глицерин и хлорид натрия являются примерами; эффективные концентрации могут быть определены осмометрией, применяя допускаемую осмотическую концентрацию раствора, равную 285-315 мОсмоль/кг для сыворотки;
(iii) Консерванты и/или противомикробные средства: мультидозные парентеральные композиции требуют добавления консервантов при достаточной концентрации, чтобы минимизировать риск заражения пациента при инъекции, и соответствующие регулирующие требования должны быть установлены; типичные консерванты включают м-крезол, фенол, метилпарабен, этилпарабен, пропилпарабен, бутилпарабен, хлорбутанол, бензиловый спирт, фенилртути нитрат, тимерозол, сорбиновую кислоту, сорбат калия, бензойную кислоту, хлоркрезол, и бензалкония хлорид;
(iv) Стабилизаторы: Стабилизация достигается за счет усиления стабилизирующих белок сил, дестабилизации денатурированного состояния или прямого связывания эксципиентов с белком; стабилизаторами могут быть аминокислоты, такие как аланин, аргинин, аспарагиновая кислота, глицин, гистидин, лизин, пролин, сахара, такие как глюкоза, сахароза, трегалоза, полиолы, такие как глицерин, маннит, сорбит, соли, такие как фосфат калия, сульфат натрия, хелатирующие средства, такие как EDTA, гексафосфат, лиганды, такие как ионы двухвалентного металла (цинк, кальций и т.д.), другие соли или органические молекулы, такие как фенольные производные; кроме того, могут быть использованы олигомеры или полимеры, такие как циклодекстрины, декстран, дендримеры, ПЭГ или ПВП или протамин или HSA;
(v) Антиадсорбционные средства: В основном ионные или неионные поверхностно-активные вещества или другие белки или растворимые полимеры применяются для покрытия или конкурентным образом адсорбируются на внутренней поверхности контейнера композиции. Например, полоксамер (Pluronic F-68), ПЭГ додециловый простой эфир (Brij 35), полисорбат 20 и 80, декстран, полиэтиленгликоль, ПЭГ-полигистидин, BSA и HSA и желатины; выбранная концентрация и тип эксципиента зависит от эффекта, которого следует избегать, но обычно монослой поверхностно-активного вещества образуется на границе раздела фаз чуть выше значения CMC;
(vi) Средства защиты от окисления: антиоксиданты, такие как аскорбиновая кислота, эктоин, метионин, глутатион, монотиоглицерин, морин, полиэтиленимин (PEI), пропилгаллат и витамин Е; хелатирующие агенты, такие как лимонная кислота, EDTA, гексафосфат и тиогликолевая кислота, также могут применяться;
(vii) Загустители или вещества, увеличивающие вязкость: в случае суспензии замедляют осаждение частиц во флаконе и шприце и используются для облегчения смешивания и ресуспендирования частиц и для облегчения введения суспензии (т.е. с малой силой на шприцевом поршне); подходящими загустителями или усилителями вязкости являются, например, карбомерные загустители, такие как Carbopol 940, Carbopol Ultrez 10, производные целлюлозы, такие как гидроксипропилметилцеллюлоза (гипромеллоза, HPMC) или диэтиламиноэтилцеллюлоза (DEAE или DEAE-C), коллоидный силикат магния (Veegum) или силикат натрия, гидроксиапатитный гель, трикальцийфосфатный гель, ксантаны, каррагинаны, такие как камедь Satia UTC 30, алифатические поли(гидроксикислоты), как например поли(D, L- или L-молочная кислота) (PLA) и поли(гликолевая кислота) (PGA) и их сополимеры (PLGA), терполимеры D, L-лактида, гликолида и капролактона, полоксамеры, гидрофильные поли(оксиэтиленовые) блоки и гидрофобные поли(оксипропиленовые) блоки для создания триблока поли(оксиэтилен)-поли(оксипропилен)-поли(оксиэтилен) (например, Pluronic®), сополимер простого полиэфира и сложного полиэфира, как например сополимер терефталат полиэтиленгликоля/терефталат полибутилена, сахарозы ацетат изобутират (SAIB), декстран или его производные, комбинации декстранов и ПЭГ, полидиметилсилоксан, коллаген, хитозан, поливиниловый спирт (PVA) и производные, полиалкилимиды, поли(акриламид-со-диаллилдиметиламмоний (DADMA)), поливинилпирролидон (ПВП), глюкозаминогликаны (GAG), такие как дерматан сульфат, хондроитин сульфат, кератан сульфат, гепарин, гепаран сульфат, гиалуронан, ABA триблок- или AB блок-сополимеры, состоящие из гидрофобных А-блоков, как например, полилактид (PLA) или поли(лактид-со-гликолид) (PLGA) и гидрофильные B-блоки, как например полиэтилтенгликоль (ПЭГ) или поливинилпирролидон; такие блок-сополимеры, как и вышеупомянутые полоксамеры, могут проявлять обратимое термическое гелеобразование (состояние жидкости при комнатной температуре для облегчения введения и состояние геля выше температуры перехода золь-гель при температуре тела после инъекции);
(viii) Лиофилизирующий или диффундирующий агент: модифицирует проницаемость соединительной ткани посредством гидролиза компонентов внеклеточного матрикса во интерстициальном пространстве, таких как, но без ограничения к этому, гиалуроновая кислота, полисахарид, обнаруженные в межклеточном пространстве соединительной ткани; лиофилизирующий агент, такой как, но без ограничения к этому, гиалуронидаза, временно снижает вязкость внеклеточной матрицы и способствует диффузии инъецированных лекарственных средств; и
(ix) Другие вспомогательные средства: такие как смачивающие средства, модификаторы вязкости, антибиотики, гиалуронидаза; кислоты и основания, такие как соляная кислота и гидроксид натрия являются вспомогательными средствами, необходимыми для установления значения pH в ходе получения.
Другим объектом настоящего изобретения является способ лечения, контроля, замедления или профилактики у пациента-млекопитающего, например, пациента-человека, одного или более состояний, которые можно лечить, контролировать, замедлять или предупреждать с помощью ПТГ, включающий стадию введения фармацевтической композиции, содержащей по меньшей мере одно соединение ПТГ контролируемого высвобождения, один раз каждые 24 часа в дозировке, составляющей не более 70% молярной эквивалентной дозы ПТГ 1-84, необходимой для поддержания уровня кальция в сыворотке крови выше 8,5 мг/дл в течение 24 часов.
Предпочтительные варианты ПТГ соединения контролируемого высвобождения описаны выше.
Предпочтительно, состояние, которое можно лечить, контролировать, замедлять или предупреждать с помощью ПТГ, выбрано из группы, состоящей из гипопаратиреоидизма, гиперфосфатаземии, остеопороза, заживления трещин, размягчения костей, размягчения костей и остеопороза у пациентов с гипофосфатазией, стероид-индуцированного остеопороза, мужского остеопороза, артрита, остеoартрита, синдрома ломких костей, фиброзной дисплазии, ревматоидного артрита, болезни Паджета, гуморальной гиперкальцемии, связанной со злокачественным новообразованием, остеопении, заболевания пародонта, перелома костей, алопеции, вызванной химиотерапией алопеции и тромбоцитопении. Более предпочтительно, состояние, которое можно лечить, контролировать, замедлять или предупреждать с помощью ПТГ, выбрано из группы, состоящей из гипопаратиреоидизма, гиперфосфатаземии, заживления трещин, артрита, остеoартрита, ревматоидного артрита, остеопении, заболевания пародонта, перелома костей, алопеции, вызванной химиотерапией алопеции и тромбоцитопении.
Наиболее предпочтительно указанным состоянием является гипопаратиреоидизм.
Предпочтительно, пациент, проходящий лечение способом согласно настоящему изобретению, является пациентом-млекопитающим, предпочтительно человеком-пациентом.
Примеры
Вещества и Способы
ПТГ(1-34) с защищенной боковой цепью (SEQ ID NO:51) на TCP смоле, имеющей защитную Boc группу на N-конце и боковой цепью Lys26 с защитной ivDde группой (синтезирован согласно Fmoc-стратегии) получили у поставщиков стандартного пептидного синтеза.
ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце (синтезирован согласно Fmoc-стратегии) получили у поставщиков стандартного пептидного синтеза.
ПЭГ 2x20 кДа - малеимид, Sunbright GL2-400MA приобрели у NOF Europe N.V., Grobbendonk, Belgium. S-Тритил-6-меркаптогексановую кислоту приобрели у Polypeptide, Strasbourg, France. HATU получили у Merck Biosciences GmbH, Schwalbach/Ts, Germany. Fmoc-N-Me-Asp(OBn)-OH получили у Peptide International Inc., Louisville, KY, USA. Fmoc-Aib-OH приобрели у Iris Biotech GmbH, Marktredwitz, Germany. Все другие химические вещества и реагенты приобрели у Sigma Aldrich GmbH, Taufkirchen, Germany, если другой производитель не указан.
Соединение 11a (примеры 11-15) синтезировали согласно методике, описанной в примере WO29095479A2, пример 1.
Шприцы, оборудованные полиэтиленовой фриттой (MultiSynTech GmbH, Witten, Germany) применяли в качестве реакционных сосудов или на стадии промывки пептидных смол.
Общая методика удаления ivDde защитной группы у ПТГ с защищенной боковой цепью на смоле: смола предварительно разбухла в DMF в течение 30 мин, и растворитель удалили. Группу ivDde удаляли путем инкубации смолы с DMF/гидразин гидратом 4/1 (об./об., 2,5 мл/г смолы) в течение 8 х 15 мин. Для каждого этапа использовали свежий раствор DMF/гидразин гидрата. Наконец, смолу промыли DMF (10 х), DCM (10 х) и высушили в вакууме.
Общая методика удаления защитной группы Fmoc у защищенного ПТГ на смоле: смола предварительно набухала в ДМФ в течение 30 мин и растворитель удаляли. Группу Fmoc удаляли путем инкубации смолы с DMF/пиперидином/DBU 96/2/2 (об./об./об., 2,5 мл/г смолы) в течение 3 x 10 мин. Для каждой стадии использовали свежий раствор DMF/пиперидин/DBU. Наконец, смолу промывали DMF (10 х), DCM (10 х) и высушили в вакууме.
Очистка посредством ОФ-ВЭЖХ:
Для препаративной ОФ-ВЭЖХ применяли управляющее устройство Waters 600 и детектор 2487 Dual Absorbance, оборудованные следующими колонками: Waters XBridge™ BEH300 Prep C18 5 мкм, 150 x 10 мм, скорость потока 6 мл/мин, или Waters XBridge™ BEH300 Prep C18 10 мкм, 150 x 30 мм, скорость потока 40 мл/мин. Применяли линейные градиенты системы растворителей A (вода, содержащая 0.1 % TFA об./об. или 0.01 % конц. HCl об./об.) и системы растворителей B (ацетонитрил, содержащий 0.1 % TFA об./об. или 0.01 % конц. HCl об./об.). ВЭЖХ-фракции, содержащие продукт, объединяли и лиофилизировали, если иного не указано.
Флэш-хроматография
Очистки посредством флэш-хроматографии осуществляли на системе Isolera One от Biotage AB, Sweden, применяя картриджи с силикагелем Biotage KP-Sil и н-гептан и этилацетат в качестве элюентов. Продукты обнаруживали при 254 нм.
Ионообменная хроматография:
Ионообменную хроматографию (IEX) осуществили с использованием системы AERTAbasic Amersham Bioscience AEKTAbasic, оборудованной катионообменной колонкой MacroCap SP (Amersham Bioscience/GE Healthcare). В качестве подвижных фаз использовали 17 мМ уксусную кислоту с pH 4,5 (растворитель А) и 17 мМ уксусной кислоты, 1 М NaCl, рН 4,5 (растворитель В).
Эксклюзионная хроматография размеров:
Эксклюзионную хроматографию размеров (SEC) проводили с использованием системы Amersham Bioscience AEKTAbasic, оснащенной обессоливающей колонкой HiPrep 26/10 (Amersham Bioscience/GE Healthcare). 0.1 % (об./об.) уксусную кислоту применяли в качестве подвижной фазы.
Аналитические методы
Аналитическую сверхвысокоэффективную LC (UPLC)-MS проводили на системе Waters Acquity, оборудованной колонкой Waters BEH300 C18 (размер частиц 2,1 x 50 мм, размер частиц 1,7 мкм, поток: 0,25 мл/мин, растворитель A: вода, содержащая 0,04% TFA (об. /об.), Растворитель В: ацетонитрил, содержащий 0,05% TFA (об./об.)), соединенной с масс-спектрометром LTQ Orbitrap Discovery от Thermo Scientific или соединенной с Waters Microsass ZQ.
Количественное определение общих концентраций ПТГ(1-34) в плазме:
Общие концентрации ПТГ(1-34) в плазме определили посредством количественной оценки сигнатурного пептида, близкого к N-концу (последовательность: IQLMHNLGK), и С-концевого сигнатурного пептида (последовательность: LQDVHNF) после осаждения белка в плазме, с последующим секвенциальным расщеплением с применением эндопротеиназны Lys-C (происхождение: Lysobacter enzymogenes) и эндопротеиназны Glu-C (происхождение: Staphylococcus aureus V8) супернатанта. Затем, анализ посредством обращеннофазовой жидкостной хроматографии и обнаружение посредством масс-спектрометрии (RP-HPLC-MS) осуществили.
Стандарты для калибровки конъюгата ПТГ (1-34) в пустой гепаринизированной плазме были получены в диапазоне концентраций от 1 до 1000 нг/мл ПТГ (1-34) экв (разведение плазмой крысы) и от 1 до 1000 нг/мл ПТГ (1- 34) экв (разведение плазмой обезьяны).
Эти растворы были использованы для генерации калибровочной кривой. Для контроля качества были подготовлены три образца независимо от калибровочных стандартных растворов, соответственно. Концентрации на нижнем конце (3-5-кратная концентрация соответствующего LLOQ), средний диапазон (0,05 - 0,1-кратная концентрация соответствующего ULOQ) и верхний конец (0,5-0,8-кратная концентрация соответствующего ULOQ).
Объемы для получения образца могут быть изменены в зависимости от целевого ответа сигнала после получения образца. Процедура обработки осаждения белка описана здесь для анализа образцов плазмы, которые встречаются у видов обезьян. Осаждение белка проводили сначала путем добавления 100 мкл раствора внутреннего стандарта (625 нг/мл дейтерированного конъюгата) и затем путем добавления 400 мкл ацетонитрила к 50 мкл образца плазмы. 2 раза 150 мкл супернатанта переносили на новый луночный планшет и выпаривали досуха (под мягким потоком азота при 50°C). Для растворения остатка использовали 50 мкл восстанавливающего растворителя (50 мМ Трис 0,5 мМ CaCl2 буфер, довели до рН 8,0). Протеолитическое расщепление осуществили следующим образом:
20 мкг Lys-C (порядковый номер 125-05061, Wako Chemicals GmbH, Neuss, Germany) растворили в 80 мкл 10 мM уксусной кислоты. 3 мкл раствора Lys-C добавили в каждый лунку, и образцы инкубировали в течение 15 часов 37°C. Затем 10 мкг Glu-C (порядковый номер V1651, Promega GmbH, Mannheim, Germany) растворили в 25 мкл воды, добавили в каждую лунку, и инкубацию продолжали в течение 1.5 часов при 37°C. После инкубирования образцы подкислили с помощь 2 мкл воды/муравьиной кислоты 4:6 (об./об.) и 10 мкл ввели в UPLC-MS систему.
Хроматографию осуществляли на аналитической колонке Waters Acquity BEH300 C18 (размер частиц 1,7 мкм, размеры применяемой колонки составляли 50x2,1 мм). В качестве подвижной фазы А использовали воду (марка UPLC), содержащую 0,1% муравьиную кислоту (об./об.), и в качестве подвижной фазы В применяли ацетонитрил (марка UPLC) с 0.1 % муравьиной кислотой.
Масс-анализ проводили на AB Sciex 6500+ QTrap в режиме мониторинга множественных реакций (MRM), отслеживая переход m/z 352.0 - 462.1 (сигнатурный пептид IQLMHNLGK), 355.4 - 467.1 (сигнатурный пептид IQLMHNLGK, внутренний стандарт), 436.9 - 631.4 (сигнатурный пептид LQDVHNF), и 441.9 - 631.4 (сигнатурный пептид LQDVHNF, внутренний стандарт).
Количественное определение концентраций ПЭГ в плазме:
Концентрации общего ПЭГ в плазме определили посредством количественной оценки полимерной части конъюгатов ПТГ(1-34) после осаждения белка в плазме и ферментативного расщепления супернатанта. Анализ посредством экслюзионной хроматографии по размеру и обнаружение посредством масс-спектрометрии (SEC-MS) последовали.
Калибровочные стандарты конъюгата ПТГ(1-34) в пустой гепаринизированной плазме макак были получены в диапазоне концентраций от 50 до 4500 нг/мл эквивалентов ПЭГ.
Эти решения были использованы для генерации квадратичной калибровочной кривой. Калибровочные кривые были увеличены 1/x. Для контроля качества были подготовлены три образца независимо от калибровочных стандартных растворов, соответственно. Концентрации на нижнем конце (2-4-кратная концентрация LLOQ), средний диапазон (0,1 - 0,2-кратная концентрация ULOQ) и верхний конец (0,8-кратная концентрация ULOQ). Осаждение белка проводили путем добавления 200 мкл предварительно охлажденного (5-10°C) метанола до 100 мкл образца плазмы. 180 мкл супернатанта переносили в новый луночный планшет и выпаривали досуха (под мягким потоком азота при 45°С). Для растворения остатка использовали 50 мкл восстанавливающего растворителя (50 мM Tris 0.5 мM CaCl2 буфер, довели до pH 8.0). Протеолитическое расщепление осуществляли следующим образом: 20 мкг Lys-C (порядковый номер 125-05061, Wako Chemicals GmbH, Neuss, Germany) растворили в 80 мкл 10 мM уксусной кислоты. 3 мкл раствора Lys-C добавили в каждый лунку, и образцы инкубировали в течение 15 часов 37°C. Затем 10 мкг Glu-C (порядковый номер V1651, Promega GmbH, Mannheim, Germany) растворили в 25 мкл воды, добавили в каждую лунку, и инкубацию продолжали в течение 1.5 часов при 37°C. После инкубирования образцы подкислили с помощь 2 мкл воды/муравьиной кислоты 4:6 (об./об.) и 10 мкл ввели в UPLC-MS систему.
Анализ LC-MS проводили с использованием Agilent 1290 UPLC, соединенного с масс-спектрометром Agilent 6460 TripleQuad с помощью зонда ESI. Получение отдельного ионного предшественника полимера было достигнуто путем применения высоковольтной фрагментация в источнике ионов (200-300 В) на MS-поверхности раздела. Хроматографию осуществляли на аналитической колонке TOSOH TSK Gel SuperAW3000 (размер частиц 4,0 мкм, размеры колонки 150 x 6.0 мм) при скорости потока 0,50 мл/мин (T = 60°C). В качестве подвижной фазы А использовали воду (марка UPLC), содержащую 0,1% муравьиную кислоту (об./об.), и в качестве подвижной фазы В применяли ацетонитрил (марка UPLC) с 0.1 % муравьиной кислотой. Хроматографическая установка для анализа образцов включает изократное элюирование с 50% В в течение 8 минут.
Анализ масс осуществили в режиме мониторинга отдельной реакции (SRM), контролируя переход m/z от 133.1 до 45.1.
Количественная оценка концентраций свободного ПТГ в плазме:
Концентрации свободного ПТГ в подкисленной плазме определяли как сумму пептидного ПТГ (1-34) и пептидного ПТГ (1-33) после осаждения белков плазмы с последующей твердофазной экстракцией. Впоследствии был проведен анализ с использованием жидкостной хроматографии, разделения и детектирования с помощью масс-спектрометрии (LC-MS).
Калибровочные стандарты ПТГ (1-34) и ПТГ (1-33) в ссылочной подкисленной крысиной ЭДТА плазме получали при концентрациях от 5,00 до 500 пг/мл в подкисленной плазме для каждого аналита. Соответствующий диапазон концентраций составляет от 7,00 до 700 пг/мл для обоих аналитов в чистой плазме, так как плазма подкисляется при объемном соотношении плазма: 0,5 М цитратный буфер, рН 4 = 1: 0,4 об/об.
Стандартные растворы были использованы для получения калибровочной кривой. Для контроля качества были приготовлены три образца независимо от стандартных калибровочных растворов при 15,0, 150 и 400 пг/мл в подкисленной плазме.
Осаждение белка осуществляли путем добавления 150 мкл холодного ацетонитрила к 150 мкл образца плазмы после добавления 50,0 мкл холодного раствора внутреннего стандарта с последующим центрифугированием. Надосадочную жидкость декантировали в новую пробирку из полипропилена и добавляли 900 мкл холодной воды. После очередной стадии центрифугирования пробирки хранили в воде со льдом до загрузки на колонку SPE.
Твердофазная экстракция: колонки для элюирования HLB кондиционировали с помощью 200 мкл метанола, а затем 200 мкл воды. В колонки загружали 3 раза 420 мкл разведенных образцов, применяя положительное давление. SPE-колонки промывали с помощью 200 мкл смеси метанол:вода 5:95 об/об. Образцы элюировали с помощью 40,0 мкл элюирующего растворителя SPE (ацетонитрил: вода: трифторуксусная кислота 60: 40: 1 об/об/об), а затем 40,0 мкл воды. Растворитель для элюирования оставляли стоять на колонках в течение 2 минут, после чего для элюирования применяли очень слабое давление.
Разделение между метаболитами и вмешивающимися эндогенными соединениями было достигнуто с помощью LC-MS с использованием колонки Xselect CSH C18 (2,1х100 мм, 2,5 мкм) при 50°С и с использованием 0,2% муравьиной кислоты и 0,5% диметилсульфоксида в воде в качестве подвижной фазы А, 0,5% диметилсульфоксида в ацетонитриле: метаноле (75:25, об./об.) в качестве подвижной фазы B, и при работе с градиентом при скорости потока 0,500 мл/мин
Тройной квадрупольный масс-спектрометр 6500, оборудованный турбоисточником ионораспыления, использовали для обнаружения в режиме положительных ионов. Для ПТГ (1-34), ПТГ (1-33) и ПТГ (1-33) (Leu-d10) 3 количественное определение было выполнено путем подсчета 5 раз одного и того же SRM перехода.
Количественная оценка основана на мониторинге множественных реакций (MRM) переходов m/z:
687.3-787.3 для ПТГ(1-34)
662.8-757.9 для ПТГ(1-33)
692.3-793.3 для ПТГ(1-34) (Leu-d10)3
667.8-763.9 для ПТГ(1-33) (Leu-d10)3
Линейная калибровочная кривая с массовым коэффициентом 1/x2 была использована для обоих аналитов.
Концентрации свободного ПТГ определяли в подкисленной плазме в качестве средства для стабилизации аналитов. Подкисленную плазму получали путем разведения крысиной ЭДТА плазмы в 1,4 раза (в случае пустых, нулевых, калибровочных и QC-образцов) или цельной крови крысы (в случае исследуемых образцов) в 1,2 раза. Предполагая, что приблизительно 50% (об/об) цельной крови является плазмой, чистые концентрации в плазме примерно в 1,4 раза выше, чем заявленные концентрации в подкисленной плазме. Концентрации свободного ПТГ рассчитывали как сумму свободного ПТГ (1-34) и свободного ПТГ (1-33) в эквивалентах ПТГ (1-34).
Из-за обратимого характера присоединения -L1- к -D измерения рецепторной активности ПТГ проводились с использованием стабильных аналогов пролекарств ПТГ согласно настоящему изобретению, т.е. они были получены с использованием аналогичных структур пролекарствам ПТГ согласно настоящему изобретению, которые вместо обратимого присоединения -Z к -D имеют стабильное присоединение.
Это было необходимо, потому что пролекарства ПТГ согласно настоящему изобретению, могло бы высвободить ПТГ в ходе эксперимента, и указанное высвобождение ПТГ повлияло бы на результат.
Пример 1
Синтез линкерного реагента 1f
Линкерный реагент 1f синтезировали согласно следующей схеме:
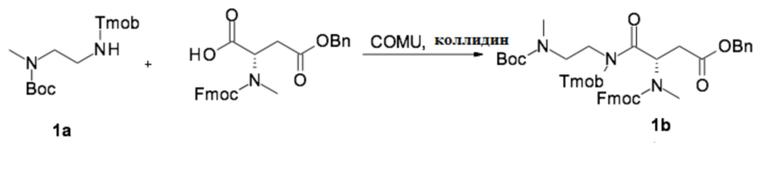


В раствор N-метил-N-Boc-этилендиамина (2 г, 11.48 ммоль) и NaCNBH3 (819 мг, 12.63 ммоль) в MeOH (20 мл) добавили 2,4,6-триметоксибензальдегид (2.08 г, 10.61 ммоль) частями. Смесь перемешивали при комнатной температуре в течение 90 мин, подкислили 3 M HCl (4 мл) и перемешивали еще 15 мин. Реакционную смесь добавили в насыщенный NaHCO3 (200 мл) и экстрагировали 5 x с помощью DCM. Объединенные органические фазы высушили над Na2SO4, и растворители выпарили в вакууме. Полученный N-метил-N-Boc-N'-Tmob-этилендиамин 1a высушили под высоким вакуумом и применяли на следующей стадии без дальнейшей стадии.
Выход: 3.76 г (11.48 ммоль, 89 % чистота, 1a: дважды Tmob защищенный продукт = 8 :1)
MS: m/z 355.22 = [M+H]+, (вычисленная моноизотопная масса = 354.21).
К раствору 1a (2 г, 5.65 ммоль) в CH2Cl2 (24 мл) COMU (4.84 г, 11.3 ммоль), N-Fmoc-N-Me-Asp(OBn)-OH (2.08 г, 4.52 ммоль) и 2,4,6-коллидин (2.65 мл, 20.34 ммоль) добавили. Реакционную смесь перемешивали в течение 3 ч при комнатной температуре, разбавили с помощью CH2Cl2 (250 мл) и промыли 3 x с помощью 0.1 M H2SO4 (100 мл) и 3 x с помощью соляного раствора (100 мл). Водные фазы повторно экстрагировали с помощью CH2Cl2 (100 мл). Объединенные органические фазы высушили над Na2SO4, отфильтровали, и остаток концентрировали до объема 24 мл. Соединение 1b очистили, применяя флэш-хроматографию.
Выход: 5.31 г (148 %, 6.66 ммоль)
MS: m/z 796.38 = [M+H]+, (вычисленная моноизотопная масса = 795.37).
К раствору 1b (5.31 г, макс. 4.52 ммоль, обозначается как N-Fmoc-N-Me-Asp(OBn)-OH) в THF (60 мл) DBU (1.8 мл, 3 % об./об.) добавили. Раствор перемешивали в течение 12 мин при комнатной температуре, разбавили с помощью DCM (400 мл) и промыли 3 x с помощью 0.1 M H2SO4 (150 мл) и 3 x с помощью соляного раствора (150 мл). Водные фазы повторно экстрагировали с помощью DCM (100 мл). Объединенные органические фазы высушили над Na2SO4 и отфильтровали. Соединение 1c выделили при выпаривании растворителя и применяли на следующей стадии без дальнейшей очистки.
MS: m/z 574.31 = [M+H]+, (вычисленная моноизотопная масса = 573.30).
Соединение 1c (5.31 г, 4.52 ммоль, неочищенное) растворили в ацетонитриле (26 мл) и COMU (3.87 г, 9.04 ммоль), 6-тритилмеркаптокапроновую кислоту (2.12 г, 5.42 ммоль) и 2,4,6-коллидин (2.35 мл, 18.08 ммоль) добавили. Реакционную смесь перемешивали в течение 4 ч при комнатной температуре, разбавили с помощью DCM (400 мл) и промыли 3 x с помощью 0.1 M H2SO4 (100 мл) и 3 x с помощью соляного раствора (100 мл). Водные фазы повторно экстрагировали с помощью DCM (100 мл). Объединенные органические фазы высушили над Na2SO4, отфильтровали и 1d выделили при выпаривании растворителя. Продукт 1d очистили, применяя флэш-хроматографию.
Выход: 2.63 г (62 %, 94 % чистота)
MS: m/z 856.41 = [M+H]+, (вычисленная моноизотопная масса = 855.41).
К раствору 1d (2.63 г, 2.78 ммоль) в i-PrOH (33 мл) и H2O (11 мл) добавили LiOH (267 мг, 11.12 ммоль), и реакционную смесь перемешивали в течение 70 мин при комнатной температуре. Смесь разбавили с помощью DCM (200 мл) и промыли 3 x с помощью 0.1 M H2SO4 (50 мл) и 3 x с помощью соляного раствора (50 мл). Водные фазы повторно экстрагировали с помощью DCM (100 мл). Объединенные органические фазы высушили над Na2SO4, отфильтровали, и соединение 1e выделили при выпаривании растворителя. Соединение 1e очистили, применяя флэш-хроматографию.
Выход: 2.1 г (88 %)
MS: m/z 878.4 = [M+Na]+, (вычисленная моноизотопная масса = 837.40).
К раствору 1e (170 мг, 0.198 ммоль) в безводном DCM (4 мл) добавили DCC (123 мг, 0.59 ммоль) и каталитическое количество DMAP. Через 5 мин N-гидрокси-сукцинимид (114 мг, 0.99 ммоль) добавили, и реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Реакционную смесь отфильтровали, растворитель удалили в вакууме, и остаток растворили в 90 % ацетонитриле плюс 0.1 % TFA (3.4 мл). Неочищенную смесь очистили посредством ОФ-ВЭЖХ. Фракции продукта нейтрализовали с помощью 0.5 M pH 7.4 фосфатного буфера и концентрировали. Оставшуюся водную фазу экстрагировали с помощью DCM, и 1f выделили при выпаривании растворителя.
Выход: 154 мг (81%)
MS: m/z 953.4 = [M+H]+, (вычисленная моноизотопная масса = 952.43).
Пример 2
Синтез линкерного реагента 2g

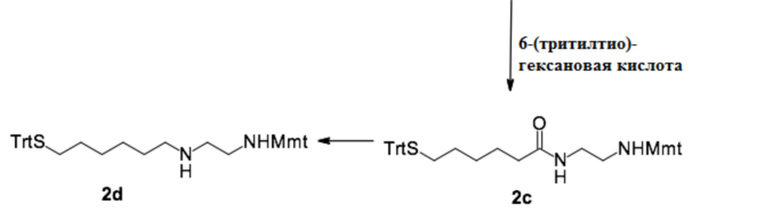

4-метокситрифенилметил хлорид (3.00 г, 9.71 ммоль) растворили в DCM (20 мл) и добавили по каплям при перемешивании в раствор этилендиамин 2a (6.5 мл, 97.3 ммоль) в DCM (20 мл). Реакционную смесь перемешивали в течение 2 ч при комнатной температуре, после чего его разбавили диэтиловым простым эфиром (300 мл), промыли 3 x соляным раствором/0.1 M NaOH 30/1 (об./об.) и один раз соляным раствором. Органическую фазу высушили над Na2SO4, и соединение 2b выделили при выпаривании растворителя.
Выход: 3.18 г (98%)
Mmt-защищенное промежуточное соединение 2b (3.18 г, 9.56 ммоль) растворили в DCM (30 мл). 6-(Тритилтио)-гексановую кислоту (4.48 г, 11.5 ммоль), PyBOP (5.67 г, 10.9 ммоль) и DIPEA (5.0 мл, 28.6 ммоль) добавили, и смесь перемешивали в течение 30 минут при комнатной температуре. Раствор разбавили простым диэтиловым эфиром (250 мл), промыли 3 x соляным раствором/0.1 M NaOH 30/1 (об./об.) и один раз соляным раствором. Органическую фазу высушили над Na2SO4, и растворитель удалили в вакууме. 2c очистили, применяя флэш-хроматографию.
Выход: 5.69 г (85 %)
MS: m/z 705.4 = [M+H]+, (вычисленная моноизотопная масса = 704.34).
Соединение 2c (3.19 г, 4.53 ммоль) растворили в безводном THF (50 мл), 1 M BH3·THF раствор в THF (8.5 мл, 8.5 ммоль) добавили, и смесь перемешивали в течение 16 ч при комнатной температуре. Еще 1 M BH3·THF раствор в THF (14 мл, 14.0 ммоль) добавили, и смесь перемешивали в течение еще 16 ч при комнатной температуре. Метанол (8.5 мл) и N,N'-диметил-этилендиамин (3.00 мл, 27.9 ммоль) добавили, и смесь нагревали с обратным холодильников в течение 3 ч. Смеси позволили охладиться, и этилацетат (300 мл) добавили. Раствор промыли 2 x водным Na2CO3 и 2 x водным NaHCO3. Органическую фазу высушили над Na2SO4, и растворитель удалили в вакууме с получением соединения 2d.
Выход: 3.22 г (103 %)
MS: m/z 691.4 = [M+H]+, (вычисленная моноизотопная масса = 690.36).
Ди-трет-бутил дикарбонат (2.32 г, 10.6 ммоль) и DIPEA (3.09 мл, 17.7 ммоль) растворили в DCM (5 мл) и добавили в раствор 2d (2.45 г, 3.55 ммоль) в DCM (5 мл). Смесь перемешивали в течение 30 минут при комнатной температуре. Раствор концентрировали в вакууме и очистили с применением флэш-хроматографии с получением продукта 2e.
Выход: 2.09 г (74 %)
MS: m/z 791.4 = [M+H]+, (вычисленная моноизотопная масса = 790.42).
Соединение 2e (5.01 г, 6.34 ммоль) растворили в ацетонитриле (80 мл). 0.4 M водную HCl (80 мл), а затем ацетонитрил (20 мл) добавили, и смесь перемешивали в течение 1 ч при комнатной температуре. Значение pH довели до pH 5.5 посредством добавления водного 5 M NaOH. Органический растворитель удалили в вакууме, и оставшийся водный раствор экстрагировали 4 x с помощью DCM. Объединенные органические фазы высушили над Na2SO4, и растворитель удалили в вакууме с получением продукта 2f.
Выход: 4.77 г (95 %)
MS: m/z 519.3 = [M+H]+, (вычисленная моноизотопная масса = 518.30).
Соединение 2f (5.27 г, 6.65 ммоль) растворили в DCM (30 мл) и добавили в раствор п-нитрофенил флорформиата (2.01 г, 9.98 ммоль) в DCM (25 мл). 2,4,6-триметилпиридин (4.38 мл, 33.3 ммоль) добавили, и раствор перемешивали в течение 45 минут при комнатной температуре. Раствор концентрировали в вакууме и очистили с применением флэш-хроматографии с получением продукта 2g.
Выход: 4.04 г (89 %)
MS: m/z 706.32 = [M+Na]+, (вычисленная моноизотопная масса = 683.30).
Пример 3
Синтез перманентного конъюгата S1 ПТГ(1-34) 3

ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце подвергли удалению Fmoc защитной группы согласно методике, приведенной в части Вещества и способы. Раствор 6-тритилмеркаптогексановой кислоты (62.5 мг, 160 мкмоль), PyBOP (80.1 мг, 154 мкмоль) и DIPEA (53 мкл, 306 мкмоль) в DMF (2 мл) добавили к 0.21 г (51 мкмоль) смолы. Суспензию встряхивали в течение 80 минут при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 10 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 3 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 36 мг (14 %), 3*8 TFA
MS: m/z 1062.31 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1062.30).
Пример 4
Синтез перманентного конъюгата K26 ПТГ(1-34) 4

ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Boc группу на N-конце и боковой цепью Lys26 с защитной ivDde группой подвергли удалению ivDde защитной группы согласно методике, приведенной в части Вещества и способы. Раствор 6-тритилмеркаптогексановой кислоты (107 мг, 273 мкмоль), PyBOP (141 мг, 273 мкмоль) и DIPEA (95 мкл, 545 мкмоль) в DMF (3 мл) добавили к 0.80 г (90.9 мкмоль) смолы. Суспензию встряхивали в течение 1 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 6 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 4 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 40 мг (8 %), 4*8 TFA
MS: m/z 1062.30 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1062.30).
Пример 5
Синтез временного конъюгата S1 ПТГ(1-34)

ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце подвергли удалению Fmoc защитной группы согласно методике, приведенной в части Вещества и способы. Раствор Fmoc-Aib-OH (79 мг, 244 мкмоль), PyBOP (127 мг, 244 мкмоль) и DIPEA (64 мкл, 365 мкмоль) в DMF (1.5 мл) добавили к 0.60 г (61 мкмоль) смолы. Суспензию встряхивали в течение 16 ч при комнатной температуре. Смолу промыли 10 x с DMF и подвергли удалению Fmoc защитной группы, как описано выше. Раствор соединения 2g (167 мг, 244 мкмоль) и DIPEA (64 мкл, 365 мкмоль) в DMF (1.5 мл) добавили к смоле. Суспензию встряхивали в течение 24 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 7 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 5 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 78 мг (24 %), 5*9 TFA
MS: m/z 1101.59 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1101.57).
Пример 6
Синтез временного конъюгата S1 ПТГ(1-34) 6
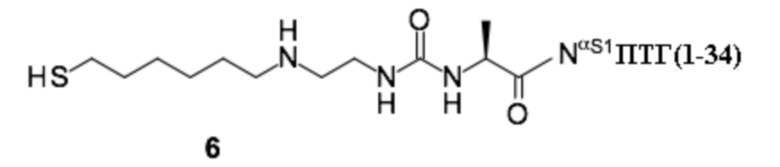
ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце подвергли удалению Fmoc защитной группы согласно методике, приведенной в части Вещества и способы. Раствор Fmoc-Ala-OH (32 мг, 102 мкмоль), PyBOP (53 мг, 102 мкмоль) и DIPEA (27 мкл, 152 мкмоль) в DMF (3 мл) добавили к 0.25 г (25 мкмоль) смолы. Суспензию встряхивали в течение 1 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Удаление защитной группы Fmoc осуществили, как описано выше. Раствор соединения 2g (69 мг, 102 мкмоль) и DIPEA (27 мкл, 152 мкмоль) в DMF (3 мл) добавили к смоле. Суспензию встряхивали в течение 1.5 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 3 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 6 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 25 мг (18 %), 6*9 TFA
MS: m/z 1098.75 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1098.07).
Пример 7
Синтез временного конъюгата S1 ПТГ(1-34) 7

ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце подвергли удалению Fmoc защитной группы согласно методике, приведенной в части Вещества и способы. Раствор Fmoc-Ser(Trt)-OH (117 мг, 205 мкмоль), PyBOP (108 мг, 207 мкмоль) и DIPEA (53 мкл, 305 мкмоль) в DMF (2 мл) добавили к 0.50 г (51 мкмоль) смолы. Суспензию встряхивали в течение 1 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Удаление защитной группы Fmoc осуществили, как описано выше. Раствор 2g (144 мг, 211 мкмоль) и DIPEA (53 мкл, 305 мкмоль) в DMF (1.8 мл) добавили к смоле. Суспензию встряхивали в течение 7 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 6 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 7 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 54 мг (20 %), 7*9 TFA
MS: m/z 1102.08 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1102.07).
Пример 8
Синтез временного конъюгата S1 ПТГ(1-34) 8
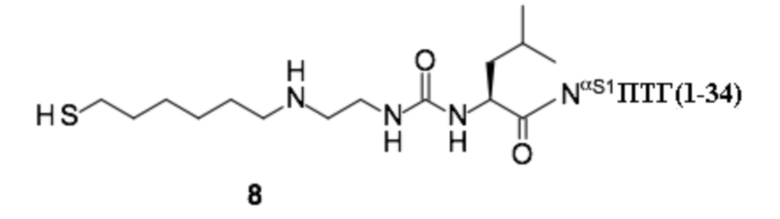
ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце подвергли удалению Fmoc защитной группы согласно методике, приведенной в части Вещества и способы. Раствор Fmoc-Leu-OH (36 мг, 102 мкмоль), PyBOP (53 мг, 102 мкмоль) и DIPEA (27 мкл, 152 мкмоль) в DMF (3 мл) добавили к 0.25 г (25 мкмоль) смолы. Суспензию встряхивали в течение 1 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Удаление защитной группы Fmoc осуществили, как описано выше. Раствор соединения 2g (69 мг, 102 мкмоль) и DIPEA (27 мкл, 152 мкмоль) в DMF (3 мл) добавили к смоле. Суспензию встряхивали в течение 1.5 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 3 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 8 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 31 мг (22 %), 8*9 TFA
MS: m/z 1109.32 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1108.58).
Пример 9
Синтез временного конъюгата S1 ПТГ(1-34) 9
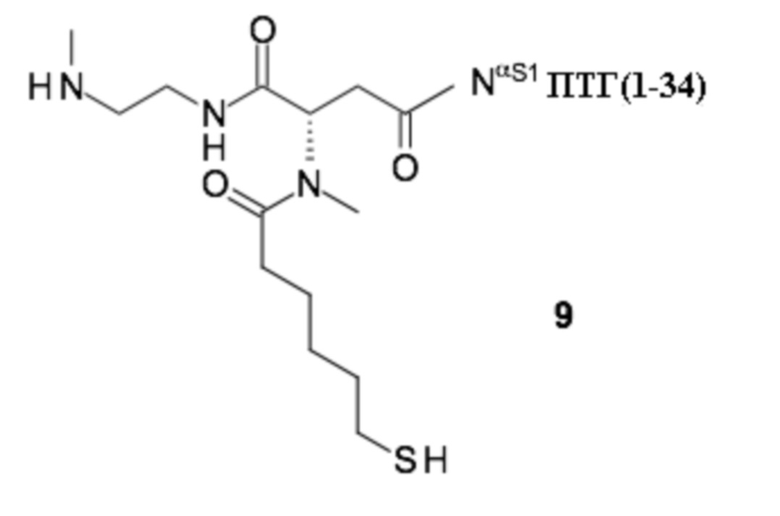
ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Fmoc группу на N-конце подвергли удалению Fmoc защитной группы согласно методике, приведенной в части Вещества и способы. Раствор соединения 1e (182 мг, 213 мкмоль), PyBOP (111 мг, 213 мкмоль) и DIPEA (93 мкл, 532 мкмоль) в DMF (5 мл) добавили к 2.00 г (107 мкмоль) смолы. Суспензию встряхивали в течение 16 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 20 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 9 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 47 мг (8 %), 9*9 TFA
MS: m/z 1108.58 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1108.57).
Пример 10
Синтез временного конъюгата K26 ПТГ(1-34) 10

ПТГ(1-34) с защищенной боковой цепью на TCP смоле, имеющей защитную Boc группу на N-конце и боковой цепью Lys26 с защитной ivDde группой подвергли удалению ivDde защитной группы согласно методике, приведенной в части Вещества и способы. Раствор соединения 1f (867 мг, 910 мкмоль) и DIPEA (0.24 мл, 1.36 ммоль) в DMF (5 мл) добавили к 1.91 г (227 мкмоль) смолы. Суспензию встряхивали в течение 1 ч при комнатной температуре. Смолу промыли 10 x с DMF, 10 x с DCM и высушили в вакууме. Отщепление пептида от смолы и удаление защитных групп достигали посредством добавления 20 мл расщепляющего коктейля 100/3/3/2/1 (об./мас./об./об./об.) TFA/DTT/TES/вода/тиоанизол и встряхивания суспензии в течение 1 ч при комнатной температуре. Неочищенное соединение 10 осадили в предварительно охлажденном простом диэтиловом эфире (-18°C). Осадок растворили в ACN/вода и очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали.
Выход: 92 мг (7 %), 10*9 TFA
MS: m/z 1108.58 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1108.57).
Пример 11
Синтез низкомолекулярного временного конъюгата S1 ПЭГ 11b

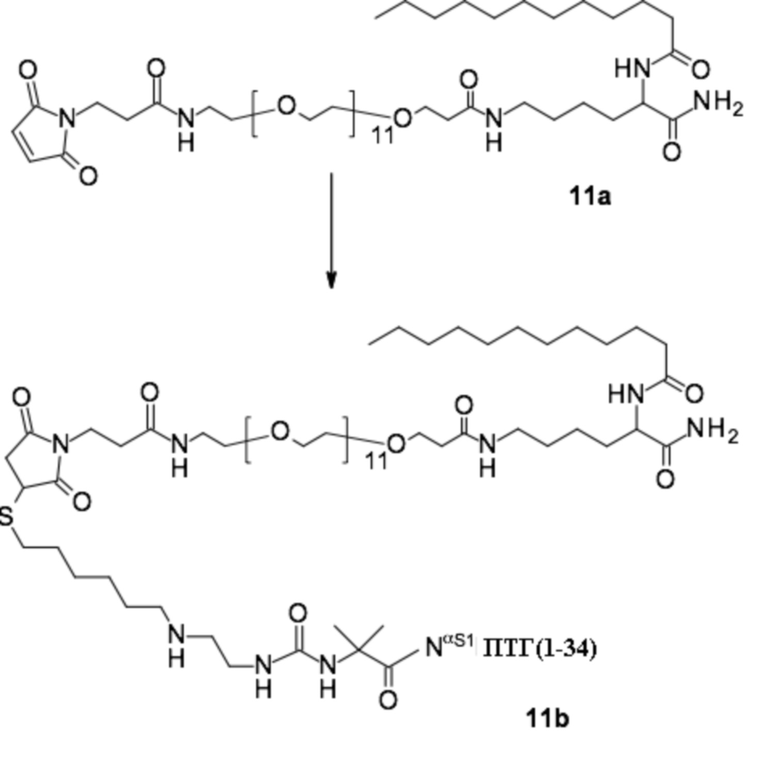
0.15 мл 0.5 M NaH2PO4 буфера (pH 7.4) добавили к 0.5 мл 20 мг/мл раствора тиола 5 (10 мг, 1.84 мкмоль) в 1/1 (об./об.) ацетонитрила/воды, содержащей 0.1 % TFA (об./об.). Раствор инкубировали при комнатной температуре в течение 10 минут, после чего 238 мкл 10 мг/мл раствора малеимида 11a (2.4 мг, 2.21 мкмоль) в 1/1 (об./об.) ацетонитрил/вода, содержащая 0.1 % TFA (об./об.) , добавили. Раствор инкубировали в течение 20 минут при комнатной температуре. 10 мкл TFA добавили, и смесь очистили посредством ОФ-ВЭЖХ. Фракции продукта лиофилизировали с получением соединения 11b.
Выход: 3.1 мг (26 %), 11b*9 TFA
MS: m/z 1097.00 = [M+4H]4+, (вычисленная моноизотопная масса для [M+5H]5+ = 1096.99).
Пример 12
Синтез низкомолекулярного временного конъюгата S1 ПЭГ 12
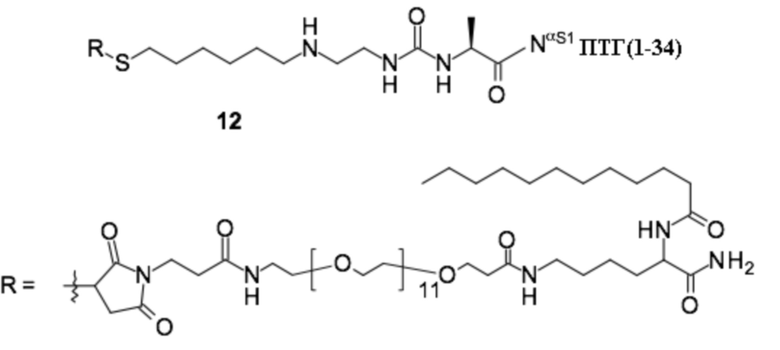
Конъюгат 12 синтезировали, как описано для 11b посредством применения тиола 6 (10 мг, 1.85 мкмоль) и малеимида 11a (2.4 мг, 2.21 мкмоль).
Выход: 10 мг (83 %), 12*9 TFA
MS: m/z 1094.20 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1094.19).
Пример 13
Синтез низкомолекулярного временного конъюгата S1 ПЭГ 13
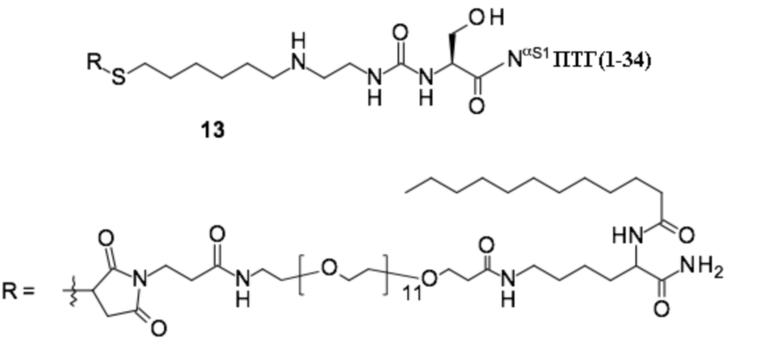
Конъюгат 13 синтезировали, как описано для 11b посредством применения тиола 7 (10 мг, 1.84 мкмоль) и малеимида 11a (2.4 мг, 2.21 мкмоль).
Выход: 8 мг (67 %), 13*9 TFA
MS: m/z 1097.40 = [M+5H]5+, (вычисленная моноизотопная масса для [M+5H]5+ = 1097.39).
Пример 14
Синтез низкомолекулярного временного конъюгата S1 ПЭГ 14

Конъюгат 14 синтезировали, как описано для 11b посредством применения тиола 8 (10 мг, 1.83 мкмоль) и малеимида 11a (2.4 мг, 2.21 мкмоль).
Выход: 4 мг (33 %), 14*9 TFA
MS: m/z 1378.01 = [M+4H]4+, (вычисленная моноизотопная масса для [M+4H]4+ = 1378.00).
Пример 15
Синтез низкомолекулярного временного конъюгата K26 ПЭГ 15
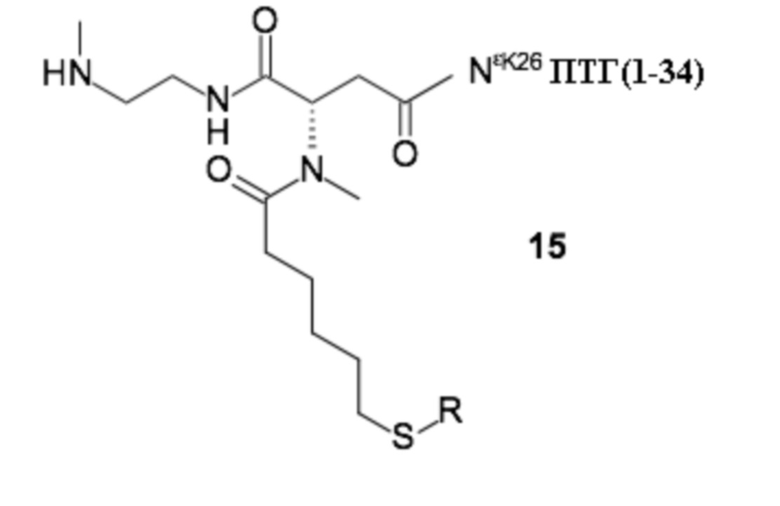

Конъюгат 15 синтезировали, как описано для 11b посредством применения тиола 10 (5.2 мг, 0.95 мкмоль) и малеимида 11a (1.23 мг, 1.14 мкмоль).
Выход: 2.1 мг (33 %), 15*9 TFA
MS: m/z 1102.60 = [M+5H]5+, (вычисленная моноизотопная масса для [M+5H]5+ = 1102.59).
Пример 16
Синтез перманентного конъюгата 2x20 кДа S1 ПЭГ 16

772 мкл раствора, содержащего тиол 3 (19.4 мг/мл, 15 мг, 3.54 мкмоль) и 2.5 мг/мл Boc-L-Met в 1/1 (об./об.) ацетонитрил/вода, содержащая 0.1 % TFA (об./об.), добавили к 1.87 мл раствора, содержащего ПЭГ 2x20 кДа - малеимид (Sunbright GL2-400MA, 187 мг, 4.32 мкмоль) и 2.5 мг/мл Boc-L-Met в воде, содержащей 0.1 % TFA (об./об.). 0.5 M NaH2PO4 буфера (0.66 мл, pH 7.0) добавили, и смесь перемешивали в течение 30 минут при комнатной температуре. 10 мкл 270 мг/мл раствора 2-меркаптоэтанола в воде добавили. Смесь перемешивали в течение 5 минут при комнатной температуре и 0.33 мл 1 M HCl добавили. Конъюгат 16 очистили посредством IEX с последующей ОФ-ВЭЖХ, применяя линейный градиент системы растворителей A (вода, содержащая 0.1 % AcOH об./об.) и системы растворителей B (ацетонитрил, содержащий 0.1 % AcOH об./об.). Фракции, содержащие раствор, лиофилизировали.
Выход: 97 мг (2.01 мкмоль, 57 %) конъюгата 16*8 AcOH
Пример 17
Синтез перманентного конъюгата 2x20 кДа K26 ПЭГ 17

Конъюгат 17 получили как описано для 16 посредством реакции тиола 4 (15 мг, 3.53 мкмоль) и ПЭГ 2x20 кДа - малеимида (Sunbright GL2-400MA, 187 мг, 4.32 мкмоль).
Выход: 80 мг (1.79 мкмоль, 51 %) конъюгата 17*8 AcOH
Пример 18
Синтез временного конъюгата 2x20 кДа S1 ПЭГ 18
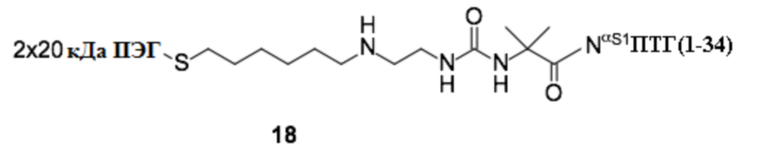
Конъюгат 18 получили как описано для 16 посредством реакции тиола 5 (37 мг, 8.40 мкмоль) и ПЭГ 2x20 кДа - малеимида (Sunbright GL2-400MA, 445 мг, 9.24 мкмоль). Реакцию погасили посредством добавления 50 мкл TFA без добавления 2-меркаптоэтанола. Конъюгат 18 очистили посредством IEX с последующей SEC для обессоливания. Фракции, содержащие раствор, лиофилизировали.
Выход: 161 мг (3.33 мкмоль, 40 %) конъюгата 18*9 AcOH
Пример 19
Синтез временного конъюгата 2x20 кДа S1 ПЭГ 19
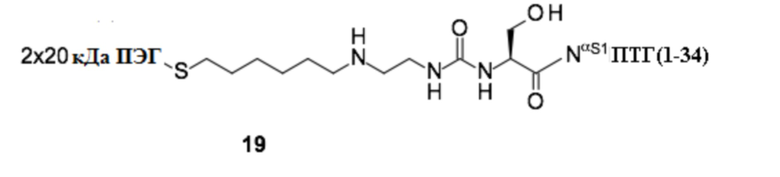
Конъюгат 19 получили как описано для 16 посредством реакции тиола 7 (27 мг, 6.14 мкмоль) и ПЭГ 2x20 кДа - малеимида (Sunbright GL2-400MA, 325 мг, 7.50 мкмоль).
Выход: 249 мг (5.16 мкмоль, 84 %) конъюгата 19*9 AcOH
Пример 20
Синтез временного конъюгата 2x20 кДа S1 ПЭГ 20
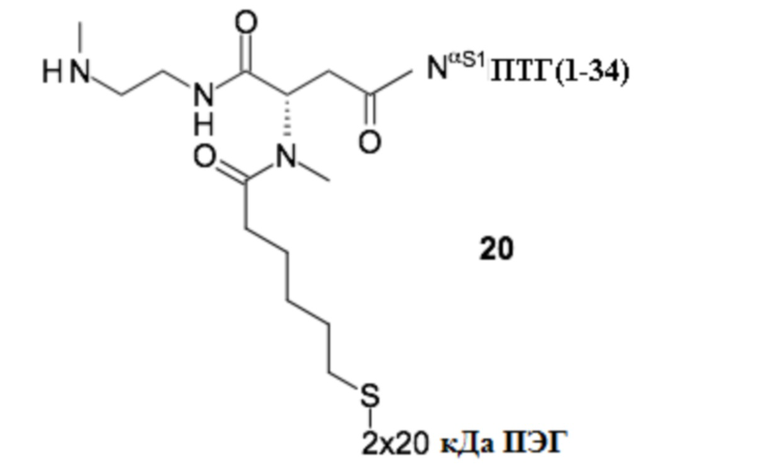
Конъюгат 20 получили как описано для 16 посредством реакции тиола 9 (38 мг, 8.59 мкмоль) и ПЭГ 2x20 кДа - малеимида (Sunbright GL2-400MA, 455 мг, 9.45 мкмоль). Реакцию погасили посредством добавления 50 мкл TFA без добавления 2-меркаптоэтанола. Конъюгат 20 очистили посредством IEX с последующей SEC для обессоливания. Фракции, содержащие раствор, лиофилизировали.
Выход: 194 мг (4.01 мкмоль, 47 %) конъюгата 20*9 AcOH
Пример 21
Синтез временного конъюгата 2x20 кДа K26 ПЭГ 21

Конъюгат 21 получили как описано для 16 посредством реакции тиола 10 (34 мг, 7.58 мкмоль) и ПЭГ 2x20 кДа - малеимида (Sunbright GL2-400MA, 401 мг, 9.26 мкмоль).
Выход: 256 мг (5.30 мкмоль, 70 %) конъюгат 21*9 AcOH
Пример 22
Кинетика высвобождения in vitro временного низкомолекулярного конъюгата ПЭГ
Конъюгаты 11b, 12, 13, 14, и 15 растворили в pH 7.4 фосфатном буфере (60 мM NaH2PO4, 3 мM EDTA, 0.01 % Tween-20, довели до pH 7.4 посредством NaOH), содержащем 0.05 мг/мл пентафторфенола в качестве внутреннего стандарта при концентрации около 1 мг конъюгата/мл. Растворы отфильтровали стерильно и инкубировали при 37°C. Взяли аликвоты во временных точках и проанализировали посредством ОФ-ВЭЖХ и ESI-MS. Фракцию высвобожденного ПТГ в момент времени вычислили по соотношению площадей УФ пиков высвобожденного ПТГ и ПЭГ конъюгата. Построили график % высвобожденного ПТГ относительно времени инкубации. Программное обеспечение для подбора кривой применяли для вычисления соответствующих периодов полувысвобождения.
Результаты:
Для конъюгата 11b период полувысвобождения 3.2 дня получили.
Для конъюгата 12 период полувысвобождения 8.7 дня получили.
Для конъюгата 13 период полувысвобождения 10.8 дня получили.
Для конъюгата 14 период полувысвобождения 25.3 дня получили.
Для конъюгата 15 период полувысвобождения 6.9 дня получили.
Пример 23
Кинетика высвобождения in vitro временных 2x20 кДа ПЭГ конъюгатов
Конъюгаты 18, 19, 20, и 21 растворили в pH 7.4 фосфатном буфере (60 мM NaH2PO4, 3 мM EDTA, 0.01 % Tween-20, довели до pH 7.4 посредством NaOH), содержащем 0.08 мг/мл пентафторфенола в качестве внутреннего стандарта при концентрации около 5 мг конъюгата/мл. Растворы отфильтровали стерильно и инкубировали при 37°C. Взяли аликвоты во временных точках и проанализировали посредством ОФ-ВЭЖХ. Фракцию высвобожденного ПТГ в момент времени вычислили по соотношению площадей УФ пиков высвобожденного ПТГ и ПЭГ конъюгата. Построили график % высвобожденного ПТГ относительно времени инкубации. Программное обеспечение для подбора кривой применяли для вычисления соответствующих периодов полувысвобождения.
Результаты:
Для конъюгата 18 период полувысвобождения 2.8 дня получили.
Для конъюгата 19 период полувысвобождения 13.4 дня получили.
Для конъюгата 20 период полувысвобождения 1.3 дня получили.
Для конъюгата 21 период полувысвобождения 7.1 дня получили.
Пример 24
ПТГ рецепторная активность перманентных 2x20 кДа ПЭГ конъюгатов 16 и 17 в анализе на основе клеток
Остаточную активность ПТГ перманентно ПЭГилированных конъюгатов 16 и 17 количественно определили посредством измерения продукции cAMP из HEK293 клеток, сверхэкспрессирующих рецептор ПТГ/ПТГrP1 (Hohenstein A, Hebell M, Zikry Н, El Ghazaly M, Mueller F, Rohde, J. Development and validation of a novel cell-based assay for potency determination of human parathyroid hormone (PTH), Journal of Pharmaceutical and Biomedical Analysis September 2014, 98: 345-350). ПТГ(1-34) из NIBSC (National Institute for Biological Standards and Control, UK) применяли в качестве ссылочного стандарта.
Результаты:
Для конъюгата 16 активность рецептора 0.12 % была обнаружена относительно ссылочного ПТГ(1-34).
Для конъюгата 17 активность рецептора 0.11 % была обнаружена относительно ссылочного ПТГ(1-34).
Результаты свидетельствуют о эффективном снижении активности рецептора в перманентных конъюгатах 2x20 кДа ПЭГ 16 и 17. Можно сделать вывод, что аналогичные конъюгаты с временно связанными с Ser1 или Lys26 ПТГ (например, 18 и 21) являются подходящими ПТГ пролекарствами, обеспечивающими низкую остаточную активность рецептора. Прямой анализ временных конъюгатов в клеточном анализе невозможен из-за расщепления линкера в условиях анализа. Высвобожденный ПТГ повлияет на результат анализа.
Пример 25
Фармакокинетическое исследование перманентных конъюгатов 2x20 кДа ПЭГ 16 и 17 на крысах
Самцы крыс породы Вистар (6 недель, 230-260 г) получали либо одну внутривенное (2 группы, n = 3 животных в каждой), либо одну подкожное (2 группы, n = 3 животных в каждой) введение 16 или 17 в дозах 29 мкг/крыса ПТГэкв и 31 мкг/крыса ПТГэкв, соответственно. Образцы крови собирали до 168 ч после введения дозы, и получали плазму. Концентрации в плазме ПТГ(1-34) определили посредством количественной оценки N-концевого сигнатурного пептида (последовательность: IQLMHNLGK) и C-концевого сигнатурного пептида (последовательность: LQDVHNF) после расщепления LysC и GluC, как описано в части Вещества и Способы.
Результаты: Введение доз хорошо переносились без видимых признаков дискомфорта во время введения и после введения. В течение всего исследования не наблюдалось никаких побочных реакций от дозы. После внутривенного введения 16 и 17 tmax для общего ПТГ (1-34) наблюдалась в момент времени 15 мин (наиболее ранний анализируемый момент времени), с последующим медленным спадом содержания общего ПТГ (1-34) с периодом полувыведения около 13 ч и 11 ч, соответственно. После подкожной инъекции концентрация общего ПТГ (1-34) достигла максимума при tmax 24 часа для 16 и 17, с момент медленным спадом содержания общего ПТГ (1-34) с периодом полувыведения около 1,5 дня для обоих конъюгатов. Биодоступность составляла около 40% и 60% соответственно. Аналогичные кривые PK были получены для N- и C-концевого сигнатурного пептида до 168 ч после введения дозы, что указывает на наличие интактного ПТГ (1-34) в конъюгате.
Благоприятные длинные PK и стабильность ПТГ в конъюгатах указывают на пригодность перманентных модельных соединений 2x20 кДа ПЭГ, так как происходит медленное высвобождение пролекарств ПТГ после подкожной инъекции. Можно сделать вывод, что аналогичные конъюгаты с временно связанным с Ser1 (например, 18) или Lys26 ПТГ являются подходящими пролекарствами ПТГ, обеспечивающими длительные уровни высвобождаемого биоактивного ПТГ.
Пример 26
Фармакокинетическое исследование временного конъюгата 2x20 кДа S1 ПЭГ 19 на яванских макаках
Самцы ранее не подверженных экспериментам яванских макак (2-4 года, 3.7-5.4 кг) получали однократное подкожное введение (n = 3 животного) конъюгата 19 при дозе 70 мкг/кг ПТГэкв. Образцы крови собирали до 504 ч после введения дозы, и получали плазму. Общие концентрации ПТГ(1-34) в плазме определили посредством количественной оценки N-концевого сигнатурного пептида (последовательность: IQLMHNLGK) и C-концевого сигнатурного пептида (последовательность: LQDVHNF) после LysC и GluC расщепления, как описано в части Вещества и Способы. Концентрации ПЭГ определяли с применением способа, описанного в части Вещества и Способы.
Результаты: Введение доз хорошо переносилось без видимых признаков дискомфорта во время введения. У одного животного обнаружили видимые признаки дискомфорта через 72 ч после введения дозы, но произошло восстановление через несколько дней. В течение всего исследования не наблюдалось никаких побочных реакций от введения дозы. Общая концентрация ПТГ (1-34) достигала максимума при tmax 24 ч, с последующим медленным спадом общего содержания ПТГ (1-34) с периодом полувыведения около 2,5 дня для N-концевого сигнатурного пептида и 0,9 дня для C-концевого сигнатурного пептида. Концентрация ПЭГ достигла максимума при tmax 24 ч, с последующим медленным спадом концентрации ПЭГ с периодом полувыведения 3.5 дня.
Можно сделать заключение, что конъюгат 19 является подходящим пролекарством для пролонгированной доставки ПТГ.
Пример 27
Фармакокинетическое исследование временного конъюгата 2x20 кДа S1 ПЭГ 18 на яванских макаках
Ранее не подверженные экспериментам яванские макаки (2-3 года, 2.5-4 кг) получали ежедневное подкожное введение (n = 2 животных - 1 самец / 1 самка) конъюгата 18 при уровнях дозы 0.2, 0.5, и 1 мкг/кг ПТГэкв в течение 28 дней. Образцы крови собирали в течение до 28 дней (на дни 1, 13 и 27 образцы собрали перед введением дозы, через 2 ч, 4 ч, 8 ч, 12 ч, и 24 ч после введения дозы) и получили плазму. Концентрации в плазме ПТГ(1-34) определили посредством количественной оценки N-концевого сигнатурного пептида (последовательность: IQLMHNLGK) и C-концевого сигнатурного пептида (последовательность: LQDVHNF) после LysC и GluC расщепления, как описано в части Вещества и Способы.
Результаты: Введение всех доз было выполнено без происшествий. В течение всего исследования не наблюдалось никаких побочных реакций от введения дозы. Линейность дозы наблюдалась в трех группах. С 1-го дня наблюдали стэкинг-эффект доз по сравнению с 13 днем и 27 днем. Общие концентрации ПТГ (1-34) определяли посредством N-концевого сигнатурного пептида (последовательность: IQLMHNLGK) в стабильном состоянии (в течение дня 27).
Низкое соотношение пика и минимума общего ПТГ(1-34) для групп всех доз ниже 3 наблюдали после ежедневного подкожного введения в стабильном состоянии у яванских макак. Поскольку концентрации свободных пептидов в стабильном состоянии коррелируют с общей концентрацией ПТГ (1-34), соотношение пика и минимума для свободного пептида ниже 4 в яванских макаках.
Пример 28
Фармакокинетическое исследование временного конъюгата 2x20 кДа S1 ПЭГ 18 на яванских макаках
Ранее не подверженные экспериментам яванские макаки (2-3.5 лет, 2-5 кг) (3-5 самцов / 3-5 самок) получали ежедневное подкожное введение соединения 18 при уровнях дозы 0.2, 0.5 и 1.5 мкг ПТГ/кг. Образцы крови собрали на; день 1:перед введением дозы, 4 ч, 8 ч, 12 ч, 18 ч, и 24 ч после введения дозы, на день 8: перед введением дозы, на день 14: перед введением дозы, 8ч, и 12 ч и на день 28: 3 ч, 6 ч, 8 ч, 12 ч, 18 ч, 24 ч, 72 ч, 168 ч, и 336 ч) и получили плазму. Общие концентрации ПТГ в плазме определили посредством количественной оценки N-концевого сигнатурного пептида (последовательность: IQLMHNLGK) после LysC и GluC расщепления, как представлено в части Вещества и Способы.
Результаты: Системное воздействие, выраженное как Cmax и AUC, увеличивалось пропорционально дозе. Системное воздействие общего ПТГ, выраженное как AUC, накапливается примерно в 3 раза с 1 по 28 день.
Низкое значение соотношения пика и минимума общего ПТГ для групп всех доз наблюдалось после ежедневного подкожного введения яванским макакам на день 28 (стабильное состояние наблюдалось со дня 8). Это низкое значение соотношения пика и минимума общего ПТГ также может быть перенесено на свободный ПТГ.
Пример 29
Фармакокинетическое исследование временного конъюгата 2x20 кДа S1 ПЭГ 18 на крысах Спрег-Доули
Крысы Спрег-Доули Crl:CD(SD) (начало введения доз с возраста 8 недель) получали ежедневное подкожное введение соединения 18 при уровнях дозы 10, 30 и 60 мкг ПТГ/кг в течение 28 дней. TK группа, содержащая 9 самцов и 9 самок на группу дозы, была поделена 3 подгруппы с 3 крысами в подгруппе. Образцы крови собирали до 28 дня с 3 крысами на один пол, на один момент времени отбора образца. Образцы собирались на день 1: перед введением, 4 ч, 8 ч, 12 ч, 18 ч и 24 ч после введения дозы, а на день 28: 3 ч, 6 ч, 8 ч, 12 ч, 18 ч, 24 ч и 336 ч, и получали плазму. Общие концентрации ПТГ в плазме определили посредством количественной оценки N-концевого сигнатурного пептида (последовательность: IQLMHNLGK) после LysC и GluC расщепления, как представлено в части Вещества и Способы.
Концентрации свободного ПТГ в плазме определяли количественно как сумму ПТГ(1-34) и ПТГ(1-33) посредством LC-MS/MS, как представлено в части материалы и способы.
Результаты: Системное воздействие общего ПТГ и свободного ПТГ, увеличивалось пропорционально дозе. Системное воздействие общего ПТГ, выраженное как среднее AUC, накапливалось 3-6-ти кратно с 1 по 28 день, и свободного ПТГ, выраженное как среднее AUC, накапливалось 2-3-ти кратно с 1 по 28 день. Системное воздействие общего ПТГ у самки крысы было примерно в 2 раза выше, чем у самцов. Системное воздействие свободного ПТГ был немного выше у самок крыс, чем у самцов.
Низкое значение соотношения пика и минимума общего ПТГ для всех групп по дозе 1.2 наблюдалось после ежедневного подкожного введения крысам Спрег-Доули на день 28 (стабильное состояние наблюдалось со дня 8). Низкое значение соотношения пика и минимума свободного ПТГ в интервале 1.5 - 2.4 наблюдалось после ежедневного подкожного введения крысам Спрег-Доули на день 28.
Аббревиатуры:
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Ascendis Pharma A/S
<120> ПТГ СОЕДИНЕНИЯ С НИЗКИМИ СООТНОШЕНИЯМИ ПИКА И МИНИМУМА
<130> CPX70584PC
<160> 122
<170> PatentIn version 3.5
<210> 1
<211> 84
<212> PRT
<213> Homo sapiens
<400> 1
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala Lys Ser Gln
<210> 2
<211> 83
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-83
<400> 2
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala Lys Ser
<210> 3
<211> 82
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-82
<400> 3
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala Lys
<210> 4
<211> 81
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-81
<400> 4
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala
<210> 5
<211> 80
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-80
<400> 5
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
<210> 6
<211> 79
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-79
<400> 6
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr
65 70 75
<210> 7
<211> 78
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-78
<400> 7
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu
65 70 75
<210> 8
<211> 77
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-77
<400> 8
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val
65 70 75
<210> 9
<211> 76
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-76
<400> 9
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn
65 70 75
<210> 10
<211> 75
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-75
<400> 10
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val
65 70 75
<210> 11
<211> 74
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-74
<400> 11
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp
65 70
<210> 12
<211> 73
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-73
<400> 12
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala
65 70
<210> 13
<211> 72
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-72
<400> 13
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys
65 70
<210> 14
<211> 71
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-71
<400> 14
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp
65 70
<210> 15
<211> 70
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-70
<400> 15
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala
65 70
<210> 16
<211> 69
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-69
<400> 16
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu
65
<210> 17
<211> 68
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-68
<400> 17
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly
65
<210> 18
<211> 67
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-67
<400> 18
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu
65
<210> 19
<211> 66
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-66
<400> 19
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser
65
<210> 20
<211> 65
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-65
<400> 20
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys
65
<210> 21
<211> 64
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-64
<400> 21
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
<210> 22
<211> 63
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-63
<400> 22
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His
50 55 60
<210> 23
<211> 62
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-62
<400> 23
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser
50 55 60
<210> 24
<211> 61
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-61
<400> 24
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu
50 55 60
<210> 25
<211> 60
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-60
<400> 25
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val
50 55 60
<210> 26
<211> 59
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-59
<400> 26
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu
50 55
<210> 27
<211> 58
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-58
<400> 27
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val
50 55
<210> 28
<211> 57
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-57
<400> 28
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn
50 55
<210> 29
<211> 56
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-56
<400> 29
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp
50 55
<210> 30
<211> 55
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-55
<400> 30
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu
50 55
<210> 31
<211> 54
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-54
<400> 31
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys
50
<210> 32
<211> 53
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-53
<400> 32
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys
50
<210> 33
<211> 52
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-52
<400> 33
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg
50
<210> 34
<211> 51
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-51
<400> 34
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro
50
<210> 35
<211> 50
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-50
<400> 35
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg
50
<210> 36
<211> 49
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-49
<400> 36
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln
<210> 37
<211> 48
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-48
<400> 37
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
<210> 38
<211> 47
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-47
<400> 38
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly
35 40 45
<210> 39
<211> 46
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-46
<400> 39
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala
35 40 45
<210> 40
<211> 45
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-45
<400> 40
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp
35 40 45
<210> 41
<211> 44
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-44
<400> 41
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg
35 40
<210> 42
<211> 43
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-43
<400> 42
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro
35 40
<210> 43
<211> 42
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-42
<400> 43
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala
35 40
<210> 44
<211> 41
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая PTH-41
<400> 44
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu
35 40
<210> 45
<211> 40
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-40
<400> 45
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro
35 40
<210> 46
<211> 39
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-39
<400> 46
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala
35
<210> 47
<211> 38
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-38
<400> 47
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly
35
<210> 48
<211> 37
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-37
<400> 48
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu
35
<210> 49
<211> 36
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-36
<400> 49
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala
35
<210> 50
<211> 35
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-35
<400> 50
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val
35
<210> 51
<211> 34
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-34
<400> 51
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe
<210> 52
<211> 33
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-33
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn
<210> 53
<211> 32
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-32
<400> 53
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
<210> 54
<211> 31
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-31
<400> 54
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val
20 25 30
<210> 55
<211> 30
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-30
<400> 55
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp
20 25 30
<210> 56
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-29
<400> 56
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln
20 25
<210> 57
<211> 28
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-28
<400> 57
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu
20 25
<210> 58
<211> 27
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-27
<400> 58
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys
20 25
<210> 59
<211> 26
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-26
<400> 59
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys
20 25
<210> 60
<211> 25
<212> PRT
<213> искусственная последовательность
<220>
<223> человеческая ПТГ 1-25
<400> 60
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg
20 25
<210> 61
<211> 84
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-84
<220>
<221> MOD_RES
<222> (84)..(84)
<223> амидирование
<400> 61
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala Lys Ser Gln
<210> 62
<211> 83
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-83
<220>
<221> MOD_RES
<222> (83)..(83)
<223> амидирование
<400> 62
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala Lys Ser
<210> 63
<211> 82
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-82
<220>
<221> MOD_RES
<222> (82)..(82)
<223> амидирование
<400> 63
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala Lys
<210> 64
<211> 81
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-81
<220>
<221> MOD_RES
<222> (81)..(81)
<223> амидирование
<400> 64
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
Ala
<210> 65
<211> 80
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-80
<220>
<221> MOD_RES
<222> (80)..(80)
<223> амидирование
<400> 65
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr Lys
65 70 75 80
<210> 66
<211> 79
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-79
<220>
<221> MOD_RES
<222> (79)..(79)
<223> амидирование
<400> 66
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu Thr
65 70 75
<210> 67
<211> 78
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-78
<220>
<221> MOD_RES
<222> (78)..(78)
<223> амидирование
<400> 67
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val Leu
65 70 75
<210> 68
<211> 77
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-77
<220>
<221> MOD_RES
<222> (77)..(77)
<223> амидирование
<400> 68
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn Val
65 70 75
<210> 69
<211> 76
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-76
<220>
<221> MOD_RES
<222> (76)..(76)
<223> амидирование
<400> 69
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val Asn
65 70 75
<210> 70
<211> 75
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-75
<220>
<221> MOD_RES
<222> (75)..(75)
<223> амидирование
<400> 70
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp Val
65 70 75
<210> 71
<211> 74
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-74
<220>
<221> MOD_RES
<222> (74)..(74)
<223> амидирование
<400> 71
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala Asp
65 70
<210> 72
<211> 73
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-73
<220>
<221> MOD_RES
<222> (73)..(73)
<223> амидирование
<400> 72
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys Ala
65 70
<210> 73
<211> 72
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-72
<220>
<221> MOD_RES
<222> (72)..(72)
<223> амидирование
<400> 73
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp Lys
65 70
<210> 74
<211> 71
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-71
<220>
<221> MOD_RES
<222> (71)..(71)
<223> амидирование
<400> 74
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala Asp
65 70
<210> 75
<211> 70
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-70
<220>
<221> MOD_RES
<222> (70)..(70)
<223> амидирование
<400> 75
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu Ala
65 70
<210> 76
<211> 69
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-69
<220>
<221> MOD_RES
<222> (69)..(69)
<223> амидирование
<400> 76
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly Glu
65
<210> 77
<211> 68
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-68
<220>
<221> MOD_RES
<222> (68)..(68)
<223> амидирование
<400> 77
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu Gly
65
<210> 78
<211> 67
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-67
<220>
<221> MOD_RES
<222> (67)..(67)
<223> амидирование
<400> 78
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser Leu
65
<210> 79
<211> 66
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-66
<220>
<221> MOD_RES
<222> (66)..(66)
<223> амидирование
<400> 79
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys Ser
65
<210> 80
<211> 65
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-65
<220>
<221> MOD_RES
<222> (65)..(65)
<223> амидирование
<400> 80
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
Lys
65
<210> 81
<211> 64
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-64
<220>
<221> MOD_RES
<222> (64)..(64)
<223> амидирование
<400> 81
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His Glu
50 55 60
<210> 82
<211> 63
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-63
<220>
<221> MOD_RES
<222> (63)..(63)
<223> амидирование
<400> 82
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser His
50 55 60
<210> 83
<211> 62
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-62
<220>
<221> MOD_RES
<222> (62)..(62)
<223> амидирование
<400> 83
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu Ser
50 55 60
<210> 84
<211> 61
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-61
<220>
<221> MOD_RES
<222> (61)..(61)
<223> амидирование
<400> 84
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val Glu
50 55 60
<210> 85
<211> 60
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-60
<220>
<221> MOD_RES
<222> (60)..(60)
<223> ацетилирование
<400> 85
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu Val
50 55 60
<210> 86
<211> 59
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-59
<220>
<221> MOD_RES
<222> (59)..(59)
<223> амидирование
<400> 86
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val Leu
50 55
<210> 87
<211> 58
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-58
<220>
<221> MOD_RES
<222> (58)..(58)
<223> амидирование
<400> 87
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn Val
50 55
<210> 88
<211> 57
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-57
<220>
<221> MOD_RES
<222> (57)..(57)
<223> амидирование
<400> 88
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp Asn
50 55
<210> 89
<211> 56
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-56
<220>
<221> MOD_RES
<222> (56)..(56)
<223> амидирование
<400> 89
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu Asp
50 55
<210> 90
<211> 55
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-55
<220>
<221> MOD_RES
<222> (55)..(55)
<223> амидирование
<400> 90
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys Glu
50 55
<210> 91
<211> 54
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-54
<220>
<221> MOD_RES
<222> (54)..(54)
<223> амидирование
<400> 91
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys Lys
50
<210> 92
<211> 53
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-53
<220>
<221> MOD_RES
<222> (53)..(53)
<223> амидирование
<400> 92
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg Lys
50
<210> 93
<211> 52
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-52
<220>
<221> MOD_RES
<222> (52)..(52)
<223> амидирование
<400> 93
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro Arg
50
<210> 94
<211> 51
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-51
<220>
<221> MOD_RES
<222> (51)..(51)
<223> амидирование
<400> 94
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg Pro
50
<210> 95
<211> 50
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-50
<220>
<221> MOD_RES
<222> (50)..(50)
<223> амидирование
<400> 95
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln Arg
50
<210> 96
<211> 49
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-49
<220>
<221> MOD_RES
<222> (49)..(49)
<223> амидирование
<400> 96
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
Gln
<210> 97
<211> 48
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-48
<220>
<221> MOD_RES
<222> (48)..(48)
<223> амидирование
<400> 97
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly Ser
35 40 45
<210> 98
<211> 47
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-47
<220>
<221> MOD_RES
<222> (47)..(47)
<223> амидирование
<400> 98
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala Gly
35 40 45
<210> 99
<211> 46
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-46
<220>
<221> MOD_RES
<222> (46)..(46)
<223> амидирование
<400> 99
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp Ala
35 40 45
<210> 100
<211> 45
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-45
<220>
<221> MOD_RES
<222> (45)..(45)
<223> амидирование
<400> 100
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg Asp
35 40 45
<210> 101
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-44
<220>
<221> MOD_RES
<222> (44)..(44)
<223> амидирование
<400> 101
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro Arg
35 40
<210> 102
<211> 43
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-43
<220>
<221> MOD_RES
<222> (43)..(43)
<223> амидирование
<400> 102
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala Pro
35 40
<210> 103
<211> 42
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-42
<220>
<221> MOD_RES
<222> (42)..(42)
<223> амидирование
<400> 103
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu Ala
35 40
<210> 104
<211> 41
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-41
<220>
<221> MOD_RES
<222> (41)..(41)
<223> амидирование
<400> 104
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro Leu
35 40
<210> 105
<211> 40
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-40
<220>
<221> MOD_RES
<222> (40)..(40)
<223> амидирование
<400> 105
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala Pro
35 40
<210> 106
<211> 39
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-39
<220>
<221> MOD_RES
<222> (39)..(39)
<223> амидирование
<400> 106
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly Ala
35
<210> 107
<211> 38
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-38
<220>
<221> MOD_RES
<222> (38)..(38)
<223> амидирование
<400> 107
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu Gly
35
<210> 108
<211> 37
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-37
<220>
<221> MOD_RES
<222> (37)..(37)
<223> амидирование
<400> 108
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala Leu
35
<210> 109
<211> 36
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-36
<220>
<221> MOD_RES
<222> (36)..(36)
<223> амидирование
<400> 109
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val Ala
35
<210> 110
<211> 35
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-35
<220>
<221> MOD_RES
<222> (35)..(35)
<223> амидирование
<400> 110
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe Val
35
<210> 111
<211> 34
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-34
<220>
<221> MOD_RES
<222> (34)..(34)
<223> амидирование
<400> 111
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn Phe
<210> 112
<211> 33
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-33
<220>
<221> MOD_RES
<222> (33)..(33)
<223> амидирование
<400> 112
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
Asn
<210> 113
<211> 32
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-32
<220>
<221> MOD_RES
<222> (32)..(32)
<223> амидирование
<400> 113
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val His
20 25 30
<210> 114
<211> 31
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-31
<220>
<221> MOD_RES
<222> (31)..(31)
<223> амидирование
<400> 114
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp Val
20 25 30
<210> 115
<211> 30
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-30
<220>
<221> MOD_RES
<222> (30)..(30)
<223> амидирование
<400> 115
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln Asp
20 25 30
<210> 116
<211> 29
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-29
<220>
<221> MOD_RES
<222> (29)..(29)
<223> амидирование
<400> 116
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu Gln
20 25
<210> 117
<211> 28
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-28
<220>
<221> MOD_RES
<222> (28)..(28)
<223> амидирование
<400> 117
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys Leu
20 25
<210> 118
<211> 27
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-27
<220>
<221> MOD_RES
<222> (27)..(27)
<223> амидирование
<400> 118
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys Lys
20 25
<210> 119
<211> 26
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-26
<220>
<221> MOD_RES
<222> (26)..(26)
<223> амидирование
<400> 119
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg Lys
20 25
<210> 120
<211> 25
<212> PRT
<213> искусственная последовательность
<220>
<223> амидированная человеческая ПТГ 1-25
<220>
<221> MOD_RES
<222> (25)..(25)
<223> амидирование
<400> 120
Ser Val Ser Glu Ile Gln Leu Met His Asn Leu Gly Lys His Leu Asn
1 5 10 15
Ser Met Glu Arg Val Glu Trp Leu Arg
20 25
<210> 121
<211> 141
<212> PRT
<213> Homo sapiens
<400> 121
Ala Val Ser Glu His Gln Leu Leu His Asp Lys Gly Lys Ser Ile Gln
1 5 10 15
Asp Leu Arg Arg Arg Phe Phe Leu His His Leu Ile Ala Glu Ile His
20 25 30
Thr Ala Glu Ile Arg Ala Thr Ser Glu Val Ser Pro Asn Ser Lys Pro
35 40 45
Ser Pro Asn Thr Lys Asn His Pro Val Arg Phe Gly Ser Asp Asp Glu
50 55 60
Gly Arg Tyr Leu Thr Gln Glu Thr Asn Lys Val Glu Thr Tyr Lys Glu
65 70 75 80
Gln Pro Leu Lys Thr Pro Gly Lys Lys Lys Lys Gly Lys Pro Gly Lys
85 90 95
Arg Lys Glu Gln Glu Lys Lys Lys Arg Arg Thr Arg Ser Ala Trp Leu
100 105 110
Asp Ser Gly Val Thr Gly Ser Gly Leu Glu Gly Asp His Leu Ser Asp
115 120 125
Thr Ser Thr Thr Ser Leu Glu Leu Asp Ser Arg Arg His
130 135 140
<210> 122
<211> 20
<212> PRT
<213> искусственная последовательность
<220>
<223> искусственная случайная спираль
<400> 122
Gly Gly Pro Gly Gly Pro Gly Pro Gly Gly Pro Gly Gly Pro Gly Pro
1 5 10 15
Gly Gly Pro Gly
20
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ЖИДКИЕ ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ КОНЪЮГАТОВ PTH | 2020 |
|
RU2817015C2 |
| РЕЖИМ ДОЗИРОВАНИЯ СОЕДИНЕНИЯ PTH КОНТРОЛИРУЕМОГО ВЫСВОБОЖДЕНИЯ | 2017 |
|
RU2777357C2 |
| Антитела против CXCR2 и их применение | 2019 |
|
RU2807067C2 |
| АМАТОКСИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2826004C2 |
| АНТИТЕЛА, СПЕЦИФИЧЕСКИЕ В ОТНОШЕНИИ CD70, И ПУТИ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2801093C2 |
| Лечение гипопаратиреоидизма | 2021 |
|
RU2827712C1 |
| КОНЪЮГАТЫ СВЯЗУЮЩЕГО И АКТИВНОГО ВЕЩЕСТВА (ADC), ИМЕЮЩИЕ ФЕРМЕНТАТИВНО РАСЩЕПЛЯЕМЫЕ ГРУППЫ | 2017 |
|
RU2761390C2 |
| МУЛЬТИСПЕЦИФИЧЕСКАЯ АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА, ОБЛАДАЮЩАЯ ЗАМЕЩАЮЩЕЙ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТЬЮ КОФАКТОРА КОАГУЛИРУЮЩЕГО ФАКТОРА КРОВИ VIII, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ УКАЗАННУЮ МОЛЕКУЛУ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2018 |
|
RU2812909C2 |
| НАЦЕЛЕННЫЕ НА ОПУХОЛЬ АГОНИСТИЧЕСКИЕ CD28-АНТИГЕНСВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ | 2019 |
|
RU2808030C2 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА ПРОТИВ CEACAM5 И CD3 | 2020 |
|
RU2827106C1 |
Изобретение относится к области медицины и фармацевтики, а именно к применению фармацевтической композиции, содержащей соединение паратиреоидного гормона (ПТГ) для лечения гипопаратиреоидизма, где ПТГ-соединение представляет собой растворимое в воде ПТГ-соединение контролируемого высвобождения формулы (IIf-i)
 (IIf-i),
(IIf-i),
где неотмеченная пунктирная линия обозначает присоединение к атому азота ПТГ-составляющей посредством амидной связи; и пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
 ,
,
где m и p независимо представляют собой целое число в интервале 400-500 включительно; где ПТГ-составляющая имеет последовательность, выбранную из SEQ ID NO:47 - SEQ ID NO:55 или SEQ ID NO:107 - SEQ ID NO:115; где после подкожного введения отличному от человека примату фармакокинетический профиль ПТГ-соединения проявляет в плазме соотношение пика и минимума менее 4 в течение одного интервала инъекции в стационарном состоянии, где период времени между двумя последовательными подкожными введениями составляет 24 часа. Изобретение обеспечивает периодическое введение ПТГ с более низким повышением маркеров костного ремоделирования за счет сниженного соотношения пика и минимума концентрации после подкожного введения, что снижает побочные эффекты терапии. 11 з.п. ф-лы, 29 пр.
1. Применение фармацевтической композиции, содержащей соединение паратиреоидного гормона (ПТГ) для лечения гипопаратиреоидизма, где ПТГ-соединение представляет собой растворимое в воде ПТГ-соединение контролируемого высвобождения формулы (IIf-i)
 (IIf-i),
(IIf-i),
где
неотмеченная пунктирная линия обозначает присоединение к атому азота ПТГ-составляющей посредством образования амидной связи; и пунктирная линия, отмеченная звездочкой, обозначает присоединение к составляющей
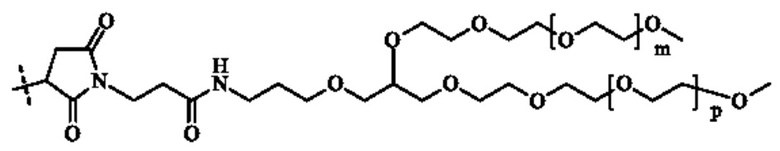 ,
,
где
m и p независимо представляют собой целое число в интервале и включая 400-500,
где ПТГ-составляющая имеет последовательность SEQ ID NO:47, SEQ ID NO:48, SEQ ID NO:49, SEQ ID NO:50, SEQ ID NO:51, SEQ ID NO:52, SEQ ID NO:53, SEQ ID NO:54, SEQ ID NO:55, SEQ ID NO:107, SEQ ID NO:108, SEQ ID NO:109, SEQ ID NO:110, SEQ ID NO:111, SEQ ID NO:112, SEQ ID NO:113, SEQ ID NO:114 или SEQ ID NO:115;
где после подкожного введения отличному от человека примату фармакокинетический профиль ПТГ-соединения проявляет в плазме соотношение пика и минимума менее 4 в течение одного интервала инъекции в стационарном состоянии, где период времени между двумя последовательными подкожными введениями составляет 24 часа.
2. Применение по п. 1, где ПТГ-составляющая имеет последовательность SEQ ID NO:51.
3. Применение по п. 1, где ПТГ-составляющая присоединена к ПТГ-соединению формулы (IIf-i) через N-концевую аминовую функциональную группу составляющей ПТГ.
4. Применение по п. 1, где подкожное введение осуществляют посредством подкожной инъекции.
5. Применение по п. 1, где подкожное введение осуществляют посредством шприца-ручки.
6. Применение по п. 1, где соотношение пика и минимума составляет менее 3.
7. Применение по п. 1, где соотношение пика и минимума составляет менее 2,4.
8. Применение по п. 1, где соотношение пика и минимума составляет менее 2,2.
9. Применение по п. 1, где соотношение пика и минимума составляет менее 2.
10. Применение по п. 1, где отличный от человека примат представляет собой яванскую макаку.
11. Применение по п. 1, где фармацевтическая композиция имеет значение pH в интервале и включая pH 3 - pH 8.
12. Применение по любому из пп. 1-11, где фармацевтическая композиция имеет значение pH в интервале и включая pH 4 - pH 5.
| US2005148763 A1, 07.07.2005 | |||
| WU M | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| Vol | |||
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| P | |||
| Прибор для переработки спирта в газовую смесь для двигателей внутреннего сгорания | 1920 |
|
SU589A1 |
| WO2014173759 A1, 30.10.2014 | |||
| WO2013024049 A1, 21.02.2013 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| и доп | |||
Авторы
Даты
2022-03-16—Публикация
2017-09-28—Подача