Перекрестная ссылка на родственные заявки
[0001] Настоящая заявка испрашивает приоритет согласно §119(e) Раздела 35 Свода законов США на основании предварительной заявки на патент США 62/291921, поданной 5 февраля 2016 года, которая полностью включена в настоящий документ посредством ссылки.
Уровень техники
[0002] Рак молочной железы является наиболее распространенной причиной смерти женщин во всем мире. Большинство случаев рака молочной железы (примерно 80%) связано с сигнальным путем, регулирующим рост клеток, опосредованным эстрогеновыми рецепторами (ЭР). Поэтому таргетная терапия ЭР или их сигнального пути остается ключевым направлением в разработке препарата для лечения рака молочной железы. Эстрогеновые рецепторы (включая ERα и ERβ) представляют собой группу рецепторов, которые активируются эстрогенным гормоном (17β-эстрадиол). Текущая терапия ЭР-положительного (ЭР+) рака молочной железы включает средства, которые ингибируют активность ЭР посредством прямого связывания с лигандсвязывающим доменом рецептора (например, тамоксифен), блокируют синтез эстрогена (например, ингибитор ароматазы, такой как анастрозол и летрозол) или индуцируют деградацию ЭР (например, фулвестрант).
[0003] Препараты, ингибирующие эстрогеновые рецепторы или блокирующие образование эстрогенов, обычно используют для лечения ЭР-положительного рака молочной железы и других гормонозависимых видов рака. Однако резистентность к лекарственным средствам остается проблемой для лечения рака молочной железы, особенно для лечения рака на поздних стадиях. Селективные ингибиторы эстрогеновых рецепторов (СИЭР) представляют собой класс малых молекул, которые связываются с эстрогеновым рецептором, что приводит к деградации эстрогенового рецептора. Исследования показали, что СИЭР особенно полезны для лечения онкологических заболеваний, устойчивых к другим лекарственным средствам, таким как тамоксифен и/или ингибиторы ароматазы (McDonnell et al., J. Med. Chem. 2015, 58, 4883-4887). Фулвестрант представляет собой СИЭР, одобренный для лечения ЭР-положительного рака молочной железы. Однако фулвестрант быстро метаболизируется, кроме того, его вводят путем внутримышечной инъекции раз в месяц, что ограничивает эффективную деградацию ЭР (деградация ЭР в клинических образцах составляет примерно 50%) по сравнению с полной деградацией ЭР, наблюдаемой в исследовании in vitro. В последнее время были обнаружены мутации ЭР в биопсийных образцах пациентов, больных раком молочной железы, с развившейся резистентностью к лечению ингибитором ароматазы. Указанные мутации чаще всего встречаются в аминокислотах 537 и 538 в лигандсвязывающем домене ЭР. Интересно, что указанные мутировавшие ЭР по-прежнему связаны и ингибируются как тамоксифеном, так и фулвестрантом в некоторой степени (Li et al., 2013 Cell Reports 4, 1116-1130; Toy et al., 2013, 45, 1439-1445; Robinson et al., Nature Genetics 2013, 45, 1446-1451). Также было показано, что фулвестрант может эффективно вызывать деградацию мутированного белка Try537Ser ЭР. В результате соединение, нацеленное на деградацию ЭР, подобное фулвестранту, может эффективно вызывать деградацию мутированного белка ЭР, а также является полезным для лечения пациентов, больных раком молочной железы, с развившейся резистентностью к ингибитору ароматазы. Поэтому очень важно разработать новые нестероидные СИЭР для лечения рака молочной железы и других заболеваний, связанных с ЭР.
Сущность изобретения
[0004] Настоящее изобретение обеспечивает соединения, такие как соединения Формулы (I) и Формулы (II), которые представляют собой селективные ингибиторы эстрогеновых рецепторов (СИЭР). Описанные в данном документе соединения полезны для лечения рака молочной железы, особенно ЭР-положительного рака молочной железы, а также заболеваний, связанных с ЭР. Также предложены фармацевтические композиции, наборы, способы и применения любого из соединений, описанных в данном документе.
[0005] В одном из аспектов настоящее изобретение обеспечивает соединения Формулы (I):
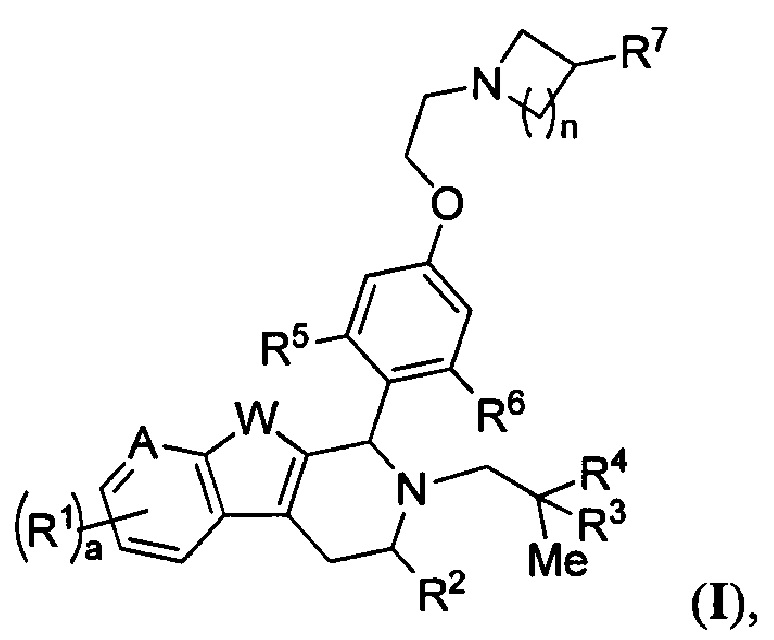
или фармацевтически приемлемые соли, причем А представляет собой -CRA= или -N= в зависимости от валентности; W представляет собой -NH-, -О- или -S-; а равно 1, 2 или 3; и n равно 1, 2, 3 или 4. Кроме того,
каждый R1 независимо представляет собой водород, галоген, замещенный или незамещенный алкил, -ORA или -CN;
R2 представляет собой водород, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил;
R3 представляет собой водород, галоген, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, -ORA или -N(RB)2;
R4 представляет собой водород, галоген, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, -ORA или -N(RB)2;
R5 представляет собой водород, галоген, замещенный или незамещенный алкил;
R6 представляет собой водород, замещенный или незамещенный алкил;
R7 представляет собой водород, галоген, замещенный или незамещенный алкил, -ORA или -N(RB)2;
RA представляет собой водород или замещенный или незамещенный алкил или кислородзащитную группу; и
RB представляет собой водород или замещенный или незамещенный алкил, азотзащитную группу, или необязательно два RB взятые вместе с промежуточными атомами образуют замещенный или незамещенный гетероциклил или замещенный или незамещенный гетероарил.
[0006] В некоторых вариантах реализации соединение Формулы (I) представляет собой соединение формулы:
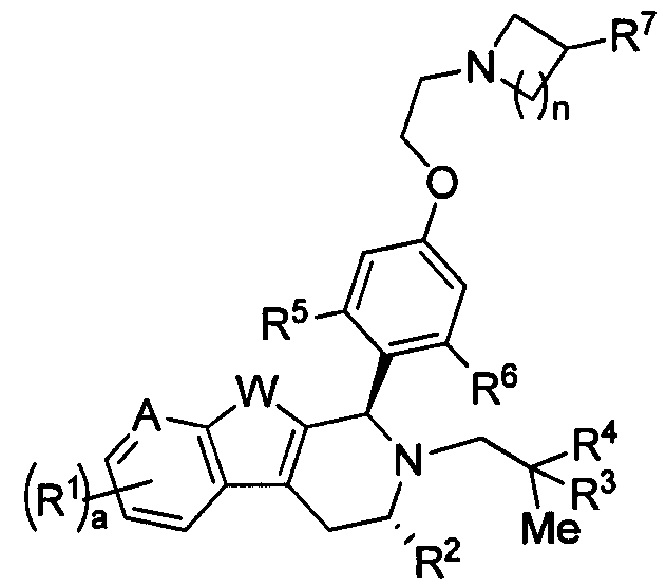 или фармацевтически приемлемую соль, причем R1, R2, R3, R4, R5, R6, R7, A, W, а и n как описаны в данном документе.
или фармацевтически приемлемую соль, причем R1, R2, R3, R4, R5, R6, R7, A, W, а и n как описаны в данном документе.
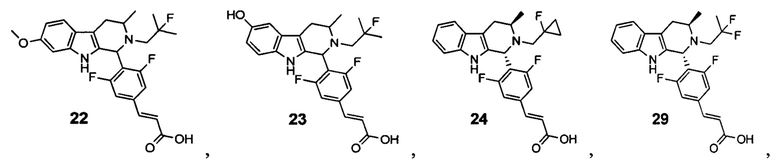
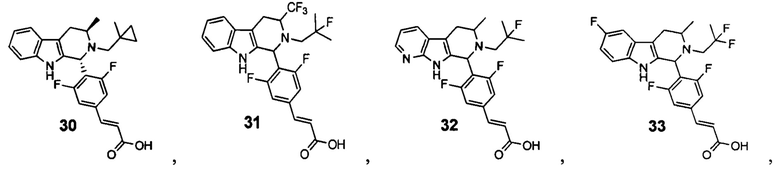
[0007] Примеры соединений Формулы (I)
[0008] включают, но не ограничиваются ими:
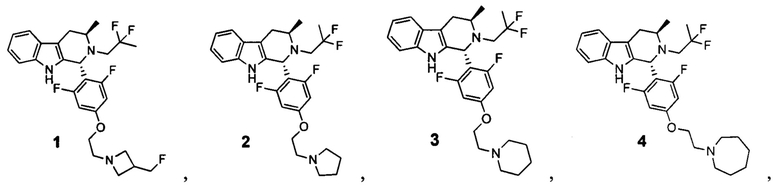
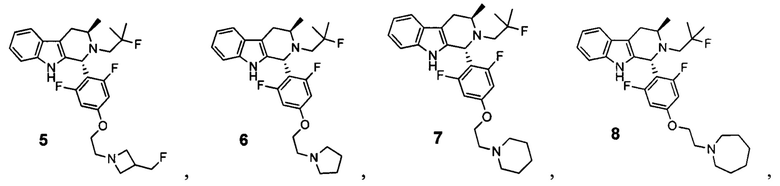
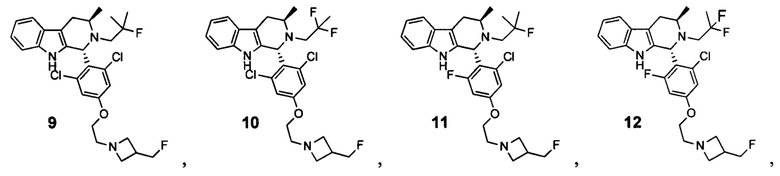
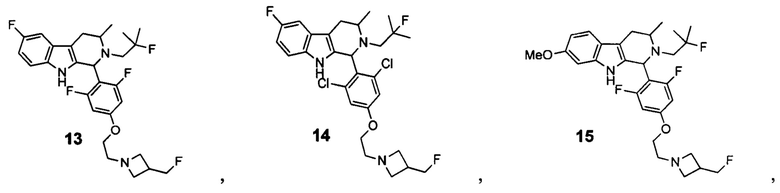
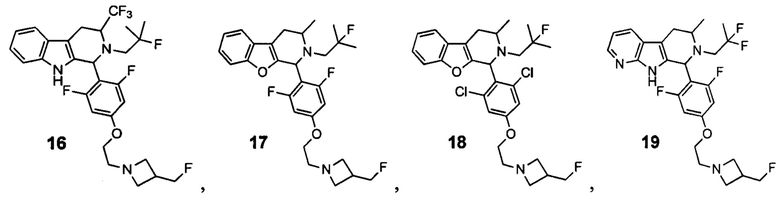 или фармацевтически приемлемые соли.
или фармацевтически приемлемые соли.
[0009] В другом аспекте настоящее изобретение обеспечивает соединения Формулы (II):
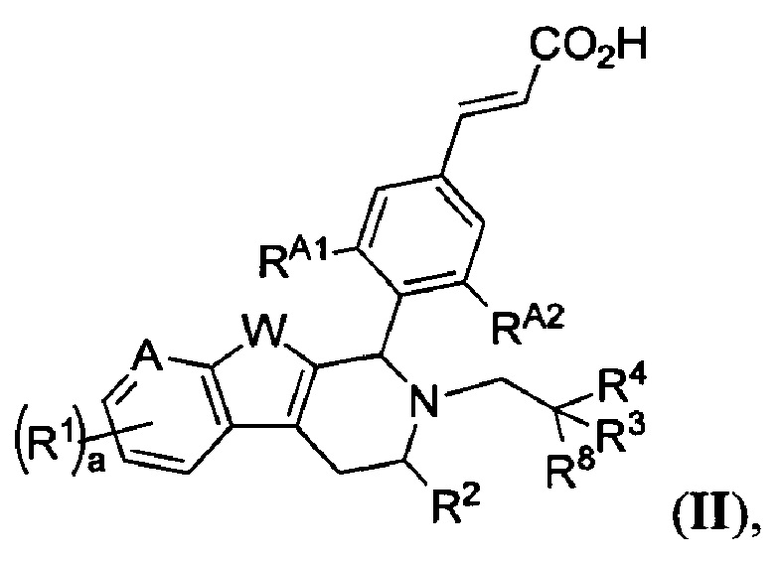
или фармацевтически приемлемые соли, причем А представляет собой -CRA= или -N= в зависимости от валентности; W представляет собой -NH-, -О- или -S-; и а равно 1, 2 или 3. Кроме того,
каждый R1 независимо представляет собой водород, галоген, замещенный или незамещенный алкил, -ORA или -CN;
R2 представляет собой водород, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил;
R3 представляет собой водород, галоген, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, -ORA или -N(RB)2;
R4 представляет собой водород, галоген, замещенный или незамещенный алкил, замещенный или незамещенный карбоциклил, замещенный или незамещенный гетероциклил, замещенный или незамещенный арил или замещенный или незамещенный гетероарил, -ORA или -N(RB)2 или R3 и R4 взятые вместе с промежуточными атомами образуют замещенный или незамещенный карбоциклил или замещенный или незамещенный гетероциклил;
R8 представляет собой водород, галоген или замещенный или незамещенный метил (например, метил);
RA1 представляет замещенный или незамещенный алкил, хлор или фтор; и
RA2 представляет собой замещенный или незамещенный алкил, хлор или фтор, при этом: (i) RA1 или RA2 представляет собой хлор; или (ii) один из RA1 и RA2 представляет собой фтор, а другой из RA1 и RA2 выбран из группы, состоящей из незамещенного алкила, хлора и фтора
RA представляет собой водород или замещенный или незамещенный алкил или кислородзащитную группу; и
RB представляет собой водород или замещенный или незамещенный алкил, азотзащитную группу, или необязательно два RB взятые вместе с промежуточными атомами образуют замещенный или незамещенный гетероциклил или замещений или незамещенный гетероарил.
[0010] В некоторых вариантах реализации соединение Формулы (II) представляет собой соединение формулы:
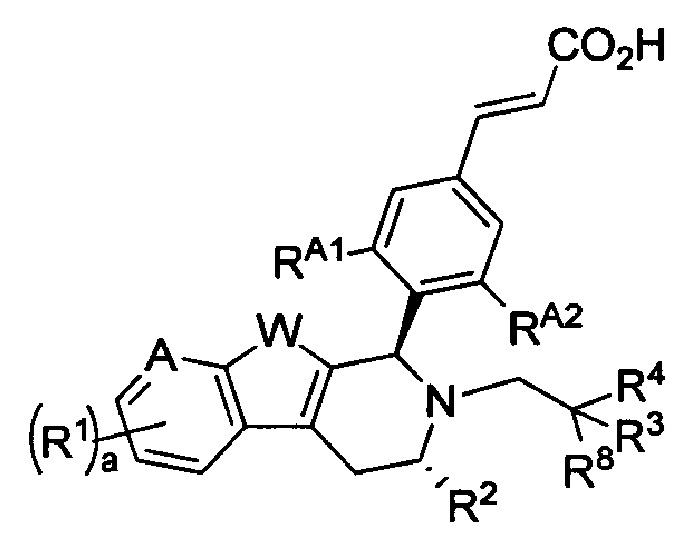
или фармацевтически приемлемую соль, причем R1, R2, R3, R4, R8, RA1, RA2, A, W и а как описаны в данном документе.
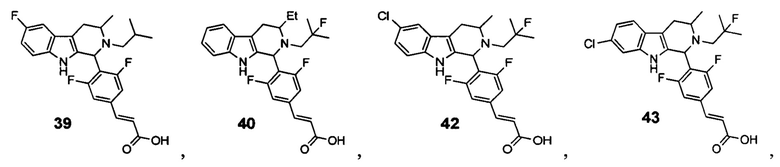
[0011] В некоторых вариантах реализации по меньшей мере один из RA1 и RA2 в Формуле(II) может представлять собой хлор. В некоторых вариантах реализации оба RA1 и RA2 в Формуле (II) могут представлять собой хлор. Примеры соединений Формулы (II) включают, но не ограничиваются ими:
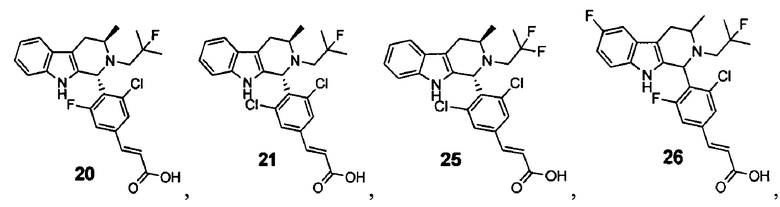
и их фармацевтически приемлемые соли.
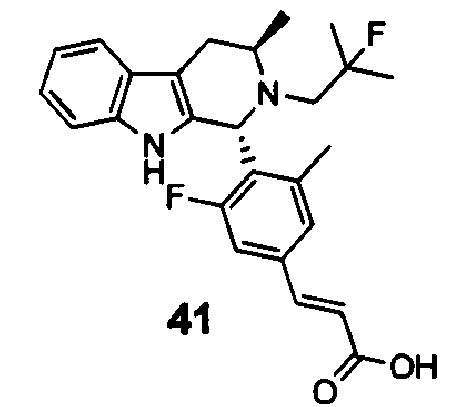
[0012] В некоторых вариантах реализации RA1 в Формуле (II) может представлять собой фтор, a RA2 может представлять собой метил, например, указанное ниже соединение 41:
[0013] В некоторых вариантах реализации, когда оба RA1 и RA2 в Формуле (II) представляют собой фтор, соединение также удовлетворяет по меньшей мере одному из следующих условий:
W представляет собой О или S;
по меньшей мере один из R1 не является водородом;
R2 не является водородом или метилом;
А представляет собой -N или -CRA, причем RA представляет собой замещенный или незамещенный алкил или кислородзащитную группу;
R3 и R4 взятые вместе с промежуточными атомами образуют замещенный или незамещенный карбоциклил или замещенный или незамещенный гетероциклил; и
по меньшей мере два из R3, R4 и R8 каждый независимо представляют собой галоген.
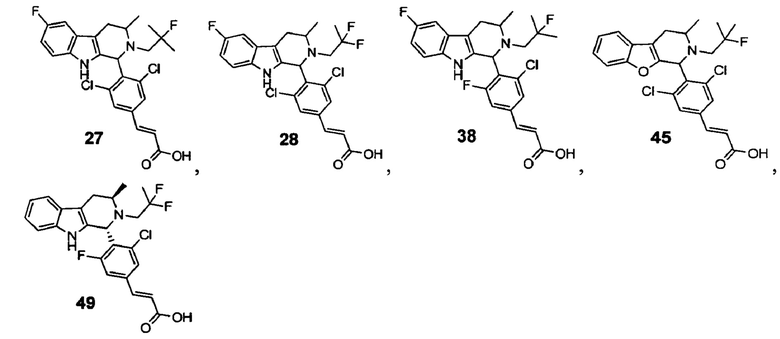
[0014] Примеры указанных соединений Формулы (II) включают, но не ограничиваются ими:

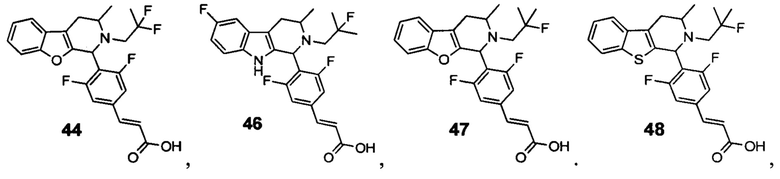 а также фармацевтически приемлемые соли.
а также фармацевтически приемлемые соли.
[0015] В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, содержащую одно или более соединений, описанных в данном документе, а также фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах реализации фармацевтические композиции, описанные в данном документе, содержат эффективное количество соединения СИЭР, описанного в данном документе. Эффективное количество в настоящем описании представляет собой терапевтически эффективное количество или профилактически эффективное количество.
[0016] В еще одном аспекте в настоящем изобретении предложены способы лечения пролиферативного заболевания (например, ЭР-положительного рака молочной железы, который может быть дикого типа или с мутациями ЭР), причем способ включает введение субъекту, нуждающемуся в лечении, эффективного количества любой из описанных в данном документе фармацевтических композиций.
[0017] В некоторых вариантах реализации целевое пролиферативное заболевание может представлять собой рак, включая, но не ограничиваясь ими, ЭР-положительный рак молочной железы или онкологические заболевания, вызванные ЭР дикого типа или ЭР с мутациями.
[0018] В некоторых вариантах реализации субъектом лечения является млекопитающее (например, человек или млекопитающее, не являющееся человеком).
[0019] Другой аспект настоящего изобретения относится к набору, включающему контейнер с соединением или его фармацевтической композицией, описанными в данном документе. Наборы, описанные в данном документе, могут включать однократную дозу или многократные дозы соединения или фармацевтической композиции. Возможно применение наборов в способе в соответствии с изобретением. В определенных вариантах реализации набор дополнительно включает инструкцию по применению соединения или фармацевтической композиции.
[0020] В еще одном аспекте настоящее изобретение обеспечивает соединения и фармацевтические композиции, описанные в данном документе, для применения для лечения пролиферативного заболевания, такого как рак, как описано в данном документе, и/или для приготовления лекарственного средства для применения для лечения целевого заболевания.
[0021] Подробности одного или более вариантов реализации изобретения изложены в описании ниже. Другие варианты реализации, задачи и преимущества настоящего изобретения будут очевидны из следующего далее подробного описания, примеров и формулы изобретения.
Определения
[0022] Более подробно определения конкретных функциональных групп и химических терминов описаны ниже. Химические элементы указаны в соответствии с Периодической таблицей элементов, версия CAS, Справочник по химии и физике (Handbook of Chemistry и Physics), 75-е изд., форзац, а определения конкретных функциональных групп приведены в настоящем описании. Кроме того, общие принципы органической химии, а также конкретные функциональные фрагменты и реакционная способность описаны в Thomas Sorrell, Organic Chemistry, University Science Books, Sausalito, 1999; Smith and March, March's Advanced Organic Chemistry, 5th Edition, John Wiley & Sons, Inc., New York, 2001; Larock, Comprehensive Organic Transformations, VCH Publishers, Inc., New York, 1989; и Carruthers, Some Modern Methods of Organic Synthesis, 3rd Edition, Cambridge University Press, Cambridge, 1987. Изобретение не ограничено каким-либо образом перечнем примеров заместителей, описанных в настоящем документе.
[0023] Соединения, описанные в настоящем документе, могут содержать один или более асимметричных центров и, таким образом, могут находиться в различных изомерных формах, например, в форме энантиомеров и/или диастереомеров. Например, соединения, описанные в настоящем документе, могут находиться в форме отдельного энантиомера, диастереомера или геометрического изомера или могут быть в форме смеси стереоизомеров, включая рацемические смеси и смеси, обогащенные одним или несколькими стереоизомерами. Изомеры могут быть выделены из смесей способами, известными специалистам в данной области техники, включая хиральную жидкостную хроматографию высокого давления (ВЭЖХ) и образование и кристаллизацию хиральных солей; предпочтительные изомеры также могут быть получены путем асимметричного синтеза. См., например, Jacques et al., Enantiomers, Racemates and Resolutions (Wiley Interscience, New York, 1981); Wilen et al., Tetrahedron 33:2725 (1977); Eliel, Stereochemistry of Carbon Compounds (McGraw-Hill, NY, 1962); и Wilen, Tables of Resolving Agents and Optical Resolutions p. 268 (E.L. Eliel, Ed., Univ. of Notre Dame Press, Notre Dame, IN 1972). Кроме того, изобретение включает соединения, описанные в данном документе как отдельные изомеры, по существу свободные от других изомеров, и, альтернативно, как смеси различных изомеров.
[0024] Диапазон значений, указанный в данном документе, включает каждое значение и поддиапазон в пределах указанного диапазона. Например, «C1-6» включает C1, С2, С3, С4, С5, С6, C1-6, C1-5, С1-4, С1-3, C1-2, C2-6, C2-5, С2-4, C2-3, С3-6, C3-5, С3-4, С4-6, С4-5 и С5-6.
[0025] Термин «алифатический» включает как насыщенную, так и ненасыщенную прямую цепь (то есть, неразветвленную), разветвленные, ациклические, циклические или полициклические алифатические углеводороды с необязательным замещением одной или несколькими функциональными группами. Как понятно специалисту в данной области техники, термин «алифатический» в настоящем описании включает, но не ограничивается ими, алкильные, алкенильные, алкинильные, циклоалкильные, циклоалкенильные и циклоалкинильные группы. Таким образом, термин "алкил" включает неразветвленные, разветвленные и циклические алкильные группы. Аналогичное определение относится к другим общим терминам, таким как «алкенил», «алкинил» и тому подобное. Кроме того, термины «алкил», «алкенил», «алкинил» и тому подобные включают как замещенные, так и незамещенные группы. В некоторых вариантах реализации термин «низший алкил» использован для обозначения алкильных групп (циклических, ациклических, замещенных, незамещенных, разветвленных или неразветвленных), содержащих 1-6 атомов углерода.
[0026] В некоторых вариантах реализации алкильная, алкенильная и алкинильная группы, используемые в описании, содержат 1-20 алифатических атомов углерода. В некоторых других вариантах реализации алкильная, алкенильная и алкинильная группы, используемые в описании, содержат 1-10 алифатических атомов углерода. В некоторых других вариантах реализации алкильная, алкенильная и алкинильная группы, использованные в описании, содержат 1-8 алифатических атомов углерода. В других вариантах реализации алкильная, алкенильная и алкинильная группы, использованные в описании, содержат 1-6 алифатических атомов углерода. В некоторых других вариантах реализации алкильная, алкенильная и алкинильная группы, использованные в описании, содержат 1-4 алифатических атома углерода. Таким образом, примеры алифатических групп включают, но не ограничиваются ими, например, метил, этил, н-пропил, изопропил, циклопропил, -СН2-циклопропил, винил, аллил, н-бутил, втор-бутил, изобутил, трет-бутил, циклобутил, -CH2-циклобутил, н-пентил, втор-пентил, изопентил, трет-пентил, циклопентил, -CH2-циклопентил, н-гексил, втор-гексил, циклогексил, -CH2-циклогексильные фрагменты и тому подобное, которые также могут иметь один или несколько заместителей. Примеры алкенильных групп включают, но не ограничиваются ими, например, этенил, пропенил, бутенил, 1-метил-2-бутен-1-ил и тому подобное. Примеры алкинильных групп включают, но не ограничиваются ими, этинил, 2-пропинил (пропаргил), 1-пропинил и тому подобное.
[0027] Термин «алкил» относится к радикалу неразветвленной или разветвленной насыщенной углеводородной группы, содержащей от 1 до 10 атомов углерода («С1-10 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 9 атомов углерода («С1-9 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 8 атомов углерода («С1-8 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 7 атомов углерода («С1-7 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 6 атомов углерода («C1-6 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 5 атомов углерода («С1-5 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 4 атомов углерода («С1-4 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 3 атомов углерода («C1-3 алкил»). В некоторых вариантах реализации алкильная группа содержит от 1 до 2 атомов углерода («С1-2 алкил»). В некоторых вариантах реализации алкильная группа содержит 1 атом углерода («C1 алкил»). В некоторых вариантах реализации алкильная группа содержит от 2 до 6 атомов углерода («С2-6 алкил»). Примеры C1-6 алкильных групп включают метил (C1), этил (С2), пропил (С3), (например, н-пропил, изопропил), бутил (С4) (например, н-бутил, трет-бутил, втор-бутил, изобутил), пентил (С5) (например, н-пентил, 3-пентанил, амил, неопентил, 3-метил-2-бутанил, третичный амил) и гексил (С6) (например, н-гексил). Дополнительные примеры алкильных групп включают н-гептил (С7), н-октил (C8) и тому подобное. Если не указано иное, каждый алкильной группы является независимо незамещенным («незамещенный алкил») или замещенным («замещенный алкил») одним или несколькими заместителями (например, галогеном, таким как F). В некоторых вариантах реализации алкильная группа представляет собой незамещенный C1-10 алкил (например, незамещенный C1-6 алкил, например, -CH3). В некоторых вариантах реализации алкильная группа представляет собой замещенный C1-10 алкил (например, замещенный C1-6 алкил, например -CF3).
[0028] «Алкенил» относится к радикалу неразветвленной или разветвленной углеводородной группы, которая содержит от 2 до 20 атомов углерода, одну или более двойную углерод-углеродную связь и не содержит тройных связей («С2-20 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 10 атомов углерода («С2-10 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 9 атомов углерода («С2-9 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 8 атомов углерода («С2-8 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 7 атомов углерода («С2-7 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 6 атомов углерода («С2-6 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 5 атомов углерода («С2-5 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 4 атомов углерода («С2-4 алкенил»). В некоторых вариантах реализации алкенильная группа содержит от 2 до 3 атомов углерода («С2-3 алкенил»). В некоторых вариантах реализации алкенильная группа содержит 2 атома углерода («С2 алкенил»). Одна или более двойных углерод-углеродных связей могут быть внутренними (например, в 2-бутениле) или концевыми (например, в 1-бутениле). Примеры С2-4 алкенильных групп включают этенил (С2), 1-пропенил (С3), 2-пропенил (С3), 1-бутенил (С4), 2-бутенил (С4), бутадиенил (С4) и тому подобное. Примеры С2-6 алкенильных групп включают указанные выше алкенильные группы С2-4, а также пентенил (С5), пентадиенил (С5), гексенил (C6) и тому подобное. Дополнительные примеры алкенила включают гептенил (С7), октенил (C8), октатриенил (C8) и тому подобное. Если не указано иное, каждый алкенильной группы является независимо необязательно замещенным, то есть незамещенным («незамещенный алкенил») или замещенным («замещенный алкенил») одним или несколькими заместителями. В некоторых вариантах реализации алкенильная группа представляет собой незамещенный С2-10 алкенил. В некоторых вариантах реализации алкенильная группа представляет собой замещенный С2-10 алкенил. В алкенильной группе двойная связь С=С, стереохимия которой не определена (например, -СН=CHCH3 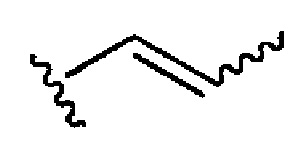 ), может представлять собой (E)- или (Z)-двойную связь.
), может представлять собой (E)- или (Z)-двойную связь.
[0029] «Алкинил» относится к радикалу неразветвленной или разветвленной углеводородной группы, содержащей от 2 до 20 атомов углерода, одну или более тройных углерод-углеродных связей и необязательно одну или более двойных связей («С2-20 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 10 атомов углерода («С2-10 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 9 атомов углерода («С2-9 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 8 атомов углерода («С2-8 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 7 атомов углерода («С2-7 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 6 атомов углерода («С2-6 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 5 атомов углерода («С2-5 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 4 атомов углерода («С2-4 алкинил»). В некоторых вариантах реализации алкинильная группа содержит от 2 до 3 атомов углерода («С2-3 алкинил»). В некоторых вариантах реализации алкинильная группа содержит 2 атома углерода («С2 алкинил»). Одна или более тройных углерод-углеродных связей могут быть внутренними (например, в 2-бутиниле) или концевыми (например, в 1-бутиниле). Примеры С2-4 алкинильных групп включают, без ограничения, этинил (С2), 1-пропинил (C3), 2-пропинил (C3), 1-бутинил (С4), 2-бутинил (С4) и тому подобное. Примеры С2-6 алкенильных групп включают указанные выше С2-4 алкинильные группы, а также пентинил (С5), гексинил (C6) и тому подобное. Дополнительные примеры алкинила включают гептинил (С7), октинил (С8) и тому подобное. Если не указано иное, каждый алкинильной группы является независимо необязательно замещенным, то есть незамещенным («незамещенный алкинил») или замещенным («замещенный алкинил») одним или несколькими заместителями. В некоторых вариантах реализации алкинильная группа представляет собой незамещенный С2-10 алкинил. В некоторых вариантах реализации алкинильная группа представляет собой замещенный С2-10 алкинил.
[0030] Термин «карбоциклильный» или «карбоциклический» относится к радикалу неароматической циклической углеводородной группы, содержащей от 3 до 10 кольцевых атомов углерода («C3-10 карбоциклил») и нулевые гетероатомы в неароматической кольцевой системе. В некоторых вариантах реализации карбоциклильная группа содержит от 3 до 8 кольцевых атомов углерода («С3-8 карбоциклил»). В некоторых вариантах реализации карбоциклильная группа содержит от 3 до 6 кольцевых атомов углерода («С3-6 карбоциклил»). В некоторых вариантах реализации карбоциклильная группа содержит от 3 до 6 кольцевых атомов углерода («С3-6 карбоциклил»). В некоторых вариантах реализации карбоциклильная группа содержит от 5 до 10 кольцевых атомов углерода («С5-10 карбоциклил»). Примеры С3-6 карбоциклильных групп включают, без ограничения, циклопропил (C3), циклопропенил (C3), циклобутил (С4), циклобутенил (С4), циклопентил (С5), циклопентенил (C5), циклогексил (C6), циклогексенил (C6), циклогексадиенил (C6) и тому подобное. Примеры С3-8 карбоциклильных групп включают, без ограничения, указанные выше С3-6 карбоциклильные группы, а также циклогептил (С7), циклогептенил (С7), циклогептадиенил (С7), циклогептатриенил (С7), циклооктил (C8), циклооктенил (С8), бицикло[2,2,1]гептанил (С7), бицикло[2,2,2]октанил (C7) и тому подобное. Примеры C3-10 карбоциклильных групп включают, без ограничения, указанные выше С3-8 карбоциклильные группы, а также циклононил (С9), циклононенил (С9), циклодецил (C10), циклодеценил (C10), октагидро-1Н-инденил (С9), декагидронафталенил (C10), спиро[4,5]деканил (C10) и тому подобное. Как следует из приведенных выше примеров, в некоторых вариантах реализации карбоциклильная группа является моноциклической («моноциклический карбоциклил») или содержит конденсированную, мостиковую или спиро-кольцевую систему, такую как бициклическая система («бициклический карбоциклил»), и может быть насыщенной или частично ненасыщенной. «Карбоциклил» также включает кольцевые системы, в которых карбоциклическое кольцо, как определено выше, соединено с одной или более арильными или гетероарильными группами, при этом точка присоединения находится на карбоциклическом кольце, и в таких случаях количество атомов углерода обозначает количество атомов углерода в карбоциклической кольцевой системе. Если не указано иное, каждый карбоциклильной группы является независимо необязательно замещенным, то есть незамещенным («незамещенный карбоциклил») или замещенным («замещенный карбоциклил») одним или несколькими заместителями. В некоторых вариантах реализации карбоциклильная группа представляет собой незамещенный C3-10 карбоциклил. В некоторых вариантах реализации карбоциклильная группа представляет собой замещенный C3-10 карбоциклил.
[0031] В некоторых вариантах реализации «карбоциклил» представляет собой моноциклическую насыщенную карбоциклильную группу, содержащую от 3 до 10 кольцевых атомов углерода («C3-10 циклоалкил»). В некоторых вариантах реализации циклоалкильная группа содержит от 3 до 8 кольцевых атомов углерода («С3-8 циклоалкил»). В некоторых вариантах реализации циклоалкильная группа содержит от 3 до 6 кольцевых атомов углерода («С3-6 циклоалкил»). В некоторых вариантах реализации циклоалкильная группа содержит от 5 до 6 кольцевых атомов углерода («С5-6 циклоалкил»). В некоторых вариантах реализации циклоалкильная группа содержит от 5 до 10 кольцевых атомов углерода («С5-10 циклоалкил»). Примеры С5-6 циклоалкильных групп включают циклопентил (С5) и циклогексил (С5). Примеры C3-6 циклоалкильных групп включают указанные выше С5-6 циклоалкильные группы, а также циклопропил (C3) и циклобутил (С4). Примеры С3-8 циклоалкильных групп включают указанные выше С3-6 циклоалкильные группы, а также циклогептил (С7) и циклооктил (С8). Если не указано иное, каждый циклоалкильной группы является независимо незамещенным («незамещенный циклоалкил») или замещенным («замещенный циклоалкил») одним или несколькими заместителями. В некоторых вариантах реализации циклоалкильная группа представляет собой незамещенный C3-10 циклоалкил. В некоторых вариантах реализации циклоалкильная группа представляет собой замещенный C3-10 циклоалкил.
[0032] «Гетероциклил» или «гетероциклический» относится к радикалу 3-10-членной неароматической кольцевой системы, содержащей кольцевые атомы углерода и от 1 до 4 кольцевых гетероатомов, причем каждый гетероатом независимо выбран из азота, кислорода, серы, бора, фосфора и кремния («3-10-членный гетероциклил»). В гетероциклических группах, содержащих один или несколько атомов азота, точкой присоединения может быть атом углерода или азота в зависимости от валентности. Гетероциклильная группа может быть моноциклической («моноциклический гетероциклил») или конденсированной, мостиковой или спиро-кольцевой системой, такой как бициклическая система («бициклический гетероциклил»), и может быть насыщенной или частично ненасыщенной. Гетероциклильные бициклические кольцевые системы могут содержать один или более гетероатомов в одном или обоих кольцах. «Гетероциклил» также включает кольцевые системы, в которых гетероциклическое кольцо, как определено выше, соединено с одной или более карбоциклильных группа, в которых точка присоединения находится на карбоциклильном или на гетероциклическом кольце, или кольцевые системы, в которых гетероциклическое кольцо, как определено выше, соединено с одной или более арильными или гетероарильными группами, в которых точка присоединения находится на гетероциклическом кольце, и в таких случаях количество членов кольца обозначает количество членов кольца в гетероциклической кольцевой системе. Если не указано иное, каждый гетероциклильной группы является независимо необязательно замещенным, то есть незамещенным («незамещенный гетероциклил») или замещенным («замещенный гетероциклил») одним или несколькими заместителями. В некоторых вариантах реализации гетероциклильная группа представляет собой незамещенный 3-10-членный гетероциклил. В некоторых вариантах реализации гетероциклильная группа представляет собой замещенный 3-10-членный гетероциклил.
[0033] В некоторых вариантах реализации гетероциклильная группа представляет собой 5-10-членную неароматическую кольцевую систему, содержащую кольцевые атомы углерода и 1-4 кольцевых гетероатома, причем каждый гетероатом независимо выбран из азота, кислорода, серы, бора, фосфора и кремния («5-10-членный гетероциклил»). В некоторых вариантах реализации гетероциклильная группа представляет собой 5-8-членную неароматическую кольцевую систему, содержащую кольцевые атомы углерода и 1-4 гетероатома, причем каждый гетероатом независимо выбран из азота, кислорода и серы («5-8-членный гетероциклил»). В некоторых вариантах реализации гетероциклильная группа представляет собой 5-6-членную неароматическую кольцевую систему, содержащую кольцевые атомы углерода и 1-4 гетероатома, причем каждый гетероатом независимо выбран из азота, кислорода и серы («5-6-членный гетероциклил»). В некоторых вариантах реализации 5-6-членный гетероциклил содержит 1-3 кольцевых гетероатома, выбранных из азота, кислорода и серы. В некоторых вариантах реализации 5-6-членный гетероциклил содержит 1-2 кольцевых гетероатома, выбранных из азота, кислорода и серы. В некоторых вариантах реализации 5-6-членный гетероциклил содержит один кольцевой гетероатом, выбранный из азота, кислорода и серы.
[0034] Примеры 3-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, азирдинил, оксиранил, тииранил. Примеры 4-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, азетидинил, оксетанил и тиетанил. Примеры 5-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, тетрагидрофуранил, дигидрофуранил, тетрагидротиофенил, дигидротиофенил, пирролидинил, дигидропирролил и пирролил-2,5-дион. Примеры 5-членных гетероциклильных групп, содержащих два гетероатома, включают, без ограничения, диоксоланил, оксасульфуранил, дисульфуранил и оксазолидин-2-он. Примеры 5-членных гетероциклильных групп, содержащих три гетероатома, включают, без ограничения, триазолинил, оксадиазолинил и тиадиазолинил. Примеры 6-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, пиперидинил, тетрагидропиранил, дигидропиридинил и тианил. Примеры 6-членных гетероциклильных групп, содержащих два гетероатома, включают, без ограничения, пиперазинил, морфолинил, дитианил и диоксанил. Примеры 6-членных гетероциклильных групп, содержащих два гетероатома, включают, без ограничения, триазинанил. Примеры 7-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, азепанил, оксепанил и тиепанил. Примеры 8-членных гетероциклильных групп, содержащих один гетероатом, включают, без ограничения, азоканил, оксеканил и тиоканил. Типичные 5-членные гетероциклильные группы, соединенные с арильным кольцом С6 (также указано в настоящем описании как 5,6-бициклическое гетероциклическое кольцо) включают, без ограничения, индолинил, изоиндолинил, дигидробензофуранил, дигидробензотиенил, бензоксазолинонил и тому подобное. Типичные 6-членные гетероциклильные группы, соединенные с арильным кольцом (также указано в настоящем описании как 6,6-бициклическое гетероциклическое кольцо), включают, без ограничения, тетрагидрохинолинил, тетрагидроизохинолинил и тому подобное.
[0035] «Арил» относится к радикалу моноциклической или полициклической (например, бициклической или трициклической) 4n+2 ароматической кольцевой системы (например, содержащей 6, 10 или 14 пи-электронов в циклической матрице), содержащей 6-14 кольцевых атомов углерода и нулевые гетероатомы в системе ароматического кольца («C6-14 арил»). В некоторых вариантах реализации арильная группа содержит шесть кольцевых атомов углерода («С6 арил»; например, фенил). В некоторых вариантах реализации арильная группа содержит десять кольцевых атомов углерода («C10 арил»; например, нафтил, такой как 1-нафтил и 2-нафтил). В некоторых вариантах реализации арильная группа содержит 14 кольцевых атомов углерода («С14 арил»; например, антрацил). «Арил» также включает кольцевые системы, в которых арильное кольцо, как определено выше, соединено с одной или более карбоциклильных или гетероциклильных групп, при этом радикал или точка присоединения находится на арильном кольце, в таких случаях количество атомов углерода обозначает количество атомов углерода в арильной кольцевой системе. Если не указано иное, каждый арильной группы является независимо необязательно замещенным, то есть незамещенным («незамещенный арил») или замещенным («замещенный арил») одним или более заместителями. В некоторых вариантах реализации арильная группа представляет собой незамещенный C6-14 арил. В некоторых вариантах реализации арильная группа представляет собой замещенный C6-14 арил.
[0036] «Аралкил» представляет собой подгруппу алкила и арила и относится к необязательно замещенной алкильной группе, замещенной необязательно замещенной арильной группой. В некоторых вариантах реализации аралкил представляет собой необязательно замещенный бензил. В некоторых вариантах реализации аралкил представляет собой бензил. В некоторых вариантах реализации аралкил представляет собой необязательно замещенный фенэтил. В некоторых вариантах реализации аралкил представляет собой фенэтил.
[0037] «Гетероарил» относится к радикалу 5-10-членной моноциклической или бициклической 4n+2 ароматической кольцевой системы (например, содержащей 6 или 10 пи-электронов в циклической матрице), содержащей кольцевые атомы углерода и 1-4 кольцевых гетероатома в системе ароматического кольца, причем каждый гетероатом независимо выбран из азота, кислорода и серы («5-10-членный гетероарил»). В гетероциклических группах, содержащих один или более атомов азота, точкой присоединения может быть атом углерода или азота, в зависимости от валентности. Гетероарильные бициклические кольцевые системы могут содержать один или более гетероатомов в одном или обоих кольцах. «Гетероарил» включает кольцевые системы, в которых гетероарильное кольцо, как определено выше, соединено с одной или более карбоциклильными или гетероциклильными группами, причем точка присоединения находится на гетероарильном кольце, в таких случаях количество членов кольца обозначает количество членов кольца в гетероарильной кольцевой системе. «Гетероарил» также включает кольцевые системы, в которых гетероарильное кольцо, как определено выше, соединено с одной или более арильными группами, при этом точка присоединения находится на арильном или гетероарильном кольце, в таких случаях количество членов кольца обозначает количество членов кольца в присоединенной (арильной/гетероарильной) кольцевой системе. Бициклические гетероарильные группы, в которых одно кольцо не содержит гетероатом (например, индолил, хинолинил, карбазолил и тому подобное), точка присоединения может быть на любом кольце, то есть или на кольце, содержащем гетероатом (например, 2-индолил), или на кольце, которое не содержит гетероатом (например, 5-индолил).
[0038] В некоторых вариантах реализации гетероарильная группа представляет собой 5-10-членную ароматическую кольцевую систему, содержащую кольцевые атомы углерода и 1-4 кольцевых гетероатома в ароматической кольцевой системе, причем каждый гетероатом независимо выбран из азота, кислорода и серы («5-10-членный гетероарил»). В некоторых вариантах реализации гетероарильная группа представляет собой 5-8-членную неароматическую кольцевую систему, содержащую кольцевые атомы углерода и 1-4 гетероатома в ароматической кольцевой системе, причем каждый гетероатом независимо выбран из азота, кислорода и серы («5-8-членный гетероарил»). В некоторых вариантах реализации гетероарильная группа представляет собой 5-6-членную ароматическую кольцевую систему, содержащую кольцевые атомы углерода и 1-4 гетероатома в ароматической кольцевой системе, причем каждый гетероатом независимо выбран из азота, кислорода и серы («5-6-членный гетероарил»). В некоторых вариантах реализации 5-6-членный гетероарил содержит 1-3 кольцевых гетероатома, выбранных из азота, кислорода и серы. В некоторых вариантах реализации 5-6-членный гетероарил содержит 1-2 кольцевых гетероатома, выбранных из азота, кислорода и серы. В некоторых вариантах реализации 5-6-членный гетероарил содержит 1 кольцевой гетероатом, выбранный из азота, кислорода и серы. Если не указано иное, каждый гетероарильной группы является независимо необязательно замещенным, то есть незамещенным («незамещенный гетероарил») или замещенным («замещенный гетероарил») одним или более заместителями. В некоторых вариантах реализации гетероарильная группа представляет собой незамещенный 5-14-членный гетероарил. В некоторых вариантах реализации гетероарильная группа представляет собой замещенный 5-14-членный гетероарил.
[0039] Примеры 5-членных гетероарильных групп, содержащих один гетероатом, включают, без ограничения, пирролил, фуранил и тиофенил. Примеры 5-членных гетероарильных групп, содержащих два гетероатома, включают, без ограничения, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил и изотиазолил. Примеры 5-членных гетероарильных групп, содержащих три гетероатома, включают, без ограничения, триазолил, оксадиазолил и тиадиазолил. Примеры 5-членных гетероарильных групп, содержащих четыре гетероатома, включают, без ограничения, тетразолил. Примеры 6-членных гетероарильных групп, содержащих один гетероатом, включают, без ограничения, пиридинил. Примеры 6-членных гетероарильных групп, содержащих два гетероатома, включают, без ограничения, пиридазинил, пиримидинил и пиразинил. Примеры 6-членных гетероарильных групп, содержащих три или четыре гетероатома, включают, без ограничения, триазинил и тетразинил, соответственно. Примеры 7-членных гетероарильных групп, содержащих один гетероатом, включают, без ограничения, азепинил, оксепинил и тиепинил. Примеры 5,6-бициклических гетероарильных групп включают, без ограничения, индолил, изоиндолил, индазолил, бензотриазолил, бензотиофенил, изобензотиофенил, бензофуранил, бензоизофуранил, бензимидазолил, бензоксазолил, бензизоксазолил, бензоксадиазолил, бензтиазолил, бензизотиазолил, бензтиадиазолил, индолизинил и пуринил. Примеры 6,6-бициклических гетероарильных групп включают, без ограничения, нафтиридинил, птеридинил, хинолинил, изохинолинил, циннолинил, хиноксалинил, фталазинил и хиназолинил.
[0040] «Гетероаралкил» представляет собой подгруппу алкила и гетероарила и относится к необязательно замещенной алкильной группе, замещенной необязательно замещенной гетероарильной группой.
[0041] Термин «ненасыщенный» или «частично ненасыщенный» относится к группе, содержащей по меньшей мере одну двойную или тройную связь. Термин «частично ненасыщенные» кольцевые системы включает кольца, содержащие множественные ненасыщенные фрагменты, но не включает ароматические группы (например, арильные или гетероарильные группы). Аналогично «насыщенный» относится к группе, которая не содержит двойную или тройную связь, то есть содержит только одинарные связи.
[0042] Алкильная, алкенильная, алкинильная, карбоциклильная, гетероциклильная, арильная и гетероарильная группы, которые являются двухвалентными мостиковыми группами, далее упоминаются с использованием суффикса «-ен», например, алкилен, алкенилен, алкинилен, карбоциклилен, гетероциклилен, арилен и гетероарилен.
[0043] Атом, фрагмент или группа, описанные в данном документе, могут быть незамещенными или замещенными, в зависимости от валентности, если явно не указано иное. Термин «необязательно замещенный» означает замещенный или незамещенный.
[0044] Группа является необязательно замещенной, если явно не указано иное. Термин «необязательно замещенный» означает замещенный или незамещенный. В некоторых вариантах реализации алкильная, алкенильная, алкинильная, карбоциклильная, гетероциклильная, арильная и гетероарильная группы необязательно являются замещенными (например, «замещенная» или «незамещенная» алкильная, «замещенная» или «незамещенная» алкенильная, «замещенная» или «незамещенная» алкинильная, «замещенная» или «незамещенная» карбоциклильная, «замещенная» или «незамещенная» гетероциклильная, «замещенная» или «незамещенная» арильная и «замещенная» или «незамещенная» гетероарильная группа). В общем случае термин «замещенный», перед которым употреблен или не употреблен термин «необязательно», означает, что по меньшей мере один присутствующий в группе водород (например, атом углерода или азота) замещен допустимым заместителем, например, заместителем, при замещении которым образуется стабильное соединение, например, соединение, которое самопроизвольно не подвергается превращению, например, в результате перегруппировки, циклизации, элиминирования или другой реакции. Если не указано иное, «замещенная» группа содержит заместитель в одном или более положениях в группе, и при замещении более чем в одном положении в любой данной структуре заместители могут быть одинаковыми или различными в каждом положении. Предполагается, что термин «замещенный» включает замещение всеми допустимыми заместителями органических соединений, всеми описанными в данном документе заместителями с образованием стабильного соединения. Настоящее изобретение включает любые указанные комбинации для получения стабильного соединения. Для целей настоящего описания гетероатомы, такие как азот, могут иметь водородные заместители и/или любой подходящий заместитель, как описано в данном документе, которые удовлетворяют валентности гетероатомов и приводят к образованию стабильного фрагмента. В некоторых вариантах реализации заместитель представляет собой заместитель атома углерода. В некоторых вариантах реализации заместитель представляет собой заместитель атома азота. В некоторых вариантах реализации заместитель представляет собой заместитель атома кислорода. В некоторых вариантах реализации заместитель представляет собой заместитель атома серы.
Примеры заместителей атома углерода включают, но не ограничиваются ими, галоген, -CN, -NO2, -N3, -SO2H, -SO3H, -ОН, -ORaa, -ON(Rbb)2, -N(Rbb)2, -N(Rbb)3+X-, -N(ORcc)Rbb, -SH, -SRaa, -SSRcc, -C(=O)Raa, -CO2H, -CHO, -C(ORcc)2, -CO2Raa, -OC(=O)Raa, -OCO2Raa, -C(=O)N(Rbb)2, -OC(=O)N(Rbb)2, -NRbbC(=O)Raa, -NRbbCO2Raa, -NRbbC(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -OC(=NRbb)Raa, -OC(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -OC(=NRbb)N(Rbb)2, -NRbbC(=NRbb)N(Rbb)2, -C(=O)NRbbSO2Raa, -NRbbSO2Raa, -SO2N(Rbb)2, -SO2Raa, -SO2ORaa, -OSO2Raa, -S(=O)Raa, -OS(=O)Raa, -Si(Raa)3, -OSi(Raa)3 -C(=S)N(Rbb)2, -C(=O)SRaa, -C(=S)SRaa, -SC(=S)SRaa, -SC(=O)SRaa, -OC(=O)SRaa, -SC(=O)ORaa, -SC(=O)Raa, -P(=O)(Raa)2, -P(=O)(ORcc)2, -OP(=O)(Raa)2, -OP(=O)(ORcc)2, -P(=O)(N(Rbb)2)2, -OP(=O)(N(Rbb)2)2, -NRbbP(=O)(Raa)2, -NRbbP(=O)(ORcc)2, -NRbbP(=O)(N(Rbb)2)2, -P(Rcc)2, -P(ORcc)2, -P(Rcc)3+X-, -P(ORcc)3+X-, -P(Rcc)4, -P(ORcc)4, -OP(Rcc)2, -OP(Rcc)3+X-, -OP(ORcc)2, -OP(ORcc)3+X-, -OP(Rcc)4, -OP(ORcc)4, -B(Raa)2, -B(ORcc)2, -BRaa(ORcc), C1-10 алкил, C1-10 пергалоалкил, С2-10 алкенил, С2-10 алкинил, C3-10 карбоциклил, 3-14-членный гетероциклил, C6-14 арил и 5-14-членный гетероарил, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rdd; где Х- представляет собой противоион;
или два геминальных атома водорода на атоме углерода заменены группой =O, =S, =NN(Rbb)2, =NNRbbC(=O)Raa, =NNRbbC(=O)ORaa, =NNRbbS(=O)2Raa, =NRbb или =NORcc;
каждый Raa независимо выбран из C1-10 алкила, C1-10 пергалоалкила, С2-10 алкенила, C2-10 алкинила, C3-10 карбоциклила, 3-14-членного гетероциклила, C6-14 арила и 5-14-членного гетероарила, или две группы Raa соединены с образованием 3-14-членного гетероциклильного или 5-14-членного гетероарильного кольца, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группой 0, 1, 2, 3, 4 или 5 Rdd;
каждый Rbb независимо выбран из водорода, -ОН, -ORaa, -N(Rcc)2, -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, -P(=O)(Raa)2, -P(=O)(ORcc)2, -P(=O)(N(Rcc)2)2, C1-10 алкила, C1-10 пергалоалкила, C2-10 алкенила, C2-10 алкинила, C3-10 карбоциклила, 3-14-членного гетероциклила, C6-14 арила и 5-14-членного гетероарила, или две Rbb группы соединены с образованием 3-14-членного гетероциклильного или 5-14-членного гетероарильного кольца, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rdd; где Х- представляет собой противоион;
каждый Rcc независимо выбран из C1-10 алкила, C1-10 пергалоалкила, С2-10 алкенила, С2-10 алкинила, C3-10 карбоциклила, 3-14-членного гетероциклила, C6-14 арила и 5-14-членного гетероарила, или две группы Rcc соединены с образованием 3-14-членного гетероциклильного или 5-14-членного гетероарильного кольца, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rdd;
каждый Rdd независимо выбран из галогена, -CN, -NO2, -N3, -SO2H, -SO3H, -ОН, -ORee, -ON(Rff)2, -N(Rff)2, -N(Rff)3+X-, -N(ORee)Rff, -SH, -SRee, -SSRee, -C(=O)Ree, -CO2H, -CO2Ree, -OC(=O)Ree, -OCO2Ree, -C(=O)N(Rff)2, -OC(=O)N(Rff)2, -NRffC(=O)Ree, -NRffCO2Ree, -NRffC(=O)N(Rff)2, -C(=NRff)ORee, -OC(=NRff)Ree, -OC(=NRff)ORee, -C(=NRff)N(Rff)2, -OC(=NRff)N(Rff)2, -NRffC(=NRff)N(Rff)2, -NRffSO2Ree, -SO2N(Rff)2, -SO2Ree, -SO2ORee, -OSO2Ree, -S(=O)Ree, -Si(Ree)3, -OSi(Ree)3, -C(=S)N(Rff)2, -C(=O)SRee, -C(=S)SRee, -SC(=S)SRee, -P(=O)(ORee)2, -P(=O)(Ree)2, -OP(=O)(Ree)2, -OP(=O)(ORee)2, С1-6 алкила, C1-6 пергалоалкила, C2-6 алкенила, С2-6 алкинила, C3-10 карбоциклила, 3-10-членного гетероциклила, C6-10 арила, 5-10-членного гетероарила, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rgg, или два геминальных заместителя Rdd могут быть соединены для образования =O или =S; где X- представляет собой противоион;
каждый Ree независимо выбран из C1-6 алкила, C1-6 пергалоалкила, С2-6 алкенила, С2-6 алкинила, C3-10 карбоциклила, C6-10 арила, 3-10-членного гетероциклила и 3-10-членного гетероарила, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rgg;
каждый Rff независимо выбран из водорода, C1-6 алкила, C1-6 пергалоалкила, С2-6 алкенила, C2-6 алкинила, C3-10 карбоциклила, 3-10-членного гетероциклила, C6-10 арила и 5-10-членного гетероарила, или две группы Rff соединены с образованием 3-14-членного гетероциклильного или 5-14-членного гетероарильного кольца, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rgg;
каждый Rgg независимо представляет собой галоген, -CN, -NO2, -N3, -SO2H, -SO3H, -ОН, -ОС1-6 алкил, -ON(C1-6 алкил)2, -N(C1-6 алкил)2, -N(C1-6 алкил)3+Х-, -NH(C1-6 алкил)2+Х-, -NH2(С1-6алкил+Х-, -NH3+X-, -N(OC1-6 алкил)(C1-6 алкил), -N(OH)(C1-6 алкил), -NH(OH), -SH, -SC1-6 алкил, -SS(C1-6 алкил), -C(=O)(C1-6 алкил), -СО2Н, -CO2(C1-6 алкил), -OC(=O)(C1-6 алкил), -OCO2(C1-6 алкил), -C(=O)NH2, -C(=O)N(C1-6 алкил)2, -OC(=O)NH(C1-6 алкил), -NHC(=O)(C1-6 алкил), -N(C1-6 алкил)С(=O)(C1-6 алкил), -NHCO2(C1-6 алкил), -NHC(=O)N(C1-6 алкил)2, -NHC(=O)NH(C1-6 алкил), -NHC(=O)NH2, -C(=NH)O(C1-6 алкил), -OC(=NH)(C1-6 алкил), -OC(=NH)OC1-6 алкил, -C(=NH)N(C1-6 алкил)2, -C(=NH)NH(C1-6 алкил), -C(=NH)NH2, -OC(=NH)N(C1-6 алкил)2, -OC(NH)NH(C1-6 алкил), -OC(NH)NH2, -NHC(NH)N(C1-6 алкил)2, -NHC(=NH)NH2, -NHSO2(C1-6 алкил), -SO2N(C1-6 алкил)2, -SO2NH(C1-6 алкил), -SO2NH2, -SO2C1-6 алкил, -SO2OC1-6 алкил, -OSO2C1-6 алкил, -SOC1-6 алкил, -Si(C1-6 алкил)3, -OSi(C1-6 алкил)3 -C(=S)N(C1-6 алкил)2, C(=S)NH(C1-6 алкил), C(=S)NH2, -C(=O)S(C1-6 алкил), -C(=S)SC1-6 алкил, -SC(=S)SC1-6 алкил, -P(=O)(OC1-6 алкил)2, -P(=O)(C1-6 алкил)2, -OP(=O)(C1-6 алкил)2, -OP(=O)(OC1-6 алкил)2, C1-6 алкил, C1-6 пергалоалкил, С2-6 алкенил, С2-6 алкинил, C3-10 карбоциклил, C6-10 арил, 3-10-членный гетероциклил, 5-10-членный гетероарил; или два геминальных заместителя Rgg могут быть соединены для образования =O или =S; где Х- представляет собой противоион.
каждый Rgg независимо представляет собой галоген, -CN, -NO2, -N3, -SO2H, -SO3H, -ОН, -ОС1-6 алкил, -ON(C1-6 алкил)2, -N(C1-6 алкил)2, -N(C1-6 алкил)3+Х-, -NH(C1-6 алкил)2+Х-, -NH2(C1-6 алкил+Х-, -NH3+Х-, -N(OC1-6 алкил)(C1-6 алкил), -N(OH)(C1-6 алкил), -NH(OH), -SH, -SC1-6 алкил, -SS(C1-6 алкил), -C(=O)(C1-6 алкил), -CO2H, -CO2(C1-6 алкил), -OC(=O)(C1-6 алкил), -OCO2(C1-6 алкил), -C(=O)NH2, -C(=O)N(C1-6 алкил)2, -OC(=O)NH(C1-6 алкил), -NHC(=O)(C1-6 алкил), -N(C1-6 алкил)С(=O)(C1-6 алкил), -NHCO2(C1-6 алкил), -NHC(=O)N(C1-6 алкил)2, -NHC(=O)NH(C1-6 алкил), -NHC(=O)NH2, -C(=NH)O(C1-6 алкил), -OC(=NH)(C1-6 алкил), -OC(=NH)OC1-6 алкил, -C(=NH)N(C1-6 алкил)2, -C(=NH)NH(C1-6 алкил), -C(=NH)NH2, -OC(=NH)N(C1-6 алкил)2, -OC(NH)NH(C1-6 алкил), -OC(NH)NH2, -NHC(NH)N(C1-6 алкил)2, -NHC(=NH)NH2, -NHSO2(C1-6 алкил), -SO2N(C1-6 алкил)2, -SO2NH(C1-6 алкил), -SO2NH2, -SO2C1-6 алкил, -SO2OC1-6 алкил, -OSO2C1-6 алкил, -SOC1-6 алкил, -Si(C1-6 алкил)3, -OSi(C1-6 алкил)3, -C(=S)N(C1-6 алкил)2, C(=S)NH(C1-6 алкил), C(=S)NH2, -C(=O)S(C1-6 алкил), -C(=S)SC1-6 алкил, -SC(=S)SC1-6 алкил, -P(=O)(OC1-6 алкил)2, -P(=O)(C1-6 алкил)2, -OP(=O)(C1-6 алкил)2, -OP(=O)(OC1-6 алкил)2, C1-6 алкил, C1-6 пергалоалкил, C2-6 алкенил, C2-6 алкинил, C3-10 карбоциклил, C6-10 арил, 3-10-членный гетероциклил, 5-10-членный гетероарил; или два геминальных заместителя Rgg могут быть соединены для образования =O или =S; где Х- представляет собой противоион.
[0045] «Противоион» или «анионный противоион» представляет собой группу с отрицательным зарядом, связанную с положительно заряженной группой для поддержания нейтральности электрона. Анионный противоион может быть одновалентным (то есть содержащим один формальный отрицательный заряд). Анионный противоион может также быть многовалентным (то есть содержащим более одного формального отрицательного заряда), например, двухвалентным или трехвалентным. Примеры противоионов включают галид-ионы (например, F-, Cl-, Br-, I-), NO3-, ClO4-, ОН-, H2PO4-, HSO4-, сульфонат-ионы (например, метансульфонат, трифторметансульфонат, п-толуолсульфонат, бензолсульфонат, 10-камфорсульфонат, нафталин-2-сульфонат, нафталин-1-сульфоновая кислота-5-сульфонат, этан-1-сульфоновая кислота-2-сульфонат и тому подобное), карбоксилат-ионы (например, ацетат, пропаноат, бензоат, глицерат, лактат, тартрат, гликолят, глюконат и тому подобное), BF4-, PF4-, PF6-, AsF6-, SbF6-, В[3,5-(CF3)2С6Н3]4]-, BPh4-, Al(ОС(CF3)3)4- и карборан-анион (например, СВ11Н12- или (HCB11Me5Br6)-). Примеры противоионов, которые могут быть многовалентными, включают СО32-, НРО42-, PO43-, B4O72-, SO42-, S2O32-, карбоксилат-анионы (например, тартрат, цитрат, фумарат, малеат, малат, малонат, глюконат, сукцинат, глутарат, адипат, пимелат, суберат, азелат, себацат, салицилат, фталаты, аспартат, глутамат и тому подобное) и карбораны.
[0046] Термин «гало» или «галоген» относится к фтору (фтор, -F), хлору (хлор, -Cl), брому (бром, -Br) или йоду (йод, -I).
[0047] «Ацил» относится к фрагменту, выбранному из группы, состоящей из -C(=O)Raa, -СНО, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -C(=O)NRbbSO2Raa, -C(=S)N(Rbb)2, -C(=O)SRaa или -C(=S)SRaa, где Raa и Rbb как определены в данном описании.
[0048] Атомы азота могут быть замещенными или незамещенными в зависимости от валентности и включают первичные, вторичные, третичные и четвертичные атомы азота. Примеры заместителей атома азота включают, но не ограничиваются ими, водород, -ОН, -ORaa, -N(Rcc)2, -CN, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRbb)Raa, -C(-NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, -P(=O)(ORcc)2, -P(=O)(Raa)2, -P(=O)(N(Rcc)2)2, C1-10 алкил, C1-10 пергалоалкил, С2-10 алкенил, С2-10 алкинил, C3-10 карбоциклил, 3-14-членный гетероциклил, C6-14 арил и 5-14-членный гетероарил, или две Rcc группы, соединенные с атомом азота, соединены с образованием 3-14-членного гетероциклильного или 5-14-членного гетероарильного кольца, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rdd, и Raa, Rbb, Rcc и Rdd как определены выше.
[0049] В некоторых вариантах реализации заместитель, присутствующий на атоме азота, представляет собой азотзащитную группу (также называемую аминозащитной группой). Азотзащитная группа включает, но не ограничивается ими, -ОН, -ORaa, -N(Rcc)2, -C(=O)Raa, -C(=O)N(Rcc)2, -CO2Raa, -SO2Raa, -C(=NRcc)Raa, -C(=NRcc)ORaa, -C(=NRcc)N(Rcc)2, -SO2N(Rcc)2, -SO2Rcc, -SO2ORcc, -SORaa, -C(=S)N(Rcc)2, -C(=O)SRcc, -C(=S)SRcc, C1-10 алкил (например, аралкил, гетероаралкил), С2-10 алкенил, С2-10 алкинил, C3-10 карбоциклил, 3-14-членный гетероциклил, C6-14 арил и 5-14-членные гетероарильные группы, при этом каждый алкил, алкенил, алкинил, карбоциклил, гетероциклил, аралкил, арил и гетероарил независимо замещен группами 0, 1, 2, 3, 4 или 5 Rdd, и Raa, Rbb, Rcc и Rdd как определены в данном документе. Азотзащитные группы хорошо известны в данной области техники и включают группы, подробно описанные в Protecting Groups in Organic Synthesis, T.W. Greene and P.G.M. Wuts, 3rd edition, John Wiley & Sons, 1999, включенном в данное описание посредством ссылки.
[0050] Например, азотзащитные группы, такие как амидные группы (например, -С (=O)Raa) включают, но не ограничиваются ими, формамид, ацетамид, хлорацетамид, трихлорацетамид, трифторацетамид, фенилацетамид, 3-фенилпропанамид, пиколинамид, 3-пиридилкарбоксамид, N-бензоилфенилаланильное производное, бензамид, п-фенилбензамид, о-нитрофенилацетамид, о-нитрофеноксиацетамид, ацетоацетамид, (N'-дитиобензилоксиациламино)ацетамид, 3-(п-гидроксифенил)пропанамид, 3-(о-нитрофенил)пропанамид, 2-метил-2-(о-нитрофенокси)пропанамид, 2-метил-2-(о-фенилазофенокси)пропанамид, 4-хлорбутанамид, 3-метил-3-нитробутанамид, о-нитроциннамид, производное N-ацетилметионина, о-нитробензамид и о-(бензоилоксиметил) бензамид.
[0051] Азотзащитные группы, такие как карбаматные группы (например, -C(=OR)aa) включают, но не ограничиваются ими, метилкарбамат, этилкарбамат, 9-флуоренилметилкарбамат (Fmoc), 9-(2-сульфо)флуоренилметилкарбамат, 9-(2,7-дибром)флуоренилметилкарбамат, 2,7-ди-трет-бутил-[9-(10,10-диоксо-10,10,10,10-тетрагидротиоксантил)]метилкарбамат (DBD-Tmoc), 4-метоксифенацилкарбамат (Phenoc), 2,2,2-трихлорэтилкарбамат (Troc), 2-триметилсилилэтилкарбамат (Теос), 2-фенилэтилкарбамат (hZ), 1-(1-адамантил)-1-метилэтилкарбамат (Adpoc), 1,1-диметил-2-галоэтилкарбамат, 1,1-диметил-2,2-дибромэтилкарбамат (DB-t-BOC), 1,1-диметил-2,2,2-трихлорэтилкарбамат (ТСВОС), 1-метил-1-(4-бифенилил)этилкарбамат (Врос), 1-(3,5-ди-трет-бутилфенил)-1-метилэтилкарбамат (t-Bumeoc), 2-(2'- и 4'-пиридил)этилкарбамат (Руос), 2-(N,N-дициклогексилкарбоксамидо)этилкарбамат, трет-бутилкарбамад (ВОС или Boc), 1-адамантилкарбамат (Adoc), винилкарбамат (Voc), аллилкарбамат (Alloc), 1-изопропилаллилкарбамат (ИПСос), циннамилкарбамат (Coc), 4-нитроциннамилкарбамат (Noc), 8-хинолилкарбамат, N-гидроксипиперидинилкарбамат, алкилдитиокарбамат, бензилкарбамат (Cbz), п-метоксибензилкарбамат (Moz), п-нитробензилкарбамат, п-бромбензилкарбамат, п-хлорбензилкарбамат, 2,4-дихлорбензилкарбамат, 4-метилсульфинилбензилкарбамат (Msz), 9-антрилметилкарбамат, дифенилметилкарбамат, 2-метилтиоэтилкарбамат, 2-метилсульфонилэтилкарбамат, 2-(п-толуолсульфонил)этилкарбамат, [2-(1,3-дитианил)]метилкарбамат (Dmoc), 4-метилтиофенилкарбамат (Mtpc), 2,4-диметилтиофенилкарбамат (Bmpc), 2-фосфониоэтилкарбамат (Реос), 2-трифенилфосфониоизопропилкарбамат (Ррос), 1,1-диметил-2-цианоэтилкарбамат, м-хлор-п-ацилоксибензилкарбамат, п-(дигидроксиборил)бензилкарбамат, 5-бензизоксазолилметилкарбамат, 2-(трифторметил)-6-хромонилметилкарбамат (Tcroc), м-нитрофенилкарбамат, 3,5-диметоксибензилкарбамат, о-нитробензилкарбамат, 3,4-диметокси-6-нитробензилкарбамат, фенил(о-нитрофенил)метилкарбамат, трет-амилкарбамат, S-бензилтиокарбамат, п- цианобензилкарбамат, циклобутилкарбамат, циклогексилкарбамат, циклопентилкарбамат, циклопропилметилкарбамат, п-децилоксибензилкарбамат, 2,2-диметоксиацилвинилкарбамат, о-(N,N-диметилкарбоксамидо)бензилкарбамат, 1,1-диметил-3-(N,N-диметилкарбоксиамидо)пропилкарбамат, 1,1-диметилпропинилкарбамат, ди(2-пиридил)метилкарбамат, 2-фуранилметилкарбамат, 2-йодоэтилкарбамат,изоборнилкарбамат, изобутилкарбамат, изоникотинилкарбамат, п-(п-метоксифенилазо)бензилкарбамат, 1-метилциклобутилкарбамат, 1-метилциклогексилкарбамат, 1-метил-1-циклопропилметилкарбамат, 1-метил-1-(3,5-диметоксифенил)этилкарбамат, 1-метил-1-(п-фенилазофенил)этилкарбамат, 1-метил-1-фенилэтилкарбамат, 1-метил-1-(4-пиридил)этилкарбамат, фенилкарбамат, п-(фенилазо)бензилкарбамат, 2,4,6-три-трет-бутилфенилкарбамат, 4-(триметиламмоний)бензилкарбамат и 2,4,6-триметилбензилкарбамат.
[0052] Азотзащитные группы, такие как сульфонамидные группы (например, -S(=O)2Raa) включают, но не ограничиваются ими, п-толуолсульфонамид (Ts), бензолсульфонамид, 2,3,6,-триметил-4-метоксибензолсульфонамид (Mtr), 2,4,6-триметоксибензолсульфонамид (Mtb), 2,6-диметил-4-метоксибензолсульфонамид (Pme), 2,3,5,6-тетраметил-4-метоксибензолсульфонамид (Mte), 4-метоксибензолсульфонамид (Mbs), 2,4,6-триметилбензолсульфонамид (Mts), 2,6-диметокси-4-метилбензолсульфонамид (iMds), 2,2,5,7,8-пентаметилхроман-6-сульфонамид (Pmc), метансульфонамид (Ms), β-триметилсилилэтансульфонамид (SES), 9-антраценсульфонамид, 4-(4',8'-диметоксинафтилметил)бензолсульфонамид (DNMBS), бензилсульфонамид, трифторметилсульфонамид и фенацилсульфонамид.
[0053] Другие азотзащитные группы включают, но не ограничиваются ими, (10)-ацилпроизводное фенотиазинила, производное N'-п-толуолсульфониламиноацила, производное N'-фениламинотиоацила, производное N-бензоилфенилаланила, производное N-ацетилметионина, 4,5-дифенил-3-оксазолин-2-он, N-фталимид, N-дитиасукцинимид (Dts), N-2,3-дифенилмалеимид, N-2,5-диметилпиррол, N-1,1,4,4-тетраметилдисилилазациклопентановый аддукт (STABASE), 5-замещенный 1,3-диметил-1,3,5-триазациклогексан-2-он, 5-замещенный 1,3-дибензил-1,3,5-триазациклогексан-2-он, 1-замещенный 3,5-динитро-4-пиридон, N-метиламин, N-аллиламин, N-[2-(триметилсилил)этокси]метиламин (SEM), N-3-ацетоксипропиламин, N-(1-изопропил-4-нитро-2-оксо-3-пироолин-3-ил)амин, четвертичные соли аммония, N-бензиламин, N-ди(4-метоксифенил)метиламин, N-5-дибензосубериламин, N-трифенилметиламин (Tr), N-[(4-метоксифенил)дифенилметил]амин (MMTr), N-9-фенилфлуорениламин (PhF), N-2,7-дихлор-9-флуоренилметиленамин, N-ферроценилметиламино (Fcm), N-2-пиколиламино N'-оксид, N-1,1-диметилтиометиленамин, N-бензилиденамин, N-п-метоксибензилиденамин, N-дифенилметиленамин, N-[(2-пиридил)мезитил]метиленамин, N-(N',N'-диметиламинометилен)амин, N,N'-изопропилиденамин, N-p-нитробензилиденамин, N-салицилиденамин, N-5-хлорсалицилиденамин, N-(5-хлор-2-гидроксифенил)фенилметиленамин, N-циклогексилиденамин, N-(5,5-диметил-3-оксо-1- циклогексенил)амин, производное N-борана, производное N-дифенилборной кислоты, N-[фенил(пентаацилхром- или вольфрам)ацил]амин, хелат N-меди, хелат N-цинка, N-нитроамин, N-нитрозамин, амин N-оксид, дифенилфосфинамид (Dpp), диметилтиофосфинамид (Mpt), дифенилтиофосфинамид (Ppt), диалкилфосфорамидаты, дибензилфосфорамидат, дифенилфосфорамидат, бензолсульфенамид, о-нитробензолсульфенамид (Nps), 2,4-динитробензолсульфенамид, пентахлорбензолсульфенамид, 2-нитро-4-метоксибензолсульфенамид, трифенилметилсульфенамид и 3-нитропириденсульфенамид (Npys).
Примеры заместителей атомов кислорода включают, но не ограничиваются ими, -Raa, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, - C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raa)3, -P(Rcc)2, -P(Rcc)3+X-, -P(ORcc)2, -P(ORcc)3+X-, -P(=O)(Raa)2, -P(=O)(ORcc)2 и -P(=O)(N(Rbb)2)2, где X-, Raa, Rbb и Rcc как определены в данном документе. В некоторых вариантах реализации заместитель атома кислорода, присутствующий на атоме кислорода, представляет собой кислородзащитную группу (также называемую группой защиты гидроксильной группы). Кислородзащитные группы хорошо известны в данной области техники и включают группы, подробно описанные в Protecting Groups in Organic Synthesis, T.W. Greene and P.G.M. Wuts, 3rd edition, John Wiley & Sons, 1999, включенном в данное описание посредством ссылки. Примеры кислородзащитных групп включают, но не ограничиваются ими, метил, трет-бутилоксикарбонил (ВОС или Boc), метоксиметил (MOM), метилтиометил (МТМ), трет-бутилтиометил, (фенилдиметилзсилил)метоксиметил (SMOM), бензилоксиметил (ВОМ), п-метоксибензилоксиметил (РМВМ), (4-метоксифенокси)метил (п-АОМ), гваяколметил (GUM), трет-бутоксиметил, 4-пентенилоксиметил (РОМ), силоксиметил, 2-метоксиэтоксиметил (MEM), 2,2,2-трихлорэтоксиметил, бис(2-хлорэтокси)метил, 2-(триметилсилил)этоксиметил (SEMOR), тетрагидропиранил (ТНР), 3-бромтетрагидропиранил, тетрагидротиопиранил, 1-метоксициклогексил, 4-метокситетрагидропиранил (МТНР), 4-метокситетрагидротиопиранил, 4-метокситетрагидротиопиранил S,S-диоксид, 1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-ил (СТМР), 1,4-диоксан-2-ил, тетрагидрофуранил, тетрагидротиофуранил, 2,3,3а,4,5,6,7,7а-октагидро-7,8,8-триметил-4,7-метанобензофуран2-ил, 1-этоксиэтил, 1-{2-хлорэтокси)этил, 1-метил-1-метоксиэтил, 1-метил-1-бензилоксиэтил, 1-метил-1-бензилокси-2-фторэтил, 2,2,2-трихлорэтил, 2-триметилсилилэтил, 2-(фенилселенил)этил, трет-бутил, аллил, п-хлорфенил, п-метоксифенил, 2,4-динитрофенил, бензил (Bn), п-метоксибензил, 3,4-диметоксибензил, о-нитробензил, п-нитробензил, п-галобензил, 2,6-дихлорбензил, п-цианбензил, п-фенилбензил, 2-пиколил, 4-пиколил, 3-метил-2-пиколил N-оксидо, дифенилметил, п,п-динитробензгидрил, 5-дибензосуберил, трифенилметил, α-нафтилдифенилметил, п-метоксифенилдифенилметил, ди(п-метоксифенил)фенилметил, три(п-метоксифенил)метил, 4-(4'-бромфенацилоксифенил)дифенилметил, 4,4',4''-трис(4,5-дихлорфталимидофенил)метил, 4,4',4''-трис(левулиноилоксифенил)метил, 4,4',4''-трис(бензоилоксифенил)метил, 3-{имидазол-1-ил)бис(4',4''-диметоксифенил)метил, 1,1-бис(4-метоксифенил)-1-пиренилметил, 9-антрил, 9-(9-фенил)ксантенил, 9-(9-фенил-10-оксо)антрил, 1,3-бензодисульфуран-2-ил, бензизотиазолил 8,8-диоксидо, триметилсилил (TMS), триэтилсилил (TES), триизопропилсилил (TIPS), диметилизопропилсилил (IPDMS), диэтилизопропилсилил (DEIPS), диметилгексилсилил, трет-бутилдиметилсилил (TBDMS), трет-бутилдифенилсилил (TBDPS), трибензилсилил, три-п-ксилилсилил, трифенилсилил, дифенилметилсилил (DPMS), трет-бутилметоксифенилсилил (TBMPS), формат, бензоилформат, ацетат, хлорацетат, дихлорацетат, трихлорацетат, трифторацетат, метоксиацетат, трифенилметоксиацетат, феноксиацетат, п-хлорфеноксиацетат, 3-фенилпропионат, 4-оксопентаноат (левулинат), 4,4-(этилендитио)пентаноат (левулиноилдитиоацетал), пивалоат, адамантоат, кротонат, 4-метоксикротонат, бензоат, п-фенилбензоат, 2,4,6-триметилбензоат (мезитоат), алкилметилкарбонат, 9-флуоренилметилкарбонат (Fmoc), алкилэтилкарбонат, алкил 2,2,2-трихлорэтилкарбонат (Troc), 2-(триметилсилил)этилкарбонат (TMSEC), 2-(фенилсульфонил)этилкарбонат (Psec), 2-(трифенилфосфонио)этилкарбонат (Реос), алкилизобктилкарбонат, алкилвинилкарбонат, алкилаллилкарбонат, алкил п-нитрофенилкарбонат, алкилбензилкарбонат, алкил п-метоксибензилкарбонат, алкил 3,4-диметоксибензилкарбонат, алкил о-нитробензилкарбонат, алкил п-нитробензилкарбонат, алкил S-бензилтиокарбонат, 4-этокси-1-нафтилкарбонат, метилдитиокарбонат, 2-йодобензоат, 4-азидобутират, 4-нитро-4-метилпентаноат, о-(дибромметилметил)бензоат, 2-формилбензолсульфонат, 2-(метилтиометокси)этил, 4-(метилтиометокси)бутират, 2-(метилтиометоксиметил)бензоат, 2,6-дихлор-4-метилфеноксиацетат, 2,6-дихлор-4-(1,1,3,3-тетрпметилбутил)феноксиацетат, 2,4-бис(1,1-диметилпропил)феноксиацетат, хлордифенилацетат, изобутират, моносукциноат, (Е)-2-метил-2-бутеноат, о-(метоксиацил)бензоат, α-нафтоат, нитрат, алкил N,N,N',N'-тетраметилфосфородиамидат, алкил N-фенилкарбамат, борат, диметилфосфинотиоил, алкил 2,4-динитрофенилсульфенат, сульфат, метансульфонат (мезилат), бензилсульфонат и тозилат (Ts).
[0054] Примеры заместителей атомов серы включают, но не ограничиваются ими, -Raa, -C(=O)SRaa, -C(=O)Raa, -CO2Raa, -C(=O)N(Rbb)2, -C(=NRbb)Raa, -C(=NRbb)ORaa, -C(=NRbb)N(Rbb)2, -S(=O)Raa, -SO2Raa, -Si(Raa)3, -P(Rcc)2, -P(Rcc)3+X-, -P(ORcc)2, -P(ORcc)3+X-, -P(=O)(Raa)2, -P(=O)(ORcc)2, b -P(=O)(N(Rbb)2)2, где Raa, Rbb и Rcc как определены в данном документе.
[0055] «Углеводородная цепь» относится к замещенной или незамещенной двухвалентной алкильной, алкенильной или алкинильной группе. Углеводородная цепь включает (1) одну или несколько цепей атомов углерода непосредственно между двумя радикалами углеводородной цепи; (2) необязательно один или несколько атомов водорода в цепи (цепях) атомов углерода; и (3) необязательно один или более заместителей («нецепочечные заместители», которые не являются водородом) в цепи (цепях) атомов углерода. Цепь атомов углерода состоит из последовательно связанных атомов углерода («атомы цепи» или «углеродные звенья») и не включает атомы водорода или гетероатомы. Однако нецепочечный заместитель углеводородной цепи может содержать любые атомы, включая атомы водорода, атомы углерода и гетероатомы. Например, углеводородная цепь -САН(CBH2CCH3) - содержит один цепочечный атом СА, один атом водорода на СА и нецепочечный заместитель -(CBH2CCH3). Термин «Сх углеводородная цепь», где х представляет собой целое положительное число, относится к углеводородной цепи, которая содержит х атомов цепи между двумя радикалами углеводородной цепи. Если существует более одного возможного значения х, для определения углеводородной цепи используется наименьшее возможное значение х. Например, -CH(C2H5)- представляет собой углеводородную цепь C1, и  представляет собой углеводородную цепь С3. При использовании диапазона значений значение диапазона соответствует описанному в данном документе. Например, C3-10 углеводородная цепь относится к углеводородной цепи, в которой число атомов цепи в самой короткой цепи атомов углерода непосредственно между двумя радикалами углеводородной цепи составляет 3, 4, 5, 6, 7, 8, 9 или 10. Углеводородная цепь может быть насыщенной (например, -(СН2)4-). Углеводородная цепь также может быть ненасыщенной и содержать одну или более связей С=С и/или С≡С в любом участке углеводородной цепи. Например, -СН=СН-(СН2)2-, -СН2-С≡С-СН2- и -С≡С-СН=СН- представляют собой все примеры незамещенной и ненасыщенной углеводородной цепи. В некоторых вариантах реализации углеводородная цепь является незамещенной (например, -С≡С- или -(СН2)4-). В некоторых вариантах реализации углеводородная цепь является замещенной (например, -СН(C2H5)- и -CF2-). Любые два заместителя в углеводородной цепи могут быть соединены с образованием необязательно замещенного карбоциклильного, необязательно замещенного гетероциклильного, необязательно замещенного арильного или необязательно замещенного гетероарильного кольца. Например,
представляет собой углеводородную цепь С3. При использовании диапазона значений значение диапазона соответствует описанному в данном документе. Например, C3-10 углеводородная цепь относится к углеводородной цепи, в которой число атомов цепи в самой короткой цепи атомов углерода непосредственно между двумя радикалами углеводородной цепи составляет 3, 4, 5, 6, 7, 8, 9 или 10. Углеводородная цепь может быть насыщенной (например, -(СН2)4-). Углеводородная цепь также может быть ненасыщенной и содержать одну или более связей С=С и/или С≡С в любом участке углеводородной цепи. Например, -СН=СН-(СН2)2-, -СН2-С≡С-СН2- и -С≡С-СН=СН- представляют собой все примеры незамещенной и ненасыщенной углеводородной цепи. В некоторых вариантах реализации углеводородная цепь является незамещенной (например, -С≡С- или -(СН2)4-). В некоторых вариантах реализации углеводородная цепь является замещенной (например, -СН(C2H5)- и -CF2-). Любые два заместителя в углеводородной цепи могут быть соединены с образованием необязательно замещенного карбоциклильного, необязательно замещенного гетероциклильного, необязательно замещенного арильного или необязательно замещенного гетероарильного кольца. Например,  и
и  представляют собой все примеры углеводородной цепи. Напротив, в некоторых вариантах реализации
представляют собой все примеры углеводородной цепи. Напротив, в некоторых вариантах реализации  не входят в объем углеводородных цепей, описанных в данном документе. При замене цепочечного атома Сх углеводородной цепи гетероатомом полученную группу называют Сх углеводородной цепью, в которой атом цепи замещен гетероатомом, в отличие от Cx-1 углеводородной цепи. Например,
не входят в объем углеводородных цепей, описанных в данном документе. При замене цепочечного атома Сх углеводородной цепи гетероатомом полученную группу называют Сх углеводородной цепью, в которой атом цепи замещен гетероатомом, в отличие от Cx-1 углеводородной цепи. Например, 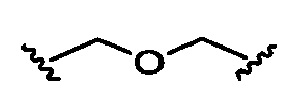 представляет собой C3 углеводородную цепь, в которой один атом цепи замещен атомом кислорода.
представляет собой C3 углеводородную цепь, в которой один атом цепи замещен атомом кислорода.
[0056] Термин «уходящая группа» имеет свое обычное значение в области органического синтеза и относится к атому или группе, способным к замещению нуклеофилом. См., например, Smith, March Advanced Organic Chemistry 6th ed.(501-502). Примеры соответствующих уходящих групп включают, но не ограничиваются ими, галоген (такой как F, Cl, Br или I (йод)), алкоксикарбонилокси, арилоксикарбонилокси, алкансульфонилокси, аренсульфонилокси, алкилкарбонилокси (например, ацетокси), арилкарбонилокси, арилокси, метокси, N,O-диметилгидроксиламино, пиксил и галоформиаты. В некоторых случаях уходящая группа представляет собой активированную замещенную гидроксильную группу (например, -OC(=O)SRaa, -OC(=O)Raa, -OCO2Raa, -OC(=O)N(Rbb)2, -OC(=NRbb)Raa, -OC(=NRbb)ORaa, -OC(=NRbb)N(Rbb)2, -OS(=O)Raa, -OSO2Raa, -OP(Rcc)2, -OP(Rcc)3, -OP(=O)2Raa, -OP(=O)(Raa)2, -OP(=O)(ORcc)2, -OP(=O)2N(Rbb)2 и -OP(=O)(NRbb)2, где Raa, Rbb и Rcc как определены в данном документе). В некоторых случаях уходящая группа представляет собой сложный эфир сульфоновой кислоты, такой как толуолсульфонат (тозилат, -OTs), метансульфонат (мезилат, -OMs), п-бромбензолсульфонилокси (брозилат, -OBs), -OS(=O)2(CF2)3CF3 (нонафлат, -ONf) или трифторметансульфонат (трифлат, -OTf). В некоторых случаях уходящая группа представляет собой брозилат, такой как п-бромбензолсульфонилокси. В некоторых случаях уходящая группа представляет собой нозилат, такой как 2-нитробензолсульфонилокси. В некоторых вариантах реализации уходящая группа представляет собой сульфонатсодержащую группу. В некоторых вариантах реализации уходящая группа представляет собой тозилатную группу. Уходящая группа также может представлять собой фосфиноксид (например, полученный во время реакции Мицунобу) или внутреннюю уходящую группу, такую как эпоксид или циклический сульфат. Другими неограничивающими примерами уходящих групп являются вода, аммиак, спирты, эфирные фрагменты, тиоэфирные фрагменты, галогениды цинка, частицы магния, соли диазония и частицы меди.
[0057] Термин «фармацевтически приемлемая соль» относится к таким солям, которые с медицинской точки зрения подходят для применения в контакте с тканями человека и низших животных без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного, и имеют разумное соотношение польза/риск. Фармацевтически приемлемые соли хорошо известны в данной области техники. Например, фармацевтически приемлемые соли подробно описаны Berge и др. в J. Pharmaceutical Sciences, 1977, 66, 1-19, включенном в данный документ посредством ссылки. Фармацевтически приемлемые соли соединений, описанных в данном документе, включают те, которые получены из соответствующих неорганических и органических кислот и оснований. Примерами фармацевтически приемлемых нетоксичных солей, полученных добавлением кислот, являются соли аминогруппы, образованные с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, фосфорная кислота, серная кислота и перхлорная кислота, или с органическими кислотами, такими как уксусная кислота, щавелевая кислота, малеиновая кислота, винная кислота, лимонная кислота, янтарная кислота или малоновая кислота, или путем использования других способов, известных в данной области техники, таких как ионный обмен. Другие фармацевтически приемлемые соли включают адипинат, альгинат, аскорбат, аспартат, бензосульфонат, бензоат, бисульфат, борат, бутират, камфорат, камфорсульфонат, цитрат, циклопентанпропионат, биглюконат, додецилсульфат, этансульфонат, формиат, фумарат, глюкогептонат, глицерофосфат, глюконат, гемисульфат, гептаноат, гексаноат, гидройодид, 2-гидрокси-этансульфонат, лактобионат, лактат, лаурат, лаурилсульфат, малат, малеат, малонат, метансульфонат, 2-нафтилсульфонат, никотинат, нитрат, олеат, оксалат, пальмитат, памоат, пектинат, персульфат, 3-фенилпропионат, фосфат, пикрат, пивалат, пропионат, стеарат, сукцинат, сульфатов, тартрат, тиоцианат, р-толуолсульфонат, ундеканоат, валератные соли и тому подобное. Соли, полученные из соответствующих оснований, включают соли щелочного металла, щелочноземельного металла, аммония и N+(C1-4 алкил)4. Примеры солей щелочного или щелочноземельного металла включают соли натрия, лития, калия, кальция, магния и тому подобное. Дополнительно фармацевтически приемлемые соли включают, в соответствующих случаях, нетоксичные катионы аммония, четвертичного аммония и амина, образованные с помощью противоионов, таких как галогенид, гидроксид, карбоксилат, сульфат, фосфат, нитрат, низший алкилсульфонат и арилсульфонат.
[0058] Термин «сольват» относится к формам соединения, которые связаны с растворителем, обычно путем реакции сольволиза. Указанное физическое соединение может включать водородную связь. Обычные растворители включают воду, метанол, этанол, уксусную кислоту, ДМСО, ТГФ, диэтиловый эфир и тому подобное. Соединения, описанные в данном документе, могут быть получены, например, в кристаллической форме и могут быть сольватированы. Подходящие сольваты включают фармацевтически приемлемые сольваты и дополнительно включают как стехиометрические сольваты, так и нестехиометрические сольваты. В некоторых случаях сольват может быть выделен, например, когда одна или более молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. «Сольват» охватывает как сольваты в жидкой фазе, так и выделяемые сольваты. Типичные сольваты включают гидраты, этанолаты и метанолаты.
[0059] Термин «гидрат» относится к соединению, связанному с водой. Как правило, количество молекул воды, содержащихся в гидрате соединения, находится в определенном соотношении к количеству молекул соединения в гидрате. Поэтому гидрат соединения может быть представлен, например, общей формулой R⋅x Н2О, где R представляет собой соединение, а х - число больше 0. Данное соединение способно образовать более одного типа гидрата, включая, например, моногидраты (х равно 1), низшие гидраты (х - число больше 0 и меньше 1, например, гемигидраты (R⋅0,5H2O)) и полигидраты (х - число больше 1, например, дигидраты (R⋅2H2O) и гексагидраты (R⋅6H2O)).
[0060] Термин «таутомеры» или «таутомерный» относится к двум или более взаимопревращаемым соединениям, полученным в результате по меньшей мере одной формальной миграции атома водорода и по меньшей мере одного изменения валентности (например, изменения одинарной связи на двойную связь, тройной связи на одинарную связь или наоборот). Точное соотношение таутомеров зависит от нескольких факторов, включающих температуру, растворитель и рН. Таутомеризация (то есть реакция, обеспечивающая таутомерную пару) может быть катализирована кислотой или основанием. Примеры таутомеризации включают таутомеризации кето-енол, амид-имид, лактам-лактим, енамин-имин и енамин-(другой) енамин.
[0061] Также следует понимать, что соединения, которые имеют одну и ту же молекулярную формулу, но различаются характером или последовательностью присоединения атомов или расположением атомов в пространстве, называются «изомерами». Изомеры, которые различаются по расположению атомов в пространстве, называются «стереоизомерами».
[0062] Стереоизомеры, которые не являются зеркальным отражением друг друга, называют «диастереомерами», а те, которые представляют не совмещаемые в пространстве зеркальные изображения друг друга, называют «энантиомерами». Если соединение имеет асимметричный центр, например, оно связано с четырьмя различными группами, возможно существование пары энантиомеров. Энантиомер может характеризоваться абсолютной конфигурацией ассимметричного центра и описывается правилами R- и S-последовательности Кана и Прелога или направлением, в котором молекула вращает плоскость поляризованного света, обозначенным как правое вращение или левое вращение (то есть как (+) или (-)-изомеры, соответственно). Хиральное соединение может находиться в виде отдельного энантиомера или в виде смеси энантиомеров. Смесь, содержащая равные пропорции энантиомеров, называется «рацемической смесью».
[0063] Термин «полиморфы» относится к кристаллической форме соединения (или его соли, гидрату или сольвату) в определенной кристаллической структуре. Все полиморфы имеют одинаковый элементный состав. Различные кристаллические формы обычно имеют разные рентгенограммы, инфракрасные спектры, точки плавления, плотность, твердость, кристаллическую форму, оптические и электрические свойства, стабильность и растворимость. Растворитель для перекристаллизации, скорость кристаллизации, температура хранения и другие факторы могут вызывать доминирование одной кристаллической формы. Различные полиморфы соединения могут быть получены путем кристаллизации в различных условиях.
[0064] Термин «пролекарства» относится к соединениям, которые имеют расщепляемые группы и становятся путем сольволиза или в физиологических условиях соединениями, описанными в данном документе, фармацевтически активными in vivo. Примеры включают, но не ограничиваются ими, производные сложных эфиров холина и тому подобное, сложные эфиры N-алкилморфолина и тому подобное. Другие производные соединений, описанных в данном документе, обладают активностью как в форме их кислоты, так и производного кислоты, однако в чувствительной к кислоте форме часто обладают преимуществами растворимости, совместимости тканей или отсроченного высвобождения в организме млекопитающих (см. Bundgard, Н., Design of Prodrugs, рр. 7-9, 21-24, Elsevier, Amsterdam 1985). Пролекарства включают кислотные производные, хорошо известные специалистам в данной области техники, такие как, например, сложные эфиры, полученные реакцией исходной кислоты с соответствующим спиртом, или амиды, полученные реакцией исходного кислотного соединения с замещенным или незамещенным амином или ангидридами кислоты или смешанными ангидридами. Простые алифатические или ароматические сложные эфиры, амиды и ангидриды, полученные из кислотных групп, являющихся боковой цепью описанных в данном документе соединений, представляют собой конкретные пролекарства. В некоторых случаях требуется получение пролекарств двойного эфирного типа, таких как (ацилокси)алкиловые эфиры или ((алкоксикарбонил)окси) алкиловые эфиры. C1-C8 алкил, С2-C8 алкенил, C2-C8 алкинил, арил, С7-С12 замещенный арил и С7-С12 арилалкиловые эфиры соединений, описанных в данном документе, могут быть предпочтительными.
[0065] Термин «ингибирование», «ингибирующий», «ингибировать» или «ингибитор» относится к способности соединения сокращать, замедлять, останавливать или предотвращать активность конкретного биологического процесса в клетке в сравнении с носителем.
[0066] Когда соединение, фармацевтическая композиция, способ, применение или набор упоминается как «выборочно», «конкретно» или «конкурентно» связывающее первый белок, соединение связывает первый белок с более высокой аффинностью связывания (например, не менее примерно в 2 раза, не менее примерно в 5 раз, не менее примерно в 10 раз, не менее примерно в 30 раз, не менее примерно в 100 раз, не менее примерно в 1000 раз или не менее примерно в 10000 раз выше), чем связывание второго белка или другого, отличающегося от первого белка. Когда соединение упоминается как «выборочно», «конкретно» или «конкурентно» модулирующее (например, увеличивающее или Ингибирующее) активность белка, соединение модулирует активность белка в большей степени (например, не менее примерно в 2 раза, не менее примерно в 5 раз, не менее примерно в 10 раз, не менее примерно в 30 раз, не менее примерно в 100 раз, не менее примерно в 1000 раз, или не менее примерно в 10000 раз), чем активность по меньшей мере одного белка, который отличается от первого белка.
[0067] Термин «аберрантная активность» относится к активности, отклоняющейся от нормальной активности. Термин «повышенная активность» относится к активности выше нормальной.
[0068] Термины «состав» и «композиция» используются как взаимозаменяемые.
[0069] Термин «субъект», которому назначено лекарство, относится к человеку (то есть мужчине или женщине любой возрастной группы, например, педиатрическому пациенту (например, младенцу, ребенку или подростку) или взрослому субъекту (например, молодежи, лицам среднего и старшего возраста)) или животным, не относящимся к человеку. Термин «пациент» относится к человеку, нуждающемуся в лечении заболевания.
[0070] Термины «вводить», «введение» или «назначение» при использовании в данном документе относятся к имплантации, абсорбции, проглатыванию, инъекции, вдыханию или введению иным образом субъекту описанного в данном документе соединения или его композиции.
[0071] Термины «лечение» и «лечить» относятся к реверсированию, облегчению, задержке начала или Ингибированию развития описанного в данном документе заболевания. В некоторых вариантах реализации лечение можно проводить после развития или выявления одного или более признаков или симптомов заболевания. В других вариантах реализации лечение можно проводить в отсутствие признаков или симптомов заболевания. Например, лечение может быть назначено восприимчивому субъекту до появления симптомов (например, с учетом истории симптомов и/или воздействия патогена) для задержки или предотвращения возникновения заболевания. Лечение также может быть продолжено после прекращения симптомов, например, для задержки или предотвращения рецидива.
[0072] Термины «состояние», «заболевание» и «нарушение» использованы как взаимозаменяемые.
[0073] «Эффективное количество» описанного в данном документе соединения относится к количеству, достаточному для получения желаемого биологического ответа, то есть лечения заболевания. Как понятно специалистам в данной области техники, эффективное количество описанного в данном документе соединения может варьироваться в зависимости от таких факторов, как желаемая биологическая конечная точка, фармакокинетика соединения, заболевание, подлежащее лечению, способ введения, а также возраст и состояние здоровья субъекта. В некоторых вариантах реализации эффективное количество представляет собой терапевтически эффективное количество. В некоторых вариантах реализации эффективное количество представляет собой количество для профилактического лечения. В некоторых вариантах реализации эффективное количество представляет собой однократную дозу соединения, описанного в данном документе. В некоторых вариантах реализации эффективное количество представляет собой несколько доз соединения, описанного в данном документе.
[0074] «Терапевтически эффективное количество» описанного в данном документе соединения представляет собой количество, достаточное для обеспечения терапевтического эффекта при лечении заболевания или для отсрочки или минимизации одного или более симптомов, связанных с заболеванием. Терапевтически эффективное количество соединения означает такое количество терапевтического агента, отдельно или в комбинации с другими лекарственными средствами, которое обеспечивает терапевтический эффект при лечении заболевания. Термин «терапевтически эффективное количество» может включать такое количество, которое улучшает лечение в целом, снижает или исключает симптомы, признаки или причины заболевания и/или усиливает терапевтическую эффективность другого терапевтического агента.
[0075] «Профилактически эффективное количество» описанного в данном документе соединения представляет собой количество, достаточное для профилактики заболевания, одного или более симптомов, связанных с заболеванием, или рецидива заболевания. Профилактически эффективное количество соединения означает такое количество терапевтического агента, отдельно или в комбинации с другими агентами, которое обеспечивает профилактический эффект при профилактике заболевания. Термин «профилактически эффективное количество» может включать такое количество, которое улучшает общую профилактику или усиливает профилактическую эффективность другого профилактического агента.
[0076] Термин «пролиферативное заболевание» относится к заболеванию, которое возникает из-за аномального роста или прорастания в результате увеличения числа клеток (Walker, Cambridge Dictionary of Biology; Cambridge University Press: Cambridge, UK, 1990). Пролиферативное заболевание может быть связано с: 1) патологической пролиферацией обычно покоящихся клеток; 2) патологической миграцией клеток из их нормальной локализации (например, метастазы неопластических клеток); 3) патологической экспрессией мутировавшего гена (например, р53, Ras и EGFR); или 4) патологическим ангиогенезом, как при пролиферативной ретинопатии и метастазировании опухолей. Примеры пролиферативных заболеваний включают онкологические заболевания (то есть «злокачественные новообразования»), доброкачественные новообразования, ангиогенез, воспалительные заболевания и аутоиммунные заболевания.
[0077] Термины «новообразование» и «опухоль» используются в данном документе взаимозаменяемо и относятся к аномальной массе ткани, в которой рост массы опережает и не соответствует росту нормальной ткани. Новообразование или опухоль могут быть «доброкачественными» или «злокачественными» в зависимости от следующих характеристик: степени клеточной дифференциации (включая морфологию и функциональность), скорости роста, локальной инвазии и метастазирования. «Доброкачественное новообразование», как правило, хорошо дифференцировано, характеризуется более медленным ростом, чем злокачественное новообразование, и остается локализованным в месте возникновения. Кроме того, доброкачественное новообразование не обладает способностью к инфильтрации, прорастанию или метастазированию в удаленные участки. Примеры доброкачественных новообразований включают, но не ограничиваются ими, липому, хондрому, аденомы, акрохордоны, старческие ангиомы, себорейные кератозы, лентиго и гиперплазию сальных желез. В некоторых случаях определенные «доброкачественные» опухоли могут впоследствии вызвать злокачественные новообразования, что может быть следствием дополнительных генетических изменений в субпопуляции неопластических клеток опухоли, и эти опухоли называются «предраковыми новообразованиями». Примером предракового новообразования является тератома. Напротив, «злокачественное новообразование» обычно слабо дифференцировано (анаплазия) и характеризуется быстрым ростом, сопровождающимся прогрессирующей инфильтрацией, инвазией и разрушением окружающей ткани. Кроме того, злокачественное новообразование обычно обладает способностью метастазировать в удаленные участки. Термин «метастаз», «метастатический» или «метастазирующий» относится к распространению или миграции раковых клеток из первичной или исходной опухоли в другой орган или ткань и обычно идентифицируется наличием «вторичной опухоли» или «вторичной клеточной массы» тканевого типа первичной или исходной опухоли, а не ткани органа или ткани, в которой расположена вторичная (метастатическая) опухоль. Например, рак молочной железы, который мигрировал в легкие, печень и кости, считается метастазирующим раком молочной железы и включает раковые клетки рака молочной железы, растущие в легких, печени и костной ткани.
[0078] Термин «рак» относится к классу заболеваний, характеризующихся развитием аномальных клеток, которые размножаются неуправляемо и обладают способностью к инфильтрации и разрушению нормальных тканей организма. См., например, Stedman's Medical Dictionary, 25th ed.; Hensyl ed.; Williams & Wilkins:Philadelphia, 1990. Примеры рака включают, но не ограничиваются ими, гемобластозы. Примеры рака включают, но не ограничиваются ими, рак мочевого пузыря; рак молочной железы (например, аденокарцинома молочной железы, папиллярная карцинома молочной железы, рак молочной железы, медуллярная карцинома молочной железы); рак шейки матки; рак уретры; рак влагалища и рак вульвы (например, болезнь Педжета вульвы).
Краткое описание чертежей
[0079] Неограничивающие варианты реализации настоящего изобретения описаны с помощью примеров со ссылкой на прилагаемые чертежи, которые являются схематическими и выполнены без соблюдения масштаба. На чертежах каждый идентичный или почти идентичный компонент, как правило, представлен одним номером. Для ясности не каждый компонент отмечен на каждой фигуре, и не каждый компонент каждого варианта реализации показан там, где иллюстрация не является необходимой для понимания изобретения специалистами в данной области техники.
[0080] На Фигуре 1 представлен график изменения объема опухоли в исследовании эффективности ксенотрансплантата xMCF-7 рака молочной железы человека на мышиной модели при лечении примером соединения 25 в сравнении с фулвестрантом, GDC-0810 и AZD9496.
[0081] На Фигуре 2 представлен график изменения объема опухоли в исследовании эффективности ксенотрансплантата xMCF-7 рака молочной железы человека на мышиной модели при лечении примерами соединений 12, 21 и 25 в сравнении с AZD9496.
[0082] На Фигуре 3 представлен график, демонстрирующий эффективность лечения комбинацией примера соединения 25 с Ингибитором CDK4/6 палбоциклибом при изменении объема опухоли в исследовании эффективности ксенотрансплантата xMCF-7 рака молочной железы человека на мышиной модели.
Подробное описание изобретения
[0083] Настоящее изобретение обеспечивает селективные Ингибиторы эстрогеновых рецепторов (СИЭР), например, соединения формулы (I), избирательно связывающие эстрогеновый рецептор и приводящие к деградации рецептора. Соединения, описанные в данном документе, полезны для снижения уровня эстрогенового рецептора (дикого типа или мутировавшего) и лечения заболевания, связанного со стероидным гормоном, таким как эстроген (например, рака молочной железы, такого как ЭР-положительный рак молочной железы). Примеры соединений СИЭР, раскрытые в данном документе, успешно индуцируют деградацию ЭР и ингибируют рост раковой клетки MCF-7, линии клеток ЭР-положительного рака молочной железы человека. Кроме того, в настоящем описании представлены фармацевтические композиции, наборы, способы применения соединений СИЭР для лечения любого из целевых заболеваний, описанных в данном документе.
Селективные ингибиторы эстрогеновых рецепторов
[0084] Один из аспектов настоящего изобретения относится к описанным в данном документе соединениям СИЭР, а также к их фармацевтически приемлемым солям, сольватам, гидратам, полиморфам, сокристаллам, таутомерам, стереоизомерам, изотопически меченным производным или пролекарствам. Указанные соединения полезны для лечения и/или профилактики пролиферативных заболеваний (таких как ЭР-положительный рак молочной железы) или заболеваний, связанных с ЭР субъекта.
[0085] В некоторых вариантах реализации соединение представляет собой соединение Формулы (I):
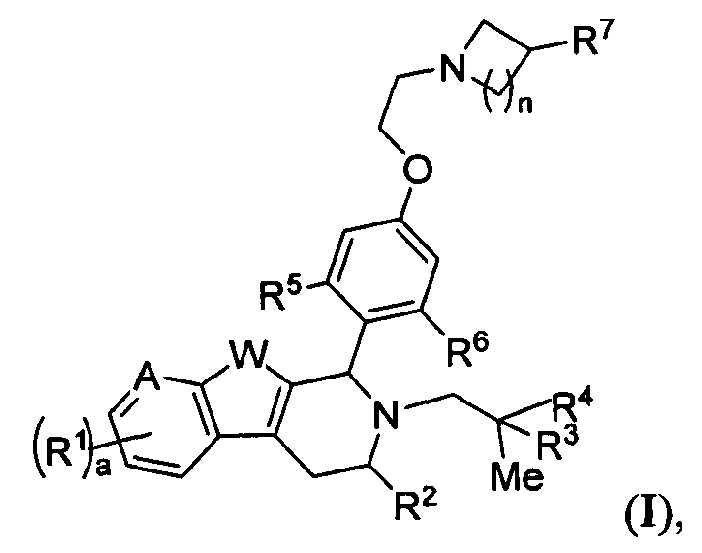 где R1-R7, A, W, а и n как описаны в данном документе, или представляет собой фармацевтически приемлемую соль, сольват, гидрат, полиморф, сокристалл, таутомер, стереоизомер, изотопически меченое производное или пролекарство.
где R1-R7, A, W, а и n как описаны в данном документе, или представляет собой фармацевтически приемлемую соль, сольват, гидрат, полиморф, сокристалл, таутомер, стереоизомер, изотопически меченое производное или пролекарство.
[0086] В Формуле (I) А и W находятся в трициклическом кольце. В некоторых вариантах реализации А может представлять собой -CRA= или -N=. В некоторых вариантах реализации А может представлять собой -CRA=, где RA как определено в данном документе. В некоторых вариантах реализации RA может представлять собой водород. В некоторых вариантах реализации RA может быть замещенным или незамещенным C1-6 алкилом (например, метилом, этилом или пропилом). В одном из примеров А может представлять собой -СН=. В другом примере А может представлять собой -СМе=. В других вариантах реализации А может представлять собой -NH=.
[0087] В некоторых вариантах реализации W может представлять собой -NH-. В некоторых вариантах реализации W может представлять собой -О-. В некоторых вариантах реализации W может представлять собой -S-.
[0088] Формула (I) включает один или более R1. В некоторых вариантах реализации а равно 1. В некоторых вариантах реализации а равно 2. В некоторых вариантах реализации а равно 3. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой водород. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации по меньшей мере один R1 может представлять собой фтор. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой хлор. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -CF3. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -ORA, где RA как определено в данном документе. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -ОМе. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -OEt. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -CN.
[0089] В Формуле (I) в некоторых вариантах реализации R2 может представлять собой водород. В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации R2 может представлять собой метил. В некоторых вариантах реализации R2 может представлять собой этил. В некоторых вариантах реализации R2 может представлять собой пропил. В некоторых вариантах реализации R2 может представлять собой -CF3. В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный карбоциклил (например, замещенный или незамещенный 3-7-членный моноциклический карбоциклил, содержащий ноль, одну или две двойные связи в системе карбоциклического кольца). В некоторых вариантах реализации R2 может представлять собой циклопропил. В некоторых вариантах реализации R2 может представлять собой циклобутил.
[0090] В Формуле (I) в некоторых вариантах реализации R3 и/или R4 могут представлять собой водород. В некоторых вариантах реализации R3 и/или R4 могут представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации R3 и/или R4 могут представлять собой фтор. В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации R3 и/или R4 могут представлять собой метил. В некоторых вариантах реализации R3 и/или R4 могут представлять собой этил. В некоторых вариантах реализации R3 и/или R4 могут представлять собой пропил. В некоторых вариантах реализации один из R3 и R4 может представлять собой фтор, а другой из R3 и R4 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил). В некоторых вариантах реализации один из R3 и R4 может представлять собой фтор, а другой из R3 и R4 может представлять собой метил. В некоторых вариантах реализации оба R3 и R4 могут представлять собой фтор. В некоторых вариантах реализации оба R3 и R4 могут представлять собой метил. В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный карбоциклил (например, замещенный или незамещенный 3-7-членный моноциклический карбоциклил, содержащий ноль, одну или две двойные связи в карбоциклической кольцевой системе). В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный гетероциклил (например, замещенное или незамещенное 5-10-членное моноциклическое или бициклическое гетероциклическое кольцо, при этом один или два атома в гетероциклическом кольце независимо представляют собой азот, кислород или серу). В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный арил (например, фенил или бензил). В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный 5-7-членный моноциклический гетероарил, при этом один, два, три или четыре атома в гетероарильной кольцевой системе независимо представляют собой азот, кислород или серу). В некоторых вариантах реализации R3 и/или R4 могут представлять собой -ORA где RA как определено в данном документе (например, -ОН, -O(замещенный или незамещенный C1-6 алкил) (например, -ОМе)). В некоторых вариантах реализации R3 и/или R4 могут представлять собой -N(RB)2, где RB как определено в данном документе (например, -NH2).
[0091] В Формуле (I)в некоторых вариантах реализации R5 и/или R6 могут представлять собой водород. В некоторых вариантах реализации R5 и/или R6 могут представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации R5 и/или R6 могут представлять собой хлор. В некоторых вариантах реализации R5 и/или R6 могут представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации оба R5 и R6 могут представлять собой галоген. В некоторых вариантах реализации оба R5 и R6 могут представлять собой фтор. В некоторых вариантах реализации оба R5 и R6 могут представлять собой хлор. В некоторых вариантах реализации один из R5 и R6 может представлять собой хлор, а другой может представлять собой фтор. В некоторых вариантах реализации один из R5 и R6 может представлять собой фтор, а другой может представлять собой замещенный или незамещенный C1-6 алкил. В некоторых вариантах реализации один из R5 и R6 может представлять собой хлор, а другой может представлять собой замещенный или незамещенный C1-6 алкил.
[0092] В Формуле (I)в некоторых вариантах реализации R7 может представлять собой водород. В некоторых вариантах реализации R7 может представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации R7 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации R7 может представлять собой соединение формулы -CH2Ra, где Ra представляет собой галоген. В некоторых вариантах реализации R7 может представлять собой -CH2F. В некоторых вариантах реализации R7 может представлять собой -ORA где RA как определено в данном документе (например, -ОН, -O(замещенный или незамещенный C1-6 алкил) (например, -ОМе)). В некоторых вариантах реализации R7 может представлять собой -N(RB)2, где RB как определено в данном документе (например, -NH2).
[0093] В Формуле (I) в некоторых вариантах реализации n может быть равно 1. В некоторых вариантах реализации n может быть равно 2. В некоторых вариантах реализации n может быть равно 3. В некоторых вариантах реализации n может быть равно 4.
[0094] В некоторых вариантах реализации описанное соединение имеет Формулу (II):
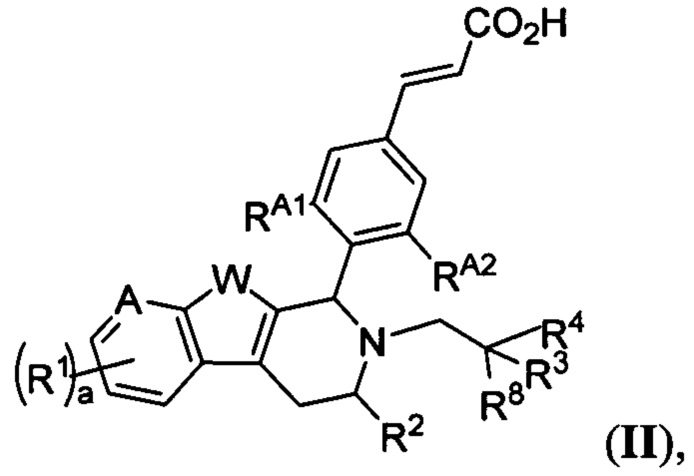
где R1-R4, R8, RA1, RA2, A, W, и а являются такими, как описано в данном документе, или представляют собой фармацевтически приемлемую соль, сольват, гидрат, полиморф, сокристалл, таутомер, стереоизомер, изотопически меченое производное или пролекарство. [0095] В Формуле (II) А и W находятся в трициклическом кольце. В некоторых вариантах реализации А может представлять собой -CRA= или -N=. В некоторых вариантах реализации А может представлять собой -CRA=, где RA как определено в данном документе. В некоторых вариантах реализации RA может представлять собой водород. В некоторых вариантах реализации RA может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В одном из примеров А может представлять собой -СН=. В одном из примеров А может представлять собой -СМе=. В других вариантах реализации А может представлять собой -NH=.
[0096] В некоторых вариантах реализации W может представлять собой -NH-. В некоторых вариантах реализации W может представлять собой -O-. В некоторых вариантах реализации W может представлять собой -S-.
[0097] Формула (II) включает один или более R1. В некоторых вариантах реализации а равно 1. В некоторых вариантах реализации а равно 2. В некоторых вариантах реализации а равно 3. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой водород. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации по меньшей мере один R1 может представлять собой фтор. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой хлор. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации по меньшей мере один R1 может представлять собой замещенный или незамещенный метил. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -CF3. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой замещенный или незамещенный этил. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой замещенный или незамещенный пропил. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -ORA где RA как определено в данном документе. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -ОН. В некоторых вариантах реализации по меньшей мере один RA может представлять собой замещенный или незамещенный C1-6 алкил. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -ОМе. В некоторых вариантах реализации по меньшей мере один R1 может представлять собой -CN.
[0098] В Формуле (II) в некоторых вариантах реализации R2 может представлять собой водород. В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный метил. В некоторых вариантах реализации R2 может представлять собой -CF3. В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный этил. В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный пропил. В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный карбоциклил (например, замещенный или незамещенный 3-7-членный моноциклический карбоциклил, содержащий ноль, одну или две двойные связи в карбоциклической кольцевой системе). В некоторых вариантах реализации R2 может представлять собой замещенный или незамещенный циклопропил.
[0099] В Формуле (II) в некоторых вариантах реализации R3 и/или R4 могут представлять собой водород. В некоторых вариантах реализации R3 и/или R4 могут представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации R3 и/или R4 могут представлять собой фтор. В некоторых вариантах реализации оба R3 и R4 могут представлять собой фтор. В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации R3 и/или R4 могут представлять собой метил. В некоторых вариантах реализации один из R3 и R4 может представлять собой фтор, а другой может представлять собой метил. В некоторых вариантах реализации один из R3 и R4 может представлять собой фтор, а другой может представлять собой водород. В некоторых вариантах реализации один из R3 и R4 может представлять собой метил, а другой может представлять собой водород. В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный карбоциклил (например, замещенный или незамещенный 3-7-членный моноциклический карбоциклил, содержащий ноль, одну или две двойные связи в карбоциклической кольцевой системе). В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный гетероциклил (например, замещенное или незамещенное 5-10-членное моноциклическое или бициклическое гетероциклическое кольцо, при этом один или два атома в гетероциклическом кольце независимо представляют собой азот, кислород или серу). В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный арил (например, фенил или бензил). В некоторых вариантах реализации R3 и/или R4 могут представлять собой замещенный или незамещенный 5-7-членный моноциклический гетероарил, при этом один, два, три или четыре атома в гетероарильной кольцевой системе независимо представляют собой азот, кислород или серу). В некоторых вариантах реализации R3 и/или R4 могут представлять собой -ORA где RA как определено в данном документе (например, -ОН, -O(замещенный или незамещенный C1-6 алкил) (например, -ОМе)). В некоторых вариантах реализации R3 и/или R4 могут представлять собой -N(RB)2, где RB как определено в данном документе (например, -NH2). В некоторых вариантах реализации R3 и R4 могут быть взяты вместе с промежуточными атомами с образованием замещенного или незамещенного карбоциклила (например, замещенного или незамещенного 3-7-членного моноциклического карбоциклила, содержащего ноль, одну или две двойные связи в карбоциклической кольцевой системе). В некоторых вариантах реализации R3 и R4 могут быть взяты вместе с промежуточными атомами с образованием замещенного или незамещенного циклопропила. В некоторых вариантах реализации R3 и R4 могут быть взяты вместе с промежуточными атомами с образованием незамещенного циклопропила, и R8 может представлять собой фтор. В некоторых вариантах реализации R3 и R4 могут быть взяты вместе с промежуточными атомами с образованием незамещенного циклопропила, и R8 может представлять собой метил. В некоторых вариантах реализации R3 и R4 могут быть взяты вместе с промежуточными атомами с образованием замещенного или незамещенного гетероциклила (например, замещенного или незамещенного 5-10-членного моноциклического или бициклического гетероциклического кольца, при этом один или два атома в гетероциклическом кольце независимо представляют собой азот, кислород или серу).
[00100] В Формуле (II) в некоторых вариантах реализации R8 может представлять собой водород. В некоторых вариантах реализации R8 может представлять собой галоген (например, F, Cl, Br или I). В некоторых вариантах реализации R8 может представлять собой фтор. В некоторых вариантах реализации R8 может представлять собой замещенный или незамещенный метил. В некоторых вариантах реализации R8 может представлять собой метил.
[00101] В Формуле (II) в некоторых вариантах реализации RA1 и/или RA2 могут представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации RA1 и/или RA2 могут представлять собой замещенный или незамещенный метил. В некоторых вариантах реализации RA1 и/или RA2 могут представлять собой замещенный или незамещенный этил. В некоторых вариантах реализации RA1 и/или RA2 могут представлять собой замещенный или незамещенный пропил. В некоторых вариантах реализации RA1 и/или RA2 могут представлять собой хлор. В некоторых вариантах реализации RA1 и/или RA2 могут представлять собой фтор. В некоторых вариантах реализации или RA1, или RA2 могут представлять собой хлор. В некоторых вариантах реализации оба RA1 и RA2 могут представлять собой хлор. В некоторых вариантах реализации один из RA1 или RA2 может представлять собой фтор, а другой из RA1 и RA2 может быть выбран из группы, состоящей из замещенного или незамещенного алкила, хлора и фтора. В некоторых вариантах реализации один из RA1 или RA2 может представлять собой фтор, а другой из RA1 и RA2 может представлять собой замещенный или незамещенный C1-6 алкил (например, метил, этил или пропил). В некоторых вариантах реализации один из RA1 или RA2 может представлять собой фтор, а другой из RA1 и RA2 может представлять собой метил. В некоторых вариантах реализации один из RA1 или RA2 может представлять собой фтор, а другой из RA1 и RA2 может представлять собой хлор. В некоторых вариантах реализации оба RA1 и RA2 могут представлять собой фтор.
[00102] В некоторых вариантах реализации соединение Формулы (I) может иметь формулу соединений, описанных в данном документе, или представлять собой их фармацевтически приемлемую соль, сольват, гидрат, полиморф, сокристалл, таутомер, стереоизомер, изотопически меченое производное или пролекарство.
[00103] В некоторых вариантах реализации соединение Формулы (II) может иметь формулу соединений, описанных в данном документе, или представлять собой их фармацевтически приемлемую соль, сольват, гидрат, полиморф, сокристалл, таутомер, стереоизомер, изотопически меченое производное или пролекарство.
[00104] Соединения, описанные в данном документе, могут быть получены из легко доступных исходных материалов с использованием способов, известных в данной области техники. Понятно, что в случаях, когда указаны типичные или предпочтительные условия реализации способа (то есть температура реакции, время, мольные соотношения реагентов, растворители, давление и так далее), также могут быть использованы другие условия реализации способа, если не указано иное. Оптимальные условия реакции могут варьироваться в зависимости от конкретных реагентов или используемого растворителя, однако такие условия могут быть определены специалистом в данной области с помощью обычных методов оптимизации. Химические вещества, используемые в описанных выше способах синтеза, могут включать, например, растворители, реагенты, катализаторы, защитные группы и реагенты для удаления защиты. Описанные выше способы также могут дополнительно включать стадии как до, так и после конкретно описанных в данном документе стадий, для добавления или удаления подходящих защитных групп с целью обеспечения в конечном итоге синтеза соединений. Кроме того, различные стадии синтеза могут быть выполнены в другой последовательности с целью получения требуемых соединений. Синтетические химические превращения и методология защитных групп (введение и удаление защитных групп), подходящих для синтеза соединений, известны из уровня техники и включают, например, описанные в R.Larock, Comprehensive Organic Transformations, VCH Publishers (1989); T.W.Greene and P.G.M.Wuts, Protective Groups in Organic Synthesis, 3rd Ed., John Wiley and Sons (1999); L.Fieser and M.Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); и L.Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995) и в последующих изданиях.
[00105] Соединения Формулы (I) и Формулы (II), обеспеченные в данном изобретении, могут быть получены из легко доступных исходных материалов с использованием обычных методов и способов. Примеры схематических иллюстраций для синтеза соединений в соответствии с изобретением, описанных в данном документе, приведены ниже. В случаях, когда указаны типичные или предпочтительные условия реализации способа (то есть температура реакции, время, мольные соотношения реагентов, растворители, давление и так далее), также могут быть использованы другие условия реализации способа, если не указано иное. Оптимальные условия реакции могут варьироваться в зависимости от конкретных реагентов или используемого растворителя, однако такие условия могут быть определены специалистом в данной области с помощью обычных методов оптимизации.
[00106] Соединения, описанные в данном документе, например, соединения Формулы (I), могут быть получены в соответствии с общей Схемой А. Соединения А1 являются коммерчески доступными или могут быть синтезированы стандартными превращениями, известными специалистам в области органической/медицинской химии. Соединения A3 могут быть получены путем реакции Пикте-Шпенглера A1 с альдегидом А2 (X=I, Br или Cl). Получение соединения А5 возможно в результате алкилирования A3 с А4. Альтернативно А5 может быть получено алкилированием А1 с А4 с последующей реакцией Пикте-Шпенглера А6 с альдегидом А2. Активированное медью или палладем образование связи С-O соединения А5 с этиленгликолем может обеспечить соединение А7. Превращение ОН-группы А7 в уходящую группу с последующим замещением А8 способно обеспечить (I).
Схема А. Пример схемы получения соединений Формулы (I)
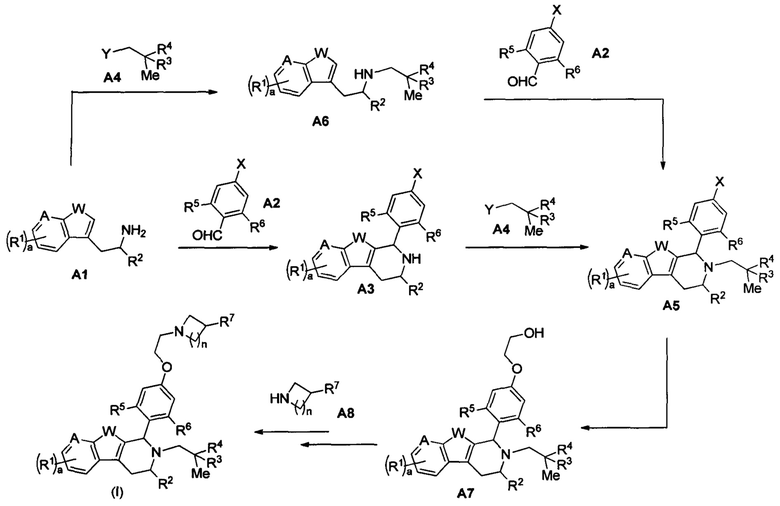
[00107] Соединения Формулы (II) могут быть получены в соответствии с общей схемой В. Соединения В3 являются коммерчески доступными или могут быть получены стандартными превращениями, известными специалистам в области органической/медицинской химии. Соединения В2 могут быть получены алкилированием А1 с В1. В результате реакции Пикте-Шпенглера В2 с альдегидом В3 может быть получено В4. Омыление В4 до (II), как правило, можно осуществить с помощью гидроксида щелочного металла в водных или смешанных водных/органических растворителях.
Схема В. Пример схемы получения соединений Формулы (II)
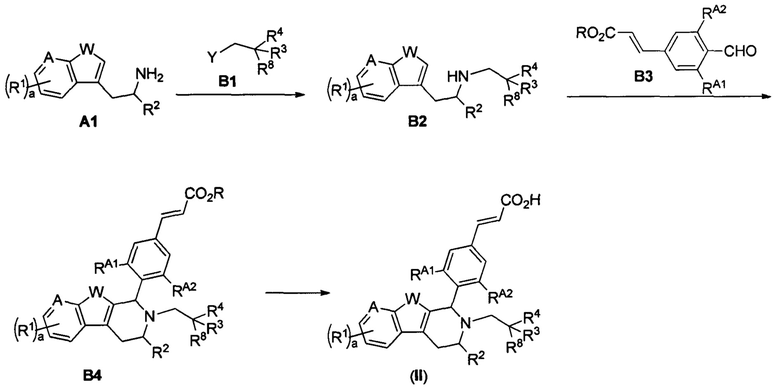
[00108] Альтернативно соединения Формулы (II) могут быть получены в соответствии с общей схемой С. В результате реакции Пикте-Шпенглера В2 с альдегидом С1 (Х=I, Br или Cl) может быть получено С2. Соединения С4 могут быть получены с помощью реакции Хека, катализируемой палладием, между С2 и С3. Омыление С4 до (II), как правило, можно осуществить с помощью гидроксида щелочного металла в водных или смешанных водных/органических растворителях.
Схема С. Пример схемы получения соединений Формулы (II)
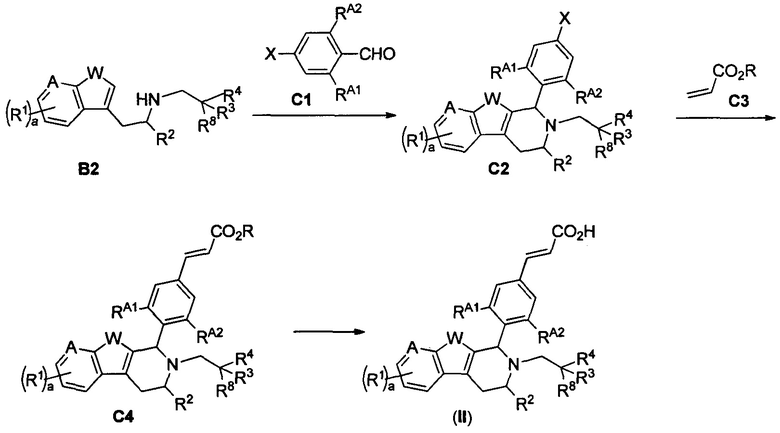
Фармацевтические композиции и наборы
[00109] Настоящее изобретение обеспечивает фармацевтические композиции, содержащие описанное в данном документе соединение или его фармацевтически приемлемую соль и необязательно фармацевтически приемлемое вспомогательное вещество. В некоторых вариантах реализации фармацевтическая композиция, описанная в данном документе, включает соединение, описанное в данном документе, или его фармацевтически приемлемую соль, а также фармацевтически приемлемое вспомогательное вещество. Описанные фармацевтические композиции полезны в лечении и/или профилактике пролиферативных заболеваний (например, ЭР-положительного рака молочной железы) или заболеваний, связанных с ЭР.
[00110] В некоторых вариантах реализации клетка, приведенная в контакт с эффективным количеством соединения или фармацевтической композиции, описанных в данном документе, находится in vitro. В некоторых вариантах реализации контактирующая клетка находится ex vivo. В некоторых вариантах реализации описанная клетка находится in vivo. В некоторых вариантах реализации описанная клетка представляет собой злокачественную клетку (например, злокачественную клетку рака молочной железы).
[00111] В некоторых вариантах реализации описанное в данном документе соединение обеспечено в эффективном количестве в фармацевтической композиции. В некоторых вариантах реализации эффективное количество представляет собой терапевтически эффективное количество (например, количество, эффективное для лечения пролиферативного заболевания у субъекта, нуждающегося в лечении). В некоторых вариантах реализации пролиферативное заболевание представляет собой рак, например, ЭР-положительный рак молочной железы. В некоторых вариантах реализации эффективное количество представляет собой профилактически эффективное количество (например, количество, эффективное для профилактики пролиферативного заболевания у субъекта, нуждающегося в этом, и/или для поддержания субъекта, нуждающегося в этом, при ремиссии пролиферативного заболевания).
[00112] Фармацевтические композиции, описанные в данном документе, могут быть получены любым способом, известным в области фармакологии. В целом способы получения включают образование связи описанного в данном документе соединения (то есть «активного ингредиента») с носителем или вспомогательным веществом и/или одним или более другими вспомогательными ингредиентами, а затем, при необходимости и/или по желанию, формование и/или упаковку продукта в требуемую однократную или многократную дозу.
[00113] Фармацевтические композиции могут быть получены, упакованы и/или проданы в общем объеме, в виде однократной дозы и/или в виде нескольких однократных доз. «Однократная доза» представляет собой дискретное количество фармацевтической композиции, содержащее заданное количество активного ингредиента. Количество активного ингредиента обычно равно дозе активного ингредиента, которая вводится субъекту, и/или удобной для применения части такой дозы, такой как половина или одна треть дозы.
[00114] Относительные количества активного ингредиента, фармацевтически приемлемого вспомогательного вещества и/или любых дополнительных ингредиентов в фармацевтической композиции, описанной в данном документе, варьируются в зависимости от особенностей, роста и/или состояния субъекта, подвергаемого лечению, а также в зависимости от пути введения композиции. Композиция может содержать от 0,1 до 100% (масс./масс.) активного ингредиента.
[00115] Фармацевтически приемлемые вспомогательные вещества, используемые при получении предложенных фармацевтических композиций, включают инертные разбавители, диспергирующие и/или гранулирующие агенты, поверхностно-активные агенты и/или эмульгаторы, агенты для улучшения распадаемости таблеток, связывающие агенты, консерванты, буферные агенты, смазывающие агенты и/или масла. В композиции также могут присутствовать такие вспомогательные вещества, как масло какао и суппозиторные основы, красители, агенты для покрытия, подсластители, ароматизаторы и отдушки.
[00116] Жидкие дозированные формы для орального и парентерального введения включают фармацевтически приемлемые эмульсии, микроэмульсии, растворы, суспензии, сиропы и эликсиры. Помимо активных ингредиентов жидкие лекарственные формы могут содержать инертные разбавители, обычно используемые в данной области, такие как, например, вода или другие растворители, солюбилизирующие агенты и эмульгаторы, такие как этиловый спирт, изопропиловый спирт, этилкарбонат, этилацетат, бензиловый спирт, бензилбензоат, пропиленгликоль, 1,3-бутиленгликоль, диметилформамид, масла (например, хлопковое, арахисовое, кукурузное, масло зародышей, оливковое, касторовое и кунжутное масла), глицерин, тетрагидрофурфуриловый спирт, полиэтиленгликоли и эфиры жирных кислот и сорбитана, а также их смеси. Помимо инертных разбавителей композиции для перорального применения могут включать адъюванты, такие как смачивающие агенты, эмульгирующие и суспендирующие агенты, подслащивающие, вкусовые и ароматизирующие агенты. В некоторых вариантах реализации для парентерального введения конъюгаты, описанные в данном документе, смешивают с солюбилизирующими агентами, такими как Cremophor®, спирты, масла, модифицированные масла, гликоли, полисорбаты, циклодекстрины, полимеры и их смеси.
[00117] Инъекционные препараты, например, стерильные инъекционные водные или масляные суспензии могут быть получены способами, известными в данной области техники, с использованием подходящих диспергирующих или смачивающих агентов и суспендирующих агентов. Стерильный инъекционный препарат может также представлять собой стерильный инъекционный раствор, суспензию или эмульсию в нетоксичном парентерально приемлемом разбавителе или растворителе, например, раствор в 1,3-бутандиоле. В качестве приемлемых носителей и растворителей могут быть использованы вода, раствор Рингера, U.S.P. и изотонический раствор хлорида натрия. Кроме того, обычно в качестве растворителя или суспензионной среды используют стерильные фиксированные масла. Для указанной цели можно использовать любое мягкое фиксированное масло, включая синтетические моно - или диглицериды. Кроме того, для приготовления инъекций используют жирные кислоты, например, олеиновую кислоту.
[00118] Инъекционные составы могут быть стерилизованы, например, путем фильтрации через бактериальный фильтр или путем включения стерилизующих агентов в форме стерильных твердых композиций, которые могут быть растворены или диспергированы в стерильной воде или другой стерильной инъекционной среде непосредственно перед применением.
[00119] Для того, чтобы продлить эффект от лекарства, чаще всего предпочтительно замедлить всасывание лекарства при подкожной или внутримышечной инъекции. Это может быть обеспечено путем использования жидкой суспензии кристаллического или аморфного материала с низкой растворимостью в воде. Скорость всасывания лекарства, кроме того, зависит от скорости его растворения, которая, в свою очередь, может зависеть от размера кристаллов и кристаллической формы. Альтернативно замедленная абсорбция парентерально введенного лекарства достигается путем растворения или суспендирования лекарства в масляном носителе.
[00120] Твердые лекарственные формы для перорального введения включают капсулы, таблетки, пилюли, порошки и гранулы. В указанных твердых лекарственных формах активный ингредиент смешивают с по меньшей мере одним инертным фармацевтически приемлемым вспомогательным веществом или носителем, таким как цитрат натрия или дикальций фосфат, и/или а) наполнителями или добавками, такими как крахмалы, лактоза, сахароза, глюкоза, маннит и кремниевая кислота, б) связующими веществами, такими как, например, карбоксиметилцеллюлоза, альгинаты, желатин, поливинилпирролидон, сахароза и камедь, в) увлажнителями, такими как глицерин, г) разрыхлителями, такими как агар, карбонат кальция, картофельный или маниоковый крахмал, альгиновая кислота, определенные силикаты, и карбонат натрия, д) раствором тормозящего вещества, такого как парафин, е) ускорителями абсорбции, такими как четвертичные аммониевые соединения, ж) смачивающими агентами, такими как, например, цетиловый спирт и моностеарат глицерина, з) абсорбентами, такими как каолин и бентонитовая глина, и и) лубрикантами, такими как тальк, стеарат кальция, стеарат магния, твердые полиэтиленгликоли, лаурилсульфат натрия, и их смесями. Лекарственная форма в виде капсул, таблеток и пилюль может также содержать буферный агент.
[00121] Твердые композиции аналогичного типа могут также применяться в качестве наполнителей в мягких и твердых наполненных желатиновых капсулах с использованием таких вспомогательных веществ, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и тому подобное. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул можно приготовить с покрытиями и оболочками, такими как энтеральные покрытия и другие покрытия, хорошо известные в области фармакологии. Они необязательно могут содержать замутнители и могут иметь состав, обеспечивающий высвобождение активного ингредиента (ингредиентов) только или предпочтительно в определенной части кишечного тракта, необязательно отсроченным образом. Примеры капсулирующих составов, которые могут быть использованы, включают полимерные вещества и воски. Твердые композиции аналогичного типа могут также применяться в качестве наполнителей в мягких и твердых наполненных желатиновых капсулах с использованием таких вспомогательных веществ, как лактоза или молочный сахар, а также высокомолекулярные полиэтиленгликоли и тому подобное.
[00122] Активный ингредиент может быть в микрокапсулированной форме с одним или более вспомогательными веществами, как указано выше. Твердые лекарственные формы таблеток, драже, капсул, пилюль и гранул можно приготовить с покрытиями и оболочками, такими как кишечнорастворимые покрытия, покрытия с контролируемым высвобождением и другие покрытия, хорошо известные в области фармацевтической разработки. В указанных твердых лекарственных формах активный ингредиент может быть смешан с по меньшей мере одним инертным разбавителем, таким как сахароза, лактоза или крахмал. Указанные лекарственные формы могут включать, что является обычной практикой, дополнительные вещества, иные, чем инертные разбавители, например, смазки для таблетирования и другие соединения, помогающие в таблетировании, такие как, магния стеарат и микрокристаллическая целлюлоза. Лекарственные формы в виде капсул, таблеток и пилюль могут содержать буферные вещества. Они необязательно могут содержать замутнители и могут иметь состав, обеспечивающий высвобождение активного ингредиента (ингредиентов) только или предпочтительно в определенной части кишечного тракта, необязательно отсроченным образом. Примеры капсулирующих агентов, которые могут быть использованы, включают полимерные вещества и воски.
[00123] Описания фармацевтических композиций, раскрытых в данном документе, в основном относятся к фармацевтическим композициям, которые подходят для введения людям, однако указанные композиции, как правило, подходят для введения животным всех видов. Модификация фармацевтических композиций, подходящих для введения людям, для получения композиций для введения различным животным хорошо известна, и ветеринар-фармаколог средней квалификации может разработать и/или осуществить такую модификацию при помощи обычного экспериментирования.
[00124] Описанные в данном документе соединения, как правило, составлены в виде однократной дозы для удобства введения и единообразия дозировки. Однако следует понимать, что общую суточную дозу соединений, описанных в данном документе, назначает лечащий врач с медицинской точки зрения. Конкретный уровень терапевтически эффективной дозы для любого конкретного субъекта или организма зависит от множества факторов, которые включают: заболевание, подлежащее лечению, а также тяжесть заболевания; активность конкретного используемого активного ингредиента; конкретную используемую композицию; возраст, массу тела, общее состояния здоровья, пол и питание пациента; время введения, пути введения и скорость выведения конкретного используемого соединения; продолжительность лечения; лекарственные препараты, используемые в комбинации или одновременно с конкретным используемым соединением, и другие подобные факторы, хорошо известные в медицине.
[00125] Также в настоящее изобретение входят наборы (например, фармацевтические пакеты). Наборы в соответствии с изобретением могут включать фармацевтическую композицию или соединение, описанное в данном документе, а также контейнер (например, флакон, ампулу, бутылку, шприц и/или дозирующую упаковку или другой подходящий контейнер). В некоторых вариантах реализации наборы могут необязательно дополнительно включать второй контейнер, содержащий фармацевтический вспомогательное вещество для разбавления или суспензию фармацевтической композиции или соединения, описанного в данном документе. В некоторых вариантах реализации фармацевтическую композицию или соединение, описанные в данном документе, обеспеченные в первом контейнере и во втором контейнере, объединяют с получением одной однократной дозированной формы.
[00126] В некоторых вариантах реализации набор, описанный в данном документе, включает первый контейнер, содержащий композицию или фармацевтическую композицию, описанные в данном документе. В некоторых вариантах реализации набор, описанный в данном документе, полезен для лечения пролиферативного заболевания (например, ЭР-положительного рака молочной железы) у субъекта, нуждающегося в лечении, и/или профилактики пролиферативного заболевания у субъекта, нуждающегося в этом. В некоторых вариантах реализации СИЭР, описанные в данном документе, полезны для лечения заболеваний и/или расстройств, связанных со стероидным гормоном, таким как эстроген.
[00127] В некоторых вариантах реализации набор, описанный в данном документе, дополнительно включает инструкцию по применению соединения или фармацевтической композиции, входящих в состав набора. Набор может также включать информацию в соответствии с требованиями регулирующего агентства, такого как Управление по контролю за продуктами и лекарствами США (FDA). В некоторых вариантах реализации информация, включенная в наборы, представляет собой инструкцию по применению препарата. В некоторых вариантах реализации наборы и инструкции обеспечивают для лечения пролиферативного заболевания у субъекта, нуждающегося в лечении, и/или профилактики пролиферативного заболевания у субъекта, нуждающегося в этом. Набор, описанный в данном документе, может включать один или более дополнительных фармацевтических агентов, описанных в данном документе, в качестве отдельной композиции.
Методы лечения
[00128] Как показано в Примерах ниже, примеры соединений СИЭР, описанные в данном документе, успешно индуцировали деградацию ЭР и ингибировали рост ЭР-положительных клеток рака молочной железы и имели лучший клиренс гепатоцитов человека, чем препарат того же класса, такой как фулвестрант, а также препараты, которые в настоящее время проходят клинические испытания, такие как GDC-0810 и AZD9496. В исследованиях на мышах указанные соединения также показали превосходные фармакокинетические профили (например, клиренс, период полураспада и AUC) по сравнению с препаратами, которые в настоящее время используются в клинических целях или проходят клинические испытания.
[00129] Соответственно, настоящее изобретение обеспечивает способы лечения пролиферативного заболевания и/или заболевания, связанного со стероидным гормоном, таким как эстроген, у субъекта, нуждающегося в лечении, при этом способы включают введение субъекту эффективного количества (например, терапевтически эффективного количества) соединения или его фармацевтической композиции, описанной в данном документе.
[00130] Другой аспект настоящего изобретения относится к способам профилактики пролиферативного заболевания у субъекта, нуждающегося в этом, при этом способы включают введение субъекту эффективного количества (например, профилактически эффективного количества) соединения или его фармацевтической композиции, описанной в данном документе.
[00131] Описанные соединения и фармацевтические композиции полезны в лечении и/или профилактике пролиферативных заболеваний. В некоторых вариантах реализации пролиферативное заболевание представляет собой рак. В некоторых вариантах реализации пролиферативное заболевание представляет собой рак молочной железы. В некоторых вариантах реализации пролиферативное заболевание представляет собой гинекологическое заболевание или рак, связанный с ЭР, такой как рак яичника, рак шейки матки или эндометрия и рак молочной железы, в частности, ЭР-положительный рак молочной железы.
[00132] В некоторых вариантах реализации описанный в данном документе способ дополнительно включает введение субъекту дополнительного фармацевтического агента. В некоторых вариантах реализации описанный в данном документе способ дополнительно включает контактирование биологического образца с дополнительным фармацевтическим агентом. В некоторых вариантах реализации описанный в данном документе способ дополнительно включает контактирование ткани с дополнительным фармацевтическим агентом. В некоторых вариантах реализации описанный в данном документе способ дополнительно включает контактирование клетки с дополнительным фармацевтическим агентом. В некоторых вариантах реализации описанный в данном документе способ дополнительно включает лучевую терапию, иммунотерапию и/или трансплантацию (например, трансплантацию костного мозга).
[00133] Соединения и композиции, обеспеченные в данном документе, могут вводиться любым путем, включая энтеральный (например, пероральный), парентеральный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, интратекальный, подкожный, интравентрикулярный, чрескожный, внутрикожный, ректальный, интравагинальный, интраперитонеальный, местный (в виде порошков, мазей, кремов и/или капель). Конкретно предусматриваемые пути включают пероральное введение, внутривенное введение (например, системная внутривенная инъекция), региональное введение через кровоток и/или лимфу и/или непосредственное введение в пораженный участок. В целом наиболее подходящий путь введения зависит от множества факторов, в том числе характера агента (например, его стабильности в среде желудочно-кишечного тракта) и/или состояния субъекта (например, способности субъекта переносить пероральное введение).
[00134] Точное количество соединения, необходимое для обеспечения терапевтически эффективного количества, для разных субъектов является различным в зависимости, например, от вида, возраста и общего состояния субъекта, тяжести побочных эффектов или расстройств, типа конкретного соединения, способа введения и тому подобного. Эффективное количество может быть включено в однократную дозу (например, однократная пероральная доза) или множество доз (например, несколько пероральных доз). В некоторых вариантах реализации, когда множество доз вводят субъекту или применяют к биологическому образцу, ткани или клетке, любые две дозы из множества доз включают различные или по существу одинаковые количества описанного в данном документе соединения. В некоторых вариантах реализации, когда множество доз вводят субъекту или применяют к биологическому образцу, ткани или клетке, частота введения множества доз субъекту или применение множества доз в ткани или клетке составляет три дозы в день, две дозы в день, одна доза в день, одна доза раз в два дня, одна доза раз в три дня или одна доза еженедельно. В некоторых вариантах реализации частота введения множества доз субъекту или применение множества доз в ткани или клетке составляет одну дозу в день. В некоторых вариантах реализации частота введения множества доз субъекту или применение множества доз в ткани или клетке составляет две дозы в день. В некоторых вариантах реализации, когда множество доз вводят субъекту или применяют к биологическому образцу, ткани или клетке, период времени между первой дозой и последней дозой из множества доз составляет один день, два дня, четыре дня, одну неделю, две недели, три недели, один месяц, два месяца, три месяца, четыре месяца, шесть месяцев, девять месяцев, один год, два года, три года, четыре года, пять лет, семь лет, десять лет, пятнадцать лет, двадцать лет или время жизни субъекта, биологического образца, ткани или клетки. В некоторых вариантах реализации период времени между первой дозой и последней дозой из множества доз составляет три месяца, шесть месяцев или один год. В некоторых вариантах реализации период времени между первой дозой и последней дозой из множества доз составляет время жизни субъекта, биологического образца, ткани или клетки. В некоторых вариантах реализации доза (например, однократная доза или любая доза из множества доз), описанная в данном документе, содержит независимо от 1 до 3 мг, от 3 до 10 мг, 10 до 30 мг, от 30 до 100 мг, от 100 до 300 мг, от 300 до 1000 мг или от 1 г до 10 г включительно описанного в данном документе соединения. В некоторых вариантах реализации описанная в данном документе доза содержит независимо от 3 мг до 10 мг включительно соединения, описанного в данном документе. В некоторых вариантах реализации описанная в данном документе доза содержит независимо от 10 мг до 30 мг включительно соединения, описанного в данном документе. В некоторых вариантах реализации описанная в данном документе доза содержит независимо от 30 мг до 100 мг включительно соединения, описанного в данном документе. В некоторых вариантах реализации описанная в данном документе доза содержит независимо от 100 мг до 300 мг включительно соединения, описанного в данном документе. В некоторых вариантах реализации описанная в данном документе доза содержит независимо от 300 мг до 1000 мг включительно соединения, описанного в данном документе.
[00135] Указанные диапазоны доз рекомендованы для введения предложенных фармацевтических композиций взрослым пациентам. Количество, которое должно вводиться, например, ребенку или подростку, может быть определено практикующим врачом или специалистом в данной области и может быть таким же, как вводится взрослому, или меньше.
[00136] Соединение или композицию, описанную в данном документе, можно вводить в комбинации с одним или несколькими дополнительными фармацевтическими агентами (например, терапевтически и/или профилактически активными агентами), полезными для лечения и/или профилактики пролиферативного заболевания. Соединения или композиции можно вводить в сочетании с дополнительными фармацевтическими агентами, которые улучшают их активность (например, активность (например, потенциал и/или эффективность) при лечении пролиферативного заболевания у субъекта, нуждающегося в лечении, и/или для профилактики пролиферативного заболевания у субъекта, нуждающегося в этом), улучшают биодоступность, улучшают безопасность, снижают резистентность к лекарственным препаратам, уменьшают и/или изменяют метаболизм, ингибируют экскрецию и/или модифицируют распределение в субъекте, биологическом образце, ткани или клетке. Следует также иметь в виду, что применяемая терапия может достигать требуемого эффекта для одного и того же расстройства и/или может иметь различные эффекты. В некоторых вариантах реализации описанная в данном документе фармацевтическая композиция, включающая описанное в данном документе соединение и дополнительный фармацевтический агент, проявляет синергический эффект, отсутствующий у фармацевтической композиции, включающей только соединение или только дополнительный фармацевтический агент, но не оба одновременно.
[00137] Соединение или композицию можно вводить одновременно, до или после одного или более дополнительных фармацевтических агентов, которые могут быть полезны, например, в качестве комбинированной терапии для лечения и/или профилактики пролиферативного заболевания. Фармацевтические агенты включают терапевтически активные агенты. Фармацевтические агенты также включают профилактически активные агенты. Фармацевтические агенты включают малые органические молекулы, такие как лекарственные соединения (например, соединения, одобренные для применения для людей или животных Управлением по контролю за продуктами и лекарствами США, как это предусмотрено в Кодексе федеральных правил (CFR)), пептиды, белки, углеводы, моносахариды, олигосахариды, полисахариды, нуклеопротеины, мукопротеины, липопротеины, синтетические полипептиды или белки, антитела, малые молекулы, связанные с белками, такими как антитела, гликопротеины, стероиды, нуклеиновые кислоты, ДНК, РНК, нуклеотиды, нуклеозиды, олигонуклеотиды, антисмысловые олигонуклеотиды, липиды, гормоны, витамины и клетки. В некоторых вариантах реализации дополнительный фармацевтический агент представляет собой фармацевтический агент, полезный для лечения пролиферативного заболевания. В некоторых вариантах реализации дополнительный фармацевтический агент представляет собой фармацевтический агент, полезный для профилактики пролиферативного заболевания. В некоторых вариантах реализации дополнительный фармацевтический агент представляет собой фармацевтический агент, одобренный регулирующим органом (например, US FDA) для лечения и/или профилактики пролиферативного заболевания. Каждый дополнительный фармацевтический агент можно вводить в дозе и/или по графику, определенному для данного фармацевтического агента. Дополнительные фармацевтические агенты также можно вводить вместе друг с другом и/или с соединением или композицией, описанной в данном документе, в однократной дозе или вводить по отдельности в разных дозах. Конкретная комбинация для использования в курсе лечения учитывает совместимость описанного в данном документе соединения с дополнительным фармацевтическим агентом (агентами) и/или желаемый терапевтический и/или профилактический эффект, который должен быть достигнут. В целом предполагается, что дополнительный фармацевтический агент (агенты) в комбинации будет использоваться в количествах, не превышающих тех, в которых он используется по отдельности. В некоторых вариантах реализации количества, используемые в комбинации, составляют меньше количеств, используемых по отдельности.
[00138] В некоторых вариантах реализации дополнительный фармацевтический агент представляет собой антипролиферативный агент (например, противораковый агент, например, иммуно-онкологические агенты (например, антитело анти-PD-1) или клетки (например, клетки CAR-T)). В некоторых вариантах реализации дополнительный фармацевтический агент представляет собой агент против ангиогенеза, противовоспалительный агент, иммунодепрессант, антибактериальный агент, противовирусное средство, сердечно-сосудистый агент, агент, понижающий уровень холестерина, антидиабетический агент, противоаллергический агент, обезболивающее средство или их комбинацию. В некоторых вариантах реализации описанные в данном документе соединения или фармацевтические композиции можно вводить в сочетании с противораковой терапией, включая, но не ограничиваясь ими, таргетную терапию (например, ингибитор, блокирующий передачу сигналов mTOR), клеточную терапию, хирургию, лучевую терапию, иммунотерапию и химиотерапию (например, доцетаксел, доксорубицин).
[00139] Без дальнейших уточнений полагаем, что специалист в данной области техники на основе приведенного выше описания может использовать настоящее изобретение в полном его объеме. Следующие конкретные варианты реализации настоящего изобретения, следовательно, должны толковаться исключительно как иллюстративные, а не ограничивающие каким-либо образом остальную часть описания. Все публикации, цитируемые в настоящем документе, включены посредством ссылки для целей или предмета изобретения, упомянутых в настоящем документе.
Примеры
[00140] Следующие далее примеры приведены для более полного понимания настоящего изобретения. Синтетические и биологические примеры, описанные в данной заявке, предложены для иллюстрации соединений, фармацевтических композиций и способов, раскрытых в данном документе, и никоим образом не должны быть истолкованы как ограничивающие их объем.
[00141] Пример 1: Синтез Соединения 1 и его производных
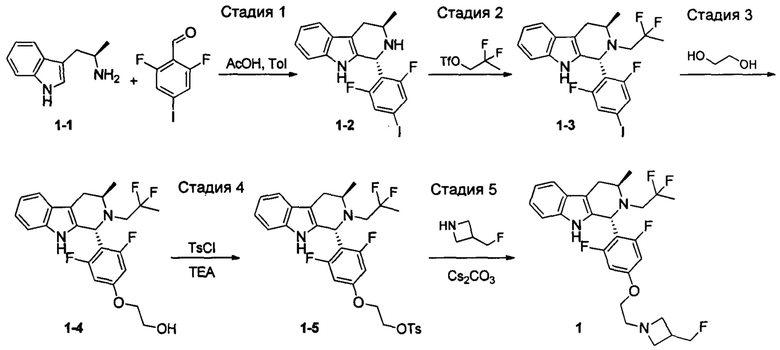
[00142] Стадия 1. Синтез 1-2
[00143] Раствор (2R)-1-(1Н-индол-3-ил)пропан-2-амина (2 г, 11,48 ммоль), уксусной кислоты (1 мл) и 2,6-дифтор-4-йодбензальдегида (3 г, 11,19 ммоль) в толуоле (20 мл) перемешивали при 80°С в течение 12 ч. Полученную смесь затем охлаждали до комнатной температуры и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/100-1/10) в качестве элюента с получением целевого продукта (2 г, выход 42%).
[00144] Стадия 2. Синтез 1-3
[00145] К раствору 1-2 (2 г, 4,71 ммоль) в 1,4-диоксане (20 мл) добавляли N,N-диизопропилэтиламин (920 мг, 7,08 ммоль) и 2,2-дифторпропилтрифторметансульфонат (1,61 г, 7,06 ммоль). Полученный раствор перемешивали при 100°С в течение 12 ч. Реакционную смесь охлаждали до комнатной температуры, а затем гасили водой (50 мл). Смесь экстрагировали этилацетатом (50 мл × 3). Органическую фазу промывали рассолом (50 мл) и концентрировали в вакууме с получением заданного продукта (1,5 г, необработанный).
[00146] Стадия 3. Синтез 1-4
[00147] К раствору 1-3 (500 мг, 1,00 ммоль) в этан-1,2-диоле (5 мл) добавляли йодид меди (94,6 мг, 0,50 ммоль), 1,10-фенантролин (18 мг, 0,10 ммоль) и карбонат цезия (649 мг, 1,99 ммоль). Полученную смесь перемешивали при 100°С в течение 2 ч. После охлаждения до комнатной температуры смесь разбавляли водой (20 мл) и экстрагировали этилацетатом (30 мл × 3). Органическую фазу промывали рассолом (20 мл) и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/100-1/10) в качестве элюента с получением целевого продукта (200 г, выход 46%).
[00148] Стадия 4. Синтез 1-5
[00149] К раствору 1-4 (50 мг, 0,11 ммоль) в тетрагидрофуране (2 мл) добавляли триэтиламин (13,9 мг, 0,14 ммоль) и 4-метилбензол-1-сульфонилхлорид (26 мг, 0,14 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 3 ч. Смесь разбавляли водой (10 мл) и экстрагировали этилацетатом (10 мл × 3). Органическую фракцию высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (50 мг, выход 74%).
[00150] Стадия 5. Синтез 1
[00151] Раствор 1-5 (50 мг, 0,08 ммоль), 3-(фторметил)азетидина (20,47 мг, 0,23 ммоль) и карбоната цезия (41,5 мг, 0,13 ммоль) в ацетонитриле (2 мл) перемешивали при 80°С в течение 12 ч. После охлаждения до комнатной температуры смесь разбавляли водой (10 мл) и экстрагировали этилацетатом (10 мл × 3). Органическую фазу концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/100-1/5) в качестве элюента с получением целевого продукта (19,7 г, выход 46%). ЖХМС (ES, m/z): а508,4. 1НЯМР (300 МГц, CDCl3,ppm): δ 7,41 (d, J=6,9 Гц, 1 Н, 7,19-7,17 (d, J=7,2 Гц, 1 Н), 7,03-6,95 (m, 2 Н) 6,64-6,59 (m, 2 H), 5,24 (s, 1 Н), 4,61 (d, J=3,9 Гц, 1 Н), 4,46 (d, J=3,9 Гц, 1 Н), 4,18-4,10 (m, 4 Н), 3,96-3,90 (m, 2 Н), 3,57-3,55 (m, 1 H), 3,44-3,41 (m, 2 H), 3,31-3,10 (m, 1 H), 3,10-2,95 (m, 2 H), 2,65-2,60(m, 2 H), 1,42 (t, J=18,9 Гц, 3 H), 1,13 (d, J=6,6 Гц, 3 H).
[00152] Аналогично были получены следующие дополнительные соединения в соответствии с изобретением.
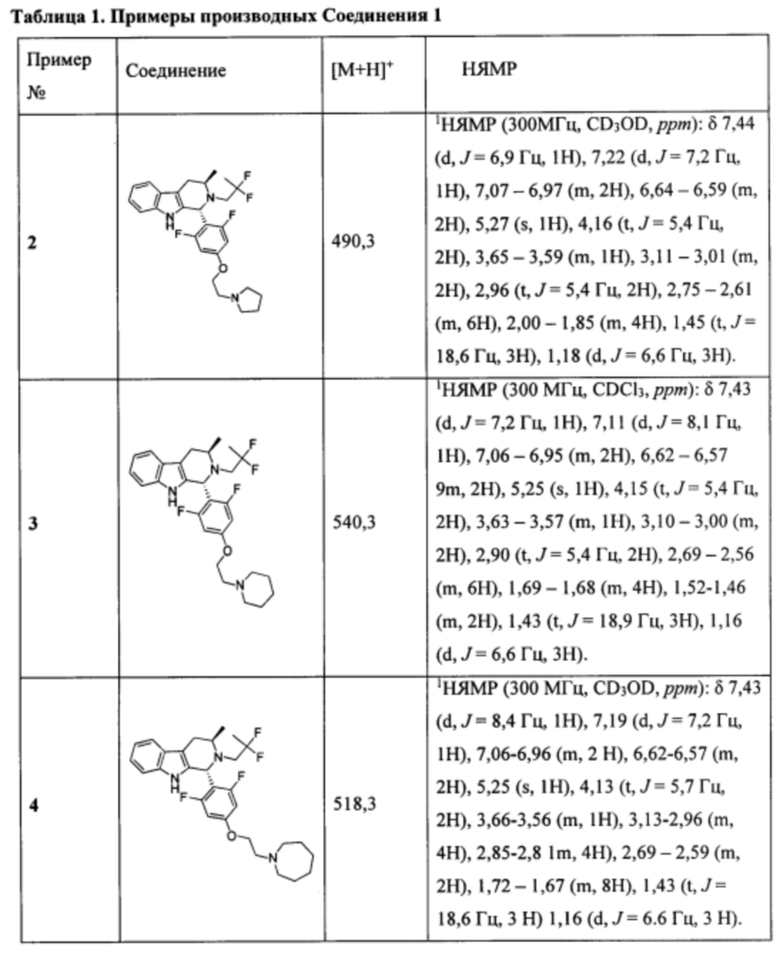
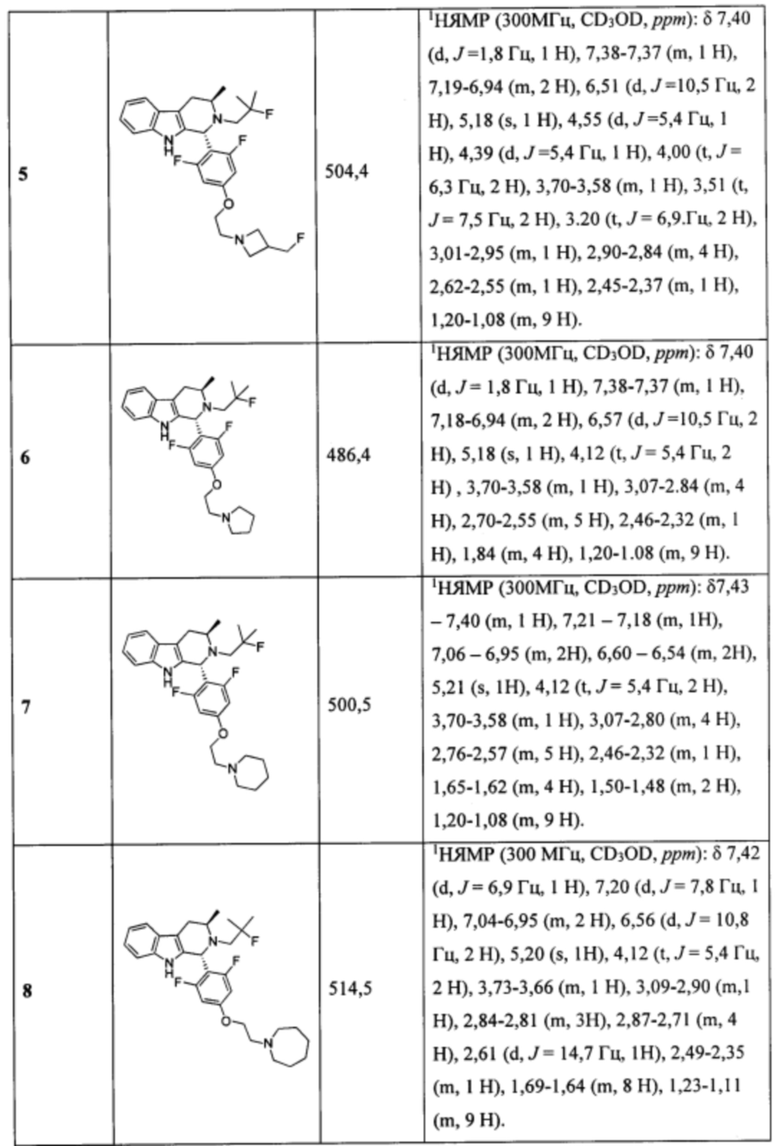
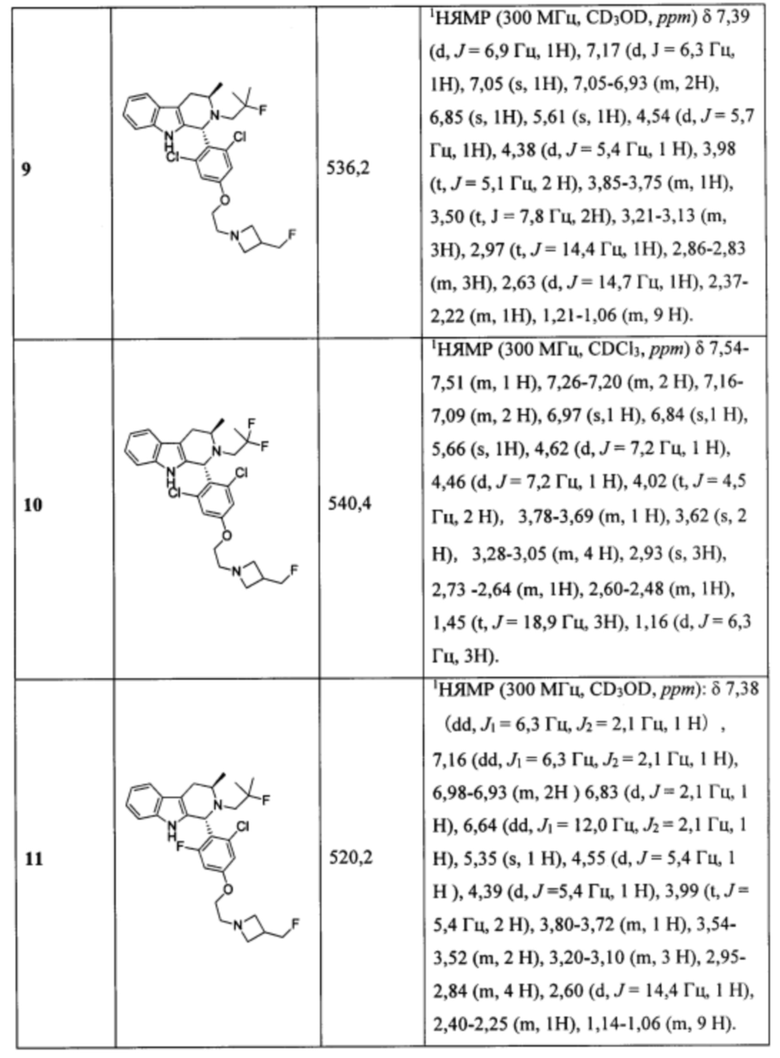
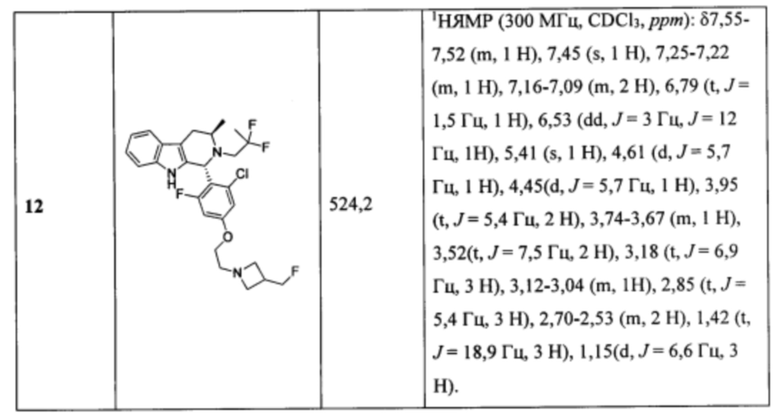
[00153] Пример 2: Синтез Соединения 13В и его производных
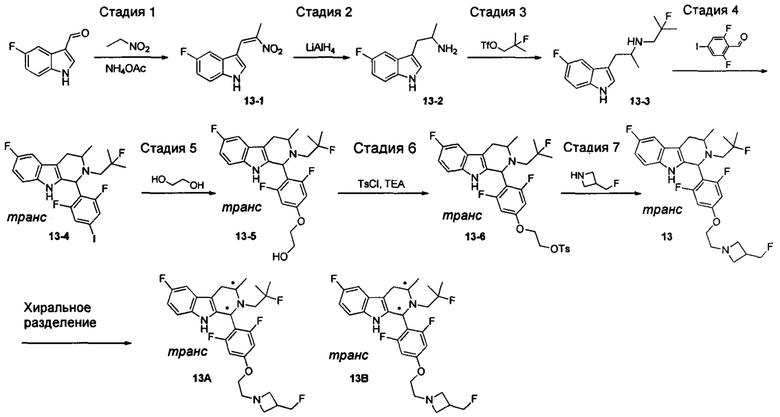
[00154] Стадия 1. Синтез 13-1
[00155] К раствору 5-фтор-1Н-индол-3-карбальдегида (2,0 г, 12,3 ммоль, 1,00 экв.) в толуоле (20 мл) добавляли ацетат аммония (1,14 г, 14,8 ммоль, 1,20 экв.) и нитроэтан (24 мл) при комнатной температуре. Полученный раствор перемешивали при 130°С в течение 5 ч. Твердое вещество отфильтровывали и осадок на фильтре промывали этилацетатом (10 мл × 3). Фильтрат концентрировали в вакууме, остаток разбавляли водой (40 мл) и экстрагировали этилацетатом (35 мл × 3). Объединенный органический слой промывали рассолом (40 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением 5-фтор-3-[(1Z)-2-нитропроп-1-ен-1-ил]1Н-индола (2,23 г, 83%) в виде желтого твердого вещества.
[00156] Стадия 2. Синтез 13-2
[00157] К раствору 5-фтор-3-[(1Z)-2-нитропроп-1-ен-1-ил]-1Н-индола (2,0 г, 9,1 ммоль, 1,00 экв.) в тетрагидрофуране (50 мл) добавляли литий алюмогидрид (1,37 г, 36,0 ммоль, 4,00 экв.) при 0°С, реакционную смесь перемешивали при 65°С в течение 1 часа. После охлаждения до комнатной температуры реакцию гасили добавлением воды (1,4 мл), водного раствора гидроксида натрия (4,2 мл, 10%). Твердое вещество отфильтровывали и осадок на фильтре промывали тетрагидрофураном (15 мл × 3). Фильтрат концентрировали в вакууме с получением 1-(5-фтор-1Н-индол-3-ил)пропан-2-амина (1,8 г, 102%) в виде коричневого масла.
[00158] Стадия 3. Синтез 13-3
[00159] К раствору 1-(5-фтор-1Н-индол-3-ил)пропан-2-амина (1,0 г, 5,2 ммоль, 1,00 экв.) в 1,4-диоксане (24 мл) добавляли N,N-диизопропилэтиламин (1,01 г, 7,8 ммоль, 1,50 экв.) и 2-фтор-2-метилпропилтрифторметансульфонат (1,28 г, 5,7 ммоль, 1,10 экв.). Полученный раствор перемешивали при 70°С в течение ночи. Реакцию гасили путем добавления воды (30 мл), смесь экстрагировали этилацетатом (30 мл × 3). Объединенный органический слой промывали рассолом (30 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:4) в качестве элюента с получением [1-(5-фтор-1Н-индол-3-ил)пропан-2-ил](2-фтор-2-метилпропил)амина (610 мг, 44%) в виде коричневого твердого вещества.
[00160] Стадия 4. Синтез 13-4
[00161] К раствору [1-(5-фтор-1Н-индол-3-ил)пропан-2-ил](2-фтор-2-метилпропил)амина (510 мг, 1,92 ммоль, 1,00 экв.) в толуоле (20 мл) добавляли уксусную кислоту (460 мг, 7,67 ммоль, 4,00 экв.) и 2,6-дифтор-4-йодбензальдегид (514 мг, 1,92 ммоль, 1,00 экв.). Полученный раствор перемешивали при 80°С в течение ночи. Реакцию гасили добавлением воды (15 мл), смесь экстрагировали этилацетатом (20 мл × 3), объединенный органический слой промывали рассолом (20 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:50) в качестве элюента с получением 1-(2,6-дифтор-4-йодфенил)-6-фтор-2-(2-фтор-2-метилпропил)-3-метил-1Н,2Н,3Н,4Н,9Н-пиридо[3,4-b]индола (800 мг, 81%) в виде светло-желтого твердого вещества.
[00162] Стадия 5. Синтез 13-5
[00163] К раствору 1-(2,6-дифтор-4-йодфенил)-6-фтор-2-(2-фтор-2-метилпропил)-3-метил-1Н,2Н,3Н,4Н,9Н-пиридо[3,4-b]индола (680 мг, 1,32 ммоль, 1,00 экв.) в этиленгликоле (20 мл) в атмосфере N2 добавляли карбонат цезия (859 мг, 2,64 ммоль, 2,00 экв.) и йодид меди (126 мг, 0,66 ммоль, 0,50 экв.). Полученный раствор перемешивали в течение ночи при 100°С, реакционную смесь охлаждали до комнатной температуры. Затем реакцию гасили путем добавления воды (20 мл) и смесь экстрагировали этилацетатом (30 мл × 3). Объединенный органический слой промывали рассолом (40 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:1) в качестве элюента с получением 2-[3,5-дифтор-4-[6-фтор-2-(2-фтор-2-метилпропил)-3-метил-1Н,2Н,3Н,4Н,9Н-пиридо[3,4-b]индол-1-ил]фенокси]этан-1-ола (600 мг, 101%) в виде светло-желтого масла.
[00164] Стадия 6. Синтез 13-6
[00165] К раствору 2-[3,5-дифтор-4-[6-фтор-2-(2-фтор-2-метилпропил)-3-метил-1Н,2Н,3Н,4Н,9Н-пиридо[3,4-b]индол-1-ил]фенокси]этан-1-ола (550 мг, 1,22 ммоль, 1,00 экв.) в дихлорметане (16 мл) добавляли триэтиламин (247 мг, 2,44 ммоль, 2,00 экв.) и N,N-диметиламинопиридин (15 мг, 0,12 ммоль, 0,10 экв.) в атмосфере N2. 4-метилбензол-1-сульфонилхлорид (280 мг, 1,45 ммоль, 1,20 экв.) добавляли при 0°С. Полученный раствор перемешивали при комнатной температуре в течение 2 ч. Реакцию гасили путем добавления воды (15 мл), смесь экстрагировали дихлорметаном (20 мл × 3). Объединенный органический слой промывали рассолом (30 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:5) в качестве элюента с получением 2-[3,5-дифтор-4-[6-фтор-2-(2-фтор-2-метилпропил)-3-метил-1Н,2Н,3Н,4Н,9Н-пиридо[3,4-b]индол-1-ил]фенокси]этил-4-метилбензол-1-сульфоната (400 мг, 54%) в виде светло-желтого масла.
[00166] Стадия 7. Синтез 13
[00167] К раствору 2-[3,5-дифтор-4-[6-фтор-2-(2-фтор-2-метилпропил)-3-метил-1Н,2Н,3Н,4Н,9Н-пиридо[3,4-b]индол-1-ил]фенокси]этил-4-метилбензол-1-сульфоната (300 мг, 0,49 ммоль, 1,00 экв.) в ацетонитриле (18 мл) добавляли карбонат цезия (1,13 г, 3,48 ммоль, 7,00 экв.) в атмосфере N2. Затем добавляли 3-(фторметил)азетидинтрифторацетил (462 мг, 2,48 ммоль, 5,00 экв.) при 0°С. Полученный раствор перемешивали при 80°С в течение ночи. Реакционную смесь охлаждали до комнатной температуры, реакцию гасили путем добавления воды (20 мл), смесь экстрагировали этилацетатом (20 мл × 3). Объединенный органический слой промывали рассолом (30 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Неочищенный продукт очищали препаративной ВЭЖХ [колонка, Xbridge, RP18, 19*150 мм; подвижная фаза. А: NH4CO3 (водн.) (5 ммоль/л). В: ацетонитрил (70% - 90% за 8 мин); скорость, 25 мл/мин; Детектор, 254 нм], для получения соединения 111 (100 мг, 38%) в виде белого твердого вещества. Соединение 111 выделяли с помощью хиральной препаративной ВЭЖХ [хиральная колонка, IA-3, 250 мм × 20 мм, 5 мкм; подвижная фаза. А: гексан (91%), В: этанол (9%); скорость, 20 мл/мин; Детектор, 254 нм] для получения 13А (время удерживания: 13,91 мин) и 13В (время удерживания: 22,37 мин).
[00168] 13А: 13,9 мг, белое твердое вещество. Хиральная ВЭЖХ [Колонка: IA, 100 мм, 4,6 мм, 0,6 мл/мин, подвижная фаза: гексан (0,1% ДЭА)/ИПС; Градиент: 10% ИПС; Детектор: 254 нм], время удерживания = 7,22 мин. ЖХ-МС (ES, m/z) [М+H]+: 522,40. 1НЯМР (300 МГц, CD3OD, ppm) δ 7,13 (dd, J=4,5 Гц, J=8,7 Гц, 1 Н), 7,07 (dd, J=2,4 Гц, 6,9 Гц, 1Н), 6,76 (td, J=2,4 Гц, 9,0 Гц, 1 Н), 6,58-6,53 (m, 2 Н), 5,19 (s, 1Н), 4,58 (d, J=7,2 Гц, 1 Н), 4,42 (d, J=7,2 Гц, 1 Н), 4,01 (t, J=6,8 Гц, 2 Н), 3,71-3,65 (m, 1Н), 3,55 (t, J=10,0 Гц, 2 Н), 3,24 (t, J=10,0 Гц, 2Н), 3,06-2,99 (m, 1Н), 2,91-2,86 (m, 3Н), 2,57 (dd, J=2,7 Гц, J=14,7 Гц, 1Н), 2,40 (dd, J=15,0 Гц, J=26,4 Гц, 1Н), 1,23-1,10 (m, 9H).
[00169] 13В: 17,8 мг, белое твердое вещество. Хиральная ВЭЖХ [Колонка: IA, 100 мм, 4,6 мм, 0,6 мл/мин, подвижная фаза: гексан (0,1% ДЭА)/ИПС; Градиент: 10% ИПС; Детектор: 254 нм], время удерживания = 12,34 мин. ЖХ-МС (ES, m/z) [M+H]+: 522,40. 1НЯМР (300 МГц, CD3OD, ppm) δ 7,13 (dd, J=4,2 Гц, J=8,7 Гц, 1 Н), 7,07 (dd, J=2,4 Гц, 6,9 Гц, 1Н), 6,77 (td, J=2,4 Гц, 9,0 Гц, 1 Н), 6,58-6,53 (m, 2 Н), 5,19 (s, 1Н), 4,58 (d, J=5,4 Гц, 1 Н), 4,42 (d, J=5,7 Гц, 1 Н), 4,01 (t, J=5,7 Гц, 2 Н), 3,71-3,65 (m, 1Н), 3,56 (t, J=7,8 Гц, 2 Н), 3,24 (t, J=7,8 Гц, 2Н), 3,06-2,99 (m, 1Н), 2,91-2,86 (m, 3Н), 2,57 (dd, J=2,7 Гц, J=14,7 Гц, 1Н), 2,40 (dd, J=15,0 Гц, J=26,4 Гц, 1Н), 1,23-1,10 (m, 9H).
[00170] Аналогично были получены следующие дополнительные соединения в соответствии с изобретением.

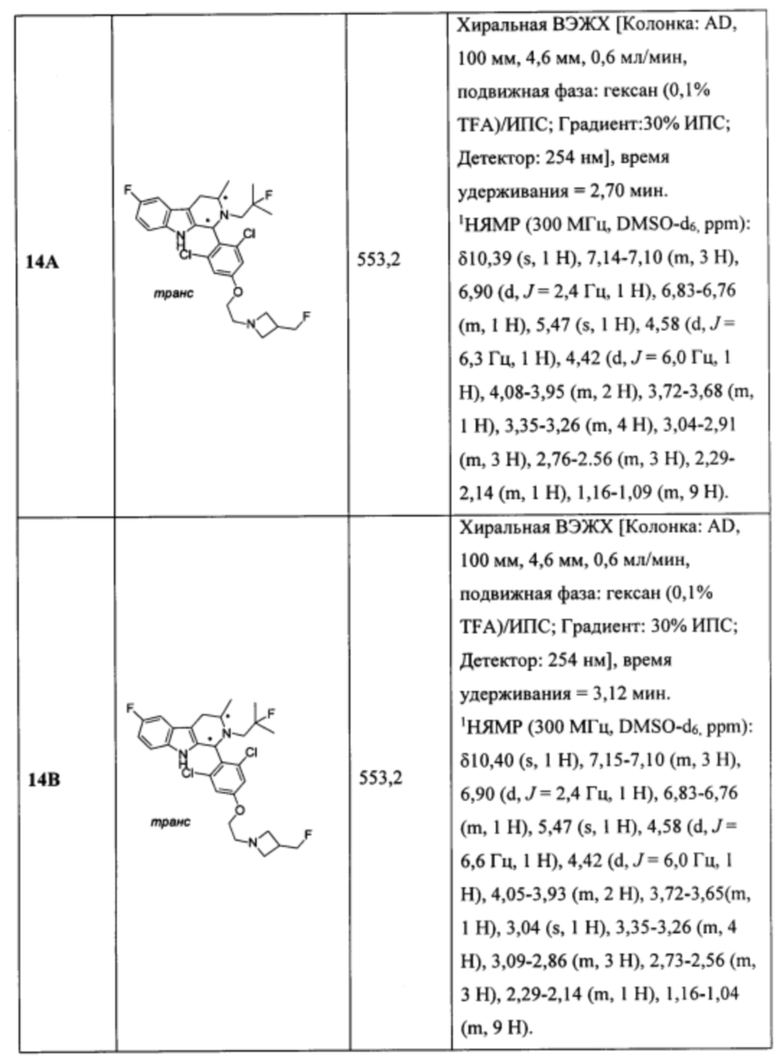
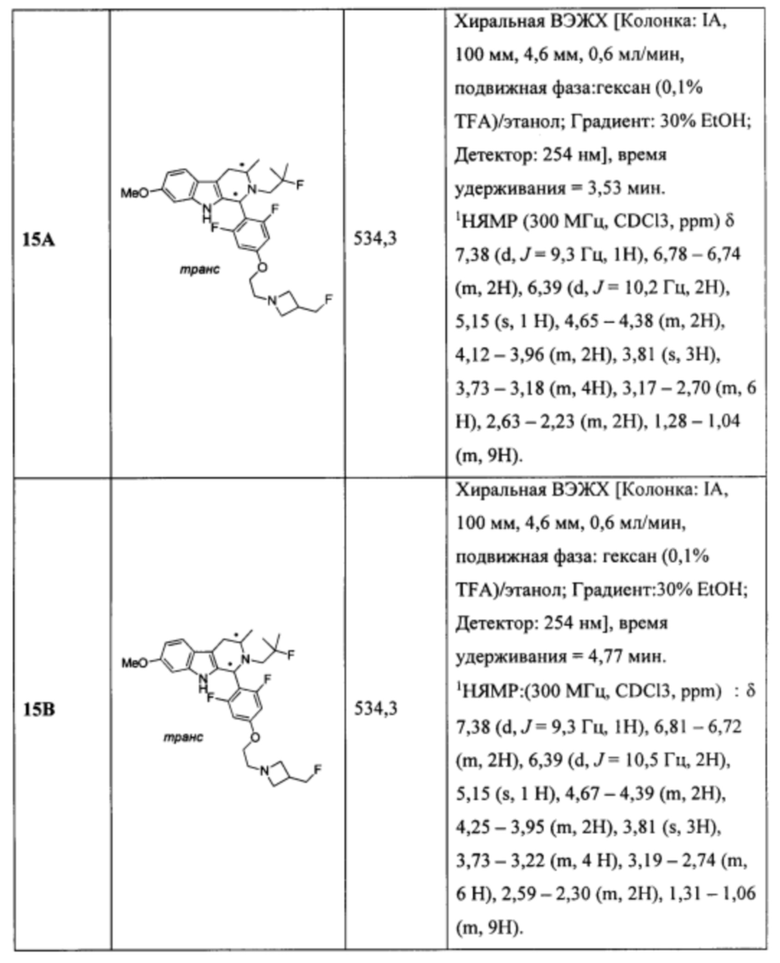
[00171] Пример 3: Синтез Соединения 16В
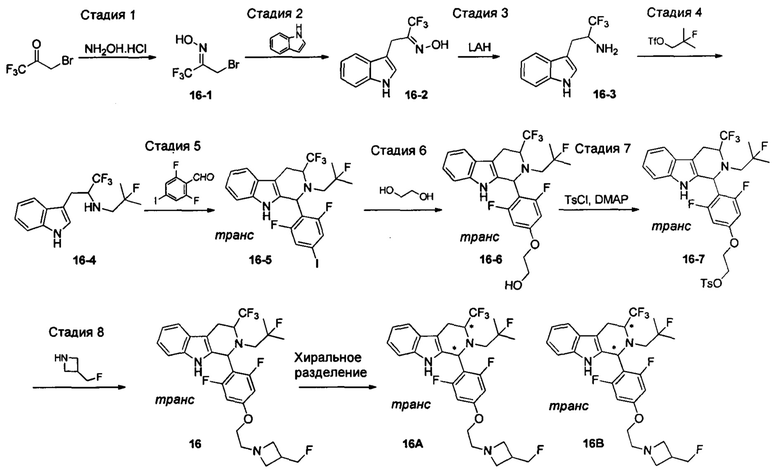
[00172] Стадия 1. Синтез 16-1
[00173] К раствору 3-бром-1,1,1-трифторпропан-2-она (10 г, 52,37 ммоль) в трихлорметане (60 мл) при комнатной температуре по каплям добавляли раствор NH2OH⋅HCl (5,46 г, 78,56 ммоль) в воде (10 мл). Полученный раствор перемешивали при 65°С в течение 24 ч. После охлаждения до комнатной температуры смесь разбавляли водой (30 мл) и экстрагировали дихлорметаном (40 мл × 3). Органическую фазу промывали рассолом (50 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали дистилляцией при пониженном давлении (0,1 МП), фракцию собирали при 70-80°С для получения целевого продукта (4,6 г, выход 43%) в виде бесцветного масла.
[00174] Стадия 2. Синтез 16-2
[00175] К раствору (Е)-N-(3-бром-1,1,1-трифторпропан-2-илиден)гидроксиламина (4 г, 19,42 ммоль) в метил-трет-бутиловом эфире (800 мл) добавляли 1H-индол (9,1 г, 77,68 ммоль) и карбонат натрия (12,5 г, 116,83 ммоль). Полученный раствор перемешивали при комнатной температуре в течение 1 дня. Твердое вещество отфильтровывали и осадок на фильтре промывали дихлорметаном (50 мл × 2). Фильтрат промывали рассолом (50 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (4 г, выход 85%) в виде светло-желтого масла.
[00176] Стадия 3. Синтез 16-3
[00177] К раствору 16-2 (4 г, 16,52 ммоль) в тетрагидрофуране (100 мл) при 0°С добавляли по частям алюмогидрид лития (2,6 г, 68,51 ммоль). Смесь перемешивали при 0°С в течение 10 минут, а затем при 70°С на протяжении ночи. Реакционную смесь охлаждали до комнатной температуры и гасили добавлением насыщенного водного раствора NH4Cl (200 мл). Твердое вещество отфильтровывали и осадок на фильтре промывали этилацетатом (100 мл × 2). Фильтрат экстрагировали этилацетатом (100 мл). Органическую фазу промывали рассолом (200 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/3) в качестве элюента с получением целевого продукта (2,4 г, выход 64%).
[00178] Стадия 4. Синтез 16-4
[00179] К раствору 16-3 (264 мг, 1,16 ммоль) и 2-фтор-2-метилпропилтрифторметансульфоната (430 мг, 1,92 ммоль) в 1,4-диоксане (1 мл) добавляли 18-краун-6 (422 мг, 1,60 ммоль) и N,N-диизопропилэтиламин (620 мг, 4,80 ммоль). Полученный раствор перемешивали при 110°С в течение 26 ч. После охлаждения до комнатной температуры реакционную смесь концентрировали в вакууме. Остаток растворяли в дихлорметане (50 мл) и промывали рассолом (30 мл × 2). Органическую фазу высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали флеш-препаративной ВЭЖХ при следующих условиях [Колонка: С18 силикагель; Подвижная фаза: MeCN/H2O (0,1% TFA)), 25%-70% MeCN; Детектор: 254 нм] с получением целевого продукта (270 мг).
[00180] Стадия 5. Синтез 16-5
[00181] К раствору 16-4 (600 мг, 1,98 ммоль) в толуоле (6 мл) добавляли 2,6-дифтор-4-йодбензальдегид (590 мг, 2,20 ммоль) и уксусную кислоту (0,2 мл). Реакционную смесь затем перемешивали при 80°С в течение 16 ч. После охлаждения смесь концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/29) в качестве элюента с получением целевого продукта (600 г, выход 55%).
[00182] Стадия 6. Синтез 16-6
[00183] К раствору 16-5 (600 мг, 1,09 ммоль) в этан-1,2-диоле (12 мл) добавляли 1,10-фенантролин (20 мг, 0,11 ммоль), CuI (105 мг, 0,55 ммоль) и карбонат цезия (711 мг, 2,18 ммоль). Реакционную смесь перемешивали при 100°С в течение 2 ч. После охлаждения смесь разбавляли водой (100 мл) и экстрагировали этилацетатом (100 мл × 2). Органическую фазу промывали рассолом (100 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:2) в качестве элюента с получением целевого продукта (270 г, выход 51%).
[00184] Стадия 7. Синтез 16-7
[00185] К раствору 16-6 (270 мг, 0,56 ммоль) в тетрагидрофуране (10 мл) добавляли п-толуолсульфонилхлорид (128 мг, 0,67 ммоль), 4-диметиламинопиридин (13 мг, 0,11 ммоль) и триэтиламин (68 мг, 0,67 ммоль). Реакционную смесь перемешивали при 30°С в течение 16 ч перед концентрированием в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (2:1) в качестве элюента с получением целевого продукта (120 г, выход 34%).
[00186] Стадия 8. Синтез 16
[00187] К раствору 3-(фторметил)азетидина (261 мг, 1,39 ммоль) в ацетонитриле (10 мл) добавляли карбонат цезия (1,02 г, 3,13 ммоль) и 16-7 (100 мг, 0,16 ммоль). Реакционную смесь перемешивали при 80°С в течение 16 ч. После охлаждения твердые вещества отфильтровывали и фильтрат концентрировали в вакууме. Остаток очищали флеш-препаративной ВЭЖХ [Колонка, С18 силикагель; подвижная фаза (А: H2O(0,05% NH4HCO3), В: MeCN), 40% MeCN до 69% MeCN за 10 мин; скорость: 80 мл/мин; Детектор, УФ 254 нм]. Неочищенный продукт затем очищали препаративной ВЭЖХ [Колонка, Xbridge RP С18, 19×150 нм; Подвижная фаза (A: H2O (0,05% NH4HCO3), В: MeCN), MeCN=50% до MeCN=80% за 8 мин, скорость: 25 мл/мин; Детектор, УФ 254 нм] с получением целевого продукта в виде рацемата (25 мг, выход 29%).
[00188] Рацемический продукт 16 разделяли с помощью хиральной препаративной ВЭЖХ [Колонка, IA; Подвижная фаза, 12% этанол/гексан (0,1% диэтиламин); 20 мл/мин; 18 мин; Детектор, 254 нм] с получением целевых продуктов.
[00189] Соединение (16А): Время удерживания = 7,7 мин. ЖХМС (ES, m/z): 558,20 [М+Н]+; 1НЯМР (300 МГц, CD3OD, ppm): δ 7,45 (d, J=6,9 Гц, 1 Н), 7,19 (d, J=6,9 Гц, 1 Н), 7,06-6,96 (m, 2 Н), 6,56 (d, J=11,1 Гц, 2 Н), 5,52 (s, 1 Н), 4,55 (d, J=5,4 Гц, 1 Н), 4,39 (d, J=5,4 Гц, 1 Н), 4,28-4,16 (m, 1 Н), 4,01-3,98 (m, 2 Н), 3,63-3,47 (m, 2 Н), 3,37-3,22 (m, 4 Н), 3,19-3,02 (m, 2 Н), 2,91-2,59 (m, 3 Н), 1,28-1.09 (m, 6 Н).
[00190] Соединение (16В): Время удерживания = 14,5 мин. ЖХМС (ES, m/z): 558,20 [М+Н]+; 1Н-ЯМР (300 МГц, CD3OD, ppm): δ 7,44 (d, J=6,9 Гц, 1 Н), 7,20 (d, J=7,2 Гц, 1 Н), 7,05-6,96 (m, 2 Н), 6,56 (d, J=13,8 Гц, 2 Н), 5,52 (s, 1 Н), 4,55 (d, J=5,4 Гц, 1 Н), 4,40(d, J=5,4 Гц, 1 Н), 4,28-4,02 (m, 1 Н), 4,01-3,98 (m, 2 Н), 3,58-3,53 (m, 2 Н), 3,34-3,25 (m, 4 Н), 3,13-3,10 (m, 2 Н), 2,92-2,88(m, 2 Н), 2,73-2,59 (m, 1 Н), 1,28-1,09 (m, 6Н).
[00191] Пример 4: Синтез Соединений 17А и 17В и их производных
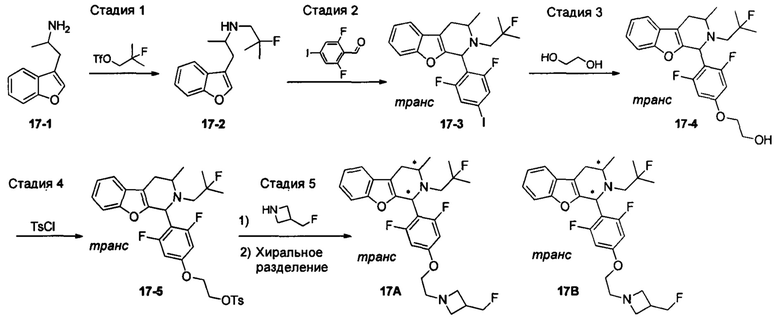
[00192] Стадия 1. Синтез 17-2
[00193] К раствору 1-(1-бензофуран-3-ил)пропан-2-амина (1,2 г, 6,85 ммоль) в 1,4-диоксане (40 мл) добавляли N,N-диизопропилэтиламин (2,6 г, 20,12 ммоль) и 2-фтор-2-метилпропилтрифторметансульфонат (1,54 г, 6,87 ммоль). Полученный раствор перемешивали при 75°С в течение 16 ч. После охлаждения смесь разбавляли ледяной водой (100 мл) и экстрагировали этилацетатом (100 мл × 3). Органическую фазу промывали рассолом (100 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (1,5 г, выход 88%).
[00194] Стадия 2. Синтез 17-3
[00195] К смеси 17-2 (820 мг, 3,29 ммоль) в толуоле (30 мл) добавляли уксусную кислоту (593 мг, 9,88 ммоль) и 2,6-дифтор-4-йодбензальдегид (883 мг, 3,29 ммоль). Полученный раствор перемешивали при 100°С в течение 2 дней. После охлаждения смесь разбавляли ледяной водой (100 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу промывали рассолом (50 мл х 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (0,3 г, выход 18%).
[00196] Стадия 3. Синтез 17-4
[00197] К смеси 17-3 (300 мг, 0,60 ммоль) в этан-1,2-диоле(10 мл) добавляли карбонат цезия (585 мг, 1,80 ммоль) и йодид меди (I) (114,2 мг). Полученный раствор перемешивали при 100°С на протяжении ночи. После охлаждения смесь разбавляли насыщенным раствором хлорида аммония (30 мл) и экстрагировали этилацетатом (30 мл × 3). Органическую фазу промывали рассолом (30 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (150 мг, выход 58%).
[00198] Стадия 4. Синтез 17-5
[00199] К раствору 17-4 (150 мг, 0,35 ммоль) в дихлорметане (10 мл) добавляли триэтиламин (35 мг, 0,35 ммоль), 4-метилбензол-1-сульфонилхлорид (79 мг, 0,41 ммоль) и 4-диметиламинопиридин (5 мг, 0,04 ммоль). Полученный раствор перемешивали при комнатной температуре на протяжении ночи. Затем реакцию гасили водой (30 мл). Полученный раствор экстрагировали дихлорметаном (20 мл × 3). Органическую фазу промывали рассолом (20 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1: 3) в качестве элюента с получением целевого продукта (0,17 г, выход 84%).
[00200] Стадия 5. Синтез 17А и 17В
[00201] К раствору 17-5 (170 мг, 0,29 ммоль) в ацетонитриле (10 мл) добавляли 3-(фторметил)азетидин (103 мг, 1,16 ммоль) и карбонат цезия (376 мг, 1,14 ммоль). Полученный раствор перемешивали при 80°С на протяжении ночи. После охлаждения смесь разбавляли ледяной водой (30 мл) и экстрагировали этилацетатом (30 мл × 3). Органическую фазу промывали рассолом (20 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали флеш-препаративной ВЭЖХ [Колонка: С 18; Подвижная фаза: CH3CN/H2O (0,05% NH4HCO3); Градиент: 70%-86% MeCN, 8 мин; Детектор: 254 нм] с получением рацемата 17 (30 мг, выход 21%) в виде белого твердого вещества.
[00202] Рацемат 17 выделяли с помощью хиральной препаративной ВЭЖХ (Колонка: AD-Н; Подвижная фаза: Гекс./EtOH; Градиент: 13% EtOH, 18 мин; Скорость: 20 мл/мин; Детектор: 254 нм] с получением целевых продуктов.
[00203] Соединение 17А: Хиральная ВЭЖХ [Колонка: AD, 100 мм, 4,6 мм, 0,6 мл/мин, подвижная фаза: гексан (0,1% TFA)/этанол; Градиент: 15% EtOH; Детектор: 254 нм], время удерживания = 3,03 мин. ЖХМС (ES, m/z): 505,4 [М+Н]+; 1НЯМР (300 МГц, CD3OD, ppm): δ 7,49-7,46 (m, 1 H), 7,32-7,29 (m, 1 H), 7,21-7,18 (m, 2 Н) 6,54 (d, J=10,8 Гц, 2 Н), 5,14 (s, 1 H), 4,55 (d, J=5,7 Гц, 1 Н), 4,40 (d, J=5,4 Гц, 1 Н), 4,01-3.98 (m, 2 H), 3,90 (d, J=5,4 Гц, 1 Н), 3,69-3,51 (m, 2 H), 3,32-3,19 (m, 2 H), 2,97-2,86 (m, 5 H), 2,86-2,57 (m, 1 H), 2,53-2,38 (m, 1 H), 1,28-1,10 (m, 9H).
[00204] Соединение 17В: Хиральная ВЭЖХ [Колонка: AD, 100 мм, 4,6 мм, 0,6 мл/мин, подвижная фаза: гексан (0,1% TFA)/этанол; Градиент: 15% EtOH; Детектор: 254 нм], время удерживания = 5,20 мин. ЖХМС (ES, m/z): 505.4 [М+Н]+; 1НЯМР (300 МГц, CD3OD, ppm): δ 7,47 (s, 1 Н, 7,30-7,19 (m, 3 H), 6,54 (d, J=11,1 Гц, 2 Н), 5,14 (s, 1 H), 4,55 (d, J=5,1 Гц, 1 Н), 4,40 (d, J=4,8 Гц, 1 Н), 4,06 (s, 2 H), 3,68 (s, 1 H), 3,56-3,51 (m, 2 H), 3,31-3,20 (m, 2 H), 3,07-2,88 (m, 5 H), 2,67-2,33 (m, 2 H), 1,63-1,40 (m, 9 H).
[00205] Аналогично были получены следующие дополнительные соединения в соответствии с изобретением.
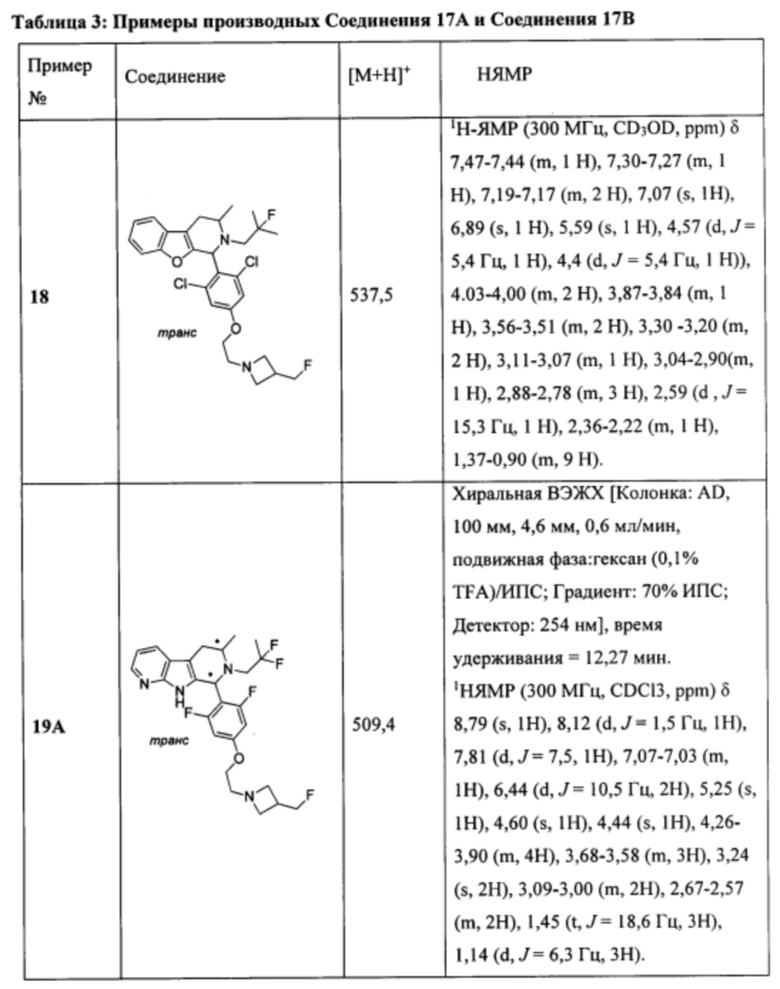
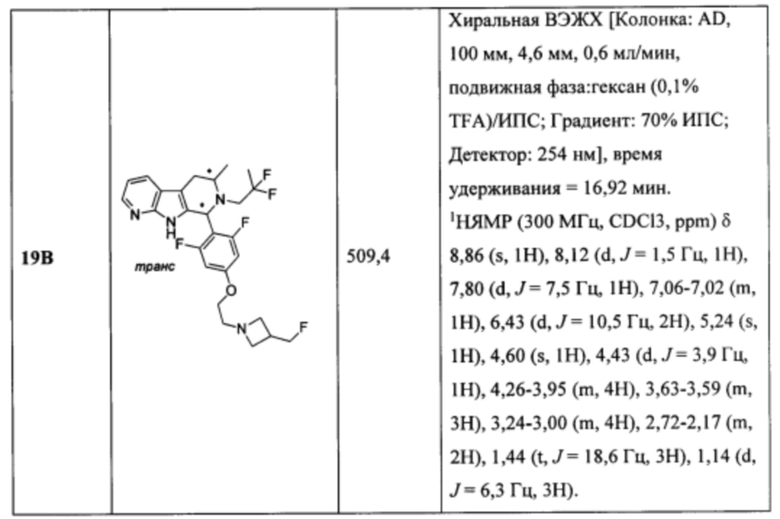
[00206] Пример 5: Синтез Соединения 20
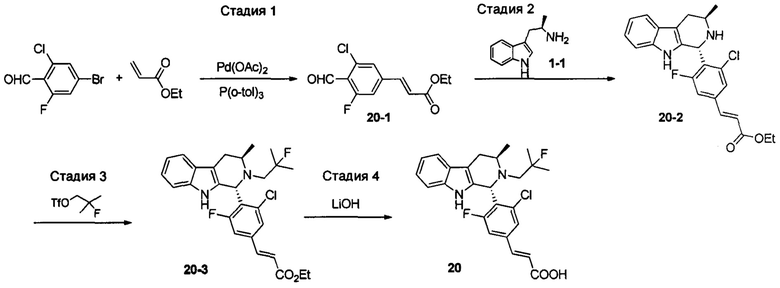
[00207] Стадия 1. Синтез 20-1
[00208] К раствору 4-бром-2-хлор-6-фторбензальдегида (1,0 г, 4,21 ммоль) в N,N-диметилформамиде (30 мл) добавляли триэтиламин (840 мг, 8,30 ммоль), ацетат палладия (47 мг, 0,21 ммоль), Р(о-тол)3 (130 мг, 0,43 ммоль) и этилпроп-2-еноат (630 мг, 6,29 ммоль). Реакционную смесь затем три раза продували азотом и перемешивали при 100°С на протяжении ночи. После охлаждения до комнатной температуры реакционную смесь гасили путем добавления ледяной воды. Смесь экстрагировали дихлорметаном (50 мл × 3). Органическую фазу промывали рассолом (30 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1: 5) в качестве элюента с получением целевого продукта (0,8 г, выход 74%).
[00209] Стадия 2. Синтез 20-2
[00210] К раствору (2R)-1-(1Н-индол-3-ил)пропан-2-амина (340 мг, 1,95 ммоль) в толуоле (10 мл) добавляли этил (2Е)-3-(3-хлор-5-фтор-4-формилфенил)проп-2-еноат (600 мг, 2,34 ммоль) и уксусную кислоту (230 мг, 3,83 ммоль). Реакционную смесь перемешивали при 80°С на протяжении ночи, затем охлаждали до комнатной температуры и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (2:5) в с получением целевого продукта (0,7 г, выход 87%).
[00211] Стадия 3. Синтез 20-3
[00212] К раствору этила 20-2 (700 мг, 1,70 ммоль) в 1,4-диоксане (20 мл) добавляли N,N-диизопропилэтиламин (1,09 г, 8,43 ммоль) и 2-фтор-2-метилпропилтрифторметансульфонат (1,14 г, 5,09 ммоль). Реакционную смесь перемешивали при 120°С на протяжении ночи, затем охлаждали до комнатной температуры и концентрировали в вакууме. Остаток очищали флеш-препаративной ВЭЖХ [Колонка: SunFire Prep С 18, 5 um, 19*150 мм; Подвижная фаза: MeCN/Вода (0,1%FA); Градиент: 71% - 86% MeCN, 6 мин, 25 мл/мин; Детектор: 220 нм] с получением целевого продукта (0,25 г, выход 30%).
[00213] Стадия 4. Синтез 20
[00214] К раствору этила 20-3 (250 мг, 0,51 ммоль) в тетрагидрофуране (30 мл) и воде (3 мл) добавляли гидроксид лития (25 мг, 1,04 ммоль). Реакционную смесь перемешивали при комнатной температуре на протяжении ночи, а затем концентрировали в вакууме. рН остатка доводили до 5-6 с помощью хлористого водорода (1 н.). Смесь экстрагировали дихлорметаном (30 мл × 3). Органическую фазу высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток растворяли в MeCN/H2O и высушивали путем лиофилизации с получением целевого продукта (75,4 мг, выход 32%). ЖХМС (ES, m/z): 459,16 [М+Н]+; 1НЯМР: (300 МГц, DMSO-d6, ppm): δ 12,55 (br s, 1 Н), 10,44 (s, 1 Н), 7,70 (s, 1 Н), 7,59-7,52 (m, 2H), 7,41 (d, J=7,2 Гц, 1 Н), 7,17 (d, J=6,9 Гц, 1 Н), 7,01-6,92 (m, 2 Н), 6,69 (d, 7=15,9 Гц, 1 Н), 5,35 (s, 1 Н), 3,68-3,61 (m, 1 Н), 3,08-2,90 (m, 2 Н), 2,64-2,59 (m, 1 Н), 2,50-2.20 (m, 1 Н), 1,16-1,05 (m, 9 Н).
[00215] Пример 6: Синтез Соединения 21
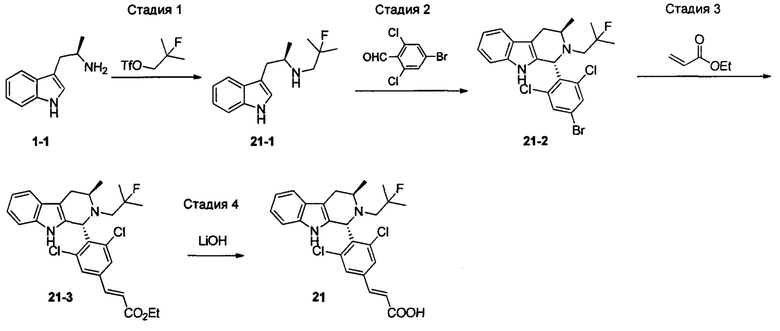
[00216] Стадия 1. Синтез 21-1
[00217] К раствору (2R)-1-(1Н-индол-3-ил)пропан-2-амина (700 мг, 4,02 ммоль) и 2-фтор-2-метилпропилтрифторметансульфоната (1,082 г, 4,80 ммоль) в 1,4-диоксане (10 мл) добавляли N,N-диизопропилэтиламин (1,56 г, 12,06 ммоль). Полученный раствор перемешивали при 70°С на протяжении ночи. После охлаждения до комнатной температуры смесь разбавляли водой (50 мл) и экстрагировали этилацетатом (100 мл × 2). Органическую фазу промывали рассолом (50 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (830 мг, выход 83%).
[00218] Стадия 2. Синтез 21-2
[00219] Раствор 21-1 (830 мг, 3,34 ммоль), 4-бром-2,6-дихлорбензальдегида (710 мг, 2,80 ммоль) и уксусной кислоты (350 мг, 5,83 ммоль) в толуоле (10 мл) перемешивали при 80°С на протяжении ночи. Затем смесь охлаждали до комнатной температуры, разбавляли водой (50 мл) и экстрагировали этилацетатом (100 мл × 2). Органическую фазу промывали рассолом (50 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (1 г, выход 74%).
[00220] Стадия 3. Синтез 21-3
[00221] Раствор 21-2 (100 мг, 0,21 ммоль), этилпроп-2-еноата (31 мг, 0,31 ммоль), Pd (OAc)2 (95 мг, 0,42 ммоль), Ph3P (110 мг) и триэтиламина (42 мг, 0,42 ммоль) в N,N-диметилформамиде (5 мл) перемешивали при 100°С в течение 48 ч. После охлаждения до комнатной температуры смесь разбавляли водой (50 мл) и экстрагировали этилацетатом (100 мл × 2). Органическую фазу промывали рассолом (50 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток растворяли в ДМФ и очищали препаративной ВЭЖХ при следующих условиях [Колонка: Х Bridge Shield RP18 OBD, 5 мкм, 19×150 мм; Подвижная фаза А: Вода (0,05% МН4НСО3), Подвижная фаза В: MeCN; Градиент: 25% MeCN до 54% за 8 мин; Детектор: УФ 254 нм] с получением целевого продукта (76 мг, выход 73%).
[00222] Стадия 4. Синтез 21
[00223] К раствору 21-3 (76 мг, 0,15 ммоль) в тетрагидрофуране (5 мл) и воде (1 мл) добавляли гидроксид лития (13 мг, 0,31 ммоль). Полученный раствор перемешивали при 25°С в течение 15 ч. Затем смесь разбавляли водой (20 мл). рН остатка доводили до 6 с помощью хлористого водорода (1 н.) и экстрагировали этилацетатом (50 мл × 2). Органическую фазу промывали рассолом (20 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток разбавляли ацетонитрилом/водой и высушивали лиофилизацией с получением целевого продукта (15,6 мг, выход 22%). ЖХМС (ES, m/z):476,38 [М+Н]+. 1НЯМР (300 МГц, CD3OD-d4, ppm): δ 7,66 (s, 1Н), 7,44-7,34 (m, 3H), 7,17 (dd, J=1,8, 6,6 Гц, 1H), 7,00-6,92 (m, 2H), 6,54 (d,J=15,9 Гц, 1H), 5,71 (s, 1H), 3,87-3,83 (m, 1H), 3,22-3,19 (m, 1H), 3,16-2,97 (m, 1H), 2,68-2,64 (m, 1H), 2,37-2,22 (m, 1H), 1,14-1,11 (m, 6H), 1,09 (d, J=10,2 Гц, 3H).
[00224] Пример 7: Синтез Соединения 22
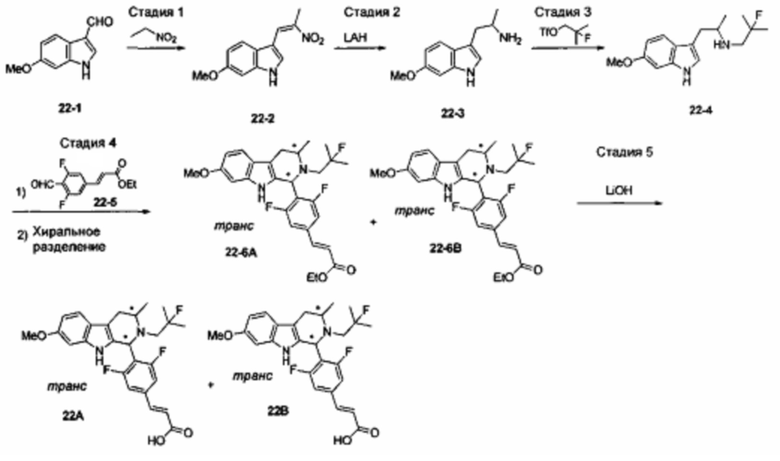
[00225] Стадия 1. Синтез 22-2
[00226] К раствору 6-метокси-1Н-индол-3-карбальдегида (2 г, 11,42 ммоль) в толуоле (20 мл) добавляли уксусную кислоту (4,4 г, 57,08 ммоль) и нитроэтан (10 мл). Полученный раствор перемешивали при 130°С в течение 6 ч. После охлаждения до комнатной температуры смесь концентрировали в вакууме. Полученный раствор разбавляли этилацетатом (100 мл). Смесь промывали водой (100 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (2,5 г, неочищенный).
[00227] Стадия 2. Синтез 22-3
[00228] К раствору 22-2 (2,5 г, 10,76 ммоль) в тетрагидрофуране (100 мл) добавляли частями алюмогидрид лития (1,63 г, 42,95 ммоль) при 0°С. Полученный раствор затем перемешивали при 65°С в течение 4 ч. После охлаждения до комнатной температуры реакцию гасили путем добавления ледяной воды (100 мл) и экстрагировали этилацетатом (100 мл × 3). Органическую фазу промывали водой (100 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (1,5 г, неочищенный).
[00229] Стадия 3. Синтез 22-4
[00230] Смесь 1-(6-метокси-1Н-индол-3-ил)пропан-2-амина (1,5 г, 7,34 ммоль), 2-фтор-2-метилпропилтрифторметансульфоната (1,8 г, 8,03 ммоль) и N,N-диизопропилэтиламина (1,05 г, 8,08 ммоль) в диоксане (20 мл) перемешивали при 70°С в течение 12 ч. После охлаждения до комнатной температуры смесь разбавляли водой (50 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу промывали рассолом (100 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/10-1/1) с получением целевого продукта (1 г, выход 49%).
[00231] Стадия 4. Синтез 22-6А и 22-6В
[00232] Смесь (2-фтор-2-метилпропил)[1-(6-метокси-1Н-индол-3-ил)пропан-2-ил]амина (1 г, 3,59 ммоль), этил (2Е)-3-(3,5-дифтор-4-формилфенил)проп-2-еноата (860 мг, 3,58 ммоль) и уксусной кислоты (1 мл) в толуоле (10 мл) перемешивали при 80°С в течение 12 ч. После охлаждения до комнатной температуры смесь разбавляли водой (50 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1/100-1/10) с получением целевого продукта в виде рацемата (750 мг). Рацемат отделяли хиральной препаративной ВЭЖХ [Колонка, IA; Подвижная фаза: гексан: EtOH=80:20, 20 мл/мин; Детектор: УФ=254 нм] с получением 22-6А (RT=4,45 мин) в виде белого твердого вещества и 22-6 В (RT=9,27 мин) в виде белого твердого вещества.
[00233] Стадия 5. Синтез 22А и 22В
[00234] К раствору 22-6А (30 мг, 0,06 ммоль) в тетрагидрофуране (2 мл) и воде (0,5 мл) добавляли гидроксид лития (4,32 мг, 0,18 ммоль). Полученную смесь перемешивали при комнатной температуре в течение 12 ч, затем разбавляли водой (5 мл). рН раствора доводили до 6 с помощью хлористого водорода (1 н.) и экстрагировали этилацетатом (5 мл × 3). Органическую фракцию высушивали над безводным натрия сульфатом и концентрировали в вакууме с получением целевого продукта 22А (12,5 мг, выход 44%). ЖХМС (ES, m/z):473,2 [М+Н]+. 1НЯМР (300 МГц, CD3OD, ppm): δ 7,57 (d,J=16,2 Гц, 1Н), 7,29 (m, 3Н), 6,75 (d,J=2,4 Гц, 1H), 6,65 (dd, J=2,1, 8,4 Гц, 1H), 6,54 (d, J=15,9 Гц, 1H), 5,31 (s, 1H), 3,76 (s, 3H), 3,69-3,67 (m, 1H), 3,05-2,98 (m, 2H), 2,62-2,38 (m, 2H), 1,20-1,1 l(m, 9H).
[00235] Аналогичным способом выполнили гидролиз 22-6В с получением 22 В. ЖХМС (ES, m/z):473,2 [М+Н]+. 1НЯМР (300 МГц, CD3OD, ppm): δ 7,57 (d, J=16,2 Гц, 1Н), 7,29-7,18 (m, 3Н), 6,75 (d, J=2,4 Гц, 1H), 6,65 (dd, J=2,1, 8,4 Гц, 1H), 6,54 (d, J=15,9 Гц, 1H), 5,31 (s, 1H), 3,76 (s, 3H), 3,69-3,67 (m, 1H), 3,05-2,98 (m, 2H), 2,62-2,38 (m, 2H), 1,20-1,11 (m, 9H).
[00236] Пример 8: Синтез Соединения 23
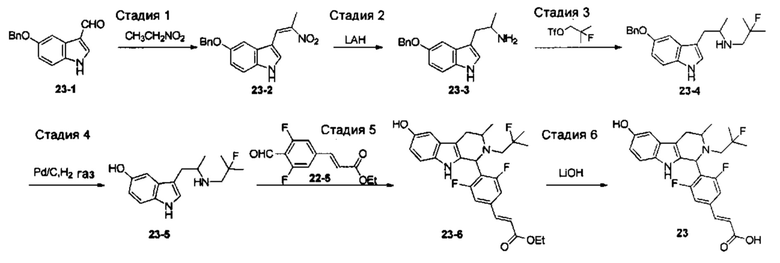
[00237] Стадия 1. Синтез 23-2
[00238] К раствору 5-(бензилокси)-1Н-индол-3-карбальдегида (2 г, 7,96 ммоль) в толуоле (20 мл) добавляли нитроэтан (24 мл) и ацетат аммония (600 мг, 8,00 ммоль). Затем смесь перемешивали при 130°С в течение 4 ч. После охлаждения до комнатной температуры смесь разбавляли водой (100 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу промывали рассолом (50 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (2,45 г, неочищенный).
[00239] Стадия 2. Синтез 23-3
[00240] К раствору литийалюминийгидрида (1,2 г, 31,62 ммоль) в тетрагидрофуране (30 мл) добавляли по каплям 5-(бензилокси)-3-[(1Z)-2-нитропроп-1-ен-1-ил]-1Н-индол (2,45 г, 7,95 ммоль) в тетрагидрофуране (20 мл). Смесь перемешивали при 0°С в течение 30 мин, а затем при 65°С в течение 5 ч. После охлаждения до комнатной температуры смесь разбавляли ледяной водой (100 мл) и экстрагировали этилацетатом (100 мл × 3). Органическую фазу промывали рассолом (100 мл × 2), высушивали над безводным сульфатом натрия, фильтровали и концентрировали в вакууме с получением целевого продукта (2,2 г, неочищенный).
[00241] Стадия 3. Синтез 23-4
[00242] К раствору 1-[5-(бензилокси)-1Н-индол-3-ил]пропан-2-амина (1,2 г, 4,28 ммоль) в 1,4-диоксане (30 мл) добавляли 2-фтор-2-метилпропилтрифторметансульфонат (960 мг, 4,28 ммоль) и N,N-диизопропилэтиламин (770 мг). Затем смесь перемешивали при 70°С на протяжении ночи. После охлаждения до комнатной температуры смесь разбавляли водой (100 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу промывали рассолом (50 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (2/3) в качестве элюента с получением целевого продукта (430 г, выход 28%).
[00243] Стадия 4. Синтез 23-5
[00244] К раствору [1-[5-(бензилокси)-1Н-индол-3-ил]пропан-2-ил](2-фтор-2-метилпропил)амина (430 мг, 1,21 ммоль) в метаноле (20 мл) добавляли палладий на угле (100 мг). Смесь перемешивали при комнатной температуре в течение 2 ч в атмосфере водорода (1 атм). Смесь отфильтровывали через целит, фильтрат концентрировали в вакууме с получением целевого продукта (280 мг, выход 87%).
[00245] Стадия 5. Синтез 23-6
[00246] К раствору 3-[2-[(2-фтор-2-метилпропил)амино]пропил]-1Н-индол-5-ола (280 мг, 1,06 ммоль) в толуоле (30 мл) добавляли этил(2Е)-3-(3,5-дифтор-4-формилфенил)проп-2-еноат (250 мг, 1,04 ммоль) и уксусную кислоту (200 мг, 3,33 ммоль). Затем смесь перемешивали при 80°С на протяжении ночи. После охлаждения до комнатной температуры смесь разбавляли водой (100 мл) и экстрагировали этилацетатом (50 мл × 3). Органическую фазу промывали рассолом (50 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:3) в качестве элюента с получением целевого продукта (180 г, выход 36%).
[00247] Стадия 6. Синтез 23
[00248] К раствору 23-6 (100 мг, 0,21 ммоль) в тетрагидрофуране (5 мл) и воде (1 мл) добавляли гидроксид лития (10 мг, 0,42 ммоль). Смесь затем перемешивали при комнатной температуре на протяжении ночи, после чего разбавляли водой (20 мл). рН раствора доводили до 6 с помощью хлористого водорода (1 н.) и экстрагировали этилацетатом (20 мл × 3). Органическую фазу промывали рассолом (20 мл × 2), высушивали над безводным сульфатом натрия и концентрировали в вакууме с получением целевого продукта (11,9 мг, выход 13%). ЖХМС (ES, m/z):459,18 [М+Н]+; 1НЯМР: (300 МГц, CD3OD, ppm): δ 7,53 (d, J=16,2 Гц, 1Н), 7,18 (d, J=9,9 Гц, 2H), 6,99 (d, J=8,7 Гц, 1H), 6,81 (d, J=2,4 Гц, 1H), 6,59- 6,50 (m, 2H), 5,26 (s, 1H), 3,69-3,63 (m, 1H), 3,08-2,87 (m, 2H), 2,56-2,50 (m, 1H), 2,46-2,32 (m, 1H), 1,32-1,09 (m, 9H).
[00249] Пример 9: Синтез Соединения 24 и его производных
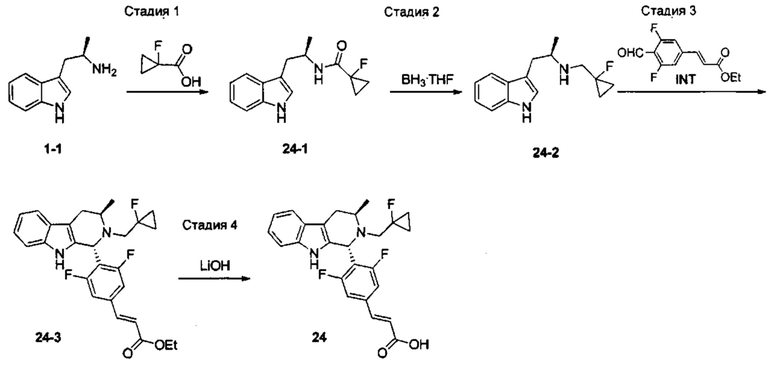
[00250] Стадия 1. Синтез 24-1
[00251] К раствору 1-фторциклопропан-1-карбоновой кислоты (700 мг, 6,73 ммоль) в N,N-диметилформамиде (10 мл) добавляли N,N-диизопропилэтиламин (1,5 г, 11,61 ммоль), HATU (2,4 г, 6,32 ммоль) и (2R)-1-(1Н-индол-3-ил)пропан-2-амин (1 г, 5,74 ммоль). После перемешивания при комнатной температуре на протяжении ночи смесь гасили путем добавления ледяной воды (20 мл). Смесь экстрагировали этилацетатом (20 мл × 3). Органическую фазу промывали рассолом (20 мл × 3), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:3) в качестве элюента с получением целевого продукта (600 мг, выход 40%).
[00252] Стадия 2. Синтез 24-2
[00253] Раствор 24-1 (600 мг, 2,30 ммоль) в BH3.THF (1 М) (20 мл) нагревали с обратным холодильником на протяжении ночи. После охлаждения до комнатной температуры смесь концентрировали в вакууме, остаток растворяли в метаноле (20 мл), затем нагревали с обратным холодильником на протяжении ночи. После охлаждения до комнатной температуры смесь концентрировали в вакууме. Остаток разбавляли водой (100 мл) и экстрагировали этилацетатом (100 мл × 3). Органическую фазу промывали рассолом (100 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Необработанную смесь очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:2) в качестве элюента с получением целевого продукта (350 мг, выход 62%).
[00254] Стадия 3. Синтез 24-3
[00255] К раствору (R)-N-((1-фторциклопропил)метил)-1-(1Н-индол-3-ил)пропан-2-амина (350 мг, 1,42 ммоль) и этил(2Е)-3-(3,5-дифтор-4-формилфенил)проп-2-еноата (341,5 мг, 1,42 ммоль) в толуоле (5 мл) добавляли уксусную кислоту (1 каплю). После перемешивания при 80°С в течение 2 ч реакционную смесь охлаждали до комнатной температуры и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:2) в качестве элюента с получением целевого продукта (120 мг, выход 18%).
[00256] Стадия 4. Синтез 24
[00257] К раствору 24-3 (120 мг, 0,26 ммоль) в тетрагидрофуране (0,9 мл) и воде (0,1 мл) добавляли гидроксид лития (12,3 мг, 0,51 ммоль). Полученный раствор перемешивали при комнатной температуре на протяжении ночи. рН раствора доводили до 6 с помощью хлористого водорода (1 н.) и экстрагировали смесь этилацетатом (20 мл × 3). Органическую фазу промывали рассолом (20 мл), высушивали над безводным сульфатом натрия и концентрировали в вакууме. Остаток очищали колоночной хроматографией на силикагеле с этилацетатом/петролейным эфиром (1:1) в качестве элюента с получением целевого продукта (49,9 мг, выход 44%). ЖХМС (ES, m/z):441,30 [М+Н]+; 1НЯМР: (300 МГц, DMSO-d6, ppm): δ 12,50 (br s, 1H), 10,59 (s, 1Н), 7,56-7,40 (m, 4Н), 7,19 (d, J=5,7 Гц, 1Н), 700-7.6.95 (m, 2Н), 6,67 (d, J=12 Гц, 1Н), 5,23 (s, 1Н), 3,58-3,56 (m, 1Н), 3,09-2,88 (m, 2Н), 2,67-2,63 (m, 2Н), 1,07 (d, J=5,1 Гц, 3Н) 0,94-0,89 (m, 2Н), 0,56-0,51 (m, 2Н).
[00258] Аналогично были получены следующие дополнительные соединения в соответствии с изобретением.
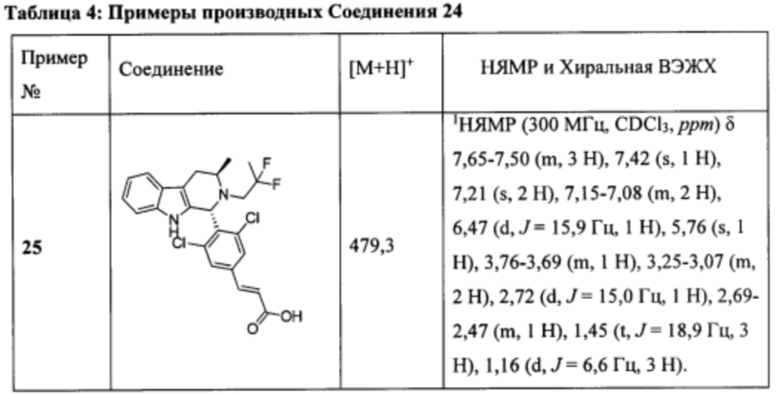
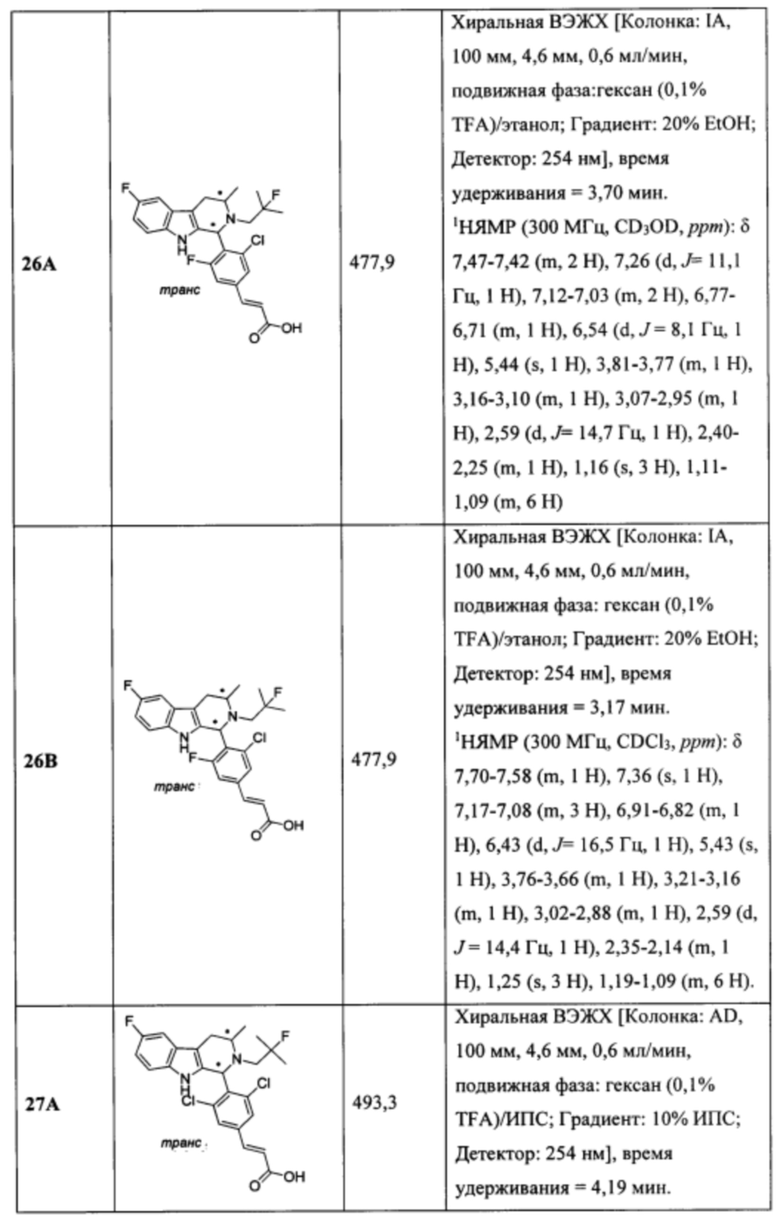
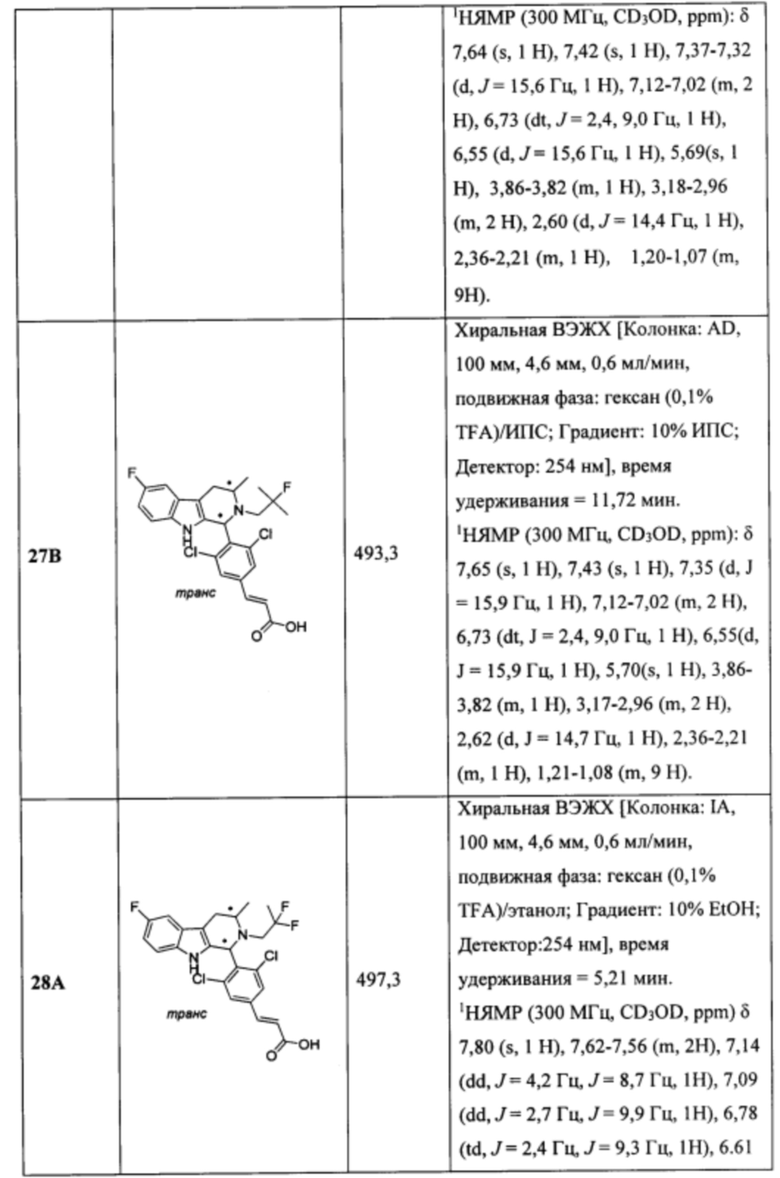
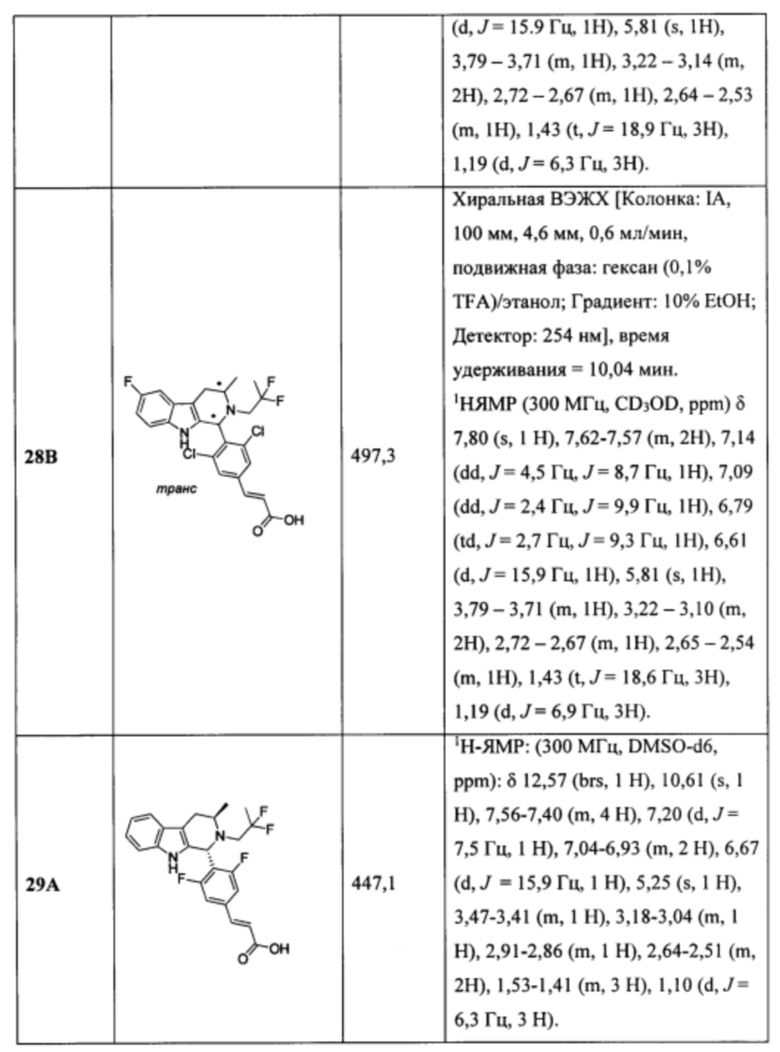
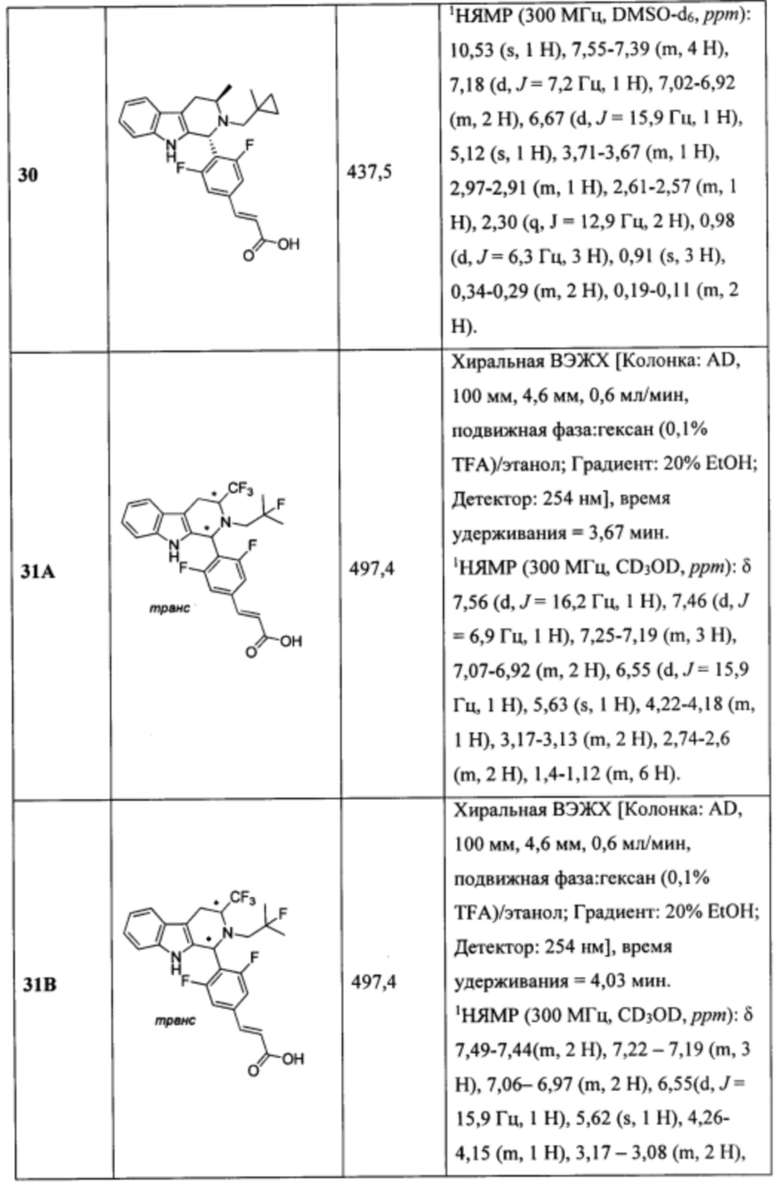
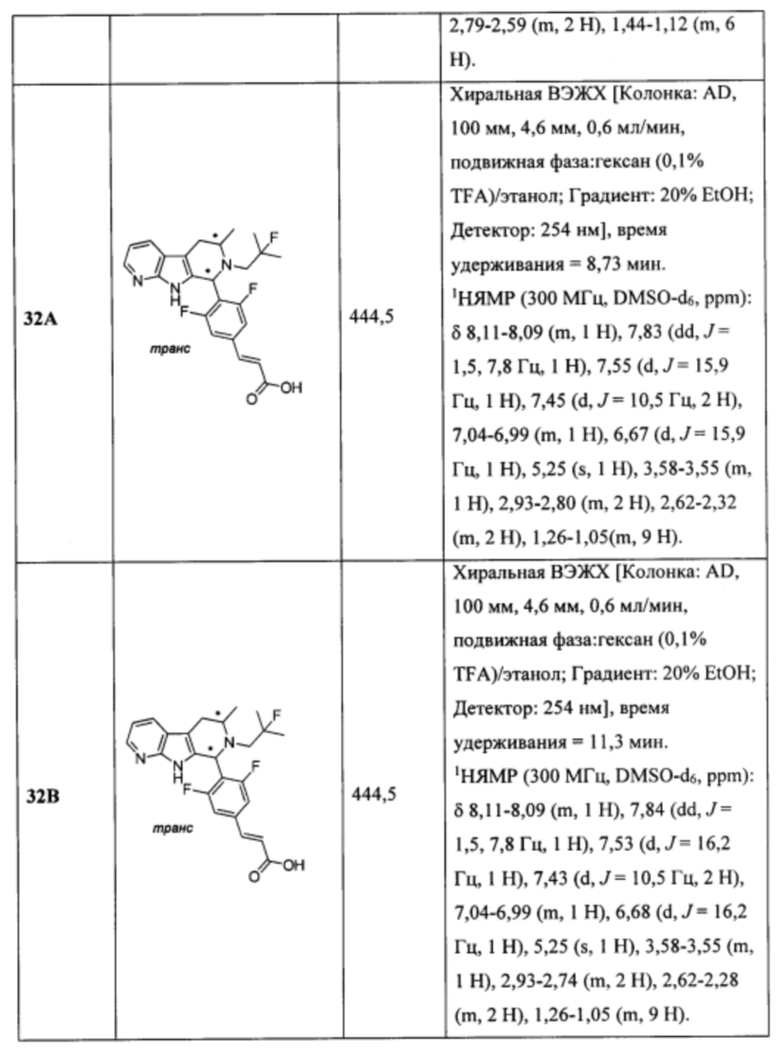
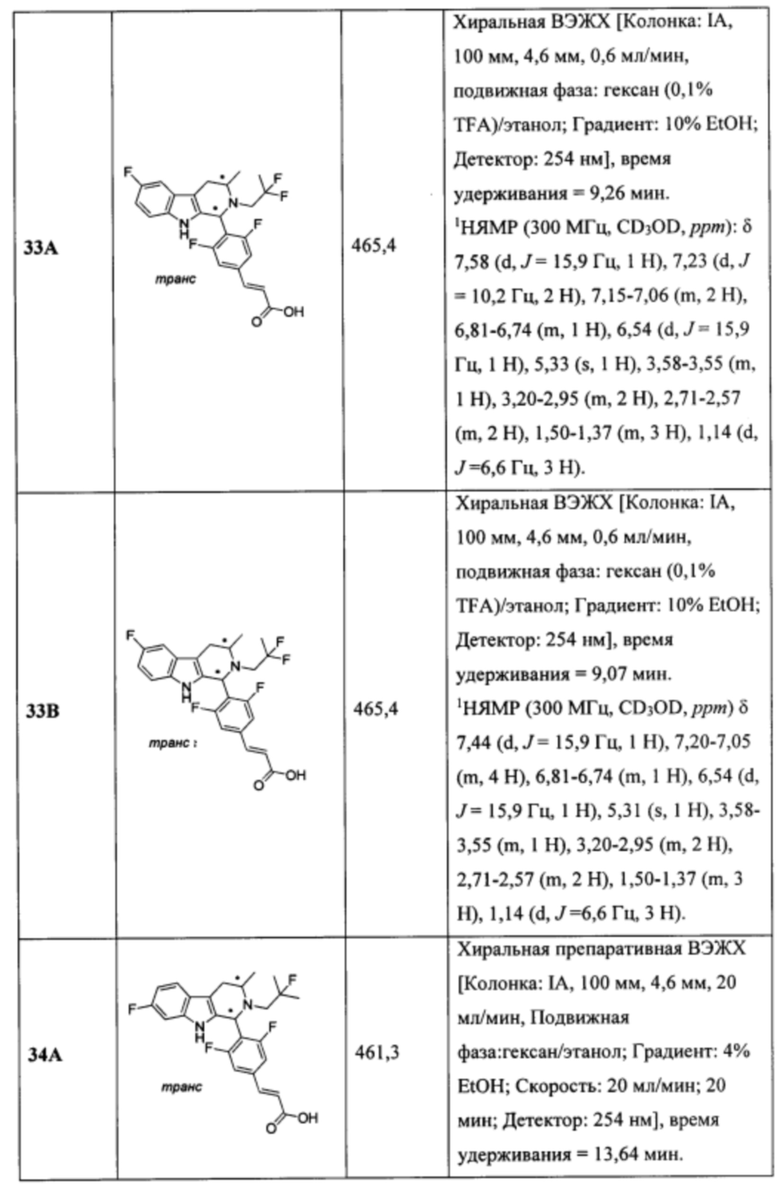
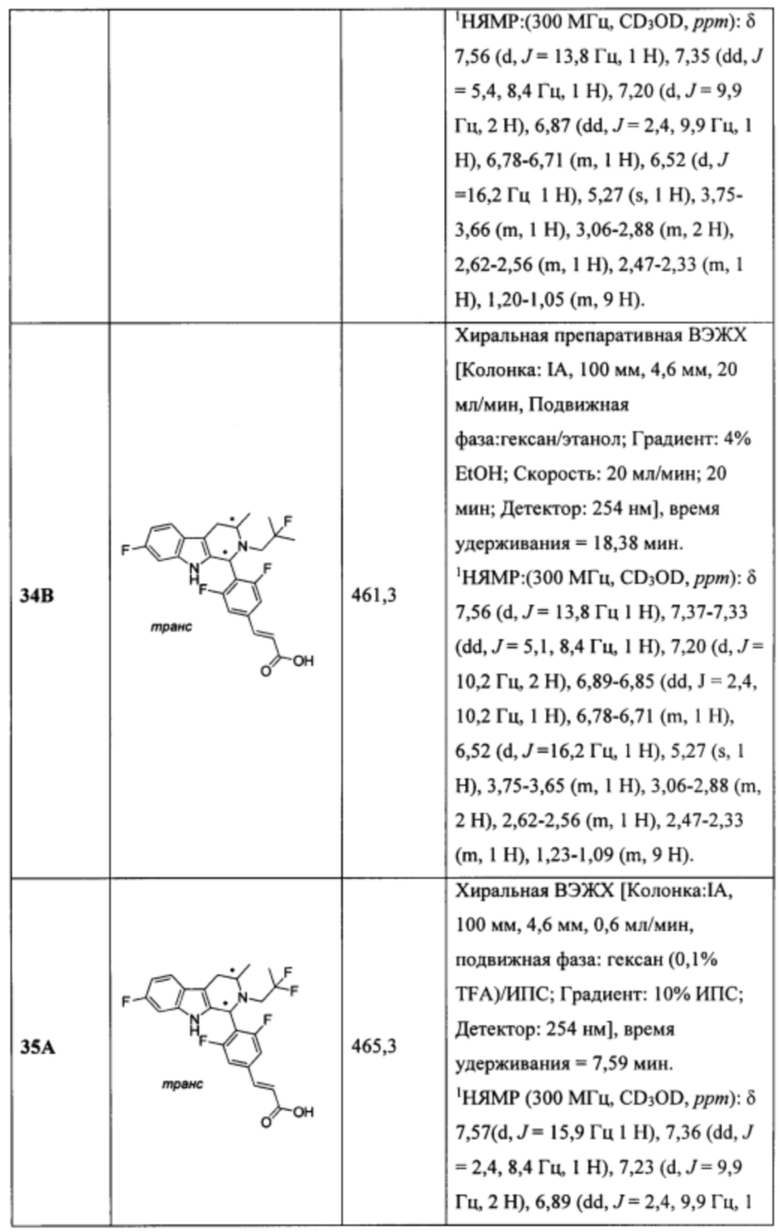
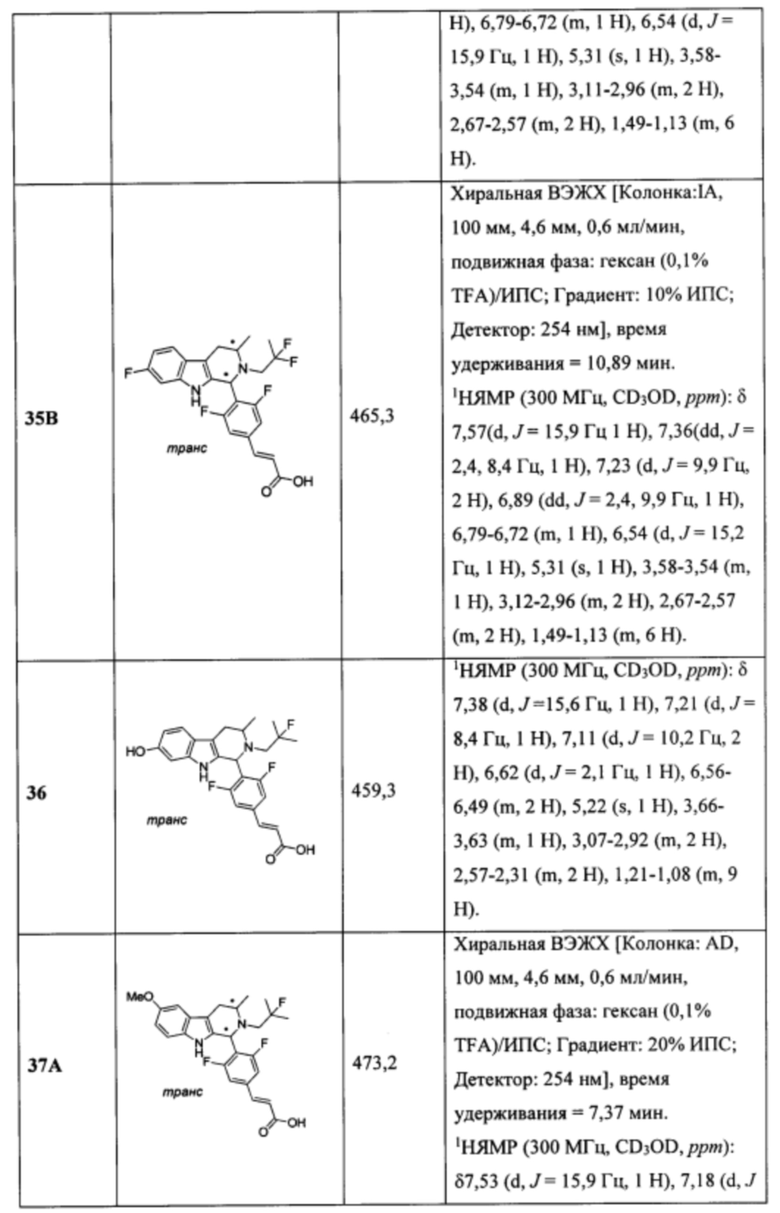
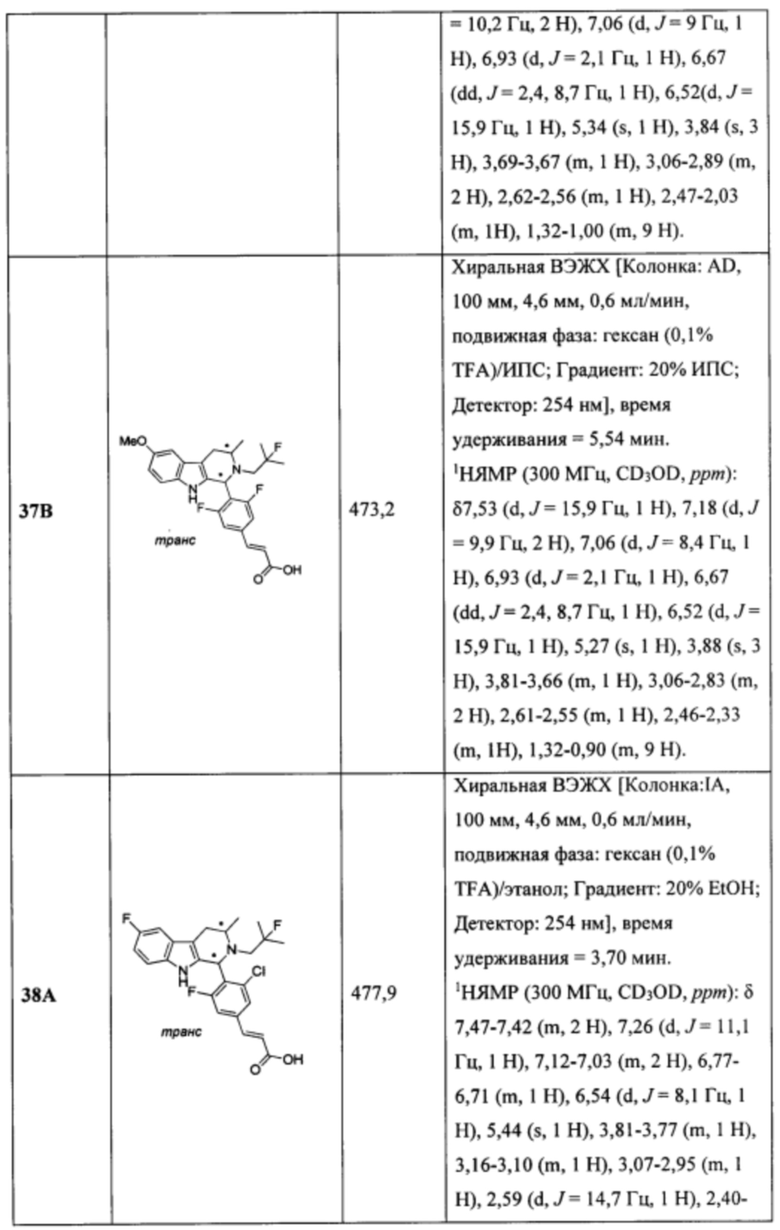
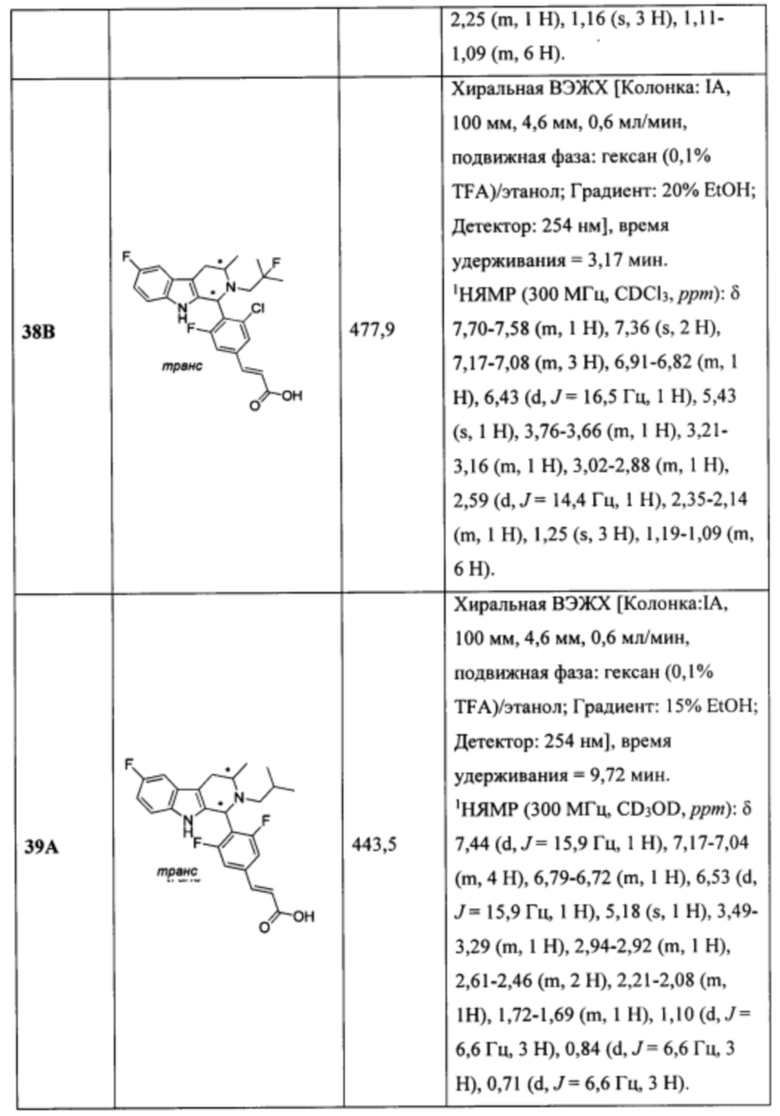
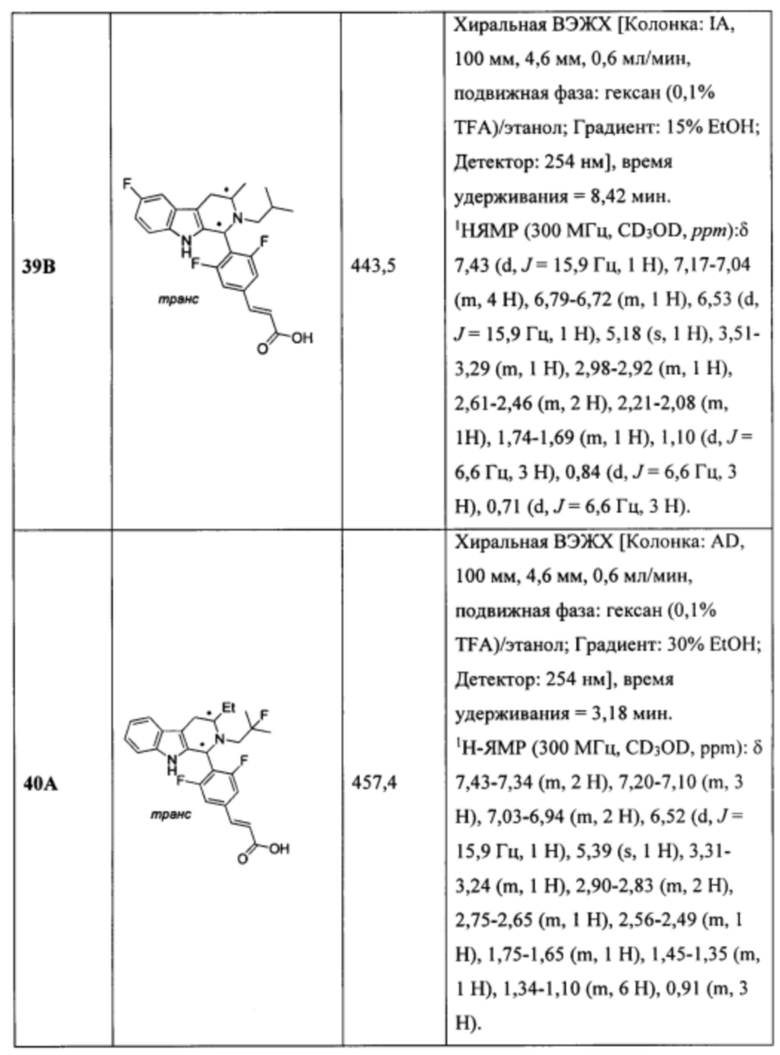
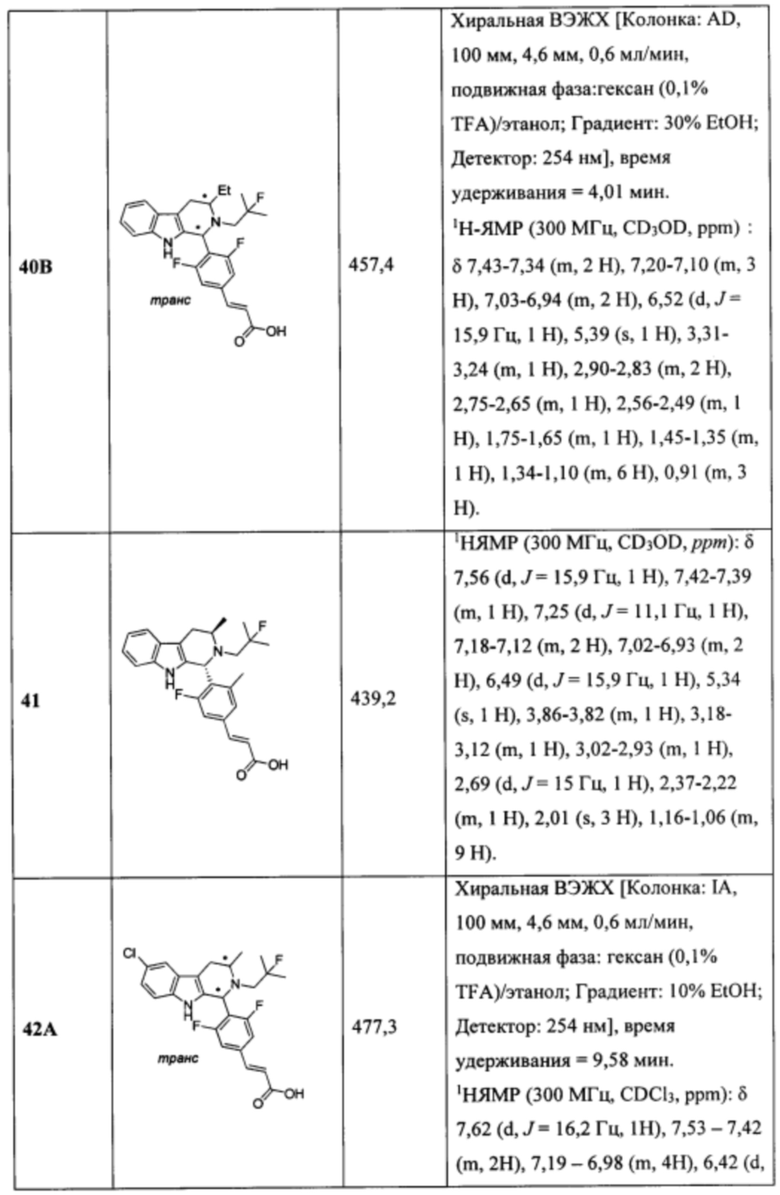
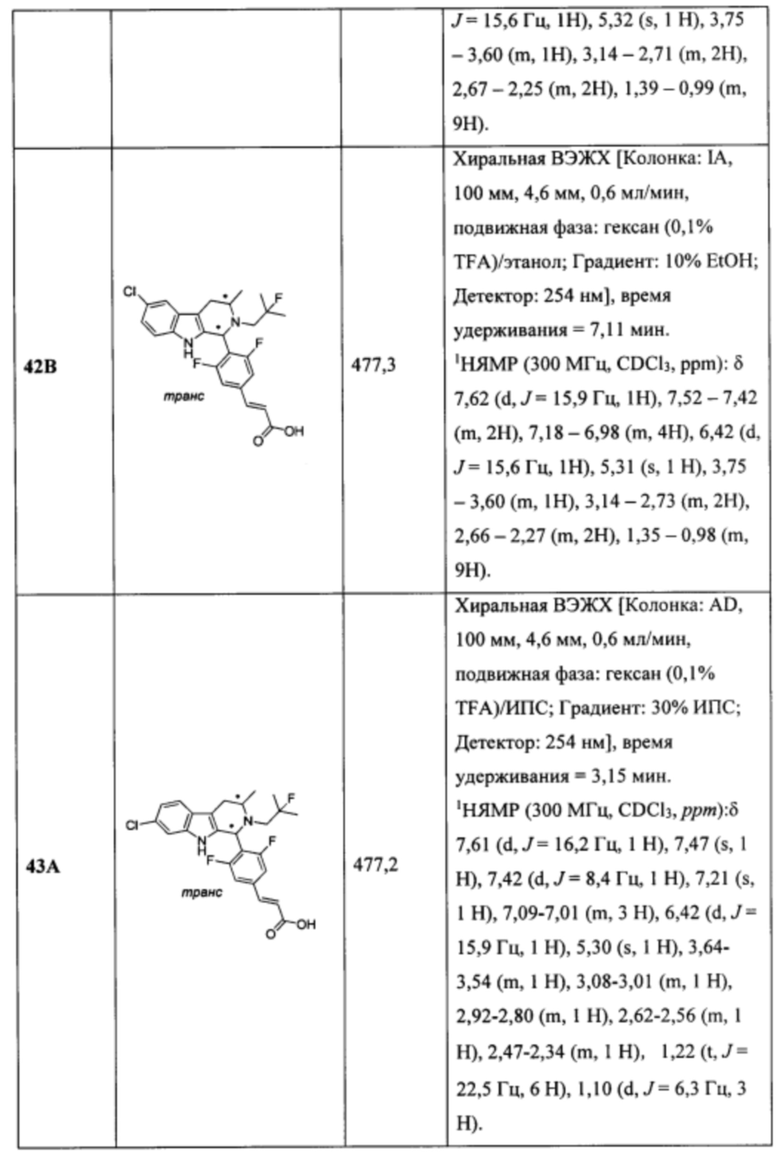
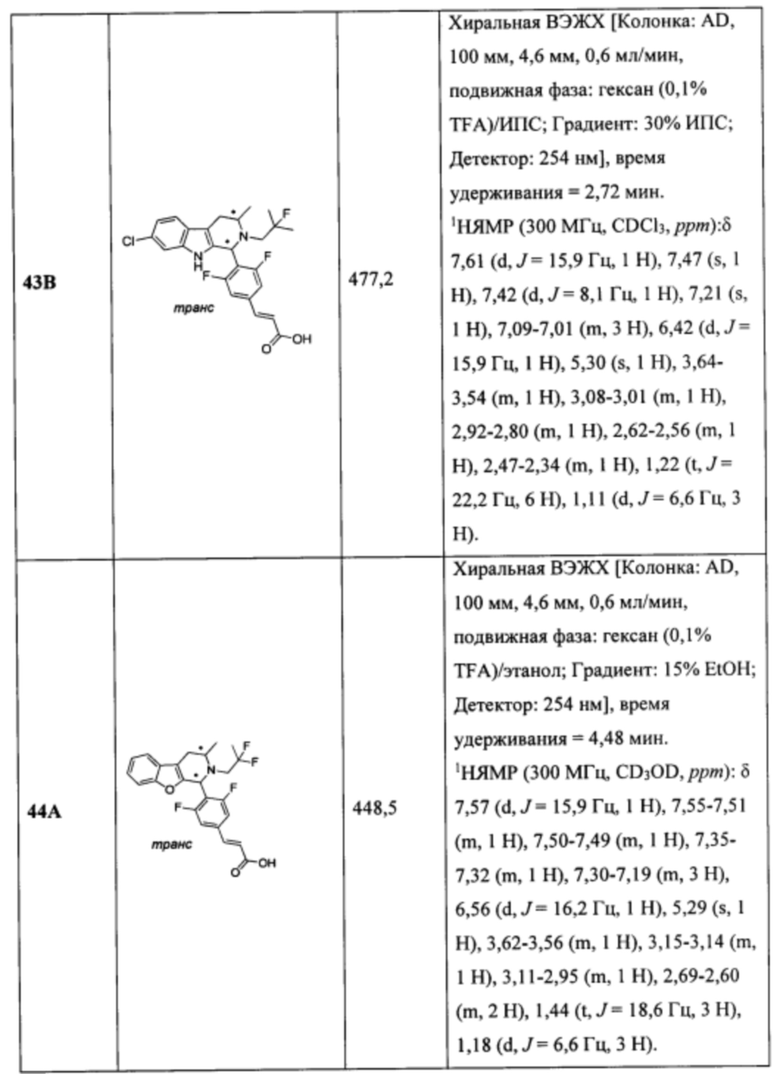
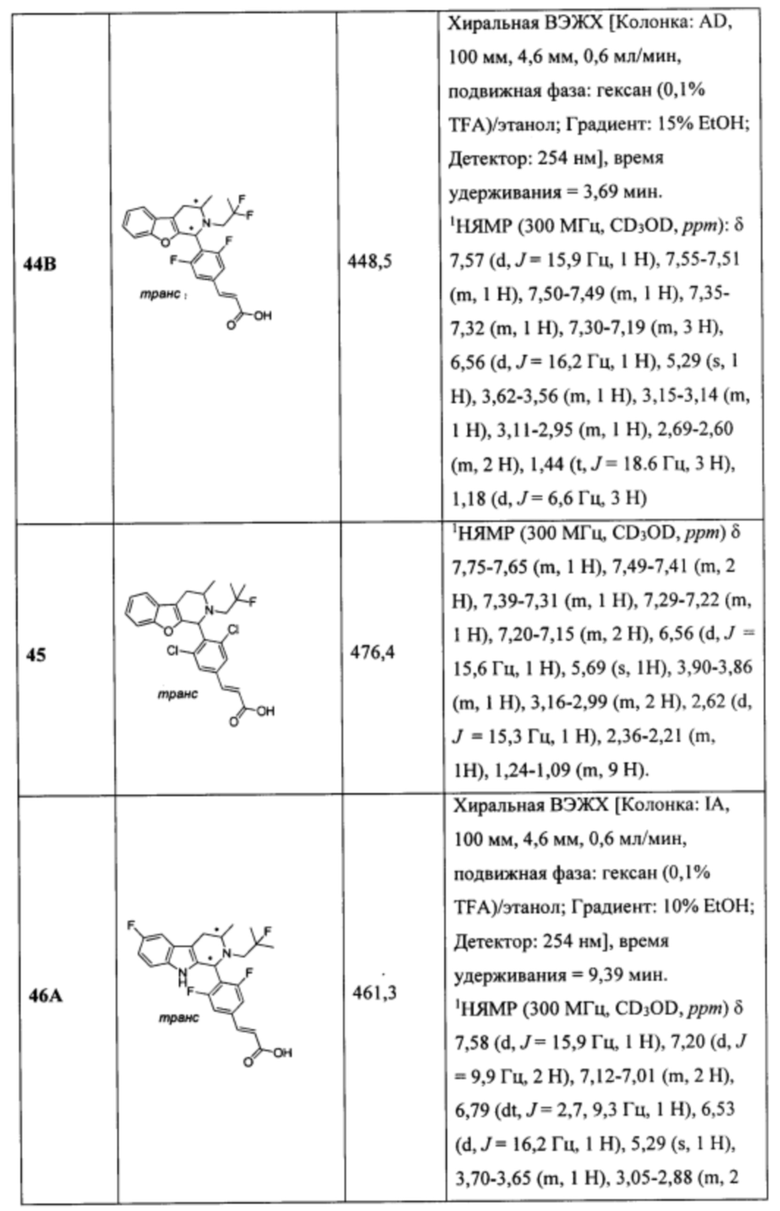
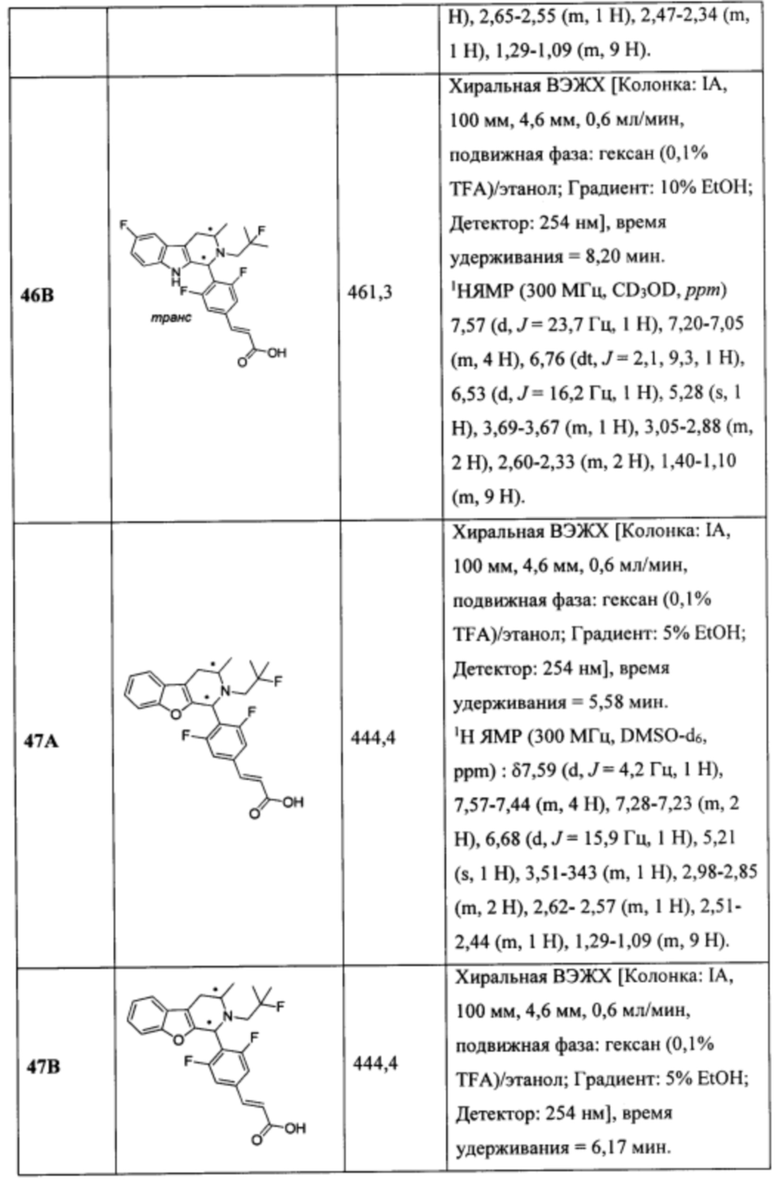
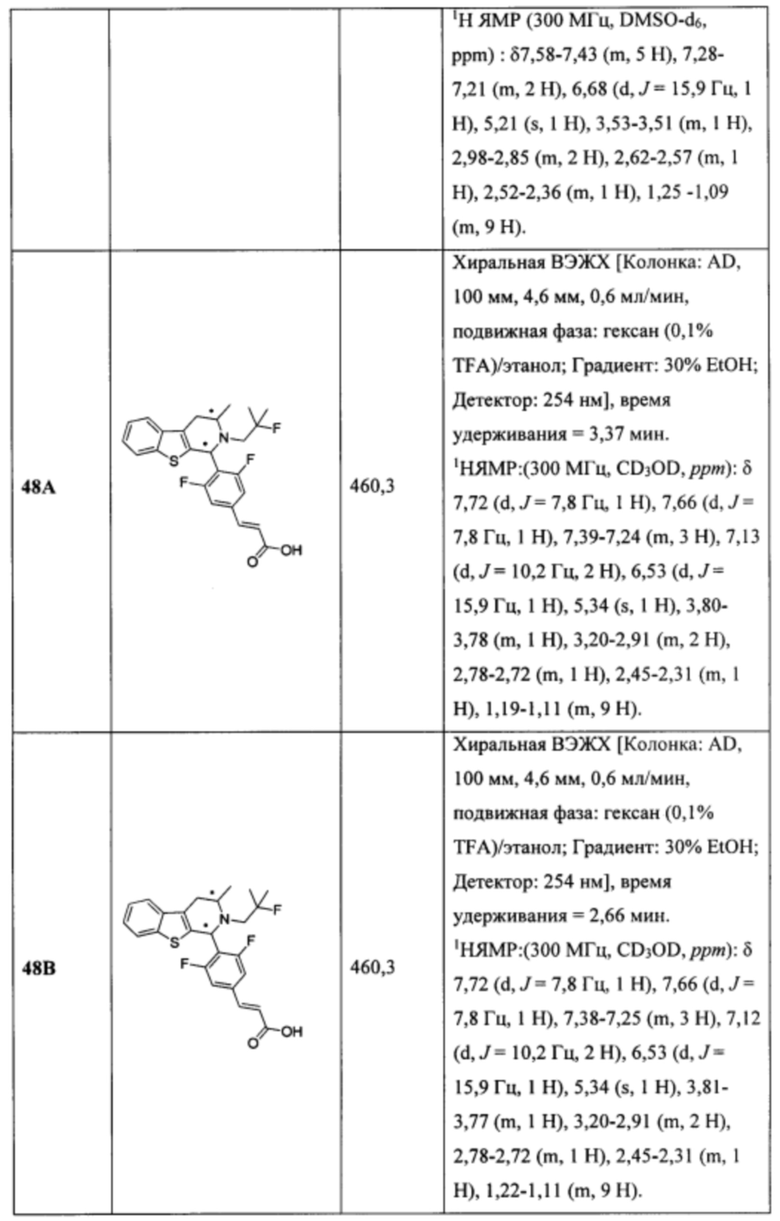
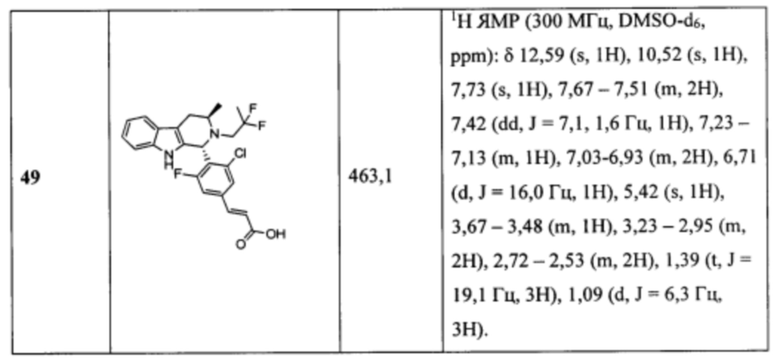
[00259] Биологический анализ примеров соединений, описанных в данном документе
[00260] Пример 9. Анализ деградации ЭР MCF-7
[00261] Уровень деградации ЭР за счет СИЭР, описанных в данном патенте, был проанализирован методом многопараметрического анализа клеток. Если описывать кратко, клетки MCF-7 ЭР-положительного рака молочной железы человека высевали в 96-луночные планшеты Grenier с плотностью 5000 клеток на лунку и выращивали в RPMI 1640 с добавлением 10% FBS (Gibco) при 37°С с 5% СО2 в течение 48 часов. Затем к клеткам добавляли 1 мкл сложного раствора (в ДМСО) для получения конечной концентрации 1 нМ на каждую лунку обработанных клеток. ДМСО с той же конечной концентрацией (%) на каждую лунку использовали для отрицательного контроля на каждой пластине. Через 4 часа или 24 часа обработки при 37°С с 5% СО2 клетки были фиксированными и проницаемыми. Среду из каждой лунки удаляли, клетки осторожно промывали 1X PBS в течение 5 минут, процедуру промывки повторяли 3 раза. Затем клетки фиксировали 4%-ным формальдегидом, свежеприготовленным в 1X PBS, при комнатной температуре в течение 20 минут, затем осторожно промывали 1X PBS 3 раза по 5 минут каждый раз. Аналитический планшет инкубировали 200 мкл 1XPBS, содержащего 0,2% Triton-X100, в течение 5 минут при комнатной температуре, затем клетки снова промывали 1XPBS 3 раза по 5 минут каждый раз. После этого клетки инкубировали с блокирующим буфером (1X PBS с 5% BSA) при комнатной температуре в течение 1 часа. Для иммуноокрашивания удаляли блокирующий буфер и в каждую лунку добавляли первичное анти-ЭР антитело (ER1D5, Santa Cruz), разбавленное в блокирующем буфере (1:400), клетки инкубировали на протяжении ночи при 4°С. На следующий день клетки промывали 1X PBS 3 раза по 5 минут каждый раз. Вторичное антитело, меченое фторхромом (козье анти-мышиное антитело IgG, конъюгат Alexa Fluor 488, ThermoFisher, Cat #: A-11001), разбавленное в 1% BSA в 1X PBS (1:1000), добавляли в каждую лунку и инкубировали с клетками в течение 45 минут при 37°С во влажной среде в темноте. Клетки промывали 1X PBS 3 раза по 5 минут каждый раз. Клетки инкубировали DAPI (Beyotime, 1 мкг/мл) в течение 10 минут и промывали 1X PBS 3 раза по 5 минут каждый раз. Для многопараметрического анализа данные планшета считывали на Cellomics ArrayScan™ XTI High Content Platform (ASN00002P) с возбуждением при 485 нм, данные изображений собирали при минимальном количестве 1000 клеток на лунку. Индуцированную СИЭР деградацию ЭР в клетках MCF-7 измеряли с использованием отрицательного контроля ДМСО в качестве основного метода.
[00262]
[00263]
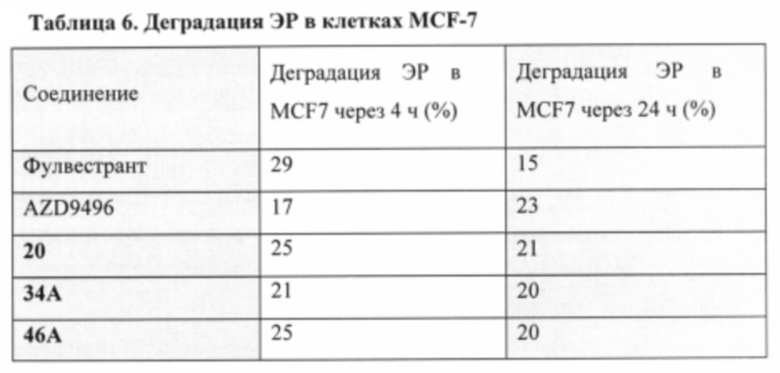
[00264] Пример 10. Изучение роста клетки MCF-7
[00265] Активность соединения оценивали с использованием люминесцентного анализа жизнеспособности клеток CellTiter-Glo (Promega #G7572) в клеточной линии рака молочной железы MCF-7. Клетки, выращенные в логарифмической фазе, трипсинизировали, сеяли в 96-луночный планшет для культивирования клеток при плотности 2×103 на лунку и инкубировали на протяжении ночи при 37°С с 5% СО2 в камере для увлажненной культуры. На следующий день соединения готовили в 100% ДМСО, серийно разбавляли и добавляли в клетки в следующих конечных концентрациях: 316, 100, 31,6, 10, 3,16, 1, 0,32, 0,1, 0,03, 0,01, 0,003 и 0,001 нМ. Для контроля в контрольные лунки в каждом планшете добавляли контрольный раствор носителя ДМСО такого же объема и концентрации. Клетки инкубировали с соединениями в культуральной камере при 37°С в течение 6 дней. Для определения жизнеспособности клеток использовали набор Celltiter-glo от компании Promega в соответствии с инструкцией производителя. Если описывать кратко, в каждую лунку добавляли 50 мкл реагента Celltiter-glo, планшет (покрытый алюминиевой фольгой) осторожно покачивали в течение 10 минут, чтобы вызвать лизис клеток при комнатной температуре. Люминесценцию измеряли с помощью считывателя SPECTRAmax i3. Ингибирование роста клеток IC50 рассчитывали с использованием программного обеспечения GraphPad Prism V5.0. % ингибирования = (1-(максимальный сигнал/минимальный сигнал))*100%.
[00266]
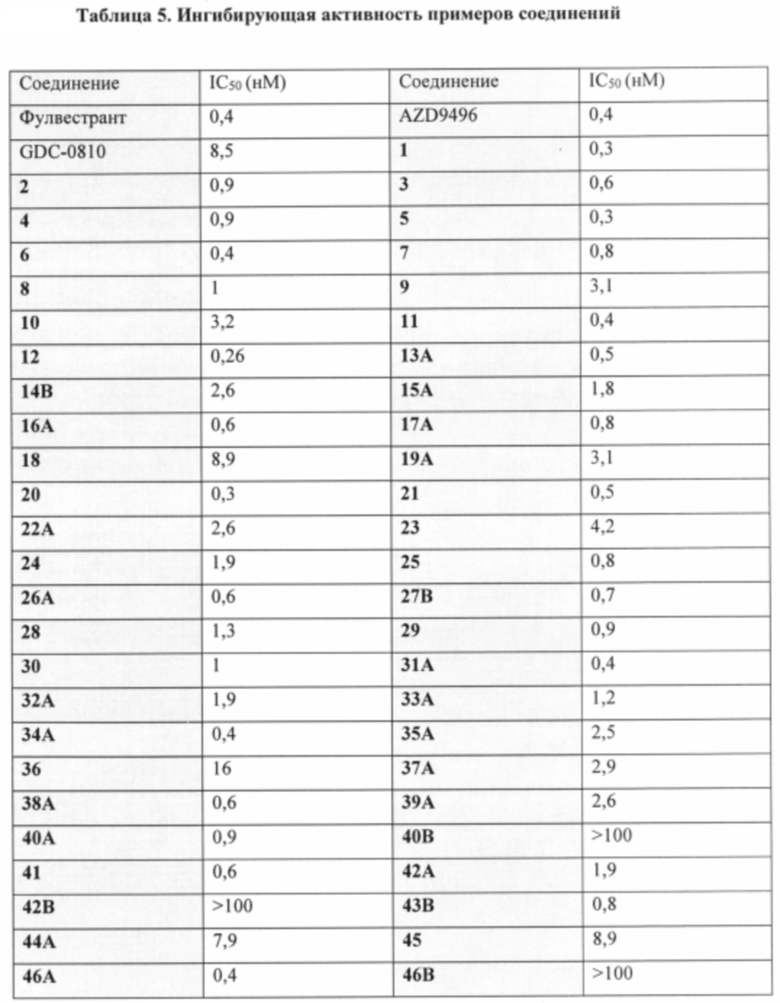

[00267] Пример 11. Исследование клиренса гепатоцитов человека
[00268] Клиренс гепатоцитов in vitro соединения, описанного в данном документе, изучали с использованием объединенных гепатоцитов человека, полученных от BioreclamationIVT (Westbury, NY, Cat # X008001, Lot # TQJ). Анализ выполняли в соответствии с инструкцией производителя. Если описывать кратко, 10 мМ исходного раствора испытываемого соединения и положительного контроля (Verapamil) готовили в 100% ДМСО. Среда для оттаивания (50 мл), использованная в исследовании, содержала: 31 мл среды Williams Е (GIBCO Cat # 12551-032); 15 мл изотонического перколла (GE Healthcare Cat # 17-0891-09); 500 мкл 100XGlutaMax (GIBCO Cat # 35050); 750 мкл HEPES (GIBCO Cat # 15630-080); 2,5 мл FBS (Corning Cat №35-076-CVR); 50 мкл инсулина человека (GIBCO Cat # 12585-014) и 5 мкл дексаметазона (NICPBP). Инкубационная среда получена из среды Williams Е с добавлением 1xGlutaMax. Среду для оттаивания и дополнительную инкубационную среду (без сыворотки) перед применением помещали на водяную баню с температурой 37°С не менее чем на 15 минут. Исходные растворы соединения разбавляли до 100 мкМ путем соединения 198 мкл 50% ацетонитрила/50% воды и 2 мкл исходного раствора 10 мМ. Верапамил использовали в качестве положительного контроля в анализе. Флаконы с криоконсервированными гепатоцитами изымали из хранилища и оттаивали на водяной бане при 37°С, аккуратно встряхивая. Содержимое флакона выливали в 50 мл коническую трубку для оттаивания. Флаконы центрифугировали при 100 г в течение 10 минут при комнатной температуре. Оттаивающую среду удаляли, а гепатоциты повторно суспендировали в инкубационной среде без сыворотки с получением примерно 1,5×106 клеток/мл. Жизнеспособность и плотность гепатоцитов подсчитывали методом исключения трипанового синего, затем клетки разбавляли инкубационной средой без сыворотки до плотности жизнеспособных клеток 0,5×106 жизнеспособных клеток/мл. Затем часть гепатоцитов при 0,5×106 жизнеспособных клеток/мл кипятили в течение 5 минут перед добавлением в планшет в качестве отрицательного контроля для устранения ферментативной активности, так что наблюдалось небольшое обновление субстрата или отсутствие обновления. Гепатоциты после кипячения использовали для приготовления отрицательных образцов. Аликвоты 198 мкл гепатоцитов распределяли в каждую лунку 96-луночного планшета без покрытия. Планшет помещали в инкубатор на орбитальном шейкере при 500 об/мин примерно на 10 минут. Аликвоты 2 мкл 100 мкМ испытываемого соединения или положительного контроля добавляли в соответствующие лунки 96-луночного планшета без покрытия для начала реакции. Проводили два параллельных анализа. Планшет инкубировали в инкубаторе на орбитальном шейкере при скорости 500 об/мин в течение определенного времени. 25 мкл содержимого переносили и смешивали с 6 объемами (150 мкл) холодного ацетонитрила с IS (200 нМ имипрамина, 200 нМ лабеталола и 200 нМ диклофенака) для прекращения реакции в моменты времени 0, 15, 30, 60, 90 и 120 минут. Образцы центрифугировали при 3220 г в течение 25 минут, для анализа ЖК-МС/МС использовали аликвоты 150 мкл супернатантов. Все расчеты для анализа данных выполняли с помощью Microsoft Excel. Площади пиков определяли на экстрагированных ионных хроматограммах. Период полужизни in vitro (t1/2) исходного соединения определяли регрессионным анализом кривой зависимости процента исчезновения исходного соединения от времени. Период полужизни in vitro (in vitro t1/2) определяли по значению наклона: in vitro t1/2=0,693/k. Преобразование in vitro t1/2 (в мин) в масштабированный внутренний клиренс несвязанного препарата (масштабированный CLint несвязанного препарата, в мл/мин/кг) выполняли с использованием следующего уравнения (среднее значение повторных определений): масштабированный CLint несвязанного препарата = kV/N × коэффициент масштабирования, где V = объем инкубации (0,5 мл); N = количество гепатоцитов на лунку (0,25 × 106 клеток). Коэффициенты масштабирования для прогнозирования внутреннего клиренса in vivo с использованием гепатоцитов человека приведены ниже: масса печени (г печени/кг массы тела): 25,7; концентрация гепатоцитов (106 клеток/г печени): 99; коэффициент масштабирования: 2544,3.
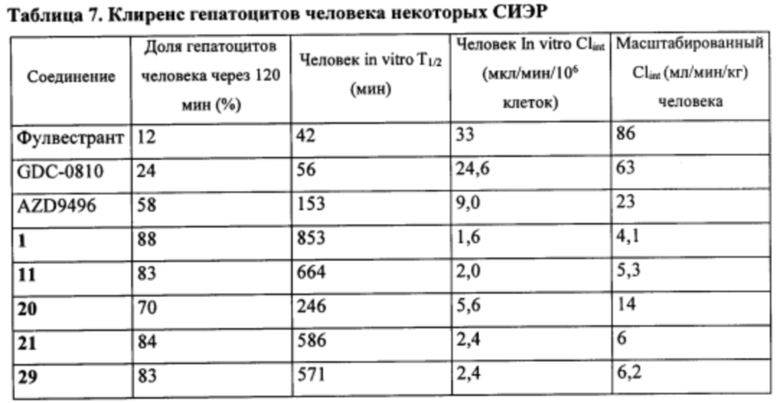
[00269] Пример 12. ФК исследования на мышах
[00270] ФК исследование на мышах PK (внутривенно 3 мг/кг массы тела и перорально 30 мг/кг массы тела) проводили с использованием самцов мышей CD1 (25-33 г), полученных от SLAC Laboratory Animal Co., LTD, Шанхай). Готовили соединение следующего состава: 5% ДМСО, 5% Солутол HS 15 и 9% HPBCD в воде. Для внутривенной (iv) дозы 3 мг/кг массы тела и пероральной (ро) дозы 30 мг/кг массы тела концентрация соединения составила 0,2 мг/мл и 1 мг/мл соответственно. Соединение готовили утром непосредственно перед введением дозы. Пероральное введение осуществляли с помощью перорального желудочного зонда в объеме 10 мл/кг, а внутривенное введение через хвостовую вену в объеме 5 мл/кг. Для каждого способа введения каждого соединения в каждой дозе использовали по три мыши. Последовательные пробы крови (30 мкл цельной крови в каждый момент времени) собирали в трубки K2 EDTA через лицевую вену в следующие моменты времени: 5 минут (только при внутривенном введении), 30 минут, 1, 2, 4, 6, 8, 12 и 24 часа. Для каждого собранного образца крови 20 мкл образца крови немедленно отбирали и тщательно перемешивали с 60 мкл воды в 96-луночном планшете (цельная кровь : вода = 1:3 об./об.). Разведенные образцы крови до проведения анализа хранили в морозильнике при -80°С.Для анализа добавляли аликвоту 20 мкл образца с 200 мкл IS (Glipizide, 100 нг/мл) в ACN. Смесь перемешивали на вортексе в течение 2 минут и центрифугировали при 5800 об/мин в течение 10 мин. Аликвоту 2 мкл супернатанта вводили для анализа ЖК-МС/МС. Для калибровочной кривой использовали соединение в количестве 2,0-3000 нг/мл в разбавленной крови мыши линии CD1. Полученные фармакокинетические данные приведены в следующей таблице:
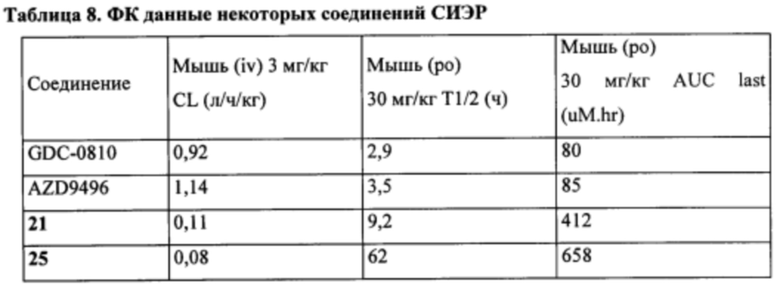
[00271] Пример 13. Исследование эффективности лечения ксенотрансплантата рака молочной железы человека xMCF-7 на мышах
[00272] Для исследования эффективности in vivo соединений СИЭР, описанных в данной заявке, самкам голых мышей инокулировали клетки ЭР-положительного рака молочной железы человека xMCF-7. Клетки xMCF-7 получали из опухоли MCF-7 (АТСС), выросшей у голой мыши. Если описывать кратко, самок мышей balb/c (возраст 6-7 недель) сначала инокулировали подкожно в спину эстрогеном в таблетках (0,5 мг, высвобождение 60 дней, от Innovative Research of America, Cat # SE-121). Через два дня каждой мыши инокулировали 5000000 клеток xMCF-7, полученных в виде 0,2 мл клеточной суспензии в смеси 1:1 MEM от Eagle для выращивания культуральной среды и Matrigel (Corning Cat №354234) для каждой инъекции. После того, как размер опухоли достигал примерно 235 мм3, мышей с ксенотрансплантатом опухоли xMCF-7 рандомизировали в группы по 10 мышей и начинали медикаментозную терапию. Каждое соединение готовили в дозирующем носителе (5% ДМСО, 5% Solutol HS15 и 10% HPBCD в воде) и вводили перорально 5 мг/кг или 30 мг/кг один раз в день в течение 28 дней, за исключением того, что фулвестрант готовили в арахисовом масле и вводили по 250 мг/кг подкожно один раз в день в течение 28 дней. В данном исследовании в результате медикаментозной терапии наблюдалось почти полное ингибирование роста опухоли, причем соединение 25 было более эффективным in vivo, чем фулвестрант, GDC-0810 и AZD9496 (Фигура 1).
[00273] В другом исследовании xMCF-7 лечение начинали, когда опухоль достигала примерно 250 мм3. Каждый препарат вводили по 2 мг/кг перорально один раз в день в течение 28 дней. Было обнаружено значительное ингибирование роста опухоли и регрессия опухоли, соединения 12, 21 и 25 были более эффективными, чем AZD9496 (Фигура 2).
[00274] Пример 14: Комбинация соединения СИЭР 25 с ингибитором CDK4/6 палбоциклибом на модели ксенотрансплантата xMCF-7.
[00275] Ингибитор CDK4/6, такой как палбоциклиб, одобрен для ЭР-положительного, Her2-отрицательного метастатического рака молочной железы. Для исследования возможности комбинации СИЭР и ингибитора CDK4 еще больше повысить эффективность лечения ЭР-положительного рака молочной железы проводили испытание соединения 25 СИЭР в комбинации с ингибитором CDK4/6 палбоциклибом на модели ксенотрансплантата рака молочной железы человека xMCF-7. В этом исследовании, когда опухоль xMCF-7 достигала примерно 250 мм3, соединение 25 вводили перорально один раз в день в течение 28 дней, палбоциклиб вводили перорально 50 мг/кг, один раз в день в течение 14 дней. Как показано на Фигуре 3, комбинация палбоциклиба и соединения 25 обеспечивает лучшую регрессию роста опухоли, чем палбоциклиб или соединение 25 при использовании по отдельности.
Эквиваленты и объем изобретения
[00276] В формуле изобретения формы единственного числа могут означать один или более одного, если не указано иное или если из контекста явно не следует иное. Пункты формулы изобретения или описания, которые включают «или» между одним или более элементами группы, считаются выполненными, если один, более одного или все члены группы присутствуют, использованы или иным образом относятся к данному продукту или процессу, если не указано иное или иное не следует из контекста. Изобретение включает варианты реализации, в которых ровно один элемент группы присутствует, использован или иным образом относится к данному продукту или процессу. Изобретение включает варианты реализации, в которых более чем один или все элементы группы присутствуют, использованы или иным образом относятся к данному продукту или процессу.
[00277] Кроме того, изобретение охватывает все варианты, комбинации и преобразования, в которых одно или более ограничений, элементов, пунктов, описательных терминов в одном или более пунктов формулы изобретения представлены в другом пункте формулы изобретения. Например, любой пункт, зависимый от другого пункта, может быть изменен для включения одного или более ограничений, содержащихся в любом другом пункте, зависимом от того же основного пункта формулы изобретения. Если элементы присутствуют в виде перечисления, например, в формате группы Маркуша, то каждая подгруппа элементов считается также раскрытой, и любой элемент (элементы) может быть удален из группы. Следует понимать, что в целом, если указано, что изобретение или аспекты изобретения включают конкретные элементы и/или особенности, то определенные варианты реализации изобретения или аспекты изобретения состоят или по существу состоят из таких элементов и/или особенностей. С целью упрощения такие варианты реализации не представлены конкретно в тех же выражениях в настоящем документе. Следует также иметь в виду, что термины «включающий» и «содержащий» подразумеваются как открытые и допускают включение дополнительных элементов или стадий. Указанные диапазоны включают предельные значения. Кроме того, если не указано иное или если иное не следует из контекста и понятно специалистам в данной области, значения, представленные в виде диапазонов, могут подразумевать любое конкретное значение или поддиапазон в пределах указанных диапазонов в других вариантах реализации изобретения до десятой части единицы нижнего предела диапазона, если из контекста явно не следует иное.
[00278] В данной заявке приведены ссылки на различные выданные патенты, опубликованные патентные заявки, журнальные статьи и другие публикации, каждая из которых включена в настоящее описание посредством ссылки. В случае противоречий между любыми включенными ссылками и настоящим описанием изобретения приоритет имеет описание изобретения. Кроме того, любой конкретный вариант реализации настоящего изобретения, который относится к предшествующему уровню техники, может быть в явной форме исключен из любого одного или более пунктов формулы изобретения. Такие варианты реализации считаются известными специалистам в данной области, поэтому их можно исключить, даже если исключение явно не выражено в настоящем описании. Любой конкретный вариант реализации настоящего изобретения может быть исключен из любого пункта формулы изобретения по любой причине независимо от того, относится ли он к предшествующему уровню техники.
[00279] Многие эквиваленты конкретных вариантов реализации, описанных в данном документе, понятны специалистам в данной области техники или могут быть установлены ими в результате не более чем стандартного проведения экспериментов. Предполагается, что объем вариантов реализации настоящего изобретения, описанных в данном документе, не ограничен приведенным выше описанием, а скорее соответствует описанию в прилагаемой формуле изобретения. Специалистам в данной области техники понятно, что различные изменения и модификации данного описания могут быть выполнены без отклонения от сущности или объема настоящего изобретения, как определено в следующей далее формуле изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, ЗАМЕЩЕННЫЕ В ПОЛОЖЕНИИ 10 ЦИКЛИЧЕСКОЙ ГРУППОЙ, ДЛЯ ИСПОЛЬЗОВАНИЯ ПРИ ЛЕЧЕНИИ РАССТРОЙСТВ ЦНС | 2019 |
|
RU2796006C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ, ИХ КОМПОЗИЦИИ И ПРИМЕНЕНИЕ | 2014 |
|
RU2696585C2 |
| ДИГИДРОПТЕРИДИНОНОВЫЕ ПРОИЗВОДНЫЕ И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2673944C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2808166C2 |
| НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2684103C2 |
| ЦИАНОТИЕНОТРИАЗОЛОДИАЗЕПИНЫ И ПУТИ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2750164C2 |
| ПРОИЗВОДНЫЕ ПОЛИМИКСИНА И ИХ ПРИМЕНЕНИЕ В КОМБИНИРОВАННОЙ ТЕРАПИИ СОВМЕСТНО С РАЗЛИЧНЫМИ АНТИБИОТИКАМИ | 2015 |
|
RU2740190C2 |
| 19-НОР C3, 3-ДИЗАМЕЩЕННЫЕ C21-N-ПИРАЗОЛИЛЬНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2675855C2 |
| 19-НОР НЕЙРОАКТИВНЫЕ СТЕРОИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2014 |
|
RU2700264C2 |
| ОКСИСТЕРОЛЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2744267C2 |
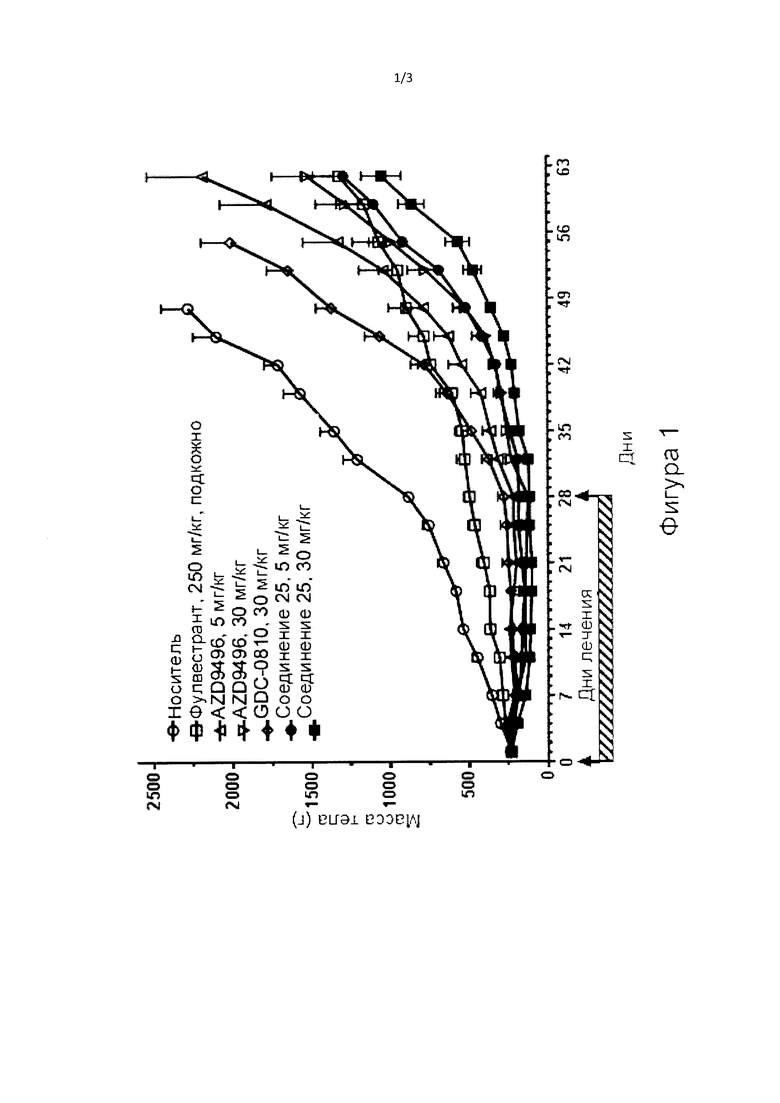
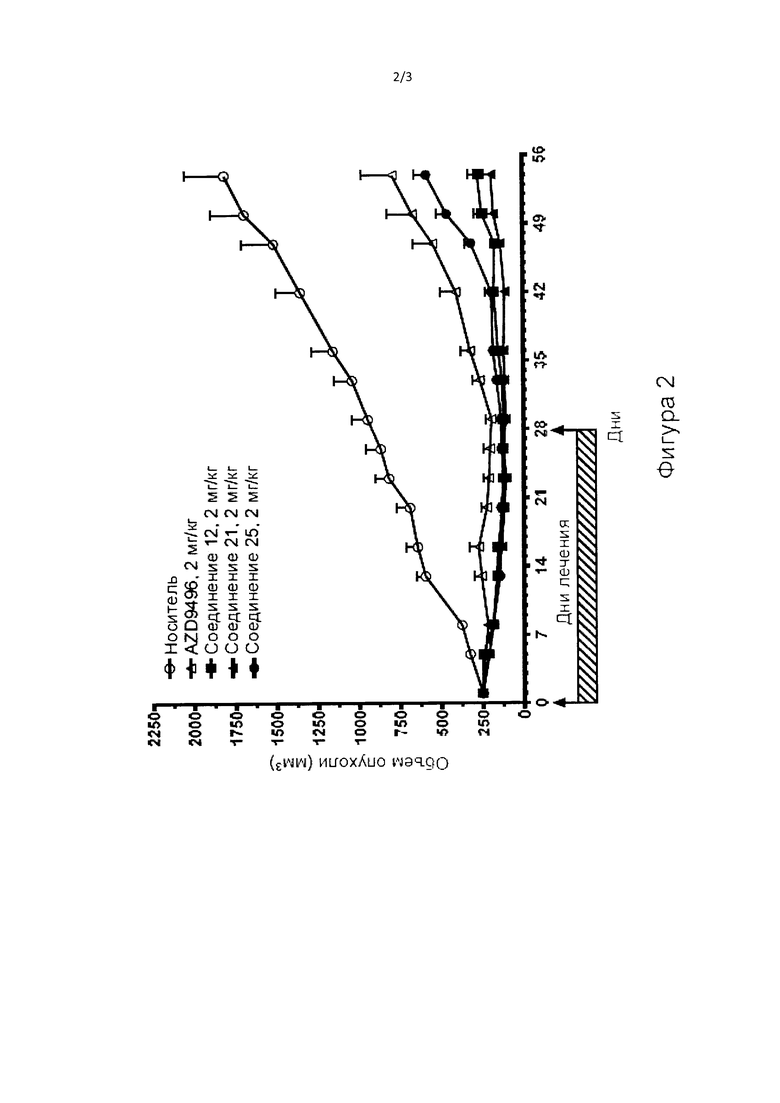
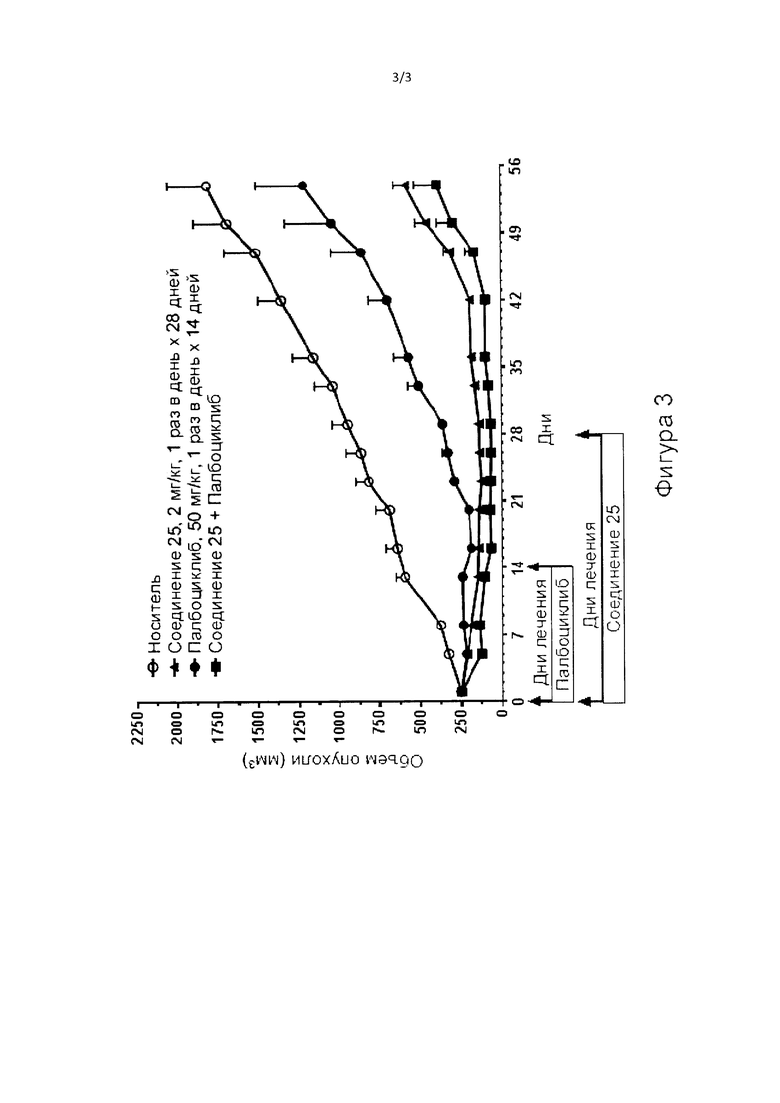
Изобретение относится к соединениям формул (I) и (II) и их фармацевтически приемлемым солям, обладающим свойствами селективных ингибиторов эстрогеновых рецепторов. В формуле (I) A представляет собой –CH= или –N= в зависимости от валентности; W представляет собой –NH– или –O–; a равно 1; n равно 1, 2, 3 или 4; каждый R1 независимо представляет собой водород, F, Cl, незамещенный C1-6 алкил, -CF3, -ORA или -CN; R2 представляет собой водород, незамещенный C1-6 алкил или CF3; R3 представляет собой водород, галоген или незамещенный C1-6 алкил; R4 представляет собой водород, галоген или незамещенный C1-6 алкил; R5 представляет собой хлор; R6 представляет собой фтор или хлор; R7 представляет собой –CH2F; RA представляет собой водород или незамещенный C1-6 алкил. В формуле (II) A представляет собой –CH= или –N= в зависимости от валентности; W представляет собой –NH–, –O– или –S–; a равно 1; каждый R1 независимо представляет собой водород, F, Cl, –CF3, незамещенный C1-6 алкил, –ORA или –CN; R2 представляет собой водород, незамещенный C1-6 алкил или –CF3; R3 представляет собой водород, F или незамещенный C1-6 алкил; R4 представляет собой водород, F или незамещенный C1-6 алкил, или R3 и R4 взятые вместе с промежуточными атомами образуют незамещенный циклопропил; R8 представляет собой водород, галоген или метил; RA1 представляет собой незамещенный C1-6 алкил, хлор или фтор; RA2 представляет собой незамещенный C1-6 алкил, хлор или фтор, при этом: (i) RA1 или RA2 представляет собой хлор или (ii) оба RA1 и RA2 представляют собой хлор; RA представляет собой водород или незамещенный C1-6 алкил. Изобретение также относится к фармацевтической композиции, содержащей эффективное количество соединений формул (I) или (II) или их фармацевтически приемлемых солей и фармацевтически приемлемое вспомогательное вещество. Описывается также способ лечения пролиферативного заболевания, связанного с активностью эстрогеновых рецепторов, включающий введение субъекту, нуждающемуся в лечении, эффективного количества фармацевтической композиции изобретения. 4 н. и 14 з.п. ф-лы, 3 ил., 8 табл., 14 пр.
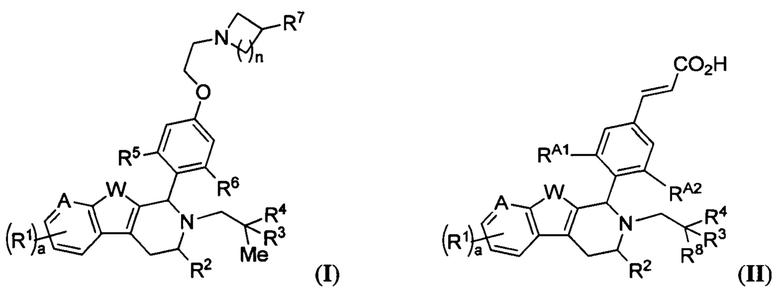
1. Соединение формулы (I)
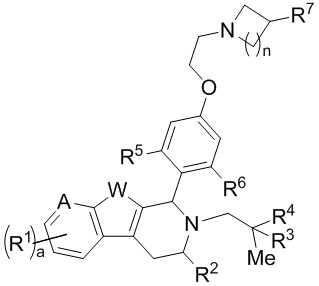 (I)
(I)
или фармацевтически приемлемая соль указанного соединения,
где:
A представляет собой –CH= или –N= в зависимости от валентности;
W представляет собой –NH– или –O–;
a равно 1;
n равно 1, 2, 3 или 4;
каждый R1 независимо представляет собой водород, F, Cl, незамещенный C1-6 алкил, -CF3, -ORA или -CN;
R2 представляет собой водород, незамещенный C1-6 алкил или CF3;
R3 представляет собой водород, галоген или незамещенный C1-6 алкил;
R4 представляет собой водород, галоген или незамещенный C1-6 алкил;
R5 представляет собой хлор;
R6 представляет собой фтор или хлор;
R7 представляет собой –CH2F;
RA представляет собой водород или незамещенный C1-6 алкил.
2. Соединение по п.1, отличающееся тем, что соединение представляет собой соединение формулы (IA)
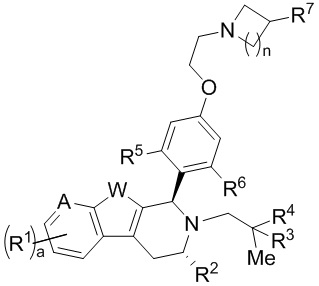 (IA)
(IA)
или фармацевтически приемлемую соль указанного соединения, где A, W, a, n, R1-R7 и RA имеют значения, указанные в п.1.
3. Соединение по любому из пп.1, 2, отличающееся тем, что соединение представляет собой соединение формулы
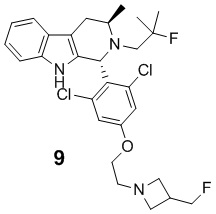 ,
, 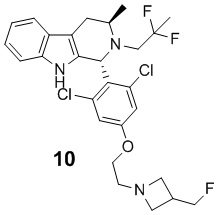 ,
, 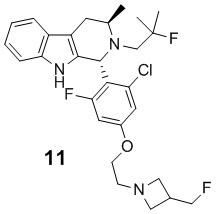 ,
, 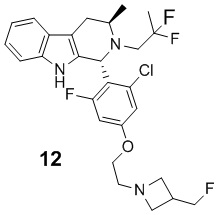 ,
, 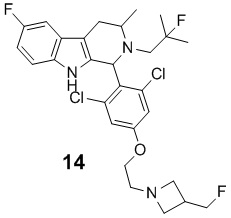 ,
, 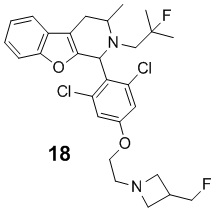
или фармацевтически приемлемую соль указанного соединения.
4. Соединение формулы (II)
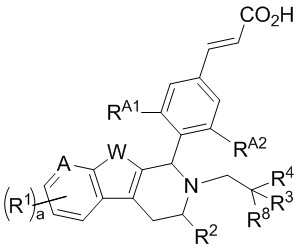 (II)
(II)
или фармацевтически приемлемая соль указанного соединения,
где:
A представляет собой –CH= или –N= в зависимости от валентности;
W представляет собой –NH–, –O– или –S–;
a равно 1;
каждый R1 независимо представляет собой водород, F, Cl, –CF3, незамещенный C1-6 алкил, –ORA или –CN;
R2 представляет собой водород, незамещенный C1-6 алкил или –CF3;
R3 представляет собой водород, F или незамещенный C1-6 алкил;
R4 представляет собой водород, F или незамещенный C1-6 алкил, или R3 и R4 взятые вместе с промежуточными атомами образуют незамещенный циклопропил;
R8 представляет собой водород, галоген или метил;
RA1 представляет собой незамещенный C1-6 алкил, хлор или фтор;
RA2 представляет собой незамещенный C1-6 алкил, хлор или фтор, при этом: (i) RA1 или RA2 представляет собой хлор или (ii) оба RA1 и RA2 представляют собой хлор;
RA представляет собой водород или незамещенный C1-6 алкил.
5. Соединение по п.4, отличающееся тем, что соединение представляет собой соединение формулы (IIA)
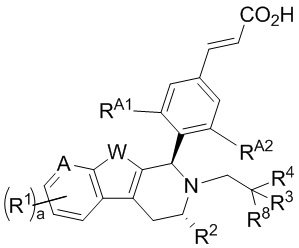 (IIA)
(IIA)
или фармацевтически приемлемую соль указанного соединения, где A, W, a, R1-R4, R8, RA1, RA2 и RA имеют значения, указанные в п.4.
6. Соединение по п.4 или 5 или фармацевтически приемлемая соль указанного соединения, где А представляет собой -СН=.
7. Соединение по любому из пп.4-6 или фармацевтически приемлемая соль указанного соединения, где W представляет собой -NH-.
8. Соединение по любому из пп.4-7 или фармацевтически приемлемая соль указанного соединения, где R1 представляет собой водород.
9. Соединение по любому из пп.4-8 или фармацевтически приемлемая соль указанного соединения, где R2 представляет собой незамещенный C1-6 алкил или -CF3.
10. Соединение по п.9 или фармацевтически приемлемая соль указанного соединения, где R2 представляет собой метил или этил.
11. Соединение по любому из пп.4-10 или фармацевтически приемлемая соль указанного соединения, где по меньшей мере один из R3, R4, R8 независимо выбран из группы, состоящей из водорода, фтора и метила.
12. Соединение по любому из пп.4-11 или фармацевтически приемлемая соль указанного соединения, где по меньшей мере один из RA1 и RA2 представляет собой хлор, а другой из RA1 и RA2 представляет собой хлор, F или метил.
13. Соединение по п.4, отличающееся тем, что соединение представляет собой соединение формулы
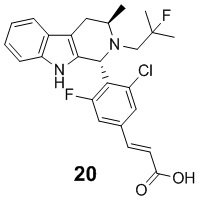 ,
, 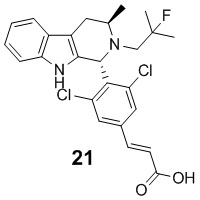 ,
, 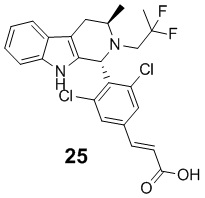 ,
, 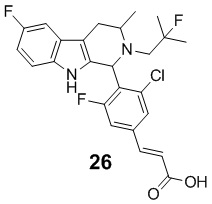 ,
, 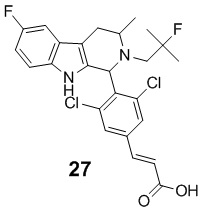 ,
, 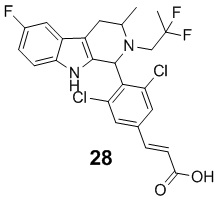 ,
, 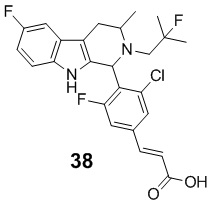 ,
, 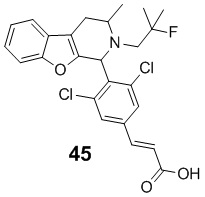 ,
,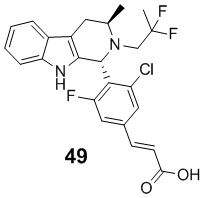
или фармацевтически приемлемую соль указанного соединения.
14. Соединение по любому из пп.4-12 или фармацевтически приемлемая соль указанного соединения, где RA1 представляет собой хлор и RA2 представляет собой хлор.
15. Фармацевтическая композиция, обладающая свойствами селективного ингибитора эстрогеновых рецепторов (ЭР), содержащая эффективное количество соединения по любому из пп.1-14 или его фармацевтически приемлемую соль и фармацевтически приемлемое вспомогательное вещество.
16. Способ лечения пролиферативного заболевания, связанного с активностью ЭР, включающий введение субъекту, нуждающемуся в лечении, эффективного количества фармацевтической композиции по п.15.
17. Способ по п.16, отличающийся тем, что пролиферативное заболевание представляет собой рак, связанный с активностью ЭР.
18. Способ по п.17, отличающийся тем, что рак является ЭР-положительным раком молочной железы.
| С.D.SAVI et al., Optimization of a Novel Binding Motif to (E)-3-(3,5-Difluoro-4-((1R,3R)-2-(2-fluoro-2-methylpropyl)-3-methyl- 2,3,4,9-tetrahydro-1H-pyrido[3,4-b]indol-1-yl)phenyl)acrylic Acid (AZD9496), a Potent and Orally Bioavailable Selective Estrogen Receptor Downregulator and Antagonist, J.MED.CHEM., 2015, V.58, No.20, p.8128-8140 | |||
| US |
Авторы
Даты
2020-10-19—Публикация
2017-02-03—Подача