Изобретение относится к экспериментальной медицине, а именно к онкологии и иммунологии, в частности к фотодинамической терапии (ФДТ), в том числе для ранней диагностики, мониторинга течения заболевания и оценки эффективности лечения, дополнительного выявления иммунологической составляющей фотодинамического воздействия, а также прогнозирования исхода заболевания по исследованию лейкограммы периферической крови и динамики изменения интегральных медицинских показателей (ИМП).
ФДТ – локо-регионарный органосохраняющий метод лечения, открывающий широкие возможности воздействия на новообразования. При проведении ФДТ сначала вводится фотосенсибилизатор (ФС), избирательно накапливающийся в злокачественных новообразованиях. Затем опухоль подвергается дистанционному облучению лазерным светом определенной длины волны, в соответствии со спектром возбуждения ФС. В результате облучения происходит фотохимическая реакция, где ФС фактически играет роль катализатора, и происходит образование активных форм кислорода (основным из которых является синглетный кислород) и различных радикалов, которые являются цитотоксическими агентами и вызывают разрушение клеток опухоли. Определенная последовательность фотохимических и фотобиологических реакций необратимо повреждает опухоли и оказывает деструкцию кровеносных сосудов, питающих опухоль. Первым ответом на ФДТ является вазоконстрикция артериол и тромбоз венул. Наиболее чувствительными к фотовоздействию являются ткани, где есть новообразованные капиллярные сосуды, а поражения мембраны связаны с водной доставкой (водорастворимые ФС). Изменения метаболизма и некроз эндотелия после ФДТ, приводит к сепарации, активации тромбоза и полиморфноядерных лейкоцитов, также к повышению проницаемости сосудов и, как следствие, к тромбогенному эффекту и нарушению микроциркуляции. ФДТ, кроме того, является «пусковым» механизмом в активации противоопухолевого иммунного ответа, связанного с усилением процесса гибели опухолевых клеток, а так же развития острого воспалительного процесса. К этим молекулам мигрируют лейкоциты и макрофаги, которые ликвидируют погибшие клетки опухоли. ФДТ действует, как локальная травма для биообъекта, вызывая хемотаксис нейтрофиллов и компонентов коплемента. В итоге опухолевая ткань инфильтрируется нейтрофилами, под влиянием целого ряда цитокинов запускается множество иммунных реакций и стимулируется неспецифический и специфический иммунный ответ. С целью оценки состояния здоровья пациента, выявления адаптационного потенциала организма (АПО) и оценки эффективности лечения, а также ранней диагностики и определения тяжести течения заболевания, развития эндогенной интоксикации (ЭИ) и выявления прогностических рисков используются показатели лейкограммы периферической крови в сочетании с динамикой изменений интегральных медицинских показателей (ИМП). ИМП обладают высокой информативностью при онкологических заболеваниях. Исследование проведено на меланоме В-16 мышей. Меланома одна из самых агрессивных злокачественных неоплазий, а методы лечения не всегда оказываются эффективными. Перспективным представляется использование ФДТ. В качестве ФС для ФДТ использовали новый отечественный препарат "Фоторан Е6", содержащий трисмеглуминовую соль хлорина е6 в комплексе с поливинилпирролидоном (ПВП, марка К-17), он накапливается в опухоли и при локальном действии лазерного излучения с длиной волны в диапазоне 660–670 нм обеспечивает фотосенсибилизирующий эффект. Активной субстанцией Фоторана является хлорин е6, который относится к природным порфиринам и выделяется из водоросли Spirullina platensis. Для улучшения селективности и повышения фотоактивности их соединили с молекулами-переносчиками (гидрофильный полимер ПВП).
Известен способ оценки противоопухолевой эффективности ФДТ по рекомендации Фармкомитета по предклинической апробации препаратов:
- по коэффициенту абсолютного прироста опухоли (К) у особей с продолженным ростом неоплазий;
- по частичной регрессии опухоли (ЧР,%) – уменьшение объема опухоли на ≥50% от исходного объема новообразования; по торможению роста опухоли (ТРО,%) по сравнению с контролем;
- по полной регрессии опухоли (ПР,%) – отсутствие видимой и пальпируемой опухоли;
- по средней продолжительности жизни (СПЖ) и увеличению продолжительности жизни (УПЖ,%) по сравнению с контролем и по критерию излеченности на 90 сутки после ФДТ (отсутствие признаков рецидивирования опухоли в течение 3-х месяцев после лечения).
Однако, из-за гетерогенности опухоли, предсказать эффективность ФДТ затруднительно, один и тот же тип опухоли реагирует по-разному на одно и тоже проводимое лечение.
Наблюдаемая тенденция изменений показателей гемограммы и изменений лейкоцитарных индексов при злокачественном росте, говорят о пролиферативных процессах, недостаточности адаптационных реакций организма, нарушениях процессов регенерации элементов крови, отражая выраженность эндотоксикоза, который вызывает деструкцию и дегенерацию клеток крови, и резкое изменение течения иммунных реакций, нарастающих по мере распространения злокачественного процесса.
Также изученные гематологические индексы показали свою информативность в интегральной оценке эффективности терапии.
Техническим результатом заявленного способа является разработка оценки противоопухолевой эффективности ФДТ по исследованию лейкограммы периферической крови и по динамике изменений интегральных медицинских показателей (ИМП), а также прогноз дальнейшего течения заболевания, или его полного излечения.
Указанный технический результат при осуществлении изобретения достигается за счет того, что так же, как и в известном способе, проводят оценку по коэффициенту (К) абсолютного прироста опухоли у особей с продолженным ростом неоплазий; по частичной регрессии опухоли (ЧР,%) – уменьшение объема опухоли на ≥50% от исходного объема новообразования; по торможению роста опухоли (ТРО,%) по сравнению с контролем; по полной регрессии опухоли (ПР,%) – отсутствие видимой и пальпируемой опухоли; по средней продолжительности жизни (СПЖ) и увеличению продолжительности жизни (УПЖ,%) по сравнению с контролем и по критерию излеченности на 90 сутки после ФДТ.
Особенность заявляемого способа заключается в том, что дополнительно проводят оценку по исследованию лейкограммы периферической крови и динамики изменения интегральных медицинских показателей (ИМП), в следующем порядке:
- вычисляют объёмы опухолей по коэффициенту абсолютного прироста опухоли (К) по формуле (1):
 , (1)
, (1)
где
d1, d2, , d3, - три взаимно перпендикулярные диаметры опухоли,
V - объем опухоли в см3,
- рассчитывают коэффициент абсолютного прироста опухоли (К) по формуле (2):
 , (2)
, (2)
где
V0 - объем опухоли до воздействия,
Vt - объем опухоли на определенный срок наблюдения,
- по проценту животных в группе с полной регрессией (ПР%) опухоли K = -1,00;
- изучают процент соотношения и морфологических характеристик клеток периферической крови мышей путем микроскопирования и дифференциального подсчета лейкограммы периферической крови;
- проводят оценку воздействия ФДТ на периферическую кровь по интегральным медицинским показателям (ИМП): ИСЛК, ЛИ, ИСНЛ, ИСНМ, ИСЛМ;
- сравнивают среднюю продолжительность жизни животных в группе (СПЖ) и увеличению продолжительности жизни (УПЖ %) по сравнению с контролем. Значимый процент УПЖ опытных животных по сравнению с контролем должен составлять ≥50%.
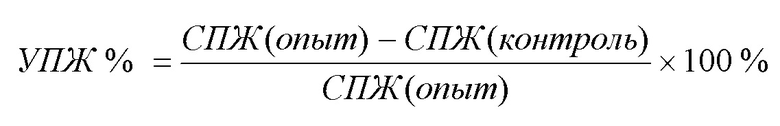 (3)
(3)
- проводят статистическую оценку результатов непараметрическими методами с использованием программ Statistica 6.0, используют U-критерий Манна–Уитни и Wilcoxon matched pairs test,
- и если различия между статистически значимыми показателями p<0,05 по сравнению с физиологической нормой, то данные свидетельствуют об эффективности проводимой терапии.
Предлагаемое решение является новым, т.к. в проанализированной авторами патентной и научно-медицинской литературе не найдено оценки противоопухолевой эффективности ФДТ по исследованию лейкограммы периферической крови и по динамике изменений интегральных медицинских показателей (ИМП).
Изобретение поясняется подробным описанием, лабораторными исследованиями и таблицами.
Способ осуществляют следующим образом.
Работа выполнена на 14 половозрелых самках мышей массой 20 г. Мыши F1 гибриды (CBA x C57 BL/6j) с перевитой под кожу в область бедра меланомой В16 Меланому перевивали в виде суспензии в объеме 0,10 - 0,15 мл. Штаммы перевиваемых опухолей были получены в ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России. Животные получены из питомника лабораторных животных ФГБУН НЦБМТ ФМБА России (филиал «Андреевка»), были здоровы, имели ветеринарный сертификат качества и состояния здоровья, и прошли 20-суточный карантин в виварии МРНЦ им. А.Ф. Цыба. Работа выполнена с соблюдением международных рекомендаций по проведению исследований с использованием лабораторных животных.
Эффективность фотодинамической терапии меланомы В-16 мышей с фотосенсибилизатором Фоторан Е6 оценивают следующим образом.
1. Вычисляют объёмы опухолей по коэффициенту абсолютного прироста опухоли (К) по формуле (1):
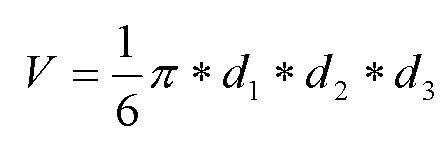 , (1)
, (1)
где
d1, d2, , d3, - три взаимно перпендикулярные диаметры опухоли,
V - объем опухоли в см3.
Коэффициент абсолютного прироста опухоли (К) рассчитывают по формуле (2):
 , (2)
, (2)
где
V0 - объем опухоли до воздействия,
Vt - объем опухоли на определенный срок наблюдения.
2. По проценту животных в группе с полной регрессией (ПР%) опухоли (K = -1,00). За полную регрессию опухоли принимают отсутствие видимой и пальпируемой опухоли.
3. По изучению процентного соотношения и морфологических характеристик клеток периферической крови мышей путем микроскопирования и дифференциального подсчета лейкограммы периферической крови. Кровь брали из хвостовой вены, мазок крови окрашивали по Паппенгейму (двухмоментная окраска).
4. Оценку воздействия ФДТ на периферическую кровь по интегральным медицинским показателям (ИМП) осуществляют следующим образом:
а) ИСЛК (нейтрофилы /лимфоциты + моноциты) – индекс сдвига лейкоцитов по Н.И. Яблучанскому;
б) ЛИ (лимфоциты / нейтрофилы) – лимфоцитарный индекс по Л.Х. Гаркави с соавт.;
в) ИСНЛ (нейтрофилы / лимфоциты) – лимфоцитарный индекс по формуле В.М. Угрюмова;
г) ИСНМ – индекс соотношения нейтрофилов и моноцитов (нейтрофилы/ моноциты);
д) ИСЛМ - индекс соотношения лимфоцитов и моноцитов (лимфоциты/ моноциты).
5. По средней продолжительности жизни животных в группе (СПЖ) и увеличению продолжительности жизни (УПЖ %) по сравнению с контролем. Значимый процент УПЖ опытных животных по сравнению с контролем должен составлять ≥50%.
 (3)
(3)
6. По критерию излеченности животных – отсутствие признаков рецидивирования опухоли в течение 3-х месяцев после лечения.
Статистическую оценку результатов проводят непараметрическими методами для групп (независимых и зависимых) с использованием программ Statistica 6.0. Параметры описательной статистики представлены в виде среднего арифметического значения и стандартной ошибки среднего (M±m); для оценки уровня значимости межгрупповых различий полученных показателей, используют U-критерий Манна–Уитни и Wilcoxon matched pairs test. Различия между показателями считают статистически значимыми при p<0,05.
Способ подтверждается лабораторными исследованиями.
В начале исследования взяты мазки периферической крови у интактных животных (физиологическая норма). Затем проводят перепассаж опухоли и, когда опухоль достигает диаметра 0,7 см (высота опухоли не больше 0,5 см), – берут мазки крови у мышей-опухоносителей на 14 сутки и этих особей разделили на две группы («Опыт» и «Контроль»).
Опытным животным-опухоленосителям проведен сеанс ФДТ. ФС вводили интраперитонеально в дозе 5,0 мг/кг. Через 90 минут после введения ФС облучали опухоль лазером. Для лазерного облучения использовали аппарат «Аткус-2» (ЗАО «Полупроводниковые приборы», Санкт-Петербург). Длина волны излучения 662 нм, плотность энергии (Е) – 150 Дж/см2, плотность мощности (Ps) – 0,25 Вт/см2, диаметр светового пятна – 1,0 см. Контрольные животные-опухоленосители без какого-либо воздействия.
На 5, 9, 12, 19 сутки после лечения и в контроле II проведены замеры опухолей и фиксация воздействия ФДТ в опыте.
Изучение противоопухолевой эффективности.
ФДТ.
В опыте через 5 суток после ФДТ в области облучения лазером наблюдался отек, и образовалась корочка некротизированной ткани и отсутствие видимой и пальпируемой опухоли. Полная регрессия опухоли сохранялась до 19 суток после ФДТ (Табл. 1).
В контрольной группе (контроль II) по всем срокам исследования наблюдался прогрессирующий рост опухоли (Табл. 1).
После 19 суток животные оставлены для дальнейшего наблюдения: определения СПЖ и УПЖ%; регистрации возможных рецидивов опухоли и определения процента излеченных животных на 90 сутки после ФДТ (Табл. 1, Табл. 2).
Таблица 1.
Показатели противоопухолевой эффективности ФДТ меланомы В16 мышей с интраперитонеальным введением Фоторана Е6 в дозе 5,0 мг/кг, при параметрах лазерного воздействия: Е – 150 Дж/см2, Ps – 0,25 Вт/см2

Примечание: (1) объем опухоли (V, см3); (2) коэффициент прироста опухоли у животных с продолженным ростом (К); (3) процент животных с полной регрессией опухоли (ПР); (4) – процент излеченных животных.
Таблица 2.
Увеличение продолжительности жизни мышей после ФДТ с интраперитонеальным введением Фоторана Е6 в дозе 5,0 мг/кг (параметры лазерного излучения: Е=150 Дж/см2, Ps=0,25 Вт/см2)

Примечание: * значимое увеличение продолжительности жизни по сравнению с контролем (УПЖ ≥ 50%).
Периферическая кровь.
I. Лейкограмма (Прил. 1, Табл. 3).
Интактные животные (физиологическая норма).
Мыши-опухоленосители (14 сутки после перепассажа).
На данный срок изменилось процентное соотношение клеток крови в лейкограмме по сравнению с физиологической нормой и появились морфологические нарушения в клетках. Хотя, масса опухоли была небольшой, наблюдалось увеличение количества сегментоядерных нейтрофилов, моноцитов и снизился процент лимфоцитов. Изменения достоверны по сравнению с физиологической нормой (p< 0.05). В крови увеличилось количество малых форм лимфоцитов с высоким ядерно-цитоплазматическим соотношением с цитоморфологическими признаками зрелых лимфоцитов. Появились морфологические изменения в клетках – фрагментоз и гиперсегментация ядра с-яд нейтрофилов.
Этих животных разделили на группы: «Контроль» и «Опыт».
Группа «Контроль».
На 19 сутки после перевивки опухоли по мере развития опухолевого процесса в периферической крови нейтрофилез (сдвиг лейкоцитарной формулы вправо – гиперсегментированные гранулоциты, уменьшение количества п-яд нейтрофилов), моноцитоз и лимфопения по сравнению с нормой (p< 0.05). Морфологические изменения в клетках аналогичны 14 суткам (Прил.1, Табл. 3).
На 26 сутки после перевивки меланомы в периферической крови усиление нейтрофилеза (также сдвиг вправо), моноцитоза и значительная лимфопения по сравнению с физиологической нормой (p< 0.05). На данный срок также отмечалось снижение количества базофилов. Морфологические изменения в клетках более многочисленны (анизоцитоз, фрагментоз и вакуолизация ядра с-яд, также обнаружены малосегментированные с-яд нейтрофилы; кариорексис лимфоцита; фрагментоз ядра моноцита; анизоцитоз и пойкилоцитоз эритроцитов. Лимфоциты средние, не было малых форм клеток.
На 33 сутки после перевивки в периферической крови нарастали изменения, уже не были обнаружены базофилы (p< 0.05) и п-яд нейтрофилы (p< 0.05) по сравнению с нормой, отмечалась еще большая нейтрофилия до 62,5% (p< 0.05), еще большая лимфопения до 26,5% (p< 0.05), моноцитоз до 11,0% (p< 0.05). Морфологические изменения в клетках аналогичны 26 суткам.
Значительное увеличение сегментоядерных нейтрофилов один из показателей развития опухолевого процесса. Лимфопения приводит к подавлению лимфоидного звена иммунитета, к снижению локальных иммунных реакций, отсутствию инактивации токсинов различного происхождения. С одной стороны это ведет к повышению риска инфекционных процессов, а с другой стороны к подавлению определенных лимфоидных популяций, что ведет к усилению процессов новообразования, а также такое снижение лимфоцитов плохой прогностический признак. На этом фоне, увеличенное количество моноцитов в течение месяца указывает на развитие патологического процесса. Отсутствие базофилов так же неблагоприятный признак, так как они участвуют в иммунологических реакциях немедленного или замедленного действия. Яркой чертой злокачественного процесса является изменение размеров клеток (анизоцитоз). Анизоцитоз отмечался у с-яд нейтрофилов и эритроцитов (полихроматофилы), а также пойкилоцитоз эритроцитов.
Проведенный опыт показал, что:
- на 5 сутки после ФДТ и 19 сутки после перепассажа у животных наблюдалась полная регрессия опухоли и некроз тканей в зоне облучения. Показатели крови мало чем отличались от Контроля на данный срок: увеличение с-яд нейтрофилов, моноцитов и снижение лимфоцитов, данные изменения показателей достоверно значимы (p< 0.05) по сравнению с физиологической нормой (Прил. 1, Табл.3). Морфологические изменения в клетках аналогичны 14 суткам (мыши-опухоленосители).
- на 12 сутки после ФДТ и 26 сутки после перепассажа и в отличие от «Контроля» началось снижение количества нейтрофилов, моноцитов, увеличение лимфоцитов. И, хотя, тенденция показателей крови кардинально отличалась от «Контроля», но еще достоверно отличалась и от физиологической нормы. Морфологические изменения в клетках не значительные (фрагментоз и гиперсегментация ядра с-яд нейтрофилов – сдвиг лейкоцитарной формулы вправо, фрагментоз ядра моноцита).
- на 19 сутки после ФДТ и 33 сутки после перевивки опухоли показатели периферической крови были уже в пределах физиологической нормы, кроме моноцитов, количество которых оставалось достоверно увеличенным. На данный срок показатели лейкограммы уже достоверно отличались от «Контроля». Морфологические изменения незначительные, еще сохранялся фрагментоз и гиперсегментация ядра с-яд нейтрофилов, отсутствие зернистости у базофилов.
Таким образом, по изучению процентного соотношения клеток и морфологических характеристик периферической крови мышей в опытной группе отмечен процесс восстановления нормальной картины крови на 19 сутки после терапии. Количество сегментоядерных нейтрофилов, лимфоцитов в пределах физиологической нормы, процент моноцитов снизился, но еще выше нормы. Показатели лейкограмы уже достоверно отличались от «Контроля» (p < 0,05). Морфологические нарушения в клетках незначительные.
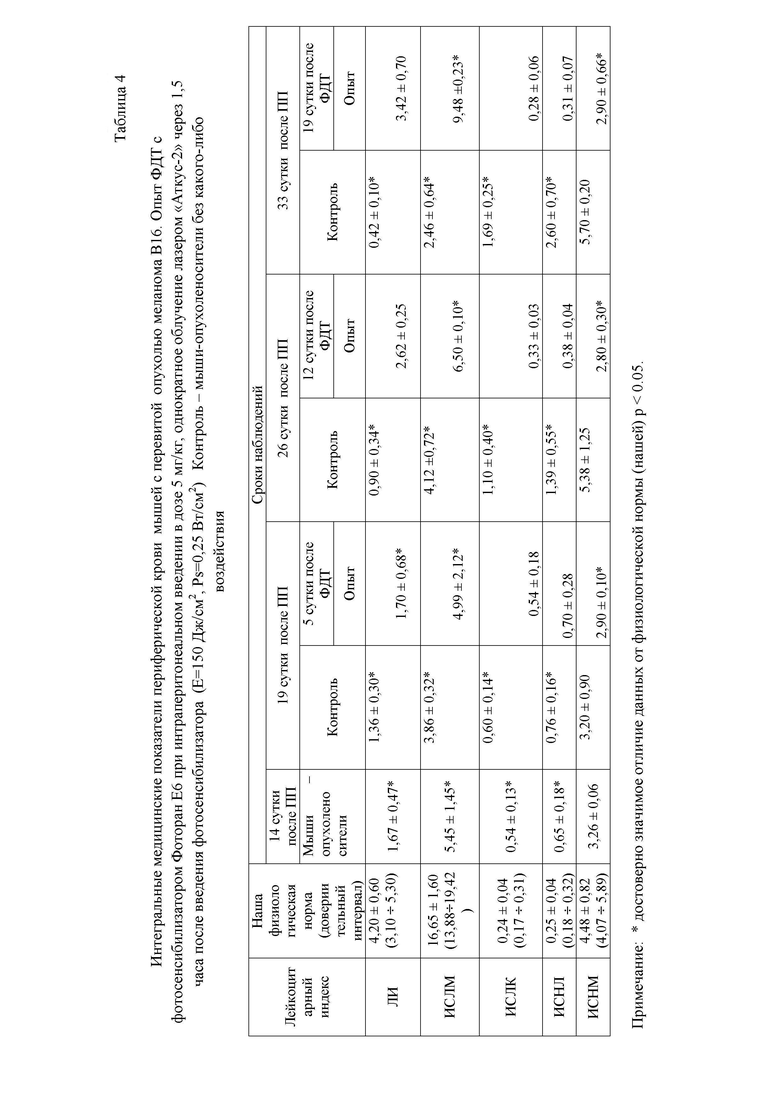
Лейкоцитарные индексы (Прил.2, Табл. 4).
ИМП обладают высокой информативностью при онкологических заболеваниях (ИСНЛ, ИСНМ, ИСЛН, ЛИ, а особенно ИСЛК).
При оценке состояния гематологических индексов у контрольных животных с меланомой В-16 отмечено достоверное снижение значений индексов неспецифической реактивности и уровня адаптации (ЛИ, ИСЛМ) и достоверное увеличение по сравнению с физиологической нормой индекса сдвига лейкоцитов крови и индекса иммунологической реактивности (ИСЛК, ИСНЛ). Данные индексы отражают соотношение клеток неспецифической и специфической защиты, тканевой деградации и уровня эндогенного токсикоза, которые прогрессировали по мере роста неоплазий. Также идет постепенное нарастание индекса ИСНМ. По изменению индекса можно судить о соотношении компонентов микрофагально-макрофагальной системы (возможно, это этап развития опухоли — избегание (escape)- она уже нечувствительна к активности иммунных клеток, мало того, обращает их активность себе на пользу . неоплазма растет, и растущее новообразование привлекает новые макрофаги, они перепрограммируются и вместо уничтожения усиливают злокачественный рост).
В опытной группе на 19 сутки после ФДТ отмечено увеличение значений индексов неспецифической реактивности и уровня адаптации (ЛИ, ИСЛМ) и нормальные величины индекса сдвига лейкоцитов крови и иммунологической реактивности (ИСЛК, ИСНЛ).
Изученные гематологические индексы показали свою информативность в интегральной оценке состояния животных с ростом меланомы (контроль), отражая выраженность эндотоксикоза, недостаточность адаптационных реакций организма, нарастающих по мере развития злокачественного процесса. И оценки эффективности лечения после ФДТ в опытной группе.
Полученные результаты показали, что Фоторан Е6 обладает высокой противоопухолевой эффективностью для ФДТ меланомы В16 мышей. Проведение ФДТ после введения ФС в дозе 5,0 мг/кг с параметрами лазерного воздействия (Е=150 Дж/см2; Ps=0,25 Вт/см2) позволяет достичь максимального ингибирующего эффекта. Восстановление нормальных показателей крови в опытной группе свидетельствуют об эффективности проводимой терапии, что подтверждается показателями лейкограммы и ИМП.
Наблюдаемая тенденция изменений показателей гемограммы и изменений лейкоцитарных индексов в контрольной группе, говорят о пролиферативных процессах, нарушениях процессов регенерации элементов крови, о тяжелых интоксикациях, которые вызывают деструкцию и дегенерацию клеток крови, резкое изменение течения иммунных реакций, нарастающих по мере распространения злокачественного процесса. Данные по показателям гемограммы и ИМП подтверждаются исследованиями СПЖ, УПЖ и критерием излечиваемости животных при наблюдении за ними на протяжении 90 суток. В опытной группе – 100% излечение, в контрольной – прогрессирующий рост и гибель животных на 38,6 ± 3,4 сутки.
Разработанный способ позволит произвести оценку контроля противоопухолевой эффективности по показателям лейкограммы в сочетании с лейкоцитарными индексами уже на ранних этапах исследования и установить достоверные изменения картины крови по сравнению с физиологической нормой (ранняя диагностика). В клинической практике на 19 сутки после ФДТ можно уже будет определить эффективность проведенного лечения. Предложенный способ может быть применен для различных гистологических форм опухоли и не требует большого количества оборудования и реактивов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ТЯЖЕСТИ ОСТРОГО ПАНКРЕАТИТА | 2010 |
|
RU2431146C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ МЕХАНИЧЕСКОЙ ЖЕЛТУХИ РАЗЛИЧНОГО ГЕНЕЗА | 2016 |
|
RU2619334C1 |
| Способ проведения фотодинамической терапии солидной карциномы Эрлиха мышей | 2021 |
|
RU2774589C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ ТЯЖЕСТИ МЕХАНИЧЕСКОЙ ЖЕЛТУХИ НЕОПУХОЛЕВОГО ГЕНЕЗА | 2008 |
|
RU2364867C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ПОВЕРХНОСТНОЙ СОЛИДНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС | 2021 |
|
RU2776449C1 |
| Способ оценки риска развития ишемического инсульта, основанный на определении гемодинамических и лейкоцитарных индексов | 2023 |
|
RU2824971C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ПЕРЕВИВНОЙ ПОВЕРХНОСТНОЙ СОЛИДНОЙ СОЕДИНИТЕЛЬНОТКАННОЙ САРКОМЫ М-1 КРЫС | 2019 |
|
RU2704202C1 |
| Способ дифференциальной диагностики бактериальных и вирусных инфекционно-воспалительных заболеваний | 2024 |
|
RU2825251C2 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИНТЕНСИВНОСТИ СИСТЕМНОЙ ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ У ГЕРИАТРИЧЕСКИХ БОЛЬНЫХ С ОСТРЫМ ИНФАРКТОМ МИОКАРДА | 2014 |
|
RU2552952C1 |
| СПОСОБ ДИФФЕРЕНЦИРОВАННОЙ КОРРЕКЦИИ АКТИВНОСТИ ВОСПАЛЕНИЯ ПРИ БРОНХОЛЕГОЧНЫХ ЗАБОЛЕВАНИЯХ | 2010 |
|
RU2430758C1 |

Изобретение относится к экспериментальной медицине, а именно к онкологии и иммунологии, и может быть использовано для исследования противоопухолевой эффективности фотодинамической терапии (ФДТ), способ включает оценку по коэффициенту абсолютного прироста опухоли (К) у особей с продолженным ростом неоплазий; по полной регрессии опухоли (ПР, %) – отсутствие видимой и пальпируемой опухоли; по средней продолжительности жизни (СПЖ) и увеличению продолжительности жизни (УПЖ, %) по сравнению с контролем и по критерию излеченности на 90 сутки после ФДТ, отличается тем, что дополнительно проводят оценку по исследованию лейкограммы периферической крови и динамики изменения интегральных медицинских показателей (ИМП) в следующем порядке:
- вычисляют по формуле объем опухоли с последующим расчётом коэффициента абсолютного прироста опухоли (К) по формуле;
- регистрируют процент животных в группе с полной регрессией (ПР%) опухоли К = -1,00;
- изучают процент соотношения и морфологических характеристик клеток периферической крови мышей путем микроскопирования и дифференциального подсчета лейкограммы периферической крови;
- проводят оценку по исследованию лейкограммы периферической крови и динамики изменения интегральных медицинских показателей (ИМП): индекса сдвига ИСЛК, ЛИ, ИСНЛ, ИСНМ, ИСЛМ в сравнении с физиологической нормой, которая для лейкограммы периферической крови составляет (в %): Базофилы 3,0±0,6; Эозинофилы 0,3±0,3; Миелоциты 0; Юные 0; Палочкоядерные 1,3±0,3; Сегментоядерные 14,3±1,8;
а для ИМП составляет: ЛИ 4,20±0,60; ИСЛМ 16,65±1,60; ИСЛК 0,24±0,04; ИСНЛ 0,25±0,04; ИСНМ 4,48±0,82. После проводят статистическую оценку результатов:
- сравнивают среднюю продолжительность жизни животных в группе (СПЖ) и увеличение продолжительности жизни (УПЖ %) по сравнению с контролем, причем значимый процент УПЖ опытных животных по сравнению с контролем должен составлять ≥50%;
- проводят статистическую оценку результатов непараметрическими методами с использованием программ Statistica 6.0, используют U-критерий Манна–Уитни и Wilcoxon matched pairs test, и если различия между статистически значимыми показателями p<0,05 по сравнению с физиологической нормой, то данные свидетельствуют об эффективности проводимой терапии. Способ позволяет повысить оценку эффективности лечения уже на ранних ее этапах за счет дополнительного выявления иммунологической составляющей фотодинамического воздействия для различных гистологических форм опухоли при отсутствии большого количества оборудования и реактивов. 4 табл., 2 ил.
Способ исследования противоопухолевой эффективности фотодинамической терапии (ФДТ), включающий оценку по коэффициенту абсолютного прироста опухоли (K) у особей с продолженным ростом неоплазий; по полной регрессии опухоли (ПР,%) – отсутствие видимой и пальпируемой опухоли; по средней продолжительности жизни (СПЖ) и увеличению продолжительности жизни (УПЖ,%) по сравнению с контролем и по критерию излеченности на 90 сутки после ФДТ, отличающийся тем, что дополнительно проводят оценку по исследованию лейкограммы периферической крови и динамики изменения интегральных медицинских показателей (ИМП, в следующем порядке:
- вычисляют объем опухоли с последующим расчётом коэффициента абсолютного прироста опухоли (K) по формуле (1):

 , (1)
, (1)
 , (2)
, (2)
где d1, d2,, d3, - три взаимно перпендикулярные диаметры опухоли,
V - объем опухоли в см3,
V0 - объем опухоли до воздействия,
Vt - объем опухоли на определенный срок наблюдения,
- регистрируют процент животных в группе с полной регрессией (ПР%) опухоли K= -1,00;
- изучают процент соотношения и морфологических характеристик клеток периферической крови мышей путем микроскопирования и дифференциального подсчета лейкограммы периферической крови;
- проводят оценку по исследованию лейкограммы периферической крови и динамики изменения интегральных медицинских показателей (ИМП): индекса сдвига лейкоцитов (ИСЛК), лимфоцитарного индекса по Л.Х. Гаркави – лимфоциты/нейтрофилы (ЛИ), лимфоцитарного индекса по формуле В.М. Угрюмова – нейтрофилы/лимфоциты (ИСНЛ), индекса соотношения нейтрофилов и моноцитов (ИСНМ), индекса соотношения лимфоцитов и моноцитов (ИСЛМ) в сравнении с физиологической нормой, которая для лейкограммы периферической крови составляет (в %):
Базофилы 3,0±0,6
Эозинофилы 0,3±0,3
Миелоциты 0
Юные 0
Палочкоядерные 1,3±0,3
Сегментоядерные 14,3±1,8;
для ИМП составляет:
ЛИ 4,20±0,60
ИСЛМ 16,65±1,60
ИСЛК 0,24±0,04
ИСНЛ 0,25±0,04
ИСНМ 4,48±0,82,
после чего проводят статистическую оценку результатов:
- сравнивают среднюю продолжительность жизни животных в группе (СПЖ) и увеличение продолжительности жизни (УПЖ %) по сравнению с контролем, причем значимый процент УПЖ опытных животных по сравнению с контролем должен составлять ≥50%:
 (3)
(3)
- проводят статистическую оценку результатов непараметрическими методами с использованием программ Statistica 6.0, используют U-критерий Манна–Уитни и Wilcoxon matched pairs test,
- и если различия между статистически значимыми показателями p<0,05 по сравнению с физиологической нормой, то данные свидетельствуют об эффективности проводимой терапии.
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ОПУХОЛЕЙ | 2012 |
|
RU2519936C2 |
| AU 7721894 B, 22.03.1995 | |||
| КАПЛАН М.А | |||
| и др | |||
| Изучение специфической фотодинамической активности фотодитазина при фотодинамической терапии у экспериментальных животных-опухоленосителей// Российский биотерапевтический журнал | |||
| Экспериментальная фотодинамическая терапия, 2003, том 2, No 4, c.23-30 | |||
| КАПЛАН М.А | |||
| и др | |||
| Оценка | |||
Авторы
Даты
2020-12-11—Публикация
2020-04-28—Подача