Изобретение относится к области микробиологии и дезинфектологии и может быть использовано для определения эффективности моющих средств на основе пробиотиков.
Моющие средства на основе пробиотиков (ПМС) представляют собой новое поколение моющих средств, которые содержат смесь спор бактерий рода Bacillus в сочетании с поверхностно-активными веществами. Их механизм действия основан на принципе «конкурентного ингибирования» (вытеснения) имеющейся на поверхностях микрофлоры и перевода ее в пассивное метаболическое состояние. Имеющиеся данные говорят о том, что ежедневная обработка поверхностей средствами на основе пробиотиков эффективно снижает уровень патогенных микроорганизмов в условиях больничной среды. Присутствие пробиотиков на поверхностях в помещениях предотвращает повторную контаминацию микроорганизмами и обуславливает поддержание стабильных гигиенических условий поверхностей.
Известен способ оценки эффективности дезинфектантов и антисептиков, заключающийся в сравнении количеств колониеобразующих единиц микроорганизмов до и после воздействия на инокулюм дезинфектанта или антисептика, причем воздействие на инокулюм дезинфектанта или антисептика проводят в цилиндре, помещенном на поверхность плотной питательной среды, содержащей естественный нейтрализатор, по истечении периода необходимой экспозиции в цилиндр вносят концентрированный искусственный нейтрализатор, через 5 мин цилиндр удаляют, и исследуемую смесь распределяют по поверхности плотной питательной среды с последующей оценкой результатов. (Патент RU №2191829, опубл. 2002).
В патенте RU 2679845, опубл. 2019, описан способ биологической дезинфицирующей пробиотической очистки и обеззараживания от патогенов бактерий и вирусов помещений медицинских учреждений, включающий этапы, на которых обрабатывают помещения медицинских учреждений, проводят сбор смывов в упомянутых помещениях, осуществляют посев смывов на питательные среды в «чашках Петри» для контроля текущей чистоты помещений, где обработку осуществляют следующим образом: один раз в день обрабатывают помещения медицинских учреждений пробиотиком; осуществляют смывы в разных местах помещений медицинских учреждений и осуществляют их посев на питательные среды в «чашках Петри» не ранее чем через пять часов после каждой обработки пробиотиком; при этом общая длительность процесса очистки и обеззараживания составляет 10 суток, причем пробиотик в первые пять дней представляет собой концентрат 5% водного раствора, который доводится до температуры 40°С, а во вторые пять дней - концентрат 1% водного раствора, который доводится до температуры 40°С.
Полученные результаты показали пролонгирующие свойства пробиотиков, при этом чистоту можно обеспечить без вредных для человека, особенно для лиц аллергическими явлениями, запахов.
В настоящее время не существует широко признанных стандартов качества, методических рекомендаций и способов по изучению эффективности использования моющих средств на основе пробиотиков.
Предлагаемый способ направлен на решение проблемы и достижение технического результата, состоящего в установлении эффективности использования моющих средств на основе пробиотиков, позволяющий наиболее достоверно и точно с минимальными затратами времени и средств проводить оценку качества действия пробиотиков, содержащихся в качестве активного ингредиента в моющих средствах.
В связи с отсутствием способов оценки эффективности моющих средств на основе пробиотиков в лабораторных условиях с максимально приближенными условиями практического применения, предлагаемый способ соответствует критерию «новизна».
Технический результат достигается описываемым способом определения эффективности моющих средств на основе пробиотиков, включающим два этапа, при этом на первом этапе тест-поверхность, контаминированную тест-микроорганизмом, после подсушивания обрабатывают раствором моющего средства на основе пробиотиков, через определенные промежутки времени с поверхности берут смывы, осуществляют посевы на твердые питательные среды и определяют время воздействия, за которое обсемененность поверхности тест-микроорганизмом снижается не менее чем на 90%, затем на втором этапе тест-поверхности ежедневно в течение не менее 14 дней контаминируют тест-микроорганизмом, при этом в первый день наносят суспензию тест-микроорганизма, содержащую 2×109 КОЕ/мл, далее ежедневно на поверхности наносят суспензию тест-микроорганизма, содержащую 106 КОЕ/мл, и после полного высыхания обрабатывают раствором моющего средства на основе пробиотиков, затем, по истечении времени воздействия, определенного на первом этапе, на тест-поверхностях определяют обсемененность тест-микроорганизмом и сравнивают результаты с данными, полученными с аналогично контамированной контрольной поверхностью, обработанной стерильной водой, и по результатам сравнения выносят суждение об эффективности моющего средства на основе пробиотиков при снижении обсемененности тест-микроорганизмом не менее чем на 99,99 % через 5-7 дней от начала обработки поверхностей.
В известном уровне техники не обнаружено сведений о данном способе определения эффективности моющих средств на основе пробиотиков, что позволяет сделать вывод о соответствии данного способа критериям охраноспособности.
Предложенный способ определения эффективности моющих средств на основе пробиотиков основан на изучении динамики гибели бактерий и грибов после однократной обработки поверхностей пробиотиками и многократной обработки в течение длительного периода.
Сущность настоящего изобретения заключается в следующем.
В качестве тест-поверхностей используют поверхности размером 10×10 см из различных материалов (кафельную, керамическую плитку, стекло, линолеум, металл, пластик).
Тест-поверхности должны быть чистыми и стерильными.
В качестве тест-микроорганизмов используют бактерии: Escherichiacoli (штаммы АТСС 10536, №1257), Pseudomonasaeruginosa (штамм АТСС 27853 или штамм АТСС 15442), Staphylococcusaureus (штаммы АТСС 6538-Р, №906); грибы Candidaalbicans(штамм АТСС 10231).
Для приготовления рабочей суспензии тест-микроорганизма используют 18-24 часовую культуру бактерий и стерильную питьевую воду.
При приготовлении рабочих растворов моющего средства на основе пробиотиков (ПМС) используют теплую воду с температурой 40-50°С.
Способ включает два этапа.
На первом этапе на тест-поверхности, расположенные горизонтально, стерильной пипеткой наносят взвесь тест-микроорганизма из расчета 0,5 мл микробной взвеси, содержащей 2×109 КОЕ/мл, на площадь в 100 см2 и равномерно распределяют ее по поверхности стерильным стеклянным шпателем. Поверхности подсушивают до полного высыхания при температуре окружающей среды (18-20)°C и относительной влажности воздуха (50-60)%, затем обрабатывают рабочим раствором ПМС.
Контрольные поверхности, контаминированные тест-микроорганизмом, после подсушивания обрабатывают стерильной водопроводной водой.
Через определенные промежутки времени (1 час; 2 часа; 4 часа; 24 часа) с поверхностей берут смывы, осуществляют посевы на твердые питательные среды и определяют для опытных поверхностей общее микробное число, обсемененность тест-микроорганизмом и спорами, а для контрольных поверхностей - обсемененность тест-микроорганизмом.
За критерий эффективности берут снижение обсемененности поверхностей тест-микроорганизмом не менее чем на 90% по отношению контролю.
На втором этапе тест-поверхности ежедневно в течение не менее 14 дней контаминируют тест-микроорганизмом и обрабатывают раствором ПМС.
В первый день на тест-поверхности пипеткой наносят суспензию тест-микроорганизма из расчета 0,5 мл взвеси, содержащей 2×109 КОЕ/мл, на 100 см2.
С последующего дня ежедневно на поверхности наносят суспензию тест-микроорганизма из расчета 0,5 мл взвеси, содержащей 106 КОЕ/мл, на 100 см2,
подсушивают до полного высыхания и затем опытные поверхности обрабатывают раствором ПМС.
По истечении времени воздействия, выбранного на 1-ом этапе, на одной поверхности определяют общее микробное число и обсемененность тест-микроорганизмом и спорами. Остальные поверхности оставляют для последующих экспериментальных дней.
Контрольные поверхности, аналогично опытным, ежедневно заражают тест-микроорганизмом и обрабатывают водой с последующим определением количества тест-микроорганизма.
Контроль эффективности обеззараживания тест-поверхностей проводят следующим образом: марлевой салфеткой (размером 5×5 см2), смоченной в растворе универсального нейтрализатора (содержащий Твин-80 (3%), сапонин (0,3-3,0%), гистидин (0,1%), цистеин (0,1%), тщательно протирают тест-поверхность, затем салфетку погружают в 10 мл этого же нейтрализатора, находящегося в пробирке с бусами. Время отмыва марлевой салфетки 10 мин при постоянном встряхивании. Отмывную жидкость сеют (на 2-3 чашки по 0,1-0,2 мл в каждую) на твердые дифференциально-диагностические питательные среды или используют пластины 3М «Petrifilm», представляющие собой готовые системы с культуральной средой, содержащей стандартный набор питательных веществ, гелеобразующий агент, тетразолиевый индикатор, и предназначенные для ускоренного определения бактерий.
В зависимости от вида тест-микроорганизма посевы выращивают в термостате при температуре 37°С.
Учет результатов осуществляют через 2 суток путем подсчета количества выросших колоний, затем рассчитывают плотность контаминации 100 см2 поверхности и % снижения уровня обсемененности тест-микроорганизма, принимая количество колоний, снятых с контрольных поверхностей, за 100%.
За критерий эффективности моющего средства на основе пробиотиков принимают снижение обсемененности тест-микроорганизмом не менее чем на 99,99 % через 5-7 дней от начала обработки поверхностей.
Изобретение иллюстрируется следующим примером.
Пример
Для исследования выбрано моющее средство Heavy Duty Sanitar Cleaner, производства «CHRISALNV», Бельгия, предназначенное для мытья различных поверхностей в санитарных помещениях и санитарно-технического оборудования в медицинских организациях.
Пробиотические культуры в составе препарата абсолютно безвредны при использовании и официально классифицированы как безопасные, согласно документам производителя.
Средство представляет собой розовую жидкость, в состав которой входят энзимы, пробиотические культуры, биоразлагаемые поверхностно-активные вещества (ПАВ) и вода.
В качестве пробиотиков в средстве используются бактерии рода Bacillus, количество которых в 2,0%-ном растворе составляет от 3·105 до 5·105 КОЕ/мл.
Готовят рабочий 2%-ный раствор средства на теплой (40-45°С) водопроводной питьевой воде.
В качестве тест-поверхностей использовали кафельную плитку, а в качестве тест-микроорганизма: Staphylococcus aureus АТСС 6538-Р - для оценки бактерицидной активности в отношении грамположительных бактерий, Escherichia coli АТСС 10536, Pseudomonas aeruginosa АТСС 27853 - для оценки бактерицидной активности в отношении грамотрицательных бактерий, грибы Candida albicans АТСС 10231 - для оценки антимикробной активности в отношении грибов и дрожжеподобных грибов.
Тест-поверхности располагали горизонтально. При обработке поверхностей способом протирания норма расхода рабочего раствора составляла 100 мл/м2 поверхности.
На 1-м этапе на опытные поверхности наносили 0,5 мл суспензии тест-микроорганизмов в 2·109 КОЕ/мл. После подсушивания поверхности обрабатывали 2%-ным раствором средства. Через 1 час, 2 часа, 4 часа, 24 часа отбирали смывы марлевой салфеткой и делали высевы на плотные питательные среды для подсчета общего микробного числа (мясо-пептонный агар), Staphylococcus aureus АТСС 6538-Р (желточно-солевой агар), E.coli (агар Эндо), P.aeruginosa (мясо-пептонный или казеиновый агар), C.albicans (агар Сабуро) и помещали их в термостат. Через двое суток проводят подсчет выросших колоний.
Контрольные поверхности обрабатывают стерильной водой и также через 1 час, 2 часа, 4 часа и 24 часа определяют обсемененность тест-культурой.
Эксперименты ставили не менее чем в трех повторности. Статистическую обработку данных проводили с помощью программы Excel. Различия считали статистически значимыми при р<0,05.
Результаты исследований представлены в Таблице 1.
Таблица 1. Микробная обсемененность поверхностей, контаминированных тест-микроорганизмами, при обработке 2,0%-ным раствором средства
КОЕ/см2
КОЕ/см2
Анализ результатов исследований показал, что споры бактерий рода Bacillus способны прорастать на неживых поверхностях и подавляют рост тест-микроорганизмов.
Как следует из представленных данных, при отборе смывов через 4 часа обсемененность поверхностей микроорганизмами начинает снижаться и увеличивается общее микробное число.
На 2-м этапе тест-поверхности ежедневно (в течение 20-28 дней) контаминировали тест-микроорганизмами из расчета 0,5 мл взвеси, содержащей 106 КОЕ/мл, на 100 см2, подсушивали и обрабатывали 2,0% раствором средства. Контрольные поверхности обрабатывали водой. Через 5 мин поверхности протирали увлажненными водой салфетками, затем с поверхностей через 4 и 24 часа отбирали смывы и делали высевы на плотные питательные среды для подсчета общего микробного числа (мясо-пептонный или казеиновый агар), S.aureus (желточно-солевой агар), E.coli (агар Эндо), P.aeruginosa (мясо-пептонный или казеиновый агар), C.albicans (агар Сабуро) и помещали их в термостат. Через двое суток проводили подсчет выросших колоний.
Результаты исследований представлены в Таблицах 2-5.
Таблица 2. Микробная обсемененность поверхностей, контаминированных Staphylococcus aureus АТСС 6538-Р, при обработке 2,0%-ным раствором средства
КОЕ/см2
КОЕ/см2
24
2,1·103
96
5,5·103
24
1,2·102
51
9,8·102
24
2,9·102
25
9,1·103
24
2,1·102
8
8,4·103
24
1,4·102
5
7,5·103
24
2,9·102
2
8,4·103
24
2,9·102
0
8,4·103
24
2,9·102
0
8,4·103
24
1,03·102
1
6,5·103
24
2,9·102
0
8,4·103
24
2,9·102
0
6,3·103
24
2,5·102
0
2,9·103
24
2,8·102
0
6,4·103
24
1,8·102
0
6,9·103
24
1,7·102
0
6,3·103
24
1,9·102
0
5,9·103
24
1,4·102
0
6,9·103
24
1,5·102
0
6,3·103
Таблица 3. Микробная обсемененность поверхностей, контаминированных E.coli АТСС 10536, при обработке 2,0% раствором средства
КОЕ/см2
КОЕ/см2
24
0
0
6,2·103
24
0
0
2,3·103
24
0
0
2,3·103
24
1
0
8,0·103
24
0
0
1,0·103
Таблица 4. Микробная обсемененность поверхностей, контаминированных P.aeruginosa АТСС 27853, при обработке 2,0% раствором средства
КОЕ/см2
КОЕ/см2
24
94
2
6,2·103
24
1,13·102
1
7,9·103
24
82
0
8,3·103
24
1,04·102
0
6,5·103
Таблица 5. Микробная обсемененность поверхностей, контаминированных C.albicans АТСС 10231, при обработке 2,0% раствором средства
КОЕ/см2
КОЕ/см2
24
194
12
5,9·103
24
1,13·102
9
7,2·103
24
98
12
8,1·103
24
1,04·102
5
7,9·103
После обработки раствором моющего средства на основе пробиотиков общая численность микроорганизмов увеличилась и достигла до 10000 микробных тел в 1 см2, которая состояла из спор бактерий рода Bacillus, а количество тест-микроорганизма резко снижалось. Как следует из полученных данных, при отборе смывов через 4 часа (Таблицы 2-4) обсемененность поверхностей тест-микроорганизмами начинает снижаться уже в 1-е сутки после начала использования средства и через 10 суток на поверхностях остаются единичные тест-микробы. При отборе смывов через 24 часа S.aureus и P.aeruginosa не обнаруживались на опытных поверхностях уже через 3-4 суток, на контрольных поверхностях КОЕ/см2 для S.aureus через трое суток составляло 2,9·102, а для P.aeruginosa – 82, для C.albicans - 98. Культура E.coli через 24 часа не была выявлена как в смывах с опытных поверхностей, так и в смывах с контрольных поверхностей. Общее микробное число на опытных поверхностях, складывающееся из споровой микрофлоры пробиотика и тест-культуры, колебалось в пределах от 102 до 104 КОЕ/см2.
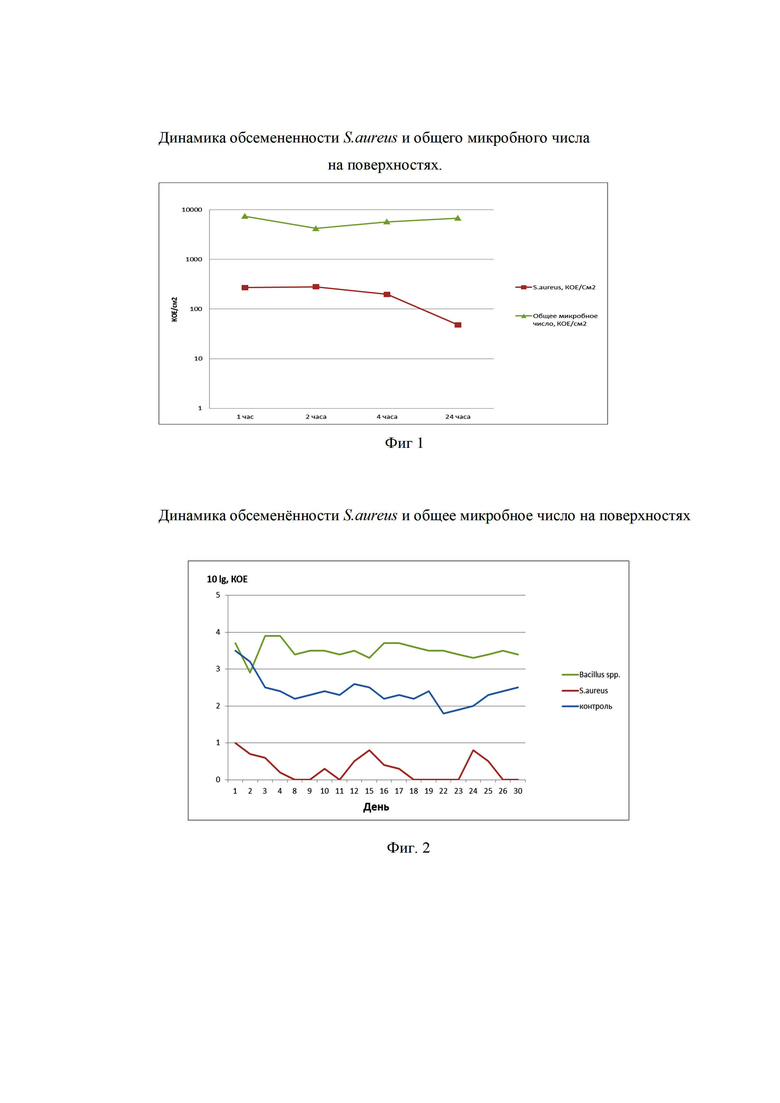
Фиг. 1. Динамика обсемененности S.aureus и общего микробного числа на поверхностях.
Фиг. 2. Динамика обсемененности S.aureus и общее микробное число на поверхностях.
Таким образом, проведенные исследования показали, что применение для мытья поверхностей моющего средства на основе спорообразующих бактерий рода Bacillus приводит к значительному снижению обсемененности поверхностей тест-микроорганизмами.
| название | год | авторы | номер документа |
|---|---|---|---|
| Дезинфицирующее средство для заправки бытовых аэрозольных баллончиков для обеззараживания воздушной среды и поверхностей в помещениях | 2017 |
|
RU2646816C1 |
| Средство для выявления и разрушения биопленок | 2023 |
|
RU2819290C1 |
| Способ определения чувствительности бактерий к антисептическим средствам в растворе | 2021 |
|
RU2781985C1 |
| ДЕЗИНФЕКЦИОННОЕ СРЕДСТВО ДЛЯ АЭРОЗОЛЬНОЙ ОБРАБОТКИ ПОМЕЩЕНИЙ "АлкоПерит" | 2011 |
|
RU2465013C1 |
| ДЕЗИНФИЦИРУЮЩЕЕ СРЕДСТВО | 2010 |
|
RU2440146C2 |
| Биоцидная краска "Экопчелит" для профилактики инфекционных и инвазионных болезней пчёл с пролонгированным антимикробным и акарицидным эффектом | 2018 |
|
RU2680313C1 |
| Способ определения чувствительности микроорганизмов к дезинфицирующим средствам | 2016 |
|
RU2650760C1 |
| Способ оценки эффективности устройства асептического хранения эндоскопов | 2019 |
|
RU2736183C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭФФЕКТИВНОСТИ ДЕЗИНФИЦИРУЮЩИХ СРЕДСТВ, ПРИМЕНЯЕМЫХ В ПРОТИВОТУБЕРКУЛЕЗНЫХ УЧРЕЖДЕНИЯХ | 2008 |
|
RU2364629C1 |
| СРЕДСТВО ДЛЯ ДЕЗИНФЕКЦИИ И САНАЦИИ ВОЗДУХА | 2008 |
|
RU2407547C2 |
Изобретение относится к способу определения эффективности моющих средств на основе пробиотиков, относящихся к новому типу моющих средств. Предлагаемый способ включает два этапа. На первом этапе определяют время воздействия, за которое обсемененность поверхности тест-микроорганизмом снижается не менее чем на 90%, путем обработки тест-поверхности, контаминированной тест-микроорганизмом, раствором моющего средства на основе пробиотиков. Берут смывы с поверхности через определенные промежутки времени и осуществляют посевы на твердые питательные среды. На втором этапе определяют обсемененность тест-микроорганизмом путем контаминирования тест-поверхности ежедневно в течение не менее 14 дней тест-микроорганизмом. При этом в первый день наносят суспензию тест-микроорганизма, содержащую 2×109 КОЕ/мл, далее ежедневно на поверхности наносят суспензию тест-микроорганизма, содержащую 106 КОЕ/мл, после полного высыхания обрабатывают раствором моющего средства на основе пробиотиков. По истечении времени воздействия, определенного на первом этапе, на тест-поверхностях определяют обсемененность тест-микроорганизмом. Сравнивают результаты с данными, полученными с аналогично контаминированной контрольной поверхностью, обработанной стерильной водой. По результатам сравнения выносят суждение об эффективности моющего средства на основе пробиотиков при снижении обсемененности тест-микроорганизмом не менее чем на 99,99 % через 5-7 дней от начала обработки поверхностей. Способ безопасен и обеспечивает достоверность и точность определения. Изобретение позволяет повысить эффективность моющих средств на основе пробиотиков. 5 табл., 1 пр., 2 ил.
Способ определения эффективности моющих средств на основе пробиотиков, включающий два этапа, заключающийся в том, что на первом этапе тест-поверхность, контаминированную тест-микроорганизмом, после подсушивания обрабатывают раствором моющего средства на основе пробиотиков, через определенные промежутки времени с поверхности берут смывы, осуществляют посевы на твердые питательные среды и определяют время воздействия, за которое обсемененность поверхности тест-микроорганизмом снижается не менее чем на 90%, затем на втором этапе тест-поверхности ежедневно в течение не менее 14 дней контаминируют тест-микроорганизмом, при этом в первый день наносят суспензию тест-микроорганизма, содержащую 2×109 КОЕ/мл, далее ежедневно на поверхности наносят суспензию тест-микроорганизма, содержащую 106 КОЕ/мл, после полного высыхания обрабатывают раствором моющего средства на основе пробиотиков, затем, по истечении времени воздействия, определенного на первом этапе, на тест-поверхностях определяют обсемененность тест-микроорганизмом и сравнивают результаты с данными, полученными с аналогично контаминированной контрольной поверхностью, обработанной стерильной водой, по результатам сравнения выносят суждение об эффективности моющего средства на основе пробиотиков при снижении обсемененности тест-микроорганизмом не менее чем на 99,99 % через 5-7 дней от начала обработки поверхностей.
| Способ биологической дезинфицирующей пробиотической очистки и обеззараживания от патогенов бактерий и вирусов помещений медицинских учреждений | 2017 |
|
RU2679845C2 |
| СПОСОБ ДЕЗИНФЕКЦИИ ПОМЕЩЕНИЙ | 1999 |
|
RU2171118C2 |
| СПОСОБ ПРОБИОТИЧЕСКОЙ ОБРАБОТКИ КЛЕТОК С СОДЕРЖАЩИМИСЯ В НИХ МЕЛКИМИ НЕПРОДУКТИВНЫМИ ЖИВОТНЫМИ В УСЛОВИЯХ ВЕТЕРИНАРНОГО ГОСПИТАЛЯ | 2010 |
|
RU2435864C1 |
Авторы
Даты
2020-12-14—Публикация
2020-04-30—Подача