Изобретение относится к биотехнологии, микробиологии, биохимии, санитарии и пищевой промышленности и представляет собой средство для выявления и/или разрушения биопленок.
Биопленка - множество микроорганизмов, расположенных на какой-либо поверхности, клетки которых прикреплены друг к другу. Термин «биопленка» был введен американским исследователем J. Costerton. Для биопленок характерными чертами являются структурная гетерогенность, генетическое разнообразие, т.к. биопленку могут образовывать различные микроорганизмы, сложные регуляторные механизмы, контролирующие отношения внутри сообщества, и наличие внеклеточного экзополимерного матрикса, образуемого из полисахаридов, белков, липидов и нуклеиновых кислот. Матрикс защищает микроорганизмы от факторов внешнего воздействия, будь то факторы внешней среды или факторы иммунной защиты организма.
Биопленки могут образовываться на поверхностях медицинских инструментов, приборов и оборудования, элементов санитарно-технического и промышленного оборудования, элементов мебели.
Образование биопленок на поверхности медицинских устройств представляет собой серьезную проблему. Биопленки образуются на различном медицинском оборудовании. При этом образовывать биопленки может множество типов организмов. Биопленки могут образовывать как грамотрицательные, так и грамположительные бактериальные организмы. Следовательно, остро стоит задача разработать средство, позволяющее обнаружить биопленки и уничтожить их.
Исходя из уровня техники, данную задачу по обнаружению и разрушению биопленок пытались решить различными путями. Причем средства для обнаружения и средства для уничтожения биопленок представляли собой чаще всего различные средства.
Так, из уровня техники известен антимикробный агент для уничтожения биопленок, содержащий:
(a) воду;
(b) от приблизительно 20% до приблизительно 60% по объему низкомолекулярного спирта;
(c) от приблизительно 0,05% до приблизительно 40% по объему пероксида или пероксидобразующего агента; и
(d) ЭДТА в концентрации от приблизительно 5 мг/мл до приблизительно 50 мг/мл
Такой антимикробный агент описан в патенте RU 2570387.
Из уровня техники известен документ RU 2759744, в котором раскрыт способ борьбы с биологическими пленками, включающий две ступени, при этом на первой ступени обнаруживают биологические пленки при помощи каталазного теста и проводят микробиологические смывы с поверхностей при помощи энзимных препаратов, а на второй ступени уничтожают микроорганизмы в состоянии биологических пленок препаратами на основе мультиферментных смесей, отличающийся тем, что
- на первом этапе первой ступени используют индикатор для проведения каталазной реакции, содержащий пероксид водорода в количестве от 0,5 до 3,0%, технологические компоненты, представляющие собой стабилизаторы перекиси водорода, ингибиторы коррозии, комплексообразователи и загустители, в количестве от 0,25 до 5,0% и краситель;
- на втором этапе первой ступени используют экспресс-тест, разрушающий экзополисахаридный матрикс (ЭПМ) биопленки, при этом индикатор для теста содержит смесь ферментов класса карбогидраз, одновременно все ферменты или раздельно в форме смеси двух, трех, четырех или пяти ферментов: декстраназу, альгинатлиазу, целлюлазу, эндоглюканазы, пергидралазу, эстэразы, манноназу, хитиназу, мутаназу;
- на второй ступени используют мультиферментную смесь, содержащую одновременно все ферменты или раздельно в форме смеси двух, трех, четырех или пяти ферментов: амилазы, липазы, протеазы, целлюлазы, декстраназы, эстеразы, манноназы, мутаназы, альгинатлиазы, пергидролазы, хитиназы -содержание в готовом растворе от 0,05 до 1%, содержание в концентрате или в порошке для приготовления растворов - от 1,0 до 5,0%;
- на второй ступени применяют активно действующие вещества, обладающие бактерицидным и фунгицидным действием в отношении отдельно растущих планктонных форм бактерий и грибов - химические активно действующие вещества дезинфицирующих средств, включая антисептические действующие вещества, или антибиотики, входящие в состав комбинированных с мультиферментными смесями препаратов.
Наиболее близким аналогом к настоящему изобретению является RU 2718910, в котором раскрыт индикатор для выявления биологических пленок бактерий на медицинских инструментах, имеющий гелеобразную структуру и содержащий пероксид водорода, стабилизатор пероксида водорода, N-кокоалкил-М,1Ч-диметиламин оксид, N,N-биc(3-аминопропил)додециламин, ингибитор коррозии, комплексообразователь, загуститель и воду при следующем соотношении компонентов, масс. %:


Однако указанные средства, известные из уровня техники, не позволяют одновременно обнаружить и удалить биопленки, а также не обладают достаточной чувствительностью к микроорганизмам, входящим в состав биопленок.
Задачей настоящего изобретения является разработка эффективного средства, позволяющего как выявить, так и разрушить биопленки на различных поверхностях, в том числе и на поверхностях медицинских инструментов, приборов и оборудования, элементов санитарно-технического и промышленного оборудования, элементов мебели, технологического оборудования в пищевой промышленности.
Техническим результатом настоящего изобретения является возможность обнаружения и разрушения биопленок, а также повышенная чувствительность и высокая скорость срабатывания средства.
Технический результат достигается за счет создания средства для выявления и разрушения биопленок, содержащего:
- пероксид водорода от 2 до 20 мас %,
- Н-пропанол от 0,3 до 10 мас %;
- изопропиловый спирт от 0,3 до 10 мас %,
- фермент из класса гидролаз или смесь ферментов из класса гидролаз в концентрации от 0,01 до 5%.
- вода - остальное
При этом средство предпочтительно предназначено как для выявления, так и для разрушения биопленок на поверхностях медицинских инструментов, приборов и оборудования, элементов санитарно-технического и промышленного оборудования, элементов мебели, технологического оборудования в пищевой промышленности.
Средство согласно изобретению дополнительно может содержать ПАВ и/или стабилизаторы и/или консерванты и/или загустители и/или красители.
Изобретение иллюстрируется следующими примерами. Пример 1.
Тест-объектом служили пластиковые пластины площадью 100 см2.
Штаммы бактерий: Staphylococcus aureus АТСС 25923, Escherichia coli АТСС 2592.
Для выращивания бактериальной биопленки использовали следующие концентрации бактерий: 1⋅108 КОЕ/мл, 1⋅107 КОЕ/мл, 1⋅106 КОЕ/мл, 1⋅105 КОЕ/мл, 1⋅104 КОЕ/мл, 1⋅103 КОЕ/мл, 1⋅102 КОЕ/мл.
Бактериальные суспензии каждой указанной концентрации, приготовленные в мясопептонном бульоне, наносили равномерным слоем на пластиковые пластины, помещали в эксикаторы и инкубировали в термостате при температуре +37°С 24 часа, после чего эксикаторы с пластинами перемещали в темное место при комнатной температуре и оставляли еще на 24 часа.
В качестве средства согласно изобретению использовали средство следующего состава:
- пероксид водорода 2 мас. %,
- Н-пропанол 0,3 мас. %;
- изопропиловый спирт 0,3 мас. %,
- протеаза EFFECTENZ Р150 0,01 мас. %,
- вода – остальное.
Результаты
При нанесении средства на тестируемую поверхность пластика с биопленкой в течение 2-5 секунд наблюдали появление мелких белых пузырьков.
Результаты эффективности действия средства представлены в таблице 1.
Таблица 1. Тестирование чувствительности средства согласно изобретению.
Количество бактерий в исходной взвеси (КОЕ/мл) Реакция индикатора на присутствие штамма микроорганизма (+/-)

Как видно из таблицы 1, нанесение средства согласно изобретению позволило регистрировать наличие биопленки грамположительных бактерий (на примере тест-штамма Staphylococcus aureus АТСС 25923) и грамотрицательных бактерий (на примере тест-штамма Escherichia coli АТСС 25922) в концентрации до 1⋅103 КОЕ/мл включительно.
Пример 2.
Тест-объектом также как и в примере 1 служили пластиковые пластины площадью 100 см2.
Штаммы бактерий: Staphylococcus aureus АТСС 25923, Escherichia coli АТСС 2592.
Для выращивания бактериальной биопленки использовали следующие концентрации бактерий: 1⋅108 КОЕ/мл, 1⋅107 КОЕ/мл, 1⋅106 КОЕ/мл, 1⋅105 КОЕ/мл, 1⋅104 КОЕ/мл, 1⋅103 КОЕ/мл, 1⋅102 КОЕ/мл.
Бактериальные суспензии каждой указанной концентрации, приготовленные в мясопептонном бульоне, наносили равномерным слоем на пластиковые пластины, помещали в эксикаторы и инкубировали в термостате при температуре +37°С 24 часа, после чего эксикаторы с пластинами перемещали в темное место при комнатной температуре и оставляли еще на 24 часа.
В качестве средства согласно изобретению использовали средство следующего состава:
- пероксид водорода 20 мас. %,
- Н-пропанол10 мас. %;
- изопропиловый спирт 10 мас. %,
- амилаза EFECTENZ S100 5 мас. %,
- вода – остальное
Результаты
При нанесении средства на тестируемую поверхность пластика с биопленкой в течение 2-5 секунд наблюдали появление мелких белых пузырьков.
Результаты эффективности действия средства представлены в таблице 1.
Таблица 2. Тестирование чувствительности средства согласно изобретению.
Количество бактерий в исходной взвеси (КОЕ/мл) Реакция индикатора на присутствие штамма микроорганизма (+/-)

Как видно из таблицы 2, нанесение средства согласно изобретению позволило регистрировать наличие биопленки грамположительных бактерий (на примере тест-штамма Staphylococcus aureus АТСС 25923) и грамотрицательных бактерий (на примере тест-штамма Escherichia coli АТСС 25922) в концентрации до 1⋅103 КОЕ/мл включительно.
Пример 3.
Тест-объектом также как и в примере 1 служили пластиковые пластины площадью 100 см2.
Штаммы бактерий: Staphylococcus aureus АТСС 25923, Escherichia coli АТСС 2592.
Для выращивания бактериальной биопленки использовали следующие концентрации бактерий: 1⋅108 КОЕ/мл, 1⋅107 КОЕ/мл, 1⋅106 КОЕ/мл, 1⋅105 КОЕ/мл, 1⋅104 КОЕ/мл, 1⋅103 КОЕ/мл, 1⋅102 КОЕ/мл.
Бактериальные суспензии каждой указанной концентрации, приготовленные в мясопептонном бульоне, наносили равномерным слоем на пластиковые пластины, помещали в эксикаторы и инкубировали в термостате при температуре +37°С 24 часа, после чего эксикаторы с пластинами перемещали в темное место при комнатной температуре и оставляли еще на 24 часа.
В качестве средства согласно изобретению использовали средство следующего состава:
пероксид водорода 10 мас. %,
- Н-пропанол 5 мас. %;
- изопропиловый спирт 4 мас. %,
- протеаза EFFECTENZ Р150 1 мас. %.
- вода – остальное.
Результаты
При нанесении средства на тестируемую поверхность пластика с биопленкой в течение 2-5 секунд наблюдали появление мелких белых пузырьков.
Результаты эффективности действия средства представлены в таблице 1.
Таблица 3. Тестирование чувствительности средства согласно изобретению.
Количество бактерий в исходной взвеси (КОЕ/мл) Реакция индикатора на присутствие штамма микроорганизма (+/-)
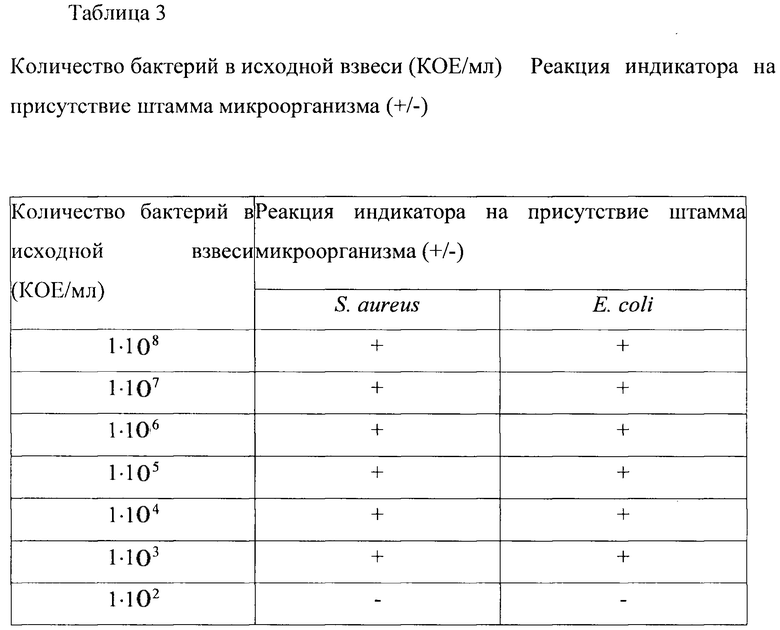
Как видно из таблицы 3, нанесение средства согласно изобретению позволило регистрировать наличие биопленки грамположительных бактерий (на примере тест-штамма Staphylococcus aureus АТСС 25923) и грамотрицательных бактерий (на примере тест-штамма Escherichia coli АТСС 25922) в концентрации до 1⋅103 КОЕ/мл включительно.
Пример 4.
Тест-объектом также как и в примере 1 служили пластиковые пластины площадью 100 см2.
Штаммы бактерий: Staphylococcus aureus АТСС 25923, Escherichia coli АТСС 2592.
Для выращивания бактериальной биопленки использовали следующие концентрации бактерий: 1⋅108 КОЕ/мл, 1⋅107 КОЕ/мл, 1⋅106 КОЕ/мл, 1⋅105 КОЕ/мл, 1⋅104 КОЕ/мл, 1⋅103 КОЕ/мл, 1⋅102 КОЕ/мл.
Бактериальные суспензии каждой указанной концентрации, приготовленные в мясопептонном бульоне, наносили равномерным слоем на пластиковые пластины, помещали в эксикаторы и инкубировали в термостате при температуре +37°С 24 часа, после чего эксикаторы с пластинами перемещали в темное место при комнатной температуре и оставляли еще на 24 часа.
В качестве средства согласно изобретению использовали средство следующего состава:
пероксид водорода 10 мас. %,
- Н-пропанол 5 мас. %;
- изопропиловый спирт 4 мас. %,
- целлюлаза Puradax EG 7000L 1 мас. %,
- пеногаситель SILFOAM SD 168 1 мас. %
- Загуститель НРМС SidleyCel 1 мас. %
- краситель (желтый) 1 мас. %
- консервант Агидол-1 0,5 мас. %
- вода – остальное.
Результаты
При нанесении средства на тестируемую поверхность пластика с биопленкой в течение 2-5 секунд наблюдали появление мелких белых пузырьков.
Результаты эффективности действия средства представлены в таблице 1.
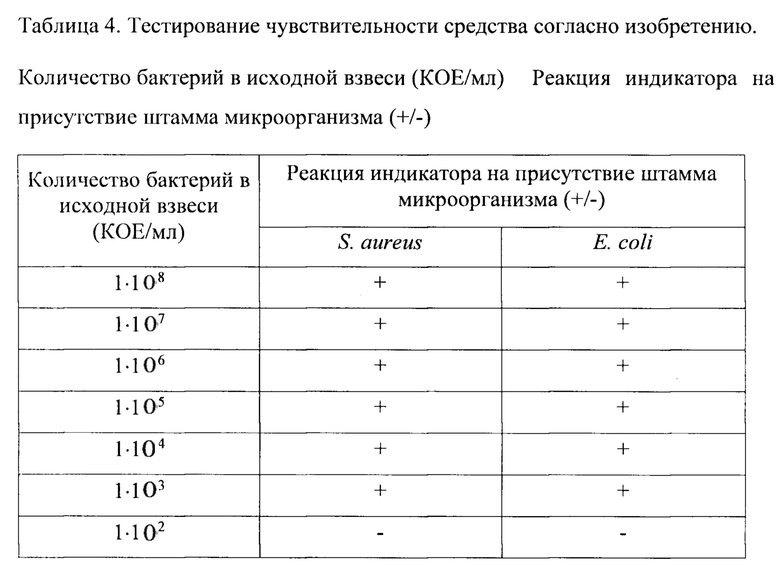
Как видно из таблицы 4, нанесение средства согласно изобретению позволило регистрировать наличие биопленки грамположительных бактерий (на примере тест-штамма Staphylococcus aureus АТСС 25923) и грамотрицательных бактерий (на примере тест-штамма Escherichia coli АТСС 25922) в концентрации до 1⋅103 КОЕ/мл включительно.
Пример 5.
Тест-объектом также как и в примере 1 служили пластиковые пластины площадью 100 см2.
Штаммы бактерий: Staphylococcus aureus АТСС 25923, Escherichia coli АТСС 2592.
Для выращивания бактериальной биопленки использовали следующие концентрации бактерий: 1⋅108 КОЕ/мл, 1⋅107 КОЕ/мл, 1⋅106 КОЕ/мл, 1⋅105 КОЕ/мл, 1⋅104 КОЕ/мл, 1⋅103 КОЕ/мл, 1⋅102 КОЕ/мл.
Бактериальные суспензии каждой указанной концентрации, приготовленные в мясопептонном бульоне, наносили равномерным слоем на пластиковые пластины, помещали в эксикаторы и инкубировали в термостате при температуре +37°С 24 часа, после чего эксикаторы с пластинами перемещали в темное место при комнатной температуре и оставляли еще на 24 часа.
В качестве средства согласно изобретению использовали средство следующего состава:
пероксид водорода 10 мас. %,
- Н-пропанол 5 мас. %;
- изопропиловый спирт 4 мас. %,
- протеаза EFFECTENZ Р150 0.5 мас. %,
- целлюлаза Puradax EG 7000L 0,5 мас. %
- ПАВ Tainolin AES-70-1NC 1 мас. %
- Загуститель НРМС SidleyCel 1 мас. %
- краситель (желтый) 1 мас. %
- пеногаситель SILFOAM SE 39 1 мас. %
- вода – остальное.
Результаты
При нанесении средства на тестируемую поверхность пластика с биопленкой в течение 2-5 секунд наблюдали появление мелких белых пузырьков.
Результаты эффективности действия средства представлены в таблице 1.
Таблица 5. Тестирование чувствительности средства согласно изобретению.
Количество бактерий в исходной взвеси (КОЕ/мл) Реакция индикатора на присутствие штамма микроорганизма (+/-)

Как видно из таблицы 5, нанесение средства согласно изобретению позволило регистрировать наличие биопленки грамположительных бактерий (на примере тест-штамма Staphylococcus aureus АТСС 25923) и грамотрицательных бактерий (на примере тест-штамма Escherichia coli АТСС 25922) в концентрации до 1⋅103 КОЕ/мл включительно.
Сравнительный пример 6.
Тест-объектом служили пластиковые пластины площадью 100 см2.
Штаммы бактерий: Staphylococcus aureus АТСС 25923, Escherichia coli АТСС 2592.
Для выращивания бактериальной биопленки использовали следующие концентрации бактерий: 1⋅108 КОЕ/мл, 1⋅107 КОЕ/мл, 1⋅106 КОЕ/мл, 1⋅105 КОЕ/мл, 1⋅104 КОЕ/мл, 1⋅103 КОЕ/мл, 1⋅102 КОЕ/мл.
Бактериальные суспензии каждой указанной концентрации, приготовленные в мясопептонном бульоне, наносили равномерным слоем на пластиковые пластины, помещали в эксикаторы и инкубировали в термостате при температуре +37°С 24 часа, после чего эксикаторы с пластинами перемещали в темное место при комнатной температуре и оставляли еще на 24 часа.
В качестве средства для сравнения использовали средство согласно патенту RU 2718910, при следующем соотношении компонентов, масс. %:

Результаты
При нанесении средства на тестируемую поверхность пластика с биопленкой в течение 1 мин визуально наблюдалось образование пузырьков в пробах с 1⋅108 до 1⋅104 КОЕ/мл. Результаты эффективности действия средства представлены в таблице 6.
Таблица 6. Тестирование чувствительности средства согласно изобретению.
Количество бактерий в исходной взвеси (КОЕ/мл) Реакция индикатора на присутствие штамма микроорганизма (+/-)

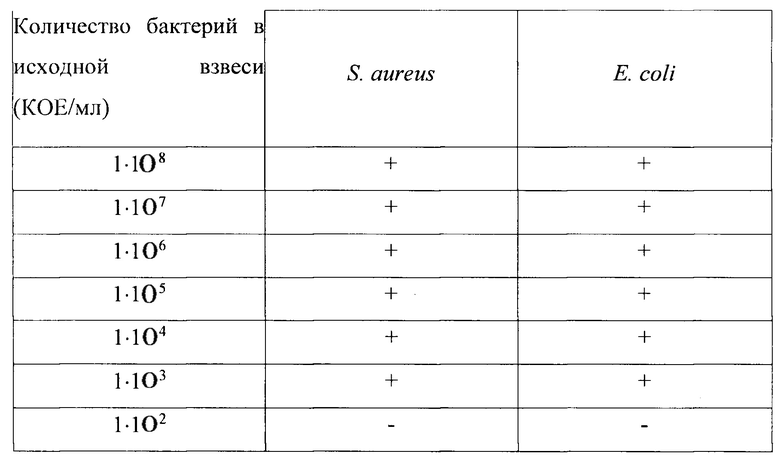
Как видно из таблицы 6, нанесение средства согласно изобретению позволило регистрировать наличие биопленки грамположительных бактерий (на примере тест-штамма Staphylococcus aureus АТСС 25923) и грамотрицательных бактерий (на примере тест-штамма Escherichia coli АТСС 25922) в концентрации только до 1⋅104 КОЕ/мл включительно.
При этом скорость срабатывания теста (скорость проведения реакции) составляет 1 минуту.
Следовательно, средство согласно изобретению обеспечивает возможность обнаружения и разрушения биопленок, а также имеет повышенную чувствительность и высокую скорость срабатывания средства по сравнению с ближайшим аналогом.
Пример 7.
Определение эффективности средства согласно изобретению в отношении микробных биопленок Для выращивания бактериальной биопленки использовали следующие концентрацию тест-бактерий S. aureus и Е. coli - 1⋅107 КОЕ/мл (Staphylococcus aureus АТСС 25923 и Escherichia coli АТСС 25922).
Микробные биопленки выращивали по указанной выше методике как в примере 1.
Далее обрабатывали каждую пластину с биопленкой средством
- 0,5% рабочий раствор средства выдерживали на пластинах 5 минут,
Рабочие растворы средств готовили путем внесения расчетного количества (100 мл) вещества в водопроводную воду с последующим перемешиванием раствора.
После дезинфекции поверхностей пластин проверяли наличие оставшихся бактерий как описано в примере 1-5.
Все эксперименты проведены в трех повторностях.
Результаты оценки эффективности тестируемых средств в отношении микробных биопленок представлены в таблице 7.
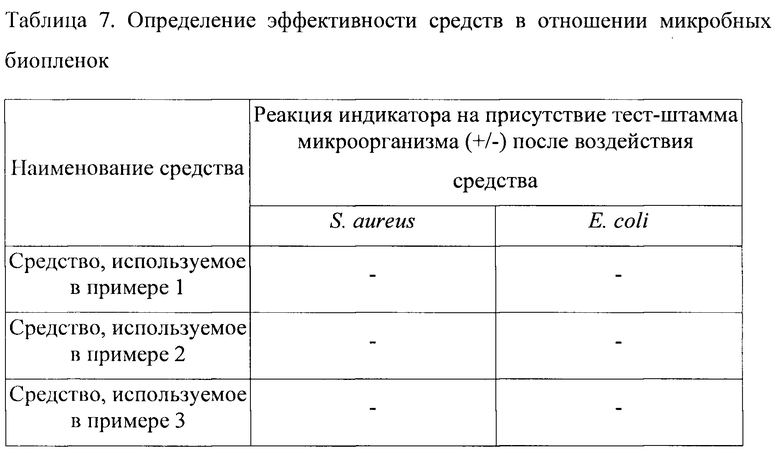
Таким образом, показана высокая эффективность средства согласно изобретению, позволяющая не только обеспечить возможность обнаружения биопленок, но и возможность их разрушения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДЕСТРУКЦИИ БИОПЛЁНОК PSEUDOMONAS AERUGINOSA КОМБИНАЦИЕЙ ОЗОНА С ПЕРОКСИДОМ ВОДОРОДА | 2023 |
|
RU2802662C1 |
| АКТИВНАЯ БИОЛОГИЧЕСКАЯ СУБСТАНЦИЯ "ИНГАЛИПТ АКТИВ ПЛЮС" (INGALIPTUM ACTIVE PLUS), ПОЛУЧЕННЫЙ НА ЕЁ ОСНОВЕ ПРЕПАРАТ МЕСТНОГО ДЕЙСТВИЯ | 2016 |
|
RU2639562C1 |
| АКТИВНАЯ БИОЛОГИЧЕСКАЯ СУБСТАНЦИЯ "ХЛОРОФИЛЛИПТ АКТИВ ПЛЮС" (CLOROPHYLLIPTUM ACTIVE PLUS), ПОЛУЧЕННЫЙ НА ЕЕ ОСНОВЕ ПРЕПАРАТ МЕСТНОГО ДЕЙСТВИЯ И УПАКОВКА К НЕМУ | 2016 |
|
RU2647460C1 |
| ШТАММ БАКТЕРИОФАГА Staphylococcus aureus SA20, ОБЕСПЕЧИВАЮЩИЙ РАЗРУШЕНИЕ БИОПЛЕНОК, ОБРАЗУЕМЫХ БАКТЕРИЯМИ РОДА Staphylococcus | 2014 |
|
RU2565824C1 |
| ШТАММ БАКТЕРИЙ Lactobacillus plantarum, ОБЛАДАЮЩИЙ ШИРОКИМ СПЕКТРОМ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТИ ПО ОТНОШЕНИЮ К ПАТОГЕННЫМ И УСЛОВНО-ПАТОГЕННЫМ МИКРООРГАНИЗМАМ | 2012 |
|
RU2482177C1 |
| ШТАММ БАКТЕРИЙ Lactobacillus rhamnosus, ОБЛАДАЮЩИЙ ШИРОКИМ СПЕКТРОМ АНТАГОНИСТИЧЕСКОЙ АКТИВНОСТИ ПО ОТНОШЕНИЮ К ПАТОГЕННЫМ И УСЛОВНО-ПАТОГЕННЫМ МИКРООРГАНИЗМАМ | 2012 |
|
RU2482176C1 |
| БИОЛОГИЧЕСКИ АКТИВНЫЙ КВАДРОКОМПЛЕКС ДЛЯ РЕГУЛЯЦИИ БИОРАЗНООБРАЗИЯ МИКРОБИОТЫ КОЖИ | 2021 |
|
RU2788358C2 |
| 3,3'[(гексано-1,6-диилбис(азанедиил)]бис-(7-гидрокси-6-метоксикарбонил-2-оксо-2H-хромен), обладающий антибактериальной активностью | 2021 |
|
RU2764522C1 |
| Водорастворимые полимерные нанокомпозиты с наночастицами меди в матрице поли-1-винил-1,2,4-триазола, обладающие антимикробной активностью | 2024 |
|
RU2836708C1 |
| Штамм энтерококков Enterococcus faecium L-3 для лечения и профилактики бактериальных и вирусных инфекций с использованием изготовленных на его основе лечебно-профилактических средств и продуктов питания и способ культивирования штамма энтерококков Enterococcus faecium L-3 | 2022 |
|
RU2800359C1 |
Изобретение относится к области биотехнологии, микробиологии и санитарии и пищевой промышленности. Изобретение представляет собой средство для выявления и разрушения биопленок, содержащее: пероксид водорода от 2 до 20 мас.%, Н-пропанол от 0,3 до 10 мас.%; изопропиловый спирт от 0,3 до 10 мас.%, фермент из класса гидролаз или смесь ферментов из класса гидролаз в концентрации от 0,01 до 5%, вода - остальное. При этом средство предназначено для разрушения и выявления биопленок на поверхностях медицинских инструментов, приборов и оборудования, элементов санитарно-технического и промышленного оборудования, элементов мебели. Средство может также содержать дополнительно ПАВ, и/или стабилизаторы, и/или консерванты, и/или загустители, и/или красители. Изобретение позволяет обеспечить возможность обнаружения и разрушения биопленок, а также повысить чувствительность и скорость срабатывания средства для обнаружения и разрушения биопленок. 2 з.п. ф-лы, 7 табл., 7 пр.
1. Средство для выявления и разрушения биопленок, содержащее:
- пероксид водорода от 2 до 20 мас.%,
- H-пропанол от 0,3 до 10 мас.%,
- изопропиловый спирт от 0,3 до 10 мас.%,
- фермент из класса гидролаз или смесь ферментов из класса гидролаз в концентрации от 0,01 до 5%.
- вода - остальное.
2. Средство по п. 1, отличающееся тем, что предназначено как для выявления, так и для разрушения биопленок на поверхностях медицинских инструментов, приборов и оборудования, элементов санитарно-технического и промышленного оборудования, элементов мебели.
3. Средство по п. 1, дополнительно содержащее ПАВ, и/или стабилизаторы, и/или консерванты, и/или загустители, и/или красители.
| Индикатор для выявления биологических плёнок бактерий на медицинских инструментах (варианты) | 2020 |
|
RU2718910C1 |
| Способ борьбы с биологическими плёнками | 2020 |
|
RU2759744C1 |
| Экспресс-тест для обнаружения биологических плёнок бактерий на абиотических поверхностях (варианты) | 2019 |
|
RU2722795C1 |
| WO 2012072980 A1, 07.06.2012 | |||
| WO 2019079107 A1, 25.04.2019 | |||
| СПОСОБ ФЕРМЕНТАТИВНОГО УДАЛЕНИЯ БИОПЛЕНКИ, КОМПОЗИЦИЯ И НАБОР | 2008 |
|
RU2495098C2 |
Авторы
Даты
2024-05-20—Публикация
2023-11-02—Подача