Область техники
Изобретение относится к биотехнологии и предназначено для использования в нефтедобывающей промышленности для определения профиля притока в горизонтальных нефтяных скважинах при помощи микробиомного анализа, что помогает определить уровень залегания нефтенасыщенных пластов.
Уровень техники
Из уровня техники известен способ определения внутрискважинных притоков флюида (см. [1] патент РФ № 2685600, МПК E21B 43/267, опубл. 22.04.2019), включающий получение флуоресцентного маркера в виде полимерных микросфер с приготовлением дисперсии смолы и люминесцирующих веществ, объединение полученного маркера с несущей средой, подаваемой в скважину, введение маркера с указанной несущей средой в скважину, отбор проб из скважины и их анализ с определением кодов и концентраций маркеров в пробах скважинной жидкости с использованием флюорометрии, определение на основе результатов указанных анализов внутрискважинных притоков флюида.
Недостатками данного аналога являются значительные затраты на получение маркеров, сложность процесса и ограниченная применимость метода, так как он работает на скважинах, где осуществляется гидроразрыв пласта (ГРП).
Из уровня техники известен способ на основе микробиомов для разведки и производства углеводородов (см. [2] WO2015103332, МПК E21B 43/22, G16B 10/00, опубл. 09.07.2015), включающий: a) получение первой информации о микробиоме в момент времени t-i из углеводородов, добытых из скважины, причем скважина имеет первую зону добычи и вторую зону добычи; b) выполнение оценки первой информации о микробиоме, при этом оценка включает: обработку на основе взаимосвязи, имеющую связанный компонент генетического материала и компонент промышленных условий; и этап биоинформатики; посредством чего идентификатор микробиома получают для каждой продуктивной зоны скважины в момент времени t-i; c) получение информации о втором микробиоме в момент времени t 2 из углеводородов, добытых из скважины; d) выполнение оценки второго информации о микробиоме, причем оценка включает: обработку на основе взаимосвязи, имеющую компонент родственного генетического материала и компонент промышленных условий; и этап биоинформатики; посредством чего второй идентификатор микробиома получается для каждой продуктивной зоны скважины в момент времени t 2; и, e) сравнение первого идентификатора микробиома и второго идентификатора микробиома; посредством чего идентифицируется любое изменение количества углеводородов, добываемых в каждой зоне.
Из уровня техники известен также способ на основе микробиомов для разведки и производства углеводородов (см. [3] US2017139078, МПК G01V 11/00, G16B 10/00, опубл. 18.05.2017), включающий доступ к производным данным микробиома, соответствующим одному или нескольким образцам из области, полученным данным микробиома, связанным с вычислительной связью данных микробиома и метаданным, относящимся к одному или нескольким образцам; сравнение полученных данных микробиома с историческими данными микробиома, соответствующими одному или нескольким дополнительным образцам из области или соответствующим дополнительным производным данным микробиома, соответствующим одному или нескольким образцам; генерирование данных прогнозирования; а также выполняют отображение прогнозирующей информации на устройстве отображения пользователя, чтобы помочь в управлении ресурсом в поле.
Общими недостатками указанных аналогов являются дороговизна технологий и отсутствие способа количественной оценки степени притока на основе данных микробиомного анализа.
Сущность изобретения
Технической задачей, стоящей перед изобретением, является определение уровня залегания нефтенасыщенных пластов и степени притока нефтенасыщенных пластов вдоль ствола скважины.
Техническим результатом заявленного изобретения является повышение точности определения профиля притока в нефтяных скважинах.
Согласно изобретению, техническая задача решается, а технический результат достигается за счет способа определения профиля притока в горизонтальных нефтяных скважинах, включающего:
• отбор образцов бурового шлама, выносимого из нефтяной скважины в процессе бурения;
• отбор образцов бурового раствора на входе и на выходе из скважины;
• отбор образцов скважинной жидкости;
• далее выполняют пробоподготовку образцов путем выделения ДНК из образцов бурового шлама и образцов скважинной жидкости, амплифицируют таргетную мишень, очищают ампликоны, и подготавливают библиотеки для ампликонового секвенирования;
• далее выполняют ампликоновое секвенирование образцов;
• далее выполняют биоинформатический анализ c помощью программного окружения QIIME2 путем фильтрации и очистки ридов, денойзинга ридов, сборки парных ридов, удаления химер, аннотации ридов;
• исключают контаминацию с буровым раствором путем вычитания микроорганизмов, выделенных из образцов бурового раствора;
• далее определяют профиль притока в скважине путем сопоставления микробиомов скважинной жидкости с микробиомами бурового шлама и поиска общих представителей в образцах с определением нефтенасыщенных зон.
Осуществление изобретения
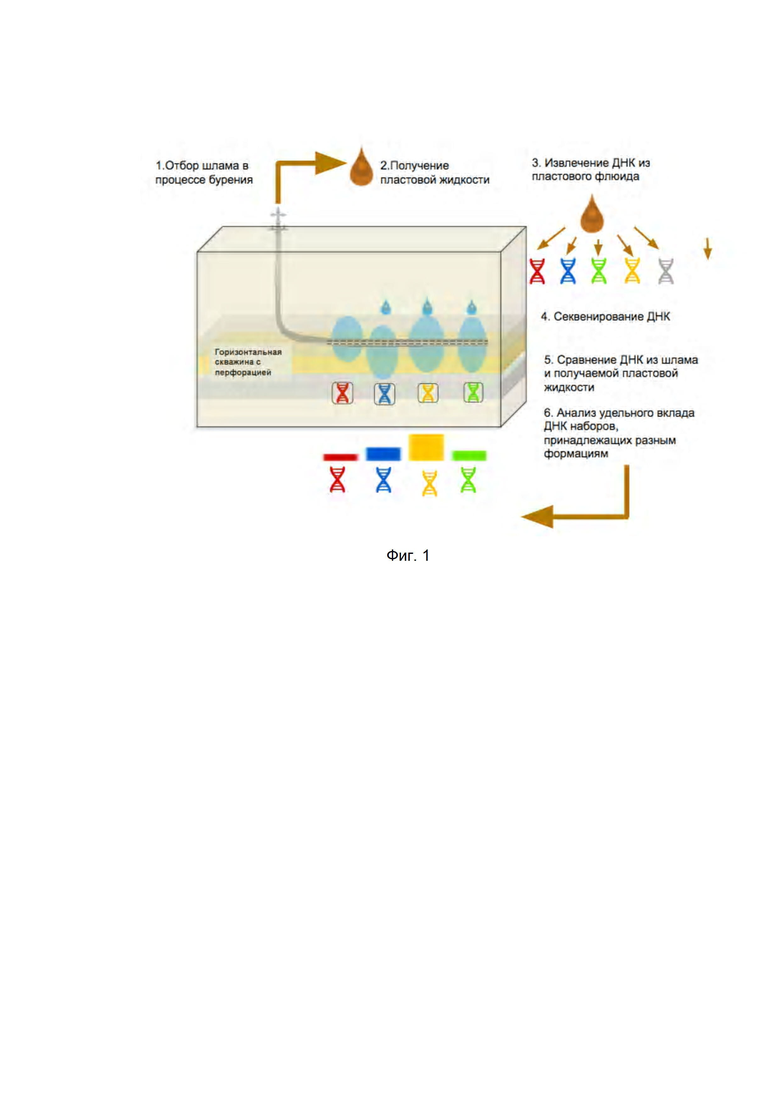
На фиг. 1 изображена общая схема определения нефтенасыщенных интервалов в скважине, а также интенсивности притока.
Заявленный способ определения профиля притока можно назвать технологией “ДНК-каротажа” заключающейся в сопоставлении генетических данных бактерий, выделенных из проб флюида (скважинной жидкости) (т.е. сырой нефти) с генетическими данными бактерий, выделенных из добываемых буровых шламов в ходе бурения скважины на нефтяных месторождениях для определения нефтенасыщенных зон.
Для осуществления “ДНК-каротажа” в процессе бурения скважины отбираются образцы бурового шлама по всему разрезу с различным шагом по глубине (например, 5-10 м), выносимого из нефтяной скважины в процессе бурения, из которых c помощью методов молекулярной биологии выделяется вся тотальная ДНК, содержащаяся в образце.
Далее амплифицируется таргетная мишень (например, малая субъединица 16S рРНК) и происходит подготовка секвенирующих библиотек. Полученные геномные библиотеки секвенируются при помощи секвенаторов 2-го поколения и с помощью современных методов микробиомного анализа определяется таксономический состав микроорганизмов, обитающих в шламах, а также определяется относительная представленность определившихся микроорганизмов. Сопоставление проб флюида и шламов основывается на сходстве или различии таксономического состава и их относительной представленности. Информация о таксономической принадлежности микроорганизмов позволяет ассоциировать часть из них с наличием углеводородов в тех или иных интервалах скважины за счет участия этих микроорганизмов в метаболизме углеводородов нефтенасыщенных залежей. Часть из них ассоциируется исключительно с наличием углеводородов в вскрываемых пластах.
Для исключения контаминации, в анализируемых образцах вычитаются микроорганизмы выделенные из проб бурового раствора. Основными преимуществами разработанной технологии является отсутствие внутрискважинных работ, что позволяет избежать аварии при монтаже оборудования на скважине; высокая точность измерений за счет технических реплик, что позволяет достоверно судить о результатах “ДНК-каротажа”; оперативность получения результатов и возможность длительного мониторинга профиля притока и отсутствие дополнительной экологической нагрузки на окружающую среду при проведении скважинных работ.
Процесс проведения “ДНК-каротажа” в скважине состоит из следующих этапов:
• отбор образцов бурового шлама, выносимого из нефтяной скважины в процессе бурения;
• отбор образцов бурового раствора на входе и на выходе из скважины;
• отбор образцов скважинной жидкости (сырой нефти);
• транспортировка в лабораторию или подготовка к выполнению работ на месте;
• пробоподготовка (выделение ДНК из шламов и образцов нефти; амплификация таргетной мишени; очистка ампликонов; подготовка библиотек для ампликонового секвенирования);
• секвенирование (получение данных, демультиплексирования данных);
• биоинформатический анализ c помощью программного окружения QIIME2, либо пакетов для языка программирования R, таких как DADA2, phyloseq и vegan (фильтрация и очистка ридов; денойзинг ридов; сборка парных ридов; удаление химер; аннотация ридов). Исключение контаминации с буровым раствором;
• Интерпретация данных ДНК-каротажа. Выделение наиболее перспективных нефтенасыщенных интервалов в скважине на основе сходства микробиомов образцов шлама и флюидов с помощью метрик бета-разнообразия.
На основе данных “ДНК-каротажа” в наклонно-направленных или горизонтальных скважинах предлагается строить распределение характерных биомаркеров по глубине (в данном случае биомаркерами являются микроорганизмы). При запуске скважины в работу отбираются пробы добываемой продукции с необходимым шагом по времени, образцы которых также секвенируются. Пробы добываемой продукции могут включать образцы бурового шлама, образцы бурового раствора, образцы скважинной жидкости. Статистическое сопоставление и корреляция генетических наборов флюидов и шлама позволяет построить зависимость интенсивности притока к стволу скважины от глубины, а также характер притока (нефть/вода). Данное исследование, в отличие от общепринятых в отрасли промысловых геофизических исследований (ПГИ) и применения химических трассеров, не требует дополнительного вмешательства в технологические процессы, производства внутрискважинных работ, остановки добычи, внесения изменения в конструкцию скважин, закачки специализированного проппанта при гидроразрыве пласта.
Для определения профиля притока из нефтяной скважины отбираются образцы следующих типов.
В процессе бурения скважины отбираются образцы выбуренной породы (бурового шлама), включая биологические реплики на расстоянии 5 и 10 метров. Сбор образцов бурового шлама проводился в соответствии с проходкой. Каждый образец был собран на так называемых виброситах. Для определения точной глубины каждого образца была определена временная задержка выхода бурового шлама. Масса каждого образца может составлять не более 50 граммов. Каждый образец должен иметь соответствующую маркировку глубины, масса и времени отбора проб. Образцы собирают в стерильные пластиковые контейнеры или в стерильные пластиковые пакеты. Образцы хранятся при температуре не выше +4°С.
Также отбираются образцы скважинной жидкости, содержащей нефть на разных этапах эксплуатации скважины. Объем каждого образца составляет не более 70 мл. Образцы скважинной жидкости отбирались на стадии разработки, отбора и эксплуатации.
Для исключения контаминации отбираются образцы бурового раствора во время фазы бурения пласта. Объем каждого образца не превышает 100 мл, и образцы собираются на входе и выходе из скважины. Образцы на выходе могут содержать определенное количество шлама в виде осадка.
Описание работы с образцами
Для выделения тотальной ДНК из образцов выбуренной породы используется “DNeasy Powersoil kit” (Qiagen). Для выделения образцов из образцов скважинной жидкости используется буфер Виноградского (Weid et al., 2008). После выделения ДНК используется ПЦР (полимеразная цепная реакция) для амплификации таргетных участков ДНК, в нашем случае – это гипервариабельные участки 16S рРНК c помощью набора NEB-Phusion master mix. ПЦР проводился с использованием амплификатора Bio-rad T100 или Eppendorf personal cycler.
Праймеры:
16S-Next-F (TCG TCG GCA GCG TCA GAT GTG TAT AAG AGA CAG) CCT ACG GGN GGC WGC AG
16S-Next-R (GTC TCG TGG GCT CGG AGA TGT GTA TAA GAG ACA G) GA CTA CHV GGG TAT CTA ATC C
В скобках указан адаптер для Illumina HiSeq2500 и MiSeq.
Для очистки от побочных продуктов в ампликонах используются магнитные частицы Ampure XP (Beckman). Для определения концентрации ДНК используется набор для определения концентрации ДНК – Qubit dsDNA HS на спектрофлуоритметре Qubit 3.0.
Список оборудования необходимого для проведения исследования:
• гомогенизатор Tissue Lyser II (Qiagen),
• настольные центрифуги eppendorf mini spin,
• центрифуги-вортексы Bio-san,
• автоматические пипетки Eppendorf (0,5-10 мкл, 10-100 мкл, 100-1000 мкл),
• центрифуга Eppendorf с охлаждением 5804R,
• амплификатор Bio-rad T100,
• амплификатор Eppendorf personal cycler,
• камера для горизонтального электрофореза Bio-rad mini,
• источник тока Bio-rad (любой на 300 вольт),
• спектрофлуоритметры Qubit 1.0 и 2.0,
• Твердотельный термостат Термит (ДНК-технология) и Eppendorf thermomixer compact.
Пример реализации
Выделение и очистка ДНК из образцов выбуренной породы (бурового шлама):
Отбор тотальной ДНК из образцов скважинных проб осуществляется следующим образом в соответствии с протоколом «DNeasy Powersoil kit»:
300 мг бурового шлама в стерильных условиях помещаются в пробирку PowerBead, содержащую деструктивные частицы и буфер, который способствует гомогенизации, растворяют гуминовые кислоты и защищают нуклеиновые кислоты от деградации. После чего аккуратно перемешивают встряхиванием. Далее добавляют 60 мкл раствора С1 и перемешивают, переворачивая 4 раза. Раствор С1 содержит додецилсульфат натрия и другие детергенты, необходимые для лизиса клеток. Пробирки Power Bead помещаются в стойку гомогенизатора Tissue Lyser II (Qiagen, Германия), хорошо закрепленную винтами. Для наиболее полной гомогенизации образцов и лизиса клеток гомогенизируют 10 минут с частотой 30 Гц.
После гомогенизации центрифугируют пробирки в течение 1 минуты при комнатной температуре со скоростью 13000 об/мин. Далее переносят 600 мкл супернатанта в чистую пробирку объемом 2 мл. Супернатант может содержать частицы шлама, что на данном этапе не является критичным. Добавляют 250 мкл раствора C2 в супернатант и встряхивают в течение 5 секунд и инкубируют в течение 5 минут на льду. Раствор С2 содержит реагенты, которые способствуют отложению разрушенных клеточных стенок, гуминовых кислот и белков, которые должны быть удалены из образца, поскольку они способны ингибировать последующую реакцию ПЦР. Пробирки центрифугируют в течение 1 минуты при комнатной температуре со скоростью 13000 об/мин. Не касаясь осадка, переносится 600 мкл супернатанта в пробирку объемом 2 мл; затем добавляется 200 мкл раствора C3 к супернатанту и перемешивается. Далее происходит инкубация в течение 5 минут на льду. На этом этапе происходит дополнительная очистка образца от веществ не нуклеиновой природы. Пробирки центрифугируют в течение 1 минуты при комнатной температуре со скоростью 13000 об/мин. Переносится 750 мкл супернатанта в чистую пробирку объемом 2 мл. Добавляется 1,2 мл раствора C4 к супернатанту и перемешивается на вортексе в течение 5 секунд.
Раствор концентрированных солей в С4 помогает ДНК связываться с фильтром на следующем этапе. Наносится 675 мкл смеси на колонку (спин-фильтр) и центрифугируется в течение 1 минуты при комнатной температуре со скоростью 13000 об/мин. На этой стадии ДНК связывается с фильтром на колонке, а примеси проходят через нее. Жидкость, содержащую примеси, выливается из пробирки для сбора и наносится еще 675 мкл смеси на колонку. Центрифугируется в течение 1 минуты при комнатной температуре со скоростью 13000 об/мин, после чего жидкость выливается. Оставшийся объем смеси наносится на колонку. Центрифугируется в течение 1 минуты при комнатной температуре со скоростью 13000 об/мин, и, супернатант сливается. Далее добавляется 500 мкл раствора C5 и центрифугируется в течение 45 секунд при комнатной температуре при 13000 об/мин. Раствор C5 представляет собой промывочный раствор, содержащий 70% этилового спирта, который удаляет остатки солей, гуминовых кислот и других загрязняющих веществ из образца, в то время как ДНК остается связанной с фильтром. Жидкость удаляется со дна пробирки, повторяется промывка, как описано выше. Колонки центрифугируются в течение еще 1 минуты при комнатной температуре со скоростью 13000 об/мин. Это необходимо для полного удаления остаточного раствора С5, который может ингибировать последующую реакцию ПЦР.
Фильтрующую колонку помещают в чистую пробирку объемом 2 мл. Добавляется 100 мкл раствора C6, предварительно нагретого до 60°C, к центру мембраны. Центрифугируется в течение 1 минуты при комнатной температуре при 13000 об / мин. На этой стадии не содержащий соли раствор C6 (10 мМ Трис-HCl, pH 8,0) удаляет чистую ДНК из фильтра. Определяется концентрацию полученной ДНК, хранение ДНК осуществляется при -20°C.
Выделение и очистка ДНК из образцов скважинной жидкости
Образцы нефтесодержащего флюида (10 мл) (скважинной жидкости) смешиваются с равным объемом буфера Виноградского и инкубируются в течение 10 мин при 80°С. Водную фазу извлекают стерильной пипеткой. Эту процедуру повторяют пять раз, собирая общий объем 50 мл водной фазы для каждого образца. Общий объем водной фазы для каждого образца осаждают центрифугированием при 1200×g в течение 20 минут при 4°С. Аликвоту (2 мл) буфера TE (10 мМ Трис; 1 мМ ЭДТА) добавляют к осадку, и экстракцию ДНК проводили далее, как описано ранее. Чтобы исключить возможность бактериального загрязнения от используемых реагентов, буфера или песка, дополнительно проводится экстракция ДНК из пустой пробирки без образца.
Амплификация 16S рРНК:
Смешивается ПЦР-микс в 0,2 мл Eppendorf на льду:
• стерильная вода - 7 мкл,
• смесь 2xPCR (NEB) - 10 мкл,
• праймер 1 - 1 мкл (10 пмоль),
• праймер 2 - 1 мкл;
• ДНК генома - 1 мкл.
Общий объем смеси для ПЦР составляет 20 мкл. Программа амплификации представлена в таблице 3.
Таблица 3. – Программа амплификации
Очистка 16S фрагментов (ампликонов)
Добавляется в ПЦР смесь магнитных частиц AMPure XP Beads (Agencourt) в присутствии 1: 0,9 (18 мкл на 20 мкл ПЦР-смеси). Инкубируется в течение 5 минут при комнатной температуре. Образцы помещаются на магнитную подставку и удерживаются до полного освещения. Удаляется надосадочная жидкость, частицы промываются 80% спиртом 2 раза. Магнитные частицы высушиваются на воздухе, пока спирт не испарится полностью. Добавляется 15 мкл стерильной воды, перемешивается пипеткой. Магнитные частицы собираются на стороне пробирки направленной к магниту, пока надосадочная жидкость полностью не просветится. Не затрагивая частицы, собирается супернатант в чистую пробирку. Измеряется концентрация очищенных ампликонов на флуориметре серии Qubit в соответствии с протоколом производителя.
Подготовка библиотек для секвенирования
Подготовка образцов для секвенирования проводилась в соответствии с протоколом, рекомендованным Illumina (https://support.illumina.com/documents/documentation/chemistry_documentation/16s/16s-metagenomic-library-prep-guide-15044223-b.pdf) с использованием набора индексированных праймеров Nextera XT index kit (Иллюмина).
Анализ данных
Файл с метаданными включает привязку образцов выбуренной породы к глубине её получения, её типу и резервуару. Образцы нефтесодержащего флюида (скважинной жидкости) классифицируются по времени отбора проб. Пробы бурового раствора также классифицируются по времени отбора проб и по категориям до входа в нефтяную скважину и на этапе выхода из нефтяной скважины.
Основная часть анализа данных выполняется программой QIIME2. Полученные прочтения (риды) переводятся в формат «.qza», который подходит для QIIME2 с использованием их внутреннего скрипта.
Преобразование ридов в формат «.qza», оценка количества и качества операций чтения, удаление ридов с низким качеством выполняется с использованием QIIME2.
Обрезка ридов по качеству, слияние парных ридов, исправление ошибок секвенирования, удаление химмер и получение окончательной таблицы операционных таксономических единиц (OTU) выполняются с использованием программы DADA2 (встроенной в QIIME2). DADA2 осуществляет кластеризацию ридов на уровне сходства 100%.
OTU, содержащиеся в буровом растворе до его поступления в скважину, рассматриваются как потенциальные источники контаминации для образцов выбуренной породы. Такие OTU опционально вычитаются из образцов выбуренной породы, например с помощью пакета DECONTAM для языка программирования R.
Для использования в дальнейшем анализе метрик сходства образцов, учитывающих данные о филогении OTU, строится множественное выравнивание репрезентативных последовательностей ДНК из разных OTU с использованием программы MAFFT, на основе которого строится филогенетическое дерево с помощью программы FastTree (обе программы могут входить в состав программы QIIME2).
Для учёта различий в количестве полученных ридов между образцами перед оценкой бета- и/или альфа-разнообразия количество ридов в разных образцах уравнивается с помощью отбора из каждого образца случайной подвыборки ридов фиксированного размера, либо для анализа используется относительное содержание OTU в каждом образце. Для оценки альфа-разнообразия в образцах используется индекс Шеннона.
Определение таксономии проводится с помощью наивного Баесовского классификатора, обученного по базе данных SILVA.
В ходе анализа в каждом образце выбуренной породы определяется относительное содержание различных OTU и/или различных таксономических групп, и используя данные о глубине отбора каждого образца, строится профиль представленности OTU и/или различных таксономических групп вдоль ствола скважины. Профиль притока строится за счёт оценки схожести OTU и/или различных таксономических групп из образцов, полученных с разной глубины, и образцов поступающего из скважины флюида. В качестве метрики сходства образцов может выступать любая метрика, используемая для оценки бета-разнообразия, такая как индекс Брей-Кертиса, взвешенный и не взвешенный UNIFRAC, или количество OTU, присутствующих одновременно в обоих образцах. Для снижения влияния зашумлённости данных целесообразно сравнивать одновременно несколько образцов флюида с несколькими, например, пятью, образцами выбуренной породы, полученной с соседних глубин и вычислять среднее значение метрик сходства между ними. Предполагается, что чем выше интенсивность притока с определённых глубин, тем выше будет уровень сходства между образцами получаемого на выходе из скважины флюида и образцами выбуренной породы, полученной с данных глубин.
Дополнительно, при одновременном сравнении сразу нескольких образцов выбуренной породы с образцами флюида возможно проводить оценку значимости полученного профиля притока, используя метод многократного случайного перемешивания данных о глубине получения образцов выбуренной породы с последующей оценкой профиля притока на таких перемешенных данных, что позволяет оценить насколько часто наблюдаемый в реальных данных уровень сходства достигается и при случайном перемешивании образцов.
Дополнительно, можно проводить кластеризацию образцов выбуренной породы и образцов флюида. Для этого между всеми образцами вычисляется одна из указанных выше метрик сходства и образцы кластеризуют с помощью методов иерархической кластеризации и/или проводят снижение размерности данных методом анализа главных координат. Предполагается, что образцы флюида будут формировать кластеры с образцами выбуренной породы, полученной с глубин, вносящих основной вклад в приток. Дополнительно, таким образом можно найти кластеры образцов выбуренной породы, обладающих схожими характеристиками.
Все скрипты были написаны с использованием открытых протоколов анализа метагеномных данных, доступных на веб-сайтах Qiime и DADA2.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ мониторинга происхождения добываемого скважинного флюида | 2021 |
|
RU2778869C1 |
| СПОСОБ, КОМПОЗИЦИЯ И НАБОР ДЛЯ СТАБИЛИЗАЦИИ ДЕЗОКСИРИБОНУКЛЕИНОВЫХ КИСЛОТ В БИОЛОГИЧЕСКИХ ОБРАЗЦАХ | 2015 |
|
RU2717644C2 |
| Способ строительства скважин для разведки и добычи флюидов, аккумулированных в трещинных резервуарах | 2019 |
|
RU2732161C1 |
| Способ малоинвазивного выделения бактериальной ДНК из биоптата ткани предстательной железы | 2024 |
|
RU2830876C1 |
| КОМПОЗИЦИИ И СПОСОБЫ | 2014 |
|
RU2664479C2 |
| СПОСОБ ВЫДЕЛЕНИЯ НЕФТЕГАЗОНОСНЫХ ИНТЕРВАЛОВ | 2009 |
|
RU2403385C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРОДУКТИВНОСТИ ПЛАСТА В ПРОЦЕССЕ БУРЕНИЯ СКВАЖИНЫ | 2012 |
|
RU2486337C1 |
| РЕАГЕНТНО-ПРОГРАММНЫЙ КОМПЛЕКС ДЛЯ ПРОВЕДЕНИЯ ТАРГЕТНОГО АНАЛИЗА | 2019 |
|
RU2744443C1 |
| СПОСОБ РАЗРАБОТКИ МЕСТОРОЖДЕНИЯ УГЛЕВОДОРОДОВ | 2005 |
|
RU2292453C2 |
| СПОСОБ РАЗРАБОТКИ НЕФТЕГАЗОВЫХ МЕСТОРОЖДЕНИЙ | 2002 |
|
RU2279539C2 |
Изобретение относится к биотехнологии и предназначено для использования в нефтедобывающей промышленности для определения профиля притока в горизонтальных нефтяных скважинах при помощи микробиомного анализа, что помогает определить уровень залегания нефтенасыщенных пластов. Технический результат - повышение точности определения профиля притока в нефтяных скважинах. По способу осуществляют отбор образцов бурового шлама, выносимого из нефтяной скважины в процессе бурения. Отбирают образцы бурового раствора на входе и на выходе из скважины и скважинную жидкость. Далее выполняют пробоподготовку образцов путем выделения ДНК из образцов бурового шлама и образцов скважинной жидкости. Амплифицируют таргетную мишень, очищают ампликоны, и подготавливают библиотеки для ампликонового секвенирования. Далее выполняют ампликоновое секвенирование образцов. Выполняют биоинформатический анализ c помощью программного окружения QIIME2 путем фильтрации и очистки ридов, денойзинга ридов, сборки парных ридов, удаления химер, аннотации ридов. Исключают контаминацию с буровым раствором путем вычитания микроорганизмов, выделенных из образцов бурового раствора. Далее определяют профиль притока в скважине путем сопоставления микробиомов скважинной жидкости с микробиомами бурового шлама и поиска общих представителей в образцах с определением нефтенасыщенных зон. 1 табл., 1 ил.
Способ определения профиля притока в горизонтальных нефтяных скважинах, включающий:
отбор образцов бурового шлама, выносимого из нефтяной скважины в процессе бурения;
отбор образцов бурового раствора на входе и на выходе из скважины;
отбор образцов скважинной жидкости;
далее выполняют пробоподготовку образцов путем выделения ДНК из образцов бурового шлама и образцов скважинной жидкости, амплифицируют таргетную мишень, очищают ампликоны и подготавливают библиотеки для ампликонового секвенирования;
далее выполняют ампликоновое секвенирование образцов;
далее выполняют биоинформатический анализ c помощью программного окружения QIIME2 путем фильтрации и очистки ридов, денойзинга ридов, сборки парных ридов, удаления химер, аннотации ридов;
исключают контаминацию с буровым раствором путем вычитания микроорганизмов, выделенных из образцов бурового раствора;
далее определяют профиль притока в скважине путем сопоставления микробиомов скважинной жидкости с микробиомами бурового шлама и поиска общих представителей в образцах с определением нефтенасыщенных зон.
| EP 3090029 A4, 07.02.2018 | |||
| СПОСОБ ПОЛНОЙ ВЫРАБОТКИ ПРОДУКТИВНЫХ ПЛАСТОВ НЕФТЕГАЗОВЫХ МЕСТОРОЖДЕНИЙ | 2005 |
|
RU2297525C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕХМЕРНОГО РАСПРЕДЕЛЕНИЯ ПРОНИЦАЕМОСТИ ПЛАСТА | 2011 |
|
RU2479714C1 |
| US 20170139078 A1, 18.05.2017 | |||
| WO 2015103332 A3, 09.07.2015. | |||
Авторы
Даты
2021-01-29—Публикация
2020-10-22—Подача