Область техники
Данное изобретение относится к способу получения γ,δ-ненасыщенного спирта.
Уровень техники
γ,δ-ненасыщенный спирт имеет двойную связь и гидроксигруппу в молекуле, и при превращении соответствующих функциональных групп он может быть превращен во множество органических соединений. Поэтому γ,δ-ненасыщенный спирт является крайне полезным соединением в области органической синтетической химии.
В качестве одного из способов получения предшествующего γ,δ-ненасыщенного спирта известен способ подвергания α-олефина любого сорта и вида и альдегида тепловой реакции в отсутствии катализатора. Например, в ПТЛ 1 и НПЛ 1 описан способ взаимодействия α-олефина и альдегида друг с другом при температуре 100-250°C в течение 2-16 часов под высоким давлением 200 атм. (20,3 МПа) или более. Однако, согласно этому способу, выход составляет не более 31% из-за образования больших количеств побочных продуктов с высокой температурой кипения.
В ПТЛ 2 описан способ взаимодействия α-олефина и альдегида при температуре в интервале 235-400°C и под давлением 1000 атмосфер или менее с получением целевого γ,δ-ненасыщенного спирта и относительно хорошим выходом, в котором рекомендовано проводить реакцию в присутствии основного соединения, такого как аммиак или гексаметилентетрамин. В ПТЛ 3 описан способ взаимодействия α-олефина и альдегида в присутствии фосфата при температуре в интервале -20-320°C под давлением 100-250 атмосфер с получением целевого γ,δ-ненасыщенного спирта с относительно хорошим выходом. Однако, исходя из описания примеров, эти способы являются проблематичными в том, что достаточный промышленный выход не может быть достигнут в отсутствие основного соединения.
В ПТЛ 4 описан способ применения растворителя спирта, имеющего 3-10 атомов углерода, в количестве 2-20 молярных раз к количеству формальдегида в растворе формальдегида, и взаимодействием при 150-350°C под давлением 30-500 атмосфер с получением продукта с селективностью не более 91%. Однако для получения удовлетворительного выхода в способе, применяемое количество α-олефина должно быть 10 молярных раз к количеству альдегида, и поэтому способ является проблематичным в том, что выход при промышленном производстве является низким.
В ПТЛ 5 описан способ взаимодействия α-олефина и безводного формальдегида при температуре в интервале 200-300°C в условиях реакции 5-80 атмосфер с получением целевого γ,δ-ненасыщенного спирта с относительно хорошим выходом. В ПТЛ 6 описан способ взаимодействия α-олефина и формальдегида в молярном отношении 2 или более при температуре в интервале 150-400°C с получением γ,δ-ненасыщенного спирта с высоким выходом. Далее, в ПТЛ 7 описан улучшенный способ из ПТЛ 6, способ добавления альдегида, предварительно нагретого при температуре 80-150°C в реакционную систему.
Однако в этих способах сказано, что альдегид применяют после удаления из него воды, и поэтому в этих способах не может применяться недорогой водный раствор формальдегида. Кроме того, исходя из описания их примеров, в способе из ПТЛ 7 применяют параформальдегид и ничего не сказано о применении водного раствора формальдегида.
В ПТЛ 8 описан способ предварительного нагревания формальдегида метанола в форме полуацеталя при температуре в интервале 280-350°C и под давлением 12-18 МПа и быстрого смешивания его с изобутиленом, также предварительно нагретым в тех же условиях с получением 3-метил-3-бутен-1-ола с высоким выходом. Однако способ проблематичен в том, что когда раствор формальдегида нагревают при 230°C или выше, формальдегид становится нестабильным и поэтому выход целевого γ,δ-ненасыщенного спирта снижается. В ПТЛ 9 описан способ предварительного нагревания метанольного раствора формальдегида при температуре в интервале 150-200°C и под давлением 15-22 МПа и распыления его на изобутилен, предварительно нагретый при температуре в интервале 220-300°C и под давлением 15-22 МПа с получением 3-метил-3-бутен-1-ола с высоким выходом. Однако, согласно описанию Сравнительного примера 2 в ПТЛ 4, выход реакции γ,δ-ненасыщенного спирта при применении метанола в качестве растворителя реакции составляет 38,0% и является низким. Далее, метанол является опасным соединением и поэтому создает проблему переработки отходов после реакции.
Список цитирования
Патентная литература
ПТЛ 1: патент США № 2335027
ПТЛ 2: JP 47-47362 B
ПТЛ 3: WO 02/051776 A
ПТЛ 4: JP 7-285899 A
ПТЛ 5: WO 2004/058670 A
ПТЛ 6: JP 50-88009 A
ПТЛ 7: JP 51-39616 A
ПТЛ 8: публикация заявки на патент Китая № 104130107
ПТЛ 9: публикация заявки на патент Китая № 105439823
Не патентная литература
НПЛ 1: Journal of the American Chemical Society (J. Am. Chem. Soc.), Vol. 77, p. 4666, 1955
Сущность изобретения
Техническая проблема
Как описано выше, способы имеют различные проблемы, связанные с их промышленной применимостью. С учетом ситуации, объектом данного изобретения является создание способа получения γ,δ-ненасыщенного спирта с высоким выходом и хорошей производительностью.
Решение проблемы
В соответствии с данным изобретением, указанный выше объект достигается с помощью [1]-[9].
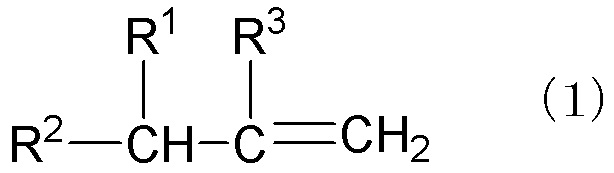
[1] Способ получения γ,δ-ненасыщенного спирта, представленного следующей общей формулой (2):
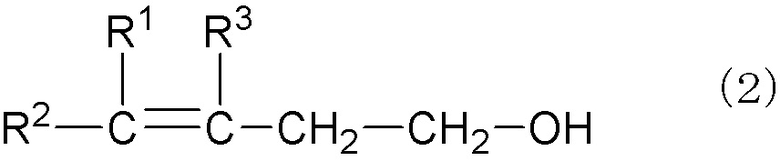
где R1 - R3 каждый независимо представляет атом водорода, алкильную группу, имеющую 1-10 атомов углерода и необязательно замещенную гидроксигруппой, алкенильную группу, имеющую 2-10 атомов углерода и необязательно замещенную гидроксигруппой, или арильную группу, имеющую 6-12 атомов углерода и необязательно замещенную гидроксигруппой, при условии, что R1 и R3 могут связываться друг с другом с образованием кольца, через реакцию α-олефина, представленного следующей общей формулой (1), и формальдегида в условиях нагревания:
где R1 - R3 такие, как определены выше:
где способ включает стадию контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода, где водный раствор формальдегида подвергают предварительному нагреванию при 30-220°C перед стадией.
[2] Способ получения согласно представленному выше [1], где время предварительного нагревания составляет менее 30 минут.
[3] Способ получения согласно представленному выше [1] или [2], где водный раствор формальдегида подвергают предварительному нагреванию при 70-190°C.
[4] Способ получения согласно любому из представленных выше [1]-[3], где применяемое количество спирта, имеющего 3-10 атомов углерода, составляет 0,5-20 моль относительно 1 моля формальдегида в водном растворе формальдегида.
[5] Способ получения согласно любому из представленных выше [1]-[4], где температуре во время реакции составляет 150-350°C.
[6] Способ получения согласно любому из представленных выше [1]-[5], где на стадии смесь α-олефина и спирта, имеющего 3-10 атомов углерода, контактирует с водным раствором формальдегида.
[7] Способ получения согласно представленному выше [6], где до стадии контакта α-олефина с водным раствором формальдегида, смесь подвергают предварительному нагреванию при 70°C или выше.
[8] Способ получения согласно представленному выше [7], где водный раствор формальдегида подвергают предварительному нагреванию при 70-190°C, и смесь подвергают предварительному нагреванию при 70-380°C.
[9] Способ получения согласно любому из представленных выше [1]-[8], где реакцию проводят в отсутствие катализатора.
Преимущества изобретения
Согласно данному изобретению, γ,δ-ненасыщенный спирт может быть получен с высоким выходом и хорошей производительностью. γ,δ-ненасыщенный спирт может быть исходным материалом или промежуточным соединением для различных органических соединений, и 3-метил-3-бутен-1-ол особенно полезен в качестве предшественника для изопрена и исходного материала для лекарственных средств и ароматизирующих веществ.
Описание вариантов
В этом описании, ограничительная формулировка «являться предпочтительным» может быть выбрана произвольно, и сочетание ограничительных формулировок с «являться предпочтительным» может быть названа более предпочтительной.
[Способ получения γ,δ-ненасыщенного спирта]
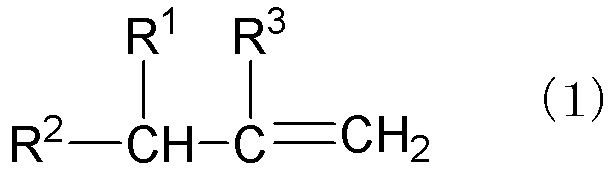
Способ получения γ,δ-ненасыщенного спирта в соответствии с данным изобретением (далее здесь может быть упрощенно назван "способ получения в соответствии с данным изобретением") является способом получения γ,δ-ненасыщенного спирта, представленного следующей формулой (2):
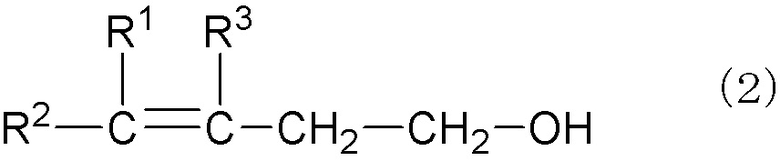
где R1 - R3 каждый независимо является атомом водорода, алкильной группой, имеющей 1-10 атомов углерода, и необязательно замещенной гидроксигруппой, алкенильной группой, имеющей 2-10 атомов углерода, и необязательно замещенной гидроксигруппой, или арильной группой, имеющей 6-12 атомов углерода, и необязательно замещенной гидроксигруппой, при условии, что R1 и R3 могут связываться друг с другом с получением кольца, через реакцию α-олефина, представленного следующей общей формулой (1), и формальдегида в условиях нагревания:

где R1 - R3 такие, как определены выше, и способ включает стадию контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода, где водный раствор формальдегида подвергают предварительному нагреванию при 30-220°C перед стадией.
Согласно способу получения в соответствии с данным изобретением, γ,δ-ненасыщенный спирт, представленный общей формулой (2), может быть получен с высоким выходом и хорошей производительностью.
В данном изобретении, предпочтительно, реакцию между α-олефином, представленным общей формулой (1), и формальдегида проводят в отсутствии катализатора. Катализатор в данном описании означает общеизвестный катализатор, применяемый в реакции присоединения α-олефина и формальдегида, и его примеры включают основное соединение и фосфорсодержащее соединение.
<α-олефин>
α-олефин для применения в соответствии с данным изобретением представлен следующей общей формулой (1):

где R1 - R3 каждый независимо является атомом водорода, алкильной группой, имеющей 1-10 атомов углерода, и необязательно замещенной гидроксигруппой, алкенильной группой, имеющей 2-10 атомов углерода, и необязательно замещенной гидроксигруппой, или арильной группой, имеющей 6-12 атомов углерода, и необязательно замещенной гидроксигруппой, при условии, что R1 и R3 могут связываться друг с другом с образованием кольца.
В следующем описании, α-олефин, представленный общей формулой (1), может быть просто назван "α-олефин".
Примеры указанных выше алкильных групп, имеющих 1-10 атомов углерода, включают метильную группу, этильную группу, этильную группу, различные пропильные группы (в термин ʺразличныеʺ включены линейные и различные разветвленные группы; далее также), различные бутильные группы, различные гексильные группы, различные октильные группы и различные децильные группы. Прежде всего, предпочтительны алкильные группы, имеющие 1-6 атомов углерода, более предпочтительны алкильные группы, имеющие 1-3 атома углерода, и наиболее предпочтительна метильная группа. Что касается замещенной гидроксигруппой алкильной группы, имеющей 1-10 атомов углерода, она особенно не ограничена, пока является группой, в которой один или более атомов водорода в алкильной группе, имеющей 1-10 атомов углерода, замещены гидроксигруппами, и количество гидроксигрупп, предпочтительно, составляет 1-3, и более предпочтительно, 1. Примеры замещенной гидроксигруппой алкильной группы включают метилольную группу, 2-гидроксиэтильную группу и 4-гидрокси-п-бутильную группу. Количество атомов углерода в замещенной гидроксигруппой алкильной группе, имеющей 1-10 атомов углерода, предпочтительно составляет 1-6, более предпочтительно, 1-3, и еще более предпочтительно, 1.
Примеры указанных выше алкенильных групп, имеющих 2-10 атомов углерода, включают винильную группу, аллильную группу, изопропенильную группу, 5-гексен-1-ильную группу, 3-гексен-1-ильную группу, 7-октен-1-ильную группу, 5-октен-1-ильную группу, 9-децен-1-ильную группу и 7-децен-1-ильную группу. Прежде всего, предпочтительна алкенильная группа, имеющая 2-6 атомов углерода, и более предпочтительна алкенильная группа, имеющая 2-4 атома углерода. Что касается замещенной гидроксигруппой алкенильной группы, имеющей 2-10 атомов углерода, она особенно не ограничена, пока является группой, в которой один или более атомов водорода в алкенильной группе, имеющей 2-10 атомов углерода, замещены гидроксигруппами, и количество гидроксигрупп, предпочтительно, составляет 1-3, и более предпочтительно, 1. Примеры замещенной гидроксигруппой алкенильной группы, имеющей 2-10 атомов углерода, включают 2-гидрокси-5-гексен-1-ильгую группу и 2-гидрокси-5-октен-1-ильную группу. Количество атомов углерода в замещенной гидроксигруппой алкенильной группе, имеющей 2-10 атомов углерода, предпочтительно составляет 3-10, более предпочтительно, 3-6, и еще более предпочтительно, 3-4.
Примеры указанной выше арильной группы, имеющей 6-12 атомов углерода, включают фенильную группу, толильную группу, этилфенильную группу, изопропилфенильную группу, ксилильную группу, триметилфенильную группу, нафтильную группу и бифенилильную группу. Прежде всего, предпочтительная арильная группа, имеющая 6-10 атомов углерода. Что касается замещенной гидроксигруппой арильной группы, имеющей 6-12 атомов углерода, она особенно не ограничена, пока является группой, в которой один или более атомов водорода в арильной группе, имеющей 6-10 атомов углерода, замещены гидроксигруппами, и количество гидроксигрупп, предпочтительно, составляет 1-3, и более предпочтительно, 1. Примеры замещенной гидроксигруппой арильной группы, имеющей 6-12 атомов углерода, включают 2-гидроксифенильную группу, 3-гидроксифенильную группу, 4-гидроксифенильную группу, 2-гидрокси-1-нафтильную группу, 3-гидрокси-1-нафтильную группу, 4-гидрокси-1-нафтильную группу, 8-гидрокси-1-нафтильную группу и 1-гидрокси-2-нафтильную группу. Количество атомов углерода в замещенной гидроксигруппой арильной группе, имеющей 6-12 атомов углерода, предпочтительно составляет 6-10.
Что касается кольца в случае, когда R1 и R3 связываются друг с другом с образованием кольца, предпочтительно представлены насыщенное алифатическое кольцо, имеющее 5-10 атомов углерода, такое как циклопентан (5-членное кольцо), циклогексан (6-членное кольцо), циклооктан (8-членное кольцо) и циклодекан (10-членное кольцо). Прежде всего, кольцом предпочтительно является циклогексан.
Из них, с точки зрения снижения количества побочных продуктов, R3 предпочтительно является алкильной группой, имеющей 1-10 атомов углерода, более предпочтительно, алкильной группой, имеющей 1-6 атомов углерода, еще более предпочтительно, алкильной группой, имеющей 1-3 атома углерода, и особенно предпочтительно, метильной группой. Кроме того, по крайней мере, один из R1 и R2 является атомов водорода. Более предпочтительно, по крайней мере, один из R1 и R2 является атомом водорода, и R3 является алкильной группой, имеющей 1-10 атомов углерода (еще более предпочтительно, алкильной группой, имеющей 1-6 атомов углерода, еще более предпочтительно, алкильной группой, имеющей 1-3 атома углерода, и особенно предпочтительно, метильной группой). Особенно предпочтительно, чтобы все R1 и R2 являлись атомом водорода, и R3 являлся алкильной группой, имеющей 1-10 атомов углерода (более предпочтительно, алкильной группой, имеющей 1-6 атомов углерода, еще более предпочтительно, алкильной группой, имеющей 1-3 атома углерода, и особенно предпочтительно, метильной группой). Более предпочтительные примеры соответствующих групп такие, как описан выше.
Конкретные примеры сочетания R1, R2 и R3 включают:
(1) сочетание, в котором все R1, R2 и R3 являются атомом водорода [α-олефин=пропилен],
(2) сочетание, в котором R1 и R2 являются атомами водорода и R3 является алкильной группой, имеющей 1-10 атомов углерода [α-олефин=изобутен (R3 является метильной группой) и т.д.],
(3) сочетание, в котором, по крайней мере, один из R1 и R2 является атомом водорода (предпочтительно, другой является алкильной группой, имеющей 1-10 атомов углерода) и R3 является алкильной группой, имеющей 1-10 атомов углерода [α-олефин=2-метил-1-бутен, 2-метил-1-пентен, 2-метил-1-гексен, 2-метил-1-гептен, 2-метил-1-октен и т.д.],
(4) сочетание, в котором все R1, R2 и R3 являются алкильными группами, каждая из которых имеет 1-10 атомов углерода [α-олефин=2,3-диметил-1-бутен и т.д.],
(5) сочетание, в котором R1 и R2 являются атомами водорода и R3 является арильной группой, имеющей 6-10 атомов углерода [α-олефин=α-метилстирол и т.д.],
(6) сочетание, в котором R2 является атомом водорода и R1 и R3 связаны друг с другом с образованием кольца [α-олефин=метиленциклогексан и т.д.],
(7) сочетание, в котором один из R1 и R2 являются атомом водорода, другой является замещенной гидроксигруппой алкильной группой, имеющей 1-10 атомов углерода, и R3 является атомом водорода [α-олефин=3-бутен-1-ол и т.д.],
(8) сочетание, в котором один из R1 и R2 является атомом водорода, другой является замещенной гидроксигруппой алкильной группой, имеющей 1-10 атомов углерода, и R3 является алкильной группой, имеющей 1-10 атомов углерода [α-олефин=3-метил-3-бутен-1-ол и т.д.].
В случае когда, по крайней мере, один из R1, R2 и R3 является алкенильной группой или арильной группой, может возникнуть ситуация образования продукта, получаемого из реакции алкенильной группы или арильной группы с формальдегидом. Что касается α-олефина, также может применяться не только отдельное соединение, но также смесь представленных выше соединений.
Количество применяемого α-олефина предпочтительно составляет 1-50 моль, более предпочтительно, 3-30 моль и еще более предпочтительно, 3-15 моль на моль формальдегида. Если применяемое количество α-олефина составляет 1 моль или более на моль формальдегида, селективность целевого γ,δ-ненасыщенного спирта улучшается; в то время как если оно составляет 50 моль или менее, оборудование, требуемое для восстановления α-олефина, становится небольшим, так что улучшается не только промышленная ценность, но также существует тенденция к повышению объемной производительности и повышению производительности.
<Водный раствор формальдегида>
Водный раствор формальдегида (формалин) является, например, водным раствором формальдегида, имеющим концентрацию 10-80% массовых. Водный раствор формальдегида предпочтителен, так как он легко доступен и легко обрабатываем. С точки зрения объемной производительности, концентрация формальдегида в водном растворе предпочтительно повышена. С другой стороны, с точки зрения профилактики отложения параформальдегида в водном растворе, концентрация формальдегида в водном растворе предпочтительно не слишком высокая. С учетом этих точек зрения, концентрация водного раствора формальдегида предпочтительно составляет 10-70% массовых, более предпочтительно, 20-65% массовых, даже более предпочтительно, 30-60% массовых, и даже более предпочтительно, 40-60% массовых.
В пределах диапазона, не умаляющего эффект данного изобретения, водный раствор формальдегида может содержать метанол или подобный, обычно добавляемый туда в качестве стабилизатора для формалина. Однако его содержание предпочтительно составляет 10% массовых или менее в водном растворе.
<Спирт, содержащий 3-10 атомов углерода>
Способ получения в соответствии с данным изобретением включает стадию контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода. Спирт, имеющий 3-10 атомов углерода, может однородно растворять α-олефин и формальдегид и, поэтому, благоприятен в качестве растворителя реакции в реакции α-олефина и формальдегида.
Примеры спирта, содержащего 3-10 атомов углерода, включают, но не ограничены ими, ациклический алифатический спирт, такой как н-пропанол, изопропиловый спирт, н-бутанол, трет-бутиловый спирт, изобутиловый спирт, втор-бутиловый спирт, н-пентанол, 3-метил-1-бутанол, 2-метил-2-бутанол, гексанол, 3-метил-3-пентанол, 2-этилгексанол, гептанол, октанол, изооктанол, 2-этил-1-гексанол, нонанол и деканол; алициклический спирт, такой как циклопентанол, циклогексанол, метилциклогексанол, циклогептанол, циклооктанол и циклодеканол; и ароматический спирт, такой как бензиловый спирт.
Можно использовать один из указанных выше спиртов, или два или более их видов можно использовать в комбинации.
С точки зрения однородного растворения α-олефина и формальдегида, количество атомов углерода в спирте предпочтительно составляет 3-8, более предпочтительно, 3-6, даже более предпочтительно, 3-5.
Также с точки зрения однородного растворения α-олефина и формальдегида, среди спиртов, имеющих 3-10 атомов углерода, предпочтительным является ациклической алифатический спирт; более предпочтителен один или более, выбранный из группы, состоящей из изопропилового спирта, изобутилового спирта, втор-бутилового спирта, трет-бутилового спирта, 3-метил-1-бутанола и 2-метил-2-бутанола; и даже более предпочтителен трет-бутиловый спирт.
Количество спирта, имеющего 3-10 атомов углерода, применяемое в этой реакции, предпочтительно составляет 0,5-20 моль по отношению к одному молю формальдегида в водном растворе формальдегида, более предпочтительно, 1-10 моль, и даже более предпочтительно, 1-5 моль. Если применяемое количество спирта, имеющего 3-10 атомов углерода, составляет 0,5 моль или более по отношению к одному молю формальдегида, можно предотвратить образование побочного продукта, алкил-м-диоксана; и если применяемое количество составляет 20 моль или менее, масштаб дистилляционного оборудования для разделения и сбора, а также количество пара и энергии, являющейся источником тепла, могут быть упрощены, поэтому проявляется тенденция к улучшению промышленной ценности изобретения.
<Предварительное нагревание>
В данном изобретении, до стадии контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода (далее упрощенно обозначенной как "стадия контакта"), водный раствор формальдегида подвергают предварительному нагреванию при 30-220°C. При предварительном нагреве системы при этой температуре, маловероятно выпадение параформальдегида в осадок, даже в случае использования высококонцентрированного водного раствора формальдегида, и поэтому стабильность реакции улучшается. Кроме того, разложение формальдегида также может затормаживаться, γ,δ-ненасыщенный спирт может быть получен с высоким выходом, и его производительность может быть повышена.
Температура предварительного нагревания водного раствора формальдегида находится в интервале 30-220°C. Если температура предварительного нагревания ниже 30°C, параформальдегид может легко осаждаться в случае применения высококонцентрированного водного раствора формальдегида для улучшения объемной производительности, что затрудняет управление производственными мощностями. Предпочтительно, реакцию α-олефина и формальдегида проводят при высокой температуре 150°C или выше и течение короткого периода времени. Причина в том, что кратковременная реакция предпочтительна для предотвращения разложения формальдегида и улучшения производительности, а высокотемпературная реакция предпочтительна для повышения степени превращения формальдегида и селективности реакции. Однако если температура предварительного нагревания водного раствора формальдегида ниже 30°C, это неблагоприятно, потому что время, требуемое для достижения целевой температуры реакции в реакционной системе после контакта α-олефина и водного раствора формальдегида, может быть длительным.
С другой стороны, если температура предварительного нагревания водного раствора формальдегида выше 220°C, усиливается реакция разложения формальдегида так, что выход целевого γ,δ-ненасыщенного спирта может снижаться.
Температура предварительного нагревания водного раствора формальдегида составляет, с точки зрения предотвращения осаждения параформальдегида в водном растворе формальдегида, с точки зрения повышения степени превращения и селективности реакции формальдегида, и с точки зрения улучшения производительности, предпочтительно, 40°C или выше, более предпочтительно, 60°C или выше, даже более предпочтительно, 70°C или выше, еще более предпочтительно, 80°C или выше, и с точки зрения предотвращения разложения формальдегида для повышения выхода продукта, температура предварительного нагревания предпочтительно составляет 190°C или ниже, более предпочтительно, 160°C или ниже, и даже более предпочтительно, 155°C или ниже.
Время предварительного нагревания водного раствора формальдегида может быть соответствующим образом выбрано в зависимости от масштаба реакции, но, с точки зрения предотвращения разложения формальдегид и улучшения производительности, желательно как можно короче. С этой точки зрения, время предварительного нагревания составляет менее 30 минут, более предпочтительно, 20 минут или менее, даже более предпочтительно, 15 минут или менее, и еще более предпочтительно, 10 минут или менее. Также предпочтительно, время предварительного нагревания составляет 10 секунд или более, более предпочтительно, 1 минуту или более, и еще более предпочтительно, 2 минуты или более.
Время предварительного нагревания водного раствора формальдегида в этом описании означает время с начала нагревания водного раствора формальдегида до времени контакта раствора с α-олефином. Если в способе получения в соответствии с данным изобретением применяют непрерывную систему, время пребывания водного раствора формальдегида в трубе для предварительного нагревания при определенной температуре предварительного нагревания может быть временем предварительного нагревания.
Способ предварительного нагревания водного раствора формальдегида особенно не ограничен. Например, в случае производства в непрерывной системе, может применяться способ предварительного нагревания, в котором водный раствор формальдегида подают в трубу для предварительного нагревания, заранее нагретую до определенной температуры предварительного нагревания, до контакта водного раствора формальдегида с α-олефином. Что касается материала трубы для предварительного нагревания, применяют такой, который не разъедается водным раствором формальдегида.
В данном изобретении, до стадии контакта α-олефина с водным раствором формальдегида (стадия контакта), при желании, α-олефин также может быть предварительно нагрет. Как описано выше, реакцию α-олефина и формальдегида предварительно проводят в условиях высокой температуры 150°C или выше и в течение короткого периода времени. Предварительное нагревание α-олефина, который взаимодействует с формальдегидом, предпочтительно, так как температура внутри реакционной системы может быть быстро повышена после контакта α-олефина и формальдегида, и так как реакция может проходить более эффективно.
Если α-олефин предварительно нагревают, температура предварительного нагревания предпочтительно составляет 70°C или выше, более предпочтительно, 70-380°C, даже более предпочтительно, 120-350°C, еще более предпочтительно, 150-320°C, и особенно предпочтительно, 180-280°C. Если температура предварительного нагревания составляет 70°C или выше, реакция может проводиться легко и эффективно, и если температура составляет 380°C или ниже, может предотвращаться разложение сырья.
Температура предварительного нагревания α-олефина может быть ниже температуры реакции между α-олефином и формальдегидом, но также может быть равна температуре реакции или выше.
Время предварительного нагревания и способ предварительного нагревания α-олефина, а также их предпочтительные варианты могут быть такими же, как описаны для предварительного нагревания указанного выше водного раствора формальдегида.
До стадии контакта спирт, имеющий 3-10 атомов углерода, также может быть предварительно нагрет. Если спирт, имеющий 3-10 атомов углерода, предварительно нагревают, может применяться, по крайней мере, один способ, выбранный из группы, состоящей из (1) самого способа предварительного нагревания спирта, имеющего 3-10 атомов углерода, (2) способа предварительного получения смеси α-олефина и спирта, имеющего 3-10 атомов углерода и предварительного нагревания смеси, или (3) способ предварительного нагревания водного раствора формальдегида и спирта, имеющего 3-10 атомов углерода, и предварительного нагревания смеси. С точки зрения производительности, способ (2) или (3) предпочтителен, и с точки зрения производительности, предотвращения разложения формальдегида и эффективности нагревания, способ (2) является предпочтительным.
Если применяют способ (1) или (2), предпочтительная температура предварительного нагревания является такой же, как температура предварительного нагревания α-олефина, и если применяется способ (3), предпочтительная температура предварительного нагревания является такой же, как температура предварительного нагревания водного раствора формальдегида.
В данном изобретении, до стадии контакта α-олефина с водным раствором альдегида (стадии контакта), более благоприятно, водный раствор формальдегида предварительно нагревают при 30-220°C, предпочтительно, 70-190°C, и смесь α-олефина и спирта, имеющего 3-10 атомов углерода, предварительно нагревают при 70°C или выше, предпочтительно, 70-380°C.
<Стадия контакта>
Способ получения в соответствии с данным изобретением включает стадию контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода (стадию контакта). После предварительного нагревания, как указано выше, α-олефин контактирует с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода, для взаимодействия α-олефина с формальдегидом, и, следовательно, реакция проходит эффективно и γ,δ-ненасыщенный спирт может быть получен с высоким выходом и хорошей производительностью.
Примеры способа контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода, включают следующие:
(I) Способ контакта α-олефина, водного раствора формальдегида и спирта, имеющего 3-10 атомов углерода друг с другом одновременно.
(II) Способ контакта смеси α-олефина и спирта, имеющего 3-10 атомов углерода с водным раствором формальдегида.
(III) Способ контакта α-олефин со смесью водного раствора формальдегида и спирта, имеющего 3-10 атомов углерода.
С точки зрения производительности, способ (II) или (III) предпочтителен, и с учетом производительности, предотвращения разложения формальдегида и эффективности нагревания, способ (II) более предпочтителен.
Если контакт проводят непрерывным способом, например, согласно способу (I), α-олефин, водный раствор формальдегида и спирт, имеющий 3-10 атомов углерода, загружают в отдельные трубы для предварительного нагревания, каждая из которых предварительно нагрета до желаемой температуры предварительного нагревания, и там предварительно нагревают, и затем объединяют на выходах из пробирок предварительного нагревания. Согласно способу (II), смесь α-олефина и спирта, имеющего 3-10 атомов углерода, и водный раствор формальдегида загружают в отдельные трубы для предварительного нагревания, каждая из которых предварительно нагрета до желаемой температуры предварительного нагревания, и там предварительно нагревают, и затем смесь и водный раствор формальдегида объединяют на выходах из пробирок предварительного нагревания. Согласно способу (III), α-олефин и смесь водного раствора формальдегида и спирта, имеющего 3-10 атомов углерода, загружают в отдельные трубы для предварительного нагревания, каждая из которых предварительно нагрета до желаемой температуры предварительного нагревания, и там предварительно нагревают, и затем α-олефин и смесь объединяют на выходах из пробирок предварительного нагревания.
Если стадию контакта проводят непрерывно, молярное отношение α-олефина, формальдегида и спирта, имеющего 3-10 атомов углерода, может корректироваться через контроль композиции исходных материалов, загружаемых в трубы для предварительного нагревания, и контроль их скорости потока в трубы для предварительного нагревания.
<Условия реакции>
Реакцию α-олефина и формальдегида проводят при нагревании. Например, объединенную жидкую смесь, которую получают после стадии контакта, прямо переносят в реактор, и α-олефин и формальдегид подвергают взаимодействию при нагревании в реакторе.
Температура во время реакции α-олефина и формальдегида (температура в условиях нагревания) предпочтительно составляет 150-350°C, более предпочтительно, 200-340°C, и даже более предпочтительно, 240-330°C. При 150°C или выше скорость реакции может быть высокой, и время реакции сокращается. Если температура реакции составляет 350°C или ниже, может предотвращаться разложение формальдегида и полученного γ,δ-ненасыщенного спирта, и может предотвращаться снижение выхода целевого γ,δ-ненасыщенного спирта.
Реактор, применяемый для реакции α-олефина и формальдегида, может быть предварительно нагрет до желаемой температуры реакции что, однако, не применимо в случае, когда температура предварительного нагревания α-олефина и спирта, имеющего 3-10 атомов углерода, вступающего со стадию контакта, не ниже, чем температура реакции. Например, если α-олефин и спирт, имеющий 3-10 атомов углерода, предварительно нагревают при температуре не ниже температуры реакции и затем проводят стадию контакта, может применяться способ переноса жидкой смеси, полученной на стадии контакта, в реактор, оборудованный средствами нагревания, с последующим взаимодействием компонентов. Такая реакция также включена в объем реакции в условиях нагревания в соответствии с данным изобретением.
Время реакции может быть подходящим образом установлено в зависимости от времени реакции, но, в общем, реакция может заканчиваться в течение 1-60 минут. Следовательно, даже в случае проведения реакции непрерывным способом, время реакции (время нахождения жидкой смеси в реакторе посте стадии контакта) предпочтительно составляет 1-60 минут, более предпочтительно, 3-40 минут.
Давление реакции является давлением паров α-олефина при температуре реакции, но при применении α-олефина, который может быть в критическом состоянии при определенной температуре или выше, предпочтительно, давление контролируют при необходимости. 3,0-50,0 МПа, более предпочтительно, 3,0-30,0 МПа, даже более предпочтительно, 5,0-30,0 МПа, и особенно предпочтительно, 10,0-30,0 МПа.
Если давление реакции не ниже давления паров α-олефина при температуре реакции, концентрация α-олефина в реакционной жидкости может быть повышена для повышения селективности γ,δ-ненасыщенного спирта, и если давление реакции выше, скорость реакции и селективность γ,δ-ненасыщенного спирта может повышаться. Если давление реакции контролируют на уровне 50,0 МПа или менее, стоимость строительства герметичных установок может быть снижена, и опасность разрушения реактора может снизиться.
Предпочтительно, для реакции применяют реактор, способный контролировать температуру реакции, время реакции и давление реакции как указано выше. Реакция может проводиться любым способом в периодической системе, полупериодической системе или непрерывной системе. Предпочтительно, реакцию проводят в непрерывной системе, в которой скорость превращения формальдегида высока, и селективность реакции и выход γ,δ-ненасыщенного спирта высок.
Определенные и предпочтительные варианты непрерывной реакции следующие. После предварительного нагревания и стадии контакта, проведенных описанным выше способом, жидкую смесь, полученную после стадии контакта и содержащую α-олефин, водный раствор формальдегида и спирт, имеющий 3-10 атомов углерода в определенном соотношении, загружают в реактор, нагретый до определенной температуры реакции при такой скорости потока, чтобы время пребывания жидкой смеси в реакторе было определенным временем пребывания. В то время как давление реакции поддерживается таким образом, что давление на выходе из трубы конденсатора, соединенной с выходом из реактора, может поддерживаться при определенном давлении, жидкая смесь остается в реакторе в течение определенного времени пребывания и взаимодействует в ней, и затем реакционную жидкость непрерывно сливают из выходного отверстия реактора. Если α-олефин остается в полученной реакционной жидкости, предпочтительно, α-олефин отделяют и снова применяют в качестве сырья.
Если α-олефин и спирт, имеющий 3-10 атомов углерода, предварительно нагревают при температуре не ниже температуры реакции, также применяют способ, в котором после указанной выше стадии контакта жидкую смесь, полученную после стадии контакта, загружают в реактор, оборудованный средствами нагревания, и там подвергают взаимодействию.
Примеры
Данное изобретение далее конкретно описано со ссылкой на Примеры, но следует понимать, что данное изобретение никаким образом не ограничено этими Примерами.
Реакционную жидкость в каждом Примере анализируют газовой хроматографией (ГХ) в следующих условиях.
<Условия анализа газовой хроматографией>
Аппарат: GC-14A (производства Shimadzu Corporation)
Колонка: G-300 (внутренний диаметр 1,2 мм × длина 20 м, толщина пленки 2 мкм), производства Chemicals Evaluation and Research Institute, Japan
Детектор: водородный пламенно-ионизационный детектор (ПИД)
Газ-носитель: гелий (260 кПа)
Скорость потока газа-носителя: 10 мл/мин
Температура колонки: 80°C → повышение температуры на 5°C/мин → выдерживание при 210°C в течение 4 минут
Температура на входе: 220°C
Температура детектора: 220°C
Объем впрыска образца: 0,2 мкл
<Пример 1>
Согласно операции, указанной ниже, изобутен и формальдегид взаимодействуют с получением γ,δ-ненасыщенного спирта, 3-метил-3-бутен-1-ола (ИПЭС). Во время получения каждую операцию проводят при давлении внутри реакционной системы 200 кг/см2 (19,6 МПа).
Водный раствор 50% масс. формальдегида (жидкий исходный материал 1A) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 1), предварительно нагретую до 80°C и имеющую внутренний диаметр 2 мм и длину 125 мм (внутренний объем 0,4 мл) при 4,7 мл/ч и предварительно нагревают. С другой стороны, смешанный раствор 55,8% масс. изобутена и 44,2% масс. трет-бутилового спирта (исходный материал 2A) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 2) при комнатной температуре (25°C), имеющую внутренний диаметр 2 мм и длину 1465 мм (внутренний объем 4,6 мл) при 55,3 мл/ч. Применяемое количество изобутена относительно 1 моля формальдегида составляет 5 моль, и применяемое количество трет-бутилового спирта составляет 3 моля.
На выходе из труб предварительного нагревания жидкий исходный материал 1A и жидкий исходный материал 2A объединяют и контактируют, и полученную жидкую смесь сразу же загружают в трубу реактора из нержавеющей стали (реактор), предварительно нагретую при 280°C и имеющую внутренний диаметр 2 мм и длину 1590 мм (внутренний объем 5 мл) так, что изобутен и формальдегид взаимодействуют в реакторе. Время нахождения каждого жидкого исходного материала в трубе предварительного нагревания составляет 5 минут, и время пребывания жидкой смеси в реакторе составляет 5 минут. Выход реактора подсоединяют к трубе конденсатора, имеющей внутренний диаметр 2 мм и длину 2000 мм, и поддерживая давление на выходе трубы конденсатора 200 кг/см2 (19,6 МПа), реакционную жидкость выпускают. Полученную реакционную жидкость анализируют ГХ в указанных выше условиях, и степень превращения формальдегида составляет 88,1%, и селективность на основе формальдегидного эквивалента целевого продукта γ,δ-ненасыщенного спирта, 3-метил-3-бутен-1-ола (ИПЭС) составляет 84,5%. Условия получения и результаты анализа показаны в таблице 1.
<Пример 2>
Смешанный раствор (жидкий исходный материал 1B) водного раствора 50% масс. формальдегида и трет-бутилового спирта в отношении 21,3/78,7 (массовых) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 1), предварительно нагретую при 80°C и имеющую внутренний диаметр 2 мм и длину 670 мм (внутренний объем 2,1 мл) при 25,4 мл/ч и предварительно нагревают там. С другой стороны, изобутен (жидкий исходный материал 2B) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 2) при комнатной температуре (25°C), имеющую внутренний диаметр 2 мм и длину 920 мм (внутренний объем 2,9 мл) при 34,6 мл/ч. Применяемое количество изобутена по отношению к 1 молю формальдегида составляет 5 моль, и применяемое количество трет-бутилового спирта составляет 3 моля.
На выходе из труб предварительного нагревания жидкий исходный материал 1В и жидкий исходный материал 2В объединяют и контактируют, и полученную жидкую смесь сразу же загружают в трубу реактора из нержавеющей стали (реактор), предварительно нагретую при 280°C и имеющую внутренний диаметр 2 мм и длину 1590 мм (внутренний объем 5 мл) так, что изобутен и формальдегид взаимодействуют в реакторе. Время пребывания каждого жидкого исходного материала в трубе предварительного нагревания составляет 5 минут, и время пребывания жидкой смеси в реакторе составляет 5 минут. Выход реактора подсоединяют к трубе конденсатора, имеющей внутренний диаметр 2 мм и длину 2000 мм, и поддерживая давление на выходе трубы конденсатора 200 кг/см2 (19,6 МПа), реакционную жидкость выпускают. Полученную реакционную жидкость анализируют ГХ в указанных выше условиях. Условия получения и результаты анализа показаны в таблице 1.
<Пример 3>
ИПЭС получают способом, описанным в Примере 1, за исключением того, что, в Примере 1, исходный жидкий материал 2A загружают в трубу для предварительного нагревания 2, нагретую при 80°C. Условия получения и результаты анализа показаны в таблице 1.
<Пример 4>
ИПЭС получают способом, описанным в Примере 1, за исключением того, что, в Примере 1, исходный жидкий материал 2A загружают в трубу для предварительного нагревания 2, нагретую при 280°C. Условия получения и результаты анализа показаны в таблице 1.
<Пример 5>
ИПЭС получают способом, описанным в Примере 1, за исключением того, что, в Примере 1, водный раствор 50% масс. формальдегида (исходный жидкий материал 1A) загружают в трубу для предварительного нагревания 1, нагретую при 40°C. Условия получения и результаты анализа показаны в таблице 1.
<Пример 6>
ИПЭС получают способом, описанным в Примере 1, за исключением того, что, в Примере 1, исходный жидкий материал 2A меняют на смешанный раствор (исходный жидкий материал 2C) 84,1% масс. изобутена и 15,9% масс. трет-бутилового спирта, что количество изобутена, применяемое для реакции, относительно 1 моля формальдегида, меняют на 7 моль, и применяемое количество трет-бутилового спирта составляет 1 моль. Условия получения и результаты анализа показаны в таблице 1.
<Примеры 7 и 8>
ИПЭС получают способом, описанным в Примере 1, за исключением того, что, в Примере 1, температуру трубы предварительного нагревания 1 меняют на такую, которая указана в таблице 1. Условия получения и результаты анализа показаны в таблице 1.
<Пример 9>
Водный раствор 37% масс. формальдегида (жидкий исходный материал 1C) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 1), нагретую при 80°C и имеющую внутренний диаметр 2 мм и длину 165 мм (внутренний объем 0,5 мл) при 6,2 мл/ч и предварительно нагревают там. С другой стороны, смешанный раствор 55,8% масс. изобутена и 44,2% масс. трет-бутилового спирта (жидкий исходный материал 2A) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 2) при комнатной температуре (25°C), имеющую внутренний диаметр 2 мм и длину 1425 мм (внутренний объем 4,5 мл) при 53,8 мл/ч. Применяемое количество изобутена для реакции относительно 1 моля формальдегида составляет 5 моль, и применяемое количество трет-бутилового спирта составляет 3 моля. Другие условия такие же, которые применяют в Примере 1, и согласно способу получают ИПЭС. Условия получения и результаты анализа показаны в таблице 1.
<Пример 10>
Водный раствор 50% масс. формальдегида (жидкий исходный материал 1A) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 1), нагретую при 80°C и имеющую внутренний диаметр 2 мм и длину 80 мм (внутренний объем 0,3 мл) при 3,0 мл/час и предварительно нагревают там. С другой стороны, смешанный раствор 71,6% масс. изобутена и 28,4% масс. трет-бутилового спирта (жидкий исходный материал 2D) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 2) при комнатной температуре (25°C), имеющую внутренний диаметр 2 мм и длину 1515 мм (внутренний объем 4,8 мл) при 57,0 мл/ч. Применяемое количество изобутена для реакции относительно 1 моля формальдегида составляет 10 моль, и применяемое количество трет-бутилового спирта составляет 3 моля. Другие условия такие же, которые применяют в Примере 1, и согласно способу получают ИПЭС. Условия получения и результаты анализа показаны в таблице 1.
<Пример 11>
Водный раствор 50% масс. формальдегида (жидкий исходный материал 1A) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 1), нагретую при 80°C и имеющую внутренний диаметр 2 мм и длину 50 мм (внутренний объем 0,1 мл) при 1,80 мл/час и предварительно нагревают там. С другой стороны, смешанный раствор 61,9% масс. изобутена и 38,1% масс. трет-бутилового спирта (жидкий исходный материал 2Е) загружают в трубу реактора из нержавеющей стали (труба предварительного нагревания 2) при комнатной температуре (25°C), имеющую внутренний диаметр 2 мм и длину 1545 мм (внутренний объем 4,9 мл) при 58,2 мл/ч. Применяемое количество изобутена для реакции относительно 1 моля формальдегида составляет 15 моль, и применяемое количество трет-бутилового спирта составляет 7 молей. Другие условия такие же, которые применяют в Примере 1, и согласно способу получают ИПЭС. Условия получения и результаты анализа показаны в таблице 1.
<Сравнительный пример 1>
ИПЭС получают способом, описанным в Примере 2, за исключением того, что, в Примере 2, жидкий исходный материал 1B загружают в трубу предварительного нагревания 1 при комнатной температуре (25°C). Условия получения и результаты анализа показаны в таблице 1.
<Сравнительные примеры 2 и 3>
ИПЭС получают способом, описанным в Примере 1, за исключением того, что, в Примере 1, температуру трубы предварительного нагревания 1 меняют на такую, которая указана в таблице 1. Условия получения и результаты анализа показаны в таблице 1.
<Сравнительный пример 4>
ИПЭС получают способом, описанным в Примере 9, за исключением того, что, в Примере 9, жидкий исходный материал 1C загружают в трубу предварительного нагревания 1 при комнатной температуре (25°C). Условия получения и результаты анализа показаны в таблице 1.
В таблице иБ является изобутеном, ТБС является трет-бутиловым спиртом, ФА является формальдегидом, ИПЭС является 3-метил-3-бутен-1-олом, МПЭД является смесью 3-метил-2-пентен-1,5-диола и 3-метиленпентан-1,5-диола, МДО является 4,4-диметил-1,3-диоксаном и МБД является 3-метил-1,3-бутандиолом. В таблице селективность указана в процентах (%) по отношению к эквиваленту формальдегида.
Таблица 1
50% ФА водн.
50% ФА водн. +ТБС
50% ФА водн.
50% ФА водн.
50% ФА водн.
50% ФА водн.
50% ФА водн.
50% ФА водн.
иБ+ТБС
иБ
иБ+ТБС
иБ+ТБС
иБ+ТБС
иБ+ТБС
иБ+ТБС
иБ+ТБС
Таблица 1 (продолжение)
37% ФА водн.
50% ФА водн.
50% ФА водн.
50% ФА водн.
+ТБС
50% ФА водн.
50% ФА водн.
37% ФА водн.
иБ+ТБС
иБ+ТБС
иБ+ТБС
иБ
иБ+ТБС
иБ+ТБС
иБ+ТБС
Промышленная применимость
Согласно данному изобретению, γ,δ-ненасыщенный спирт может быть получен с высоким выходом и хорошей производительностью. γ,δ-ненасыщенный спирт может быть сырьем или промежуточным соединением для различных органических соединений, и в частности, 3-метил-3-бутен-1-ол применяют в качестве предшественника изопрена, и более того, в качестве исходного сырья или промежуточного соединения для лекарственных средств и ароматизирующих веществ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ γ, δ-НЕНАСЫЩЕННЫХ СПИРТОВ | 2015 |
|
RU2692801C2 |
| СПОСОБ ПРОИЗВОДСТВА СОПРЯЖЕННЫХ ДИЕНОВ | 2016 |
|
RU2723241C2 |
| ПОЛИИЗОЦИАНАТ, СОДЕРЖАЩИЙ АЛЛОФАНАТНЫЕ И СИЛАНОВЫЕ ГРУППЫ, ЕГО ПРИМЕНЕНИЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2539985C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННЫХ ЧАСТИЦ | 2009 |
|
RU2516389C2 |
| Способ получения 3-метил-3-бутен-1-ола | 2020 |
|
RU2744099C1 |
| НОВОЕ ПРОИЗВОДНОЕ ПРОСТАГЛАНДИНА | 2017 |
|
RU2748837C2 |
| ФТОРСОДЕРЖАЩИЙ СОПОЛИМЕР (ВАРИАНТЫ), ФТОРСОДЕРЖАЩИЙ ОЛЕФИН (ВАРИАНТЫ), КОМПОЗИЦИЯ ТЕРМОПЛАСТИЧНОЙ СМОЛЫ | 1995 |
|
RU2142449C1 |
| СПОСОБ ПОЛУЧЕНИЯ СОПРЯЖЕННОГО ДИЕНА | 2017 |
|
RU2734778C2 |
| СПОСОБЫ ПОЛУЧЕНИЯ ЭПЛЕРЕНОНА | 2003 |
|
RU2339642C9 |
| ЦИКЛОПЕНТАДИЕНИЛЬНЫЕ ПРОИЗВОДНЫЕ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 1996 |
|
RU2159758C2 |
Настоящее изобретение относится к способу получения γ,δ-ненасыщенного спирта, представленного следующей общей формулой (2):
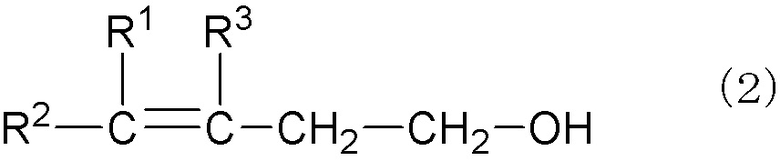
где R1 - R3 каждый независимо представляет атом водорода, алкильную группу, имеющую 1-10 атомов углерода и необязательно замещенную гидроксигруппой, алкенильную группу, имеющую 2-10 атомов углерода и необязательно замещенную гидроксигруппой, или арильную группу, имеющую 6-12 атомов углерода и необязательно замещенную гидроксигруппой, при условии, что R1 и R3 могут связываться друг с другом с образованием кольца. Способ заключается в реакции α-олефина, представленного следующей общей формулой (1)
где R1 - R3 такие, как определены выше, с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода, при этом водный раствор формальдегида подвергают предварительному нагреванию при 30-220°C перед стадией. Предлагаемый способ позволяет получить целевой продукт с высоким выходом и хорошей производительностью. 8 з.п. ф-лы, 1 табл., 15 пр.
1. Способ получения γ,δ-ненасыщенного спирта, представленного следующей общей формулой (2):
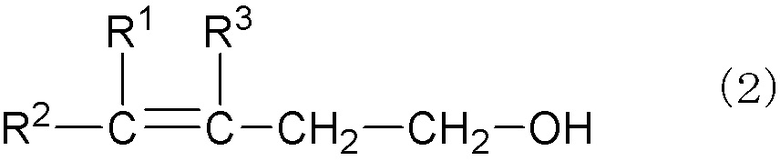
где R1 - R3 каждый независимо представляет атом водорода, алкильную группу, имеющую 1-10 атомов углерода и необязательно замещенную гидроксигруппой, алкенильную группу, имеющую 2-10 атомов углерода и необязательно замещенную гидроксигруппой, или арильную группу, имеющую 6-12 атомов углерода и необязательно замещенную гидроксигруппой, при условии, что R1 и R3 могут связываться друг с другом с образованием кольца, через реакцию α-олефина, представленного следующей общей формулой (1), и формальдегида в условиях нагревания:
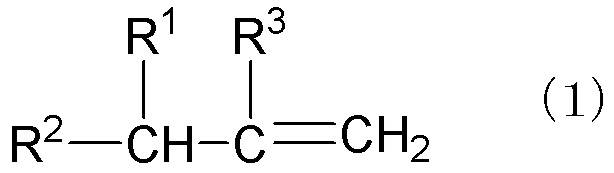
где R1 - R3 такие, как определены выше,
где способ включает стадию контакта α-олефина с водным раствором формальдегида в присутствии спирта, имеющего 3-10 атомов углерода, где водный раствор формальдегида подвергают предварительному нагреванию при 30-220°C перед стадией.
2. Способ получения по п. 1, где время предварительного нагревания составляет менее 30 мин.
3. Способ получения по п. 1 или 2, где водный раствор формальдегида подвергают предварительному нагреванию при 70-190°C.
4. Способ получения по п. 1 или 2, где применяемое количество спирта, имеющего 3-10 атомов углерода, составляет 0,5-20 моль относительно 1 моля формальдегида в водном растворе формальдегида.
5. Способ получения по п. 1 или 2, где температура во время реакции составляет 150-350°C.
6. Способ получения по п. 1 или 2, где на стадии смесь α-олефина и спирта, имеющего 3-10 атомов углерода, контактирует с водным раствором формальдегида.
7. Способ получения по п. 6, где до стадии контакта α-олефина с водным раствором формальдегида смесь подвергают предварительному нагреванию при 70°C или выше.
8. Способ получения по п. 7, где водный раствор формальдегида подвергают предварительному нагреванию при 70-190°C и смесь подвергают предварительному нагреванию при 70-380°C.
9. Способ получения по п. 1 или 2, где реакцию проводят в отсутствие катализатора.
| WO 2015186699 A1, 10.12.2015 | |||
| JP 7285899 A, 31.10.1995 | |||
| CN 102206136 A, 05.10.2011 | |||
| Устройство для закалки | 1983 |
|
SU1275049A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИЗОАМИЛЕНОВОГО СПИРТА | 0 |
|
SU249371A1 |
Авторы
Даты
2021-02-04—Публикация
2018-01-26—Подача