ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится медицине, в частности к медицинской технике, используемой для диагностики и/или лечения воспалительных, инфекционных, доброкачественных и/или злокачественных заболеваний поджелудочной железы, желчевыводящих протоков и/или печени.
УРОВЕНЬ ТЕХНИКИ
В уровне техники известны многочисленные устройства и приспособления, используемые в целях диагностики и/или лечения воспалительных, инфекционных, доброкачественных и/или злокачественных заболеваний поджелудочной железы, желчевыводящих протоков и/или печени.
Согласно руководству по диагностике и лечению рака поджелудочной железы основными методиками, позволяющими подтвердить гистологический тип новообразования, являются тонкоигольная чрескожная трепан биопсия, тонкоигольная аспирационная биопсия, цитологический анализ соскоба эпителия, также называемый браш-биопсией (brush-биопсией), диагностическая лапароскопия с биопсией, а также цитологический анализ смывов из брюшной полости во время лапароскпоии или лапаротомии (Pancreatic adenocarcinoma guidelines National Cancer Comprehensive Network. 2019 Version 2.2019). Данные официально рекомендуемые методики биопсии основаны на иных принципах, в связи с чем их не следует считать аналогами настоящего изобретения.
В частности, известен способ ультразвукового исследования поджелудочной железы (Минько А.Б. Комплексная лучевая диагностика заболеваний поджелудочной железы / А.Б. Минько, B.C. Пручанский, Л.И. Корытова. - СПб: Гиппократ, 2001. – 134 с.; Martínez-Noguera A, Montserrat E, Torrubia S et al (2001) Ultrasound of the pancreas: update and controversies. Eur Radiol 11:1594-1606). Данный способ основан на оценке изменения отражения и поглощения волн от ткани органа и позволяет оценить характер контуров железы, печени, чередования гиперэхогенных или гипоэхогенных зон. Кроме того, этот известный способ позволяет установить наличие образования и диаметр вирсунгова протока, желчевыводящих протоков, а также наличие образований и их диаметра. Главным недостатком этого известного способа является то, что результат исследования напрямую зависит от квалификации специалиста и разрешающей способности аппарата. Чувствительность ультразвукового исследования в данном случае составляет 70-80%. При размере образования менее 1,5 см эффективность этого способа резко снижается. В частности, данный способ не позволяет выявлять внутрипротоковые неоплазии, полноценно оценивать панкреатический проток, а также не позволяет оценивать биохимический состав как панкреатического сока, так и желчи, и выполнять цитологическое их исследование.
Кроме того, известен способ эндоскопического ультразвукового исследования, основанного на том же принципе, что и вышеописанный известный способ (см. Ogawa М., Kawaguchi Y., 2011, Iglesias-Garcia J., 2012). Преимуществом по сравнению с предыдущим известным способом является возможность выполнять биопсию в непосредственной близости от интересуемого участка. При наличии конвексного датчика можно выполнить тонкоигольную аспирационную биопсию подозрительного образования с последующим цитологическим исследованием. Недостатками же данного способа являются необходимость в наличии высококвалифицированного специалиста, анестезиологического пособия, а также высокая стоимость, невозможность выполнения исследования в ряде случаев вследствие некоторых анатомических особенностей. Кроме того, этот известный способ не подходит для цитологической диагностики печени и желчевыводящих протоков, а также позволяет получить путем аспирации лишь небольшой объем цитологического материала, что затрудняет интерпретацию этого полученного цитологического материала, что в итоге приводит к получению высокой доли как ложно-положительных результатов, так и ложно-отрицательных результатов. Кроме того, данный известный способ не позволяет оценить качественный состав желчи и панкреатического сока.
Кроме того, известен способ тонкоигольной трепан биопсии, используемый всегда в сочетании с двумя вышеописанными способами и позволяющий получить материал для гистологического исследования (Hruban R.H., Takaori K., Klimstra D.S. //An illustrated consensus on the classification of pancreatic intraepithelial neoplasia and intraductal papillary mucinous neoplasms (Am. J. Surg. Pathol. 2004. V.28(8). P.977-87). Данный известный способ является основным для гистологической верификации заболеваний поджелудочной железы. Недостатками же данного способа является риск осложнений: кровотечения, формирования свищей, абсцессов, диссеминации раковых клеток по ходу пункционного канала, а также неинформативные, ложноположительные или ложноотрицательные результаты гистоцитологического исследования. Кроме того, этот известный способ не подходит для диагностики заболеваний желчевыводящих протоков, желчного пузыря, а также для лабораторной оценки желчи и панкреатического сока.
Кроме того, известен способ спиральной компьютерной томографии с внутривенным контрастированием (МСКТ) (Callery М.Р., et al., 2009; Klaub M., et al., 2009). Этот способ основан на компьютерной обработке тонких «срезовых» томограмм и оценке степени поглощения контрастного вещества тканью железы, опухоли, а также на измерении диаметра протоков. Данный способ позволяет визуализировать образования, а также сделать заключение об остром или хроническом воспалительном изменении соответствующего органа на основании изменения денситометрических показателей органов. Недостаткамм же данного способа являются значительное снижение его чувствительности при размере образования менее 1,5 см, а также низкая чувствительность и специфичность при диагностике внутрипротоковых неоплазий. Кроме того, этот известный способ не позволяет гистологически подтвердить заболевание и выполнить анализ секрета поджелудочной железы.
Кроме того, известен способ эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) (Kawaguchi Y., Ogawa М., Omata F. // Randomized controlled trial of pancreatic stenting to prevent pancreatitis after endoscopic retrograde cholangiopancreatography. // World Journal of Gastroenterology 2012. Vol. 18(14). P.1635-1641). В данном известном способе очаговые образования и конкременты выявляются в виде дефектов наполнения. Недостатками же данного способа являются необходимость в наличии анестезиологического пособия, ряд ограничений, не позволяющих выполнять определенные манипуляции, и травматиченость процедуры, вследствие которой может развиться деструктивный панкреатит или острый холангит.
Кроме того, известен способ аспирации панкреатического сока эндоскопически из полости двенадцатиперстной кишки с помощью стимуляции экскреторной функции поджелудочной железы с помощью препарата Chirhostim™, представляющего собой синтетический аналог секретина (Suenaga M., Sadakari Y., Almario J.A., et al. Using an endoscopic distal cap to collect pancreatic fluid from the ampulla. Gastrointest Endosc. 2017; 86(6): 1152–1156; Kanda M., Sadakari Y., Borges M., et al. Mutant TP53 in Duodenal samples of pancreatic juice from patients with pancreatic cancer or high-grade dysplasia. Clin Gastroenterol Hepatol. 2013; 11(6): 719–730). Данный известный способ применяют для формированного забора материала для его последующего цитологического исследования и/или молекулярно-генетического исследования. Недостатками же данного способа являются его непризнанность общепринятой методикой, ограничение действием препарата количества забираемого секрета поджелудочной железы и короткая длительность процедуры. Следует отметить, что состав панкреатического сока при введении секретина меняется, так что забираемый в данном случае секрет поджелудочной железы не имеет свой истинный состав, в результате чего невозможно оценить истинный клиренс секреции панкреатического сока, поскольку функция стимулируется препаратом. Не подходит этот известный способ и для сбора и анализа желчи.
Кроме того, известен способ магнитно-резонансной томографии (МРТ), который является стандартным при выявлении новообразований и воспалительных изменений поджелудочной железы и/или желчевыводящих протоков (Akisik M.F., Sandrasegaran K., Aisen A.A. // Dynamic secretin enhanced MR cholangiopancreatography. // RadioGraphics. 2006. Vol.26. P.665-677). Данный способ не является инвазивным, при этом применение в качестве дополнения контрастирования или стимуляция функции поджелудочной железы позволяет увеличить чувствительность и специфичность этого известного способа. Недостатком же этого известного способа является невозможность оценки как состава, так и клиренса желчи или панкреатического сока, а также невозможность их последующего цитологического исследования.
Кроме того, известен способ назопанкреатического или назобилиарного дренирования с последующим изолированным забором субстрата (Handa K., Minami T., Shimizu A., et al. Roles of ERCP in the Early Diagnosis of Pancreatic Cancer. Diagnostics 2019, 9(1), 30; https://doi.org/10.3390/diagnostics9010030; Будзинский С.А., Шаповальянц С.Г., Федоров Е.Д., Шабрин А.В. Эндоскопическое транспапиллярное панкреатическое стентирование в лечении свищей поджелудочной железы (с комментарием А.Г. Кригера). Хирургия. Журнал им. Н.И. Пирогова. 2017; (2):32-44. https://doi.org/10.17116/hirurgia2017232-44). Данный известный способ используют как для лечения воспалительных заболеваний поджелудочной железы, так и для цитологической верификации, при этом он также подходит и для анализа состава. Кроме того, этот известный способ является единственным способом изолированного забора как панкреатического сока, так и желчи. Недостатком же данного известного способа является сложность его реализации. Впервые применение этого способа было описано еще в 1980 году, тем не менее он не является рутинным и используется только в высокоспециализированных учреждениях, причем преимущественно для узкого круга задач, преимущественно для лечения острого панкреатита. В ряде случаев, в том числе вследствие наличия некоторых анатомических особенностей, этот способ может быть не выполним, а также может вызывать такие осложнения как панкреатит, холангит и кровотечения.
Кроме того, известен двухканальный зонд Дрейлинга, используемый в уровне техники для осуществления дуоденального зондирования (Stevens T., Conwell D.L., Zuccaro G., et al. A prospective crossover study comparing secretin-stimulated endoscopic and Dreiling tube pancreatic function testing in patients evaluated for chronic pancreatitis. Gastrointestinal Endoscopy. 2008. 67(3). 5 P. 458-466; Pollack BJ, Grendell JH. Where have all the dreiling tubes gone? Am J Gastroenterol. 2006 Feb;101(2):356-9.). Данный известный катетер позволяет осуществить атравматичный забор панкреатического сока и желчи для их последующего биохимического анализа и/или цитологического анализа и для определения суточного клиренса. Недостаток известного зонда Дрейлинга заключается в том, что он не обеспечивает возможность селективного забора содержимого двенадцатиперстной кишки, что приводит к ретроградному забору кишечного содержимого. Пассивный забор экскрета приводит к тому, что его часть вследствие перистальтики двенадцатиперстной кишки теряется в дистальных отделах. Однако следует отметить, что пассивная постановка за счет тяжести оливы в дистальной части зонда и перистальтики желудочно-кишечного тракта приводит к чрезмерным тратам времени только на позиционирование зонда и рентгенологическую корректировку его положения, при этом сложно обеспечить правильное расположение каналов зонда для забора панкреатического сока и желчи. Применение стимулирующих препаратов, таких как, например, секретин, нельзя воспринимать полноценным, поскольку они увеличивают лишь экскрецию бикорбонатного буфера клетками поджелудочной железы, то есть стимулируется лишь деятельность выстилающих протоки эпителиоцитов, при этом большая часть экзокринного аппарата железы остается неактивной. Таким образом, этот зонд Дрейлинга не позволяет стимулировать функции аденокарцином, муцинозных неоплазий и нейроэндокринных опухолей. Кроме того, этот известный зонд Дрейлинга по сути является альтернативой эндоскопической ретроградной холангиопанкреатографии и по сути может быть использован исключительно для диагностики хронического панкреатита, при этом внутрипротоковые муцинозные и кистозные образования, а также карциномы in situ не могут быть выявлены с его использованием. Кроме того, при использовании этого зонда Дрейлинга достаточно сложно оценить холерез из-за пассажа части желчи и панкреатического сока по двенадцатиперстной кишке, минуя указанный зонд.
Кроме того, известен назопанкреатический стент, который с помощью эндоскопической методики может быть установлен в главный проток поджелудочной железы (Osnes M., Petersen H., Schrumpf E. Comparison of juice obtained during duodenal aspiration and cannulation of the main pancreatic duct after stimulation with exogenous secretin in man. Scand J Gastroenterol. 1978;13(4):453-8.; Minami T., Hanada K., Hirano N., et al. Clinical Usefulness of Serial Pancreatic-Juice Aspiration Cytological Examination and Endoscopic Ultrasound-Guided Fine-Needle Aspiration in Small Pancreatic Cancer. 152, Issue 5, Supplement 1, Page S897; Bi Y., Ji B., Raimondo M. How to suction pancreatic juice from the duodenum: Endoscope, 5 catheter, or cap-assisted? 86(6).2017 Gastrointestinal endoscopy. P. 1157-1159). Применение данного назопанкреатического стента позволяет при эндоскопической папилосфинктеротомии ввести зонд и получить непосредственно секрет поджелудочной железы. Недостатком данного назопанкреатического стента является его травматичность, что может стать причиной развития панкреатита, холангита или механической желтухи. Выполнение эндоскопической ретроградной холангиопанкреатографии в 3-10% случаев может служить причиной острого панкреатита, поэтому в данном случае всем пациентам приходится назначать специальную профилактическую терапию. Кроме того, при проведении папилосфинктеротомии можно повредить крупный сосуд, что может привести к кровотечению. Следует отметить, что известный назопанкреатический стент может быть использован только в высоко специализированных центрах при наличии специалиста, владеющего данной методикой.
Кроме того, известен двупросветный дуоденальный зонд, устанавливаемый через носовой проход под контролем эндоскопа с обеспечением его продвижения через пилородуоденальную зону (Bi Y., Ji B., Raimondo M. How to suction pancreatic juice from the duodenum: Endoscope, catheter, or cap-assisted? 86(6).2017 Gastrointestinal endoscopy. P. 1157-1159; Go VL, Hofmann AF, Summerskill WH. Simultaneous measurements of total pancreatic, biliary, and gastric outputs in man using a perfusion technique. Gastroenterology 1970;58:321-8). Недостаток такого дуоденального зонда заключается в невозможности осуществления селективного забора панкреатического сока и желчи, а также в отсутствии препятствия перемешиванию экскрета с кишечным и желудочным содержимым, что приводит к активизации ферментов и разрушения содержащегося в нём биологического материала. Кроме того, следует отметить, что конструкция такого дуоденального зонда не позволяет влиять непосредственно на отток панкреатического сока из поджелудочной железы, вследствие чего для выполнения исследования необходимо стимулировать секретином поджелудочную железу.
Кроме того, известно устройство для аспирации панкреатического сока с помощью эндоскопа в виде насаживаемого на фиброскоп колпачка, который после стимулирования экзокринной функции органа позволяет собирать секрет поджелудочной железы (Suenaga M, Sadakari Y, Almario JA, et al. Using an endoscopic distal cap to collect pancreatic fluid from the ampulla (with video). Gastrointest Endosc 2017;86:1152-6). Недостатками данного известного устройства являются сложность процедуры, провести которую можно лишь в высокоспециализированных центрах, и небольшое количество получаемого секрета поджелудочной железы, являющееся критическим аспектом при молекулярном тестировании. В данном случае процедуру, основанную на использовании этого известного устройства, выполняют с использованием анестезиологического пособия, при этом она не может выполняться длительно.
Известен способ диагностики в крови вирусных гепатитов с помощью серологических и молеклярно-генетических методов, тем не менее в 20% случаевзаболевание остаётся не верифицированным, что обсуловлено, в частности, жизненным циклом вируса, а также обусловлено тропностью не только к гепатоцитам, но и к эпителию желчных протоков, вызывая вирусный холангит и хронизацию заболевания (Шахгильдян И.В., Михайлов М.И., Онищенко Г.Г. Парентеральные вирусные гепатиты (эпидемиология, диагностика, профилактика). М.: ГОУ ВУНМЦ МЗ РФ, 2003; ; Burgart L.J. Cholangitis in Viral Disease. Mayo Clinic Proceedings; V. 73 (5); 479 -482).
Известен способ диагностики заболеваний печени (вирусные гепатиты, аутоиммунные гепатиты, склерозирующий холангит, опухоли печени) с помощью чрескожной биопсии, с последующим гистологическим и молекулярно-генетическим анализом (Bunt E.M. Liver Biopsy Diagnosis of Hepatitis: Clues to Clinically-Meaningful Reporting. Mo Med. 2010; 107(2): 113–118). В ряде случаев применение такого известного способа приводит к осложнениям (кроовотечения, желчный перитонит), а также не выявляет до 30% патологических изменений.
Кроме того, известен способ лечения острого панкреатита, путем стентирования главного панкреатического протока для восстановления оттока ферментов поджелудочной железы. Данный способ используют для лечения и профилактики панкреатита после выполнения эндоскопической ретроградной холангиопанкреатографии (Можаровский В.В., Мутных А.Г., Жуков И.Н., Можаровский К.В. Влияние стентирования главного панкреатического протока на результаты лечения больных с острым панкреатитом. Хирургия. Журнал им. Н.И. Пирогова. 2019; (9):13-17; Dumonceau JM., Andriulli A., Elmunzer BJ., et al. Prophylaxis of post-ERCP pancreatitis: European Society of Gastrointestinal Endoscopy (ESGE) Guideline - updated June 2014. Endoscopy. 2014 Sep; 46(9):799-815). Недостаток данного известного способа заключается в том, что процедура стентирования может быть осуществлена только в высоко специализированных центрах, при этом в ряде случаев указанная процедура вообще не может быть осуществлена по причине анатомических особенностей строения протоковой системы пациента, а главное она не решает проблему панкреатита по причине нарушения оттока панкреатического сока вследствие пареза двенадцатиперстной кишки.
Наиболее близким аналогом (прототипом) предлагаемого изобретения является устройство для лечения панкреатита (патент РФ №2607929; A61M 25/01, A61M 25/04, A61M 25/14; опубл. 11.01.2017), выполненного в виде дуоденального зонда или катетера. Катетер, описанный в RU 2607929, использует тот же самый принцип забора биологических жидкостей, в частности панкреатического сока и желчи, что и предложенное изобретение, а именно создание вокруг дуоденального сосочка отрицательного давления (разрежения воздуха).
Недостаток катетера по RU 2607929 заключается в чрезмерных трудозатратности и длительности процесса правильной установки данного катетера в просвете двенадцатиперстной кишки пациента по отношению к дуоденальным сосочкам, что обусловлено, в частности, необходимостью точного позиционирования фиксирующего приспособления этого известного катетера над дуоденальными сосочками. Следует также отметить, что в ряде случаев, например, в случае прорастания рака поджелудочной железы в просвет двенадцатиперстной кишки, необходимость точного позиционирования фиксирующего приспособления над дуоденальными сосочками делает процесс правильной установки катетера по RU 2607929 вообще невозможным или крайне длительным и трудозатратным.
Таким образом, очевидна потребность в дальнейшем совершенствовании катетеров для забора биологических жидкостей из дуоденальных сосочков, в частности для ускорения процесса установки таких катетеров по отношению к дуоденальным сосочкам в просвете двенадцатиперстной кишки пациента.
Следовательно, техническая проблема, решаемая настоящим изобретением, состоит в создании катетера для забора биологических жидкостей из дуоденальных сосочков, в котором по меньшей мере частично устранен обозначенный выше недостаток известного катетера для забора биологических жидкостей из дуоденальных сосочков, заключающийся в чрезмерной длительности установки данного известного катетера в просвете двенадцатиперстной кишки пациента по отношению к дуоденальным сосочкам.
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Задача настоящего изобретения состоит в создании катетера для забора биологических жидкостей из дуоденальных сосочков, решающего по меньшей мере обозначенную выше техническую проблему.
В одном из аспектов настоящего изобретения поставленная задача решена благодаря тому, что в предложенном 5 катетере для забора биологических жидкостей из дуоденальных сосочков, содержащем удлиненное тело, выполненное с возможностью его установки в просвет двенадцатиперстной кишки человека, указанное тело оснащено двумя баллонами, выполненными с возможностью раздувания с обеспечением возможности изолирования между ними пространства двенадцатиперстной кишки, в котором находится дуоденальный сосочек, причём в указанном теле проходит аспирационный канал с впускным отверстием, выполненным в указанном теле между указанными баллонами, а аспирационный канал обеспечивает возможность создания в указанном изолированном пространстве разряжения воздуха с обеспечением возможности забора из него биологических жидкостей, получаемых из дуоденальных сосочков.
Катетер для забора биологических жидкостей из дуоденальных сосочков согласно настоящему изобретению обеспечивает технический результат, заключающийся в упрощении установки такого катетера в просвете двенадцатиперстной кишки человека для обеспечения забора биологических жидкостей, получаемых из дуоденальных сосочков, в частности благодаря отсутствию необходимости в точном позиционировании аспирационного отверстия напротив дуоденальных сосочков, поскольку в настоящем изобретении в целом достаточно изолировать, посредством изолирующих баллонов катетера, пространство в просвете двенадцатиперстной кишки человека, в котором будут находиться дуоденальные сосочки, от других отделов желудочно-кишечного тракта, а разрежение воздуха, которое может быть создано в указанном изолированном пространстве благодаря наличию аспирационного канала, проходящего в теле катетера, обеспечит забор указанных биологических жидкостей путем их всасывания через аспирационное отверстие вне зависимости от места нахождения биологических жидкостей по отношению к аспирационному отверстию или местоположения аспирационного отверстия по отношению к дуоденальным сосочкам.
В одном из вариантов реализации настоящего изобретения в теле катетера может проходить дополнительный канал, обеспечивающий возможность подачи в указанные баллоны текучей среды для их раздувания. Подача текучей среды в баллоны катетера по дополнительному каналу, выполненному в теле катетера, для их раздувания обеспечивает дополнительный технический результат, заключающийся в упрощении поддержания или сохранения размеров баллонов, необходимых для изолирования пространства в просвете двенадцатиперстной кишки, в котором находится дуоденальный сосочек, а также позволяет регулировать размеры или степень раздутия баллонов катетера.
Еще в одном варианте реализации настоящего изобретения в теле катетера может проходить ещё один канал, выполненный с возможностью подачи в него текучей среды и имеющий выпускное отверстие, выполненное на дистальном конце катетера, используемом для вставки катетера в просвет двенадцатиперстной кишки человека. Наличие подобного канала в теле катетера обеспечивает дополнительный технический результат, заключающийся в обеспечении возможности санации желудка и двенадцатиперстной кишки пациента при одновременном осуществлении забора биологических жидкостей из дуоденальных сосочков и/или возможности подачи смеси для энтерального питания, которая может полностью обеспечивать потребность организма пациента в основных питательных веществах, энергии, витаминах, макронутриентах, микронутриентах и/или т.п., в полость желудка и двенадцатиперстной кишки при одновременном осуществлении забора биологических жидкостей из дуоденальных сосочков, что в конечном итоге позволяет осуществлять забор биологических жидкостей, получаемых из дуоденальных сосочков, в течение продолжительного периода времени.
Еще в другом варианте реализации настоящего изобретения каналы в катетере могут быть герметично изолированы друг от друга. Герметичное изолирование каналов в катетере обеспечивает дополнительный технический результат, заключающийся, в частности, в предотвращении возможности попадания различного содержимого в аспирационный канал из других каналов катетера и, следовательно, его смешивания с биологическими жидкостями, что могло бы оказать влияние на достоверность или показательность результатов последующего анализа таких биологических жидкостей.
В некоторых вариантах реализации настоящего изобретения канал катетера с выпускным отверстием на дистальном конце катетера может быть дополнительно снабжен отверстиями, выполненными в теле катетера за пределами его части, ограниченной баллонами катетера. Наличие таких дополнительных отверстий в теле катетера обеспечивает дополнительный технический результат, заключающийся в предотвращении или исключении возможности формирования застойных и/или воспалительных процессов в двенадцатиперстной кишке пациента вследствие, в частности, накопления слизи и прочего желудочного содержимого в двенадцатиперстной кишке пациента за пределами надутого изолирующего баллона, расположенного дальше или наиболее удаленного от дистального конца катетера, поскольку в настоящем изобретении указанные слизь и прочее желудочное содержимое могут попасть в одни из таких дополнительных отверстий, выполненных в теле катетера за пределами баллона катетера, наиболее удаленного от дистального конца катетера, и выйти из других таких дополнительных отверстий, выполненных в теле катетера за пределами баллона катетера, приближенного к дистальному концу катетера.
В других вариантах реализации настоящего изобретения аспирационное отверстие катетера может находиться между двумя ограждающими выступами, которыми может быть дополнительно снабжено тело катетера. Выступы, ограждающие аспирационное отверстие на теле катетера, обеспечивают дополнительный технический результат, заключающийся в предотвращении возможности всасывания или засасывания ткани слизистой двенадцатиперстной кишки в аспирационное отверстие, поскольку благодаря таким ограждающим выступам аспирационное отверстие не сможет войти в прямой контакт с указанной слизистой или непосредственно приблизиться к ней на расстояние, достаточное для её засасывания при создании разрежения воздуха в пространстве двенадцатиперстной кишки, изолированном баллонами катетера.
В одном из вариантов реализации настоящего изобретения ограждающие выступы тела катетера могут иметь кольцевую форму и могут быть расположены рядом или вплотную к аспирационному отверстию. Такие форма ограждающих выступов и их расположение по отношению к аспирационному отверстию также обеспечивают сформулированный выше дополнительный технический результат, заключающийся в предотвращении возможности всасывания или засасывания ткани слизистой двенадцатиперстной кишки в аспирационное отверстие.
В другом аспекте настоящего изобретения поставленная задача решена благодаря тому, что в предложенной системе для забора биологических жидкостей из дуоденальных сосочков, содержащей аспирационное устройство, соединенное с аспирационным каналом с обеспечением возможности отсасывания из него воздуха, имеется катетер для забора биологических жидкостей из дуоденальных сосочков согласно любому из вышеописанных вариантов реализации.
Еще в одном спекте настоящего изобретения поставленная задача решена благодаря тому, что предложенный способ забора биологических жидкостей из дуоденальных сосочков включает в себя установку катетера по любому из пп. 1-7 в просвет двенадцатиперстной кишки человека; раздувание баллонов катетера для изолирования между ними пространства двенадцатиперстной кишки, в котором находится дуоденальный сосочек; и создание, посредством аспирационного канала катетера, в указанном изолированном пространстве разрежения воздуха для забора из него биологических жидкостей, получаемых из дуоденальных сосочков.
В одном из вариантов реализации настоящего изобретения при установке катетера один из его баллонов может быть размещен в луковице двенадцатиперстной кишки человека. Размещение одного из баллонов катетера в луковице двенадцатиперстной кишки человека при его установке обеспечивает дополнительный технический результат, заключающийся в улучшении фиксации катетера в просвете двенадцатиперстной кишки человека в месте его установки.
В другом аспекте настоящего изобретения установка катетера может быть осуществлена под контролем эндоскопа. Контроль установки катетера эндоскопом обеспечивает дополнительный технический результат, заключающийся в повышении точности позиционирования катетера в двенадцатиперстной кишке человека, возможности визуального контроля степени раздутия баллонов катетера и предотвращении возможности повреждения слизистой по мере продвижения катетера в место его установки в просвете двенадцатиперстной кишки человека.
Предложенный катетер для забора биологических жидкостей из дуоденальных сосочков согласно любому из вышеописанных вариантов реализации настоящего изобретения может быть применен для диагностики или мониторинга течения по меньшей мере одного из следующих заболеваний: гастрит, панкреатит, рак поджелудочной железы, рак желчевыводящих протоков, холангиокарцинома, гепатоцеллюлярный рак, холангит, желчнокаменная болезнь, аутоиммунный гепатит и инфекционный гепатит.
Кроме того, предложенный катетер для забора биологических жидкостей из дуоденальных сосочков согласно любому из вышеописанных вариантов реализации настоящего изобретения может быть применен для лечения по меньшей мере одного из следующих заболеваний: панкреатит и холангит.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Прилагаемые чертежи, которые приведены для обеспечения лучшего понимания сущности настоящего изобретения, составляют часть настоящего документа и включены в него для иллюстрации нижеописанных вариантов реализации настоящего изобретения. Прилагаемые чертежи в сочетании с приведенным ниже описанием служат для пояснения сущности настоящего изобретения. На чертежах:
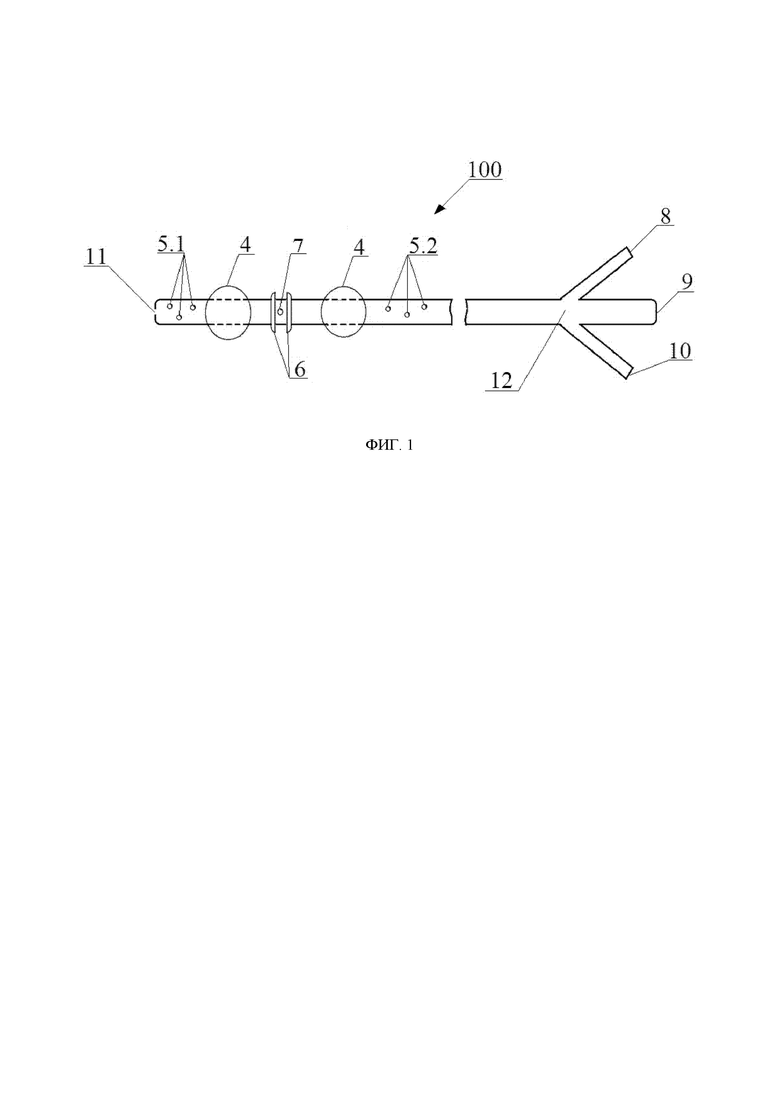
на фиг. 1 схематически показан катетер согласно настоящему изобретению;
на фиг. 2 схематически показана часть катетера, показанного на фиг. 1, с аспирационным отверстием.
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
В настоящее время наиболее перспективным методом диагностики для выявления рака поджелудочной железы в начальной стадии и предраковой трансформации является жидкостная биопсия, основанная на выявлении в биологических жидкостях организма (таких как кровь и панкреатический сок) циркулирующих патологических клеток или циркулирующую опухолевую ДНК, а также циркулирующие опухолевые экзосомы.
Одним из критических аспектов данного исследовании является количество получаемого материала, в связи с чем для выполнения диагностики необходимо иметь достаточное количество получаемого материала. Еще одним критическим аспектом данного исследовании является определение локализации опухоли, поскольку выделенный из образца патологический генетический материал может быть присущ ракам различных органов. По этой причине для диагностики рака, муцинозных и интраэпителиальных неоплазм поджелудочной железы наиболее подходящей диагностической жидкостью, в которой следует выявлять циркулирующие опухолевые клетки, ДНК экзосомы, является панкреатический сок. Однако, именно забор панкреатического сока и является наиболее сложной задачей.
Следует отметить, что сам дуоденальный или Фатеров сосок или сосочек представляет собой анатомическую структуру в виде полусферического, конусовидного или уплощенного возвышения, расположенного на конце продольной складки слизистой оболочки в середине нисходящей части двенадцатиперстной кишки примерно на 12-14 см. ниже привратника, при этом в большинстве случаев он открывается в просвет двенадцатиперстной кишки одним отверстием, общим для желчного и панкреатического протоков, а в остальных случаях панкреатический проток открывается на 2-4 см выше дуоденального сосочка. В дуоденальном сосочке располагается печеночно-поджелудочная ампула, в которую поступает желчь и пищеварительные соки поджелудочной железы, а также расположен сфинктер Одди, регулирующий поступление желчи и панкреатического сока в двенадцатиперстную кишку и не допускающий попадание содержимого кишечника в желчный и панкреатический протоки.
В частности, для обеспечения попадания панкреатического сока в просвет двенадцатиперстной кишки требуется создание за счет перистальтики самого кишечника отрицательного давления вокруг фатерова или дуоденального сосочка на уровне 70-100 мм.вод.ст., являющееся физиологическим давлением (Физиология пищеварения. С. Теэсалу. 1987. Тарту. Тартуский 5 государственный университет. С. 84; The Pancreas. Third edition. 2018. Blackwell. UK. 1300). Ещё одним критерием является необходимость изолированного забора панкреатического сока без желудочного и дуоденального содержимого с неактивными дигестивными ферментами, поскольку в противном случае энзимы будут расщеплять необходимые для диагностики аминокислоты, экзосомы, ДНК и клетки.
На фиг. 1 и 2 схематически показан катетер 100 согласно настоящему изобретению, который представляет собой зонд, устанавливаемый пользователем в просвет двенадцатиперстной кишки пациента, при этом корпус или тело катетера 100 выполнено в виде гибкой полой трубки, которой приданы размеры, в частности длина и 15 толщина, подходящие для её вставки или продвижения пользователем в место установки в просвете двенадцатиперстной кишки пациента. В качестве пользователя катетера 100 может выступать любой надлежащим образом, обученный медицинский работник, такой как, например, врач-хирург, врач-онколог, врач-эндоскопист и т.п. В качестве пациента, для которого используют катетер 100, может выступать человек.
Катетер 100, показанный на фиг. 1, снабжен осевым отверстием 11 на своём дистальном конце, которым катетер 100 вставляют или вводят в носовой ход пациента с последующим продвижением в двенадцатиперстную кишку пациента в место его установки в двенадцатиперстной кишке пациента, и снабжен тройником 12 на своём проксимальном конце, противоположном дистальному концу катетера 100 и находящемся за пределами тела пациента при установке катетера 100 в двенадцатиперстную кишку пациента.
Как показано на фиг. 1, тройник 12 в катетере 100 представляет собой патрубок или трубку с тремя ответвлениями или выводами: центральным выводом 9 и двумя боковыми выводами 8, 10, герметически изолированными от центрального вывода 9, при этом указанные выводы 8, 9, 10 снабжены каждый на своём свободном конце соответствующим отверстием и выполнены каждый с возможностью подключения или присоединения соответствующего функционального устройства или приспособления.
Центральный вывод 9 в тройнике 12 выполнен с возможностью подключения или присоединения к нему приспособления или устройства для подачи текучей среды (не показано), например смеси для энтерального питания. В качестве такого устройства для подачи текучей среды, соединяемого с центральным выводом 9, может быть использован, например, медицинский шприц, наполненный, например, смесью для энтерального питания, которая может полностью обеспечивать потребность организма пациента в основных питательных веществах, энергии, витаминах, макронутриентах, микронутриентах и/или т.п., а также медицинская 5 капельница, наполненная, например, смесью для энтерального питания, или другие устройства и приспособления, в том числе автоматизированные или полуавтоматизированные, подходящие для подключения к центральному выводу 9 с обеспечением подачи в него текучей среды, например смеси для энтерального питания. Таким образом, устройство для подачи текучей среды, подключенное или присоединенное к центральному выводу 9, может быть использовано для обеспечения, например, нутритивной поддержки или клинического питания пациента при установке в просвете его двенадцатиперстной кишки катетера 100. Кроме того, устройство для подачи текучей среды, подключенное или присоединенное к центральному выводу 9, может быть использовано для санации желудка и двенадцатиперстной кишки пациента.
Боковой вывод 8 в тройнике 12 выполнен с возможностью подключения или присоединения к нему медицинского отсасывателя, аспирационного устройства или аспиратора (не показан), содержащего накопительный контейнер или накопительную ёмкость для сбора жидкости или текучей среды (не показана) и воздушный компрессор (не показан) для высасывания или отсасывания воздуха.
Другой боковой вывод 10 в тройнике 12 выполнен с возможностью подключения или присоединения к нему приспособления или устройства для подачи текучей среды под напором или давлением (не показано), например воды, при этом в качестве такого устройства для подачи текучей среды может быть использован, например, медицинский шприц, наполненный подаваемой текучей средой, а также медицинская капельница, наполненая подаваемой текучей средой, или другие устройства и приспособления, в том числе автоматизированные или полуавтоматизированные, подходящие для подключения к боковому выводу 10 с обеспечением подачи в него указанной текучей среды.
Следует отметить, что устройство для подачи текучей среды (не показано), такой как, например, смесь для энтерального питания, соединяемое с центральным выводом 9 катетера 100, аспирационное устройство (не показано), соединяемое с боковым выводом 8 катетера 100, и/или устройство для подачи текучей среды (не показано), такой как, например, вода, соединяемое с боковым выводом 10 катетера 100, в сочетании с самим катетером 100, показанным на фиг. 1-2, могут образовывать систему для забора биологической жидкости (не показана), в частности панкреатического сока и желчи, или входить в состав такой системы.
Кроме того, как показано на фиг. 1-2, тело катетера 100 снабжено со своей наружной стороны двумя изолирующими баллонами 4, которые представляют собой каждый расправляющийся или раздувающийся мягкий резервуар и которые расположены на заданном расстоянии друг от друга и от дистального конца катетера 100. Между изолирующими баллонами 4 в теле катетера 100 выполнено аспирационное устье или отверстие 7, при этом при установке катетера 100 в просвет двенадцатиперстной кишки пациента один из изолирующих баллонов 4, наиболее удаленный от дистального конца катетера 100, оказывается расположенным в луковице двенадцатиперстной кишки, а аспирационное отверстие 7 находится напротив дуоденального сосочка или рядом с ним.
Кроме того, катетер 100 содержит три отдельных функциональных канала, выполненных в удлиненном теле катетера 100: основной канал 1, подающий канал 2 для подачи текучей среды, герметически изолированный от основного канала 1 и снабженный отверстиями, выполненными в теле катетера 100 и открытыми каждое внутрь соответствующего одного из изолирующих баллонов 4, и аспирационный канал 3, отделенный от подающего канала 2 и герметически изолированный от основного канала 1, при этом подающий канал 2 и аспирационный канал 3 проходят в пределах части основного канала 1 по его длине.
Основной канал 1, проходящий в целом по всей длине катетера 100, сообщается с центральным выводом 9 тройника 12, при этом основной канал 1 имеет входное или впускное отверстие, соответствующее отверстию, выполненному в центральном выводе 9 на проксимальном конце катетера 100, и выходное или выпускное отверстие, соответствующее осевому отверстию 11 на дистальном конце катетера 100. При установке катетера 100 в просвет двенадцатиперстной кишки пациента впускное отверстие основного канала 1 оказывается открытым наружу с обеспечением сообщения с внешней или окружающей средой, а выпускное отверстие основного канала 1 оказывается открытым в полость желудка и двенадцатиперстной кишки. Таким образом, при присоединении к центральному выводу 9 тройника 12 вышеописанного устройства для подачи энтерального питания (не показано) обеспечена возможность подачи под напором или давлением смеси для энтерального питания из указанного устройства сначала в центральный вывод 9 через выполненное в нём отверстие, далее из центрального вывода 9 в основной канал 1, а затем из основного канала 1 в полость желудка и двенадцатиперстной кишки через осевое отверстие 11.
Подающий канал 2, проходящий в целом вдоль части длины катетера 100, сообщается с каждым из изолирующих баллонов 4 посредством соответствующего одного из выходных отверстий 13, 14, 5 выполненных в теле катетера 100, как показано на фиг. 2, и сообщается с боковом выводом 10 тройника 12, при этом подающий канал 2 имеет входное или впускное отверстие, соответствующее отверстию, выполненному в боковом выводе 10 на проксимальном конце катетера 100. При установке катетера 100 в просвет двенадцатиперстной кишки пациента впускное отверстие подающего канала 2 оказывается открытым наружу с обеспечением сообщения с внешней или окружающей средой. Таким образом, при присоединении к боковому выводу 10 тройника 12 вышеописанного устройства для подачи подачи текучей среды (не показано) обеспечена возможность подачи под напором текучей среды, например воды, в заданном объеме из указанного устройства сначала в боковой вывод 10 через выполненное в нём отверстие, далее из бокового вывода 10 в подающий канал 2, а затем из подающего канала 2 в оба изолирующих баллона 4 через соответствующие отверстия, выполненные в теле катетера 100, в результате чего происходит заполнение или наполнение изолирующих баллонов 4 водой с использованием, в частности, подающего канала 2 катетера 100 с обеспечением их раздувания, характеризующегося увеличением их размера или объема. Следует отметить, что увеличение размера или объема изолирующих баллонов 4 в результате приводит к двустороннему обтурированию или закупориванию просвета двенадцатиперстной кишки пациента, в котором установлен катетер 100, что позволяет изолировать часть катетера 100 с аспирационным отверстием 7 между раздутыми изолирующими баллонами 4 в двенадцатиперстной кишке пациента. Таким образом, раздутые изолирующие баллоны 4 позволяют изолировать дуоденальный сосок двенадцатиперстной кишки пациента от проксимальных и дистальных отделов желудочно-кишечного тракта и, следовательно, исключить или предотвратить смешивание целевой биологической жидкости, которая по сути представляет собой смесь панкреатического сока и желчи, с иными биологическими жидкостями, такими как желудочное содержимое и/или дуоденальное содержимое с неактивными дигестивными ферментами, а также позволяет зафиксировать катетер 100 в просвете двенадцатиперстной кишки пациента за счет плотного прилегания баллонов 4 своей наружной стороной к слизистой двенадцатиперстной кишки. В одном из вариантов реализации настоящего изобретения изолирующие баллоны 4 могут быть выполнены каждый в виде, например, самонадувающихся баллонов или баллонов, надуваемых воздухом, подаваемым в подающий канал 2 катетера 100 через отверстие бокового вывода 10 тройника 12, или баллон, раздуваемый любым иным способом, известным в уровне техники.
В одном из вариантов реализации настоящего изобретения боковой вывод 10 в тройнике 12 может быть дополнительно снабжен запорным клапаном (не показан) с ручным управлением, который препятствует обратному ходу или выходу текучей среды, в частности воды, находящейся в изолирующих баллонах 4, подающем канале 2 и боковом выводе 10. Следует также отметить, что вышеописанный запорный клапан может быть использован пользователем катетера 100 для регулирования степени раздувания изолирующих баллонов 4, которую пользователь может визуально контролировать посредством эндоскопа, в частности пользователь может уменьшать размеры или объем надутых изолирующих баллонов 4 путем отведения или стравливания воды из подающего канала 4 при ручном приоткрытии запорного клапана пользователем.
Аспирационный канал 3, проходящий в целом вдоль части длины катетера 100, сообщается с боковым выводом 8 тройника 12, при этом аспирационный канал 3 имеет входное или впускное отверстие, соответствующее аспирационному отверстию 7, и выходное или выпускное отверстие, соответствующее отверстию, выполненному в боковом выводе 8 на проксимальном конце катетера 100. Таким образом, при присоединении к боковому выводу 8 тройника 12 вышеописанного аспирационного устройства (не показано) с накопительной ёмкостью обеспечена возможность создания и поддержания разрежения воздуха в пространстве двенадцатиперстной кишки, которое может быть изолировано надутыми изолирующими баллонами 4, как это описано выше. Разрежение воздуха (также называемое техническим вакуумом), созданное в изолированном пространстве двенадцатиперстной кишки, способствует эвакуации или выводу биологической жидкости, представляющей собой желчь и панкреатический сок или секрет поджелудочной железы, через дуоденальный сосочек из поджелудочной железы с обеспечением возможности его отведения из указанного изолированного пространства сначала в аспирационный канал 3 через аспирационное отверстие 7, далее из аспирационного канала 3 в боковой вывод 8, а затем из бокового вывода 8 в накопительную ёмкость аспирационного устройства через соответствующее отверстие, выполненное в боковом выводе 8.
Следует отметить, что включение пользователем аспирационного устройства, присоединённого к боковому выводу 8 тройника 12, приводит в действие воздушный компрессор, входящий в состав этого аспирационного устройства. Приведенный в действие воздушный компрессор обеспечивает выкачивание или отсасывание воздуха из пространства двенадцатиперстной кишки пациента, изолированного надутыми изолирующими баллонами 4 вышеописанным образом, и из свободного пространства в накопительной ёмкости аспирационного устройства, которое не заполнено биологической жидкостью, представляющей собой 5 желчь и панкреатический сок или секрет поджелудочной железы, для создания разрежения воздуха в указанном изолированном пространстве в просвете двенадцатиперстной кишки пациента, что приводит к забору указанной биологической жидкости через аспирационное отверстие 7 и её отведению или доставке посредством аспирационного канала 3 в накопительную ёмкость аспирационного устройства, в которой эта биологическая жидкость может постепенно накапливаться или собираться в течение заданного периода времени.
В одном из вариантов реализации настоящего изобретения в теле катетера 100 могут быть выполнены только вышеописанный подающий канал 2 для подачи текучей среды (например, воды) в изолирующие баллоны 4, сообщающийся с вышеописанным боковым выводом 10, и вышеописанный аспирационный канал 3, сообщающийся с вышеописанным боковым выводом 8.
Кроме того, тело катетера 100 снабжено со своей наружной стороны двумя в целом одинаковыми выпуклостями 6, которые выполнены каждая в виде кольцеобразного выступа или кольца, радиус которого больше радиуса тела катетера 100 и меньше радиуса любого из надутых изолирующих баллонов 4, и каждая из которых расположена по длине тела катетера 100 по одну из сторон от аспирационного отверстия 7 рядом с ним или вплотную к нему, при этом выпуклости 6 предпочтительно расположены на одинаковом расстоянии от аспирационного отверстия 7 в промежутке между изолирующими баллонами 4. Следует отметить, что при установке катетера 100 в просвет двенадцатиперстной кишки пациента выпуклости 6, по сути выполняющие функцию выступающих бортов, ограждающих аспирационное отверстие 7, предотвращают контакт или приближение аспирационного отверстия 7 к слизистой указанной двенадцатиперстной кишки на расстояние, достаточное для всасывания или засасывания ткани указанной слизистой в аспирационное отверстие 7 при включении пользователем аспирационного устройства, подключенного к аспирационному каналу 3 катетера 100 и, следовательно, создании разрежения в изолированном пространстве в просвете двенадцатиперстной кишки, что может привести к повреждению ткани слизистой двенадцатиперстной кишки. В одном из вариантов реализации настоящего изобретения выпуклости 6 могут иметь любую другую форму, отличную от кольцевой или кольцеобразной формы, при условии эта форма позволяет исключить контакт аспирационного отверстия 7 со слизистой двенадцатиперстной кишки пациента или сближение аспирационного отверстия 7 со слизистой двенадцатиперстной кишки пациента на расстояние, достаточное для всасывания указанной слизистой в аспирационное отверстие 7 при создании разрежения в изолированном пространстве двенадцатиперстной кишки, в которое открыто это аспирационное отверстие 7.
Кроме того, за пределами изолирующих баллонов 4 и, следовательно, части катетера 100 с аспирационным отверстием 7, ограниченной изолирующими баллонами 4, в теле катетера 100 выполнены по три вспомогательных отверстия 5.1, 5.2, при этом при установке катетера 100 в просвет двенадцатиперстной кишки пациента вспомогательные отверстия 5.2, расположенные дальше от дистального конца катетера 100, выполняют функцию впускных отверстий, а вспомогательные отверстия 5.1, расположенные ближе к дистальному концу катетера 100, выполняют функцию выпускных отверстий. Следует отметить, что вспомогательные отверстия 5.1, 5.2 обеспечивают возможность пропускания желудочного содержимого и/или дуоденального содержимого с неактивными дигестивными ферментами в дистальные отделы двенадцатиперстной кишки без попадания указанного содержимого в область двенадцатиперстной кишки пациента с дуоденальным сосочком, изолированную надутыми изолирующими баллонами 4 катетера 100, что в конечном итоге предотвращает или исключает возможность формирования застойных и/или воспалительных процессов в двенадцатиперстной кишке пациента вследствие, в частности, накопления слизи и прочего желудочного содержимого в двенадцатиперстной кишке пациента за пределами надутого изолирующего баллона 4, расположенного дальше или наиболее удаленного от дистального конца катетера 100.
В одном из вариантов реализации настоящего изобретения катетер 100 может иметь длину 130 см. В данном варианте реализации настоящего изобретения изолирующие баллоны 4 находятся соответственно на расстоянии 15 и 25 см от дистального конца катетера 100, которым его вставляют полость желудка и просвет двенадцатиперстной кишки пациента, так что при расправлении или раздувании изолирующие баллоны 4 позволяют изолировать зону двенадцатиперстной кишки длиной по меньшей мере 10 см. В данном варианте реализации настоящего изобретения аспирационное отверстие 7 может находиться посередине между изолирующими баллонами 4, т.е. на расстоянии 5 см от каждого из изолирующих баллонов 4 и на расстоянии 20 см от дистального конца катетера 100.
Использование катетера 100 согласно настоящему изобретению заключается в его установке пользователем в просвет двенадцатиперстной кишки пациента под контролем эндоскопа (не показан) таким образом, чтобы один из изолирующих баллонов 4, наиболее удаленный от дистального конца катетера 100, находился в луковице двенадцатиперстной кишки пациента, при этом манипулировать эндоскопом может как указанный пользователь, так и врач-эндоскопист, ассистирующий указанному пользователю. Следует отметить, что процесс установки катетера 100 в просвет двенадцатиперстной кишки пациента, процесс удаления катетера 100 из просвета двенадцатиперстной кишки пациента после забора необходимого количества биологической жидкости и сам процесс аспирации являются атравматичными и не зависят от анатомических особенностей как самого пациента, так и новообразования.
Согласно одному из примеров, катетер 100 может быть предварительно снабжен по меньшей мере одной петлей, подходящей для её захвата биопсийными щипцами. Для установки катетера 100 в необходимое место установки в двенадцатиперстной кишке пациента дистальный конец катетера 100, хорошо смазанный вазелиновым маслом, вводят через носовой ход и продвигают в полость желудка, в дальнейшем через ротовую полость пациента параллельно катетеру 100 в полость желудка пациента вводят или продвигают эндоскоп с обеспечением захвата биопсийными щипцами эндоскопа катетера 100 за его петли, а затем захваченный катетер 100 проводят или продвигают одновременно с эндоскопом в двенадцатиперстную кишку пациента. В дальнейшем под контролем эндоскопа размещают один из изолирующих баллонов 4 катетера 100, наиболее удаленный от дистального конца катетера 100, в луковице двенадцатиперстной кишки пациента.
Согласно еще одному примеру, в основной канал 1 катетера 100 может быть предварительно введен или вставлен металлический проволочный направитель. Для установки катетера 100 в необходимое место установки в двенадцатиперстной кишке пациента дистальный конец катетера 100, хорошо смазанный вазелиновым маслом, вводят через носовой ход и продвигают в полость желудка с использованием металлического проволочного направителя катетера 100, а затем через ротовую полость пациента параллельно катетеру 100 в полость желудка пациента вводят или продвигают эндоскоп с обеспечением захвата биопсийными щипцами эндоскопа первой лигатуры при обнаружении дистального конца катетера 100 и прижатия катетера 100 к эндоскопу путем подтягивания катетера 100 за захваченную первую лигатуру. В дальнейшем эндоскоп с прижатым к нему катетером 100 проводят через привратник в двенадцатиперстную кишку пациента и размещают под контролем эндоскопа один из изолирующих баллонов 4 катетера 100, наиболее удаленный от дистального конца катетера 100, в луковице двенадцатиперстной кишки пациента.
В дальнейшем к боковому выводу 10 тройника 12 пользователь подключает или присоединяет устройство для подачи текучей среды (не показано), которое обеспечивает подачу текучей среды, такой как, например, вода, в подающий канал 2 катетера 100 в необходимом объеме, в частности 40 мл, происходит расправление и раздувание изолирующих баллонов 4 с их плотным прилеганием к слизистой двенадцатиперстной кишки, что приводит к изолированию необходимой зоны двенадцатиперстной кишки пациента, содержащей дуоденальный сосочек, в частности от попадания в неё желудочного содержимого и/или дуоденального содержимого с неактивными дигестивными ферментами. В частности, следует отметить, что автором данного документа в результате экспериментальных исследований было выявлено, что 40 мл воды будет достаточно для раздувания изолирующих баллонов 4 до размеров, обеспечивающих двустороннее обтурирование или закупоривание просвета двенадцатиперстной кишки пациента, в котором установлен катетер 100.
В дальнейшем пользователь подключает или присоединяет к аспирационному каналу 3 аспирационное устройство (не показано), которое должно быть предварительно настроено на постоянный или переменный режим работы, обеспечивающий необходимое рабочее давление, в зависимости от поставленной цели. Включенное пользователем аспирационное устройство (не показано) обеспечивает возможность отсасывания через аспирационное отверстие 7 и сообщающийся с ним аспирационный канал 3 воздух из пространства изолированной зоны двенадцатиперстной кишки пациента, соответствующей периампулярной зоне двенадцатиперстной кишки, с обеспечением создания в указанном пространстве отрицательного давления, соответствующего исходному давлению двенадцатиперстной кишки, создаваемому за счет перистальтики самого кишечника, в частности отрицательного давления на уровне 70-100 мм.вод.ст. (9-14 кПа). Разрежение воздуха, созданное в изолированном пространстве двенадцатиперстной кишки пациента, способствует эвакуации или выводу биологической жидкости в виде панкреатического сока или секрета поджелудочной железы в сочетании с желчью через дуоденальный сосочек из поджелудочной железы с обеспечением возможности её отведения, посредством аспирационного отверстия 7 и аспирационного канала 3, из изолированной зоны двенадцатиперстной кишки пациента и возможности её сбора в накопительной емкости аспирационного устройства (не показана). В дальнейшем биологическая жидкость, собранная в накопительной емкости аспирационного устройства (не показана), может быть отправлена на цитологическое исследование и/или молекулярно-генетическое исследование для оценки характеристик морфологической структуры клеточных элементов секрета поджелудочной железы, позволяющих устанавливать или выявлять наличие патологических процессов, характерных, например, для внутрипротоковых 5 новообразований, нейроэндокринных опухолей или рака поджелудочной железы, а также выявлять новообразования на ранней стадии развития и проводить дифференциальную диагностику между различными типами опухолей путем определения экспрессии специфических маркеров (NKX2, S100P, РЭА, MUC1, MUC2, MUC5, ANXA1, А2, KRT7, ММР7, ММР9, IGFBP3, PSCA, PRSS2, SHh, KRas, TР53, SMAD4, BRCA1).
Следует отметить, что катетер 100 согласно настоящему изобретению может находиться в установленном состоянии в течение достаточно длительного периода времени, например в течение суток (24 часа) за счет физиологических параметров человека, что позволяет собрать секрет поджелудочной железы в количестве, достаточном для достоверного выявления и верифицирования патологического опухолевого материала, что в целом улучшает эффективность диагностики и, следовательно, последующего лечения рака поджелудочной железы. Кроме того, длительный забор позволяет увеличить вероятность выявления патологических клеток не только панкреатических раков, но и желчевыводящих протоков, в том числе холангиокарцином и/или гепатоцеллюлярного рака.
Следует также отметить, что при использовании катетера 100 не требуется стимулировать выделение панкреатического сока и желчи, благодаря чему подвергающийся забору или собираемый биологический материал имеет истинный биохимический и физиологический профиль, отражающий истинную функцию печени, желчевыводящих протоков, сократительной способности желчного пузыря, а также поджелудочной железы.
При необходимости, для оценки экскреторной функции поджелудочной железы может быть исследован биохимический состав секрета поджелудочной железы, собранного вышеописанным образом в накопительной емкости (не показана) в сочетании с желчью с использованием катетера 100 согласно настоящему изобретению.
Кроме того, качественный и количественный анализ собранных панкреатического сока и желчи позволяет оценить истинный биохимический профиль обоих биологических материалов, а также установить объем суточной секреции и тем самым непосредственно диагностировать функциональное состояние органа.
Вышеописанный катетер 100, согласно настоящему изобретению, может быть применен для диагностики или мониторинга течения по меньшей мере одного из следующих заболеваний: гастрит, острый или хронический панкреатит, рак поджелудочной железы, холангит, желчнокаменная болезнь, аутоиммуный гепатит и инфекционные гепатиты.
Кроме того, при использовании катетера 100 наблюдается лечебный или терапевтический эффект, достигаемый за счет восстановления эвакуации желчи и панкреатического сока из соответствующих протоков в двенадцатиперстную кишку. В патогенезе острых воспалительных заболеваний, таких как панкреатит и холангит, лежит соответственно нарушение оттока панкреатического сока и желчи, обусловленное, в частности, нарушениями моторики двенадцатиперстной кишки человека, так что отрицательное давление на уровне 70-100 мм.вод.ст, создаваемое при осуществлении аспирации панкреатического сока и желчи с использованием катетера 100, позволяет решить эту медицинскую проблему и, следовательно, способствовать лечению вышеуказанных острых заболеваний.
ПРИМЕРЫ
Пример №1. Пациент №1 поступил с жалобами на опоясывающие боли в верхних отделах живота. Амилаза в крови составляла 1150 Ед/л. Результаты ультразвукового исследования (УЗИ): поджелудочная железа увеличена, головка 35 мм, тело 32 мм, хвост 21 мм, резко неоднородная, контур размыт, парапанкреатическая клетчатка отечна, жидкости не определяются. МСКТ картина соответствует острому отечному панкреатиту. Пациенту начата терапия согласно рекомендациям российского общества хирургов, при этом в двенадцатиперстную кишку пациента был установлен катетер 100 согласно настоящему изобретению на 24 часа, и применен метод активной аспирации. Через 24 часа уровень амилазы в крови снизился до 230 Ед/л, а болевой синдром был купирован.
Пример №2. Пациент №2 поступил с клинической картиной механической желтухи. В результате обследования был выявлен повышенный уровень лейкоцитов до 14,1*109, при этом общий билирубин составлял 145 мкмоль/л, а прямой билирубин составлял 113,2 мкмоль/л. Амилаза в крови составляла 57 Ед/л, аланинаминотрансфераза (АЛТ) составляла 391 Ед/л, а аспартатаминотрансфераза (АсТ) составляла 90 Ед/л. Результаты УЗИ: в желчном пузыре множественные конкременты до 1,3 см в диаметре, а желчные протоки расширены до 11 мм. Результаты магнитно-резонансной томографии (МРТ): в дистальном отделе холедоха имеется тень, соответствующая конкременту размером 6 мм. Результаты эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ): выявлен единичный конкремент размером 8 мм, и в дальнейшем был эндоскопически удален. Для профилактики острого панкреатита в двенадцатиперстную кишку пациента был установлен катетер 100 согласно настоящему 5 изобретению на 24 часа, и применен метод активной аспирации. В послеоперационном периоде уровень амилазы в крови не повышался более 87 Ед/л.
Пример №3. Пациент №3 поступил в плановом порядке для обследования и лечения. На выполненном ранее МСКТ выявлено образование тела поджелудочной железы. При проведении эндоскопического УЗИ был выявлено образование тела, имеющего размер 2 см х 3 см, при этом выполнение тонкоигольной биопсии оказалось технически невозможным. Для селективного забора панкреатического сока в двенадцатиперстную кишку пациента был установлен катетер 100 согласно настоящему изобретению. В результате цитологического исследования в полученном панкреатическом соке были обнаружены клетки аденокарциномы.
Пример №4. Пациент №4 поступил с клинической картиной механической желтухи. Результаты МРТ: выявлен блок на уровне конфлюенса долевых правого и левого печеночных протоков, что соответствует опухоли Клацкина типа IIA. В двенадцатиперстную кишку пациента был установлен катетер 100 согласно настоящему изобретению, и применен метод активной аспирации. В результате цитологического исследования в полученной желчи были обнаружены атипичные клетки.
Пример №5. Пациентке №5 был поставлен диагноз хронический панкреатит. Несмотря на проводимую гастроэнтерологом терапию, в том числе прием пациенткой назначенных ферментативных препаратов, у пациентки отмечались снижение массы тела, расстройства дефекации и диареи. Для оценки функционального состояния поджелудочной железы в двенадцатиперстную кишку пациента был установлен катетер 100 согласно настоящему изобретению на 24 часа, и применен метод активной аспирации. В результате биохимического исследования полученного панкреатического сока были выявлены снижение уровня альфа амилазы и липазы в крови, а также снижение объема суточной экскреции панкреатического сока и желчи. В итоге, была увеличена доза ферментативных препаратов, принимаемых пациенткой, а также были дополнительно назначены препараты урсодезоксихолевой кислоты и желчезаменители.
Пример № 6. Пациент № 6 поступил в клинический инфекционный стационар города с клиникой желтухи. При физикальном осмотре печень была увеличена, при этом результаты биохимического анализа крови были следующие: общий билирубин 329 мкмоль/л, прямой билирубин 141 мкмоль/л, АЛТ 1040 Ед/л, АсТ 804 Ед/л. Серологический анализ крови на ангтигены HCV, HBsAg отрицательный. Больному был установлен катетер 100, при этом в результате активной аспирации было получено 100 мл желчи, а в результате П 5 ЦР была выявлена высокая копийность вируса HCV.
Таким образом, вышеописанный катетер 100 позволяет осуществить или выполнить функциональное исследование состояния поджелудочной железы, а также желчевыводящих протоков и печени. Кроме того, исследование и/или лабораторный анализ биологической жидкости, собранной с использованием катетера 100, позволяет с высокой точностью дифференциально диагностировать воспалительные образования, доброкачественные образования и злокачественные образования. Следует также отметить, что катетер 100 согласно настоящему изобретению или вышеописанная система для забора биологической жидкости, в состав которой может входить катетер 100, обеспечивает возможность получения большого объема биологического материала в нормофизиологическом состоянии без дополнительной стимуляции экскреторной функции поджелудочной железы, в частности только благодаря созданию в изолированной зоне двенадцатиперстной кишки, в просвет которой вставлен катетер 100, отрицательного давления, соответствующего отрицательному физиологическому давлению, создаваемому за счет перистальтики самого кишечника.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТЕТЕР И СПОСОБ ДЛЯ СОЗДАНИЯ ИЗОЛИРОВАННОЙ ЗОНЫ В ПОЛОМ ОРГАНЕ МЛЕКОПИТАЮЩЕГО, А ТАКЖЕ СИСТЕМА НА ОСНОВЕ ТАКОГО КАТЕТЕРА И ПРИМЕНЕНИЕ ТАКОГО КАТЕТЕРА | 2020 |
|
RU2761080C1 |
| ПРИМЕНЕНИЯ КАТЕТЕРА ДЛЯ СОЗДАНИЯ ИЗОЛИРОВАННОЙ ЗОНЫ В ПОЛОМ ОРГАНЕ МЛЕКОПИТАЮЩЕГО (ВАРИАНТЫ) | 2021 |
|
RU2783089C1 |
| ПРИМЕНЕНИЯ КАТЕТЕРА ДЛЯ СОЗДАНИЯ ИЗОЛИРОВАННОЙ ОБЛАСТИ В ПОЛОМ ОРГАНЕ МЛЕКОПИТАЮЩЕГО ДЛЯ ЛЕЧЕНИЯ ПОВРЕЖДЕНИЯ СТЕНКИ ТОЩЕЙ КИШКИ ИЛИ ПОДВЗДОШНОЙ КИШКИ (ВАРИАНТЫ) | 2022 |
|
RU2807166C1 |
| ПРИМЕНЕНИЯ КАТЕТЕРА ДЛЯ СОЗДАНИЯ ИЗОЛИРОВАННОЙ ЗОНЫ В ПОЛОМ ОРГАНЕ МЛЕКОПИТАЮЩЕГО (ВАРИАНТЫ) | 2022 |
|
RU2805216C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОГО ПАНКРЕАТИТА СО СТЕНОЗОМ ГЛАВНОГО ПАНКРЕАТИЧЕСКОГО ПРОТОКА | 2007 |
|
RU2341203C1 |
| СПОСОБ ПРОФИЛАКТИКИ ОСТРОГО ПАНКРЕАТИТА ПОСЛЕ РАДИКАЛЬНОЙ ДУОДЕНОПЛАСТИКИ ПО ПОВОДУ ОСЛОЖНЕННЫХ ОКОЛОСОСОЧКОВЫХ ЯЗВ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2006 |
|
RU2340289C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ДУОДЕНАЛЬНОГО СВИЩА ПРИ НЕСОСТОЯТЕЛЬНОСТИ КУЛЬТИ ПОСЛЕ РЕЗЕКЦИИ ЖЕЛУДКА И ГАСТРЭКТОМИИ | 2010 |
|
RU2452411C1 |
| СПОСОБ ЛЕЧЕНИЯ НАРУЖНОГО СВИЩА ПРОКСИМАЛЬНОГО ОТДЕЛА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ ПОСЛЕ ГАСТРЭКТОМИИ ИЛИ РЕЗЕКЦИИ ЖЕЛУДКА С РЕКОНСТРУКЦИЕЙ ПО БИЛЬРОТ-II ПОД КОНТРОЛЕМ УЛЬТРАЗВУКА И РЕНТГЕНОСКОПИИ | 2019 |
|
RU2726603C1 |
| Способ эндоскопического лечения холедохолитиаза и профилактики постманипуляционных осложнений | 2016 |
|
RU2644307C1 |
| СПОСОБ ВЫПОЛНЕНИЯ ЧРЕСКОЖНОГО ЧРЕСПЕЧЕНОЧНОГО ДРЕНИРУЮЩЕГО ВМЕШАТЕЛЬСТВА У БОЛЬНЫХ МЕХАНИЧЕСКОЙ ЖЕЛТУХОЙ | 2019 |
|
RU2712008C1 |

Группа изобретений относится к медицине, в частности к медицинской технике, используемой для диагностики и/или лечения воспалительных, инфекционных, доброкачественных и/или злокачественных заболеваний поджелудочной железы, желчевыводящих протоков и/или печени. Катетер для забора биологических жидкостей из дуоденальных сосочков содержит удлиненное тело, выполненное с возможностью его установки в просвет двенадцатиперстной кишки человека. Указанное тело оснащено двумя баллонами, выполненными с возможностью раздувания с обеспечением возможности изолирования между ними пространства двенадцатиперстной кишки, в котором находятся дуоденальные сосочки. В указанном теле проходит аспирационный канал с впускным отверстием, выполненным в указанном теле между указанными баллонами. Аспирационный канал обеспечивает возможность создания в указанном изолированном пространстве разрежения воздуха с обеспечением возможности забора из него биологических жидкостей, получаемых из дуоденальных сосочков. Система для забора биологических жидкостей из дуоденальных сосочков содержит вышеописанный катетер и аспирационное устройство, соединенное с аспирационным каналом с обеспечением возможности отсасывания из него воздуха. Способ забора биологических жидкостей из дуоденальных сосочков включает в себя установку вышеописанного катетера в просвет двенадцатиперстной кишки человека, раздувание баллонов катетера для изолирования между ними пространства двенадцатиперстной кишки, в котором находится дуоденальный сосочек, создание, посредством аспирационного канала катетера, в указанном изолированном пространстве разрежения воздуха для забора из него биологических жидкостей, получаемых из дуоденальных сосочков. Вышеописанный катетер может применяться для диагностики или мониторинга течения по меньшей мере одного из следующих заболеваний: гастрит, панкреатит, рак поджелудочной железы, рак желчевыводящих протоков, холангиокарцинома, гепатоцеллюлярный рак, холангит и желчнокаменная болезнь, аутоиммунный гепатит и инфекционный гепатит. Вышеописанный катетер может применяться для лечения по меньшей мере одного из следующих заболеваний: панкреатит и холангит. Технический результат заключается в упрощении установки такого катетера в просвете двенадцатиперстной кишки человека для обеспечения забора биологических жидкостей, получаемых из дуоденальных сосочков, в частности благодаря отсутствию необходимости в точном позиционировании аспирационного отверстия напротив дуоденальных сосочков. 5 н. и 8 з.п. ф-лы, 2 ил.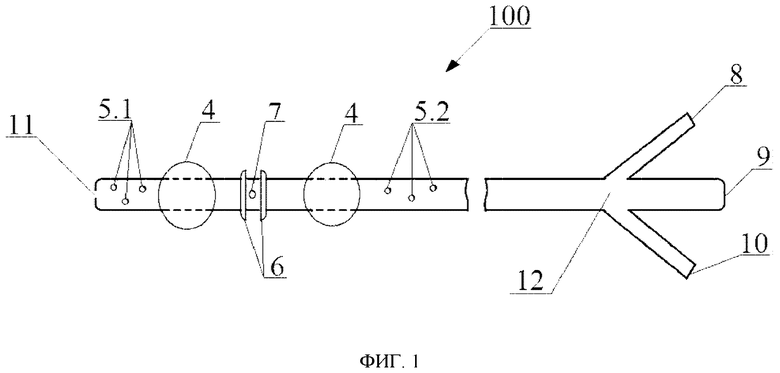
1. Катетер для забора биологических жидкостей из дуоденальных сосочков, содержащий:
удлиненное тело, выполненное с возможностью его установки в просвет двенадцатиперстной кишки человека,
отличающийся тем, что
указанное тело оснащено двумя баллонами, выполненными с возможностью раздувания с обеспечением возможности изолирования между ними пространства двенадцатиперстной кишки, в котором находятся дуоденальные сосочки,
причём в указанном теле проходит аспирационный канал с впускным отверстием, выполненным в указанном теле между указанными баллонами, а
аспирационный канал обеспечивает возможность создания в указанном изолированном пространстве разрежения воздуха с обеспечением возможности забора из него биологических жидкостей, получаемых из дуоденальных сосочков.
2. Катетер по п. 1, в котором в указанном теле проходит дополнительный канал, обеспечивающий возможность подачи в указанные баллоны текучей среды для их раздувания.
3. Катетер по любому из пп. 1, 2, в котором в указанном теле проходит ещё один канал, выполненный с возможностью подачи в него текучей среды и имеющий выпускное отверстие, выполненное на дистальном конце катетера, используемом для вставки катетера в просвет двенадцатиперстной кишки человека.
4. Катетер по п. 3, в котором указанные каналы герметично изолированы друг от друга.
5. Катетер по п. 3, в котором указанный ещё один канал дополнительно снабжен отверстиями, выполненными в указанном теле за пределами его части, ограниченной указанными баллонами.
6. Катетер по любому из пп. 1-5, в котором указанное аспирационное отверстие находится между двумя ограждающими выступами, которыми дополнительно снабжено тело катетера.
7. Катетер по п. 6, в котором указанные ограждающие выступы имеют кольцевую форму и расположены рядом или вплотную к аспирационному отверстию.
8. Система для забора биологических жидкостей из дуоденальных сосочков, содержащая:
катетер по любому из пп. 1-7 и
аспирационное устройство, соединенное с аспирационным каналом с обеспечением возможности отсасывания из него воздуха.
9. Способ забора биологических жидкостей из дуоденальных сосочков, включающий в себя:
установку катетера по любому из пп. 1-7 в просвет двенадцатиперстной кишки человека,
раздувание баллонов катетера для изолирования между ними пространства двенадцатиперстной кишки, в котором находится дуоденальный сосочек,
создание, посредством аспирационного канала катетера, в указанном изолированном пространстве разрежения воздуха для забора из него биологических жидкостей, получаемых из дуоденальных сосочков.
10. Способ по п. 9, согласно которому при установке катетера один из его баллонов размещают в луковице двенадцатиперстной кишки человека.
11. Способ по любому из пп. 9, 10, согласно которому установку катетера осуществляют под контролем эндоскопа.
12. Применение катетера по любому из пп. 1-7 для диагностики или мониторинга течения по меньшей мере одного из следующих заболеваний: гастрит, панкреатит, рак поджелудочной железы, рак желчевыводящих протоков, холангиокарцинома, гепатоцеллюлярный рак, холангит и желчнокаменная болезнь, аутоиммунный гепатит и инфекционный гепатит.
13. Применение катетера по любому из пп. 1-7 для лечения по меньшей мере одного из следующих заболеваний: панкреатит и холангит.
| Устройство для лечения панкреатита | 2015 |
|
RU2607929C2 |
| Катетер | 1985 |
|
SU1461471A1 |
| Катетер | 1976 |
|
SU651817A1 |
| US 4368739 A1, 18.01.1983 | |||
| Станок для придания концам круглых радиаторных трубок шестигранного сечения | 1924 |
|
SU2019A1 |
Авторы
Даты
2021-02-15—Публикация
2019-12-31—Подача