ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к особым имидазолонилхинолиновым соединениям и к их применению для ингибирования, регуляции и/или модуляции сигнальной трансдукции посредством киназ, в частности, киназы ATM, кроме того к фармацевтическим композициям, которые содержат данные соединения, и к применению соединений для лечения заболеваний, которые имеют отношение к киназе ATM, в частности, злокачественного новообразования.
Серин/треонин-протеинкиназа ATM (мутантная атаксия-телеангиэктазия киназа) принадлежит к семейству PIKK киназ, имеющих каталитические домены, которые гомологичны с фосфоинозитид-3 киназами (PI3 киназа, PI3K). Данные киназы вовлечены во множество ключевых клеточных функций, таких как рост клеток, пролиферация клеток, миграция, дифференциация, выживаемость и адгезия клеток. В частности, данные киназы реагируют на повреждение ДНК путем активации ареста клеточного цикла и программ репарации ДНК (DDR: ответ на повреждение ДНК). ATM является продуктом гена ATM и играет ключевую роль в репарации повреждения двухцепочечной ДНК (DSB, двухцепочечные разрывы) путем гомологической рекомбинации и негомологичного соединения концов (NHEJ). Двухцепочечное повреждение данного типа является особенно цитотоксичным.
Одной из постоянных особенностей опухолей у людей является их геномная нестабильность, причем особые недостатки механизма репарации ДНК в большинстве типов злокачественного новообразования до настоящего времени неизвестны. Данная нестабильность представляет собой терапевтическую отправную точку для химиотерапии, которая преимущественно практиковалась в течение некоторого времени. Кроме того, существует несколько синдромов, в которых основной генетический воздействующий фактор может быть приписан мутации, сопровождаемой потерей функции, гена, который модулирует реакцию на повреждение двухцепочечной ДНК. Они включают атаксия-телеангиэктазию, которая вызывается дефектным геном ATM. Общей особенностью всех этих синдромов является то, что они вызывают чрезвычайную чувствительность к облучению (Lavin & Shiloh (1997) Annu. Rev. Immunol. 15: 177; Rotman & Shiloh (1998) Hum. Mol. Genet. 7: 1555, включены во всей своей полноте в настоящее описание в качестве ссылки). ATM-дефектные клетки соответственно чувствительны к средствам и мерам, которые вызывают повреждение двухцепочечной ДНК, что делает ATM привлекательной мишенью для хемо- и радиосенсибилизации для лечения злокачественного новообразования.
Хотя молекулы кофеина и вортманнина, которые были первоначально исследованы ввиду вышеизложенного, проявили радиосенсибилизационное действие, приписываемое, среди прочего, ингибированию ATM, они, однако, слишком токсичны in vivo для возможного терапевтического применения. Исходя из химической структуры ингибитора PI3K, а именно соединения LY294002, компания KuDOS Pharmaceuticals разработала первый сильный и селективный ингибитор ATM: KU-55933 (2-морфолино-6-(тиантрен-1-ил)-4Н-пиран-4-он). Это облегчило сенсибилизацию к ионизирующему излучению и повреждающим двухцепочечную ДНК химиотерапевтическим средствам (Hickson, I., и др. (2004). Cancer Res 64, 9152-9159, включен во всей своей полноте в настоящее описание в качестве ссылки). Однако, KU-55933 оказался непригодным для применения in vivo, предположительно вследствие его высокой липофильности. На основе KU-55933 были разработаны KU-60019 (2-((2S,6R)-2,6-диметилморфолино)-N-(5-(6-морфолино-4-оксо-4Н-пиран-2-ил)-9Н-тиоксантен-2-ил)ацетамид) и KU-559403 (2-(4-метилпиперазин-1-ил)-N-[5-(6-морфолино-4-оксопиран-2-ил)тиоксантен-2-ил]ацетамид) с небольшой модификацией основной структуры, что позволило улучшить растворимость и действенность. В то же время сообщалось, например, что с помощью KU-60019 можно было безопасно и эффективно сенсибилизировать к облучению инициирующие глиобластому клетки, из чего было сделано заключение, что KU-60019 способен функционировать в качестве соедства для сенсибилизации к облучению целой серии опухолей головного мозга (Vecchio D. и др. (2015), Int. J. Cancer 136: 1445, включен во всей своей полноте в настоящее описание в качестве ссылки).
Является желательным и представляет цель настоящего изобретения обеспечение малых молекул, которые эффективно ингибируют, регулируют и/или модулируют сигнальную трансдукцию посредством киназ, в частности, киназы ATM.
Более того, желательно, чтобы ингибиторы киназы данного типа были селективными, т.е. не проявляли или проявляли значительно более низкую активность по отношению к другим киназам. Таким образом, побочное действие или связанная токсичность может быть снижена.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Цель изобретения неожиданно была достигнута с помощью соединений формулы (I)

где
R1 означает А,
R3 означает А или Н,
А в каждом случае независимо означает неразветвленный или разветвленный алкил, содержащий 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов С, где, независимо друг от друга, 1, 2, 3, 4, 5, 6 или 7 атомов Н могут быть заменены на Hal,
Het1 означает моно- или бициклический гетероарил, содержащий 2, 3, 4, 5, 6, 7, 8 или 9 атомов С и 1, 2, 3 или 4 атома N, О и/или S, который может быть незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -Het2 и/или -SO2-Het2,
Het2 означает моноциклический насыщенный гетероцикл, содержащий 2, 3, 4, 5, 6 или 7 атомов С и 1, 2, 3 или 4 атома N, О и/или S, который может быть незамещен или монозамещен посредством А,
НЕТ означает 5- или 6-членный ароматический гетероцикл, содержащий 1, 2 или 3 атома N и необязательно атом О или атом S, где данный гетероцикл присоединен к атому N скелета через кольцевой атом С и где данный гетероцикл может быть незамещен или замещен одним, двумя или тремя заместителями, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, А, Het2, CN, -(CY2)p-OY, -(CY2)p-OZ, -(CY2)p-O-Het2, -(CY2)p-O-(CY2)t-Het2, -(CY2)p-O-(CY2)t-NYY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -SO2-Het2, CyA, -(CY2)p-O-(CY2)t-SO2-Y, -(CY2)p-NY-SO2-Y и -(CY2)p-SO2-Y, и где данный гетероцикл может быть частью бициклического 11- или 12-членного ароматического гетероцикла, где данный бициклический ароматический гетероцикл может быть во всех своих частях незамещен или замещен одним, двумя, тремя или большим числом заместителей, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, A, Het2, -CN, -(CY2)p-OY, -(CY2)p-OZ, -(CY2)p-O-Het2, -(CY2)p-O-(CY2)t-Het2, -(CY2)p-O-(CY2)t-NYY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -SO2-Het2, CyA, -(CY2)p-O-(CY2)t-SO2-Y, -(CY2)p-NY-SO2-Y и -(CY2)p-SO2-Y,
Y означает H или A,
Z означает неразветвленный или разветвленный алкенил, содержащий 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов С, где, независимо друг от друга, 1, 2, 3, 4, 5, 6 или 7 атомов Н могут быть заменены на Hal,
CyA означает циклоалкил, содержащий 3, 4, 5, 6, 7 или 8 кольцевых атомов С, который незамещен или моно- или полизамещен, независимо друг от друга, посредством Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY и/или -(CY2)p-NY-COY,
Hal означает F, Cl, Br или I, и
p означает 0, 1, 2, 3, 4, 5 или 6
t означает 1, 2, 3, 4, 5 или 6,
и/или их фармацевтически пригодных производных, солей, сольватов, таутомеров, стереоизомеров, включая их смеси во всех соотношениях.
Как указано более подробно ниже, соединения следует понимать таким образом, что атомы, такие как, например, Н, С, N, в каждом случае также включают более тяжелые изотопы таких атомов. Это применимо, в частности, к атомам Н, в случае которых можно успешно использовать дейтерий, как показано на примерах.
Неожиданно было доказано, что соединения в соответствии с изобретением являются сильными ингибиторами киназы ATM. Еще более неожиданной является селективность в отношении других родственных киназ, таких как, например, mTOR (мишень рапамицина в клетках млекопитающих) киназа, дополнительная протеинкиназа из семейства киназ PIK (также известного как класс IV PI3K).
В полную противоположность настоящему изобретению, международная заявка на патент WO 2010/139731 раскрывает, что описанные и заявленные в ней имидазолонилхинолиновые соединения предпочтительно являются ингибиторами класса I PI3 киназ и/или mTOR киназы. Киназы класса I PI3 представляют собой липидкиназы. Соответственно, экспериментальные данные показывают значения IC50 для mTOR в диапазоне вплоть до менее 3 нМ, т.е. очень сильное ингибирование.
Соединения в соответствии с изобретением с другой стороны ярко подтверждают, что структурные различия, которые на первый взгляд кажутся относительно небольшими, оказывают решающее влияние на биологическую активность.
Кроме того, соединения в соответствии с изобретением также отличаются отсутствием часто наблюдаемого нежелательного ингибирования ионных каналов сердца, в частности, Kv1.11 hERG, блокировка которых может привести к угрожающей жизни аритмии.
Таким образом, соединения в соответствии с изобретением открывают совершенно новые возможности в терапии рака, например, в качестве монотерапии в случае опухолей, характеризующихся нарушенной способностью репарации двухцепочечной ДНК, или в комбинации с радио- или химиотерапией, в частности, в качестве радио- и хемосенсибилизаторов для лечения злокачественного новообразования, особенно предпочтительно в качестве радиосенсибилизаторов.
Соединения формулы (I) вследствие этого можно применять для подавления злокачественного новообразования и для сенсибилизации раковых клеток к противоопухолевым средствам и/или ионизирующему излучению. Изобретение также относится к применению соединений формулы (I) для лечения злокачественного новообразования, опухолей и/или метастазов в комбинации с радиотерапией и/или противоопухолевым средством, предпочтительно радиотерапией.
Выше и ниже, радикалы R1, R3, Y, A, Z, СуА, Het1, Het2, НЕТ и Hal, а также р и t имеют значения, указанные выше в случае формулы (I), если явным образом не указано иное. В случае наличия нескольких отдельных остатков в рамках соединения или радикала, остатки принимают, независимо друг от друга, указанные значения, если явным образом не указано иное. Например, остатки YY в радикале -NYY, в котором они могут встречаться несколько раз, являются одинаковыми или различными, но предпочтительно в каждом случае выбраны, независимо друг от друга, из значений, указанных выше и/или ниже (например, метила и/или этила), если явным образом не указано иное. В случае наличия нескольких Y, радикал альтернативно также может быть обозначаться посредством Y', Y'', Y''' и Y''''. Соответствующее условие применяется к другим остаткам или переменным числового типа. Соответственно, формулировка "циклоалкил, который незамещен или моно- или полизамещен, независимо друг от друга, посредством Hal, А, … и/или -(CY2)p-NY-COY" означает, что циклоалкильный радикал может быть монозамещен одним из указанных заместителей, или может иметь множество заместителей, которые выбирают, независимо друг от друга, из упомянутых в случае циклоалкила заместителей Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY и/или -(CY2)p-NY-COY, т.е., как, например, циклогексил, содержащий три заместителя - фтор, хлор и -CH2-NH2.
Термины, использованные в данной заявке для определения соединений, обычно базируются на правилах организации ИЮПАК для химических соединений, и, в частности, органических соединений. Термины для пояснения упомянутых выше соединений изобретения всегда имеют следующие значения, если не указано иное в описании или формуле изобретения.
Термин "незамещенный" означает, что радикал, группа или остаток не несет заместителей. Термин "замещенный" означает, что радикал, группа или остаток несет один или несколько заместителей. Если ниже в отношении определенной группы или определенного радикала, замещение которого определяется конкретно в связи с приведенной выше формулой (I), упоминается только термин "замещенный", само собой разумеется, что это замещение соответствует таковому, упомянутому выше, если специально не указано иное. Также само собой разумеется, в смысле изобретения, что в данном случае радикал может принимать все значения, упомянутые ранее в описании для соответствующего радикала посредством ссылки на "упомянутое выше значение" без более подробно его описания.
"А" означает неразветвленный или разветвленный алкил, содержащий 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов С, где, независимо друг от друга, 1, 2, 3, 4, 5, 6 или 7 атомов Н могут быть заменены на Hal. "А" особенно предпочтительно означает неразветвленный или разветвленный алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов С, где, независимо друг от друга, 1, 2, 3, 4 или 5 атомов Н могут быть заменены на Hal, т.е. F, Cl, Br и/или I. Само собой разумеется, что Hal при этом может означать различные галогены F, Cl, Br, I, т.е., например, 1 H может быть заменен на F, другие Н могут быть заменены на Cl. Чрезвычайное предпочтение отдают С1-4-алкилу, где, независимо друг от друга, 1, 2 или 3 атома Н могут быть заменены на Hal. C1-4-алкил данного типа представляет собой, например, метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, фторметил, дифторметил, трифторметил, пентафторэтил, 1,1,1-трифторэтил или бромметил, наиболее предпочтительно метил, этил, фторметил, дифторметил или трифторметил. Само собой разумеется, что соответствующие значения "А" в радикалах формулы в соответствии с изобретением являются независимыми друг от друга.
"Алкил" в данном документе означает насыщенный углеводородный радикал, который является неразветвленным (линейным) или разветвленным и предпочтительно содержит 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов С, т.е. С1-10-алкил. Примерами алкильных радикалов являются метил, этил, пропил, изопропил, 1,1-, 1,2- или 2,2-диметилпропил, 1-этилпропил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил, бутил, изобутил, втор-бутил, трет-бутил, 1-, 2- или 3-метилбутил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2-этилбутил, пентил, изопентил, неопентил, трет-пентил, 1-, 2-, 3- или 4-метилпентил, гексил.
"Z" в данном документе означает неразветвленный или разветвленный алкенил, содержащий 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов С, где, независимо друг от друга, 1, 2, 3, 4, 5, 6 или 7 атомов Н могут быть заменены на Hal. Алкенилы содержат по меньшей мере одну С-С двойную связь, однако, в частности, могут также содержать две двойные связи (диены). Примерами подходящих алкенилов являются винил, аллил, пропенил -(СН2СН=СН2; -СН=СН-СН3; -С(=СН2)-СН3), 1-, 2- или 3-бутенил, изобутенил, 2-метил-1- или 2-бутенил, 3-метил-1-бутенил, 1,3-бутадиенил, 2-метил-1,3-бутадиенил, 2,3-диметил-1,3-бутадиенил, 1-, 2-, 3- или 4-пентенил и гексенил, особенно предпочтительно аллил.
Термин "СуА" в данном документе означает циклоалкил, в частности, циклический алкил, содержащий 3, 4, 5, 6, 7 или 8 кольцевых атомов С, т.е. С3-6-циклоалкил, который может быть незамещен или моно- или полизамещен, например, ди- или тризамещен, независимо друг от друга, посредством Hal, А, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY и/или -(CY2)p-NY-COY. Примерами незамещенных циклоалкилов являются циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Незамещенные циклоалкильные группы в данном случае являются предпочтительными, в частности, циклопропил.
"Het1" в данном документе означает моно- или бициклический ароматический гетероцикл, т.е. гетарил или гетероарил, который содержит 2, 3, 4, 5, 6, 7, 8 или 9 атомов С и 1, 2, 3 или 4 атома N, О и/или S, т.е. по меньшей мере один гетероатом, и который может быть незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -Het2 и/или -SO2-Het2.
"Het1" таким образом означает 5, 6, 7, 8, 9, 10, 11, 12, 13, 14 или 15, предпочтительно 5-10-членный моно- или бициклический ароматический углеводородный радикал, который включает по меньшей мере 1, в соответствующем случае также 2, 3, 4 или 5 гетероатомов, в частности, атомов азота, кислорода и/или серы, где гетероатомы могут быть одинаковыми или различными. Число атомов азота предпочтительно равно 0, 1, 2, 3 или 4, и число атомов кислорода и серы равно, независимо друг от друга, 0 или 1, причем должен присутствовать по меньшей мере один гетероатом. Гетероциклы, содержащие атомы азота, являются предпочтительными. "Het1" может быть выбран, независимо от дальнейших замещений, из, например, следующих гетероциклов: фурил, в частности, 2- или 3-фурил, тиенил, в частности, 2- или 3-тиенил, пирролил, в частности, 1-, 2- или 3-пирролил, имидазолил, в частности, 1-, 2-, 4- или 5-имидазолил, пиразолил, в частности, 1-, 3-, 4- или 5-пиразолил, оксазолил, в частности, 2-, 4- или 5-оксазолил, изоксазолил, в частности, 3-, 4- или 5-изоксазолил, тиазолил, в частности, 2-, 4- или 5-тиазолил, изотиазолил, в частности, 3-, 4- или 5-изотиазолил, пиридил, в частности, 2-, 3- или 4-пиридил, где пиридил и пиридинил используются в данном документе в качестве синонимов, пиримидинил, в частности, 2-, 4-, 5- или 6-пиримидинил, триазолил, в частности, 1,2,3-триазол-1-, -4- или -5-ил, 1,2,4-триазол-1-, -3- или 5-ил, триазинил, тетразолил, в частности, 1- или 5-тетразолил, оксадиазолил, в частности, 1,2,3-оксадиазол-4- или -5-ил, 1,2,4-оксадиазол-3- или -5-ил, тиадиазолил, в частности, 1,3,4-тиадиазол-2- или -5-ил, 1,2,4-тиадиазол-3- или -5-ил, 1,2,3-тиадиазол-4- или -5-ил, пиридазинил, в частности, 3- или 4-пиридазинил, пиразинил, индолил, в частности, 1-, 2-, 3-, 4-, 5-, 6- или 7-индолил, изоиндолил, в частности, 4- или 5-изоиндолил, бензимидазолил, в частности, 1-, 2-, 4- или 5-бензимидазолил, индазолил, в частности, 1-, 2-, 3-, 4-, 5-, 6- или 7-индазолил, бензопиразолил, в частности, 1-, 3-, 4-, 5-, 6- или 7-бензопиразолил, бензоксазолил, в частности, 2-, 4-, 5-, 6- или 7-бензоксазолил, бензизоксазолил, в частности, 3-, 4-, 5-, 6-, или 7-бензизоксазолил, бензотиазолил, в частности, 2-, 4-, 5-, 6- или 7-бензотиазолил, бензизотиазолил, в частности, 2-, 4-, 5-, 6- или 7-бензизотиазолил, 4-, 5-, 6- или 7-бенз-2,1,3-оксадиазолил, хинолил, в частности, 2-, 3-, 4-, 5-, 6-, 7- или 8-хинолил, изохинолил, в частности, 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолил, циннолинил, в частности, 3-, 4-, 5-, 6-, 7- или 8-циннолинил, хиназолинил, в частности, 2-, 4-, 5-, 6-, 7- или 8-хиназолинил, хиноксалинил, в частности, 5- или 6-хиноксалинил, 2-, 3-, 5-, 6-, 7- или 8-2Н-бензо[1,4]-оксазинил, 1,3-бензодиоксол-5-ил, 1,4-бензодиоксан-6-ил, 2,1,3-бензотиадиазол-4- или -5-ил, 2, 1,3-бензоксадиазол-5-ил, фталазинил, индолизинил и птеридинил. Присоединение "-"Het1 может осуществляется через любой кольцевой член гетероарильной группы, при условии, что это представляется химически подходящим, где связь через атом С является предпочтительной. Если только одно из двух колец в бициклическом ароматическом гетероцикле (аннелированные кольца) содержит один или несколько гетероатомов, присоединение предпочтительно имеет место через кольцо, которое содержит гетероатом(-ы). Одно кольцо не содержит гетероатома, если ни один из атомов, образующих кольцо, не является гетероатомом, включая атомы, которые должны быть отнесены к обоим кольцам. Особенно предпочтительные варианты осуществления Het1 упоминаются ниже.
"Het2" в данном документе означает моноциклический насыщенный гетероцикл, содержащий 2, 3, 4, 5, 6 или 7 атомов С и 1, 2, 3 или 4 атома N, О и/или S, который может быть незамещен или монозамещен посредством А. "Het2" предпочтительно означает моноциклический насыщенный гетероцикл, содержащий 3, 4 или 5 атомов С и 1 или 2 атома N и/или О. Примерами Het2 являются азиридинил, оксиранил, тиаранил, азетидинил, оксетанил, диоксетанил, тиетанил, пирролидинил, тетрагидрофуранил, дитиоланил, оксазолидинил, пиперидинил, тетрагидропиранил, пиперазинил, диоксанил, тиоморфолинил, морфолинил, оксепанил, тиепанил и азепанил. N-содержащие моноциклические насыщенные гетероциклы являются предпочтительными, например, азетидинил, пирролидинил, пиперидинил, пиперазинил и морфолинил, где они в соответствии с общим определением могут быть незамещены или монозамещены посредством А. Среди предпочтительных вариантов осуществления числятся незамещенные азетидинил, пирролидинил, пиперидинил, пиперазинил и морфолинил, особенно предпочтительно азетидинил и пиперазинил. Более того, тетрагидропиранил также является предпочтительным. Присоединение "-"Het2 в группе -SO2-Het2 типично осуществляется через атом С. Иным образом, т.е., например, в качестве заместителя НЕТ, связь может осуществляться через любой кольцевой член гетероциклической группы, при условии, что это представляется химически подходящим, причем и здесь присоединение через атом С является предпочтительным.
Для целей настоящего изобретения, "НЕТ" означает 5- или 6-членный ароматический гетероцикл, содержащий 1, 2 или 3 атома N и необязательно атом О или атом S, где данный гетероцикл присоединен к атому N скелета через кольцевой атом С и где данный гетероцикл может быть незамещен или замещен одним, двумя или тремя заместителями, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, A, Het2, CN, -(CY2)p-OY, -(CY2)p-OZ, -(CY2)p-O-Het2, -(CY2)p-O-(CY2)t-Het2, -(CY2)p-O-(CY2)t-NYY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -SO2-Het2, CyA, -(CY2)p-O-(CY2)t-SO2-Y, -(CY2)p-NY-SO2-Y и -(CY2)p-SO2-Y, и где данный гетероцикл может быть частью бициклического 11- или 12-членного ароматического гетероцикла, где данный бициклический ароматический гетероцикл может быть во всех своих частях незамещен или замещен одним, двумя, тремя или большим числом заместителей, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, A, Het2, -CN, -(CY2)p-OY, -(CY2)p-OZ, -(CY2)p-O-Het2, -(CY2)p-O-(CY2)t-Het2, -(CY2)p-O-(CY2)t-NYY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -SO2-Het2, CyA, -(CY2)p-O-(CY2)t-SO2-Y, -(CY2)p-NY-SO2-Y и -(CY2)p-SO2-Y. Другими словами, второе кольцо бициклического ароматического гетероцикла также может быть соответственно замещенным. Таким образом, в первом варианте осуществления, "НЕТ" означает моноциклический 5- или 6-членный ароматический гетероцикл, а во втором варианте осуществления означает бициклический 11- или 12-членный ароматический гетероцикл, причем следует понимать, что связь к имидазолонилхинолиновому скелету имеет место через кольцо бициклического гетероцикла, которое соответствует моноциклическому НЕТ. В особенности, это означает, что, в случае, например, бензаннелированных систем, связь имеет место через кольцо, которое содержит гетероатом(-ы), при условии, что гетероатом(-ы) должен(-ны) входить в состав только одного кольца (и не вовлечен(-ы) в связь со вторым кольцом). В бициклическом 11- или 12-членном ароматическом гетероцикле оба кольца являются ароматическими. Указание на факт, что бициклический гетероцикл может быть во всех своих частях замещен одним, двумя, тремя или большим числом заместителей, таким образом, равносильно тому, что эти заместители могут быть расположены в целом в любой желаемой точке гетероцикла (т.е. по желанию на любой из кольцевых частей).
Термин "Hal", или также "галоген", "атом галогена", "галогенный заместитель", в данном документе означает один или несколько атомов фтора (F), брома (Br), хлора (Cl) или йода (I). Термины "дигалоген", "тригалоген" и "пергалоген" относятся к двум, трем или четырем заместителям, где каждый заместитель может быть выбран, независимо друг от друга, из группы, состоящей из F, Cl, Br или I. "Галоген" предпочтительно означает F, Cl или Br. F и Cl являются особенно предпочтительными, в частности, если галогены являются заместителями алкильной (галогеналкил) или алкоксигруппы (например, CF3 и CF3O).
"CN" могут означать как циано, так также и изоциано, где значение циано (-CN) является предпочтительным.
-POAA, -COOY, -CO-NYY, -COOY и -NY-COY являются условными обозначениями для следующих групп:

Индекс р предпочтительно означает 0, 1, 2 или 3, особенно предпочтительно 0.
Индекс t предпочтительно означает 1, 2, 3 или 4, особенно предпочтительно 2.
Примерами -(CY2)p-OY, -(CY2)p-OZ, -(CY2)p-O-Het2, -(CY2)p-O-(CY2)t-Het2, -(CY2)p-O-(CY2)t-NYY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY, -(CY2)p-O-(CY2)t-SO2-Y, -(CY2)p-NY-SO2-Y и -(CY2)p-SO2-Y таким образом являются -OY, -ОН, -O-A, -О-СН3, -O-CHF2, -O-CH2F, -O-CH2CH3, -(CH2)p-OY, -CH2-O-CH3, -CH2-O-CH2CH3, -O-CH=CH2, -CH2-O-CH=CH2, -O-CH2-CH=CH2, -CH2-O-CH2-CH=CH2, -O-Het2, -O-CH2-Het2, -O-CH2CH2-Het2, -O-CH2-NYY, -O-CH2CH2-NYY, -O-CH2-NH2, -O-CH2CH2-NH2, -O-CH2-NHCH3, -O-CH2CH2-NHCH3, -O-CH2-OY, -O-CH2CH2-OY, -O-CH2CH2CH2-OY, -O-CH2-OH, -O-CH2CH2-OH, -O-CH2CH2CH2-OH, -O-CH2-OA, -O-CH2CH2-OA, -O-CH2CH2CH2-OA, -O-CH2-OCH3, -O-CH2CH2-OCH3, -O-CH2CH2CH2-OCH3, -O-CH2-SO2-Y, -O-CH2-SO2-CH3, -NYY, -NH2, -NHA, -NAA, -NHCH3, -N(CH3)2, -CH2-NYY, -CH2-NH2, -CH2-NHA, -CH2-NAA, -CH2-NHCH3, -CH2-N(CH3)2, -COOY, -COOA, -CH2-COOY, -CH2-COOA, -CH2-COOCH3, -CO-NYY, -CO-NAA, -CO-NHA, -CO-NH-CH3, -CH2-CO-NYY, -CH2-CO-NAA, -(CH2)p-NY-COY, -(CH2)p-NY-COA.
Соответственно, изобретение относится к соединениям формулы (I), в которой по меньшей мере один из вышеуказанных радикалов имеет одно из значений, указанных выше. Радикалы, не указанные более подробно в контексте одного из вариантов формулы (I), ее подформул или любого остатка на них, должны иметь значения, указанные в случае формулы (I), как раскрыто в данной заявке, с целью достижения цели изобретения. Это означает, что упомянутые радикалы могут принимать все значения, приписываемые им, как описано выше или ниже, включая любые предпочтительные варианты осуществления, без ограничения последними, и независимо от их присутствия в другом конкретном контексте. Самой собой разумеется, в частности, что каждый вариант осуществления определенного радикала можно комбинировать с каждым вариантом осуществления одного или нескольких других радикалов.
В иллюстративном варианте осуществления
Het1 означает моно- или бициклический гетероарил, содержащий 2, 3, 4, 5, 6, 7, 8 или 9 атомов С и 1, 2, 3 или 4 атома N, О и/или S, который может быть незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY и/или -SO2-Het2,
НЕТ означает 5- или 6-членный ароматический гетероцикл, содержащий 1, 2 или 3 атома N и необязательно атом О или атом S, где данный гетероцикл присоединен к атому N скелета через кольцевой атом С и где данный гетероцикл может быть незамещен или замещен одним, двумя или тремя заместителями, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, А, Het2, CN, -(CY2)p-OY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY или -SO2-Het2; и может быть частью бициклического 11- или 12-членного ароматического гетероцикла, где данный бициклический ароматический гетероцикл может быть во всех своих частях незамещен или замещен одним, двумя, тремя или большим числом заместителей, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, A, Het2, -CN, -(CY2)p-OY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY или -SO2-Het2,
Hal означает F, Cl, Br или I,
p означает, независимо друг от друга, 0, 1, 2, 3, 4, 5 или 6 и
t означает 1, 2, 3, 4, 5 или 6.
Соединения формулы (I), где R3=А, также могут быть изображены следующим образом:
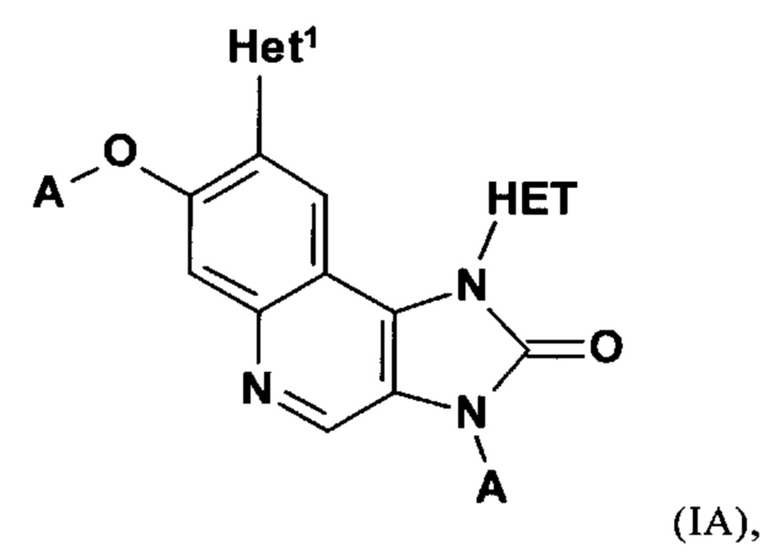
где следует понимать, что группы А могут иметь одинаковые или разные значения.
В предпочтительных вариантах осуществления соединений формулы (I) или (IA), R1 означает незамещенный или замещенный C1-С3-алкил, особенно предпочтительно метил. Соответственно, настоящее изобретение обеспечивает предпочтительные соединения следующей формулы (II):

и альтернативные варианты, где R3=Н.
В предпочтительных вариантах осуществления соединений формул (I) или (IA) и (II), R3 означает Н или, более предпочтительно, неразветвленный или разветвленный алкил, содержащий 1, 2, или 3 атома С, где 1, 2, 3, 4, или 5 атомов Н могут быть заменены, независимо друг от друга, на Hal. R3 особенно предпочтительно означает метил. Таким образом, настоящее изобретение также обеспечивает соединения следующих формул (III) и (IV):


В каждой из формул (I), (II), (III) и (IV), Het1 предпочтительно означает моноциклический гетероарил, содержащий 2, 3 или 4 атома С и 1, 2 или 3 атома N, который может быть незамещен или замещен, как определено для соединения формулы (I). Более того, Het1 (в каждой из показанных формул) особенно предпочтительно выбирают из пиридинила, пиримидинила, пиразолила, триазолила и имидазолила, которые могут быть незамещены или замещены согласно вышеприведенному определению, где пиразолил и триазолил, в частности, 1,2,3-триазолил, являются особенно предпочтительными.
Het1 может быть, например, незамещен или замещен одним или двумя заместителями, которые предпочтительно выбирают, независимо друг от друга, из следующих: Hal, A, -(CY2)p-OY, -(CY2)p-NYY и -Het2, особенно предпочтительно алкил, который может быть незамещен или моно- или полизамещен галогеном, в частности, F; -OY, -NYY, галоген, и -Het2, особенно предпочтительно метил, этил, амино, метокси, фторметил, дифторметил, фтор, азетидинил, где метил и этил являются особенно предпочтительными.
Het1 (в каждой из показанных формул) особенно предпочтительно выбирают из следующих: 1Н-пиразол-4-ил, 2Н-пиразол-3-ил, 1Н-пиразол-3-ил, 1-метил- 1Н-пиразол-4-ил, 3-метил-1Н-пиразол-4-ил, 5-метил-1Н-пиразол-3-ил, 4-метил-1Н-пиразол-3-ил, 1-фторметил-1Н-пиразол-4-ил, 1-дифторметил-1Н-пиразол-4-ил, 1,3-диметил-1Н-пиразол-4-ил, 1-этил-1Н-пиразол-4-ил, 1-этил-3-метил-1Н-пиразолил, 3-фтор-1-метил-1Н-пиразол-4-ил, 3-амино-1Н-пиразол-5-ил, 2Н-1,2,3-триазол-4-ил, 3Н-1,2,3-триазол-4-ил-, 1-метил-1Н-1,2,3-триазол-4-ил, 2-метил-2Н-1,2,3-триазол-4-ил, 2-амино-1Н-имидазол-4-ил, 6-метоксипиридин-3-ил и 1-(азетидин-3-ил)-3-метил-1Н-пиразол-4-ил. Het1 особенно предпочтительно означает пиразолил, который может быть незамещен или замещен согласно вышеприведенному определению, и может быть выбран, например, из следующих: 1Н-пиразол-4-ил, 2Н-пиразол-3-ил, 1Н-пиразол-3-ил, 1-метил-1Н-пиразол-4-ил, 3-метил-1Н-пиразол-4-ил, 5-метил-1Н-пиразол-3-ил, 4-метил-1Н-пиразол-3-ил, 1-фторметил-1Н-пиразол-4-ил, 1-дифторметил-1Н-пиразол-4-ил, 1,3-диметил-1Н-пиразол-4-ил, 1-этил-1Н-пиразол-4-ил, 1-этил-3-метил-1Н-пиразолил, 3-фтор-1-метил-1Н-пиразол-4-ил, 3-амино-1H-пиразол-5-ил, где 1Н-пиразол-4-ил, 2Н-пиразол-3-ил, 1Н-пиразол-3-ил, 1-метил-1Н-пиразол-4-ил, 3-метил-1Н-пиразол-4-ил, 5-метил-1Н-пиразол-3-ил, 4-метил-1Н-пиразол-3-ил, 1-фторметил-1Н-пиразол-4-ил, 1,3-диметил-1Н-пиразол-4-ил и 1-этил-1Н-пиразол-4-ил являются особенно предпочтительными. Альтернативно, Het1 предпочтительно означает триазолил, который может быть незамещен или замещен согласно вышеприведенному определению, и может быть выбран, например, из 2Н-1,2,3-триазол-4-ила, 3Н-1,2,3-триазол-4-ила-, 1-метил-1Н-1,2,3-триазол-4-ила, 2-метил-2Н-1,2,3-триазол-4-ила, особенно предпочтительно означает 2-метил-2Н-1,2,3-триазол-4-ил.
В других вариантах соединений любой из формул (I), (II), (III) и (IV), Het1 может быть бициклическим гетероарилом, содержащим 6, 7 или 8 атомв C и 1, 2, или 3 атома N, который может быть незамещен или замещен согласно вышеприведенному определению. Предпочтительными заместителями являются, аналогично моноциклическим гетероарилам, Hal, A, -(CY2)p-OY, -(CY2)p-NYY и -Het2, особенно предпочтительно алкил. Например, Het1 может быть выбран из бензимидазолила, имидазо[4,5-b]пиридинила, бензодиазолила, которые могут быть незамещены или замещены, как упомянуто в качестве предпочтительных вариантов в отношении формулы (I) и выше, предпочтительно, например, 2-метил-3Н-бензимидазол-5-ила, 3Н-бензимидазол-5-ила, 2-метил-1Н-имидазо[4,5-b]пиридин-6-ила.
В предпочтительных вариантах осуществления соединений любой из формул (I), (II), (III) и (IV), НЕТ выбирают из следующих ароматических гетероциклов, которые в каждом случае могут быть незамещены или замещены согласно вышеприведенному определению:
НЕТ означает, независимо от возможного замещения, пирролил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиразолил, имидазолил, 1-окса-2,3-диазолил, 1-окса-2,4-диазолил, 1-окса-3,4-диазолил, 1-окса-2,5-диазолил, 1-тиа-2,3-диазолил, 1-тиа-2,4-диазолил, 1-тиа-3,4-диазолил, 1-тиа-2,5-диазолил, 1,2,3-триазолил, 1,3,4-триазолил и тетразолил; пиридинил, пиримидинил, пиразинил и пиридазинил; индолил, изоиндолил, бензимидазолил, индазолил, бензоксазолил, бензотиазолил, бензотриазолил, пирроло[2,3-b]пиридинил, пирроло[2,3-с]пиридинил, пирроло[3,2-b]пиридинил, пирроло[3,2-с]пиридинил, имидазо[4,5-b]пиридинил, имидазо[4,5-с]пиридинил, пиразоло[4,3-d]пиридинил, пиразоло[4,3-с]пиридинил, пиразоло[3,4-с]пиридинил, пиразоло[3,4-b]пиридинил, пуринил, индолизинил, имидазо[1,2-а]пиридинил, имидазо[1,5-а]пиридинил, пиразоло[1,5-а]пиридинил, пирроло[1,2-b]пиридазинил, имидазо[1,2-с]пиримидинил, хинолинил, изохинолинил, циннолинил, хиназолинил, хиноксалинил, фталазинил, 1,6-нафтиридинил, 1,7-нафтиридинил, 1,8-нафтиридинил, 1,5-нафтиридинил, 2,6-нафтиридинил, 2,7-нафтиридинил, пиридо[3,2-d]пиримидинил, пиридо[4,3-d]пиримидинил, пиридо[3,4-d]пиримидинил, пиридо[2,3-d]пиримидинил, пиридо[2,3-d]пиразинил, пиридо[3,4-b]пиразинил, пиразино[2,3-b]пиразинил, пиримидо[5,4-d]пиримидинил, пиримидо[4,5-d]пиримидинил, бензоксазолил, бензотиазолил, бензизоксазолил, бензизотиазолил, фуропиридинил и тиенопиридинил.
НЕТ особенно предпочтительно выбирают из следующих 5- или 6-членных моноциклических ароматических гетероциклов, которые в каждом случае могут быть незамещены или замещены согласно вышеприведенному определению: пиридинил, пиримидинил, пиразолил, тиазолил, имидазолил.
Данные предпочтения для НЕТ также применимы, в частности, к соединениям формул (I), (II), (III) и (IV), в комбинации с предпочтительными вариантами осуществления для Het1, в частности, вариантом Het1, выбранным из пиридинила, пиримидинила, пиразолила, триазолила и имидазолила, а также бензимидазолила, имидазо[4,5-b]пиридинила, бензодиазолила, которые в каждом случае могут быть незамещены или замещены согласно вышеприведенному определению, например, 1Н-пиразол-4-ила, 2Н-пиразол-3-ила, 1Н-пиразол-3-ила, 1-метил-1H-пиразол-4-ила, 3-метил-1H-пиразол-4-ила, 5-метил-1H-пиразол-3-ила, 4-метил-1Н-пиразол-3-ила, 1-фторметил-1Н-пиразол-4-ила, 1-дифторметил-1Н-пиразол-4-ила, 1,3-диметил-1Н-пиразол-4-ила, 1-этил-1Н-пиразол-4-ила, 1-этил-3-метил-1H-пиразолила, 3-фтор-1-метил-1H-пиразол-4-ила, 3-амино-1Н-пиразол-5-ила, 2Н-1,2,3-триазол-4-ила, 3Н-1,2,3-триазол-4-ила-, 1-метил-1Н-1,2,3-триазол-4-ила, 2-метил-2Н-1,2,3-триазол-4-ила, 2-амино-1H-имидазол-4-ила, 6-метоксипиридин-3-ила и 1-(азетидин-3-ил)-3-метил-1Н-пиразол-4-ила, 2-метил-3Н-бензимидазол-5-ила, 3Н-бензимидазол-5-ила, 2-метил-1Н-имидазо[4,5-b]пиридин-6-ила, и особенно, в частности, также с вариантами, в которых Het1 означает пиразолил, который может быть незамещен или замещен согласно вышеприведенному определению и может быть выбран, например, из 1Н-пиразол-4-ила, 2Н-пиразол-3-ила, 1Н-пиразол-3-ила, 1-метил-1Н-пиразол-4-ила, 3-метил-1H-пиразол-4-ила, 5-метил-1H-пиразол-3-ила, 4-метил-1H-пиразол-3-ила, 1-фторметил-1Н-пиразол-4-ила, 1,3-диметил-1Н-пиразол-4-ила, 1-этил-1Н-пиразол-4-ила.
Из возможных заместителей на НЕТ, предпочтение отдают следующим: Hal, в частности, F, Cl; А, в частности, метил, этил, пропил; Het2, в частности, азетидинил, тетрагидропиранил, пиперазинил; CN; -(CY2)p-OY, -(CY2)p-OA, -(CY2)p-OH, где предпочтительно в каждом случае р=0, 1, 2, 3; -(CY2)p-OZ, -(CY2)p-O-Het2, -O-Het2, -(CY2)p-O-(CY2)t-Het2, -O-(CY2)t-Het2, -O-(CH2)t-Het2, -(CY2)p-O-(CY2)t-NYY, -O-(CY2)t-NYY, -(CY2)p-O-(CY2)t-OY, -O-(CY2)t-OY, -O-(CY2)t-OA, -O-(CY2)t-OH, -O-(CH2)t-OA, -O-(CH2)t-OH, -(CY2)p-CO-NYY, -(CY2)p-CO-NHA, CyA, -(CY2)p-O-(CY2)t-SO2-Y, -O-(CY2)t-SO2-Y, -O-(CY2)t-SO2-A, -(CY2)p-SO2-Y, -(CY2)p-SO2-A. Например, ароматические гетероциклы НЕТ в общем, и предпочтительные варианты осуществления в частности, например, пиридинил, пиримидинил, пиразолил, тиазолил, имидазолил, могут в каждом случае быть замещены одним, двумя, тремя или большим числом заместителей, которые выбирают, независимо друг от друга, из группы, состоящей из F, Cl, метила, этила, пропила, изопропила, метокси, этокси, пропокси, пиперазинила, тетрагидропиранила, -CN, 2-метоксиэтокси, 2-гидроксиэтокси, фторметокси, дифторметокси, N-метилкарбамоила (-C(=O)-NH-CH3), 2-метиламиноэтокси, 1-метилазетидин-3-илметокси, тридейтерометокси, трифторметокси, метилсульфонилметокси, метилсульфонила, циклопропила, аллилокси, пиперазинила и азетидинилокси. Предпочтительным является отсутствие замещения, моно- или дизамещение.
Предпочтительным вариантом осуществления НЕТ является незамещенный или замещенный пиридинил, например, моно- или дизамещенный пиридинил. Монозамещенные пиридинилы предпочтительно замещены в положении 3 пиридинового кольца и присоединены через положение 2 или 4, дизамещенные пиридинилы предпочтительно замещены в положениях 3 и 5 пиридинового кольца и присоединены через положение 2 или 4. Данный предпочтительный вариант осуществления можно с успехом комбинировать с предпочтительными вариантами осуществления Het1, в частности, предпочтительными вариантами осуществления, в которых Het1 означает незамещенный или замещенный пиразолил или альтернативно незамещенный или замещенный триазолил, и, в частности, с упомянутыми выше особенно предпочтительными вариантами осуществления.
В других предпочтительных вариантах осуществления НЕТ является незамещенным, но предпочтительно моно- или дизамещенным пиразолом. Данный вариант осуществления также можно с успехом комбинировать с предпочтительными вариантами осуществления Het1, в частности, предпочтительными вариантами осуществления, в которых Het1 означает незамещенный или замещенный пиразолил или альтернативно незамещенный или замещенный триазолил, и в частности с упомянутыми выше особенно предпочтительными вариантами осуществления.
В дальнейшем предпочтительном варианте осуществления, НЕТ является незамещенным, но предпочтительно монозамещенным пиримидином, где пиримидин предпочтительно замещен в положении 5 и присоединен через положение 2 или 4. Данный вариант осуществления также можно с успехом комбинировать с предпочтительными вариантами осуществления Het1, в частности, предпочтительными вариантами осуществления, в которых Het1 является незамещенным или замещенным пиразолилом или альтернативно незамещенным или замещенным триазолилом, и, в частности, с упомянутыми выше особенно предпочтительными вариантами осуществления.
В предпочтительных вариантах осуществления любой из формул (I), (II), (III) и (IV), НЕТ может быть выбран, например, из следующих 5- или 6-членных моноциклических ароматических гетероциклов: пиридин-2-ил, пиридин-4-ил, 5-аллилокси-3-фторпиридин-2-ил, 5-(азетидин-3-илокси)-3-фторпиридин-2-ил, 5-хлор-3-фторпиридин-2-ил, 3-циклопропилпиридин-4-ил, 3-циклопропил-5-фторпиридин-4-ил, 3,5-дифторпиридин-2-ил, 3,5-дифторпиридин-4-ил, 5-дифторметокси-3-фторпиридин-2-ил, 3-дифторметокси-5-фторпиридин-4-ил, 5-этокси-3-фторпиридин-2-ил, 3-фтор-5-(1-метилазетидин-3-илметокси)пиридин-2-ил, 3-фтор-5-метоксипиридин-4-ил, 3-фтор-5-метоксипиридин-2-ил, 3-фтор-5-фторметоксипиридин-2-ил, 3-фтор-5-фторметоксипиридин-4-ил, 3-фторпиридин-2-ил, 3-фтор-5-метилсульфонилметоксипиридин-2-ил, 3-фтор-5-метилсульфонилпиридин-2-ил, 3-фтор-5-(2-метиламиноэтокси)пиридин-2-ил, 3-фтор-5-метилпиридин-4-ил, 3-фтор-5-метилпиридин-2-ил, 3-фторпиридин-4-ил, 3-фторпиридин-2-ил, 3-фтор-5-пиперазин-1-илпиридин-2-ил, 3-хлорпиридин-4-ил, 3-этилпиридин-4-ил, 3-этил-5-фторпиридин-4-ил, 3-этил-5-метилпиридин-4-ил, 5-фторпиридин-2-ил, 3-метилпиридин-4-ил, 3-метоксипиридин-4-ил, 2-цианопиридин-4-ил, 3-цианопиридин-4-ил, 3-цианопиридин-6-ил, 3-циано-5-фторпиридин-4-ил, 3-фтор-5-(2-метоксиэтокси)пиридин-2-ил, 3-фтор-5-(2-гидроксиэтокси)пиридин-2-ил, 3-фтор-5-(тридейтерометокси)пиридин-4-ил, 3-фтор-5-(тридейтерометокси)пиридин-2-ил, 5-фтор-3-(N-метилкарбамоил)пиридин-6-ил, 5-фторпиримидин-2-ил, 5-фторпиримидин-4-ил, пиримидин-2-ил, пиримидин-5-ил, 1Н-пиразол-4-ил, 1-этил-3-метил-1Н-пиразол-4-ил, 1,2-диметил-1Н-пиразол-4-ил, 1,3-диметил-1Н-пиразол-4-ил, 1-метил-1Н-пиразол-4-ил, 1-(тетрагидропиран-4-ил)-1H-пиразол-4-ил, 2-метил-2Н-пиразол-3-ил, 3-метил-1Н-пиразол-4-ил, 3,5-диметил-1Н-пиразол-4-ил, 3-фтор-1-метилпиразол-4-ил, тиазол-2-ил, 2-метилтиазол-4-ил и 1-метил-1Н-имидазолил. Особое предпочтение отдают 5-хлор-3-фторпиридин-2-илу, 3,5-дифторпиридин-2-илу, 3,5-дифторпиридин-4-илу, 5-дифторметокси-3-фторпиридин-2-илу, 3-дифторметокси-5-фторпиридин-4-илу, 5-этокси-3-фторпиридин-2-илу, 3-фтор-5-метоксипиридин-4-илу, 3-фтор-5-метоксипиридин-2-илу, 3-фтор-5-фторметоксипиридин-2-илу, 3-фтор-5-фторметоксипиридин-4-илу, 3-фторпиридин-2-илу, 3-фтор-5-метилсульфонилметоксипиридин-2-илу, 3-фтор-5-метилпиридин-4-илу, 3-фтор-5-метилпиридин-2-илу, 3-фторпиридин-4-илу, 3-этилпиридин-4-илу, 3-этил-5-фторпиридин-4-илу, 3-метилпиридин-4-илу, 3-метоксипиридин-4-илу, 3-фтор-5-(2-метоксиэтокси)пиридин-2-илу, 3-фтор-5-(2-гидроксиэтокси)пиридин-2-илу, 3-фтор-5-(тридейтерометокси)пиридин-4-илу, 3-фтор-5-(тридейтерометокси)пиридин-2-илу, 5-фторпиримидин-2-илу, 5-фторпиримидин-4-илу, 1,3-диметил-1H-пиразол-4-илу, 1-метил-1H-пиразол-4-илу, 1-(тетрагидропиран-4-ил)-1Н-пиразол-4-илу и 2-метилтиазол-4-илу.
Предпочтения для упомянутых выше 5- или 6-членных моноциклических ароматических циклов или гетероциклов также применимы, в частности, к соединениям формул (I), (II), (III) и (IV), в комбинации с предпочтительными вариантами осуществления для Het1, в частности, вариантом Het1, выбранным, из пиридинила, пиримидинила, пиразолила, триазолила и имидазолила, которые могут быть незамещены или замещены согласно вышеприведенному определению, и особенно, в частности, также с вариантами, в которых Het1 означает пиразолил, который может быть незамещен или замещен согласно вышеприведенному определению и может быть выбран, например, из примеров, прямо упомянутых выше. Они также применяются, в частности, к вариантам осуществления, в которых Het1 означает триазолил, и может быть выбран, например, из примеров, прямо упомянутых выше.
В других иллюстративных вариантах осуществления любой из формул (I), (II), (III) и (IV), НЕТ может быть выбран из пирроло[3,2-с]пиридинила, пирроло[2,3-b]пиридинила и хинолинила, которые в каждом случае могут быть незамещены или замещены, как упомянуто для соединения (I) и, в частности, для предпочтительных моноциклических вариантов. Примерами являются 1Н-пирроло[3,2-с]пиридин-6-ил, 1Н-пирроло[2,3-b]пиридин-6-ил или 5-фтор-1Н-пирроло[2,3-b]пиридин-6-ил, в каждом случае, в частности, также в комбинации с одним из предпочтительных вариантов осуществления Het1, упомянутых выше.
Чрезвычайное предпочтение отдают соединениям, показанным в Таблице 1 ниже, и их фармацевтически пригодным производным, солям, сольватам, таутомерам и/или стереоизомерам, или свободным формам, включая их смеси во всех соотношениях.










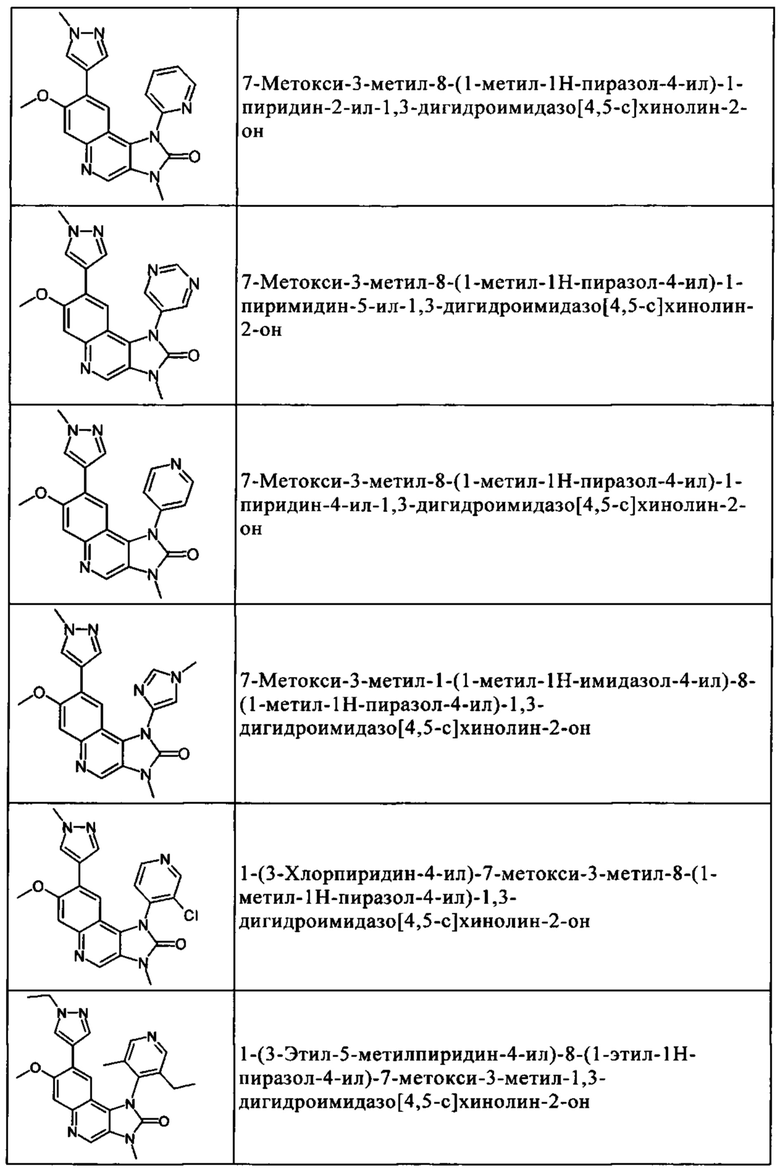










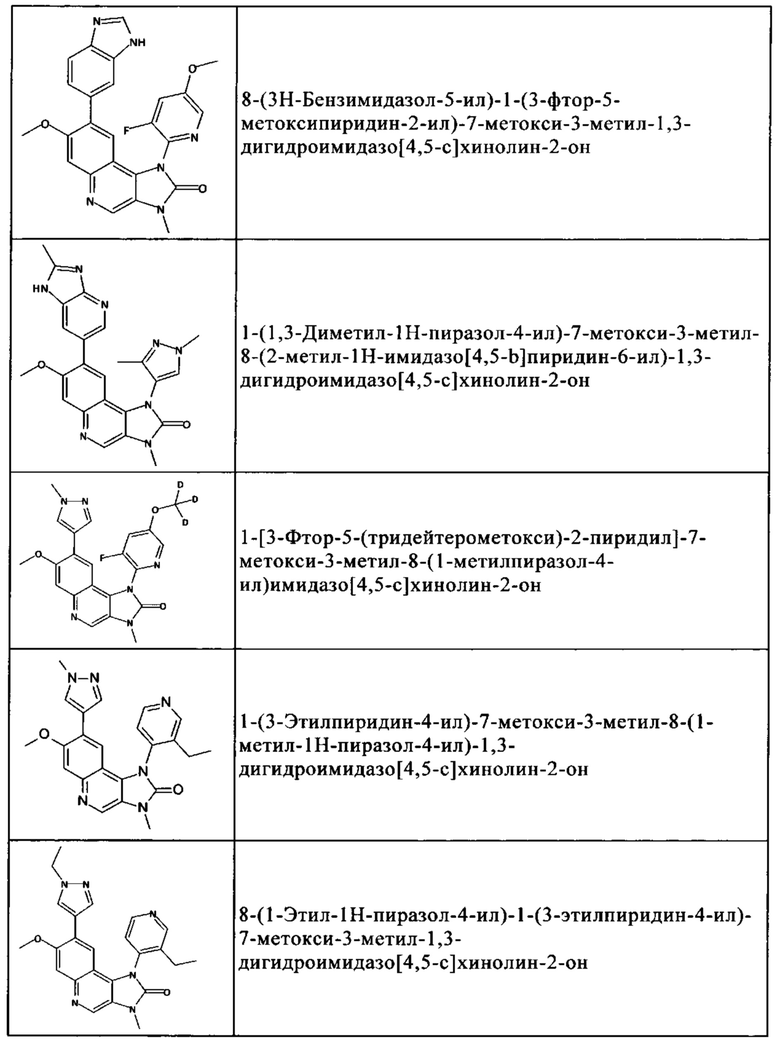



Каждое из значений R1, R3, НЕТ и Het1, раскрытых в контексте вышеуказанных предпочтительных соединений, также следует рассматривать в качестве предпочтительного значения соответствующего радикала, независимо от другого замещения основной структуры молекулы, т.е. в качестве возможных значений R1, R3, НЕТ и Het1 в каждом случае независимо друг от друга.
Получение
Соединения формулы (I), а также исходные вещества для их получения получают методами, сами по себе известными, как описано в литературе (например, в стандартных работах, таких как Houben-Weyl, Methoden der organischen Chemie [Методы органической химии], Georg-Thieme-Verlag, Штутгарт) и/или методами, известными специалисту в данной области техники, и при реакционных условиях, которые известны и являются подходящими для упомянутых реакций. Также можно применять варианты, которые сами по себе известны и не упомянуты здесь более подробно. Соединения в соответствии с изобретением можно получить с помощью или аналогично синтезам, описанным подробно в ПРИМЕРАХ 1-13 путем подходящего выбора или адаптации исходных веществ. Для большинства соединений в соответствии с изобретением, синтез, описанный в ПРИМЕРЕ 1, может быть подходящим образом изменен и, таким образом, использован аналогично. Аминопроизводные и сложные эфиры бороновой кислоты или аналоги, которые могут применяться в соответствующих синтезах, обобщены ниже на Схеме 4. Кроме того, также делается ссылка на раскрытие WO 2010/139731, которое должно быть включено во всей своей полноте в настоящее раскрытие путем ссылки.
Способ и последующее выделение продукта реакции из реакционной смеси можно в основном осуществлять в форме периодической или непрерывной методики проведения реакции. Непрерывная методика проведения реакции включает, например, реакцию в реакторе непрерывного действия с мешалкой, каскадном реакторе с мешалкой, петлевом реакторе или реакторе с пересекающимися потоками, в проточной трубе или в микрореакторе. Реакционные смеси необязательно обрабатывают, при необходимости, путем фильтрования через твердые фазы, хроматографии, разделения между несмешивающимися фазами (например, экстрагирования), адсорбции на твердых подложках, удаления растворителей и/или азеотропных смесей путем перегонки, селективной перегонки, сублимации, кристаллизации, сокристаллизации или путем нанофильтрования на мембранах.
Исходные соединения обычно известны. Если они являются новыми, их можно получить с помощью методов, которые сами по себе известны. При необходимости, исходные вещества могут быть образованы in situ без выделения их из реакционной смеси, а вместо этого с незамедлительным превращением далее в соединения в соответствии с изобретением. Подобным образом можно проводить реакцию постадийно.
Фармацевтически пригодные формы
Для целей изобретения соединения в соответствии с изобретением определяются таким образом, чтобы они также включали фармацевтически пригодные производные, соли, сольваты, включая гидраты, предшественники соединений, таутомеры и оптически активные формы (такие как, например, стереоизомеры, диастереомеры, энантиомеры, рацематы). Изобретение также относится к применению смесей соединений формулы (I), например, смесей двух диастереомеров, например, в соотношении 1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 или 1:1000. Особенно предпочтительными являются смеси стереоизомерных соединений.
Под сольватами соединений подразумевают аддукции молекул инертного растворителя на соединениях, которые образуются благодаря силе их взаимного притяжения. Сольватами являются, например, моно- или дигидраты или алкоголяты.
Под фармацевтически пригодными производными подразумевают, например, соли соединений в соответствии с изобретением и так называемые предшественники или пролекарства соединений. Под предшественниками или пролекарствами подразумевают, например, соединения формулы (I), модифицированные с помощью алкильной или ацильной групп, Сахаров или олигопептидов, которые быстро расщепляются в организме с получением действующих соединений в соответствии с изобретением. Они также включают поддающиеся биологическому разложению полимерные производные соединений в соответствии с изобретением, как описано, например, в Int. J. Pharm. 115, 61-67 (1995). Любое соединение, которое может превращаться in vivo в биологически активный компонент, то есть соединения формулы (I), является предшественником в смысле данного изобретения. Любое биологически активное соединение, которое получается вследствие in vivo метаболизирования соединения в соответствии с изобретением, является метаболитом в смысле настоящего изобретения.
Вышеуказанные соединения в соответствии с изобретением могут применяться в своей заключительной, несолевой форме. С другой стороны, настоящее изобретение также охватывает применение данных соединений в форме их фармацевтически приемлемых солей, которые могут быть получены из различных органических и неорганических кислот и оснований с помощью методик, известных в данной области техники. Фармацевтически приемлемые солевые формы соединений в соответствии с изобретением получают, главным образом, с помощью обычных методов. В случае, если соединения содержат карбоксильную группу, то одна из их пригодных солей может быть образована с помощью реакции соединения с пригодным основанием с получением соответствующей соли присоединения основания. Такими основаниями являются, например, гидроксиды щелочных металлов (например, гидроксид калия, гидроксид натрия и гидроксид лития), гидроксиды щелочноземельных металлов (например, гидроксид бария и гидроксид кальция), алкоголяты щелочных металлов (например, этилат калия и пропилат натрия) и различные органические основания, такие как пиперидин, диэтаноламин и N-метилглутамин. Основание может быть превращено в ассоциативную соль присоединения кислоты с использованием кислоты, например, по реакции эквивалентных количеств основания и кислоты в инертном растворителе, таком как, например, этанол, и последующего упаривания. Пригодными кислотами для этой реакции являются, в частности, те кислоты, которые дают физиологически приемлемые соли, такие как, например, галогеноводороды (например, хлороводород, бромоводород или йодоводород), другие минеральные кислоты и их соответствующие соли (например, сульфат, нитрат или фосфат и т.п.), алкил- и моноарилсульфонаты (например, этансульфонат, толуолсульфонат и бензолсульфонат) и другие органические кислоты и их соответствующие соли (например, ацетат, трифторацетат, тартрат, малеат, сукцинат, цитрат, бензоат, салицилат, аскорбат и т.п.). Соли с физиологически неприемлемыми кислотами, например, пикраты, могут применяться для выделения и/или очистки соединений в соответствии с изобретением.
Что касается изложенного выше, можно видеть, что выражение "фармацевтически пригодная соль", или также "фармацевтически приемлемая соль" в данной связи следует понимать в значении соединения в соответствии с изобретением, которое находится в форме одной из его солей, в частности, если такая солевая форма соединения придает улучшенные фармакокинетические свойства по сравнению с его свободной формой. Фармацевтически приемлемая солевая форма соединения также может обеспечивать данное соединение желательным фармакокинетическим свойством впервые и может даже оказать положительное влияние на фармакодинамику соединения в отношении его терапевтического действия в организме.
Соединения в соответствии с изобретением могут быть хиральными благодаря их молекулярной структуре и, соответственно, встречаются в различных энантиомерных формах. Вследствие этого они могут существовать в рацемической или в оптически активной форме. Поскольку фармацевтическая активность рацематов или стереоизомеров соединений формулы I может отличаться, может быть желательным применение энантиомеров. В этих случаях, конечный продукт или даже промежуточный продукт может быть разделен на энантиомерные соединения с помощью химических или физических мер, известных специалисту в данной области техники или даже используемых в качестве таковых в синтезе.
Общеизвестно, что атомы могут иметь атомные массы или массовые числа, которые могут отличаться от обычно встречающихся в природе атомных масс или массовых чисел. Примерами изотопов, которые являются коммерчески доступными и которые могут быть включены в соединение в соответствии с изобретением с помощью известных методов, являются изотопы водорода, углерода, азота, кислорода, фосфора, фтора и хлора, например, 2Н, 3Н, 13С, 14С, 15N, 18O, 17O, 31Р, 32Р, 35S, 18F и 36CI. Включение более тяжелых изотопов, в частности, дейтерия (2Н), в соединение в соответствии с изобретением имеет терапевтические преимущества, которые заключаются в более высокой метаболической стабильности данного меченого изотопами соединения. Более высокая метаболическая стабильность непосредственно приводит к увеличению периода полувыведения in vivo, что позволяет применение более низкой дозировки.
Следовательно, определения атомов Н, С, N, и т.д., используемые в соединениях в соответствии с изобретением, также относятся к более тяжелым изотопам таких атомов.
Особое предпочтение отдают в соответствии с изобретением применению D (дейтерий, 2Н) взамен водорода (1Н). Дейтерий может быть включен в соединения в соответствии с изобретением, например, с помощью подходящего заместителя на НЕТ, например, тридейтерометила или тридейтерометокси.
Применение
Неожиданно было обнаружено, что соединения в соответствии с изобретением оказывают специфическое ингибирование протеинкиназ, в особенности киназы ATM. Соответственно, настоящее изобретение обеспечивает ингибиторы ATM, которые выбирают из соединений в соответствии с изобретением.
В рамках представленного в данной заявке изобретения новые 2,3-дигидро-1H-имидазол[4,5-с]хинолиновые соединения были обеспечены впервые. Соединения в соответствии с изобретением контролируют серин/треонин-протеинкиназы, в частности, киназу ATM, с отличной аффинностью и/или селективностью. Соединения формулы (I) и их производные отличаются высокой специфичностью и стабильностью, низкой стоимостью получения и удобством в обращении. Такие свойства лежат в основе воспроизводимого способа действия и надежного и безопасного взаимодействия с соответствующими целевыми структурами. Изобретение также включает применение данных 2,3-дигидро-1H-имидазол[4,5-с]хинолиновых производных для ингибирования, регуляции и/или модуляции сигнального каскада серин/треонин-протеинкиназ, в частности, киназы ATM, и таким образом предлагает новые инструменты для исследований и/или диагностики.
Следовательно, изобретение также относится к применению соединений в соответствии с изобретением и/или их физиологически приемлемых сольватов, солей, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, для ингибирования серин/треонин-протеинкиназ, в частности, киназы ATM. Термин "ингибирование" относится к любому снижению активности, которое основано на действии особых соединений в соответствии с изобретением в том смысле, что последние способны взаимодействовать с целевой молекулой таким образом, что делается возможным распознавание, связывание и блокировка. Соединения отличаются высокой аффинностью к киназе ATM, обеспечивающей надежное связывание и предпочтительно полную блокировку активности киназы. Более того, данные соединения очень селективны и таким образом позволяют исключительное и прямое распознавание киназы ATM. Термин "распознавание" относится в данном случае к любому типу взаимодействия между соединением и указанными целевыми молекулами, в частности, ковалентным или нековалентным связям, таким как, например, ковалентная связь, гидрофобные/гидрофильные взаимодействия, силы Ван-дер-Ваальса, притяжение ионов, водородные связи, лиганд/рецепторные взаимодействия, взаимодействия пар оснований нуклеотидов или взаимодействия между эпитопом и сайтом связывания антитела.
Соединения в соответствии с изобретением и/или их физиологически приемлемые соли, таутомеры и/или стереоизомеры, включая их смеси во всех соотношениях, являются подходящими для применения для лечения заболеваний, которые вызываются, опосредуются и/или распространяются активностью серин/треонин-протеинкиназ, в частности, киназой ATM.
Настоящее изобретение относится к соединениям в соответствии с изобретением и/или их физиологически приемлемым производным, сольватам, солям, таутомерам и/или стереоизомерам, включая их смеси во всех соотношениях, для применения в качестве лекарственного средства.
Изобретение раскрывает соединения в соответствии с изобретением и/или его физиологически приемлемые соли, таутомеры и/или стереоизомеры, включая их смеси во всех соотношениях, для применения для лечения заболеваний, которые вызываются, опосредуются и/или распространяются активностью серин/треонин-протеинкиназ, в частности, киназой ATM.
Следовательно, настоящее изобретение также относится к соединениям в соответствии с изобретением и/или их физиологически приемлемым производным, сольватам, солям, таутомерам и/или стереоизомерам, включая их смеси во всех соотношениях, для применения для лечения заболеваний, которые вызываются, опосредуются и/или распространяются активностью серин/треонин-протеинкиназ, в частности, киназой ATM. Соответственно, настоящее изобретение также относится к применению соединений в соответствии с изобретением и/или их физиологически приемлемых производных, сольватов, солей, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, для получения лекарственного средства для лечения заболеваний, которые вызываются, опосредуются и/или распространяются активностью серин/треонин-протеинкиназ, в частности, киназой ATM. Другими словами, настоящее изобретение также раскрывает соединение в соответствии с изобретением и/или его фармацевтически пригодное производное, соль, сольват, таутомер или стереоизомер для применения для лечения заболеваний, которые находятся под влиянием ингибирования киназы ATM.
Для определения соответствующего сигнального пути и с целью обнаружения взаимодействия между различными сигнальными путями, были разработаны пригодные модели или модельные системы, например, модели культур клеток (Khwaja и др. (1997) ЕМВО 16: 2783) и модели трансгенных животных (White и др. (2001) Oncogene 20: 7064). С целью определения определенных стадий в сигнальном каскаде, взаимодействующие соединения могут применяться с целью модулирования сигнала (Stephens и др. (2000) Biochemical J 351: 95). Кроме того, соединения в соответствии с изобретением также могут применяться в качестве реагентов для тестирования зависимых от киназ сигнальных путей в животных моделях и/или в модели культур клеток или при клинических заболеваниях, упомянутых в данной заявке. Как уже было указано здесь, эти сигнальные пути являются важными для различных заболеваний. Соответственно, соединения в соответствии с изобретением полезны для профилактики, терапии и/или борьбы с развитием заболеваний, которые зависят от сигнальных путей с участием серин/треонин-протеинкиназ, предпочтительно киназы ATM.
Настоящее изобретение также относится к соединениям в соответствии с изобретением и/или их физиологически приемлемым производным, сольватам, солям, таутомерам и/или стереоизомерам, включая их смеси во всех соотношениях, для применения для лечения злокачественного новообразования, опухолей и/или метастазов, и к их применению для получения лекарственного средства для конкретно этих целей.
Опухоль выбирают, в частности, из группы, включающей заболевания плоского эпителия, мочевого пузыря, желудка, почек, головы, шеи, пищевода, шейки матки, щитовидной железы, кишечника, печени, головного мозга, предстательной железы, мочеполового тракта, лимфатической системы, гортани, легкого, кожи, крови и иммунной системы, и/или злокачественное новообразование выбирают из группы, включающей моноцитарный лейкоз, аденокарциному легкого, мелкоклеточную карциному легкого, рак поджелудочной железы, глиобластому, карциному кишечника, карциному молочной железы, острый миелобластный лейкоз, хронический миелобластный лейкоз, острый лимфобластный лейкоз, хронический лимфобластный лейкоз, лимфому Ходжкина и неходжскинскую лимфому.
Настоящее изобретение дополнительно относится к способу получения лекарственного средства, предпочтительно для применения для лечения злокачественного новообразования и/или опухолей, предпочтительно злокачественного новообразования или опухоли упомянутого выше типа, включающему:
i. определение того, что концентрация, при которой соединение в соответствии с изобретением и/или его фармацевтически пригодное производное, соль, сольват, таутомер или стереоизомер обеспечивает 50% ингибирование активности киназы ATM, составляет 500 нМ или менее, предпочтительно 100 нМ, 10 нМ, 1 нМ или менее, и
ii. получение фармацевтической композиции, которая содержит данное соединение.
Определение параметров 50% ингибирования активности киназы ATM предпочтительно осуществляют в данном случае с помощью описанного здесь анализа (IC50 ATM).
Соединения в соответствии с изобретением и/или их физиологически приемлемые производные, сольваты, соли, таутомеры и/или стереоизомеры, включая их смеси во всех соотношениях, также могут быть подходящими для применения для замедлении процессов старения, где замедление имеет место в отношении сравнения продолжительности жизни получающего лечение/обработанных организма "хозяина" или его клеток, культур клеток, тканей или органов с соответствующими положительными или отрицательными контролям и/или статистикой.
Более того, изобретение предлагает способ лечения злокачественного новообразования, опухолей и/или метастазов, в котором эффективное количество по меньшей мере одного соединения в соответствии с изобретением и/или его физиологически приемлемых производных, сольватов, солей, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, вводят субъекту, получающему лечению. Предпочтительными субъектами в смысле изобретения являются люди или животные, особенно предпочтительно люди. В этом случае специалисту в данной области техники известно, что он может вводить соединения в соответствии с изобретением, которые могут, несомненно, также применяться в виде фармацевтической композиции в соответствии с изобретением, в организм, в частности, пациенту-человеку, в различных дозах. Эффективное количество и тип введения могут быть определены специалистом в данной области техники с помощью обычных экспериментов. Предыдущая идея изобретения и его вариантов является действительной и может применяться без ограничений в способах лечения, если это представляется подходящим.
Соединения в соответствии с изобретением, их соли, изомеры, таутомеры, энантиомеры, диастереомеры, рацематы, производные, пролекарственные препараты и/или метаболиты являются эффективными не только в случае указанных клинических картин, но также в диагностике и терапии всех заболеваний, связанных с ATM-сигнальным каскадом, в особенности в целях ингибирования пролиферации клеток и миграции.
Кроме того, ингибиторы в соответствии с изобретением можно применять для лечения ретровирусных заболеваний путем подавления ретровирусной интеграции (R. Daniel (1999) Science 284: 644). В заключение, ингибиторы в соответствии с изобретением могут применяться в качестве иммуномодуляторов и модуляторов сохранения теломер.
Более того, настоящее изобретение относится к применению соединения в соответствии с изобретением и/или его фармацевтически пригодного производного, соли, сольвата, таутомера или стереоизомера для ингибирования протеинкиназы, в частности, киназы ATM in vitro.
Указанное применение соединений в соответствии с изобретением и/или их фармацевтически пригодных производных, сольватов, солей, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, для ингибирования серин/треонин-протеинкиназы, в частности, киназы ATM, может иметь место в in vitro или in vivo моделях. Восприимчивость отдельной клетки к обработке соединениями в соответствии с изобретением можно определить с помощью тестирования in vitro. Типично, культуру клеток инкубируют с соединением в соответствии с изобретением при различных концентрациях в течение периода времени, достаточного для индуцирования активными агентами некроза клеток или для ингибирования пролиферации клеток, жизнеспособности клеток или миграции, обычно в диапазоне между приблизительно одним часом и одной неделей. Для тестирования in vitro, могут быть использованы культивируемые клетки из биопсийного образца. Затем определяют количество клеток, оставшихся после обработки. Применение in vitro осуществляют, в частности, на образцах видов млекопитающих, которые страдают от злокачественного новообразования, опухолей, метастазов, нарушений ангиогенеза, ретровирусных заболеваний, иммунопатологических заболеваний и/или патогенных процессов старения. "Хозяин" или пациент может принадлежать к любому виду млекопитающих, например, к приматам, в частности людям, а также грызунам (включая мышей, крыс и хомячков), кроликам, лошадям, коровам, собакам, кошкам, и т.д. Животные модели представляют интерес для экспериментальных исследований, обеспечивая модель для лечения заболевания человека.
Тестирование множества особых соединений позволяет выбрать активное соединение, которое представляется наиболее пригодным для лечения пациента. Дозу in vivo выбранного соединения преимущественно подбирают исходя из восприимчивости киназы и/или тяжести заболевания пациента принимая во внимание данные in vitro, в результате чего терапевтическое действие заметно увеличивается. Доза варьирует в зависимости от используемого особого соединения, конкретного заболевания, состояния пациента и т.д. Терапевтической дозы обычно достаточно для существенного уменьшения популяции нежелательных клеток в целевой ткани, в то время как жизнеспособность пациента сохраняется.
Идея раскрытого здесь изобретения и его вариантов осуществления, относящихся к применению соединений в качестве или для получения лекарственного средства для лечения заболеваний, является действительной и может применяться без ограничений к применению соединений для ингибирования активности киназ, если это представляется подходящим.
Лечение, как правило, продолжают до достижения значительного снижения, например, по меньшей мере, около 50% снижения клеточной нагрузки, и может быть продолжено до тех пор, пока в организме по существу не будут обнаруживаются нежелательные клетки. В тестах этого типа, соединения в соответствии с изобретением демонстрируют и вызывают ингибирующее действие, которое, как правило, подтверждается значениями IC50 в подходящем диапазоне, предпочтительно в микромолярном диапазоне и более предпочтительно в наномолярнном диапазоне. Киназа ингибируется, в частности, до степени 50%, если концентрация соединений составляет меньше чем 1 мкМ, предпочтительно равна или меньше чем 0.5 мкМ, особенно предпочтительно меньше чем 0.1 мкМ, 0.05 мкМ или 0.001 мкМ. Эту концентрацию называют значением IC50 и предпочтительно определяют с помощью описанного здесь анализа (IC50 ATM). В соответствии с обычной номенклатурой "мкМ" означает микромоли на литр, "нМ" означает наномоли на литр.
Анализы
Соединения в соответствии с изобретением демонстрируют полезную биологическую активность, которая может быть продемонстрирована в ходе тестов, описанных в данной заявке, таких как, например, ферментные анализы.
Измерение киназной активности представляет собой способ, хорошо известный специалисту в данной области техники. Общие тестовые системы для определения киназной активности с использованием субстратов, например, гистона (Alessi и др. (1996) FEBS Lett. 399(3): 333) или основного миелинового белка, описаны в литературе ( & Glenney (1992) JBC 267:14535). Различные системы для анализа доступны для идентификации ингибиторов киназы. В анализе сцинтилляционной схожести (Sorg и др. (2002) J Biomolecular Screening 7: 11) и анализе флэш-планшетов радиоактивное фосфорилирование белка или пептида в качестве субстрата измеряют с использованием АТФ. В присутствии ингибиторного соединения выявляется снижение радиоактивного сигнала, или не выявляется никакого сигнала вообще. Более того, в качестве аналитических методов полезны методы гомогенного переноса энергии флуоресцентного резонанса с разрешением во времени (HTR-FRET) и флуоресцентной поляризации (FP) (Sills и др. (2002) J Biomolecular Screening 191). В других нерадиоактивных методах анализа на основе ELISA используются специфические фосфо-антитела (фосфо-АТ). Фосфо-АТ связываются только с фосфорилированным субстратом. Это связывание может быть определено с помощью хемолюминисценции с использованием вторичного антиовечьего антитела, конъюгированного с пероксидазой.
& Glenney (1992) JBC 267:14535). Различные системы для анализа доступны для идентификации ингибиторов киназы. В анализе сцинтилляционной схожести (Sorg и др. (2002) J Biomolecular Screening 7: 11) и анализе флэш-планшетов радиоактивное фосфорилирование белка или пептида в качестве субстрата измеряют с использованием АТФ. В присутствии ингибиторного соединения выявляется снижение радиоактивного сигнала, или не выявляется никакого сигнала вообще. Более того, в качестве аналитических методов полезны методы гомогенного переноса энергии флуоресцентного резонанса с разрешением во времени (HTR-FRET) и флуоресцентной поляризации (FP) (Sills и др. (2002) J Biomolecular Screening 191). В других нерадиоактивных методах анализа на основе ELISA используются специфические фосфо-антитела (фосфо-АТ). Фосфо-АТ связываются только с фосфорилированным субстратом. Это связывание может быть определено с помощью хемолюминисценции с использованием вторичного антиовечьего антитела, конъюгированного с пероксидазой.
Для целей настоящего изобретения, ингибирование активности ATM предпочтительно определяли с помощью следующего анализа:
Анализ активности киназы ATM - определение ингибирования ATM (IC50 ATM):
Значение IC50 определяли с помощью биохимического анализа активности киназы ATM. Анализ состоит из двух стадий: ферментативной реакции и стадии детектирования. Прежде всего ATM (мутированный при атаксии-телеангиэктазии) белок и исследуемое вещество инкубируют при разных концентрациях с добавлением субстратного белка р53 и АТФ. ATM опосредует фосфорилирование р53 по нескольким положениям, в том числе по аминокислоте S15. Количество фосфорилированного р53 определяют с помощью специфических антител и методов TR-FRET. Ферментативный анализ с использованием ATM осуществляют в виде 384-луночного анализа на основе TR-FRET (HTRF™, Cisbio Bioassays). На первой стадии очищенную человеческую рекомбинантную ATM (человеческая ATM, полноразмерная, GenBank ID NM_000051, экспрессированная в клеточной линии млекопитающего) инкубируют в аналитическом буфере в течение 15 минут с ингибитором ATM при различных концентрациях исследуемого вещества и без него в качестве отрицательного или нейтрального контроля. Аналитический буфер содержит 25 мМ HEPES pH 8.0, 10 мМ Mg(CH3COO)2, 1 мМ MnCl2, 0,1% BSA и 0,01% Brij® 35, 5 мМ дитиотреитол (DTT). Растворы исследуемого вещества распределяют в микротитрационные планшеты, используя ECHO 555 (Labcyte). На второй стадии добавляют очищенную человеческую рекомбинантную cmyc-меченую р53 (человеческая р53, полноразмерная, GenBank ID ВС003596, экспрессированная в Sf21 клетках насекомых) и АТФ, и реакционную смесь инкубируют при 22°С в течение 30-35 минут. Фармакологически релевантный анализируемый объем составляет 5 мкл. Конечные концентрации в анализе во время инкубирования реакционной смеси составляют 0.3-0.4 нМ ATM, 50-75 нМ р53 и 10 мкМ АТФ. Ферментативную реакцию останавливают путем добавления EDTA. Образование фосфорилированной р53 в результате ATM-опосредованной реакции в присутствии АТФ детектируют с помощью специфических антител [меченых флуорофорен европием (Eu) в качестве донора и d2 в качестве акцептора (Cisbio Bioassays)], которые позволяют FRET. К реакционной смеси добавляют 2 мкл останавливающего раствора, содержащего антитела (12.5 мМ HEPES pH 8.0, 125 мМ EDTA, 30 мМ хлорид натрия, 300 мМ фторид калия, 0.1006% Твин-20, 0.005% Brij® 35, 0.21 нМ анти-фосфо-р53 (ser15)-Eu антитело и 15 нМ анти-cmyc-d2 антитело). После инкубирования, обычно в течение 2 часов (в диапазоне между 1.5 и 15 ч), что требуется для проявления сигнала, планшеты анализируют в планшет-ридере (EnVision, PerkinElmer) с использованием TRF метода (и с лазерным возбуждением). После возбуждения донора - европия на длине волны 340 нм, измеряют испускаемый флуоресцентный свет как акцептора d2 на длине волны 665 нм, так и донора Eu на длине волны 615 нм. Количество фосфорилированной р53 прямо пропорционально частному от деления количеств испускаемого света, т.е. относительных единиц флуоресценции (RFU) на длинах волн 665 нм и 615 нм. Данные измерений обрабатывали с помощью программного обеспечения Genedata Screener. Определение значений IC50 осуществляли, в частности, путем подгонки кривой доза/действие к точкам данных с помощью нелинейного регрессионного анализа.
IC50 = полумаксимальная ингибирующая концентрация
АТФ = аденозинтрифосфат
TR-FRET = время разрешенный флуоресцентный индуктивно-резонансный перенос энергии
HTRF® = гомогенная флуоресценция с временным разрешением
HEPES = 2-(4-(2-гидроксиэтил)-1-пиперазинил)этансульфоновая кислота
Mg(CH3COO)2 = ацетат магния
MnCl = хлорид марганца(II)
BSA = альбумин бычьей сыворотки
EDTA = этилендиаминтетраацетат
TRF = флуоресценция с временным разрешением
Активность веществ в соответствии с изобретением в клеточном окружении можно определить с помощью приведенного ниже анализа:
Клеточный pCHK2 анализ:
Для идентификации веществ, которые ингибируют фосфорилирование протеинкиназы CHK2 по аминокислоте треонину 68, использовали "многопараметрический" анализ на основе иммунофлюоресценции в клетках НСТ116.
In vitro клеточный иммунофлюоресцентный анализ для идентификации ингибиторов индуцированного блеомицином фосфорилирования CHK2 (фосфо-Thr68) в клеточной линии карциномы ободочной кишки человека НСТ116:
НСТ116 клетки высевают при определенной плотности клеток в 384-луночные планшеты в культуральную среду (DMEM с высоким содержанием глюкозы, 2 мМ GlutaMax, 1 мМ пируват Na, 10% FCS) и инкубируют в течение ночи при 37°С и 10% CO2. На следующий день добавляют исследуемые вещества в определенном интервале концентраций (от 1 нМ до 30 мкМ) в комбинации с 10 мкМ блеомицином, причем концентрацию растворителя ДМСО поддерживают постоянной на уровне 0.5%. После инкубирования в течение четырех часов при 37°С и 10% СО2, клетки фиксируют (5 мин, 4% формальдегид в PBS), пермеабилизируют (10 мин, 0.2% тритон Х-100 в PBS) и, после блокирования неспецифических сайтов связывания (10% сыворотка козла, 1% BSA в PBS), инкубируют в течение ночи при 4°С со специфическим анти-pCHK2 антителом (cell signalling #2661). pCHK2 (Thr68) определяют с использованием Alexa488-меченого вторичного антитела против кроличьего IgG. Параллельное окрашивание ДНК йодидом пропидия делает возможным определение числа клеток. pCHK2 сигнал детектируют с использованием а многопараметрического визуализирующего прибора (Molecular Devices IMX Ultra) и автоматического анализа изображений с использованием программного обеспечения MetaXpress, прилагающегося к прибору. Определяют число ядер клеток, которые имеют сигнал pCHK2 выше определенного фонового значения.
Более того, действие, в частности, ингибирование, в отношении других киназ, и, таким образом, селективность соединений в соответствии с изобретением, можно определить с помощью следующего анализа:
mTOR (человека)
mTOR (человека) инкубируют с 50 мМ HEPES pH 7.5, 1 мМ EGTA, 0.01% Твин 20, 2 мг/мл субстрата, 3 мМ MnCl2 и [γ- 33Р-АТФ] (удельная радиоактивность приблизительно 500 число импульсов в минуту/пмоль, в требуемой концентрации). Реакцию инициируют путем добавления раствора MgATФ. После инкубирования при комнатной температуре в течение 40 минут, реакцию останавливают путем добавления 3% фосфорной кислоты. 10 мкл реакционного раствора затем по каплям переносят на Р30 Filtermat и три раза промывают в течение 5 мин в 75 мМ фосфорной кислоте и один раз в метаноле, сушат и оценивают с помощью подсчета импульсов в жидкой фазе.
PI3K р110α/р85α (человека), нерадиоактивный анализ
PI3K р110α/р85α (человека) инкубируют в аналитическом буфере, содержащем 10 мкМ 4,5-бисфосфата фосфатидилинозитола и MgATФ (в требуемой концентрации). Реакцию инициируют путем добавления раствора MgATФ. После инкубирования при комнатной температуре в течение 40 минут, реакцию останавливают путем добавления раствора, состоящего из EDTA и биотинилированного 3,4,5-трифосфата фосфатидилинозитола. В заключение добавляют детектирующий буфер, состоящий из меченого европием анти-GST моноклонального антитела, GST-меченого GRP1 РН домена и стрептавидин аллофикоцианина. Планшеты считывают посредством гомогенной флуоресценции с временным разрешением (HTRF) и соответствующие сигналы оценивают по формуле HTRF = 10000 × (Em 665 нм/Em 620 нм).
PI3K р110β/р85α (человека), нерадиоактивный анализ
PI3K р110β/р85α (человека) инкубируют в аналитическом буфере, содержащем 10 мкМ 4,5-бисфосфата фосфатидилинозитола и MgATФ (в требуемой концентрации). Реакцию инициируют путем добавления раствора MgATФ. После инкубирования при комнатной температуре в течение 30 мин, реакцию останавливают путем добавления раствора, состоящего из EDTA и биотинилированного 3,4,5-трифосфата фосфатидилинозитола. В заключение добавляют детектирующий буфер, состоящий из меченого европием анти-GST моноклонального антитела, GST-меченого GRP1 РН домена и стрептавидин аллофикоцианина. Планшеты считывают посредством гомогенной флуоресценции с временным разрешением (HTRF) и соответствующие сигналы оценивают по формуле HTRF = 10000 × (Em 665 нм/Em 620 нм).
PI3K р110δ/р85α (человека), нерадиоактивный анализ
PI3K p110δ/р85α (человека) инкубируют в аналитическом буфере, содержащем 10 мкМ 4,5-бисфосфата фосфатидилинозитола и MgATФ (в требуемой концентрации). Реакцию инициируют путем добавления раствора MgATФ. После инкубирования при комнатной температуре в течение 30 мин, реакцию останавливают путем добавления раствора, состоящего из EDTA и биотинилированного 3,4,5-трифосфата фосфатидилинозитола. В заключение добавляют детектирующий буфер, состоящий из меченого европием анти-GST моноклонального антитела, GST-меченого GRP1 РН домена и стрептавидин аллофикоцианина. Планшеты считывают посредством гомогенной флуоресценции с временным разрешением (HTRF) и соответствующие сигналы оценивают по формуле HTRF = 10000 × (Em 665 нм/Em 620 нм).
PI3K (р120γ) (человека), нерадиоактивный анализ
PI3K (р120γ) (человека) инкубируют в аналитическом буфере, содержащем 10 мкМ 4,5-бисфосфата фосфатидилинозитола и MgATФ (в требуемой концентрации). Реакцию инициируют путем добавления раствора MgATФ. После инкубирования при комнатной температуре в течение 30 мин, реакцию останавливают путем добавления раствора, состоящего из EDTA и биотинилированного 3,4,5-трифосфата фосфатидилинозитола. В заключение добавляют детектирующий буфер, состоящий из меченого европием анти-GST моноклонального антитела, GST-меченого GRP1 РН домена и стрептавидин аллофикоцианина. Планшеты считывают посредством гомогенной флуоресценции с временным разрешением (HTRF) и соответствующие сигналы оценивают по формуле HTRF = 10000 × (Em 665 нм/Em 620 нм).
MgATФ = магний 5'-O-[гидрокси({[(гидроксифосфинато)окси]фосфинато}окси)фосфорил]аденозин
MgCl2 = дихлорид магния
EGTA = этиленгликоль бис(аминоэтиловый простой эфир)-N,N,N',N'-тетрауксусная кислота
Твин 20 = полисорбат 20
Лекарственное средство/фармацевтическая композиция
Изобретение также относится к лекарственному препарату или лекарственному средству, содержащему по меньшей мере одно соединение в соответствии с изобретением и/или его физиологически приемлемые производные, сольваты, соли, таутомеры и/или стереоизомеры, включая их смеси во всех соотношениях.
Более того, изобретение относится к фармацевтической композиции, содержащей эффективное количество по меньшей мере одного соединения в соответствии с изобретением и/или одной из его физиологически приемлемых производных, солей, сольватов, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, необязательно вместе с по меньшей мере одним фармацевтически переносимым адъювантом, или необязательно наполнителем и/или адъювантом.
"Лекарственный препарат", "лекарственное средство" и "фармацевтическая композиция" или "фармацевтический состав" следует понимать в значении любой композиции, которая может применяться для профилактики, терапии, борьбы с развитием или последующего лечения пациентов, которые, по меньшей мере временно, демонстрируют патогенное изменение общего состояния или состояния отдельных частей организма, предпочтительно в результате злокачественного новообразования, опухолей и/или метастазов.
С целью усиления защитного или терапевтического действия соединений в соответствии с изобретением могут быть добавлены фармацевтически переносимые адъюванты. Для целей изобретения, любое вещество, которое содействует, усиливает или модифицирует действие соединений в соответствии с изобретением, является "адъювантом". Известными адъювантами являются, например, соединения алюминия, такие как, например, гидроксид алюминия или фосфат алюминия, сапонины, такие как, например, QS 21, мурамил-дипептид или мурамил-трипептид, белки, такие как, например, гамма-интерферон или TNF, MF 59, фосфатидилхолин, сквален или полиолы. Совместное применение яичного альбумина в полном адъюванте Фрейнда подобным образом может приводить к повышенному клеточно-опосредованному иммунитету и таким образом поддерживать действие сформированных нейтрализующих антител. Кроме того, ДНК, которая обладает иммуностимулирующим свойством, или которая кодирует белок с адъювантным действием, такой как, например, цитокин, может применяться параллельно или в конструкции.
Введение фармацевтической композиции в клетку или организм можно осуществить в соответствии с изобретением любым способом, который обеспечивает контактирование киназ с соединениями, присутствующими в композиции, в результате чего вызывается ответ. Фармацевтическая композиция настоящего изобретения может быть введена перорально, трансдермально, чресслизисто, трансуретрально, вагинально, ректально, пульмонально, энтерально и/или парентерально. Путь введения выбирают в зависимости от показаний, дозы подлежащей введению, индивидуально-специфических параметров, и т.д. В частности, различные пути введения облегчают сайт-специфическую терапию, которая сводит к минимуму побочные действия и снижает дозу активного соединения. Чрезвычайно предпочтительными инъекциями являются внутрикожные, подкожные, внутримышечные или внутривенные инъекции. Введение может осуществляться, например, с помощью так называемых прививочных пистолетов или с помощью шприцов. Кроме того, можно обеспечить вещество в виде аэрозоля, который вдыхают организмом, предпочтительно пациентом-человеком.
Лекарственные формы фармацевтических композиций получают с использованием обычных твердых или жидких наполнителей и/или разбавителей и обычно используемых вспомогательных средств, соответствующих желаемому пути введения в подходящей дозировке и способом, самим по себе известным. Таким образом, фармацевтически приемлемые наполнители, известные специалисту в данной области техники, могут в основном формировать часть фармацевтической композиции в соответствии с изобретением, где количество наполнителя - вещества, которое комбинируют с активным соединением с целью приготовления разовой дозы варьируется в зависимости от представителя, подвергающегося лечению, и пути введения. Такие фармацевтически переносимые добавки включают соли, буфера, филлеры, стабилизаторы, комплексообразующие вещества, антиоксиданты, растворители, связующие вещества, смазывающие вещества, покрытия для таблеток, вкусовые ароматизирующие вещества, красители, консерванты, регуляторы и т.п. Примерами наполнителей данного типа являются вода, растительные масла, бензиловые спирты, алкиленгликоли, полиэтиленгликоль, коллифор, триацетат глицерина, желатин, углеводы, такие как, например, лактоза или крахмал, гидроксипропилметилцеллюлоза (НРМС), стеарат магния, тальк и вазелин. Фармацевтический состав может находиться в виде таблетки, таблетки с пленочной оболочкой, драже, пастилки, капсулы, пилюли, порошка, гранул, сиропа, сока, капель, раствора, дисперсии, суспензии, суппозитория, эмульсии, имплантата, крема, геля, мази, пасты, лосьона, сыворотки, масла, спрея, аэрозоля, адгезива, пластыря или повязки. Приготовляемыми пероральными лекарственными формами предпочтительно являются таблетки, таблетки с пленочной оболочкой, драже, пастилки, капсулы, пилюли, порошки, гранулы, сиропы, соки, капли, растворы, дисперсии или суспензии - в том числе в форме депо. Более того, следует рассматривать парентеральные формы лекарственных средств, такие как, например, суппозитории, суспензии, эмульсии, имплантаты или растворы, предпочтительно масляные или водные растворы. Для местного применения активное соединение лекарственного средства вводят в состав обычным способом с по меньшей мере одним фармацевтически приемлемым носителем, таким как, например, микрокристаллическая целлюлоза, и необязательно дополнительными вспомогательными средствами, такими как, например, увлажняющие вещества, с получением твердых составов, которые можно наносить на кожу, таких как, например, кремы, гели, мази, пасты, порошки или эмульсии, или с получением жидких составов, которые можно наносить на кожу, таких как, например, растворы, суспензии, лосьоны, сыворотки, масла, спреи или аэрозоли. Фармацевтическая композиция предпочтительно находится в форме раствора для инъекции. Для получения раствора для инъекции можно использовать водную среду, такую как, например, дистиллированная вода или физиологические растворы, где последние включают дополнительные кислые и основные соли. Фармацевтическая композиция также может находиться в виде твердой композиции, например, в лиофилизированном состоянии, причем позже, перед применением, ее переводят в конечную форму путем добавления растворяющего агента, такого как, например, дистиллированная вода. Специалист в данной области техники знаком с основными принципами приготовления лиофилизатов.
Концентрация активного соединения в составе может составлять от 0.1 до 100 процентов по массе. Ключевым является то, что фармацевтическая композиция включает, в качестве активного соединения, эффективное количество соединения вместе с фармацевтически переносимыми вспомогательными средствами. Термины "эффективное количество" или "эффективная доза" используются здесь взаимозаменяемо и означают количество фармацевтического активного соединения, которое имеет профилактически или терапевтически подходящее действие на заболевание или патологическое изменение в клетке, ткани, органе или млекопитающем. "Профилактическое действие" предотвращает появление заболевания или даже заражение патогеном после проникновения отдельных представителей таким образом, что последующее их распространение значительно уменьшается или оно даже полностью деактивируется. "Профилактическое действие" также включает усиление нормальной физиологической функции. Профилактика является целесообразной, в частности, если у отдельного представителя есть предрасположенность к возникновению вышеупомянутых заболеваний, такая как, например, семейный анамнез, генный дефект или недавно перенесенное заболевание. "Терапевтически подходящее действие" освобождает частично или полностью от одного, более чем одного или всех симптомов заболевания или приводит к частичной или полной реверсии одного, более чем одного или всех физиологических или биохимических параметров, которые связаны с или причинно участвуют в заболевании или патологическом изменении, в нормальное состояние. Борьба с развитием также считается типом терапевтического лечения, если соединения вводят в определенные промежутки времени, например, для того, чтобы полностью устранить симптомы заболевания. Соответствующая доза или диапазон доз для введения соединений в соответствии с изобретением является достаточно большой(-им) для достижения желаемого профилактического или терапевтического эффекта - индукции биологического или медицинского ответа. В общем, доза варьируется в зависимости от возраста, конституции и пола пациента, но также принимается во внимание и тяжесть заболевания. Само собой разумеется, что конкретная доза, частота и длительность введения, кроме того, зависят от ряда факторов, таких как, например, нацеливающая и связывающая способность соединений, особенности питания отдельного представителя, подвергающегося лечению, путь введения, скорость экскреции и комбинация с другими лекарственными препаратами. Индивидуальная доза может быть установлена как в отношении первичного заболевания, так и в связи с возникновением любых осложнений. Точная доза может быть установлена специалистом в данной области техники с помощью известных средств и методов. Эта идея изобретения действенна и может применяться без ограничения к фармацевтической композиции, содержащей соединения в соответствии с изобретением, при условии, что это представляется подходящим.
В одном варианте осуществления изобретения, соединения вводят в дозе от 0.01 мг до 1 г на единицу дозирования, предпочтительно от 1 до 700 мг, особенно предпочтительно от 5 до 100 мг. Суточная доза находится, в частности, в диапазоне между 0.02 и 100 мг/кг массы тела.
Благодаря их неожиданно сильному и/или селективному ингибированию киназ, в частности, ингибированию киназы ATM, которая регулирует клеточные процессы посредством репарации двухцепочечной ДНК, соединения изобретения можно с успехом вводить в низкой дозе, обеспечивая при этом схожее или даже лучшее биологическое действие по сравнению с менее сильными или менее селективными ингибиторами. Сниженную дозу типично связывают с ослаблением медицинскими побочными действиями. Кроме того, высокоселективное ингибирование обычно также находит отражение в снижении нежелательных побочных действий.
Все указанные и дополнительные составляющие или компоненты лекарственного средства или фармацевтического состава хорошо знакомы специалисту в данной области и могут быть специально подобраны в соответствии с идеей настоящего изобретения в обычных экспериментах.
Комбинированная терапия
Лекарственные средства и фармацевтические композиции, которые содержат соединения в соответствии с изобретением, и применение данных соединений для лечения опосредуемых киназой нарушений представляют(-ет) многообещающий подход для широкого спектра методов лечения, дающий возможность достичь непосредственного и немедленного облегчения симптомов у людей и животных. Это особенно выгодно для эффективной борьбы с тяжелыми заболеваниями, такими как злокачественное новообразование, либо в виде монотерапии, как указано выше, либо в комбинации с другими методами лечения, такими как, например, химио- или радиотерапия. Ключевое участие ATM в процессах репарации ДНК и доказательства того, что дефицит киназы ATM позволяет клеткам млекопитающих становиться более чувствительными к облучению, позволяет терапевтическое применение АТМ-специфических ингибиторов в качестве части лечения, например, солидных раковых опухолей посредством лучевой терапии и/или химиотерапии, предпочтительно направленных на повреждение двухцепочечной ДНК.
Соответственно, с целью поддержки лечебного действия, фармацевтическая композиция может в одном варианте осуществления изобретения также содержать одно или несколько дополнительных активных соединений, например, противоопухолевое средство, причем является возможным одновременное или последовательное введение. Терапевтическое действие фармацевтической композиции в соответствии с изобретением может выражаться, например, в определенных противоопухолевых средствах, которые обладают лучшим действием посредством ингибирования киназ или характеризуются меньшим числом побочных действий, достигаемым снижением дозы. Соответственно, соединения в соответствии с изобретением можно вводить в комбинации с другими активными соединениями, включая противоопухолевые средства.
В предпочтительном варианте осуществления изобретения, фармацевтическую композицию в соответствии с изобретением комбинируют с противоопухолевым средством, или она содержит его. Соответственно, настоящее изобретение также относится к соединению в соответствии с изобретением и/или его фармацевтически пригодному производному, соли, сольвату, таутомеру или стереоизомеру для применения для лечения злокачественного новообразования, опухолей и/или метастазов в комбинации с по меньшей мере одним противоопухолевым средством.
Как используется здесь, термин "противоопухолевое средство" относится к любому средству, которое вводят пациенту со злокачественным новообразованием, опухолями и/или метастазами с целью лечения злокачественного новообразования.
Противоопухолевое средство особенно предпочтительно выбирают из группы, включающей цитокины, хемокины, проапоптозные средства, интерфероны, радиоактивные соединения, модуляторы эстрогеновых рецепторов, модуляторы андрогенных рецепторов, модуляторы ретиноидных рецепторов, цитотоксические агенты, цитостатические средства, ингибиторы пренил-протеин трансферазы и ингибиторы ангиогенеза или их комбинации. Предпочтительно, противоопухолевое средство модифицирует, в частности, снижает, метаболизм нуклеиновых кислот и/или белков, клеточное деление, репликацию ДНК, биосинтез пуринов, пиримидинов и/или аминокислот, экспрессию генов, процессинг мРНК, синтез белков, апоптоз, или приводит к комбинации таких эффектов.
Противоопухолевыми средствами, которые являются предпочтительными в соответствии с изобретением, являются те, которые повреждают ДНК опухолевых клеток и таким образом, участвуют в репликации ДНК, транскрипции ДНК или экспрессии генов. В частности, для этой цели являются подходящими следующие средства:
- алкилирующие средства, такие как алтретамин, бендамустин, бусульфан, кармустин, хлорамбуцил, хлорметин, циклофосфамид, дакарбазин, ифосфамид, импросульфан тозилат, ломустин, мелфалан, митобронитол, митолактол, нимустин, ранимустин, темозоломид, тиотепа, треосульфан, мехлорэтамин, карбоквон, апазиквон, фотемустин, глюфосфамид, палифосфамид, пипоброман, трофосфамид, урамустин,
- соединения платины, такие как карбоплатин, цисплатин, эптаплатин, мириплатин гидрат, оксалиплатин, лобаплатин, недаплатин, пикоплатин, сатраплатин;
- ингибиторы DDR (ответа на повреждение ДНК), такие как ингибиторы топоизомеразы, например, этопозид, иринотекан, разоксан, собузоксан, топотекан, камптотецин, доксорубицин, амсакрин; ингибиторы поли-(АДФ-рибоза)-полимеразы (PARP), например, талазопариб, олапариб, велипариб, рукапариб, СЕР 9722, MK4827, BGB-290; ингибиторы ATR (атаксия-телеангиэктазия и Rad3-родственный белок), например, VE-822, AZ20, AZD6738;
- ДНК-модифицирующие средства, такие как амрубицин, бисантрен, децитабин, митоксантрон, прокарбазин, трабектедин, клофарабин, амсакрин, бросталлицин, пиксантрон, ларомустин;
- противораковые антибиотики, такие как блеомицин, дактиномицин, доксорубицин, эпирубицин, идарубицин, левамизол, милтефозин, митомицин С, ромидепсин, стрептозоцин, валрубицин, циностатин, зорубицин, даунорубицин, пликамицин, акларубицин, пепломицин, пирарубицин;
- излучающие альфа-частицы вещества, такие как альфарадин (дихлорид 223Ra, хофиго), 211At, 225Bi, 225Ac, 227Th;
Особое предпочтение отдают блеомицину, альфарадину и ингибиторам DDR, например, этопозиду, иринотекану, разоксану, собузоксану, топотекану, камптотецину, доксорубицину, амсакрину, талазопарибу, олапарибу, велипарибу, рукапарибу, СЕР 9722, MK4827, BGB-290; VE-822, AZ20, AZD6738.
Изобретение также может быть осуществлено в виде набора, который содержит соединения в соответствии с изобретением. Набор состоит из отдельных упаковок (а) эффективного количества соединения в соответствии с изобретением и/или его физиологически приемлемого производного, соли, таутомера и/или стереоизомера, включая их смеси во всех соотношениях, и (б) эффективного количества дополнительного активного соединения. Дополнительное активное соединение предпочтительно представляет собой противоопухолевое средство.
Набор включает пригодные контейнеры, такие как, например, коробочки или картонные коробки, отдельные бутылки, пакеты или ампулы. Набор может включать, например, отдельные ампулы, каждая из которых содержит эффективное количество соединения в соответствии с изобретением и/или его фармацевтически пригодных производных, сольватов, солей, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, или эффективное количество дополнительного активного соединения лекарственного средства в растворенной или лиофилизированной форме. Набор изобретения также может включать вкладыш, который содержит письменные инструкции или указывает потребителю на письменные инструкции, которые разъясняют обращение с соединениями изобретения.
Дополнительный вариант осуществления настоящего изобретения относится к соединениям в соответствии с изобретением в комбинации с радиотерапией и/или по меньшей мере одним дополнительным активным соединением, предпочтительно в комбинации с радиотерапией и/или противоопухолевым средством. Другими словами, дополнительный вариант осуществления настоящего изобретения относится к соединениям в соответствии с изобретением для применения для лечения злокачественного новообразования, опухолей и/или метастазов в комбинации с радиотерапией. Более того, настоящее изобретение относится к соединению в соответствии с изобретением или его фармацевтически пригодному производному, соли, сольвату, таутомеру и/или стереоизомеру для применения для сенсибилизации раковых клеток к противоопухолевому средству и/или ионизирующему излучению.
Технические методы облучения, которые применяют в клинической практике, предпочтительно включают фотонное облучение (классическое, электромагнитное рентгеновское/гамма облучение), протонное облучение, облучение тяжелыми ионами (ионизированный углерод) и нейтронное облучение, без ограничения перечисленными. Данные типы радиотерапии и другие подходящие типы лучевой терапии в смысле изобретения известны специалисту в данной области техники, как, например, из работы Herrmann и др. (2006) Klinische Strahlenbiologie [Clinical Radiation Biology], Elsevier Munich, 4-e изд., 67-68; Bhide & Nutting (2010) BMC Medicine 8: 25; Choi & Hung (2010) Current Urology Reports 11(3): 172. В качестве наиболее частого применения, фотонное облучение было усовершенствовано технически посредством метода IMRT (модулированная по интенсивности радиотерапия) и методов визуализации (трехмерная конформная радиотерапия) для планирования облучения и выполнения наиболее точной фокусировки. Соединения в соответствии с изобретением приводят к синергетическим эффектам в существующих методах лечения и облучения и/или восстанавливают действие существующих методов лечения и облучения. Еще один дополнительный вариант осуществления изобретения относится к применению по меньшей мере одного соединения и/или его физиологически пригодных производных, солей, сольватов, таутомеров и/или стереоизомеров, включая их смеси во всех соотношениях, для сенсибилизации раковых клеток к противоопухолевому средству и/или ионизирующему излучению (радиотерапии), при условии, что сенсибилизация не имеет места in vivo в организме человека или животного.
Сенсибилизацию предпочтительно проводят ex vivo или in vitro путем введения соединений в клетки, культуры клеток, ткани или органы, которые содержат серин/треонин-протеинкиназы. Применение ex vivo осуществляют, в частности, в случае клеток животного, которые происходят из организма животного, который поражен заболеванием, которое выбрано из группы злокачественного новообразования, опухолей, метастазов и/или нарушений ангиогенеза. Клетки, обработанные ex vivo, можно либо продолжать сохранять в культуре для последующих исследований, либо переносить в животное, которое может быть животным - "хозяином" или другим животным. Сенсибилизация ех vivo в соответствии с изобретением является особенно полезной для тестирования специфического действия соединений, так что in vivo доза может быть установлена предварительно соответствующим образом путем оценки таких ex vivo данных. В результате этого терапевтический эффект существенно возрастает. Альтернативно, изобретение также предназначено для in vivo применения и относится к по меньшей мере одному соединению в соответствии с изобретением и/или его физиологически приемлемым солям, таутомерам и/или стереоизомерам, включая их смеси во всех соотношениях, для применения для сенсибилизации раковых клеток к противоопухолевому средству и/или ионизирующему излучению.
В заключение следует отметить, что соединения в соответствии с изобретением можно применять отдельно и/или в комбинации с другими мерами лечения, такими как, например, хирургические вмешательства, иммунотерапия, радиотерапия и/или химиотерапия. Последняя относится к направленной терапии любым желаемым NME (т.е. NCE и/или NBE) в качестве монотерапии и/или направленной/ненаправленной комбинированной терапии.
Все документы, приведенные в описании, таким образом предназначены для включения в полном объеме в раскрытие настоящего изобретения в качестве ссылки.
Само собой разумеется, что данное изобретение не ограничивается конкретными соединениями, фармацевтическими композициями, применениями и способами, описанными в данной заявке, так как такие обстоятельства могут варьироваться. Более того, само собой разумеется, что терминология, используемая в данной заявке, служит исключительно цели описания отдельных вариантов и не предназначена для ограничения объема изобретения. Как используется здесь в описании, в том числе формуле изобретения, словоформы в единственном числе, включают эквивалент и во множественном числе, при условии, что в контексте конкретно не указывают на иное. Например, ссылка на "соединение" включает одно соединение или несколько соединений, которые в свою очередь могут быть одинаковыми или разными, или ссылка на "способ" включает эквивалентные стадии и способы, которые известны специалисту в данной области техники.
ДОПОЛНИТЕЛЬНЫЕ СОЕДИНЕНИЯ
Помимо упомянутых выше соединений формулы (I) изобретение охватывает соединения следующей общей формулы (X):
в которой
R1 означает А или -(CY2)n-Ar,
R2 означает Y, -(CY2)p-(C[YR4])s-R5 или -Alk-R5,
R3 означает Y, -(CY2)p-COOY или -(CY2)p-CO-NYY,
R4 означает Y, Hal, -(CY2)n-NYY, -(CY2)n-NY-COO-(CY2)n-SiA3, -(CY2)n-COOY, -CO-NYY, -CO-NY-(CY2)n-OY, -CO-NY-(CY2)n-NYY или -SO2A,
R5 означает -(CY2)p-Ar или -(CY2)p-Het1,
X означает CH2, O, S или одинарную связь,
Y означает H или А,
А означает неразветвленный или разветвленный алкил, содержащий 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов С, где 1, 2, 3, 4, 5, 6 или 7 атомов Н могут быть заменены, независимо друг от друга, на Hal,
Alk означает алкенилен, содержащий 2, 3, 4, 5 или 6 атомов С, где 1, 2, 3 или 4 атома Н могут быть заменены, независимо друг от друга, на Hal и/или OY,
СуА означает циклоалкил, содержащий 3, 4, 5, 6, 7 или 8 кольцевых атомов С, который незамещен или моно- или полизамещен, независимо друг от друга, посредством Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY и/или -(CY2)p-NY-COY,
Ar означает фенил, который незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal, A, CN, -NO2, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY и/или -(CY2)p-NY-COY,
Het1 означает моно- или бициклический гетероарил, содержащий 2, 3, 4, 5, 6, 7, 8 или 9 атомов С и 1, 2, 3 или 4 атома N, О и/или S, который может быть незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal, A, CN, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY и/или -SO2-Het2,
Het2 означает моноциклический насыщенный гетероцикл, содержащий 2, 3, 4, 5, 6 или 7 атомов С и 1, 2, 3 или 4 атома N, О и/или S, который может быть незамещен или монозамещен посредством А,
НЕТ означает 5- или 6-членный ароматический гетероцикл, содержащий 1, 2 или 3 атома N и необязательно атом О или атом S, где данный гетероцикл присоединен к атому N скелета через кольцевой атом С и где данный гетероцикл может быть незамещен или замещен одним, двумя или тремя заместителями, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, А, Het2, -CN, -(CY2)p-OY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY или -SO2-Het2; и может быть частью бициклического 11- или 12-членного ароматического гетероцикла, где данный бициклический ароматический гетероцикл может быть во всех своих частях незамещен или замещен одним, двумя, тремя или большим числом заместителей, которые выбирают, независимо друг от друга, из группы, состоящей из: Hal, A, Het2, CN, -(CY2)p-OY, -(CY2)p-O-(CY2)t-OY, -(CY2)p-O-(CY2)t-POAA, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY, -(CY2)p-NY-COY или -SO2-Het2,
Hal означает F, Cl, Br или I,
m означает 0, 1, 2, 3 или 4,
n, p, s, независимо друг от друга, означают 0, 1,2, 3, 4, 5 или 6 и
t означает 1, 2, 3, 4, 5 или 6,
и/или их фармацевтически пригодные соли, сольваты, таутомеры и стереоизомеры, включая их смеси во всех соотношениях,
где, в дополнение к или в отличие от формулы (I), не возможен вариант, в котором одновременно
R1 и R3 означает А, и X означает одинарную связь, R2 означает -(CY2)p-(C[YR4])s-R5, где p и s = 0 и R5 означает -(CY2)p-Het1, где p = 0.
Термин "Alk" в данной заявке означает неразветвленный или разветвленный алкенилен, содержащий 2, 3, 4, 5 или 6 атомов С, т.е. С2-6-алкенилы, где, независимо друг от друга, 1, 2, 3 или 4 атома Н могут быть заменены на Hal и/или OY. Алкенилы содержат по меньшей мере одну С-С двойную связь, однако, в частности, могут также содержать два двойные связи (диены). Примерами подходящих алкениленов являются двухвалентные алкеновые радикалы на основе винила, аллила, пропенила (-СН2СН=СН2; -СН=СН-СН3; -С(=СН2)-СН3), 1-, 2- или 3-бутенила, изобутенила, 2-метил-1- или 2-бутенила, 3-метил-1-бутенила, 1,3-бутадиенила, 2-метил-1,3-бутадиенила, 2,3-диметил-1,3-бутадиенила, 1-, 2-, 3- или 4-пентенила и гексенила, т.е. -СН=СН-, -СН2-СН=СН-, -СН=СН-СН2-, -С(=СН2)-СН2-, -С(СН3)=СН-,.-СН=С(СН3)-, -СН=СН-СН2-СН2-, -СН2-СН=СН-СН2-, -СН2-СН2-СН=СН-, -СН=С(СН3)-СН2-, -СН2-С(СН3)=СН-, -СН=СН-СН(СН3)-, -С(СН3)=СН-СН2-, -CH=CH-CH=CH-, -СН=С(СН3)-СН=СН-, -СН=С(СН3)-С(СН3)=СН-, -CH=CH-CH2-CH2- CH2-, -CH2-CH=CH-CH2-CH2-, -CH2-CH2-CH=CH-CH2-, -CH2-CH2-CH2-CH=CH-, -CH=CH-CH2-CH2-CH2-CH2-, -CH2-CH=CH-CH2-CH2-CH2-, -CH2-CH2-CH=CH-CH2-CH2-, -СН2-СН2-СН2-СН=СН-СН2-, -СН2-СН2-СН2-СН2-СН=СН-. "Alk" особенно предпочтительно означает алкенилен, содержащий 2 или 3 атома С, где 1 или 2 атома Н могут быть заменены на Hal и/или ОН. Чрезвычайно предпочтительными его примерами являются этенилен (-СН=СН-) и пропенилен (пропендиил, -СН=СН-СН2-). Само собой разумеется, что соответствующие значения "Alk" в радикалах формулы в соответствии с изобретением являются независимыми друг от друга.
"Ar" в данном документе означает фенил, который незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal, A, CN, NO2, -(CY2)p-OY, -(CY2)p-NYY, -(CY2)p-COOY, -(CY2)p-CO-NYY или -(CY2)p-NY-COY. "Ar" особенно предпочтительно означает фенил, который незамещен или моно-или дизамещен посредством Hal. Само собой разумеется, что соответствующие значения "Ar" в радикалах формулы в соответствии с изобретением являются независимыми друг от друга. Примерами подходящих "Ar" являются, в частности, (незамещенный), фенил, о-, м- или n-толил, о-, м- или n-этилфенил, о-, м- или n-пропилфенил, о-, м- или n-изопропилфенил, о-, м- или n-трет-бутилфенил, о-, м- или n-трифторметилфенил, о-, м- или n-фторфенил, о-, м- или n-бромфенил, о-, м- или n-хлорфенил, о-, м- или n-гидроксифенил, о-, м- или n-метоксифенил, о-, м- или n-нитрофенил, о-, м- или n-аминофенил, о-, м- или n-метиламинофенил, о-, м- или n-диметиламинофенил, о-, м- или n-аминокарбонилфенил, о-, м- или n-карбоксифенил, о-, м- или n-метоксикарбонилфенил, о-, м- или n-этоксикарбонилфенил, о-, м- или n-ацетилфенил, о-, м- или n-формилфенил, о-, м- или n-цианофенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дифторфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дихлорфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дибромфенил, 2,3,4-, 2,3,5-, 2,3,6-, 2,4,6- или 3,4,5-трихлорфенил, n-йодфенил, 4-фтор-3-хлорфенил, 2-фтор-4-бромфенил, 2,5-дифтор-4-бромфенил или 2,5-диметил-4-хлорфенил.
Определения и предпочтительные значения или варианты осуществления, упомянутые в связи с соединениями формулы (I), применяются в отношении других переменных, радикалов и заместителей.
В соединениях формулы (X), R1 может означать А, предпочтительно незамещенный или замещенный C1-С3-алкил, особенно предпочтительно метил. Соответственно, настоящее изобретение обеспечивает соединения следующих формул:

Кроме того, предпочтительно R3 означает Y, т.е. Н или А, или Hal. R3 особенно предпочтительно означает А, в частности, неразветвленный или разветвленный алкил, содержащий 1, 2, или 3 атома С, где 1, 2, 3, 4 или 5 атомов Н могут быть заменены, независимо друг от друга, на Hal. R3 особенно предпочтительно означает незамещенный C1-3 алкил и особенно предпочтительно метил.
Соответственно, настоящее изобретение обеспечивает соединения следующих формул:


ПРИМЕРЫ
Изобретение разъясняется ниже более подробно со ссылкой на неограничивающие примеры отдельных вариантов осуществления. Примеры (в частности, соединения - примеры) следует, в частности, интерпретировать таким образом, чтобы они не ограничивались специально проиллюстрированными комбинациями признаков, однако, вместо этого, иллюстративные признаки в свою очередь можно свободно комбинировать при условии, что достигается цель изобретения.
Аналитические методы
ЯМР (1Н) проводили со следующими параметрами.
Приборы: Bruker Avance DRX 500, Bruker Avance 400, Bruker DPX 300
Стандартные условия (различные в отдельных случаях)
Эталон: ТМС
TD (временной интервал = число точек данных или цифровое разрешение): 65536
Растворитель: ДМСО-d6
NS (= число сканирований): 32
SF (частота спектрометра): см. выше
ТЕ (температура): 297 K
Постоянные взаимодействия (J) указаны в герцах (Гц)
ВЭЖХ-МС проводили со следующими параметрами.
Приборы:
- Shimadzu LCMS-2020
- Shimadzu SP-M20A 2010EV
- Shimadzu UFLC-MS 2010EV
Используемые колонки:
- Shim-pack VP-ODS
- Shim-pack XR-ODS
- Kinetex XB-C18 100A
- Xbridge ВЕН C18
- Gemini-NX 3u C18 110A
- ACE UltraCore 2.5 SuperC18
Методы: градиенты растворителей:
- А: вода + 0.1% муравьиной кислоты, В: ацетонитрил + 0.1% муравьиной кислоты
- А: вода + 0.05% трифторуксусной кислоты, В: ацетонитрил + 0.05% трифторуксусной кислоты
- А: вода + 5 мМ карбонат аммония, В: ацетонитрил
Длина волны детектирования: 220 нм
Тип МС: API-ES
Описание синтезов
ПРИМЕР 1: Синтез 1-(3-фтор-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (Соединение - Пример 14)
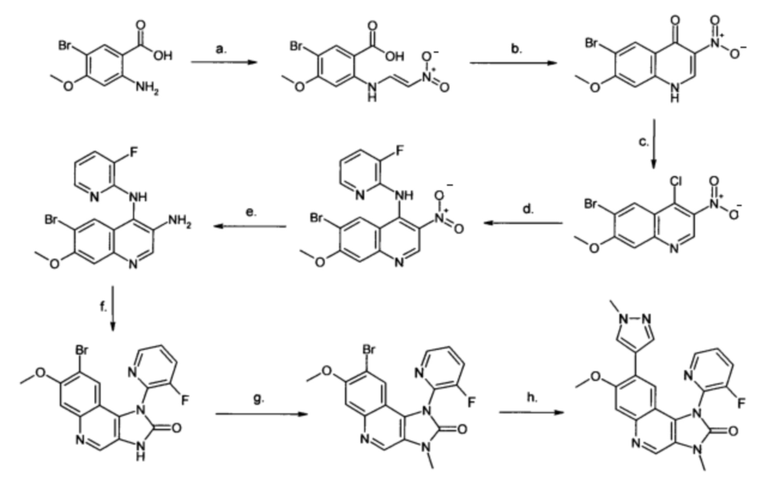
Схема 1: Синтез Соединения - Примера 14
а. Синтез 5-бром-4-метокси-2-[[(Е)-2-нитровинил]амино]бензойной кислоты
Нитрометан (0.63 мл, 11.7 ммоль) по каплям добавляли при комнатной температуре при перемешивании к раствору гидроксида натрия (14.7 г, 368 ммоль) в воде (33 мл). Смесь вслед за этим медленно нагревали при 45°С в течение 5 минут при перемешивании. Реакционный раствор затем охлаждали до комнатной температуры, и снова по каплям добавляли нитрометан (0.63 мл, 11.7 ммоль). Реакционную смесь вслед за этим перемешивали еще 10 минут, в течение чего образовался прозрачный, красноватый раствор. После непродолжительного нагревания (5 минут) при 50°С, смесь охлаждали до комнатной температуры и декантировали на лед (11 г). Водный раствор осторожно подкисляли до pH < 2, используя конц. соляную кислоту, и вслед за этим незамедлительно добавляли при перемешивании к раствору 2-амино-5-бром-4-метоксибензойной кислоты (8.00 г, 32.5 ммоль) в воде (259 мл), подкисленной с использованием конц. соляной кислоты (126 мл, 2.75 моль).
Полученную суспензию перемешивали в течение ночи и вслед за этим фильтровали. Остаток сушили при 50°С с получением 9.60 г (93%) 5-бром-4-метокси-2-[[(Е)-2-нитровинил]амино]бензойной кислоты в виде бесцветного твердого вещества.
b. Синтез 6-бром-7-метокси-3-нитро-1Н-хинолин-4-она
5-Бром-4-метокси-2-((Е)-2-нитровиниламино)бензойную кислоту (4.0 г, 12.6 ммоль) растворяли в N,N-диметилформамиде (150 мл). Вслед за этим при комнатной температуре при перемешивании добавляли 1,1'-карбонилдиимидазол (3.07 г, 18.9 ммоль). Реакционный раствор перемешивали в течение ночи при комнатной температуре. Вслед за этим добавляли ацетонитрил (120 мл). Полученную суспензию охлаждали и затем фильтровали. Желтый остаток промывали диэтиловым эфиром и сушили в течение ночи при 40°С с получением 3.0 г (80%) 6-бром-7-метокси-3-нитро-1Н-хинолин-4-она в виде бесцветного твердого вещества.
c. Синтез 6-бром-4-хлор-7-метокси-3-нитрохинолина
6-Бром-7-метокси-3-нитро-1Н-хинолин-4-он (2.50 г, 8.36 ммоль) сначала помещали в атмосферу сухого азота. Вслед за этим добавляли фосфорилхлорид (20 мл, 215 ммоль) и N,N-диметилформамид (0.13 мл, 1.68 ммоль). Реакционный раствор нагревали при 115°С в течение 12 часов при перемешивании. Смесь вслед за этим упаривали в вакууме, и полученный остаток очищали с помощью хроматографии на силикагеле (петролейный эфир/этил ацетат=87:13, объемные доли), с получением 2.40 г (90%) 6-бром-4-хлор-7-метокси-3-нитрохинолина в виде бесцветного твердого вещества.
d. Синтез 6-6ром-N-(3-фтор-2-пиридил)-7-метокси-3-нитрохинолин-4-амина
3-Фторпиридин-2-амин (390 мг, 3.48 ммоль), растворенный в N,N-диметилформамиде (10 мл), сначала помещали в атмосферу сухого азота. Вслед за этим к раствору добавляли гидрид натрия (630 мг, 26.3 ммоль), и смесь перемешивали при комнатной температуре в течение еще 5 минут. Затем к реакционной смеси добавляли 6-бром-4-хлор-7-метокси-3-нитрохинолин (1.00 г, 3.15 ммоль), смесь перемешивали при комнатной температуре в течение 30 минут, и реакцию вслед за этим завершали путем добавления ледяной воды (100 мл). Водный раствор три раза экстрагировали этилацетатом, каждый раз порцией 100 мл. Объединенные органические фазы сушили над безводным сульфатом натрия, фильтровали и упаривали досуха в вакууме с получением 1.0 г (81%) 6-бром-N-(3-фтор-2-пиридил)-7-метокси-3-нитрохинолин-4-амина в виде желтого твердого вещества.
e. Синтез 6-бром-N-4-(3-фтор-2-пиридил)-7-метоксихинолин-3,4-диамина
6-Бром-N-(3-фтор-2-пиридил)-7-метокси-3-нитрохинолин-4-амин (1.0 г, 2.54 ммоль), растворенный в метаноле (50 мл), сначала помещали в атмосферу защитного газа - азота. Вслед за этим к раствору добавляли Ni Ренея (100 мг, 1.17 ммоль), и реакционную смесь перемешивали в атмосфере водорода при атмосферном давлении в течение 30 минут. После аэрации азотом суспензию фильтровали, и фильтрат упаривали досуха в вакууме с получением 0.8 г (87%) 6-бром-N-4-(3-фтор-2-пиридил)-7-метоксихинолин-3,4-диамина в виде желтого твердого вещества.
f. Синтез 8-бром-1-(3-фтор-2-пиридил)-7-метокси-3Н-имидазо[4,5-с]хинолин-2-она
Сначала вносили 6-бром-N-4-(3-фтор-2-пиридил)-7-метоксихинолин-3,4-диамин (0.8 г, 2.20 ммоль), растворенный в тетрагидрофуране. Вслед за этим добавляли 1,1'-карбонилдиимидазол (1.78 г, 11.0 ммоль) и основание Хюнига (1.42 г, 11.0 ммоль). Реакционный раствор нагревали при 40°С при перемешивании в течение 2 часов. Затем реакцию завершали путем добавления ледяной воды (200 мл). Водную фазу три раза экстрагировали этилацетатом, каждый раз порцией 50 мл. Объединенные органические фазы сушили над безводным сульфатом натрия, фильтровали и упаривали досуха в вакууме с получением 0.8 г (93%) 8-бром-1-(3-фтор-2-пиридил)-7-метокси-3Н-имидазо[4,5-с]хинолин-2-она в виде бледно-желтого твердого вещества.
g. Синтез 8-бром-1-(3-фтор-2-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-она
8-Бром-1-(3-фтор-2-пиридил)-7-метокси-3Н-имидазо[4,5-с]хинолин-2-он (0.8 г, 2.06 ммоль), растворенный в N,N-диметилформамиде (10 мл), сначала помещали в защитную атмосферу сухого азота. Вслед за этим добавляли гидрид натрия (412 мг, 17.2 ммоль) и метилйодид (1.46 г, 10.3 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение одного часа. Реакцию вслед за этим завершали путем добавления ледяной воды (100 мл). Полученный осадок отфильтровывали и сушили в вакууме с получением 0.6 г (72%) 8-бром-1-(3-фтор-2-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-она в виде бледно-желтого твердого вещества.
h. Синтез 1-(3-фтор-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (Соединение - Пример 14)
8-Бром-1-(3-фтор-2-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-он (150 мг, 0.37 ммоль), 1-метил-4-(тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол (93 мг, 0.45 ммоль), Pd(PPh3)4 (43 мг, 0.04 ммоль) и карбонат калия (103 мг, 0.75 ммоль) в 1,4-диоксане (10 мл) и воде (3 мл) в атмосфере инертного газа - аргона сначала вносили в герметичный аппарат. Реакционную смесь нагревали при 80°С в течение 2 часов при перемешивании. Смесь вслед за этим охлаждали до комнатной температуры, и реакционную смесь упаривали досуха в вакууме. Остаток предварительно очищали с помощью хроматографии на силикагеле (этилацетат/метанол = 10:1, объемные доли). Элюат упаривали досуха, и полученный сырой продукт подвергали окончательной очистке с помощью препаративной ОФ-ВЭЖХ (вода/ацетонитрил). Упаривание содержащих продукт фракций приводило к получению 1-(3-фтор-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (60 мг, 40%, Соединение -Пример 14) в виде бесцветного твердого вещества.
ПРИМЕР 2: Синтез 7-метокси-3-метил-8-(1-метилпиразол-4-ил)-1-тиазол-2-илимидазо[4,5-с]хинолин-2-она (Соединение - Пример 47)
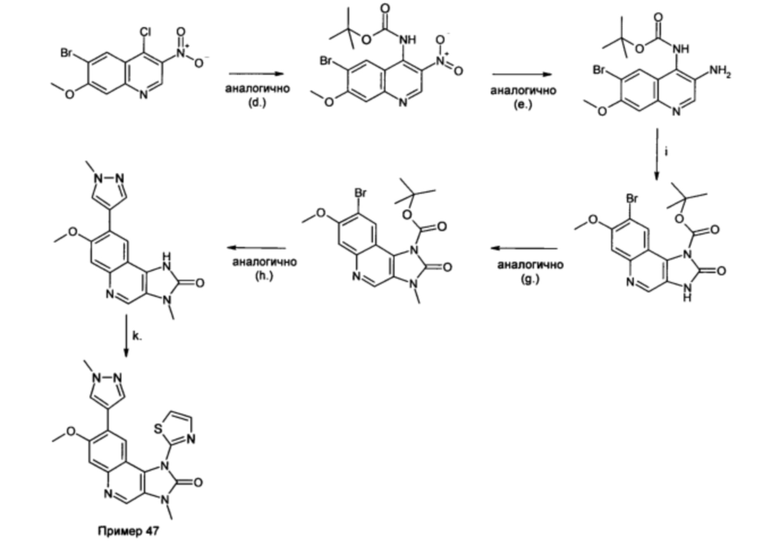
Схема 2: Синтез Соединения - Примера 47
i. Синтез трет-бутил 8-бром-7-метокси-2-оксо-3Н-имидазо[4,5-с]хинолин-1-карбоксилата
трет-Бутил N-(3-амино-6-бром-7-метоксихинолин-4-ил)карбамат (50.0 мг, 0.14 ммоль), дитрихлорметилкарбонат (119 мг, 0.40 ммоль) и триэтиламин (0.18 мл, 1.29 ммоль) растворяли в дихлорметане (3 мл) и перемешивали при 25°С в течение 2 часов. Смесь упаривали досуха в вакууме, и остаток очищали с помощью хроматографии на силикагеле (этилацетат:метанол = 10:1, объемные доли), с получением 50.0 мг (93%) трет-бутил 8-бром-7-метокси-2-оксо-3Н-имидазо[4,5-с]хинолин-1-карбоксилата в виде бесцветного твердого вещества.
k. Синтез 7-метокси-3-метил-8-(1-метилпиразол-4-ил)-1-тиазол-2-илимидазо[4,5-с]хинолин-2-она
7-Метокси-3-метил-8-(1-метилпиразол-4-ил)-1Н-имидазо[4,5-с]хинолин-2-он (20 мг, 0.06 ммоль), 2-бром-1,3-тиазол (20 мг, 0.12 ммоль), CuI (20.00 мг, 0.11 ммоль), K3PO4 (50 мг, 0.24 ммоль) вносили в толуол (4 мл) в атмосфере аргона в герметичном реакционном сосуде. Вслед за этим добавляли (1S,2S)-1-N,2-N-диметилциклогексан-1,2-диамин (30 мг, 0.21 ммоль) при комнатной температуре. Смесь нагревали при 100°С в течение 18 часов при перемешивании. Охлажденный раствор упаривали досуха в вакууме, и остаток очищали с помощью хроматографии на силикагеле (вода/0.05% NH4HCO3 : ацетонитрил = 10:1), с получением 10 мг (43%) 7-метокси-3-метил-8-(1-метилпиразол-4-ил)-1-тиазол-2-илимидазо[4,5-с]хинолин-2-она в виде бесцветного твердого вещества.
ПРИМЕР 3: Синтез 1-[5-(азетидин-3-илметокси)-3-фторпиридин-2-ил]-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она

i. 1-(5-Бензилокси-3-фтор-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (1.1 г, 2.15 ммоль), МеОН (200 мл) и Pd/C (229 мг, 2.15 ммоль) сначала вносили в 500 мл круглодонную колбу, колбу продували Н2 и атмосферу Н2 сохраняли. Раствор перемешивали при комнатной температуре в течение 8 часов. Твердое вещество отфильтровывали, и смесь упаривали в вакууме с получением 740 мг (80%) 1-(3-фтор-5-гидрокси-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ii. 1-(3-Фтор-5-гидрокси-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (100 мг, 0.23 ммоль, 98%), 3-(бромметил)азетидин 1-трет-бутилкарбамат (80 мг, 0.32 ммоль), карбонат калия (66.2 мг, 0.48 ммоль) и N,N-диметилформамид (10 мл) сначала вносили в 30 мл реакционный сосуд. Раствор перемешивали при 50°С в течение ночи. Затем реакцию завершали путем добавления 10 мл воды. Раствор затем три раза экстрагировали этилацетатом, каждый раз порцией 10 мл, объединенные органические фазы сушили над безводным сульфатом натрия, фильтровали и упаривали в вакууме с получением 160 мг (>100%) 3-[[5-фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]-3-пиридил]оксиметил]азетидин 1-трет-бутилкарбамата в виде желтого масла.
iii. 3-[[5-Фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]-3-пиридил]оксиметил]азетидин 1-трет-бутилкарбамат (160 мг, 0.27 ммоль, 99%), дихлорметан (5 мл) и трифторуксусную кислоту (1 мл) сначала вносили в 50 мл круглодонную колбу. Раствор перемешивали при 25°С в течение ночи. Полученный сырой продукт очищали с помощью препаративной ВЭЖХ с получением 30 мг (21%) 1-[5-(азетидин-3-илметокси)-3-фторпиридин-2-ил]-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде желтого твердого вещества.
ПРИМЕР 4: Синтез 1-(3-фтор-5-фторметоксипиридин-2-ил)-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она (Соединение - Пример 110)
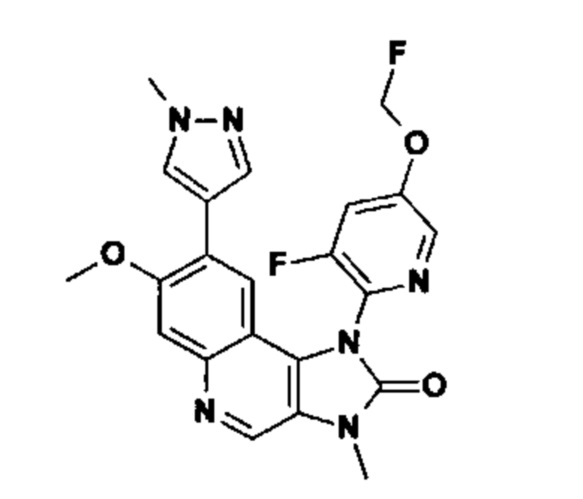
1-(3-Фтор-5-гидрокси-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (80 мг, 0.19 ммоль, 98%), карбонат калия (52.4 мг, 0.38 ммоль), N,N-диметилформамид (5 мл) и бромфторметан (43.0 мг, 0.36 ммоль, 95%) сначала вносили в герметичный 30 мл реакционный сосуд. Раствор перемешивали при комнатной температуре в течение 2 часов. Затем реакцию завершали путем добавления воды. Раствор затем три раза экстрагировали этилацетатом, каждый раз порцией 10 мл, и органические фазы объединяли. Остаток предварительно очищали на силикагеле с помощью EtOAC/MeOH (97/3). Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 45 мг (53%) 1-(3-фтор-5-фторметоксипиридин-2-ил)-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 5: Синтез 1-(5-дифторметокси-3-фторпиридин-2-ил)-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она (Соединение - Пример 114)

1-(3-Фтор-5-гидрокси-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (80 мг, 0.18 ммоль, 95%), карбонат калия (52.5 мг, 0.36 ммоль, 95%), N,N-диметилформамид (5 мл) сначала вносили в герметичный 8 мл реакционный сосуд, сосуд продували хлордифторметаном и хлордифторметановую атмосферу поддерживали при -30°С. Раствор перемешивали при 40°С в течение 2 дней. Затем реакцию завершали путем добавления 20 мл ледяной воды. Раствор три раза экстрагировали этилацетатом, каждый раз порцией 50 мл, и органические фазы объединяли. Смесь один раз промывали 20 мл солевого раствора, сушили над безводным сульфатом натрия и упаривали в вакууме. Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 27.7 мг (32%) 1-(5-дифторметокси-3-фторпиридин-2-ил)-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 6: Синтез 1-[5-(диметилфосфиноилметокси)-3-фторпиридин-2-ил]-8-(1,3-диметил-1Н-пиразол-4-ил)-7-метокси-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-она

8-(1,3-Диметилпиразол-4-ил)-1-(3-фтор-5-гидрокси-2-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-он (80 мг, 0.18 ммоль, 98%), хлор(диметилфосфорил)метан (76.3 мг, 0.54 ммоль, 90%), карбонат калия (50 мг, 0.36 ммоль) и N,N-диметилформамид (5 мл) сначала вносили в 8 мл реакционный сосуд, который был продут аргоном и выдерживался в атмосфере инертного газа - аргона. Реакционную смесь нагревали при 180°С в течение 2 часов (микроволновая печь). Полученные твердые вещества отфильтровывали. Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 11.7 мг (12%) 1-[5-(диметилфосфиноилметокси)-3-фторпиридин-2-ил]-8-(1,3-диметил-1Н-пиразол-4-ил)-7-метокси-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде твердого вещества.
ПРИМЕР 7: Синтез 8-(1,3-диметил-1Н-пиразол-4-ил)-1-(3-фтор-5-метилсульфонилметоксипиридин-2-ил)-7-метокси-3-метил-1,3-дигидроимидазо[4,5-с]схинолин-2-она (Соединение - Пример 201)
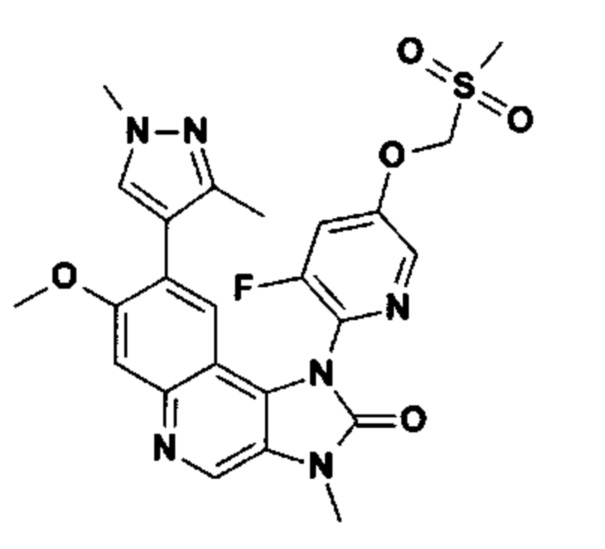
i. 8-(1,3-Диметилпиразол-4-ил)-1-(3-фтор-5-гидрокси-2-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-он (80 мг, 0.18 ммоль, 98%), N,N-диметилформамид (5 мл), карбонат калия (50 мг, 0.36 ммоль) и хлор(метилсульфанил)метан (110 мг, 1.09 ммоль, 95%) сначала вносили в 25 мл круглодонную колбу. Раствор перемешивали в течение ночи при 25°С. Затем реакцию завершали путем добавления 50 мл воды. Раствор четыре раза экстрагировали этилацетатом, каждый раз порцией 30 мл, и органические фазы объединяли. Смесь упаривали в вакууме. Остаток предварительно очищали на силикагеле с помощью MeOH:EtOAc (6:94) с получением 80 мг (85%) 8-(1,3-диметилпиразол-4-ил)-1-[3-фтор-5-(метилсульфанилметокси)-2-пиридил]-7-метокси-3-метилимидазо[4,5-с]хинолин-2-она в виде желтого твердого вещества.
ii. 8-(1,3-Диметилпиразол-4-ил)-1-[3-фтор-5-(метилсульфанилметокси)-2-пиридил]-7-метокси-3-метилимидазо[4,5-с]хинолин-2-он (80 мг, 0.15 ммоль, 95%), МеОН (5.00 мл) и раствор пероксодисульфата калия (220 мг, 0.77 ммоль, 95%) в воде (0.5 мл) сначала вносили в 25 мл круглодонную колбу. Раствор перемешивали при 25°С в течение 3 часов. Остаток предварительно очищали на силикагеле с помощью EtOAc:MeOH (70:30), и сырой продукт очищали с помощью препаративной ВЭЖХ с получением 15 мг (18%) 8-(1,3-диметил-1Н-пиразол-4-ил)-1-(3-фтор-5-метилсульфонилметоксипиридин-2-ил)-7-метокси-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 8: Синтез 1-[3-фтор-5-(тридейтерометокси)-2-пиридил]-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (Соединение - Пример 155)
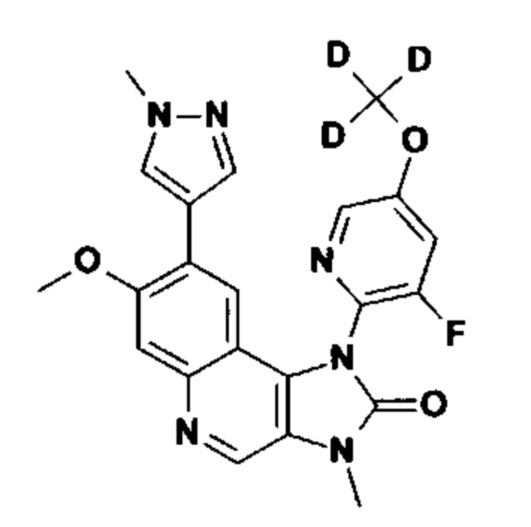
1-(3-Фтор-5-гидрокси-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (80 мг, 0.19 ммоль, 98%), N,N-диметилформамид (5.00 мл), карбонат калия (51.7 мг, 0.37 ммоль) и йод(D3)метан (57.1 мг, 0.37 ммоль, 95%) сначала вносили в 25 мл круглодонную колбу. Раствор перемешивали при комнатной температуре в течение 30 минут. Протекание реакции контролировали с помощью ЖХМС (дихлорметан/МеОН = 10:1). Затем реакцию завершали путем добавления 50 мл ледяной воды. Раствор три раза экстрагировали этилацетатом, каждый раз порцией 20 мл, и органические фазы объединяли. Смесь упаривали в вакууме с получением 38.5 мг (47%) 1-[3-фтор-5-(тридейтерометокси)-2-пиридил]-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 9: Синтез 1-(3-фтор-5-пиперазин-1-илпиридин-2-ил)-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она (Соединение - Пример 123)

1-(5-Хлор-3-фтор-2-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (100 мг, 0.22 ммоль, 95%), пиперазин 1-трет-бутилкарбамат (128 мг, 0.65 ммоль, 95%), Pd2(dba)3 (21 мг, 0.02 ммоль), ксантфос (27 мг, 0.05 ммоль), Cs2CO3 (150 мг, 0.46 ммоль) и толуол (10 мл) сначала вносили в герметичный 30 мл реакционный сосуд, который был продут аргоном и выдерживался в атмосфере инертного газа - аргона. Смесь перемешивали при 90°С в течение ночи и вслед за этим упаривали в вакууме. Остаток очищали на силикагеле с помощью EtOAC/MeOH (95:5, в единицах объема), с получением 120 мг (94%) 4-[5-фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]-3-пиридил]пиперазин 1- трет-бутилкарбамата в виде желтого твердого вещества.
ii. 4-[5-Фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]-3-пиридил]пиперазин 1-трет-бутилкарбамат (115 мг, 0.18 ммоль, 92%), дихлорметан (10 мл) и трифторуксусную кислоту (4 мл) сначала вносили в 25 мл круглодонную колбу. Смесь перемешивали в течение 30 минут при 0°С на бане вода/лед и упаривали в вакууме. Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 50 мг (55%) 1-(3-фтор-5-пиперазин-1-илпиридин-2-ил)-7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 10: Синтез 5-фтор-6-[7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]-N[-метилникотинамида (Соединение - Пример 138)
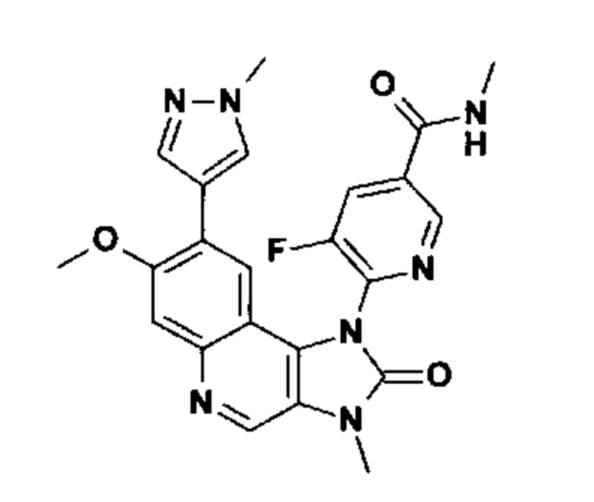
i. Раствор серной кислоты (2 мл, 98%) в воде (2 мл) и 5-фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]пиридин-3-нитрил (110 мг, 0.26 ммоль) сначала вносили в 8 мл реакционный сосуд. Смесь перемешивали при 80°С в течение ночи. Для доведения pH до 8 использовали гидроксид натрия (4 моль/л). Смесь упаривали в вакууме, и остаток очищали на силикагеле с помощью 0.5% водного раствора NH4HCO3 и CH3CN (82/18) с получением 70 мг (61%) 5-фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]пиридин-3-карбоновой кислоты в виде белого твердого вещества.
ii. 5-Фтор-6-[7-метокси-3-метил-8-(1-метилпиразол-4-ил)-2-оксоимидазо[4,5-с]хинолин-1-ил]пиридин-3-карбоновую кислоту (65.0 мг, 0.14 ммоль), раствор метиламина (10 мг, 0.32 ммоль) в тетрагидрофуране (0.5 мл), триэтиламин (44 мг, 0.43 ммоль), ВОР (64.9 мг, 0.15 ммоль) и тетрагидрофуран (5 мл) сначала вносили в герметичный 30 мл реакционный сосуд. Раствор перемешивали при комнатной температуре в течение 18 часов и упаривали в вакууме, остаток разбавляли 10 мл EtOAc. Смесь сушили над безводным сульфатом натрия и упаривали в вакууме. Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 20 мг (30%) 5-фтор-6-[7-метокси-3-метил-8-(1-метил-1Н-пиразол-4-ил)-2-оксо-2,3-дигидроимидазо[4,5-с]хинолин-1-ил]-N-метилникотинамида в виде белого твердого вещества.
ПРИМЕР 11: Синтез 1-[3-фтор-5-(тридейтерометокси)-4-пиридил]-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (Соединение - Пример 145)

1-(3-Фтор-5-гидрокси-4-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-он (145 мг, 0.33 ммоль, 97%), CD3OD (0.3 мл), карбонат калия (143 мг, 1.03 ммоль) и N,N-диметилформамид (3 мл) сначала вносили в герметичный 8 мл реакционный сосуд. Смесь перемешивали при 100°С в течение ночи. Затем реакцию завершали путем добавления 10 мл воды. Раствор три раза экстрагировали этилацетатом, каждый раз порцией 10 мл. Органические фазы объединяли, сушили над безводным сульфатом натрия и упаривали в вакууме. Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 20 мг (14%) 1-[3-фтор-5-(тридейтерометокси)-4-пиридил]-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 12: Синтез 1-(3-фтор-5-метоксипиридин-4-ил)-8-(1-фторметил-1Н-пиразол-4-ил)-7-метокси-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-она (Соединение - Пример 140)

1-(3-Фтор-5-метокси-4-пиридил)-7-метокси-3-метил-8-(1Н-пиразол-4-ил)имидазо[4,5-с]хинолин-2-он (60 мг, 0.14 ммоль, 97%), карбонат калия (57.6 мг, 0.42 ммоль) и N,N-диметилформамид (5 мл) сначала вносили в герметичный 30 мл реакционный сосуд. Смесь перемешивали при комнатной температуре в течение 5 минут и охлаждали до 0°С. Добавляли бромфторметан (165 мг, 1.39 ммоль, 95%), смесь нагревали до комнатной температуры и перемешивали в течение еще одного часа. Затем реакцию завершали путем добавления 50 мл воды. Раствор три раза экстрагировали этилацетатом, каждый раз порцией 30 мл, органические фазы объединяли и упаривали в вакууме. Сырой продукт очищали с помощью препаративной ВЭЖХ с получением 5 мг (8%) 1-(3-фтор-5-метоксипиридин-4-ил)-8-(1-фторметил-1Н-пиразол-4-ил)-7-метокси-3-метил-1,3-дигидроимидазо[4,5-с]хинолин-2-она в виде белого твердого вещества.
ПРИМЕР 13: Синтез 1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (Соединение - Пример 4)

Схема 3: Синтез Соединения - Примера 4
a. Синтез 6-бром-N-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-нитрохинолин-4-амина
3-Фтор-5-метоксипиридин-4-амин (447 мг, 3.02 ммоль), растворенный в N,N-диметилформамиде (5 мл), сначала помещали в атмосферу сухого азота. Вслед за этим к раствору добавляли гидрид натрия (504 мг, 12.6 ммоль, 60%), и смесь перемешивали при комнатной температуре в течение еще 5 минут. Затем к реакционной смеси добавляли 6-бром-4-хлор-7-метокси-3-нитрохинолин (800 мг, 2.52 ммоль), смесь перемешивали при комнатной температуре в течение 15 минут, и реакцию вслед за этим завершали путем добавления ледяной воды (100 мл). Выпавший осадок отфильтровывали, промывали ледяной водой и сушили с получением 1.0 г (94%) 6-бром-N-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-нитрохинолин-4-амина в виде желтого твердого вещества.
b. Синтез 6-бром-N4-(3-фтор-5-метокси-4-пиридил)-7-метоксихинолин-3,4-диамина 6-Бром-N-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-нитрохинолин-4-амин (990 мг, 2.20 ммоль), растворенный в метаноле (100 мл), сначала помещали в атмосферу защитного газа - азота. Вслед за этим добавляли Ni Ренея (100 мг, 1.17 ммоль), и реакционную смесь перемешивали в атмосфере водорода при атмосферном давлении в течение 30 минут. После аэрации азотом суспензию фильтровали, и фильтрат упаривали досуха в вакууме. Остаток кристаллизовали из смеси этилацетат/петролейный эфир с получением 0.86 г (99%) 6-бром-N4-(3-фтор-5-метокси-4-пиридил)-7-метоксихинолин-3,4-диамина в виде желтого твердого вещества.
c. Синтез 8-бром-1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3Н-имидазо[4,5-с]хинолин-2-она
Сначала вносили 6-бром-N4-(3-фтор-5-метокси-4-пиридил)-7-метоксихинолин-3,4-диамин (0.85 г, 2.20 ммоль), растворенный в тетрагидрофуране (20 мл). Вслед за этим добавляли 1,1'-карбонилдиимидазол (1.84 г, 11.3 ммоль) и основание Хюнига (1.46 г, 11.3 ммоль). Реакционный раствор нагревали при 40°С в течение 16 часов при перемешивании. Затем реакцию завершали путем добавления ледяной воды (200 мл). Выпавший осадок отфильтровывали, промывали ледяной водой и сушили с получением 0.87 г (94%) 8-бром-1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3Н-имидазо[4,5-с]хинолин-2-она в виде бледно-желтого твердого вещества.
d. Синтез 8-бром-1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-она
8-Бром-1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3Н-имидазо[4,5-с]хинолин-2-он (0.86 г, 1.94 ммоль), растворенный в N,N-диметилформамиде (5 мл), сначала помещали в защитную атмосферу сухого азота. Вслед за этим добавляли гидрид натрия (388 мг, 9.71 ммоль, 60%) и метилйодид (2.76 г, 19.4 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение 10 минут. Реакцию вслед за этим завершали путем добавления ледяной воды (100 мл). Полученный осадок отфильтровывали и сушили в вакууме с получением 0.70 г (80%) 8-бром-1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-она в виде бледно-желтого твердого вещества.
e. Синтез 1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (Соединение - Пример 4)
8-Бром-1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-метилимидазо[4,5-с]хинолин-2-он (150 мг, 0.33 ммоль), 1-метил-4-(тетраметил-1,3,2-диоксаборолан-2-ил)-1Н-пиразол (88.4 мг, 0.44 ммоль), Pd(PPh3)4 (76.6 мг, 0.07 ммоль) и карбонат калия (91.6 мг, 0.66 ммоль) в 1,4-диоксане (15 мл) и воде (5 мл) в атмосфере инертного газа - аргона сначала вносили в герметичный аппарат. Реакционную смесь нагревали при 80°С в течение 2 часов при перемешивании. Реакционную смесь вслед за этим охлаждали до комнатной температуры и упаривали досуха в вакууме. Остаток предварительно очищали с помощью хроматографии на силикагеле (этилацетат/метанол = 97:3, объемные доли). Элюент упаривали досуха, и полученный сырой продукт подвергали окончательной очистке с помощью препаративной ОФ-ВЭЖХ (вода/ацетонитрил). Упаривание содержащих продукт фракций приводило к получению 1-(3-фтор-5-метокси-4-пиридил)-7-метокси-3-метил-8-(1-метилпиразол-4-ил)имидазо[4,5-с]хинолин-2-она (70 мг, 47%, Соединение - Пример 4) в виде бесцветного твердого вещества.
Сокращения, используемые выше, которые являются обычными в области знаний специалиста, имеют следующие значения: МеОН: метанол; Рd(РРh3)4: тетракис(трифенилфосфин)палладий; EtOAc: этилацетат; ВОР: гексафторфосфат бензотриазолилокситрис(диметиламино)фосфония; Pd2(dba)3: трис(дибензилиденацетон)дипалладий
ПРИМЕР 14: Соединения - примеры, полученные согласно или аналогично ПРИМЕРАМ 1-13, показаны в Таблице 2 ниже. Использованные аминопроизводные, сложные эфиры бороновой кислоты или аналоги обобщены на Схеме 4 ниже.
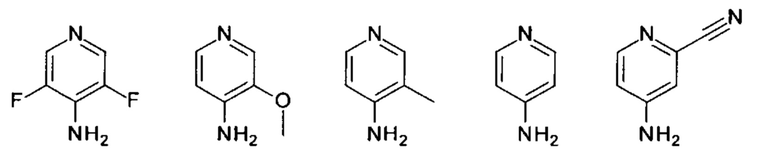













Схема 4: Аминопроизводные, сложные эфиры бороновой кислоты или аналоги
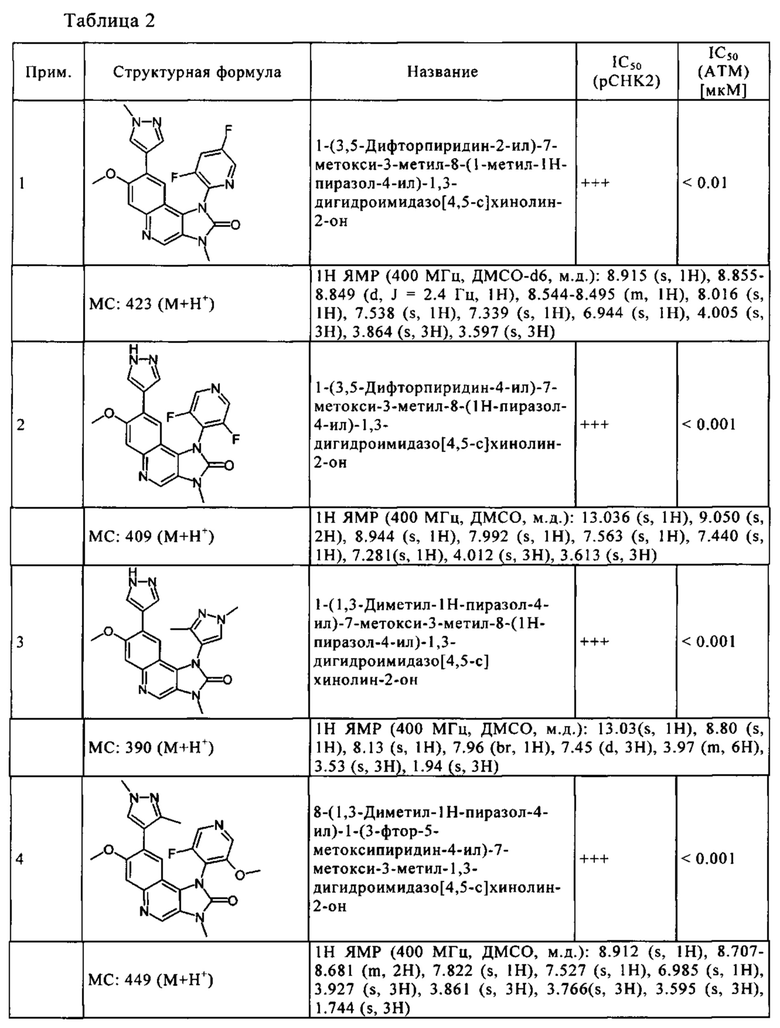

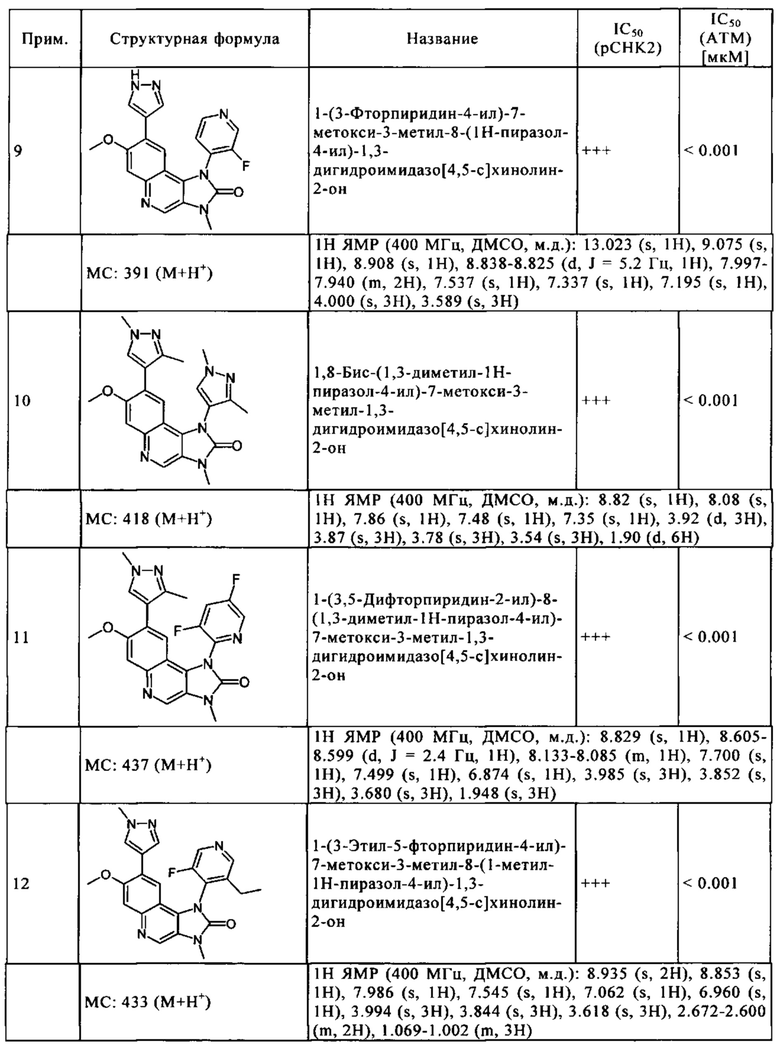














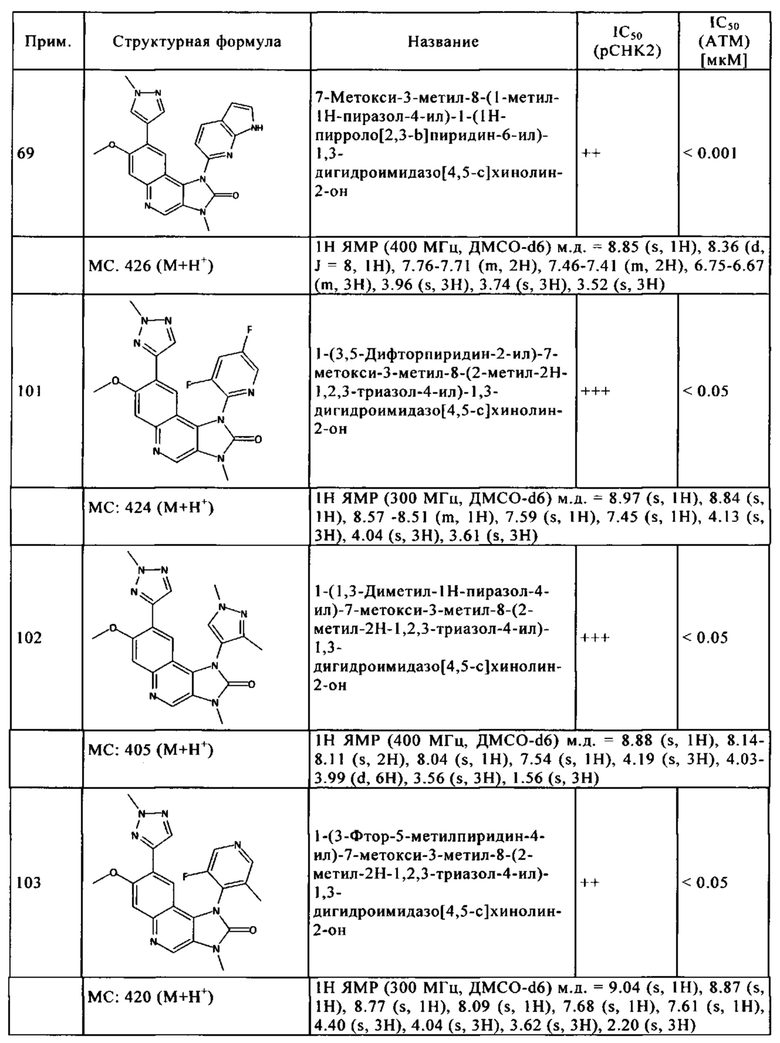



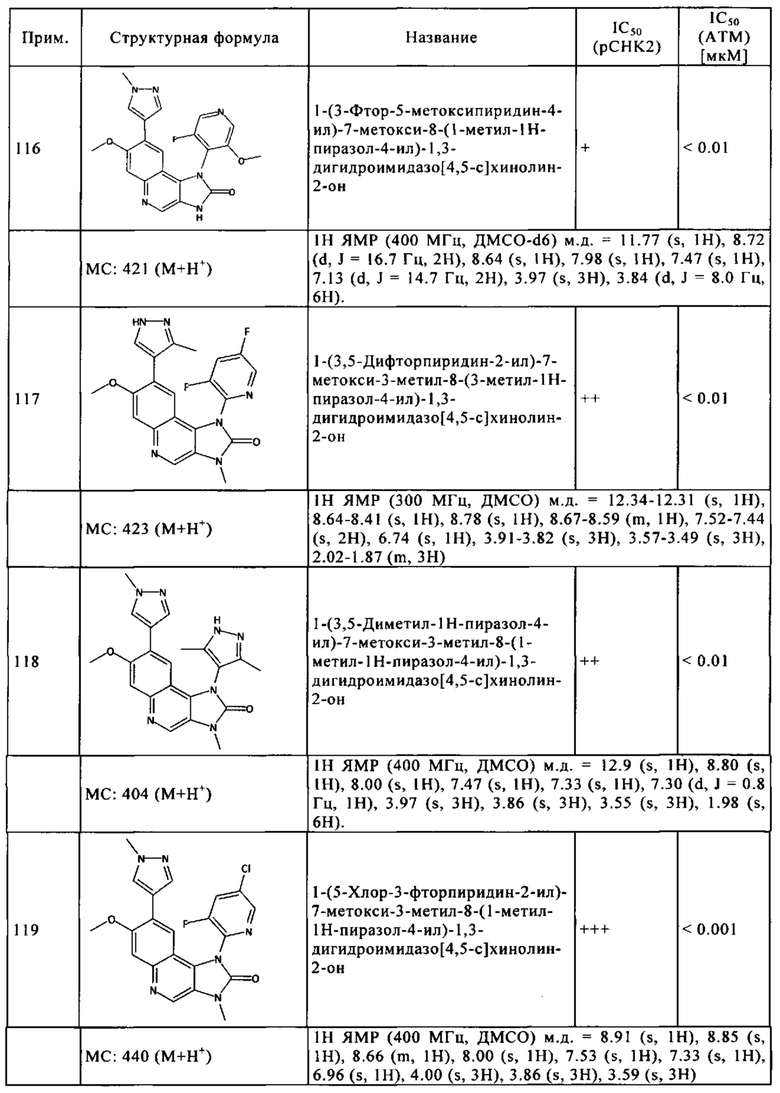








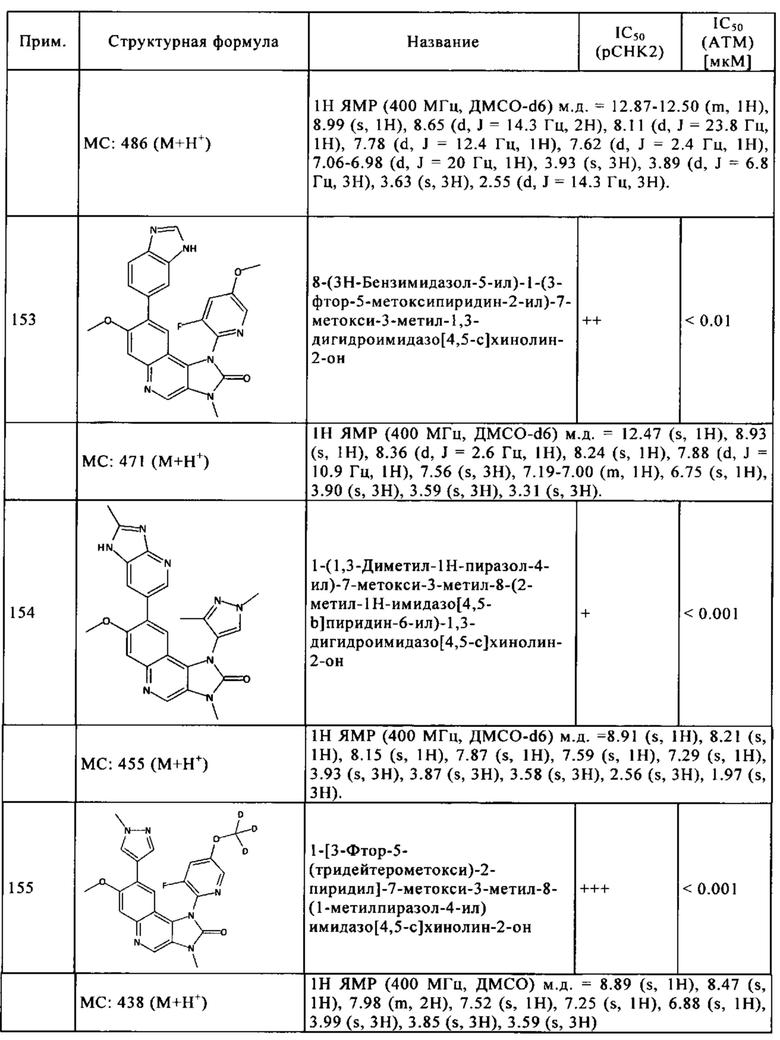



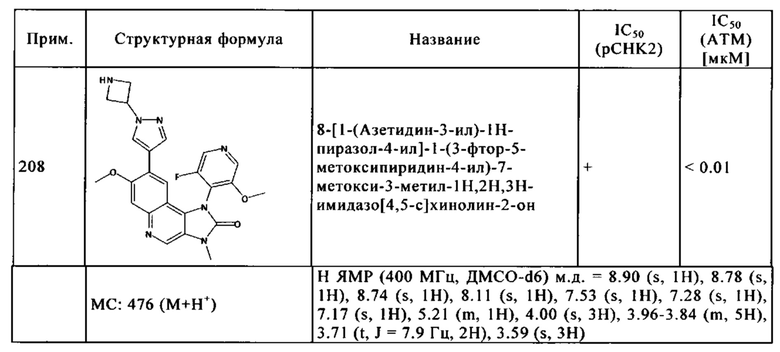
+++: 0.2 мкМ или меньше
++: от >0.2 мкМ до 1 мкМ
+: от >1 мкМ до 2 мкМ
Соединения в соответствии с изобретением не только демонстрируют очень хорошее ингибирование киназы ATM, они к тому же являются и очень селективными по отношению к другим киназам, таким как, например, mTOR, PIK3-альфа, РI3K-бета, РI3K-дельта и РI3K-гамма, что подтверждается экспериментальными данными, приведенными в Таблице 3 ниже:
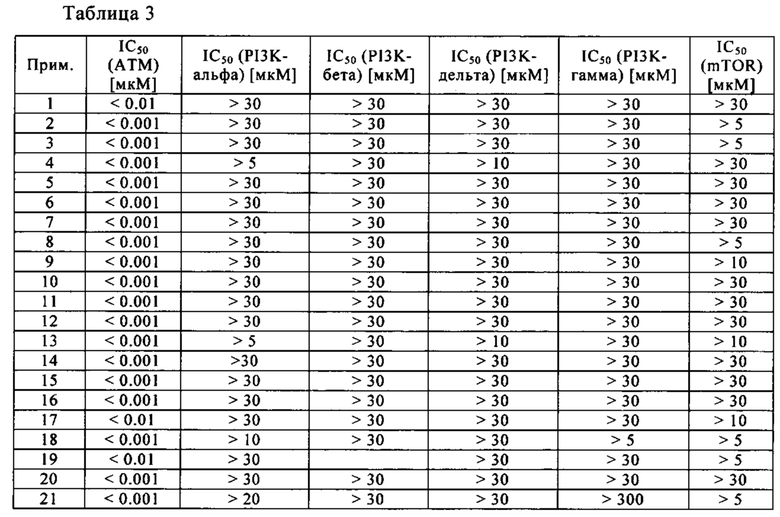

Для других соединений - примеров были определены следующие выгодные значения:
В отношении mTOR, следующие соединения - примеры обладают значением IC50 (ATM), которое выше по меньшей мере в 2000 раз (по сравнению с IC50 (mTOR)), где соотношение IC50 (ATM): IC50 (mTOR) в случае некоторых соединений - примеров даже превышает 100,000: 114, 118, 120, 121, 122, 125, 126, 136, 138, 140, 141, 145, 147, 149, 157, 159, 201.
В отношении PI3Kальфа, следующие соединения - примеры обладают значением IC50 (ATM), которое выше по меньшей мере в 2000 раз: 66, 67, 105, 108, 110, 114, 117, 120, 122, 123, 125, 126, 155, 201, 205.
В отношении PI3Kбета, следующие соединения - примеры обладают значением IC50 (ATM), которое выше по меньшей мере в 2000 раз (по сравнению с IC50 (РI3Kбета)), где соотношение IC50 (ATM): IС50(PI3Kбета) в случае некоторых соединений - примеров превышает 10,000: 108, 118, 125, 136, 137, 140, 145, 149, 159, 201.
В отношении PI3Kдельта, следующие соединения - примеры обладают IC50 (ATM) которое выше по меньшей мере 2000 в раз: 66, 67, 105, 108, 110, 114, 117, 120, 122, 123, 125, 126, 145, 155, 201, 205.
В отношении PI3Kгамма, следующие соединения - примеры обладают IC50 (ATM), которое выше по меньшей мере в 2000 раз: 66, 67, 105, 108, 110, 114, 117, 120, 122, 123, 125, 126, 136, 145, 149, 155, 201, 205.
ПРИМЕР 15: Дальнейшие соединения, которые могут быть получены согласно или аналогично ПРИМЕРАМ 1-12, показаны в Таблице 4 ниже.

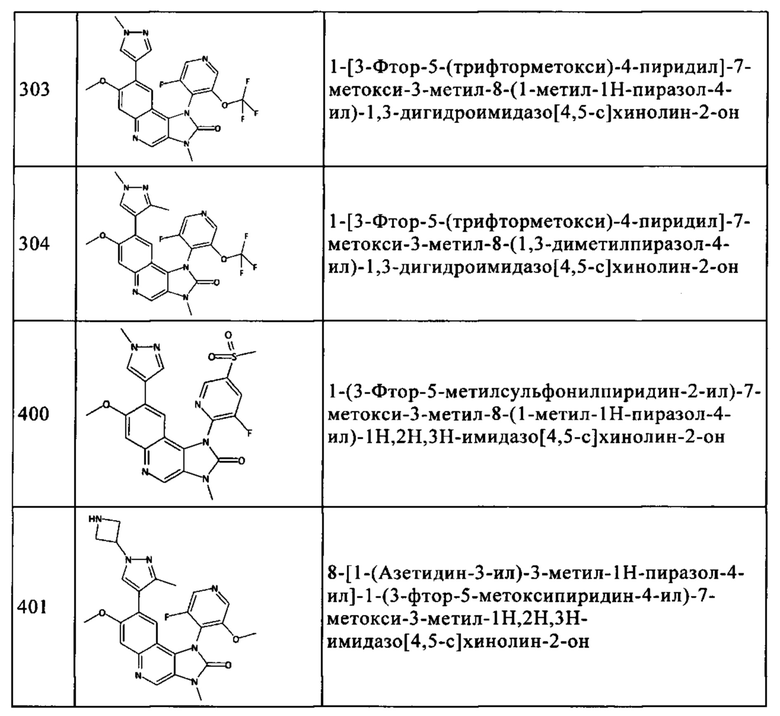
ПРИМЕР 16: Фармацевтические композиции
Пример А: Флаконы для инъекций
Значение рН раствора 100 г активного соединения в соответствии с изобретением и 5 г Na2НРO4 в 3 л бидистиллированной воды устанавливают на 6.8, используя 2 н. соляную кислоту, стерилизуют фильтрацией, переносят во флаконы для инъекций, лиофилизуют в стерильных условиях и запечатывают в стерильных условиях. Каждый флакон для инъекций содержит 5 мг активного соединения в соответствии с изобретением.
Пример В: Суппозитории
Смесь 20 г активного соединения в соответствии с изобретением расплавляют с 100 г соевого лецитина и 1400 г какаового масла, разливают в формы и позволяют охладиться. Каждый суппозиторий содержит 20 мг активного соединения в соответствии с изобретением.
Пример С: Раствор
Раствор приготовляют из 1 г активного соединения в соответствии с изобретением, 9.38 г NaH2PO4 *2 Н2O, 28.48 г Na2HPO4 *12 Н2O и 0.1 г бензалконийхлорида в 940 мл бидистиллированной воды. Значение рН устанавливают на 6.8, и объем раствора доводят до 1 л и стерилизуют путем облучения. Этот раствор может использоваться в форме глазных капель.
Пример D: Мазь
500 мг активного соединения в соответствии с изобретением смешивают с 99.5 г вазелина в асептических условиях.
Пример Е: Таблетки
Смесь 1 кг активного соединения в соответствии с изобретением, 4 кг лактозы, 1.2 кг картофельного крахмала, 0.2 кг талька и 0.1 кг стеарата магния спрессовывают обычным способом с получением таблеток таким образом, чтобы каждая таблетка содержала 10 мг активного соединения в соответствии с изобретением.
Пример F: Драже
Таблетки спрессовывают аналогично Примеру Е и затем покрывают обычным способом покрытием из сахарозы, картофельного крахмала, талька, трагаканта и красителя.
Пример G: Капсулы
2 кг активного соединения в соответствии с изобретением помещают в твердые желатиновые капсулы обычным способом таким образом, чтобы каждая капсула содержала 20 мг активного соединения в соответствии с изобретением.
Пример Н: Ампулы
Раствор 1 кг активного соединения в соответствии с изобретением в 60 л бидистиллированной воды стерилизуют фильтрацией, переносят в ампулы, лиофилизуют в стерильных условиях и запечатывают в стерильных условиях. Каждая ампула содержит 10 мг активного соединения в соответствии с изобретением.
Пример I: Ингаляционный аэрозоль
14 г активного соединения в соответствии с изобретением растворяют в 10 л изотонического раствора NaCl, и раствор помещают в стандартные коммерчески доступные емкости для аэрозолей с насосным механизмом. Раствор можно впрыскивать в рот и нос. Одно впрыскивание аэрозоля (приблизительно 0.1 мл) соответствует дозе приблизительно 0.14 мг.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ФУРО[3,2-В]- И ТИЕНО[3,2-В]ПИРИДИНА В КАЧЕСТВЕ ИНГИБИТОРОВ TBK1 И IKKε | 2013 |
|
RU2622034C2 |
| АРИЛХИНАЗОЛИНЫ | 2014 |
|
RU2701193C2 |
| ПРОИЗВОДНЫЕ ИНДОЛА | 2000 |
|
RU2256659C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗОПИРИДИНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1995 |
|
RU2156251C2 |
| Соединения имидазолонилхинолина и их терапевтическое применение | 2020 |
|
RU2822479C2 |
| ПРОИЗВОДНЫЕ БОРОНОВОЙ КИСЛОТЫ | 2015 |
|
RU2717558C2 |
| ЦИКЛИЧЕСКИЕ (АЗА) ИНДОЛИЗИНКАРБОКСАМИДЫ, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2010 |
|
RU2539574C2 |
| АМИНО-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ 3-ГЕТЕРОАРОИЛАМИНОПРОПИОНОВОЙ КИСЛОТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2012 |
|
RU2605600C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ С ИСПОЛЬЗОВАНИЕМ СОЕДИНЕНИЙ ПИРИМИДИНА И ПИРИДИНА С BTK ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ | 2016 |
|
RU2765154C2 |
| ПРОИЗВОДНЫЕ ПИПЕРИДИНМОЧЕВИНЫ | 2014 |
|
RU2666894C2 |
Изобретение относится к имидазолонилхинолиновым соединениям, применимым для ингибирования активности киназ. Предложено соединение формулы (IV), в котором Het1 означает пиразолил, который может быть незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal или А; А в каждом случае независимо означает неразветвленный или разветвленный алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов С, где, независимо друг от друга, 1, 2, 3, 4 или 5 атомов Н могут быть заменены на Hal; Hal означает F, Cl, Вr или I; НЕТ выбирают из 3-дифторметокси-5-фторпиридин-4-ила, 3-фтор-5-метоксипиридин-4-ила, 3-фтор-5-фторметоксипиридин-4-ила, 3-фтор-5-(тридейтерометокси)пиридин-4-ила, а также его фармацевтически пригодная соль, таутомер или стереоизомер. Предложена также фармацевтическая композиция, ингибирующая активность киназы АТМ, содержащая предложенное соединение. Технический результат – обеспечение малых молекул, которые эффективно и селективно ингибируют, регулируют и/или модулируют сигнальную трансдукцию посредством киназы АТМ. 2 н. и 2 з.п. ф-лы, 4 табл., 16 пр.
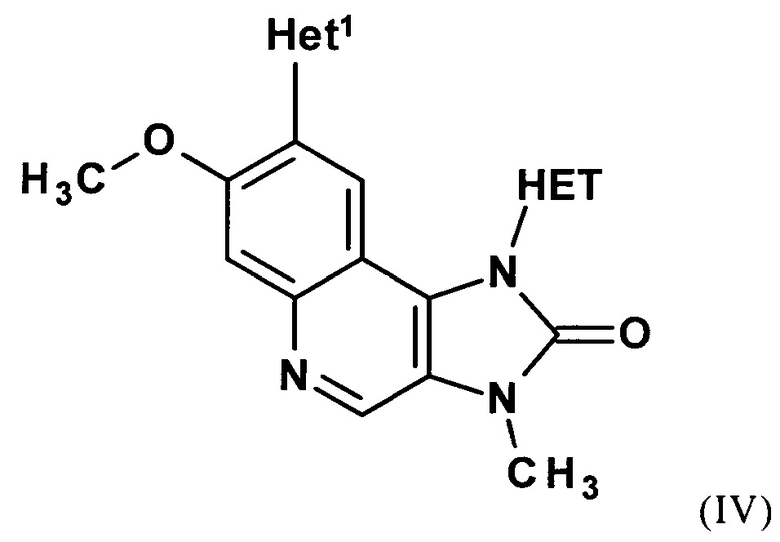
1. Соединение формулы (IV)

где Het1 означает пиразолил, который может быть незамещен или моно-, ди- или тризамещен, независимо друг от друга, посредством Hal или А,
А в каждом случае независимо означает неразветвленный или разветвленный алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов С, где, независимо друг от друга, 1, 2, 3, 4 или 5 атомов Н могут быть заменены на Hal,
Hal означает F, Cl, Вr или I,
НЕТ выбирают из 3-дифторметокси-5-фторпиридин-4-ила, 3-фтор-5-метоксипиридин-4-ила, 3-фтор-5-фторметоксипиридин-4-ила, 3-фтор-5-(тридейтерометокси)пиридин-4-ила,
и/или его фармацевтически пригодная соль, таутомер или стереоизомер.
2. Соединение формулы (IV) по п. 1, где
Het1 выбирают из 1Н-пиразол-4-ила, 2Н-пиразол-3-ила, 1Н-пиразол-3-ила, 1 -метил-1 Н-пиразол-4-ила, 3-метил-1Н-пиразол-4-ила, 5-метил-1Н-пиразол-3-ила, 4-метил-1Н-пиразол-3-ила, 1-фторметил-1Н-пиразол-4-ила, 1-дифторметил-1Н-пиразол-4-ила, 1,3-диметил-1Н-пиразол-4-ила, 1-этил-1Н-пиразол-4-ила, 1-этил-3-метил-1Н-пиразолила, 3-фтор-1-метил-1Н-пиразол-4-ила,
и/или его фармацевтически пригодная соль, таутомер или стереоизомер.
3. Соединение по п. 1, выбранное из следующих:



и/или его фармацевтически пригодная соль.
4. Фармацевтическая композиция, ингибирующая активность киназы ATM, содержащая эффективное количество по меньшей мере одного соединения по любому из пп. 1-3 и/или его фармацевтически пригодной соли, сольвата, таутомера или стереоизомера.
| WO 2010139731 A1, 09.12.2010 | |||
| WO 2011054846 A1, 12.05.2011 | |||
| RU 2007139008 A, 27.04.2009 | |||
| RU 2010153582 A, 20.07.2012. |
Авторы
Даты
2021-02-17—Публикация
2016-03-31—Подача