Изобретение относится к области молекулярной иммунобиотехнологии и может быть использовано в производстве высокочувствительных тест-систем для количественного определения любых соединений способных к стереоспецифическим взаимодействиям (антигенов, антител, нуклеиновых кислот, биологически активных макромолекул).
К настоящему времени достаточно хорошо известны системы гомогенного ЯМР-анализа, основанные на способности магнитных наноматериалов изменять время продольной (Т1) или поперечной (Т2) релаксации окружающих протонов воды [1]. Ключевой особенностью данных методов является кластеризация (или декластеризация) магнитных нано- или микрочастиц при наличии в исследуемом образце определяемого соединения (аналита). Отдельные частицы и кластеры имеют различную релаксивность (способность изменять Т1 или Т2). Таким образом, концентрацию аналита можно определить путем измерения времени релаксации. К преимуществам таких анализов можно отнести сокращение времени анализа и простоту аранжировки. Несмотря на это подобные методы анализа имеют, как правило, относительно низкую чувствительность и специфичность из-за отсутствия этапов промывки, которые позволили бы удалить присутствующие в образце примеси, в первую очередь белковые молекулы, способные к неспецифическому связыванию, что, кроме того, снижает надежность и воспроизводимость результатов анализа.
С этих позиций привлекательное значение имеют методы гетерогенного анализа, основанные на сорбции связывающих аналит соединений (анти-аналитов) на твердую фазу. Эти методы имеют более высокую чувствительность и специфичность, так как процедура их постановки включает в себя этапы промывки на каждой стадии, а также этап блокирования неспецифических сайтов связывания, что само по себе существенно снижает уровень фонового сигнала. Актуальность разработки методов анализа с высокой чувствительностью определяется необходимостью детектировать соединения, которые находятся в биологических средах в следовых количествах и/или низких концентрациях и являются маркерами опасных заболеваний (онкологических заболеваний, инфекций различной этиологии); либо вещества, даже малые количества которых могут представлять опасность для жизни. Разработка таких методов анализа может способствовать не только повышению эффективности диагностики, в первую очередь ранней, но и появлению возможности своевременного вмешательства в процесс проводимой терапии. При этом особое значение приобретают воспроизводимость и надежность используемых методов анализа.
Наиболее близким к заявляемому способу по технической сущности и достигаемому результату является метод иммуноферментного анализа, в котором в качестве детектирующих реагентов чаще всего используются ферментные конъюгаты пероксидазы хрена с распознающими молекулами. Детекцию и количественную оценку аналита, в данном методе проводят спектрофотометрически. На сегодняшний день иммуноферментный анализ является наиболее широко используемым и надежным методом лабораторной диагностики.
С позиции критики должно отметить тот факт, что в методе иммуноферментного анализа в качестве метки используется фермент, как правило, пероксидаза хрена, имеющий ряд недостатков: высокая стоимость синтеза и требовательность к условиям его приведения, что также относится к условиям хранения и транспортировки готового продукта (тест-систем) [2]. Например, известно, что активность пероксидазы хрена существенно снижается при использовании в анализе реагентов, в состав которых включен такой широко используемый консервант, как азид натрия. Низкая стабильность реагентов, применяемых в процедуре анализа, а также их чувствительность к окружающей среде приводит к снижению как надежности, так и воспроизводимости результатов. К непривлекательным сторонам ИФА относятся также токсичность субстратов, необходимых для проведения ферментной детекции, нестойкость продуктов реакции и процедурная сложность анализа.
Заявляемый способ позволяет решать задачу повышения воспроизводимости и надежности результатов анализа, за счет использования высокостабильных (фиг. 1 и фиг. 2) конъюгатов железоуглеродных наночастиц с распознающими молекулами в тандеме с высокочувствительным методом детекции на основе ЯМР-релаксометрии в аранжировке твердофазного гетерогенного анализа. Это имеет существенное значение, особенно в ситуациях, когда определяемый аналит (маркер), является индикатором таких серьезных и потенциально угрожающих жизни патологических процессов, как например, злокачественные новообразования. В подобных случаях надежность и воспроизводимость получаемых предлагаемым способом результатов играет существенную роль для принятия решений в части своевременного начала лечения и коррекции в ходе проводимой терапии.
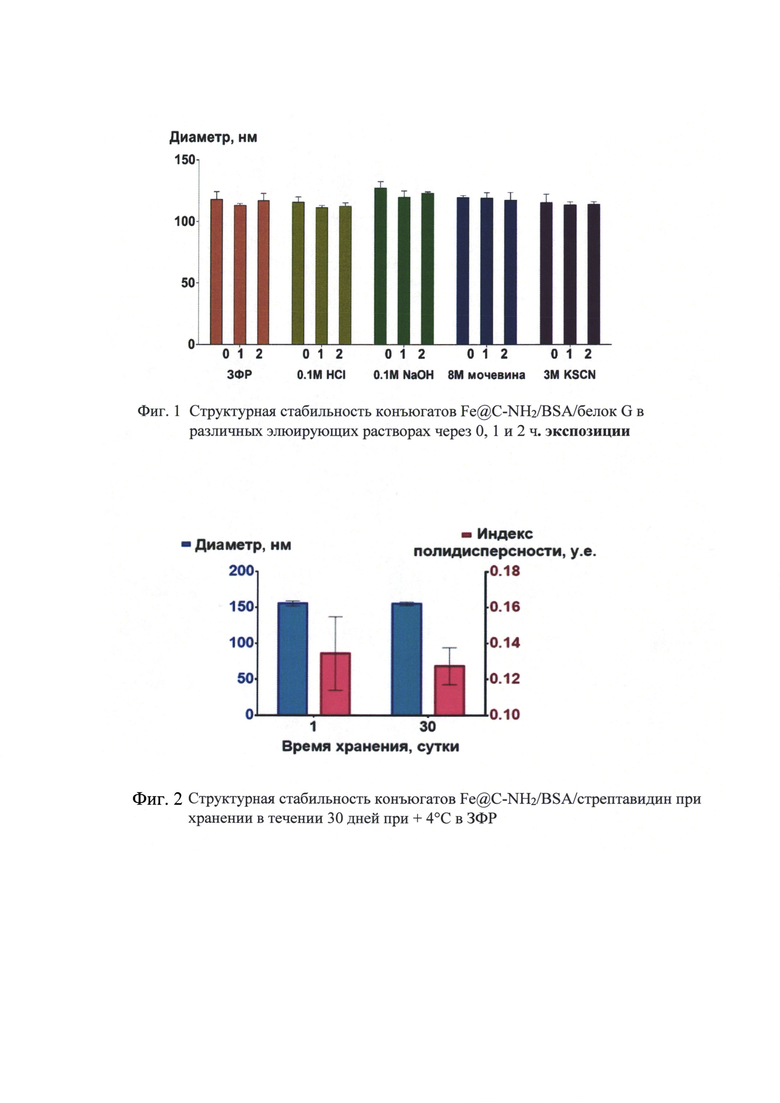
Известно, что для конструирования надежных систем анализа важную роль играет надежность используемых реагентов. В реализации предлагаемого способа использовали конъюгаты, синтезированные по авторской методике [3]. Для исследования стабильности диагностических реагентов были использованы конъюгаты магнитных железоуглеродных наночастиц с белком G стрептококков, обладающим способностью аффинно связываться с Fc-фрагментами IgG человека и большинства животных [4] и магнитных железоуглеродных наночастиц с стрептавидином, способным активно связываться с любыми биотинилированными соединениями [4]. Условно такие конъюгаты обозначают, как Fe@C-NH2/BSA4/балок G и Fe@C-NH2/BSA/стрептавидин. На фиг. 1. представлены результаты исследования структурной стабильности конъюгатов Fe@C-NH2/BSA/белок G в различных элюирующих растворах через 0, 1 и 2 ч. экспозиции. Фиг. 2 иллюстрирует результаты исследования структурной стабильность конъюгатов Fe@C-NH2/BSA/стрептавидин при хранении в течении 30 дней при +4°С в ЗФР.
Сущность изобретения. Стенки лунок стандартного иммунологического планшета сенсибилизируют соединением (анти-аналитом), способным специфически связывать определяемое соединение. Описанная процедура является предварительным этапом, приводящим к формированию твердофазного реагенты (иммуносорбента), пригодного для конструирования соответствующей тест-системы. В ходе реализации аналитической процедуры в лунки планшета вносят исследуемый образец, содержащий определяемое соединение (аналит). После соответствующей инкубации и промывки в лунки планшета вносят детектирующий реагент, представляющий собой конъюгат железоуглеродных наночастиц с соединением, специфично взаимодействующим с определяемым соединением. После инкубации лунки отмывают буферным раствором. В результате проведенных процедур на стенках лунок планшета образуется комплекс, состоящий из связывающего соединения, определяемого аналита и конъюгата. В дальнейшем в лунки вносят раствор NaOH, что приводит к освобождению наночастиц конъюгата из связанного состояния и перехода их в раствор. Лунки отделяют от планшета и помещают в измерительную ячейку ЯМР-релаксометра для измерения времени релаксации протонов в данном образце. По данному показателю прибор количественно позволяет оценить содержание определяемого соединения в образце в соответствии с ранее проведенной калибровкой.
Признаки способа, отвечающие критерию новизны, состоят в том, что измерение величины времени релаксации протонов (Т2), обусловленного количеством магнитных наночастиц извлеченных из специфического комплекса, осуществляется в суспензии, лишенной примесей. При этом уровень измеряемого параметра находится в прямой зависимости от количества определяемого аналита. Проведение специфической реакции по отношению к определяемому аналиту в формате твердофазного анализа позволяет освободится от примесных компонентов, содержащихся в анализируемом образце и способных значимо и невоспроизводимо влиять на результат измерения. Перевод наночастиц, количество которых пропорционально количеству определяемого аналита, в суспензию позволяет с высокой точностью измерить время релаксации протонов, прямо зависящее от количества наночастиц, с помощью ЯМР-релаксометра.
Предлагаемый способ позволяет решить любую аналитическую (диагностическую) задачу, связанную с количественным определение любого маркера (аналита), который в ходе аналитической процедуры может быть включен в специфично формирующийся комплекс, например, антитела (антианалит)-антиген (определяемый аналит)-антитела/магнитные наночастицы (конъюгат). Дальнейшее измерение времени релаксации протонов с помощью извлеченных из комплекса наночастиц и ЯМР регистрации объективно не зависит от природы определяемого маркера, что обеспечивает универсальность и мультиплексность предлагаемого способа.
Предлагаемое техническое решение иллюстрируется следующими примерами.
Нижеследующие примеры приводятся только с целью демонстрации возможностей настоящего изобретения, и никоим образом не ограничивают спектр соединений, которые могут быть определены при помощи предлагаемого способа анализа.
Приводимые в примерах конкретные количественные параметры, даже в области указываемых диапазонов, не фиксируются формулой изобретения, потому что не являются принципиальными условиями осуществления заявляемого способа.
Пример 1. Количественное определение простатспецифического антигена в формате твердофазного анализа с использованием конъюгата железо-углеродных наночастиц с моноклональными антителами (клон 1А6), специфичными к ПСА человека (Fe@C-1А6).
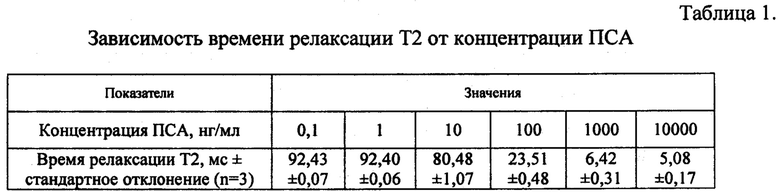
На стенки лунок разборного полистирольного планшета для иммунологических реакций сорбируют из объема 100 мкл мышиные моноклональные антитела (МКА) из клона 3А6 (производитель - Биалекса, Россия), специфичные к ПСА, разведенные в 0,2 М карбонатном буфере с рН 9,6 до концентрации 0,05 мг/мл. Сорбцию производят в течение 2 часов при температуре 37°С. Лунки планшета трижды промывают 250 мкл 0,15М раствора NaCl, забуференного 0,015М Na-фосфатами и содержащим 0,1% азида натрия и 0,1% твин-20, рН 7,25 (ЗФРТ), используя устройство для промывки микропланшетов, затем добавляют 200 мкл блокирующего буфера (ЗФТР + 2% казеин + 1% БСА), планшеты выдерживают в течение 1 часа. В отмытые после блокирования лунки добавляют образцы ПСА в объеме 100 мкл, разведенные кратно 10-ти в блокирующем буфере, начиная с концентрации 0,01 мг/мл и инкубируют в течение 60-ти мин., после чего в промытые как описано выше лунки вносят суспензию Fe@C-1А6 (100 мкл, 0,05 мг/мл) в ЗФРТ + 2% казеина. Время инкубации 60 минут. В отмытые лунки вносят по 100 мкл элюирующего раствора (0,1М NaOH) и через 60 мин. измеряют время релаксации протонов в каждой лунке, для чего каждую лунку отделяют от планшета и помещают в измерительную ячейку релаксометра. Результаты измерений для приведенного примера представлены в таблице 1. Все этапы анализа, за исключением этапов промывки и измерения, выполняют при +37°С. Общее время анализа 180-200 мин., без учета времени подготовки твердой фазы, что может быть выполнено заблаговременно.
Пример 2. Количественное непрямое определение антител (Ат) к столбнячному анатоксину на твердой фазе с использованием конъюгата железо-углеродных наночастиц с белком G (Fe@С-белок G).
На стенки лунок разборного полистирольного планшета для иммунологических реакций сорбируют из объема 100 мкл столбнячный анатоксин, разведенный в 0,2 М карбонатном буфере с рН 9,6 до концентрации 0,05 мг/мл. Сорбцию производят в течение 2 часов при температуре 37°С. Лунки планшета трижды промывают 250 мкл 0,15М раствора NaCl, забуференного 0,015М Na-фосфатами и содержащим 0,1% азида натрия и 0,1% твин-20, рН 7,25 (ЗФРТ), используя устройство для промывки микропланшетов, затем добавляют 200 мкл блокирующего буфера (ЗФТР + 2% казеин + 1% БСА), планшеты выдерживают в течение 1 часа. В отмытые после блокирования лунки добавляют образцы антител к столбнячному анатоксину в объеме 100 мкл, разведенные кратно 4-м в отрицательной сыворотке крови кролика (предварительно разведенной в 100 раз в блокирующем буфере), начиная с концентрации 100 мМЕ/мл и инкубируют в течение 60-ти мин., после чего в промытые как описано выше лунки вносят суспензию Fe@C - белок G (100 мкл, 0,05 мг/мл) в ЗФРТ + 2% казеина. Время инкубации 60 минут. В отмытые лунки вносят по 100 мкл элюирующего раствора (0,1М NaOH) и после 60-ти минутной инкубации измеряют время релаксации протонов, для чего каждую лунку отделяют от планшета и помещают в измерительную ячейку релаксометра. Результаты измерений для приведенного примера представлены в таблице 2. Все этапы анализа, за исключением этапов промывки и измерения, выполняют при +37°С. Общее время анализа 180-200 мин., без учета времени подготовки твердой фазы, что может быть выполнено заблаговременно. 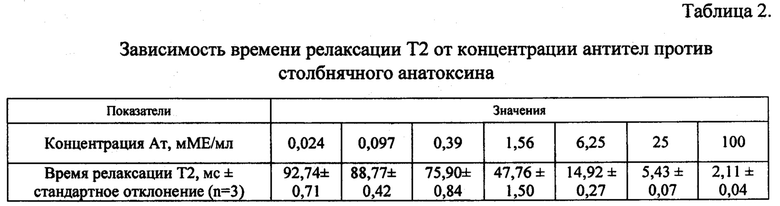
Одной из основных задач, решаемой при помощи разработанного способа, было повышение воспроизводимости и точности результатов анализа, поскольку эти аналитические характеристики важны для получения надежных достоверных данных в диагностических процедурах. С целью подтверждения высокой воспроизводимости и точности предлагаемого метода были проведены соответствующие исследования.
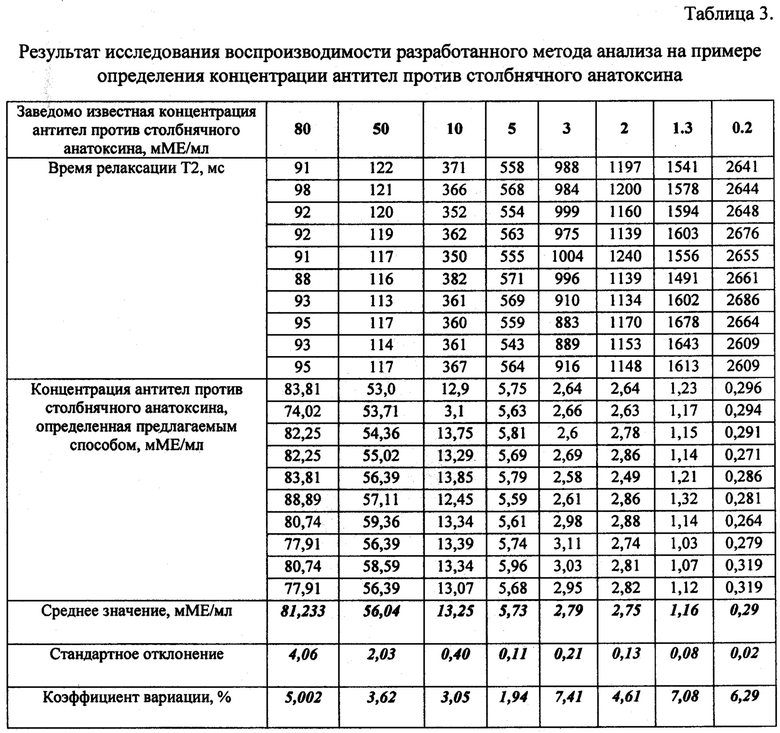
Для оценки воспроизводимости анализа в отрицательную предварительно разведенную в 100 раз блокирующим буфером кроличью сыворотку вносили известное количество антител к столбнячному анатоксину. Всего было проанализировано 8 образцов с концентрацией от 0.2 до 80 мМЕ/мл в 10 повторностях. Во всех образцах коэффициент вариации не превышал 7,5% (таблица 3), что соответствует допустимым пределам [5].
Для подтверждения точности разработанного анализа была проведена оценка степени извлечения методом добавок (spike-recovery test). Использовали образцы кроличьей сыворотки крови с известным содержанием антител (5, 3 и 1.3 мМЕ/мл) против столбнячного анатоксина. Предлагаемым методом определяли концентрацию Ат. Далее рассчитывали степень извлечения (таблица 4). Степень извлечения, выраженная в процентах, находилась в допустимых пределах [5].

Таким образом, технологический результат от использования предлагаемого изобретения заключается, в том, что разработанный способ анализа объективно не зависит от применения дорогостоящих реагентов и позволяет получать надежные результаты с высокой воспроизводимостью и точностью за счет применения эффективных реагентов: конъюгатов магнитных наночастиц, которые стабильны и не теряют своих структурных и функциональных свойств в течении длительного времени хранения (фиг. 1, 2), а также за счет разработанного способа, предусматривающего возможность в ходе анализа освободиться от примесей, влияющих на его результат.
Применение разработанного способа анализа может найти свою реализацию не только при создании эффективных тест-систем, предназначенных для диагностики различный заболеваний и аналитических исследований, но и в решении таких актуальных проблем как разработка способов оценки загрязнения окружающей среды и продуктов питания различными агентами.
Библиографический список
1. Zhang Y. et al. Recent Advances on Magnetic Relaxation Switching Assay-Based Nanosensors // Bioconjugate Chemistry. 2017. Vol. 28. №4. P. 869-879.
2. Huang Y., Ren J., Qu X. Nanozymes: Classification, Catalytic Mechanisms, Activity Regulation, and Applications // Chemical Reviews. 2019. Vol. 119. №6. P. 4357-4412.
3. Способ получения конъюгата на основе магнитных металл-углеродных наночастиц, пригодного для диагностических и аналитических целей, с использованием ЯМР-релаксометрии в качестве метода детекции // Патент РФ №2684325. 2019. Бюл. №10. / Раев М.Б., Храмцов П.В., Бочкова М.С. и др.
4. Khramtsov P. et al. Conjugation of carbon coated-iron nanoparticles with biomolecules for NMR-based assay // Colloids and Surfaces B: Biointerfaces, 2019. Vol. 176. P. 256-264
5. Bioanalytical Method Validation Guidance for Industry/ U.S. Department of Health and Human Services, Food and Drug Administration / [Электронный ресурс]. - Режим доступа: URL: https://www.fda.gov/media/70858/download (дата обращения: 20.02.2020).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения конъюгата на основе магнитных металл-углеродных наночастиц, пригодного для диагностических и аналитических целей, с использованием ЯМР-релаксометрии в качестве метода детекции | 2018 |
|
RU2684325C1 |
| Способ оценки эффективности вакцинации против коклюша, дифтерии и столбняка | 2016 |
|
RU2626679C1 |
| СПОСОБ ФУНКЦИОНАЛИЗАЦИИ ПОВЕРХНОСТИ МАГНИТНЫХ НАНОЧАСТИЦ | 2013 |
|
RU2543631C2 |
| Способ идентификации биологических маркеров, обнаруживаемых в биологических материалах человека в связи с возможным наличием патологических состояний организма человека, в том числе онкологических заболеваний, осуществляемый путем мультиплексного иммуноферментного сэндвич-иммуноанализа | 2021 |
|
RU2779104C1 |
| Способ конкурентного иммуноферментного анализа для детекции аналита в образце с помощью мультимодальных наночастиц | 2023 |
|
RU2836697C1 |
| Способ детекции аналита в образце с помощью иммунохроматографии | 2023 |
|
RU2835200C1 |
| МИКРОТИТРОВАЛЬНАЯ ПЛАТА | 1999 |
|
RU2158179C1 |
| Способ проведения микроскопического анализа клеточного образца | 2023 |
|
RU2835203C1 |
| Способ биоимиджинга | 2023 |
|
RU2838135C1 |
| Способ доставки нуклеиновой кислоты в клетку | 2023 |
|
RU2835201C1 |
Изобретение относится к области молекулярной иммунобиотехнологии. Раскрыт способ определения биологических макромолекул, включающий сорбцию молекул соединения, способного специфически связывать определяемое соединение (аналит), на поверхности лунок иммунологического планшета, последовательные инкубации с образцом, содержащим аналит, и конъюгатом железоуглеродных наночастиц, функционализированных узнающими молекулами, специфичными к определяемому аналиту, с промывками лунок ЗФРТ между каждой операцией. При этом детекцию результатов анализа осуществляют измеряя время релаксации протонов (Т2), обратно пропорционально связанное с количеством наночастиц, при помощи ЯМР-релаксометра; в процессе измерения участвуют наночастицы, образующиеся за счет освобождения наночастиц конъюгата из связанного состояния в структуре специфического комплекса и перехода их в раствор при добавлении раствора NaOH в лунки планшета. Изобретение обеспечивает повышение воспроизводимости и надежности результатов анализа. 2 ил., 4 табл., 2 пр.
Способ определения биологических макромолекул, включающий сорбцию молекул соединения, способного специфически связывать определяемое соединение (аналит), на поверхности лунок иммунологического планшета, последовательные инкубации с образцом, содержащим аналит, и конъюгатом железоуглеродных наночастиц, функционализированных узнающими молекулами, специфичными к определяемому аналиту, с промывками лунок ЗФРТ между каждой операцией, отличающийся тем, что детекцию результатов анализа осуществляют измеряя время релаксации протонов (Т2), обратно пропорционально связанное с количеством наночастиц, при помощи ЯМР-релаксометра, при этом в процессе измерения участвуют наночастицы, образующиеся за счет освобождения наночастиц конъюгата из связанного состояния в структуре специфического комплекса и перехода их в раствор при добавлении раствора NaOH в лунки планшета.
| СПОСОБ ФУНКЦИОНАЛИЗАЦИИ ПОВЕРХНОСТИ МАГНИТНЫХ НАНОЧАСТИЦ | 2013 |
|
RU2543631C2 |
| Способ получения конъюгата на основе магнитных металл-углеродных наночастиц, пригодного для диагностических и аналитических целей, с использованием ЯМР-релаксометрии в качестве метода детекции | 2018 |
|
RU2684325C1 |
| KOH | |||
| I | |||
| et al | |||
| Sensitive NMR Sensors Detect Antibodies To Influenza // Angew Chem | |||
| Int | |||
| Ed | |||
| Engl., 2008, V.47, pp.4119-4121 | |||
| KHRAMTSOV P | |||
| et al | |||
| Conjugation of carbon coated-iron nanoparticles with biomolecules for NMR-based assay // Colloids and Surfaces B: Biointerfaces, 01.04.2019, V.176, | |||
Авторы
Даты
2021-02-18—Публикация
2020-03-26—Подача