Изобретение относится к медицинской технике, а именно к устройствам для проведения исследований, и может быть использовано для диагностики и тестирования биологических образцов из таких источников, как цельная кровь, сыворотка крови, спинномозговая жидкость, образцы тканей, а также проб, взятых из окружающей среды.
В последние годы актуальной задачей является микроминиатюризация объема пробы для одновременного анализа нескольких аналитов из одного образца. Это связано с делением ограниченного объема пробы на несколько порций. В связи с этим проектирование микротитровальных плат пошло по пути уменьшения размеров лунок и увеличения их количества, так, в стандартных платах размером 8 х 12 см количество микролунок доходит до десяти тысяч. Уменьшение размеров лунок позволяет уменьшить объемы образца и реагентов, используемых при проведении анализов, что удешевляет процедуру тестирования или диагностики, а отбор микроколичеств исследуемого образца, например крови, является привлекательным при масс-скрининге населения.
Однако микроминиатюризация объема образца приводит к появлению ряда проблем. Уменьшение размеров лунок и увеличение их количества в титровальной плате стандартного размера (8 х 12 см) приводит к усложнению дозирующих устройств, значительному увеличению времени дозирования.
Но главной проблемой является детектирование результатов анализов. Использование микрообъемов для анализа существенно уменьшает, например, интенсивность эмиссии флуоресценции исследуемого образца, делая технику детектирования чрезвычайно чувствительной к сигналам детектируемого фона. Например, микролунки с объемом 0,5 мкл производят сигнал, который составляет 0,1-0,2% от сигнала, производимого лункой в 96-луночном планшете, что связано с пропорциональным снижением концентрации иммобилизованного на твердой фазе аналита.
Кроме того, в современном масс-скрининге предпочтительно используются сухие пятна крови и микроколичества образцов цельной крови для одновременного выявления нескольких маркеров инфекционных и/или соматических заболеваний. Это связано с ограниченным объемом биологического материала, например, при масс-скрининге врожденных аномалий у новорожденных, когда требуется определение четырех и более маркеров в сухом пятне крови, взятой из пятки новорожденного.
Известны микротитровальные платы для проведения анализа химических и биологических образцов (РСТ, патент N 99/49974, ЕР, патент N 0542422, РФ, патент N 2108156, кл. МКИ B O1 L 3/00).
Платы содержат большое количество микрососудов (микролунок) и позволяют проводить большое количество анализов при использовании микроколичеств образцов и реагентов.
Однако при использовании для анализа сухих образцов крови (сухих пятен крови) возникают проблемы, связанные с тем, что сухое пятно крови либо дробится на мелкие порции, либо растворяется в дополнительных сосудах и образец крови вносится в реакционные микрососуды в виде раствора. И в том и в другом случае увеличивается время для проведения анализа за счет дополнительных операций и резко снижается чувствительность при определении отдельных аналитов за счет уменьшения объема исследуемого образца при его дроблении на порции.
Известна микротитровальная плата, используемая в лабораторных условиях для длительных исследований биологических жидкостей, в том числе и для иммунохимических исследований (США, патент N Re.34.133, кл. НКИ 422-99). Микротитровальная плата выполнена в виде основания с углублениями, в которые вставляются индивидуальные микрососуды, образующие, при необходимости проведения большого числа анализов, ряды и колонны. Микрососуды могут быть заранее обработаны различными материалами (антигенами, антителами и т.п.), высушены и сохраняться до проведения анализов. При необходимости проведения анализов подготовленные сосуды вставляются в углубления основания в необходимом количестве и комбинации, так что одна группа микрососудов может быть использована для осуществления различных тестов в образце биологических жидкостей одного пациента. Микрососуды могут использоваться индивидуально, либо в виде группы, в которой сосуды связаны коротким стержнем, перемычкой, полоской и т.п., что позволяет, при необходимости, легко отделять их друг от друга. Дно микрососудов может быть выполнено плоским, U-образным, прямоугольным и т.п.
Недостатком устройства при исследовании сухих пятен крови и микроколичеств цельной крови является большой расход исследуемых образцов при осуществлении многоаналитного анализа, т.к. каждый сосуд, независимо от его размера, предназначен для определения только одного аналита.
Наиболее близкой является микроплата для проведения множества микроанализов (ЕР, патент N 0844025, кл. МКИ B O1 L 3/00). Микроплата содержит непрозрачную матрицу с отверстиями цилиндрической или любой другой формы, в которые вставляются индивидуальные микрососуды для образцов. Дно микрососудов выполнено прозрачным для пропускания света от образца, а сами микрососуды экранированы друг от друга за счет выступов у их дна и вершины, образованных непрозрачной матрицей. Микроплата может содержать от 96 до 384 микрососудов, зафиксированных относительно друг друга.
Недостатком 96-луночной микроплаты при проведении анализов с использованием сухого пятна и микроколичеств цельной крови является большой расход исследуемых образцов при многоаналитном тестировании, а для 384-луночной добавляется операция деления (дробления) сухого пятна крови, что резко снижает чувствительность из-за снижения концентрации маркера в пробе и соответственно порогового детектируемого уровня сигнала и увеличивает время анализа.
Задачей изобретения является создание микротитровальной платы для одновременного выявления нескольких маркеров инфекционных и/или соматических заболеваний при использовании сухих пятен крови или микроколичеств цельной крови, в том числе при ограниченном количестве биологического материала, когда дробление его на порции приводит к существенному снижению чувствительности и точности и даже невозможности количественного детектирования ряда маркеров.
Техническим результатом, достигаемым при использовании изобретения, является возможность проведения мультикомпонентного анализа без операции деления образца крови на отдельные порции, пропорциональные площади или объему микрососуда, при сохранении высокой чувствительности.
Поставленная задача решается предлагаемым изобретением.
Сущность изобретения заключается в том, что в микротитровальной плате, содержащей индивидуальные микрососуды, имеющие стенки и дно для иммуносорбента, и непрозрачную матрицу с углублениями для размещения микрососудов, все микрососуды разделены на изолированные друг от друга вертикальные ячейки сплошными перегородками, выполненными из того же материала, что и стенки микрососудов, при этом высота перегородок меньше высоты стенок микрососудов. Сущность изобретения заключается также в том, что высота перегородок равна 0,5-4 мм.
Сущность изобретения заключается также и в том, что высота перегородок меньше высоты стенок микрососудов по крайней мере на 1-2 мм.
Сущность изобретения заключается и в том, что объем ячеек равен 25-100 мкл.
Авторам не известны технические решения, имеющие подобную заявляемой совокупность признаков, следовательно, предлагаемое изобретение отвечает критерию новизны.
Предлагаемое изобретение отличается от прототипа тем, что микрососуды разделены на изолированные друг от друга вертикальные секции сплошными перегородками, высота которых меньше высоты стенок микрососудов. Это позволяет на дне каждой изолированной секции микрососуда сорбировать различные маркеры, а сухое пятно крови или микроколичество образца цельной крови размещать в объеме всего микрососуда. При проведении реакции весь определяемый аналит, содержащийся в образце крови, связывается с сорбированным в одной из секций маркером, что позволяет при микроминиатюризации анализов сохранить высокую чувствительность детектирования сигналов и экономно расходовать образцы крови. Авторам не известны технические решения, имеющие совокупность отличительных признаков в формуле изобретения, подобную заявляемой. Следовательно, предлагаемое решение отвечает критерию уровня техники.
Предлагаемая микроплата найдет широкое применение при проведении массовых анализов, там, где требуется высокая чувствительность детектирования при ограниченном объеме диагностируемого материала, например для скрининга врожденных аномалий новорожденных, иммунодиагностике вирусных гепатитов и ВИЧ-инфекций. Микроплата может быть изготовлена из отечественных материалов АО "Медполимер" совместно с ГНЦ ГосНИИ БП. Следовательно, предлагаемое изобретение отвечает критерию промышленной применимости.
На фиг.1 показаны варианты выполнения микротитровальной платы: фиг. 1 а, б - ячейки, полученные делением стандартного микрососуда (плата 8 х 12 см, 96 микрососудов) на четыре части; фиг. 1 в,г - ячейки, полученные делением стандартного микрососуда на шестнадцать частей.
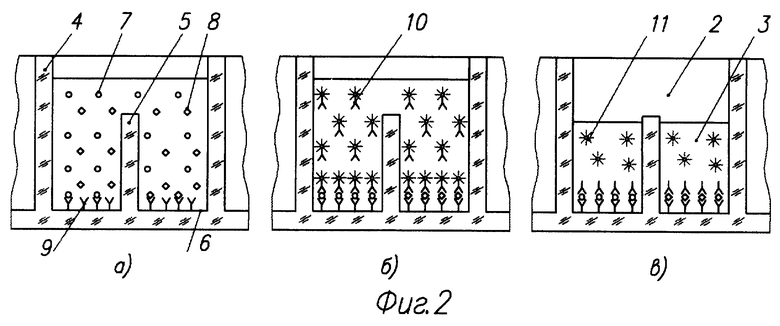
На фиг. 2 показана схема выполнения диссоциативного анализа микрообразца цельной крови в ячейках микрососуда: фиг. 2 а - введение микрообразца крови в ячейки; фиг. 2 б - введение конъюгата; фиг. 2 в - люминесцентная метка в объеме ячейки - детектирование сигнала.
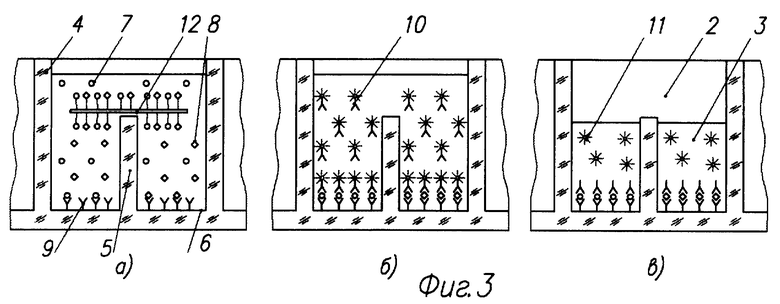
На фиг. З показана схема выполнения диссоциативного анализа сухого пятна крови в ячейках микрососуда: фиг. З а - введение сухого пятна крови в ячейки и экстрагирование аналита; фиг. 3 б - введение конъюгата; фиг. З в - люминесцентная метка в объеме ячейки - детектирование сигнала.
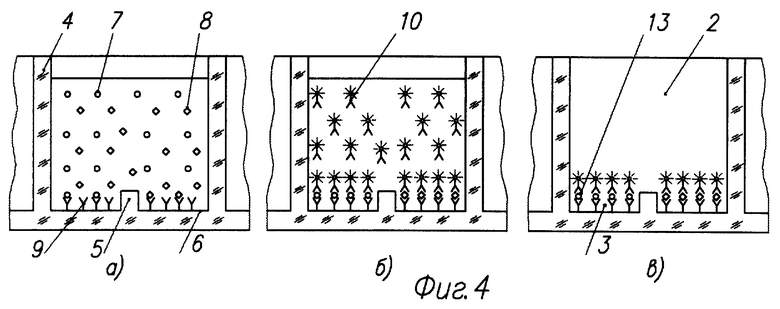
На фиг. 4 показана схема выполнения недиссоциативного анализа микрообразца цельной крови в ячейках микрососуда: фиг. 4 а - введение микрообразца крови в ячейки; фиг. 4 б - введение конъюгата; фиг.4 в - люминесцентная метка на дне ячейки - детектирование сигнала.
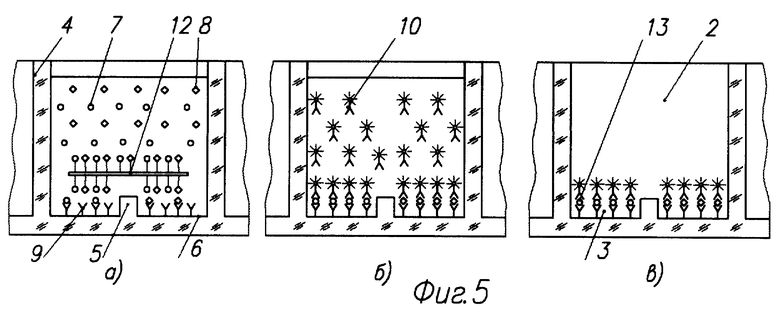
На фиг. 5 показана схема выполнения недиссоциативного анализа сухого пятна крови в ячейках микрососуда: фиг. 5 а - введение сухого пятна крови в ячейки и экстрагирование аналита; фиг. 5 б - введение конъюгата; фиг.5 в - люминесцентная метка на дне ячейки - детектирование сигнала.
Микротитровальная плата 1 (фиг. 1) содержит микрососуды 2, ячейки 3; микрососуды 2 содержат стенки 4, перегородки 5 и дно 6.
На фиг. 2-5 показаны микрососуд 2, ячейка 3, стенка микрососуда 4, перегородка 5 между ячейками 3, дно микрососуда 6, аналиты 7,8, сорбированные антитела 9, конъюгат с люминесцентной меткой 10, люминесцентная метка в объеме пробы 11, сухое пятно крови 12, люминесцентный комплекс антитело-аналит-меченое антитело 13 на дне 6 микрососуда 2.
Микрососуды могут быть разделены на любое количество ячеек. Оптимальным является количество ячеек от 2 до 16. При более мелких ячейках начинает падать чувствительность детектирования аналитов из-за уменьшения количества реагентов, необходимых для осуществления анализа.
Форма микрососудов и соответственно ячеек может быть любой: кpуглoй, овальной, прямоугольной, т.к. результаты анализа зависят только от концентрации аналита, связавшегося с антителами.
Устройство работает следующим образом.
Пример 1. Одновременное определение в одной лунке четырех маркеров сыворотки крови: тиротропина, тироксина, альфафетопротеина и хориогонадотропина осуществляют с помощью 96-луночной микротитровальной платы, емкостью 400 мкл, разделенной перегородками высотой 4 мм на 4 ячейки (по 60 мкл каждая).
Дно ячеек сенсибилизируют (обрабатывают) антителами, специфичными к соответствующим маркерам, и свободные места связывания на дне и стенках ячеек блокируют сывороточным альбумином. В лунки (микрососуды) подготовленного таким образом планшета вносят пробу (сыворотку крови) в объеме 300 мкл. При этом содержимое свободно может перемещаться между ячейками, так как верхний край жидкости пробы на 1,5-2 мм выше верхнего края перегородок между ячейками. После инкубации в течение 4-х часов пробу удаляют промывкой ячеек в промывателе с 384-ячеечной моющей головкой. Затем в ячейки вносят конъюгаты в объеме 30 мкл каждый, специфичные к одному из 4-х маркеров и меченные люминесцентной меткой. После 2-х часовой инкубации с конъюгатами вновь промывают ячейки и на заключительной стадии в них вносят по 30 мкл проявляющего реагента для диссоциации люминесцентной метки в объем. В качестве люминесцентной метки используют ионы европия в составе хелатного комплекса. В качестве проявляющего реагента используют усиливающий раствор для усиления люминесценции ионов европия в пробе. Регистрацию сигнала осуществляют путем последовательного возбуждения сигнала в объеме ячеек и измерения интенсивности люминесценции в режиме временного разрешения с помощью флуориметра (см. фиг. 2).
Предлагаемая микротитровальная плата позволяет повысить чувствительность выявления тиротропина, тироксина, хориогонадотропина и альфафетопротеина по сравнению с 384-луночным планшетом в 1,8-2,3 раза за счет существенного увеличения объема материала (300 мкл) вместо 80 мкл в каждой лунке.
Пример 2. Одновременное определение в одной лунке 4-х маркеров из сухого пятна крови, взятой у новорожденного: тиротропина, тироксина, иммунореактивного трипсина и 17OH гидроксипрогестерона с помощью 96-луночной микротитровальной платы, каждый микрососуд которой, емкостью 400 мкл, разделен перегородками высотой 4 мм на 4 ячейки (по 50 мкл каждая).
Дно ячеек сенсибилизируют антителами, специфичными к соответствующим маркерам, и свободные места связывания на дне и стенках ячеек блокируют сывороточным альбумином. Затем в лунки вносят сухое пятно крови в виде бумажного диска диаметром 4,0 мм, заливают экстрагирующим раствором так, что он может свободно перемещаться между ячейками, так как верхний край жидкости пробы на 1-1,5 мм выше верхнего края перегородок и материала сухого пятна. После инкубации в течение 4-х часов бумажный диск с кровью удаляют отсасыванием с помощью дискоудалителя, экстрагирующий буфер удаляют промывкой ячеек промывателем с 384-ячеечной моющей головкой. Затем в каждую ячейку вносят конъюгаты в объеме 30 мкл, специфичные к одному из 4-х маркеров и меченные люминесцентной меткой. После 2-х часовой инкубации с конъюгатами ячейки вновь промывают на промывателе и на заключительной стадии в них вносят по 30 мкл проявляющего реагента для диссоциации люминесцентной метки в объем. В качестве люминесцентной метки используют ионы европия в составе хелатного комплекса. Регистрацию сигнала осуществляют на флуориметре с временным разрешением люминесценции в объеме ячейки (см. фиг.З). Предлагаемый планшет позволяет повысить чувствительность выявления тиротропина, тироксина, хориогонадотропина и альфафетопротеина из сухого пятна крови по сравнению с 384-луночным планшетом в 3-3,5 раза за счет существенного увеличения объема материала (пятно крови диаметром 5,0 мм) вместо пятна диаметром 2,5 мм при использовании 384-луночного планшета.
Пример 3. Одновременное определение в одной лунке четырех маркеров сыворотки крови: тиротропина, тироксина, альфафетопротеина и хориогонадотропина с помощью 96-луночной микротитровальной платы каждая лунка которой, емкостью 400 мкл, разделена перегородками высотой 0,5 мм на 4 ячейки. В качестве конъюгата с люминесцентными метками используют недиссоциативные люминесцентные метчики и регистрацию сигнала осуществляют непосредственно со дна ячеек.
Предварительно дно ячеек сенсибилизируют антителами, специфичными к соответствующим маркерам, свободные места связывания на дне и стенках ячеек блокируют сывороточным альбумином. В лунки вносят пробу (сыворотку крови) в объеме 300 мкл. При этом содержимое свободно может перемещаться между ячейками лунки. После инкубации в течение 4-х часов пробу удаляют промывкой ячеек лунок на промывателе с 384-ячеечной моющей головкой. Затем в ячейки вносят конъюгаты в объеме 30 мкл в виде смеси, содержащей антитела, специфичные к одному из 4-х маркеров и меченные люминесцентной меткой (металлопорфирином или хелатным комплексом ионов европия). После 2-х часовой инкубации с конъюгатами ячейки вновь промывают и на заключительной стадии в них вносят по 30 мкл проявляющего реагента для оптимизации люминесцентных характеристик без процедуры диссоциации метки, а регистрацию сигнала осуществляют непосредственно со дна ячеек (см. фиг.4). В качестве люминесцентной метки используют ионы европия в составе хелатного комплекса.
Предлагаемый планшет позволяет повысить чувствительность выявления тиротропина, тироксина, хориогонадотропина и альфафетопротеина по сравнению с анализом в 384-луночном планшете в 2,8-3 раза за счет существенного увеличения объема материала 300 мкл вместо 80 мкл в случае использования 384-луночного планшета.
Пример 4. Одновременное определение в одной лунке 4-х маркеров из сухого пятна крови, взятой у новорожденного: тиротропина, тироксина, иммунореактивного трипсина и 17OH гидроксипрогестерона с помощью 96-луночного планшета, каждая лунка которого, емкостью 400 мкл, разделена перегородками высотой 0,5 мм на 4 ячейки.
Дно ячеек сенсибилизируют антителами, специфичными к соответствующим маркерам, свободные места связывания на дне и стенках ячеек блокируют сывороточным альбумином. В лунки подготовленного таким образом планшета вносят сухое пятно крови диаметром 5,0 мм. Сухое пятно заливают 30 мкл экстрагирующего раствора. Проводят инкубацию и промывку аналогично примеру 2. В качестве конъюгата с люминесцентными метками используют недиссоциативные люминесцентные метчики. Затем в ячейки вносят конъюгаты в объеме 30 мкл в виде смеси, содержащей антитела, специфичные к одному из 4-х маркеров и меченные люминесцентной меткой (металлопорфирином или хелатным комплексом ионов европия). После 2-х часовой инкубации с конъюгатами ячейки вновь промывают и на заключительной стадии в них вносят 30 мкл проявляющего реагента для оптимизации люминесцентных характеристик без процедуры диссоциации метки, а регистрацию сигнала осуществляют непосредственно со дна ячеек (см. фиг. 5). В качестве люминесцентной метки используют ионы европия в составе хелатного комплекса. Предлагаемый планшет позволяет повысить чувствительность выявления указанных маркеров по сравнению с 384-луночным планшетом в 2,8-3 раза за счет существенного увеличения объема исследуемого материала - пятно крови диаметром 5,0 мм вместо пятна диаметром 2,5 мм при использовании 384-луночного планшета.
Минимальная высота перегородок (0,5 мм) достаточна для проведения иммобилизации антител и последующего детектирования с помощью недиссоциативного варианта иммунологического и молекулярно-генетического анализа, когда не требуется специальных буферных растворов, при считывании сигнала с твердой фазы - дна ячеек.
Максимальная высота перегородок в микрососудах (4 мм) необходима для проведения диссоциативного анализа с переводом маркеров (например, люминесцентной метки) в объем пробы.
Чтобы обеспечить размещение сухого пятна крови в микрососуде и экстракцию из него исследуемого материала с последующей иммобилизацией во все ячейки или размещение жидкой пробы образца и иммобилизацию из нее исследуемого материала в ячейки, высота перегородок в микрососудах должна быть на 1-2 мм ниже стенок микрососуда.
Увеличение количества лунок у микротитровальной платы - прототипа по сравнению со стандартной платой (8 х 12 см, 96 лунок) приводит к необходимости деления сухого пятна крови или микрообразца цельной крови на более мелкие порции. Это снижает концентрацию аналита в лунке (микрососуде) и соответственно пороговый детектируемый уровень сигнала. Например, уменьшение площади сухого пятна крови до 1-2 мм2 не позволяет проводить достоверный анализ такого маркера на врожденный гипотиреоз, как тиротропин, с требуемой точностью (~10%) ни одним из известных методов детектирования (хемилюминесценция, различные типы люминесцентного и иммунного анализа и т. д.).
В предлагаемой микротитровальной плате при увеличении числа ячеек размер микрососуда, в котором они находятся, остается постоянным. Это обеспечивает возможность использования всей пробы для детектирования каждого маркера при многокомпонентном анализе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МНОГОАНАЛИТНОГО ИММУНОАНАЛИЗА | 2001 |
|
RU2184970C1 |
| СПОСОБ ОДНОВРЕМЕННОГО ДЕТЕКТИРОВАНИЯ ТИРОТРОПИНА И ОБЩЕГО ТИРОКСИНА В СУХИХ ПЯТНАХ КРОВИ | 2012 |
|
RU2480772C1 |
| СПОСОБ ОБНАРУЖЕНИЯ И ИДЕНТИФИКАЦИИ КЛЕТОК МИКРООРГАНИЗМОВ И ВИРУСОВ | 2001 |
|
RU2197732C1 |
| СПОСОБ ОДНОВРЕМЕННОГО ДЕТЕКТИРОВАНИЯ НЕСКОЛЬКИХ МАРКЕРОВ ВРОЖДЕННЫХ ЗАБОЛЕВАНИЙ В СУХИХ ПЯТНАХ КРОВИ | 2013 |
|
RU2541164C2 |
| УСТРОЙСТВО ДЛЯ ИЗМЕРЕНИЯ ЛЮМИНЕСЦЕНЦИИ БИОЛОГИЧЕСКИХ ОБРАЗЦОВ | 2000 |
|
RU2190208C2 |
| СПОСОБ ДЕТЕКТИРОВАНИЯ КОНЦЕНТРАЦИИ АНАЛИТА С ШИРОКИМ ДИНАМИЧЕСКИМ ДИАПАЗОНОМ | 2012 |
|
RU2519023C2 |
| СПОСОБ МНОГОАНАЛИТНОГО ИММУНОАНАЛИЗА | 2014 |
|
RU2593787C2 |
| СПОСОБ МНОГОАНАЛИТНОГО ИММУНОАНАЛИЗА С ИСПОЛЬЗОВАНИЕМ МИКРОЧАСТИЦ | 2007 |
|
RU2339953C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭКОЛОГИЧЕСКОЙ ОБСТАНОВКИ В РЕГИОНЕ | 2000 |
|
RU2180961C2 |
| СПОСОБ МНОГОАНАЛИТНОГО ИММУНОАНАЛИЗА С ИСПОЛЬЗОВАНИЕМ МИКРОЧАСТИЦ | 2008 |
|
RU2379691C1 |
Изобретение относится к медицинской технике, а именно к устройствам для проведения исследований, может быть использовано для диагностики и тестирования биологических образцов из таких источников, как цельная кровь, сыворотка крови, спинномозговая жидкость и т.д. и позволяет при использовании проводить мультикомпонентный анализ без операции деления образца крови на порции, пропорциональные площади или объему микрососуда, при сохранении высокой чувствительности. Микротитровальная плата содержит индивидуальные сосуды, имеющие стенки и дно для иммуносорбента, и непрозрачную матрицу, в углублении которой размещены микрососуды; все микрососуды разделены на вертикальные ячейки сплошными перегородками, выполненными из того же материала, что и стенки микрососудов, при этом высота перегородок меньше высоты стенок микрососудов по крайней мере на 1-2 мм и равна 0,5-4 мм. Достигается повышение информативности и упрощение анализа. 1 з.п.ф-лы, 5 ил.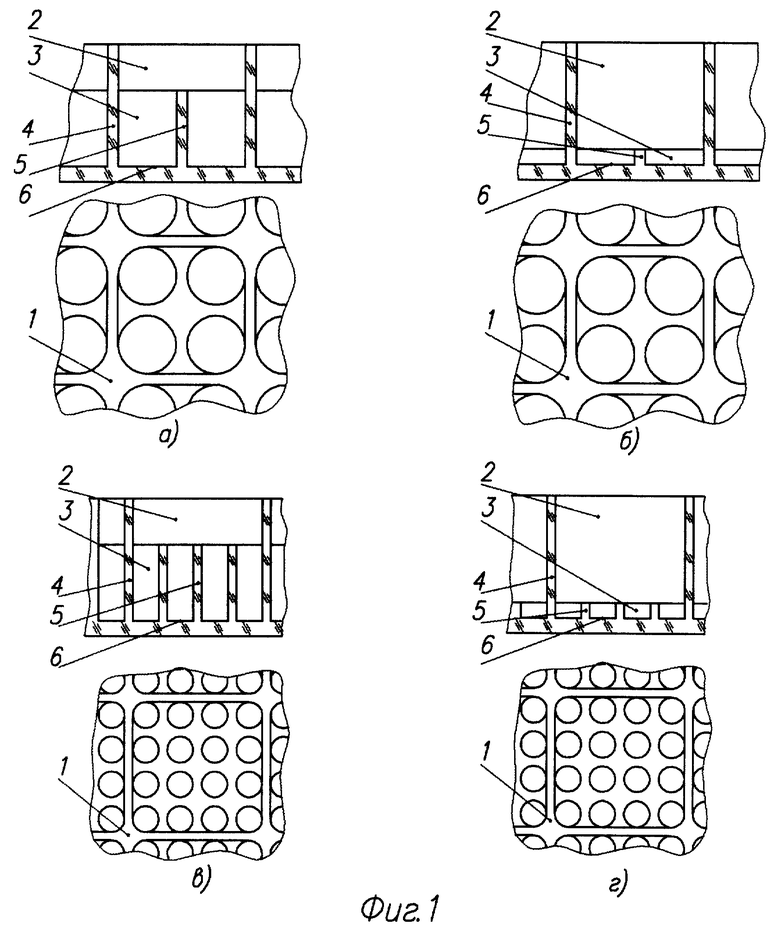
| Сепаратор | 1977 |
|
SU844025A1 |
| ТЕСТИРУЮЩЕЕ УСТРОЙСТВО, СПОСОБ ВЫПОЛНЕНИЯ (БИО- И/ИЛИ ИММУННО) ХИМИЧЕСКОГО ТЕСТА (ВАРИАНТЫ), ДОЗИРУЮЩЕЕ УСТРОЙСТВО И НАБОР | 1992 |
|
RU2108156C1 |
| RU 2014002 C1, 15.06.1994 | |||
| Кювета для проведения иммунных исследований с помощью оптических средств | 1990 |
|
SU1809780A3 |
| Способ культивирования | 1967 |
|
SU611597A3 |
| US 3877877 A, 15.04.1975 | |||
| US 5011663 A, 30.04.1991 | |||
| GB 21147378 A, 24.08.1983 | |||
| УСТРОЙСТВО для КОНТРОЛЯ КАЧЕСТВА ПОВЕРХНОСТЕЙ плоского ИЗДЕЛИЯ | 0 |
|
SU408144A1 |
Авторы
Даты
2000-10-27—Публикация
1999-12-30—Подача