РОДСТВЕННАЯ ЗАЯВКА
Настоящая заявка испрашивает приоритет согласно параграфу 119(e) раздела 35 Свода законов США на основании предварительной заявки на патент США №61/426957, поданной 23 декабря 2010 года.
УРОВЕНЬ ТЕХНИКИ
Эллагитаннины представляют собой мономерные, олигомерные и полимерные полифенолы, в больших количествах присутствующие в некоторых фруктах, ягодах и орехах, таких как гранат, малина, клубника, ежевикообразная малина, грецкие орехи и миндаль. Указанные фрукты и ягоды широко употребляют в свежем виде и в виде напитков, таких как сок, и существуют данные о том, что они способствуют укреплению здоровья.
В коммерческих способах переработки фруктовых соков эллагитаннины, которые в особенно больших количествах присутствуют в кожуре некоторых фруктов, в больших количествах экстрагируются соком. Эллагитаннины относятся к химическому классу гидролизуемых таннинов, которые высвобождают эллаговую кислоту при гидролизе. Исследования in vitro позволили предположить, что эллагитаннины в 10-100 микромолярных (мкМ) концентрациях обладают потенциальным антиоксидантным, антиатерогенным, антитромботическим, противовоспалительным и антиангиогенным действием. Во фруктах могут преобладать разные эллагитаннины - например, во фруктовом соке, полученном из граната, преобладающим эллагитаннином является пуникалагин [2,3-гексагидроксидифеноил-4,6-галлагилглюкоза], встречающийся в виде смеси изомеров. Описанные сильные антиоксидантные свойства гранатового сока объясняют высоким содержанием изомеров пуникалагина, которое может достигать уровней >2 г/л сока. Эллагитаннины также были идентифицированы в качестве активных антиатерогенных соединений в гранатовом соке. Также было высказано предположение, что эллагитаннины граната и фруктовые экстракты граната ингибируют пролиферацию раковых клеток человека и модулируют субклеточные пути передачи сигнала воспаления и апоптоз. См., например, Seeram et al. (2005) J Nutr Biochem. 16:360-7; Adams et al. (2006) J Agric Food Chem. 54:980-85; Afaq et al. (2005) Photochem Photobiol. 81:38-45; Afaq et al. (2005) Int J Cancer. 113:423-33. Также существуют данные о том, что экстракт плодов граната уменьшает рост опухоли предстательной железы и уровни простатического антигена в сыворотке (PSA) у бестимусных мышей линии nude с имплантированными клетками предстательной железы CWR22Rv1. Malik et al. (2005) Proc Natl Acad Sci. 102:14813-8.
К сожалению, эллагитаннины в большинстве своем плохо всасываются в кишечнике человека. Однако ряд метаболитов, получаемых из эллагитаннинов, всасывается в кишечнике человека, включая некоторые метаболиты, в конечном итоге образуемые в кишечнике комменсальными микроорганизмами (т.е. микрофлорой кишечника).
Эллагитаннины высвобождают эллаговую кислоту в физиологических условиях in vivo, а эллаговая кислота затем постепенно метаболизируется кишечной микрофлорой в кишечнике с образованием уролитина (urolithin) D, уролитина С, уролитина A (UA) и уролитина В (UB). После всасывания метаболиты подвергаются глюкуронированию и после попадания в печень далее метаболизируются с образованием глюкуронидов и/или сульфатов с образованием комбинации метаболитов, секретируемых в желчь.
Уролитины представляют собой метаболиты эллаговой кислоты, пуникалагина (РА), пуникалина (РВ), теллимаграндина (TL) и других эллагитаннинов (Cerda, Espin et al. 2004; Cerda, Periago et al. 2005). Эллаговая кислота (EA) в больших количествах присутствует в гранатовом соке (Gil, Tomas-Barberan et al. 2000). Эллагитаннин теллимаграндин (TL) был ранее выделен из граната и других растений и охарактеризован (Tanaka, Nonaka et al. 1986; Tanaka, Nonaka et al. 1986; Satomi, Umemura et al. 1993). Структурные формулы UA, PA, РВ, EA и TL представлены на ФИГ. 1.
Были предприняты значительные усилия для понимания механизма нарушений метаболизма, нейродегенерации и снижения когнитивных функций для более эффективной разработки методов лечения, включая методы лечения на основе натуральных продуктов. Одно из ключевых наблюдений заключалось в том, что снижение выработки энергии митохондриями, соответствующее повышенному окислительному стрессу и апоптозу, играет значительную роль в дегенеративных заболеваниях и процессе старения. В настоящее время показано, что множество дегенеративных заболеваний вызвано мутациями в генах митохондрий, кодируемых митохондриальной ДНК (мтДНК) или ядерной ДНК (яДНК). Важно отметить, что соматические мутации мтДНК накапливаются с возрастом в постмитотических тканях в сочетании с возрастным снижением функции митохондрий и, как считается, являются важным фактором, влияющим на старение и увядание. Наследственные заболевания могут являться следствием замены оснований мтДНК и мутаций, связанных с перестройкой, и могут поражать ЦНС, сердечную и скелетную мышцу, и почечную, эндокринную и гематологическую систему.
Митохондрии вырабатывают большую часть клеточной энергии путем окислительного фосфорилирования (OXPHOS), и они продуцируют большинство токсичных активных форм кислорода (АФК) в качестве побочного продукта. Генетические дефекты, ингибирующие OXPHOS, также вызывают перенаправление электронов OXPHOS в процесс образования АФК, таким образом, увеличивая окислительный стресс. Снижение выработки энергии митохондриями и увеличение окислительного стресса может нарушать открытие митохондриальных мегаканалов (mitochondrial permeability transition pore, mtPTP) и инициировать запрограммированную гибель клеток (апоптоз). Считается, что взаимодействие данных трех факторов играет главную роль в патофизиологии дегенеративных заболеваний и процессе старения, поражающем все ткани организма.
В головном мозге в норме оптимальная когнитивная функция главным образом зависит от активности и связи между нейронами - очень сложными клетками, способными передавать электрические сигналы и вызывать химическую нейротрансмиссию. Функция нейронов зависит от длинных и сложных клеточных отростков, которые могут простираться на сантиметры или даже метры для соединения нейронов или целевых клеток, и могут совершать более 100000 синаптических контактов. Таким образом, нейроны сильно зависят от энергоснабжения и, следовательно, подвержены повреждению в результате окислительного стресса. Когнитивная функция зависит от точного баланса внутриклеточной передачи сигнала, происходящей в сложной сети нейронов. Оптимальная когнитивная функция может быть нарушена многочисленными факторами, такими как старение, клеточный стресс, хронический стресс и нейродегенеративные нарушения. Уменьшение когнитивной функции можно охарактеризовать снижением показателей мышления, обучения, памяти, внимательности и/или нарушением психологических навыков, а также депрессией и тревогой.
Также было показано, что функция митохондрий имеет важное значение при нарушениях метаболизма. Диабет и ожирение соотносили с нарушениями функции митохондрий. Было высказано предположение, что эффективность взаимодействия в митохондриях или доля потребления кислорода, необходимая для получения АТФ, связана с уровнями ожирения; высокая эффективность взаимодействия, возможно, приводит к большему отложению запасов жира (Harper, Green et al. 2008). В недавних работах было высказано предположение, что при диабете дисфункция митохондрий является причиной нечувствительности к инсулину в миоцитах и адипоцитах в результате недостаточного энергоснабжения или дефектов в пути передачи инсулинового сигнала (Wang, Wang et al., 2010).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям, содержащим соединения или предшественники соединений, которые могут быть использованы для различных терапевтических применений, включая, например, лечение и/или предотвращение заболеваний или нарушений, связанных с пониженной или недостаточной активностью митохондрий, включая старение или стресс, диабет, ожирение и нейродегенеративные заболевания. Эти же соединения и композиции также можно предпочтительно применять у в целом здоровых индивидуумов для увеличения или поддержания скорости метаболизма, снижения процента жира в организме, увеличения или поддержания мышечной массы, контроля массы тела, улучшения или поддержания умственной деятельности (включая память), улучшения или поддержания мышечной деятельности, улучшения или поддержания настроения и контроля стресса.
Задачей настоящего изобретения является обеспечение растительного экстракта, его активной фракции или одного или более активных компонентов или метаболитов, выделяемых из него или синтезируемых, для применения для профилактики или лечения болезненного состояния, инициированного или характеризующегося (i) недостаточной активностью митохондрий; (ii) нарушениями метаболизма, такими как диабет и ожирение; (iii) снижением когнитивной функции; или (iv) нарушениями настроения.
Соответственно, согласно первому аспекту настоящего изобретения предложен фруктовый экстракт, его активная фракция или один или более активных компонентов, выделяемых из него, для применения в качестве индуктора функции митохондрий.
В настоящем описании термин «фракция» относится к очищенным или частично очищенным экстрактам.
В соответствии с другим аспектом настоящего изобретения предложен фруктовый экстракт, его активная фракция или один или более активных компонентов, выделяемых из него, для применения для профилактики или лечения болезненного состояния, инициированного или характеризующегося пониженной функцией митохондрий.
В соответствии с другим аспектом настоящего изобретения предложено применение фрукта или экстракта, или его активной фракции, или одного или более активных компонентов, выделяемых из него, определенных выше, для получения лекарственного средства для применения для (i) профилактики или лечения болезненного состояния, инициированного или характеризующегося пониженной функцией митохондрий; или (ii) улучшения когнитивной или мышечной функции. Такие болезненные состояния могут включать, без ограничения, нейродегенеративное заболевание, когнитивное расстройство, расстройство настроения, тревожное расстройство, нарушение метаболизма, сахарный диабет и ожирение.
В соответствии с другим аспектом настоящего изобретения предложен способ получения лекарственного средства для применения для (i) профилактики или лечения болезненного состояния, инициированного или характеризующегося пониженной функцией митохондрий; или (ii) улучшения когнитивной или мышечной функции; где указанный способ характеризуется использованием в качестве основного ингредиента лекарственного средства фрукта или экстракта, или его активной фракции, или одного или более активных компонентов, выделяемых из него, определенных выше.
В соответствии с другим аспектом настоящего изобретения предложена фармацевтическая композиция, содержащая активный компонент, полученный из фрукта или экстракта, или активной фракции, или одного или более активных компонентов, выделяемых из него, определенных выше, и фармацевтически приемлемый носитель.
Задачей настоящего изобретения является обеспечение растительных экстрактов, их активной фракции или одного или более активных компонентов или метаболитов, выделяемых из их или синтезируемых, для применения для лечения заболеваний или нарушений у субъекта, в отношении которых увеличение активности митохондрий оказало бы полезный эффект, для улучшения (i) функции головного мозга, (ii) метаболической функции, включая диабет или ожирение, (iii) мышечной деятельности и (iv) увеличения уровней АТФ в тканях.
Задачей настоящего изобретения является обеспечение экстрактов, композиций и соединений, которые являются нейропротекторными, нейротрофическими и/или способствуют росту нейритов и, следовательно, улучшают когнитивную функцию, а также обеспечение способов применения данных соединений и композиций.
Задачей настоящего изобретения является обеспечение соединений и композиций, которые улучшают, защищают и поддерживают функцию головного мозга и когнитивную функцию. Другая задача настоящего изобретения заключается в улучшении, защите от расстройств настроения и контроля расстройств настроения. Другая задача настоящего изобретения заключается в защите от вызванных стрессом или связанных со стрессом нарушений или симптомов.
Задачей настоящего изобретения является обеспечение нейропротекторных соединений для защиты головного мозга от инсультов, а также улучшения когнитивной деятельности и памяти у взрослых в нормальном состоянии. Другая задача настоящего изобретения заключается в обеспечении новых соединений, стимулирующих пластичность нейронов. Хорошо известно, что пластичность нейронов является ключевым процессом, необходимым для функции памяти и когнитивной функции. Такие соединения могут влиять на рост нейритов, число разветвлений на клетку, среднее количество отростков на клетку и даже количество образованных синапсов.
Настоящее изобретение также относится к нескольким полифенольным соединениям и их производным, относящимся к эллагитаннинам, в качестве биоактивных природных соединений, обнаруживаемых в гранате и других фруктах, а также биоактивным природным экстрактам, содержащим данные соединения. Данные соединения включают эллагитаннины, пуникалагин и эллаговую кислоту, все из которых обнаружены в гранате, но могут быть также выделены из других фруктов и ягод, а также метаболиты данных соединений. Как описано в настоящем документе, в настоящее время было показано, что данные соединения оказывают полезные эффекты в отношении (i) функции митохондрий, (ii) клеточного метаболизма и (iii) пластичности нейронов.
С использованием моделирования роста нейритов и образования отростков в культуре нейронных клеток и первичных клетках in vitro, исследовали различные соединения на предмет их полезных эффектов. Как описано выше, старение, нейродегенерация и хронический стресс оказывают отрицательное влияние на рост нейритов. Примечательным является то, что было обнаружено, что соединения согласно настоящему изобретению обладают нейропротекторными свойствами, демонстрируют сильную стимулирующую активность в клетках PC-12 и первичных мезэнцефалических нейронах, и улучшают когнитивную функцию, и память в моделях у животных.
В соответствии с одним из аспектов настоящее изобретение относится к композиции, такой как фармацевтическая, продукту лечебного питания, функциональному продукту питания, пищевой добавке или добавке к рациону, содержащей соединения или их смесь согласно настоящему изобретению. Указанная композиция также может необязательно содержать дополнительный терапевтический агент или может быть введена в комбинации с другим терапевтическим соединением. Также предложены упакованные продукты, содержащие вышеуказанную композицию и этикетку и/или инструкции по применению, для улучшения памяти и когнитивной деятельности и/или для лечения заболевания или состояния, связанного с повреждением головного мозга, характерным для состояний, встречающихся у взрослого в процессе старения.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество экстракта граната, для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество эллагитаннина, для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество пуникалагина, для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество эллаговой кислоты, для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество уролитина, для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой ожирение.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой сниженную скорость метаболизма.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой метаболический синдром.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой сахарный диабет.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой сердечнососудистое заболевание.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой гиперлипидемию.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой нейродегенеративное заболевание.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой когнитивное расстройство.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой расстройство настроения.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой стресс.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой тревожное расстройство.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации продукт питания или питательная добавка предназначены для контроля массы тела.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации продукт питания или питательная добавка предназначены для усиления мышечной деятельности.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации продукт питания или питательная добавка предназначены для усиления умственной деятельности.
Один из аспектов настоящего изобретения представляет собой способ усиления или поддержания функции митохондрий. Указанный способ включает этап приведения клеток в контакт с эффективным количеством уролитина или его предшественника с обеспечением усиления функции митохондрий.
Один из аспектов настоящего изобретения представляет собой способ лечения, предотвращения или контроля связанного с митохондриями заболевания или состояния, ассоциируемого с измененной функцией митохондрий или пониженной плотностью митохондрий. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения заболевания или состояния, ассоциируемого с измененной функцией митохондрий или пониженной плотностью митохондрий.
Один из аспектов настоящего изобретения представляет собой способ увеличения скорости метаболизма. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением увеличения скорости метаболизма.
Один из аспектов настоящего изобретения представляет собой способ предотвращения или лечения метаболического синдрома. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением предотвращения или лечения метаболического синдрома.
Один из аспектов настоящего изобретения представляет собой способ предотвращения или лечения ожирения. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением предотвращения или лечения ожирения.
Один из аспектов настоящего изобретения представляет собой способ предотвращения или лечения сердечнососудистого заболевания. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением предотвращения или лечения сердечнососудистого заболевания.
Один из аспектов настоящего изобретения представляет собой способ лечения гиперлипидемии. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением лечения гиперлипидемии. В одном из вариантов реализации гиперлипидемия представляет собой гипертриглицеридемию. В одном из вариантов реализации гиперлипидемия представляет собой повышенное количество свободных жирных кислот.
Один из аспектов настоящего изобретения представляет собой способ лечения нарушения метаболизма. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения нарушения метаболизма. В одном из вариантов реализации указанное нарушение метаболизма представляет собой сахарный диабет. В одном из вариантов реализации указанное нарушение метаболизма представляет собой ожирение.
Один из аспектов настоящего изобретения представляет собой способ лечения нейродегенеративного заболевания. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения нейродегенеративного заболевания. В одном из вариантов реализации указанное нейродегенеративное заболевание выбрано из группы, состоящей из комплекса СПИД-деменция, болезни Альцгеймера, бокового амиотрофического склероза, адренолейкодистрофии, болезни Александера, болезни Альперса, атаксии-телеангиэктазии, болезни Баттена, коровьей губчатой энцефалопатии (BSE), болезни Канавана, кортикобазальной дегенерации, болезни Крейтцфельдта-Якоба, деменции с тельцами Леви, фатальной семейной бессонницы, лобно-височной лобарной дегенерации, болезни Хантингтона, болезни Кеннеди, болезни Краббе, болезни Лайма, болезни Мачадо-Джозефа, рассеянного склероза, множественной системной атрофии, нейроакантоцитоза, болезни Ниманна-Пика, болезни Паркинсона, болезни Пика, первичного бокового склероза, прогрессирующего надъядерного паралича, болезни Рефсума, болезни Сандгоффа, диффузного миелинокластического склероза, спиноцеребеллярной атаксии, подострой комбинированной дегенерации спинного мозга, сухотки спинного мозга, болезни Тея-Сакса, токсической энцефалопатии, трансмиссивной губчатой энцефалопатии и синдрома шатающегося ежа. В одном из вариантов реализации указанное нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, бокового амиотрофического склероза, болезни Хантингтона и болезни Паркинсона. В одном из вариантов реализации указанное нейродегенеративное заболевание представляет собой болезнь Альцгеймера.
Один из аспектов настоящего изобретения представляет собой способ улучшения когнитивной функции. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением улучшения когнитивной функции. В одном из вариантов реализации когнитивная функция выбрана из группы, состоящей из восприятия, памяти, внимания, понимания речи, образования речи, понимания прочитанного, формирования образов, обучения и мышления. В одном из вариантов реализации когнитивная функция выбрана из группы, состоящей из восприятия, памяти, внимания и мышления. В одном из вариантов реализации когнитивная функция представляет собой память.
Один из аспектов настоящего изобретения представляет собой способ лечения когнитивного расстройства. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения когнитивного расстройства. В одном из вариантов реализации указанное когнитивное расстройство выбрано из группы, состоящей из делирия, деменции, нарушения способности к обучению, синдрома дефицита внимания (СДВ) и синдрома дефицита внимания и гиперактивности (СДВГ). В одном из вариантов реализации указанное когнитивное расстройство представляет собой
нарушение способности к обучению. В одном из вариантов реализации указанное когнитивное расстройство представляет собой синдром дефицита внимания (СДВ). В одном из вариантов реализации указанное когнитивное расстройство представляет собой синдром дефицита внимания и гиперактивности (СДВГ).
Один из аспектов настоящего изобретения представляет собой способ лечения вызванного стрессом или связанного со стрессом когнитивного расстройства. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения вызванного стрессом или связанного со стрессом когнитивного расстройства.
Один из аспектов настоящего изобретения представляет собой способ лечения расстройства настроения. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения расстройства настроения. В одном из вариантов реализации указанное расстройство настроения выбрано из группы, состоящей из депрессии, послеродовой депрессии, дистимии и биполярного расстройства. В одном из вариантов реализации указанное расстройство настроения представляет собой депрессию. В одном из вариантов реализации указанное расстройство настроения представляет собой дистимию.
Один из аспектов настоящего изобретения представляет собой способ лечения вызванного стрессом или связанного со стрессом расстройства настроения. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения вызванного стрессом или связанного со стрессом расстройства настроения.
Один из аспектов настоящего изобретения представляет собой способ лечения тревожного расстройства. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения тревожного расстройства. В одном из вариантов реализации указанное тревожное расстройство выбрано из группы, состоящей из генерализованного тревожного расстройства, панического расстройства, панического расстройства в сочетании с агорафобией, агорафобии, социального тревожного расстройства, обсессивно-компульсивного расстройства и посттравматического стрессового расстройства. В одном из вариантов реализации указанное тревожное расстройство представляет собой генерализованное тревожное расстройство. В одном из вариантов реализации указанное тревожное расстройство представляет собой посттравматическое стрессовое расстройство.
Один из аспектов настоящего изобретения представляет собой способ лечения вызванной стрессом или связанной со стрессом тревоги. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения вызванной стрессом или связанной со стрессом тревоги.
Один из аспектов настоящего изобретения представляет собой способ усиления мышечной деятельности. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением усиления мышечной деятельности. В одном из вариантов реализации мышечная деятельность выбрана из группы, состоящей из силы, скорости и выносливости.
Один из аспектов настоящего изобретения представляет собой способ лечения мышечного или нервно-мышечного заболевания. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения мышечного или нервно-мышечного заболевания. В одном из вариантов реализации указанное мышечное или нервно-мышечное заболевание представляет собой миопатию. В одном из вариантов реализации указанное мышечное или нервно-мышечное заболевание представляет собой мышечную дистрофию. В одном из вариантов реализации указанное мышечное или нервно-мышечное заболевание представляет собой мышечную дистрофию Дюшенна.
Один из аспектов настоящего изобретения представляет собой способ способствования росту нейритов. Указанный способ включает этап приведения нервной клетки в контакт с эффективным количеством уролитина или его предшественника с обеспечением способствования росту нейритов. В одном из вариантов реализации указанное приведение в контакт включает введение нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением способствования росту нейритов.
Следующие варианты реализации могут относиться к каждому описанному аспекту и варианту реализации настоящего изобретения, и в соответствующих случаях друг к другу.
В одном из вариантов реализации уролитин или его предшественник представляет собой выделенный уролитин.
В одном из вариантов реализации уролитин или его предшественник представляет собой выделенный предшественник уролитина.
В одном из вариантов реализации уролитин выбран из группы, состоящей из уролитина А, уролитина В, уролитина С, уролитина D, а также их метаболитов, включая в качестве примера их глюкуронидированные, метилированные и сульфатированные формы, и комбинаций данных уролитинов.
В одном из вариантов реализации уролитин или его предшественник вводят в виде натурального пищевого продукта, выбранного из группы, состоящей из ягод, винограда, граната, плодов шиповника и орехов.
В одном из вариантов реализации уролитин или его предшественник вводят в виде переработанного продукта питания, включая в качестве примера сок, концентрат или экстракт, на основе натурального пищевого продукта, выбранного из группы, состоящей из ягод, винограда, граната, плодов шиповника и орехов.
В одном из вариантов реализации уролитин или его предшественник вводят в виде сока, концентрата или экстракта граната.
В одном из вариантов реализации уролитин или его предшественник вводят в виде эллагитаннина.
В одном из вариантов реализации уролитин или его предшественник вводят в виде пуникалагина.
В одном из вариантов реализации уролитин или его предшественник вводят в виде эллаговой кислоты.
В одном из вариантов реализации уролитин или его предшественник вводят в виде уролитина.
В одном из вариантов реализации уролитин или его предшественник вводят перорально.
В одном из вариантов реализации уролитин или его предшественник вводят парентерально.
В одном из вариантов реализации уролитин или его предшественник вводят по меньшей мере еженедельно. В различных вариантах реализации уролитин или его предшественник вводят 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27 или 28 раз еженедельно.
В одном из вариантов реализации уролитин или его предшественник вводят по меньшей мере ежедневно. В различных вариантах реализации уролитин или его предшественник вводят 1, 2, 3, 4, 5, 6, 7 или 8 раз ежедневно.
В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 0,1-150 миллиграмм (мг) уролитина на килограмм (кг) массы тела. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 2-120 мг уролитина на кг массы тела. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 4-90 мг уролитина на кг массы тела. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 8-30 мг уролитина на кг массы тела.
В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения по меньшей мере 0,001 микромолярного (мкМ) пикового уровня в сыворотке. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 0,01 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 0,1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 10 мкМ.
В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения по меньшей мере 0,001 микромолярного (мкМ) долговременного уровня в сыворотке. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 0,01 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 0,1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 10 мкМ.
В одном из вариантов реализации субъект не получает уролитин или его предшественник для лечения другого состояния, требующего введения уролитина или его предшественника, или метаболита, выбранного из группы, состоящей из атеросклероза, тромбоза, рака, нежелательного ангиогенеза, инфекции и воспаления.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фиг. 1 изображены структурные формулы уролитина A (UA), эллаговой кислоты (ЕА), теллимаграндина (TL), пуникалагина (РА) и пуникалина (РВ).
На Фиг. 2 изображена эллаговая кислота (ЕА) и ее метаболиты, уролитин D (UD), уролитин С (UC), уролитин A (UA) и уролитин В (UB), образуемые микрофлорой кишечника у животных, включая людей.
Фиг. 3 представляет собой пару гистограмм, изображающих уровни экспрессии генов митохондрий в ответ на указанные концентрации эллаговой кислоты (верхнее изображение) и уролитина А (нижнее изображение).
Фиг. 4 представляет собой гистограмму, изображающую активность цитратсинтазы (CS), измеренную in vitro в присутствии указанных концентраций пуникалагина, эллаговой кислоты, уролитина А или отрицательного контроля.
Фиг. 5А представляет собой коллаж иммуноблотов (IB), изображающий влияние эллаговой кислоты (ЕА) и уролитина A (UA) в указанных концентрациях на уровни АМФ-активируемой протеинкиназы (АМРК) и активированной фосфорилированной АМРК (Р-АМРК). Р-АМРК: фосфорилированная АМРК. Контроль: отрицательный контроль; RSV: положительный контроль ресвератролом.
Фиг. 5В представляет собой гистограмму, изображающую денситометрический анализ полос на Фиг. 5А, демонстрирующий относительный уровень активированной Р-АМРК после обработок по сравнению с клетками, обработанными контролем.
Фиг. 6 представляет собой гистограмму, изображающую общие количества клеток для культур клеток PC-12 после обработки 0,5 мкМ указанных соединений. РА, пуникалагин; РВ, пуникалин; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг.7 представляет собой гистограмму, изображающую средний рост нейритов (мкм) в клетках PC-12 после обработки 0,5 мкМ указанных соединений. Рост выражен на клетку. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; РА, пуникалагин; РВ, пуникалин; UA, уролитин А; ЕА, эллаговая кислота; Т1, теллимаграндин.
Фиг. 8 представляет собой гистограмму, изображающую процент клеток PC-12, демонстрирующих обширный рост нейритов (>20 мкм) после обработки 0,5 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; РА, пуникалагин; РВ, пуникалин; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг. 9 представляет собой гистограмму, изображающую среднее образование отростков в клетках PC-12 после обработки 0,5 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; РА, пуникалагин; РВ, пуникалин; UA, уролитин А; ЕА, эллаговая кислота; Т1, теллимаграндин.
Фиг. 10 представляет собой гистограмму, изображающую средний рост на клетку первичных дофаминергических тирозингидроксилаза (ТН)-положительных нейронов после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Т1, теллимаграндин.
Фиг. 11 представляет собой гистограмму, изображающую процент первичных дофаминергических ТН-положительных нейронов, демонстрирующих обширный рост нейритов (>20 мкм) после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг. 12 представляет собой гистограмму, изображающую среднее количество отростков, образованных в первичных дофаминергических ТН-положительных нейронах после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг. 13 представляет собой гистограмму, изображающую максимальную длину отростков в первичных дофаминергических ТН-положительных нейронах после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг. 14 представляет собой гистограмму, изображающую среднее количество ответвлений для одного первичного дофаминергического ТН-положительного нейрона после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг.15 представляет собой гистограмму, изображающую среднее количество дендритов для одного первичного дофаминергического ТН-положительного нейрона после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг. 16 представляет собой гистограмму, изображающую среднюю длину дендритов для одного первичного дофаминергического ТН-положительного нейрона после обработки 0,1 мкМ указанных соединений. SP, SP600125; дбцАМФ, дибутирильный циклический АМФ; UA, уролитин А; ЕА, эллаговая кислота; Тl, теллимаграндин.
Фиг. 17 представляет собой три серии гистограмм, изображающих влияние лечения уролитином А, пуникалагином и экстрактом граната (ЭГ) лечение на появление ожирения у мышей, получавших рацион питания с высоким содержанием жиров (HFD). Уролитин А вводили в виде добавки к пище; ЭГ и пуникалагин вводили через желудочный зонд. (А) Наблюдение за массой тела, выраженное в виде увеличения процента по сравнению с исходной массой тела. (В) Процент жировой массы, измеренный путем магнитно-резонансной томографии (EchoMRI) после 5 недель лечения. (С) Процент безжировой массы, измеренный путем EchoMRI после 5 недель лечения. Состав группы: контроль HFD (добавка к пище): n=10; контроль HFD (желудочный зонд): n=10; HFD плюс уролитин А (добавка к пище): n=9; HFD плюс пуникалагин (желудочный зонд): n=8; HFD плюс ЭГ (желудочный зонд): n=7. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента). Для изображений А результаты анализировали путем двухфакторного дисперсионного анализа (ANOVA). Значения р указаны.
Фиг. 18 представляет собой две пары гистограмм, изображающих влияние эллаговой кислоты и уролитина А на безжировую массу и жировую массу у мышей, получавших стандартный кормовой рацион питания. (А) Процент безжировой массы (мышца), измеренный путем EchoMRI после 2 недель лечения. (В) Процент жировой массы (мышца), измеренный путем EchoMRI после 2 недель лечения. Состав группы: кормовой рацион питания, контроль (добавка к пище): n=8; кормовой рацион питания плюс эллаговая кислота (добавка к пище): n=7; кормовой рацион питания плюс уролитин А (добавка к пище): n=7. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента).
Фиг. 19 представляет собой пару графиков и соответствующую пару гистограмм, изображающих влияние эллаговой кислоты и уролитина А на потребление кислорода у мышей, получавших стандартный кормовой рацион питания. (А) Наблюдение за потреблением кислорода в течение 20-часового периода. Закрашенные столбцы соответствуют темной фазе (с 7 вечера до 7 утра). Остальные соответствуют световой фазе. (В) Потребление кислорода представлено в виде площади под кривой (ППК). Состав группы: кормовой рацион питания, контроль (добавка к пище): n=8; кормовой рацион питания плюс эллаговая кислота (добавка к пище): n=7; кормовой рацион питания плюс уролитин А (добавка к пище): n=7. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента). Для изображений А результаты анализировали путем двухфакторного ANOVA. Значение р указано (кормовой рацион питания, контроль по сравнению с кормовым рационом питания плюс лечение).
Фиг. 20 представляет собой серию графиков и соответствующую серию гистограмм, изображающих влияние уролитина А, пуникалагина и экстракта граната (ЭГ) на потребление кислорода у мышей, получавших рацион питания с высоким содержанием жиров (HFD). (А) Наблюдение за потреблением кислорода в течение 20-часового периода. Закрашенные столбцы соответствуют темной фазе (с 7 вечера до 7 утра). Остальные соответствуют световой фазе. (В) Потребление кислорода представлено в виде площади под кривой (ППК). Состав группы: контроль HFD (добавка к пище): n=10; контроль HFD (желудочный зонд): n=10; HFD плюс уролитин А (добавка к пище): n=9; HFD плюс пуникалагин (желудочный зонд): n=8; HFD плюс ЭГ (желудочный зонд): n=7. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента). Для изображений А результаты анализировали путем двухфакторного ANOVA.
Фиг. 21 представляет собой пару графиков и соответствующую пару гистограмм, изображающих влияние эллаговой кислоты и уролитина А на дыхательный коэффициент (RER) у мышей, получавших стандартный кормовой рацион питания. (А) Наблюдение за RER в течение 20-часового периода. Закрашенные столбцы соответствуют темной фазе (с 7 вечера до 7 утра). Остальные соответствуют световой фазе. (В) RER представлен в виде среднего RER. Состав группы: кормовой рацион питания, контроль (добавка к пище): n=8; кормовой рацион питания плюс эллаговая кислота (добавка к пище): n=7; кормовой рацион питания плюс уролитин А (добавка к пище): n=7. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента). Для изображений А результаты анализировали путем двухфакторного ANOVA. Значение р указано (кормовой рацион питания, контроль по сравнению с кормовым рационом питания плюс лечение).
Фиг. 22 представляет собой серию графиков и соответствующую серию гистограмм, изображающих влияние уролитина А, пуникалагина и экстракта граната (ЭГ) на дыхательный коэффициент (RER) у мышей, получавших рацион питания с высоким содержанием жиров (HFD). (А) Наблюдение за RER в течение 20-часового периода. (В) RER представлен в виде среднего RER. Состав группы: контроль HFD (добавка к пище): n=10; HFD плюс уролитин А (добавка к пище): n=9; HFD плюс пуникалагин (добавка к пище): n=10; HFD плюс ЭГ (добавка к пище): n=10. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента). Для изображений А результаты анализировали путем двухфакторного ANOVA.
Фиг. 23 представляет собой две серии графиков, изображающих влияние уролитина А, пуникалагина и экстракта граната (ЭГ) на триглицериды и свободные жирные кислоты у мышей, получавших рацион питания с высоким содержанием жиров (HFD). (А) Уровни триглицеридов в плазме крови у мышей, получавших HFD, которых лечили в течение 14 недель. (В) Уровни свободных жирных кислот в плазме крови у мышей, получавших HFD, которых лечили в течение 14 недель. Состав группы: контроль HFD (добавка к пище): n=10; контроль HFD (желудочный зонд): n=10; HFD плюс уролитин А (добавка к пище): n=9; HFD плюс пуникалагин (желудочный зонд): n=8; HFD плюс ЭГ (желудочный зонд): n=7. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента).
Фиг. 24 представляет собой серию графиков, изображающих влияние уролитина А, эллаговой кислоты и пуникалагина на гликемию у мышей, получавших рацион питания с высоким содержанием жиров (HFD). (А) Проба на толерантность к глюкозе у мышей, получавших HFD, которых лечили добавкой к пище с уролитином А в течение 10 недель. (В) Проба на толерантность к глюкозе у мышей, получавших HFD, которых лечили добавкой к пище с эллаговой кислотой в течение 10 недель. (С) Проба на толерантность к глюкозе у мышей, получавших HFD, которых лечили добавкой к пище с пуникалагином в течение 10 недель. Состав группы: контроль HFD (добавка к пище): n=10; HFD плюс уролитин А (добавка к пище): n=9; HFD плюс пуникалагин (добавка к пище): n=10. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента).
Фиг. 25 представляет собой линейный график и гистограмму, изображающую влияние уролитина A (UA) на основное и разобщенное дыхание (потребление кислорода) у взрослой (10-дневной) нематоды С. elegans. (А) Основное и разобщенное дыхание (FCCP) у 10-дневных контрольных червей, которых обрабатывали 0,1% ДМСО, и 10-дневных червей, которых обрабатывали 30 мкМ уролитином А в 0,1% ДМСО. (В) Типичная площадь под кривой (ППК) разобщенного (FCCP) дыхания у 10-дневных контрольных червей, которых обрабатывали носителем (0,1% ДМСО) или 30 мкМ уролитином А в 0,1% ДМСО. Результаты выражены в виде среднего значения ± SEM. * р<0,05 (t-критерий Стьюдента). OCR, скорость потребления кислорода.
Фиг. 26 представляет собой гистограмму, изображающую влияние уролитина А на митохондрии в мышце С. elegans. Трансгенный штамм С. elegans SJ4103 демонстрирует флуоресценцию вследствие мышце-специфичной экспрессии зеленого флуоресцентного белка (GFP), нацеленного на мембрану митохондрий. Присутствие митохондрий в мышце С. elegans показано увеличением флуоресценции. Результаты выражены в виде среднего значения ± SEM. * р=0,0014 (t-критерий Стьюдента).
Фиг. 27 представляет собой гистограмму, изображающую подвижность мышей, подвергнутых хроническому стрессу, с лечением экстрактом граната или без него.
Фиг. 28 представляет собой гистограмму, изображающую степень ответного «замирания» у мышей в среде, вызывающей тревогу, с лечением экстрактом граната или без него.
Фиг. 29 представляет собой гистограмму, изображающую влияние введения экстракта граната у мышей на степень вызванного тревогой подавления подъема на задние лапы.
Фиг. 30 представляет собой гистограмму, изображающую влияние введения экстракта граната на степень вызванного тревогой подавления у мышей ухода за собой.
Фиг. 31 представляет собой линейный график, изображающий исчезновение памяти на конкретную неблагоприятную среду при повторном воздействии данной среды в отсутствии неблагоприятного эффекта. Данные представлены для мышей, которые испытали стресс в начале жизни, нормально поднимающихся на задние лапы контрольных мышей и мышей, которые испытали стресс в начале жизни, но которых лечат эллагитаннином пуникалагином. Замирание (%) выражено в виде процента времени замирания во время первоначального воздействия среды.
Фиг. 32 представляет собой график, изображающий влияние хронического стресса у мышей на эффективное обучение в водном лабиринте Морриса.
Фиг. 33 представляет собой гистограмму, изображающую влияние введения экстракта граната у подверженных хроническому стрессу мышей на характеристики обучения в водном лабиринте Морриса.
Фиг. 34 представляет собой график, изображающий суммарное расстояние от скрытой платформы для нескольких исследований во время фазы обучения в водном лабиринте Морриса, измерение когнитивного обучения. Данные представлены для мышей, которые испытали стресс в начале жизни, нормально поднимающихся на задние лапы контрольных мышей и мышей, которые испытали стресс в начале жизни, но которых лечат эллагитаннином пуникалагином. Расстояние до платформы представляет собой сумму расстояний между мышью и скрытой платформой для всех измеренных интервалов (25 интервалов/сек) во время периода наблюдения (60 сек).
Фиг. 35 представляет собой гистограмму, изображающую память старых крыс в тесте социального узнавания при лечении либо экстрактом граната 1108, либо контролем (Ctrl).
Фиг. 36 представляет собой гистограмму, изображающую результаты водного лабиринта Морриса для старых крыс, которых лечили экстрактом граната 1108 или контролем (Ctrl).
Фиг. 37 представляет собой гистограмму, изображающую процент правильных изменений в Y-лабиринте для модели болезни Альцгеймера 5XFAD у мышей, как получавших лечение, так и не получавших лечение, а также нормальных контрольных мышей. Значимость: **р<0,01, *р<0,05, однофакторный ANOVA.
Фиг. 38 представляет собой гистограмму, изображающую результаты водного лабиринта Морриса для трансгенных мышей, моделирующих болезнь Альцгеймера (hAPP-Tg), получавших лечение экстрактами 31008, 61109, 71109, полученными из граната, или контролем (носитель). Также представлены результаты для мышей дикого типа (не-Tg), получавших лечение контролем (носитель).
Фиг. 39 представляет собой гистограмму, изображающую результаты теста с темно-светлой камерой для мышей, которые испытали стресс в начале жизни, по сравнению с нормально поднимающимися на задние лапы контрольными мышами и мышами, испытавшими стресс в начале жизни и которых лечили эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM. Значимость: *р<0,05, (t-критерий Стьюдента).
Фиг. 40 представляет собой гистограмму, изображающую результаты теста с приподнятым О-лабиринтом для мышей, которые испытали стресс в начале жизни, по сравнению с нормально поднимающимися на задние лапы контрольными мышами и мышами, испытавшими стресс в начале жизни и которых лечили эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM. Значимость: *р<0,05, (t-критерий Стьюдента).
Фиг. 41 представляет собой гистограмму, изображающую результаты теста принудительного плавания для мышей, которые испытали стресс в начале жизни, по сравнению с нормально поднимающимися на задние лапы контрольными мышами и мышами, испытавшими стресс в начале жизни и которых лечили эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM. Значимость: *р<0,05, **р<0,01 (t-критерий Стьюдента).
Фиг. 42 представляет собой гистограмму, изображающую результаты обучения в модели контекстуальной выработки условного рефлекса страха (contextual fear conditioning paradigm) во время первого слабого удара, происходящего на 4 минуте. Результаты представлены для мышей, которые испытали стресс в начале жизни, по сравнению с нормально поднимающимися на задние лапы контрольными мышами и мышами, которые испытали стресс в начале жизни и которых лечили эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM.
Фиг. 43 представляет собой гистограмму, изображающую исчезновение памяти на конкретную неблагоприятную среду при повторном воздействии данной среды в отсутствии неблагоприятного эффекта. Данные представлены для мышей, которые испытали стресс в начале жизни, нормально поднимающихся на задние лапы неподверженных стрессу контрольных мышей и мышей, которые испытали стресс в начале жизни и прошли лечение эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM. Значимость: *р<0,05, #р=0,05 (t-критерий Стьюдента). Нормальных неподверженных стрессу животных сравнивают с животными, которые испытали стресс в начале жизни (т.е. отделение от матери). Получающих лечение пуникалагином животных, которые испытали стресс в начале жизни, сравнивают с не получающими лечение животными, которые испытали стресс в начале жизни.
Фиг. 44 представляет собой линейный график, изображающий уровень усвоения двигательного навыка, измеренный по задержке в секундах перед падением с вращающегося стержня. Данные представлены для мышей, которые испытали стресс в начале жизни, нормально поднимающихся на задние лапы контрольных мышей и мышей, которые испытали стресс в начале жизни и которых лечили эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM.
Фиг. 45 представляет собой график, изображающий задержку спасения в секундах из водного лабиринта Морриса во время фазы обучения, измерение когнитивного обучения. Данные представлены для мышей, которые испытали стресс в начале жизни, нормально поднимающихся на задние лапы контрольных мышей и мышей, которые испытали стресс в начале жизни и которых лечили эллагитаннином пуникалагином. Результаты выражены в виде среднего значения ± SEM. Значимость: * р<0,05 (t-критерий Стьюдента).
Фиг. 46 представляет собой гистограмму, изображающую влияние соединений, полученных из граната, на узнавание среды у нормальных мышей, либо не получавших лечение, либо получавших лечение пуникалагином или уролитином А. Результаты выражены в виде среднего значения ± SEM. Значимость: *р<0,05 (t-критерий Стьюдента).
Фиг. 47 представляет собой гистограмму, изображающую влияние соединений, полученных из граната, на сохранение памяти на конкретную среду у нормальных мышей, либо не получавших лечение, либо получавших лечение пуникалагином или уролитином А. Результаты выражены в виде среднего значения ± SEM. Значимость: данные анализировали с использованием либо однофакторного ANOVA, либо ANOVA с повторными измерениями, с последующим использованием апостериорного критерия множественного сравнения Фишера LSD (наименьшая значимая разность). *р<0,05.
Фиг. 48 представляет собой линейный график, демонстрирующий мышечную деятельность и двигательные навыки, измеренные по задержке в секундах перед падением с вращающегося стержня. Данные представлены для нормально поднимающихся на задние лапы не получавших лечение контрольных мышей и мышей, которых лечили эллагитаннином пуникалагином. Значимость: * р<0,05 по анализу ANOVA.
Фиг. 49 представляет собой линейный график, демонстрирующий уровень мышечной деятельности и выносливости, измеренный по способности мыши бегать на беговой дорожке с повышенными скоростями. Данные представлены для нормально поднимающихся на задние лапы не получавших лечение контрольных мышей и мышей, которых лечили уролитином А. Значимость: *р<0,05, **р<0,01 (t-критерий Стьюдента).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В биологии и психологии термин «стресс» относится к последствию неспособности человека или другого животного надлежащим образом реагировать на физиологические, эмоциональные или физические угрозы, независимо от того, являются они реальными или воображаемыми. Термин «стресс» был впервые использован в биологическом контексте эндокринологом Гансом Селье в 1930-х годах. Позже он расширил и популяризовал данное понятие таким образом, что оно стало включать неадекватную физиологическую реакцию на какое-либо требование. Он охватывает широкий диапазон явлений от легкого раздражения до резкой дисфункции, которая может вызывать сильное ухудшение здоровья.
Все данные психобиологические особенности стресса могут представлять собой проявления окислительного стресса, дисбаланса между выработкой и проявлением активных форм кислорода, и способностью биологической системы легко нейтрализовывать реакционноспособные промежуточные соединения или устранять полученное повреждение. Нарушения нормального состояния окисления-восстановления тканей могут вызывать токсические эффекты за счет выработки пероксидов и свободных радикалов, которые повреждают все компоненты клетки, включая белки, липиды и ДНК. Некоторые реакционноспособные окислительные соединения могут даже выступать в качестве мессенджеров за счет явления, называемого «окислительно-восстановительной передачей сигнала».
У людей окислительный стресс вовлечен во многие заболевания. Примеры включают атеросклероз, болезнь Паркинсона, сердечную недостаточность, инфаркт миокарда, болезнь Альцгеймера, шизофрению, биполярное расстройство, синдром ломкой Х-хромосомы и синдром хронической усталости.
Одним из источников реакционноспособного кислорода в нормальных условиях у людей является «утечка» активного кислорода из митохондрий во время окислительного фосфорилирования.
Другие ферменты, способные образовывать супероксид (О2-), представляют собой ксантиноксидазу, НАДФН-оксидазы и цитохромы Р450. Пероксид водорода, другой сильный окислитель, вырабатывается широким спектром ферментов, включая несколько оксидаз. Активные формы кислорода играют важную роль в передаче сигнала в клетке, процессе, называемом окислительно-восстановительной передачей сигнала. Таким образом, для поддержания должного клеточного гомеостаза должен соблюдаться баланс между выработкой и потреблением реакционноспособного кислорода.
Наиболее изученными клеточными антиоксидантами являются ферменты супероксиддисмутаза (СОД), каталаза и глутатионпероксидаза. Менее хорошо изученные ферментные антиоксиданты включают пероксиредоксины и недавно обнаруженный сульфиредоксин. Другие ферменты, обладающие антиоксидантными свойствами (хотя данная роль не является основной), включают параоксоназу, глутатион-S-трансферазы и альдегиддегидрогеназы.
Окислительный стресс вносит вклад в повреждение тканей после облучения и гипероксии. Существует предположение, что он играет важную роль при нейродегенеративных заболеваниях, включая болезнь Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз (ALS) и болезнь Хантингтона. Также считается, что окислительный стресс связан с некоторыми сердечнососудистыми заболеваниями, т.к. окисление липопротеина низкой плотности (ЛПНП) в эндотелии сосудов предшествует образованию бляшек. Окислительный стресс также играет роль в ишемическом каскаде вследствие реперфузионного повреждения кислородом после гипоксии. Данный каскад включает как инсульты, так и сердечные приступы. Окислительный стресс также вовлечен в синдром хронической усталости.
Авторы настоящего изобретения неожиданно обнаружили, что некоторые соединения, полученные из эллагитаннинов, полезны в лечении и предотвращении физиологических и психологических проявлений стресса, включая окислительный стресс. Не являясь связанными рамками какого-либо конкретного механизма действия, считается, что указанные соединения оказывают полезные эффекты в отношении митохондрий, стимулируя и восстанавливая ключевые функции митохондрий и противодействуя вызванной стрессом дисфункции митохондрий. Было обнаружено, что эти же соединения согласно настоящему изобретению полезны в лечении и предотвращении любого из множества состояний, заболеваний и нарушений, связанных с дисфункцией митохондрий, включая, без ограничения, нейродегенеративные заболевания и когнитивные расстройства, нарушения метаболизма, включая резистентность к инсулину, расстройства настроения и тревожные расстройства.
Эллагитаннины (ETs) представляют собой полифенолы, входящие в группу так называемых «гидролизуемых таннинов», в которых гексагидроксидифеновая кислота образует сложные диэфиры с сахарами (чаще всего β-D-глюкозой). ЕТ могут встречаться в виде сложных полимеров, достигающих молекулярной массы до 4000 и выше. Данные полимеры могут быть гидролизованы кислотами или основаниями с получением эллаговой кислоты (ЕА), которая может быть опосредованно использована для количественного определения ETs. ЕА в свою очередь является источником дополнительных продуктов метаболизма, включая уролитины.
Многие виды растений, содержащие эллагитаннины, использовали для лечения заболеваний, в частности, в Азии (Okuda et al., 2009). Они включают в том числе Репешок волосистый (агримониин) (Agrimonia pilosa, agrimoniin), Камелию японскую (камеллиатаннин A) (Camelia japonica, camelliatannin А), Дерен лекарственный (корнуссин A) (Cornus officinalis, comussin А), Герань Тунберга (гераниин) (Geranium thunbergii, geraniin), Гравилат японский (гемин-А) (Geum japonicum, gemin-A), Ликвидамбар формозский (казуариктин) (Liquidambar formosana, casuarictin), Маллотус японский (маллотузиновая кислота) (Mallotus japonicas, mallotusinic acid), Энотеру красночашелистную (оенотеин В) (Oenothera erythrosepala, oenothein В), гранат обыкновенный (гранат) (гранатин В) (Punica granatum, granatin В), Шиповник морщинистый (ругосин) (Rosa rugosa, rugosin) и Терминалию хебула (хебулиновая кислота) (Terminalia chebula, chebulinic acid). Основные виды применения данных лекарственных растений были связаны с их антиоксидантной, противодиарейной, противомикробной и иммуномодулирующей активностью.
Эллагитаннины также присутствуют в значительных количествах во многих ягодах, включая клубнику, обыкновенную и ежевикообразную малину (Zafrilla et al., 2001), чернику и ежевику. Эллагитаннины также были обнаружены в яблоках, вишне, морошке, клюкве, смородине, винограде, лайме, манго, ананасе, гранате, черносливе, ревене. Serrano et al. (2009) Mol Nutr Food Res. 53:S310-29. Эллагитаннин рубусуавиин С (rubusuaviin С) может быть выделен из листьев китайского сладкого чая Rubus suavissimus S. Lee. Эллагитаннины также были идентифицированы в существенных количествах в орехах, включая грецкие орехи (Fukuda et al., 2003), фисташки, орехи кешью, каштаны, желуди дуба (Cantos et al., 2003), пекан (Villarreal-Lozoya et al., 2007) и арахис.
Они также в больших количествах присутствуют в гранате (Gil et al., 2000) и мускатном винограде (Lee and Talcott, 2002), и являются важными составляющими дерева, особенно дуба (Glabasnia and Hofmann, 2006). Эллагитаннины могут входить в состав продуктов питания, таких как вина и виски, за счет миграции из дерева в пищевую матрицу во время разных процессов созревания. Эллаговая кислота также была обнаружена в нескольких типах меда, и она была предложена в качестве цветочного маркера верескового меда (Ferreres et al., 1996). Свободная эллаговая кислота и различные гликозидные производные также присутствуют в данных продуктах питания, включая глюкозиды, рамнозиды, арабинозиды и соответствующие ацетилэфиры (Zafrilla et al., 2001).
Ряд исследований показал, что содержание эллагитаннинов в некоторых продуктах питания может быть достаточно высоким (Таблица 1). Например, стакан гранатового сока (200 мл) может обеспечить до 1 г эллагитаннинов и эллаговой кислоты в общей сложности, порция малины (100 г малины) примерно 300 мг, порция клубники 70 мг и четыре грецких ореха примерно 400 мг эллагитаннинов.
Типичные эллагитаннины в рационе питания включают пуникалагин граната, сангуиин-Н-6 (sanguiin-Н-6) клубники и малины, и педункулагин (pedunculagin) грецких орехов. Все данные соединения высвобождают эллаговую кислоту при гидролизе, хотя также могут быть получены другие метаболиты и они отличаются от индивидуальных эллагитаннинов (например, галлаговая и трет-галлаговая кислоты).

Эллагитаннины обладают огромной вариабельностью структур, образуя димерные и олигомерные производные. Они также имеют более широкую распространенность, чем галлотаннины. Дополнительные эллагитаннины и их описанные источники представлены в Таблице 2.
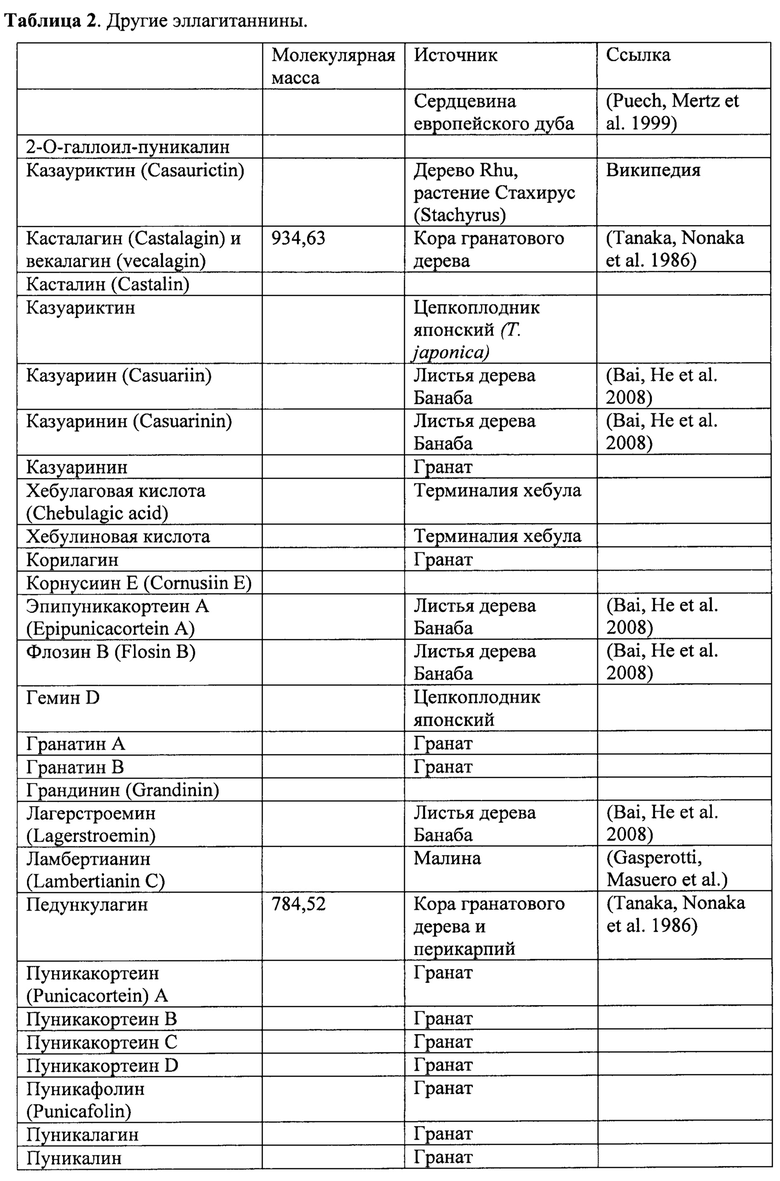
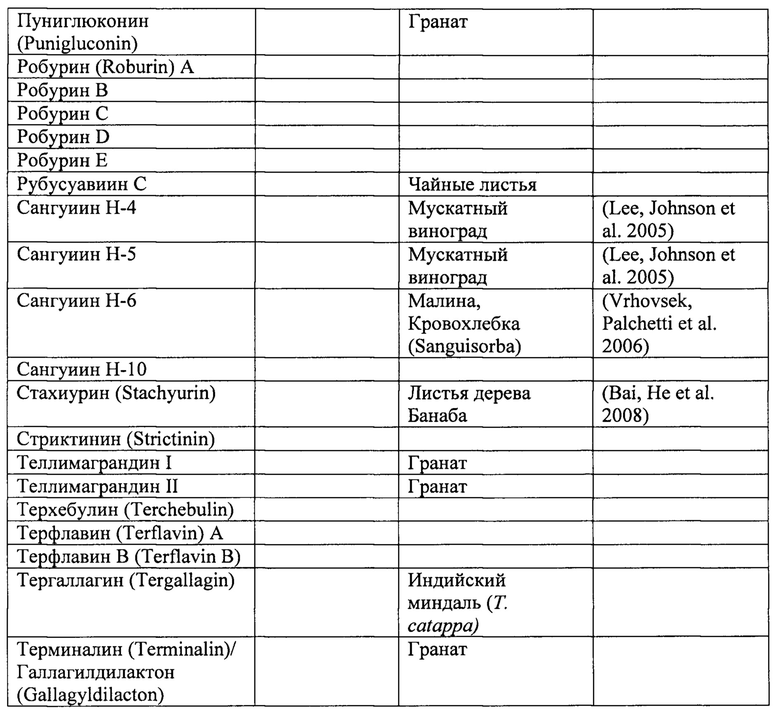
Многие потенциально активные эллагитаннины могут быть выделены из различных видов растений рода Терминалия (Terminalia). В частности, как пуникалагин, так и пуникалин были идентифицированы в нескольких видах Терминалии, включая, например, Индийский миндаль, Т. хебула (Retz), Т. многоплодную (Т. Myriocarpa) и Т. цитрина (Т. citrine). Пуникалагин также был выделен из Ладанника шалфеелистного (Cistus salvifolius) (средиземноморский кустарник) и Комбретума бархатнолистного (Combretum molle) (африканский кустарник).
Эллаговая кислота обычно встречается в относительно малых количествах в тканях растений. Считается, что эллаговая кислота происходит из эллагитаннинов, которые при распаде образуют гексагидроксидифеновую кислоту, которая самопроизвольно превращается в эллаговую кислоту. Некоторые дополнительные источники эллаговой кислоты представлены в Таблице 3.
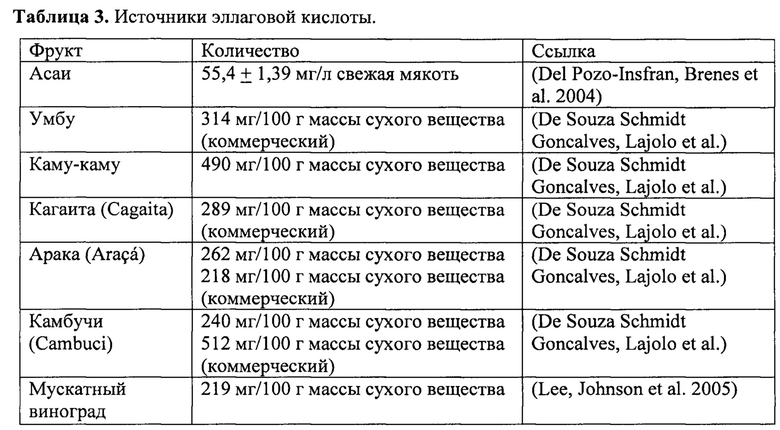
Плоды граната (Граната обыкновенного) представляют собой древние лекарственные пищевые продукты, которые использовали на протяжении веков в народной медицине. Их употребляют в свежем виде и в виде сока, который является превосходным источником эллагитаннинов и эллаговой кислоты. Эллагитаннины в кожуре плодов и соке граната включают пуникалин, пуникалагин, корилагин, казуаринин, терминалин/галлагилдилактон, педункулагин, теллимаграндин, гранатин А и гранатин В. Другие части гранатового растения содержат дополнительные эллагитаннины, включая пуникафолин, пуникакортеин А, пуникакортеин В, пуникакортеин С, пуникакортеин D и пуниглюконин. Коммерческие соки содержат эллагитаннины галлагилового типа, включая изомеры пуникалагина (1500-1900 мг/л), неопределенные гидролизуемые таннины (400-500 мг/л) и эллаговую кислоту, и ее гликозиды (120-260 мг/л) (Gil et al., 2000). Пуникалагины, эллагитаннины, в которых галлаговая и эллаговая кислоты соединены с молекулой глюкозы, в большом количестве присутствуют в кожуре граната. Изомеры пуникалагина и производные эллаговой кислоты не присутствуют в соке зерен, но во время промышленной переработки сока их экстрагируют из кожуры и мембраны, окружающей зерна, и в больших количествах вводят в сок.
Экстракты согласно настоящему изобретению могут быть получены сначала путем выжимания сока из фруктов, например, сок из граната может быть выжат с использованием стандартных промышленных способов выжимания сока, известных в данной области техники, которые могут включать выжимание сока из целых фруктов путем приложения давления к целым фруктам или сначала путем снятия кожуры с граната, а затем приложения давления к оставшемуся сырью, состоящему из зерен, мембранного сырья, которое удерживает зерна, и материалу кожуры, полученному в ходе процесса снятия кожуры. В качестве альтернативы, кожура, которая является богатым источником эллагитаннинов, в частности, пуникалагина может подвергаться процессу выжимания сока, который включает водную экстракцию. В альтернативных способах неводной экстракции можно использовать другие растворители, такие как этанол, ацетон или метанол в качестве примера.
Экстракт, как правило, представляет собой водный экстракт, который по существу может состоять из сока фруктов, возможно с добавлением дополнительного количества воды. Такие водные экстракты можно концентрировать, обогащать или конденсировать, например, стандартными способами, например, способами выпаривания при пониженном давлении и фильтрации. Примерами концентратов являются концентраты, которые являются концентрированными по меньшей мере в 2 раза, чаще по меньшей мере в 4 раза, например, по меньшей мере в 8 раз, по меньшей мере в 40 раз, по меньшей мере в 100 раз, по меньшей мере в 200 раз или по меньшей мере в 1000 раз.
Экстракты можно фракционировать с выделением в них одного или более активных компонентов, например, путем фильтрации по молекулярной массе или хроматографии на подходящем твердом носителе, таком как гель сефарозы (для эксклюзионной хроматографии) или ионообменной колонке с использованием ВЭЖХ на подходящим образом обработанном диоксиде кремния или оксиде алюминия, например, диоксиде кремния с покрытием ODS, или путем экстракции растворителем.
Исследования с имитацией пищеварения in vitro показали, что в целом эллагитаннины достаточно стабильны в физиологических условиях желудка. Кислые условия (HCl, рН 1,8-2,0) и ферменты желудка не гидролизуют исходные эллагитаннины с высвобождением свободной эллаговой кислоты (ЕА), и распада эллагитаннинов не наблюдали (Tomas-Barberan et al., 2009). Тогда как желудок представляется первым важным местом для абсорбции свободной ЕА, эллагитаннины не абсорбируются. Однако в физиологических условиях тонкого кишечника происходит высвобождение свободной ЕА из эллагитаннинов. Данный гидролиз, по-видимому, обусловлен условиями рН (рН от нейтрального до слабощелочного, 7,0-7,3), а не действием ферментов поджелудочной железы и солей желчных кислот (Larrosa et al., 2006).
Для оценки биодоступности и метаболизма ЕА и эллагитаннинов также использовали исследования на животных. Doyle и Griffiths (1980) сообщали о быстрой абсорбции и метаболизме ЕА у крыс. Данные авторы детектировали уролитин A (UA) и другой метаболит (вероятнее всего уролитин В (UB)) в кале и моче. Было продемонстрировано, что происхождением как UA, так и UB является микрофлора, т.к. ни один из них не был обнаружен у стерильных животных. Неизмененная ЕА не была детектирована в моче или кале. Данные уролитины в значительной степени абсорбируются и глюкуронидируются клетками кишечника. В этом случае метиловые эфиры не образуются, т.к. UA и UB не содержат орто-дигидроксильных групп в молекулах и, следовательно, не являются субстратами для катехол-О-метилтрансферазы (СОМТ). В случае UB дополнительный гидроксил может быть введен с помощью цитохрома Р450 и это увеличивает вероятность глюкуронирования, и усиливает экскрецию метаболита. Teel и Martin (1988) обнаружили, что как свободная ЕА, так и некоторые конъюгаты (сульфатный эфир-, глюкуронид- и глутатион-конъюгаты) были детектированы в моче, желчи и крови у мышей. Абсорбция 3Н-ЕА происходила в основном в течение двух часов после перорального введения. Уровни в крови, желчи и тканях были низкими, и абсорбированные соединения выводились с мочой. Больше половины вводимой 3Н-ЕА оставалось в желудочно-кишечном тракте через 24 часа.
Был оценен метаболизм различных пищевых производных ETs и ЕА у людей. В исследовании с участием сорока здоровых добровольцев, разделенных на четыре группы, вводили разные продукты питания, содержащие ЕТ, включая клубнику (250 г), малину обыкновенную (225 г), грецкие орехи (35 г) и выдержанное в дубовой бочке красное вино (300 мл). Клубника и малина обе содержат ЕТ сангуиин-Н-6; грецкие орехи содержат ЕТ педункулагин; и выдержанное в дубовой бочке вино содержит ЕТ вескалагин. После потребления собирали пять фракций мочи через 8, 16, 32, 40 и 56 часов. Ни ETs, ни ЕА не были детектированы в моче с использованием анализа ЖХ-МС/МС. Однако микробный метаболит 3,8-дигидрокси-6Н-дибензо[b,d]пиран-6-он (уролитин В), конъюгированный с глюкуроновой кислотой, был детектирован среди фракций, начиная с 32 часов до 56 часов, у всех субъектов независимо от потребленного продукта питания. В соответствии с полученными результатами производные уролитина В выводились независимо от потребленного ЕТ. Распространенным мономерным фрагментом в потребленных ETs являлась ЕА (m/z- при 301), что может означать, что данная субъединица, относящаяся к молекулам ЕТ, представляла собой критическую молекулу для образования производных уролитина В. Схожее метаболическое превращение в эллаговую кислоту и уролитин наблюдали для эллагитаннинов у людей, потребляющих гранатовый сок (Cerda, Espin et al. 2004; Cerda, Periago et al. 2005).
Одним из основных факторов, влияющих на метаболизм и биодоступность эллагитаннинов, является их микробное превращение с образованием серии производных уролитина (ФИГ. 2). Среди них наиболее хорошо изученными и известными являются уролитин А и В, но в тонком кишечнике промежуточные соединения с тремя и четырьмя гидроксилами также образуются, абсорбируются и выводятся с желчью после конъюгации с метиловыми эфирами и глюкуронидами (Espin et al., 2007). Эксперименты на животных показывают, что данные метаболиты начинают образовываться в тонком кишечнике, что указывает на то, что ответственными за это могут быть анаэробные бактерии. Метаболизм продолжается по желудочно-кишечному тракту, начиная с уролитинов D и С и заканчивая образованием уролитинов А и В. Различия в образовании данных метаболитов у людей-добровольцев показывают, что они могут образовываться за счет активности конкретных микроорганизмов, присутствующих в кишечнике.
В желудочно-кишечном тракте и в других тканях (главным образом в печени), ЕА и микробные метаболиты эллагитаннина далее метаболизируются ферментами либо I Фазы (гидроксилирование), либо II Фазы (метилирование, глюкуронирование и сульфатирование) с образованием более растворимых метаболитов, которые могут распределяться между тканями, а затем выводиться с мочой.
Таким образом, UB может гидроксилироваться с образованием UA, а он может гидроксилироваться далее с образованием тригидроксипроизводных.
Также образуются продукты II Фазы, и в разных тканях и в моче детектируют метиловые эфиры (продукты СОМТ), а также различные глюкуронидные конъюгаты. Сульфатные конъюгаты метаболитов эллагитаннина менее распространены у животных и людей, чем глюкуронидные конъюгаты. Данные конъюгаты сначала образуются в клетках кишечника, а затем метаболизируются в печени перед выведением с мочой или желчью.
Подводя итог, эллагитаннины, в целом, не абсорбируются в кишечнике. Напротив, они высвобождают ЕА в кишечнике, которая лишь плохо абсорбируется в желудке и тонком кишечнике. ЕА в значительной степени метаболизируется неидентифицированными бактериями в полости кишечника с образованием уролитинов. Микробный метаболизм начинается в тонком кишечнике и первые образованные метаболиты сохраняют четыре фенольных гидроксила (уролитин D, четыре гидроксильные группы), и данные вещества далее метаболизируются в кишечном тракте с удалением гидроксильных фрагментов, что приводит к уролитину С (три гидроксила), уролитину А (два гидроксила) и В (один гидроксил) в дистальных частях толстой кишки (ФИГ. 2). Абсорбированные метаболиты конъюгируются с глюкуроновой кислотой (одним или двумя звеньями) и/или метиловыми эфирами (когда присутствуют орто-дигидроксильные группы). Конъюгаты уролитина А и В являются основными метаболитами, детектируемыми в плазме крови и моче, хотя некоторые тригидроксипроизводные (гидроксил-UA) или ЕА-диметиловый эфир-глюкуронид также были детектированы в меньших количествах. Тетрагидроксиуролитины, тригидроксиуролитины и производные ЕА, в целом, не детектируются в периферийной плазме крови, но они абсорбируются в тонком кишечнике и переносятся в печень, где они далее метаболизируются и выводятся с желчью в тонкий кишечник, устанавливая кишечно-печеночную циркуляцию, ответственную за относительно долгую «жизнь» уролитинов в плазме крови и моче.
В дополнение к природным источникам пищевых продуктов, за последние двадцать лет появилось много работ по биосинтезу, выделению и биологической активности таннинов, особенно эллагитаннинов (например, Xie et al., 1995, Yoshida et al., 1982, 1984, 1985, 1986, 1989, 1990a/b, 1991a-d, 1992a/b, 1995, Nonaka et al., 1980, 1984, 1989a-c, 1990, Tanaka et al., 1986a/b, 1990, 1992a/b, 2001, Hatano et al., 1988, 1989, 1990a-c, 1991, 1995, Lin et al., 1990, Nishizawa et al., 1982, 1983, Haddock et al., 1982a/b, Kashiwada et al., 1992a/b, 1993, Kadota et al., 1990, Okuda et al., 1982a-e, 1983a/b, El-Mekkawy et al., Chemistry and Biology of Ellagitannins 154 1995, Tsai et al., 1992, Han et al., 1995, Chen et al., 1995, Morimoto et al., 1986a/b, Saijo et al., 1989). Доступ к чистым эллагитаннинам путем выделения из природных источников может быть обременительным и давать лишь относительно малые количества чистых натуральных продуктов. См., например, Okuda et al., (1982) Chem Pharm Bull. 30:4230-4233; Okuda et al. (1982) Chem Pharm Bull. 30:234-4236. Поэтому интересно отметить, что известны способы полного синтеза многих эллагитаннинов. См., например, Khanbabaee, К., Strategies for the synthesis of ellagitannins, In: Chemistry and Biology of Ellagitannins, Ed. S. Quideau, World Scientific Publishing, Singapore, 2009, pp. 152-202, включая приведенные там ссылки.
Антиоксидантная активность пищевых экстрактов, богатых эллагитаннинами, была определена с использованием различных анализов in vitro и широко сообщается о высокой активности клубники (Meyers et al., 2003, Aaby et al., 2005, 2007), малины (Liu et al., 2002, Beekwilder et al., 2005), морошки ( et al., 2001) и других ягод рода Рубус (Rubus) (Wada and Ou, 2002), граната (Gil et al., 2000) и грецких орехов (Anderson et al., 2001), и их эллагитаннинах. Эти продукты питания также занимают высокие позиции по сравнению с другими продуктами питания на основе растений.
et al., 2001) и других ягод рода Рубус (Rubus) (Wada and Ou, 2002), граната (Gil et al., 2000) и грецких орехов (Anderson et al., 2001), и их эллагитаннинах. Эти продукты питания также занимают высокие позиции по сравнению с другими продуктами питания на основе растений.
Меньше известно о влиянии потребления продуктов питания, богатых эллагитаннинами, на антиоксидантный статус in vivo. У пожилых женщин общая антиоксидантная способность сыворотки увеличивалась примерно на 10% в течение 4-часового периода после потребления 240 г клубники (Cao et al., 1998). Однократная доза стандартизированного экстракта граната (Mertens-Talcott et al., 2006) и длительное потребление гранатового сока (Rosenblat et al., 2006) также улучшали некоторые антиоксидантные параметры у людей-добровольцев. Однако ежедневное потребление грецких орехов в течение трех недель не оказывало влияния на антиоксидантный статус субъектов с метаболическим синдромом (Davis et al., 2007).
Рост раковых клеток зависит от баланса между пролиферацией и апоптозом. Нерегулируемая пролиферация клеток и подавление апоптоза являются ключевыми этапами в инициировании и прогрессировании рака. Имеется значительное количество доказательств того, что экстракты продуктов питания, богатых эллагитаннинами, уменьшают рост раковых клеток in vitro путем ингибирования пролиферации клеток, индуцирования апоптотической гибели клеток и модулирования кинетики клеточного цикла, и путей передачи сигнала.
Исследования in vitro, проведенные с использованием линий раковых клеток, показали, что клубника (Meyers et al., 2003, Olsson et al., 2004, Ramos et al., 2005, Wang et al., 2005, Wu et al., 2007), малина (Liu et al., 2002, Olsson et al., 2004, Wu et al., 2007), морошка (Wu et al., 2007) и плоды шиповника (Olsson et al., 2004) ингибируют пролиферацию клеток, индуцируют апоптоз и вызывают остановку клеточного цикла в клетках рака толстой кишки, печени, легкого, молочной железы или шейки матки человека. В данных исследованиях не оценивали вклад эллагитаннинов в активность экстрактов ягод. Однако недавнее исследование (Ross et al., 2007) позволяет предположить, что антипролиферативная активность малины связана преимущественно с эллагитаннинами.
Также существуют данные о том, что гранатовый сок и его эллагитаннины ингибируют пролиферацию, индуцируют апоптоз и подавляют передачу сигнала в клетке при воспалении в линиях клеток рака толстой кишки (Seeram et al., 2005, Adams et al., 2006, Larrosa et al., 2006). Подобным образом, полифенолы в кожице мускатного винограда ингибируют рост клеток рака толстой кишки и индуцируют апоптоз (Yi et al., 2005). Фракции, выделенные из красного мускатного винограда и богатые эллаговой кислотой, гликозидами эллаговой кислоты и эллагитаннинами, индуцируют апоптоз, уменьшают количество клеток и вызывают изменения кинетики клеточного цикла в клетках карциномы толстой кишки (Mertens-Talcott et al., 2006).
Сок плодов граната эффективен в отношении клеток рака предстательной железы in vitro, но не в отношении нормальных эпителиальных клеток предстательной железы. Лечение высокоагрессивных клеток рака предстательной железы человека экстрактом плодов граната приводило к ингибированию роста и жизнеспособности клеток, и индукции апоптоза (Malik et al., 2005, Malik and Mukhtar, 2006).
В соответствии с настоящим изобретением в настоящее время было обнаружено, что эллагитаннины и их метаболиты, включая эллаговую кислоту и особенно уролитины, неожиданно демонстрируют защитное и восстановительное действие в отношении митохондрий. Не являясь ограниченными рамками какого-либо конкретного механизма, считается, что различные типы стресса приводят к стрессовому повреждению митохондрий, что таким образом уменьшает их способность выполнять многочисленные функции, необходимые для общего функционирования клетки. Способы согласно настоящему изобретению подходят для лечения состояний, включающих стрессовое повреждение митохондрий; указанное повреждение может проявляться любым из ряда способов, включая, но не ограничиваясь им, митохондриальное заболевание.
Митохондрии являются «силовыми центрами» клеток. Данные органеллы с двойной мембраной играют критическую роль в выработке подавляющего большинства клеточной энергии (АТФ) через окислительное фосфорилирование. Митохондрии также необходимы для других ключевых метаболических функций, таких как β-окисление жирных кислот, катаболизм аминокислот, кетогенез и образование активных форм кислорода (АФК) с важными функциями передачи сигнала, и контроль гомеостаза кальция.
Матрикс митохондрий содержит ферментативный механизм β-окисления жирных кислот, в результате которого образуется ацетил-КоА из ацильных цепей, и восстановления эквивалентов в форме восстановленного никотинамидадениндинуклеотида (НАДН) и восстановленного флавинадениндинуклеотида (ФАДН2) в данном процессе. Ацетил-КоА служит «топливом» для цикла трикарбоновых кислот (ТСА), также известного как цикл лимонной кислоты или цикл Кребса, который также продуцирует НАДН и ФАДН2. Данные продукты отдают электроны электронтранспортной цепи (ETC), что приводит к созданию градиента протонов на внутренней мембране митохондрий. Рассеивание данного градиента за счет АТФ-синтазы митохондрий вырабатывает энергию в форме АТФ.
ETC состоит из 4 больших мультисубъединичных комплексов (комплексы с I по IV), которые переносят электроны, генерируемые циклом ТСА, к конечному акцептору, молекулярному кислороду (О2), образуя Н2О в комплексе IV. Перенос электронов сопровождается выделением больших количеств свободной энергии, большая часть которой используется для перемещения протонов (Н+) из матрикса в межмембранное пространство (протондвижущая сила); оставшаяся часть рассеивается в виде тепла. Энергия, содержащаяся в электрохимическом градиенте Н+, созданном ETC, затем объединяется с образованием АТФ по мере обратного притока Н+ в матрикс за счет АТФ-синтазы митохондрий. Таким образом, окислительное фосфорилирование происходит в результате переноса электронов, создания градиента протонов и последующего притока протонов, связанного с АТФ-синтазой митохондрий.
АФК также могут активировать разобщающие белки (UCPs), которые рассеивают градиент протонов без образования АТФ. UCPs считаются природными регуляторами данного процесса, реагирующими на и контролирующими образование АФК путем уменьшения образования большого градиента протонов. Кроме того, UCPs и разобщение дыхания вовлечены в многочисленные важные физиологические и патологические процессы, такие как адаптивный термогенез, регуляция окисления жирных кислот, участие в воспалении, предотвращение образования АФК, гомеостаз глюкозы, регуляция массы тела и старение.
Цитратсинтаза является начальным ферментом митохондриального цикла ТСА. Данный фермент катализирует реакцию между ацетил-коэнзимом А (Ацетил-КоА) и щавелевоуксусной кислотой с образованием лимонной кислоты. Активность данного фермента отражает как митохондриальный биогенез, так и митохондриальное окислительное фосфорилирование, т.к. его активность увеличивается пропорционально плотности митохондрий (количество митохондрий на клетку) и активности митохондриального дыхания. Следовательно, измерение цитратсинтазы обеспечивает общую оценку функционального состояния митохондрий, при этом более высокая активность указывает на повышенное окислительное фосфорилирование и синтез АТФ, а более низкая активность указывает на противоположное.
Для лучшего понимания лежащего в основе молекулярного механизма, приводящего к улучшению функции митохондрий, могут быть получены характеристики ключевых генов митохондрий (кодирующих митохондриальную и геномную ДНК), охватывающие окислительное фосфорилирование, цепные комплексы митохондрий, цикл ТСА, разобщающие белки, факторы транскрипции, кофакторы и белки, утилизирующие АФК.
Традиционное учение в биологии и медицине заключается в том, что митохондрии функционируют только как «фабрики по производству энергии» для клетки. Однако более 95% (2900 из 3000) генов, кодирующих белки митохондрий, вовлечены в другие функции, связанные со специализированными функциями дифференцированных клеток, в которых они находятся. Данные функции эволюционируют в ходе развития от эмбриона до взрослого и по мере роста, созревания и адаптации к послеродовой среде. Эти другие не связанные с АТФ функции тесно связаны с большинством основных метаболических путей, используемых клеткой для строительства, расщепления и рециркуляции молекулярных строительных блоков. Клетки даже не могут образовывать РНК и ДНК, необходимые им для роста и функционирования, без митохондрий. Строительными блоками РНК и ДНК являются пурины и пиримидины. Митохондрии содержат ферменты, лимитирующие скорость, для биосинтеза пиримидинов (дигидрооротатдегидрогеназа) и синтеза гема (синтетаза d-аминолевулиновой кислоты), необходимого для образования гемоглобина. В печени митохондрии приспособлены для нейтрализации аммиака в цикле мочевины. Митохондрии также необходимы для метаболизма холестерина, для синтеза эстрогена и тестостерона, метаболизма нейромедиаторов и для выработки и нейтрализации свободных радикалов. Митохондрии выполняют все эти функции в дополнение к окислению жиров, белков и углеводов, потребляемых с рационом питания.
Митохондриальные заболевания являются результатом либо наследственных, либо спонтанных мутаций в митохондриальной ДНК или ядерной ДНК, которые приводят к изменению функций белков или молекул РНК, которые обычно находятся в митохондриях. Однако проблемы с функцией митохондрий могут влиять только на некоторые ткани вследствие факторов, возникающих во время развития и роста, которые еще не полностью изучены. Даже при учете тканеспецифических изоформ белков митохондрий, трудно объяснить вариабельные модели пораженных систем органов при клинически наблюдаемых синдромах митохондриальных заболеваний.
Митохондриальные заболевания являются следствием «неисправностей» митохондрий, специализированных компартментов, присутствующих в каждой клетке организма, за исключением эритроцитов. Митохондрии ответственны за выработку более 90% энергии, необходимой организму для поддержания жизни и поддержания роста. Когда они выходят из строя, внутри клетки вырабатывается все меньше и меньше энергии. За этим следует повреждение клетки и даже гибель клетки. Если данный процесс повторяется по всему организму, целые системы начинают давать сбой и жизнь человека, у которого это происходит, подвергается большой опасности. Митохондриальные заболевания главным образом поражают детей, но возникновение у взрослых становится все более узнаваемым.
Заболевания митохондрий, по-видимому, вызывают наибольшее повреждение клеток головного мозга, сердца, печени, скелетных мышц, почек и эндокринной, и дыхательной систем.
Многие симптомы при митохондриальных нарушениях являются неспецифическими. Симптомы также могут демонстрировать эпизодическое течение с периодическими обострениями. Эпизодическое состояние мигрени, а также миалгии, желудочно-кишечные симптомы, шум в ушах, депрессия, хроническая усталость и диабет были упомянуты среди различных проявлений митохондриальных нарушений в обзорных статьях по митохондриальной медицине (Chinnery and Turnbull (1997) QJM 90:657-67; Finsterer (2004) Eur J Neurol. 11:163-86). У пациентов с митохондриальными нарушениями клиническая симптоматика, как правило, проявляется в периоды более высокой потребности в энергии, связанной с физиологическими стрессорами, такими как болезнь, голодание, чрезмерная физическая нагрузка и перепады температуры окружающей среды. Кроме того, психологические стрессоры также часто запускают симптоматику, предположительно из-за более высоких потребностей головного мозга в энергии, на которые пациент не может отвечать достаточной выработкой АТФ.
В зависимости от того, какие клетки поражены, симптомы могут включать потерю двигательного контроля, мышечную слабость и боль, желудочно-кишечные расстройства и трудности с глотанием, слабый рост, заболевание сердца, заболевание печени, диабет, дыхательные осложнения, судороги, проблемы со зрением/слухом, лактоцидоз, задержки в развитии и восприимчивость к инфекции.
Митохондриальные заболевания включают, без ограничения, болезнь Альперса; синдром Барта; дефекты бета-окисления; дефицит карнитина; дефицит карнитин-ацилкарнитина; синдром хронической прогрессирующей внешней офтальмоплегии; дефицит кофермента Q10; дефицит Комплекса I; дефицит Комплекса II; дефицит Комплекса III; дефицит Комплекса IV; дефицит Комплекса V; дефицит СРТ I; дефицит СРТ II; синдром дефицита креатина; дефицит цитохром-с-оксидазы; глутарацидурию II типа; синдром Кирнса-Сейра; лактоцидоз; дефицит длинноцепочечной ацил-КоА-дегидрогеназы (LCHAD); наследственную оптическую нейропатию Лебера; болезнь Лея; смертельную детскую кардиомиопатию; болезнь Люфта; дефицит среднецепочечной ацил-КоА-дегидрогеназы (MAD); митохондриальную цитопатию; истощение митохондриальной ДНК; митохондриальную энцефаломиопатию, лактоцидоз и инсульт-подобные симптомы; митохондриальную энцефалопатию; митохондриальную миопатию; синдром митохондриальной рецессивной атаксии; мышечные дистрофии, миоклоническую эпилепсию и болезнь разорванных красных волокон; мионейрогенную желудочно-кишечную энцефалопатию; невропатию, атаксию, пигментный ретинит и птоз; синдром Пирсона; мутации POLG; дефицит пируваткарбоксилазы; дефицит пируватдегидрогеназы; дефицит короткоцепочечной ацил-КоА-дегидрогеназы (SCHAD); и дефицит очень длинноцепочечной ацил-КоА-дегидрогеназы.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество экстракта граната: для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
В настоящем описании термин «продукт питания» относится к продукту, полученному из натурального пищевого продукта. Неограничивающие примеры продуктов питания включают соки, вина, концентраты, джемы, желе, консервы, пасты и экстракты. В настоящем описании термин «питательная добавка» относится к продукту, подходящему для потребления или другого введения главным образом из-за его свойств, способствующих укреплению здоровья, а не калорийности.
В настоящем описании термин «метаболический синдром» относится к комбинации нарушений, которые при одновременном возникновении увеличивают риск развития сердечнососудистого заболевания и диабета. Он поражает одного из пяти человек в Соединенных Штатах, и распространенность увеличивается с возрастом. Некоторые исследования продемонстрировали, что распространенность в Соединенных Штатах по оценкам составляет 25% населения. В соответствии с согласованным всемирным определением Международной федерации диабета (International Diabetes Foundation) (2006), метаболический синдром представляет собой центральное ожирение плюс любые два показателя из следующих:
- Повышенные триглицериды: >150 мг/дл (1,7 ммоль/л) или специальное лечение данной аномалии липидов;
- Пониженный холестерин липопротеинов высокой плотности (ЛПВП): <40 мг/дл (1,03 ммоль/л) у мужчин, <50 мг/дл (1,29 ммоль/л) у женщин или специальное лечение данной аномалии липидов;
- Повышенное артериальное давление: систолическое АД>130 или диастолическое АД>85 мм рт. ст., или лечение ранее диагностированной гипертонии; и
- Повышенная концентрация глюкозы в плазме крови натощак: (FPG)>100 мг/дл (5,6 ммоль/л) или ранее диагностированный диабет 2 типа.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество эллагитаннина: для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
В некоторых вариантах реализации в соответствии с этим и другими аспектами настоящего изобретения эллагитаннин выбран из группы, состоящей из 2-О-галлоил-пуникалина, казауриктина, касталагина и векалагина, касталина, казуариктина, казуариина, казуаринина, хебулаговой кислоты, хебулиновой кислоты, корилагина, корнусиина Е, эпипуникакортеина А, флозина В, гемина D, гранатина А, гранатина В, грандинина, лагерстроемина, ламбертианина С, педункулагина, пуникакортеина А, пуникакортеина В, пуникакортеина С, пуникакортеина, D, пуникафолина, пуникалагина, пуникалина, пуниглюконина, робурина А, робурина В, робурина С, робурина D, робурина Е, рубусуавиина С, сангуиина Н-4, сангуиина Н-5, сангуиина Н-6, сангуиина Н-10, стахиурина, стриктинина, теллимаграндина I, теллимаграндина II, терхебулина, терфлавина А, терфлавина В, тергаллагина и терминалина/галлагилдилактона. Конечно, дополнительные эллагитаннины также предусмотрены настоящим изобретением.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество пуникалагина: для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество эллаговой кислоты: для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
Один из аспектов настоящего изобретения представляет собой продукт питания или питательную добавку, содержащую эффективное количество уролитина: для лечения или предотвращения состояния, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечнососудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивного расстройства, расстройства настроения, стресса и тревожного расстройства; для контроля массы тела или для усиления мышечной деятельности или умственной деятельности.
В некоторых вариантах реализации в соответствии с этим и другими аспектами настоящего изобретения уролитин представляет собой уролитин А. В некоторых вариантах реализации в соответствии с этим и другими аспектами настоящего изобретения уролитин представляет собой уролитин В. В некоторых вариантах реализации в соответствии с этим и другими аспектами настоящего изобретения уролитин представляет собой уролитин С. В некоторых вариантах реализации в соответствии с этим и другими аспектами настоящего изобретения уролитин представляет собой уролитин D.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой ожирение.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой сниженную скорость метаболизма.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой метаболический синдром.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой сахарный диабет.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой сердечнососудистое заболевание.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой гиперлипидемию.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой нейродегенеративное заболевание.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой когнитивное расстройство.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой расстройство настроения.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой стресс.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации состояние представляет собой тревожное расстройство.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации продукт питания или питательная добавка предназначены для контроля массы тела.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации продукт питания или питательная добавка предназначены для усиления мышечной деятельности.
В соответствии с каждым из вышеприведенных аспектов в одном из вариантов реализации продукт питания или питательная добавка предназначены для усиления умственной деятельности.
Один из аспектов настоящего изобретения представляет собой способ усиления или поддержания функции митохондрий. Указанный способ включает этап приведения клеток в контакт с эффективным количеством уролитина или его предшественника с обеспечением усиления функции митохондрий.
Один из аспектов настоящего изобретения представляет собой способ лечения, предотвращения или контроля связанного с митохондриями заболевания или состояния, ассоциируемого с измененной функцией митохондрий или пониженной плотностью митохондрий. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения заболевания или состояния, ассоциируемого с измененной функцией митохондрий или пониженной плотностью митохондрий.
Один из аспектов настоящего изобретения представляет собой способ усиления скорости метаболизма. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением увеличения скорости метаболизма. Как описано в иных местах настоящего документа, предшественники уролитина могут включать, без ограничения, эллагитаннин, пуникалагин и эллаговую кислоту.
Один из аспектов настоящего изобретения представляет собой способ предотвращения или лечения метаболического синдрома. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением предотвращения или лечения метаболического синдрома.
Один из аспектов настоящего изобретения представляет собой способ предотвращения или лечения ожирения. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением предотвращения или лечения ожирения.
Один из аспектов настоящего изобретения представляет собой способ предотвращения или лечения сердечнососудистого заболевания. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением предотвращения или лечения сердечнососудистого заболевания.
Один из аспектов настоящего изобретения представляет собой способ лечения гиперлипидемии. Указанный способ включает этап введения нуждающемуся в этом субъекту эффективного количества уролитина или его предшественника с обеспечением лечения гиперлипидемии. В одном из вариантов реализации гиперлипидемия представляет собой гипертриглицеридемию. В одном из вариантов реализации гиперлипидемия представляет собой повышенное количество свободных жирных кислот.
Один из аспектов настоящего изобретения представляет собой способ лечения нарушения метаболизма. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения нарушения метаболизма. В одном из вариантов реализации указанное нарушение метаболизма представляет собой сахарный диабет. В одном из вариантов реализации указанное нарушение метаболизма представляет собой ожирение.
Старение
Безусловно, самым большим фактором риска нейродегенеративных заболеваний, таких как болезнь Альцгеймера (БА), болезнь Паркинсона (БП) и боковой амиотрофический склероз (ALS), является старение. Считалось, что митохондрии вносят вклад в старение за счет накопления мутаций митохондриальной ДНК (мтДНК) и общего образования активных форм кислорода (АФК). Хотя большинство белков митохондрий кодируется ядерным геномом, митохондрии содержат множество копий собственной ДНК. мтДНК человека представляет собой кольцевую молекулу с 16569 парами оснований, кодирующую 13 полипептидных компонентов дыхательной цепи, а также рРНК и тРНК, необходимые для поддержания внутримитохондриального синтеза белка с использованием собственного генетического кода. Известно, что наследственные мутации в мтДНК вызывают различные заболевания, большинство из которых поражает головной мозг и мышцы - ткани с большой потребностью в энергии. Была высказана гипотеза о том, что соматические мутации мтДНК, приобретаемые в ходе старения, вносят вклад в ухудшение физиологического состояния, происходящее с возрастом, и возрастную нейродегенерацию. Точно установлено, что мтДНК накапливает мутации с возрастом, особенно крупномасштабные делеции и точечные мутации. В контрольной области мтДНК точечные мутации в конкретных участках могут накапливаться до высоких уровней в некоторых тканях: T414G в культивированных фибробластах, A189G и Т408А в мышце и С150Т в лейкоцитах. Однако данные «горячие точки» контрольной области не наблюдали в головном мозге. Точечные мутации в отдельных нуклеотидах, по-видимому, происходят на низких уровнях в головном мозге, хотя общий уровень может быть высоким. С использованием стратегии полимеразная цепная реакция (ПЦР)-клонирование-секвенирование было обнаружено, что средний уровень точечных мутаций в двух кодирующих белки областях мтДНК головного мозга пожилых субъектов составлял ~2 мутации на 10 кб. Некодирующие области, которые могут находиться под меньшим давлением отбора, вероятно, накапливают в два-четыре раза больше. Накопление данных делеций и точечных мутаций с возрастом коррелирует со снижением функции митохондрий. Например, была обнаружена отрицательная корреляция между активностью цитохромоксидазы головного мозга и повышенными уровнями точечных мутаций в гене цитохромоксидазы (CO1).
Общее образование АФК представляет собой другой важный механизм, за счет которого митохондрии, как считается, вносят вклад в старение. Митохондрии содержат многочисленные переносчики электронов, способные продуцировать АФК, а также развитую сеть антиоксидантной защиты. Повреждения митохондрий, включая само окислительное повреждение, могут вызывать дисбаланс между образованием и удалением АФК, приводящий к общему образованию АФК. Большое значение общего образования АФК в митохондриях для старения подтверждается наблюдениями, что усиление антиоксидантной защиты митохондрий может увеличивать продолжительность жизни. У дрозофилы (Drosophila) сверхэкспрессия антиоксидантных ферментов митохондрий марганец-супероксиддисмутазы (МnСОД) и метионинсульфоксидредуктазы увеличивает продолжительность жизни. Данная стратегия имеет наибольший успех у короткоживущих штаммов дрозофилы, и не оказывает никакого влияния у уже долгоживущих штаммов. Однако недавно было показано, что сверхэкспрессия катал азы, экспериментально прицельно направленная на митохондрии, увеличивала продолжительность жизни у уже долгоживущего штамма мыши.
Наблюдали, что снижение когнитивной функции при старении происходит у стареющих животных и считается, что оно происходит в результате изменений в синаптической физиологии стареющих нейронов. Считается, что данные изменения приводят к суммарной общей потере интегративной функции передачи сигнала нейронами в головном мозге (Bishop, Lu et al. 2010) и повышенной восприимчивости к длительным последствиям окислительного стресса и воспаления (Joseph, Shukitt-Hale et al. 2005). Считается, что потеря клеток, происходящая в ходе естественного старения, происходит главным образом вследствие окислительного стресса из-за свободных радикалов, образующихся за счет неэффективного и частично разобщенного окислительного пути. Действительно, было показано, что общей чертой при старении среди разных видов (С. elegans, чернобрюхая дрозофила (D. melanogaster), мыши, крысы, шимпанзе и люди) являлся факт пониженной функции митохондрий. Данная интерпретация также подтверждается наблюдением, что значительное нарушение функции митохондрий сокращает продолжительность жизни как у С. elegans (Rea, Ventura et al. 2007), так и мышей (Trifunovic, Wredenberg et al. 2004; Kujoth, Hiona et al. 2005). Улучшение функции митохондрий за счет сверхэкспрессии каталазы у мышей приводило к увеличению продолжительности жизни (Schriner, Linford et al. 2005).
С возрастом и снижением функции митохондрий нейроны в головном мозге становятся более уязвимыми к возрастным патологиям, а также гибели клеток. Это приводит к потере связей между нейронами, а также нарушению функции нейронов (потеря нейромедиаторов, отсутствие возбуждения). Также имеется все большее число подтверждений тому, что нейроны реагируют на невосстановленное повреждение ДНК путем сайленсинга экспрессии генов по эпигенетическим механизмам, что, таким образом, приводит к дальнейшему подавлению функций клеток. Кроме того, стареющие нейронные клетки у всех видов демонстрируют повышенную экспрессию генов, вовлеченных в пути стрессовых реакций.
Многие признаки данных изменений наблюдают в культуре стареющих нейронных клеток in vitro, демонстрирующих сниженный рост нейритов и образование отростков. Снижение, обратное развитие которого может быть вызвано факторами роста нейронов (Rozovsky, Wei et al., 2005).
Нейродегенеративные нарушения
Нейродегенеративные заболевания представляют собой гетерогенную группу нарушений, характеризующихся постепенно прогрессирующей селективной потерей анатомически или физиологически связанных нейронных систем. Прототипические примеры включают болезнь Альцгеймера (БА), болезнь Паркинсона (БП), боковой амиотрофический склероз (ALS) и болезнь Хантингтона (HD).
На ранних стадиях нейродегенерация имеет много таких же признаков, что и при спаде, наблюдаемом при старении. Интересно отметить, что такие заболевания, как болезнь Альцгеймера, демонстрируют рост заболеваемости с возрастом; более 50% взрослых в возрасте старше 85 лет имеют данное заболевание (Hebert, Scherr et al., 2003). Как рассмотрено выше, снижение функции митохондрий, по-видимому, является признаком старения. Данное снижение функции нейронов, вероятно, оказывает значительное влияние на популяции нейронов с большими биоэнергетическими потребностями, одной из таких групп нейронов являются крупные пирамидальные нейроны, которые дегенерируют при болезни Альцгеймера (Bishop, Lu et al., 2010). Уменьшение данных классов нейронов в ответ на нарушение функции митохондрий может быть ответственным за начало нейродегенеративного заболевания. Влияние нейродегенеративных нарушений на выживаемость нейронов может быть смоделировано in vitro. Когда нейронные клетки N2 инкубируют совместно с А-бета (Аβ) пептидом, который считается возбудителем болезни Альцгеймера, происходит значительное влияние на рост нейритов, которое может быть «отменено» антиоксид антами. Manczak et al. (2010) J Alzheimers Dis. 20 Suppl 2:S609-31.
Наиболее распространенной формой гибели клеток при нейродегенерации является гибель по внутреннему митохондриальному апоптотическому пути. Данный путь контролирует активацию каспазы-9 путем регуляции высвобождения цитохрома С из межмембранного пространства митохондрий. Концентрация АФК, обычных побочных продуктов активности дыхательной цепи митохондрий, отчасти опосредована митохондриальными антиоксидантами, такими как марганец-супероксиддисмутаза (СОД2) и глутатионпероксидаза. Сверхвыработка АФК (окислительный стресс) является центральным признаком всех нейродегенеративных нарушений. В дополнение к образованию АФК, митохондрии также связаны с функциями поддержания жизни, включая гомеостаз кальция, деление и слияние митохондрий, концентрацию липидов в мембранах митохондрий и изменение проницаемости митохондрий (МРТ). В митохондриальное заболевание, приводящее к нейродегенерации, вероятно, по меньшей мере на некотором уровне вовлечены все данные функции (DiMauro and Schon, 2008).
Существует подтверждение того, что дисфункция митохондрий и окислительный стресс играют причинную роль в патогенезе нейродегенеративных заболеваний, включая четыре из наиболее известных заболеваний: болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона и боковой амиотрофический склероз (также известный как болезнь Лу Герига).
Болезнь Альцгеймера (БА) клинически характеризуется прогрессирующим снижением когнитивной функции и патологически характеризуется присутствием сенильных бляшек, главным образом состоящих из β-амилоидного пептида (Аβ), и нейрофибриллярных клубков, в основном образованных гиперфосфорилированным тау-белком. Примерно 5-10% случаев являются наследственными, возникающими с ранним началом по аутосомно-доминантному типу. Известно, что с такими наследственными случаями связаны три белка: белок-предшественник амилоида (АРР) - который последовательно расщепляется β- и γ-секретазами с образованием Аβ - и пресенилины 1 и 2 (PS1 и PS2), один из которых является компонентом каждого комплекса γ-секретазы. Большое количество литературы подтверждает роль дисфункции и окислительного повреждения митохондрий в патогенезе БА. Окислительное повреждение в головном мозге при БА происходит рано, до возникновения значительной патологии в виде бляшек. Окислительное повреждение также предшествует отложению Аβ у трансгенных мышей с АРР, с повышающей регуляцией генов, связанной с митохондриальным метаболизмом и апоптозом, происходящей еще раньше, и колокализацией с нейронами, подвергающимися окислительному повреждению.
Недавно было обнаружено несколько путей, связывающих окислительный стресс и патологию БА. Окислительный стресс может активировать пути передачи сигнала, которые изменяют процессинг АРР или тау-белка. Например, окислительный стресс увеличивает экспрессию β-секретазы через активацию аминоконцевой киназы c-Jun и митоген-активируемой протеинкиназы р38 (МАРК), и увеличивает аберрантное фосфорилирование тау-белка путем активации киназы-3 гликогенсинтетазы. Индуцированная окислителем инактивация критических молекул также может иметь важное значение. В протеомическом исследовании было обнаружено, что пролилизомераза PIN1 является особенно чувствительной к окислительному повреждению. PIN1 катализирует конформационные изменения белка, влияющие на процессинг как АРР, так и тау-белка. Выключение гена (knockout) Pin1 увеличивает процессинг амилоидогенного АРР и внутриклеточные уровни Аβ у мышей. Мыши с выключенным геном Pin1 также демонстрируют гиперфосфорилирование тау-белка, двигательный дефект и поведенческий дефицит, и дегенерацию нейронов. Таким образом, индуцированное окислителем повреждение PIN1 и подобных чувствительных белков может иметь важное значение в способствовании нейродегенеративным процессам.
Митохондрии также играют важную роль в болезни Паркинсона (БП), которая клинически характеризуется прогрессирующей ригидностью, брадикинезией и тремором, и патологически характеризуется потерей пигментированных нейронов в черном веществе и присутствием телец Леви - отличительных цитоплазматических включений, которые дают окрашивание с использованием иммунной метки на предмет α-синуклеина и убиквитина.
Митохондрии впервые были связаны с БП из-за того, что 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МРТР), метаболит МРР+ которого ингибирует комплекс I электронтранспортной цепи митохондрий, вызывал паркинсонизм у употребляющих наркотики кустарного производства. С тех пор данная модель была усовершенствована у лабораторных животных, у которых постоянная инфузия ротенона - другого ингибитора комплекса-I - или МРТР клинически приводит к паркинсоническому фенотипу и патологически приводит к дегенерации черного вещества с цитоплазматическими включениями, иммунореактивными в отношении α-синуклеина и убиквитина. В механизм токсичности в данных моделях ингибирования комплекса-I, вероятно, вовлечен окислительный стресс. Было показано, что ингибирование комплекса-I и окислительный стресс соответствуют естественным образом возникающей БП, когда дефицит комплекса-I и истощение глутатиона обнаруживали в черном веществе пациентов с идиопатической БП и у пациентов с предсимптоматической БП.
Многие гены, ассоциируемые с БП, также вовлекают митохондрии в патогенез указанного заболевания. До настоящего времени мутации или полиморфизмы в мтДНК и по меньшей мере девяти названных ядерных генах были идентифицированы в качестве вызывающих БП или влияющих на риск возникновения БП: α-синуклеин, паркин, убиквитин-карбоксиконцевая гидролаза L1, DJ-1, индуцируемая гомологом фосфатазы и тензина (PTEN) киназа 1 (PINK1), богатая лейцином повторная киназа 2 (LRRK2), ядерный рецептор NURR1, HTRA2 и тау-белок. Из указанных ядерных генов α-синуклеин, паркин, DJ-1, PINK1, LRRK2 и HTRA2 напрямую или опосредованно вовлекают митохондрии. В малом числе случаев наследственные мутации мтДНК приводят к паркинсонизму, как правило, в виде одного признака более крупного синдрома. В одной из групп мутацию G11778A при атрофии зрительных нервов (болезнь Лебера) ассоциировали с паркинсонизмом, реагирующим на 1-DOPA, переменно возникающим вместе с деменцией, дистонией, офтальмоплегией и атаксией. В частности, данная мутация находится в субъединице комплекса I. Мутации в кодируемом ядром гене полимеразы-γ мтДНК (POLG) нарушают репликацию мтДНК и приводят к многочисленным делециям мтДНК, как правило, вызывающим хроническую прогрессирующую внешнюю офтальмоплегию и миопатию. В таких группах мутации POLG также косегрегируют (cosegregate) с паркинсонизмом.
Боковой амиотрофический склероз (ALS) клинически характеризуется прогрессирующей слабостью, атрофией и спастичностью мышечной ткани, отражающей дегенерацию верхних и нижних двигательных нейронов в коре головного мозга, стволе головного мозга и спинном мозге. Приблизительно 90% случаев являются спорадическими (SALS) и 10% являются наследственными (FALS). Примерно 20% наследственных случаев вызваны мутациями в Cu/Zn-супероксиддисмутазе (SOD1). Как при SALS, так и при FALS посмертные образцы и биопсийные образцы спинного мозга, нервов и мышц демонстрируют нарушения структуры, количества и локализации митохондрий. В мышце и спинном мозге также были детектированы дефекты активности комплексов дыхательной цепи.
Болезнь Хантингтона (HD) клинически характеризуется хореей, психическими нарушениями и деменцией, и патологически характеризуется потерей длинных проекционных нейронов в коре головного мозга и полосатом теле. HD наследуется по аутосомно-доминантному типу и обусловлена экспансией тринуклеотидного повтора CAG в гене гентингтина (huntingtin) (НТТ), которая приводит к протяженному удлинению полиглутамина в соответствующем белке. Нормальное число повторов CAG (Q) составляет менее 36; число повторов более 40 ассоциируют с заболеванием человека. Различные данные демонстрируют вовлечение дисфункции митохондрий в HD. Спектроскопия ядерного магнитного резонанса выявляет повышенное содержание лактата в коре головного мозга и базальных ганглиях. Биохимические исследования демонстрируют пониженную активность комплексов II и III электронтранспортной цепи в головном мозге человека с HD. В клетках полосатого тела мутантных эмбрионов мыши с включенным (knock-in) геном Htt митохондриальное дыхание и выработка АТФ значительно нарушены.
Один из аспектов настоящего изобретения представляет собой способ лечения нейродегенеративного заболевания, возрастной гибели или дисфункции нейронов. В настоящем описании термин «нейродегенеративное заболевание» или эквивалентно «нейродегенеративное нарушение» относится к любому состоянию, в которое вовлечена прогрессирующая потеря функциональных нейронов в центральной нервной системе. В одном из вариантов реализации указанное нейродегенеративное заболевание ассоциируют с возрастной гибелью клеток. Типичные нейродегенеративные заболевания включают, без ограничения, болезнь Альцгеймера, болезнь Паркинсона, болезнь Хантингтона, боковой амиотрофический склероз (также известный как ALS и как болезнь Лу Герига), а также комплекс СПИД-деменция, адренолейкодистрофию, болезнь Александера, болезнь Альперса, атаксию-телеангиэктазию, болезнь Баттена, коровью губчатую энцефалопатию (BSE), болезнь Канавана, кортикобазальную дегенерацию, болезнь Крейтцфельдта-Якоба, деменцию с тельцами Леви, фатальную семейную бессонницу, лобно-височную лобарную дегенерацию, болезнь Кеннеди, болезнь Краббе, болезнь Лайма, болезнь Мачадо-Джозефа, рассеянный склероз, множественную системную атрофию, нейроакантоцитоз, болезнь Ниманна-Пика, болезнь Пика, первичный боковой склероз, прогрессирующий надъядерный паралич, болезнь Рефсума, болезнь Сандгоффа, диффузный миелинокластический склероз, спиноцеребеллярную атаксию, подострую комбинированную дегенерацию спинного мозга, сухотку спинного мозга, болезнь Тея-Сакса, токсическую энцефалопатию, трансмиссивную губчатую энцефалопатию и синдром шатающегося ежа.
В одном из вариантов реализации указанный способ применяют для лечения возрастной гибели или дисфункции нейронов. Такой способ направлен на нейродегенерацию, которую нельзя отнести к конкретному нейродегенеративному заболеванию, например, болезни Альцгеймера, боковому амиотрофическому склерозу, болезни Хантингтона и болезни Паркинсона.
В одном из вариантов реализации нейродегенеративное заболевание выбрано из группы, состоящей из болезни Альцгеймера, бокового амиотрофического склероза, болезни Хантингтона и болезни Паркинсона.
В одном из вариантов реализации нейродегенеративное заболевание представляет собой болезнь Альцгеймера.
Указанный способ включает этап введения субъекту, нуждающемуся в лечении нейродегенеративного заболевания, терапевтически эффективного количества уролитина или его предшественника, что таким образом позволяет лечить указанное нейродегенеративное заболевание.
В соответствии с этим и другими способами согласно настоящему изобретению в настоящем описании термин «уролитин» относится к любому одному или комбинации уролитина А, уролитина В, уролитина С и уролитина D (см., например, ФИГ. 1 и ФИГ. 2). В одном из вариантов реализации уролитин представляет собой уролитин А, уролитин В, уролитин С, уролитин D или любую комбинацию уролитина А, уролитина В, уролитина С и уролитина D. В одном из вариантов реализации уролитин представляет собой уролитин А, уролитин В или комбинацию уролитина А и уролитина В. В одном из вариантов реализации уролитин представляет собой уролитин А. В одном из вариантов реализации уролитин представлен в виде выделенного уролитина, например, выделенного из природного источника, или полученного путем полного синтеза. Выделенные уролитины могут быть синтезированы de novo. См., например, публикацию заявки на патент США №2008/0031862 Ghosal, полное содержание которой включено в настоящее описание посредством ссылки.
В одном из вариантов реализации уролитин А (3,8-дигидроксидибензо-α-пирон) синтезировали путем двухстадийного синтеза следующим образом. 1 Стадия представляет собой реакцию, катализируемую медью, протекающую в присутствии основания (реакция Хартли (Hurtley)), в которой исходные вещества 2-бром-5-метоксибензойную кислоту и резорицинол (resoricinol) подвергают реакции друг с другом с образованием дигидродибензопиронового остова. На 2 Стадии деметилирование бензопирона с помощью BBr3 позволяет получать 3,8-дигидроксидибензо-α-пирон (уролитин А).
Смесь 2-бром-5-метоксибензойной кислоты 1 (27,6 г), резорцинола (resorcinol) 2 (26,3 г) и гидроксида натрия (10,5 г) в воде (120 мл) нагревали в колбе с обратным холодильником в течение 1 часа. Затем добавляли 5% водный раствор сульфата меди (3,88 г CuSO4, 5Н2О в 50 мл воды) и смесь нагревали в колбе с обратным холодильником в течение еще 30 минут. Смеси давали охладиться до комнатной температуры и твердое вещество фильтровали на фильтре Бюхнера. Остаток промывали холодной водой (50 мл) с получением бледно-красного твердого вещества (38,0 г), которое растирали в горячем МеОН (200 мл). Суспензию оставляли на ночь при 4°С. Фильтровали полученный светло-красный осадок и промывали холодным МеОН (75 мл) с получением соединения 3, указанного в заголовке, в виде светло-коричневого твердого вещества. 1Н ЯМР соответствует структуре 3.
К суспензии 3 (10,0 г; 41 ммоль; 1,0 экв.) в сухом дихлорметане (100 мл) при 0°С добавляли 1 М раствор трибромида бора в сухом дихлорметане (11,93 мл чистого BBr3 в 110 мл безводного дихлорметана). Смесь оставляли при 0°С в течение 1 часа, а затем давали нагреться до комнатной температуры. Перемешивали раствор при данной температуре в течение 17 часов. Фильтровали желтый осадок и промывали холодной водой (50 мл) с получением желтого твердого вещества, которое нагревали в колбе с обратным холодильником в уксусной кислоте (400 мл) в течение 3 часов. Быстро фильтровали горячий раствор и осадок промывали уксусной кислотой (50 мл), затем диэтиловым эфиром (100 мл) с получением соединения 4, указанного в заголовке, в виде желтого твердого вещества. Структуру и чистоту определяли путем 1Н и 13С-ЯМР.
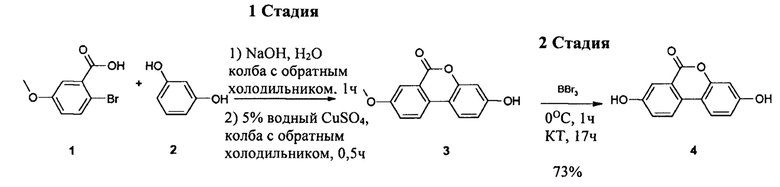
В одном из вариантов реализации в настоящем описании термин «уролитин» представляет собой или может включать глюкуронированный, метилированный и сульфатированный уролитин.
В соответствии с этим и другими способами согласно настоящему изобретению в настоящем описании термин «предшественник уролитина» относится к эллагитаннину или метаболиту эллагитаннина, включая, но не ограничиваясь ей, эллаговую кислоту (ЕА). В одном из вариантов реализации предшественник уролитина представляет собой пуникалагин (РА). В одном из вариантов реализации предшественник уролитина представляет собой пуникалин (РВ). См., например, ФИГ. 1. В одном из вариантов реализации предшественник уролитина представляет собой эллаговую кислоту (ЕА). В одном из вариантов реализации предшественник уролитина представлен в виде выделенного предшественника уролитина, например, выделенного из природного источника, или полученного путем полного синтеза. Выделенные предшественники уролитина обычно очищают из природных источников или синтезируют de novo; некоторые предшественники уролитина, включая ЕА, коммерчески доступны от поставщиков, таких как Sigma Aldrich.
Также в соответствии с этим и другими способами согласно настоящему изобретению предшественники уролитинов также включают натуральные пищевые продукты, содержащие эллагитаннины и эллаговую кислоту, особенно натуральные пищевые продукты, богатые эллагитаннинами, эллаговой кислотой или как эллагитаннинами, так и эллаговой кислотой. Такие продукты включают некоторые ягоды, виноград, гранат, плоды шиповника и орехи. В одном из вариантов реализации натуральный пищевой продукт представляет собой гранат.
Кроме того, предшественники уролитинов включают переработанные продукты питания и напитки, полученные из таких натуральных пищевых продуктов. Переработанный продукт питания может принимать любую форму, включая, например, джемы, желе, консервы, пасты, пастообразные продукты, соки, вина, экстракты, концентраты и т.п. В одном из вариантов реализации переработанный продукт питания представляет собой гранатовый сок.
В одном из вариантов реализации предшественник уролитина представлен в виде экстракта, например, фруктового экстракта.
В одном из вариантов реализации предшественник уролитина представлен в виде концентрата, например, концентрата фруктов или концентрата фруктового сока.
Указанный способ согласно настоящему изобретению можно использовать отдельно или в комбинации с любым способом или соединением, которое, как известно, подходит для лечения нейродегенеративного заболевания. Например, в одном из вариантов реализации способ согласно настоящему изобретению можно комбинировать с использованием любого одного или более ингибиторов ацетилхолинэстеразы, таких как донезепил (Арисепт®) (donezepil, Aricept®), галантамин (Разадин®) (galantamine, Razadyne®) и ривастигмин (Экселон®) (rivastigmine, Exelon®), и антагонистов рецептора N-метил-D-аспартата (NMDA), таких как мемантин (Наменда®) (memantine, Namenda®).
Один из аспектов настоящего изобретения представляет собой способ улучшения когнитивной функции. В настоящем описании термин «когнитивная функция» относится к любому умственному процессу, включающему оперирование символами, например, восприятию, памяти, вниманию, пониманию речи, образованию речи, пониманию прочитанного, формированию образов, обучению и мышлению. В одном из вариантов реализации термин «когнитивная функция» относится к любому одному или более из: восприятие, память, внимание и мышление. В одном из вариантов реализации термин «когнитивная функция» относится к памяти.
Указанный способ включает этап введения субъекту, нуждающемуся в улучшении когнитивной функции, терапевтически эффективного количества уролитина или его предшественника, что таким образом позволяет улучшать когнитивную функцию.
Способы измерения когнитивной функции хорошо известны и могут включать, например, индивидуальные тесты или батарею тестов для любого аспекта когнитивной функции. Одним из таких тестов является тест Прудо (Prudhoe) для определения когнитивной функции. Margallo-Lana et al. (2003) J Intellect Disability Res. 47:488-492. Другим таким тестом является краткое исследование психического состояния (Mini Mental State Exam, MMSE), предназначенное для оценки ориентации во времени и пространстве, фиксирования, внимания и расчета, вспоминания, использования языка и понимания, повторения и сложных команд. Folstein et al. (1975) J Psych Res. 12:189-198. Другие тесты, подходящие для измерения когнитивной функции, включают Шкалу оценки болезни Альцгеймера, когнитивную подшкалу (Alzheimer Disease Assessment Scale-Cognitive, ADAS-Cog) (Rosen et al. (1984) Am J Psychiatry. 141(11): 1356-64) и Кембриджскую батарею тестов нейропсихологической оценки (Cambridge Neuropsychological Test Automated Battery, CANTAB) (Robbins et al. (1994) Dementia. 5(5):266-81). Такие тесты можно использовать для оценки когнитивной функции объективным образом для того, чтобы можно было измерять и сравнивать изменения когнитивной функции, например, в ответ на лечение в соответствии со способами согласно настоящему изобретению.
Указанный способ согласно настоящему изобретению можно использовать отдельно или в комбинации с любым способом или соединением, которое, как известно, улучшает когнитивную функцию. Например, в одном из вариантов реализации указанный способ согласно настоящему изобретению комбинируют с использованием кофеина или никотина, или обоих.
В одном из вариантов реализации у субъекта нет когнитивного расстройства. Например, указанный способ можно использовать для усиления когнитивной функции у субъекта, демонстрирующего нормальную когнитивную функцию.
Один из аспектов настоящего изобретения представляет собой способ лечения когнитивного расстройства. В настоящем описании термин «когнитивное расстройство» относится к любому состоянию, нарушающему когнитивную функцию. В одном из вариантов реализации термин «когнитивное расстройство» относится к любому одному или более из: делирий, деменция, нарушение способности к обучению, синдром дефицита внимания (СДВ) и синдром дефицита внимания и гиперактивности (СДВГ). В одном из вариантов реализации указанное когнитивное расстройство представляет собой нарушение способности к обучению. В одном из вариантов реализации указанное когнитивное расстройство представляет собой синдром дефицита внимания (СДВ). В одном из вариантов реализации указанное когнитивное расстройство представляет собой синдром дефицита внимания и гиперактивности (СДВГ).
Указанный способ включает этап введения субъекту, нуждающемуся в лечении когнитивного расстройства, терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения указанного когнитивного расстройства.
Указанный способ согласно настоящему изобретению можно использовать отдельно или в комбинации с любым способом или соединением, которое, как известно, подходит для лечения когнитивного расстройства. Например, в одном из вариантов реализации способ согласно настоящему изобретению комбинируют с использованием стимулятора, такого как метилфенидат (например, Риталин® (Ritalin®)), декстроамфетамин (Декседрин® (Dexedrine®)), смешанные соли амфетамина (Аддералл® (Adderall®)), декстрометамфетамин (Дезоксин® (Desoxyn®)) и лиздексамфетамин (Виваназ® (Vyvanase®)).
Один из аспектов настоящего изобретения представляет собой способ лечения или предотвращения вызванной стрессом или связанной со стрессом когнитивной дисфункции. В настоящем описании термин «вызванная стрессом или связанная со стрессом когнитивная дисфункция» относится к нарушению когнитивной функции, вызванному стрессом или связанному со стрессом. Указанный способ включает этап введения субъекту, нуждающемуся в лечении или предотвращении вызванной стрессом или связанной со стрессом когнитивной дисфункции, терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения или предотвращения указанной вызванной стрессом или связанной со стрессом когнитивной дисфункции.
Расстройства настроения
Для тканей головного мозга необходим высокий уровень энергии для метаболизма, включая поддержание трансмембранного потенциала, передачу сигнала и синаптическое ремоделирование. Увеличение психических симптомов и нарушений, в частности, депрессии, вероятно, имеет место у пациентов с митохондриальными нарушениями.
Было показано, что структура и функция митохондрий, измеряемые множеством различных методов, являются аномальными у пациентов с расстройствами настроения, включая глубокую депрессию, а также в случае других расстройств аффективного спектра.
Два исследования показали, что в несколько раз повышенная вероятность развития депрессии может наследоваться по материнской линии наряду с мтДНК, что убедительно подтверждает то, что варианты последовательности мтДНК могут индуцировать дисфункцию митохондрий, которая может предрасполагать индивидуумов к развитию депрессии (Boles et al., 2005; Burnett et al., 2005).
Связь между дисфункцией митохондрий и монополярной депрессией была исследована в нескольких исследованиях. В исследованиях головного мозга субъектов после смерти с вероятной или диагностированной глубокой депрессией, из которых большинство субъектов получали (вероятно) лечение лекарственными средствами, не удавалось детектировать увеличение распространенной делеции 5 кб мтДНК (Kato et al., 1997; Sabunciyan et al., 2007; Shao et al., 2008, Stine et al., 1993). Изменения продуктов трансляции, связанные с функцией митохондрий, обнаруживали в лобной, префронтальной и третичной зрительной коре (Karry et al., 2004; Whatley et al., 1996). Существуют данные об изменениях четырех расположенных в митохондриях белков в передней поясной коре (Beasley et al., 2006). Также существуют данные о пониженной экспрессии генов для 6 из 13 кодируемых мтДНК транскриптов в ткани лобной коры (поля Бродмана (ВА) 9 и 46) (Shao et al., 2008), и кодируемой нДНК митохондриальной мРНК и белков в мозжечке при глубокой депрессии (Ben-Shachar and Karry, 2008). В недавнем исследовании было обнаружено, что уровни субъединицы комплекса I электронтранспортной цепи (NDUFS7) и активность комплекса I в посмертной префронтальной коре ниже или находятся в самом низком диапазоне по сравнению с нормальными контролями в половине случаев большого депрессивного расстройства (Andreazza et al., 2010). В двух более поздних исследованиях авторы не смогли детектировать какое-либо влияние лечения лекарственными средствами на результаты.
Уменьшения соотношений ферментов дыхательной цепи и объемов выработки АТФ, и повышенная распространенность мелких делеций мтДНК (но не распространенной 5 кб делеции мтДНК) были обнаружены в мышце пациентов с поставленным в течение жизни диагнозом глубокой монополярной депрессии с сопутствующими физическими симптомами. Лечение лекарственными средствами, по-видимому, не влияло на результаты (Gardner et al., 2003b). Клиническая значимость была предположена в результате обнаружения того, что по существу каждый находящийся в состоянии депрессии субъект с очень высокой степенью соматических жалоб, демонстрировал низкие объемы выработки АТФ в мышце, полученной методом биопсии (Gardner and Boles, 2008а).
Один из аспектов настоящего изобретения представляет собой способ лечения расстройства настроения (также известного как аффективное расстройство). В настоящем описании термин «расстройство настроения» относится к нарушению эмоционального состояния, такому как описано в Руководстве по диагностике и статистике психических расстройств (Diagnostic and Statistical Manual of Mental Disorders), опубликованном Американской психиатрической ассоциацией (American Psychiatric Association). Расстройства настроения включают, но не ограничиваются ими, глубокую депрессию, послеродовую депрессию, дистимию и биполярное расстройство. В одном из вариантов реализации указанное расстройство настроения представляет собой глубокую депрессию.
Указанный способ включает этап введения субъекту, нуждающемуся в лечении расстройства настроения, терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения указанного расстройства настроения.
Указанный способ согласно настоящему изобретению можно использовать отдельно или в комбинации с любым способом или соединением, которое, как известно, подходит для лечения расстройства настроения. Например, в одном из вариантов реализации способ согласно настоящему изобретению комбинируют с использованием антидепрессанта. Антидепрессанты хорошо известны в данной области техники и включают селективные ингибиторы обратного захвата серотонина (SSRI), ингибиторы обратного захвата серотонина-норадреналина (SNRIs), норадренергические и специфические серотонинергические антидепрессанты, ингибиторы обратного захвата норадреналина, ингибиторы обратного захвата норадреналина-дофамина, селективные ингибиторы обратного захвата серотонина, дис-ингибиторы (disinhibitors) норадреналина-дофамина, трициклические антидепрессанты и ингибиторы моноаминоксидазы.
Один из аспектов настоящего изобретения представляет собой способ лечения или предотвращения вызванного стрессом или связанного со стрессом расстройства настроения. В настоящем описании термин «вызванное стрессом или связанное со стрессом расстройство настроения» относится к нарушению эмоционального состояния, вызванному стрессом или связанному со стрессом. Такие расстройства настроения иногда называют реактивными расстройствами настроения и их следует отличать от других расстройств настроения, например, так называемых органических расстройств настроения. Указанный способ включает этап введения субъекту, нуждающемуся в лечении или предотвращении вызванного стрессом или связанного со стрессом расстройства настроения, эффективного количества уролитина или его предшественника с обеспечением лечения или предотвращения указанного вызванного стрессом или связанного со стрессом расстройства настроения.
Один из аспектов настоящего изобретения представляет собой способ лечения тревожного расстройства. В настоящем описании термин «тревожное расстройство» относится к дисфункциональному состоянию страха и тревоги, например, страха и тревоги, несоизмеримой со стрессовой ситуацией или ожиданием стрессовой ситуации. В одном из вариантов реализации тревожное расстройство представляет собой любое одно или комбинацию из: генерализованное тревожное расстройство, паническое расстройство, паническое расстройство в сочетании с агорафобией, агорафобия, социальное тревожное расстройство, обсессивно-компульсивное расстройство и посттравматическое стрессовое расстройство. В одном из вариантов реализации тревожное расстройство представляет собой любое одно или комбинацию из: генерализованное тревожное расстройство, обсессивно-компульсивное расстройство, паническое расстройство, посттравматическое стрессовое расстройство и социальное тревожное расстройство. В одном из вариантов реализации тревожное расстройство представляет собой генерализованное тревожное расстройство. В одном из вариантов реализации тревожное расстройство представляет собой посттравматическое стрессовое расстройство. В одном из вариантов реализации тревожное расстройство представляет собой вызванное стрессом тревожное расстройство.
Указанный способ включает этап введения субъекту, нуждающемуся в лечении тревожного расстройства, терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения указанного тревожного расстройства.
Указанный способ согласно настоящему изобретению можно использовать отдельно или в комбинации с любым способом или соединением, которое, как известно, подходит для лечения тревожного расстройства. Например, в одном из вариантов реализации способ согласно настоящему изобретению комбинируют с использованием любого одного или комбинации из: психотерапия, бензодиазепины, буспирон (Буспар®) (buspirone, Buspar®) или бета-блокаторы. Бензодиазепины хорошо известны в данной области техники и включают, без ограничения, клоназепам (Клонопин®) (clonazepam, Klonopin®), лоразепам (Ативан®) (lorazepam, Ativan®) и алпразолам (Ксанакс®) (alprazolam, Xanax®). Дополнительные лекарственные средства, которые могут быть использованы в комбинации со способами согласно настоящему изобретению, включают имипрамин (Тофранил®) (imipramine, Tofranil®) и венлафаксин (Эффексор®) (venlafaxine, Effexor®).
Один из аспектов настоящего изобретения представляет собой способ лечения или предотвращения вызванного стрессом или связанного со стрессом тревожного расстройства. В настоящем описании термин «вызванное стрессом или связанное со стрессом тревожное расстройство» относится к дисфункциональному состоянию страха и тревоги, вызванному стрессом или связанному со стрессом. Такие тревожные расстройства иногда называют реактивными тревожными расстройствами и их следует отличать от других тревожных расстройств, например, так называемых органических тревожных расстройств. Указанный способ включает этап введения субъекту, нуждающемуся в лечении или предотвращении вызванного стрессом или связанного со стрессом тревожного расстройства, эффективного количества уролитина или его предшественника с обеспечением лечения или предотвращения указанного вызванного стрессом или связанного со стрессом тревожного расстройства.
Один из аспектов настоящего изобретения представляет собой способ способствования росту нейритов. В одном из вариантов реализации указанный способ представляет собой способ in vitro. В одном из вариантов реализации указанный способ представляет собой способ in vivo. В настоящем описании термин «нейрит» относится к любому выступу от клеточного тела нейрона. В одном из вариантов реализации такой выступ представляет собой аксон. В одном из вариантов реализации такой выступ представляет собой дендрит. Указанный термин часто употребляют, когда говорят о незрелых или развивающихся нейронах, особенно о клетках в культуре, потому что может быть трудно отличить аксоны от дендритов до завершения дифференцировки. Нейриты часто «упакованы» с пучками микротрубочек, рост которых стимулируется фактором роста нервов (NGF), а также тау-белками, ассоциированным с микротрубочками белком 1 (MAP1) и ассоциированным с микротрубочками белком 2 (МАР2). Молекула адгезии нервных клеток N-CAM одновременно комбинируется с другой N-CAM и рецептором фактора роста фибробластов, для стимуляции активности тирозинкиназы данного рецептора с индуцированием роста нейритов.
Рост нейритов можно измерять морфологически и функционально. Морфологическое измерение, как правило, влечет за собой микроскопическое исследование с измерением длины и/или количества нейритов.
В настоящем описании термин «способствование» относится к усилению или индуцированию. В одном из вариантов реализации термин «способствование» означает индуцирование. Например, рост нейритов в отрицательном контрольном образце может быть ничтожно малым, в то время как рост нейритов в экспериментальном образце или образце лечения может быть значительным. В одном из вариантов реализации термин «способствование» означает усиление. Например, рост нейритов в отрицательном контрольном образце может быть значительным, в то время как рост нейритов в экспериментальном образце или образце лечения может быть статистически значительно большим, чем отрицательный контроль. Конечно, в настоящем описании термин «способствование» может включать как усиление, так и индуцирование.
В одном из вариантов реализации указанный способ включает этап приведения нервной клетки в контакт с эффективным количеством уролитина или его предшественника с обеспечением способствования росту нейритов.
В одном из вариантов реализации указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением способствования росту нейритов.
Указанные способы согласно настоящему изобретению можно использовать отдельно или в комбинации с любым способом или соединением, которое, как известно, подходит для способствования росту нейритов. Например, в одном из вариантов реализации способ согласно настоящему изобретению может быть комбинирован с использованием любого одного или более из: NGF, тау-белок, MAP1, МАР2, N-CAM, или агента, индуцирующего экспрессию любого одного или более из: NGF, тау-белок, MAP1, МАР2, N-CAM или рецептор фактора роста фибробластов.
Использование нейронных клеток in vitro для скрининга соединений на предмет нейропротекторной активности
В процессах старения и нейродегенерации прогрессирующее ухудшение когнитивной функции по существу обусловлено потерей элементов, поддерживающих нейронную связь. Данные элементы по существу состоят из тел нейронных клеток, нейритов и синаптических контактов, которые соединяют их с целевыми клетками. Нейроны демонстрируют очень сложную морфологию. Наиболее сложные типы нейронных клеток, такие как двигательные нейроны, распространяющие аксональные отростки до одного метра длиной, или дофаминергические нейроны черного вещества, составляющие более 150000 синаптических контактов, часто будут наиболее уязвимыми при естественном старении или заболевании. Для поддержания такой сложной структуры и эффективной передачи электрических и нейрохимических сигналов, нейроны сильно зависят от энергоснабжения. Следовательно, аксональный транспорт, синаптическая активность и поддержание ионных градиентов сильно зависят от функции митохондрий. Для выполнения данных требовательных клеточных функций нейроны со временем испытывают трудности поддержания неустойчивого баланса митохондриальной активности и последующего окислительного стресса. Такой дисбаланс часто считается причиной дисфункции нейронов или ранней дегенерации.
Следовательно, ожидается, что любое лечение, способствующее выживаемости нейронов или образованию нейронных отростков и синаптических контактов, составляющих сложную структуру нейронов, положительно влияет на функции нейронов. Измерение влияния соединений на функцию нейронов, как правило, основано на длительном наблюдении за поведенческими результатами у животных, которое не поддается скринингу на предмет биологической активности средней или высокой производительности. Модели in vitro на основе линий клеток нейробластомы или первичных культур нейронов являются общепринятым посредником для оценки влияния соединений на критические морфологические параметры, которые будут отражать способность нейронов поддерживать нормальную функцию в головном мозге млекопитающих. Такие показатели, как число отростков, их длина или сложность, покажут влияние соединений на критические этапы внутриклеточной передачи сигнала. Хотя следует иметь в виду, что такие параметры лишь косвенно отражают выполнение высших функций головного мозга, они обеспечивают ценную оценку эффективности соединения, которая может преобразовываться в улучшение когнитивных или двигательных функций в нормальном состоянии или болезненных состояниях.
Нарушения метаболизма
Функция митохондрий в ключевых тканях, участвующих в метаболизме (печень, мышцы, жировая ткань, поджелудочная железа), вовлечена в патогенез болезней обмена веществ. В каждой из данных тканей окислительная активность митохондрий должна быть подходящей для полного окисления множества питательных веществ, в частности, жирных кислот. Отсутствие полного окисления может приводить к накоплению промежуточных липидных соединений, продуктов неполного окисления жирных кислот, и АФК. В целом, данные клеточные явления вносят вклад в накопление жира, резистентность к инсулину, изменение секреции инсулина, неспецифичное воспаление и окислительный стресс, все из которых являются компонентами сахарного диабета II типа и ожирения.
Важное значение активности митохондрий в патогенезе болезней обмена веществ было установлено в нескольких исследованиях у людей. Например, резистентность к инсулину в скелетной мышце была ассоциирована с дефектом окислительного фосфорилирования митохондрий, когда 30% снижение активности митохондрий наблюдают у инсулинрезистентного потомства пациентов с диабетом 2 типа по сравнению с контрольными субъектами. Petersen KF, et al. (2004) New Engl J Med. 350:664-71. Также наблюдали, что пациенты, страдающие ожирением, демонстрируют 20% снижение активности митохондрий наряду с 35% уменьшением размера митохондрий по сравнению со здоровыми худощавыми субъектами. Petersen KF, et al. (2003) Science 300:1140-2. Наконец, ассоциируемое с возрастом снижение функции митохондрий вносит вклад в резистентность к инсулину у пожилых людей. Соответственно, существуют данные о 40% снижении окислительной и фосфорилирующей активности митохондрий у пожилых людей по сравнению с молодыми субъектами. Данные наблюдения связывают нарушение функции митохондрий с нарушениями метаболизма, особенно «диажирением» ("diabesity") (Kelley DE, et al. (2002) Diabetes 51:2944-50).
Окислительную активность митохондрий, также называемую окислительным фосфорилированием, можно считать ключевым фактором, лежащим в основе риска возникновения болезней обмена веществ. Снижение активности митохондрий может быть опосредовано генетическими факторами (например, семейный анамнез, этническая принадлежность), эпигенетическими механизмами, воздействиями на развитие, пищевым поведением и старением.
Когда непрерывный избыток топлива (например, в результате переедания или нарушения отложения жира) превосходит потребность в энергии и/или окислительную способность, и/или соответствующих компенсаторных механизмов недостаточно (например, вследствие неактивности или неспособности митохондрий адаптироваться к более высоким окислительным потребностям клеток), существует повышенный риск возникновения нарушений метаболизма. Возникающее в связи с этим накопление липидов и окислительный стресс могут изменять транскрипционные реакции и повреждать митохондрии, что дополнительно снижает способность окислительного фосфорилирования, усугубляя вредное влияние избытка топлива, повышающее риск возникновения нарушений метаболизма.
Достаточность полностью окислять жирные кислоты находится в равновесии между: (i) общей окислительной активностью митохондрий (определяемой необходимостью вырабатывать энергию для удовлетворения потребностей клеток, например, сокращения и переноса ионов) и (ii) наличием топлива (определяемым приемом пищи, ожирением и способностью накапливать жир). Равновесие достигается, когда окислительная активность равна или превышает запасы топлива.
В нормальных гомеостатических условиях как окислительная активность, так и наличие клеточного топлива могут меняться для обеспечения функции митохондрии, подходящей для окружающей метаболической среды. Например, потребность клеток в энергии может возрастать вследствие физической нагрузки, а наличие топлива может быть снижено вследствие потери массы тела и/или уменьшения потребления пищи. В данном контексте межиндивидуальные вариации окислительной способности и/или активности, запаса топлива или способности модулировать активность митохондрий (острая реакция), повышать способность митохондрий (хроническая реакция) или устранять окислительный стресс могут определять установление метаболического равновесия. Такие различия могут стать заметными особенно в среде, ведущей к развитию ожирения (среда, характеризующаяся условиями, способствующими увеличению общего потребления пищи, потреблению продуктов питания, не укрепляющих здоровье, и физической инертности). Следовательно, индивидуумы с высокой окислительной способностью или адаптивными реакциями будут демонстрировать высокую переносимость больших запасов топлива. И наоборот, индивидуумы с пониженной окислительной способностью и/или субоптимальными адаптивными реакциями будут неустойчивыми к уменьшению больших запасов топлива, что приводит к накоплению липидов, неполному окислению, образованию АФК и резистентности к инсулину.
Со временем недостаточная компенсация приведет к хронической резистентности к инсулину и нарушениям метаболизма. Недостаточная окислительная способность могла бы быть разрешена компенсаторными механизмами, которые увеличивают окислительную способность (например, физические упражнения) или уменьшают запас топлива (потеря массы тела). Однако данные изменения образа жизни обычно оказываются недостаточными или недостижимыми для большинства субъектов с избыточной массой тела/ожирением и субъектов с диабетом 2 типа или предрасположенных к диабету.
Митохондрии имеют особенно важное значение для функции скелетных мышц, учитывая высокие окислительные требования, накладываемые на данную ткань периодическим сокращением. Митохондрии играют критическую роль в обеспечении достаточных уровней АТФ, необходимых для сокращения саркомером мышц. Данная потребность саркомеров в высоком уровне АТФ, вероятно, вносила вклад в особые субсарколеммные и связанные с саркомерами популяции митохондрий в мышце. Более того, мышечные клетки должны сохранять метаболическую гибкость, способность быстро модулировать окисление субстрата в зависимости от окружающих гормональных и энергетических условий. Например, здоровая мышечная ткань преимущественно окисляет липид в состоянии воздержания от приема пищи, о чем свидетельствует низкий дыхательный коэффициент (RQ), с последующим переходом к окислению углеводов (увеличенный RQ) в сытом состоянии. Наличие топлив, в частности, липидов, и способность их окислять в митохондриях также имеют критическое значение для длительной физической нагрузки. Таким образом, функциональная способность митохондрий, вероятно, напрямую влияет на метаболическую функцию мышц и из-за ее большого вклада в общую массу тела оказывает значительное влияние на метаболизм всего организма. Данная возможность подтверждается данными повышенного содержания митохондрий в скелетной мышце у индивидуума с гиперметаболизмом и устойчивостью к увеличению массы тела (синдром Люфта).
Резистентность к инсулину и сахарный диабет
Скелетная мышца представляет собой крупнейший чувствительный к инсулину орган у людей, обеспечивающий более 80% стимулируемой инсулином утилизации глюкозы. Таким образом, резистентность к инсулину в данной ткани оказывает основное влияние на гомеостаз глюкозы во всем организме. Действительно, были обнаружены многочисленные метаболические дефекты в мышце резистентных к инсулину, но нормогликемических субъектов с высоким риском развития диабета, включая: (i) сниженный синтез гликогена, стимулируемый инсулином; (ii) изменения передачи сигнала инсулина; и (iii) повышенное накопление липидов мышцах. Хотя в настоящее время остается неясным играет ли какой-либо из данных дефектов причинную роль в резистентности к инсулину, интрамышечноклеточный избыток липидов прочно коррелирует с тяжестью резистентности к инсулину, даже после поправки на степень ожирения, и его наблюдали в мышцах с многочисленными типами волокон. Кроме того, избыток липидов был экспериментально связан с индукцией резистентности к инсулину и изменениями передачи сигнала инсулина. Таким образом, один из возможных механизмов, по которым нарушенная функция митохондрий может вносить вклад в резистентность к инсулину, представляет собой механизм через измененный метаболизм жирных кислот. Повышенная липидная нагрузка в ткани, как в случае ожирения и/или длительного отсутствия активности, может приводить к накоплению жирного ацил-коэнзима А (КоА), диацилглицеринов, церамидов, продуктов неполного окисления и АФК, все из которых были экспериментально связаны с уменьшенной передачей сигнала и действием инсулина. Дополнительные механизмы, вероятно связывающие нарушенную окислительную функцию митохондрий с резистентностью к инсулину, включают: (i) сниженный синтез АТФ для энергопотребляющих функций, таких как стимулируемое инсулином усвоение глюкозы; (ii) аномалии в гомеостазе кальция (необходимом для индуцируемого физической нагрузкой усвоения глюкозы); и (iii) сниженную выработку АТФ во время физической нагрузки, вероятно, вносящую вклад в снижение аэробной способности, мышечное утомление и снижение произвольной физической нагрузки со времени - дополнительно «питающее» порочный круг резистентности к инсулину, поддерживаемой отсутствием активности.
Способность митохондрий занимает центральное место в ключевой функции секреции инсулина, регулируемой бета (β)-клетками поджелудочной железы. Как быстрая (первая фаза), так и более длительная (вторая фаза) секреция инсулина зависят от метаболизма глюкозы и окислительной способности митохондрий; окисление глюкозы увеличивает соотношение АТФ/АДФ, ингибируя каналы К-АТФ плазматической мембраны и позволяя потенциалзависимым кальциевым каналам открываться. Затем повышенный цитоплазматический кальций запускает экзоцитоз гранул инсулина, «состыкованных» с плазматической мембраной (первая фаза). Последующее привлечение гранул к плазматической мембране (вторая фаза), по-видимому, зависит от митохондриальных метаболитов, продуцируемых путем анаплероза. Митохондриальный метаболизм также необходим для переходного контролируемого образования АФК, которое необходимо для митохондриальных путей передачи сигнала, которые запускают экзоцитоз гранул.
Диабет с митохондриальным наследованием развивается только при старении; средний возраст возникновения составляет от 35 до 40 лет для наследованного по материнской линии диабета с глухотой (MIDD) и 48 лет для 14577 Т/С, миссенс-мутации митохондриальной ДНК при наследованном по материнской линии диабете 2 типа. Это отличается от возникновения диабета в раннем детстве при таких синдромах как диабет зрелого возраста у молодых (MODY2), при котором мутация глюкокиназы, первый этап гликолиза, приводит к уменьшенной стимулируемой глюкозой выработке АТФ и секреции инсулина. Эти данные позволяют предположить, что диабет с митохондриальным наследованием более вероятно является следствием постепенного ухудшения функции β-клеток, а не острого функционального нарушения из-за недостаточной выработки АТФ.
Функция митохондрий в тканях, вовлеченных в патогенез сахарного диабета (печень, мышца, жировая ткань и (β)-клетки поджелудочной железы) имеет критическое значение для множества аспектов клеточного метаболизма. В каждой из данных тканей окислительная активность митохондрий должна быть подходящей для полного окисления множества питательных веществ, в частности, жирных кислот. Отсутствие полного окисления может приводить к накоплению липидных промежуточных соединений, продуктов неполного окисления жирных кислот и АФК, индуцирующему как резистентность к инсулину (мышца, печень, жировая ткань), так и изменение секреции β-клетки).
Умеренный дефицит активности митохондрий и/или неспособность повышать активность и способность в ответ на потребность клеток в энергии могут объяснить снижение способности к физической нагрузке, наблюдаемое у индивидуумов с семейным анамнезом сахарного диабета. Со временем данный фенотип может вносить вклад в сниженную произвольную физическую нагрузку и увеличивать вероятность дисбаланса между активностью митохондрий и запасом жирных кислот. Во-вторых, хронический дисбаланс в энергетическом метаболизме вследствие избыточного питания, ожирения и отсутствия активности может напрямую вносить вклад в увеличение клеточного и митохондриального образования АФК. В свою очередь, избыточные АФК могут индуцировать как резистентность к инсулину, так и дисфункцию митохондрий. Например, рацион питания с высоким содержанием жиров, высоким содержанием сахарозы у предрасположенной к диабету мыши C57BL6 вызывает изменения в митохондриях параллельно с повышенным образованием АФК и нарушенной чувствительностью к инсулину. Подобным образом, воздействие на мышечные клетки in vitro насыщенными жирными кислотами или питание с высоким содержанием жиров у мышей приводит к изменениям структуры митохондрий и резистентности к инсулину, обратное развитие обоих из которых вызывается антиоксидантами. Таким образом, окислительный стресс может индуцировать дисфункцию митохондрий параллельно с резистентностью к инсулину - возможно, адаптивный ответ, направленный на ограничение дальнейшего окислительного повреждения. Важно отметить, что устранение окислительного стресса может вызывать обратное развитие резистентности к инсулину.
Мышечная деятельность
В других вариантах реализации настоящего изобретения предложены способы повышения мышечной деятельности путем введения терапевтически эффективного количества усиливающего или активирующего митохондрии экстракта, состава или соединения. Например, экстракты, содержащие эллагитаннины или эллаговую кислоту, или композиции, содержащие эллагитаннины, эллаговую кислоту или уролитины, действуют таким образом, чтобы активировать митохондрии и могут подходить для повышения физической выносливости (например, способности выполнять физическую задачу, такую как физические упражнения, физический труд, занятия спортом), ингибирования или замедления физической усталости, повышения уровней кислорода в крови, повышения энергии у здоровых индивидуумов, повышения работоспособности и выносливости, снижения мышечного утомления, уменьшения стресса, повышения сердечной функции и функции сердечнососудистой системы, повышения половой способности, увеличения уровней АТФ в мышцах и/или уменьшения молочной кислоты в крови. В некоторых вариантах реализации способы включают введение количества природного экстракта, содержащего эллагитаннины или эллаговую кислоту, или композиций, содержащих эллагитаннины, эллаговую кислоту или уролитин, которые увеличивают активность митохондрий, увеличивают митохондриальный биогенез и/или увеличивают массу митохондрий.
Термин «спортивная подготовка» (sports performance) относится к способности мышц спортсмена выполнять работу при участии в занятиях спортом. Повышенную спортивную подготовку, силу, скорость и выносливость измеряют по увеличению силы мышечного сокращения, увеличению амплитуды мышечного сокращения или уменьшению времени реакции мышц между стимуляцией и сокращением. Термин «спортсмен» относится к индивидууму, который принимает участие в занятиях спортом на любом уровне и который стремится достичь повышенного уровня силы, скорости и выносливости в своей деятельности, такому как, например, бодибилдеры, велосипедисты, бегуны на длинные дистанции и бегуны на короткие дистанции. Повышенная спортивная подготовка проявляется по способности преодолевать мышечное утомление, способности поддерживать активность в течение более длительных периодов времени и более эффективно тренироваться.
Предполагается, что композиции и способы согласно настоящему изобретению также будут эффективны в лечении связанных с мышцами патологических состояний, включая миопатии, нервно-мышечные заболевания, такие как мышечная дистрофия Дюшенна, острая саркопения, например, атрофия мышц и/или кахексия, связанная с ожогами, постельный режим, иммобилизацию конечности или обширное торакальное, абдоминальное и/или ортопедическое оперативное вмешательство.
Хронический стресс
Существуют данные о том, что хронический стресс также оказывает значительное влияние на когнитивную деятельность, точнее говоря на процессы обучения и памяти (Sandi 2004; Sandi and Pinelo-Nava 2007). Некоторые факторы определяют влияние, которое хронический стресс будет оказывать на когнитивную функцию. Уровни стресса имеют важное значение при определении того, будет ли стресс облегчать когнитивную функцию или будет оказывать вредное воздействие. Считается, что в ответ на стрессовые ситуации организм индуцирует гормоны стресса, которые оказывают обратный U-эффект в отношении обучения, памяти и пластичности. Baldi et al. (2005) Nonlinearity Biol Toxicol Med. 3(1) 9-21; Joels (2006) Trends Pharmacol Sci. 27(5):244-50. Таким образом, уровень стресса оказывает большое влияние на когнитивную функцию, при этом высокие уровни стресса приводят к высоким уровням гормонов стресса и снижению деятельности.
Было показано, что длительность стресса, хронического относительного острого, также играет важную роль с различным влиянием на когнитивную функцию, а также структуру и функцию головного мозга (Sandi and Loscertales 1999; Pinnock and Herbert 2001). Кроме того, стресс влияет на процесс формирования памяти, приводя к разным результатам, при этом острый стресс облегчает консолидацию (хранилище памяти) и ингибирует извлечение (мнемоническое воспроизведение) (Roozendaal, 2003). Кроме того, предсказуемость стресса также играет роль в отношении тяжести наблюдаемого влияния на когнитивную деятельность (Maier and Watkins, 2005).
Кроме того, ситуация, при которой возникает хронический стресс, а также индивидуальные различия стрессовой реакции, свойственной индивидуумам и полам, играют важную роль в определении конечного влияния хронического стресса на когнитивную функцию (Bowman, Beck et al., 2003; Shors, 2004; Joels, Pu et al., 2006).
Биологическая основа влияния хронического стресса еще хорошо не определена. Однако общим наблюдаемым признаком является ключевая роль глюкокортикоидов в опосредовании как облегчающего, так и ослабляющего действия стресса в отношении разных процессов и фаз памяти. Тогда как механизм действия глюкокортикоидов еще должен быть выяснен, in vitro было показано, что он ослабляет рост нейронов, индуцируемый фактором роста нервов (NGF). Unsicker et al. (1978) Proc Natl Acad Sci USA. 75:3498-502. Более того, структура нейронов и рост нейритов, индуцируемый такими факторами как NGF, прочно коррелируют с их нейропротекторной активностью, что снова позволяет предположить, что структура нейронов имеет важное значение для когнитивной функции.
Стресс и структурное ремоделирование
Первоначально, гиппокамп представлял собой область головного мозга, которой уделялось пристальное внимание из-за многочисленных сообщений, указывающих на ухудшающее влияние хронического стресса на задачи для памяти, зависящей от гиппокампа. Однако в настоящее время тщательные исследования подтверждают более целостное влияние хронического стресса на весь головной мозг, при этом также существуют данные об основных изменениях для префронтальной коры и миндалевидного тела. Изменения дендритного ветвления и синаптогенеза, происходящие в миндалевидном теле, являются вероятными кандидатами для участия в изменениях настроения, вызванных стрессом. Кроме того, считается, что изменения, происходящие на уровне гиппокампа и префронтальной коры, играют ключевую роль в изменениях настроения, вызванных стрессом.
Гиппокамп. Гиппокамп хорошо известен своей решающей ролью в процессах памяти. На гиппокамп-зависимые задачи, в целом, влияют воздействия как острого, так и хронического стресса. В нейровизуализационных исследованиях у людей сообщали об атрофии гиппокампа в сочетании с когнитивными и нейропсихическими изменениями, связанными со стрессом и глюкокортикоидами, включая депрессию.
У грызунов заметным и много раз повторяемым эффектом является дендритная атрофия апикальных дендритов пирамидальных нейронов СА3. Данное сниженное ветвление дендритов было ассоциировано с (i) уменьшением синаптической плотности возбуждающих глутаматергических синапсов; (ii) уменьшением объема сложных дендритных шипиков, называемых дендритными наростами, которые расположены на проксимальном апикальном дендрите и соме пирамидальных клеток СА3, и которые служат в качестве постсинаптических мишеней для синаптического входа мшистых волокон; и (iii) реорганизацией синаптических пузырьков и митохондрий в окончаниях афферентных мшистых волокон. В свою очередь, также существуют данные о синаптическом ремоделировании - с точки зрения изменений синаптических характеристик - для области гиппокампа СА1.
Префронтальная кора. Префронтальная кора (PFC) и, в частности, ее медиальная часть (mPFC), играет ключевую роль в высших когнитивных процессах (включая исполнительную функцию, рабочую память, внимание), а также в интеграции когнитивной и эмоционально соответствующей информации. Следует отметить, что mPFC содержит высокие уровни глюкокортикоидных рецепторов и вовлечена в регуляцию вызванной стрессом активности гипоталамо-гипофизарно-надпочечниковой (HPA) системы. Как отмечено выше, клинические данные позволяют выделить mPFC как область, претерпевающую заметные изменения в широком спектре нервно-психических расстройств, включая депрессию.
Существует важное подтверждение вызванного стрессом сокращения дендритов в PFC на основе исследований на грызунах. В частности, было описано, что основное ремоделирование нейронов происходит в слое II/III mPFC вследствие повторяющегося воздействия хронического стресса или повторного лечения глюкокортикоидами. Основными описанными изменениями в данной области являются: (i) атрофия дендритов, включая уменьшение как общей длины, так и числа апикальных дендритов пирамидальных нейронов; и (ii) уменьшение плотности апикальных дендритных шипиков (теряется приблизительно одна треть всех аксо-шипиковых синапсов на апикальных дендритах пирамидальных нейронов).
Влияние антидепрессантов. Было показано, что лечение атипичным (модифицированным трициклическим) антидепрессантом тианептином (tianeptine) вызывает обратное развитие атрофии дендритов, вызванной хроническим стрессом, в пирамидальных нейронах СА3 у крыс. Кроме того, также существуют данные о том, что антидепрессанты облегчают аксональное и дендритное прорастание. Эти данные позволяют предположить, что антидепрессанты могут оказывать основное влияние на ремоделирование нейронов, обеспечивая основу для соответствующих схем, реорганизуемых в ходе восстановления от депрессии.
Стресс в начале жизни
Один из аспектов настоящего изобретения представляет собой способ лечения влияния стресса в начале жизни на настроение. Указанный способ включает этап введения нуждающемуся в этом субъекту терапевтически эффективного количества уролитина или его предшественника с обеспечением лечения влияния стресса в начале жизни на настроение, депрессии, тревоги и рискованного поведения.
Существуют данные о том, что стресс в начале жизни оказывает значительное отрицательное влияние на когнитивную деятельность, включая психологические параметры, такие как повышенные уровни или подверженность депрессии, тревоге и аномальному рискованному поведению. Heim С, Nemeroff СВ. (2001) Biol Psychiatry 49:1023-1039. Существуют данные о повышенных уровнях синдрома дефицита внимания и гиперактивности (СДВГ), посттравматического стрессового расстройства (ПТСР) и глубокой депрессии у индивидуумов, испытавших стресс в начале жизни. Famularo R et al. (1992) J Am Acad Child Adolesc Psychiatry 31:863-867; Pelcovitz D et al. (1994) J Am Acad Child Adolesc Psychiatry 33:305-312. Считается, что стресс в начале жизни оказывает влияние на гипоталамо-гипофизарно-надпочечниковую (HPA) ось. Ladd СО et al. (2000) Prog Brain Res 122:81-103. Ключевым эффектором, который, как считается, контролирует отвечаемость оси НРА на стресс, являются основные рилизинг-факторы кортикотропина (CRF).
CRF представляет собой 41-аминокислотный пептид, распространенный по всей ЦНС. Это включает клеточные тела медиальной мелкоклеточной области паравентрикулярного ядра гипоталамуса (PVN), центрального компонента оси НРА. При стрессе CRF высвобождается из нервных окончаний медианного возвышения в гипоталамо-гипофизарное кровообращение в системе воротной вены и переносится в переднюю долю гипофиза, где он связывается с рецепторами CRF (CRF1 и CRF2). Связывание CRF с рецептором CRF1 оказывает эффекты, которые напоминают о стрессе, депрессии и тревоге. Связывание CRF с рецептором CRF2 стимулирует выработку и высвобождение адренокортикотропного гормона (АКТГ), который в свою очередь стимулирует выработку глюкокортикоидов, вовлеченных в стрессовую реакцию.
В моделях стресса в начале жизни, вызванного отделением от матери, наблюдают соответствующий длительный повышенный уровень мРНК CRF. Plotsky РМ et al. (2005) Neuropsychopharmacology 30:2192-2204. Было показано, что такие повышения CRF оказывают влияние на уровень миндалевидного тела при увеличении реакции на тревогу. Считается, что постоянная сенсибилизация нейроцепей CRF ответственна за аномально повышенную тревогу, депрессию и рискованное поведение, наблюдаемое у мышей, подвергнутых стрессу в начале жизни.
Современные стратегии с использованием антидепрессантов для облегчения психологических расстройств, обусловленных стрессом в начале жизни
Ряд исследований продемонстрировал, что антидепрессанты снижают активность CRF в оси НРА у грызунов и приматов, включая людей. Banki CM et al. (1992) J Affect Disord 25:39-45; Brady LS et al. (1992) Brain Res 572:117-125; Brady LS et al. (1991) J Clin Invest 87:831-837; De Bellis MD et al. (1993) Am J Psychiatry 150:656-657; Veith RC et al. (1993) Psychiatry Res 46:1-8. Некоторые классы антидепрессантов, по-видимому, вызывают уменьшение активности одной или более нейронных систем CRF. Они включают селективные ингибиторы обратного захвата 5-НТ (SSRI), которые, как было показано, эффективны в лечении некоторых психических расстройств, которые ассоциировали со стрессом в начале жизни (например, депрессия и ПТСР). Hidalgo RB et al. (2000) J Psychopharmacol 14:70-76. В частности, в рандомизированном плацебо-контролируемом исследовании субъекты, испытавшие стресс в начале жизни и страдающие ПТСР, реагировали на флуоксетин (fluoxetine), van der Kоlk ВA et al. (1994) J Clin Psychiatry 55:517-522. Кроме того, SSRI, включая флуоксетин и пароксетин (paroxetine), демонстрируют значительную эффективность по сравнению с плацебо в лечении депрессии с ранним началом у детей и подростков. Martin A et al. (2000) Child Adolesc Psychiatr Clin N Am 9:135-157. Также было обнаружено, что трициклические антидепрессанты «отменяют» повышенную реактивность оси НРА на стресс у взрослых приматов, подвергнутых материнской депривации. Suomi SJ. (1991) Ciba Found Symp 156:171-183. Представляется, что некоторые доступные лекарственные средства, включая SSRIs, могут оказывать полезный эффект в лечении детей и взрослых, подвергнутых стрессу в начале жизни. Fisher PA et al. (2000) J Am Acad Child Adolesc Psychiatry 39:1356-1364.
Дополнительные показания
Настоящее изобретение также найдет применение в лечении любого из множества дополнительных заболеваний и состояний, при которых нарушенная или сниженная активность митохондрий участвует в патофизиологии заболевания и состояния или при которых повышенная функция митохондрий будет производить желаемый полезный эффект. В качестве примера, настоящее изобретение также включает способы и соединения, которые можно применять для лечения мужского бесплодия, ассоциируемого со сниженной подвижностью сперматозоидов. Nakada et al. (2006) Proc Natl Acad Sci USA. 103:15148-53. В качестве другого примера, настоящее изобретение также включает способы и соединения, которые можно применять для лечения дегенерации желтого пятна и некоторых других возрастных и наследственных болезней глаз. Khandhadia et al. (2010) Expert Rev Mol Med. 12:e34; Jarrett et al. (2010) Ophthalmic Res. 44:179-90. Другим примером является способ лечения потери слуха, включая, но не ограничиваясь ею, возрастную потерю слуха. В случае каждого из этих и других показаний указанный способ включает введение субъекту, нуждающемуся в таком лечении, эффективного количества уролитина или его предшественника, описанного в настоящем документе, для лечения указанного показания.
Составы и клиническое применение
В настоящем описании термин «субъект» относится к живому позвоночному. В одном из вариантов реализации субъект представляет собой млекопитающее. В одном из вариантов реализации субъект представляет собой человека.
В настоящем описании термин «лечить», употребляемый в отношении заболевания, нарушения или состояния субъекта, означает уменьшать на детектируемую величину по меньшей мере одно клиническое или объективное проявление указанного заболевания, нарушения или состояния субъекта. В одном из вариантов реализации термин «лечить», употребляемый в отношении заболевания, нарушения или состояния субъекта, означает вылечивать указанное заболевание, нарушение или состояние субъекта.
Уролитин или его предшественник может быть введен субъекту (например, млекопитающему) отдельно или совместно с другим агентом различными способами. Например, уролитин или его предшественник может быть введен перорально или парентерально. Термин «парентерально» включает, без ограничения, внутривенно, внутримышечно, интраперитонеально, подкожно, интраартикулярно, внутрь сустава, интраокулярно, интратекально, местно или посредством ингаляции. Таким образом, форма дозы уролитина или его предшественника может представлять собой различные формы, включая натуральные пищевые продукты, переработанные продукты питания, натуральные соки, концентраты и экстракты, растворы для инъекций, микрокапсулы, нанокапсулы, липосомы, пластыри, ингаляционные формы, спреи для носа, капли для носа, глазные капли, сублингвальные таблетки и препараты с замедленным высвобождением.
Соединения согласно настоящему изобретению могут быть представлены в выделенной форме. В настоящем описании термин «выделенный» означает по существу отделенный от других соединений или компонентов, с которыми представляющее интерес соединение может встречаться в ином случае, например, встречаться в природе. В одном из вариантов реализации соединение является выделенным, когда оно по существу полностью отделено от других соединений или компонентов, с которыми представляющее интерес соединение может встречаться в ином случае. В одном из вариантов реализации соединение является выделенным, когда оно является чистым.
Соединения согласно настоящему изобретению могут быть включены в различные составы для терапевтического введения. В частности, соединения согласно настоящему изобретению могут быть включены в состав фармацевтических композиций путем комбинирования с соответствующими фармацевтически приемлемыми носителями или разбавителями, и могут быть включены в состав препаратов в твердой, полутвердой, жидкой или газообразной формах, таких как таблетки, капсулы, порошки, гранулы, мази, растворы, суппозитории, препараты для инъекций, препараты для ингаляции, гели, микросферы и аэрозоли. Таким образом, введение соединений можно осуществлять различными способами, включая пероральное, трансбуккальное, ректальное, парентеральное, интраперитонеальное, внутрикожное, трансдермальное и внутритрахеальное введение. Активный агент может оказывать системное действие после введения или может быть локализован путем использования регионарного введения, интрамурального введения или использования имплантата, который действует таким образом, чтобы поддерживать активную дозу в месте имплантации.
Соединения согласно настоящему изобретению также могут быть представлены в виде пищевых добавок, пищевых ингредиентов, функциональных продуктов питания, добавок к рациону, продуктов лечебного питания, нутрицевтиков или биологически активных добавок.
В фармацевтических лекарственных формах соединения могут быть введены в форме их фармацевтически приемлемых солей. Они также могут быть использованы в соответствующем сочетании с другими фармацевтически активными соединениями. Следующие методы и наполнители являются лишь иллюстративными и никоим образом не ограничивающими.
Для пероральных препаратов соединения могут быть использованы отдельно или в комбинации с соответствующими добавками с получением таблеток, порошков, гранул или капсул, например, с традиционными добавками, такими как лактоза, маннит, кукурузный крахмал или картофельный крахмал; со связующими веществами, такими как кристаллическая целлюлоза, производные целлюлозы, аравийская камедь, кукурузный крахмал или желатин; с разрыхлителями, такими как кукурузный крахмал, картофельный крахмал или натрийкарбоксиметилцеллюлоза; со смазывающими веществами, такими как тальк или стеарат магния; и при необходимости с разбавителями, буферными агентами, увлажняющими агентами, консервантами и ароматизаторами.
Соединения могут быть включены в состав препаратов для инъекций путем растворения, суспендирования или эмульгирования их в водном или неводном растворителе, таком как растительные или другие подобные масла, синтетические глицериды алифатических кислот, сложные эфиры высших алифатических кислот или пропиленгликоль; и при необходимости с традиционными добавками, такими как солюбилизаторы, изотонические агенты, суспендирующие агенты, эмульгаторы, стабилизаторы и консерванты.
Соединения могут быть использованы в составе для аэрозоля для введения посредством ингаляции. Соединения согласно настоящему изобретению могут быть включены в состав приемлемых пропеллентов, находящихся под давлением, таких как дихлордифторметан, пропан, азот и т.п.
Кроме того, соединения могут быть введены в состав суппозиториев путем смешивания с различными основаниями, такими как эмульгирующие основания или водорастворимые основания. Соединения согласно настоящему изобретению могут быть введены ректально посредством суппозитория. Указанный суппозиторий может содержать носители, такие как масло какао, карбовоски и полиэтиленгликоли, которые плавятся при температуре тела, но остаются твердыми при комнатной температуре.
Могут быть получены единичные лекарственные формы для перорального или ректального введения, такие как сиропы, эликсиры и суспензии, при этом каждая единица дозирования, например, чайная ложка, столовая ложка, таблетка или суппозиторий, содержит заранее определенное количество композиции, содержащей одно или более соединений согласно настоящему изобретению. Подобным образом, единичные лекарственные формы для инъекции или внутривенного введения могут содержать соединение согласно настоящему изобретению в композиции в виде раствора в стерильной воде, физиологическом растворе или другом фармацевтически приемлемом носителе, при этом каждая единица дозирования, например, мл или л, содержит заранее определенное количество композиции, содержащей одно или более соединений согласно настоящему изобретению.
Имплантаты для составов с замедленным высвобождением хорошо известны в данной области техники. Имплантаты получают в виде микросфер; пластинок и т.д., с биоразлагаемыми или небиоразлагаемыми полимерами. Например, полимеры молочной кислоты и/или гликолевой кислоты образуют распадаемый полимер, который хорошо переносится хозяином. Имплантат, содержащий ингибирующие соединения, может быть помещен рядом с представляющим интерес участком так, чтобы локальная концентрация активного агента увеличивалась по сравнению с остальной частью организма.
В настоящем описании термин «единичная лекарственная форма» относится к физически раздельным объектам, подходящим для использования в качестве единичных доз для введения субъектам, представляющим собой человека и животное; причем каждая доза содержит заранее определенное количество соединений согласно настоящему изобретению, рассчитанное в количестве, достаточном для обеспечения необходимого эффекта, совместно с фармацевтически приемлемым разбавителем, носителем или наполнителем. Описание новых единичных лекарственных форм согласно настоящему изобретению зависит от конкретного используемого соединения и достигаемого эффекта, и фармакодинамики, ассоциируемой с каждым соединением в организме хозяина.
Фармацевтически приемлемые наполнители, такие как носители, адъюванты, носители или разбавители, общедоступны. Кроме того, фармацевтически приемлемые вспомогательные вещества, такие как агенты, регулирующие рН, и буферные агенты, агенты, регулирующие тоничность, стабилизаторы, смачивающие агенты и т.п., общедоступны.
Для клинического применения уролитин или предшественник уролитина вводят в терапевтически эффективном количестве. В настоящем описании термин «эффективное количество» относится к количеству, которое является достаточным для оказания необходимого биологического действия. В настоящем описании термин «терапевтически эффективное количество» относится к количеству, достаточному для оказания, в однократной дозе или многократных дозах, необходимого терапевтического эффекта. Специалист в данной области техники может определить терапевтически эффективные количества на основе исследований in vitro, доклинических или клинических исследований, или любой их комбинации.
Введение доз, как правило, будет происходить ежедневно-еженедельно. В одном из вариантов реализации введение доз происходит по меньшей мере еженедельно. Например, субъект может получать одну дозу один раз в неделю, два раза в неделю, три раза в неделю или через день. В одном из вариантов реализации введение доз происходит по меньшей мере ежедневно. Например, субъект может получать одну или более доз ежедневно.
Для клинического применения уролитин, как правило, будут вводить в количестве в диапазоне от примерно 0,2-150 миллиграмм (мг) уролитина на килограмм (кг) массы тела субъекта. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 2-120 мг уролитина на кг массы тела субъекта. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 4-90 мг уролитина на кг массы тела субъекта. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, равной или эквивалентной 8-30 мг уролитина на кг массы тела субъекта. В случае, когда предшественник уролитина должен быть введен вместо уролитина, его вводят в количестве, эквивалентном вышеуказанным количествам уролитина.
Любая конкретная доза может быть введена в виде однократной дозы или в виде разделенных доз.
В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения по меньшей мере 0,001 микромолярного (мкМ) пикового уровня в сыворотке. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 0,01 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 0,1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 5 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения пикового уровня в сыворотке, составляющего по меньшей мере 10 мкМ.
В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения по меньшей мере 0,001 микромолярного (мкМ) долговременного уровня в сыворотке. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 0,01 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 0,1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 1 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 5 мкМ. В одном из вариантов реализации уролитин или его предшественник вводят в дозе, достаточной для достижения длительного уровня в сыворотке, составляющего по меньшей мере 10 мкМ. Длительный уровень в сыворотке может быть измерен с использованием любого подходящего метода, например, высокоэффективной жидкостной хроматографии (ВЭЖХ) или ВЭЖХ-МС.
В одном из вариантов реализации уролитин или его предшественник вводят в виде гранатового сока в количестве, составляющем от 25 мл до 5 л, или эквивалентной дозы эллагитаннинов, эллаговой кислоты, уролитинов или их любой комбинации. В Таблице 4 показано поглощение различных соединений граната для различных уровней гранатового сока. Диапазон охватывает различия в концентрации соединений среди разных сортов граната. Для расчетов эквивалентов эллаговой кислоты считали, что метаболизм каждого моля пуникалагина приводил к высвобождению 1 моля эллаговой кислоты, и что данное превращение происходило со 100% эффективностью. Уровни уролитина определяли путем предположения, что вся присутствующая эллаговая кисла, включая получаемую из пуникалагина, превращалась в уролитин со 100% эффективностью. Другие источники эллаговой кислоты кроме пуникалагина и эллаговой кислоты, не учитывали.
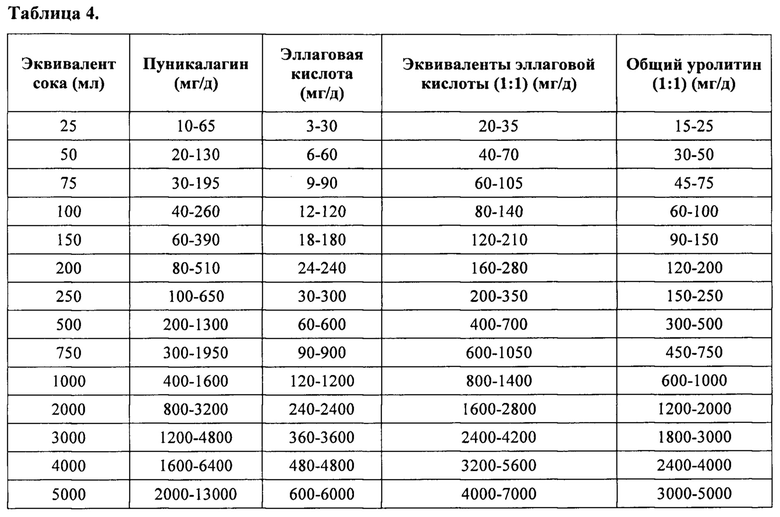
В одном из вариантов реализации субъект не принимает уролитин или его предшественник для какой-либо цели, отличной от лечения состояния в соответствии со способами согласно настоящему изобретению. В одном из вариантов реализации субъект не принимает уролитин или его предшественник для лечения атеросклероза, тромбоза, рака, нежелательного ангиогенеза, инфекции или воспаления.
ПРИМЕРЫ
Ниже следует подробное описание изобретения, которое будет легче понять из приведенных далее примеров, включенных исключительно с целью иллюстрации определенных аспектов и вариантов реализации настоящего изобретения и не ограничивающих область изобретения.
Пример 1
Приготовление функциональных экстрактов из соединений граната
Содержащие специфические молекулы экстракты граната, описанные в настоящей заявке, готовили методом экстракции, основанной на адсорбции полифенолов в стандартной колонке для адсорбции полимеров согласно описанию. Для приготовления экстрактов 31008 и 1108, полученных из сока граната, плоды граната выжимали с использованием стандартного метода отжима сока и производственного процесса, затем чистый сок адсорбировали на полимерной хроматографической смоле. Полупрепаративную колонку заполняли смолой Amberlite XAD-16 (Rohm&Haas) и загружали экстрагированным соком. Колонку промывали водой до полного удаления сахаров (уровни по шкале Брикса были ниже 0,1%). Полифенолы элюировали 100% этанолом. Остаточный этанол выпаривали под вакуумом для получения концентрированного экстракта, содержащего 4,5 г общих полифенолов на литр, которые определяли с помощью реакции Фолина для оценки общего содержания полифенолов. Экстракт 1011 готовили тем же способом, что и экстракты 31008 и 1108, однако жидкий экстракт затем сушили распылением с использованием распылительной сушилки для получения конечного порошкового экстракта. Используя ВЭЖХ-МС для идентификации соединений, было обнаружено, что экстракты 31008, 1108 и 1011 содержат молекулы пуникалагин, пуникалин, теллимаграндин и педункулагин.
Экстракт 71109, полученный из кожицы граната, был приготовлен вручную путем отделения кожицы от семенных оболочек мякоти граната с последующим прессованием ручным прессом для фруктов. Чтобы экстрагировать максимальное количество полифенолов брикет/жмых прессованных частей граната последовательно вымачивали в воде в течение нескольких периодов времени (5 минут) для повышения эффективности экстракции. Экстрагированный из граната раствор осветляли центрифугированием перед адсорбцией на полимерной хроматографической смоле Amberlite XAD-16 (Rohm & Haas), упакованной в полупрепаративную колонку, и загружали водой, экстрагированной из кожицы граната. Колонку промывали водой до полного удаления сахаров (уровни по шкале Брикса были ниже 0,1%). Полифенолы элюировали 100% этанолом. Остаточный этанол выпаривали под вакуумом с получением концентрированного экстракта, содержащего 17,1 г общих полифенолов на литр, которые определяли с помощью реакции Фолина для оценки общего содержания полифенолов. Эта методика является модификацией способов, известных в данной области техники, как описано в нескольких опубликованных методах очистки полифенолов из различных растений и ягод. Tuck, K.L. and P.J. Hayball (2002) «Major phenolic compounds in olive oil: metabolism and health effects» J Nutr Biochem 13(11):636-644; и Schieber, A., P. Hilt, et al. (2003) «A new process for the combined recovery of pectin and phenolic compounds from apple pomace.» Innovative Food Sci. Emerging Technol. 4:99-107.
Для приготовления экстракта 61109 водный экстракт граната фракционировали с использованием центробежной распределительной хроматографии. Выделенные фракции лиофилизировали для получения экстракта 61109, обогащенного пуникалагином (>90%).
Очистка пуникалагина
Приготовление экстракта
Экстракт граната растворяли в 16 мл смеси органической/водной фазы (1:1) и фильтровали через тефлоновый фильтр (0,45 мкм).
Отделение пуникалагина от экстракта с использованием центробежной распределительной хроматографии
Пуникалагин отделяли от экстракта граната методом центробежной распределительной хроматографии (ЦРХ). ЦРХ проводили на устройстве FCPC® 1000, предоставленном Kromaton Technologies (Анжер, Франция) и оснащенном ротором емкостью 1000 мл. Растворители закачивали 4-плунжерным бинарным градиентным насосом высокого давления. Образцы вводили в колонку для ЦРХ через клапан высокого давления для впрыска (Rheodyne), снабженный пробоотборной петлей емкостью 20 мл. Элюат контролировали с помощью диодноматричного детектора (DAD), снабженного проточной препаративной ячейкой. Фракции собирали, используя коллектор фракций. Этапы отделения проводили при комнатной температуре.
Для проведения экстракции в колонку сначала вводили стационарную фазу в восходящем режиме без вращения, затем через стационарную фазу закачивали подвижную фазу до достижения равновесного состояния. После этого увеличивали скорость вращения от 0 до 1000 оборотов в минуту и закачивали подвижную фазу в колонку при скорости потока 20 мл/мин. После введения 10 г экстракта граната фракции объемом по 20 мл собирали каждую минуту. Состав выходящей органической фазы контролировали, измеряя поглощение в УФ-диапазоне при λ=260 нм в режиме реального времени.
Методику элюирования-экструзии использовали для выделения всех соединений из колонки: после классического элюирования в течение 100 мин подвижную фазу заменили стационарной фазой, которую использовали в качестве подвижной жидкости до полного вытеснения всего содержащегося в колонке объема (1000 мл). Фракцию, содержащую пуникалагины (смесь А- и В-изомеров), хроматографическая чистота которой составила 94-97%, получили в промежуток времени между 51-й и 63-й минутами элюции, вторую фракцию с хроматографической чистотой 85-88% получили между 64-й и 79-й минутами.
Для определения уровня чистоты очищенный образец исследовали методом ВЭЖХ и контролировали с помощью диодноматричного детектора при длине волны детекции 260 нм. Образец разделяли на колонке Prosontil С18, 5 мкм, 250×4 мм. Использовали такие растворители как H2O mQ+9,1% ТФУ/ацетонитрил + 0,1% ТФУ при скорости потока 1 мл/мин.
Пример 2
Скрининговое исследование in vitro соединений, способствующих повышению экспрессии митохондриальных генов в прототипной линии клеток скелетных мышц (миобласты линии С2С12).
Скелетные мышцы играют ключевую роль в регуляции метаболического гомеостаза, поскольку они участвуют в метаболических функциях, таких как потребление энергии и поддержание чувствительности к инсулину. Эти функции тесно связаны с митохондриальной активностью, и нарушение функции митохондрий имеет причинную связь с дефектным метаболическим гомеостазом и развитием нарушений обмена веществ, таких как диабет 2 типа, ожирение и дислипидемия. Профиль экспрессии генов, участвующих в поддержании митохондриальной активности в дифференцированных клетках С2С12 (мышечные трубочки), является подходящей моделью для оценки влияния соединений на активность митохондрий, посредством исследования многочисленных путей, которые отражают активность митохондрий, например, митохондриальный биогенез, гликолиз, β-окисление жирных кислот, функционирование электрон-транспортной цепи (ЭТЦ), митохондриальная динамика.
Чтобы оценить влияние соединений на экспрессию митохондриальных генов миобласты линии С2С12 дифференцировали в мышечные трубочки, удаляя сыворотку из культуральной среды на 4 дня ( et al. (2009) Nature. 458:1056-60). Мышечные трубочки инкубировали в течение 48 ч с эллаговой кислотой или уролитином А в конечной концентрации 1, 10 или 50 мкМ (все соединения были растворены в ДМСО, конечная концентрация 0,1%). ДМСО использовали в качестве контроля (конечная концентрация 0,1%). В конце обработки клетки промывали фосфатно-солевым буфером (PBS), после чего немедленно экстрагировали мРНК в соответствии с инструкциями производителя (Trizol Reagent, Invitrogen), добавляя 1 мл реагента тризола. После экстракции кДНК получали обратной транскрипцией в соответствии с инструкциями производителя.
et al. (2009) Nature. 458:1056-60). Мышечные трубочки инкубировали в течение 48 ч с эллаговой кислотой или уролитином А в конечной концентрации 1, 10 или 50 мкМ (все соединения были растворены в ДМСО, конечная концентрация 0,1%). ДМСО использовали в качестве контроля (конечная концентрация 0,1%). В конце обработки клетки промывали фосфатно-солевым буфером (PBS), после чего немедленно экстрагировали мРНК в соответствии с инструкциями производителя (Trizol Reagent, Invitrogen), добавляя 1 мл реагента тризола. После экстракции кДНК получали обратной транскрипцией в соответствии с инструкциями производителя.
Уровень экспрессии генов (PGC-1α, Tfam, PFKFB3, CPT1b, MCAD, LCAD, Ndufa2, Cyt с и Mfn2), контролирующих митохондриальную функцию, оценивали методом количественной ПЦР в реальном времени (Watanabe et al. (2004) J Clin Invest. 113:1408-18) с помощью следующего набора праймеров (Fwd: прямой праймер, Rev: обратный праймер):

PGC-1α (PPARγ-корегулятор 1α) и Tfam (митохондриальный транскрипционный фактор) являются управляющими регуляторами функции митохондрий, в частности митохондриального биогенеза и митохондриального фосфорилирующего окисления (mOXPHOS). Увеличение уровня их экспрессии выявляет общее повышение активности митохондрий. Оценка других генов-мишеней, участвующих в ключевых функциях митохондрий, позволяет определить пути с повышенной активностью. PFKFB3 (6-фосфофрукто-2-киназа/фруктозо-2,6-бифосфатаза 3) является ключевым ферментом гликолиза, т.е. процесса использования глюкозы для получения энергии. В аэробных условиях (т.е. когда есть поступление кислорода) пируват, полученный из глюкозы в процессе гликолиза, используется митохондриями для производства энергии (АТФ) в цикле Кребса. CPT1b (карнитин О-пальмитоилтрансфераза 1b), MCAD (ацил-КоА дегидрогеназа жирных кислот со средней длиной цепи) и LCAD (ацил-КоА дегидрогеназа жирных кислот с длинной цепью) играют ключевую роль в митохондриальном поглощении жирных кислот и β-окислении - двух важных стадиях производства энергии из жирных кислот. Ndufa2 (субъединица 2 подкомплекса НАДН дегидрогеназа [убихинон] 1 альфа) и Cyt с (цитохром С) являются субъединицами комплекса I и IV митохондриальной электрон-транспортной цепи, соответственно. Эти белки играют важную роль в дыхательной цепи митохондрий и производстве энергии из восстановленных эквивалентов, синтезированных в цикле Кребса. Mfn2 (митофузин 2) участвует в митохондриальной динамике и слиянии. Его экспрессия увеличивается при повышенном митохондриальном ремоделировании и/или митохондриальном биогенезе (увеличение количества митохондрий на клетку).
Данные, приведенные на ФИГ. 3, четко показывают, что эллаговая кислота и уролитин А повышают активность митохондрий дозазависимым образом, модулируя экспрессию множества генов, которые вовлечены в регуляцию некоторых путей митохондриального метаболизма.
Пример 3
Скрининговое исследование in vitro соединений, способствующих повышению митохондриальной активности в прототипной линии клеток скелетных мышц (миобласты линии С2С12)
Цитратсинтаза - это первый фермент цикла трикарбоновых кислот (ЦТК) и ее активность является лимитирующей стадией вхождения в ЦТК. В ЦТК производятся НАДН2 и ФАДН2, которые затем служат в качестве источников энергии для электрон-транспортной цепи, генерирующей протонный (энергетический) градиент, который будет использован при синтезе АТФ. Таким образом, цитратсинтаза является уникальным маркером количества митохондрий и их активности. Измеряя влияние соединений или составов на активность фермента цитратсинтазы можно оценить способность соединений стимулировать активность митохондрий (т.е. OXPHOS и синтез АТФ).
Фермент цитратсинтаза катализирует реакцию между ацетил-коферментом А (ацетил-КоА) и щавелевоуксусной кислотой с образованием лимонной кислоты. Ацетил-КоА добавляет 2 атома углерода к 4 атомам углерода в оксалоацетате, в результате чего образуется цитрат, содержащий 6 атомов углерода. Гидролиз сложного тиоэфира ацетил-КоА приводит к образованию КоА с тиольной группой (KoA-SH). Активность цитратсинтазы измеряют посредством реакции между тиолом KoA-SH и ДТНБ в смеси с образованием 5-тио-2-нитробензойной кислоты (ТНБ). Образование желтого продукта (ТНБ) наблюдают спектрофотометрически, измеряя оптическую плотность при 412 нм (набор для определения цитратсинтазы, каталожный номер CS0720, Sigma Aldrich).
Миобласты линии С2С12 дифференцировали в мышечные трубочки, удаляя из культуральной среды сыворотку на 4 дня ( et al. (2009) Nature. 458:1056-60). Мышечные трубочки инкубировали в течение 48 ч с пуникалагином в конечной концентрации 1 или 10 мкМ или с эллаговой кислотой или уролитином А в конечной концентрации 1, 10 или 50 мкМ (все соединения были растворены в ДМСО, конечная концентрация 0,1%). ДМСО использовали в качестве контроля (конечная концентрация 0,1%). В конце обработки клетки промывали 3 раза фосфатно-солевым буфером и исследовали на активность цитратсинтазы в соответствии с инструкциями производителя (набор для определения цитратсинтазы, каталожный номер CS0720, Sigma Aldrich).
et al. (2009) Nature. 458:1056-60). Мышечные трубочки инкубировали в течение 48 ч с пуникалагином в конечной концентрации 1 или 10 мкМ или с эллаговой кислотой или уролитином А в конечной концентрации 1, 10 или 50 мкМ (все соединения были растворены в ДМСО, конечная концентрация 0,1%). ДМСО использовали в качестве контроля (конечная концентрация 0,1%). В конце обработки клетки промывали 3 раза фосфатно-солевым буфером и исследовали на активность цитратсинтазы в соответствии с инструкциями производителя (набор для определения цитратсинтазы, каталожный номер CS0720, Sigma Aldrich).
Как показано на ФИГ. 4, пуникалагин, эллаговая кислота и уролитин А увеличивают активность цитратсинтазы дозазависимым образом, что указывает на общее увеличение активности митохондрий и/или плотности митохондрий (количество митохондрий в клетках). Эти результаты подтверждают результаты, полученные на основании профиля экспрессии митохондриальных генов (пример 1), который демонстрирует повышение активности митохондрий и митохондриального биогенеза в обработанных дифференцированных С2С12.
Статистика: однофакторный дисперсионный анализ *р<0,05.
Пример 4
Скрининговое исследование in vitro соединений повышающих активность 5'АМФ-активируемой протеинкиназы (АМФК) в прототипной линии клеток скелетных мышц (мышечные трубочки С2С12)
АМФК действует как главный метаболический выключатель, регулирующий несколько внутриклеточных систем, включая клеточное поглощение глюкозы, β-окисление жирных кислот, а также биогенез транспортера глюкозы 4 (GLUT4) и митохондрий. Способность АМФК воспринимать изменения энергетического статуса может быть связана со способностью фермента детектировать и реагировать на колебания соотношения АМФ:АТФ, которые происходят во время отдыха и физических упражнений (стимуляция мышц). Например, во время серии физических упражнений активность АМФК возрастает (фосфорилирование АМФК, P-АМФК), тогда как мышечная клетка испытывает метаболический стресс, вызванный чрезвычайно сильной потребностью клетки в АТФ. После активации (фосфорилирование АМФК, Р-АМФК) АМФК увеличивает энергетические уровни в клетке, ингибируя анаболические энергоемкие пути (синтез жирных кислот, синтез белка и т.д.) и стимулируя производящие энергию катаболические пути (окисление жирных кислот, транспорт глюкозы и т.д.). Следовательно, активация АМФК приводит к усилению митохондриальной функции, включая повышенный OXPHOS и митохондриальный биогенез.
Миобласты С2С12 дифференцировали в мышечные микротрубочки путем удаления сыворотки из культуральной среды на 4 дня ( et al. (2009) Nature. 458:1056-60). Мышечные трубочки инкубировали в течение 1 часа с ресвератролом (RSV), который служил в качестве положительного контроля, или эллаговой кислотой (ЕА) или уролитином A (UL) в конечной концентрации 50 мкМ (все соединения были растворены в ДМСО, конечная концентрация 0,1%). ДМСО использовали в качестве контроля (конечная концентрация ДМСО 0,1%). В конце обработки клетки промывали 3 раза фосфатно-солевым буфером и оценивали активность АМФ-активируемой протеинкиназы (АМФК) методом Вестерн-блоттинга. После обработки соединением клетки линии С2С12 лизировали в буфере, содержащем ингибиторы фосфатазы, концентрацию белка определяли с помощью стандартного анализа Брэдфорда. Эквивалент 25 мкг белка использовали для разделения на 10% ДСН-ПААГ геле и затем переносили с помощью стандартных методик для вестерн-блоттинга. Для детектирования фермента использовали антитела к АМФК (Cell Signaling) и фосфорилированной АМФК (Р-АМФК, Cell Signaling).
et al. (2009) Nature. 458:1056-60). Мышечные трубочки инкубировали в течение 1 часа с ресвератролом (RSV), который служил в качестве положительного контроля, или эллаговой кислотой (ЕА) или уролитином A (UL) в конечной концентрации 50 мкМ (все соединения были растворены в ДМСО, конечная концентрация 0,1%). ДМСО использовали в качестве контроля (конечная концентрация ДМСО 0,1%). В конце обработки клетки промывали 3 раза фосфатно-солевым буфером и оценивали активность АМФ-активируемой протеинкиназы (АМФК) методом Вестерн-блоттинга. После обработки соединением клетки линии С2С12 лизировали в буфере, содержащем ингибиторы фосфатазы, концентрацию белка определяли с помощью стандартного анализа Брэдфорда. Эквивалент 25 мкг белка использовали для разделения на 10% ДСН-ПААГ геле и затем переносили с помощью стандартных методик для вестерн-блоттинга. Для детектирования фермента использовали антитела к АМФК (Cell Signaling) и фосфорилированной АМФК (Р-АМФК, Cell Signaling).
Как показано на ФИГ. 5, Вестерн-блоттинг анализ фосфорилированной и, таким образом, активированной формы АМФК, т.е. Р-АМФК, показал, что уровни фосфорилирования АМФК (Р-АМФК) и, следовательно, активации АМФ-активируемой протеинкиназы (АМФК) действительно повышались в клетках, обработанных эллаговой кислотой или уролитином А по сравнению с контрольными необработанными клетками. Эти данные показывают, что оба соединения - эллаговая кислота и уролитин А - являются активаторами АМФК. Этот результат дополнительно подтверждает наблюдение, что эллаговая кислота и уролитин А вызывают увеличение функции митохондрий.
Пример 5
Скрининговое исследование соединений, усиливающих рост нейритов в клетках линии РС-12
Было показано, что рост нейритов и среднее количество отростков на клетку в культуре нейронов соответствует функциональному статусу нейронов. Хронический стресс, как было показано, приводит к уменьшению как длины дендритов, так и числа ответвлений, причем это действие было обратимым после прекращения стресса. Кроме того, было показано, что подобная обратимость действия ингибируется с возрастом (Bloss, Janssen et al., 2010). Существует также еще одно доказательство того, что обучение и новый сенсорный опыт связаны с увеличением образования дендритных шипиков и устранением удлиненных отростков. Следовательно, структурная синаптическая пластичность играет важную роль в обучении и памяти (Yang, Pan et al., 2009). Действительно уровень роста нейритов и количество отростков, индуцированное соединениями, такими как фактор роста нервов (NGF), строго коррелирует с их нейропротекторными способностями. С возрастом синаптическая пластичность ухудшается, при этом увеличивается потеря шипиков и снижается плотность синапсов (Dumitriu, Нао et al., 2010). Нейродегенеративные заболевания также влияют на рост нейритов. Пептид А-бета (Аβ), играющий важную роль в болезни Альцгеймера, ингибирует рост нейритов в клетках нейробластомы мыши. Таким образом, соединения и составы, обладающие нейропротекторным действием на нейроны при хроническом стрессе, стареющие нейроны и нейроны, присутствующие при нейродегенеративных заболеваниях, могут быть идентифицированы путем исследования их влияния на рост нейритов in vitro.
Влияние различных эллагитаннинов и их метаболитов, таких как пуникалагин (РА), пуникалин (РВ), теллимаграндин (TL), эллаговая кислота (ЕА) и уролитин A (UA), на рост нейритов исследовали in vitro на клетках линии норадренергической феохромоцитомы крысы (клетки РС-12), которые, как было показано, дифференцируются в ответ на фактор роста нервов (ФРН) (Greene and Tischler 1976). Было показано, что рост нейритов в дифференцированных клетках РС-12 значительно усиливается дибутирил ц-АМФ (дбцАМФ) (Gunning, Landreth et al., 1981), это соединение использовали в качестве положительного контроля. В качестве отрицательного контроля использовали SP600125 - специфический ингибитор N-концевой киназы Януса (INK), который, как было показано, уменьшает различные параметры роста нейритов (Xiao, Pradhan et al., 2006). Эллагитаннины и их метаболиты, испытанные в исследовании, были синтезированы или приобретены у поставщиков, которые включали Funakoshi, Sigma и Chemos. Исходные растворы были разделены на аликвоты и хранились при -20°С.
Клетки РС-12 (АТСС CRL-1721) культивировали при 37°С, 5% CO2 в колбах для культур, покрытых поли-L-лизином, в полной культуральной среде (RPMI 1640+10% инактивированной нагреванием сыворотки лошади + 5% фетальной бычьей сыворотки).
Дифференцировку клеток проводили в колбах для культивирования через 24 ч после посева в полной среде, содержащей 100 нг/мл ФРН (2,5 S ФРН, Invitrogen). Среду с добавлением ФРН обновляли каждый третий день, дифференцировку индуцировали в течение 8-дневного периода.
Все испытываемые соединения готовили непосредственно перед экспериментом в виде 50 мМ исходного раствора в диметилсульфоксиде (ДМСО). Конечная концентрация ДМСО в среде всех экспериментальных групп была 0,1%.
Для измерения роста нейритов дифференцированные клетки промывали фосфатно-солевым буфером (PBS), собирали после открепления от подложки и высевали в плотности 5000 клеток/лунку (96-луночный планшет, BD BioCoat™ imaging) в полной среде, содержащей 100 нг/мл ФРН с/без 10 мкМ SP600125 (отрицательный контроль), 1 мМ дбц-АМФ (положительный контроль), или испытываемого соединения в концентрации 5×10-7 М. В контрольной группе после повторного высевания недифференцированных клеток ФРН в среду не вносили.
Через 72 ч культивирования клетки РС-12 промывали фосфатно-солевым буфером и фиксировали в 1%-ном растворе параформальдегида в течение 20 минут. После 3 промывок фосфатно-солевым буфером проводили иммунофлуоресцентное окрашивание с использованием малеимидного производного зонда Texas Red, который вступает в реакцию с тиольной группой остатков цистеина белков, что позволяет визуализировать морфологию целых клеток, в том числе нейритов.
Иммунофлуоресцентный анализ проводили методом автоматизированной конфокальной микроскопии. Изображения были получены с помощью BD Pathway™ 855 системы под 20-кратным объективом с полем монтажа 8×8. Рост нейритов затем измеряли в полученных изображениях с помощью модуля программного обеспечения Metamorph® для анализа нейритов. Было проведено исследование общего и среднего роста, общего и среднего числа отростков в клетке, а также общего числа и доли клеток с интенсивным ростом нейритов (определенным как рост на расстояние более 20 мкм).
Все соединения, за исключением РА и РВ, увеличивали количество клеток РС-12 в лунках на >30%, как показано на ФИГ. 6, что указывает на трофическое действие этих соединений в концентрации 0,5 мкМ (р<0,001 для UA ЕА и TL по сравнению с дифференцированными контрольными клетками (ctrl)).
Увеличение роста нейритов
Как показано на ФИГ. 7 и ФИГ. 8, все испытанные соединения (РА, РВ, TL, ЕА и UA) были способны индуцировать мощный рост нейритов в дифференцированных клетках РС-12. Средняя величина роста (ФИГ. 7) увеличилась на >30% по сравнению с дифференцированными контрольными клетками для всех испытанных соединений. Процент клеток, демонстрирующих существенный рост (ФИГ. 8), был значительно больше, чем тот, который наблюдали в дифференцированных клетках для всех испытанных соединений (р<0,05 для UA и РВ (26% увеличение), р<0,01 для РА (>26% увеличение), р<0,001 для ЕА и TL (>37% увеличение)).
Усиление формирования отростков и ветвления
Соединения РА, РВ, UA, ЕА и TL все вызвали увеличение количества отростков, когда их применяли на дифференцированных клетках РС-12. Соединения (UA, р<0,05 (15,7% увеличение); РА, р<0,01 (26,3% увеличение); ЕА и TL, р<0,001 (>31% увеличение) усиливали формирование отростков с сопоставимой либо большей эффективностью по сравнению с дбц-АМФ, который использовали в качестве положительного контроля (ФИГ. 9).
Ветвление нейритов было значительно более выраженным, чем наблюдаемое в дифференцированных контрольных клетках, причем большая часть соединений индуцировала двукратное увеличение ветвления.
Пример 6
Скрининговое исследование соединений, усиливающих рост нейритов в первичной культуре дофаминергических ТГ-положителъных нейронов
Первичные культуры нейронов благодаря нетрансформированному состоянию нейрональных клеток служат хорошей in vitro моделью для изучения влияния соединений на маркеры пластичности и дифференцировки нейронов, такие как рост нейронов и формирование дендритов и отростков. Было исследовано влияние различных эллагитанинновых метаболитов, таких как пуникалагин (РА), уролитин A (UA), эллаговая кислота (ЕА) и теллимаграндин (TL) на этот процесс. Соединения, испытанные в данном исследовании, были приобретены у поставщиков, которые включали Funakoshi и Sigma, или химически синтезированы. Исходные растворы были разделены на аликвоты и хранились при -20°С.
Первичные культуры среднего мозга были получены из эмбрионов крыс Е14. Вентральную часть среднего мозга тщательно иссекали и диссоциировали. Затем клетки высевали в среду DMEM/F12, содержащую 10% инактивированной нагреванием сыворотки лошади, в плотности 100000 клеток/лунку (96-луночного планшета), с или без JNK-специфического ингибитора SP600125 (10 мкМ) (который служил в качестве отрицательного контроля) или дбц-АМФ (1 мМ) (который служил в качестве положительного контроля) или испытываемых соединений, каждое в дозе 0,1 мкМ.
Через 72 ч после посева измеряли влияние соединений на рост нейритов дофаминергических тирозингидроксилаза (ТН)-положительных нейронов на изображениях, полученных методом автоматизированной конфокальной микроскопии (4-кратный объектив, монтаж 4×4), охватывающей всю поверхность лунки, и количественно оценивали, используя модуль программного обеспечения Metamorph® для оценки роста нейритов. Таким образом, были получены некоторые типичные параметры роста нейритов: исследовали общий и средний рост, общее и среднее число отростков в клетке, а также общее количество и долю клеток с интенсивным ростом нейритов (определенным как рост на расстояние более 20 мкм). Все эксперименты проводили в четырех повторах.
Усиление роста нейритов
Как показано на ФИГ. 10-16, соединения, выбранные в приведенном выше скрининговом исследовании клеток РС-12, также были способны индуцировать рост нейритов в первичных нейронах среднего мозга в концентрации 0,1 мкМ. Эффективность большинства соединений была сопоставимой с таковой дбц-АМФ в отношении усиления роста нейритов на клетку (>25% увеличение роста) согласно результатам измерений среднего роста на клетку, как показано на Фиг. 10 (р<0,001 для UA, GA, ЕА, TL по сравнению с контролем). Эффективность всех испытанных соединений была сопоставимой или превышала наблюдаемую для дбц-АМФ (ФИГ. 11).
Увеличение числа отростков нейритов и ветвления
Все тестируемые соединения показали значительное увеличение среднего количества отростков на клетку (>10%) (ФИГ. 12), а также максимальной длины отростков (>10%) (ФИГ. 13).
Первичные клетки демонстрировали увеличение ветвления в присутствии положительного контроля (дбц-АМФ). Тем не менее ингибитор JNK SP600125 не ингибировал ветвление первичных клеток, как в клетках линии РС-12, однако был способен стимулировать ветвление, хотя и не в той же степени, что дбц-АМФ (60% по сравнению с 86% увеличением, которое наблюдали в отношении дбц-АМФ). Соединения UA, ЕА и TL были способны усиливать ветвление на том же уровне, что и дбц-АМФ (>111% увеличение ветвления, ФИГ. 14).
Увеличение числа дендритов на клетку и длины дендритов
Число дендритов значительно увеличилось при действии UA, ЕА и TL на уровнях, превышающих уровень, наблюдаемый для дбц-АМФ, при этом все соединения продемонстрировали увеличение >18% (ФИГ. 15).
Эллаговая кислота, уролитин А и теллимаграндин увеличивали длину дендритов >26%, эта величина выше, чем наблюдаемая для дбц-АМФ (ФИГ. 16).
Пример 7
Экстракт граната, пуникалагин, эллаговая кислота и уролитин А снижают прибавку массы тела и жировой массы у мышей, получавших пищу с высоким содержанием жира
Самцов мышей линии C57BL6/J приобрели в лаборатории Charles River (L'Arbresle, Франция) в возрасте 7 недель и акклиматизировали к виварию в течение 2 недель до начала экспериментов. Мышей содержали в группах по 5 в стандартных условиях содержания при 12-часовом цикле свет/темнота и свободном доступе к пище и воде. Начиная с возраста 9 недель, мыши получали пищу с высоким содержанием жира (HFD) (60% ккал из жира, D12492; Research Diets Inc., Нью-Брансуик, Нью-Джерси, США) в течение четырнадцати недель. Массу тела контролировали еженедельно.
Мышам в различных группах лечения вводили (i) уролитин, смешанный с пищей (пищевая добавка), для достижения дозировки в 55 мг/кг массы тела/сутки (мг/кг/сут); (ii) эллаговую кислоту, смешанную с пищей (пищевая добавка), для достижения дозировки в 75 мг/кг/сут; (iii) пуникалагин (кормление через желудочный зонд) для достижения дозировки в 90 мг/кг/сут; или (iv) экстракт граната (ЭГ) (кормление через желудочный зонд) для достижения дозировки общих полифенолов 140 мг/кг/сут. Типичный экстракт граната, использованный в этих экспериментах, имел следующий состав: полифенолы, 140 мг/кг/сут; пуникалагин, 13,1 мг/кг/сут; и эллаговая кислота, 13,2 мг/кг/сут. Животным, получающим пищу через зонд, зонд вводили ежедневно (7 дней/неделю) между 8:00 и 10:00 утра; соединения смешивали с физиологическим раствором (0,9% NaCl) и предоставляли в конечном объеме 5 мл/кг массы тела. Мыши в контрольной группе с высоким содержанием жиров, получали тот же корм, что и экспериментальные животные. Мыши в различных соответствующих контрольных группах получали только пищу с высоким содержанием жира либо пищу с высоким содержанием жира и растворитель (физиологический раствор) ежедневно через желудочный зонд. Другую контрольную группу мышей кормили стандартной пищей.
Состав тканей тела контролировали с помощью эхо-МРТ (Echo Medical Systems, Хьюстон, Техас, США) через 5 недель после начала обработки для мышей, получивших пищу с высоким содержанием жира, и через 2 недели после начала обработки для мышей, получавших стандартную пищу. Животных помещали индивидуально в пластиковый цилиндр и затем вносили в систему эхо-МРТ примерно на 2 мин для сканирования состава тканей тела (масса нежировых тканей и жира).
Результаты показаны на ФИГ. 17 и 18.
У мышей, получавших пищу с высоким содержанием жира (HFD), развилось тяжелое ожирение по сравнению с контрольными мышами, которых кормили стандартной пищей (CD) (ФИГ. 17А). Прибавка массы тела у необработанных мышей, получавших пищу с высоким содержанием жира, была связана с увеличением доли жировой массы (ФИГ. 17В) и уменьшением доли мышечной массы (масса нежировых тканей) (ФИГ. 17С), согласно результатам измерений методом эхо-МРТ после 5 недель обработки. У мышей, получавших пищу с высоким содержанием жира, обработка уролитином А (введение с пищевой добавкой), пуникалагином или экстрактом граната (ЭГ) (оба соединения вводили через зонд) предотвращала развитие ожирения, при этом у обработанных мышей, получавших пищу с высоким содержанием жира, наблюдали сильное снижение прибавки массы тела по сравнению с контрольными мышами, получавшими пищу с высоким содержанием жира (ФИГ. 17А). Наряду с этим наблюдением было установлено, что масса жира была значительно снижена у получавших пищу с высоким содержанием жира мышей, обработанных уролитином А, пуникалагином или ЭГ, по сравнению с не получавшими лечение мышами, которые получали пищу с высоким содержанием жира (ФИГ. 17В).
Мыши, получавшие стандартную пищу и обработанные эллаговой кислотой или уролитином А, также демонстрировали снижение жировой массы с сопутствующим увеличением мышечной массы (масса нежировых тканей), это указывает на то, что обработка этими соединениями способствуют управлению массой тела и массой нежировых тканей или мышечными физическими данными (ФИГ. 18В).
Пример 8
Экстракт граната, пуникалагин, эллаговая кислота и уролитин А увеличивают мышечную массу у нормальных и мышей с ожирением
Самцов мышей линии C57BL6/J распределяли по группам и обрабатывали, как описано в примере 7.
В обеих группах мышей как получающих стандартную пищу, так и пищу с высоким содержанием жира обработка ЭГ, пуникалагином, эллаговой кислотой или уролитином А привела к статистически значимому увеличению доли массы нежировых тканей. У мышей, получивших пищу с высоким содержанием жира и обработанных уролитином А, пуникалагином или ЭГ, наблюдали снижение жировой массы с сопутствующим увеличением мышечной массы (массы нежировых тканей) (ФИГ. 17В и 17С). У мышей, получивших стандартную пищу и обработанных эллаговой кислотой или уролитином А, также наблюдали снижение жировой массы с сопутствующим увеличением мышечной массы (массы нежировых тканей), это указывает на то, что обработка способствует управлению массой нежировых тканей или мышечными физическими данными (ФИГ. 18А и 18В). Так как масса нежировых тканей представлена преимущественно мышечной массой, эти результаты показывают, что обработка любым из ЭГ, пуникалагина, эллаговой кислоты или уролитана А приводит к увеличению доли мышечной массы как у нормальных мышей, так и мышей с ожирением по отношению к общей массе тела. Этот эффект наблюдали уже после двух недель лечения.
Пример 9
Экстракт граната, пуникалагин, эллаговая кислота и уролитин А увеличивают расход энергии у нормальных и мышей с ожирением
Самцов мышей линии C57BL6/J распределяли по группам и обрабатывали, как описано в примере 7. Далее расход энергии в начальных условиях, через 8 недель после начала обработки для мышей, получавших пищу с высоким содержанием жира, и через 2 недели после начала обработки для мышей, получавших стандартную пищу, измеряли методом непрямой калориметрии по потреблению кислорода, выработке диоксида углерода и коэффициенту дыхательного газообмена с использованием комплексной системы мониторинга лабораторных животных (CLAMS; Columbus Instruments, Колумбус, Огайо, США). Животных сначала акклиматизировали в течение 22 ч к клеткам CLAMS (комнатная температура 22°С±1°С) начиная с 11 до 12 часов утра. Затем проводили измерение в течение 20 ч в тех же условиях. Измерение включало полный цикл свет/темнота. Параметры, измеренные CLAMS, включали: (i) потребление кислорода (VO2 в мл/кг/ч): VO2 напрямую зависит от расхода энергии; (ii) выработку диоксида углерода (VCO2 в мл/кг/ч); и (iii) коэффициент дыхательного газообмена (RER): VCO2/VO2: RER является показателем использования энергетических субстратов. В равновесном состоянии RER эквивалентен дыхательному коэффициенту (RQ). Использование только углеводов дает RER=1, в то время как сжигание только жира дает RER=0,7. Смешанный рацион дает RER=0,85.
Результаты показаны на ФИГ. 19 и ФИГ. 20.
Потребление кислорода является физиологическим маркером активности митохондрий и расхода энергии. Обработка ЭГ, пуникалагином, эллаговой кислотой или уролитином А значительно увеличила потребление кислорода у мышей. Эллаговая кислота и уролитин А повышали расход энергии у мышей, получавших стандартную пищу (ФИГ. 19А и 19В). Этот эффект наблюдали уже через 2 недели обработки. Обработка экстрактом граната (ЭГ), пуникалагином и уролитином А увеличила расход энергии у мышей, получавших пищу с высоким содержанием жира (ФИГ. 20А и 20В).
Пример 10
Экстракт граната, пуникалагин, эллаговая кислота и уролитин А увеличивают использование жирных кислот в качестве энергетических субстратов у нормальных мышей и мышей с ожирением
Самцов мышей линии C57BL6/J распределяли по группам и обрабатывали, как описано в примере 9.
Как упомянуто выше, помимо потребления кислорода метод непрямой калориметрии также позволяет контролировать выработку диоксида углерода. Соотношение между выработкой диоксида углерода (VCO2) и потреблением кислорода (VO2) называется коэффициент дыхательного газообмена (RER). RER является отличным индикатором использования энергетических субстратов. В равновесном состоянии RER эквивалентен дыхательному коэффициенту (RQ). Преимущественное использование углеводов в качестве энергетического субстрата дает значение RER, близкое к 1, в то время как использование жиров в качестве энергетического субстрата (сжигание жиров) дает более низкое значение RER, которое близко к 0,7 при предпочтительном использовании жирных кислот.
Как показано на ФИГ. 21 и ФИГ. 22, обработка ЭГ, пуникалагином, эллаговой кислотой и уролитином А приводила к значительному снижению RER в обеих группах мышей как получающих стандартную пищу, так и пищу с высоким содержанием жира. Это влияние было наиболее выраженным у мышей, получавших стандартную пищу и обработанных эллаговой кислотой и уролитином А (ФИГ. 21). Полученные результаты подтверждают вывод о сдвиге состава тканей тела, который наблюдали после потребления ЭГ, пуникалагина, эллаговой кислоты или уролитина А, способствующих развитию более мускулистого (нежирового) телосложения с ограниченным содержанием жиров.
Пример 11
Экстракт граната, пуникалагин и уролитин А снижают плазматические уровни триглщеридов и свободных жирных кислот у мышей с ожирением
Самцов мышей линии C57BL6/J распределяли по группам и обрабатывали, как описано в примере 7. Далее через 14 недель после начала обработки проводили биохимический анализ крови с использованием стандартного автоматизированного биохимического анализатора (Dimension Xpand, SIEMENS). Животных не кормили в течение 12 часов (с 8 вечера до 8 утра) до забора крови. Приблизительно по 500 мкл крови собирали из полой вены у животных, анестезированных изофлураном. Кровь собирали в пробирки с гепарином и сразу же помещали на лед. Плазму готовили центрифугированием (1500 g, 15 мин, 4°С). Образцы плазмы затем переносили в чистую микропробирку объемом 1,5 мл и хранили при -80°С до момента проведения биохимических измерений на стандартном автоматизированном биохимическом анализаторе (Dimension Xpand, SIEMENS) с использованием соответствующих наборов.
Уровни циркулирующих триглицеридов и свободных жирных кислот измеряли стандартными биохимическими методами в крови контрольных и обработанных мышей, получавших пищу с высоким содержанием жира (ФИГ. 23). Обработка ЭГ, пуникалагином и уролитином А привела к статистически значимому улучшению плазматических уровней триглицеридов и свободных жирных кислот. Эти результаты показывают, что ЭГ, пуникалагин и уролитин А эффективны при лечении дислипидемии у мышей с ожирением, и, следовательно, могут улучшать функцию сердечно-сосудистой системы и предотвращать развитие сердечно-сосудистых заболеваний.
Пример 12
Пуникалагин, эллаговая кислота и уролитин А улучшают толерантность к глюкозе у мышей с ожирением
Самцов мышей линии C57BL6/J распределяли по группам и обрабатывали, как описано в примере 7. Далее у получавших пищу с высоким содержанием жира мышей, с развившимся нарушением толерантности к глюкозе, проводили тест на толерантность к глюкозе (ГТТ). Толерантность к глюкозе контролировали через 10 недель после начала обработки при помощи перорального теста на толерантность к глюкозе (пГТТ). Животных не кормили в течение 12 часов (с 8 вечера до 8 утра) до проведения пГТТ. В день проведения пГТТ из латеральной хвостовой вены брали небольшую каплю крови (<2 мкл) и контролировали гликемию с помощью глюкометра (AccuCheck Aviva, Roche Diagnosis). Каждое животное затем получило в 0-й момент времени D-глюкозу внутрь в дозе 2 г/кг массы тела. Гликемию контролировали на 15, 30, 45, 60, 90, 120 и 150 мин после пероральной нагрузки глюкозой.
Как и у людей, кормление мышей пищей с высоким содержанием жира привело к наступлению ожирения и сахарного диабета 2 типа, который характеризуется тяжелым нарушением толерантности к глюкозе, о чем свидетельствует последующая оценка гликемии сразу после воздействия глюкозы (2 г/кг массы тела) (тест толерантности к глюкозе) (ФИГ. 24). Как показано на ФИГ. 24, обработка пуникалагином, эллаговой кислотой и уролитином А улучшала толерантность к глюкозе у мышей, получавших пищу с высоким содержанием жира. Следовательно, подобная обработка может также быть эффективным терапевтическим подходом для лечения диабета 2 типа.
Пример 13
Уролитин А увеличивает функцию митохондрий у старых нематод С. elegans
Штаммы С. elegans культивировали при 20°С в чашках с агаром, приготовленным на ростовой среде для нематод (NGM) и инокулированных штаммом Е. coli ОР50. Используемый штамм представлял собой дикий тип Bristol N2, предоставленный Генетическим центром Caenorhabditis (Университет Миннесоты). Уролитин А растворяли в ДМСО. Животных подвергали воздействию соединений на стадии яйца на чашках, инокулированных живым штаммом бактерии Е. coli ОР50. Контрольные чашки готовили с соответствующей концентрацией ДМСО (0,1%).
Измерение потребления кислорода является индикатором активности митохондрий. Действие уролитина А на активность митохондрий у старых С. elegans (10 дней) оценивали путем обработки С. elegans уролитином А в течение 10 дней взрослой жизни, на протяжении этого периода потребление кислорода измеряли с помощью прибора Seahorse XF24 (Seahorse Bioscience Inc., Северная Биллерика, Массачусетс, США). Чтобы исследовать каждое условие использовали по 250 особей 10-дневных С. elegans. С. elegans извлекали из чашек с NGM средой, содержащей М9, три раза промывали в 2 мл М9 для устранения остаточных бактерий и ресуспендировали в 500 мкл среды М9. Червей переносили в стандартные 24-луночные планшеты Seahorse (каталожный номер 100777-004) (по 50 червей на лунку) и измеряли потребление кислорода. Потребление кислорода червями в начальных условиях измеряли в течение первых 30 минут с 5-минутным интервалом (0 мин, 5 мин, 15 мин, 20 мин, 25 мин и 30 мин) с 5 повторами для каждого интервала. Интенсивность дыхания нормировали на точное количество червей на лунку, которое определяли после завершения эксперимента с использованием стереомикроскопа. После определения потребления кислорода в начальных условиях измеряли потребление кислорода митохондриями в присутствии разобщителя, которое создавали путем добавления в среду карбонилцианид-р-(трифторметокси) фенилгидразона (FCCP) в 30 мин временной точке, чтобы оценить максимальную мощность потребления кислорода и максимальную митохондриальную мощность. Потребление кислорода в присутствии разобщителя измеряли с 5-минутными интервалами (35 мин, 40 мин, 45 мин, 50 мин, 55 мин и 60 мин) для оценки функции митохондрий с течением времени. FCCP является химическим разобщающим веществом, которое устраняет обязательную связь между дыхательной цепью и системой фосфорилирования, наблюдаемую в интактньгх митохондриях. Его действие обусловлено амфипатическими свойствами молекулы, которая растворяется в митохондриальном фосфолипидном бислое. Это значительно увеличивает ионную проницаемость мембраны митохондрий и создает очень сильную утечку протонов, которая приводит к увеличению потребления кислорода из-за тушения кислородом электронов, закачиваемых в дыхательную цепь параллельно с утечкой протонов. Так как потребление кислорода отделяется (разобщается) от производства АТФ (окислительное фосфорилирование), FCCP увеличивает потребление кислорода при снижении выработки энергии (АТФ) в митохондриях. Полностью разобщенные митохондрии, что достигается с помощью FCCP, демонстрируют максимальную мощность митохондриальной дыхательной цепи (максимальное потребление кислорода) без «препятствий», которые представляют собой процессы окислительного фосфорилирования и производства энергии.
Результаты, приведенные на ФИГ. 25, показывают, что уролитин А увеличивает максимальную мощность митохондрий у старых С. elegans, о чем свидетельствует более длительное действие на повышенное разобщенное дыхание червей, получавших уролитин А, по сравнению с контрольными, обработанными ДМСО червями. У контрольных необработанных червей наблюдали кратковременное увеличение интенсивности дыхания в присутствии разобщителя, которое быстро вернулось к начальному уровню потребления кислорода. У обработанных уролитином А червей увеличение интенсивности потребления кислорода было более длительным. Степень повышенной активности митохондрий показана путем сопоставления площади под кривой (AUC) в течение периода разобщения со средней интенсивностью дыхания при связанных процессах, которую использовали в качестве базовой линии. Было отмечено, что уролитин А существенно увеличивает интенсивность дыхания в присутствии разобщителя у старых червей по сравнению с контрольными необработанными червями в течение 30-минутного исследованного периода.
Пример 14
Уролитин А увеличивает активность митохондрий С. elegans
Штаммы С. elegans культивировали при 20°С в чашках с агаром, приготовленным на ростовой среде для нематод, инокулированных бактериями НТ115 и содержащих 50 мкМ уролитина А или соответствующую концентрацию ДМСО в качестве контроля. Червей обрабатывали в течение 24 часов. В экспериментах был использован штамм SJ4103 (zcIs14[myo-3::GFP (mit)]), который является стабильной трансгенной линией, экспрессирующей локализованный в митохондриях зеленый флуоресцентный белок (GFP) с расщепляемым сигнальным пептидом, отвечающим за митохондриальный импорт, под контролем промотора mуо -3, специфичного для мышц стенок тела. Оценку экспрессии и количественное определение GFP проводили в соответствии с протоколом, описанным ранее (Durieux et al., 2011). Червей обрабатывали 50 мкМ уролитина на стадии яиц, экспрессию GFP контролировали через один день, после того как особи становились взрослыми. Флуориметрическое исследование проводили с использованием планшетного ридера для регистрации множественных меток Victor Х4l (Perkin-Elmer Life Science). Восемьдесят червей выбирали случайным образом (по 20 червей на лунку 96-луночного планшета с черными стенками), каждую лунку анализировали четыре раза и усредняли результаты.
Результаты, приведенные на ФИГ. 26, показывают, что обработка червей уролитином А индуцирует экспрессию митохондриальной GFP-репортерной метки, находящейся у С. elegans под контролем промотора mуо-3, специфического для мышц. Это поразительное увеличение экспрессии GFP убедительно доказывает, что под действием уролитина А мощность митохондрий увеличилась. Чтобы обеспечить такое увеличение наблюдаемого сигнала GFP митохондрии в мышцах червей должны иметь либо увеличенный размер, либо быть более многочисленными.
Пример 15
Влияние соединений, полученных из граната, на настроение и когнитивные способности при хроническом стрессе
7-недельных самцов мышей дикого типа C57BL/6J подвергали воздействию хронического непредсказуемого стресса в течение четырех недель. Ряд поведенческих экспериментов проводили до, во время и после периода хронического стресса, чтобы определить влияние на настроение и когнитивные способности. Как уже сообщалось ранее, хронический стресс отрицательно влияет на настроение и когнитивные способности. Природные соединения, полученные из граната, вводили мышам для того чтобы определить, какое влияние эти соединения будут отказывать на облегчение данного отрицательного воздействия на настроение и когнитивные способности.
Мышей приучали к виварию исследователей в течение 9 дней до начала эксперимента. Всех мышей размещали в стандартных пластиковых клетках группами по трое и содержали при 12-часовом цикле свет/темнота (7:00 утра - 7:00 вечера) и свободном доступе к пище и воде. Все проводимые процедуры были выполнены в соответствии со Швейцарским национальным институциональным Руководством по проведению экспериментов на животных и были одобрены Швейцарским кантональным комитетом ветеринарного управления по проведению экспериментов на животных.
Характеристика животных
После адаптации к виварию все мыши были охарактеризованы в отношении массы тела, поведения сходного с тревожностью в приподнятом циркулярном лабиринте с частичными стенками (EZM), передвижения и исследовательской активности в открытом поле и исследования новых объектов. Цель этих экспериментов заключалась в сопоставлении поведения животных в соответствии с частотой развития тревожности и исследовательской активности, чтобы установить экспериментальные и контрольные группы, которые являются эквивалентными по этим характеристикам.
Приподнятый циркулярный лабиринт с частичными стенками
Уровень тревожности измеряли в приподнятом циркулярном лабиринте с частичными стенками (EZM). За мышами наблюдали в EZM (кольцевая дорожка шириной 5,5 см и диаметром 46 см, приподнятая над землей на 46 см) в течение 5 мин в условиях слабого и рассеянного освещения. Два противоположных сектора шириной 90° были защищены внутренней и наружной стенками, имеющими 13,5 см в высоту. Таким образом, три зоны были определены следующим образом: промежуточная зона, состоящая из четырех сегментов шириной 30° на концах защитных стен, разделенных двумя закрытыми/защищенными зонами шириной 50° и двумя открытыми/незащищенными зонами поиска шириной 70°. С помощью этих границ вход в открытые секторы детектировали только тогда, когда животное вступало в них всеми четырьмя лапами. Траектории каждой мыши автоматически записывали с помощью системы видеонаблюдения (Ethovision 3.0, Noldus, Вагенинген, Нидерланды). Общее число входов во все секторы служило показателем спонтанной двигательной активности, в то время как различия в количестве входов и времени, проведенном в открытых секторах, были приняты в качестве индикаторов тревожности. В период между сессиями лабиринт очищали 4% смесью этанол/вода.
Открытое поле и новый объект
Передвижение и реактивность в открытом поле (OF) оценивали в белой квадратной коробке (50×50×37 см) в условиях слабого и рассеянного света. Мышь помещают в центр поля и позволяют свободно двигаться в течение 10 мин. Исследовали общее расстояние, на которое перемещалась мышь, частоту входов в центр, время и процент времени в центре открытого поля. Избегание внутренних или «незащищенных» областей поля интерпретируют как сходное с тревожностью поведение. Оценки общего расстояния используют в качестве индекса активности. Исследовательское поведение оценивали с использованием теста для нового объекта (NO). NO тест проводили сразу же после теста в открытом поле. Небольшой, металлический предмет (3×1,5×5 см) помещали в центр открытого поля, когда мышь находилась внутри. Затем мышам позволяли 5 мин свободно исследовать новый объект. В тесте исследовали время пребывания в центре и на периферии отсека, количество и латентный период входов в центр, а также общее расстояние, на которое перемещалась мышь, в центре и во всем отсеке. Процент времени и расстояние, которое мыши проводили в центре, исследуя новый объект, рассматривали как показатели «целенаправленной» исследовательской активности.
Обработка экстрактом, полученным из граната
За три недели до начала протокола индукции хронического стресса мышей разделили на четыре группы. Одна группа получала стандартный корм для мышей (контроль), а остальные три группы получали различные дозы экстракта 1011 - экстракта, полученного из сока граната. Низкая доза соответствовала дозе экстракта в 21 мг/кг/сут полифенолов в эквивалентах галловой кислоты (ПЭГ в ЭГК), средняя доза соответствовала дозе экстракта в 43 мг/кг/сут ПЭГ в ЭГК, высокая доза соответствовала дозе экстракта в 86 мг/кг/сут ПЭГ в ЭГК (см. таблицу 5).

Обработка соединениями, смешанными с пищей, началась за три недели до начала протокола индукции хронического стресса и продолжалась до окончания эксперимента.
Обработка уролитином А, полученным из граната метаболитом
За три недели до начала протокола индукции хронического стресса мышей разделили на две группы. Одна группа получала стандартный корм для мышей (контроль), тогда как другая группа получала пищу, содержащую уролитин А, в количестве для введения дозы в 25 мг/кг/сут.
Хронический непредсказуемый стресс
Протокол индукции непредсказуемого хронического стресса включал воздействие на животных ежедневной стрессовой ситуации в непредсказуемый момент времени в течение 4 недель (с 8 утра до 4 вечера, случайным образом распределенный на протяжении 28 дней). Использовали следующие стрессовые стимулы: подвешивание за хвост в течение 6 мин, неизбегаемое электроболевое раздражение лап 3×0,4 мА; воздействие загрязненных, влажных опилок в течение 4 ч; нахождение на приподнятой платформе в течение 2 ч; иммобилизация в пластиковой трубке в течение 1 ч; 30-минутное воздействие температуры в 16°С; воздействие обратного цикла свет/темнота в течение 2 дней; воздействие более старых, агрессивных животных того же вида в течение 10 мин; интенсивное воздействие света (600 люкс); нахождение 2 ч в переполненной клетке (6 мышей) и 8 ч в наклоненной на 40° клетке. Всех животных взвешивали и регулярно оценивали состояние их шерсти (раз в 3-5 дней). В ходе этого эксперимента одну группу мышей подвергали воздействию хронического стресса, тогда как другую группу животных оставили в покое и использовали в качестве контроля.
Исследование поведения
Тест с подвешиванием за хвост
Тест с подвешиванием за хвост (TST) используется в качестве модели для оценки антидепрессант-подобной активности у мышей. Тест основан на том факте, что животные, подвергнутые краткосрочному (6 мин), неизбегаемому стрессу при подвешивании за хвост, будут неподвижными. Мышей подвешивали на металлическом стержне с помощью липкой ленты, размещенной в 20 мм от края хвоста. Расстояние между полом и стержнем составляло около 25 см. Неподвижность определяется как отсутствие инициированного движения и включает пассивное раскачивание. Время изучения, включавшее неподвижность, борьбу и карабканье, оценивали на основании записей системы видеонаблюдения.
Как показано на ФИГ. 27, хронический стресс привел к увеличению неподвижности в TST, который является индикатором увеличившейся депрессии и чувства беспомощности. Тем не менее, мыши, получавшие увеличивающиеся дозы экстракта граната, продемонстрировали реверсию этой модели и восстановление подвижности и борьбы до уровня, который наблюдали у нестрессовых мышей. Таким образом, экстракт граната предотвращает развитие депрессивной реакции, наблюдаемой у необработанных мышей, подвергшихся хроническому стрессу.
Контекстуальное распознавание
Контекстуальное условно-рефлекторное замирание представляет собой меру способности животного помнить конкретный контекст. В этом тесте мышей помещают в коробку, затем животные получают два мягких удара током с интервалом в одну минуту. В ответ на удар током мыши замирают. Способность мышей распознавать контекст, в котором они получили удар током, проверяют путем помещения их обратно в коробку в более поздней временной точке. Если мыши распознают контекст, то они замрут в ожидании удара током.
У нормальных мышей способность распознавать контекст, в отсутствие каких-либо шоковых воздействий, является мерой контекстуальной памяти. Мыши с лучшей контекстуальной памятью распознают исходный контекст лучше и, следовательно, имеют более высокий уровень замирания.
Этот тест также может быть использован для измерения тревожности у подвергшихся стрессу мышей. У подвергшихся стрессу мышей повышенное беспокойство можно было наблюдать при повышенном времени реакции замирания в ответ на первоначальные шоковые воздействия, а также более длительном периоде ослабления памяти о контексте. Ослабление контекстуальной памяти измеряют, помещая мышь в тот же контекст один раз в день в течение нескольких дней при отсутствии начального неблагоприятного стимула. Со временем мыши разучиваются ассоциировать контекст с неблагоприятным стимулом, о чем свидетельствует постепенное уменьшение замирания. У подвергшихся стрессу мышей, демонстрирующих тревожность, ослабление памяти о неблагоприятном событии занимает больше времени.
Контекстуальное условно-рефлекторное замирание использовали для того чтобы испытать влияние экстракта граната на индукцию тревожности (т.е. приобретенной тревожности) у мышей в ответ на распознавание контекста. Обучение и тестирование проходило в камере кондиционирования грызунов (20×20×28 см), помещенной в коробку из плексигласа и освещенной 20 Вт лампочкой. Боковые стенки камеры для кондиционирования были построены из белого метакрилата, дверь и верхняя крышка были изготовлены из плексигласа. Пол состоял из 20 стальных стержней, через которые можно было подавать нерегулярные шоковые импульсы от шокового генератора. Вентиляторы создавали фоновый шум в 68 дБ (вся система: Panlab, SL, Барселона, Испания). Тест на условно-рефлекторное замирание в отношении контекста проводили в течение третьей недели протокола хронического стресса в группе, подвергающейся стрессу. В день проведения теста на условно-рефлекторное замирание мышей транспортировали из комнаты для колоний в соседнюю поведенческую лабораторию и помещали в кондиционную камеру. Обучение включало воздействие на мышей вызывающего условный рефлекс контекста в течение 3 мин, за которым следовали три электроболевых раздражения лап (2 сек, 0,4 мА) с интервалом в одну минуту. После последнего электроболевого раздражения лап животное осталось в камере в течение 30 с. Камеру для проведения теста на условно-рефлекторное замирание тщательно очищали 0,5% уксусной кислотой, перед тем как поместить каждую мышь в коробку. Для определения влияния хронического стресса и различных доз экстракт граната на уровень тревожности, индуцированной контекстной памятью, измеряли уровень поведенческих реакций, вызванных тревожностью, в ответ на этот контекст. Исследовали следующие поведенческие реакции, которые, как известно, чувствительны к уровню тревожности: % замирания, % подъема на задние лапы и % ухода за собой. Измерения поведенческих реакций проводили через 48 ч после повторного воздействия на мышей кондиционирующего контекста в течение 8 мин. После сессий обучения и тестирования животных немедленно возвращали в их домашние клетки. Поведение животных регистрировали с последующей оценкой результатов наблюдателем, заслепленным в отношении обработки животных, с использованием собственного программного обеспечения.
Замирание, определяемое как отсутствие движения, за исключением сердцебиения и дыхания, оценивали и использовали в качестве индекса тревожности. Время замирания пересчитывали как процент уровня замирания. Действие экстракта граната зависело от дозы, при этом самая высокая доза вызывала значительное снижение % замирания (ФИГ. 28), что указывает на защиту от тревожности. Сходное снижение уровня тревожного поведения наблюдают в отношении воспитания со значительной и дозазависимой защитой воспитательного поведения после введения экстракта граната (ФИГ. 29). Эти наблюдения также дополняются сильным подавлением вызванного тревожностью ингибирования ухода за собой после введения самых высоких доз экстракта граната (ФИГ. 30). Результаты показывают, что экстракт и соединения, полученные из граната, снижают вызванную опытом тревожность у мышей.
Снижение вызванной опытом тревожности у мышей, подвергшихся хроническому стрессу, наблюдали и для уролитина А, который является метаболитом пуникалагина. В настоящем исследовании уровни тревожности измеряли как ослабление памяти о неблагоприятном контексте, предъявленном в тесте на условно-рефлекторное замирание, описанном выше. В данном исследовании мышей, которые прошли обучение с использованием контекстной парадигмы условно-рефлекторного замирания, подвергают воздействию этого же контекста каждый день в течение четырех дней, но в отсутствие какого-либо неблагоприятного стимула. Способность распознавать контекст измеряют как замирание в течение 3-минутного периода наблюдения. Было показано, что повышенные уровни тревожности вели к более длительному периоду ослабления памяти о неблагоприятном контексте. Как показано на ФИГ. 31, мыши, которые подверглись хроническому стрессу, демонстрировали более длительный период ослабления по сравнению с нормальными мышами. Тем не менее, после обработки уролитином А в дозе 25 мг/кг/сут мыши, которые подверглись хроническому стрессу, продемонстрировали значительное улучшение времени ослабления памяти о неблагоприятном событии, это указывает на то, что уролитин А, как и пуникалагин, способен уменьшить тревожность у мышей, которые подверглись хроническому стрессу.
Водный лабиринт Морриса
Хронический стресс оказывает неблагоприятное воздействие на пространственную память и обучение. Водный лабиринт Морриса состоит из большого белого круглого бассейна (140 см в диаметре), заполненного непрозрачной окрашенной водой (25°С±1°С), с платформой (10×10 см2), которая погружена под воду на 1 см. Водный лабиринт окружен серыми шторами (25 см от края бассейна), на которых имеется несколько видимых визуальных стимулов. Перед тестированием мышь обучают определять расположение платформы. Используя видимые визуальные стимулы, мышь учится определять местоположение платформы. Фаза обучения начинается с фазы привыкания, в которой мыши знакомятся с комнатой, устройством, а также водой путем предоставления им возможности свободно плавать в течение 2 мин в бассейне без платформы. Данные собирают с использованием видеокамеры, прикрепленной к потолку и подключенной к системе видеонаблюдения (Ethovision 3.0, Noldus, Вагенинген, Нидерланды).
После сессии привыкания (0-й день) мышей подвергали воздействию различных протоколов для того чтобы последовательно оценить их способности к пространственному обучению (с 1-го по 3-й день). Сессии пространственного обучения проводили в течение трех последовательных дней (с 1-го по 3-й день), выполняя по четыре испытания в день с 6-минутным интервалом между испытаниями (ITI).
Каждое испытание начиналось со знакомства мыши с лабиринтом с помощью чашки, обращенной в сторону стенки бассейна, и в одной из четырех возможных позиций, которые были случайным образом распределены между испытаниями и днями. Расстояние между мышью и платформой измеряли в каждый момент проведения замера, при этом частота замеров составляла 25 раз в секунду. Эти расстояния затем суммировали для 60-секундного периода, чтобы получить расстояние до платформы (см) в каждом испытании. Если мышь не находила платформу в течение 60 секунд, то животное осторожно направляли к ней. Каждая мышь должна была оставаться на платформе в течение 20 секунд, прежде чем она была возвращена в свою клетку для ожидания.
Результаты этого примера показали, что хронический стресс оказал значительное отрицательное влияние на обучение и пространственную память. Во время обучающей сессии наблюдали значительное увеличение расстояния, которое требовалось преодолеть, чтобы достигнуть платформы по сравнению с контрольными мышами, которые не подвергались стрессу, этот результат указывает на то, что хронический стресс ухудшает нормальное формирование памяти в процессе обучения (ФИГ. 32). Обработка мышей экстрактом граната защищала от указанного отрицательного влияния хронического стресса на обучение и связанную с ним память. Дозазависимое действие наблюдали у мышей, получавших экстракт граната, обработанные и подвергнутые хроническому стрессу мыши были способны выполнять тесты на том же уровне, что и контрольные животные, не подвергшиеся стрессу (ФИГ. 33).
Как показано на ФИГ. 34, аналогичное действие наблюдали у мышей, обработанных уролитином А. Мыши, прошедшие протокол индукции хронического стресса, показали неустойчивое обучение, о чем свидетельствует высокая изменчивость между последовательными испытаниями. Обработка мышей, подвергшихся хроническому стрессу, уролитином А в дозе 25 мг/кг/сут продемонстрировала стабилизацию этой изменчивости. Этот результат подчеркивает тот факт, что уролитин А, который является последующим метаболитом пуникалагина, также может защитить от данного отрицательного влияния хронического стресса на когнитивные способности, включая обучение и память.
Таким образом, в совокупности эти результаты показывают, что экстракт граната и полученные из него соединения, такие как уролитин А, способны уменьшать отрицательное влияние хронического стресса на когнитивные способности, включая память и обучение. Более того, экстракт граната и полученные из него соединения обладают антидепрессивной активностью, как наблюдали в тесте с подвешиванием за хвост, и снижают тревожность, вызванную хроническим стрессом. Результаты также показывают, что экстракт граната предотвращает ухудшение памяти, эффективности обучения и пространственного распознавания, обычно наблюдаемых после хронического стресса.
Пример 16
Влияние на память и когнитивные способности в крысиной модели старения Старение оказывает ряд воздействий на когнитивные способности и память, которые могут быть обобщены в крысиной модели старения. См. обзор Gallagher and Rapp (1977) Аnnu Rev Psychol. 48:339-70. Крысиная модель старения широко используется для характеристики воздействия старения на память и когнитивные способности. В экспериментах, представленных в настоящей заявке, в присутствии экстракта граната наблюдали повышение эффективности выполнения задач.
Старые крысы линии Спраг-Даулей (начиная с возраста 19 месяцев) получили экстракт граната (1108) с питьевой водой в концентрации 0,34 мг/мл полифенолов (ПЭГ). Содержание полифенолов измеряли спектрофотометрическим методом Фолина-Чокальтеу, содержание фенолов выражали как эквивалент галловой кислоты. Раствор для контрольной обработки содержал 1,36% сахарозы, 0,12% D-глюкозы и 0,12% D-фруктозы, растворенных в воде. Крысы в среднем потребляли 30 мл/сут контрольного раствора и экстракта 1108 (см. таблицу 6), средняя масса крысы составляла примерно 660 г. Доза ПЭГ составила 15 мг/кг/сут или 1,1 мг пуникалагина/кг/сут для животных, получавших экстракт 1108.

После 2,5 месяцев обработки кратковременную рабочую память оценивали с помощью задачи на социальное распознавание, стандартного теста, включающего социальное познание. Thor and Halloway (1981) Animal Learning Behavior. 9:561-5. В этой задаче каждую старую крысу помещали в ее домашнюю клетку вместе с молодым самцом Спраг-Даулей (<5 недель) на 5 минут. Через тридцать минут точно такую же процедуру повторили с тем же молодым самцом для того чтобы во второй раз определить степень взаимодействия между двумя животными. Во время второго взаимодействия ожидали меньшую степень контакта, так как двое животных ранее уже взаимодействовали. Уменьшение контакта между животным является мерой когнитивных функций и сохранения информации в памяти. Через тридцать минут другую молодую крысу помещали на 5 минут вместе со старой крысой для того чтобы определить может ли животное различать между собой двух разных молодых особей. В течение каждого периода контакта между двумя животными общее время контакта измеряли для оценки интенсивности социального взаимодействия.
Результаты показаны на ФИГ. 35. Контрольные старые животные не продемонстрировали какого-либо предпочтения в отношении знакомого объекта и провели равное время, исследуя оба объекта - эффект, который ранее был показан у старых крыс и, по-видимому, отражал ухудшение памяти временного порядка при старении. Hauser et al. (2009) Behav Neurosci. 123:1339-45. Тем не менее крысы, обработанные экстрактом 1108, показали уменьшение времени, проведенного с той же молодой особью в течение второго периода экспозиции, а также увеличение времени взаимодействия с новой молодой крысой. Наблюдаемая разница иллюстрирует защитное действие экстракта 1108 в отношении формирования памяти и удержания информации.
Пример 17
Влияние на пространственную память в крысиной модели старения
Сообщалось, что старение также влияет на пространственную память, при этом в результате старения снижается способность выполнять задачи. Bergado et al. (e-pub October 29, 2010) Spatial and emotional memory in aged rats: a behavioral analysis. Neuroscience. Для того чтобы исследовать влияние экстракта граната на ухудшение пространственной памяти при старении старые крысы Спраг-Даулей (начиная с возраста 19 месяцев) получали экстракт граната 1108 или контрольный раствор с питьевой водой, как описано в примере 16.
Старых крыс обрабатывали экстрактом 1108 или изокалорийным контролем в течение трех месяцев, после чего оценивали их способность к обучению и память, используя задачи в водном лабиринте Морриса, описанном в примере 15.
Способности к обучению каждого животного оценивали по их способности выполнять обратную задачу (три испытания). В этой задаче животные сначала изучали расположение платформы в квадранте (Запад) на протяжении трех обучающих испытаний. Затем расположение платформы изменяли и помещали ее в противоположный квадрант (Восток). Животных подвергали трем новым обучающим сессиям для изучения нового расположения платформы. Усилия, затраченные на определение нового местоположения платформы, измеряли путем оценки расстояния, пройденного до момента определения размещения платформы. Результаты показаны на ФИГ. 36. Животные, обработанные экстрактом, более эффективно определяли местоположение платформы в обратном тесте (однофакторный дисперсионный анализ, р<0,02; контроль N=11; PJ: N=13; экстракт: N=14), что свидетельствует о терапевтической пользе введенного экстракта в отношении этого аспекта пространственной памяти.
Пример 18
Влияние соединений, полученных их граната, на пространственную и рабочую память при болезни Альцгеймера
Было показано, что болезнь Альцгеймера (А) оказывает неблагоприятное воздействие на пространственную память - эффект, который наблюдается также в мышиной модели болезни Альцгеймера. Чтобы определить влияние соединений, полученных их граната, на улучшение пространственной и рабочей памяти при AD различные экстракты граната и пуникалагин испытывали в двух поведенческих исследованиях пространственной памяти: Y-лабиринте и водном лабиринте Морриса.
Y-лабиринт
В этом исследовании использовали мышиную модель болезни Альцгеймера 5XFAD. Мышиная модель болезни Альцгеймера 5XFAD основана на генетических модификациях (введение мутантных генов АРР и PS1 человека), приводящих к образованию амилоидного β-пептида (Ар) в тканях головного мозга. Было установлено, что у этих мышей когнитивная функция в Y-лабиринте значительно снижается уже в 7-месячном возрасте.
Для того чтобы определить влияние соединений, полученных из граната, экстракт (ЭГ), полученный из целого граната, вводили через желудочный зонд в дозе 60 мг/кг/сут полифенолов, которая включает приблизительно 5,6 мг/кг/сут пуникалагина. Начиная с 3-месячного возраста и до конца обработки, мышам вводили экстракт через желудочный зонд 3 раза в неделю. Мышей тестировали в 7-месячном возрасте, чтобы установить влияние ЭГ на рабочую память в Y-лабиринте. Мышей помещали в Y-лабиринт на 15 минут и давали исследовать два рукава, третий рукав оставался закрытым. Через четыре часа животное вновь помещали в лабиринт на пять минут, на этот раз с открытым третьим рукавом, и давали мыши возможность свободно исследовать все три рукава. Исследовательская активность в новом рукаве позволяла оценить способность животного распознавать на основании пространственных стимулов, что данная зона еще не была исследована. Мышей оценивали как делающих правильный логический выбор во время исследования, если они исследовали каждый из трех рукавов, а не только два, представленные первыми.
Как показано на ФИГ. 37, у мышей линии 5XFAD, получавших ЭГ, наблюдали значительное улучшение рабочей памяти, что измеряется по количеству правильных логических выборов.
Водный лабиринт Морриса
Экстракты граната 31008, 61109 и 71109 тестировали на второй трансгенной животной модели болезни Альцгеймера, экспрессирующей обе амилоидные мутации: Лондонскую мутацию и мутацию пренисилин-1 человека. У этих модельных животных к 4-месячному возрасту развиваются бляшки, а к 6-месячному - нарушения памяти. Нагрузка плотными бляшками видна через 7 месяцев.
В одной серии экспериментов четырехмесячные трансгенные мыши APP-PS1 получали с питьевой водой фиксированную дозу полифенолов примерно в 97 мг /кг/сут, которая включает примерно 15 мг/кг/сут пуникалагина экстракта 31008, полученного из целого граната. В другой серии экспериментов четырехмесячные трансгенные мыши АРР-PS1 получали с питьевой водой фиксированную общую дозу в 468 мг/кг/сут экстракта 61109, который был высоко обогащен пуникалагином (>91%). В другой серии экспериментов четырехмесячные трансгенные мыши APP-PS1 получали с питьевой водой фиксированную дозу примерно в 180 мг общих полифенолов/кг/сут экстракта 71109, который был получен из кожицы граната. После 3-х месяцев кормления мышей (7-месячных) испытывали в водном лабиринте Морриса с пространственным тестом.
Тест в водном лабиринте Морриса проводили в течение 84-87 дней обработки. Бассейн (белый, круглый сосуд диаметром 1 м), содержал воду при 20°С с диоксидом титана в качестве лишенной запаха, нетоксичной добавки, чтобы скрыть спасательную платформу (1 см ниже уровня воды). Плавание каждой мыши фиксировали системой видеонаблюдения и анализировали (Ethovision, Noldus information Technology, Вагенинген, Нидерланды). До обучения каждую мышь помещали на поверхность платформы на 15 секунд. В ходе испытаний на определение местоположения платформы мышей обучали находить скрытую платформу в пяти блоках из трех испытаний в течение трех дней подряд. Каждое испытание состоит из теста принудительного плавания в течение максимум 120 секунд, за которыми следуют 60 секунд отдыха. Время, которое необходимо каждой мыши, чтобы найти платформу измеряли в течение пяти последовательных блоков обучения для определения кривой обучения для каждой мыши.
Через двадцать четыре часа после последнего обучения каждое животное подвергали испытанию конечной точки с удаленной платформой. Мышам давали возможность поиска отсутствующей платформы в течение 60 секунд, затем измеряли время поиска, проведенное в каждом квадранте бассейна, а также число пересечений исходного положения платформы. Как показано на ФИГ. 38, мыши, которых кормили экстрактом 31008, показали увеличение производительности в последнем тесте, о чем свидетельствует увеличение частоты пересечения области, в которой формально находилась платформа. Мыши, которых кормили экстрактами 61109 и 71109, имели еще более высокую производительность.
Композиции экстрактов 61109, использованные в данном эксперименте, представлены в таблице 7.

Пример 19
Влияние соединений, полученных из граната, на депрессию, тревожность и когнитивные способности в ответ на стресс в раннем периоде жизни
Полученные из граната соединения оценивали в отношении их способности улучшать функции мозга, включая когнитивные способности, депрессию и тревожность, в модели стресса в ранний период жизни, вызванном разлучением с матерью.
Стресс в ранний период жизни оказывает существенное влияние на когнитивные функции в последующей взрослой жизни, включая (i) увеличение частоты принятия отклоняющихся от нормы и чрезмерно рискованных решений; (ii) восприимчивость к повышенной частоте депрессий и тревожности, и (iii) нарушенное обучение и память.
Все проведенные процедуры были выполнены в соответствии со Швейцарским национальным институциональным Руководством по проведению экспериментов на животных и одобрены Швейцарским кантональным ветеринарным комитетом управления по проведению экспериментов на животных.
Стресс в ранний период жизни, вызванный разлучением с матерью
В 1-й день после рождения детенышей отбирали, чтобы иметь по 6 детенышей от матери. С 1-го по 14-й день после рождения проводили непредсказуемое разлучение с матерью в течение 3 часов в день. Разлучение с матерью осуществляли в случайные моменты времени (с 8 утра до 2 часов), чтобы избежать привыкания матери к процедуре. Протокол включал удаление детенышей от матери в другую клетку при комнатной температуре в течение 3 часов, после чего они были возвращены в прежнее гнездо. Эти группы обозначены на рисунках как стресс в ранний период жизни. Контрольную группу самок/детенышей не подвергали стрессу и обозначали на рисунках как нормальную.
Обработка пуникалагином, выделенным из граната
Через неделю после разлучения с матерью мышей разделили на две группы. Одна контрольная группа получала стандартную пищу для мышей (необработанные), в то время как другая группа получала эллагитаннин и пуникалагин, смешанные с кормом и в количестве, обеспечивающем доставку мышам дозы 90 мг/кг/сут. Обработка соединениями, смешанными с пищей, началась через 1 неделю после окончания процедуры разлучения с матерью.
Поведенческие тесты
Влияние стресса в ранний период жизни на депрессию, тревожность и когнитивные способности исследовали с использованием перечисленных ниже поведенческих тестов, которые проводили через 166 дней после завершения протокола разлучения с матерью. Выращенных в нормальных условиях мышей сравнивали с разлученными с матерью мышами (стресс в ранний период жизни) и разлученными с матерью мышами, получавшими пуникалагин.
Тест с темной/светлой коробкой
В этом тесте мышей помещают в коробку из ПВХ, которая разделена на два отсека: темный отсек (15×20×25 см, черный ПВХ, закрытый сверху) и освещенный отсек (30×20×25 см, белый ПВХ, освещенный с интенсивностью 200 люкс), оба отсека связаны между собой смежной дверкой (5×5 см) (Лигна, Париж, Франция). Эксперимент начинают, помещая животных в темный отсек, после чего камера записывает в течение 5-минутного периода количество времени, которое мышь проводит в освещенной области, число переходов из темной в освещенную область и латентный период, чтобы убежать из темной в освещенную область.
Как правило, мыши будут избегать освещенной области в коробке. Разлученные с матерью мыши проводили аномально длительное время в освещенном отсеке, как следствие их стресса в ранний период жизни, по сравнению с другой частью их помета, которую не отделяли от матери (ФИГ. 39). Увеличение времени, проведенного исследуя освещенную область, отражает нарушенное поведение в отношении принятия решений, которое характеризуется ненормальным и чрезмерно рискованным поведением.
Обработка пуникалагином разлученных с матерью мышей вызывала реверсию и нормализовала наблюдаемое чрезмерно рискованное поведение, а также восстанавливала нормальный процесс принятия решений (ФИГ. 39).
Приподнятый циркулярный лабиринт (ЕОМ)
Другим поведенческим тестом, который позволяет оценить чрезмерно рискованное поведение, является тест в приподнятом циркулярном лабиринте (ЕОМ). В этом тесте аппарат, состоящий из кольца диаметром 41,5/46,5 см (внутренний/внешний диаметр), делится на четыре равные части. Две части кольца, расположенные напротив друг друга, отгорожены стенками по 5 см в высоту. Оставшиеся две части кольца не имеют стенок. Лабиринт возвышается на 1 м над полом. Естественное стремление мышей заключается в том, чтобы избежать открытых поверхностей и проводить больше времени в закрытых участках кольца, которые имеют 5 см стены, в отличие от открытых участков кольца.
Чтобы исследовать эффект стресса в ранний период жизни мышей помещали на входе в одну из областей лабиринта с 5-сантиметровыми стенками, при этом нос животного был ориентирован в сторону закрытого рукава, и позволяли исследовать ЕОМ в течение 5 мин. В течение этого периода поведение животных регистрировали на видеопленку. Рассчитывали время, проведенное в каждом рукаве (закрытый по сравнению с открытым), при этом считали, что животное вошло в рукав, только если оно касалось рукава всеми четырьмя лапами.
Как правило, мыши, помещенные в приподнятый циркулярный лабиринт, будут избегать открытых участков кольца, и проводить ограниченное время, исследуя эту область. Мыши, подвергшиеся стрессу при разлучении с матерью, проводили аномально долгое время в открытых участках О-лабиринта по сравнению с другой частью помета, не подвергшейся стрессу (ФИГ. 40). Сходно с результатами, которые наблюдали в тесте с темной/светлой коробкой, этот факт отражает нарушенное поведение в отношении принятия решений у мышей, подвергшихся стрессу в раннем периоде жизни, которое характеризуется ненормальным и чрезмерно рискованным поведением.
Обработка пуникалагином разлученных с матерью мышей вызывала реверсию и нормализовала ненормальное и чрезмерно рискованное поведение, вызванное ранним стрессом (ФИГ. 40).
Тест принудительного плавания
Тест Парсолта или тест принудительного плавания обычно используют для проверки лечения антидепрессантами (Porsolt et al., 1977а; Porsolt et al., 1977b). Для этого поведенческого теста мышь помещают в цилиндр объемом 5 л (11 см в диаметре и 25 см в высоту), заполненный на две трети водой при 23°С. Считалось, что животное плавает и передвигается, если имелось очевидное перемещение тела. Животные, плавающие с минимальным движением во время теста, считались неподвижными. Поведение животных записывали в течение 6-минутного периода тестирования с использованием камеры и зеркала за цилиндром. Первые 2 минуты и последние 4 минуты плавания анализировали по отдельности для определения плавательной активности мыши. Повышающийся уровень депрессии коррелирует с увеличением неподвижности мыши, особенно в последние 4 минуты. Животные, которые перенесли стресс в раннем периоде жизни, показали значительное увеличение неподвижности по сравнению с другой частью их помета, не подвергшейся стрессу, что указывает на повышенный уровень депрессии (ФИГ. 41). Обработка пуникалагином разлученных с матерью мышей вызывала реверсию ненормального поведения (повышенная неподвижность) и повышала плавательную активность до уровня, который наблюдали у мышей, не подвергшихся стрессу. Такой поведенческий эффект пуникалагина демонстрирует его активность в качестве антидепрессанта (ФИГ. 41).
Контекстуальное условно-рефлекторное замирание
Тест на контекстуальное условно-рефлекторное замирание использовали для того чтобы определить влияние эллагитаннина пуникалагина на восприимчивость к тревожности взрослых животных, подвергшихся стрессу в раннем периоде жизни. Животных обучали в камере для проведения теста на контекстуальное условно-рефлекторное замирание (контекст А, ш×д×в: 30 см × 24 см × 26 см) (PanLab), которая содержала сетчатый пол, изготовленный из стержней из нержавеющей стали, и была связана с генератором шоковых импульсов, разработанным Panlab. Во время обучения животных помещали в камеру по одному за один раз. Через четыре минуты исследовательской активности внутри камеры применяли одно электроболевое раздражение лап животного (2 секунды и 0,4 мА), а затем через одну минуту второе (2 секунды и 0,4 мА). Через тридцать секунд после второго электроболевого раздражения мышь помещали обратно в домашнюю клетку. Поведение животных контролировали каждые 2 секунды на протяжении всего эксперимента. Период, который мыши провели неподвижными в камере, рассматривали как «замирание» и оценивали в течение этих периодов. Время, которое мыши провели неподвижно после первого удара током, регистрировали в течение 60 секундного периода и выражали в процентах.
Поведение мышей оставаться неподвижными и «замирать» в ответ на электроболевое раздражение лап является мерой их уровня тревожности. Чем больше продолжительность «замирания» на протяжении этого поведенческого теста, тем более высокий уровень тревожности у животных.
Различия в продолжительности замирания между испытанными группами (нормальные, не подвергшиеся стрессу мыши; перенесшие стресс в раннем периоде жизни мыши; перенесшие стресс в раннем периоде жизни мыши + пуникалагин) наблюдали после первого электроболевого раздражения лап (ФИГ. 42). Стресс в раннем периоде жизни привел к повышенной тревожности мышей, о чем свидетельствует увеличение времени, проведенного в замершем состоянии после электроболевого раздражения лап, по сравнению с другой частью их помета, не подвергшейся стрессу (ФИГ. 42). Обработка пуникалагином снижала и нормализовала повышенные уровни тревожности, вызванные стрессом в раннем периоде жизни, как наблюдали по уменьшению времени замирания после электроболевого раздражения лап (ФИГ. 42). Наблюдения, полученные на модели стресса в раннем периоде жизни, иллюстрируют анксиолитическое действие пуникалагина.
Повышенную тревожность, которую испытывали животные, подвергшиеся воздействию стресса в раннем периоде жизни, также наблюдали по ослаблению (т.е. исчезновению) контекстуальной памяти (т.е. памяти, которая связывает контекст окружающей среды с ударом током), вызванной тестом. Чтобы исследовать интенсивность тревожности, которая развилась во время теста на контекстуальное условно-рефлекторное замирание (как описано выше), животных помещали в ту же камеру и контекст на 3 мин в день (то же время суток, однако на этот раз без удара током) в течение 12 дней после первоначального испытания. Замирание, вызванное простым узнаванием животными камеры, где они получили первый удар током, измеряли в течение каждого из этих ежедневных 3-минутных периодов.
Группы животных (нормальные не подвергшиеся стрессу мыши, перенесшие стресс в раннем периоде жизни мыши и перенесшие стресс в раннем периоде жизни мыши+пуникалагин) имели некоторые различия в отношении снижения их контекстуального узнавания удара током в течение последующих 12 дней (ФИГ. 43). На этом графике продолжительность замирания представлена как процент времени, проведенного в неподвижном состоянии на 1-й день (например, если мышь была неподвижна в течение 60 секунд в 1-й день и 30 секунд на 8-й день, неподвижность составляет 100% в 1-й день и 50% на 8-й день).
Нормальные не подвергшиеся стрессу мыши демонстрировали предсказуемое снижение контекстуального узнавания в течение 12 дней (ФИГ. 43). Перенесшие стресс в раннем периоде жизни мыши имели повышенное контекстуальное узнавание, о чем свидетельствует высокий уровень замирания по сравнению с другой частью их помета, не подвергшейся стрессу (ФИГ. 43). Это свидетельствует о более продолжительном повышенном уровне тревожности у таких мышей, разлученных с матерью. Обработка пуникалагином мышей, перенесших стресс в раннем периоде жизни, оказывала заметное влияние на снижение тревожности, что наблюдали по ослаблению контекстуального узнавания. У обработанных мышей, перенесших стресс в раннем периоде жизни, контекстуальное узнавание исчезало быстрее, чем у необработанных мышей, перенесших стресс в раннем периоде жизни, характеризующихся снижением времени, которое они проводят в замершем состоянии между 8-м и 12-м днями (ФИГ. 43).
Ротарод
Чтобы оценить влияние соединений, полученных из граната, на отрицательный когнитивный эффект разлучения с матерью воздействие на моторные навыки исследовали с использованием поведенческого теста на ротароде. Аппарат ротарод состоит из стержня с диаметром 2 см. Мышь помещают на вращающийся стержень, который начинает вращаться с начальной скоростью 5 оборотов в минуту (об/мин). Скорость вращения стержня постепенно увеличивается с шагом в 8 об/мин, пока не достигнет скорости в 45 об/мин. Латентный период до падения измеряли при временной точке отсечения равной 300 сек. Как показано на ФИГ. 44, мыши, которые подверглись стрессу в раннем периоде жизни, имели расстройство двигательных навыков. Мыши, разлученные с матерью, выпадали из ротарода быстрее, чем нормальные не подвергшиеся стрессу мыши. Обработка пуникалагином восстанавливала моторные навыки у мышей, перенесших стресс в раннем периоде жизни, до уровней активности, которые наблюдали в другой нормальной части их помета, не подвергшейся стрессу.
Водный лабиринт Морриса
Поведенческий тест в водном лабиринте Морриса использовали для того чтобы оценить как влияет разлучение с матерью на когнитивные способности. В этом тесте когнитивное обучение измеряют по способности мыши определять местоположение скрытой платформы в бассейне с непрозрачной водой. Аппарат состоит из бассейна (с диаметром 140 см), наполненного водой с температурой 22°С. Мыши выбирались из воды, плывя к скрытой круглой платформе (15 см в диаметре), размещенной на 1 см ниже поверхности воды. С помощью визуальных стимулов, расположенных за пределами лабиринта, мыши могут находить платформу и узнавать ее расположение во время последующих испытаний. Во время фазы обучения мышей помещали на две стартовые позиции (попеременно) каждый час. Тест в водном лабиринте Морриса выполняли с 8 испытаниями в Т1, 6 испытаниями в Т2 и 4 испытаниями в Т3 (на 1, 2 и 3-й дни). Мыши имели максимум 60 с, чтобы достичь платформы. Латентный период выхода из воды для достижения платформы измеряли с помощью системы видеонаблюдения. Как можно видеть на ФИГ. 45, стресс в раннем периоде жизни оказывал существенное влияние на когнитивное обучение, при этом мышам требовался более длительный период времени, чтобы выучить расположение скрытой платформы, о чем свидетельствует увеличенный латентный период выхода по сравнению с нормальными не подвергшимися стрессу мышами. Обработка разлученных с матерью мышей пуникалагином устраняла отрицательное влияние стресса в раннем периоде жизни, уменьшая время, которое требуется для того чтобы выучить расположение скрытой платформы до уровня, наблюдаемого у нормальных не подвергшихся стрессу мышей. Эти результаты демонстрируют способность пуникалагина устранять долгосрочное отрицательное когнитивное влияние стресса в раннем периоде жизни на обучение и формирование памяти.
Соединения, полученные из граната
В совокупности данные, приведенные выше, показывают, что соединения, полученные из эллагитаннинов, способны устранять долгосрочное отрицательное влияние разлучения с матерью в раннем периоде жизни на депрессию, тревожность и когнитивные способности.
Пример 20
Влияние соединений, полученных из граната, на память и когнитивные способности у нормальных мышей
Обработка соединениями, полученными из граната
Начиная с 3-месячного возраста, мыши получали (i) стандартную контрольную пищу, например, AIN-93G; (ii) пищу, содержащую пуникалагин в концентрации 0,87 мг/кг, таким образом чтобы введенная доза составляла примерно 90 мг/кг/сут (в течение 3-х месяцев), или (iii) пищу, содержащую уролитин А в концентрации 0,57 мг/кг, таким образом чтобы введенная доза составляла примерно 55 мг/кг/сут (в течение 2,5 месяца). Фактические дозы незначительно различались в зависимости от потребления пищи каждой отдельной мышью, а также от массы мыши. Поведенческую оценку когнитивных способностей проводили после этого периода.
Поведенческий тест для оценки влияния соединений, полученных из граната, на когнитивные способности
Чтобы исследовать влияние соединений, полученных из граната, на память и когнитивные способности оценивали улучшение контекстуальной памяти мышей, используя тест на контекстуальное условно-рефлекторное замирание. Мышей обучали в камере для изучения условно-рефлекторного замирания, как описано в примере 19.
Во время обучения животных помещали в камеру по одному за один раз. Через четыре минуты исследовательской активности внутри камеры применяли одно электроболевое раздражение лап (2 секунды и 0,4 мА), а затем через одну минуту второе (2 секунды и 0,4 мА). Через тридцать секунд после второго электроболевого раздражения лап мышь помещали обратно в домашнюю клетку.
Через день обученных животных возвращали в камеру на три минуты. В течение этого периода контролировали движение мышей. Количество времени, проведенное в неподвижном или «замершем» состоянии, оценивали как процент от общего времени (3 минуты), в течение которого наблюдали за животным. Время, проведенное в неподвижном состоянии, является мерой прочности памяти мышей в отношении узнавания контекста, в котором они были обучены. Обработка как эллагитаннином пуникалагином, полученным из граната, так и метаболитом эллаговой кислоты уролитином А привела к значительным улучшениям контекстуальной памяти по сравнению с необработанными контрольными мышами согласно оценке их контекстуальной памяти через 24 часа после периода обучения (ФИГ. 46).
Для того чтобы определить как соединения, полученные из граната, влияют на сохранение информации в памяти у нормальных мышей, которых кормили (i) контрольной пищей; (ii) пуникалагином (в течение 3 месяцев), либо (iii) уролитином А (в течение 2,5 месяцев), исследовали вызов памяти в 1, 2, 3, 4 и 5-й дни после первоначального контекстуального обучения для выработки условно-рефлекторного замирания.
После первоначального тестирования животных помещали в ту же камеру и контекст на 3 мин в день (то же время суток, однако на этот раз без удара током) на протяжении 5 дней. Замирание, вызванное простым контекстуальным распознаванием животными камеры, где они получили первоначальный удар током, измеряли в течение каждого из этих ежедневных 3-минутных периодов. Способность распознавать эту среду в отсутствие стимула является мерой контекстуальной памяти.
С каждым последующим днем память контрольных необработанных мышей об этом контекстуальном стимуле начинает ослабевать, о чем свидетельствует снижение степени замирания (ФИГ. 47). Мыши, обработанные пуникалагином или уролитином А, демонстрировали улучшенное сохранение информации в памяти по сравнению с контрольными, необработанными мышами. Этот вывод подтверждается способностью помнить исходный контекст в течение более длительного периода, о чем свидетельствует значительно более длительный период ослабления контекстуальной памяти (ФИГ. 47).
Эти результаты показывают, что обработка пуникалагином или уролитином А приводит к улучшению когнитивных способностей, о чем свидетельствует существенное увеличение распознавания контекста и улучшенное сохранение информации в памяти.
Пример 21
Влияние соединений, полученных из граната, на улучшение работы мышц у нормальных мышей
Эллагитаннин-производные соединения пуникалагин и уролитин А оценивали по их способности улучшать работу мышц. Чтобы исследовать преимущества пуникалагина и уролитина А в отношении улучшения работы мышц их действие изучали с использованием двух поведенческих тестов: (i) испытания на ротароде, который измеряет работу мышц и моторных навыков, включая координацию и (ii) испытания на беговой дорожке, которое позволяет измерять работу мышц и выносливость.
Поведенческие тесты для измерения влияния соединений, полученных из граната, на работу мышц
Ротарод
Начиная с 3-месячного возраста, мыши получали либо стандартную контрольную пищу, например, AIN-93G, либо пищу, содержащую пуникалагин в количестве, обеспечивающем введение дозы в 90 мг/кг/сут в течение 3 месяцев.
Чтобы исследовать влияние соединений, полученных из граната, на работу мышц и моторные навыки мышей испытывали на ротароде. Аппарат ротарод состоит из стержня диаметром 2 см и 5 отсеков по 5 см в ширину. Мышь помещают на вращающийся стержень, который начинает вращаться с начальной скоростью 5 об/мин. Скорость стержня постепенно увеличивается с шагом в 8 об/мин. Латентный период выпадения измеряли при временной точке отсечения данных равной 300 с. Мышей тестировали в четырех испытаниях. Латентный период выпадения является мерой работы мышц и моторных навыков мышей, при этом более высокая работоспособность отражается более длительным латентным периодом выпадения. Были протестированы контрольные необработанные и пуникалагин-обработанные мыши. Эллагитаннин-производное пуникалагин существенно улучшало работу мышц и моторные навыки по сравнению с необработанными мышами. Пуникалагин-обработанные мыши были способны оставаться на ротароде в течение более длительного времени и на более высоких скоростях по сравнению с необработанными мышами в течение последовательных периодов испытания (ФИГ. 48).
Испытание на выносливость
Нормальных 8-недельных мышей акклиматизировали в течение 2 недель до начала исследования. Мыши, получали стандартную пищу для грызунов (корм) или пищу, содержащую уролитин А, смешанный с кормом в количестве, обеспечивающем введение дозы в 55 мг/кг/сут. После 6 недель лечения испытывали работу мышц мышей с помощью теста на выносливость.
Тест на выносливость проводили с использованием беговой дорожки, движущейся с переменной скоростью, которая была вставлена в камеру из плексигласа со стимулирующим устройством, состоящим из электрошоковой сетки, прикрепленной к задней части дорожки (Panlab, Барселона, Испания). Мыши бежали при скорости дорожки 10 см/с и наклоне 0° в течение 5 мин. Скорость затем увеличивали на 2 см/с каждые 5 мин до обессиливания мышей. Регистрировали пробег и количество ударов током, полученных в течение 5-минутных интервалов. Мышей считали обессилевшими и удаляли из эксперимента, когда они получали примерно 20 ударов током в течение 1 мин. Было проведено испытание и сравнение работы мышц контрольных не получавших лечение мышей и мышей, получавших лечение уролитином А.
На улучшенную работу мышц и выносливость указывает способность бежать при более высоких скоростях на беговой дорожке. Мыши будут стремиться избежать удара током, и будут бежать, несмотря на увеличение скорости. В определенный момент времени мыши теряют способность бежать со скоростью беговой дорожкой и получают удар током. При достижении порогового уровня ударов током мышей удаляют с беговой дорожки. Мыши, имеющие более высокую производительность мышц и улучшенную выносливость, смогут продолжать бежать с ростом скорости беговой дорожкой и будут получать меньше ударов током на определенной скорости. Обработанные уролитином А мыши бежали с более высокой скоростью, чем необработанные контрольные мыши в этом поведенческом тесте, это свидетельствует о том, что уролитин А улучшает производительность мышц и выносливость в этом контексте (ФИГ. 49).
Эти результаты показывают, что эллагитаннин пуникалагин и его метаболит уролитин А способны улучшать производительность мышц и моторные навыки у млекопитающих.
ЭКВИВАЛЕНТЫ
В настоящей заявке изобретение было описано в широком смысле и общих чертах. Специалисты в данной области техники смогут легко представить ряд других способов и/или структур для выполнения функций и/или получения результатов и/или одного или более преимуществ, описанных в настоящей заявке, и каждое из таких изменений и/или модификаций рассматривают как включенное в область настоящего изобретения. В целом для специалистов в данной области техники должно быть очевидно, что все параметры, размеры, материалы и конфигурации, описанные в настоящей заявке, предназначены для иллюстративных целей и что фактические параметры, размеры, материалы и/или конфигурации будут зависеть от конкретного применения и применений, для которых используют(ся) принцип(ы) настоящего изобретения. Для специалистов в данной области техники будут очевидны, либо могут быть установлены с помощью рутинных экспериментальных методик, многие эквиваленты конкретных вариантов реализации изобретения, описанных здесь. Таким образом, следует понимать, что вышеприведенные варианты реализации настоящего изобретения представлены только в качестве примера и что в рамках объема прилагаемой формулы изобретения и ее эквивалентов изобретение может быть реализовано иначе, чем конкретно описано и заявлено. Настоящее изобретение относится к каждому отдельному признаку, системе, статье, материалу, набору, и/или способу, описанному в настоящей заявке. Кроме того, любая комбинация из двух или более таких признаков, систем, статьей, материалов, наборов и/или способов, если такие признаки, системы, статьи, материалы, наборы и/или способы не являются взаимно противоречивыми, включена в объем настоящего изобретения. Кроме того, каждый из узких видов и подродовых группировок, входящих в обобщенное описание, также является частью настоящего изобретения. Это включает общее описание изобретения с оговоркой или отрицательным ограничением, удаляющим любой предмет из рода, независимо от того, имеется ли в настоящем описании специальная ссылка на удаленный материал.
ВКЛЮЧЕНИЕ ПОСРЕДСТВОМ ССЫЛКИ
Содержание статей, патентов и патентных заявок, а также все другие документы и доступная в электронном виде информация, которая упоминается или цитируется в настоящей заявке, полностью включены в настоящее описание посредством ссылки в той же мере, как если бы каждая отдельная публикация была конкретно и индивидуально указана как включенная посредством ссылки. Авторы изобретения оставляют за собой право физически включить в настоящую заявку любые материалы и информацию из любых указанных статей, патентов, патентных заявок, или других физических и электронных документов.
Использованные источники
Bai, N., K. Не, et al. (2008). "Active compounds from Lagerstroemia speciosa, insulin-like glucose uptake-stimulatory/inhibitory and adipocyte differentiation-inhibitory activities in 3T3-L1 cells." J Agric Food Chem 56(24): 11668-74.
Bishop, N.A., T. Lu, et al. (2010). "Neural mechanisms of ageing and cognitive decline." Nature 464(7288): 529-35.
Bloss, E.В., W.G. Janssen, et al. (2010). "Interactive effects of stress and aging on structural plasticity in the prefrontal cortex." J Neurosci 30(19): 6726-31.
Bowman, R.E., K.D. Beck, et al. (2003). "Chronic stress effects on memory: sex differences in performance and monoaminergic activity." Horm Behav 43(1): 48-59.
Cerda, В., J.C. Espin, et al. (2004). "The potent in vitro antioxidant ellagitannins from pomegranate juice are metabolised into bioavailable but poor antioxidant hydroxy-6H-dibenzopyran-6-one derivatives by the colonic microflora of healthy humans." Eur J Nutr 43(4): 205-20.
Cerda, В., P. Periago, et al. (2005). "Identification of urolithin a as a metabolite produced by human colon microflora from ellagic acid and related compounds." J Agric Food Chem 53(14): 5571-6.
De Souza Schmidt Goncalves, A.E., F.M. Lajolo, et al. "Chemical composition and antioxidant/antidiabetic potential of Brazilian native fruits and commercial frozen pulps." J Agric Food Chem 58(8): 4666-74.
Del Pozo-Insfran, D., С.H. Brenes, et al. (2004). "Phytochemical composition and pigment stability of Acai (Euterpe oleracea Mart.)." J Agric Food Chem 52(6): 1539-45.
Dumitriu, D., J. Hao, et al. (2010). "Selective changes in thin spine density and morphology in monkey prefrontal cortex correlate with aging-related cognitive impairment." JNeurosci 30(22): 7507-15.
Gasperotti, M., D. Masuero, et al. "Profiling and accurate quantification of Rubus ellagitannins and ellagic acid conjugates using direct UPLC-Q-TOF HDMS and HPLC-DAD analysis." J Agric Food Chem 58(8): 4602-16.
Gil, M.I., F.A. Tomas-Barberan, et al. (2000). "Antioxidant activity of pomegranate juice and its relationship with phenolic composition and processing." J Agric Food Chem 48(10): 4581-9.
Greene, L.A. and A.S. Tischler (1976). "Establishment of a noradrenergic clonal line of rat adrenal pheochromocytoma cells which respond to nerve growth factor." Proc Natl Acad Sci USA 73(7): 2424-8.
Gimning, P.W., G.E. Landreth, et al. (1981). "Differential and synergistic actions of nerve growth factor and cyclic AMP in PC12 cells." J Cell Biol 89(2): 240-5.
Harper, M.E., K. Green, et al. (2008). "The efficiency of cellular energy transduction and its implications for obesity." Annu Rev Nutr 28: 13-33.
Hebert, L.E., P.A. Scherr, et al. (2003). "Alzheimer disease in the US population: prevalence estimates using the 2000 census." Arch Neurol 60(8): 1119-22.
Joels, M., Z. Pu, et al. (2006). "Learning under stress: how does it work?" Trends Cogn Sci 10(4): 152-8.
Joseph, J.A., B. Shukitt-Hale, et al. (2005). "Reversing the deleterious effects of aging on neuronal communication and behavior: beneficial properties of fruit polyphenolic compounds." Am J Clin Nutr 81(1 Suppl): 313S-316S.
Kujoth, G.C., A. Hiona, et al. (2005). "Mitochondrial DNA mutations, oxidative stress, and apoptosis in mammalian aging." Science 309(5733): 481-4.
Lee, J.H., J.V. Johnson, et al. (2005). "Identification of ellagic acid conjugates and other polyphenolics in muscadine grapes by HPLC-ESI-MS." J Agric Food Chem 53(15): 6003-10.
Maier, S.F. and L.R. Watkins (2005). "Stressor controllability and learned helplessness: the roles of the dorsal raphe nucleus, serotonin, and corticotropin-releasing factor." Neurosci Biobehav Rev 29(4-5): 829-41.
Puech, J.L., C. Mertz, et al. (1999). "Evolution of castalagin and vescalagin in ethanol solutions. Identification of new derivatives." J Agric Food Chem 47(5): 2060-6.
Pinnock, S.B. and J. Herbert (2001). "Corticosterone differentially modulates expression of corticotropin releasing factor and arginine vasopressin mRNA in the hypothalamic paraventricular nucleus following either acute or repeated restraint stress." Eur J Neurosci 13(3): 576-84.
Rea, S.L., N. Ventura, et al. (2007). "Relationship between mitochondrial electron transport chain dysfunction, development, and life extension in Caenorhabditis elegans." PLoS Biol 5(10): e259.
Roozendaal, В. (2003). "Systems mediating acute glucocorticoid effects on memory consolidation and retrieval." Prog Neuropsychopharmacol Biol Psychiatry 27(8): 1213-23.
Rozovsky, I., M. Wei, et al. (2005). "Reversible age impairments in neurite outgrowth by manipulations of astrocytic GFAP." Neurobiol Aging 26(5): 705-15.
Sandi, C. (2004). "Stress, cognitive impairment and cell adhesion molecules." Nat Rev Neurosci 5(12): 917-30.
Sandi, C. and M. Loscertales (1999). "Opposite effects on NCAM expression in the rat frontal cortex induced by acute vs. chronic corticosterone treatments." Brain Res 828(1-2): 127-34.
Sandi, C. and M. T. Pinelo-Nava (2007). "Stress and memory: behavioral effects and neurobiological mechanisms." Neural Plast 2007: 78970.
Satomi, H., K. Umemura, et al. (1993). "Carbonic anhydrase inhibitors from the pericarps of Punica granatum L." Biol Pharm Bull 16(8): 787-90.
Schriner, S.E., N.J. Linford, et al. (2005). "Extension of murine life span by overexpression of catalase targeted to mitochondria." Science 308(5730): 1909-11.
Shors, T.J. (2004). "Learning during stressful times." Learn Mem 11(2): 137-44.
Tanaka, K., G. Nonaka, et al. (1986). "Tannins and Related Compounds. XLI. 1) Isolation and Charactherization of Novel Ellagitannins, Punicacorteins А, В, C, and Punigluconin from the brak of Punica granatum L." Chem. Pharm. Bull 34(2): 656-663.
Tanaka, K., G. Nonaka, et al. (1986). "Tannins and Related Compounds. XLI. 1) Isolation and Charactherization of Novel Ellagitannins, Punicacorteins А, В, C, and Punigluconin from the brak of Punica granatum L." Chem. Pharm. Bull 34(2): 656-663.
Tanaka, K., G. Nonaka, et al. (1986). "Tannins and Related Compounds. XLI. 1). Revision of the Structures of Punicalin and Punicalagin, and Isolation and Charactherization of 2-O-Galloylpunicalin from the Bark of Punica granatum L." Chem. Pharm. Bull 34(2): 650-655.
Trifunovic, A., A. Wredenberg, et al. (2004). "Premature ageing in mice expressing defective mitochondrial DNA polymerase." Nature 429(6990): 417-23.
Vrhovsek, U., A. Palchetti, et al. (2006). "Concentration and mean degree of polymerization of Rubus ellagitannins evaluated by optimized acid methanolysis." J Agric Food Chem 54(12): 4469-75.Wang, С.H., С.C. Wang, et al. (2010). "Mitochondrial dysfunction in insulin insensitivity: implication of mitochondrial role in type 2 diabetes." Ann N Y Acad Sci 1201: 157-65.
Xiao, J., A. Pradhan, et al. (2006). "Functional role of JNK in neuritogenesis of PC12-N1 cells." Neurosci Lett 392(3): 231-4.
Yang, G., F. Pan, et al. (2009). "Stably maintained dendritic spines are associated with lifelong memories." Nature 462(7275): 920-4.
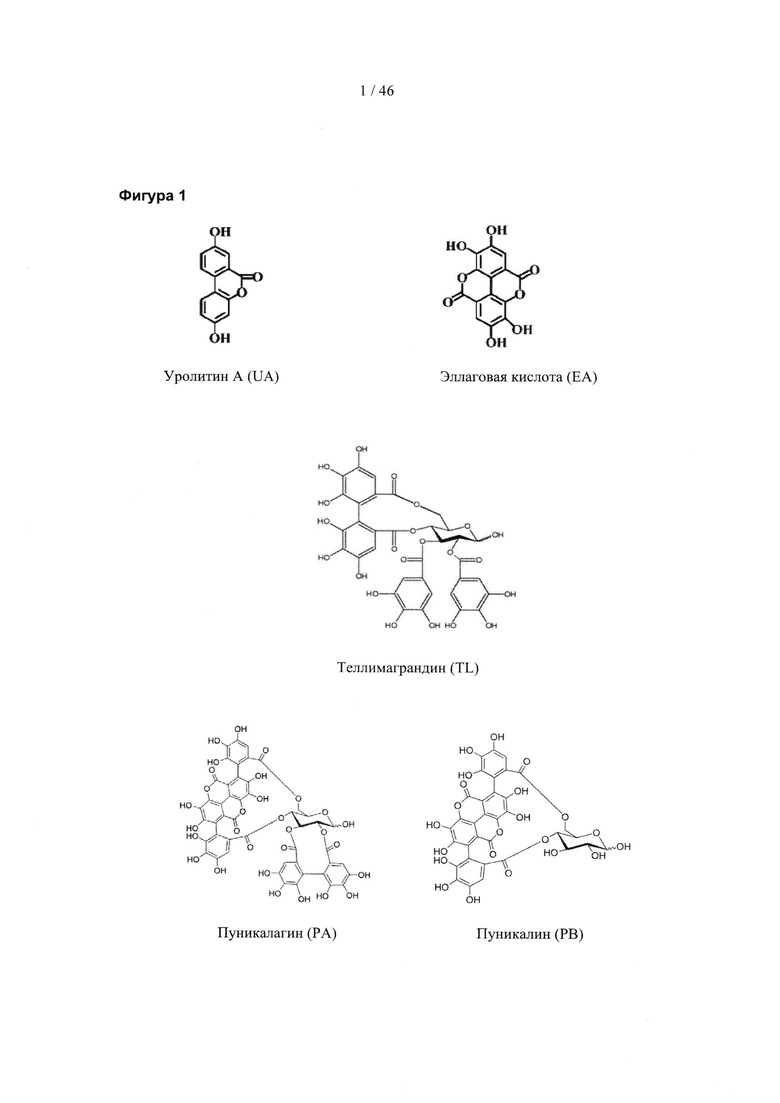
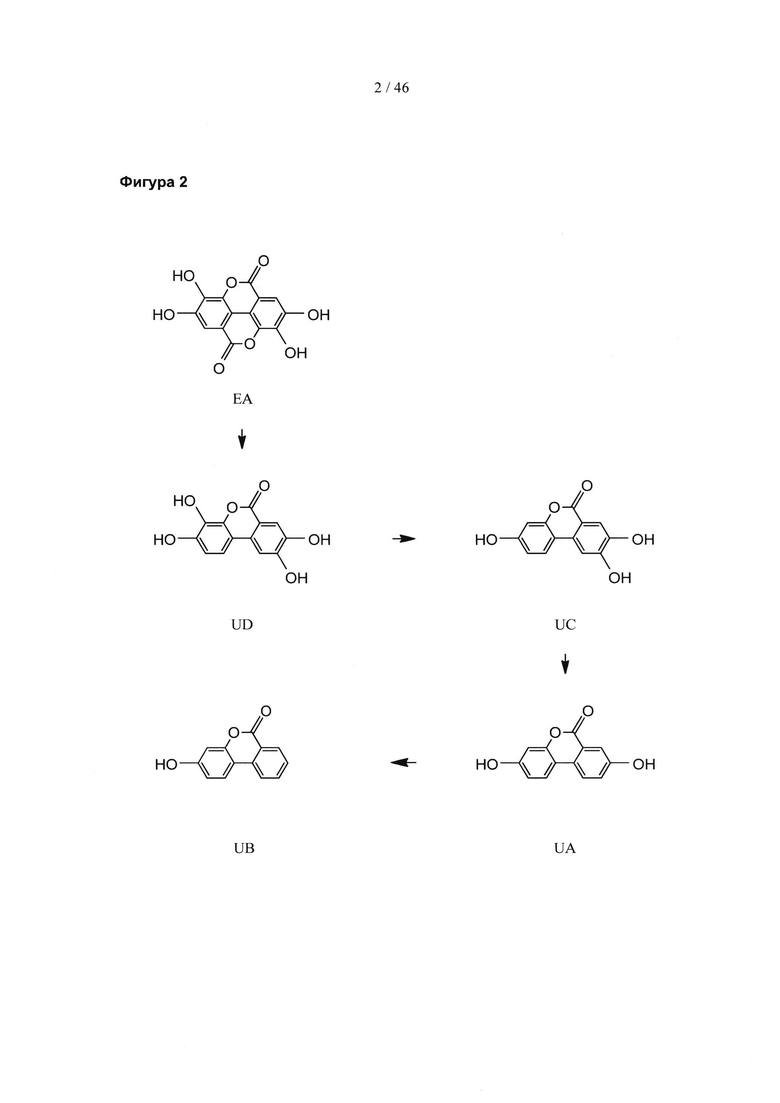
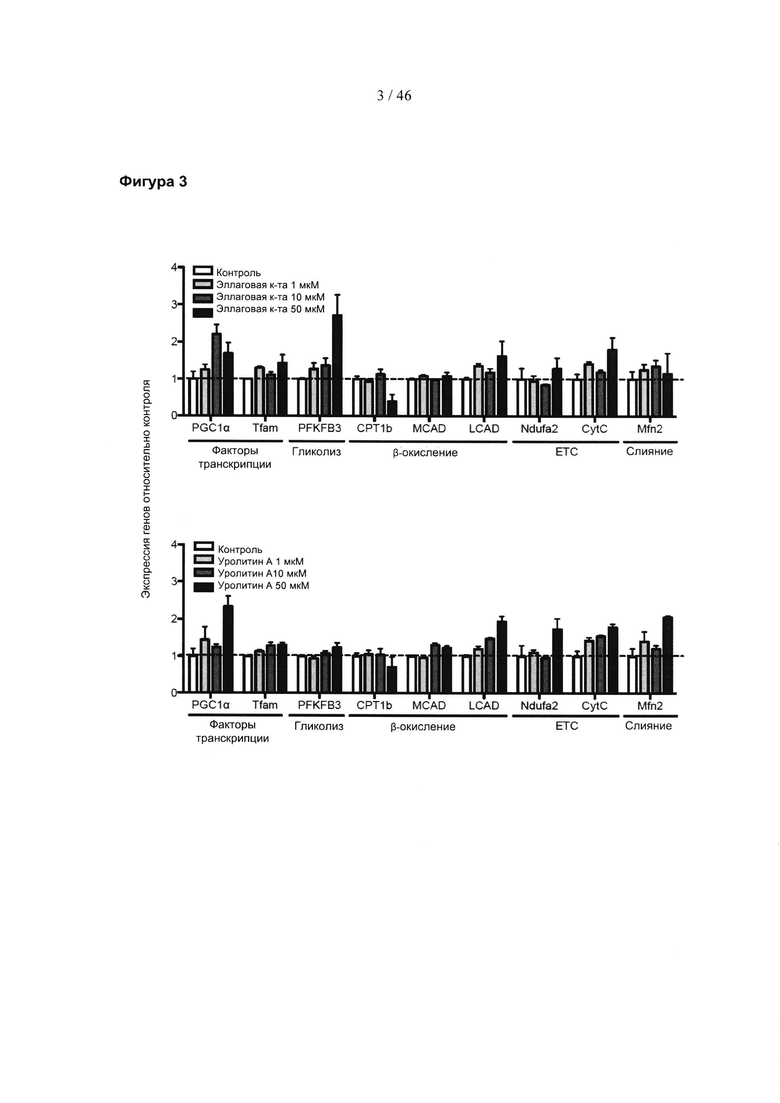
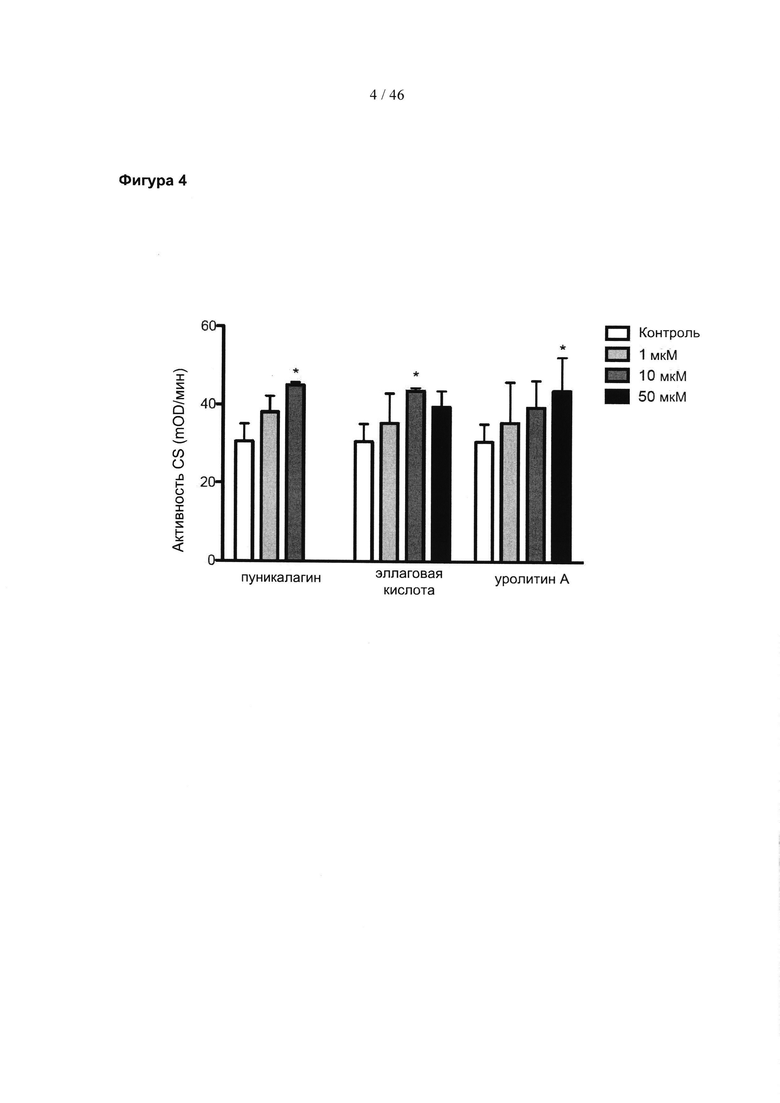
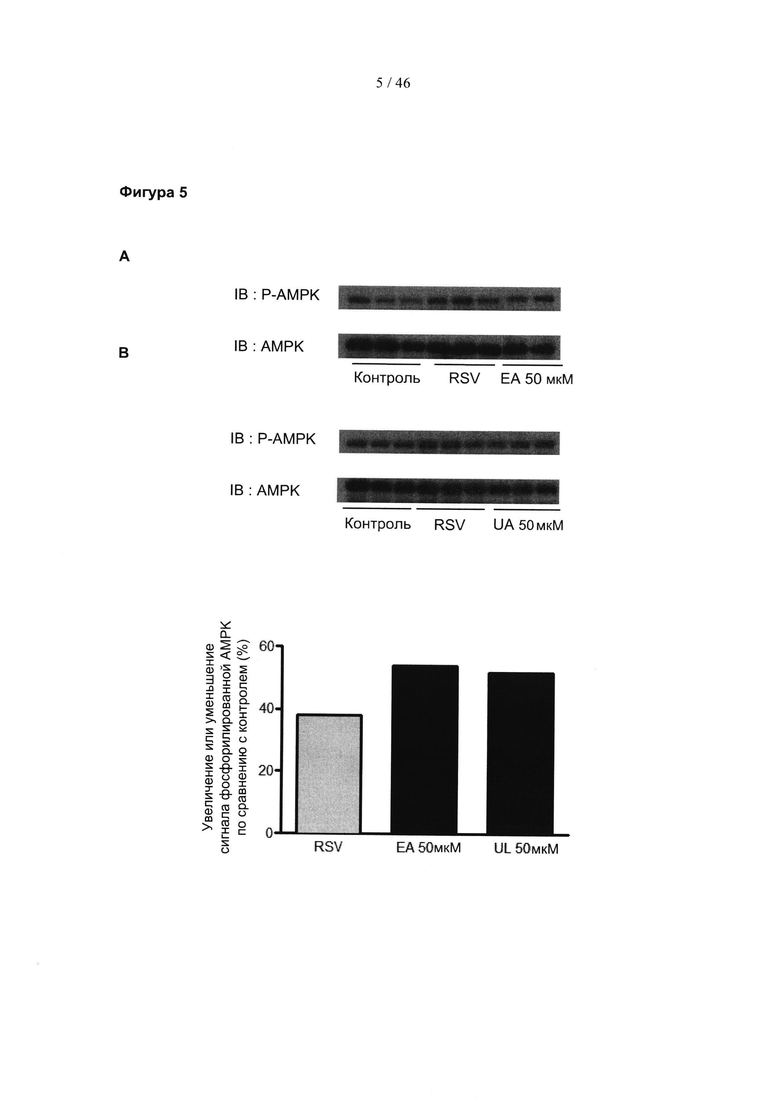
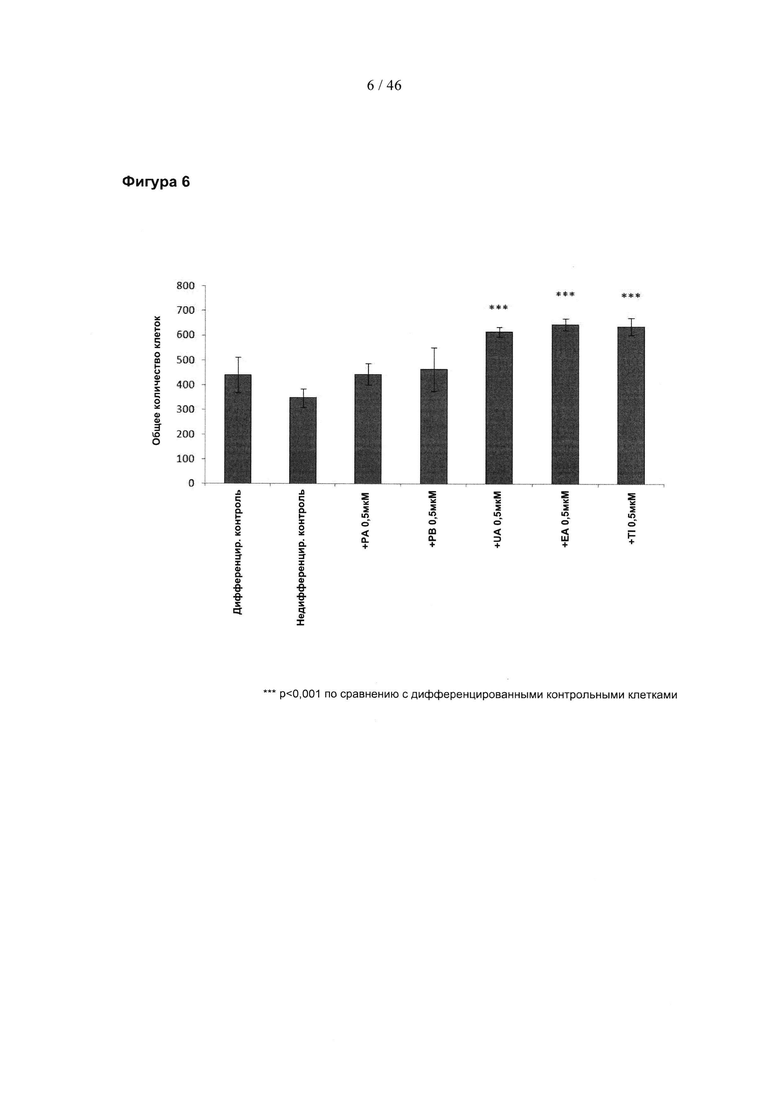
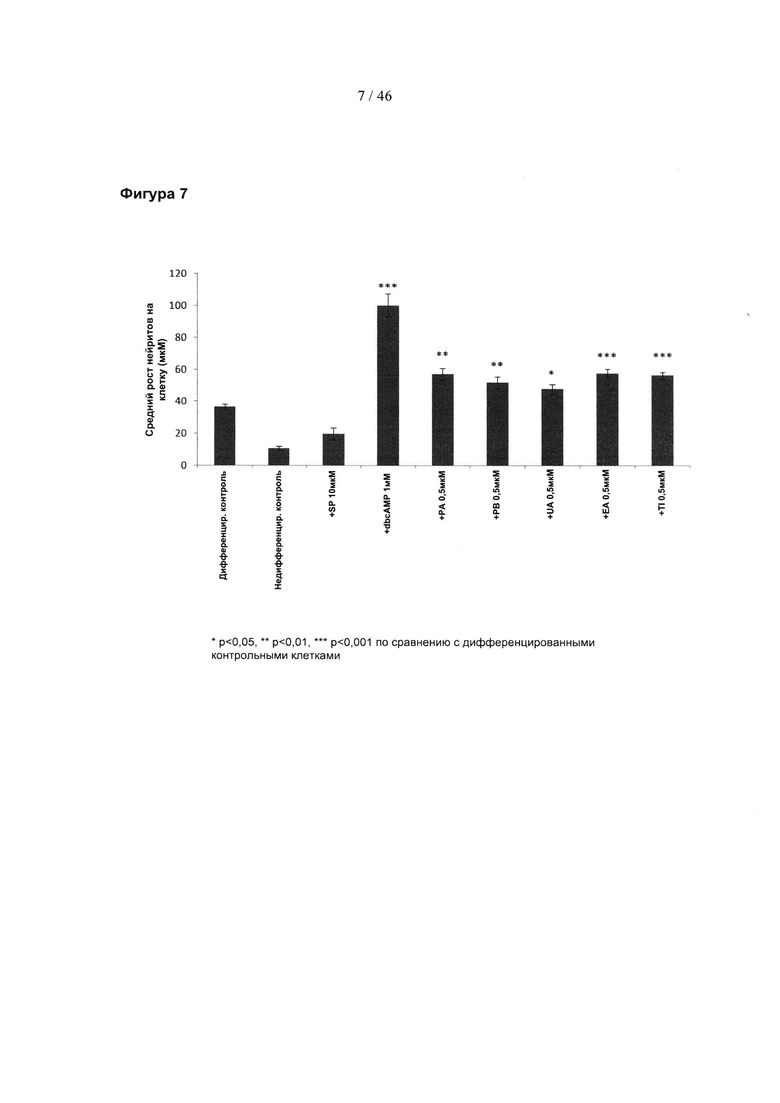
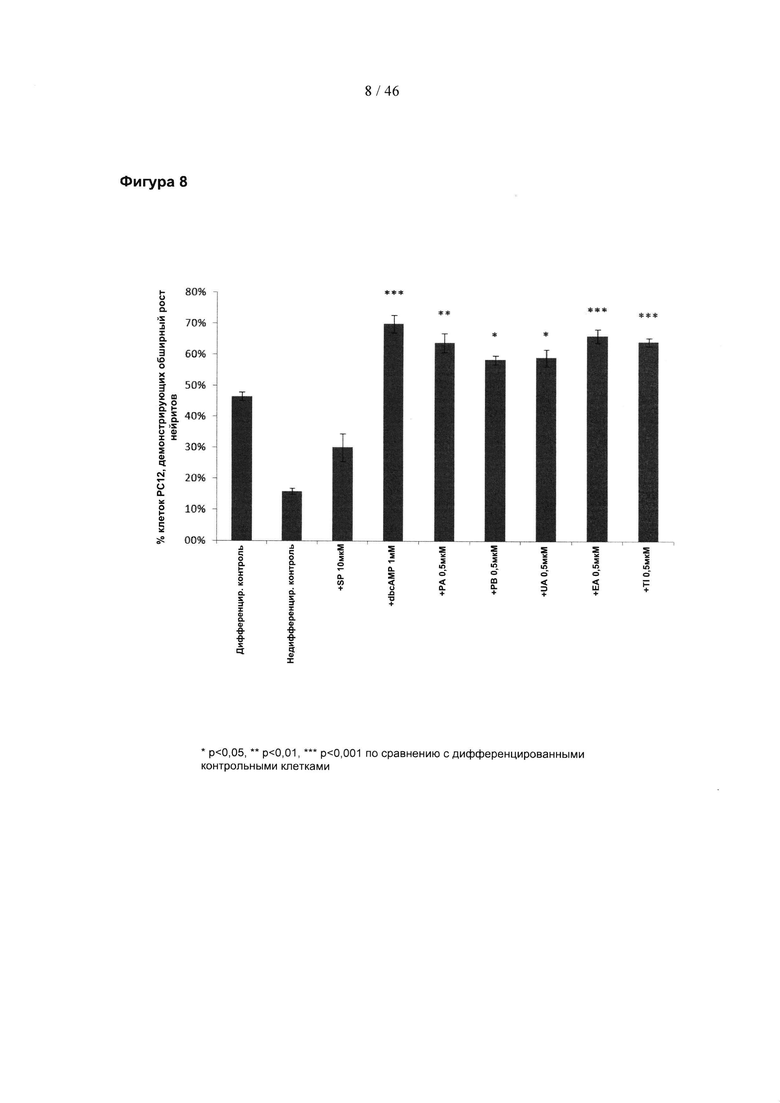
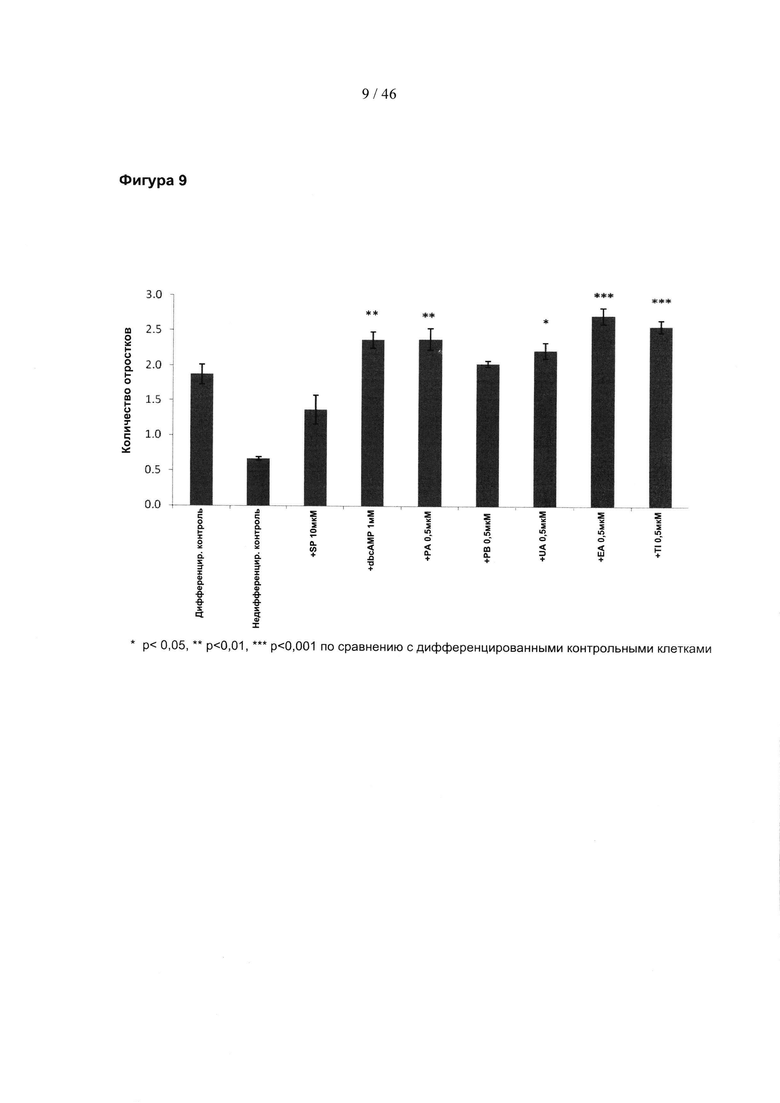
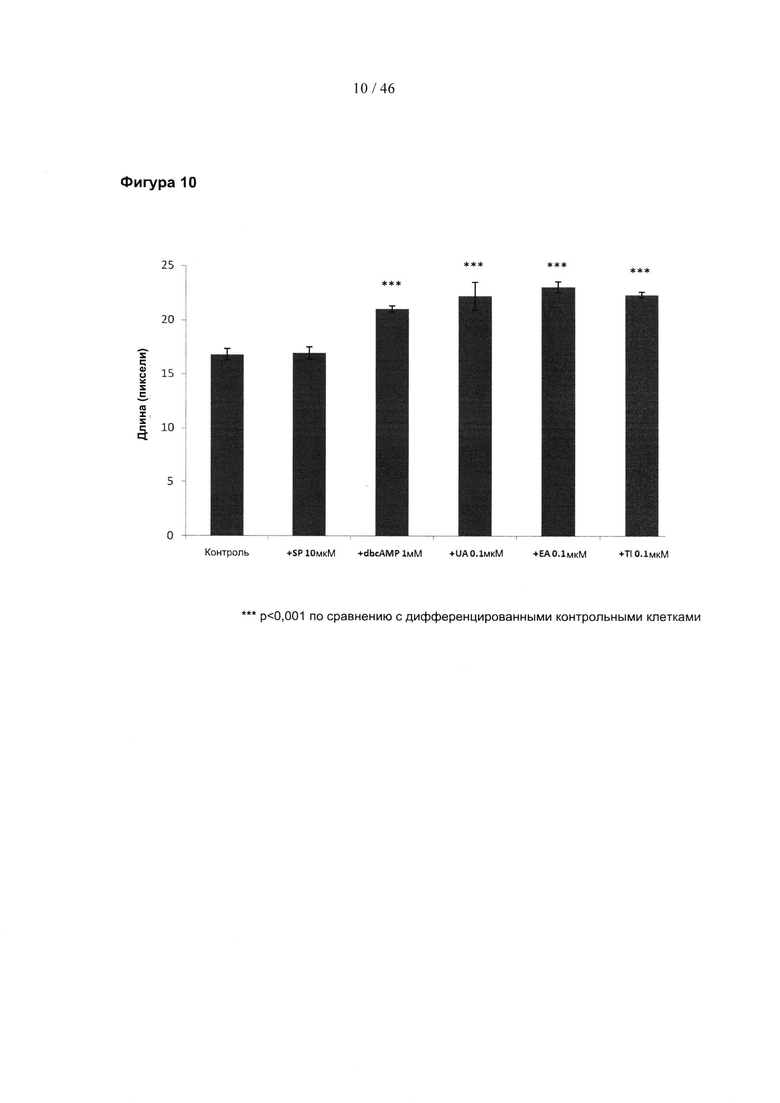
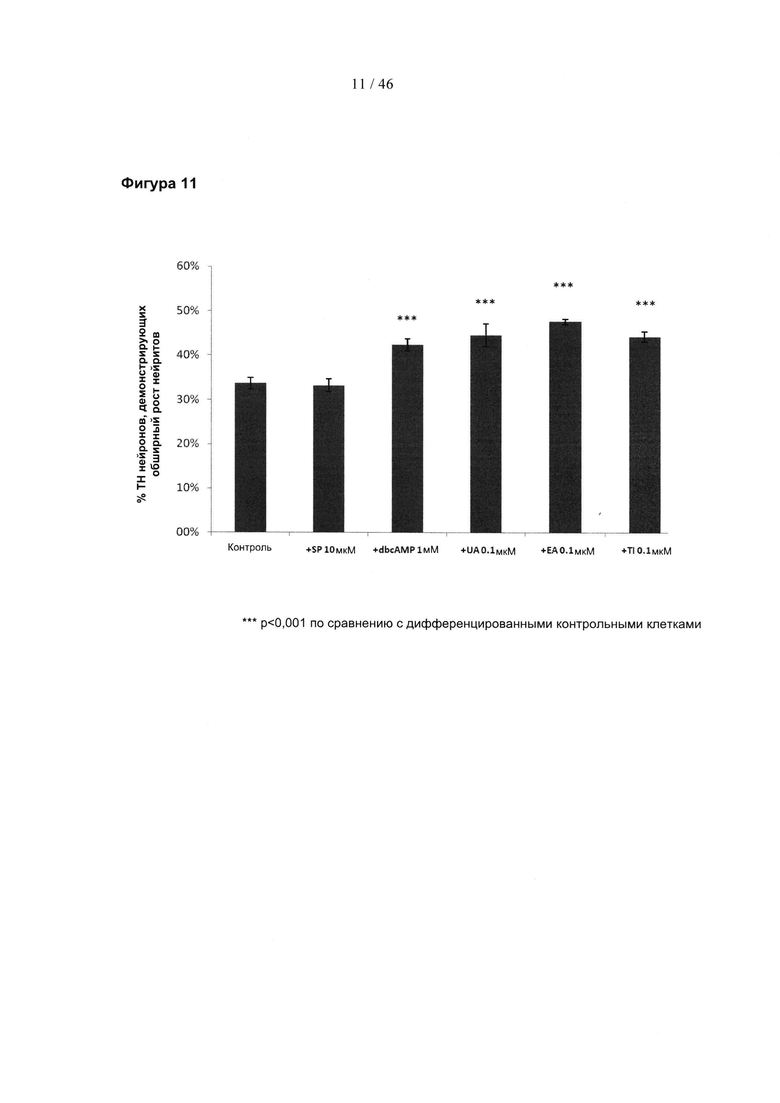
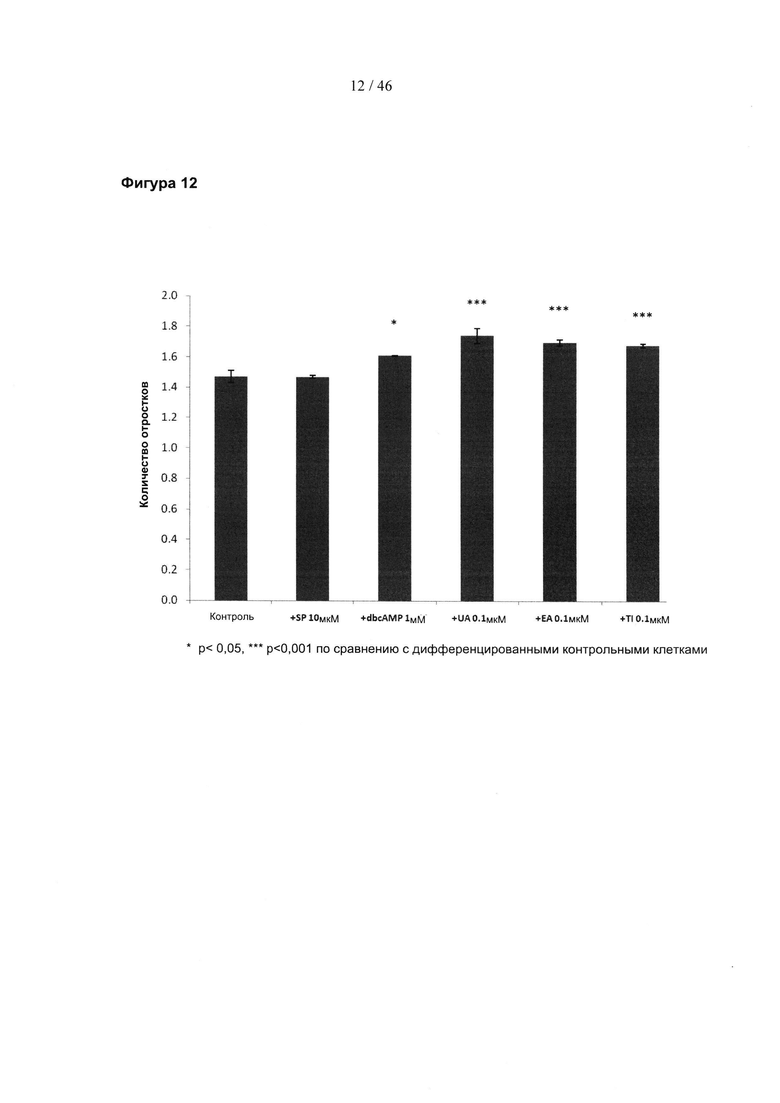
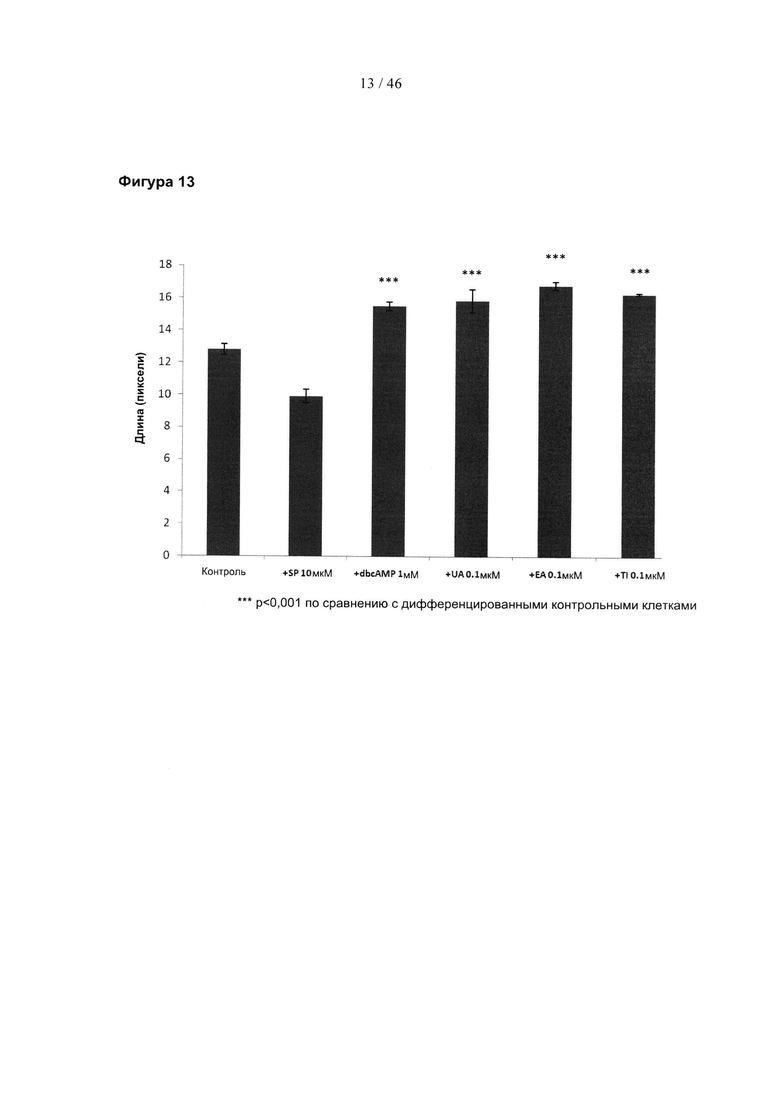
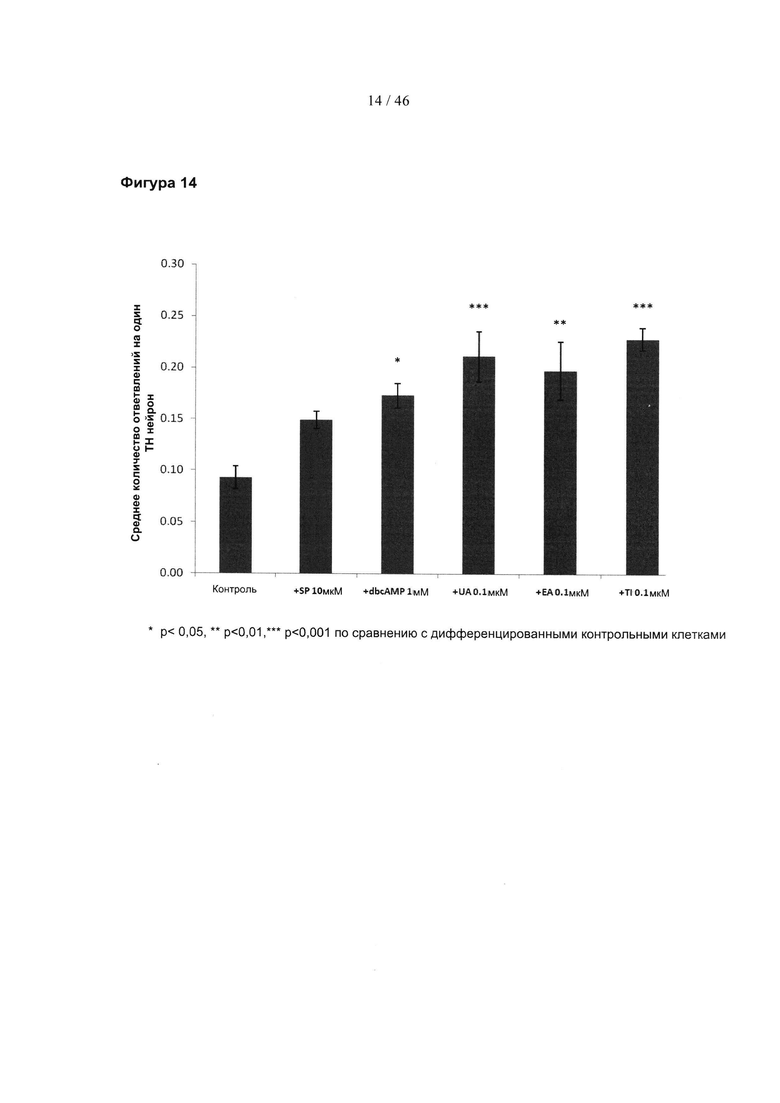
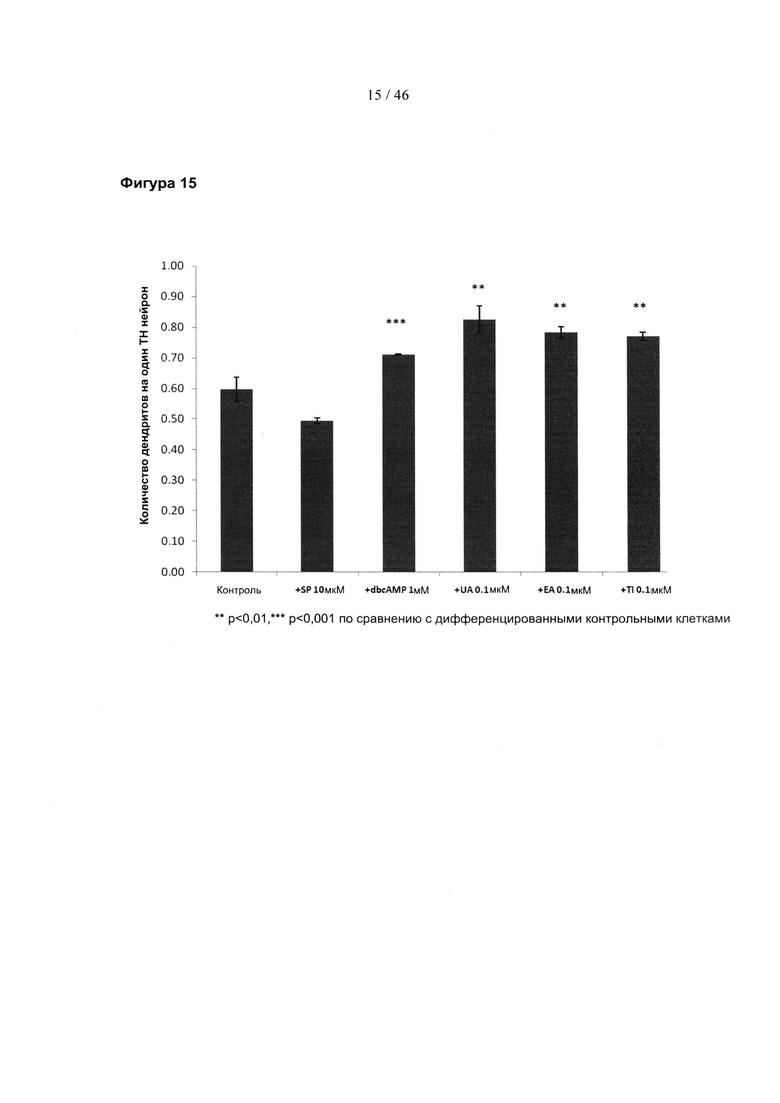
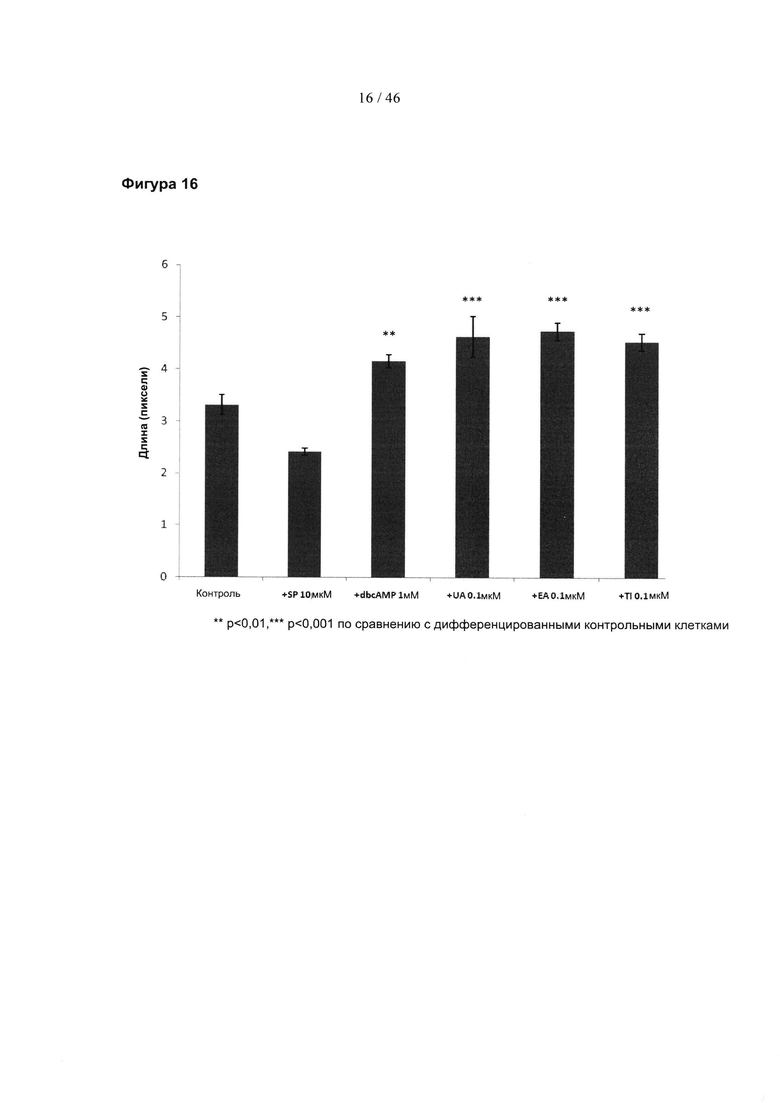
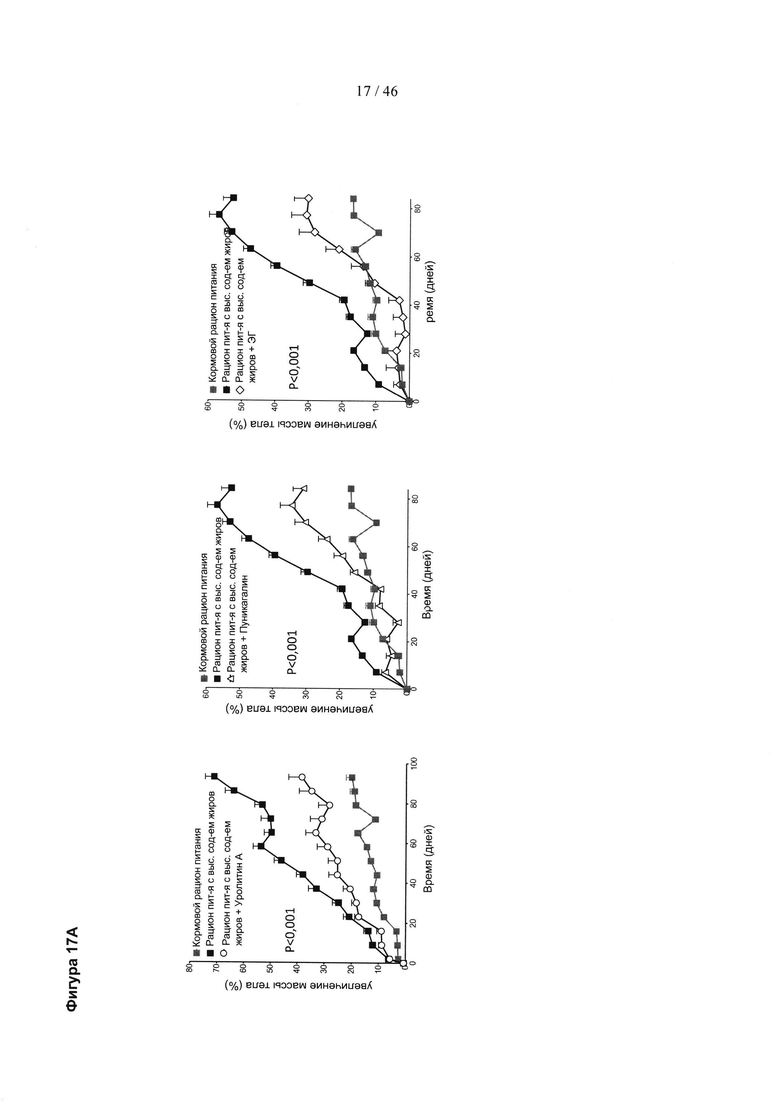
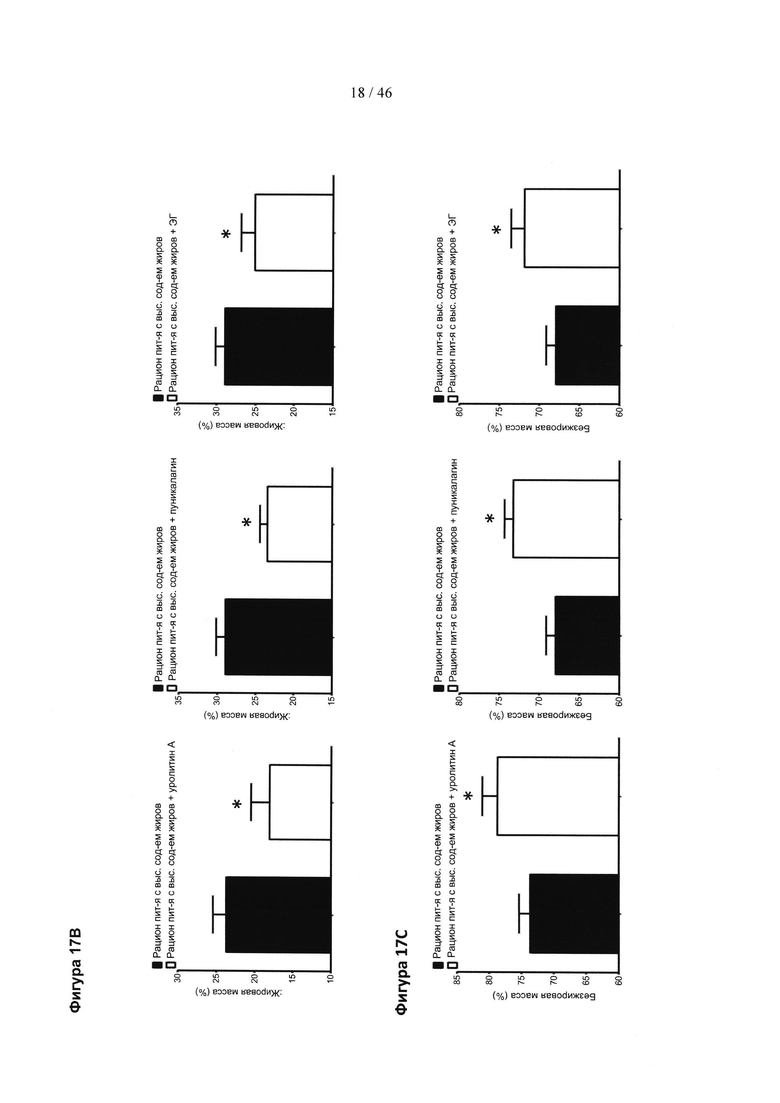

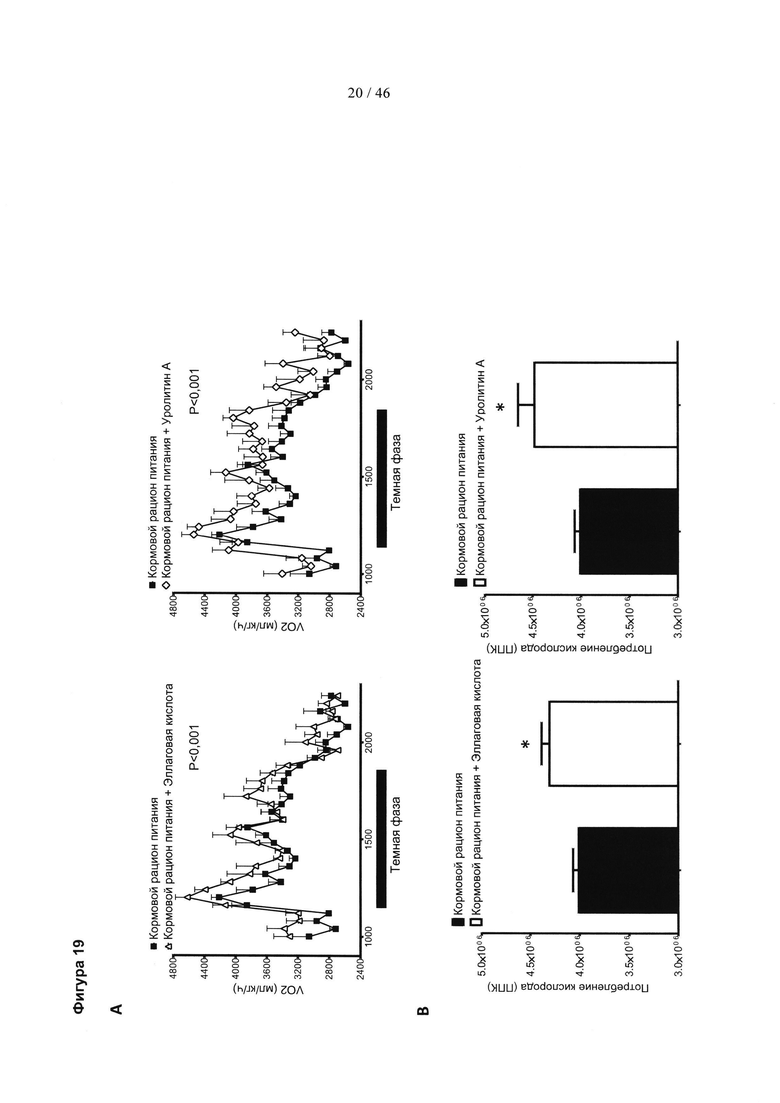
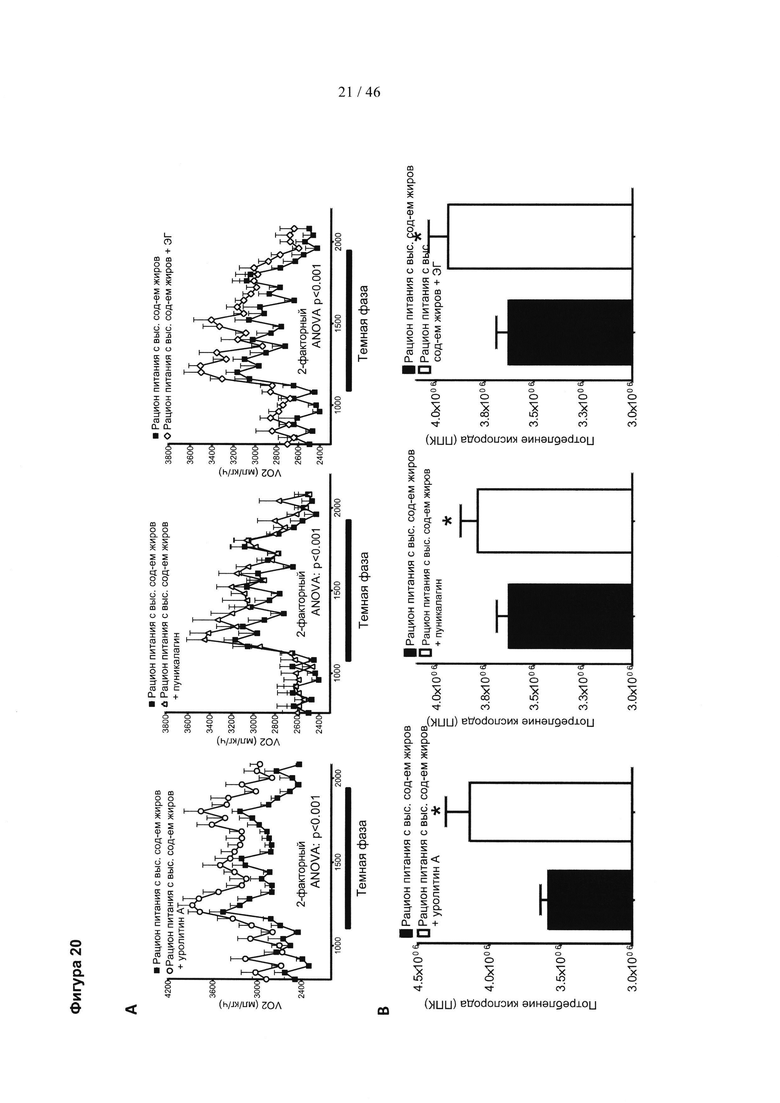
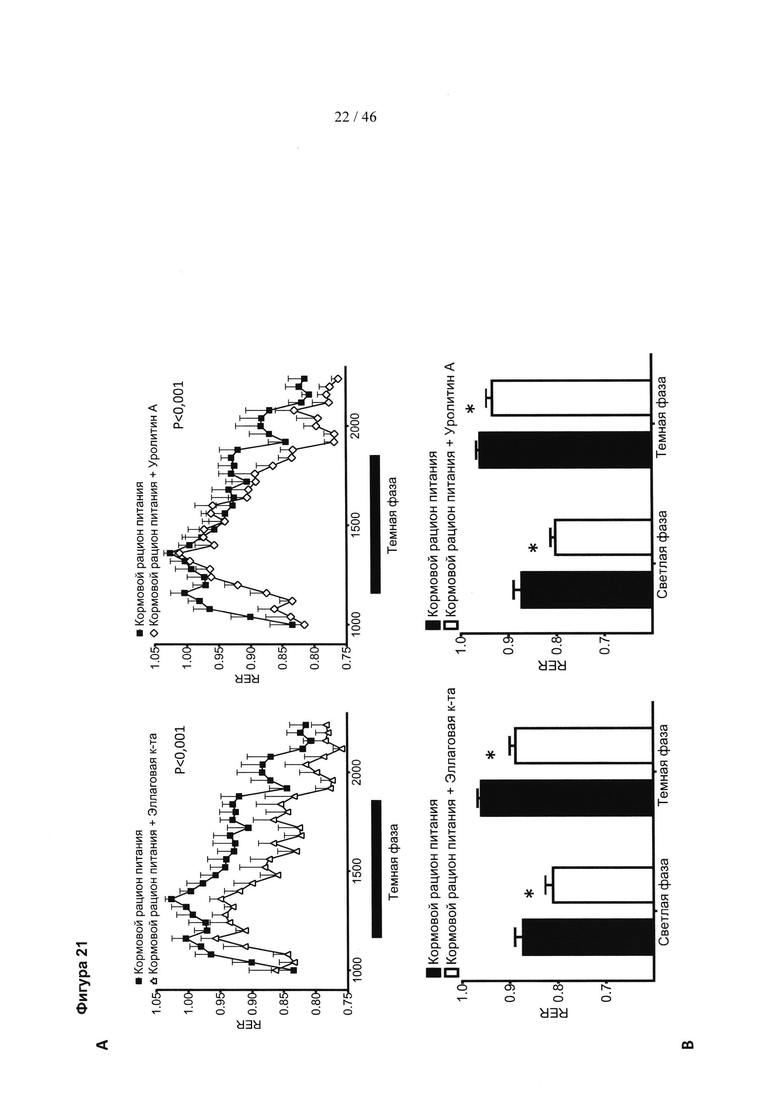
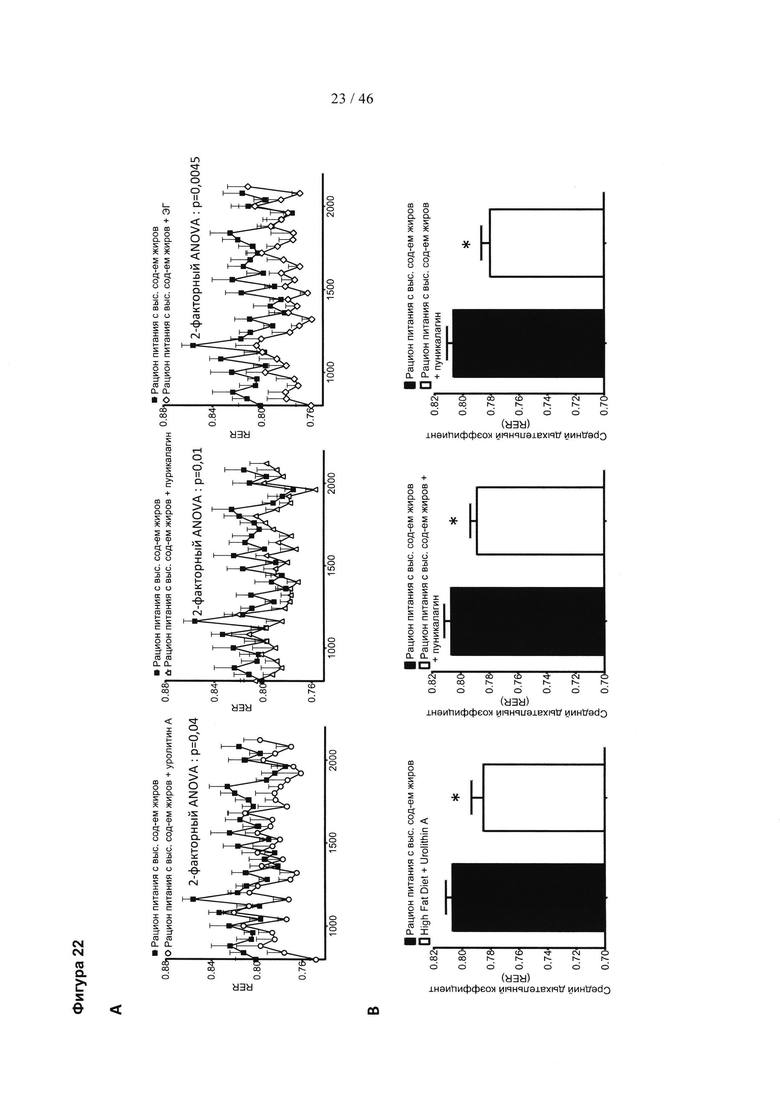
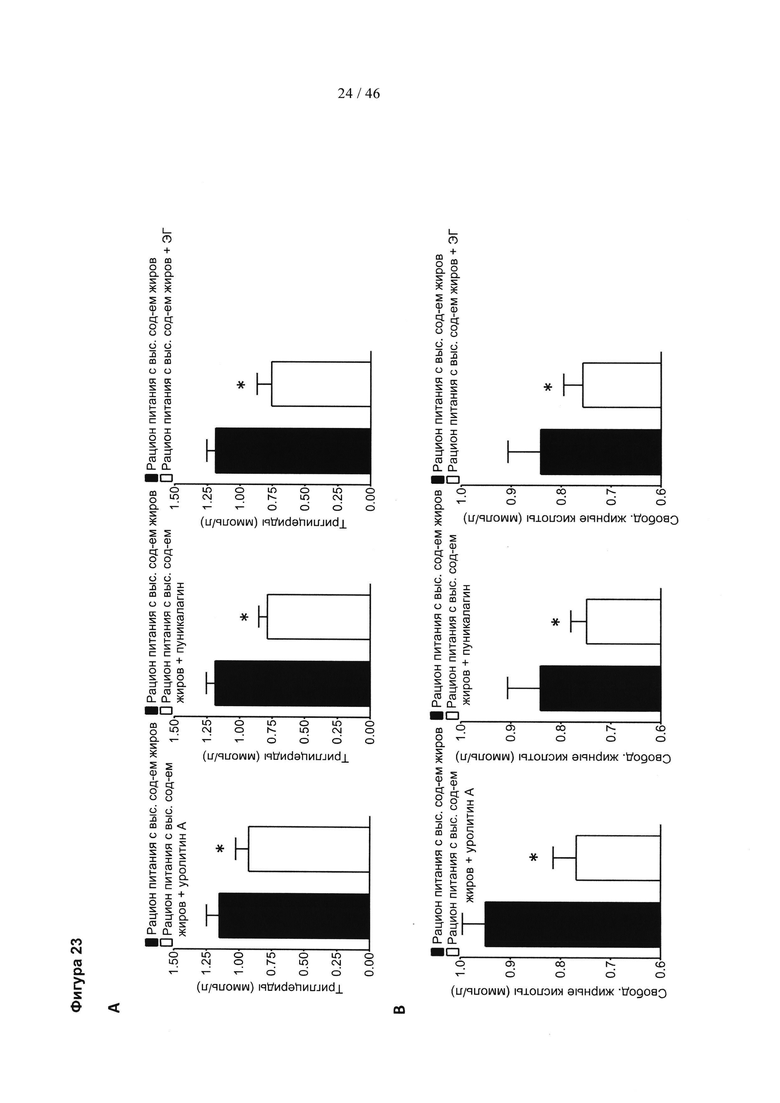
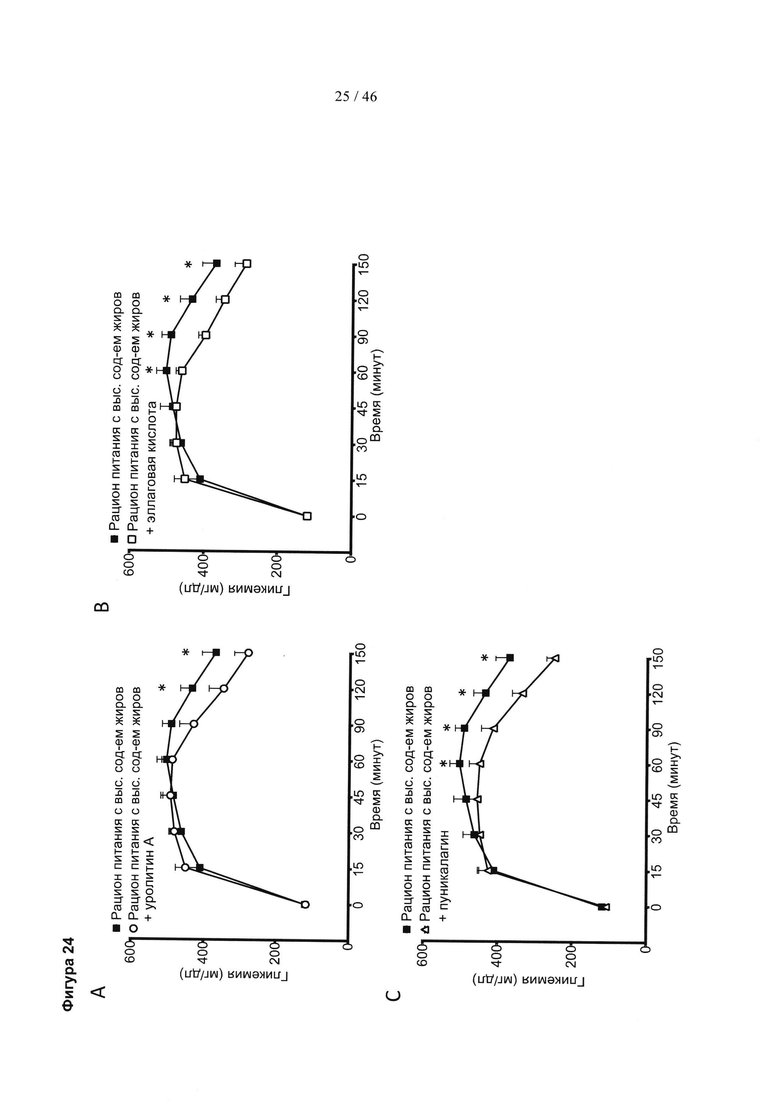
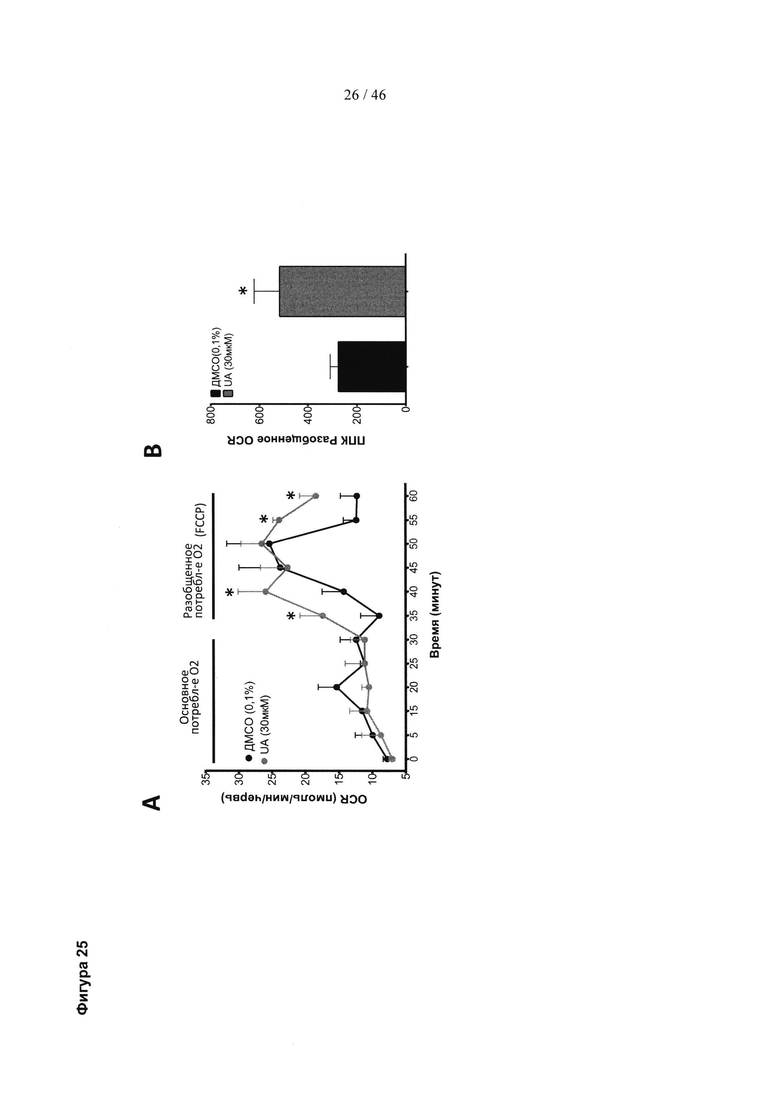
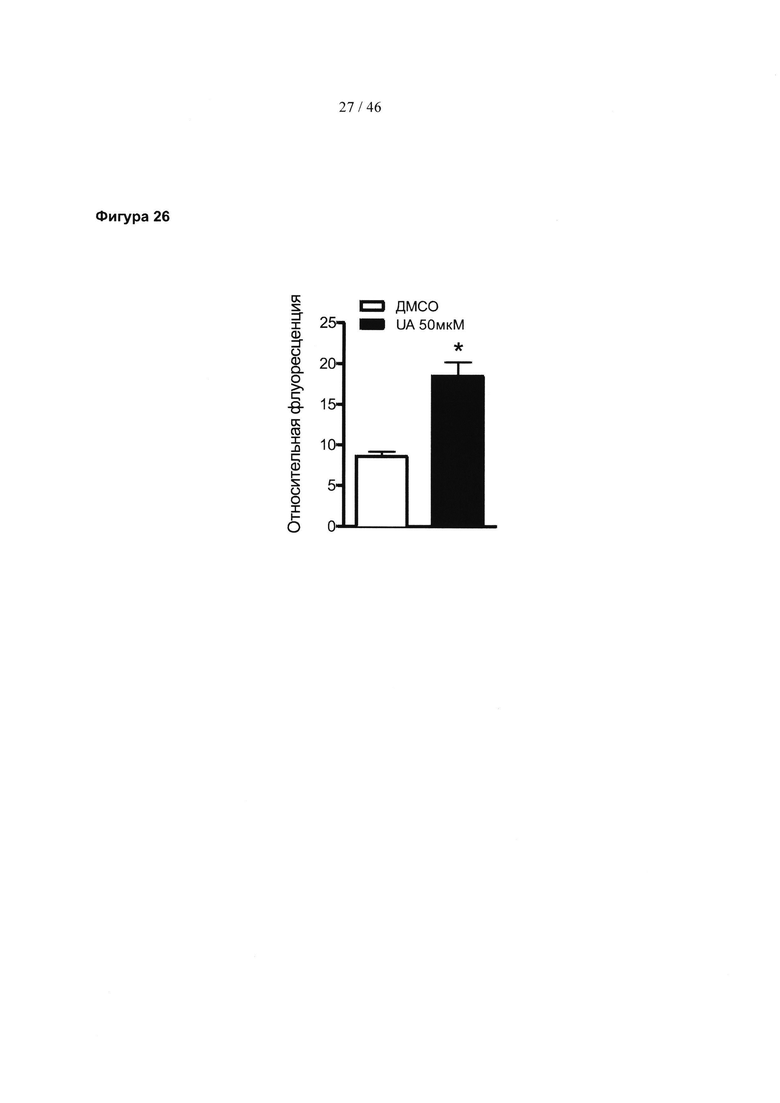
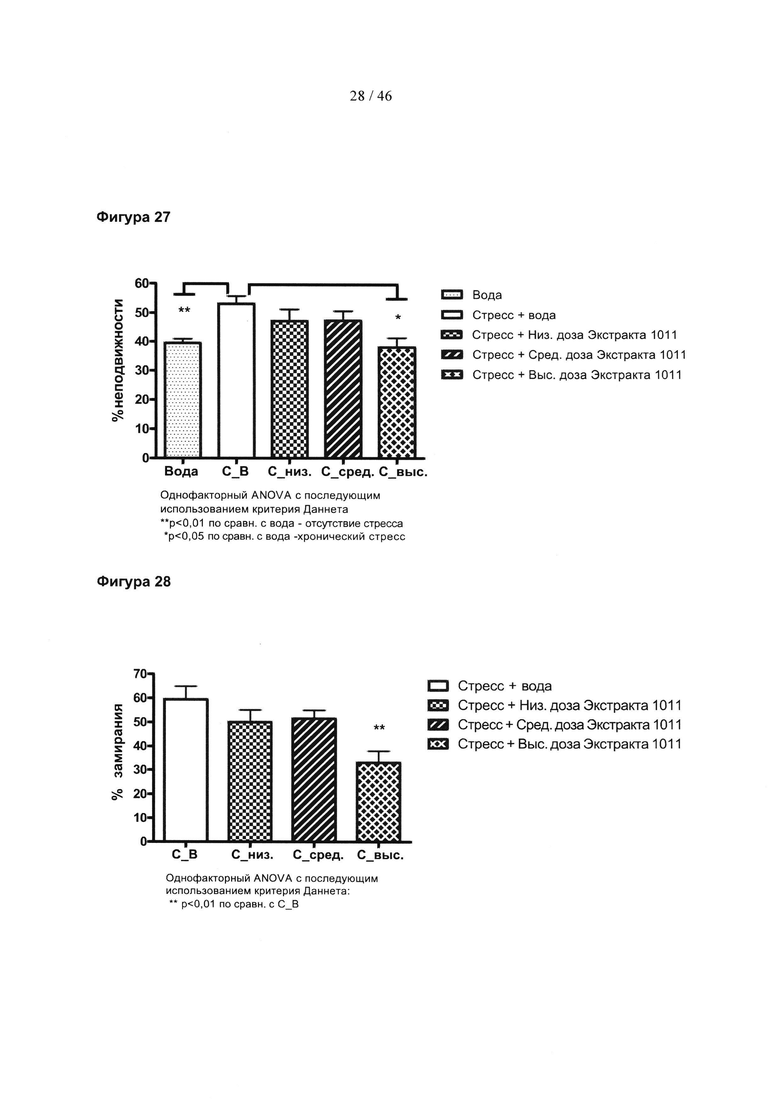
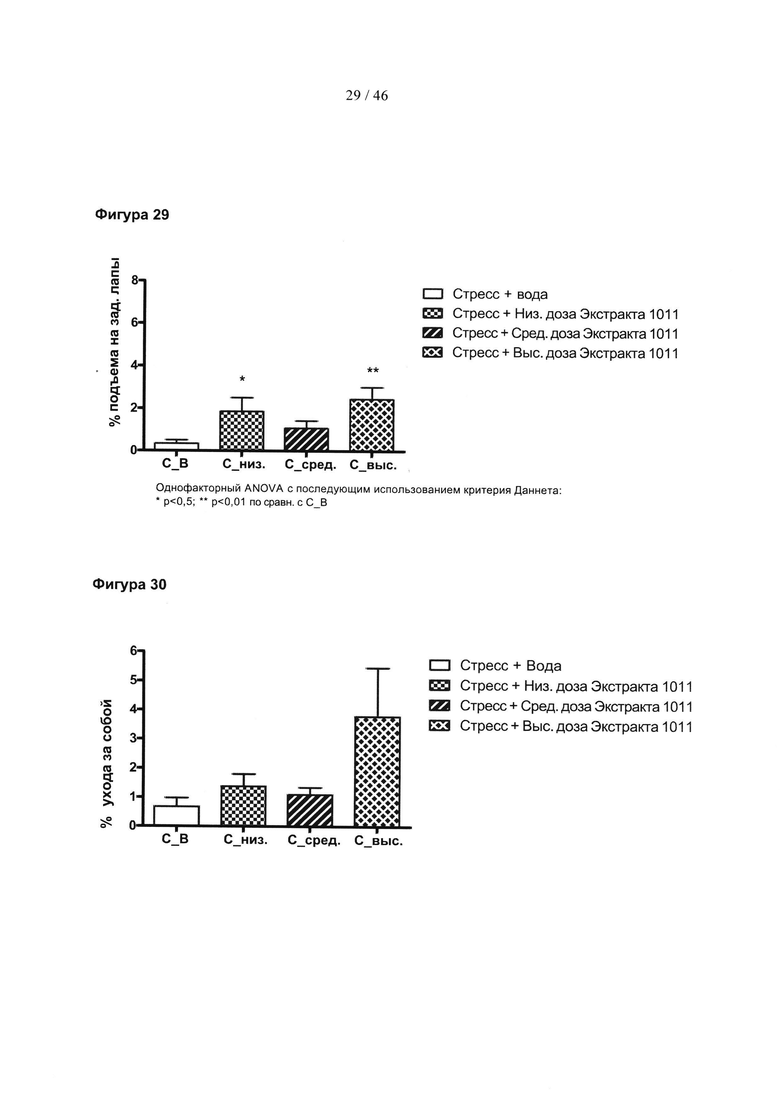
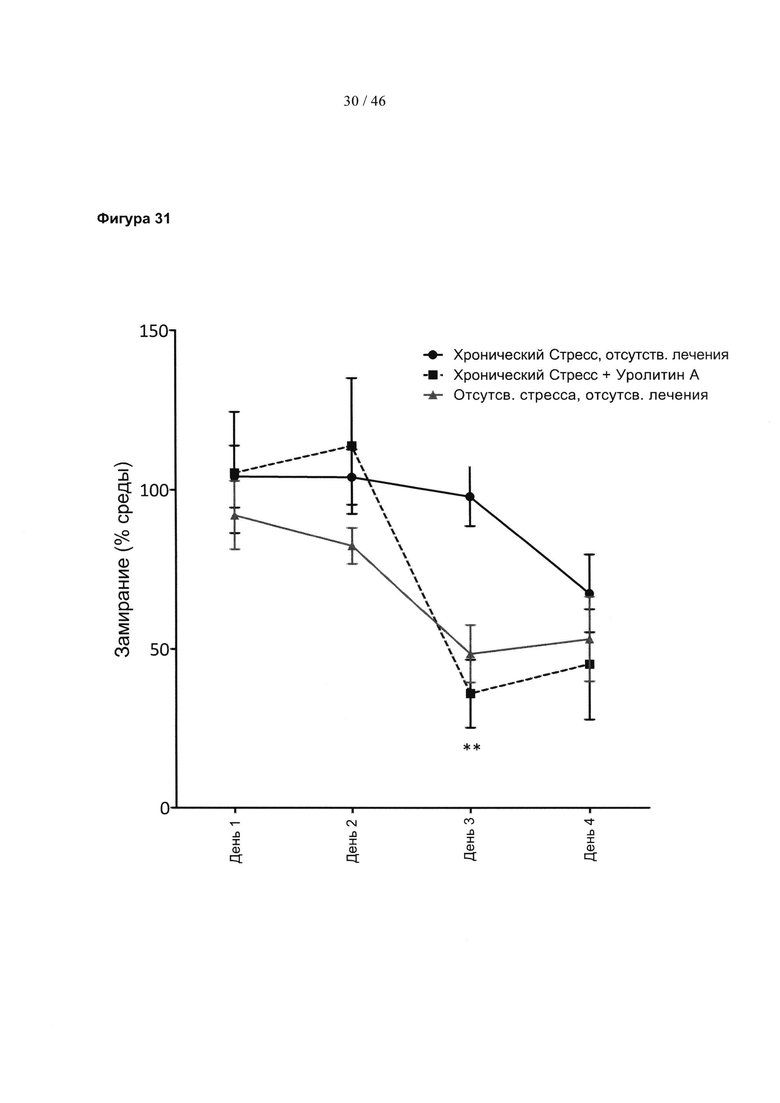
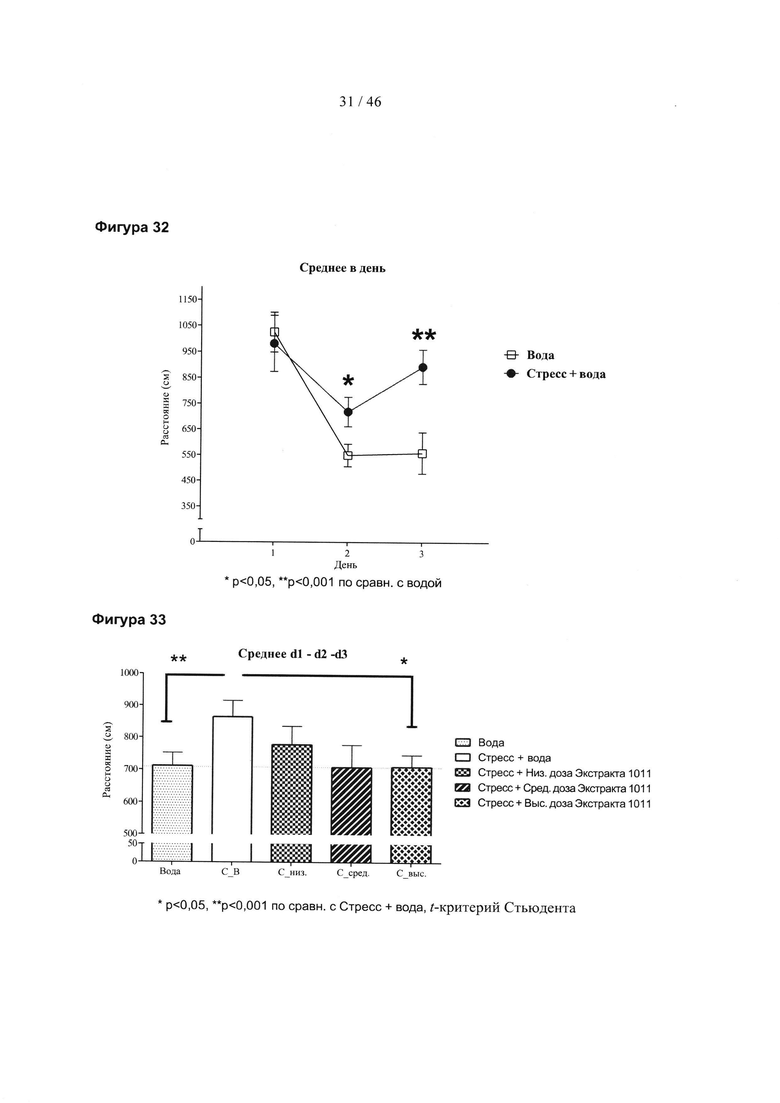
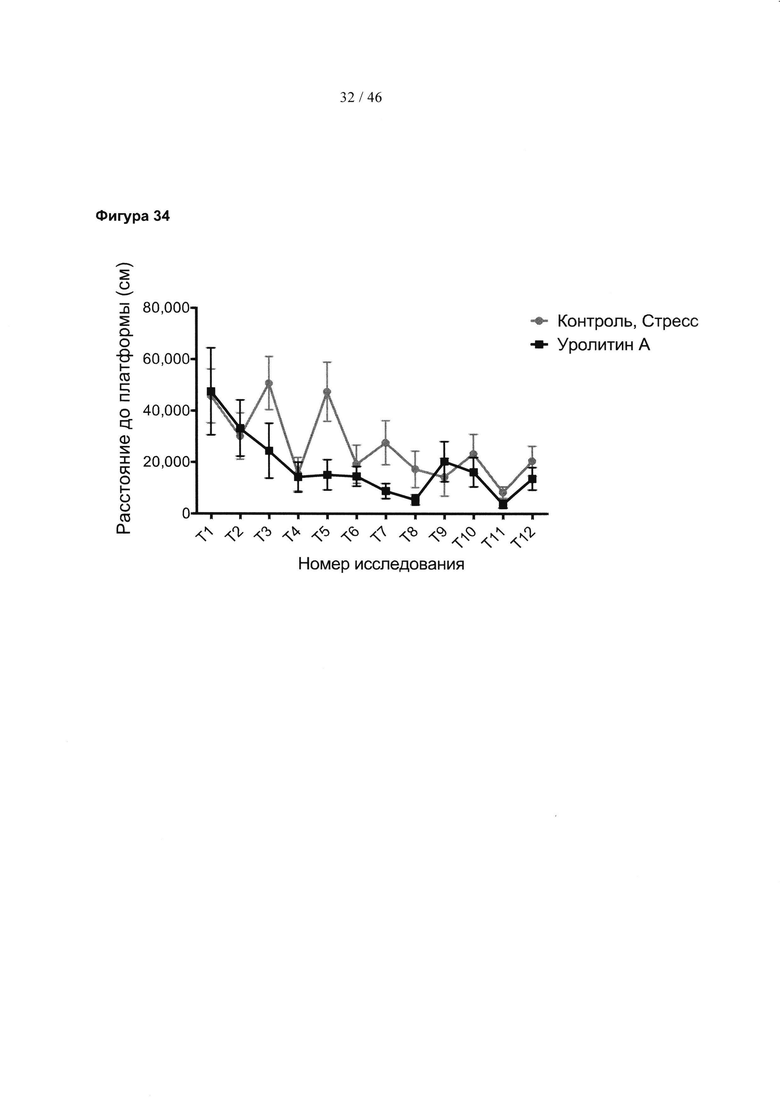
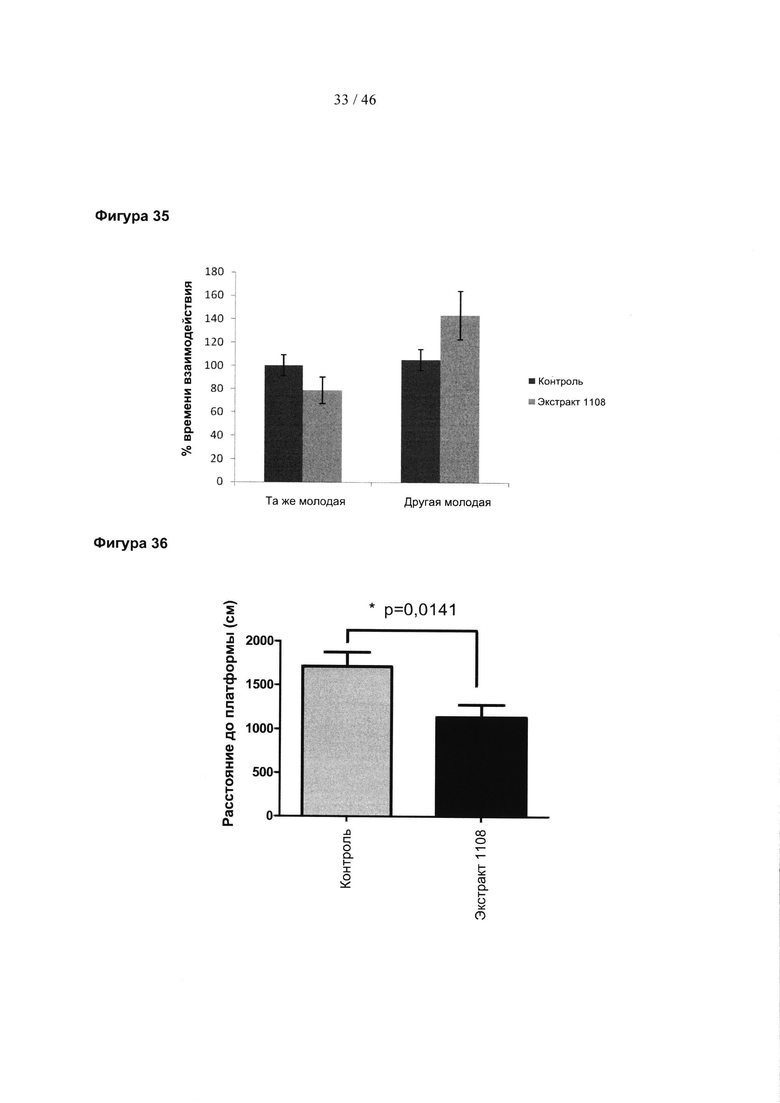
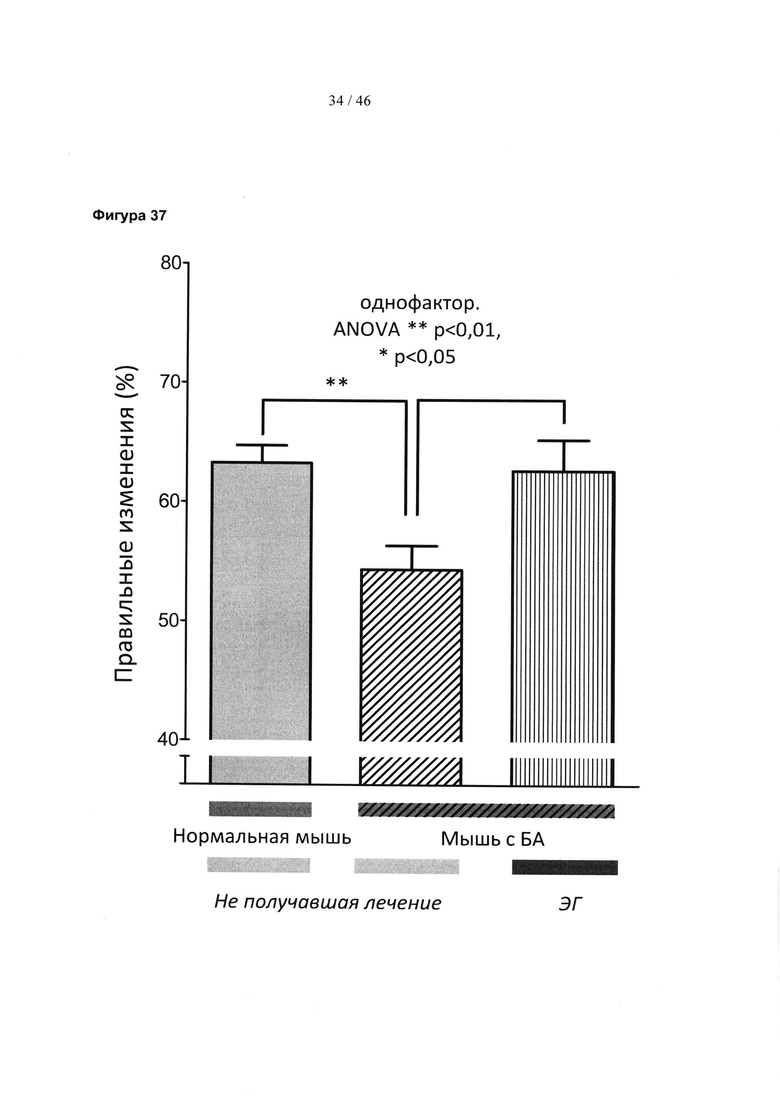
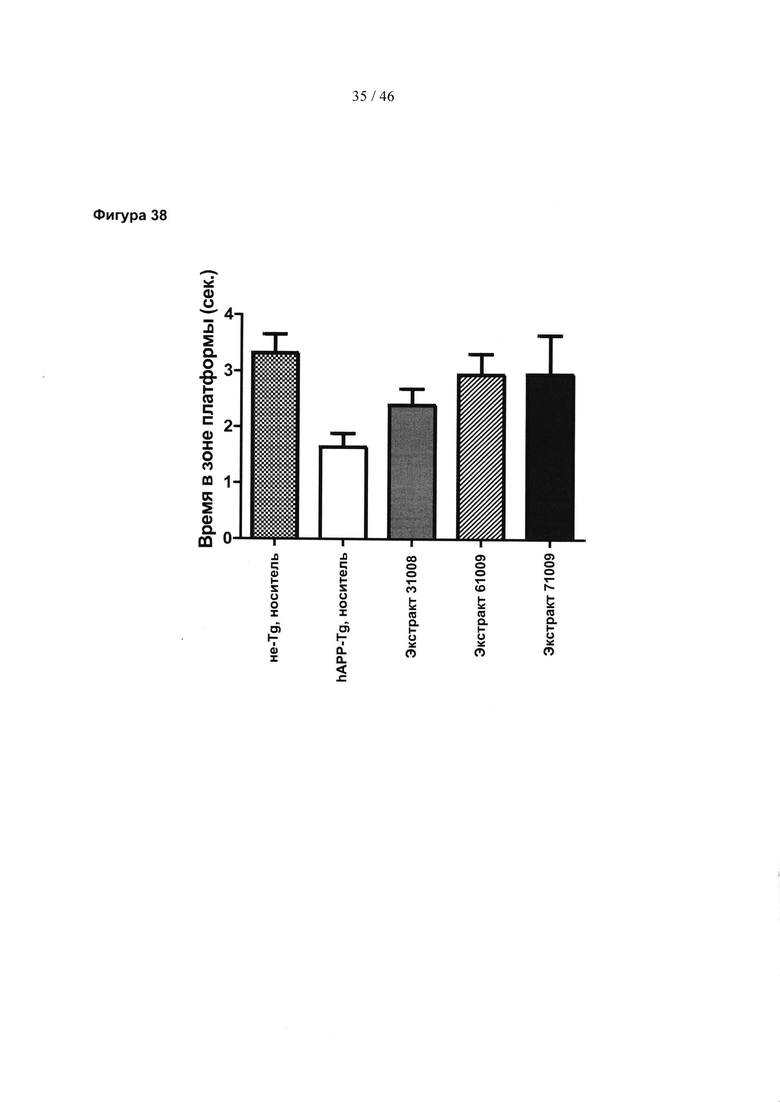
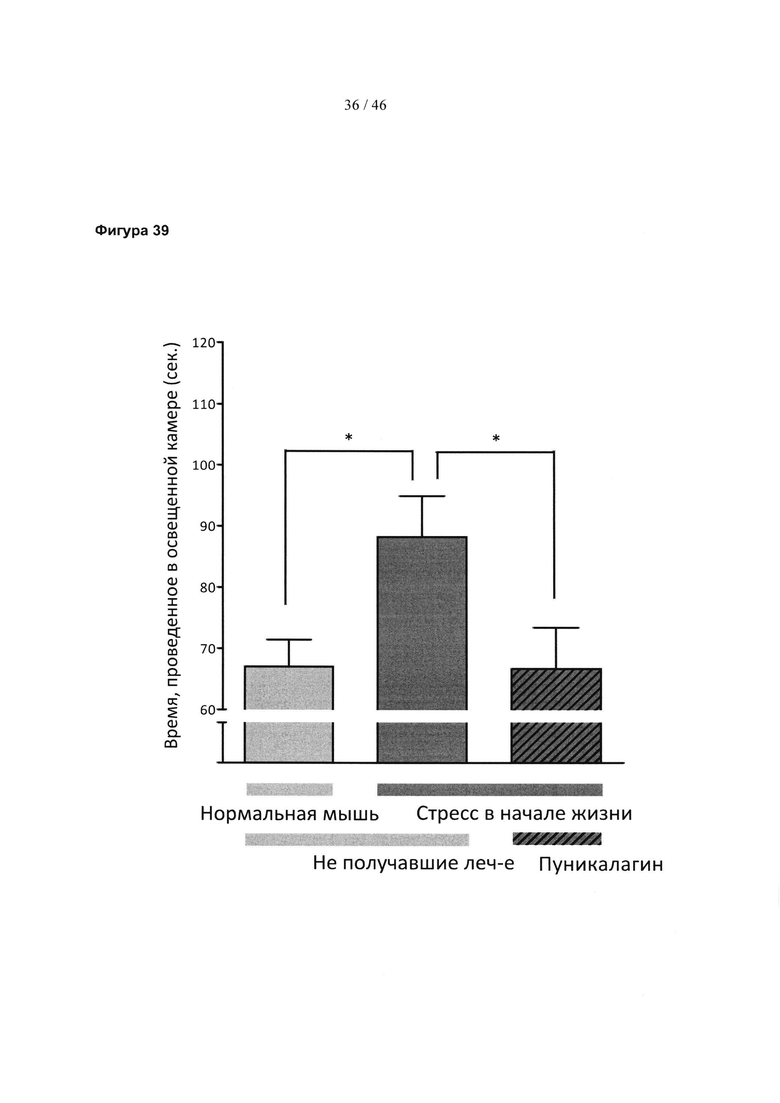
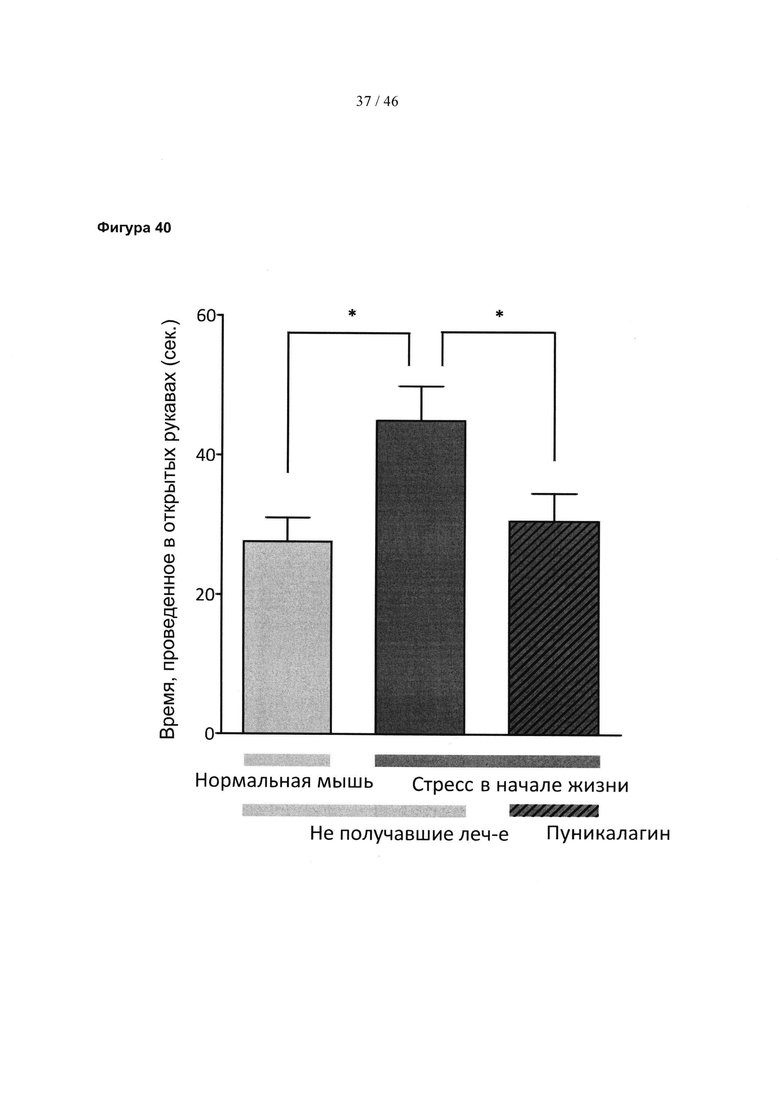
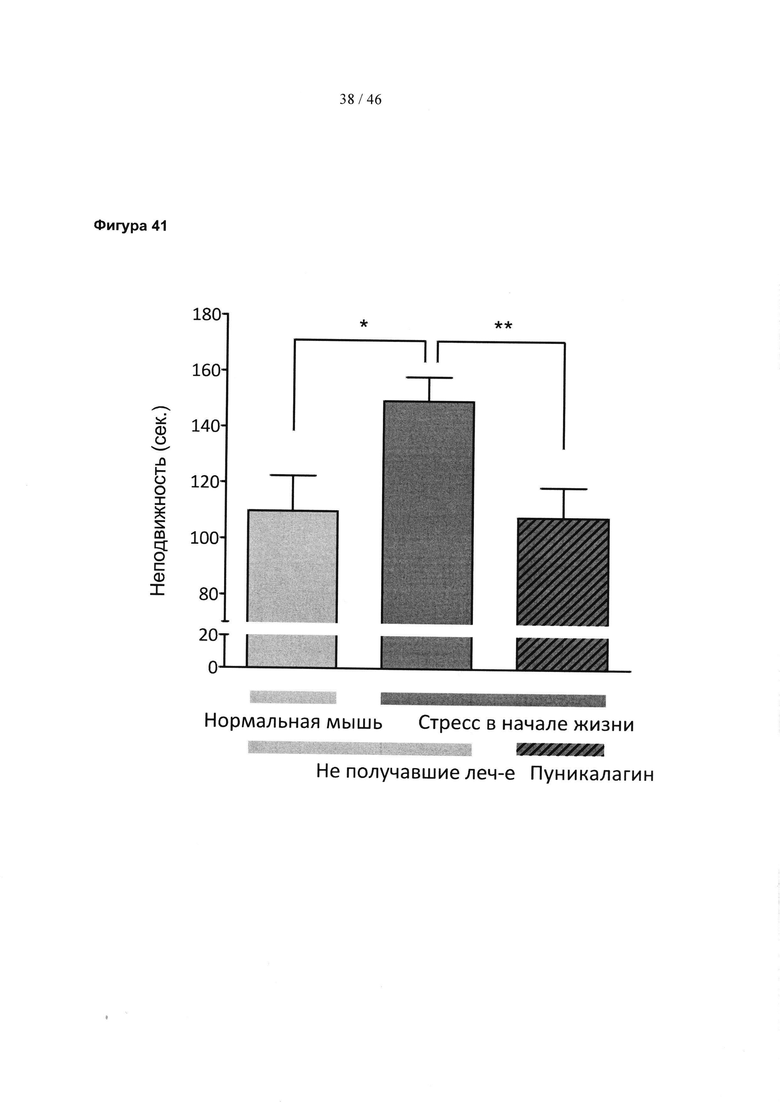
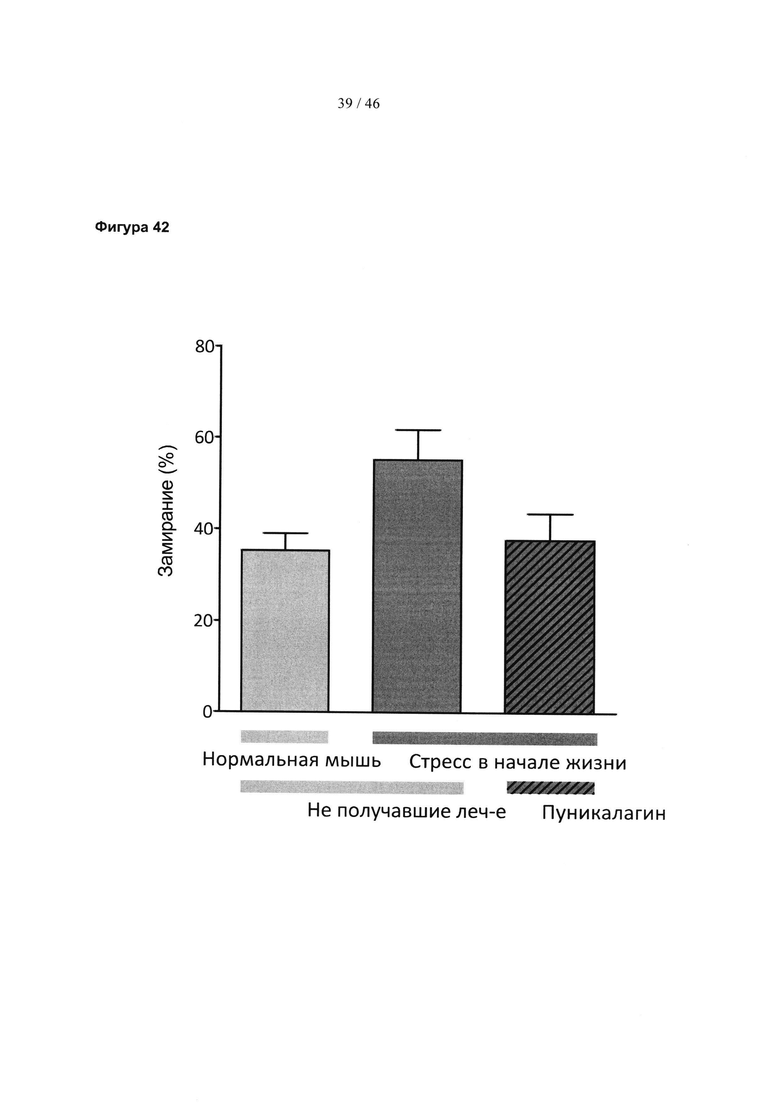
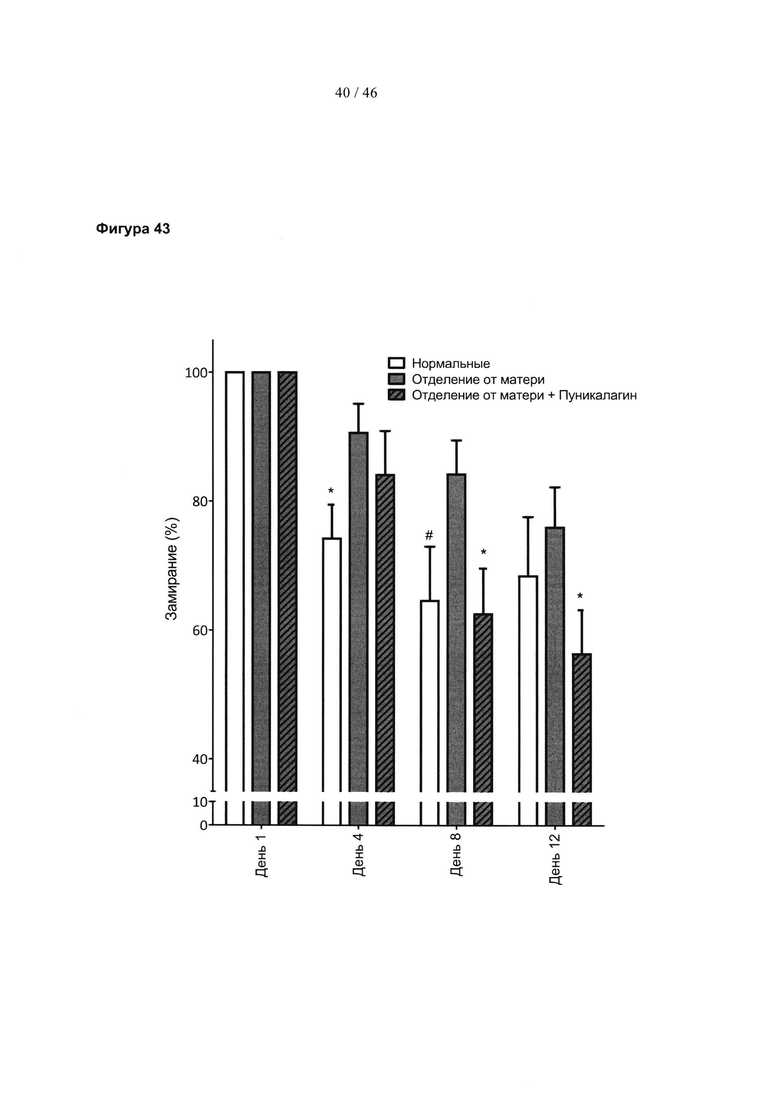
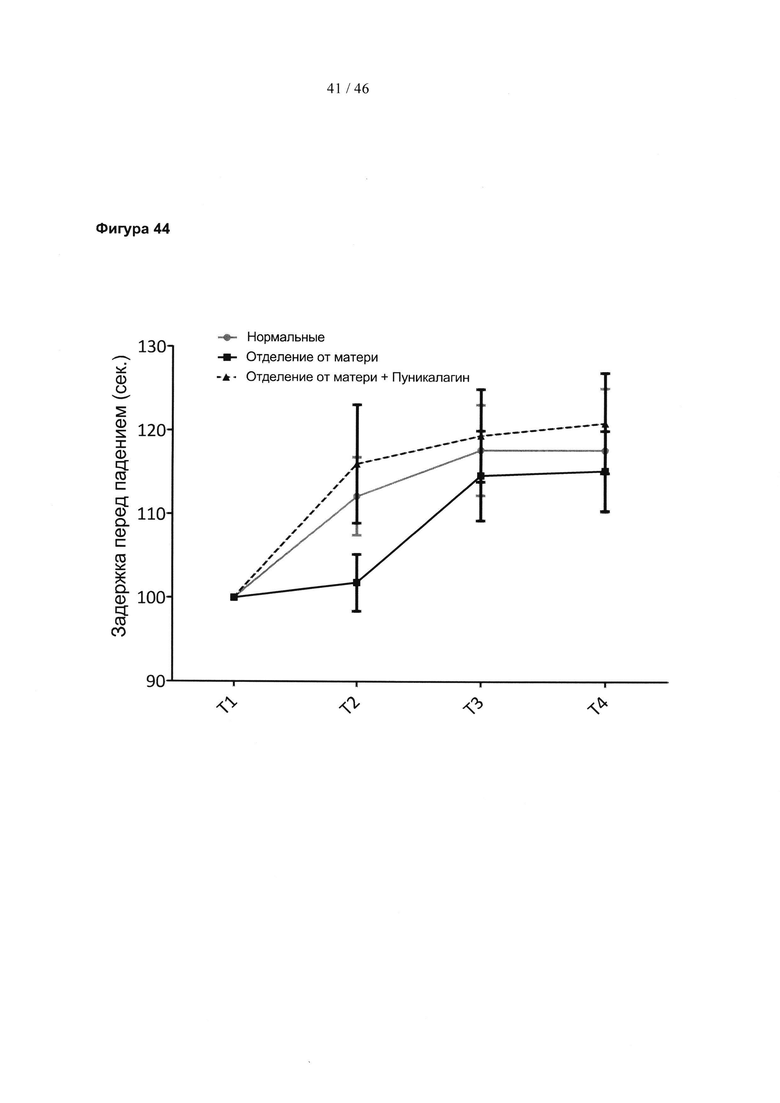
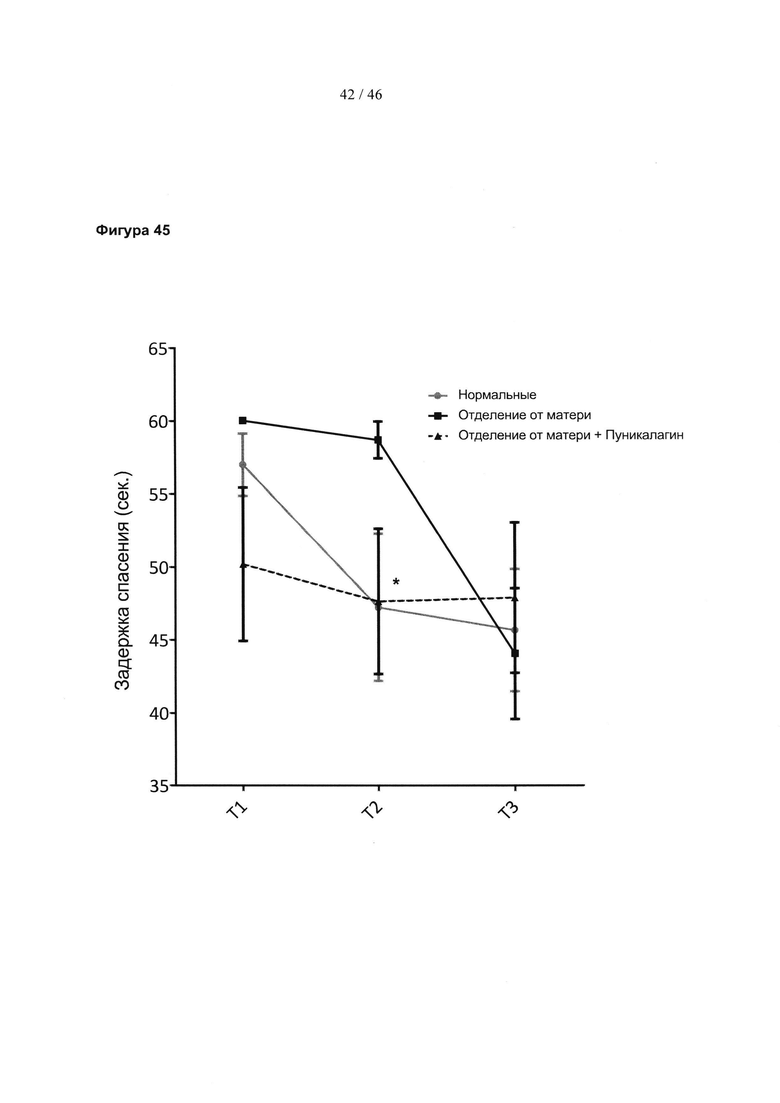
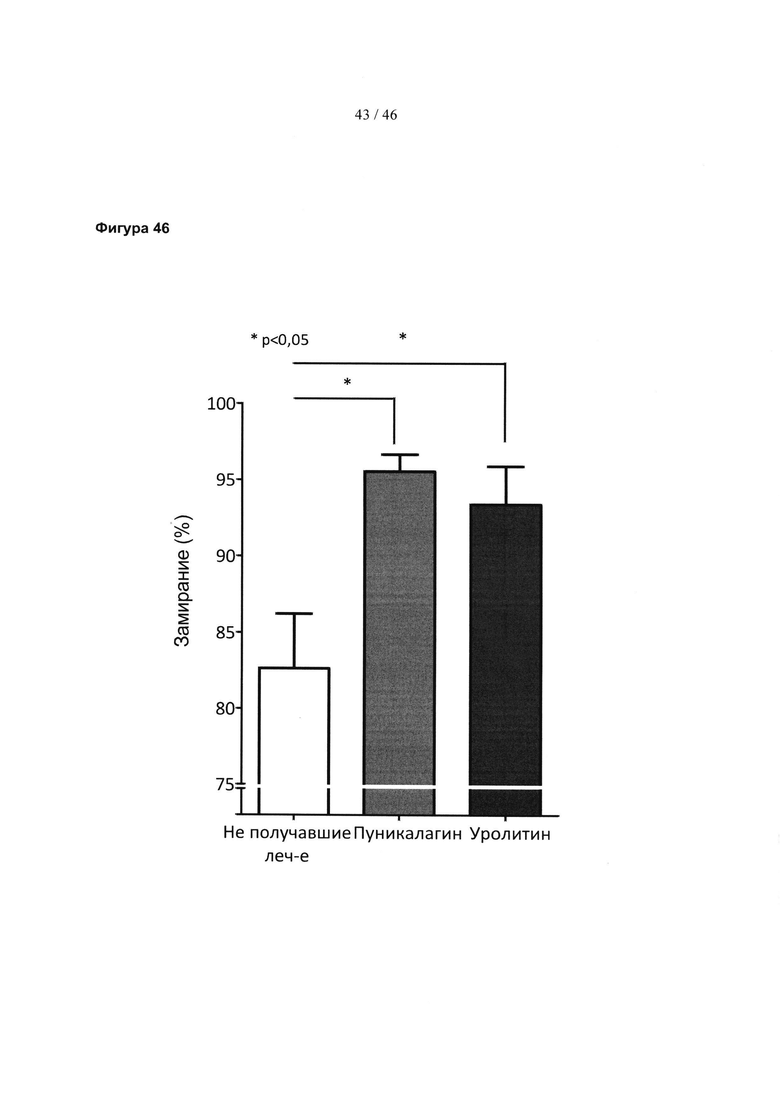
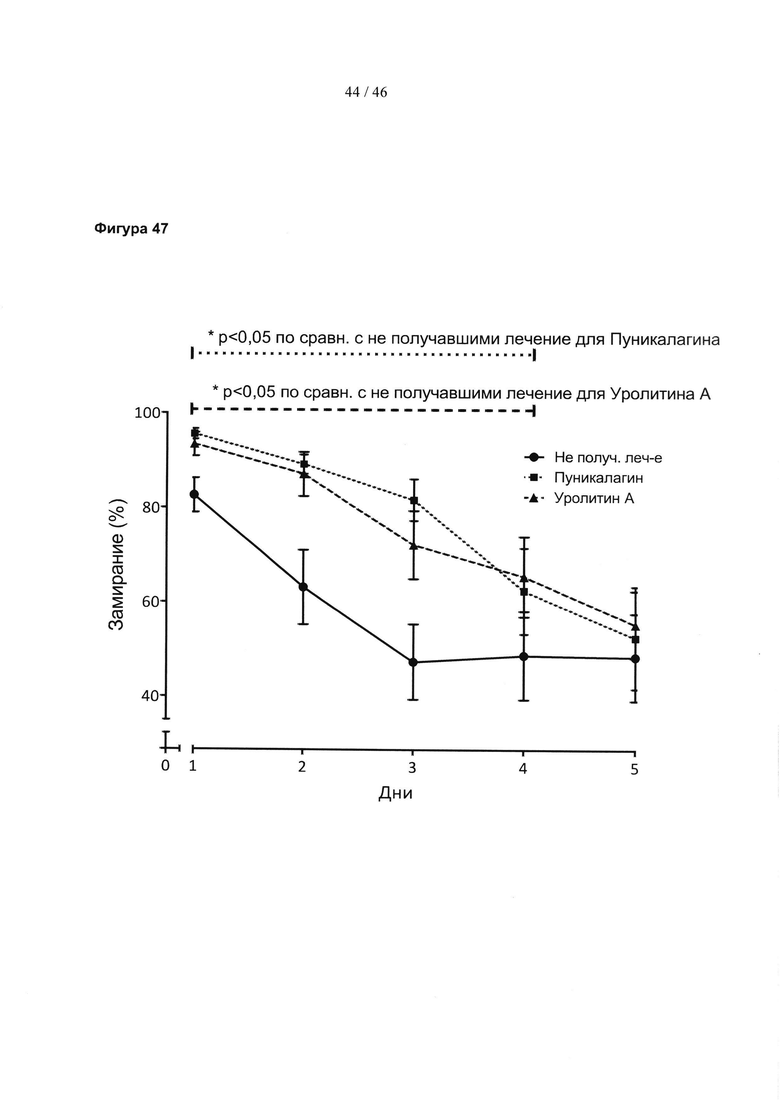
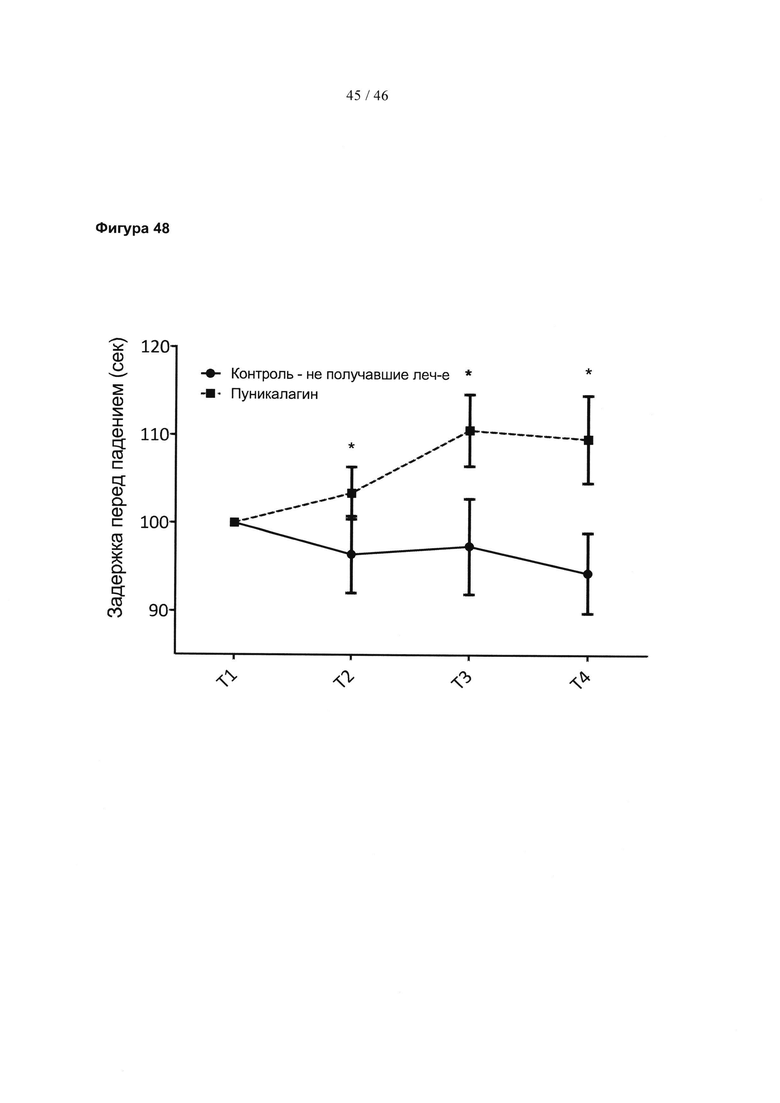
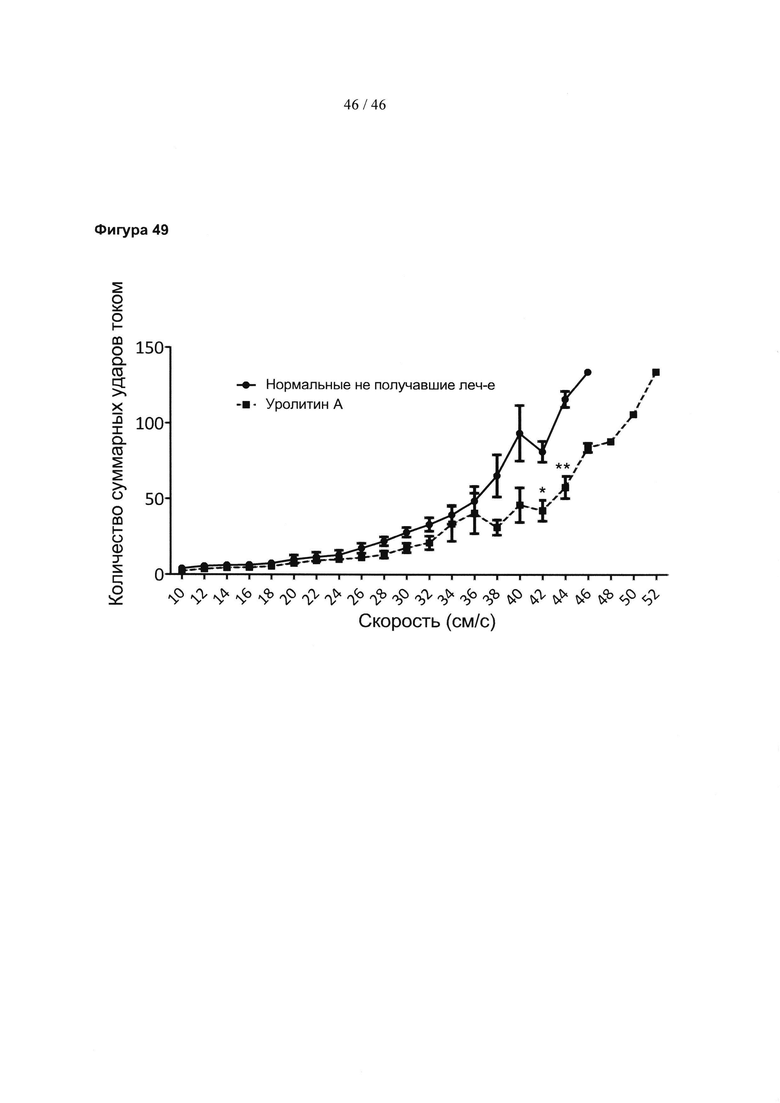
Группа изобретений относится к фармацевтической промышленности, а именно к композиции для лечения или предотвращения состояния, связанного с дисфункцией митохондрий. Фармацевтическая композиция для лечения или предотвращения состояния, связанного с дисфункцией митохондрий, содержащая эффективное количество уролитина, причем указанное состояние выбрано из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивной функции или расстройства, расстройства настроения, стресса и тревожного расстройства; и причем уролитин выбран из группы, состоящей из уролитина A, уролитина B, уролитина C и уролитина D. Способ лечения или предотвращения состояния, связанного с дисфункцией митохондрий, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивной функции или расстройства, расстройства настроения, стресса и тревожного расстройства, включающий: введение нуждающемуся в этом субъекту терапевтически эффективного количества уролитина, причем уролитин выбран из группы, состоящей из уролитина A, уролитина B, уролитина C и уролитина D. Применение уролитина для приготовления лекарственного средства для лечения или предотвращения состояния, связанного с дисфункцией митохондрий, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивной функции или расстройства, расстройства настроения, стресса и тревожного расстройства; причем уролитин выбран из группы, состоящей из уролитина A, уролитина B, уролитина C и уролитина D. Вышеописанные соединения и композиции на их основе эффективны для лечения или предотвращения состояния, связанного с дисфункцией митохондрий. 3 н. и 36 з.п. ф-лы, 7 табл., 21 пр., 49 ил.
1. Фармацевтическая композиция для лечения или предотвращения состояния, связанного с дисфункцией митохондрий, содержащая эффективное количество уролитина, причем указанное состояние выбрано из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивной функции или расстройства, расстройства настроения, стресса и тревожного расстройства; и причем уролитин выбран из группы, состоящей из уролитина A, уролитина B, уролитина C и уролитина D.
2. Фармацевтическая композиция по п. 1 для повышения или поддержания функции митохондрий.
3. Фармацевтическая композиция по п. 1 для увеличения скорости метаболизма.
4. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой ожирение.
5. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой сниженную скорость метаболизма.
6. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой метаболический синдром.
7. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой сахарный диабет.
8. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой сердечно-сосудистое заболевание.
9. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой гиперлипидемию.
10. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой нейродегенеративное заболевание.
11. Фармацевтическая композиция по п. 10, отличающаяся тем, что указанное нейродегенеративное заболевание выбрано из группы, состоящей из комплекса СПИД-деменция, болезни Альцгеймера, бокового амиотрофического склероза, адренолейкодистрофии, болезни Александера, болезни Альперса, атаксии-телеангиэктазии, болезни Баттена, коровьей губчатой энцефалопатии (BSE), болезни Канавана, кортикобазальной дегенерации, болезни Крейтцфельдта-Якоба, деменции с тельцами Леви, фатальной семейной бессонницы, лобно-височной лобарной дегенерации, болезни Хантингтона, болезни Кеннеди, болезни Краббе, болезни Лайма, болезни Мачадо-Джозефа, рассеянного склероза, множественной системной атрофии, нейроакантоцитоза, болезни Ниманна-Пика, болезни Паркинсона, болезни Пика, первичного бокового склероза, прогрессирующего надъядерного паралича, болезни Рефсума, болезни Сандгоффа, диффузного миелинокластического склероза, спиноцеребеллярной атаксии, подострой комбинированной дегенерации спинного мозга, сухотки спинного мозга, болезни Тея-Сакса, токсической энцефалопатии, трансмиссивной губчатой энцефалопатии и синдрома шатающегося ежа.
12. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние представляет собой когнитивную функцию или расстройство.
13. Фармацевтическая композиция по п. 12, отличающаяся тем, что указанная когнитивная функция выбрана из группы, состоящей из восприятия, памяти, внимания, понимания речи, образования речи, понимания прочитанного, формирования образов, обучения и мышления.
14. Фармацевтическая композиция по п. 12, отличающаяся тем, что указанное когнитивное расстройство выбрано из группы, состоящей из делирия, деменции, нарушения способности к обучению, синдрома дефицита внимания (СДВ) и синдрома дефицита внимания с гиперактивностью (СДВГ).
15. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанное состояние выбрано из группы, состоящей из расстройства настроения, стресса, и тревожного расстройства.
16. Фармацевтическая композиция по любому из пп. 1-15, отличающаяся тем, что указанный уролитин выбран из группы, состоящей из уролитина А и уролитина B.
17. Фармацевтическая композиция по любому из пп. 1-15, отличающаяся тем, что указанный уролитин представляет собой уролитин А.
18. Фармацевтическая композиция по любому из предшествующих пунктов, дополнительно содержащая фармацевтически приемлемые носители или разбавители.
19. Способ лечения или предотвращения состояния, связанного с дисфункцией митохондрий, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивной функции или расстройства, расстройства настроения, стресса и тревожного расстройства, включающий: введение нуждающемуся в этом субъекту терапевтически эффективного количества уролитина, причем уролитин выбран из группы, состоящей из уролитина A, уролитина B, уролитина C и уролитина D.
20. Способ по п. 19, отличающийся тем, что субъект представляет собой человека.
21. Способ по п. 19 или 20, отличающийся тем, что указанный уролитин выбран из группы, состоящей из уролитина А и уролитина B.
22. Способ по п. 19 или 20, отличающийся тем, что указанный уролитин представляет собой уролитин А.
23. Способ по любому из пп. 19-22, отличающийся тем, что указанный уролитин вводят перорально или парентерально.
24. Способ по любому из пп. 19-23, отличающийся тем, что указанный уролитин вводят по меньшей мере еженедельно или по меньшей мере ежедневно.
25. Применение уролитина для приготовления лекарственного средства для лечения или предотвращения состояния, связанного с дисфункцией митохондрий, выбранного из группы, состоящей из ожирения, сниженной скорости метаболизма, метаболического синдрома, сахарного диабета, сердечно-сосудистого заболевания, гиперлипидемии, нейродегенеративного заболевания, когнитивной функции или расстройства, расстройства настроения, стресса и тревожного расстройства; причем уролитин выбран из группы, состоящей из уролитина A, уролитина B, уролитина C и уролитина D.
26. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой ожирение.
27. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой сниженную скорость метаболизма.
28. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой метаболический синдром.
29. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой сахарный диабет.
30. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой сердечно-сосудистое заболевание.
31. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой гиперлипидемию.
32. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой нейродегенеративное заболевание.
33. Применение по п. 32, отличающееся тем, что указанное нейродегенеративное заболевание выбрано из группы, состоящей из комплекса СПИД-деменция, болезни Альцгеймера, бокового амиотрофического склероза, адренолейкодистрофии, болезни Александера, болезни Альперса, атаксии-телеангиэктазии, болезни Баттена, коровьей губчатой энцефалопатии (BSE), болезни Канавана, кортикобазальной дегенерации, болезни Крейтцфельдта-Якоба, деменции с тельцами Леви, фатальной семейной бессонницы, лобно-височной лобарной дегенерации, болезни Хантингтона, болезни Кеннеди, болезни Краббе, болезни Лайма, болезни Мачадо-Джозефа, рассеянного склероза, множественной системной атрофии, нейроакантоцитоза, болезни Ниманна-Пика, болезни Паркинсона, болезни Пика, первичного бокового склероза, прогрессирующего надъядерного паралича, болезни Рефсума, болезни Сандгоффа, диффузного миелинокластического склероза, спиноцеребеллярной атаксии, подострой комбинированной дегенерации спинного мозга, сухотки спинного мозга, болезни Тея-Сакса, токсической энцефалопатии, трансмиссивной губчатой энцефалопатии и синдрома шатающегося ежа.
34. Применение по п. 25, отличающееся тем, что указанное состояние представляет собой когнитивную функцию или расстройство.
35. Применение по п. 34, отличающееся тем, что указанная когнитивная функция выбрана из группы, состоящей из восприятия, памяти, внимания, понимания речи, образования речи, понимания прочитанного, формирования образов, обучения и мышления.
36. Применение по п. 34, отличающееся тем, что указанное когнитивное расстройство выбрано из группы, состоящей из делирия, деменции, нарушения способности к обучению, синдрома дефицита внимания (СДВ) и синдрома дефицита внимания с гиперактивностью (СДВГ).
37. Применение по п. 25, отличающееся тем, что указанное состояние выбрано из группы, состоящей из расстройства настроения, стресса, и тревожного расстройства.
38. Применение по любому из пп. 25-37, отличающееся тем, что указанный уролитин выбран из группы, состоящей из уролитина А и уролитина B.
39. Применение по любому из пп. 25-37, отличающееся тем, что указанный уролитин представляет собой уролитин А.
| MAR LARROSA et al | |||
| Anti-inflammatory properties of a pomegranate extract and its metabolite urolithin-A in a colitis rat model and the effect of colon inflammation on phenolic metabolism //The Journal of Nutritional Biochemistry, vol.21, issue 8, august 2010, pp.717-725 | |||
| LARROSA M | |||
| Urolithins, ellagic acid-derived metabolites produced by human |
Авторы
Даты
2021-03-25—Публикация
2011-12-23—Подача