Изобретение относится к экспериментальной биологии, фармакологии, медицине и может быть использовано при создании лекарственных препаратов для профилактики интерстициальных пневмоний, в том числе сопровождающихся острым респираторным дистресс-синдромом.
В настоящее время наблюдается неуклонный рост вирусных интерстициальных пневмоний, развивающихся как осложнение острых респираторных вирусных инфекций.
Интерстициальная пневмония - прогрессирующий воспалительный процесс, затрагивающий стенки альвеол и соединительную ткань паренхимы, с возможной вторичной внутри альвеолярной экссудацией и исходом в фиброзную перестройку легочных структур.
Современная медицина располагает весьма обширным арсеналом традиционных и перспективных лекарственных средств медикаментозной терапии пневмонии, однако пандемия COVID-19 выдвинула на первый план разработку эффективных средств профилактики вирусных интерстициальных пневмоний. Известно, что особенностью коронавирусной пневмонии является преобладание в ее патогенезе острого респираторного дистресс-синдрома и раннее развитие фибротических осложнений.
Для лечения и профилактики острого респираторного дистресс-синдрома и пневмонии описано использование производных 4-(4-циано-2-тиоарил)-дигидропиримидинонов, которые являются ингибиторами нейтрофильной эластазы. В патогенезе повреждения ткани легких при интерстициальной пневмонии нейтрофильная эластаза может выступать в качестве одного из повреждающих легочную ткань агентов, однако ее роль не однозначна и нет убедительных данных in vivo, подтверждающих высокую лечебную и профилактическую эффективность ингибиторов нейтрофильной эластазы при пневмониях и остром респираторном дистресс-синдроме [патент на изобретение РФ №2497813 «4-(циано-2-тиоарил)-дигидропиримидиноны и их применение», опубл. 10.11.2013, Бюл. №31].
Для задержки развития легочных осложнений, в частности бронхитов и пневмоний, предложено использовать ингибитор альфа-1 протеиназы (A1PI) путем ингаляции [патент на изобретение РФ №2635482 «Ингибитор альфа-1 протеиназы для задержки начала или прогрессирования легочных обострений», опубл. 13.11.2017, Бюл. №31]. A1PI ингибирует трипсин, химотрипсин и различные формы эластаз, кожную коллагеназу, ренин, урокиназу и протеазы полиморфонуклеарных лимфоцитов. Одна из эндогенных ролей A1PI заключается в регуляции активности эластазы нейтрофилов, которая разрушает чужеродные белки и повреждает нативную ткань, присутствующую в легких. Основным недостатком заявляемого изобретения является ограниченный контингент больных, у которых снижено содержание A1PI, и они подвержены потенциальному риску легочных осложнений, в том числе и пневмонии. В патенте также отсутствуют какие-либо данные подтверждающие эффективность A1PI для профилактики интерстициальных пневмоний, особенно вирусной этиологии.
Для лечения гриппа и пневмонии предложено использовать комбинацию филлирина и филлигенина. Оба соединения являются основными биологически активными веществами плодов Форзиции пониклой (сем. Маслиновые) и обладают противовирусным, антибактериальным, антиоксидантным, противоопухолевым и противовоспалительным эффектом. По сведениям авторов патента, комбинация филлирина и филлигенина обладает более выраженным противовирусным действием на моделях in vivo и in vitro, чем традиционные противовирусные средства, такие как осельтамивир и рибавирин, при этом заявляемая композиция обладает противовоспалительным, жаропонижающим фармакологическим действием, которое потенциально может облегчать симптомы гриппа и пневмонии и может рассматриваться в качестве перспективного лекарственного средства [патент на изобретение РФ №2655616 «Применение композиции филлирина/филлигенина при приготовлении медикамента или продукта медицинского назначения для облегчения и/или назначения для лечения вирусных заболеваний, и медикамент или продукт медицинского назначения для лечения вирусных заболеваний», опубл. 29.05.2018, Бюлл. №16]. Недостатком настоящего изобретения является отсутствие у заявляемой композиции профилактического эффекта при вирусной интерстициальной пневмонии. В то время как в настоящее время арсенал противовоспалительных, жаропонижающих средств для лечения интерстициальных вирусных пневмоний достаточно обширный. Однако несмотря на широкий спектр медикаментозных средств лечения интерстициальной пневмонии, особенно вирусной этиологии, ранняя профилактика этого тяжелого заболевания является приоритетной и обусловливает в последующем его более легкое клиническое течение.
Для лечения и профилактики гриппа и пневмонии, вызываемой вирусом гриппа по-прежнему актуален поиск эффективных ингибиторов нейраминидазы. Так, в качестве эффективных ингибиторов нейраминидазы вируса гриппа предложено использовать фторзамещенные (3r,4r,5s)-5-гуанидино-4-ациламино-3-(пентан-3-илокси)циклогексен-1-карбоновые кислоты и их эфиры [патент на изобретение РФ №2489422, «Фторозамещенные (3R,4R,5S)-5-гуанидино-4-ациламино-3-(пентан-3-илокси) циклогексен-1-карбоновые кислоты, их эфиры и способ применения», опубл 10.08.2013 Бюл. №22]. Указанные соединения могут быть использованы для лечения и профилактики гриппа и пневмонии, вызванной этим вирусом. Недостатком заявляемых соединений является их узкая специфичность относительно вируса гриппа, и профилактическое действие этих соединений не распространяется на другие вирусы, не обладающие нейраминидазной активностью.
Известны иммуномодуляторы, которые также обладают комплексным фармакологическим действием (противовоспалительным, антиоксидантным, иммуностимулирующим, интерферон индуцирующим и т.д.), при лечении острых респираторных инфекций. К таким соединениям можно отнести азоксимера бромид (полиоксидоний) [Булгакова В.А. Иммуномодуляторы для профилактики и лечения острых респираторных инфекций: эффективность Азоксимера бромида // Терапевтический архив. 2014. Т. 86. №12, С. 92-97] и циклоферон [патент на изобретение РФ №2281097 «Лекарственное средство, включающее циклоферон, способ его приготовления и применения», опубл. 10.08.2006 Бюл. №22]. Недостатком полиоксидония является отсутствие данных in vivo, подтверждающих его эффективность для профилактики интерстициальных пневмоний.
Известно применение для лечения вирусной пневмонии комбинации противовирусных средств с разным механизмом действия компонентов, например, комбинации для лечения вирусной гриппозной пневмонии, включающей риамиловир и осельтамивир [патент на изобретение РФ №2703535 «Комбинация противовирусных средств для лечения вирусной гриппозной пневмонии и ее применение», опубл. 21.10.2019, Бюлл. №30]. Недостатком заявляемой противовирусной композиции является то, что она ориентирована только на лечение гриппозной пневмонии, а также отсутствием данных о профилактике интерстициальной пневмонии с помощью заявляемой композиции противовирусных средств, особенно для пневмоний, вызванных вирусами, без выраженной нейраминидазной активности.
Пандемия COVID-19 отличается от всех ранее известных острых респираторных вирусных инфекций прежде всего высокой частотой развития тяжелых форм вирусной интерстициальной пневмонии, средства лечения которой до сих пор находятся в стадии интенсивного поиска, а также массивными фиброзными осложнениями после перенесенной коронавирусной пневмонии. К этому также следует добавить весьма высокую летальность при коронавирусной пневмонии. Учитывая тяжесть этого заболевания, отсутствие специфических медикаментозных средств его лечения наиболее перспективным направлением представляется профилактика вирусной интерстициальной пневмонии с использованием неспецифических медикаментозных средств направленных на разные звенья патогенеза, в частности на острый респираторный дистресс-синдром, характерный в том числе для пневмонии вызванной вирусом COVID-19. Сепсис и острый респираторный дистресс-синдром (ОРДС) являются общими элементами патогенеза тяжелых форм COVID-19.
Описан экспериментальный подход в определении перспективности применения медикаментозных средств, в частности, гексапептида формулы H-Tyr-D-Ala-Gly-Phe-Leu-Arg-OH (I) или его фармацевтически приемлемой соли, для профилактики пневмонии [патент на изобретение РФ №2728938 «Применение даларгина для производства средств лечения профилактики пневмонии», опубл. 03.08.2020, Бюл №22], в том числе, вызванной COVID-19 [патент на изобретение РФ №2728939 «Применение даларгина для производства средств лечения коронавирусной инфекции Covid-19», опубл. 03.08.2020 Бюл. №22]. Учитывая сложность моделирования данного заболевания in vivo, предложено использовать модель пневмонии, индуцированной внутри трахеальным введением липополисахарида (ЛПС-индуцированная пневмония), которая также как и коронавирусная пневмония развивается в виде интерстициальной пневмонии с преобладанием острого респираторного дистресс-синдрома. Подобная экспериментальная модель описана и в других источниках с разными вариантами технического исполнения и критериями оценки тяжести патологического процесса, преимущественно морфологическими и иммунологическими [Рыбакова А.В., Макарова М.Н., Соколов В.Д., Крышень К.Л, Ходько С.В., Макаров В.Г Методические указания по экспериментальному Моделированию ЛПС индуцированной острой пневмонии у крыс // Международный вестник ветеринарии, 2013. №4, С. 106-116; Кательникова А.Е. и соавт. Экспериментальные модели острого бронхита на животных // Лабораторные животные для научных исследований, 2019, №1, С.127-150; Голубев A.M., Кузовлев А.Н., Сундуков Д.В., Голубев М.А. Морфологическая характеристика легких при ингаляции липополисахарида и перфторана // Общая реаниматология, 2015, Том 11, №1, С. 7-13].
Наиболее близким к заявляемому техническому решению (прототипом) является применение неспецифического лекарственного средства, содержащего гексапептид формулы H-Tyr-D-Ala-Gly-Phe-Leu-Arg-OH (I) или его фармацевтически приемлемую соль, для профилактики интерстициальной пневмонии [патент на изобретение РФ №2728938 «Применение даларгина для производства средств лечения профилактики пневмонии», опубл. 03.08.2020, Бюл. №22]. В заявляемом лекарственном средстве гексапептид формулы (I) содержится в количестве 0,01 - 1,0 масс. %, остальное фармацевтические наполнители и вспомогательные вещества. Примеры вспомогательных веществ: очищенная вода, вода для инъекций, пропелленты, растворители, антимикробные консерванты, поверхностно-активные вещества, стабилизирующие агенты, эмульгаторы, буферные компоненты для поддержания значения рН на уровне 3,0-8,5. Согласно прототипу гексапептид формулы (I) вводят интраназально, внутримышечно или ингаляционно. Заявленное лекарственное средство применяют в количестве от 0,1 до 50 мг в одной дозе. К не эксклюзивным примерам возбудителей пневмонии, при которой гексапептид формулы (I) профилактирует пневмонию, являются вирусы гриппа Alphainfluenzavirus (серотипы H1N1, H1N2,H2N2, H3N2, H5N1, H7N9) и Betainfluenzavirus; коронавирусы SARS-CoV, SARS-CoV-2, MERS; респираторно-синцитиальный вирус человека Human orthopneumovirus; бактерии Streptococcus pneumoniae, Haemophilus influenzae, Legionella pneumophila, Escherichia coli; грибы Aspergillus, Mucor, Candida, Blastomyces, Coccidioides, Histoplasma, Pneumocystis, C. albicans, P. Carinii. Заявленное средство тестировали на модели пневмонии у мышей, индуцированной внутри трахеальным введением липополисахарида. После введения липополисахарида и индуцирования пневмонии гексапептид формулы (I) вводился мышам опытных групп интраназально, внутримышечно и ингаляционно в дозе 10 мкг/кг в течение 5 дней. Через 120 часов после индукции пневмонии у животных извлекали легкие, высушивали до постоянного веса и определяли соотношение сухого веса к влажному весу легкого (критерий оценки - отек легкого), профилактическое введение гексапептида (I) достоверно предупредило отек легкого, один из симптомов пневмонии, в экспериментальной модели пневмонии. Недостатком средства по прототипу является его недостаточная эффективность.
Задачей, на решение которой направлено заявляемое изобретение, является повышение эффективности профилактики интерстициальной пневмонии.
Техническим результатом, достигаемым при осуществлении изобретения, является снижение степени выраженности патологических морфологических изменений в легочной ткани, характерных для интерстициальной пневмонии.
Решение поставленной задачи достигается тем, что в качестве профилактического средства используют окисленный декстран с м.М. от 10 до 50 кДа в виде водного раствора с концентрацией 0,5 - 10,0 масс. %.
Раскрытие сущности изобретения
Средство для профилактики интерстициальной пневмонии включает окисленный декстран с м.М. от 10 до 50 кДа в виде водного раствора с концентрацией 0,5 - 10,0 масс. %.
Окисленный декстран представляет собой декстран, содержащий карбонильные группы. Он может быть получен известными способами на основе химического или радиационного окисления декстрана. В частности, окисленный декстран может быть получен химическим путем, например, путем окисления декстрана ("Fluka", Швейцария) периодатом натрия и осаждения окисленного декстрана этанолом [патент на изобретение РФ №2125451 «Способ получения конъюгата изониазид-декстран», дата публикации 27.01.1999].
Окисленный декстран может быть также получен путем окисления декстрана перманганатом калия в кислой среде при нагревании (80-100°С), после чего примеси удаляют путем отделения жидкости от осадка, выпавшего на стадии окисления декстрана и содержащего двуокись марганца; окисленный декстран осаждают из надосадочной жидкости этанолом [Евразийский патент на изобретение №011718 «Способ получения диальдегиддекстрана», дата публикации 28.04.2009].
В качестве исходного продукта для получения заявленного средства используют декстран с молекулярной массой 10-50 кДа в виде водного или водно-солевого раствора концентрации 1-10%.
В качестве фармацевтически приемлемого растворителя может быть использована вода для инъекций.
Для сравнительной оценки профилактического действия заявляемого средства и гексапептида в виде фармакопейного препарата «Даларгин», описанного в прототипе, проводили гистологическое исследование легких мышей линии ACR при профилактике ЛПС-индуцированной интерстициальной пневмонии ингаляционным способом. Исследование проведено на 30 мышах-самцах линии ACR, которым интраназально вводили 20 мкл раствора (концентрация 20 мг/мл) липополисахарида (ЛПС) Escherichia coli с последующим ингаляционным введением в опытных группах окисленного декстрана или гексапептида формулы (I) в течение 5 минут с последующим выведением из эксперимента через 24 часа. Все животные в исследовании были разделены на 5 групп: 1 группа - контрольная - мыши-самцы линии ACR с интраназальным введением 20 мкл раствора ЛПС (2 мг/мл) и последующим выведением из эксперимента через 24 часа; 2 группа - мыши-самцы линии ACR с интраназальным введением 20 мкл раствора ЛПС (2 мг/мл) с последующим ингаляционным введением раствора гексапептида формулы (I) с концентрацией 1 мг/мл (фармакопейный препарат «Даларгин») в течение 5 мин и выведением из эксперимента через 24 часа; 3 группа - мыши-самцы линии ACR с интраназальным введением 20 мкл раствора ЛПС (2 мг/мл) с последующим ингаляционным введением 2% раствора окисленного декстрана с м.М. 40 кДа в течение 5 мин и выведением из эксперимента через 24 часа; 4 группа - мыши-самцы линии ACR с интраназальным введением 20 мкл раствора ЛПС (2 мг/мл) с последующим ингаляционным введением 0,5% раствора окисленного декстрана с м.М. 50 кДа в течение 5 мин и выведением из эксперимента через 24 часа; 5 группа - мыши-самцы линии ACR с интраназальным введением 20 мкл раствора ЛПС (2 мг/мл) с последующим ингаляционным введением 10% раствора окисленного декстрана с м.М. 10 кДа в течение 5 мин и выведением из эксперимента через 24 часа. Материалом для гистологического исследования служили образцы легочной ткани (правая нижняя доля), которые подвергали стандартной гистологической обработке с последующим окрашиванием гематоксилином и эозином для визуализации методом прямой световой микроскопии. Гистологические исследования проводили с помощью микроскопа AxioImager А1 с фотокамерой AxioCam MRc (Carl Zeiss, Германия). При этом в срезах образцов легочной ткани мышей оценивали следующие патоморфологические изменения: степень выраженности интерстициального и альвеолярного отека, гемоциркуляторных нарушений, клеточной воспалительной инфильтрации, деструктивных изменений (участков эмфиземы, ателектазов, дистрофии и некроза эпителия бронхов). Морфологические критерии оценки профилактического действия заявленного средства на модели ЛПС-индуцированной пневмонии расширены в сравнении с прототипом, для более полного учета развивающегося на этой модели острого респираторного дистресс-синдрома, который, является важным патофизиологическим звеном тяжелой интерстициальной пневмонии, в том числе при COVID-19.
Результаты сравнительного исследования профилактического действия заявленного средства и средства по прототипу представлены в Таблице 1.
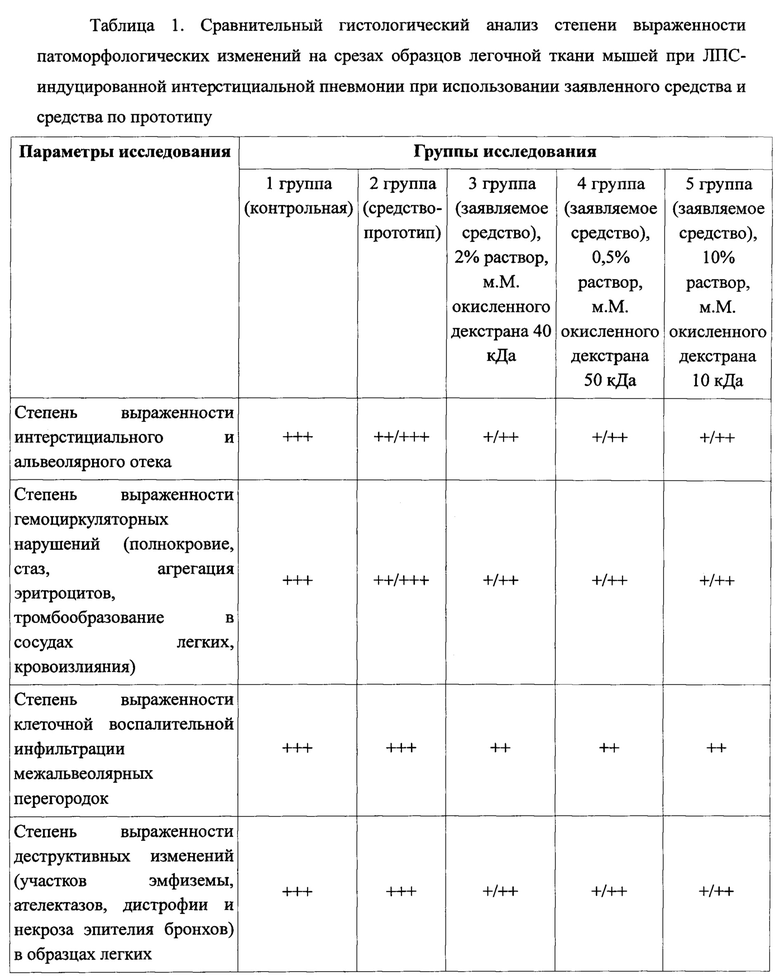
Примечание: +++- резко выраженные изменения, ++- умеренные изменения, + слабые изменения. Когда стоит смешанный вариант, например, "+/++", то это значит, что изменения носят в зависимости от полей зрения на препарате под микроскопом от слабых изменений до умеренных.
Как видно из представленных результатов, заявленное средство по морфологическим критериям оценки обладает в сравнении со средством-прототипом, более выраженным профилактическим действием на модели ЛПС-индуцированной пневмонии.
Выбранный в заявленном средстве диапазон концентраций окисленного декстрана подобран экспериментально. При концентрациях раствора окисленного декстрана менее 0,5 масс. % профилактическое действие растворов окисленного декстрана в отношении интерстициальной пневмонии снижается, а использование растворов окисленного декстрана свыше 10 масс. % нецелесообразно ввиду высокой вязкости, снижающей образование стабильных аэрозолей при ингаляции стандартными небулайзерами.
Кроме того, использованный диапазон молекулярных масс окисленных декстранов, обусловлен доступностью и стоимостью первичного сырья (декстранов). Использование декстранов с молекулярными массами менее 10 кДа и свыше 50 кДа ограничено доступностью их сырьевой базы и эти декстраны имеют высокую стоимость, что, в конечном счете, ведет к существенному удорожанию конечного продукта для широкого медицинского использования в профилактике вирусных интерстициальных пневмоний.
Осуществление изобретения
Заявленное техническое решение иллюстрируется следующими примерами конкретного выполнения.
Пример 1. Приготовление заявленного средства для ингаляций.
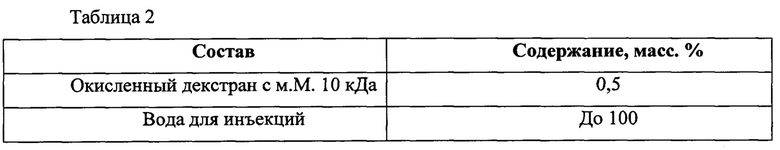
Для приготовления заявленного средства для ингаляций, окисленный декстран с м.М. 10 кДа растворяют в очищенной воде в соотношениях, указанных в таблице 2 и полученный раствор стерилизуют фильтрацией через микропористые фильтры с диаметром пор 0,2 мкм, затем разливают в стерильные флаконы или ампулы в атмосфере азота. Для профилактики пневмонии полученный раствор вводится субъекту, нуждающемуся в этом, ингаляционно в виде аэрозоля с помощью небулайзера.
Пример 2. Приготовление заявленного средства для ингаляций.
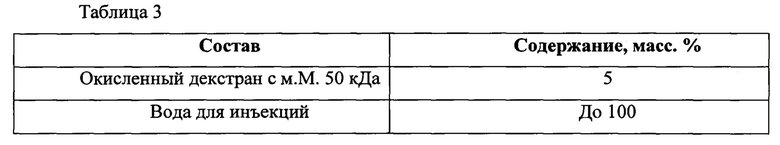
Для приготовления заявленного средства для ингаляций, окисленный декстран с м.М. 50 кДа растворяют в очищенной воде в соотношениях, указанных в таблице 3 и полученный раствор стерилизуют фильтрацией через микропористые фильтры с диаметром пор 0,2 мкм, затем разливают в стерильные флаконы или ампулы в атмосфере азота. Для профилактики пневмонии полученный раствор вводится субъекту, нуждающемуся в этом, ингаляционно в виде аэрозоля с помощью небулайзера.
Пример 3
Приготовление заявленного средства для ингаляций.
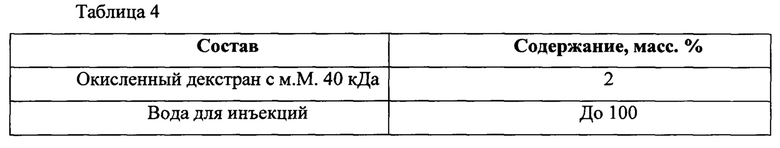
Для приготовления заявленного средства для ингаляций, окисленный декстран с м.М. 40 кДа растворяют в очищенной воде в соотношениях, указанных в таблице 4 и полученный раствор стерилизуют фильтрацией через микропористые фильтры с диаметром пор 0,2 мкм, затем разливают в стерильные флаконы или ампулы в атмосфере азота. Для профилактики пневмонии полученный раствор вводится субъекту, нуждающемуся в этом, ингаляционно в виде аэрозоля с помощью небулайзера.
Пример 4
Приготовление заявленного средства для ингаляций.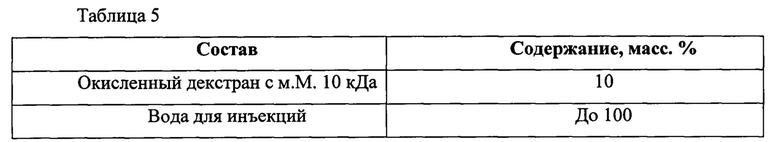
Для приготовления заявленного средства для ингаляций, окисленный декстран с м.М. 10 кДа растворяют в очищенной воде в соотношениях, указанных в таблице 5 и полученный раствор стерилизуют фильтрацией через микропористые фильтры с диаметром пор 0,2 мкм, затем разливают в стерильные флаконы или ампулы в атмосфере азота. Для профилактики пневмонии полученный раствор вводится субъекту, нуждающемуся в этом, ингаляционно в виде аэрозоля с помощью небулайзера.
Пример 5
Приготовление заявленного средства для ингаляций.

Для приготовления заявленного средства для ингаляций, окисленный декстран с м.М. 30 кДа растворяют в очищенной воде в соотношениях, указанных в таблице 6 и полученный раствор стерилизуют фильтрацией через микропористые фильтры с диаметром пор 0,2 мкм, затем разливают в стерильные флаконы или ампулы в атмосфере азота. Для профилактики пневмонии полученный раствор вводится субъекту, нуждающемуся в этом, ингаляционно в виде аэрозоля с помощью небулайзера.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство и способ профилактики интерстициальной пневмонии инфекционной этиологии | 2021 |
|
RU2784177C1 |
| Ингаляционный гексапептид для лечения респираторных заболеваний, связанных с интерлейкином-6 | 2020 |
|
RU2737799C1 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРОГО РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА ДАЛАРГИНОМ И ЛЕГОЧНЫМ СУРФАКТАНТОМ | 2020 |
|
RU2728821C1 |
| Средство для снижения риска и облегчения симптомов заражения бета-коронавирусной инфекцией | 2021 |
|
RU2747890C1 |
| Способ лечения болезней легких ингаляционным введением мезенхимальных стромальных клеток и гексапептида | 2022 |
|
RU2770364C1 |
| ПРИМЕНЕНИЕ ИНГИБИТОРА АЛЬФА1-ПРОТЕИНАЗЫ (АЛЬФА1-АНТИТРИПСИНА) ДЛЯ ПРОФИЛАКТИКИ И/ИЛИ ЛЕЧЕНИЯ ОСТРОГО РЕСПИРАТОРНОГО ДИСТРЕСС СИНДРОМА И СПОСОБ ПРОФИЛАКТИКИ И/ИЛИ ЛЕЧЕНИЯ ОСТРОГО РЕСПИРАТОРНОГО ДИСТРЕСС СИНДРОМА С ИСПОЛЬЗОВАНИЕМ АЛЬФА1-АНТИТРИПСИНА | 2020 |
|
RU2757875C1 |
| СТАБИЛЬНАЯ ВОДНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГАЛЯЦИЙ, СОДЕРЖАЩАЯ ГЕКСАПЕПТИД | 2020 |
|
RU2739573C1 |
| ПРИМЕНЕНИЕ ДАЛАРГИНА ДЛЯ ПРОИЗВОДСТВА СРЕДСТВ ЛЕЧЕНИЯ КОРОНАВИРУСНОЙ ИНФЕКЦИИ COVID-19 | 2020 |
|
RU2728939C1 |
| Применение энисамия йодида для профилактики и/или лечения острого респираторного дистресс-синдрома (ОРДС) | 2022 |
|
RU2799328C1 |
| Биомедицинский клеточный продукт на основе мезенхимальных стромальных клеток млекопитающих и гексапептида | 2022 |
|
RU2781968C1 |
Настоящее изобретение относится к области медицины, а именно к применению средства для профилактики интерстициальной пневмонии, включающего окисленный декстран с м.М. от 10 до 50 кДа в виде водного раствора с концентрацией 0,5-10,0 масс. %. Настоящее изобретение обеспечивает снижение степени выраженности патологических морфологических изменений в легочной ткани, характерных для интерстициальной пневмонии. 5 пр., 6 табл.
Применение средства для профилактики интерстициальной пневмонии, включающего окисленный декстран с м.М. от 10 до 50 кДа в виде водного раствора с концентрацией 0,5-10,0 масс. %.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ГРИППА | 2014 |
|
RU2572332C1 |
| СРЕДСТВО ПРОФИЛАКТИКИ ПТИЧЬЕГО ГРИППА У МЛЕКОПИТАЮЩИХ | 2010 |
|
RU2437664C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА ДЛЯ ИЗГОТОВЛЕНИЯ КОСМЕТИЧЕСКИХ СРЕДСТВ | 2012 |
|
RU2500385C1 |
| Железобетонный корпус высокого давления | 1985 |
|
SU1321153A1 |
| EP 3636269 A1, 15.04.2020 | |||
| Potapova O.V | |||
| et al., Preventive Effects of Oxidized Dextran on Functional Activity of Pulmonary Macrophages in Mice Infected with Influenza A Virus / Bulletin of Experimental Biology and Medicine, Vol.165, No.1, | |||
Авторы
Даты
2021-05-06—Публикация
2020-11-24—Подача