Изобретение относится к биологии и экспериментальной медицине, а именно к экспериментальной кардиологии, патофизилогии, патанатомии и может быть использовано для изучения пато-, и морфогенеза ранних стадий инфаркта миокарда, а также при разработке новых методов диагностики и лечения острых коронарных событий.
Сердечно-сосудистые заболевания (ССЗ) занимают лидирующую позицию в структуре смертности населения Российской Федерации, составив в 2019 году, согласно данным федеральной службы государственной статистики, 46,4% от всех причин смерти. Несмотря на достигнутые успехи в борьбе со смертностью от инфаркта миокарда, он сохраняет достаточно устойчивые позиции в структуре смертности от сердечно-сосудистых заболеваний, составляя от 11% до 20% в различных субъектах Российской Федерации [1, 2, 3, 6]. С другой стороны в исходе инфаркта миокарда возможно развитие хронической ишемической болезни сердца, сердечной недостаточности, нарушений ритма, вклад которых в заболеваемость, стойкую утрату трудоспособности и смертность является определяющим в снижении экономически активного возраста и продолжительности жизни населения Российской Федерации и ряда стран мирового сообщества [4, 5, 14, 15]. Экспериментальное моделирование острого инфаркта миокарда с использованием лабораторных животных и в частности крыс позволяет изучать морфологию и патогенез с целью разработки новых методов диагностики и терапии. Созданные in vivo известные модели инфаркта миокарда у крыс отличаются высокой ранней смертности, необходимостью использования животных молодого возраста с целью возможного повышения их выживаемости, недостаточным уровнем успешности формирования сопоставимого с ожидаемым результатом очагов некроза в миокарде миокарда и необходимостью специализированного дорогостоящего оборудования [7].
Известен способ моделирования очаговых повреждений миокарда (2. Богородская С.Л., Голубев С.С., Микашова М.Б., Бадуев Б.К. Авт. св. №2286606, G09B 23/28 (2006.01). Для этого предварительно лабораторному животному внутрибрюшинно вводят 5%-ный раствор кетамина в дозе 0,065 мг на 100 г веса, а затем 0,1%-ный раствор адреналина гидрохлорида в дозе 0,5 мг на 100 г веса животного. Способ обеспечивает получение модели множественных очаговых повреждений миокарда.
Недостатком данного метода является возникновение других органных побочных эффектов, связанных с действием адреналина. Развитие периферической гипоперфузии, формирует повреждение органов и тканей. Кроме этого, действие адреналина приводит к тяжелым метаболическим нарушениям, в частности гипергликемии, нарушению процессов окислительного фосфорилирования, что вызывает повреждения миокарда не только циркулярного генеза.
Известен способ моделирования ишемического повреждения миокарда у крыс (З. Епинетов М.А. Авт. св. №2243595, G09B 23/28 (2006.01). Для этого через 2-3 минуты после подкожного введения крысе 0,1 миллилитра 0,1% раствора адреналина гидрохлорида животное "поднимают" на барокамерную высоту 11000 метров и ведут непрерывное мониторное наблюдение за электрокардиограммой в условиях высотной гипоксии, появление в течение 2-3 минут наблюдения горизонтального снижения сегмента ST на 1 миллиметр и ниже от исходной величины свидетельствует об ишемическом повреждении миокарда.
Недостатком данного метода является использование дорогостоящей аппаратуры, сложность проведения методики. Кроме этого, основной повреждающий механизм - гипоксическая гипоксия, что вызывает повреждение других органов и тканей, не связанное с инфарктом миокарда.
Известен способ моделирования инфаркта миокарда (2. Большов П.С., Чижмак А.О., Мульский С.В., Куликова С.Г., статья «Разработка модели инфаркта миокарда в хроническом эксперименте у крыс», Международный журнал прикладных и фундаментальных исследований. - 2015. - №5-1. - С. 52-53). Эксперимент проводился с использованием золетил-ксилазинового наркоза. Операция проходила с помощью искусственной вентиляции легких через трахеостому с использованием аппарата «ВИТА-1» (СССР). Доступ к сердцу осуществлялся за счет межреберной торакотомии. Торакотомия выполнялась в 6 межреберье. При ревизии плевральной полости вскрывался перикард, с помощью надавливания на грудную клетку сердце пролабировало в рану. Под левую венечную артерию проводилась игла атравматическая (шелк 7/0), произведена перевязка артерии. Выполнялся прокол грудной клетки в VIII межреберье противоположной стороны, установлен плевральный дренаж. В дальнейшем проводилось послойное ушивание торакотомной раны непрерывными швами. С помощью шприца через дренаж аспирирован воздух из плевральной полости, после чего плевральный дренаж удалялся. П-образным швом ушита трахея. После удаления дыхательной трубки шов затянут, проведено послойное ушивание раны непрерывным швом.
Недостатком данного является - использование дорогостоящей аппаратуры, сложность проведения, большая стоимость создания модели. Высокая смертность при использовании данной модели. Кроме этого, методика сопряжена с формированием двухстороннего пневмоторакса, который ухудшает не только вентиляцию, но и перфузию, что является дополнительным повреждающим фактором, который влияет на чистоту модели острого инфаркта миокарда
Известен способ моделирования инфаркта миокарда (A new technique of coronary artery ligation: Experimental myocardial infarction in rats in vivo with reduced mortality/ Jian Ye, Luojia Yang, Rajat Sethi, John Copps, Bram Ramjiawan, Randy Summers, Roxanne Deslauriers// Molecular and Cellular Biochemistry, - 1997. - Vol. 176. - P. 227-233). В этом способе животное наркотизировали внутрибрюшинным введением 1% раствора тиопентала натрия из расчета 40 мг/кг. В асептических условиях тупо вскрывали грудную клетку слева, с помощью ранорасширителей раздвигали 5-6 ребра, выводили сердце в рану и осуществляли перевязку левой коронарной артерии на 1 мм ниже края ушка левого предсердия; игла проводилась в толще миокарда перпендикулярно к оси сердца. Затем сердце вправляли в грудную полость, на мышцы и кожу накладывали швы. Общая продолжительность операции занимала 15-20 минут, грудная клетка оставалась открытой 45-60 секунд, что дало возможность использовать неингаляционный наркоз.
Недостатки данного метода схожим предыдущей методикой. Следует отметить, что использование тиопентал натрия способствует дополнительному органному повреждению в результате гипотонии, связанной с его эффектами. Кроме этого, происходит угнетение дыхания, что формирует гипоксическую гипоксию и дополнительное, не связанное с инфарктом повреждение сердца и других органов.
Наиболее близким к заявленному является метод (Ранцев М.А., Сарапульцев П.А., Дмитриев А.Н, Авт. св. №2407062, G09B 23/28 2006.01), где для этого рассекают кожу грудной клетки и обнажают мышцы, разводят грудные мышцы с обнажением реберных дуг и межреберных мышц. Производят рассечение межреберных мышц в 4-5 межреберье на протяжении 1 см. Визуализируют сердце; выполняют коагуляцию веточек левой венечной артерии в ее средней или нижней трети. Коагуляцию выполняют инструментом Г-образной формы с прижигающей поверхностью размерами 2,5×3,0 мм, который разогревают на спиртовой горелке. Ушивают торакотомную рану непрерывным швом атравматичной иглой, шприцем с иглой ликвидируют пневмоторакс, зашивают кожу. Способ обеспечивает повышение вероятности получения положительного результата при минимальных трудозатратах при минимизации времени операции и большом времени самого эксперимента.
При анализе перечисленных известных способов создания экспериментальной модели инфаркта миокарда следует отметить, что к их недостаткам в целом относятся:
- необходимость использования редкого и дорогостоящего оборудования;
- длительная временная продолжительность опыта, в условиях общей анестезии, что увеличивает частоты побочных реакций и осложнений;
- сложность технического выполнения с необходимостью проведения объемного оперативного вмешательства, с высокой частотой интра - и послеоперационных осложнений;
- большинстве случаев необходимость применения адреномимиметиков, наложения искусственных дыхательных путей с продолжительным временем наркоза, что влияет на системный сосудистый тонус и перфузию тканей с последующими изменениями на тканевом и клеточном уровнях, искажающих полученные результаты при работе с изучаемыми медикаментозными препаратами;
- высокая вероятность развития осложнений, в частности пневмоторакса, что приводит к высокой смертности лабораторных животных;
- в большинстве моделей используются молодые животные, в то время как в реальной практике острые коронарные события с развитием инфаркта миокарда встречаются в различных возрастных группах с высокой долей лиц пожилого и старческого возраста.
В отличие от указанных методов моделирования инфаркта миокарда у крыс в заявляемом нами способе используется инъекционное введение препарата этоксисклерол путем пункции миокарда иглой с силиконовым покрытием 30G в переднюю стенку сердца, тем самым вызывая очаговый некроз ткани и развитие острого инфаркта миокарда.
Преимуществами предложенного метода являются:
- относительно низкая смертность животных (9%);
- малая инвазивность вмешательства;
- простота и короткое время проведения операции;
- отсутствие системного действия препарата и продолжительного наркоза;
- высокая безопасность метода проявлялась в том факте, что в экспериментальных группах были животные различного возраста, в том числе в возрасте 17-18 месяцев, что сопоставимо с продолжительностью жизни человека и составляет 75 лет и старше, которые успешно перенесли эксперимент моделирования острого инфаркта и не имели значимых операционных осложнений;
- применение препаратов без значимых системных реакций на другие органы и ткани.
Критерии «новизна» и «изобретательский уровень» предлагаемого способа заключаются в техническом решении условий моделирования острого инфаркта миокарда на взрослых лабораторных животных массой 280-500 грамм. Животное помещалось в индукционную камеру, проводилась ингаляция паров Севорана, Abbot (жидкость для ингаляций, состав: севофлюран 100%) до утраты двигательной активности и реакции на болевой раздражитель в виде укола лапы иглой. Животное фиксировалось на манипуляционном стенде. В асептических условиях проводился разрез кожи грудной клетки размером около 2 см, обнажались мышцы, разводились грудные мышцы с обнажением реберных дуг и межреберных мышц. Выполнялась пальпация верхушечного толчка сердца, далее иглой 30G SF Medical Products GMBH, Германия (тройное покрытие силиконом позволяет игле входит в ткань не разрезая, а раздвигая волокна), в межреберном промежутке выполнялся прокол. После выполнения аспирационная пробы, иглу подтягивают на 0,5 см, в толщу миокарда вводился этоксисклорол 1,5% - 0,25 мл. Кожа ушивалась узловыми швами, шов обрабатывался хлоргексидином. Время проведение опыта около 3-5 мин. Через 10 мин у животного восстанавливались сознание и двигательная активность. Через 24 часа, забор крови из яремной вены, эвтаназия на фоне седации севофлюраном, путем декапитации гильотинированием, сердце извлекали и ножницами и помещали в забуференный 10% раствор формалина.
Пример использования изобретения.
Проведено исследование влияния различных медикаментов (кетамина, десмедотимидина) для оценки их кардиопротективных свойств и профилактики повреждения ЦНС. В эксперименте использовались 25 взрослых особей. Возраст животных в опытной группе составлял 17-18 месяцев, в контрольной группе 5-6 месяцев и 17-18 месяцев. Кроме этого, в качестве контроля наличия повреждения были использованы 10 лабораторных животных сравнимого возраста, которым была произведена эвтаназия такой же методикой, как и в экспериментальных группах. Всем животным был создан экспериментальное острое повреждение миокарда по описанной методике. При исследовании макропрепаратов сердца отмечалось наличие участков некроза. Также проведено микроскопическое исследование миокарда. Для оценки использовалась методика окраса по ГОФП. Название метода окраски по ГОФП произошло от первых букв используемых красителей: гематоксилин - основной фуксин - пикриновая кислота. Под названием «фуксиноррагический метод» он был описан Lie и соавторами в 1971 году. В том же году Bouchardy В. и Majno G. предложили диагностировать ранние повреждения по так называемой «волнистости миокарда». В последующем работами Hoch - Ligeti С., Lan C.W. и Pesonen Е. Была доказана применимость обоих методов для обнаружения повреждений миокарда в секционном материале. В результате по всех экспериментальных группах отмечается наличие повреждение миокарда на макро и микроскопическом уровне (фиг. 1 и фиг. 2).
Литературные ссылки:
1. Бунова, С.С., Динамика заболеваемости инфарктом миокарда в регионах Российской Федерации за 11-летний период (2002-2012 гг.) / С.С. Бунова, Е.В. Усачева, О.В. Замахина // Социальные аспекты здоровья населения. - 2014. - 40 (6). - С. 3.
2. Возжаев, А.В. Вторичная профилактика сердечно-сосудистых заболеваний у пациентов, перенесших инфаркт миокарда (фармакоэпидемиологическое исследование) / А.В. Возжаев // автореф. дис. … канд. биол. наук - Старая Купавна., 2009. - 23 с
3. Сайгитов, Р.Т. Сердечно-сосудистые заболевания в контексте социальноэкономических приоритетов долгосрочного развития России / Р.Т. Сайгитов, А.А. Чулок // Вестник Российской академии медицинских наук. - 2015. - 70 (3). - С. 286-299.
4. Чазова, Л.В. Основные эпидемиологические методы изучения сердечно-сосудистых заболеваний: (Методические материалы) / Л.В. Чазова, А.М Калинина // М. - 1993. - 73.
5. Гафаров, В.В. Программа Всемирной Организации Здравоохранения «Регистр острого инфаркта миокарда» как аудит оценки здоровья населения / В.В. Гафаров, А.В. Гафарова // Вестник НГУЭУ. - 2015. - (4). - С. 200-222.
6. Гарганеева, А.А. Программа ВОЗ "Регистр острого инфаркта миокарда" возможности и перспективы в изучении и прогнозировании исходов социально значимых патологий на популяционном уровне / А.А. Гарганеева, С.А. Округин, К.Н. Борель // СМЖ. - 2015. - 2. - С. 125-130.
7. Андреева, Н.С. Системы оценки достоверности научных доказательств и убедительности рекомендаций: сравнительная характеристика и перспективы унификации / Н.С. Андреева, О.Ю. Реброва, Н.А. Зорини др. // Медицинские Технологии Оценка И Выбор. - 2012. - 4 (10). - С. 10-24.
8. Сичинава, Д.П. Характеристика пациентов, перенесших острый инфаркт миокарда, включенных в регистр «Профиль-ИМ»/ Д.П. Сичинава, Е.П. Калайджян, С.Ю. Марцевич, Н.П. Кутншенко // Кардиосоматика. - 2017. - №1. - С. 5-88
9. Богородская С.Л., Голубев С.С., Микашова М.Б., Бадуев Б.К. Авт. св. №2286606, G09B 23/28 (2006.01)
10. Епинетов М.А. Авт. св. №2243595, G09B 23/28 (2006.01)
11. Большое П.С., Чижмак А.О., Мульский С.В., Куликова С.Г., статья «Разработка модели инфаркта миокарда в хроническом эксперименте у крыс», Международный журнал прикладных и фундаментальных исследований. - 2015. - №5-1. - С. 52-53
12. Ранцев М.А., Сарапульцев П.А., Дмитриев А.Н, Авт. св. №2407062, G09B 23/28 2006.01
13. A new technique of coronary artery ligation: Experimental myocardial infarction in rats in vivo with reduced mortality/ Jian Ye, Luojia Yang, Raj at Sethi, John Copps, Bram Ramjiawan, Randy Summers, Roxanne Deslauriers// Molecular and Cellular Biochemistry, - 1997. - Vol. 176. - P. 227-233
14. Benjamin, E.J. Heart disease and stroke statistics 2017 update: a report from the American Heart Association / E.J. Benjamin, M.J. Blaha, S. Chiuve et al. // Circulation. - 2017. -135 (10). - P. 146-603.
15. Ryan, T.J. ACC/AHA guidelines for the management of patients with acute myocardial infarction: A report of the American College of cardiology/American Heart Association Task Force on Practice Guidelines (Committee on Management of Acute Myocardial Infarction) / T.J. Ryan, J.L. Anderson, E.M. Antman et al. // J Am Coll Cardiol. - 1996. - 28 (5). - P. 1328- 428
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
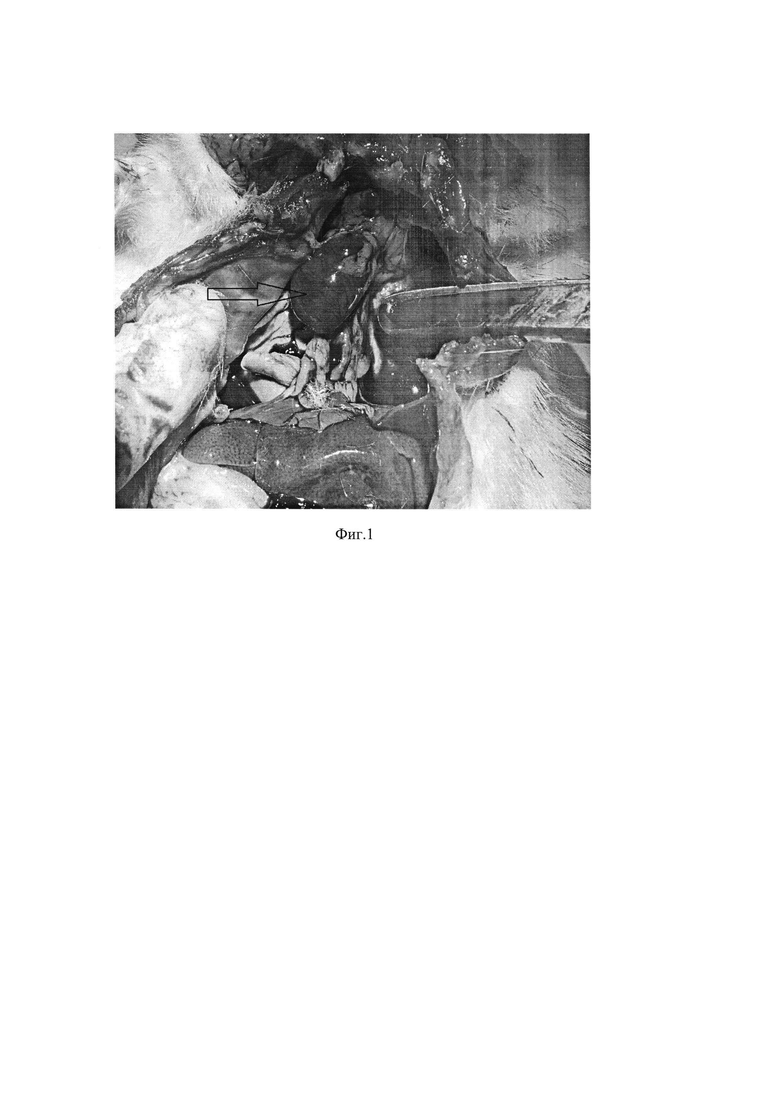
Фиг. 1. Зона очагового повреждения миокарда
На фиг. 1 представлен макропрепарат. На нем вскрытая грудная клетка лабораторного животного (белая крыса породы Wistar) после декапитации, в центре клетки выведено сердце. На передне - боковой стенке отмечается очаг ишемического повреждения миокарда диаметром 1,5*1 см (отмечено стрелкой), темно - бордового цвета, неправильной формы с нечеткими контурами.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 2. Микроскопическая картина острого повреждения миокарда. Окраска: ГОФП-метод (окраска гематоксилин-основной фуксин-пикриновая кислота). Увеличение х250.
На фиг. 2 визуализируются многочисленные сливающиеся очаги слабой и умеренной фуксинофилии цитоплазмы кардиомиоцитов в виде сплошных участков и мелких их фрагментов, окрашенных в фиолетово - красный цвет на бледно-зеленом фоне интактного миокарда.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, обладающее кардиопротекторной активностью | 2019 |
|
RU2791641C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ИНФАРКТА МИОКАРДА У КРЫС | 2007 |
|
RU2407062C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ОЧАГОВЫХ НЕКРОЗОВ МИОКАРДА | 1994 |
|
RU2095854C1 |
| СПОСОБ ВОСПРОИЗВЕДЕНИЯ КАРДИОГЕННОГО ШОКА НА МЕЛКИХ ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2003 |
|
RU2239874C1 |
| СПОСОБ ЭКСПЕРИМЕНТАЛЬНОЙ ТЕРАПИИ ИНФАРКТА МИОКАРДА | 2005 |
|
RU2288738C2 |
| Применение фосфолипидной эмульсии, содержащей эффективное количество дигидрокверцетина, для лечения синдрома ишемии-реперфузии у пациентов с ишемическими поражениями органов и конечностей | 2021 |
|
RU2766681C1 |
| Способ моделирования инфаркта миокарда | 1990 |
|
SU1793456A1 |
| СПОСОБ ЛЕЧЕНИЯ ИШЕМИЧЕСКОЙ БОЛЕЗНИ СЕРДЦА С ДИСТАЛЬНЫМ ИЛИ ДИФФУЗНЫМ ПОРАЖЕНИЕМ КОРОНАРНЫХ АРТЕРИЙ | 2011 |
|
RU2481839C2 |
| Средство, ослабляющее постинфарктное ремоделирование миокарда | 2020 |
|
RU2740895C1 |
| Способ кардиопротекции ишемических и реперфузионных повреждений в остром периоде инфаркта миокарда | 2019 |
|
RU2712448C1 |

Изобретение относится к биологии и экспериментальной медицине, а именно экспериментальной кардиологии, и может быть использовано для изучения пато- и морфогенеза ранних стадий инфаркта миокарда. Способ моделирования острого инфаркта миокарда у животных включает создание очага ишемического повреждения в сердце взрослых крыс возраста 6-18 месяцев. При этом ишемическое воздействие осуществляется местным введением в толщу миокарда склерозирующего препарата этоксисклерол 1,5% - 0,25 мл под общей анестезией с использованием атравматической иглы с силиконовым покрытием. Данный способ позволяет моделировать острый инфаркт миокарда при минимальном инвазивном воздействии на организм животного. Изобретение обеспечивает низкую смертность животных, простоту и короткое время проведения операции. 2 ил., 1 пр.
Способ моделирования острого инфаркта миокарда у животных, включающий создание очага ишемического повреждения в сердце взрослых крыс возраста 6-18 месяцев, отличающийся тем, что ишемическое воздействие осуществляется местным введением в толщу миокарда склерозирующего препарата этоксисклерол 1,5% - 0,25 мл под общей анестезией с использованием атравматической иглы с силиконовым покрытием, позволяющий моделировать острый инфаркт миокарда при минимальном инвазивном воздействии на организм животного.
| СПОСОБ МОДЕЛИРОВАНИЯ ИНФАРКТА МИОКАРДА У КРЫС | 2007 |
|
RU2407062C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ИШЕМИЧЕСКОГО ПОВРЕЖДЕНИЯ МИОКАРДА У КРЫС | 2002 |
|
RU2243595C2 |
| ОВСЕПЯН А.А | |||
| и др | |||
| Моделирование инфаркта миокарда на мышах: методология, мониторинг, патоморфология / Acta naturae, 2011, т | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ получения борнеола из пихтового или т.п. масел | 1921 |
|
SU114A1 |
| ПЛЕЧЕВ В.В | |||
| и др | |||
| МОДЕЛЬ ОСТРОГО ИНФАРКТА МИОКАРДА / Медицинский вестник Башкортостана, 2012, стр | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
| SAEZ P | |||
| et al | |||
| Computational | |||
Авторы
Даты
2021-06-28—Публикация
2020-07-15—Подача