Изобретение относится к биотехнологии, а именно к способу стабилизации коллагеназы растворами гиалуроновой кислоты и графт-сополимерами с полисахаридной основной цепью из карбоксиметилцеллюлозы (КМЦ) или хитозана (ХТЗ) с боковыми цепями из гомополимеров N-винилимидазола (ВИ) или N,N-диметиламиноэтилметакрилата (ДМАЭМА). Изобретение может быть использовано в химико-фармацевтической промышленности, медицинской практике, косметологии.
Коллагеназа (КФ 3.4.4.19) - фермент, обладающий протеолитической активностью с узко специфической направленностью к гидролизу коллагена с выделением свободной аминокислоты - оксипролина. Коллагеназа расщепляет крайне устойчивые к действию других протеаз коллагеновые волокна с образованием высокомолекулярных фрагментов, выполняет в организме человека и животных важнейшие функции: участвует в превращениях соединительной ткани при росте и морфогенезе, а также в устранении некоторых патологических процессов при артритах, опухолевых метастазах и т.д.
Коллагеназа содержится в составе безводной композиции для обработки ран [Патент RU 2585373 С2, МПК A61K 38/48, A61K 9/10, A61K 47/30, A61K 47/44, А61Р 17/02, C12N 9/00, опубл. 27.05.2016, Бюл. №15]. Описана мазь для заживления ожоговых и инфицированных ран, которая содержит коллагеназу Clostridium histolyticum в качестве протеолитического фермента, в качестве антибиотика - гентамицина сульфат, а в качестве мазевой основы - полиэтиленоксиды с молекулярными массами 400 и 1500 Да и глицерин. Изобретение обеспечивает щадящее, бескровное энзиматическое очищение ран, стимулирует развитие здоровых грануляций и не препятствует процессам эпителизации [Патент RU 2174389 С2, МПК A61K 9/06, A61K 38/43, А61Р 17/02, опубл. 10.10.2001, Бюл. №28]. Известна высокоэффективная нетоксичная, неаллергенная фармацевтическая композиция для заживления и очищения раневых, ожоговых и других повреждений кожи на основе коллагеназы микробного происхождения [Патент RU 2166950 С1, МПК A61K 35/74, C12Q 1/37, опубл. 20.05.2001, Бюл. №14]. Коллагеназу используют для лечения нерубцовой алопеции [Патент RU 2695364 С1, МПК A61K 35/50, A61K 35/28, A61K 35/51, А61Р 17/04, опубл. 23.07.2019, Бюл. №21]. Коллагеназа содержится в повязке, которая представляет собой комплекс из трех лейкопластырей или раневых покрытий с разными составами хитозановых прокладок для последовательного лечения инфицированных раневых повреждений [Патент RU 2014113441 А, МПК A61K 9/70, В82 В 1/00, опубл. 27.10.2015, Бюл. №30].
Гиалуроновая кислота является природным линейным несульфатированным гликозаминогликаном, состоящим из D-глюкуроновой кислоты и N-ацетил-D-глюкозамина, соединенных между собой β-1,3 и β-1,4-гликозидными связями. Гиалуроновая кислота - амфифильное соединение, проявляет гидрофильные (благодаря наличию групп -СООН и -ОН) и гидрофобные свойства (участки из 8 СН-единиц).
Описана активная против акне добавка к парфюмерно-косметическим продуктам, содержащая гиалуроновую кислоту [Патент RU 2678307 С1, МПК A61K 8/00, A61K 8/18, A61K 8/34, A61K 8/36, A61K 8/42, A61K 8/67, A61K 8/64, А61Р 17/10, A61Q 19/00, опубл. 25.01.2019, Бюл. №3]. Известен препарат для коррекции дефектов кожи, включающий гиалуроновую кислоту, который обеспечивает выработку ее собственных компонентов, а именно гиалуроновой кислоты, коллагена и эластина, при этом обладает сильными антиоксидантными свойствами и выраженным длительным эффектом коррекции кожных дефектов кожи [Патент RU 2659959 С1, МПК A61K 8/73, A61K 8/34, A61K 8/64, A61K 8/96, A61Q 19/08, опубл. 04.07.2018, Бюл. №19]. Гиалуроновая кислота входит в состав композиций для омоложения кожи [Патент RU 2629593 С1, МПК A61K 8/98, A61K 8/73, A61Q 19/08, опубл. 30.08.2017, Бюл. №25]. Гиалуроновая кислота с молекулярной массой менее 40 кДа представляет собой трансдермальный переносчик в составе косметического крема для ухода за кожей [Патент RU 2666602 С1, МПК A61K 8/04, A61K 8/34, A61K 8/73, A61K 8/92, A61K 8/97, A61K 8/9767, A61Q 19/08, опубл. 11.09.2018, Бюл. №26].
Графт-сополимеры карбоксиметилцеллюлозы или хитозана с боковыми цепями из N-винилимидазола или N,N-диметиламиноэтилметакрилата за счет наличия основной цепи из модифицированного природного полисахарида с молекулярной массой в интервале 10-600 кДа могут образовывать растворы с различной вязкостью, зависящей как от массы исходного полисахарида, так и от количества вносимого графт-сополимера [A. Benchabane, K. Bekkour. Rheological properties of carboxymethyl cellulose (CMC) solutions. 2008. Colloid and Polymer Science. Vol. 286. P. 1173-1180.]. Кроме того, такие полимеры могут использоваться в биомедицинских целях, например, в качестве носителя для цитостатического антибиотика широкого спектра действия «Паклитаксела» при пероральном и/или инфузионном введении [V. А. Kuznetsov, А. V. Sorokin, М. S. Lavlinskaya et al. Graft copolymers of carboxymethyl cellulose with N-vinylimidazole: synthesis and application for drug delivery. 2019. Polymer Bulletin. Vol. 76. P. 4929-4949; V. A. Kuznetsov, A. V. Sorokin, M. S. Lavlinskaya. Synthesis of graft copolymers of carboxymethyl cellulose and N,N-dimethylaminoethyl methacrylate and their study as Paclitaxel carriers. 2020. Polymer Bulletin. DOI: 10.1007/s00289-020-03250-z].
На данный момент нет сведений о комплексах коллагеназы с гиалуроновой кислотой и полисахаридами, модифицированными виниловыми мономерами, такими как графт-сополимеры карбоксиметилцеллюлозы (КМЦ) или хитозана (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА).
Известен способ получения гетерогенного препарата на основе коллагеназы и хитозана [Патент RU 2678435 С2, МПК A61K 31/722, A61K 38/43, А61Р 17/02, C12N 11/10, опубл. 29.01.2019, Бюл. №4]. Данный способ включает иммобилизацию коллагеназы в буферном растворе на матрицу кислоторастворимого среднемолекулярного или высокомолекулярного хитозана в соотношении 20 мл буферного раствора коллагеназы в концентрации 1 мг/мл на 1 г указанной матрицы, при этом в качестве буферного раствора для иммобилизации используют 0.05 М глициновый буфер с рН 8.6 для среднемолекулярного и с рН 10.5 для высокомолекулярного хитозана; далее проводят инкубирование в течение 5 часов при комнатной температуре с периодическим перемешиванием; затем промывают образовавшийся осадок 50 мМ трис-HCl буфером с рН 7.5 до отсутствия в промывных водах коллагеназы.
Недостатком способа является получение ферментного препарата в твердой фазе, не позволяющей проникать молекулам коллагеназы в глубокие слои кожи.
Запатентован способ стабилизации ферментов - пепсина, химотрипсина, трипсина, панкреатина, папаина и других протеаз, путем добавления в их растворы полисахаридов - гуаровой камеди, ксантановой камеди, камеди бобов рожкового дерева, крахмала, декстрана, пуллулана, альгиновой кислоты, гиалуроновой кислоты, каррагинана, пектина, хитозана и прочих полисахаридов, а также производных целлюлозы: карбоксиметилцеллюлозы, метилцеллюлозы, этилцеллюлозы, гидроксипропилцеллюлозы [JPH034791A].
Известен способ получения препарата коллагеназы в геле на основе пищевого хитозана и сукцината хитозана, включающий иммобилизацию коллагеназы в буферном растворе на матрицу хитозана, инкубирование при комнатной температуре с периодическим перемешиванием, промывку образовавшегося осадка буфером, отличающегося тем, что иммобилизацию проводят на матрицу пищевого хитозана с молекулярной массой менее 100 кДа или сукцината хитозана, в качестве буфера используют 0.05 М ацетатный буфер с рН 5.8 или 0.05 М глициновый буфер с рН 9.0, инкубация проводится в течение 2 часов [Патент RU 2712528, МПК C12N 11/10, А61K 31/722, опубл. 29.01.2020 Бюл. №4].
В отличие от этих двух способов предложенное нами использование полисахаридов (карбоксиметилцеллюлозы и хитозана), модифицированных виниловыми мономерами (N-винилимидазолом или N,N-диметиламиноэтилметакрилатом) обеспечивает большее количество связей между полисахаридом и ферментом в ходе иммобилизации, что увеличивает прочность образуемого комплекса и пролонгирует процесс высвобождения фермента в область поврежденных тканей. Кроме того, добавление в препарат гиалуроновой кислоты будет способствовать его более глубокому проникновению в различные слои кожи.
Известно, что полимеры на основе поли-β-гликозидов (целлюлозы и ее производных, хитозана, гиалуроновой кислоты и т.д.) склонны к образованию пленок, которые могут защитить кожу от пересыхания или обеспечить дополнительную защиту на поверхности раневого повреждения. Однако способность образовывать конъюгаты у таких полимеров несколько ограничена рядом факторов: поверхностным зарядом, типом функциональной группы и т.д. Поэтому для придания ряда новых свойств целесообразно проводить химическую модификацию природных полисахаридов. Так, например, введение азольных заместителей повышает комплексообразующую способность полисахаридов и снижает поверхностный отрицательный заряд карбоксиметилцеллюлозы [V.А. Kuznetsov, А.V. Sorokin, М. S. Lavlinskaya et al. Graft copolymers of carboxymethyl cellulose with N-vinylimidazole: synthesis and application for drug delivery. 2019. Polymer Bulletin. Vol. 76. P. 4929-4949], а введение звеньев N,N-диметиаминоэтилметакрилата не только снижает поверхностный заряд, но придает водному раствору модифицированного полисахарида стимулочувствительные свойства [V.A. Kuznetsov, А.V. Sorokin, М.S. Lavlinskaya. Synthesis of graft copolymers of carboxymethyl cellulose and N,N-dimethylaminoethyl methacrylate and their study as Paclitaxel carriers. 2020. Polymer Bulletin. DOI: 10.1007/s00289-020-03250-z].
В качестве прототипа служила топическая противомикробная дерматологическая композиция [Патент RU 2668827 С2, МПК A61K 38/08, А61K 31/728, А61Р 31/00, А61Р 17/00, А61K 31/722, опубл. 02.10.2018, Бюл. №28], предложенная в качестве лекарственного средства в медицине и ветеринарии, включающая комбинацию по меньшей мере одного положительно заряженного противомикробного пептида, соединенного с липидом, и гиалуроновой кислоты со средним молекулярным весом от 100 кДа до 800 кДа или одной из ее солей, причем противомикробный пептид представляет собой гексапептид, соединенный с пальмитиновой кислотой, содержащий дисульфидные мостики.
В отличие от прототипа в качестве действующего вещества мы используем не противомикробный пептид, а фермент коллагеназу, которая способна избирательно гидролизовать коллаген, входящий в состав соединительной ткани живого организма, расщепляя крайне устойчивые к действию других протеаз коллагеновые волокна, выполняет в организме человека и животных важнейшие функции, участвует в превращениях соединительной ткани при росте и морфогенезе, а также в устранении некоторых патологических процессов при артритах, опухолевых метастазах и т.д., при гнойных ранах коллагеназа способствует быстрому удалению нежизнеспособных тканей и эксудата, раннему появлению грануляционной ткани, эпителизации, применение коллагеназы предупреждает развитие грубых рубцов, при этом сохраняется подвижность кожи и мягких тканей.
Кроме того, добавление нами в раствор графт-сополимеров карбоксиметилцеллюлозы (КМЦ) или хитозана (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) позволяет путем включения в полисахаридный гель (один из способов физической иммобилизации ферментов) дополнительно стабилизировать коллагеназу и обеспечить ей пролонгированное действие.
Технический результат заявленного изобретения заключается в разработке способа получения иммобилизованного жидкого или гелеобразного ферментного препарата на основе коллагеназы, полисахаридов, модифицированных виниловыми мономерами, и гиалуроновой кислоты низкомолекулярной (300 кДа), среднемолекулярной (500 кДа) или высокомолекулярной (800 кДа), благодаря чему растворы коллагеназы можно хранить при температурах от 4 до 25°С в течение 21 суток, а фермент при этом становится более стабильным в сравнении с нативным и способен проникать в глубокие слои кожи, при этом внесение в состав препарата модифицированных полисахаридов позволяет не только варьировать вязкость и консистенцию образцов (от жидкого состояния до геля с различной текучестью), но также способствует образованию конъюгатов с ферментом с большим количеством связей и взаимодействий между полисахаридом и ферментом, по сравнению с немодифицированными карбоксиметилцеллюлозой и хитозаном, что дополнительно повышает стабильность препарата и концентрацию активного вещества в пораженном участке кожи, а также обеспечивает контролируемое (порционное) высвобождение коллагеназы, поддерживая ее необходимую концентрацию в течение длительного времени. Кроме того, способность модифицированных полисахаридов образовывать устойчивые пленки защищает фермент и обрабатываемый участок кожи от пересыхания, позволяет легко удалить препарат вместе с гноем и экссудатом.
Технический результат достигается тем, что в способе получения иммобилизованного ферментного препарата на основе коллагеназы, полисахаридов, модифицированных виниловыми мономерами, и гиалуроновой кислоты, включающем растворение коллагеназы в водном растворе низкомолекулярной гиалуроновой кислоты 300 кДа или среднемолекулярной гиалуроновой кислоты 500 кДа или высокомолекулярной гиалуроновой кислоты 800 кДа в соотношении 10 мг коллагеназы на 2 мл водного раствора низкомолекулярной гиалуроновой кислоты 300 кДа или среднемолекулярной гиалуроновой кислоты 500 кДа или высокомолекулярной гиалуроновой кислоты 800 кДа в концентрации 1.5%, перемешивание осуществляют до полного растворения при комнатной температуре; затем проводят иммобилизацию коллагеназы путем добавления к полученной смеси графт-сополимера карбоксиметилцеллюлозы 50-100 кДа (КМЦ) или хитозана 50-100 кДа (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) в количестве от 100 до 290 мг для получения жидкого препарата или от 300 до 500 мг для получения геля.
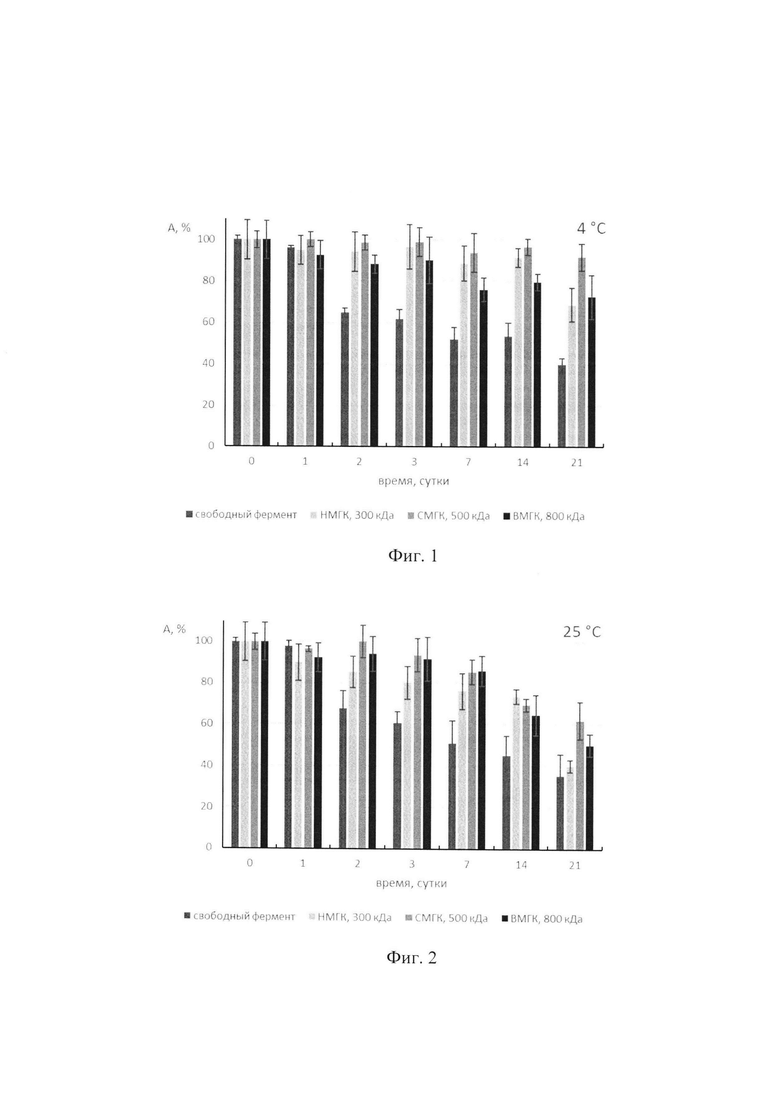
Фиг. 1. Диаграмма значений каталитической активности (А) коллагеназы в присутствии гиалуроновой кислоты различной молекулярной массы после его хранения при 4°С.
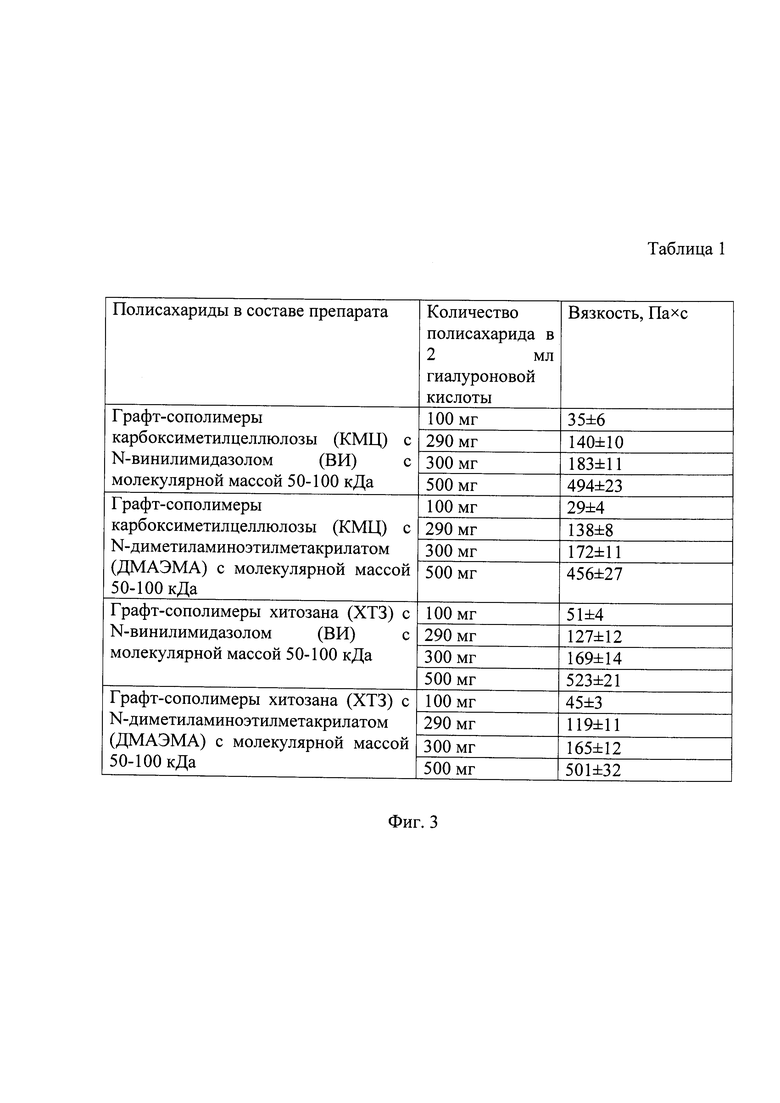
Фиг. 2. Диаграмма значений каталитической активности (А) коллагеназы в присутствии гиалуроновой кислоты различной молекулярной массы после его хранения при 25°С.
Фиг. 3. Таблица 1. Вязкость препаратов, содержащих коллагеназу, гиалуроновую кислоту и полисахариды, модифицированные виниловыми мономерами.
Пример реализации способа.
В качестве объекта исследования была выбрана коллагеназа из Clostridium histolyticum фирмы «Sigma-Aldrich», субстратом для гидролиза служил азоказеин фирмы «Sigma-Aldrich». В качестве стабилизирующих агентов применяли три вида гиалуроновой кислоты (ООО «Лаборатория Гиалика») с молекулярной массой 300 (НМГК), 500 (СМГК) и 800 (ВМГК) кДа. В качестве матрицы для иммобилизации коллагеназы применяли графт-сополимеры карбоксиметилцеллюлозы (КМЦ) или хитозана (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) с молекулярной массой 50-100 к Да.
Стабилизацию коллагеназы осуществляли путем растворения ее навески массой 10 мг в 2 мл водного раствора гиалуроновой кислоты с молекулярной массой 300 (НМГК), 500 (СМГК) или 800 (ВМГК) кДа в концентрации 1.5% с последующим перемешиванием при комнатной температуре до полного растворения. Затем к полученной смеси добавляли для иммобилизации коллагеназы графт-сополимер карбоксиметилцеллюлозы (КМЦ) или хитозана (ХТЗ) (при молекулярной массе полисахарида 50-100 кДа) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) в количестве от 100 до 290 мг для получения жидкого препарата или от 300 до 500 мг для получения геля (табл. 1).
Содержание белка в иммобилизованных препаратах коллагеназы определяли методом Лоури [Lowry О.Н., Rosebrough N.J., Faar A.L., Randall R.J. Protein measurement with folin-phenol reagent // J. Biol. Chem. - 1951. -V.193. - P. 265-275]. Измерение уровня протеолитической активности фермента проводили на субстрате азоказеине [Garcia-Carreno, F. L. The digestive proteases of langostilla (Pleuroncodes planipes, Decapoda): their partial characterization and the effect of feed on their composition //Comparative Biochemistry and Physiology Part B: Comparative Biochemistry - 1992. - V. 103. - P. 575-578]. К 200 мкл образца добавляли 200 мкл трис-HCl буфера (рН 7.5), 800 мкл азоказеина (0.5% в 50 мМ трис-HCl буфере, рН 7.5) и инкубировали 2 часа при 37°С. Далее добавляли 800 мкл трихлоруксусной кислоты (ТХУ) (5%), инкубировали 10 минут при минус 4°С, затем центрифугировали в течение 3 мин при 13 000 об/мин для удаления негидролизованного азоказеина. К 1200 мкл супернатанта добавляли 240 мкл 3% NaOH для нейтрализации кислоты, после чего измеряли оптическую плотность опытной пробы при 410 нм в 1 см кювете. Контрольная проба содержала 800 мкл азоказеина, 800 мкл ТХУ, 200 мкл трис-HCl буфера и 200 мкл образца, который вносили после инкубации смеси в течение 2 часов при 37°С. За единицу каталитической активности коллагеназы принимали количество фермента, которое в условиях эксперимента гидролизует 1 мкМ субстрата за 1 мин. Удельную протеолитическую активность коллагеназы рассчитывали по формуле:
ПА = D*1000/120/200/C,
где ПА - протеолитическая активность, мкМ/мин на 1 мг белка,
D - оптическая плотность пробы при 410 нм,
С - концентрация белка в пробе, мг/мл, измеренная по методу Лоури,
120 - время инкубации в минутах,
200 - объем пробы, в мкл,
1000 - пересчет в мкМ.
Статистическую обработку полученных результатов проводили при уровне значимости 5% с использованием t-критерия Стьюдента.
Были проведены исследования стабильности коллагеназы в растворах гиалуроновой кислоты (300, 500 и 800 кДа) по сравнению с нативным энзимом. Препараты инкубировали при 4 и 25°С в течение 0, 1, 2, 3, 7, 14 и 21 суток с дальнейшим измерением протеолитической активности. Полученные результаты отражены на фиг. 1, 2.
В ходе наших экспериментов было выявлено, что гиалуроновая кислота не ингибирует коллагеназу.
На фиг. 1 представлена диаграмма зависимости каталитической активности энзима от времени его хранения при 4°С. Установлено, что нативная коллагеназа сохраняет 52-53% своей активности после 7-14 суток инкубации при 4°С, а после 3 недель хранения активна на 40% от исходного препарата. Коллагеназа в растворе низкомолекулярной гиалуроновой кислоты (300 кДа) на 14 день хранения сохраняет более 90% каталитической способности от неинкубированного образца. После 21 дня инкубации активность коллагеназы в растворе низкомолекулярной гиалуроновой кислоты составляет 69% от начальной. Раствор коллагеназы со среднемолекулярной гиалуроновой кислотой (500 кДа) незначительно теряет свою активность в течение всего периода инкубации и сохраняет 91% своей ферментативной способности на 21 сутки хранения. Коллагеназа в растворе высокомолекулярной гиалуроновой кислоты (800 кДа) постепенно инактивируется: на 3 сутки активность энзима снижается на 10%, на 7 сутки - на 14%, а после 21 дня хранения каталитическая способность фермента составляет 72% от исходной.
На фиг. 2 изображена диаграмма изменения каталитической активности коллагеназы после ее хранения при 25°С. На 7 сутки хранения при температуре 25°С свободный энзим сохраняет 51% активности, препарат коллагеназы в растворе среднемолекулярной гиалуроновой кислоты (500 кДа) - 87%, раствор коллагеназы в высокомолекулярной гиалуроновой кислоте (800 кДа) - 86%, коллагеназа в растворе низкомолекулярной гиалуроновой кислоты (300 кДа) - 76%. Нативная коллагеназа на 14 и 21 сутки эксперимента активна соответственно на 45 и 36%, комплексы фермента со среднемолекулярной гиалуроновой кислотой - на 71 и 63%, с высокомолекулярной гиалуроновой кислотой - на 65 и 50%, с низкомолекулярной гиалуроновой кислотой - 74 и 40%.
Выявлено, что раствор коллагеназы в среднемолекулярной гиалуроновой кислоте (500 кДа) после инкубации при температурах 4 и 25°С оказался наиболее стабильным по сравнению с другими препаратами.
Таким образом, был разработан способ получения иммобилизованного ферментного препарата на основе коллагеназы, низкомолекулярной (300 кДа), среднемолекулярной (500 кДа) и высокомолекулярной (800 кДа) гиалуроновой кислоты с последующим добавлением графт-сополимера карбоксиметилцеллюлозы (КМЦ) или хитозана (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) для иммобилизации коллагеназы.
При этом полученный предложенным способом препарат можно хранить при температурах от 4 до 25°С в течение 21 суток, а коллагеназа при этом становится более стабильной в сравнении с нативной и способна проникать в глубокие слои кожи. Внесение в состав препарата модифицированных полисахаридов позволяет не только варьировать вязкость и консистенцию образцов (от жидкого состояния до геля с различной текучестью), но также способствует образованию конъюгатов с ферментом с большим количеством связей и взаимодействий между полисахаридом и ферментом, по сравнению с немодифицированными карбоксиметилцеллюлозой и хитозаном, что дополнительно повышает стабильность препарата и концентрацию активного вещества в пораженном участке кожи, а также обеспечивает контролируемое (порционное) высвобождение коллагеназы, поддерживая ее необходимую концентрацию в течение длительного времени. Кроме того, способность модифицированных полисахаридов образовывать устойчивые пленки защищает фермент и обрабатываемый участок кожи от пересыхания, позволяет легко удалить препарат вместе с гноем и экссудатом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ ПАПАИНА, ГИАЛУРОНОВОЙ КИСЛОТЫ И ПОЛИСАХАРИДОВ, МОДИФИЦИРОВАННЫХ ВИНИЛОВЫМИ МОНОМЕРАМИ | 2020 |
|
RU2750378C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ ТРИПСИНА, ГИАЛУРОНОВОЙ КИСЛОТЫ И ПОЛИСАХАРИДОВ, МОДИФИЦИРОВАННЫХ ВИНИЛОВЫМИ МОНОМЕРАМИ | 2020 |
|
RU2750376C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ БРОМЕЛАЙНА, ГИАЛУРОНОВОЙ КИСЛОТЫ И ПОЛИСАХАРИДОВ, МОДИФИЦИРОВАННЫХ ВИНИЛОВЫМИ МОНОМЕРАМИ | 2020 |
|
RU2750377C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО ФЕРМЕНТНОГО ПРЕПАРАТА НА ОСНОВЕ ФИЦИНА, ГИАЛУРОНОВОЙ КИСЛОТЫ И ПОЛИСАХАРИДОВ, МОДИФИЦИРОВАННЫХ ВИНИЛОВЫМИ МОНОМЕРАМИ | 2020 |
|
RU2744457C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА БРОМЕЛАЙНА И КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2788454C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА ПАПАИНА И КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2795425C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ФИЦИНА В ГЕЛЕ НА ОСНОВЕ КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ | 2021 |
|
RU2771183C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО ПРЕПАРАТА ФИЦИНА И N-МАЛЕОИЛХИТОЗАНА В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2792784C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ПРЕПАРАТА БРОМЕЛАЙНА И АЛЬГИНАТА НАТРИЯ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2792785C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ПРЕПАРАТА ПАПАИНА И АЛЬГИНАТА НАТРИЯ В ВИДЕ ГУСТОГО РАСТВОРА | 2022 |
|
RU2788455C1 |
Настоящее изобретение относится к области химико-фармацевтической промышленности и медицины, а именно к способу получения иммобилизованного ферментного препарата на основе коллагеназы, полисахаридов, модифицированных виниловыми мономерами, и гиалуроновой кислоты, включающему растворение коллагеназы в водном растворе низкомолекулярной гиалуроновой кислоты 300 кДа или среднемолекулярной гиалуроновой кислоты 500 кДа или высокомолекулярной гиалуроновой кислоты 800 кДа в соотношении 10 мг коллагеназы на 2 мл водного раствора низкомолекулярной гиалуроновой кислоты 300 кДа или среднемолекулярной гиалуроновой кислоты 500 кДа или высокомолекулярной гиалуроновой кислоты 800 кДа в концентрации 1.5%, при этом осуществляют перемешивание до полного растворения при комнатной температуре; затем проводят иммобилизацию коллагеназы путем добавления к полученной смеси графт-сополимера карбоксиметилцеллюлозы 50-100 кДа (КМЦ) или хитозана 50-100 кДа (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) в количестве от 100 до 290 мг для получения жидкого препарата или от 300 до 500 мг для получения геля. Настоящее изобретение обеспечивает разработку способа получения иммобилизованного жидкого или гелеобразного ферментного препарата на основе коллагеназы, полисахаридов, модифицированных виниловыми мономерами, и гиалуроновой кислоты низкомолекулярной (300 кДа), среднемолекулярной (500 кДа) или высокомолекулярной (800 кДа), благодаря чему растворы коллагеназы можно хранить при температурах от 4 до 25°С в течение 21 суток, а фермент при этом становится более стабильным в сравнении с нативным и способен проникать в глубокие слои кожи, при этом внесение в состав препарата модифицированных полисахаридов позволяет не только варьировать вязкость и консистенцию образцов (от жидкого состояния до геля с различной текучестью), но также способствует образованию конъюгатов с ферментом с большим количеством связей и взаимодействий между полисахаридом и ферментом, по сравнению с немодифицированными карбоксиметилцеллюлозой и хитозаном, что дополнительно повышает стабильность препарата и концентрацию активного вещества в пораженном участке кожи, а также обеспечивает контролируемое (порционное) высвобождение коллагеназы, поддерживая ее необходимую концентрацию в течение длительного времени. 3 ил., 1 пр.
Способ получения иммобилизованного ферментного препарата на основе коллагеназы, полисахаридов, модифицированных виниловыми мономерами, и гиалуроновой кислоты, включающий растворение коллагеназы в водном растворе низкомолекулярной гиалуроновой кислоты 300 кДа или среднемолекулярной гиалуроновой кислоты 500 кДа или высокомолекулярной гиалуроновой кислоты 800 кДа в соотношении 10 мг коллагеназы на 2 мл водного раствора низкомолекулярной гиалуроновой кислоты 300 кДа или среднемолекулярной гиалуроновой кислоты 500 кДа или высокомолекулярной гиалуроновой кислоты 800 кДа в концентрации 1.5%, при этом осуществляют перемешивание до полного растворения при комнатной температуре; затем проводят иммобилизацию коллагеназы путем добавления к полученной смеси графт-сополимера карбоксиметилцеллюлозы 50-100 кДа (КМЦ) или хитозана 50-100 кДа (ХТЗ) с N-винилимидазолом (ВИ) или N,N-диметиламиноэтилметакрилатом (ДМАЭМА) в количестве от 100 до 290 мг для получения жидкого препарата или от 300 до 500 мг для получения геля.
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА КОЛЛАГЕНАЗЫ | 2003 |
|
RU2236460C1 |
| Liliana Gianfreda et al., Enzyme stabilization: state of the art/ Molecular and Cellular Biochemistry, 1991 | |||
| Vol | |||
| Облицовка комнатных печей | 1918 |
|
SU100A1 |
| Холявка М | |||
| Г | |||
| и др., Исследование процессов УФ-модификации свободной и иммобилизованной на матрице хитозана коллагеназы / Радиационная биология | |||
| Радиоэкология, 2019, T | |||
| Устройство для охлаждения водою паров жидкостей, кипящих выше воды, в применении к разделению смесей жидкостей при перегонке с дефлегматором | 1915 |
|
SU59A1 |
| Способ приготовления сернистого красителя защитного цвета | 1915 |
|
SU63A1 |
Авторы
Даты
2021-06-28—Публикация
2020-07-27—Подача