Область техники, к которой относится изобретение
[1] Настоящее изобретение относится к композиции для профилактики, облегчения течения или лечения рака крови, содержащей новый олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, включающий, по меньшей мере, один 1-β-D-арабинофуранозилцитозин в качестве модифицированной нуклеиновой кислоты, обладающей терапевтической эффективностью, или его фармацевтически приемлемую соль в качестве активного компонента.
[2]
Уровень техники
[3] Рак крови (гематологические опухоли) относится к онкологическому заболеванию, при котором различные клетки крови перерождаются в раковые клетки, и к типу онкологического заболевания, которое поражает кровь, костный мозг и/или лимфатическую систему. Данный тип рака включает лейкоз, лимфому и множественную миелому. Лейкоз представляет рак крови, при котором раковые клетки, которые подверглись перерождению из гемопоэтических стволовых клеток, образующих различные клетки крови, вызывают сверхпродукцию лейкозных клеток, и препятствуют нормальной выработке нормальных клеток крови, что приводит к развитию инфекции, анемии, кровотечению и тому подобное. Лимфома представляет рак, возникающий в лимфатической системе, который включает неходжкинскую лимфому и ходжкинскую лимфому. Множественная миелома представляет рак крови, вызванный аномальной дифференцировкой и пролиферацией плазматических клеток, которые являются видом лейкоцитов крови. Более конкретно, рак крови выбран из группы, состоящей из неходжкинской лимфомы, ходжкинской лимфомы, множественной миеломы, лейкоза, лимфомы, миелодиспластического синдрома, острого лимфобластного лейкоза, острого миелоидного лейкоза, хронического лимфоцитарного лейкоза, хронического миелоидного лейкоза, солитарной миеломы и апластической анемии.
[4] Каждый год новые случаи лейкоза, ходжкинской лимфомы и неходжкинской лимфомы и миеломы составляют почти 10% от всех вновь диагностированных случаев рака. В условиях демографического старения общества число пожилых людей, страдающих раком крови, возрастает, но их выживаемость очень низкая. В частности, выживаемость пациентов в возрасте 65 лет и старше составляет всего 9,4%, а выживаемость пациентов в возрасте 80 лет и старше равна 0% (Blood, 2012, 120; 1165-1174).
[5] Рак крови (гематологические опухоли) представляет заболевание, вызванное перерождением мутантных клеток в раковые клетки, образующихся в крови и лимфатической системе, когда мутантные клетки переносятся по всему телу, и существует примерно 70 различных типов рака крови. Следовательно, пациенты, у которых диагностирован рак крови, сначала получают индукционную химиотерапию с целью достижения ремиссии для удаления всех иммунных клеток из организма для уничтожения мутантных аномальных клеток. Затем проводится консолидирующая химиотерапия, включающая введение токсичных химических соединений только в аномальные клетки. Индукционная химиотерапия с целью достижения ремиссии осуществляется посредством введения в высоких дозах комбинации высокоцитотоксических противоопухолевых препаратов, которые очень токсичны и вызывают многочисленные побочные эффекты и, следовательно, не применимы для введения пациентам пожилого возраста. Это является причиной того, что выживаемость среди пожилых пациентов с раком крови очень низкая (Blood, 2010,116: 5818-5823).
[6] Кроме того, терапевтическое действие на рак крови отсутствует, потому что пациенты с раком крови не отвечают на индукционную химиотерапию для достижения ремиссии даже в высоких дозах, или имеются нереализованные потребности медицины, связанные с раком крови, за счет высокой степени резистентности и высокой частоты рецидивов в течение пяти лет.
[7] В настоящее время разработаны таргетные способы лечения с использованием антител и ингибиторов киназ, но лечение рака крови все еще существенно зависит от химиотерапии и лучевой терапии (The New England Journal of Medicine, 2014, 371: 1005-1015). Противоопухолевые лекарственные средства, используемые в качестве химиотерапевтических препаратов при раке крови, представляют собой цитотоксические противоопухолевые лекарственные средства с высокой общей токсичностью, которые вводят в очень высоких дозах за счет низкой биодоступности и сложности таргетной доставки к раковым клеткам. Это вызывает тяжелые побочные эффекты у пациентов, что затрудняет лечение. Следовательно, существует необходимость в новых терапевтических агентах, имеющих более низкую токсичность и эффективную терапевтическую эффективность.
[8] Известно, что специфические гуанозин-богатые олигонуклеотиды оказывают ингибирующее действие на клеточный рост в широком диапазоне раковых клеток и функционируют с регуляцией клеточного цикла посредством связывания со специфическими белками в клетках, например, белками, важными для роста и гибели клеток, такими как белки eEF1A, JNK, Ki-ras, нуклеолин, stat3, теломераза и топоизомераза, при лечении раковых клеток ими, и известно, что эти белки сверхэкспрессируются в раковых клетках на уровне выше, чем в нормальных клетках (Christopher R. Ireson et al. Molecular cancer therapy, 2006, 2957-2962; Naijie Jing et al. Cancer research, 2004, 6603-6609; Christophe Marchand et al. The Journal of Biological Chemistry, 2002, 8906-8911).
[9] Такие гуанозин-богатые олигонуклеотиды имеют особые структурные свойства в дополнение к тройной водородной связи с цитозином. Гуанозин-богатые олигонуклеотиды могут иметь четырехцепочечную структуру за счет внутримолекулярного связывания или межмолекулярного связывания. Вместо формирования структуры двойной спирали через общую водородную связь между аденозином и тиамином и между гуанозином и цитидином, четыре гуанозина располагаются в одной плоскости с образованием хугстиновских водородных связей, которые образуют G-квадруплекс. Два или более таких G-квадруплексов упорядоченно располагаются с образованием тетраспиральной структуры. В общем, существуют трудности в разработке олигонуклеотидов в качестве лекарственных средств за счет их низкой стабильности в крови и их низкого проникновения в клетки. Однако известно, что олигонуклеотиды, составляющие такой G-квадруплекс, обладают относительно высокой стабильностью в крови и проницаемостью в клетки благодаря их структурным характеристикам.
[10] Как описано в патенте США № 7314926 и в публикации заявки на патент США № 2007-105805, известно, что олигонуклеотиды, составляющие такой G-квадруплекс, связываются со специфическими белками, которые высоко экспрессируются на поверхности раковых клеток, и затем проникают в раковые клетки посредством эндоцитоза, и связываются с белками, участвующими в гибели клеток, с ингибированием роста клеток. Сообщалось, что такие олигонуклеотиды вызывают апоптоз в большей степени за счет цитостатических эффектов, а не цитотоксических эффектов (Paula J. Bates et al. The Journal of Biological Chemistry, 1999, 26369-26377; Bruna et al. FEBS journal, 2006, 1350-1361).
[11] Кроме того, известно, что помимо эффекта ингибирования роста раковых клеток, олигонуклеотиды, составляющие G-квадруплексы, обладают различными функциями и регуляторными функциями in vivo, например, в патенте США № 5567604 раскрыто, что олигонуклеотиды, составляющие G-квадруплексы, обладают противовирусным действием. В патенте США № 6994959 раскрывается, что олигонуклеотиды, составляющие G-квадруплексы, обладают иммуномодулирующей активностью, и в публикации заявки на патент США № 2007-105805 раскрыто, что олигонуклеотиды, составляющие G-квадруплексы, оказывают терапевтическое действие при болезни Гентингтона (Cheryl A. Stoddart et al., Antimicrob. и Chemotherapy, 1998, 2113-2115; Michael Skogen et al., BMC Neuroscience, 2006, 7:65).
[12] Такие олигонуклеотиды, составляющие G-квадруплексы, вызывают апоптоз за счет цитостатического эффекта, в результате уровень апоптоза не является относительно высоким. Следовательно, трудно вводить олигонуклеотиды в комбинации с высокотоксичным химиотерапевтическим препаратом (Paula J. Bates и др. Experimental and Molecular Pathology, 2009, 151-164; Christopher R. Ireson et al. Molecular Cancer Therapy, 2006, 2957-2962).
[13] В корейском патенте № 10-0998365 раскрыт пример повышения апоптотического эффекта введением модифицированной нуклеиновой кислоты, обладающей терапевтической эффективностью, обеспечивающей апоптотический эффект, в олигонуклеотиды, образующие G-квадруплексы. Однако в патенте не раскрываются ни олигонуклеотиды, содержащие модифицированные нуклеиновые кислоты, по настоящему изобретению, ни их терапевтический эффект при раке крови и их апоптотический эффект на резистентные к лекарственным препаратам раковые клетки крови.
[14]
[15] Предшествующие уровень техники
[16] Патентные документы
[17] Корейский патент № 10-0998365
[18] Патент США № 7314926
[19] Выложенная заявка на патент США № 2007-105805
[20] Патент США № 5567604
[21] Патент США № 6994959
[22] Выложенная заявка на патент США № 2007-105805
[23]
[24] Непатентные документы
[25] (Непатентный документ 1) Christopher R. Ireson et al., Molecular Cancer Therapy, 2006, 2957-2962; Naijie Jing et al., Cancer Research, 2004, 6603-6609; Christophe Marchand et al., The Journal of Biological Chemistry, 2002, 8906-8911.
[26] (Непатентный документ 2) Paula J. Bates et al., The Journal of Biological Chemistry, 1999, 26369-26377; Bruna et al., FEBS journal 2006 1350-1361]
[27] (Непатентный документ 3) Cheryl A. Stoddart et al. Antimicrobial Agents and Chemotherapy, 1998, 2113-2115; Michael Skogen et al., BMC Neuroscience, 2006, 7:65.
[28] (Непатентный документ 4) Paula J. Bates et al., Experimental and Molecular Pathology, 2009, 151-164; Christopher R. Ireson et al., Molecular Cancer Therapy, 2006, 2957-2962.
[29]
Раскрытие изобретение
Техническая проблема
[30] С учетом вышеуказанных проблем заявители настоящего изобретения ввели один или более 1-β-D-арабинофуранозилцитозинов, которые представляют модифицированную нуклеиновую кислоту, обладающую терапевтической эффективностью, для индукции апоптоза посредством цитотоксического эффекта, в обладающий цитостатическим эффектом олигонуклеотид, который является гуанозин-богатым, и за счет этого образует G-квадруплекс, для повышения стабильности в крови и проникновения в клетки, и более эффективного ингибирования роста раковых клеток крови, и тем самым индукции гибели клеток, и синтезировали новый олигонуклеотид, имеющий такую структуру, и на основании сравнения цитотоксичности установили, что олигонуклеотид обладает значительно повышенным эффектом индукции гибели раковых клеток крови, в частности, обладает высоким противоопухолевым действием (в концентрации на уровне нМ) на резистентные к лекарственным средствам раковые клетки крови, которые затрудняют лечение, поскольку они не отвечают на обычные лекарственные препараты, применяемые для лечения рака крови, и имеет высокую терапевтическую эффективность при раке крови. Наконец, на основании этого открытия настоящее изобретение было завершено.
[31] Следовательно, одной целью настоящего изобретения является обеспечение нового олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, включающего, по меньшей мере, один 1-β-D-арабинофуранозилцитозин в качестве модифицированной нуклеиновой кислоты, обладающей терапевтическим эффектом, и который является гуанозин-богатым.
[32] Другой целью настоящего изобретения является обеспечение композиции для профилактики, облегчения течения или лечения рака крови, содержащей олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, или его фармацевтически приемлемую соль в качестве активного ингредиента.
[33]
Решение технической проблемы
[34] В одном аспекте настоящее изобретение относится к олигонуклеотиду, содержащему модифицированную нуклеиновую кислоту, включающему соединение, представленное следующей формулой 2, с образованием G-квадруплексной структуры:
[35] Формула 2
[36]
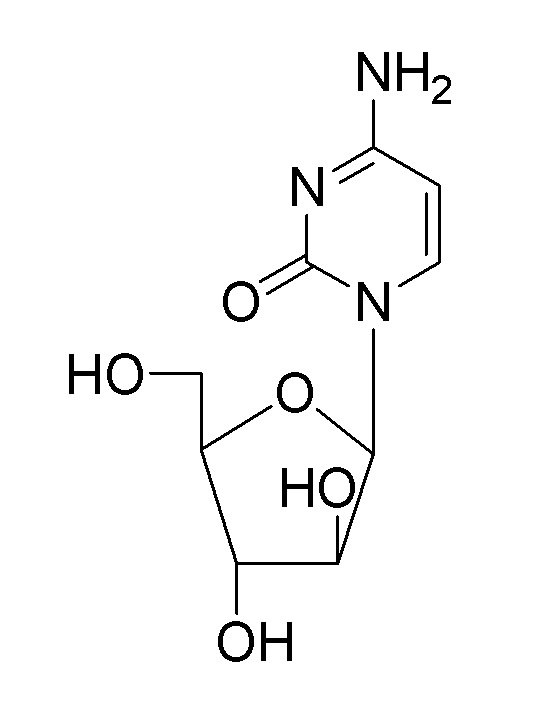
[37] Олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, может быть представлен следующей последовательностью:
[38] последовательность 1) GGTGGTGGTTNTGGTGGTGG;
[39] последовательность 2) GGTGGTGGTNNTGGTGGTGG;
[40] последовательность 3) NGGTGGTGGTTGTGGTGGTGG; или
[41] последовательность 4) NNGGTGGTGGTTGTGGTGGTGG;
[42] где G представляет гуанозин или производное гуанозина, T представляет тимин или производное тимина, и N представляет 1-β-D-арабинофуранозилцитозин.
[43] В еще одном аспекте настоящее изобретение относится к композиции для профилактики, облегчения течения или лечения рака крови, содержащей олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, или его фармацевтически приемлемую соль в качестве активного ингредиента.
[44]
Преимущественные эффекты изобретения
[45] Новый олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, по настоящему изобретению представляет соединение с новой структурой, способной образовывать G-квадруплекс, включением, по меньшей мере, одного 1-β-D-арабинофуранозилцитозина и гуанозина, и, таким образом, он пригоден в качестве профилактического и терапевтического средства для рака крови за счет высокой апоптотической активности и противоопухолевой терапевтической эффективности для раковых клеток крови, а также резистентных к лекарственным препаратам раковых клеток крови.
[46]
Краткое описание фигур
[47] Вышеуказанные и другие цели, признаки и другие преимущества настоящего изобретения будут более понятны из следующего подробного описания, представленного в сочетании с прилагаемыми фигурами, на которых:
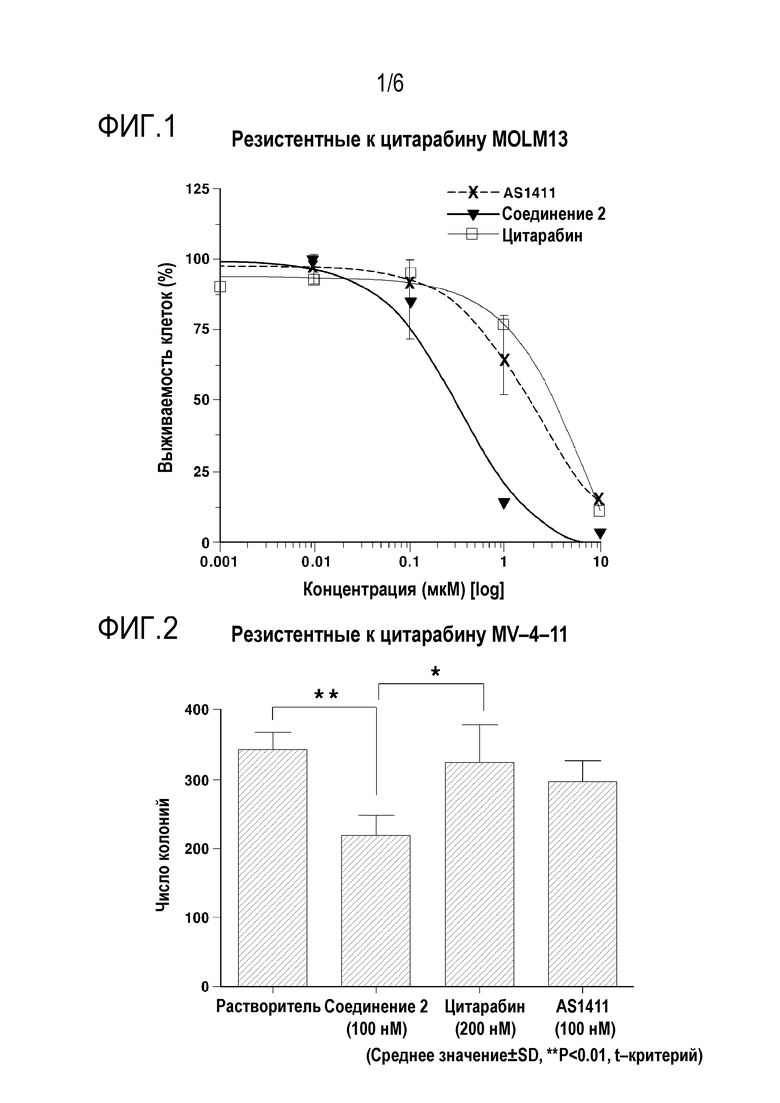
[48] На фиг. 1 представлен график, показывающий цитотоксическое действие олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на клетки AML (резистентные к цитарабину MOLM13) с лекарственной резистентностью к цитарабину (основному терапевтическому агенту при раке крови).
[49] На фиг. 2 представлен график, показывающий антипролиферативное действие олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на раковые клетки крови (резистентные к цитарабину MV-4-11) с лекарственной резистентностью к цитарабину.
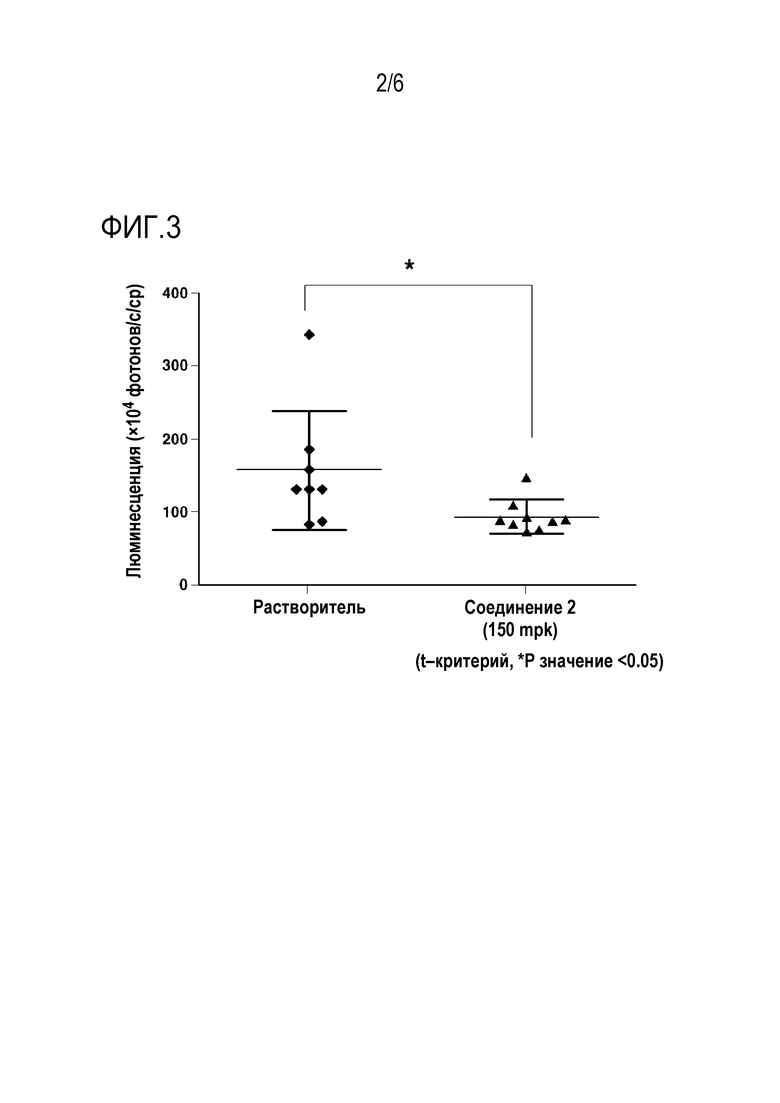
[50] На фиг. 3 представлен график, показывающий цитотоксичность in vivo олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на ксенотрансплантатной модели рака крови (Luc-MOLM13).
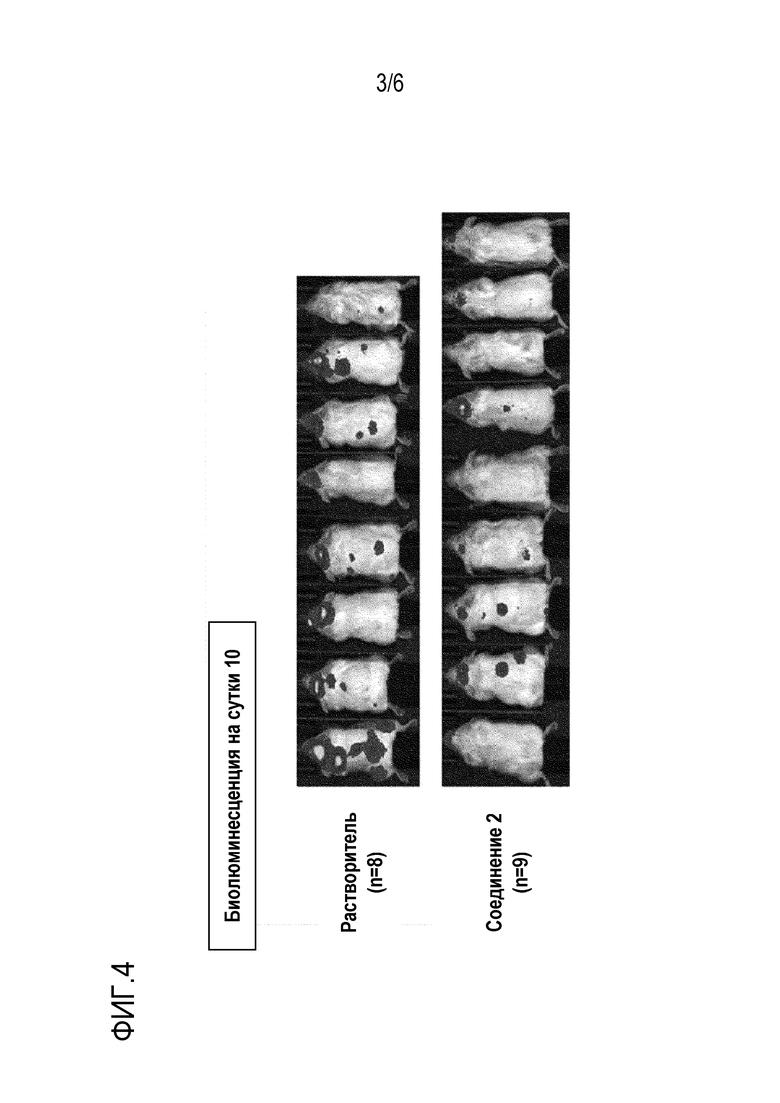
[51] На фиг. 4 представлено изображение, показывающее цитотоксическую эффективность in vivo олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на животной модели рака крови (Luc-MOLM13).
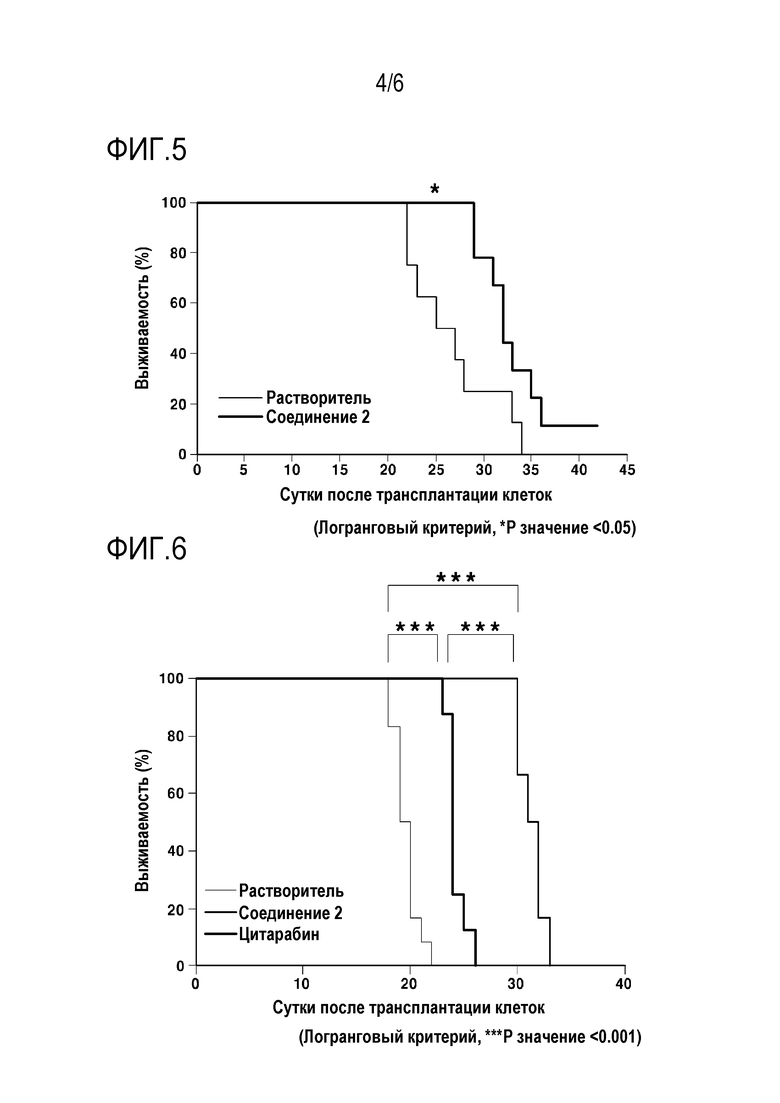
[52] На фиг. 5 представлен график, показывающий антипролиферативную эффективность и выживаемость при использовании олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на животной модели рака крови (Luc-MOLM13).
[53] На фиг. 6 показана противоопухолевая эффективность и выживаемость при использовании олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на сингенной мышиной модели рака крови (C1498).
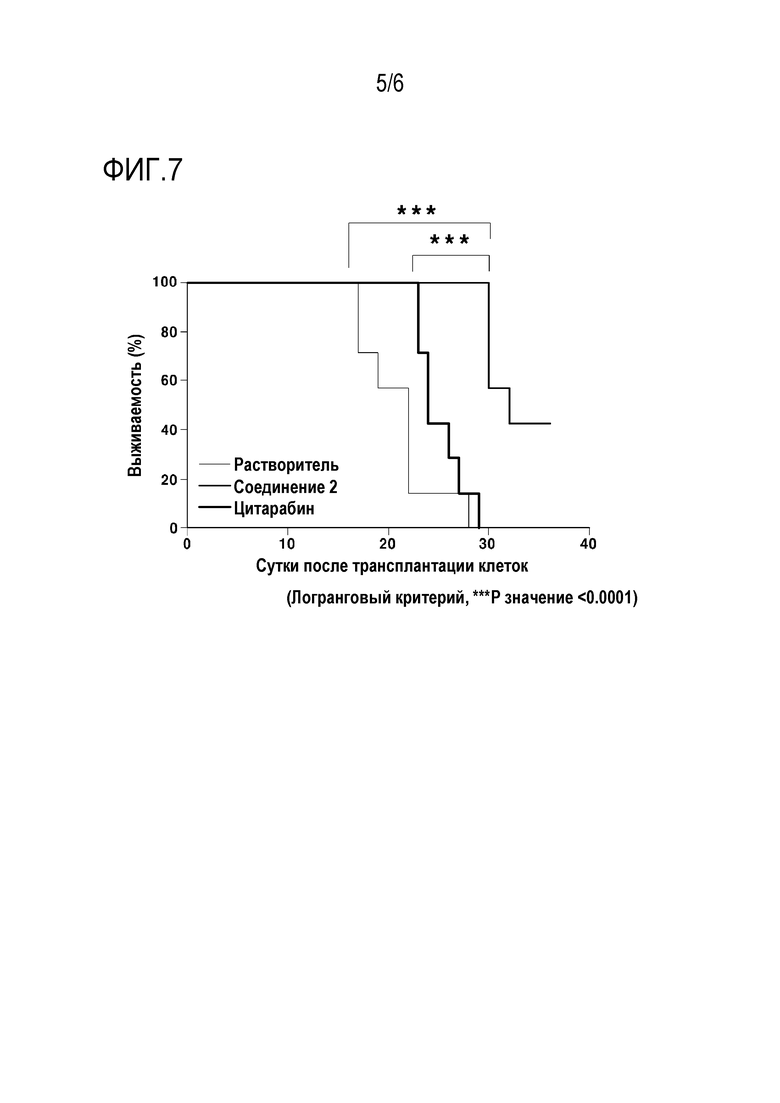
[54] На фиг. 7 показана противоопухолевая эффективность и выживаемость при использовании олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на сингенной мышиной модели рака крови (WEHI-3); и
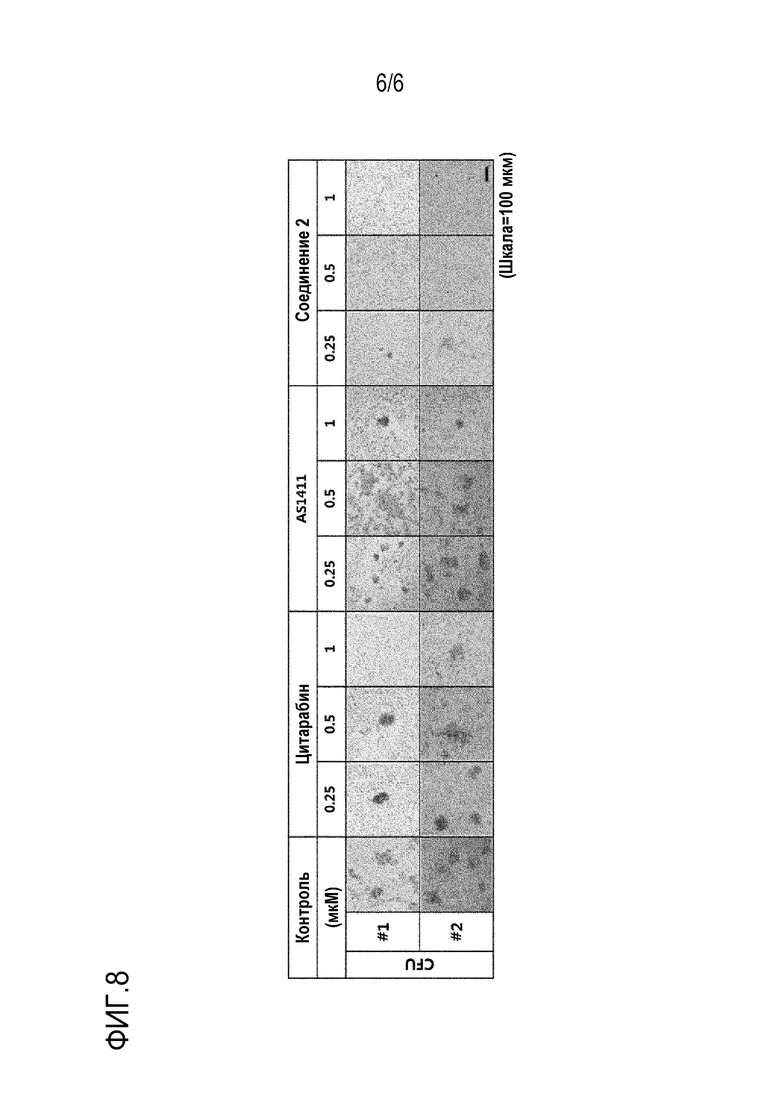
[55] На фиг. 8 показана антипролиферативная эффективность олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, на мононуклеарных клетках костного мозга, полученных от пациентов с рецидивирующим/рефрактерным раком крови.
[56]
Предпочтительные варианты осуществления изобретения
[57] Теперь будет сделана подробная ссылка на предпочтительные варианты осуществления настоящего изобретения, примеры которых иллюстрированы на прилагаемых фигурах.
[58] Следует понимать, что в описании, когда диапазон относится к параметру, то параметр охватывает все цифровые значения, включая конечные точки, раскрытые в пределах диапазона. Например, диапазон от 5 до 10 включает в себя числа 5, 6, 7, 8, 9 и 10, а также произвольные поддиапазоны, такие как диапазоны от 6 до 10, от 7 до 10, от 6 до 9, и от 7 до 9 и любые цифровые значения, такие как 5,5, 6,5, 7,5, 5,5 до 8,5 и от 6,5 до 9, между соответствующими целыми числами, попадающими в диапазон. Кроме того, например, диапазон «от 10% до 30%» включает все целые числа, которые включают целые числа, такие как 10%, 11%, 12% и 13%, а также 30%, и любые поддиапазоны 10% до 15%, от 12% до 18% или от 20% до 30%, а также любые цифровые значения, такие как 10,5%, 15,5% и 25,5%, между соответствующими целыми числами, попадающими в диапазон.
[59] Далее настоящее изобретение будет описано подробно.
[60] В одном аспекте настоящее изобретение относится к олигонуклеотиду, содержащему модифицированную нуклеиновую кислоту, включающему соединение, представленное следующей формулой 1, с образованием G-квадруплекса:
[61] Формула 1
[62]
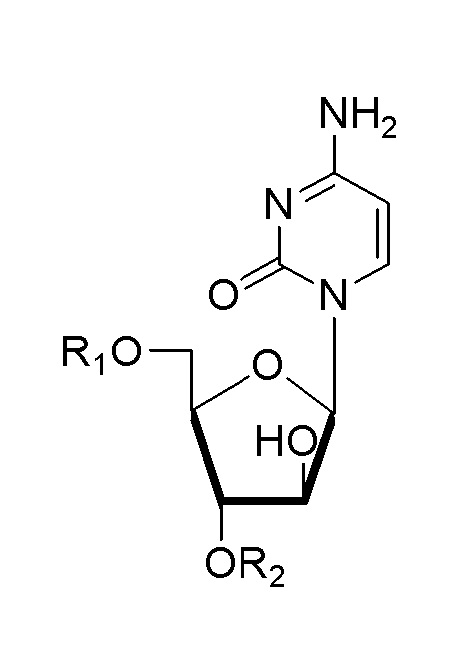
[63] где R1 представляет атом водорода или фосфора фосфатной группы другой нуклеиновой кислоты, и R2 представляет атом водорода или фосфора фосфатной группы другой нуклеиновой кислоты.
[64] В одном аспекте настоящее изобретение относится к олигонуклеотиду, содержащему модифицированную нуклеиновую кислоту, где соединение представлено следующей формулой 2:
[65] Формула 2
[66]
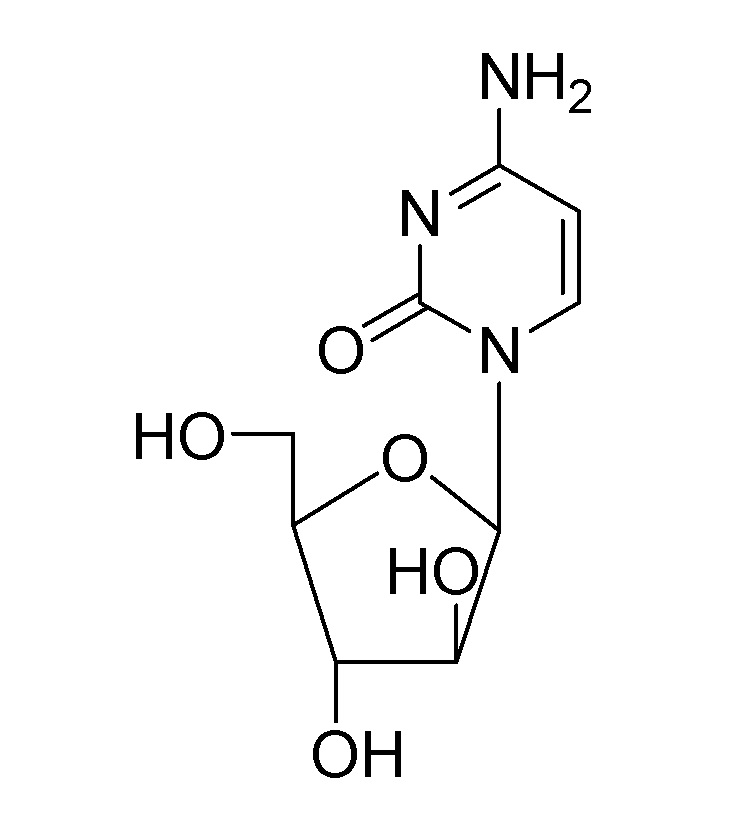
[67] В одном аспекте настоящего изобретения олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, может быть представлен следующей последовательностью:
[68] GaTbNc
[69] где G представляет гуанозин или производное гуанозина, T представляет тимин или производное тимина, N представляет модифицированную нуклеиновую кислоту 1-β-D-арабинофуранозилцитозин или его производное, G, T и N случайным образом распределены посредством пермутации, a представляет целое число, выбранное из 1-30, b представляет целое число, выбранное из 0-30, и c представляет целое число, выбранное из 1-30, при условии, что общее число a, b и c не превышает 60.
[70] В одном аспекте настоящего изобретения олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, может быть представлен следующей последовательностью:
[71] последовательность 1) GGTGGTGGTTNTGGTGGTGG;
[72] последовательность 2) GGTGGTGGTNNTGGTGGTGG;
[73] последовательность 3) NGGTGGTGGTTGTGGTGGTGG; или
[74] последовательность 4) NNGGTGGTGGTTGTGGTGGTGG.
[75] В вышеприведенной последовательности G представляет гуанозин или производное гуанозина, T представляет тимин или производное тимина, и N представляет 1-β-D-арабинофуранозилцитозин в качестве модифицированной нуклеиновой кислоты.
[76] В одном аспекте настоящего изобретения гуанозин или производное гуанозина может включать одно или более соединений, выбранных из 2-дезоксигуанозина, гуанозина, 2'-O-метилгуанозина, 2'-фторгуанозина, LNA (замкнутой нуклеиновой кислоты)гуанозина, D-дезоксигуанозина и D-гуанозина.
[77] В еще одном аспекте настоящее изобретение относится к композиции для профилактики, облегчения течения или лечения рака крови, содержащей, по меньшей мере, один олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, выбранный из описанных выше, или его фармацевтически приемлемую соль в качестве активного ингредиента.
[78] В еще одном аспекте рак крови включает, по меньшей мере, одно из неходжкинской лимфомы, ходжкинской лимфомы, множественной миеломы, лейкоза, лимфомы, миелодиспластического синдрома (MDS), острого лимфобластного лейкоза, острого миелоидного лейкоза, хронического лимфоцитарного лейкоза, хронического миелоидного лейкоза и солитарной миеломы.
[79] Далее варианты осуществления настоящего изобретения будут описаны более подробно.
[80] В одном аспекте настоящее изобретение относится к новому олигонуклеотиду, содержащему модифицированную нуклеиновую кислоту, включающему в качестве модифицированной нуклеиновой кислоты, обладающей терапевтической эффективностью, по меньшей мере, один 1-β-D-арабинофуранозилцитозин, и который является гуанозин-богатым.
[81] В еще одном аспекте настоящее изобретение относится к композиции для профилактики, облегчения течения или лечения рака крови, содержащей олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, или его фармацевтически приемлемую соль в качестве активного ингредиента.
[82] Как здесь используется, термин «G-квадруплекс» относится к олигонуклеотиду, который содержит большое количество одного или более из 2-дезоксигуанозина, гуанозина, 2'-O-метилгуанозина, 2'-фторгуанозина, LNA (замкнутой нуклеиновой кислоты)гуанозина, D-дезоксигуанозина и D-гуанозина, вместе упоминаемые как «гуанозин (G)» [см. фиг. 1] и, следовательно, имеет тетраспиральную структуру, в случае определенной последовательности, на основе хугстиновских водородных связей, образованных четырьмя гуанозинами, расположенными в одной плоскости. Следовательно, его синтезируют так, что в такую структуру вводят модифицированную нуклеиновую кислоту, обладающую терапевтическим эффектом.
[83] Известно, что олигонуклеотиды, которые образуют G-квадруплексную структуру, за счет того, что они являются гуанозин-богатыми, более избирательно связываются с раковыми клетками и ингибируют рост раковых клеток посредством различных механизмов внутри клеток.
[84] Олигонуклеотиды, образующие G-квадруплексы, в которые включена одна или более модифицированных нуклеиновых кислот, переносятся в раковые клетки. Затем G-квадруплекс проявляет эффект ингибирования роста клеток, и модифицированная нуклеиновая кислота, которая проявляет терапевтический эффект при расщеплении нуклеазой, непосредственно ингибирует рост клеток, тем самым синергетически приводя к гибели раковых клеток. Поскольку олигонуклеотиды, образующие G-квадруплекс, обладают только ингибирующей активностью на рост клеток, то когда они используются самостоятельно, уровень гибели клеток не является относительно высоким, и в течение определенного периода времени необходимо длительное лечение. Однако заявители настоящего изобретения установили, что включение модифицированной нуклеиновой кислоты, оказывающей терапевтическое действие на рак крови, непосредственно усиливает эффект гибели клеток, тем самым быстро повышая уровень гибели клеток.
[85] В одном аспекте модифицированная нуклеиновая кислота, обладающая терапевтической эффективностью, может представлять собой 1-β-D-арабинофуранозилцитозин.
[86] В конкретном варианте осуществления производное цитидина, модифицированная нуклеиновая кислота (N), обладающая терапевтической эффективностью, используемая здесь, представляет производное цитидина, представленное следующей формулой 2, где нуклеотид может быть получен в форме фосфорамидита обычным способом [Oligonucleotides and Analogues: A Practical Approach 1991 Fritz Eckstein et al. IRL Press: Oxford], или может быть получен включением в гуанозин-богатый олигонуклеотид, фосфорамидит нуклеотида, полученный от компании Glen Research Corporation, Berry & Associates Inc., Okeanos Technologies, LLC., ChemGenes Corp., Proligo Corp. и т.п. твердофазным синтезом с использованием ДНК-синтезатора в соответствии с общепринятым способом.
[87] Формула 2
[88]
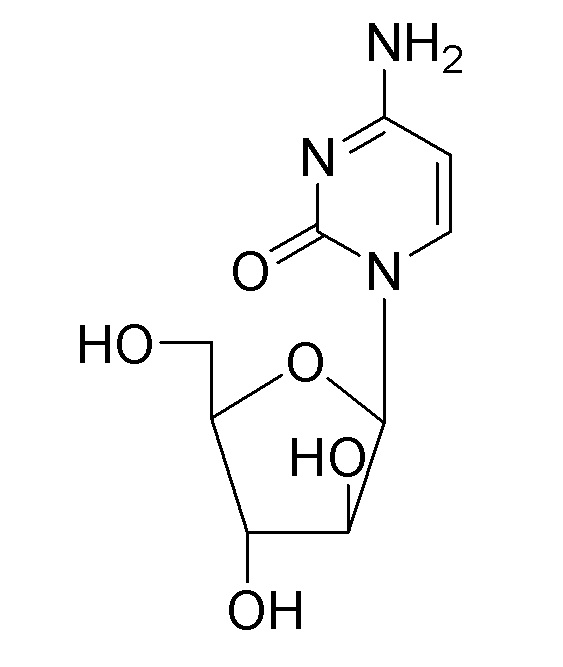
[89] Олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, можно получить обычным способом с использованием модифицированной нуклеиновой кислоты, полученной в форме фосфорамидита, с помощью твердофазного синтезатора.
[90] То есть, модифицированную нуклеиновую кислоту в форме фосфорамидита синтезируют растворением в безводном ацетонитриле и загрузкой в ДНК-синтезатор. Олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, синтезируют с использованием обычных методов синтеза и очистки со ссылкой на указания (руководство), предоставленные Glen Research Corporation и патенты США № 5457187 и 5614505.
[91] Кроме того, типичными последовательностями олигонуклеотидов, содержащих модифицированные нуклеиновые кислоты, которые можно синтезировать с использованием модифицированной нуклеиновой кислоты, как описано выше, являются следующие:
[92] последовательность 1) GGTGGTGGTTNTGGTGGTGG;
[93] последовательность 2) GGTGGTGGTNNTGGTGGTGG;
[94] последовательность 3) NGGTGGTGGTTGTGGTGGTGG; или
[95] последовательность 4) NNGGTGGTGGTTGTGGTGGTGG.
[96] Соединения на основе последовательностей, в которые включены модифицированные нуклеиновые кислоты в правильных положениях, проявляют высокие апоптотические эффекты на раковые клетки крови и резистентные к лекарственным препаратам раковые клетки крови, но не оказывают существенного влияния на нормальные клетки. Результатами экспериментов на животных также было установлено, что соединения на основе указанных последовательностей обладают высокой терапевтической эффективностью при раке крови.
[97] Следовательно, новый нуклеотид с модифицированной нуклеиновой кислотой можно получить введением цитидина в качестве модифицированной нуклеиновой кислоты по настоящему изобретению в последовательность олигонуклеотидов, обладающих биологической активностью, с образованием G-квадруплексов посредством замещения.
[98] Модифицированная нуклеиновая кислота (N), обладающая терапевтической эффективностью, находится в виде соединения, представленного следующей формулой 1, в олигонуклеотиде, содержащем модифицированную нуклеиновую кислоту.
[99] Формула 1
[100]
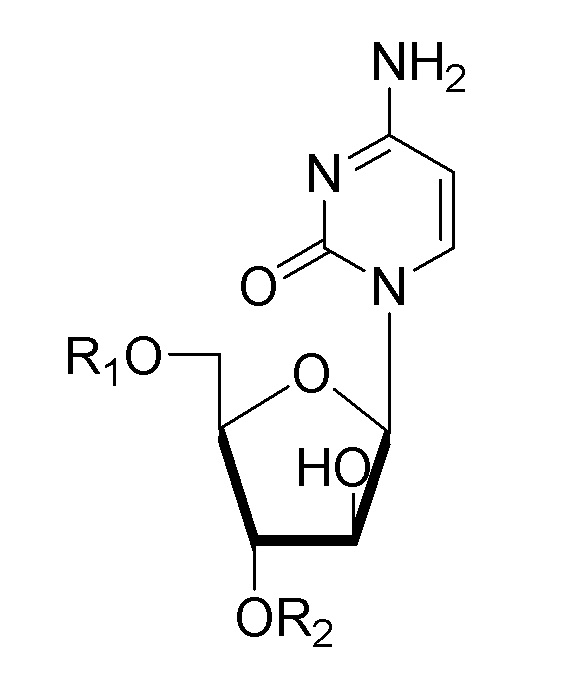
[101] где R1 представляет атом водорода или фосфора фосфатной группы другой нуклеиновой кислоты, и R2 представляет атом водорода или фосфора фосфатной группы другой нуклеиновой кислоты.
[102] В последовательности G представляет гуанозин и предпочтительно включает одно или более, выбранных из 2-дезоксигуанозина, гуанозина, 2'-O-метилгуанозина, 2'-фторгуанозина, LNA (замкнутой нуклеиновой кислоты)гуанозина, D-дезоксигуанозина и D-гуанозина, и N представляет 1-β-D-арабинофуранозилцитозин в качестве модифицированной нуклеиновой кислоты, производного цитидина.
[103] Обычные нуклеозидсодержащие терапевтические агенты, обладающие терапевтическими эффектами, могут проявлять побочные эффекты, такие как системная токсичность и лекарственная резистентность, и многие раковые клетки могут иметь резистентность к таким терапевтическим нуклеозидным противоопухолевым лекарственным препаратам, что может потребовать выбора других лекарственных средств. Когда нуклеозид, обладающий такими терапевтическими эффектами, включается в олигонуклеотиды G-квадруплекса, которые являются относительно более селективными для раковых клеток, то воздействие на нормальные клетки in vivo может быть минимизировано, и уровни гибели (апоптоза) даже резистентных к лекарственным препаратам злокачественных клеток опухолей могут возрастать.
[104] Данная G–-квадруплексная структура является более стабильной, когда присутствуют ионы калия (K+), и, таким образом, имеет стабильную структуру в течение длительного периода времени в общих физиологических условиях, таких как имеют место в крови. Следовательно, в настоящем изобретении олигонуклеотид G-квадруплекса, содержащий модифицированную нуклеиновую кислоту, обладающую терапевтическим эффектом, стабилизируют с использованием раствора KCl с определенной концентрацией (от 30 до 70 мМ) или тому подобное перед применением.
[105] Новый олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, по настоящему изобретению демонстрирует значительно улучшенные апоптотические эффекты для раковых клеток крови и резистентных к лекарственным препаратам раковых клеток крови по сравнению с обычными терапевтическими агентами, содержащими нуклеозиды, обладающие терапевтическим эффектом, и проявляют высокую противоопухолевую терапевтическую эффективность при оценке противоопухолевой эффективности с использованием животных моделей.
[106] Следовательно, настоящее изобретение обеспечивает композицию для профилактики, облегчения течения или лечения рака, содержащую олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, или его фармацевтически приемлемую соль в качестве активного ингредиента. Фармакологически приемлемые соли включают, например, соли металлов, соли органических оснований, соли неорганических кислот, соли органических кислот, соли основных или кислотных аминокислот и тому подобное. Подходящие соли металлов включают соли щелочных металлов, такие как соли натрия и соли калия; соли щелочноземельных металлов, такие как соли кальция, соли магния и соли бария; и соли алюминия и тому подобное. Подходящие примеры солей органических оснований включают соли триметиламина, триэтиламина, пиридина, пиколина, 2,6-лутидина, этаноламина, диэтаноламина, триэтаноламина, циклогексиламина, дициклогексиламина, N, N-дибензилэтилендиамина и тому подобное. Подходящие примеры солей неорганических кислот включают соли хлористоводородной кислоты, бромистоводородной кислоты, азотной кислоты, серной кислоты, фосфорной кислоты и тому подобное. Подходящие примеры солей органических кислот включают соли муравьиной кислоты, уксусной кислоты, трифторуксусной кислоты, фталевой кислоты, фумаровой кислоты, щавелевой кислоты, винной кислоты, малеиновой кислоты, лимонной кислоты, янтарной кислоты, метансульфоновой кислоты, бензолсульфоновой кислоты, п-толуолсульфоновой кислоты и тому подобное.
[107] Подходящие примеры солей основных аминокислот включают соли аргинина, лизина, орнитина и тому подобное. Подходящие примеры солей кислых аминокислот включают соли аспарагиновой кислоты, глутаминовой кислоты и тому подобное. Особенно предпочтительные соли включают, когда соединение имеет кислотную функциональную группу, неорганические соли, такие как соли щелочных металлов (например, соли натрия и соли калия) и соли щелочноземельных металлов (например, соли кальция, соли магния и соли бария) и органические соли, такие как соли аммония. Когда соединение имеет основную функциональную группу, то особенно предпочтительные соли включают соли неорганических кислот, такие как хлористоводородная кислота, бромистоводородная кислота, азотная кислота, серная кислота и фосфорная кислота, и соли органических кислот, такие как уксусная кислота, фталевая кислота, фумаровая кислота щавелевая кислота, винная кислота, малеиновая кислота, лимонная кислота, янтарная кислота, метансульфоновая кислота и п-толуолсульфоновая кислота.
[108] Композиция для профилактики, облегчения течения или лечения рака, содержащая олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, по настоящему изобретению, может содержать фармацевтически приемлемый носитель в дополнение к активному ингредиенту. В случае инъекционного раствора фармацевтически приемлемый носитель может представлять собой смесь консерванта, изотонического агента, анестезирующего агента, солюбилизирующего агента, буфера, стабилизирующего агента или тому подобное. Для перорального введения фармацевтически приемлемый носитель может представлять собой солюбилизирующий агент, связующее вещество, эксципиент, диспергирующий агент, стабилизирующий агент, суспендирующий агент, краситель, дезинтегрирующий агент, смазывающее вещество, ароматизатор или тому подобное. Для местного применения фармацевтически приемлемый носитель может представлять собой основу, эксципиент, смазывающее вещество, консервант или тому подобное.
[109] Формуляцию композиции по настоящему изобретению можно проводить по-разному в виде смеси с фармацевтически приемлемым носителем. Кроме того, композицию можно приготовить в виде ампулы с разовой лекарственной формой или множеством разовых лекарственных форм для инъекций и в форме таблетки, эликсира, капсулы, суспензии, пастилки, облатки, сиропа или тому подобное для перорального введения, и может быть формулирована в виде таблетки, пилюли, капсулы, препарата с замедленным высвобождением или тому подобное.
[110] Между тем, примеры подходящих носителей, эксципиентов и разбавителей для формуляции включают микрокристаллическую целлюлозу, ксилит, эритрит, метилцеллюлозу, поливинилпирролидон, крахмал, гуммиарабик, альгинат, желатин, лактозу, декстрозу, сахарозу, пропилгидроксибензоат, целлюлозу, воду, метилгидроксибензоат, воду, стеарат магния, тальк, сорбит, маннит, мальтит, фосфат кальция, силикат кальция, минеральное масло или тому подобное.
[111] Как здесь используется, термин «введение» означает введение определенного соединения пациенту любым подходящим способом. Путь введения активного ингредиента может представлять любой общий путь, позволяющий доставлять лекарственное средство к ткани-мишени. Примеры пути введения включают, не ограничиваясь этим, внутривенное, подкожное, пероральное, внутримышечное, внутрибрюшинное, интрапульмональное, ректальное, местное, интраназальное и внутрикожное введение. Однако поскольку олигонуклеотиды расщепляются при пероральном введении, то композицию для перорального введения необходимо готовить таким образом, чтобы она могла распадаться и всасываться в желудочно-кишечном тракте. Предпочтительно ее можно вводить инъекцией или интраназальным путем.
[112] Содержание активного ингредиента в препарате по настоящему изобретению может быть соответствующим образом выбрано в зависимости от всасываемости активного ингредиента в организме, степени инактивации, степени экскреции, возраста, пола и состояния потребителя и тому подобное. Доза активного ингредиента по настоящему изобретению может составлять от 1 до 1000 мг/кг, предпочтительно от 3 до 100 мг/кг, и ее можно вводить постоянно 1-3 раза в сутки или путем инфузии в течение заранее определенного периода времени.
[113]
Способ осуществления изобретения
[114] Далее настоящее изобретение будет подробно описано со ссылкой на следующие примеры, и оно не ограничивается ими.
[115]
[116] Пример 1: синтез нового олигонуклеотида, содержащего модифицированную нуклеиновую кислоту
[117] Синтез ДНК проводили в объеме 1 мкмоль с использованием обычного твердофазного ДНК-синтезатора. В отношении фосфорамидитов, используемых для синтеза, то фосфорамидиты дезоксигуанозин, тимидин и 1-β-D-арабинофуранозилцитозин получали от компании Glen Research Corporation, которые растворяли в концентрации 0,067 М в сухом ацетонитриле и загружали в твердофазный ДНК-синтезатор производства Polygene Inc. Реакция протекает в направлении 3'→5', и 3'-гидроксильная группа первого нуклеотида присоединяется к смоле. При добавлении каждого основания повторяли четырехстадийные химические реакции, включающие детритилирование 5'-конца, связывание нового основания, кэпирование несвязанной цепи ДНК и окисление фосфатной группы. После завершения реакции защитную группу удаляли и смолу с синтезированным CPG погружали в водный раствор аммиака и выдерживали при 55°С в течение 5 ч. Затем водный раствор аммиака выпаривали с получением белого порошка. Очистку проводили путем увеличения 1М раствора NaCl до 5-70% в системе ВЭЖХ с использованием колонки для анионообменной ВЭЖХ Waters. Собирали основные пики, добавляли 100% этанол и олигонуклеотиды осаждали и затем высушивали. В результате с использованием ВЭЖХ получали олигонуклеотиды, имеющие чистоту 85% или выше, и измеряли молекулярные массы с использованием ESI-LC-MS (Q-TRAP 2000 ESI-MS), для определения того, был ли синтез успешным.
[118] Олигонуклеотиды, содержащие модифицированные нуклеиновые кислоты, можно получить таким же способом, как описано выше для олигонуклеотидных последовательностей, о которых уже сообщалось в целях терапевтического лечения, или различных последовательностей, которые проявляют физиологическую активность при образовании G-квадруплексов в дополнение к последовательностям, приведенным в следующей таблице 1.
[119]
[120]
[121] Пример 2: приготовление раствора нового одигонуклеотида, содержащего модифицированную нуклеиновую кислоту
[122] Каждый олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, разбавляли 10 мМ раствором Трис-HCl (рН 7,4) до конечной концентрации 100 мкМ. Разбавленный раствор выдерживали при 94°С в течение 5 мин, и затем пробирку помещали на лед. К полученному раствору добавляли 2М раствор KCl, так что конечная концентрация раствора KCl становилась равной 50 мМ, выдерживали при 60°С в течение 3 ч и медленно охлаждали до комнатной температуры. Каждый олигонуклеотид разбавляли 10 мМ раствором Трис-HCl (рН 7,4) до концентрации 10 мкМ и выдерживали при 94°С в течение 5 мин, и пробирку помещали на лед. К полученному раствору добавляли 2М раствор KCl, так что конечная концентрация раствора KCl становилась равной 50 мМ, и выдерживали при 60°С в течение 3 ч, и затем медленно охлаждали до комнатной температуры, затем данный раствор использовали для настоящего примера.
[123]
[124] Экспериментальный пример 1: цитотоксическая эффективность на раковых клетках крови и на резистентных к лекарственным препаратам раковых клетках крови in vivo
[125] За день до постановки эксперимента 190 мкл культуральной среды (с титром от 104 до 105 клеток/мл), содержащей раковые клетки крови, такие как клеточные линии HL60, MV-4-11, CCRF-CEM, MOLT-4 и MOLM-13, и резистентные к лекарственным препаратам раковые клетки крови, такие как клеточные линии резистентные к азацитидину (AZA-1) MOLM13, резистентные к децитабину (Dec-5) MOLM13, и резистентные к цитарабину (AraC-1) MOLM13, и нормальные клетки, такие как клетки WI38, CCD-18co и Fa2N4 высевали в 96-луночный планшет. На следующий день добавляли 10 мкл раствора олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, приготовленного в примере 2, и затем культивировали в течение 5 дней.
[126] Через пять дней после обработки препаратом проводили МТТ-тест для оценки цитотоксичности для клеточных линий [см. JBC 1999, 26369].
[127] Результаты оценки цитотоксичности новых олигонуклеотидов, содержащих модифицированные нуклеиновые кислоты, по настоящему изобретению, показали, как следует из таблицы 2 со значениями IC50 новых олигонуклеотидов, содержащих модифицированные нуклеиновые кислоты, т. е. соединений 1, 2, 3 и 4 по настоящему изобретению, что они проявляли высокое цитотоксическое действие на различных клеточных линиях рака крови [таблица 2].
[128] Кроме того, можно видеть, что новые олигонуклеотиды, содержащие модифицированные нуклеиновые кислоты, по настоящему изобретению проявляют высокое цитотоксическое действие также на различных резистентных к лекарственным препаратам раковых клетках крови [таблица 3].
[129] Кроме того, можно видеть, что новые олигонуклеотиды, содержащие модифицированные нуклеиновые кислоты, по настоящему изобретению проявляют высокое цитотоксическое действие на различных раковых клетках крови, а также на различных резистентных к лекарственным препаратам раковых клетках крови, в то время как они почти не влияют на нормальные клетки [таблица 4].
[130] Результаты оценки цитотоксических эффектов приведены в таблицах 2-4 ниже. Кроме того, установлены цитотоксические эффекты олигонуклеотидов, содержащих модифицированные нуклеиновые кислоты, по настоящему изобретению, на резистентные к лекарственным препаратам раковые клетки крови, и результаты показаны на фиг. 1 и 2.
[131]
[132]
[133] Таблица 2 относится к цитотоксическим эффектам на раковых клетках крови.
[134]
[135]
HL-60
MV-4-11
MOLM13
MOLM13
[136] Таблица 3 относится к цитотоксическим эффектам на резистентных к лекарственным препаратам раковых клетках крови.
[137]
[138]
[139] Таблица 4 относится к цитотоксическим эффектам на нормальных клетках.
[140]
[141] Экспериментальный пример 2: противоопухолевая эффективность на ксенотрансплантатной мышиной модели раковых клеток крови человека (Lu-MOLM13) in vivo
[142] Для оценки эффективности на человеческих раковых клетках крови на животной модели, у мышей NOD-SCID индуцировали рак крови для оценки противоопухолевой эффективности in vivo.
[143] Сначала индукцию рака крови проводили конкретно следующим образом. Экспериментальные группы состояли из группы с введением растворителя (8 мышей) и группы с введением лекарственного препарата (9 мышей).
[144] Клетки Luc-MOML-13 (человеческие клеточные линии MDS/AML) вводили внутривенно из расчета 107 (клеток/мышь) 8-недельным мышам NOD-SCID. Соединение 2, которое использовали в качестве лекарственного препарата для введения, растворяли в калийном буфере в концентрации 2 мМ, и раствор выдерживали при 94°С в течение 5 мин и медленно охлаждали до комнатной температуры в течение 3 ч, затем данный раствор использовали для настоящего примера.
[145] Препарат вводили внутривенно (150 мг/кг) ежедневно в течение двух недель, пять раз в неделю, начиная со второго дня после инокуляции клеток, и оценивали выживаемость животных. Результаты показаны на фиг. 5. Кроме того, через 10 дней после начала введения лекарственного препарата цитотоксический эффект для раковых клеток крови сравнивали с таковым в группе с введением растворителя с помощью биомедицинской визуализации, и результаты приведены на фиг. 3 и 4.
[146] Как видно из фиг. 3 и 4, число раковых клеток крови в группе с введением лекарственного препарата было достоверно ниже по сравнению с группой с введением растворителя.
[147] Как видно из фиг. 5, выживаемость в группе с введением лекарственного препарата была достоверно выше по сравнению с группой с введением растворителя.
[148]
[149] Экспериментальный пример 3: противоопухолевая эффективность на сингенной мышиной модели AML (C1498) in vivo
[150] Для оценки эффективности in vivo на раковые клетки крови с участием иммунной системы, определяли выживаемость мышей после прививки раковых клеток крови, полученных от мышей (C1498), на мышах C57BL/6.
[151] Индукцию рака крови проводили конкретно следующим образом. Экспериментальные группы состояли из группы с введением растворителя (8 мышей), группы с введением лекарственного препарата (9 мышей) и контрольной группы (8 мышей). Соединение 2, которое использовали в качестве лекарственного препарата, вводили в дозе 300 мг/кг, и цитарабин вводили мышам, которых использовали в качестве положительного контроля, в дозе 30 мг/кг (цитарабин в том же объеме, что и соединение 2 в дозе 300 мг/кг).
[152] Клетки C1498 (мышиная клеточная линия AML) инъецировали внутривенно из расчета 5×105 (клеток/мышь) 8-недельным мышам C57BL/6. Соединение 2, которое использовали в качестве лекарственного препарата для введения, растворяли в калийном буфере в концентрации 2 мМ, и раствор выдерживали при 4°С в течение 6 ч.
[153] Препарат вводили подкожно два раза в день в течение двух недель, начиная со второго дня после инокуляции клеток, и определяли выживаемость. Результаты показаны на фиг. 6.
[154] Как видно на фиг. 6, выживаемость в группе с введением препарата была достоверно выше по сравнению с группой с введением растворителя, и выживаемость в группе с введением лекарственного препарата была намного выше, чем в группе положительного контроля.
[155]
[156] Экспериментальный пример 4: противоопухолевая эффективность на сингенной мышиной модели AML (WEHI-3) in vivo
[157] Для оценки эффективности in vivo на клетках AML с участием иммунной системы, оценивали жизнеспособность мышей посредством трансплантации раковых мышиных клеток крови (WEHI-3) мышам Balb/c.
[158] Индукцию рака крови проводили конкретно следующим образом. Экспериментальные группы состояли из группы с введением растворителя (7 мышей), группы с введением лекарственного препарата (7 мышей) и контрольной группы (7 мышей). Соединение 2, которое использовали в качестве лекарственного препарата, вводили в дозе 300 мг/кг, и цитарабин вводили мышам, которых использовали в качестве положительного контроля, в дозе 30 мг/кг (цитарабин в том же объеме, что и соединение 2 в дозе 300 мг/кг).
[159] Клетки WEHI (мышиная клеточная линия AML) инъецировали внутривенно из расчета 5×105 (клеток/мышь) 8-недельным мышам C57BL/6. Соединение 2, которое использовали в качестве лекарственного препарата для введения, растворяли в калийном буфере в концентрации 2 мМ, и раствор выдерживали при 4°С в течение 6 ч.
[160] Препарат вводили подкожно два раза в день в течение двух недель, начиная со второго дня после инокуляции клеток, и определяли выживаемость. Результаты показаны на фиг. 7.
[161] Как видно на фиг. 7, выживаемость в группе с введением лекарственного препарата была достоверно выше по сравнению с группой с введением растворителя, и выживаемость в группе с введением лекарственного препарата была намного выше, чем в группе положительного контроля.
[162]
[163] Экспериментальный пример 5: противоопухолевая эффективность на мононуклеарных клетках костного мозга, полученных от пациентов с рецидивирующим/рефрактерным острым миелоидным лейкозом
[164] Для оценки противоопухолевой эффективности на реальных клетках пациентов с раком крови, мононуклеарные клетки костного мозга, полученные от пациентов с рецидивирующим/рефрактерным (О/Р) острым миелоидным лейкозом, использовали для образования колоний для сравнительной оценки соединения 2 и цитарабина (AS1411), соответственно. Клетки были предоставлены после одобрения IRB в медицинском центре Asan в Сеуле. Мононуклеарные клетки костного мозга высевали на колониеобразующую среду и затем обрабатывали 0,25 мкМ; 0,5 мкМ и 1 мкМ каждого препарата и культивировали в течение 16 дней, и подсчитывали количество колоний.
[165] Как видно из фиг. 8, препарат, представляющий положительный контроль, в той же концентрации оказывал недостаточное терапевтическое действие на клетки рецидивирующего/рефрактерного рака крови, тогда как соединение 2 обладало достоверно более высоким противоопухолевым эффектом.
[166]
[167] Экспериментальный пример 6: оценка токсичности
[168] Оценку токсичности активных ингредиентов по настоящему изобретению проводили следующим образом.
[169] Соединение 2 растворяли в калийном буфере, и раствор инъецировали мышам в дозе 1 г/кг (10 мышей на группу) и затем наблюдали за животными в течение 7 дней. В результате ни одна мышь не пала, означая, что среднелетальная доза (LD50) составляла, по меньшей мере, 1 г/кг.
[170] Кроме того, когда лекарственный препарат вводили нормальным мышам, у которых не было рака крови, в тех же условиях, что и в экспериментальном примере 4, то количество нормальных лейкоцитов быстро снижалось в контрольной группе, тогда как в группе с введением лекарственного препарата, у мышей которым вводили соединение 2, сохранялся относительно высокий уровень лейкоцитов в крови (среднее значение для группы с растворителем: 6,29, диапазон значений в группе с растворителем: 4,70-8,97, среднее значение для группы с введением лекарственного препарата: 4,07, диапазон значений в группе с введением лекарственного препарата: 3,36-4,77, среднее значение для контрольной группы: 2,34, диапазон значений в контрольной группе: 0,95-4,31), что демонстрирует высокую безопасность препарата. Таким образом, результаты экспериментальных примеров 3-5 показали, что соединение 2 специфически индуцирует гибель раковых клеток крови и сводит к минимуму гибель нормальных клеток крови, демонстрируя тем самым отличные характеристики для его применения в качестве терапевтического средства против рака крови.
[171]
[172] Пример получения 1: приготовление инъекционного раствора
[173] Инъекционный раствор, содержащий 10 мг соединения 2, готовили следующим способом.
[174] 1 г соединения 2, 0,6 г хлорида натрия и 0,1 г аскорбиновой кислоты растворяли в дистиллированной воде для приготовления 100 мл раствора. Колбу заполняли раствором и стерилизовали нагреванием при 20°С в течение 30 мин.
[175] Ингредиенты для инъекционного раствора являются следующими:
[176] 1 г активного ингредиента
[177] 0,6 г хлорида натрия
[178] 0,1 г аскорбиновой кислоты
[179] Соответствующее количество дистиллированной воды
[180]
[181] Несмотря на то, что предпочтительные варианты осуществления настоящего изобретения были раскрыты для иллюстративных целей, специалистам в данной области техники должно быть понятно, что возможны различные модификации, дополнения и замены, не отступая от объема и сущности изобретения, которые раскрыты в прилагаемой формуле изобретения.
Свободный текст перечня последовательностей
[182] Последовательность 1) GGTGGTGGTTNTGGTGGTGG
[183] Последовательность 2) GGTGGTGGTNNTGGTGGTGG
[184] Последовательность 3) NGGTGGTGGTTGTGGTGGTGG
[185] Последовательность 4) NNGGTGGTGGTTGTGGTGGTGG
--->
Список последовательностей
<110> Aptabio Therapeutics Ltd.
<120> Терапевтический агент для лечения рака крови
<130> PCT-2018-0544
<160> 4
<170> KoPatentIn 3.0
<210> 1
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> модифицированный олигонуклеотид
<400> 1
ggtggtggtt ntggtggtgg 20
<210> 2
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> модифицированный олигонуклеотид
<400> 2
ggtggtggtn ntggtggtgg 20
<210> 3
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> модифицированный олигонуклеотид
<400> 3
nggtggtggt tgtggtggtg g 21
<210> 4
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> модифицированный олигонуклеотид
<400> 4
nnggtggtgg ttgtggtggt gg 22
<---
Изобретение относится к области биотехнологии. Описана группа изобретений, включающая олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, для профилактики, облегчения течения или лечения рака крови с образованием структуры G-квадруплекса, композицию для профилактики, облегчения течения или лечения рака крови, содержащую эффективное количество вышеуказанного олигонуклеотида, композицию для профилактики, облегчения течения или лечения рака крови, резистентного по меньшей мере к одному из цитарабина, децитабина и азацитидина, в качестве ингибиторов ДНК-синтетазы или ДНК-метилтрансферазы, композицию для профилактики, облегчения течения или лечения острого миелоидного лейкоза, имеющую эффекты индукции апоптоза на мононуклеарных клетках костного мозга, полученных от пациентов с рецидивирующим/трудно поддающимся лечению острым миелоидным лейкозом, и композицию для облегчения течения или лечения рака крови, имеющую более высокие эффекты индукции апоптоза в раковых клетках, чем в нормальных клетках. Изобретение расширяет арсенал средств для профилактики, облегчения течения или лечения рака крови. 5 н. и 2 з.п. ф-лы, 8 ил., 4 табл., 9 пр.
1. Олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, для профилактики, облегчения течения или лечения рака крови с образованием структуры G–квадруплекса,
где олигонуклеотид, содержащий модифицированную нуклеиновую кислоту, представлен следующей последовательностью:
последовательность 1) GGTGGTGGTTNTGGTGGTGG;
последовательность 2) GGTGGTGGTNNTGGTGGTGG;
последовательность 3) NGGTGGTGGTTGTGGTGGTGG; или
последовательность 4) NNGGTGGTGGTTGTGGTGGTGG;
где G представляет гуанозин или производное гуанозина;
T представляет тимин или производное тимина; и
N представляет 1–β–D–арабинофуранозилцитозин в качестве модифицированной нуклеиновой кислоты;
где модифицированная нуклеиновая кислота включена в олигонуклеотид для непосредственного ингибирования роста раковых клеток крови при расщеплении нуклеазой.
2. Олигонуклеотид, содержащий модифицированную нуклеиновую кислоту по п.1, где гуанозин или производное гуанозина включает одно или более выбранных из 2–дезоксигуанозина, гуанозина, 2'–O–метилгуанозина, 2'–фторгуанозина, LNA (закрытой нуклеиновой кислоты)гуанозина, D–дезоксигуанозина и D–гуанозина.
3. Композиция для профилактики, облегчения течения или лечения рака крови, содержащая эффективное количество олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, по любому из пп.1, 2 или его фармацевтически приемлемой соли в качестве активного ингредиента, и фармацевтически приемлемый носитель.
4. Композиция для профилактики, облегчения течения или лечения рака крови по п.3, где рак крови включает по меньшей мере одно из неходжкинской лимфомы, ходжкинской лимфомы, множественной миеломы, лейкоза, лимфомы, миелодиспластического синдрома (MDS), острого лимфобластного лейкоза, острого миелоидного лейкоза, хронического лимфоцитарного лейкоза, хронического миелоидного лейкоза и солитарной миеломы.
5. Композиция для профилактики, облегчения течения или лечения рака крови, резистентного по меньшей мере к одному из цитарабина, децитабина и азацитидина, в качестве ингибиторов ДНК–синтетазы или ДНК–метилтрансферазы, содержащая эффективное количество олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, по любому из пп.1, 2 или его фармацевтически приемлемой соли в качестве активного ингредиента, и фармацевтически приемлемый носитель.
6. Композиция для профилактики, облегчения течения или лечения острого миелоидного лейкоза, имеющая эффекты индукции апоптоза на мононуклеарных клетках костного мозга, полученных от пациентов с рецидивирующим/трудно поддающимся лечению острым миелоидным лейкозом, содержащая эффективное количество олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, по любому из пп.1, 2 или его фармацевтически приемлемой соли в качестве активного ингредиента, и фармацевтически приемлемый носитель.
7. Композиция для облегчения течения или лечения рака крови, имеющая более высокие эффекты индукции апоптоза в раковых клетках, чем в нормальных клетках, содержащая эффективное количество олигонуклеотида, содержащего модифицированную нуклеиновую кислоту, по любому из пп.1, 2 или его фармацевтически приемлемой соли в качестве активного ингредиента, и фармацевтически приемлемый носитель.
| WO 2011002200 A2, 06.01.2011 | |||
| НОВЫЙ ПИРИМИДИНОВЫЙ НУКЛЕОЗИД ИЛИ ЕГО СОЛЬ | 2006 |
|
RU2395517C2 |
| Kurz, M., Göbel, K., Hartel, C., & Göbel, M | |||
| W | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
| Acridine-Labeled Primers as Tools for the Study of Nonenzymatic RNA Oligomerization | |||
| Helvetica Chimica Acta, 81(5-8), 1156-1180 | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
Авторы
Даты
2021-07-12—Публикация
2018-11-30—Подача