Изобретение относится к области медицины, в частности, к области разработки терапевтических и косметических композиций и их применения для доставки неорганических частиц, конкретно, наночастиц диоксида церия, через кожу.
Наночастицы диоксида церия - перспективный материал для биомедицинского применения. Вследствие высокой кислородной нестехиометрии наночастицы CeO2 существенно влияют на протекание редокс-процессов в живой клетке, что позволяет регулировать условия окислительного стресса, вызываемого активными формами кислорода; при этом низкая токсичность обеспечивает сравнительную безопасность применения нанодисперсного диоксида церия in vivo. К специфическим свойствам наночастиц CeO2 следует отнести также способность к регенерации кислородной нестехиометрии, которая выражается в том, что после участия в окислительно-восстановительном процессе за сравнительно небольшой промежуток времени наночастицы CeO2 способны возвращаться к исходному состоянию, что обеспечивает их пролонгированное действие in situ [Щербаков А.Б., Иванов В.К., Жолобак Н.М., и др. Нанокристаллический диоксид церия - перспективный материал для биомедицинского применения // Биофизика. 2011, 56(6), 995-101].
Наночастицы диоксида церия способны защищать клетки кожи от окислительного стресса, вызванного действием неблагоприятных факторов - активных форм кислорода и химических токсинов, в случае термических и механических ран или солнечных ожогов. Показана эффективность применения наночастиц CeO2 при терапии ряда заболеваний - в том числе трофических язв у больных сахарным диабетом [Mohammad G., Pandey Н.P., Tripathib K. Diabetic wound healing and its angiogenesis with special reference to nanoparticles // Journal of Nanomaterials and Biostructure. 2008, 3, 203-208]; запатентована композиция для лечения диабетических и других кожных ран, содержащая наночастицы диоксида церия [US 20130195927]. В последнее время рассматривается возможность терапии с помощью наночастиц диоксида церия некоторых онкологических заболеваний [US 20130337070]. При этом вопрос доставки наночастиц диоксида церия через кожный барьер в зону терапевтического действия остается одним из наиболее актуальных.
Основные пути проникновения вещества в организм через кожу - трансэпидермальный, трансгландулярный и трансфолликулярный. Два последних способа используются преимущественно для транспорта липосомальных (высокомолекулярных) и заряженных частиц. При трансэпидермальном пути возможен транспорт как через клетки эпидермиса, так и между ними. При этом направленное движение вещества осуществляется за счет пассивной диффузии, т.е. в переносе из области с большей концентрацией в область с меньшей концентрацией. Несмотря на сложность создания трансэпидермальных форм, количество лекарственных субстанций, доставляемых путем диффузии через кожу, постоянно растет. Для улучшения доставки фармацевтических и косметических препаратов через кожу широко используют физические и химические методы. Из физических наиболее распространенными являются электропорация, ионо- и сонофорез, локальная термообработка и термодиффузия, а также механическое нарушение целостности дермы - перфорация или использование аппликаторов или валиков с микроиголками. Из химических наиболее распространено использование специфических растворителей-пенетраторов, среди которых известны спирты (этанол, пентанол, бензиловый спирт, лауриловый спирт, пропиленгликоль, глицерин), монотерпены (D-лимонен, карвон и анисовое масло), сульфоксиды (диметилсульфоксид), фосфолипиды (лецитин), жирные кислоты (олеиновая кислота, линолевая кислота, валериановая кислота и лауриновая кислота) и их эфиры, амины (диэтаноламин и триэтаноламин), амиды (мочевины, диметилацетамид, диметилформамид и производные пирролидона), углеводороды (алканы и сквалены) и поверхностно-активные вещества (лауреат натрия, цетилтриметиламмонийбромид, оксиэтилированные жирные спирты или кислоты, холат натрия) и пр. [Ahad A., Aqil М., Kohli K., et al. Chemical penetration enhancers: a patent review // Expert OpinTher Pat. 2009, 19(7), 969-988; Subedi R.K., Oh S.Y., Chun M.K., Choi H.K. Recent advances in transdermal drug delivery // Arch Pharm Res. 2010, 33(3), 339-351]. В медицинских композициях для доставки лекарственных препаратов через stratum corneum и в глубокие слои кожи наиболее широко используют диметилсульфоксид (ДМСО), однако, для доставки наночастиц его применение практически не описано. Данный факт связан еще и с тем, что до недавнего времени вопрос доставки наночастиц через кожу вообще не рассматривался.
В патенте [US 8715736] в качестве наноразмерного носителя через stratum corneum предложено использовать твердые липидные наночастицы. С целью доставки лекарственных препаратов, в том числе и трансдермальной, перспективны наночастицы полисахаридов [Liu Z., Jiao Y., Wang Y., et al. Polysaccharides-based nanoparticles as drug delivery systems // Advanced Drug Delivery Reviews. 2008, 60(15), 1650-1662], (например, наночастицы модифицированного крахмала [Santander-Ortega М.J., Stauner Т., Loretz В., et al. Nanoparticles made from novel starch derivatives for transdermal drug delivery // Journal of controlled release. 2010, 141(1), 85-92]). В работе [Kuo, Т.R., Wu, C.L., Hsu, С.Т., et al. Chemical enhancer induced changes in the mechanisms of transdermal delivery of zinc oxide nanoparticles // Biomaterials. 2009, 30(16), 3002-3008] показано, что олеиновая кислота, этиловый спирт или их комбинация облегчает подкожную доставку наночастиц ZnO. В работе [Zhao Q.Н., Zhang Y., Liu Y., et al. Anticancer effect of realgar nanoparticles on mouse melanoma skin cancer in vivo via transdermal drug delivery // Medical Oncology. 2010, 27(2), 203-212] для терапии рака кожи (меланомы) использовали наночастицы сульфида мышьяка; с целью трансдермальной доставки эти наночастицы в соотношении 1:4 (весовых частей) вводили в кремообразную эмульсию, состоящую из глицерилмоностеарата, гидроксипропилметилцеллюлозы, изопропилмиристата, метилпарабена, пропилпарабена, полиоксил (40) стеарата и воды в соотношении 10:1:10:1:1:11:66 (весовых частей). В патенте [US 7371738] для доставки магнитных наночастиц ¥е2Оз через кожу предложено использовать поперечносшитую гиалуроновую кислоту. Авторы [RU 2500381] показали возможность повышения эффективности подкожной доставки наночастиц золота с использованием серосодержащих органических соединений - диметилсульфоксида и тиофансульфоксида. В патенте показано, что препарат, содержащий 0.1 мл 96% раствора диметилсульфоксида на 1 мл гелевой основы (либо 0.1 мл 20% раствора тиофансульфоксида на 1 мл гелевой основы) существенно повышал проникновение наночастиц золота диаметром 140 нм под кожу, особенно если после нанесения указанного препарата участки кожи были подвергнуты ультразвуковому воздействию с частотой 1 МГц, мощностью 2 Вт и продолжительностью 2 минуты.
Данное изобретение является наиболее близким к заявляемому, и принято за прототип.
Известно, что металлическое золото (в том числе и в виде наночастиц) имеет повышенную тропность к серосодержащим соединениям: так, ДМСО прочно адсорбируется на поверхности золота [ С, Roelfs В., Solomun Т. The interaction of dimethylsulfoxide with a gold surface // Surface science. 1997, 380(1), L441-L445] и способен выполнять одновременно роль стабилизатора наночастиц и пенетратора для их проникновения через кожу. Для оксидов редкоземельных элементов химическое (и сильное физическое) взаимодействие между ДМСО и поверхностью наночастиц отсутствует, поэтому в случае наночастиц диоксида церия подход, заявленный в прототипе, неприменим.
С, Roelfs В., Solomun Т. The interaction of dimethylsulfoxide with a gold surface // Surface science. 1997, 380(1), L441-L445] и способен выполнять одновременно роль стабилизатора наночастиц и пенетратора для их проникновения через кожу. Для оксидов редкоземельных элементов химическое (и сильное физическое) взаимодействие между ДМСО и поверхностью наночастиц отсутствует, поэтому в случае наночастиц диоксида церия подход, заявленный в прототипе, неприменим.
Изобретение направлено на расширение количества материалов (композиций) медицинского и косметического назначения, активные компоненты которых могут быть доставлены трансдермальным способом.
Технической задачей изобретения является разработка композиции, содержащей нанокристаллический диоксид церия, обеспечивающей доставку наночастиц CeO2 через кожу.
Технический результат достигается тем, что предложена композиция для трансдермальной доставки наночастиц, содержащая диметилсульфоксид в качестве пенетратора, отличающаяся тем, что в качестве наночастиц используют нанокристаллический диоксид церия, связанный со стабилизатором, представляющим собой полисахарид, при следующем соотношении компонентов, мас. %:
- наночастицы диоксида церия - 1.7
- стабилизатор - 8.3
- диметилсульфоксид - 90.
Целесообразно, что в качестве стабилизатора используют полисахариды, в том числе низкомолекулярные полиглюканы.
Компоненты, входящие в состав композиции, могут использоваться в различных сочетаниях, которые в зависимости от характера заболевания могут обеспечивать оптимальное сочетание глубины проникновения и терапевтического эффекта. Концентрация наночастиц диоксида церия в ДМСО предпочтительно составляет 10-100 г/л, массовое соотношение CeO2 к стабилизатору - от 1:1 до 1:5. Стабилизаторы выбирают исходя из уровня техники, они должны удовлетворять нескольким условиям: способность прочно связываться с поверхностью наночастиц диоксида церия, нетоксичность, растворимость/совместимость с пенетратором (ДМСО). В частности, известно, что диоксид церия образует стабильные золи с мальтодекстрином, декстраном [RU 2615688], D-пантенолом [Zholobak N.М., Shcherbakov А.В., Bogorad-Kobelska A.S., et al. Panthenol-stabilized cerium dioxide nanoparticles for cosmeceutic formulations against ROS-induced and UV-induced damage. // Journal of Photochemistry and Photobiology B: Biology. 2014, 130, 102-108], и др.
Сущность изобретения заключается в том, что предложена композиция на основе нанокристаллического диоксида церия, эффективный компонент которой может быть доставлен через кожу за счет того, что в композиции присутствует стабилизатор, взаимодействующий с поверхностью наночастицы и совместимый с ДМСО.
Изобретение проиллюстрировано следующими фигурами.
Фиг. 1. Электронно-микроскопические фотографии среза кожи хвоста мыши, обработанного композицией, содержащей 1.7 мас. % наночастиц диоксида церия, 8.3 мас. % мальтодекстрина и 90 мас. % ДМСО. Фотографии представляют собой последовательность увеличенных фрагментов с разным разрешением одного и того же участка среза кожи. А - видны агломераты наночастиц неправильной формы размером 10-50 нм; Б - скопления агломератов наночастиц как на поверхности кожи, так и вне ее; В - агломераты наночастиц присутствуют в межклеточном эпидермальном пространстве; Г - агломераты наночастиц визуализируются на глубине до 10 мкм.
Фиг. 2. Электронно-микроскопические фотографии среза уха мыши, обработанного раствором для накожного применения, содержащим 1.7 мас. % наночастиц диоксида церия, 8.3 мас. % мальтодекстрина и 90 мас. % ДМСО. Фотографии представляют собой последовательность увеличенных фрагментов с разным разрешением одного и того же участка среза кожи. А - диффузное скопление наночастиц на поверхности эпидермиса; Б - видны округлые агломераты частиц, адсорбированные на поверхности клеток, а также в межклеточном эпидермальном пространстве; В - исходное изображение среза кожи уха мыши, обработанного продуктом; на отслаивающемся эпидермисе видны адсорбированные агломераты наночастиц; Г - в глубоких тканях уха присутствуют агломераты наночастиц; Д - видно послойное накопление наночастиц в эпидермисе кожи: наибольшее содержание наночастиц - в поверхностных слоях; толщина наружного слоя, содержащего максимальное количество наночастиц - 1 мкм; Е - увеличенное поле среза кожи уха мыши; наночастицы визуализируются в тканях уха на глубине около 20 мкм, наблюдается заметное уплотнение эпителиального слоя. Уплотнение эпителия имеет равномерный характер и наблюдается на всем протяжении исследованных образцов кожи.
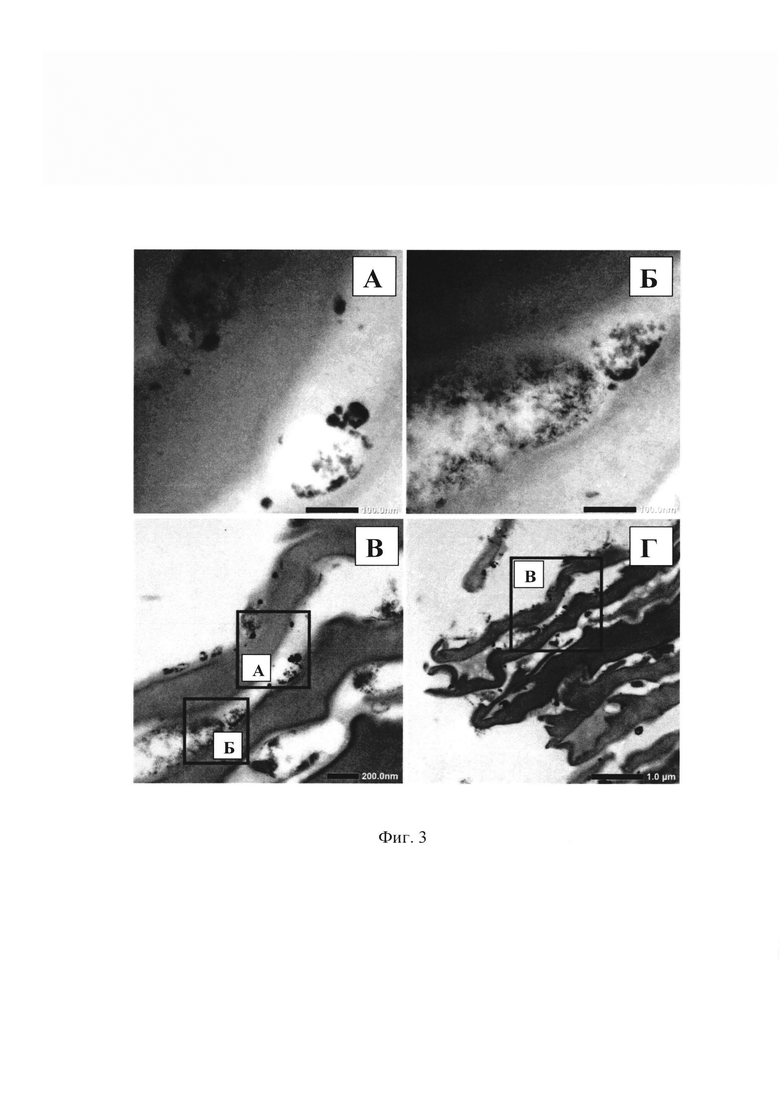
Фиг. 3. Электронно-микроскопические фотографии среза уха мыши, обработанного композицией, содержащей 1.7 мас. % наночастиц диоксида церия, 8.3 мас. % мальтодекстрина, 90 мас. % воды. Фотографии представляют собой последовательность увеличенных фрагментов с разным разрешением одного и того же участка среза кожи. А, Б - видны диффузные скопления и агломераты наночастиц неправильной формы размером 10-50 нм; В - агломераты наночастиц присутствуют на поверхности эпидермиса и в межклеточном пространстве; Г - агломераты наночастиц визуализируются на глубине не более 5 мкм.
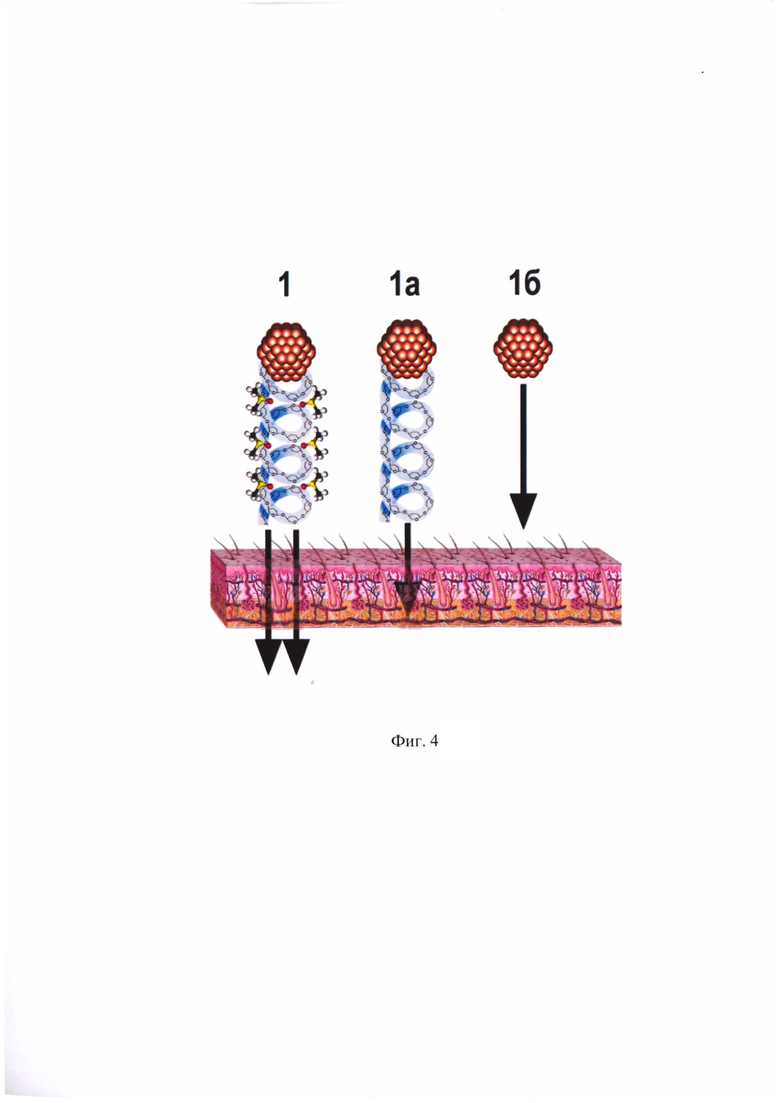
Фиг. 4. Схема проникновения наночастиц заявляемой композиции по сравнению с композициями, не содержащими один из целевых компонентов. 1 - стабилизированные полиглюканами наночастицы диоксида церия в присутствии носителя-пенетратора (ДМСО) обладают повышенной проницаемостью через неповрежденную кожу. 1а - стабилизированные полиглюканами наночастицы диоксида церия в отсутствии носителя-пенетратора обладают меньшей проникающей способностью. 1б - нестабилизированные наночастицы диоксида церия в отсутствии носителя-пенетратора не проникают через кожный барьер.
Ниже приведены примеры иллюстрирующие, но не ограничивающие предложенное изобретение.
Пример 1
Приготовление композиции.
Наночастицы диоксида церия, стабилизированные
мальтодекстрином, получали в высушенном виде (безводная форма) в соответствии с патентом [RU 2484832]. Затем 10 г ДМСО смешивали с 1 г полученного порошкообразного продукта (17 мас. % наночастиц диоксида церия размером 5-6 нм). Получали композицию для транедермальной доставки наночастиц, содержащую 1.7 мас. % наночастиц диоксида церия и 8.3 мас. % мальтодекстрина в ДМСО.
Пример 2
Демонстрация транедермальной доставки наночастиц.
Объектом для тестирования способа транедермальной доставки наночастиц диоксида церия были избраны белые рандомбредные мыши (самки массой 38-40 г). Выбор самок был обусловлен известными половыми различиями толщины эпидермиса кожи мышей (у самцов он более тонкий); на разных участках толщина эпидермиса составляет от 8 до 16 мкм [Dao Н Jr, Kazin RA. Gender differences in skin: a review of the literature // Gend Med. 2007, 4, 308-328]. Животных содержали на стандартном брикетированном корме с добавлением сырых овощей. Корм и воду животные получали без ограничения. Поскольку кожа на разных участках тела отличается по своей плотности, композицию наносили мышам на кожу хвоста (максимально жесткая и плотная) и уха (нежная и тонкая). Обработку кожи проводили один раз в сутки в течение трех дней: на участок площадью 0.5 см2 наносили 0.1 мл композиции, фиксируя животных, до ее полного высыхания или впитывания в кожу. В течение всего периода наблюдения двигательная и пищевая активность животных, получавших накожные аппликации препаратов, не отличалась от показателей контрольной группы. Результаты анализа показали наличие наночастиц в дерме на глубину до 20 мкм при нанесении как на кожу хвоста, так и уха. Микрофотографии представлены на Фиг. 1 и 2 соответственно.
Пример 3
Демонстрация целевого назначения ДМСО заявляемой композиции для транедермальной доставки наночастиц.
Композицию готовили аналогично примеру 1, за исключением следующего: вместо ДМСО использовали дистиллированную воду. Наносили эту композицию на кожу хвоста и уха мыши. Результаты анализа показали наличие наночастиц в дерме только при нанесении на ухо, микрофотографии представлены на Фиг. 3.
Пример 4
Демонстрация целевого назначения стабилизатора и ДМСО заявляемой композиции для транедермальной доставки наночастиц.
Композицию получали аналогично примеру 3, за исключением следующего: вместо стабилизированных мальтодекстрином наночастиц диоксида церия использовали нестабилизированные наночастицы размером 5-6 нм, полученные по методике [Иванов В.К., Полежаева О.С., Щербаков А.Б. Гидротермально микроволновой синтез стабильных золей нанокристаллического диоксида церия для биомедицинского применения // Журн. Неорг. Химии. 2010, 55(1), 3-8.]. Наносили раствор на кожу хвоста и уха мыши. Результаты анализов показали отсутствие наночастиц в дерме при любом способе нанесения, микрофотографирование не производили.
Таким образом, приведенные примеры свидетельствуют, что композиция согласно изобретению обеспечивает максимальное проникновение наночастиц диоксида церия через кожный барьер мышей (на глубину до 20 мкм) - в отличие от стабилизированных полисахаридами наночастиц диоксида церия на водной основе, проникающих до 5 мкм вглубь кожи, или нестабилизированных наночастиц диоксида церия на водной основе, которые вообще не проникают в неповрежденную кожу, что схематично представлено на Фиг. 4.
Предложенная композиция может быть использована в различных областях медицины, например в онкологии, дерматологии, косметологии, ветеринарной медицине как сама по себе, так и в составе препаративной формы для космецевтического применения в виде мази, геля, крема, компресса, пленки или пластыря.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ НА ОСНОВЕ НАНОЧАСТИЦ ДИОКСИДА ЦЕРИЯ И ПОЛИСАХАРИДОВ БУРЫХ ВОДОРОСЛЕЙ ДЛЯ ЛЕЧЕНИЯ РАН | 2018 |
|
RU2699362C2 |
| Пептидный толерогенный компаунд | 2021 |
|
RU2766340C1 |
| Способ получения противовоспалительного препарата на основе пептидов селезенки млекопитающих, препарат, полученный данным способом, и его применение | 2021 |
|
RU2790158C1 |
| Способ получения стабильных водных коллоидных растворов наночастиц диоксида церия | 2016 |
|
RU2615688C1 |
| МИКРОЭМУЛЬСИОННЫЕ КОМПОЗИЦИИ ДЛЯ СОЗДАНИЯ ТРАНСДЕРМАЛЬНЫХ И ТРАНСМУКОЗАЛЬНЫХ ФОРМ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ И КОСМЕТИЧЕСКИХ ПРЕПАРАТОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2012 |
|
RU2481822C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОКРЫТОГО СТАБИЛИЗИРУЮЩЕЙ ОБОЛОЧКОЙ НАНОКРИСТАЛЛИЧЕСКОГО ДИОКСИДА ЦЕРИЯ | 2012 |
|
RU2484832C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО КОМПОЗИТА НА ОСНОВЕ НАНОКРИСТАЛЛИЧЕСКОГО ДИОКСИДА ЦЕРИЯ И КУРКУМИНА | 2017 |
|
RU2665378C1 |
| ТРАНСДЕРМАЛЬНЫЙ ПЛАСТЫРЬ | 2019 |
|
RU2705896C1 |
| Способ получения золя диоксида церия в неводной среде | 2022 |
|
RU2798099C1 |
| СИСТЕМА ЭНХАНСЕРОВ ТРАНСДЕРМАЛЬНОГО ПЕРЕНОСА И КОСМЕТИЧЕСКИЕ КОМПОЗИЦИИ НА ЕЕ ОСНОВЕ | 2020 |
|
RU2736504C1 |


Изобретение относится к области медицины, в частности к области разработки терапевтических и косметических композиций и их применения для доставки неорганических частиц, конкретно наночастиц диоксида церия, через кожу. Предложена композиция для трансдермальной доставки наночастиц, содержащая диметилсульфоксид в качестве пенетратора и нанокристаллический диоксид церия в качестве наночастиц, связанный со стабилизатором, представляющим собой полисахарид, при следующем соотношении компонентов, мас. %: наночастицы диоксида церия – 1,7; стабилизатор – 8,3; диметилсульфоксид - 90. В качестве стабилизатора могут быть использованы низкомолекулярные полиглюканы. Изобретение обеспечивает максимальное проникновение наночастиц диоксида церия через кожный барьер на глубину до 20 мкм. 1 з.п. ф-лы, 4 ил., 4 пр.
1. Композиция для трансдермальной доставки наночастиц, содержащая диметилсульфоксид в качестве пенетратора, отличающаяся тем, что в качестве наночастиц используют нанокристаллический диоксид церия, связанный со стабилизатором, представляющим собой полисахарид, при следующем соотношении компонентов, мас. %:
2. Композиция по п. 1, отличающаяся тем, что в качестве стабилизатора используют низкомолекулярные полиглюканы.
| СПОСОБ ВВЕДЕНИЯ НАНОЧАСТИЦ ЗОЛОТА ПУТЕМ МЕСТНОГО НАНЕСЕНИЯ НА КОЖУ | 2012 |
|
RU2500381C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОКРЫТОГО СТАБИЛИЗИРУЮЩЕЙ ОБОЛОЧКОЙ НАНОКРИСТАЛЛИЧЕСКОГО ДИОКСИДА ЦЕРИЯ | 2012 |
|
RU2484832C1 |
| Способ получения стабильных водных коллоидных растворов наночастиц диоксида церия | 2016 |
|
RU2615688C1 |
| US 10201571 B2, 12.02.2019 | |||
| ЩЕРБАКОВ А.Б | |||
| и др | |||
| Наноматериалы на основе диоксида церия: свойства и перспективы использования в биологии и медицине | |||
| Биотехнология, 2011, т.4, N1, с.9-28 | |||
| ЩЕРБАКОВ А.Б | |||
| Синтез и антиоксидантная активность биосовместимых водных золей | |||
Авторы
Даты
2021-08-19—Публикация
2021-01-26—Подача