ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение, главным образом, относится к области здоровья свиней. Свиньи подвержены воздействию многих патогенных микроорганизмов. Контроль инфекций обычно проводят посредством контроля за фермой и кормом, лечения фармацевтическими препаратами, такими как противовирусные лекарственные средства и антибиотики, или профилактического лечения с использованием вакцин. В частности, изобретение относится к вакцинам против цирковируса свиней 2 типа (PCV2 или PCV–2), Mycoplasma hyopneumoniae, вируса репродуктивно–респираторного синдрома свиней (PRRS) и необязательно Lawsonia intracellularis, и к способу защиты животного от таких инфекций с использованием таких вакцин.
УРОВЕНЬ ТЕХНИКИ
PCV–2 связан с синдромом послеотъемного мультисистемного изнурения (PMWS), наблюдаемым у молодых свиней. Это заболевание впервые обнаружено в Канаде в 1991 году. Клинические признаки и патология впервые были опубликованы в 1996 году и включают прогрессирующее изнурение, диспноэ, тахипноэ и иногда иктеричность и желтуху.
Nayar et al., Can. Vet. J. Volume 38, June 1997, выявили цирковирус свиней с клиническими симптомами PMWS и сделали заключение, что PCV, в отличие от известного PCV, признанного естественным обитателем клеток PK–15, может быть связан с PMWS. Более поздние публикации (Hamel et al., J.Virol., 72(6), 5262–5267, 1998; Meehan et al., J. Gen.Virol., 79, 2171–2179, 1998) подтвердили эти данные, и было предложено (Meehan et al., выше) обозначать новый патогенный PCV как PCV–2, в то время как исходный изолят культуры клеток PK–15 (Tischer et al., Nature 295, 64–66, 1982) должен обозначаться как PCV–1.
PCV–2 представляет собой мелкий (17–22 нм) икосаэдрический безоболочечный вирус, содержащий кольцевой одноцепочечный ДНК–геном. Длина генома PCV–2 составляет приблизительно 1768 п.н. Изоляты PCV–2, происходящие из различных регионов мира, по–видимому, являются близкородственными друг другу и проявляют приблизительно 95–99% идентичность нуклеотидных последовательностей (Fenaux et al., J.Clin. Micorbiol., 38(7), 2494–2503, 2000). ORF2 PCV кодирует капсидный белок вируса. Ген ORF2 PCV2 кодирует белок размером приблизительно 233 аминокислоты. Гены ORF 2 всех изолятов PCV–2 обладают 91–100% идентичностью нуклеотидной последовательности и 90–100% идентичностью установленных аминокислотных последовательностей.
Mycoplasma hyopneumoniae (Mhyo) представляет собой вид бактерий, о которых известно, что они вызывают заболевание энзоотическую пневмонию свиней, высококонтагиозное заболевание, которым страдают свиньи. Mhyo является мелким по размеру (400–1200 нм), имеет мелкий геном (893–920 тысяч пар оснований (т.п.н.)) и лишен клеточной стенки. Mhyo прикрепляется к ресничкам эпителиальных клеток легких свиней. Он вызывает остановку дыхания ресничек, сращение и утрату ресничек и в конечном итоге приводит к гибели эпителиальных клеток. Это является источником очагов повреждений, встречающихся в легких свиней с энзоотической пневмонией свиней. Это повреждение препятствует нормальному мукоцилиарному клиренсу, и часто развиваются вторичные инфекции. Это вызывает значительное уменьшение прироста массы животных. Потери в США ранее были оценены как вплоть до 1 миллиарда долларов в год. Энзоотическая пневмония свиней является эндемической по всему миру и Mhyo присутствует практически в каждом стаде свиней. Иммунный ответ, индуцированный присутствием Mhyo у свиней, является медленным и неэффективным. Таким образом, лечение этого заболевания имеет чрезвычайную важность, но ограничивается антибиотиками, которые в настоящее время являются только частично эффективными, поскольку они не устраняют инфекцию полностью. Было обнаружено, что вакцины уменьшают тяжесть заболевания, но полностью не предупреждают возникновение заболевания у инфицированных свиней.
Первое сообщение о вирусе PRRS в Северной Америке и Центральной Европе датируется 1987 годом. Вирус PRRS представляет собой мелкий оболочечный РНК–вирус. Он содержит одноцепочечный РНК–геном с положительной цепью, имеющий размер приблизительно 15 тысяч пар оснований. Геном содержит девять открытых рамок считывания. Вирус является представителем рода Arterivirus, семейства Arteriviridae, отряда Nidovirales. Двумя прототипными штаммами PRRSV являются североамериканский штамм VR–2332 и европейский штамм, вирус Lelystad (LV). Европейский и североамериканский штаммы PRRSV вызывают сходные клинические симптомы. Недавно в Китае появился высокопатогенный штамм североамериканского генотипа. Этот штамм, HP–PRRSV, является более вирулентным, чем все другие штаммы, и вызывает значительные потери в странах Азии. Клинические признаки включают неспособность к размножению у свиноматок, такую как выкидыши и рождение мертворожденных или мумифицированных плодов, и цианоз уха и вульвы. У новорожденных свиней заболевание вызывает расстройство дыхания с увеличением предрасположенности к респираторным инфекциям, таким как болезнь Глассера.
Lawsonia intracellularis вызывает пролиферативную энтеропатию, также известную как илеит, которая является частым кишечным заболеванием послеотъемных свиней по всему миру. Характерным очагом повреждения является пролиферация незрелых энтероцитов в кишечных криптах подвздошной кишки; эти клетки обычно содержат бактерии, являющиеся этиологическим фактором, в их апикальной цитоплазме. При аутопсии гистологические очаги повреждения могут быть подтверждены как Lawsonia–положительные посредством визуализации бактерий вибриоидной формы длиной 1,5–2,5 мкм, особенно в энтероцитах, но также часто в макрофагах, расположенных в собственной пластинке между криптами и в мезентериальных лимфатических узлах. Выведение бактерий из энтероцитов приводит к разрешению ассоциированных пролиферативных очагов повреждения, что указывает на прямой локальный эффект бактерий на крипты. Присутствие Lawsonia intracellularis в этих очагах повреждения продемонстрировано с использованием ПЦР как у животных с признаками заболевания, так и животных, у которых проявляется только субклиническая инфекция. Клинические случаи обычно присутствуют в период выращивания–откармливания; у некоторых свиней более старшего возраста регистрируется острая геморрагическая форма.
Вакцины против указанных выше патогенов широко известны. Обычная вакцина для профилактического лечения животных, в частности свиней, от инфекции PCV 2 может быть основана на целом инактивированном вирусе PCV–2 в качестве (не реплицирующегося) иммуногена. Также в данной области показано, что кодируемый ORF2 капсидный белок (например, когда он рекомбинантно экспрессируется) пригоден в качестве субъединичного иммуногена цирковируса свиней 2 типа для применения в адекватной вакцине. Это может быть понятно, поскольку эта субъединица в кровеносной системе имеет практически такой же путь, как и сам вирус (она образует вирусоподобные частицы), по существу отличающиеся только тем, что ДНК и неструктурные белки не присутствуют внутри капсида. В данной области несколько вакцин против PCV2 являются коммерчески доступными. Porcilis® PCV (доступная от MSD Animal Health, Boxmeer, Нидерланды) представляет собой вакцину для защиты свиней от цирковируса свиней 2 типа для применения у свиней в возрасте трех недель и старше. При введении в качестве вакцины, вводимой двукратно (двумя дозами), длительность иммунитета (DOI) составляет 22 недели, что практически полностью охватывает период откорма свиней. Ingelvac CircoFlex® (доступный от Boehringer Ingelheim, Ingelheim) представляет собой вакцину для защиты свиней от цирковируса свиней 2 типа для применения у свиней в возрасте двух недель и старше. Она зарегистрирована в качестве вводимой только однократно (одной дозой). Circovac® (доступная от Merial, Lyon, Франция) представляет собой вакцину для защиты свиней от цирковируса свиней 2 типа для применения у свиней в возрасте трех недель и старше. Suvaxyn® PCV (доступная от Zoetis, Capelle a/d IJssel, Нидерланды) представляет собой вакцину для защиты свиней от цирковируса свиней 2 типа для применения у свиней в возрасте трех недель и старше. Другие вакцины против PCV2 описаны, например, в WO2007/028823, WO 2007/094893 и WO2008/076915.
Что касается Mycoplasma hyopneumoniae, существует множество коммерческих вакцин, и их в плановом порядке используют в большинстве коммерческих свиноферм. Как правило, эти вакцины содержат не реплицирующиеся иммуногены, такие как субъединичные белки и/или бактерины (т.е. композиция, содержащая убитые бактерии, либо в виде целых клеток, либо в виде (частично) лизированных, либо в виде гомогенизированных, либо подвергнутых обработке на френч–прессе, либо их комбинацию, или содержащая убитые бактерии в другой форме при условии, что композиция происходит из убитой бактериальной культуры), которые обычно вводят посредством парентеральной инъекции. Некоторыми примерами являются: RespiSure® (Zoetis), Ingelvac® M. hyo, и MycoFLEX® (Boehringer Ingelheim), Hyoresp® (Merial), Stellamune® Mycoplasma (Elanco Animal Health), Fostera® PCV MH (Zoetis) и M+Pac® и Porcilis® Mhyo (обе доступны от MSD Animal Health).
Что касается вируса PRRS, хотя были описаны и являются коммерчески доступными инактивированные вирусные вакцины, основным иммунологическим инструментом его контроля является модифицированный живой вирус (вакцины MLV), содержащий либо европейский тип (тип I), либо североамериканский тип (тип II) в живой аттенуированной форме. В данной области несколько вакцин являются коммерчески доступными. Porcilis® PRRS (доступная от MSD Animal Health, Boxmeer, Нидерланды) представляет собой вакцину, содержащую живой аттенуированный вирус PRRS типа I, она зарегистрирована для снижения инфекции (виремии), вызываемой инфицированием вирусом PRRS. Ingelvac PRRS® MLV (доступная от Boehringer Ingelheim, Ingelheim) представляет собой вакцину, которая способствует уменьшению заболевания, вызываемого вирусом PRRS, и которая обеспечивает перекрестную защиту против штаммов различных типов. Fostera® PRRS (доступная от Zoetis, Florham Park, New Jersey, США) также представляет собой вакцину MLV и зарегистрирована для защиты как от респираторных, так и репродуктивных форм заболевания, вызываемого вирусом PRRS. Другой вакциной MLV против PRRS является PrimePac PRRS (тип II), доступная от Merck Animal Health, Madison, NJ, США. Другие вакцины против PRRS описаны, например, в WO2006/074986, US 8728487 и WO2014/048955.
Вакцины для борьбы с Lawsonia intracellularis посредством индукции активной защиты коммерчески доступны и описаны в данной области. Эти вакцины доступны под товарными наименованиями Enterisol® Ileitis (Boehringer Ingelheim Vetmedica, США), которая представляет собой живую аттенуированную вакцину, и Porcilis® Ileitis (Merck Animal Health, США), которая представляет собой вакцину, содержащую не реплицирующийся иммуноген Lawsonia intracellularis в форме бактерина.
ЗАДАЧА ИЗОБРЕТЕНИЯ
Существует постоянная потребность в удобных, безопасных и эффективных способах контроля здоровья свиней. В частности, существует потребность в удобных, безопасных и эффективных вакцинах, которые можно использовать для профилактического лечения свиней от инфекции цирковирусом свиней 2 типа, инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Чтобы выполнить задачу изобретения, была разработана первая вакцина и вторая вакцина, причем первая вакцина содержит не реплицирующийся иммуноген цирковируса свиней 2 типа (PCV2) и не реплицирующийся иммуноген Mycoplasma hyopneumoniae, и вторая вакцина содержит живой аттенуированный вирус репродуктивно–респираторного синдрома свиней (PRRS), где комбинация предназначена для применения для профилактического лечения животного от инфекции цирковирусом свиней 2 типа, инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS посредством ассоциированного не смешанного введения первой вакцины и второй вакцины животному.
Хотя для каждого патогена, упоминаемого в настоящем описании выше, вакцины известны и коммерчески доступны, не доступна комбинация вакцин для ассоциированного не смешанного введения, которая обеспечивает требуемую эффективность и в то же время является безопасной для применения у животных, в частности, у молодых животных. Как широко известно, не все предполагаемые или предлагаемые комбинации антигенов могут обеспечивать безопасную и эффективную комбинированную вакцину. Соответственно, ассоциированное не смешанное применение вакцин, также упоминаемое как сопутствующее введение, можете вызывать взаимодействия, приводящие к проблемам безопасности или сниженному ответу на индивидуальные иммуногены, присутствующие в вакцинах. В случае живых вакцин, может появляться вакцинный штамм со сниженной репликацией. Интерференция различных иммуногенов может быть результатом различных иммунологических событий, таких как антигенная конкуренция. Антигенная конкуренция относится к явлению, состоящему в том, что иммунный ответ на конкретный иммуноген (также упоминаемый как антиген) может уменьшаться в присутствии других иммуногенов по сравнению с тем, когда тот же иммуноген вводят отдельно.
В качестве доказательства общеизвестной проблемы интерференции вакцин даже при введении без смешения служит руководство, опубликованное 18 июля 2013 года Комитетом по медицинским продуктам для ветеринарного применения (CVMP) Европейского агентства по лекарственным средствам (EMA) под названием "Guideline on the requirements for combined вакцины and associations of immunological veterinary medicinal products (IVMP)" (EMA/CVMP/IWP/594618/2010). В разделе 5.1 утверждается, что "основанием для ассоциации IVMP должна быть демонстрация приемлемой безопасности и отсутствия серьезной интерференции между вовлеченными IVMP. Если профиль безопасности для ассоциации является менее благоприятным, чем профиль безопасности, установленный для отдельных продуктов, ассоциация должна быть подвергнута надлежащему обоснованию польза–риск, где польза ассоциации должна отчетливо перевешивать риски уменьшения безопасности. В таких ситуациях SPC отдельных продуктов должен быть изменен так, чтобы он отражал профиль безопасности вследствие ассоциированного применения IVMP. Если некоторый уровень интерференции между продуктами в ассоциации приводит к уменьшению эффективности, ассоциация IVMP должна быть далее обоснована в индивидуальном порядке. Также следует отметить. что изменения, которые оказывают влияние на продукцию или композицию какого–либо из имеющих отношение IVMP, также потребуют переоценки совместимости ассоциации".
Более того, в частности, для любого комбинированного введения с живым вирусом PRRS: во всяком случае ожидается, что будет присутствовать отрицательное влияние на эффективность в отношении других иммуногенов, поскольку широко известно, что вирус PRRS является иммуносупрессивным. См. например Can J Vet Res. 2012 Oct;76(4):255–60: "Suppression of immune responses in pigs by nonstructural protein 1 of porcine reproductive and respiratory syndrome virus.", Zhou Y1, Bai J, Li Y, Wang X, Wang X, Jiang P.
В общем, широко известно, что комбинированная вакцинация против нескольких патогенов является непростой и требует экспериментирования для определения безопасности и эффективности, в частности, когда комбинированная вакцинация вовлекает живой вирус PRRS.
Следует отметить, что настоящее изобретение также относится к набору, содержащему первую вакцину, содержащую не реплицирующийся иммуноген цирковируса свиней 2 типа (PCV2) и не реплицирующийся иммуноген Mycoplasma hyopneumoniae, и отдельно вторую вакцину, содержащую живой аттенуированный вирус PRRS, для применения для профилактического лечения животного против инфекции цирковирусом свиней 2 типа, инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS посредством ассоциированного не смешанного введения первой вакцины и второй вакцины животному.
Также изобретение относится к способу профилактического лечения животного против инфекции цирковирусом свиней 2 типа (PCV2), инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS посредством ассоциированного не смешанного введения первой вакцины, содержащей не реплицирующийся иммуноген цирковируса свиней 2 типа и не реплицирующийся иммуноген Mycoplasma hyopneumoniae, и второй вакцины, содержащей живой аттенуированный вирус PRRS.
Также изобретение относится к вакцине, содержащей не реплицирующийся иммуноген цирковируса свиней 2 типа (PCV2) и не реплицирующийся иммуноген Mycoplasma hyopneumoniae, для применения для профилактического лечения животного против инфекции цирковирусом свиней 2 типа, инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS, посредством ассоциированного не смешанного введения вакцины с другой вакциной, содержащей живой аттенуированный вирус репродуктивно–респираторного синдрома свиней (PRRS) животному. Соответственно, изобретение относится к вакцине, содержащей живой аттенуированный вирус репродуктивно–респираторного синдрома свиней (PRRS), для применения для профилактического лечения животного против инфекции цирковирусом свиней 2 типа, инфекции Mycoplasma hyopneumoniae и инфекция вирусом PRRS, посредством ассоциированного не смешанного введения вакцины с другой вакциной, содержащей не реплицирующийся иммуноген цирковируса свиней 2 типа (PCV2) и не реплицирующийся иммуноген Mycoplasma hyopneumoniae, животному. Каждый из конкретных вариантов осуществления, как описано в настоящем описании ниже в разделе "Варианты осуществления изобретения", можно комбинировать с этими двумя вакцинами для применения в соответствии с настоящим изобретением.
Следует отметить, что в вакцине иммуноген (также называемый антигеном) обычно комбинирован с фармацевтически приемлемым носителем, т.е. биосовместимой средой, а именно, средой, которая после введения не индуцирует значительных неблагоприятных реакций у данного животного и способна презентировать иммуноген иммунной системе животного–хозяина после введения вакцины, такой как жидкость, содержащая воду и/или любой другой биосовместимый растворитель, или твердый носитель, такой как носитель, обычно используемый для получения лиофилизированных вакцин (на основе сахаров и/или белков), необязательно содержащий иммуностимулирующие средства (адъюванты), которые при введении животному индуцируют иммунный ответ для лечения животного против инфекции микроорганизмом дикого типа, т.е. для способствования предупреждению, смягчению или излечению такой инфекции или нарушения, возникающего в результате нее. Необязательно добавляют другие вещества, такие как стабилизаторы, модификаторы вязкости или другие компоненты в зависимости от предполагаемого применения или требуемых свойств вакцины.
ОПРЕДЕЛЕНИЯ
Вакцина представляет собой фармацевтическую композицию, которая является безопасной для введения животному и способна индуцировать защитный иммунитет у этого животного против патогенного микроорганизма, т.е. индуцировать успешное профилактическое лечение, как определено в настоящем описании ниже.
Не реплицирующийся иммуноген патогена представляет собой любое вещество или соединение, соответствующее патогену, отличное от живого реплицирующегося патогена в целом (либо в форме дикого типа, либо в аттенуированной форме), против которого индуцируется иммунологический ответ, так что соответствующий вирулентный патоген или один или несколько его факторов вирулентности распознаются иммунной системой хозяина в результате этого иммунного ответа и в конечном итоге по меньшей мере частично нейтрализуются. Типичными примерами не реплицирующихся иммуногенов являются убитые целые патогены (этот термин включает эти патогены в лизированной форме) и субъединицы этих патогенов, такие как капсидные белки, экспрессируемые на поверхности молекулы (например, рекомбинантно экспрессируемые белки и липополисахариды), и экскретируемые молекулы, такие как токсины.
Живой аттенуированный патоген является жизнеспособной компетентной в отношении репликации формой патогена, имеющей сниженную вирулентность. Процесс аттенуации включает использование инфекционного патогена и изменение его таким образом, чтобы он становился безвредным или менее вирулентным, как правило, либо посредством многократного пассирования патогена через клеточные системы, либо посредством генной модификации патогена.
Профилактическое лечение инфекции патогеном представляет собой способствование предупреждению, смягчению или излечению от инфекции этим патогеном или нарушения вследствие этой инфекции, возникающих в результате заражения патогенов после лечения, в частности, для снижения его нагрузки у хозяина после такого заражения и необязательно для способствования предупреждению или смягчению одного или нескольких клинических проявлений в результате инфицирования патогеном после лечения.
Ассоциированное не смешанное введение вакцин, также называемое сопутствующим введением, представляет собой введение этих вакцин по отдельности, таким образом, не смешивая перед введением, данному животному, но в пределах таких временных рамок, чтобы могла произойти иммунологическая интерференция, как правило, в пределах 24 часов. Примерами ассоциированного не смешанного применения являются одновременное введение в различные области у данного животного, и введение в одну или в различные области применения, но в различные моменты времени, как правило, разделенные на 1–6 часов.
Одновременное введение вакцины означает введение практически в одно время или по меньшей мере в пределах временных рамок, составляющих 1 час, предпочтительно в пределах 55, 50, 45, 40, 35, 30, 25, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2 минут или даже в пределах временных рамок, составляющих 1 минуту.
Введение однократной дозы вакцины для применения в профилактическом лечении означает, что для обеспечения защитного иммунитета вакцинация не требует вспомогательной иммунизации посредством второго введения вакцины. В режиме с двукратным введением первая (примирующая) вакцинация обычно усиливается в течение 6 недель после первого введения, обычно в течение 3 или даже 2 недель после первого введения, и только после второго (усиливающего) введения может быть достигнут защитный иммунитет, т.е. успешное профилактическое лечение, как определено в настоящем описании выше.
ВАРИАНТЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
В одном варианте комбинации первой и второй вакцины для применения в соответствии с изобретением ассоциированное не смешанное введение происходит одновременно. Этот вариант осуществления имеет преимущество, состоящее в том, что животное необходимо держать только один раз для введения обеих вакцин.
В другом варианте комбинации вакцин по настоящему изобретению вторую вакцину вводят в дерму животного. Было показано, что такое введение по меньшей мере вакцины PRRS является безопасным и эффективным, и в то же время менее стрессовым для животного по сравнению с внутримышечным введением. Что касается введения в дерму (также называемого внутридермальным введением), хотя такое введение часто проводят с использованием безыгольного устройства для вакцинации, такого как вакцинатор IDAL® (доступный от MSD Animal Health, Boxmeer, Нидерланды), "внутридермальное" введение само по себе не должно приравниваться к "безыгольному" введению. Всемирная организация здравоохранения статье от 27 августа 2009 года по названием "Intradermal Delivery of Vaccines; A review of the literature and the potential for development for use in low– и middle–income countries" действительно явно указывает, что "безыгольная" вакцинация не обязательно означает "внутридермальную" вакцинацию (см. таблицу 1, стр.3 обзора). Только когда безыгольное устройство "предназначено для внутридермальной вакцинации", тогда вакцина действительно может доставлена (по меньшей мере частично) в дерму. В ином случае вакцина целиком может быть доставлена подкожно или внутримышечно.
В другом варианте комбинации первой и второй вакцин, первая вакцина содержит не реплицирующийся иммуноген Lawsonia intracellularis. В этом варианте осуществления новая комбинация вакцин способна обеспечивать защиту против четырех основных патогенов свиней с использованием только одного протокола вакцинации. В одном варианте осуществления иммуноген Lawsonia intracellularis комбинируют с иммуногеном PCV2 и Mycoplasma hyopneumoniae в пределах 24 часов до введения, предпочтительно в пределах 6 часов до введения. Комбинирование антигенов непосредственно перед введением обеспечивает больше свободы выбора эксципиентов, поскольку длительной стабильности, хотя она и известна для многих фармацевтических композиций, даже для комбинированных вакцин, включающих антиген PCV2 ORF2 (например, Porcilis® PCV M Hyo, доступная от MSD Animal Health), как известно, может быть непросто достигнуть, по меньшей мере не для любых и всех композиций фармацевтически приемлемых носителей. В следующем варианте осуществления иммуноген Lawsonia intracellularis добавляют в вакцину в форме композиции, содержащей лиофилизированные убитые цельные клетки Lawsonia intracellularis.
В другом варианте новой комбинации первой и второй вакцины первую и вторую вакцины вводят в виде одной дозы. Было обнаружено, что введение одной дозы приводило к эффективной вакцинации против всех патогенов. Это обеспечивает очень удобный и экономичный способ защиты животных против этих патогенов.
В другом варианте осуществления не реплицирующийся иммуноген представляет собой рекомбинантно экспрессируемый белок, кодируемый геном ORF2 PCV2, например, экспрессируемый бакуловирусом, как известно в данной области. Было показано, что этот рекомбинантный белок является пригодным для применения в рамках настоящего изобретения. В частности, белок ORF2 может быть экспрессирован посредством бакуловирусной системы экспрессии, как описано WO2007/028823, WO 2007/094893 или WO2008/076915.
В другом варианте осуществления не реплицирующийся иммуноген Mycoplasma hyopneumoniae содержит убитые цельные Mycoplasma hyopneumoniae. Такой антиген Mhyo относительно просто получить, и он имеет хорошую историю эффективности в повседневной практике свиноводства.
Далее изобретение объяснено более подробно с использованием приведенных ниже примеров.
ПРИМЕРЫ
ИССЛЕДОВАНИЕ 1 : Безопасность и защита против заражения PRRSv посредством ассоциированного не смешанного применения Porcilis® PCV MHyo с восстановленным в ней иммуногеном Lawsonia, и Porcilis® PRRS.
Это исследование проводили для оценки безопасности и эффективности Porcilis® PRRS в ассоциированном не смешанном применении с лиофилизированными убитыми цельными клетками Lawsonia intracellularis (также называемыми "лиофилизированными Lawsonia"), восстановленными в Porcilis® PCV M Hyo.
Исследование проводили с использованием шестидесяти отрицательных по антителам к PRRSV поросят, равным образом распределенных на 5 групп по 12 поросят в каждой. Четыре группы вакцинировали в возрасте 3 недель посредством либо 2 мл Porcilis® PRRS внутримышечно (в/м; группы 1 и 3), либо 0,2 мл Porcilis® PRRS внутридермальным путем (в/д; группы 2 и 4). Просят из групп 1 и 2 вакцинировали лиофилизированными Lawsonia, восстановленными в Porcilis® PCV M Hyo (2 мл; в/м) в пределах пары минут после введения вакцины PRRS. Просят в группе 5 (также 12 поросят) не вакцинировали, и они служили в качестве невакцинированных контролей с заражением. Через четыре недели после вакцинации всех поросят заражали интраназальным (и/н) путем с использованием гетерологичного вирулентного штамма PRRSV типа 1 (изолят 2).
После заражения определяли следующие параметры: клинические признаки, ректальная температура и виремия PRRSV и серология.
Не наблюдалось клинических признаков, связанных с заражением PRRSV, ни водной из групп.
Ректальную температуру измеряли в течение 12 суток, начиная с одних суток до заражения и до 10 суток после заражения. Не наблюдали каких–либо значимых отличий между какими–либо из вакцинированных групп. Ректальная температура всех вакцинированных против PRRS групп была более низкой по сравнению с контрольной группой в несколько моментов времени после заражения. Отсутствовали как статистические отличия между группами, вакцинированными в/м или в/д, так и между группами, в которых вводили Porcilis® PRRS отдельно или Porcilis PRRS в комбинации с лиофилизированными Lawsonia, восстановленными в Porcilis® PCV M Hyo.
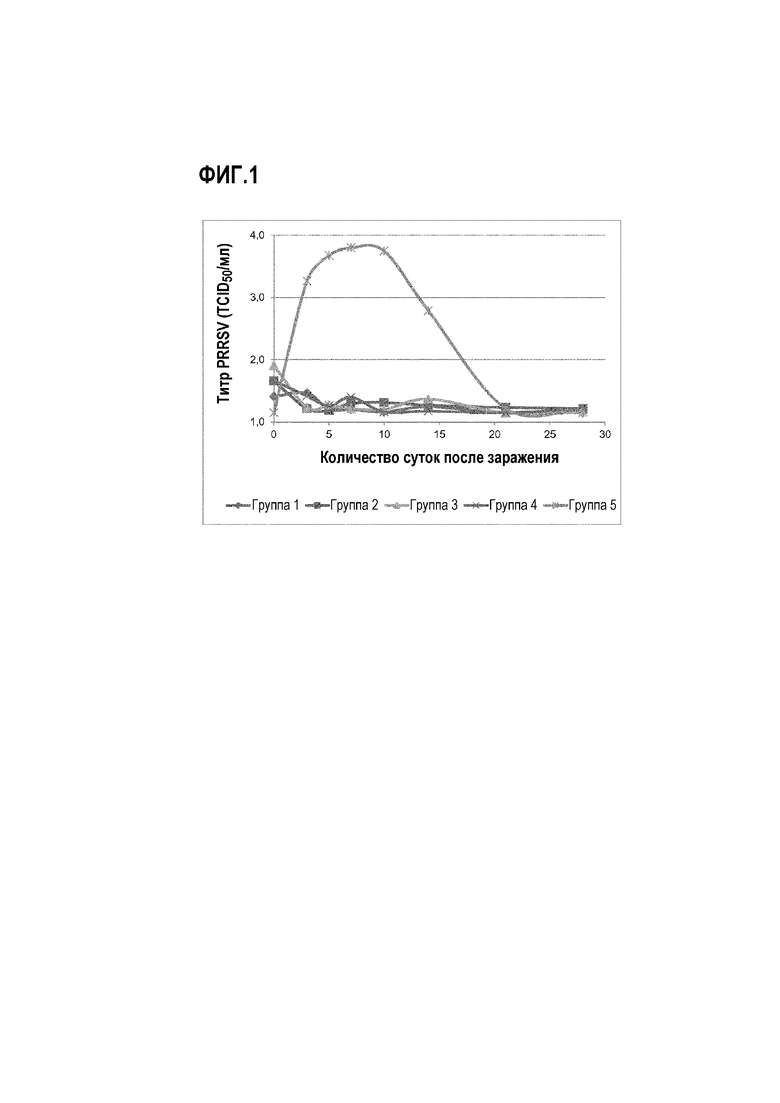
Значительное уменьшение виремии PRRSV по сравнению с невакцинированными контролями было выявлено, когда поросят вакцинировали Porcilis® PRRS и когда поросят вакцинировали Porcilis® PRRS в комбинации с вакцинацией лиофилизированными Lawsonia, восстановленными в Porcilis® PCV M Hyo (фиг.1). Не было обнаружено значимых отличий между однократным и не смешанным ассоциированным применением Porcilis® PRRS при введении в/м или в/д путем.
Все вакцинированные группы продемонстрировали титр антител против PRRSV через 4 недели после вакцинации в день заражения, в то время как контрольная группа не продемонстрировала его. Через четыре недели после заражения все группы продемонстрировали титр антител против PRRSV и титр в вакцинированных группах был более высоким, чем в день заражения. Не было выявлено статистически значимых отличий между однократным и не смешанным ассоциированным применением Porcilis® PRRS при введении в/м или в/д путем.
В заключение, сопутствующее введение лиофилизированных Lawsonia, восстановленных в Porcilis® PCV M Hyo. не имело отрицательного эффекта на вакцинацию посредством Porcilis® PRRS либо в/м, либо в/д путем. Было неожиданным, что ассоциированное применение тройной вакцины Lawsonia–PCV–Mhyo совсем не имело отрицательного эффекта на эффективность вакцины PRRS (см. исследование 5).
ИССЛЕДОВАНИЕ 2: Исследование эффективности в отношении PCV2 при ассоциированном не смешанном применении Porcilis® PCV MHyo с иммуногеном Lawsonia, восстановленном в ней, и Porcilis® PRRS.
Всего 45 поросят с от низкого до умеренного титра материнских антител против PCV2 (< 5,5 log2), без вирусной нагрузки PCV2 и без титров антител против PRRSV распределяли на 3 группы введения: 3 группы по 15 поросят в каждой. Поросят вакцинировали один раз в возрасте 3 недель. Поросят в группе 1 и 2 вакцинировали Lawsonia FD, растворенным в Porcilis PCV M Hyo, в обоих случаях в однократной дозе (внутримышечный путь; в/м) и поросят из группы 1 также вакцинировали приблизительно в то же время Porcilis PRRS (посредством как внутримышечного, так и внутридермального пути; в/м и в/д). Животные из группы 3 оставались невакцинированными (контроль).
В возрасте 5 недель (через 2 недели после вакцинации), каждое животное инфицировали с использованием вируса PCV2 дикого типа, внесенного интраназально. Через 21 сутки после заражения всех животных умерщвляли и получали образцы лимфатических узлов, миндалевидных желез и легких для обнаружения PCV2.
Взятие образцов сыворотки проводили в момент вакцинации, через одни сутки после заражения, через 2 и 3 недели после заражения. Образцы исследовали в отношении антител против PCV2 и вирусной нуклеиновой кислоты. Мазки фекалий и из носовой полости, взятые за одни сутки до заражения, через 2 и 3 недели после заражения, исследовали в отношении вирусной нуклеиновой кислоты.
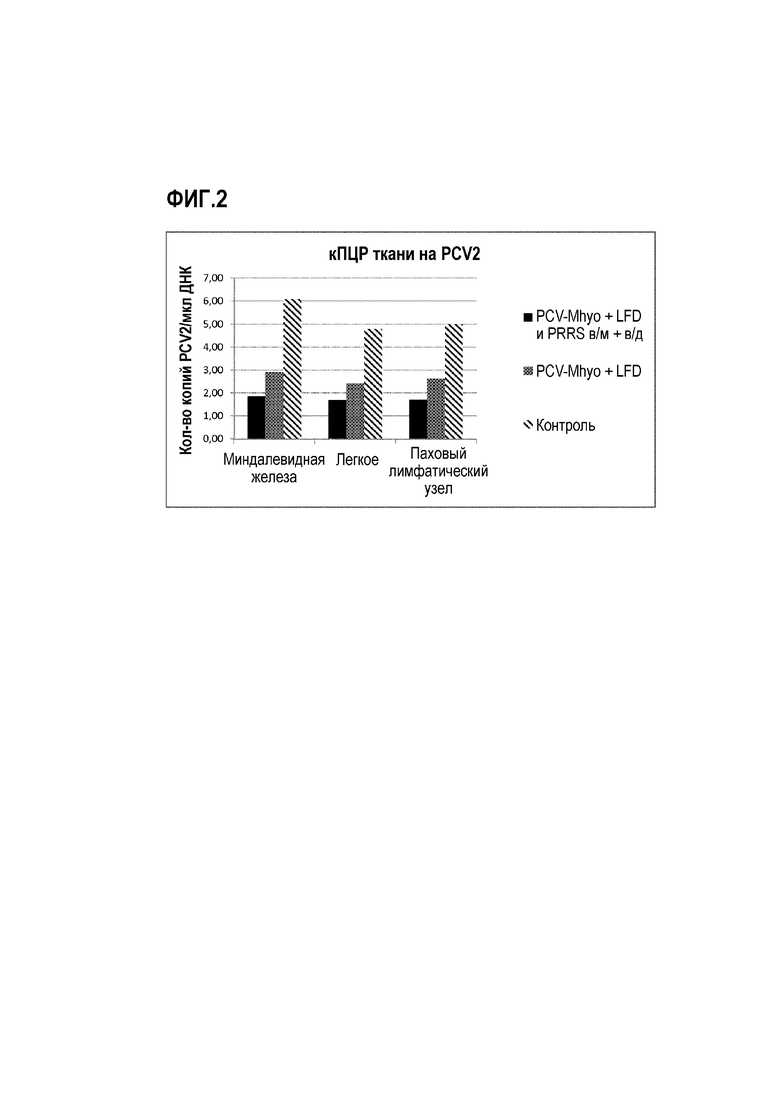
Серология продемонстрировала, что в обеих вакцинированных группах образовывались антитела против PCV2 на сравнимом уровне (6 log2) в момент заражения, в то время как уровень антител в контрольной группе был значительно снижен. После заражения уровень антител в вакцинированной группе возрос до приблизительно 13 log2 при определении через 3 недели после заражения. В контрольной группе в этот момент времени уровень составлял 5 log2. После заражения вирусную нуклеиновую кислоту можно было обнаружить у контрольных животных в сыворотке, мазках из носа и фекалий. У вакцинированных животных уровень был существенно более низким. В образцах фекалий животные, вакцинированные обеими вакцинами, не имели поддающихся обнаружению уровней вирусной нуклеиновой кислоты, что указывает на то, что эта группа была наилучшим образом защищена от заражения PCV2. Это неожиданно открытие возможной улучшенной защиты было подтверждено посредством количественного определения с использованием кПЦР в ткани, как можно видеть на фиг.2 (что соответствует копиям PCV2, найденным в миндалевидных железах, легких и паховых лимфатических узлах, соответственно, слева направо). Наиболее низкие величины вирусной нагрузки стабильно обнаруживались у животных, которым вводили обе вакцины (левые столбики), которые были даже более низкими, чем у животных, которым вводили коммерческую вакцину против PCV Porcilis® PCV M Hyo (средние столбики), которые, тем не менее, были значительно более низкими, чем у контролей (правые столбики).
ИССЛЕДОВАНИЕ 3 : Эффективность лиофилизированных Lawsonia, восстановленных в Porcilis® PCV M Hyo, использованных совместно с Porcilis® PRRS у свиней, против заражения Lawsonia.
Для этого исследования использовали семьдесят пять поросят в возрасте 3 недель, подразделенных на три группы. Группу 1 вакцинировали лиофилизированным антигеном Lawsonia, восстановленным в Porcilis® PCV M Hyo (2 мл, в/м), введенным одновременно (в пределах 1 часа) с Porcilis® PRRS (2 мл в/м+0,2 мл в/д), группу 2 вакцинировали лиофилизированным антигеном Lawsonia, восстановленным в Porcilis PCV M Hyo (2 мл, в/м) и группу 3 оставляли в качестве невакцинированных контролей. В возрасте 7 недель (4 недели после вакцинации) всех поросят перорально заражали гомогенизированной инфицированной Lawsonia слизистой оболочкой кишечника. После заражения свиней наблюдали каждые сутки в отношении клинических признаков. Проводили взятие образцов сыворотки крови (для серологии) и фекалий (для кПЦР) через регулярные промежутки времени до и после заражения. Через три недели после заражения свиней умерщвляли и проводили посмертное исследование. Кишечник проверяли под микроскопом в отношении инфекции Lawsonia intracellularis и образцы подвздошной кишки собирали для кПЦР и (иммуно)гистологической оценки.
В день вакцинации большинство свиней были серонегативными по Lawsonia, в то время как остальные имели титр антител от низкого до умеренного. После вакцинации титр в группах 1 и 2 продемонстрировал сходное повышение титра антител, в то время как контроли продемонстрировали небольшое уменьшение, и у них сохранялся низкий уровень. В день вакцинации свиньи имели титры материнских антител против PCV от низких до умеренных. После вакцинации титр антител против PCV в группах 1 и 2 продемонстрировал сходное повышение, в то время как контроли продемонстрировали снижение уровня материнских антител. В день вакцинации свиньи были серонегативными в отношении Mhyo и PRRSv. После вакцинации группы 1 и 2 продемонстрировали сходный антительный ответ на Mhyo, в то время как контрольная группа 3 оставалась серонегативной до конца испытания. Группа 1 отвечала на вакцинацию PRRS, в то время как группы 2 и 3 оставались серонегативными до заражения.
Результаты для различных параметров после заражения Lawsonia обобщенно представлены в таблице 1 ниже (Данные ПЦР в log10 пг ДНК/мкл на 21 сутки после заражения).
Таблица 1.
Из результатов можно сделать заключение, что лиофилизированный антиген Lawsonia, растворенный в Porcilis® PCV M Hyo, введенный одновременно с Porcilis® PRRS (группа 1), индуцировал значительную защиту против инфекции Lawsonia через 4 недели после вакцинации. Это было продемонстрировано посредством значительного уменьшения выделения микроорганизма, инфекции (кПЦР слизистой оболочки подвздошной кишки), макроскопических показателей повреждения подвздошной кишки, а также микроскопических показателей повреждения подвздошной кишки. Не наблюдалось отрицательного влияния Porcilis® PRRS на эффективность Lawsonia. Напротив, группа ассоциированного смешанного применения имела тенденцию к лучшим упомянутым выше параметрам.
Исследование 4 : Эффективность ассоциированного не смешанного применения Porcilis® PCV M Hyo с лиофилизированными Lawsonia, восстановленными в ней, с Porcilis® PRRS у поросят SPF в возрасте трех недель против заражения M. hyopneumoniae через 4 недели после вакцинации.
Для этого исследования использовали сто поросят из свободного от M. hyopneumoniae и PRRS стада в возрасте 3 недель в группах по 25 животных. Одну группу вакцинировали в/м посредством Porcilis® PCV M Hyo+лиофилизированные Lawsonia и одновременно посредством Porcilis® PRRS (в/м+в/д; см. в настоящем описании выше); одну группу вакцинировали посредством Porcilis® PCV M Hyo и приблизительно в то же время (в пределах 1 часа) посредством Porcilis® PRRS (в/м+в/д) и одну группу вакцинировали посредством Porcilis® PCV M Hyo; четвертую группу не вакцинировали, и она служила в качестве контроля заражения. Через четыре недели после вакцинации всех животных инфицировали вирулентным штаммом M. hyopneumoniae и через три недели всем животным проводили посмертное исследование в отношении очагов повреждения в легких.
Все животные были серологически негативными в отношении M. hyopneumoniae при вакцинации, и невакцинированные животные оставались серологически негативными до заражения. Вакцинированные группы продемонстрировали сходные серологические ответы против M. hyopneumoniae через четыре недели после вакцинации и три недели после заражения.
Для всех вакцинированных групп наблюдали значительное уменьшение показателя повреждения по сравнению с невакцинированными животными. Животные, которых вакцинировали Porcilis® PCV M Hyo+лиофилизированные Lawsonia одновремено с Porcilis® PRRS имели снижение 90%, животные, вакцинированные Porcilis® PCV M Hyo одновременно с Porcilis® PRRS имели снижение 95%. Porcilis® PCV M Hyo индуцировала 100% уменьшение среднего показателя повреждений M. hyopneumoniae. Отличия между вакцинированными группами не были значимыми.
Можно сделать заключение, что ассоциированное не смешанное применение Porcilis® PCV M Hyo отдельно или в комбинации с лиофилизированным антигеном Lawsonia и Porcilis® PRRS является эффективным в отношении сокращения индуцированных M. hyopneumoniae очагов повреждения в легких.
ИССЛЕДОВАНИЕ 5 : Эффект применения инактивированной вакцины против PCV в отношении эффективности живой вакцины против PRRS
В этом эксперименте исследовали эффект смешения первой вакцины, содержащей не реплицирующийся иммуноген цирковируса свиней 2 типа (CircoFLEX, Boehringer Ingelheim), и второй вакцины, содержащей живой аттенуированный вирус репродуктивного и респираторного синдрома свиней (Ingelvac PRRS, Boehringer Ingelheim). Поскольку выживаемость живого вируса PRRS является основным ключевым параметром при смешении этих двух вакцин, исследовали выживаемость вируса PRRS после инкубации в течение 1, 2 и 4 часов.
На сутки –1 клетки MA104 высевали в количестве 105 клеток/мл и помещали в лунки в количестве 225 мкл на лунку. Эти клетки поддерживали при 37°C на воздухе с содержанием диоксида углерода 5%. На 0 сутки Ingelvac PRRS предварительно разбавляли в PBS до титра 5,3 log10 TCID50/мл. Эту смесь либо разбавляли посредством PBS (контроль), либо разбавляли посредством CircoFLEX (две различных партии) до конечного титра 5,0 log10 TCID50/мл. Конечные смеси инкубировали при комнатной температуре в течение 1, 2 и 4 часов для имитации реальных условий в хлеву при вакцинации вновь смешанной комбинированной вакциной. После этого 25 мкл каждой из инкубированных смесей инкубировали в клетках MA 104 в течение 7 суток при 37°C и 5% диоксиде углерода для выращивания вируса PRRS. На 7 сутки проводили определение вируса PRRS. Данные приведены в настоящем описании ниже в таблице 2.
Таблица 2 Титр PRRS в 10 log TCID50/мл после инкубации с PCV
Как можно видеть из таблицы, вирус PRRS утрачивает жизнеспособность в результате кратковременной инкубации с вакциной PCV при комнатной температуре. Снижение тира вакцины будет негативно влиять на эффективность вакцины.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНАЦИЯ ВАКЦИН ДЛЯ ПРОФИЛАКТИЧЕСКОГО ЛЕЧЕНИЯ СВИНЕЙ | 2021 |
|
RU2834834C1 |
| ВАКЦИНА ПРОТИВ ЦИРКОВИРУСА СВИНЕЙ 2 ТИПА | 2014 |
|
RU2712155C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ ВНУТРИКОЖНОГО ВВЕДЕНИЯ | 2020 |
|
RU2835620C1 |
| ВАКЦИНА ДЛЯ ВНУТРИКОЖНОГО ПРИМЕНЕНИЯ ПРОТИВ ИНФЕКЦИИ ВИРУСА PCV2 И PRRS | 2017 |
|
RU2746127C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА ДЛЯ СВИНЕЙ | 2017 |
|
RU2761453C2 |
| ВАКЦИНА ПРОТИВ LAWSONIA INTRACELLULARIS И СВИНОГО ЦИРКОВИРУСА 2-ГО ТИПА | 2014 |
|
RU2672251C1 |
| КОМБИНИРОВАННАЯ ВАКЦИНА PCV/MYCOPLASMA HYOPNEUMONIAE | 2013 |
|
RU2615443C2 |
| ВАКЦИНА ДЛЯ ЗАЩИТЫ ОТ LAWSONIA INTRACELLULARIS, MYCOPLASMA HYOPNEUMONIAE, ЦИРКОВИРУСА СВИНЕЙ | 2009 |
|
RU2496520C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА PCV/MYCOPLASMA HYOPNEUMONIAE/PRRS (PCV/MYCOPLASMA HYOPNEUMONIAE/PRRS COMBINATION VACCINE) | 2013 |
|
RU2644256C2 |
| ВАКЦИНА ПРОТИВ МИКОПЛАЗМЫ И PRRSV | 2007 |
|
RU2408386C2 |
Настоящее изобретение относится к способу профилактического лечения животного против инфекции цирковирусом свиней 2 типа (PCV2), инфекции Mycoplasma hyopneumoniae и инфекции вирусом репродуктивно–респираторного синдрома (PRRS) посредством ассоциированного несмешанного введения первой вакцины, содержащей нереплицирующийся иммуноген цирковируса свиньи 2 типа (PCV2) и нереплицирующийся иммуноген Mycoplasma hyopneumoniae, и второй вакцины, содержащей живой аттенуированный вирус репродуктивно–респираторного синдрома (PRRS) животному. Данный способ позволяет усилить защиту от PCV2 при введении PRRS ассоциированным несмешиваемым способом. 2 н. и 7 з.п. ф-лы, 2 ил., 2 табл., 5 пр.
1. Способ профилактического лечения животного против инфекции цирковирусом свиней 2 типа, инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS посредством ассоциированного несмешанного введения животному первой вакцины, содержащей нереплицирующийся иммуноген цирковируса свиньи 2 типа (PCV2) и нереплицирующийся иммуноген Mycoplasma hyopneumoniae, и второй вакцины, содержащей живой аттенуированный вирус репродуктивно–респираторного синдрома (PRRS), причем нереплицирующийся иммуноген PCV2 представляет собой рекомбинантно экспрессируемый белок, кодируемый геном ORF2, PCV2, и причем нереплицирующийся иммуноген Mycoplasma hyopneumoniae содержит убитые целые Mycoplasma hyopneumoniae.
2. Способ по п. 1, отличающийся тем, что ассоциированное несмешанное введение происходит одновременно.
3. Способ по любому из пп. 1 или 2, отличающийся тем, что вторую вакцину вводят в дерму животного.
4. Способ по любому из пп. 1-3, отличающийся тем, что первая вакцина содержит нереплицирующийся иммуноген Lawsonia intracellularis.
5. Способ по п. 4, отличающийся тем, что иммуноген Lawsonia intracellularis добавляют к первой вакцине в пределах 24 часов до введения вакцины.
6. Способ по п. 5, отличающийся тем, что иммуноген Lawsonia intracellularis содержит лиофилизированные убитые цельные клетки Lawsonia intracellularis.
7. Способ по любому из пп. 1-6, отличающийся тем, что первую и вторую вакцину вводят посредством однократной дозы.
8. Способ по п. 1, отличающийся тем, что нереплицирующийся иммуноген PCV2 представляет собой экспрессируемый бакуловирусом белок PCV2.
9. Способ профилактического лечения животного против инфекции цирковирусом свиней 2 типа (PCV2), инфекции Mycoplasma hyopneumoniae и инфекции вирусом PRRS посредством ассоциированного несмешанного введения первой вакцины, содержащей нереплицирующийся иммуноген цирковируса свиней 2 типа и нереплицирующийся иммуноген Mycoplasma hyopneumoniae, и второй вакцины, содержащей живой аттенуированный вирус PRRS.
| FLEXFAMILY Mixing Guides", 11 March 2016 (2016-03-11), http://www.bi-vetmedica.com/sites/default/files/dam/internet/ah/vetmedica/com_EN/images/swine/FLEX%20Family%20Mixing%20Guide.pdf XP002773133, весь документ | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| ВАКЦИННАЯ КОМПОЗИЦИЯ ПРОТИВ РЕПРОДУКТИВНОГО И РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ (PRRS) И СПОСОБ ЕЕ ПОЛУЧЕНИЯ, СПОСОБ ИММУНИЗАЦИИ СВИНЕЙ | 1996 |
|
RU2166327C2 |
| ИНСТРУКЦИЯ по применению вакцины "Порцилис PCV M Hyo" (Вакцина против | |||
Авторы
Даты
2021-10-05—Публикация
2018-04-12—Подача