ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к области фармацевтических композиций для лечения патологических состояний, связанных с диабетом. Более конкретно, настоящее изобретение предусматривает фармацевтические композиции, содержащие ацилированное производное длительного действия аналога инсулина человека, и медицинское применение таких композиций для терапии путем введения базального инсулина.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Первичная цель инсулинотерапии при лечении метаболических расстройств заключается в получении гликемии на устойчивом близком к нормальному уровне путем замены или дополнения секреции эндогенного инсулина физиологическим образом, насколько это возможно, в послеобеденное время, а также между приемами пищи и в течение ночи. Разделение потребностей в базальном и связанном с приемом пищи (болюсный) инсулином представляет собой систематический подход в отношении подкожной инсулинотерапии.
Наиболее значимые фармакологические характеристики любого указанного инсулина - начало действия, профиль максимального эффекта, продолжительность действия и т.д., - главным образом определяются кинетикой его всасывания из места подкожной инъекции в системный кровоток.
Нековалентная опосредованная цинком олигомеризация представляет собой хорошо описанное свойство инсулиновых продуктов. При физиологическом значении рН инсулин человека растворим, но обладает тенденцией к самосборке в четко определенные гексамеры (т.е. частицу из шести единиц инсулина) путем координации двух ионов цинка (Zn++) с участками связывания с высокой аффинностью (B10His). Также хорошо известно, что фенольные лиганды, особенно фенол, специфически связываются с гексамером инсулина и способствуют образованию R-состояния гексамера. После инъекции фенольные лиганды быстро диффундируют из места инъекции. В отсутствие фенола в месте инъекции конформапия и размер олигомера инсулина могут изменяться, также как и вязкость инсулинсодержащего раствора, что влияет на профиль пролонгированного действия.
В Jonassen et al, Pharm. Res. 2012 29 2104-2114 описан механизм продления действия инсулина деглудек, производного инсулина с цепью, апилированной двумя остатками жирной кислоты, для введения один раз в день, и описана корреляция между высокой концентрацией цинка и продлением действия. В WO 2009/115469 описаны различные производные инсулина длительного действия с цепями, апилированными двумя остатками жирной кислоты. В WO 2013/153000 описан состав тех производных инсулина длительного действия для подкожного введения, которые содержат высокий уровень цинка (не менее 3,5 Zn++/шесть молей производных инсулина). Они были сконструированы с целью получения пролонгированной продолжительности действия, соотносящейся с профилем введения один раз в неделю. Высокое содержание Zn++ в составах, описанных в WO 2009/115469, приводит к получению пролонгированного профиля PK.
В WO 2009/063072 раскрыты фармацевтические композиции для парентерального введения, содержащие производное базального инсулина (например, деглудек) и производное GLP-1 (например, лираглутид). Поскольку мономер лираглутида связывается с пинком с образованием дигептамера, в комбинированном составе необходим уровень цинка выше, чем в моносоставе с деглудеком, для достижения сравнимого профиля PK деглудека и достижения приемлемой физической стабильности.
КРАТКОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
В соответствии с настоящим изобретением был разработан новый состав с производными инсулина длительного действия, который способен обеспечивать конформационное состояние и паттерн олигомеризации, в большей степени близко сходные с таковыми инсулина человека, т.е. гексамерами, особенно гексамерами R6.
В другом аспекте настоящее изобретение предусматривает фармацевтическую композицию, содержащую выбранное производное инсулина длительного действия в уникальной комбинации вспомогательных веществ, внимательно составленную с целью снижения степени образования олигомеров в месте инъекции, которая при этом все еще демонстрирует свойства PK/PD, подходящие для введения один раз в неделю.
В другом аспекте настоящее изобретение предусматривает фармацевтическую композицию со сниженной вязкостью после инъекции и, соответственно, пониженной склонностью к причинению какого-либо дискомфорта после инъекции.
В другом аспекте настоящее изобретение предусматривает фармацевтическую композицию с повышенной стабильностью.
В другом аспекте настоящее изобретение предусматривает фармацевтическую композицию для применения в качестве лекарственного препарата для лечения метаболического расстройства.
Другие цели настоящего изобретения будут очевидны для специалиста в данной области, исходя из следующих подробного описания и примеров.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
В своем первом аспекте настоящее изобретение предусматривает фармацевтическую композицию, содержащую производное инсулина, выбранное из группы, состоящей из
человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30; (соединение 1);
человеческого инсулина А14Е, В16Н, В25Н, B29K(Nεгексадекандиоил-γGlu), desB30 (соединение 2);
человеческого инсулина А14Е, В16Н, В25Н, B29K(Nε-эйкозандиоил-γGlu), desB30 (соединение 3) и
человеческого инсулина А14Е, В25Н, desB27, B29K(Nε-октадекандиоил-γGlu), desB30 (соединение 4), и дополнительно содержащую от приблизительно 1 до приблизительно 2% (вес/вес) глицерина; от приблизительно 45 до приблизительно 75 мМ фенола; от приблизительно 0 до приблизительно 19 мМ м-крезола; от приблизительно 1,5 до приблизительно 2,5 моль ионов цинка на шесть молей указанного производного инсулина; не более приблизительно 75 мМ хлорида натрия; и характеризующуюся значением рН в диапазоне от 7,2 до 8,0.
В другом аспекте настоящее изобретение предусматривает фармацевтические композиции, дополнительно содержащие соединение, представляющее собой инсулинотропный GLP-1, и, в частности, соединение, представляющее собой инсулинотропный GLP-1, известное как семаглутид.
Семаглутид может быть описан с помощью структуры Aib8,Lys26(OEG-OEG-гамма-Glu-C18-дикислота),Arg34)GLP-1 H(7-37)-ОН, которая также может быть обозначена как (N-эпсилон26-[2-(2-{2-[2-(2-{2-[(S)-4-карбокси-4-(17-карбоксигептадеканоиламино)бутириламино]этокси}этокси)ацетиламино]этокси}этокси)ацетил][Aib8, Arg34]CLP-1-(7-37), схожее раскрытие в WO 2006/097537.
Настоящее изобретение может быть дополнительно охарактеризовано с помощью ссылки на один или более приведенных далее признаков или вариантов осуществления.
1. Фармацевтическая композиция по настоящему изобретению, содержащая производное инсулина, которое представляет собой человеческий инсулин А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
2. Фармацевтическая композиция по настоящему изобретению, содержащая производное инсулина, которое представляет собой человеческий инсулин А14Е, В16Н, В25Н, B29K(Nεгексадекандиоил-γGlu), desB30 (соединение 2).
3. Фармацевтическая композиция по настоящему изобретению, содержащая производное инсулина, которое представляет собой человеческий инсулин А14Е, В16Н, В25Н, B29K(Nε-эйкозандиоил-γGlu), desB30 (соединение 3).
4. Фармацевтическая композиция по настоящему изобретению, содержащая производное инсулина, которое представляет собой человеческий инсулин А14Е, В25Н, desB27, B29K(Nε-октадекандиоил-γGlu), desB30 (соединение 4).
5. Фармацевтическая композиция согласно предыдущим вариантам осуществления, где производное инсулина находится в диапазоне от приблизительно 3,5 до приблизительно 5,0 мМ.
6. Фармацевтическая композиция согласно предыдущим вариантам осуществления, где производное инсулина находится в диапазоне от приблизительно 4,0 до приблизительно 4,5 мМ.
7. Фармацевтическая композиция согласно предыдущим вариантам осуществления, где производное инсулина составляет приблизительно 4,2 мМ.
8. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 1 до приблизительно 2% (вес/вес) глицерина.
9. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 1,4 до приблизительно 1,8% (вес/вес) глицерина.
10. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 1,5% или 1,6% (вес/вес) глицерина.
11. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 45 до приблизительно 75 мМ фенола.
12. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 50 до приблизительно 70 мМ фенола.
13. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 55 до приблизительно 65 мМ фенола.
14. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69 или 70 мМ фенола.
15. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 0 до приблизительно 19 мМ м-крезола.
16. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая 0 мМ, 1 мМ, 2 мМ, 3 мМ, 4 мМ м-крезола.
17. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 0 до приблизительно 15 мМ м-крезола.
18. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 5 мМ, 6 мМ, 7 мМ, 8 мМ, 9 мМ, 10 мМ, 11 мМ, 12 мМ, 13 мМ, 14 мМ, 15 мМ, 16 мМ, 17 мМ, 18 мМ или 19 мМ м-крезола.
19. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 1,5 до приблизительно 2,5 моль ионов цинка на шесть молей производного инсулина.
20. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 2,0 до приблизительно 2,4 моль ионов цинка на шесть молей производного инсулина.
21. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 2,0 или 2,1 моль ионов цинка на шесть молей производного инсулина.
22. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 2,2 или 2,3 моль ионов цинка на шесть молей производного инсулина.
23. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 2,4 или 2,5 моль ионов цинка на шесть молей производного инсулина.
24. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая менее приблизительно 75 мМ хлорида натрия.
25. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 5 до приблизительно 50 мМ хлорида натрия.
26. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 10 до приблизительно 25 мМ хлорида натрия.
27. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 15 до приблизительно 25 мМ хлорида натрия.
28. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 20 мМ, 50 мМ или 75 мМ хлорида натрия.
29. Фармацевтическая композиция согласно предыдущим вариантам осуществления, которая характеризуется значением рН в диапазоне от 7,2 до 8,0.
30. Фармацевтическая композиция согласно предыдущим вариантам осуществления, которая характеризуется значением рН в диапазоне от 7,2 до 7,6.
31. Фармацевтическая композиция согласно предыдущим вариантам осуществления, которая характеризуется значением рН приблизительно 7,2, 7,3, 7,4, 7,5, 7,6, 7,7, 7,8 или 7,9.
32. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
от приблизительно 4,0 до приблизительно 4,5 мМ производного инсулина;
от приблизительно 1 до приблизительно 2% (вес/вес) глицерина;
от приблизительно 50 до приблизительно 70 мМ фенола;
от приблизительно 0 до приблизительно 15 мМ м-крезола;
от приблизительно 2,0 до приблизительно 2,5 моль ионов цинка на шесть молей производного инсулина;
менее приблизительно 50 мМ хлорида натрия и
которая характеризуется значением рН в диапазоне от 7,2 до 7,6.
33. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
приблизительно 4,2 мМ производного инсулина;
приблизительно 1,5% (вес/вес) глицерина;
приблизительно 60 мМ фенола;
приблизительно 0 мМ м-крезола;
приблизительно 2,0 моль ионов цинка на шесть молей производного инсулина;
приблизительно 20 мМ хлорида натрия и
которая характеризуется значением рН приблизительно 7,4.
34. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
приблизительно 4,2 мМ производного инсулина;
приблизительно 1,5% (вес/вес) глицерина;
приблизительно 60 мМ фенола; приблизительно 10 мМ м-крезола;
приблизительно 2,0 моль ионов цинка на шесть молей производного инсулина;
приблизительно 20 мМ хлорида натрия и
которая характеризуется значением рН приблизительно 7,4.
35. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
приблизительно 4,2 мМ производного инсулина;
приблизительно 1,5% (вес/вес) глицерина;
приблизительно 60 мМ фенола;
приблизительно 0 мМ м-крезола;
приблизительно 2,2 моль ионов цинка на шесть молей производного инсулина;
приблизительно 20 мМ хлорида натрия и
которая характеризуется значением рН приблизительно 7,4.
36. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
приблизительно 4,2 мМ производного инсулина;
приблизительно 1,5% (вес/вес) глицерина;
приблизительно 60 мМ фенола;
приблизительно 10 мМ м-крезола;
приблизительно 2,2 моль ионов цинка на шесть молей производного инсулина;
приблизительно 20 мМ хлорида натрия и
которая характеризуется значением рН приблизительно 7,4.
37. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
приблизительно 4,2 мМ производного инсулина;
приблизительно 1,5% (вес/вес) глицерина;
приблизительно 60 мМ фенола;
приблизительно 0 мМ м-крезола;
приблизительно 2,4 моль ионов цинка на шесть молей производного инсулина;
приблизительно 20 мМ хлорида натрия и
которая характеризуется значением рН приблизительно 7,4.
38. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая
приблизительно 4,2 мМ производного инсулина;
приблизительно 1,5% (вес/вес) глицерина;
приблизительно 60 мМ фенола;
приблизительно 10 мМ м-крезола;
приблизительно 2,4 моль ионов цинка на шесть молей производного инсулина;
приблизительно 20 мМ хлорида натрия и
которая характеризуется значением рН приблизительно 7,4.
39. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 4,2 мМ производного инсулина; от приблизительно 1 до приблизительно 2% (вес/вес) глицерина; от приблизительно 45 до приблизительно 75 мМ фенола; от приблизительно 0 до приблизительно 15 мМ м-крезола; от приблизительно 1,5 до приблизительно 2,5 моль ионов цинка на шесть молей указанного производного инсулина; не более приблизительно 50 мМ хлорида натрия, и которая характеризуется значением рН в диапазоне от 7,2 до 8,0.
40. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 0 мМ м-крезола.
41. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 5 до приблизительно 10 мМ м-крезола.
42. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 10 мМ м-крезола.
43. Фармацевтическая композиция согласно предыдущим вариантам осуществления, дополнительно содержащая семаглутид.
44. Фармацевтическая композиция, содержащая человеческий инсулин А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1) и семаглутид и дополнительно содержащая от приблизительно 1 до приблизительно 2% (вес/вес) глицерина; от приблизительно 45 до приблизительно 75 мМ фенола; 0-15 мМ м-крезола; от приблизительно 1,5 до приблизительно 2,5 моль ионов цинка на шесть молей указанного производного инсулина; не более приблизительно 25 мМ хлорида натрия, и которая характеризуется значением рН в диапазоне от 7,2 до 8,0.
45. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 0,20 до приблизительно 0,70 мМ семаглутида.
46. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 0,30 до приблизительно 0,70 мМ семаглутида.
47. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 3,5 мМ до приблизительно 5,0 мМ человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
48. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая от приблизительно 0,30 до приблизительно 0,70 мМ семаглутида и от приблизительно 3,5 мМ до приблизительно 5,0 мМ человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
49. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 0,30 мМ семаглутида и от приблизительно 3,5 мМ до приблизительно 5,0 мМ человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
50. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 0,40 мМ семаглутида и 4,2 мМ человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
51. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 0,49 мМ или 0,50 мМ семаглутида и 4,2 мМ человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
52. 35. Фармацевтическая композиция согласно предыдущим вариантам осуществления, содержащая приблизительно 0,60 мМ семаглутида и 4,2 мМ человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1).
53. Фармацевтическая (совместный состав) композиция, содержащая человеческий инсулин А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1) и семаглутид и дополнительно содержащая приблизительно 1,5% (вес/вес) глицерина; приблизительно 60 мМ фенола; приблизительно 0 мМ м-крезола; приблизительно 2,2 моль ионов цинка на шесть молей указанного производного инсулина; приблизительно 20 мМ хлорида натрия, и которая характеризуется значением рН приблизительно 7,4.
54. Фармацевтическая (совместный состав) композиция, содержащая человеческий инсулин А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1) и семаглутид и дополнительно содержащая приблизительно 1,5% (вес/вес) глицерина; приблизительно 60 мМ фенола; приблизительно 10 мМ м-крезола; приблизительно 2,2 моль ионов цинка на шесть молей указанного производного инсулина; приблизительно 20 мМ хлорида натрия, и которая характеризуется значением рН приблизительно 7,4.
55. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту при интервалах с меньшей частотой, чем один раз в день (т.е. при интервалах более 24 часов), в течение периода времени, составляющего по меньшей мере 3 месяца, по меньшей мере 6 месяцев или по меньшей мере 1 год.
56. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту с частотой в диапазоне от каждого 2го дня до каждого 11го дня, в среднем.
57. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту с частотой в диапазоне от каждого 3го дня до каждого 10го дня, в среднем.
58. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту с частотой в диапазоне от каждого 4го дня до каждого 9го дня, в среднем.
59. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту с частотой в диапазоне от каждого 5го дня до каждого 8го дня, в среднем.
60. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту с частотой в диапазоне от каждого 6го дня до каждого 7го дня, в среднем.
61. Фармацевтическая композиция согласно предыдущим вариантам осуществления для введения нуждающемуся в этом субъекту один раз в неделю, т.е. каждый 7ой день, в среднем, в течение периода времени, составляющего по меньшей мере 3 месяца, по меньшей мере 6 месяцев или по меньшей мере 1 год.
62. Способ получения инъекционной фармацевтической композиции включает приведенное далее.
(i) Получение раствора путем растворения человеческого инсулина А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 в воде.
(ii) Получение раствора путем растворения консервантов и средств, регулирующих изотоничность, в воде.
(iii) Получение раствора путем растворения ионов цинка в воде.
(iv) Смешивание раствора а) и раствора b).
(v) Добавление раствора с) к раствору а+b.
(vi) Растворение семаглутида в объединенном растворе а+b+с.
(vii) Регулирование рН смеси f) до необходимого значения рН с последующей стерильной фильтрацией.
Любая комбинация из двух или более вариантов осуществления, описанных в данном документе, рассматривается в рамках объема настоящего изобретения.
Биологическая активность
В другом аспекте настоящее изобретение предусматривает фармацевтические композиции, применимые в качестве лекарственных препаратов для лечения метаболических заболеваний, расстройств или состояний и, в частности, заболеваний, расстройств или состояний, связанных с диабетом.
В одном варианте осуществления фармацевтическая композиция по настоящему изобретению предназначена для применения в лечении или облегчении заболевания, расстройства или состояния, связанного с диабетом, диабетом 1 типа, диабетом 2 типа, нарушением толерантности к глюкозе, гипергликемией, дислипидемией, ожирением или метаболическим синдромом (метаболический синдром X, синдром резистентности к инсулину).
В другом варианте осуществления фармацевтическая композиция по настоящему изобретению предназначена для применения в лечении или облегчении заболевания, расстройства или состояния, связанного с диабетом и, в частности, диабетом 1 типа, диабетом 2 типа.
Фактическая доза зависит от природы и тяжести заболевания, подлежащего лечению, и находится в рамках компетенции врача, и может варьироваться путем титрования дозы в отношении конкретных обстоятельств по настоящему изобретению для получения необходимого терапевтического эффекта.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Настоящее изобретение дополнительно проиллюстрировано с помощью ссылки на сопутствующие графические материалы, на которых представлено следующее.
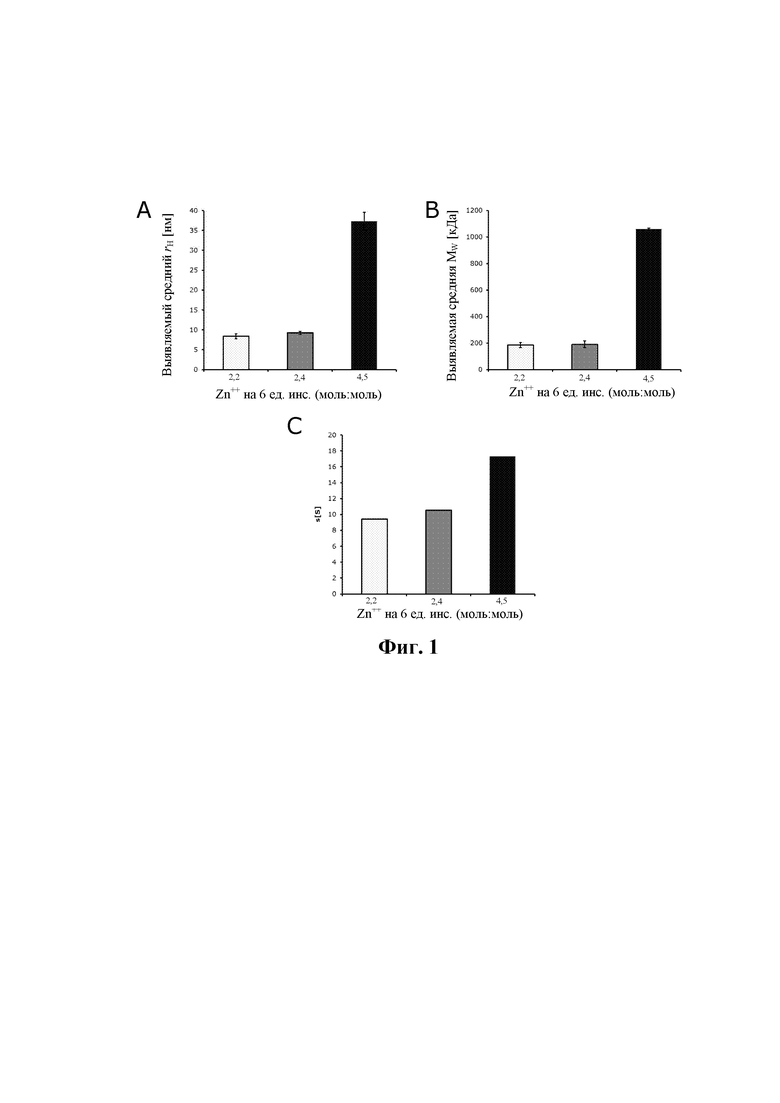
На фиг. 1 показана олигомеризация моносоставов А, В и С на основе соединения 1 при смоделированных условиях в месте инъекции.
Фиг. 1А: выявляемый средний гидродинамический радиус (rH) [нм], измеренный с помощью DLS.
Фиг. 1В: выявляемая средняя молекулярная масса, измеренная с помощью CG-MALS.
Фиг. 1С: выявляемый средний коэффициент седиментации (S), измеренный с помощью AUC.
Белые столбцы: соединение 1, состав С с 2,2 Zn++ на шесть единиц инсулина (моль: моль).
Серые столбцы: соединение 1, состав В с 2,4 Zn++ на шесть единиц инсулина (моль: моль).
Черные столбцы: соединение 1, состав А, содержащий 4,5 Zn++ на шесть единиц инсулина (моль:моль).
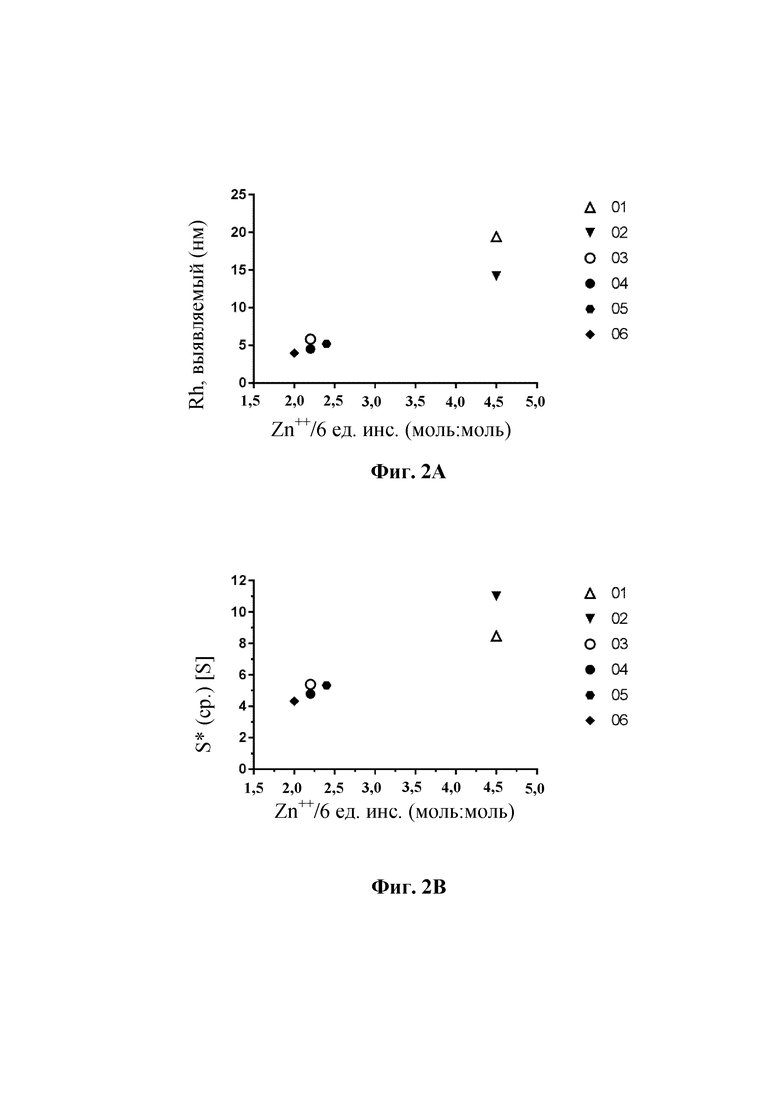
На фиг. 2 показана олигомеризация моносоставов 01-06 на основе соединения 1 при смоделированных условиях в месте инъекции.
Фиг. 2А: выявляемый средний гидродинамический радиус (Rh, ср.) [нм], измеренный с помощью DLS.
Фиг. 2В: выявляемый средний коэффициент седиментации (S*), измеренный с помощью AUC.
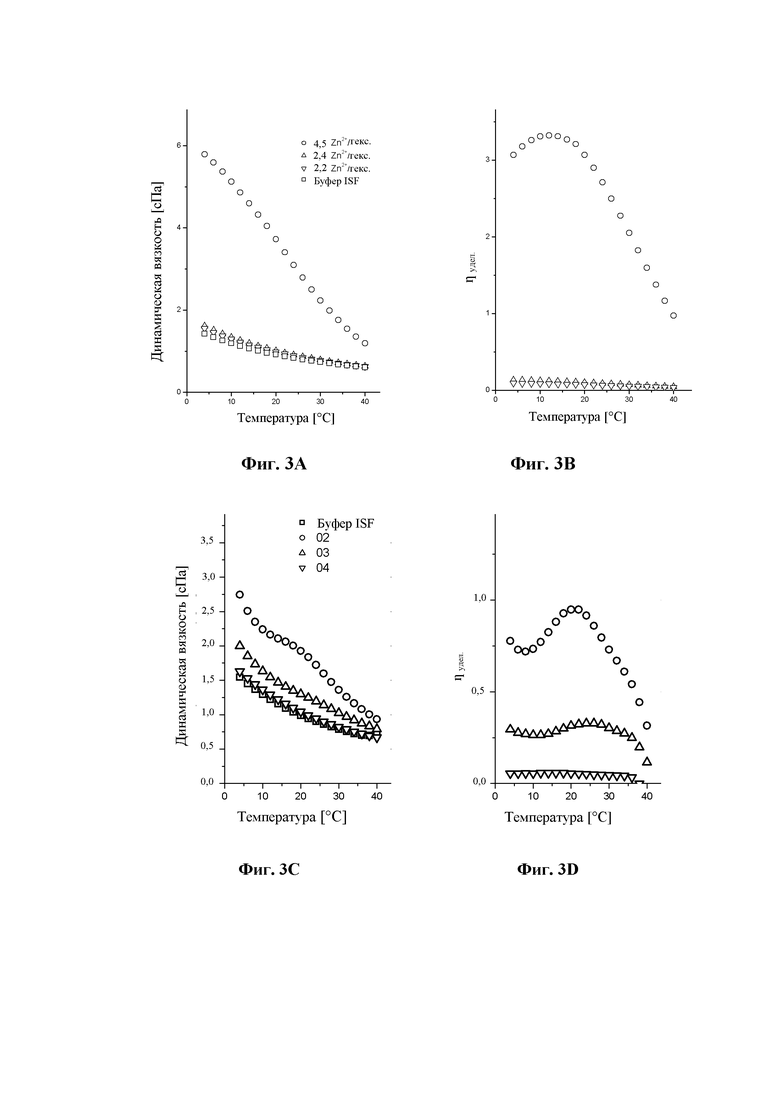
На фиг. 3 показана выявляемая динамическая вязкость [сПа] (фиг. 3А и фиг. 3С) и удельная вязкость [η удел.] (фиг. 3В, фиг. 3D) различных подвергнутых замене буфера составов соединения 1 и буфера интерстициальной жидкости (ISF) в зависимости от температуры [°С].
Фиг. 3А и фиг. 3В: состав А; состав В; состав С; буфер ISF.
Фиг. 3С и фиг. 3D: состав 02; состав 03; состав 04; буфер ISF.
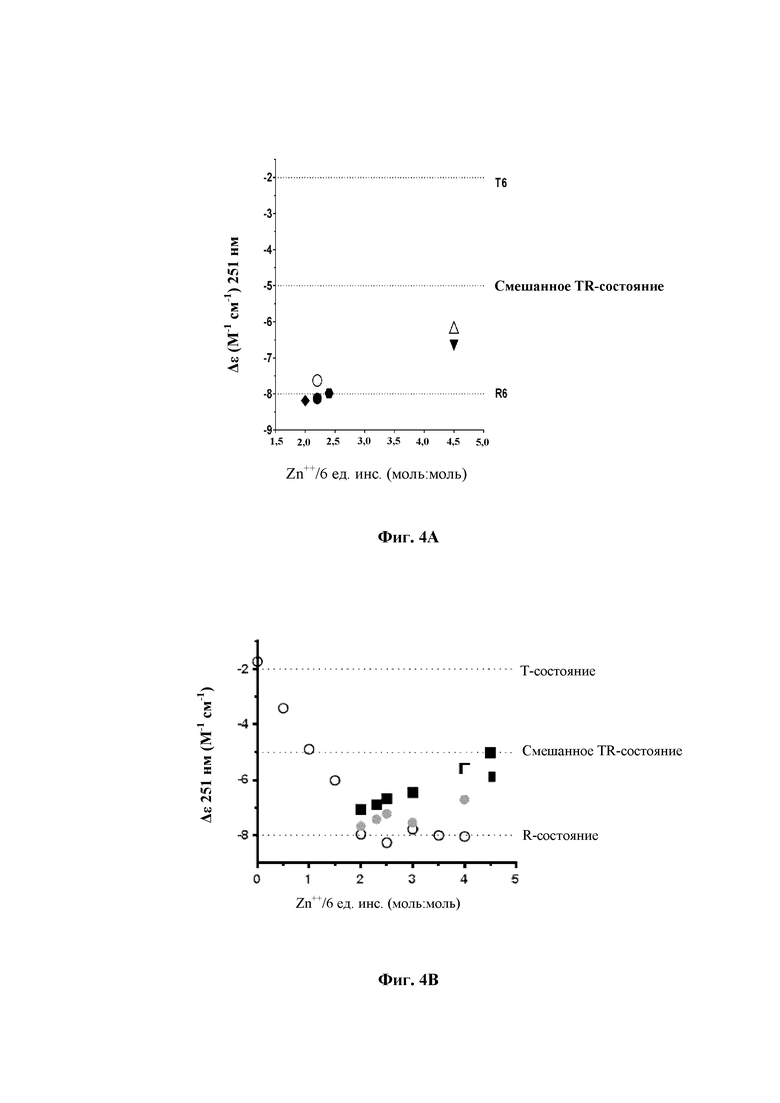
На фиг. 4 показано конформационное состояние соединения 1 в составах.
Фиг. 4А: CD-спектроскопия в близком к УФ спектре [Δε251 нм(М-1 см-1)], демонстрирующий конформапионные изменения (Т-состояние; смешанное TR-состояние; R-состояние) в зависимости от Zn++ на шесть единиц инсулина (моль:моль) для составов 01-06.
Фиг. 4В: CD-спектроскопия в близком к УФ спектре [Δε251 нм(М-1 см-1)], демонстрирующий конформапионные изменения (Т-состояние; смешанное TR-состояние; R-состояние) в зависимости от Zn++ на шесть единиц инсулина (моль:моль) для составов В1-В6, D1-D7 и составов с инсулином человека с различным уровнем цинка.
Незакрашенные круги: инсулин человека (600 нмоль/мл инсулина человека, 30 мМ фенола, 150 мМ NaCl, рН 7,4).
Черные квадраты: соединение 1, составленное с 25 мМ фенола, 25 мМ м-крезола и 20 мМ NaCl.
Серые круги: соединение 1, составленное с 60 мМ фенола, 10 мМ м-крезола и 20 мМ NaCl.
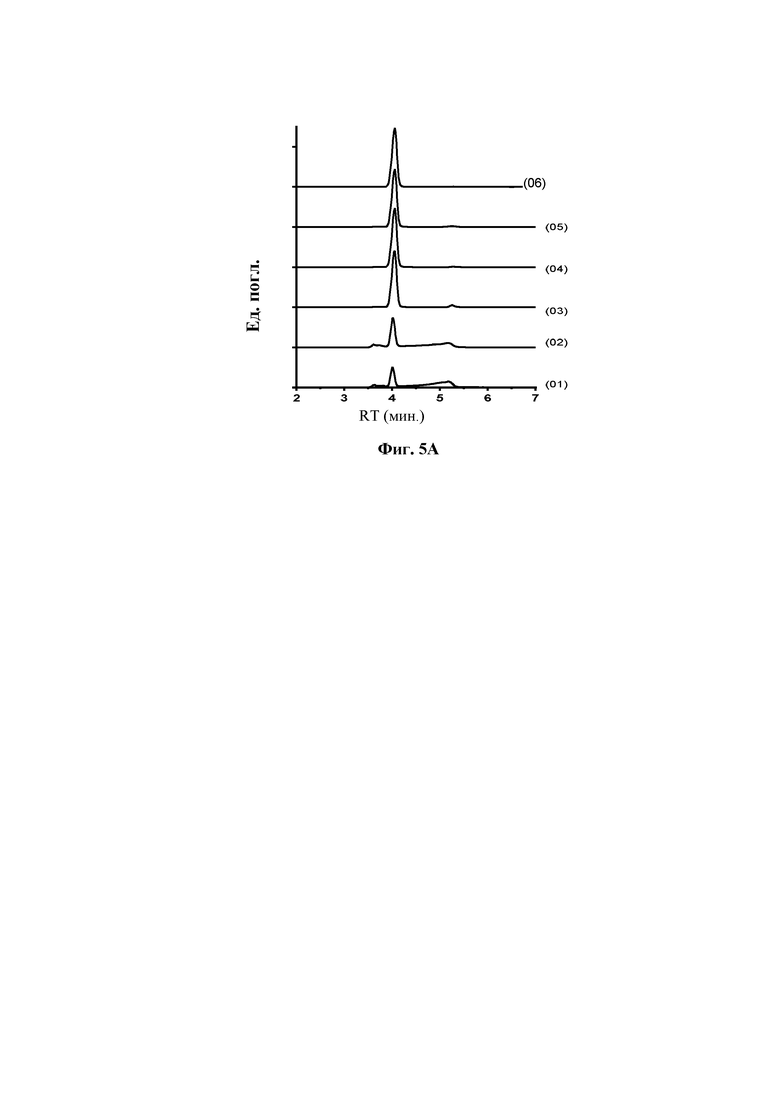
На фиг. 5 показано распределение олигомеров соединения 1 в составах с применением SEC.
На фиг. 5А показана нативная хроматограмма SEC составов 01, 02, 03, 04, 05 и 06.
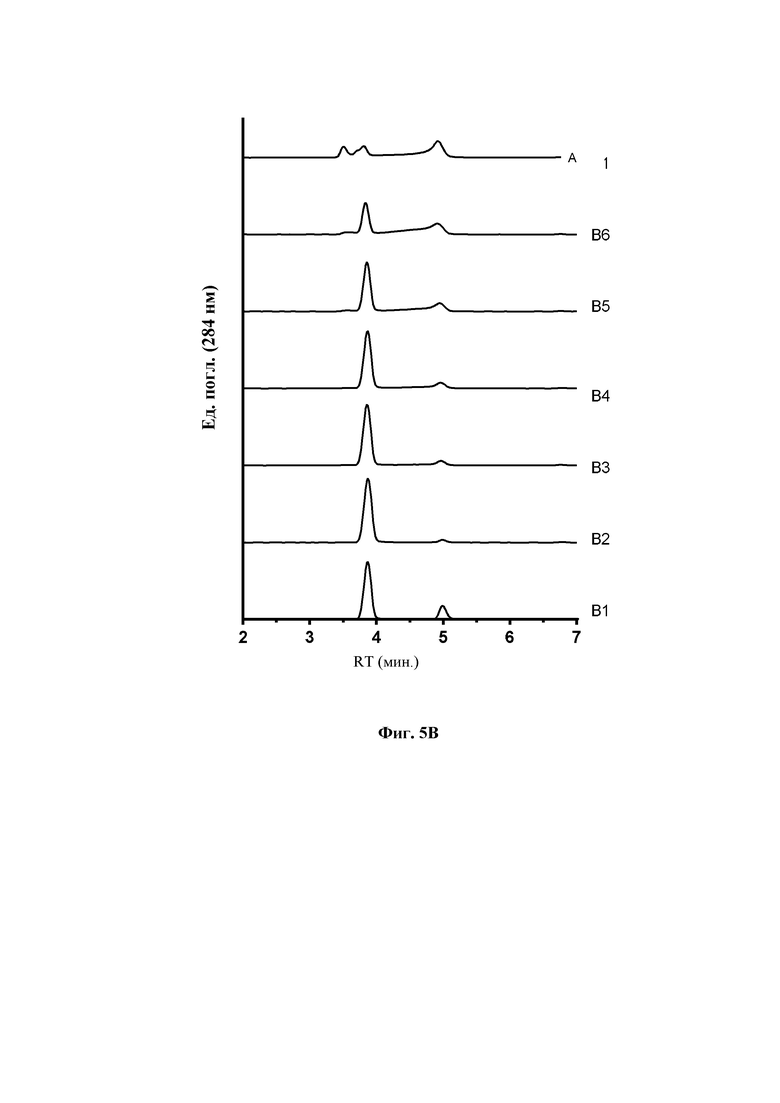
На фиг. 5В показана нативная хроматограмма SEC составов А и В1-В6.
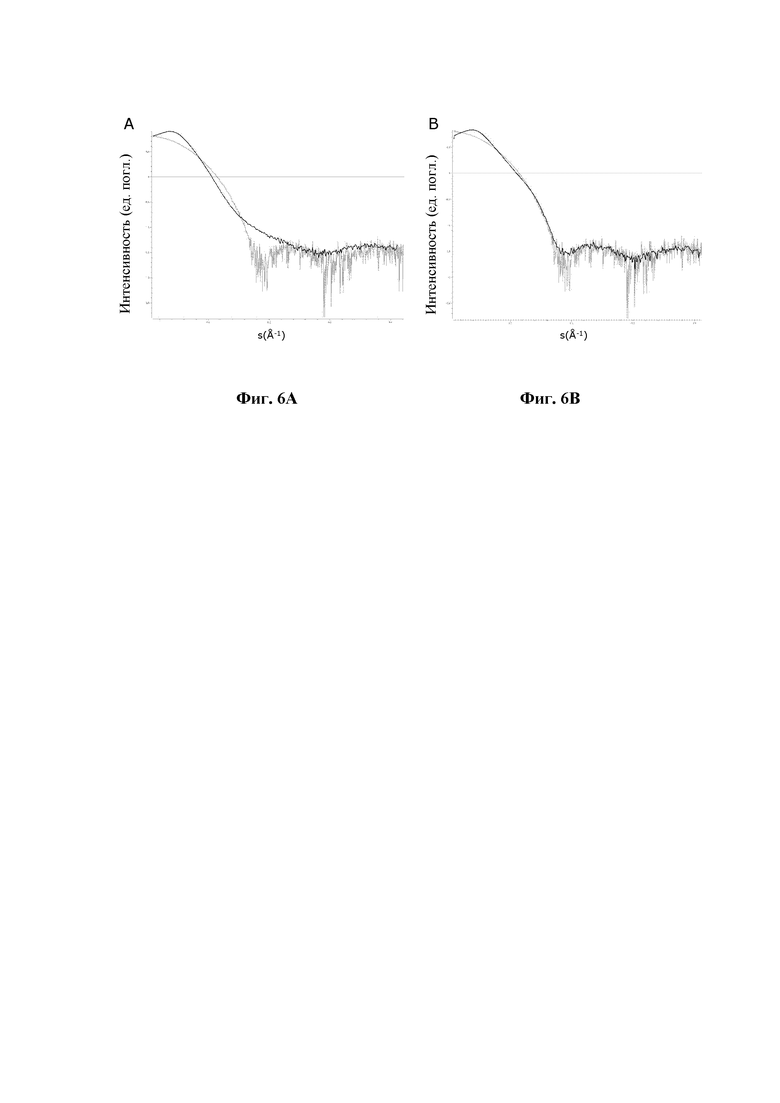
На фиг. 6 показаны данные SAXS-рассеяния [интенсивность (ед. погл.) относительно 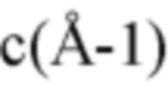 ] соединения 1 и инсулина человека в составленном состоянии.
] соединения 1 и инсулина человека в составленном состоянии.
Фиг. 6А: кривые рассеяния состава А с соединением 1 показаны черным цветом и инсулина человека показаны серым цветом (соединение 1, 4,2 мМ, 4,5 Zn/гексамер; инсулин человека 0,6 мМ, 2,2 Zn/гексамер).
Фиг. 6В: кривые рассеяния состава С с соединением 1 показаны черным цветом и инсулина человека показаны серым цветом (соединение 1, 4,2 мМ, 2,2 Zn/гексамер; инсулин человека 0,6 мМ, 2,2 Zn/гексамер (R6-гексамер)).
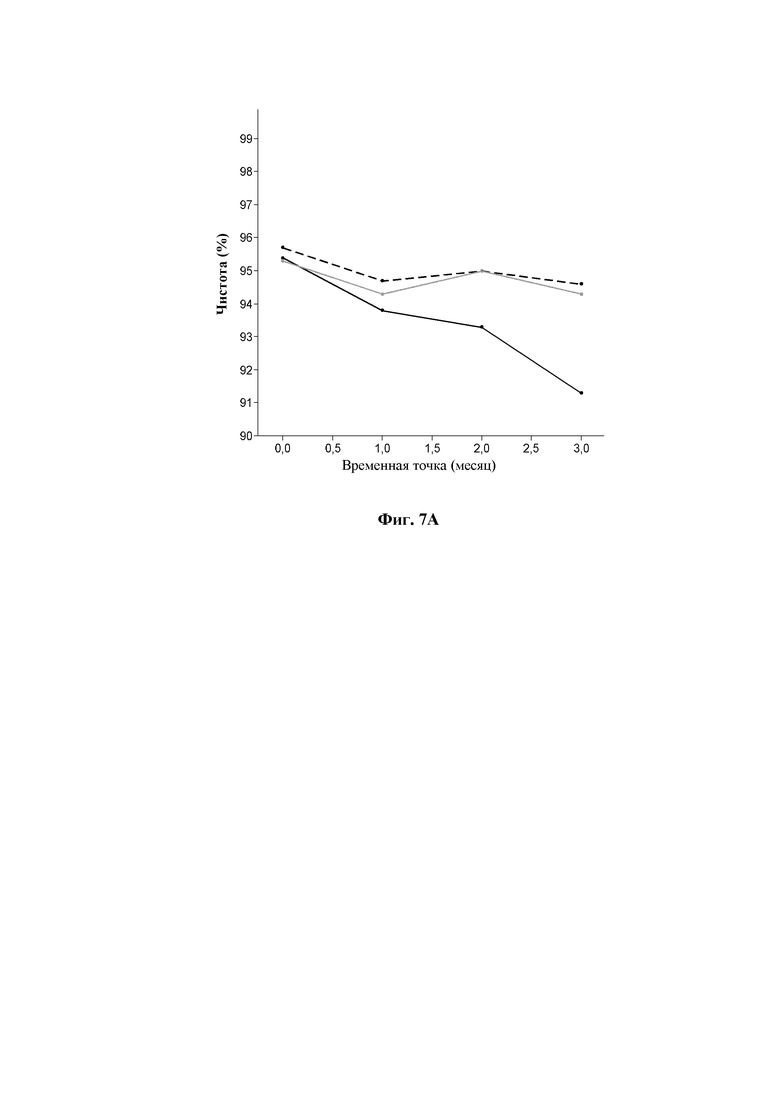
На фиг.7 показана чистота соединения 1 в составах.
На фиг.7А показана чистота (% общего пептида) при хранении при 30°С [временная точка (месяц)] для состава А (черная линия), состава В (серая линий) и состава С (пунктирная линия) с соединением 1.
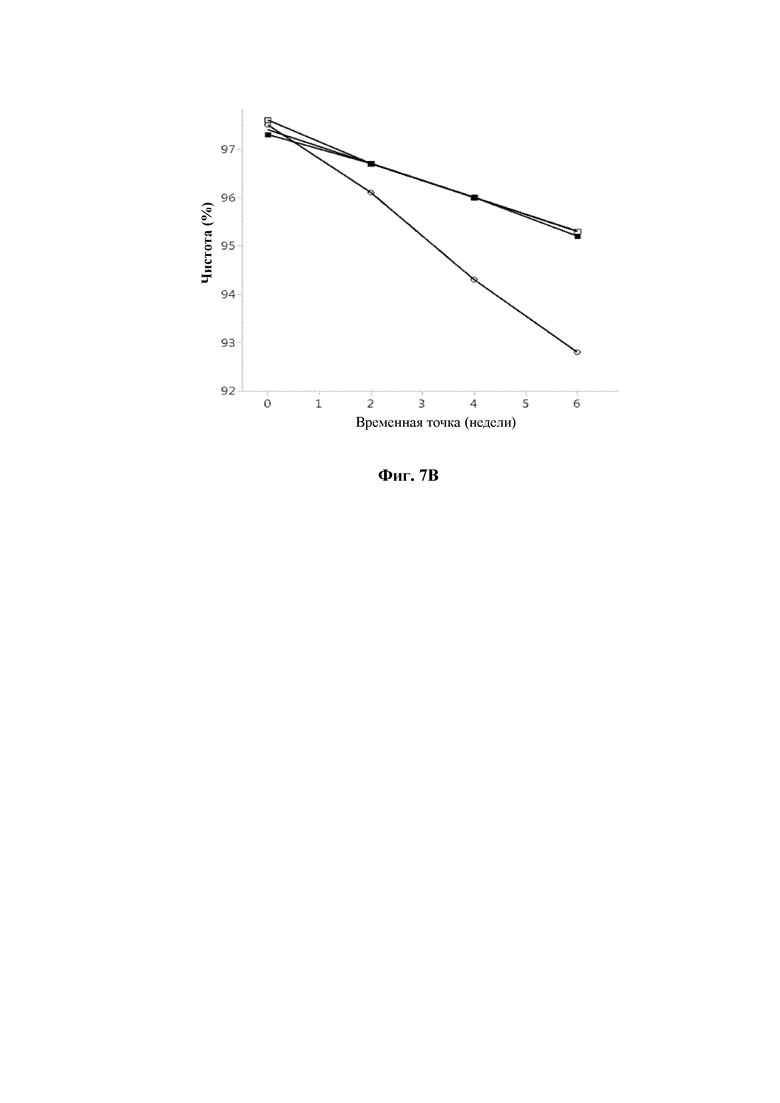
На фиг.7В показана чистота (% общего пептида) при хранении при 37°С [временная точка (недели)] для составов 01, 04, 05 и 06 с соединением 1.
Белые круги: состав 01, черные круги: состав 04, белые квадраты: состав 05, черные квадраты: состав 06.
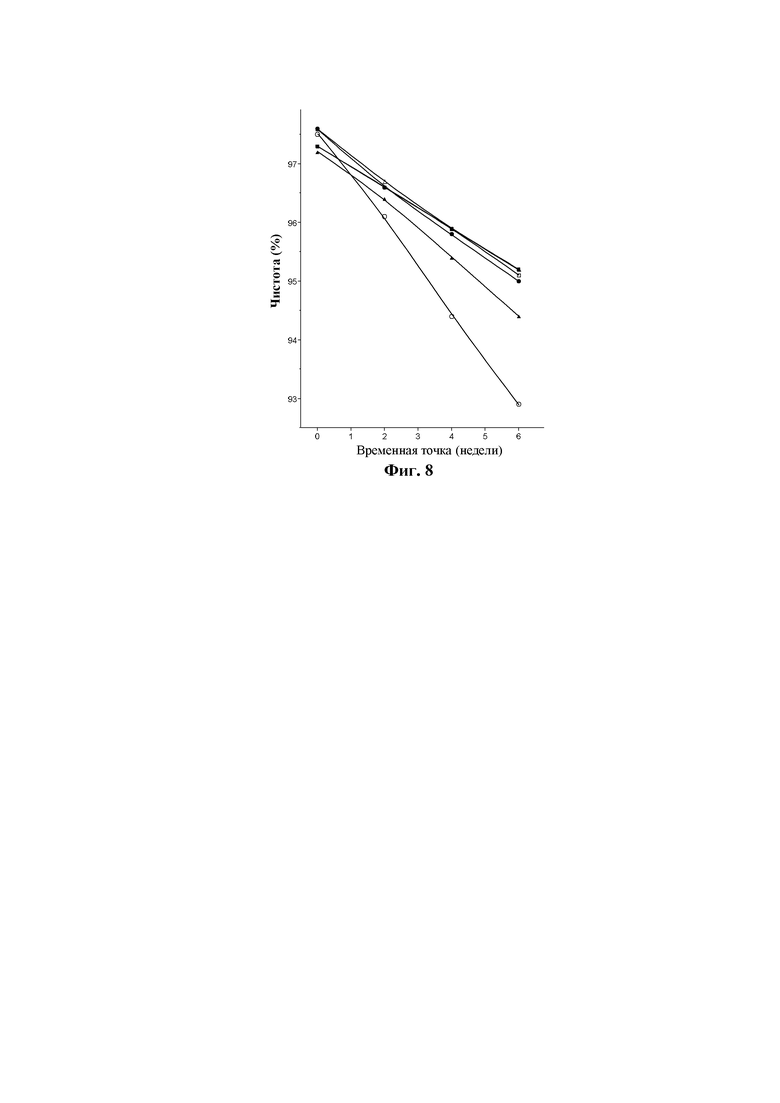
На фиг. 8 показана чистота соединения 1 (% общего соединения 1) при хранении при 37°С [временная точка (недели)] в комбинированных составах с семаглутидом.
Белые круги: комбинированный состав I, черные круги: комбинированный состав II, белые треугольники: комбинированный состав III, черные треугольники: комбинированный состав IV, белые квадраты: комбинированный состав V, черные квадраты: комбинированный состав VI.
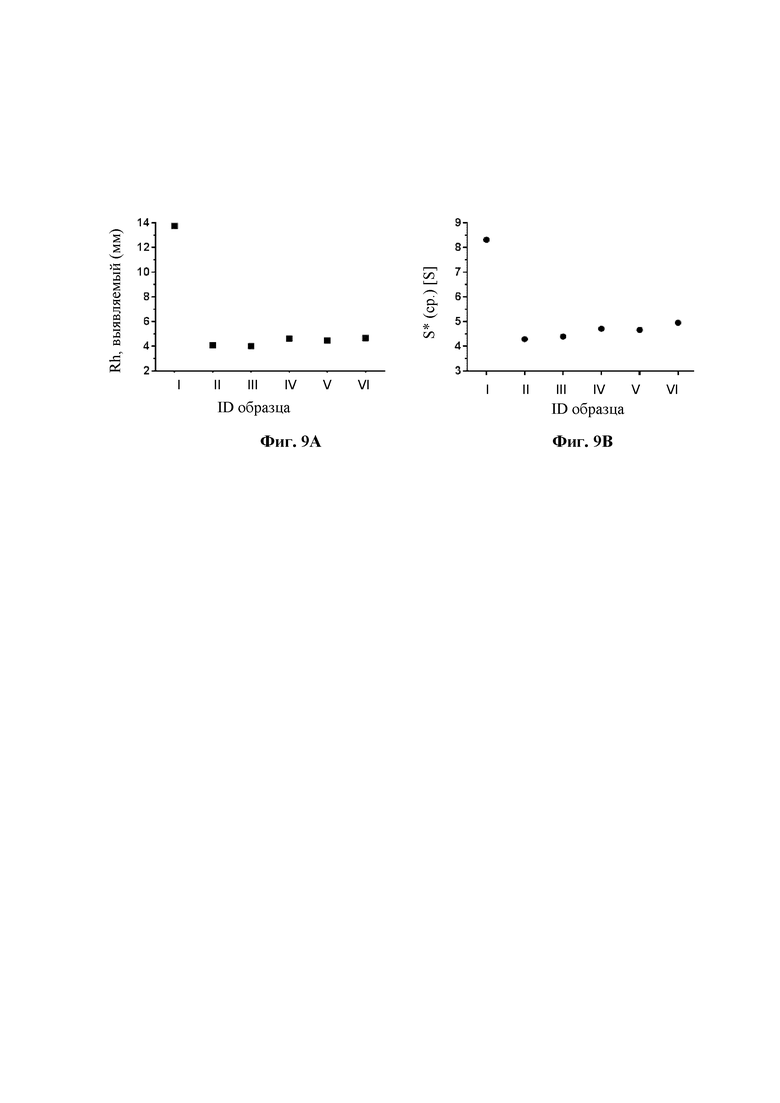
На фиг. 9 показана олигомеризация комбинированных составов в моделированных условиях в месте инъекции.
Фиг. 9А: выявляемый средний гидродинамический радиус (rH) [нм], измеренный с помощью DLS.
Фиг. 9 В: показан размер олигомеров комбинированных составов после замены буфера, наблюдаемый с помощью AUC (S*).
ПРИМЕРЫ
Настоящее изобретение дополнительно проиллюстрировано с помощью ссылки на следующие примеры, которые не предназначены каким-либо образом ограничивать объем настоящего изобретения, который заявлен.
Пример 1
Улучшенные биофизические свойства при смоделированных условиях в месте инъекции
Протокол
API составов представляет собой человеческий инсулин А14Е, В16Н, В25Н, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30 (соединение 1), полученный, как описано, например, в WO 2009/115469, см. пример 33.
Олигомеризацию соединения 1 определяли при смоделированных условиях в месте инъекции. Смоделированные условия в месте инъекции получали путем уменьшения количества фенола и/или метакрезола соответственно и замены буфера на смоделированный буфер интерстициальной жидкости. Данная процедура фактически обеспечивала удаление всех фенольных лигандов, но сохраняла соотношение цинк/инсулин исходного состава.
Составы подвергали замене буфера на буфер интерстициальной жидкости (ISF) с помощью колонки PD-MidiTrap G-25 в соответствии с протоколом изготовителя.
Колонки уравновешивали с помощью целевого буфера путем промывания колонки достаточным объемом целевого буфер, и применяли состав в подходящем объеме, и элюировали с помощью целевого буфера. Буфер ISF состоял из 140 мМ NaCl, 4 мМ KCl, 1 мМ MgSO4, 2 мМ CaCl2, 10 мМ Hepes, рН 7,4.
Если не указано иное, процедура являлась следующей:
замена буфера при 22°С;
последующая инкубация при 37°С в течение 14-18 часов и
последующее измерение при 22°С (если не указано иное).
Как правило, измерения проводили через приблизительно 1 ч. после окончания инкубации при 37°С. Если это было невозможно, образцы хранили при 22°С до проведения измерения.
Если не указано иное, образцы измеряли неразбавленными. Следует отметить, что размер олигомеров, полученный в результате процедуры описанного уменьшения количества фенолов, является зависимым от способа, и в случае данного состава он может варьироваться в зависимости от факторов, таких как время, температура и партия колонки. Следовательно, необходимо, чтобы измерения для данного набора составов сравнивались в рамках одного и того же эксперимента, а не среди экспериментов. Следовательно, в случае одного и того же стандарта состав тестировали вместе с отличным составом по настоящему изобретению в различных экспериментах. Например, состав А по сравнению с составом В и С; состав 01 по сравнению с составами 02-06.
Выявляемый средний гидродинамический радиус (rH) измеряли с помощью динамического светорассеяния (DLS) с применением DynaPro PR™ (Wyatt technology, Санта-Барбара, Калифорния, США). Перед анализом образцы центрифугировали в течение 5 минут при 1200 об./мин. для удаления каких-либо частиц пыли в растворе. Измерения проводили при 25°С с применением 40 операций получения данных и при времени получения данных 2 сек.
Выявляемую среднюю молекулярную массу (кДа) измеряли с помощью многоуглового статического светорассеяния с градиентом состава (CG-MALS) с применением системы, состоящей из блока титратора Calypso II от Wyatt Technology Corporation (WTC), присоединенного к детектору светорассеяния DAWN8+ от WTC (эксплуатируемому при 664 нм) и рефрактометру Optilab T-rEX от WTC (эксплуатируемому при 660 нм), при 25°С. Образцы фильтровали через фильтр 0,45 мкм, а затем через фильтр 0,22 мкм перед проведением измерения.
Эксперименты в отношении скорости седиментации (SV) проводили с помощью аналитической ультрацентрифуги XL-I (BeckmanCoulter, Брея, Калифорния) в двухсекторных вкладышах 12-мм или 3-мм, покрытых сапфировыми окошками. Образцы центрифугировали при 40000 об./мин и 20°С до завершения седиментации и отслеживали с помощью интерференционной оптики прибора. Распределения коэффициента седиментации (SCD) рассчитывали с помощью SedFit, версия 11.8 (www.analyticalultracentrifiigation.com) с применением модели c(s) с сеткой из 100 s-значений в диапазоне, достаточном для описания всего седиментационного материала, исходя из rmsd и характера распределения остатков. Соотношение коэффициента трения f/fo принимали в качестве переменной, подлежащей оптимизации во время аппроксимации (Р Schuck, MA Perugini, NR Gonzales, GJ Howlett and D Schubert: Size-distribution analysis of proteins by analytical ultracentrifugation: strategies and application to model systems; (Biophys. J. 2002 82:1096). Средние значения коэффициента седиментации получали посредством интеграции полученных в результате с(s)-распределений.
Значения зависимой от температуры динамической вязкости измеряли с помощью вискозиметра шарикового типа Lovis2000 (Anton Paar, Грац, Австрия). Температуру понижали с 40°С до 4°С по 2°С за этап с обеспечением 5 минут для установления равновесия температуры между этапами. Плотность буфера одновременно измеряли с помощью денситометра DMA5000, также от Anton Paar.
Получали три моносостава, т.е. состав А, характерный для существующего уровня техники (см., например WO 2013/153000), и составы В, С, характерные для настоящего изобретения (60 мМ фенола/10 мМ м-крезола).
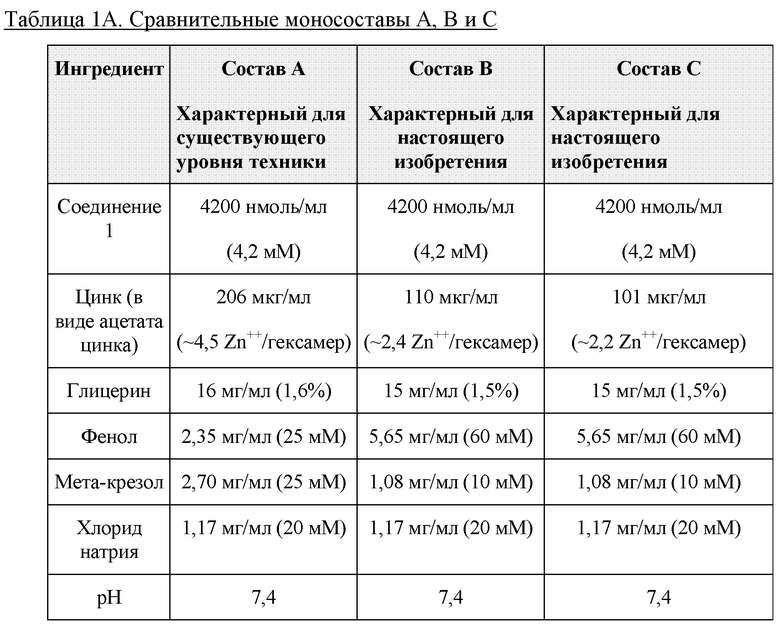
Получали еще шесть моносоставов, т.е. состав 01 (такой же, как состав А) и составы 02, 03, 04, 05 и 06, характерные для настоящего изобретения (таблица 1 В). Содержание цинка варьировало от 4,5 Zn++/шесть единиц инсулина до 2,4, 2,2 и 2,0 Zn++/шесть единиц инсулина. Кроме того, протестировали системы консервантов из либо 25/25 мМ фенола/м-крезола, либо 60/0 мМ фенола/м-крезола.
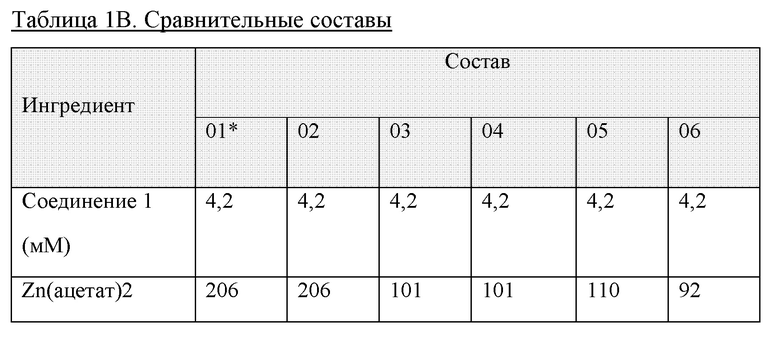
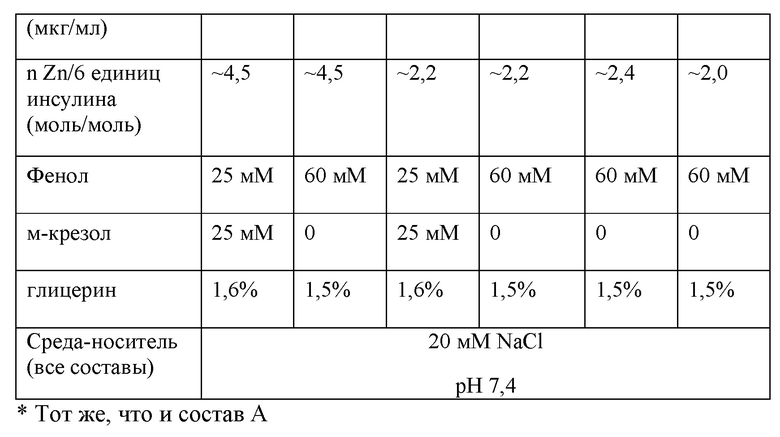
Повышенный размер олигомерову подвергнутых замене буфера моносоставов, содержащих 60 мМ фенола и 10 м-крезола (таблица 2А; фиг. 1А, 1В и 1С)
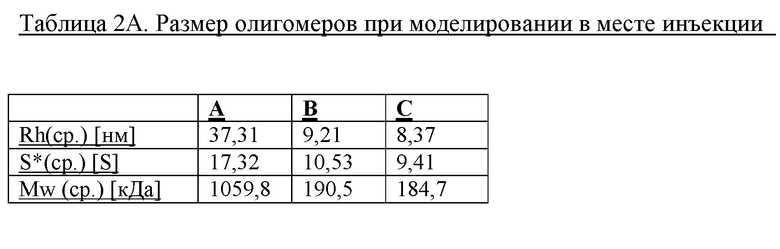
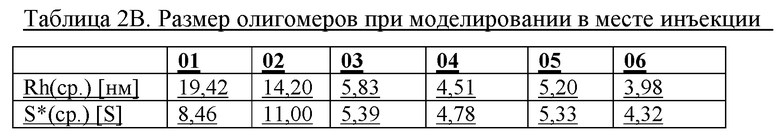
Повышенный размер олигомерову подвергнутых замене буфера моносоставов, содержащих 60 мМ фенола и 0 м-крезола (таблица 2 В; фиг. 2А и 2В)
Вывод
Содержание цинка понижали с 4,5 Zn++/шесть единиц инсулина в составе А до 2,4 и 2,2 Zn++/шесть единиц инсулина в составах В и С (с повышенным содержанием фенола и пониженным содержанием мета-крезола) соответственно. Данное понижение содержания цинка сопровождалось уменьшением размера олигомеров (см. фиг. 1А, 1В и 1С), определенным при смоделированных условиях в месте инъекции с помощью способа, описанного выше.
Результаты для составов 01-06 дополнительно подтверждают, что размер олигомеров уменьшается, если содержание Zn понижается с 4,5 Zn++/шесть единиц инсулина до 2,2±0,2 Zn++/шесть единиц инсулина. В случае 2,2±0,2 Zn++/шесть единиц инсулина размер олигомеров дополнительно уменьшается, если содержание фенола/крезола понижают с 25 мМ/25 мМ до 60 мМ/0 мМ. См. фиг. 2А и 2В.
Улучшенная вязкость у подвергнутых замене буфера моносоставов, содержащих 60 мМ фенола и 10 мМ м-крезола (см. таблицу 3А; фиг. 3А и 3В)
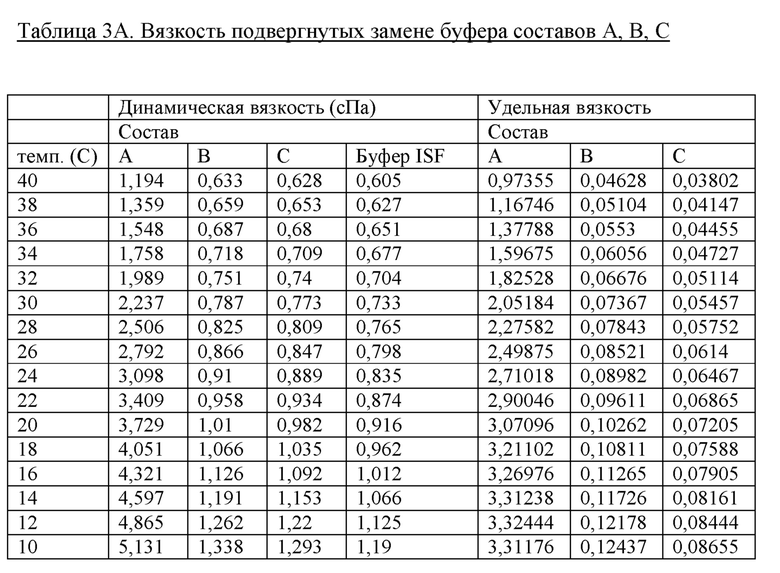
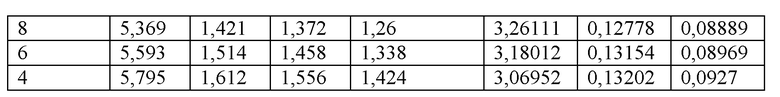
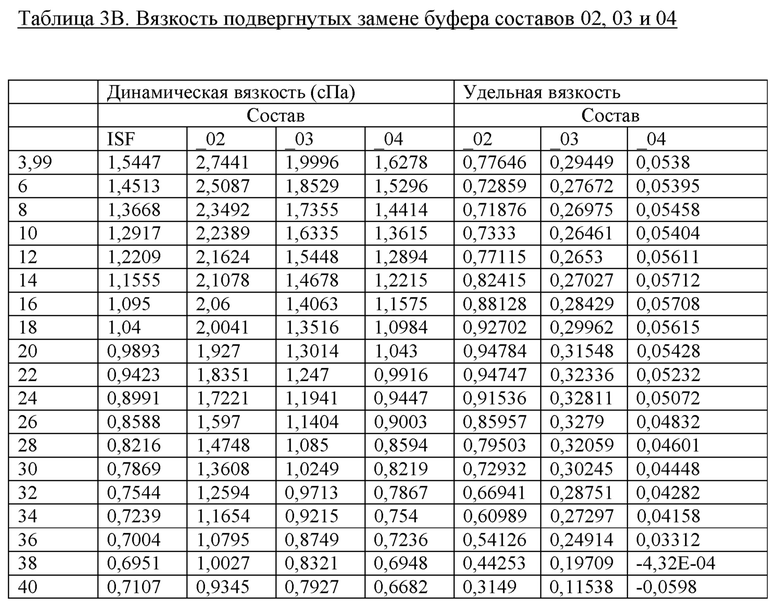
Улучшенная вязкость подвергнутых замене буфера моносоставов, содержащих 60 мМ фенола и 0 м-крезола (см. таблицу 3В; фиг. 3С и 3D)
Вывод
Данные эксперименты демонстрируют, что вязкость состава при смоделированных условиях в месте инъекции в соответствии с данным способом в высокой степени зависят от содержания цинка таким образом, что уменьшение соотношения цинка приводит к более низкой вязкости.
Пример 2
tmax и t1/2 выведения
tmax представляет собой период времени до достижения максимальной концентрации (максимальное содержание в плазме крови), и t1/2 представляет собой период полувыведения, в течение которого половина соединения удаляется из плазмы крови после введения.
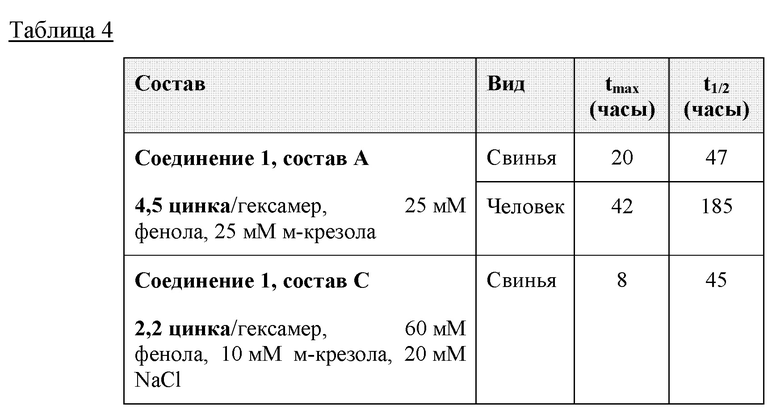
Измененные биофизические свойства, описанные в примере 1, соответствуют PK-профилю с демонстрацией раннего наступления tmax у свиней (см. таблицу 3). Это указывает на то, что время нахождения соединения 1 в подкожном слое уменьшается при составлении в соответствии с настоящим изобретением, и в отличие от того же соединения, которое предусмотрено в составе в соответствии с уровнем техники.
Неожиданно, пониженный уровень цинка почти не оказывает влияния на продолжительность действия (т.е. не влияет на t1/2 выведения), что делает состав в соответствии с настоящим изобретением и состав согласно существующему уровню техники в одинаковой степени подходящими для введения один раз в неделю.
Вывод
Данные эксперименты демонстрируют, что время нахождения в подкожном слое (tmax) соединения 1 в значительной степени снижено в результате уменьшения содержания Zn++/гексамер. Наблюдение соответствует данным, представленным в примере 1, из которых видно уменьшение размера олигомеров, образовавшихся при смоделированных условиях в месте инъекции.
Таким образом, при составлении в соответствии с настоящим изобретением соединение 1 обеспечивает образование олигомеров меньшего размера в месте инъекции, что приводит к получению профиля PK/PD с более коротким временем нахождения в подкожном слое (сниженное tmax).
Но, неожиданно, несмотря на то, что время нахождения в подкожном слое (tmax) соединения 1 в значительной степени снижено, образования по настоящему изобретению сохраняют тот же период полувыведения (на t1/2 выведения не оказано влияния). Это означает, что составы по настоящему изобретению могут способствовать более быстрому достижению производными инсулина длительного действия максимальной концентрации в кровотоке с сохранением при этом все еще максимальной концентрации на протяжении более длительного периода.
Это неожиданное обнаружение также позволяет ограничивать образования больших олигомеров в месте инъекции с сохранением при этом длительной продолжительности действия, соответствующей профилю введения один раз в неделю. Образование больших олигомеров с высокой вязкостью в месте инъекции может вызывать дискомфорт после инъекции.
Пример 3
Улучшенное конформационное состояние в составе
В присутствии цинка инсулин человека существует в составе в виде гексамеров. Гексамеры инсулина человека могут принимать два различных конформационных состояния в зависимости от конформации мономеров. Восемь N-концевых аминокислотных остатков В-цепи мономера инсулина могут быть либо в растянутой конформации (Т-состояние), либо в α-спиральной конформации (R-состояние). В присутствии фенола и NaCl инсулин человека принимает R-конформацию, которая является предпочтительной конформацией в отношении физической и химической устойчивости (Dunn MF. Zinc-ligand interactions modulate assembly and stability of the insulin hexamer: A review. Biometals 2005; 18; 295-303).
Протокол
Конформапионные изменения гексамера инсулина отслеживали по характерной особенности, полученной с помощью CD-спектроскопии при 251 нм ( Gilge G, Cabuk Y and Wollmer A; Biol. Chem. Hoppe-Seyler 1990 371 669-673). Образцы измеряли с применением прибора Jasco 815 и с ходом луча 0,02 см. Отнимали фоновые титрования и полученную в результате Δε при 251 нм наносили на график относительно Zn/6 ед. инс.(моль/моль).
Gilge G, Cabuk Y and Wollmer A; Biol. Chem. Hoppe-Seyler 1990 371 669-673). Образцы измеряли с применением прибора Jasco 815 и с ходом луча 0,02 см. Отнимали фоновые титрования и полученную в результате Δε при 251 нм наносили на график относительно Zn/6 ед. инс.(моль/моль).
Конформационное состояние моносоставов, содержащих 60 мМ фенола/0 м-крезола
Конформационное состояние составов 01-06 показано в таблице 5А и на фигуре 4А.
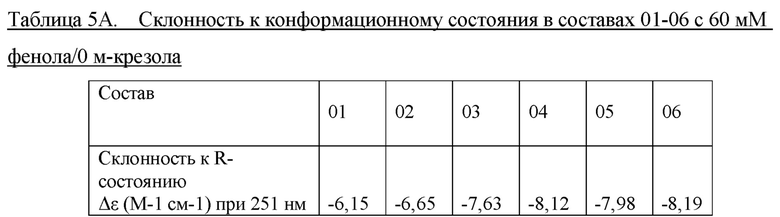
На фиг. 4А показаны конформапионные изменения (Т-состояние; смешанное TR-состояние; R-состояние) в зависимости от Zn++ на шесть единиц инсулина (моль:моль) для составов 01-06.
Конформационное состояние моносоставов, содержащих 60 мМ фенола и 10 мМ м-крезола
Получали две серии составов. Все составы содержали 4,2 мМ соединения 1, 16 мг/мл (1,6%) глицерина, 20 мМ NaCl с рН 7,4. Составы серии В содержали 60 мМ фенола и 10 мМ м-крезола с уровнем цинка, варьирующем в пределах 1,5 (В1), 2,0 (В2), 2,3 (В3), 2,5 (В4), 3,0 (В5) и 4,0 (В6) на 6 единиц инсулина. Серия D содержала 25 мМ фенола и 25 мМ м-крезола с уровнем цинка, варьирующем в пределах 1,5, 2,0, 2,3, 2,5, 3,0, 4,0 и 4,5 на 6 единиц инсулина. Также получали серии составов инсулина человека с различным уровнем цинка. Конформационное состояние показано в таблице 5В и на фигуре 4В.
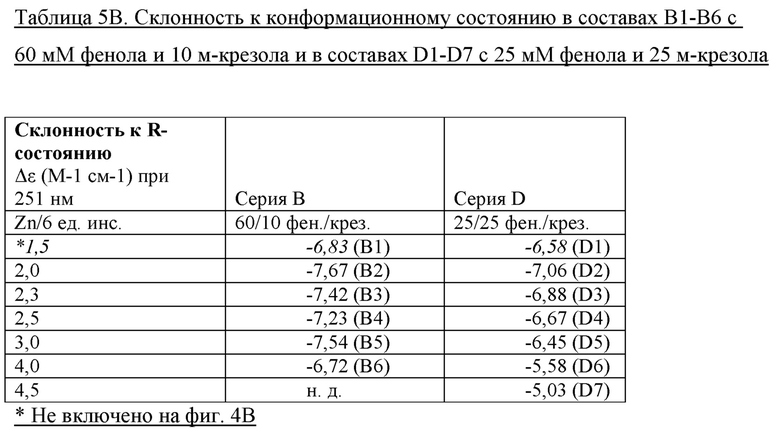
На фиг. 4В показаны конформапионные изменения (Т-состояние; смешанное TR-состояние; R-состояние) в зависимости от Zn++ на шесть единиц инсулина (моль:моль) для составов серии В и серии D и составов с инсулином человека.
Вывод
Из данных CD-спектроскопии в близком к УФ спектре видно, что конформация T/R соединения 1 зависела от концентрации цинка. Снижению содержания цинка сопутствовало изменение в конформационном состоянии соединения 1 в составе из смешанного T/R-состояния в R-состояние, которому также сопутствовал более высокий уровень гексамера, образованного в составах (см. пример 4 ниже). R-состояние и уровень гексамера дополнительно возрастали путем изменения соотношения фенол/мета-крезол с 25/25 мМ до 60/10 мМ (фиг. 4В).
Из данных составов 01-06 видно, что R-состояние соединения 1 в составах дополнительно обогащалось путем уменьшения содержания Zn с 4,5 до 2,2 Zn ± 0,2 Zn /6 частей соединения 1 и отказа от м-крезола (фиг. 4А).
Пример 4
Улучшенное распределение олигомеров в составе
Протокол
Эксклюзионная хроматография представляет собой чувствительный способ для количественного определения распределения нековалентных олигомеров составов с инсулином. SEC проводили с применением колонки ВЕН200, 1,7 мкм 4,6×150 мм с подвижным буфером, состоящим из 8,0 мМ фенола, 140 мМ NaCl, 10 мМ Трис-HCl, рН 7,4. Хроматографию проводили при 22°С с применением объема впрыска 2 мкл и потока, составляющего 0,3 мл/мин. В качестве стандартов молекулярной массы применяли альбумин, ковалентный гексамер инсулина и мономерный инсулин. Хроматограммы анализировали путем интеграции с представлением частиц больше гексамера (3,0-3,8 мин.), гексамера (3,8-4,3 мин.) и частиц меньше гексамера (4,3-5,5 мин.). Следует отметить, что точные границы интеграции в случае каждого набора данных будут немного варьироваться по причине вариаций в характеристиках колонки.
Данные малоуглового рентгеновского рассеяния (SAXS) собирали с применением прибора BioSAXS-2000, оснащенного проточной кюветой и детектором Dectris 100K с охватом q-диапазона 0,008-0,661 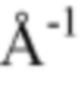 . Измерения буфера вычитали из измерений образца для получения профилей рассеяния белка. Данные эталонного образца инсулина человека в гексамерном состоянии с R-конформапией собирали согласно той же процедуре из образца, составляющего 0,6 мМ инсулина человека, 3 Zn++/шесть единиц инсулина, 16 мМ фенола, 20 мМ NaCl и 7 мМ фосфатного буфера, рН 7,4.
. Измерения буфера вычитали из измерений образца для получения профилей рассеяния белка. Данные эталонного образца инсулина человека в гексамерном состоянии с R-конформапией собирали согласно той же процедуре из образца, составляющего 0,6 мМ инсулина человека, 3 Zn++/шесть единиц инсулина, 16 мМ фенола, 20 мМ NaCl и 7 мМ фосфатного буфера, рН 7,4.
Распределение олигомеров для составов, содержащих 60 мМ фенола и 0 м-крезола Была получена нативная хроматограмма SEC со сравнением составов 01, 02, 03, 04, 05 и 06 (см. таблицу 6 и фиг. 5А).
Распределение олигомеров для составов, содержащих 60 мМ фенола и 10 мМ м-крезола
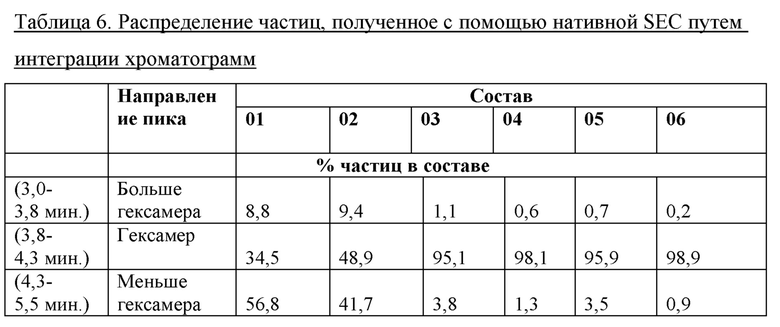
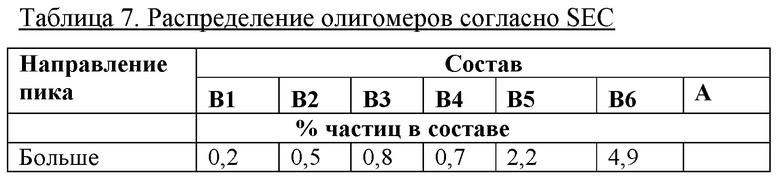
Была получена нативная хроматограмма SEC со сравнением составов В1-В6 и состава А (см. таблицу 6 и фиг. 5В). Площадь под кривой являлась сходной у всех хроматограмм. Хроматограммы анализировали путем интеграции с представлением частиц больше гексамера (3,0-3,8 мин.), гексамера (3,8-4,3 мин.) и частиц меньше гексамера (4,3-5,5 мин.). Следует отметить, что точные границы интеграции в случае каждого набора данных будут немного варьироваться по причине вариаций в характеристиках колонки.
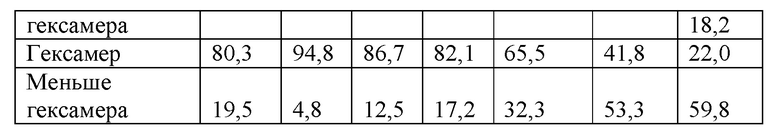
Вывод
Из данных SEC составов 01-06 (таблица 6, фиг. 5А) видно, что распределение олигомеров состава 01 с соединением 1 характеризуется широкими полосами без явно преобладающих частиц олигомеров. Распределение олигомеров соединения 1 в составах 03-06 является более узким по сравнению с составами 01 и 02. Время удерживания основного пика составов 03-06 соответствует гексамеру, и малый пик со временем удерживания 5 минут соответствует мономеру или димеру.
Из данных SEC составов В1-В6 и А (таблица 7, фиг. 5В) также видно, что при 2,0-2,5 цинка/6 единиц инсулина пик гексамера является насыщенным по сравнению с 4,0 или 4,5 Zn.
Следовательно, пик гексамера является насыщенным при низком содержании цинка (например, от 2,0 Zn до 2,5 Zn) по сравнению с высоким содержанием цинка (например, 4,0 или 4,5 Zn). Как при 4,5 Zn, так и при 2,2 Zn гексамер является насыщенным при 60 мМ/0 или 10 мМ фенола/м-крезола относительно 25/25 мМ фенола/м-крезола. При составлении в соответствии с настоящим изобретением содержание гексамера увеличивается, и олигомеризация становится более четко определенной.
Данные SAXS также подтверждают, что характер олигомеризации состава А с соединением 1 с 4,5 Zn++/гексамер не соответствует классическому гексамеру инсулина человека, при этом структура соединения 1 на основе гексамера является преобладающей в составе С (фиг. 6). При составлении в соответствии с настоящим изобретением (состав С) характер олигомеризации становится более четко определенным и соответствующим структуре на основе гексамера, сходной с инсулином человека.
Пример 5
Улучшенные химическая стабильность и физическая стабильность
Из экспериментальных результатов в данном примере видно, что как химическая стабильность, так и физическая стабильность соединения 1 в новых составах улучшена по сравнению с эталонным составом А. В частности, при высоком уровне фенола и низком уровне м-крезола и химическая стабильность, и физическая стабильность соединения 1 повышается, если снижается концентрация цинка.
Протокол
Чистоту определяли с помощью обращенно-фазовой ультравысокоэффективной жидкостной хроматографии (RP-UHPLC), где образцы анализировали с применением Acquity CSH Fluoro Phenyl, 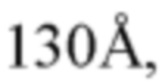 1,7 мкм, колонка 2,1×150 мм, градиентное элюирование с помощью ацетонитрила в мобильной фазе ацетонитрила и фосфорсодержащего буфера в воде с последующим УФ-обнаружением (215 нм) при скорости потока 0,30 мл/мин. с объемом впрыска образца 2-3 мкл. Чистоту оценивали как площадь основного пика, деленную на площадь всех пиков, х 100%.
1,7 мкм, колонка 2,1×150 мм, градиентное элюирование с помощью ацетонитрила в мобильной фазе ацетонитрила и фосфорсодержащего буфера в воде с последующим УФ-обнаружением (215 нм) при скорости потока 0,30 мл/мин. с объемом впрыска образца 2-3 мкл. Чистоту оценивали как площадь основного пика, деленную на площадь всех пиков, х 100%.
Химическая стабильность состава с соединением 1 с 60 мМ фенола и 10 мМм-крезола
Стабильность, измеренная как % чистоты общего пептида с помощью RP-UHPLC, демонстрирует в значительной степени повышенную стабильность соединения 1 в составе В и составе С, которые содержали 60 мМ фенола и 10 мМ м-крезола, по сравнению с составом А с соединением 1, который содержал 25 мМ фенола и 25 мМ м-крезола. См. таблицу 8 и фиг. 7А.
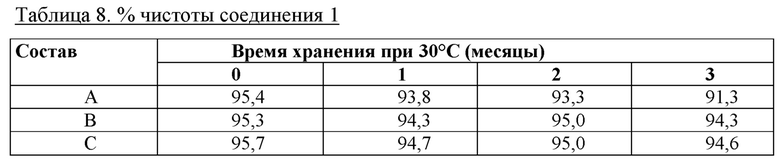
Химическая стабильность составов с соединением 1 с 60 мМ фенола и 0 м-крезола
Стабильность составов, представленных в таблице 9, измеренная как % чистоты общего пептида с помощью RP-UHPLC, дополнительно подтверждает, что химическая стабильность соединения 1 повышается в зависимости от концентрации цинка в составах с относительно высоким уровнем фенола и низким уровнем м-крезола. Из результатов видна повышенная стабильность соединения 1, если содержание цинка понижалось с 4,5 Zn++/шесть единиц инсулина до 2,4, 2,2 и 2,0 Zn++/шесть единиц инсулина в составах с изменением в системе консервантов с 25/25 мМ фенола/м-крезола на 60 мМ фенола и 0 м-крезола. См. таблицу 9 и фиг. 7В.
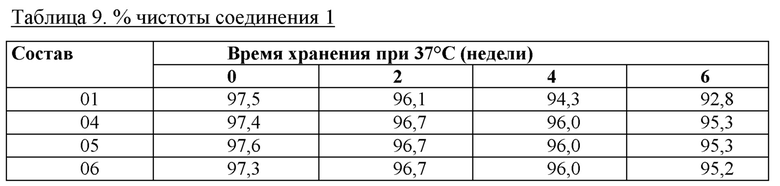
Вывод
При составлении в соответствии с настоящим изобретением (см. составы В, С, 04, 05 и 06; таблицы 8 и 9 и фиг. 7А и фиг. 7В) химическая стабильность повышается по сравнению с уровнем техники (составы А и состав 01).
Физическая стабильность
Протокол
Составы с соединением 1 тестировали в 96-луночном микротитрационном планшете с 4 повторностями по 200 мкл. К 1,0 мл каждого состава добавляли ThT (тиофлавин Т) до 1 мкМ. Анализ с применением тиофлавина Т (ThT) в отношении склонности к образованию амилоидных фибрилл проводили в Thermo Fluoroskan, встряхивание при 960 об./мин., 37°С, в течение 45 часов. Испускание ThT сканировали до и после анализа. Период задержки перед началом испускания флуоресценции ThT представляет собой измерение физической стабильности. Периоды задержки определяли на основе кривых флуоресценции, усредненных для 4 повторностей. Более длительный период задержки свидетельствует о более высокой физической стабильности.
Следует отметить, что результаты с ThT, полученные в результате описанного протокола, могут варьироваться между экспериментами. Следовательно, необходимо, чтобы измерения для данного набора составов сравнивались в рамках одного и того же эксперимента, а не среди экспериментов. В данном примере один и тот же стандартный состав тестировали вместе с различными составами по настоящему изобретению в различных экспериментах. Например, состав А по сравнению с составом С; состав 01 по сравнению с составами 04-06.
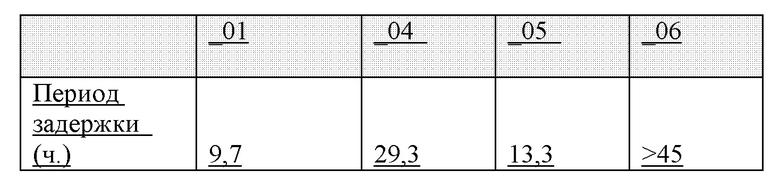
Периоды задержки показаны в таблице 10 ниже. Состав А или состав 01 в качестве эталонного состава для сравнения.
Результаты показаны в таблице 10А и таблице 10В.
Физическая стабильность соединения 1 в составах с 60 мМ фенола и 10 м-крезола

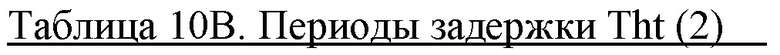
Вывод
Периоды задержки, полученные при анализе с ThT, указывают на то, что физическая стабильность соединения 1 повышена в составах с низким уровнем цинка, высоким уровнем фенола и низким уровнем м-крезола. Из данных видно, что снижение содержания цинка с 4,5 Zn/6 ед. инс.до 2,2±0,2 Zn/6 ед. инс., и сопутствующее повышение содержания фенола с 25 мМ до 60 мМ, и снижение содержания м-крезола с 25 мМ до 10 мМ приводит к получению более длительного периода задержки и, таким образом, повышенной физической стабильности. При удалении м-крезола физическая стабильность соединения 1 дополнительно повышалась в составах с низким уровнем цинка (см. таблицу 10В).
Пример 6
Комбинированные составы и их химическая и физическая стабильность
Соединение 1 может быть совместно составлено вместе с аналогом GLP-1 семаглутидом для применения один раз в неделю для получения комбинации с фиксированным соотношением.
Получали следующие комбинированные составы 1-6 соединения 1 и семаглутида. Также получали моносостав соединения 1 в качестве эталонного моносостава 1. Прогнозируемые целевые значения показаны в таблице 11 ниже.
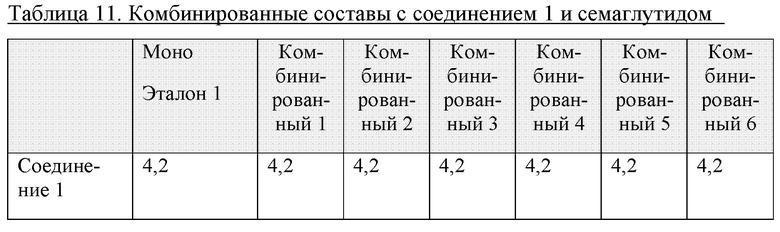
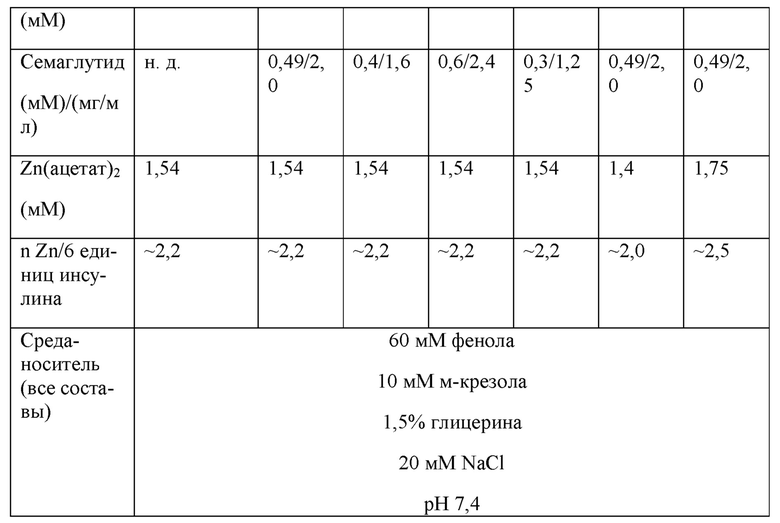
Концентрации соединения 1 и семаглутида в полученных составах измеряли с применением RP-HPLC и эталонных материалов. Эти концентрации указаны в таблице 12А и 12В ниже.
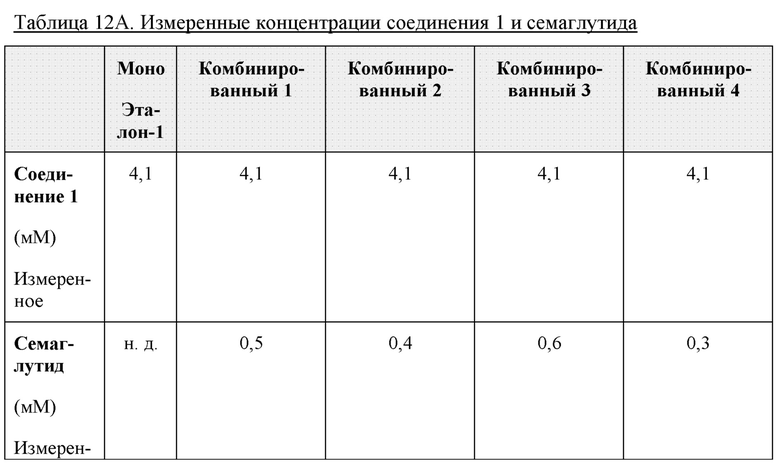

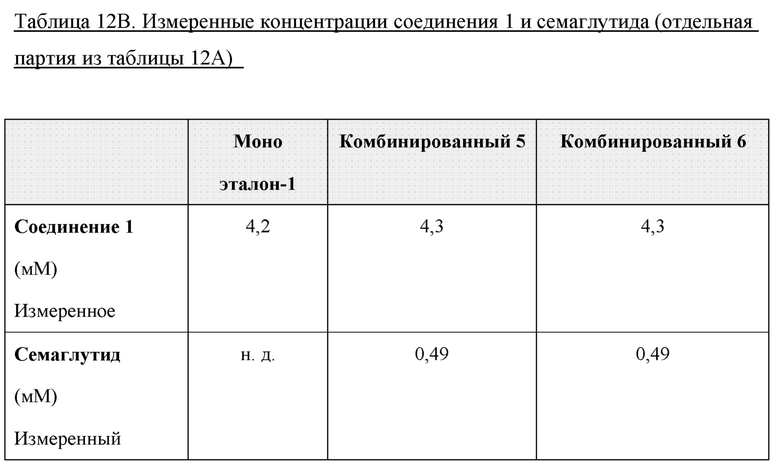
Таким образом, измеренные концентрации отклонялись на менее 3% от прогнозируемых целевых значений.
Также позже получали следующие комбинированные составы I-VI соединения 1 и семаглутида. Получали моносостав соединения 1 в качестве эталонного моносостава 2. Прогнозируемые целевые значения показаны в таблице 13 ниже.
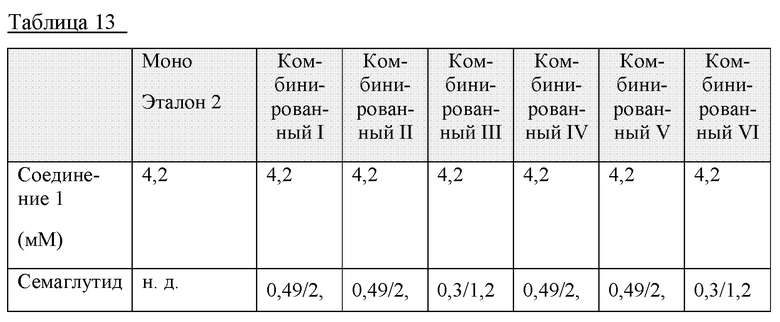
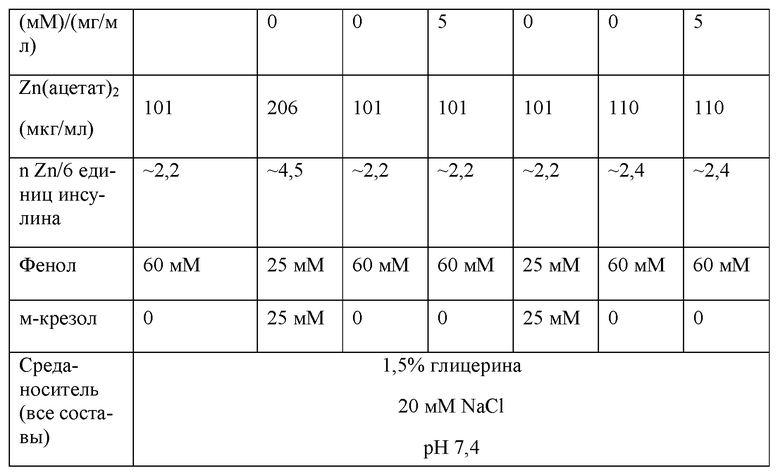
Физическая стабильность
Протокол
Составы тестировали в 96-луночном микротитрационном планшете с 8 повторностями по 200 мкл. К 1,0 мл каждого состава добавляли ThT (тиофлавин Т) до 1 мкМ. Анализ с применением тиофлавина Т (ThT) в отношении склонности к образованию амилоидных фибрилл проводили в Thermo Fluoroskan, встряхивание при 960 об./мин, 37°С, в течение 45 часов. Испускание ThT сканировали до и после анализа. Период задержки перед началом испускания флуоресценции ThT (образование амилоидных фибрилл) представляет собой измерение физической стабильности. Периоды задержки определяли на основе кривых флуоресценции, усредненных для 8 повторностей. Периоды задержки тестировали дважды в случае комбинированных составов 1-4 и комбинированных составов 5 и 6 соответственно; и в случае каждого тестировали с моносоставом в качестве эталона, чтобы сделать результаты сравнимыми. Более длительный период задержки свидетельствует о более высокой физической стабильности.
Эталон, представляющий собой моносостав соединением 1, и комбинированные составы тестировали в анализе с применением 96-луночного микротитрационного планшета с тиофлавином Т (ThT) в отношении склонности к образованию амилоидных фибрилл.
Периоды задержки показаны в таблицах 14А, 14 В, 14С ниже.
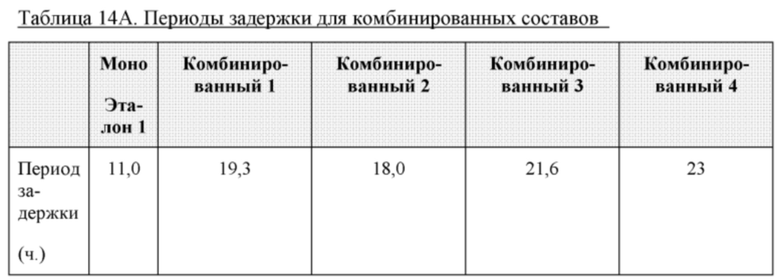
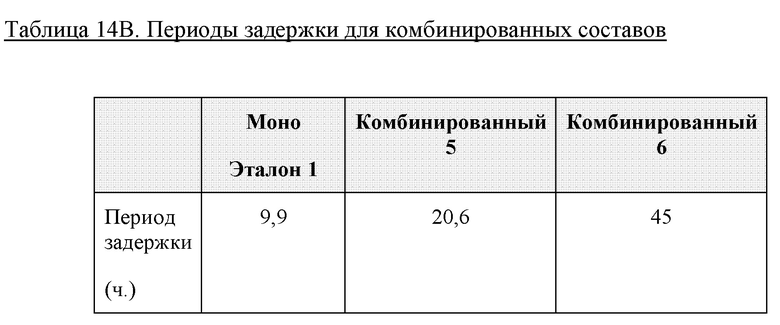


Вывод
Анализ с применением ThT показал, что без повышения уровня цинка комбинированные составы соединения 1 и семаглутида не характеризовались нарушением физической стабильности соединения 1 по сравнению с таковой моносоставов с соединением 1. Действительно, периоды задержки комбинированных составов были намного продолжительнее, чем таковые моносостава с соединением 1, что демонстрирует то, совместное составление соединения 1 с семаглутидом фактически стабилизирует состав в отношении нежелательного образования амилоидных фибрилл. При сравнении с комбинированным составом другого производного инсулина длительного действия и производного GLP-1 (например, деглудека и лираглутида) это наблюдение является неожиданным и удивительным.
Из результатов из таблицы 14С видно, что понижение уровня м-крезола может обеспечивать дополнительное повышение физической стабильности комбинированного состава соединения 1 и семаглутида; и повышение уровня фенола также обеспечивает повышение физической стабильности комбинированного состава соединения 1 и семаглутида.
Из результатов из таблицы 14С также видно, что при совместном составлении соединения 1 с семаглутидом в составе в соответствии с настоящим изобретением физическая стабильность соединения 1 повышается по сравнению с применением состава из существующего уровня техники (состав I) в случае комбинированного состава соединения 1 и семаглутида. Химическая стабильность Протокол
Чистоту определяли с помощью обращенно-фазовой ультравысокоэффективной жидкостной хроматографии (RP-UHPLC), где образцы анализировали с применением Acquity CSH Fluoro Phenyl,  1,7 мкм, колонка 2,1×150 мм, градиентное элюирование с помощью ацетонитрила в мобильной фазе ацетонитрила и фосфорсодержащего буфера в воде с последующим УФ-обнаружением (215 нм) при скорости потока 0,30 мл/мин. с объемом впрыска образца 2-3 мкл. Чистоту оценивали как площадь основного пика, деленную на площадь всех пиков, х 100%.
1,7 мкм, колонка 2,1×150 мм, градиентное элюирование с помощью ацетонитрила в мобильной фазе ацетонитрила и фосфорсодержащего буфера в воде с последующим УФ-обнаружением (215 нм) при скорости потока 0,30 мл/мин. с объемом впрыска образца 2-3 мкл. Чистоту оценивали как площадь основного пика, деленную на площадь всех пиков, х 100%.
Стабильность составов, представленных в таблице 15, измеряли как % чистоты общего соединения 1 с помощью RP-UHPLC.
Результаты подтверждают повышенную химическую стабильность соединения 1 в комбинированных составах, если содержание цинка понижено с 4,5 Zn++/шесть единиц инсулина до 2,4, 2,2 и 2,0 Zn++/шесть единиц инсулина (таблица 15, фиг. 8). Изменение системы консерванты с 25/25 мМ фенола/м-крезола до 60 мМ фенола и 0 м-крезола приводит в результате к дополнительному улучшению химической стабильности соединения 1 в комбинированном составе.
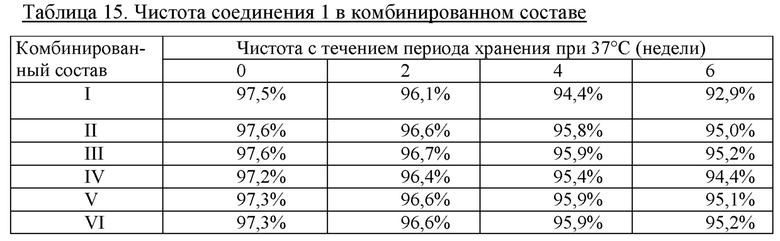
Вывод
При совместном составлении соединения 1 с семаглутидом в составе в соответствии с настоящим изобретением химическая стабильность соединения 1 повышается по сравнению с применением состава из существующего уровня техники (состав I) в случае комбинированного состава соединения 1 и семаглутида.
Пример 7
PK-свойства совместных составов с семаглутидом на модели свиней LYD для определения PK-свойств Определяли характеристики эталонного моносостава с соединением 1, и комбинированного состава 1, и комбинированного состава 2 из составов, полученных в примере 6, на модели свиней LYD для определения PK-свойств. Важно, чтобы PK-параметры tmax и t1/2 соединения 1, а также среднее время нахождения (MRT) соединения 1 не изменялись в значительной степени после совместного составления с семаглутидом.
Проводили перекрестное исследование с использованием 16 животных (n=8 для каждого состава).
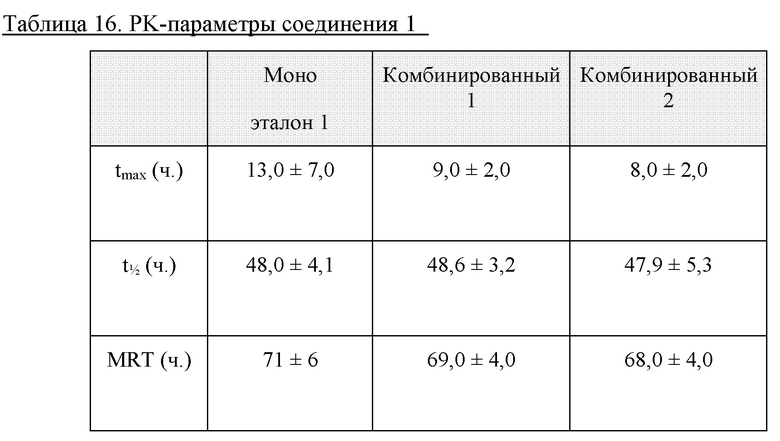
Показаны средние значения ± стандартное отклонение.
PK-параметры соединения 1 при совместном составлении с семаглутидом в комбинированный состав 1 и комбинированный состав 2 не изменялись в значительной степени по сравнению с соединением 1, вводимым в виде моносостава. Значения tmax были немного ниже у совместных составов, но со стандартным отклонением в отношении эталона с соединением 1 значения являются перекрывающимися. Значения t1/2 и MRT являлись очень сходными у соединения 1 в совместных составах по сравнению с эталонным моносоставом. В заключение, совместный состав с семаглутидом в значительной степени не оказывал влияния в отношении PK-свойств соединения 1.
Пример 8
Улучшенный размер олигомеров подвергнутых замене буфера совместных составов 60/0
Олигомеризацию комбинированных составов I-VI, имеющую место при смоделированных условиях в месте инъекции в отношении соединения 1 определяли в соответствии с протоколом, описанным в примере 1. Результаты показаны в таблице 17 и на фиг. 9А и фиг. 9В.
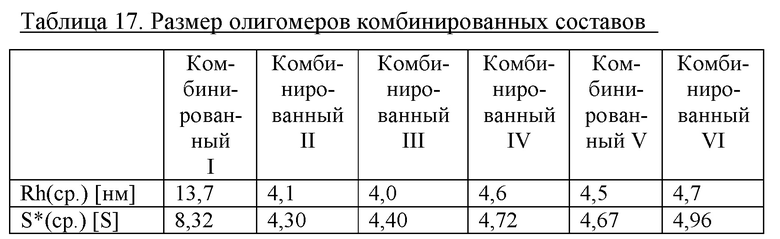
Вывод
Эти эксперименты демонстрируют, что размер олигомеров, образовавшихся при смоделированных условиях в месте инъекции, в высокой степени зависит от содержания цинка.
Средний размер олигомеров, образовавшихся при использовании комбинированных составов при смоделированных условиях в месте инъекции, в значительной степени уменьшен в составах с низким уровнем цинка (например, 2,4 и 2,2 Zn++/шесть единиц инсулина) по сравнению с составами с высоким уровнем цинка (например, 4,5 Zn++/шесть единиц инсулина). Повышение уровня фенола и понижение уровня м-крезола обеспечивает дополнительное уменьшение среднего размера олигомеров, образовавшихся при использовании комбинированных составов при смоделированных условиях в месте инъекции.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИНСУЛИН | 2017 |
|
RU2832680C1 |
| СТАБИЛИЗИРОВАННЫЕ ПО ОТНОШЕНИЮ К ПРОТЕАЗАМ АЦИЛИРОВАННЫЕ АНАЛОГИ ИНСУЛИНА | 2009 |
|
RU2571857C2 |
| ПРОИЗВОДНЫЕ ИНСУЛИНА, СОДЕРЖАЩИЕ ДОПОЛНИТЕЛЬНЫЕ ДИСУЛЬФИДНЫЕ СВЯЗИ | 2011 |
|
RU2598273C2 |
| НОВОЕ ПРОИЗВОДНОЕ АНАЛОГА ИНСУЛИНА | 2014 |
|
RU2673185C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИНСУЛИНА И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2015 |
|
RU2684456C2 |
| АНАЛОГИ ИНСУЛИНА С АЦИЛЬНОЙ И АЛКИЛЕНГЛИКОЛЕВОЙ ГРУППИРОВКОЙ | 2008 |
|
RU2514430C2 |
| АНАЛОГИ ИНСУЛИНА, УСТОЙЧИВЫЕ К ПРОТЕАЗАМ | 2007 |
|
RU2524150C2 |
| КОМПЛЕКС, СОДЕРЖАЩИЙ АНАЛОГ ЧЕЛОВЕЧЕСКОГО ИНСУЛИНА, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 1995 |
|
RU2152399C2 |
| ПРЕПАРАТ, СОДЕРЖАЩИЙ ИНСУЛИН, НИКОТИНАМИД И АМИНОКИСЛОТУ | 2010 |
|
RU2533217C2 |
| КОМПЛЕКС АНАЛОГА ИНСУЛИНА И ПРОТАМИНА, СПОСОБ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ДИАБЕТА | 1995 |
|
RU2154494C2 |
Группа изобретений относится к фармацевтической промышленности, а именно к фармацевтической композиции и её применению. Фармацевтическая композиция для лечения патологического состояния, связанного с диабетом, включает: производное инсулина, представляющего собой человеческий инсулин A14E, B16H, B25H, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино}этокси)этокси]ацетил)), desB30; глицерин; фенол; м-крезол; ионы цинка; хлорид натрия, взятые в определенном количестве и имеющая значение pH 7,4. Применение фармацевтической композиции для лечения или облегчения заболевания, расстройства или состояния, выбранного из группы: связанного с диабетом 1 типа, диабетом 2 типа, нарушением толерантности к глюкозе, гипергликемией, дислипидемией, ожирением или метаболическим синдромом. Вышеописанное изобретение заключается в разработке нового состава с уникальной комбинацией вспомогательных веществ, который позволяет снизить степени образования олигомеров в месте инъекции. 2 н. и 1 з.п. ф-лы, 9 ил., 17 табл., 8 пр.
1. Фармацевтическая композиция для лечения патологического состояния, связанного с диабетом, содержащая:
4,2 мМ производного инсулина, представляющего собой человеческий инсулин A14E, B16H, B25H, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино} этокси)этокси]ацетил)), desB30;
1,5% вес/вес глицерина;
60 мМ фенола;
0 или 10 мМ м-крезола;
2,2±0,2 моль ионов цинка на шесть молей указанного производного инсулина;
20 мМ хлорида натрия,
и имеющая значение pH 7,4.
2. Фармацевтическая композиция по п. 1, содержащая
4,2 мМ производного инсулина, представляющего собой человеческий инсулин A14E, B16H, B25H, B29K((Nεэйкозандиоил-γGlu-[2-(2-{2-[2-(2-аминоэтокси)этокси]ацетиламино} этокси)этокси]ацетил)), desB30;
1,5% вес/вес глицерина;
60 мМ фенола;
10 мМ м-крезола;
2,2 моль ионов цинка на шесть молей указанного производного инсулина;
20 мМ хлорида натрия;
и имеющая значение pH 7,4.
3. Применение фармацевтической композиции по любому из пп. 1, 2 для лечения или облегчения заболевания, расстройства или состояния, выбранного из группы: связанного с диабетом 1 типа, диабетом 2 типа, нарушением толерантности к глюкозе, гипергликемией, дислипидемией, ожирением или метаболическим синдромом.
| WO 2013153000 А2, 17.10.2013 | |||
| WO 2009115469 А1, 24.09.2009 | |||
| WO 2015052088 А1, 16.04.2015 | |||
| ПРОИЗВОДНЫЕ ИНСУЛИНА, СОДЕРЖАЩИЕ ДОПОЛНИТЕЛЬНЫЕ ДИСУЛЬФИДНЫЕ СВЯЗИ | 2011 |
|
RU2598273C2 |
Авторы
Даты
2021-10-28—Публикация
2017-12-15—Подача