Изобретение относится к медицине, точнее к радиотерапии, и может найти применение в лучевой терапии онкологических больных.
Тотальное облучение тела человека (ТОТ) фотонами высоких энергий применяется для лечения онкологических заболеваний, таких как множественная миелома, лейкозы, лимфомы, так же при лечении некоторых солидных опухолей. Главной физико-технической задачей тотального облучения является получение в теле пациента равномерного распределения поглощенной дозы. В сочетании с химиотерапией ТОТ может применяться, как часть режима кондиционирования при трансплантации гемопоэтических стволовых клеток.
Существующие в настоящее время способы ТОТ человека ионизирующим излучением основаны на:
- использовании неподвижных источников излучения и больших расстояний от источника излучения до пациента (400-500 см), что делает возможным получение полей облучения, соизмеримых с ростом пациента;
- применении специальной, движущейся с заданной скоростью мимо источника, тележки с пациентом;
- облучении пациента путем сложения нескольких полей облучения;
- облучении с применением методов объемно-модулированной лучевой терапии и методом томотерапии, которые позволяют контролировать дозу облучения в органах риска.
На сегодняшний день известны различные способы и методы ТОТ.
Известен способ ТОТ облучения пациента неподвижным полем с горизонтальным пучком излучения. Пациент располагается на большом расстоянии источник-поверхность пациента (РИП) от 4-5 м, для создания размера поля равного росту человека. С целью создания равномерного дозного распределения применяются выравнивающие компенсаторы. Облучение производится латерально с двух сторон [Ильин Н.В. и др., авт. св. №1769418, A61N 5/10]. Недостатками этого метода являются необходимость наличия процедурного помещения нестандартных размеров, невозможность облучения пациентов большого роста и использование малых доз облучения, за счет больших расстояний от источника излучения, что увеличивает длительность процедуры лечения.
Известен способ тотального облучения с использованием стационарно расположенного излучателя с вертикальным пучком излучения и движущимся лечебным столом - тележкой с пациентом для охвата пучком излучения всего тела человека [The Radiotherapy of Malignant Disease, Springer-Ver., 1985, p. 362]. Этот способ заключается в использовании специальной тележки на рельсовом ходу, на которую укладывается пациент. Тележка движется с заданной скоростью под вертикальным пучком ионизирующего излучения от неподвижного источника таким образом, что пучком излучения охватывается все тело. Облучение также проводится с двух сторон путем переворачивания тела пациента. Способ позволяет обеспечить необходимую равномерность распределения поглощенной дозы в теле пациента и небольшое время процедуры. Однако необходимость использования специального устройства - тележки на рельсовом ходу в процедурном помещении, не позволяет использовать последнее для других видов лучевой терапии, например, стандартных методов лучевой терапии. Способ позволяет получить распределение поглощенной дозы по телу пациента с неравномерностью +/-10%.
Известен «Способ тотального облучения тела пациента» [Червяков A.M. и др., Патент РФ №2159135, A61N 5/10]. Способ заключается в ротации источника ионизирующего излучения со скоростью, определяемой по отношению замеренной и требуемой поглощенных доз, при этом замеренную поглощенную дозу устанавливают при ротации источника излучения вокруг фантома, моделирующего размеры пациента, со скоростью 1 град/с. Пациент укладывается на расстоянии L = А/2 ctg ниже изоцентра ротации, где А - рост пациента в см, α - половина угла ротации источника. Над пациентом устанавливают поглотитель ионизирующего излучения переменной толщины (D), определяемой по формуле:
D=-1/μ ln [РИО+√(L2+X2)/РИО+√(L2+A2/4),
где РИО - расстояние между источником ионизирующего излучения и изоцентром ротации в см, Х - расстояние от центра пациента на продольной оси до пересекающей ее плоскости, в которой определяют толщину в см, μ - линейный коэффициент ослабления материала фильтра.
Способ позволяет равномерно распределить поглощенную дозу по телу пациента в любом процедурном помещении с ротационным источником излучения, но имеет ряд недостатков, основным из которых является использование поглотителя ионизирующего излучения. Кроме того, изготовление поглотителя переменной толщины для каждого пациента является трудоемким, длительным, затратным процессом. Это удлиняет не только процедуру облучения, но и предлучевую подготовку, связанную с необходимостью как изготовления и установки поглотителя, так и использованием водного фантома, для предварительного определения равномерности распределения поглощенной дозы по телу пациента.
Известен метод ТОТ с применением объемно-модулированной лучевой терапии с использованием устройства многолепесткового коллиматора. «Total-body irradiation using linac-based volumetric modulated arc therapy: Its clinical accuracy, feasibility and reliability» [Radiother Oncol. 2018 Dec; 129(3):527-533. doi: 10.1016/j.radonc.2018.08.005. Epub 2018 Aug 29]. Данный метод включает в себя полноценную предлучевую подготовку: получение КТ-изображения всего тела пациента, оконтуривание органов риска, органов мишени. Причем из-за того, что движение лечебного стола линейного ускорителя имеет ограничение, то для людей с ростом больше, чем 120 см, делают два КТ-изображения. Лечебный план рассчитывается в специальной дозиметрической системе планирования с применением метода Vmat, который включает в себя лечение с несколькими изоцентрами (обычно три изоцентра) и стыковкой нескольких арок. Области стыковок между фиксированными размерами полей может доходить до двух сантиметров. Дозиметрическая система планирования учитывает область стыковок в процессе обратной оптимизации, применяя специальные алгоритмы расчета методом монте-карло. Такой метод позволяет снизить дозу на органы риска, сохраняя заданную дозу для мишени.
Существенным недостатком метода объемно-модулированной лучевой терапии является требование специальных компьютерных систем расчета дозы. При этом методика является трудоемкой и требует сложного расчета дозы в большом объеме, а также дополнительной индивидуальной проверки плана для каждого пациента и дозиметрического оборудования на котором будет проводиться проверка плана.
Известен метод ТОТ, выполняемый на аппарате томотерапии с применением лучевой терапии с модуляцией интенсивности. «Total marrow irradiation with helical tomotherapy along the entire patient’s axis: a planning technique to merge helical dose distributions producing uniform dose in the junction region» [Intl J Radiat Oncol Biol Phys 2010, 78: S821-S822]. Основным недостатком, которого является наличие аппарата томотерапии, который на сегодняшний день в России есть всего в трех центрах. Обычно этот метод применяется у детей и подростков в связи с имеющимися ограничениями по росту пациента. Основное отличие заключается в технологии доставки дозы (методе облучения) аппаратом томотерапии, в котором облучение происходит по спирали, радиационным полем, формируемым специальным бинарным многолепестковым коллиматором. При этом методика также является трудоемкой и требует сложного расчета дозы в большом объеме и дополнительной индивидуальной проверки плана для каждого пациента.
Таким образом, общими недостатками вышеуказанных способов являются: необходимость специального помещения нестандартных размеров, оборудование процедурного помещения дополнительными приспособлениями для проведения облучения, применение специальной разработанной для этого метода аппаратуры, применение и изготовление для каждого пациента поглотителей ионизирующего излучения.
Наиболее близким к предлагаемому является «Способ тотального облучения тела пациента» [Червяков A.M. и др., Патент РФ №2361634, A61N 5/10], который взят нами в качестве прототипа.
Согласно прототипу, ротационное облучение пациента проводят при размещении его на лечебном столе в плоскости ротации источника ионизирующего облучения, вращаемого вокруг изоцентра ротации. При этом угол ротации α определяли по формуле:
 ,
,
где А - рост пациента, L - расстояние от изоцентра до середины передне-заднего размера пациента, Р0 - половина передне-заднего размера пациента на уровне середины его тела. Затем осуществляли статическое облучение пациента передне-задними полями с использованием клиновидного фильтра, направляя основание его к середине тела пациента, при этом углы наклона консоли от вертикали β со стороны нижних конечностей и со стороны головы облучаемого пациента определяют по формуле:
 ,
,
где Р - половина передне-заднего размера пациента на уровне входа статического поля облучения. Отпускаемую дозу D с каждого поля рассчитывают по формуле:
 ,
,
где Dr - доза, отпускаемая с ротационного поля, R - расстояние от источника до центра ротации.
Принимая во внимание эффективность предложенного способа-прототипа, следует отметить, что он не лишен ряда недостатков.
Во-первых, серьёзным недостатком прототипа является необходимость стыковки статических полей с клином и ротационным полем в местах, где возникает падение дозы выше 10%, которое зависит от передне-заднего размера (ПЗР) пациента. При стыковке статических полей с ротационным полем могут появиться зоны переоблучения или недооблучения. Таким образом, способ-прототип требует необходимости многократной прямой индивидуальной дозиметрии, перед сеансами ТОТ. С учетом загрузки радиотерапевтических аппаратов пациентами, получающими другие методики облучения, подготовка к лечению одного пациента для ТОТ может занимать от одного до нескольких дней, в зависимости от количества больных на линейном ускорителе электронов. Особенно тяжело ситуация обстоит в клиниках, где установлен всего один линейный ускоритель электронов. Обычно такие клиники отказываются от проведения ТОТ, так как увеличивается время подготовки к облучению пациента, а также ограничивается пропускная способность процедурного помещения.
Во-вторых, недостатком прототипа является невыполнение требований ТОТ современным протоколам, в которых минимальная доза в коже пациента должна быть не менее 90% от заданной. В отличие от традиционных методов лучевой терапии, при которых нередко требуется бережное отношение к коже, для ТОТ предпочтительно, чтобы кожа получила полную предписанную дозу радиации. Это связано с заболеваниями, которые лечатся с помощью ТОТ, например, таких как лейкозы, где клетки, которые необходимо облучить, могут циркулировать в объеме крови кожи.
В связи с этим, мы считаем, что такой способ ТОТ является сложно выполнимым и трудоемким, и негативно сказывается на здоровье пациентов.
Технический результат настоящего изобретения состоит в осуществлении универсального, пригодного для широкого клинического использования способа тотального облучения, что достигается за счет регулирования количества мониторных единиц внутри отдельных сегментов сектора ротационного облучения.
Этот результат достигается тем, что в известном способе тотального облучения тела пациента, включающем ротационное облучение пациента заданной дозой облучения при размещении его на лечебном столе в плоскости ротации линейного ускорителя электронов, вращаемого вокруг изоцентра ротации с заданным на ускорителе полем и углом ротации, согласно изобретению, дополнительно перед ротационным облучением пациента выполняют разделение сектора вращения облучателя на сегменты, для каждого из них рассчитывают взвешивающий фактор wF(a) по формуле:

где 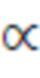 - угол облучателя,
- угол облучателя,  - расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см,
- расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см,  - расстояние от изоцентра до половины ПЗР фантома,
- расстояние от изоцентра до половины ПЗР фантома, 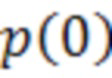 - половина ПЗР фантома,
- половина ПЗР фантома,  - толщина органического стекла,
- толщина органического стекла,  - линейный коэффициент ослабления пучка для материала фантома,
- линейный коэффициент ослабления пучка для материала фантома,  - линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека. Иколичество мониторных единиц с учетом заданной дозы и взвешивающего фактора по формуле:
- линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека. Иколичество мониторных единиц с учетом заданной дозы и взвешивающего фактора по формуле:
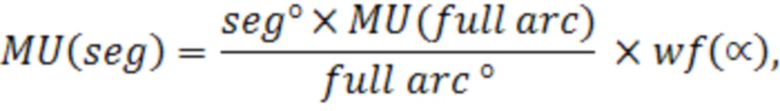
где MU(seg) - количество мониторных единиц на заданный сегмент, seg° - значение сегмента в градусах, MU (full arc) - экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри, равным 0°, по центру светового поля, на половине его ПЗР будет заданная доза, full arc - размер полной дуги 110°, wf(∝) - усредненный относительный взвешивающий фактор для заданного сегмента, после чего пациента размещают на лечебном столе в плоскости ротации ускорителя, так чтобы при значении гантри равном 0° центр светового поля находился на половине роста пациента, над пациентом сверху на расстоянии 55 см от лечебного стола устанавливают экран из органического стекла толщиной 1 см и проводят облучение с заданным полем 10.6×40 см и углом ротации 110°.
Разделение сектора вращения облучателя на сегменты перед ротационным облучением пациента позволяет исключить из схемы ТОТ статические поля с клиньями, при этом сохранить равномерное распределение заданной дозы в пациенте. Разделение сектора вращения облучателя было выполнено на 11 сегментов (350°-10°; 10°-20°; 20°-30°; 30°-40°; 40°-50°; 50°-55° и 305°-310°; 310°-320°; 320°-330°; 340°-350°) по 5 сегментов в каждую сторону, от центрального сегмента (350°-10°), что позволяет регулировать подводимую дозу, в отдельных сегментах.
Определение взвешивающего фактора wF(a) по формуле:
 ,
,
где 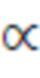 - угол облучателя;
- угол облучателя;  - расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см;
- расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см;  - расстояние от изоцентра до половины ПЗР фантома;
- расстояние от изоцентра до половины ПЗР фантома; 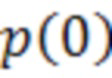 - половина ПЗР фантома;
- половина ПЗР фантома;  - толщина органического стекла;
- толщина органического стекла;  - линейный коэффициент ослабления пучка для материала фантома;
- линейный коэффициент ослабления пучка для материала фантома;  - линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека позволяет рассчитать отношение заданной поглощенной дозы, полученной под углом гантри равным 0° к поглощенной дозе, полученной под другим углом гантри на половине ПЗР пациента. Получение экспериментальных значений поглощенной дозы является очень трудоемким процессом, так как зависит от многих параметров: угла облучателя, толщины пациента, расстояния источник изоцентр и расстояния от изоцентра вращения до половины ПЗР пациента (фантома), толщины рассеивающего экрана и расстояния положения этого экрана от пациента. В дальнейшем значение усредненного относительного взвешивающего фактора для каждого сегмента, необходимо для расчета мониторных единиц с каждого отдельного сегмента с учетом заданной дозы облучения.
- линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека позволяет рассчитать отношение заданной поглощенной дозы, полученной под углом гантри равным 0° к поглощенной дозе, полученной под другим углом гантри на половине ПЗР пациента. Получение экспериментальных значений поглощенной дозы является очень трудоемким процессом, так как зависит от многих параметров: угла облучателя, толщины пациента, расстояния источник изоцентр и расстояния от изоцентра вращения до половины ПЗР пациента (фантома), толщины рассеивающего экрана и расстояния положения этого экрана от пациента. В дальнейшем значение усредненного относительного взвешивающего фактора для каждого сегмента, необходимо для расчета мониторных единиц с каждого отдельного сегмента с учетом заданной дозы облучения.
Для облучения пациентов со среднестатистическими физическими данными достаточно рассчитать относительный взвешивающий фактор для ПЗР 20 см и 14 см. ПЗР 20 см моделирует толщину пациента в направлении от центра к голове, а ПЗР 14 см моделирует толщину пациента от центра к ногам. Для наиболее уязвимых областей таких как щиколотки, шея возможно дополнительное использование тканеэквивалентных болюсов.
Определение количество мониторных единиц с учетом заданной дозы и взвешивающего фактора по формуле:
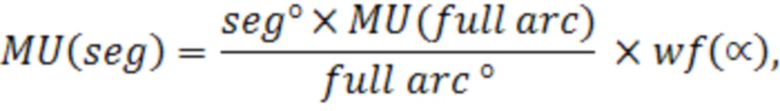
где MU(seg) - количество мониторных единиц на заданный сегмент; seg° - значение сегмента в градусах; MU(full arc) - экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри равным 0° по центру светового поля, на половине его ПЗР будет заданная доза; full arc° - размер полной дуги 110°; wf(∝) - усредненный относительный взвешивающий фактор для заданного сегмента, позволяет получить значение мониторных единиц для линейного ускорителя электронов, которое будет соответствовать заданному значению отпускаемой поглощенной дозы. Так же значение мониторных единиц является важным параметром, который необходим для создания в системе управления ускорителем лечебного плана. Лечебный план включает в себя набор радиационных полей облучения, каждое из которых соответствует сегменту с определенным сектором вращения, размером радиационного поля и количеством отпускаемых мониторных единиц.
Размещение пациента на лечебном столе в плоскости ротации ускорителя осуществляется по световому полю при значении угла гантри равному 0°, так чтобы центр светового поля ускорителя был на уровне середины длины тела пациента (фиг 1). Угол ротации 110° (305°-55°) градусов позволяет проводить равномерное облучение пациентов с ростом до 2 м. Начальный (305°) и конечный (55°) углы гантри выбраны таким образом, чтобы световое поле, при установке облучателя в заданный угол, было вне пациента, при этом край поля должен совпадать с началом тела пациента.
Поле облучения, равное 10.6×40 см2 в изоцентре вращения линейного ускорителя, выбирается в зависимости от значения РИП до кушетки, на которой расположен пациент, чтобы обеспечить на половине заданного ПЗР пациента равного 20 см, 80 см в направлении право-лево и 20 см в направлении голова-ноги пациента. Такое поле облучения позволяет равномерно облучить человека с ростом до 2 м.
Установка органического стекла толщиной 1 см на расстоянии 55 см над лечебной кушеткой сверху необходима для увеличения минимальной дозы в коже пациента не менее 95% от заданной. Экран из органического стекла по необходимости (в зависимости от подводимой дозы) так же может использоваться для установки дополнительных блоков, экранирующих органы риска.
Таким образом, предварительное однократное выполнение вышеперечисленных шагов позволяет создать равномерное распределение заданной поглощенной дозы в теле для большинства пациентов среднестатистических физических данных. При этом значительно сокращается время предлучевой подготовки, требующей расчета угла ротации индивидуально для каждого пациента, а также индивидуального дополнительного расчета углов положения гантри для статических радиационных полей облучения в области стыковки.
Сущность способа поясняется примерами.
Для проверки данного способа перед клинической апробацией на пациентах, все расчеты и измерения были применены к дозиметрическим фантомам, которые позволяют моделировать процессы поглощения и рассеяния излучения в пациенте.
Пример №1.
В первом примере был взят твердотельный пластинчатый фантом SP34 плотностью 1.045 г/см3 фирмы IBA Dosimetry. Фантом состоит из 29 пластин толщиной 1 см, 1 пластины толщиной 1 мм, 2-х пластин толщиной 2 мм, и 1 пластины толщиной 5 мм. Изготовлен из белого полистирола типа RW3. Размеры пластин 30×30×30 см. Фантом относится к типу водоэквивалентного геометрического фантома, который хорошо воспроизводит дозиметрические свойства воды, которая рекомендована в качестве стандартной среды для калибровочных измерений.
С помощью формулы для каждого угла гантри от 305° до 55° был определен свой весовой коэффициент для толщины фантома ПЗР 20 см и 14 см.
Пример расчета взвешивающего фактора wf(α) для угла гантри равного 1° и ПЗР фантома равного 20 см.
Перевод градусов в радианы:



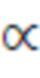 - угол облучателя равный 0.017 рад;
- угол облучателя равный 0.017 рад;
 - расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см;
- расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см;
 - расстояние от изоцентра ускорителя до половины ПЗР фантома равно 99 см;
- расстояние от изоцентра ускорителя до половины ПЗР фантома равно 99 см;
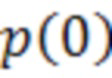 - половина ПЗР фантома, равно 10 см;
- половина ПЗР фантома, равно 10 см;
 - толщина органического стекла, равно 1 см;
- толщина органического стекла, равно 1 см;
 - линейный коэффициент ослабления пучка для материала фантома равен 0.0707;
- линейный коэффициент ослабления пучка для материала фантома равен 0.0707;
 - линейный коэффициент ослабления пучка для материала экрана равен 0.0797;
- линейный коэффициент ослабления пучка для материала экрана равен 0.0797;




Пример расчета взвешивающего фактора wf для угла гантри равного 55° и ПЗР фантома равного 20 см.
Перевод градусов в радианы



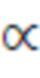 - угол облучателя равный 55°
- угол облучателя равный 55°
 - расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см;
- расстояние от источника до изоцентра ускорителя (точки вращения облучателя) равное 100 см;
 - расстояние от изоцентра ускорителя до половины ПЗР фантома равно 99 см;
- расстояние от изоцентра ускорителя до половины ПЗР фантома равно 99 см;
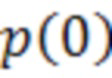 - половина ПЗР фантома, равно 10 см.
- половина ПЗР фантома, равно 10 см.
 - толщина органического стекла, равно 1 см.
- толщина органического стекла, равно 1 см.
 - линейный коэффициент ослабления пучка для материала фантома равен 0.0707;
- линейный коэффициент ослабления пучка для материала фантома равен 0.0707;
 - линейный коэффициент ослабления пучка для материала экрана равен 0.0797;
- линейный коэффициент ослабления пучка для материала экрана равен 0.0797;

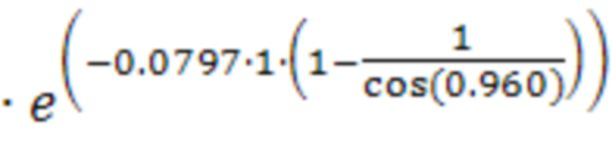


Таблица 1. Расчеты для ПЗР 20 см.
Таблица 2. Расчеты для ПЗР 14 см.
Далее полученные весовые коэффициенты были усреднены для следующих сегментов: 350°-10°; 10°-20°; 20°-30°; 30°-40°; 40°-50°; 50°-55° и в противоположенном направлении 305°-310°; 310°-320°; 320°-330°; 340°-350°.
Для укладки пациента в направлении указнном на Фиг.1, ПЗР для расчета взвешивающего фактора берется 20 см для сегметов 350°-10°; 10°-20°; 20°-30°; 30°-40°; 40°-50°; 50°-55° и 14 см для сегментов 305°-310°; 310°-320°; 320°-330°; 340°-350°.
Таблица 3. Усредненные значения взвешивающего фактора были посчитаны для следующих углов гантри w(f) ПЗР=20 см.
Таблица 4. Усредненные значения взвешивающего фактора были посчитаны для следующих углов гантри w(f) ПЗР=14 см.
Далее экспериментально было полученно 
 значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме для ПЗР=20 см и ПЗР=14 см, установленном под углом гантри равным 0° по центру светового поля, на половине его ПЗР будет заданная доза. Для этого на фантом было отпущено 500М.Е. при этом полученная поглощенная доза составила для ПЗР=20см 12.717 сГр, а для ПЗР=14см 13.056 сГр. По пропорции были получены М.Е. для дозы 100сГр: 3931.745 и 3829.657 для ПЗР 20см и 14 см.
значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме для ПЗР=20 см и ПЗР=14 см, установленном под углом гантри равным 0° по центру светового поля, на половине его ПЗР будет заданная доза. Для этого на фантом было отпущено 500М.Е. при этом полученная поглощенная доза составила для ПЗР=20см 12.717 сГр, а для ПЗР=14см 13.056 сГр. По пропорции были получены М.Е. для дозы 100сГр: 3931.745 и 3829.657 для ПЗР 20см и 14 см.


Количество мониторных единиц (МЕ) для каждого сегмента рассчитывался по формуле:


 - количество мониторных единиц на заданный сегмент;
- количество мониторных единиц на заданный сегмент;

 - значение сегмента в градусах;
- значение сегмента в градусах;

 - экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри равным 0° по центру светового поля, на половине его ПЗР будет заданная доза;
- экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри равным 0° по центру светового поля, на половине его ПЗР будет заданная доза;

 - размер полной дуги 110°;
- размер полной дуги 110°;

 - усредненный относительный взвешивающий фактор для заданного сегмента;
- усредненный относительный взвешивающий фактор для заданного сегмента;
Пример расчета 
 для сегмента 350°-10°
для сегмента 350°-10°
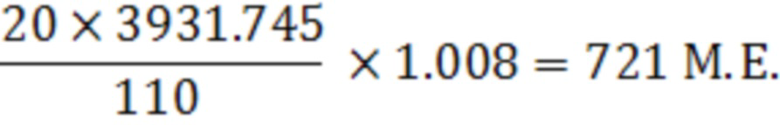
Пример расчета 
 для сегмента 40°-50° (ПЗР=20см)
для сегмента 40°-50° (ПЗР=20см)

Пример расчета 
 для сегмента 310°-320° (ПЗР=14см)
для сегмента 310°-320° (ПЗР=14см)

Таблица 5. Мониторные единицы для заданных сегментов.
Для центрального сегмента 350°-10° значение мониторных единиц рассчитывается для ПЗР 20 см.
Значение мониторных единиц округляется до целого значения, так как на линейном ускорителе электронов невозможно отпустить дробное количество мониторных единиц.
Полученные расчетные данные были проверены экспериментально, для разной толщины (разного ПЗР) фантома, а также его положения относительно центральной точки (значение гантри равное 0°). Фантом смещался вдоль поля излучения и измерения проводились ионизационной камерой фармеровского типа фирмы IBA Dosimetry FC65-G, каждые 10 см. Ионизационная камера при этом была установлена в центре фантома на половине его ПЗР. Толщина (ПЗР) фантома составила: 7, 14, 20, 26 см. Расчетные мониторные единицы со всех сегментов отпускались для каждого отдельного положения и толщины фантома через каждые 10 см от центра (точки, соответствующей центратору ускорителя при гантри равному 0°) к периферии. Сверху на расстоянии 55 см от лечебного стола был установлен экран из органического стекла толщиной 1 см. Облучение проводилось с заданным полем 10.6×40 см и углом ротации 110°.
Таблица 6. Полученные значения поглощенной дозы в Гр, для расчета МЕ на фантом толщиной (ПЗР) 20 см.
Таблица 7. Процент отклонения поглощенной дозы для различных толщин и положения фантома от значения поглощенной дозы в центральной точке для толщины фантома 20 см.
Таблица 8. Полученные значения поглощенной дозы в Гр, для расчета МЕ на фантом толщиной (ПЗР) 14 см.
Таблица 9. Процент отклонения поглощенной дозы для различных толщин и положения фантома от значения поглощенной дозы в центральной точке для толщины фантома 14 см.
При этом знак «-» говорит о превышении полученной поглощенной дозы от заданной поглощенной дозы, а знак «+» наоборот о занижении.
Значения поглощенной дозы были измерены для всего диапазона предполагаемой длины и нескольких разных значений толщины (ПЗР) фантома для того, чтобы знать ограничения данного способа. Полученные данные соответствуют теоретическим расчетам, доза в измеренных точках не превышает заданный диапазон ± 5%. Большие отклонения в значениях поглощенной дозы в основном связаны с несоответствием значения толщины (ПЗР) фантома в заданной точке с ПЗР пациента. Например, ПЗР для щиколотки ноги не может быть равен значению 26 см.
Так же была проведена проверка распределения дозы с глубиной, при смещении фантома на 88 см от центра. Для этого значение поглощенной дозы было измерено на глубине фантома 2 см и 16 см для ПЗР 18 см и на глубине 1.5 и 18.5 см для ПЗР 20 см, максимальное отклонение дозы в этих точках составило 10%.
Пример №2.
Для подтверждения данных и получения более расширенной информации по дозному распределению, такие же мониторные единицы были отпущены на специальный дозиметрический антропоморфный фантом ATOM Adult male Phantom Model c установленными в него радиохромными пленками Gafchromic EBT 3. Данный фантом моделирует торс взрослого мужчины ростом 173 см и весом 73 кг. и состоит из трех частей: головы с шейным отделом позвоночника, торса (грудной клетки) и таза. Без имитаторов рук и ног.
Фантом выполнен из ткане-эквивалентного материала (ТЭМ), право на который принадлежит компании CIRS. Линейные коэффициенты ослабления имитируемых тканей совпадают с коэффициентами для воды и костной ткани в пределах 1%, а для лёгких в пределах 3% для диапазона энергии излучения от 50 кэВ до 25 МэВ. Имеются имитаторы ткани лёгких в стандартной конфигурации плотностью 0,2 г/см3. Имитируемые в фантоме ткани - это усреднённые мягкая и костная ткани, хрящи, спинной мозг, позвоночные диски, лёгкие, мозг, пазухи, полости трахеи и бронхов. Расчётные значения линейных коэффициентов ослабления (см-1), физическая и электронная плотность ткане-эквивалентных материалов, применяемых в дозиметрических фантомах (для взрослого) приведены в таблице 3.3. 6 руководства к фантому.
Анатомия скелета в фантоме включает в себя гомогенные композиции костной ткани, в которых применены усреднённые отношения кортикальной и трабекулярной составляющих и возраст-специфичные минеральные плотности.
Всего в фантом было установлено 12 пленок различной длины и шириной 6 см (Фиг. 2). Пленки устанавливались вертикально вдоль центральной линии фантома. Доза отпускалась 1Гр в положении фантома на спине, затем фантом переворачивался на живот, и доза 1Гр отпускалась повторно.
Пленка №3, установленная в изоцентре между 33 и 32 пластиной фантома является референсной пленкой (Фиг. 3). Относительно нее сравнивались все остальные пленки.
Таблица 10 Расположение и размер пленок в фантоме.
Уровня Th9-Th10
Th5-6
без учета болюса
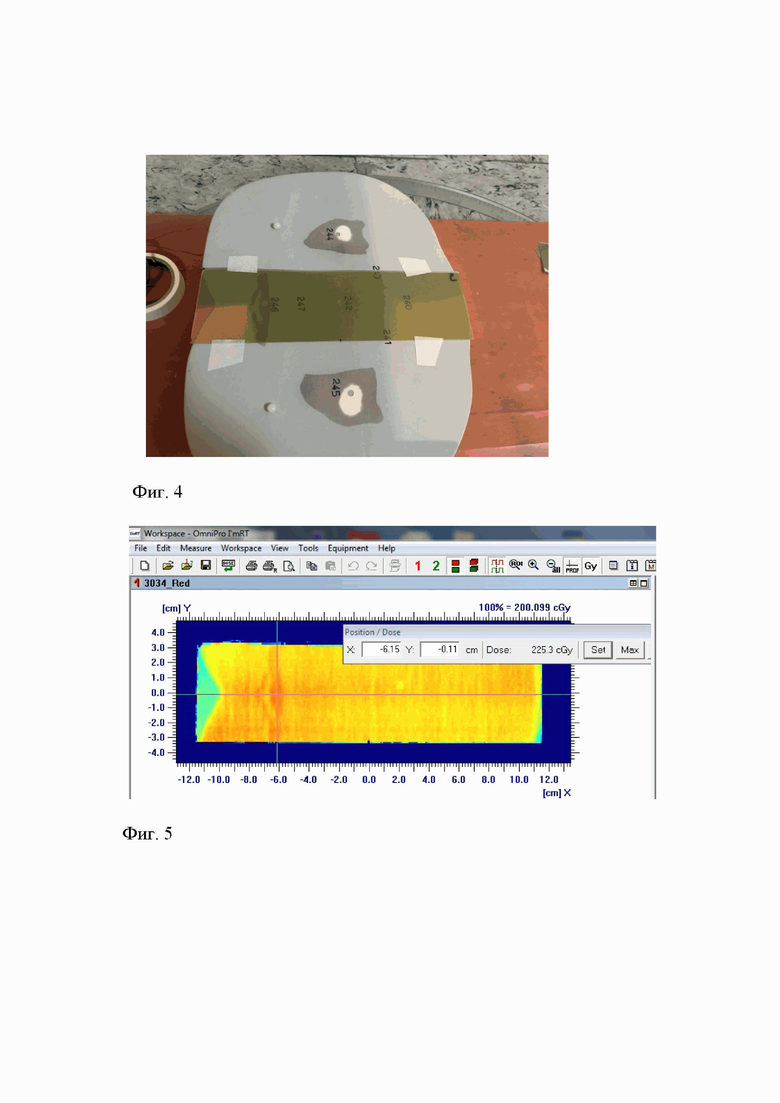
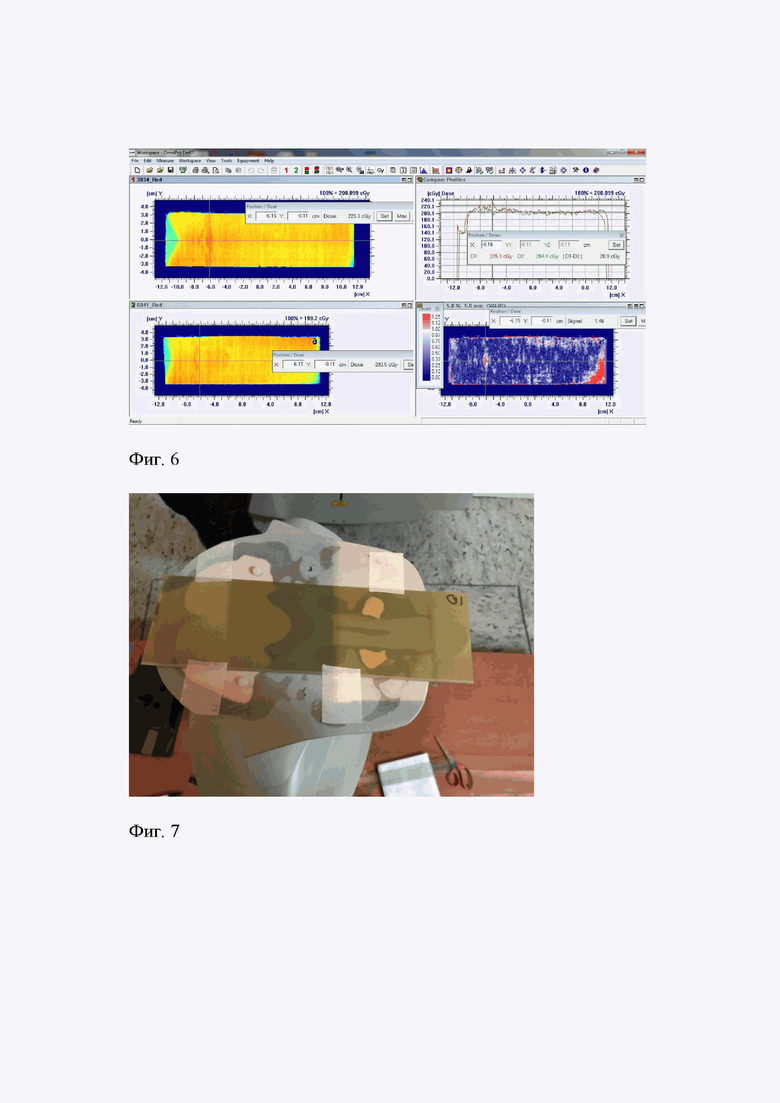
При анализе облученных пленок было установлено, что референсная пленка №3 равномерно облучена в дозе 2Гр, за исключением максимума возникающего на уровне позвоночного диска, (Фиг. 4, Фиг. 5). Максимальная точка 2.25 Гр.
Для пленок №№2, 4, 5, 6, 7, 8, 9 гамма индекс составил от 95.5%-98.6%, наилучший результат получился для пленки №6, на уровне Th12 позвонка ( Фиг 6).
Для пленок №№1, 10, 11, 12 гамма индекс был равен: 48.9%; 63.7%; 65.1%; 77.7% для критерия (5%, 5 мм), при этом для пленок 11, 12 и критерия (7%, 3мм) гамма индекс составил 73.7% и 90.2%)
На пленке №1 фиксируется превышение дозы на 10%, что объясняется малым размером ПЗР равным 13.5 см и не большим расстоянием (12.5 см) от центральной части, где расчет выполнен на ПЗР 20 см. Исходя из опыта для наших пациетов в этой области ПЗР обычно составляет от 15-20 см. Остальные пленки показывают достаточно приемлемый результат.
На неравномерное распределение дозы у пленок №10 и №11, могут оказывать влияние воздушные полости пазух носа и наличие плотной костной ткани вокруг этих полостей (Фиг. 7).
Анализ облученных радиохромных пленок показал, что на половине ПЗР пациента доза составила требуемых 2 Гр. При этом пленки №2, 3, 4, 5, 6, 7, 8, 9 облучены равномерно в дозе 2Гр по глубине, за исключением локальных максимумов, в которых доза не превышает 10%. На пленке №1 наблюдается равномерное превышение дозы 10-15% связанное с малым размером ПЗР. У пленок под номерами 10, 11, 12 превышения по дозе составили 15-25%, которые находятся в области носовых пазух, костях и частично в прилегающих мягких тканях. Так же важно отметить превышение дозы в тканях легких на 25%, которая связана с малой плотностью тканей легкого. Поглощенная доза на половине ПЗР фантома находится в пределах ±5%.
Для лучшего понимания приводим иллюстрации:
Фиг. 1 - схема тотального облучения тела пациента на линейном ускорителе электронов.
Фиг. 2 - антропоморфный фантом ATOM с радиохромными пленками и тканеэквивалентным болюсом на области шеи.
Фиг. 3 - нумерация пластин антропоморфного фантома ATOM.
Фиг. 4 - вид антропоморфного фантома ATOM в разрезе, с установленной референсной радиохромной пленкой №3.
Фиг. 5 - анализ дозового распределения облученной пленки №3 в программной среде OmniPro IMRT IBA Dosimetry.
Фиг. 6 - сравнение полученных дозных распределений пленок №3 и №6 в программной среде OmniPro IMRT IBA Dosimetry.
Фиг. 7 - аксиальный срез в фантоме ATOM на котором была установлена пленка №10.
Предлагаемый способ по сравнению с известными обладает следующими преимуществами:
1. Не требует наличия специального помещения нестандартных размеров или дополнительного оборудования в виде стола-тележки на рельсовом ходу. Может применяться в любом помещении, в котором установлен медицинский линейный ускоритель электронов.
2. Не зависит от производителя и может быть реализован на любом современном линейном ускорителе электронов с опцией ротационной терапии и наличием сглаживающего фильтра.
3. Не требует специальных коммерческих компьютерных систем расчета дозы, а также дополнительной индивидуальной проверки плана для каждого пациента.
4. Значительно сокращает время предлучевой подготовки.
5. Проведенные измерения показали, что данный способ обеспечивает равномерное распределение поглощенной дозы в твердотельном фантоме моделирующим размеры человека с ПЗР до 30 см и ростом до 2 м, с точностью ±5% на половине ПЗР.
6. Способ сокращает время подготовки пациентов к лечению и является универсальным для 95% пациентов.
Способ разработан в отделе лучевых и комбинированных методов лечения «РНЦРХТ им. Ак. А.М. Гранова» МЗ РФ и может быть рекомендован для проведения тотального облучения тела пациентов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования острой лучевой болезни в эксперименте | 2023 |
|
RU2811270C1 |
| СПОСОБ ТОТАЛЬНОГО ОБЛУЧЕНИЯ ТЕЛА ПАЦИЕНТА | 1999 |
|
RU2159135C1 |
| СПОСОБ ТОТАЛЬНОГО ОБЛУЧЕНИЯ ТЕЛА ПАЦИЕНТА | 2008 |
|
RU2361634C1 |
| МНОГОФУНКЦИОНАЛЬНЫЙ КОМПЛЕКС ДЛЯ ДИАГНОСТИКИ, ДИСТАНЦИОННОЙ СТЕРЕОТАКСИЧЕСКОЙ РАДИОХИРУРГИИ И РАДИОТЕРАПИИ | 2019 |
|
RU2712303C1 |
| УСТРОЙСТВО ДЛЯ РОТАЦИОННОЙ ЛУЧЕВОЙ ТЕРАПИИ | 1997 |
|
RU2147900C1 |
| СПОСОБ ЛЕЧЕНИЯ РАСПРОСТРАНЕННОГО РАКА ЯИЧНИКОВ С ОТДАЛЕННЫМИ МЕТАСТАЗАМИ | 2008 |
|
RU2395314C2 |
| АДАПТИВНЫЙ АЛГОРИТМ ВАЛИДАЦИИ ДОЗИМЕТРИЧЕСКОЙ МОДЕЛИ ТОНКОГО СКАНИРУЮЩЕГО ПРОТОННОГО ПУЧКА В ОБЛАСТИ ПРОТОННОЙ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2022 |
|
RU2797781C1 |
| Компактный однокабинный комплекс протонной лучевой терапии | 2016 |
|
RU2697232C2 |
| Способ лечения плоскоклеточного рака головы и шеи | 2020 |
|
RU2744748C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДОЗНОГО РАСПРЕДЕЛЕНИЯ В ОБЪЕКТЕ | 1989 |
|
SU1823194A1 |


Способ относится к медицине, а именно к лучевой терапии, и может быть использовано для тотального облучения тела пациента. Проводят ротационное облучение пациента заданной дозой облучения при размещении его на лечебном столе в плоскости ротации линейного ускорителя электронов, вращаемого вокруг изоцентра ротации с заданным на ускорителе полем и углом ротации. При этом дополнительно перед ротационным облучением пациента выполняют разделение сектора вращения облучателя на 11 сегментов, для каждого из них рассчитывают поправочный коэффициент k(∝) по формуле:
 , где
, где 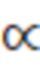 - угол облучателя,
- угол облучателя,  - расстояние от источника до изоцентра ускорителя, равное 100 см,
- расстояние от источника до изоцентра ускорителя, равное 100 см,  - расстояние от изоцентра до половины передне-заднего размера фантома,
- расстояние от изоцентра до половины передне-заднего размера фантома, 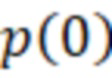 - половина передне-заднего размера фантома,
- половина передне-заднего размера фантома, 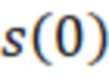 - толщина органического стекла,
- толщина органического стекла,  - линейный коэффициент ослабления пучка для материала фантома,
- линейный коэффициент ослабления пучка для материала фантома,  - линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека. Определяют количество мониторных единиц с учетом заданной дозы и поправочного коэффициента по формуле:
- линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека. Определяют количество мониторных единиц с учетом заданной дозы и поправочного коэффициента по формуле:
 где MU(seg) – количество мониторных единиц на заданный сегмент, seg° - значение сегмента в градусах, MU(full arc) – экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри равным 0° по центру светового поля , на половине его переднезаднего размера будет заданная доза, full arc°- размер полной дуги 110°, k(∝) - усредненный поправочный коэффициент для заданного сегмента. После чего пациента размещают на лечебном столе в плоскости ротации ускорителя, так чтобы при значении гантри равном 0° центр светового поля находился на половине роста пациента. Над пациентом сверху на расстоянии 55 см от лечебного стола устанавливают экран из органического стекла толщиной 1 см и проводят облучение с заданным полем 10,6x40 см и углом ротации 110°. Способ обеспечивает создание равномерного распределения заданной поглощенной дозы в теле для большинства пациентов за счет регулирования количества мониторных единиц внутри отдельных сегментов сектора ротационного облучения. 7 ил., 10 табл., 2 пр.
где MU(seg) – количество мониторных единиц на заданный сегмент, seg° - значение сегмента в градусах, MU(full arc) – экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри равным 0° по центру светового поля , на половине его переднезаднего размера будет заданная доза, full arc°- размер полной дуги 110°, k(∝) - усредненный поправочный коэффициент для заданного сегмента. После чего пациента размещают на лечебном столе в плоскости ротации ускорителя, так чтобы при значении гантри равном 0° центр светового поля находился на половине роста пациента. Над пациентом сверху на расстоянии 55 см от лечебного стола устанавливают экран из органического стекла толщиной 1 см и проводят облучение с заданным полем 10,6x40 см и углом ротации 110°. Способ обеспечивает создание равномерного распределения заданной поглощенной дозы в теле для большинства пациентов за счет регулирования количества мониторных единиц внутри отдельных сегментов сектора ротационного облучения. 7 ил., 10 табл., 2 пр.
Способ тотального облучения тела пациента, включающий ротационное облучение пациента заданной дозой облучения при размещении его на лечебном столе в плоскости ротации линейного ускорителя электронов, вращаемого вокруг изоцентра ротации с заданным на ускорителе полем и углом ротации, отличающийся тем, что дополнительно перед ротационным облучением пациента выполняют разделение сектора вращения облучателя на 11 сегментов, для каждого из них рассчитывают поправочный коэффициент k(∝) по формуле:
 ,
,
где  - угол облучателя,
- угол облучателя, 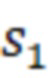 - расстояние от источника до изоцентра ускорителя, равное 100 см,
- расстояние от источника до изоцентра ускорителя, равное 100 см,  - расстояние от изоцентра до половины передне-заднего размера фантома,
- расстояние от изоцентра до половины передне-заднего размера фантома,  - половина передне-заднего размера фантома,
- половина передне-заднего размера фантома, 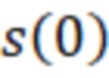 - толщина органического стекла,
- толщина органического стекла, 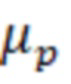 - линейный коэффициент ослабления пучка для материала фантома,
- линейный коэффициент ослабления пучка для материала фантома,  - линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека, и количество мониторных единиц с учетом заданной дозы и поправочного коэффициента по формуле:
- линейный коэффициент ослабления пучка для материала экрана, предназначенного для увеличения дозы на поверхности тела человека, и количество мониторных единиц с учетом заданной дозы и поправочного коэффициента по формуле:

где MU(seg) – количество мониторных единиц на заданный сегмент, seg° - значение сегмента в градусах, MU(full arc) – экспериментально полученное значение мониторных единиц для ротационного пучка гантри от 305° до 55°, при котором в пластиковом фантоме, установленном под углом гантри, равным 0°, по центру светового поля, на половине его передне-заднего размера будет заданная доза, full arc° - размер полной дуги 110°, k(∝) - усредненный поправочный коэффициент для заданного сегмента; после чего пациента размещают на лечебном столе в плоскости ротации ускорителя, так чтобы при значении гантри, равном 0°, центр светового поля находился на половине роста пациента, над пациентом сверху на расстоянии 55 см от лечебного стола устанавливают экран из органического стекла толщиной 1 см и проводят облучение с заданным полем 10,6×40 см и углом ротации 110°.
| СПОСОБ ТОТАЛЬНОГО ОБЛУЧЕНИЯ ПОВЕРХНОСТИ ТЕЛА ПАЦИЕНТА | 2010 |
|
RU2440162C1 |
| СПОСОБ ТОТАЛЬНОГО ОБЛУЧЕНИЯ ТЕЛА ПАЦИЕНТА | 2008 |
|
RU2361634C1 |
| СПОСОБ ТОТАЛЬНОГО ОБЛУЧЕНИЯ КОЖИ ПАЦИЕНТА | 2001 |
|
RU2185215C1 |
| СПОСОБ ТОТАЛЬНОГО ОБЛУЧЕНИЯ ТЕЛА ПАЦИЕНТА | 1999 |
|
RU2159135C1 |
| US 6730924 B1, 04.05.2004 | |||
| ЛЕБЕДЕНКО И | |||
| М | |||
| и др | |||
| Проведение тотального облучения пациента перед трансплантацией костного мозга | |||
| Радиационная онкология и ядерная медицина | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| SPRINGER A | |||
| et al | |||
| Total body irradiation | |||
Авторы
Даты
2021-11-29—Публикация
2021-03-10—Подача