Изобретение относится к области биофизики, биотехнологии, в части применения молекулярной диагностики с использованием биологических жидкостей (маркеров). Изобретение может быть использовано в разработке высокочувствительных биосенсоров различных биомолекулярных маркеров, в том числе социально-значимых заболеваний, а так же к технологии изготовления сенсорных структур на основе твердотельного полупроводника и функционального органического покрытия и может быть использовано при создании биосенсоров на основе полевых транзисторов или структур. Изобретение позволяет получать более достоверные, специфичные и селективные результаты при выявлении биологических маркеров с помощью сенсоров на основе КНИ-транзисторов в автоматическом режиме.
В заявляемом изобретении используются следующие термины:
КНИ-транзистор - транзистор, изготовленный по технологии «кремний на изоляторе»
КНИ-структура - структура кремний на изоляторе
ДНК - дезоксирибонуклеиновая кислота;
дц - двуцепочечная;
НК - нуклеиновая кислота (ДНК или РНК);
п.н. - пары нуклеотидов;
ПЦР - полимеразная цепная реакция;
РНК - рибонуклеиновая кислота;
ФГ- фосфорилгуанидиновая группа;
ФГ-олигонуклеотиды - производные олигонуклеотидов, содержащие одну или более фосфатных групп, в которых на атоме фосфора введен остаток гуанидина или замещенного гуанидина.
В настоящее время основными методами клинической диагностики инфекционных заболеваний человека являются иммуноанализ и полимеразная цепная реакция. Детекция нуклеиновых кислот востребована в различных областях молекулярной биологии, биомедицинской химии и медицины. Нуклеиновые кислоты могут являться биомаркерами определенных заболеваний. В качестве биомаркеров в последнее время все более часто используются микроРНК - малые регуляторные РНК молекулы, уровень которых напрямую может быть связан с патологическими процессами, происходящими в организме. Для детекции специфических последовательностей нуклеиновых кислот в настоящее время разработано большое количество разнообразных подходов. Созданы биосенсоры, чья работа основана на различных принципах. Одним из критериев по которому можно разделить все сенсоры является наличие специфических меток, которые позволяют детектировать целевые объекты, так называемые меточные и безметочные подходы. Для первых типов сенсоров необходимой стадией является введение меток в систему измерений необходимых для детекции, например, флуоресцентных, электрохимических, оптических и др.
Все эти методы обладают рядом существенных недостатков: низкая чувствительность для иммунохроматографического анализа; необходимость в квалифицированных специалистах и дорогостоящем оборудовании; продолжительное время анализа; высокая вероятность возникновения ложноположительного результата в случае полимеразной цепной реакции. В связи с этим успешно развиваются новые высокочувствительные аналитические системы регистрации биомолекул, основанные на сочетании современных молекулярно-биологических и физических методов, обеспечивающих детекцию немеченых молекул (label free) (Dmitrienko E.V., Naumova O.V., Fomin В.I., Kupryushkin M.S., Volkova (Poryvaeva) A.V., Amirkhanov N.V., Semenov D.V., Pyshnaya I.A., Pyshnyi. Surface modification of SOI-FET sensors for label-free and specific detection of short RNA analyte // Nanomedicine (Lond). 2016 Aug;11(16):2073-2082. doi: 10.2217/nnm-2016-0071.).
Нанопроволочные, полевые со структурой кремний на изоляторе - КНИ-транзисторы - являются высокочувствительными сенсорными элементами, широко используемыми для качественного и количественного анализа биологических молекул и химических веществ. Принцип действия таких сенсорных элементов основан на модуляции проводимости нано(?и микро)проволоки при осаждении на ее поверхность заряженной частицы, либо экранировании заряда молекул раствора адсорбируемой частицей. При этом детектируемая частица действует как локальный виртуальный затвор. Если размер области обеднения, индуцированной адсорбируемой частицей, сопоставим с размерами нанопроволоки, то достигается чувствительность сенсорного элемента на уровне единичной частицы на проволоку. Это определяет требования к размерам нанопроволок, которые должны быть сопоставимы с пространственными размерами детектируемого объекта - от сотен до единиц нанометров (от вирусов до белков и фрагментов нуклеиновых кислот), для достижения максимальной чувствительности биосенсора.
Известно техническое решение, являющееся современным, технологичним и перспективным методом детекции биомолекулярных маркеров (O.V. Naumova, V.P. Popov, L.N. Safronov, B.I. Fomin, D.A. Nasimov, A.V. Latyshev, A.L. Aseev, Yu.D. Ivanov and A.I. Archakov, Ultra-Thin SOI Layer Nanostructuring and Nanowire Transistor Formation for FemtoMole Electronic Biosensors, ECS Transactions, 2009, т. 25, №10, стр. 83-87)). Способ использует наноразмерные кремниевые проволоки шириной от нескольких сотен нанометров до нескольких микрометров, расположенные на слое из диоксида кремния, толщиной 300-500 нм, «лежащего» на кремниевой подложке, так называемые КНИ-структуры (кремний на изоляторе). Заряды адсорбированных биомолекул при связывании их с поверхностью нанопроволоки индуцируют возникновение компенсирующих зарядов в полупроводнике, изменению его поверхностного потенциала и, как следствие, к изменению силы тока, проходящей через сенсорный элемент, которое фиксируется аналогово-цифровым преобразователем. Данное техническое решение продемонстрировано только в отношении белкового аналита, при этом отсутствуют данные о специфичности (избирательности) взаимодействия. В процессе измерения отсутствует одновременное измерение сигнала контрольных (референсных) и специфичных нанопроволок. В качестве специфического сигнала используют измерение тока, значения которого не превышают микроамперных значений, что накладывает дополнительные ограничения на аппаратную базу детекции сигнала. Вышеперечисленные аспекты приводят к ряду недостатков известного технического решения. Продемонстрированное выявление только белковой молекулы не дает представления о возможном использовании предложенного сенсора для детекции других аналитов, при этом не продемонстрирована избирательность выявления конкретного аналита, что может приводить к невозможности детекции конкретного аналита в присутствии молекул подобного строения (что необходимо для успешного применения биосенсора). Измерение тока в качестве специфического сигнала приводит к необходимости использования высокоточных приборов для детекции и приводит к понижению чувствительности и достоверности измерений. Отсутствие одновременного измерения сигналов контрольных (референсных) и специфичных нанопроволок в процессе измерения приводит к снижению достоверности анализа.
Известно техническое решение, представленное в устройстве регистрации макромолекул при медицинской диагностике (Патент РФ №168546, «Устройство регистрации макромолекул при медицинской диагностике», МПК G01N 33/53, G01N 33/50, опубликован 08.02.2017 г.). С помощью роботов-раскапывателей исключительно на рабочую поверхность биочипа ковалентно иммобилизуется монослой макромолекул маркеров заболевания. Формирование монослоя макромолекул маркеров заболевания на поверхности биочипа приводит к изменению проводимости нанопроволок биочипа, которая находится в зависимости от количества ковалентно иммобилизованных на поверхности биочипа макромолекул маркеров заболевания. При этом рабочая поверхность биочипа на основе нанопроволочной структуры кремний на изоляторе модифицирована слоем органофункционального силана, за счет которого иммобилизованы зондовые макромолекулы на рабочую поверхность биочипа.
Недостатком данного технического решения является ковалентная иммобилизация зондовых молекул осуществляется за счет органофункционального силана. При этом формировуется толстый слой (5-20 нм) на поверхности нанопроволочных сенсоров, что приводит к снижению чувствительности, достоверности и воспроизводимости анализа. Другой стороной этого являются необходимость контроля толщины данного покрытия путем контроля условий проведения реакции. Важным критерием при фиксации биомолекулярных зондов на поверхность биочипа на основе нанопроволочной структуры кремний на изоляторе является минимизация расстояния между поверхностью нанопроволоки и выявляемой молекулой, поскольку максимальное влияние на проводимость оказывает ближайшее окружение нанопроволоки. При использовании органофункциональных силанов возрастает вероятность экранирования зарядов молекулы маркера [Sorgenfrei S. Et al. Nano Lett. (2011), Stern E. et al. Nano Lett. (2007)]. Поскольку сенсор направлен на выявление биологических маркеров, исключить наличие низкомолекулярных ионов не представляется возможным, в связи с этим необходимо максимально приблизить к поверхности иммобилизованную молекулу и строго контролировать расстояние между поверхностью биочипа и анализируемой молекулой, которое непосредственно влияет на величину изменения проводимость нанопровлок биочипа, и следовательно, эффективность и чувствительность анализа.
Известно техническое решение, представленное в способе изготовления биосенсорной структуры (Патент РФ №2644979 «Способ изготовления биосенсорной структуры», МПК H01L51/40, опубликовано 15.02.2018 г.). Способ изготовления биосенсорной структуры включает модификацию полупроводникового электрохимического преобразователя для создания эффективного отрицательного электростатического заряда, а также послойную адсорбцию слоя поликатионных молекул полимера и слоя полианионных молекул фермента из водного раствора. При этом используют пластину монокристаллического кремния с электронным типом проводимости, а его модификацию проводят путем кипячения полупроводниковой пластины в перекисно-аммиачном растворе, а в процессе адсорбции молекул фермента, либо предварительно непосредственно перед процессом адсорбции, на поверхность структуры «n-Si/SiO-2/полиэтиленимин» осуществляют освещение структуры со стороны раствора с интенсивностью, достаточной для изменения плотности заряда поверхности полупроводниковой структуры за время адсорбции.
Недостатками известного технического решения является использование поликатионных и полианионных слоев при фиксации биомолекул на поверхности сенсора, так как существенное влияние оказывает эффективный заряд поверхности нанопроволоки, и наличие большого количества зарядов на поверхности приводит к снижению отклика системы на формирование комплекса между иммобилизованным зондом и анализируемым маркером, что в результате приводит к снижению чувствительности и избирательности детекции.
Наиболее близким к предлагаемому изобретению является способ безметочного выявления коротких фрагментов РНК с помощью наноструктур кремний на изоляторе, представленный в статье (Dmitrienko E.V., Naumova O.V., Fomin В.I., Kupryushkin M.S., Volkova (Poryvaeva) A.V., Amirkhanov N.V., Semenov D.V., Pyshnaya I.A., Pyshnyi. Surface modification of SOI-FET sensors for label-free and specific detection of short RNA analyte // Nanomedicine (Lond). 2016 Aug;11(16):2073-2082. doi: 10.2217/nnm-2016-0071.) и выбранный в качестве прототипа. Способ включает модификацию нанопроволочного транзистора, присоединение олигонуклеотидных зондов, специфичных по отношению к коротким РНК-маркерам. Авторы демонстрируют преимущества использования короткого модифицирующего линкера на основе карбонилдиимидазола по сравнению со стандартным подходом, основанным на использовании модифицированного силана. Впервые показывают возможность использования незаряженных аналогов нуклеиновых кислот на основе фосфорилгуанидиновых производных в качестве специфичных зондов на поверхности КНИ-транзисторов. В предложенном техническом решении продемонстрировано выявление только коротких РНК аналитов. При этом не продемонстрирована возможность специфичного выявления правильных последовательностей РНК, в том числе с возможностью дискриминации однонуклеотидных несоответствий, что существенно ограничивает диагностический потенциал предложенного подхода. Кроме того, отсутствует одновременное измерение сигнала контрольных (референсных) и специфичных образцов. К недостатку предложенного технического решения относится измерение тока в качестве специфического сигнала, что накладывает дополнительные требования на установку и измеритель тока - высокое качество соединений и высокая чувствительность амперметра. В предложенном способе отсутствует автоматизация измерений, а также нет возможности задания всех параметров измерения. Перечисленные факторы приводят к снижению чувствительности и специфичности анализа, не позволяют проводить селективный анализ близких по строению соединений. Также все перечисленные технические решения не позволяют проводить параллельный анализ нескольких маркеров, что не позволяет рассматривать предложенные сенсоры в качестве мультиплексных диагностических платформ.
Перед авторами изобретения ставилась задача разработать способ и устройство для его реализации, позволяющее в автоматическом режиме проводить параллельную, безметочную, селективную и чувствительную детекцию одновременно нескольких биологических маркеров.
Поставленная задача решается тем, в способе автоматизации параллельной безметочной детекции биологического маркера включающий подготовку сенсорного элемента посредством очистки и последовательной функционализации покрытием толщиной менее 100 нм и биосенсорным покрытием, с возможностью селективного взаимодействия с исследуемым биологическим маркером; подача постоянного напряжения, проведение измерений отклика транзисторного узла на наличие исследуемого биологического маркера, выявление биологического маркера, дополнительно формируют систему с зоной, содержащей хотя бы один нанопроволочный транзистор с нанесенным функционализирующим покрытием и биосенсорным покрытием и одного референсного транзисторного узла без нанесенного биосенсорного покрытия для контроля с возможностью измерения одновременно нескольких транзисторных узлов, генерируют управляющие сигналы первому источнику питания постоянного напряжения, второму источнику питания постоянного напряжения и блоку измерения для переключения между выбранным числом транзисторных узлов и с возможностью переключения между ними последовательно, преобразовывают постоянный ток в напряжение посредством блока преобразования тока в напряжение и определяют напряжение, зависимое от отклика транзисторного узла на исследуемый биологический маркер, регистрируют разность напряжения между хотя бы одним транзисторный узлом с нанесенным биосенсорным покрытием и хотя бы одним референсным транзисторным узлом без нанесенного биосенсорного покрытия, регистрируют зависимость измеряемого напряжения транзисторного узла с нанесенным биосенсорным покрытием и без нанесенного биосенсорного покрытия от времени, определяют температурный режим транзисторного блока, передают в блок анализа, далее формируют сигнал для блока управления с возможностью проведения измерений исследуемого биологического маркера, при этом функционализирующее покрытие выполняют с нейтральным зарядом и толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов без использования модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере, один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм, либо функционализирующее покрытие выполняют толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов с использованием модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм, далее биосенсорное покрытие выполняют в виде нейтрально- заряженных аналогов нуклеиновых кислот, либо биосенсорное покрытие выполняют в виде биополимера белковой природы, либо биосенсорное покрытие выполняют в виде биополимера нуклеотидной природы, либо биосенсорное покрытие выполняют в виде низкомолекулярноего соединения белковой природы либо биосенсорное покрытие представляет собой низкомолекулярное соединение нуклеотидной природы, при этом нейтрально-заряженное биосенсорное покрытие выполняют в виде низкомолекулярного соединения синтетических аналогов нуклеотидной природы, далее первый источник питания постоянного напряжения постоянного тока выполняют с возможностью подачи напряжения в диапазоне 0-100 В, далее второй источник питания постоянного напряжения постоянного тока выполняют с возможностью подачи напряжения в диапазоне 0-10 В, при этом выявление биологического маркера осуществляют в воде, либо биологического маркера осуществляют в буферном растворе с концентрацией ионов от 0.1 до 100 мМ.
Способ реализуется с помощью устройства для автоматизации параллельной безметочной детекции биологического маркера которое содержит корпус; первый источник питания постоянного напряжения; второй источник питания постоянного напряжения; сенсорный элемент, который состоит из транзисторного блока, который включает в себя затвор и хотя бы один транзисторный узел, каждый из которых состоит из хотя бы одного нанопроволочного транзистора, с нанесенными функционализирующим покрытием толщиной не более 100 нм и биосенсорным покрытием с возможностью селективного взаимодействия с исследуемым биологическим маркером, нанесенным на хотя бы один транзисторный узел; блок измерения; блок управления; блок анализа; блок управления переключением транзисторными узлами и оно дополнительно оснащено блоком преобразования тока в напряжение, которое выполнено преобразующим постоянный ток в напряжение и определяющим напряжение, зависимое от отклика транзисторного узла на исследуемый биологический маркер, и регистрирующим разность напряжения между хотя бы одним транзисторный узлом с нанесенным биосенсорным покрытием и хотя бы одним транзисторным узлом без нанесенного биосенсорного покрытия и измерителем постоянного напряжения, который выполнен регистрирующим напряжение, выдаваемое транзисторным узлом с нанесенным биосенсорным покрытием и без нанесенного биосенсорного покрытия, в зависимости от напряжения на затворе транзисторного узла и с возможностью изменения напряжения на затворе транзисторного узла во временном периоде, датчиком температурного режима выполненного определяющим температурный режим транзисторного блока и формирующим сигнал посредством блока анализа для блока управления с возможностью проведения измерений исследуемого биологического маркера и расположенным вблизи сенсорного элемента, а блок управления выполнен формирующим систему с зоной, содержащей хотя бы один нанопроволочный транзистор с нанесенным функционализирующим покрытием и биосенсорным покрытием и одного референсного транзисторного узла без нанесенного биосенсорного покрытия для контроля исследуемого биологического маркера и генерирующим управляющие сигналы первому источнику питания постоянного напряжения, второму источнику питания постоянного напряжения и блоку измерения для переключения между выбранным числом транзисторных узлов, с возможностью переключения ме>кду ними последовательно для получения зависимости напряжения, измеряемого блоком преобразования тока в напряжение от транзисторного узла с нанесенным биосенсорным покрытием и без нанесенного биосенсорного покрытия, от напряжения первого источника питания постоянного напряжения, второго источника питания постоянного напряжения и времени посредством блока управления переключением транзисторными узлами, при этом функционализирующее покрытие выполнено с нейтральным зарядом и толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов без использования модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере, один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм, либо функционализация покрытием выполнено толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов с использованием модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента столщиной функционализирующего слоя не более 100 нм, далее биосенсорное покрытие выполнено в виде нейтрально- заряженных аналогов нуклеиновых кислот, либо биосенсорное покрытие выполнено в виде биополимера белковой природы, либо биосенсорное покрытие выполнено в виде биополимера нуклеотидной природы, либо биосенсорное покрытие выполнено в виде низкомолекулярного соединения белковой природы, либо биосенсорное покрытие выполнено в виде низкомолекулярного соединение нуклеотидной природы либо биосенсорное покрытие выполнено в виде низкомолекулярного соединения синтетического аналога нуклеотидной природы, при этом первый источник питания постоянного напряжения постоянного выполнен с возможностью подачи напряжения в диапазоне 0-100 В, далее второй источник питания постоянного напряжения выполнен с возможностью подачи напряжения в диапазоне 0-10 В.
Технический эффект заявляемого технического решения заключается в повышении достоверности, чувствительности и специфичности детекции биологических маркеров, повышении быстродействия, в обеспечении возможности стандартизации проведения измерений и удобства проведения анализа, а также в расширении ассортимента устройств данного назначения.
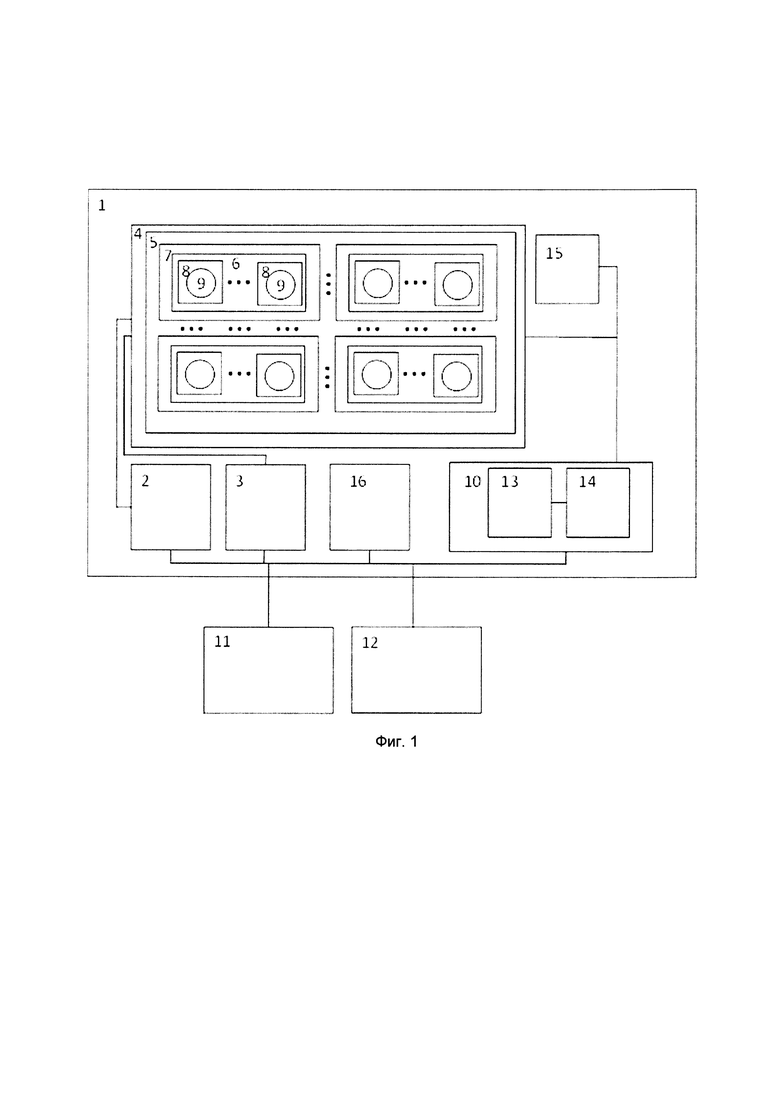
Заявляемый способ автоматизации параллельной, безметочной детекции биологического маркера реализуется с помощью устройства, которое поясняется блок-схемой, представленной на фиг. 1, где 1 -корпус, 2 - первый источник питания постоянного напряжения, 3- второй источник питания постоянного напряжения, 4 - сенсорный элемент, 5 - транзисторный блок, 6 - затвор, 7 - транзисторый узел, 8 - нанопроволочный транзистор, 9 - исследуемый биологический маркер, 10- блок измерения, 11 - блок управления, 12 - блок анализа, 13 - блок преобразования тока в напряжение, 14 - измеритель постоянного напряжения, 15 - датчик температурного режима, 16 - блок управления переключения между транзисторными узлами.
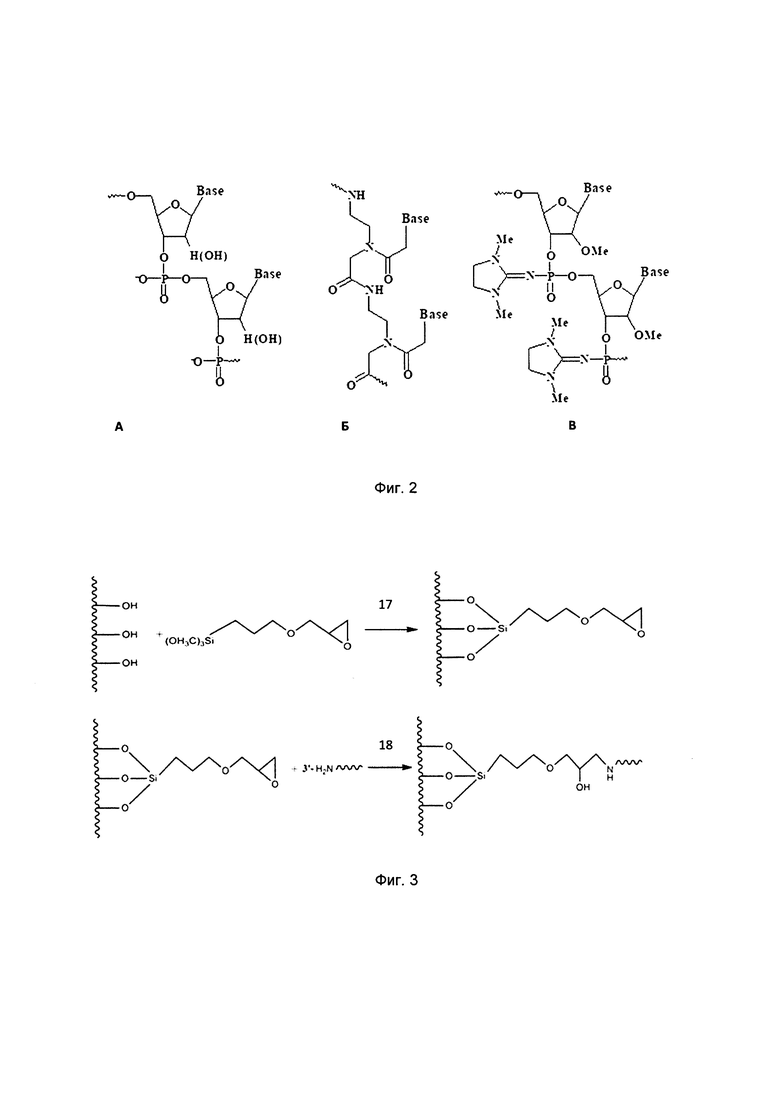
На фиг .2 представлено строение а) немодифицированных олигодезоксирибонуклеотидов, б) ФГ-олигонуклеотидов и в) ПНК-олигонуклеотидов.
На фиг 3 представлена схема нанесения функционализирующего покрытия на основе использования модифицированных силанов и биосенсорного покрытия, где 17 - нанесение модифицированного силана (5% раствор в спирте), 2 часа; 18 - нанесение биосенсорного покрытия, 6 часов.осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов с использованием модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм, далее биосенсорное покрытие выполнено в виде нейтрально-заряженных аналогов нуклеиновых кислот, либо биосенсорное покрытие выполнено в виде биополимера белковой природы, либо биосенсорное покрытие выполнено в виде биополимера нуклеотидной природы, либо биосенсорное покрытие выполнено в виде низкомолекулярного соединения белковой природы, либо биосенсорное покрытие выполнено в виде низкомолекулярного соединение нуклеотидной природы либо биосенсорное покрытие выполнено в виде низкомолекулярного соединения синтетического аналога нуклеотидной природы, при этом первый источник напряжения постоянного тока выполнен с возможностью подачи напряжения в диапазоне 0-100 В, далее второй источник напряжения постоянного напряжения выполнен с возможностью подачи напряжения в диапазоне 0-10 В.
Технический эффект заявляемого технического решения заключается в повышении достоверности, чувствительности и специфичности детекции биологических маркеров, повышении быстродействия, в обеспечении возможности стандартизации проведения измерений и удобства проведения анализа, а так же в расширении ассортимента устройств данного назначения.
Заявляемый способ автоматизации параллельной, безметочной детекции биологического маркера реализуется с помощью устройства, которое поясняется блок-схемой, представленной на фиг. 1, где 1 -корпус, 2 - первый источник питания постоянного напряжения, 3 - второй источник питания постоянного напряжения, 4 - сенсорный элемент, 5 - транзисторный блок, 6 - затвор, 7 - транзисторый узел, 8 - нанопроволочный транзистор, 9 - исследуемый биологический маркер, 10 - блок измерения, 11 - блок управления, 12 - блок анализа, 13 - блок преобразования тока в напряжение, 14 - измеритель постоянного напряжения, 15 - датчик температурного режима, 16 - блок управления переключения между транзисторными узлами.
На фиг. 2 представлено строение а) немодифицированных олигодезоксирибонуклеотидов, б) ФГ-олигонуклеотидов и в) ПНК-олигонуклеотидов.
На фиг 3 представлена схема нанесения функционализирующего покрытия на основе использования модифицированных силанов и биосенсорного покрытия, где 17 - нанесение модифицированного силана (5% раствор в спирте), 2 часа; 18 - нанесение биосенсорного покрытия, 6 часов.
На фиг 4 представлена схема нанесения функционализирующего покрытия на основе использования бифункциональных реагентов и биосенсорного покрытия, где 19 - концентрация бифункционального реагента 10 мг/мл, растворитель ацетонитрилл, температура комнатная в течение 20 часов; 20 - буферный раствор рН 8,3, температура комнатная в течение 6 часов.
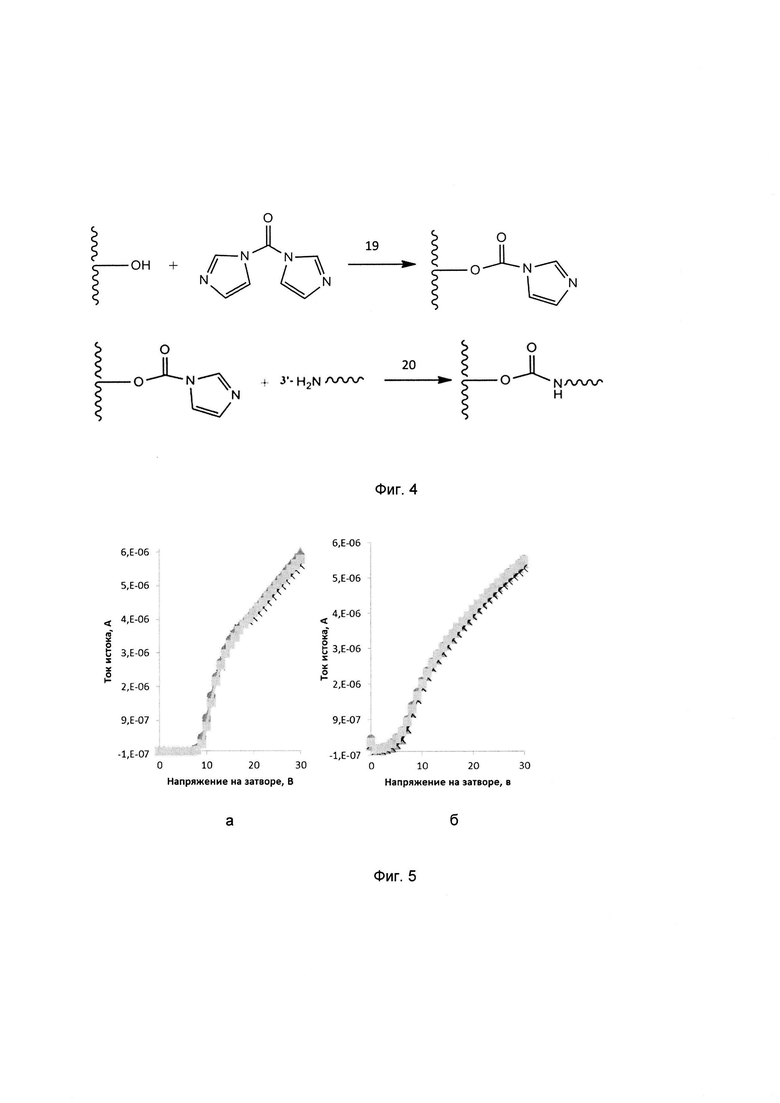
На фиг. 5 представлен стандартный вид сток-затворных характеристик транзисторов (3 мкм) с иммобилизованными ФГ-зондами до (а) и после (б) гибридизации с короткой ДНК-мишенью в концентрации 10"15 М.
На фиг. 6. представлен стандартный вид сток-затворных характеристик транзисторов (3 мкм) с иммобилизованными ФГ-зондами до (а) и после (б) гибридизации с протяженной РНК-мишенью в концентрации 10~15 М. (в) - отклик транзисторов при образовании гибридизационного комплекса с протяженной РНК- мишенью при напряжении на затворе 15 В.
На фиг. 7. представлено схематичное изображение сенсорной поверхности с зонами функционализированными полностью (выделено овалом) и частично (выделено прямоугольником) специфичными мишени ФГ-олигонуклеотидами (а) структура полностью комплементарного (I), (б) содержащего два мисматча (II) дуплекса зонд/мишень.
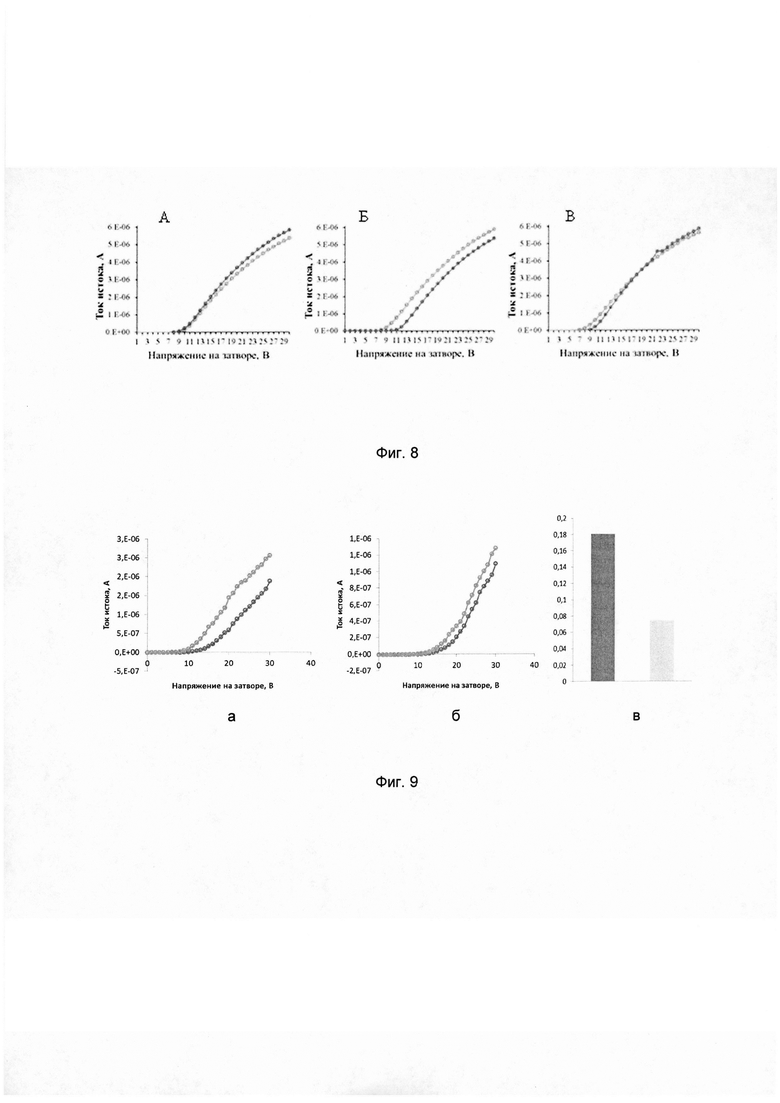
На фиг.8 представлена детекция однонуклеотидного несоответствия в составе маркера с использованием ФГ-олигонуклеотида как биосенсорного покрытия. Приведены сток-затворные характеристики КНИ-биосенсора (3 мкм), функционализированного с использованием ФГ-олигонуклеотидов до (светлая кривая) и после (темная кривая) гибридизации с РНК-мишенью в зависимости от зоны, (а) - контрольная зона, не содержащая ФГ-зонда, (б) - полностью комплементарный ФГ-зонд, (в) - зонд, содержащий два мисматча.
На фиг. 9 представлены сток-затворные характеристики КНИ-биосенсора (3 мкм), функционализированного с использованием биотина до (светлая кривая) и после (тесная кривая) связывания с белком: авидином - специфическое связываение, (а) и неспецифическим контрольным белком БСА (б). В - отклик микропроволочного транзистора (3 мкм) с иммобилизованным функциональным слоем (биотином) после связывания со специфическим белком авидином (темный столбец) и неспецифическим контрольным белком БСА (светлый столбец) в концентрации 10"12 М.
Заявляемый способ автоматизации параллельной безметочной детекции биологического маркера основанный на использовании устройства для его реализации работает следующим образом. В корпусе 1 располагается сенсорный элемент 4 состоящий из транзисторного блока 5, который включает в себя затвор 6 и хотя бы один транзисторный узел 7, каждый из которых состоит из хотя бы одного нанопроволочного транзистора 8. На нанопроволочный транзистор 8 нанесено функционализирующее покрытие толщиной не более 100 нм и биосенсорное покрытие с возможностью селективного взаимодействия с исследуемым биологическим маркером 9. Одним из наиболее важных этапов изготовления физико- биологического сенсора, который получается за счет последовательного нанесения функционализирующего покрытия толщиной и биосенсорного покрытия, является функционализация поверхности кремния и последующая ковалентная или нековалентная иммобилизация на ней специфических биомолекулярных зондов (формирование сенсибилизирующего слоя). При этом следует учитывать особенности твердотельного носителя, представленного в виде нанопроволочного транзистора, а также метода выявления биомаркеров. Так, при разработке физико- биологического сенсора на основе электрофизической детекции и КНИ-структур большое значение имеет эффективный заряд поверхности нанопроволоки, поскольку наличие большого количества зарядов на поверхности может приводить к снижению отклика системы на формирование комплекса между иммобилизованным зондом и анализируемым маркером; расстояние между поверхностью проволоки и выявляемой молекулой, поскольку максимальное влияние на проводимость оказывает ближайшее окружение нанопроволоки в пределах длины экранирования Дебая; ионная сила раствора аналита, которая может экранировать заряды молекул- маркеров, связывающихся с функционализированной поверхностью биосенсора.
Функционализирующее покрытие с нейтральным зарядом и толщиной не более 100 нм формируется последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов с или без использования модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере 1 (один) остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм. А биосенсорное покрытие может быть выполнено в виде нейтрально-заряженных аналогов нуклеиновых кислот, представлять собой биополимер белковой природы либо нуклеотидной природы, либо низкомолекулярное соединение белковой природы либо низкомолекулярное соединение нуклеотидной природы либо низкомолекулярное соединение синтетических аналогов нуклеотидной природы. На подготовленный нанопроволочный транзистор 8 наносят исследуемый биологический маркер 9 и подается напряжение от первого источника питания постоянного напряжения 2 и второго источника постоянного напряжения 3. Блока управления 11 позволяет изменять напряжение первого источника питания постоянного напряжения 2 в диапазоне 0-10 В и второго источника постоянного напряжения 3 в диапазоне 0-100 В.
Устройство дополнительно оснащено блоком преобразования тока в напряжение 13, преобразующим постоянный ток в напряжение, зависимое от отклика транзисторного узла 7 на исследуемый биологический маркер 9, и регистрирующим разность напряжения между хотя бы одним транзисторный узлом 7 с нанесенным биосенсорным покрытием и хотя бы одним транзисторным узлом 7 без нанесенного биосенсорного покрытия и измерителем постоянного напряжения 14, регистрирующим напряжение, выдаваемое транзисторным узлом 7, в зависимости от напряжения на затворе 6 транзисторного узла 7 и с возможностью изменения напряжения на затворе 6 транзисторного узла 7 во временном периоде. Блок преобразования тока в напряжение 13 позволяет повысить точность и достоверность измерения сигнала выдаваемого транзисторным узлом 7, за счет высоких значений напряжения измеряемых обычным измерителем постоянного напряжения, что приводит к отсутствию необходимости использования высокоточных измерителей тока через транзисторный узел 7 использованных в прототипах.
Так же заявляемое устройство оснащено датчиком температурного режима 15 который определяет температурный режим транзисторного блока 5 и формирует сигнал посредством блока анализа 12 для блока управления 11 с возможностью проведения измерений исследуемого биологического маркера. Изменения температурного режима позволяет повысить селективность работы устройства за счет разрушения неспецифических взаимодействий при повышении температуры, при сохранности специфических. Датчик температурного режима 15 располагают вблизи сенсорного элемента 4.
Для осуществления автоматизации параллельной детекции исследуемого биологического маркера 9 блок управления 11 формирует систему с зоной, содержащей хотя бы один нанопроволочный транзистор 8 с нанесенным функционализирующим покрытием и биосенсорным покрытием и одного референсного транзисторного узла без нанесенного биосенсорного покрытия для контроля и генерирующим управляющие сигналы первому источнику питания постоянного напряжения 2, второму источнику питания постоянного напряжения 3 и блоку измерения 10 для переключения между выбранным числом транзисторных узлов 7, с помощью блока управления переключением транзисторными узлами 16, с возможностью переключения между ними последовательно для получения зависимости напряжения, измеряемого блоком преобразования тока в напряжение 13, получаемого от транзисторного узла 7, в зависимости от напряжения первого источника питания постоянного напряжения 2, второго источника питания постоянного напряжения 3 и времени. За счет этого переключения достигается возможность измерения напряжения от различных транзисторных узлов со скоростью, при которой сигнал от специфического взаимодействия между биосенсорным покрытием и исследуемым биологическим маркером не претерпевает значительных изменений. При этом изменение напряжения на затворе 6 транзисторного узла 7 происходит от самого факта взаимодействия между биосенсорным покрытием и исследуемым биологическим маркером и не требует введения дополнительной системы детекции данного взаимодействия.
Таким образом, разработана универсальная платформа для детекции широкого спектра биологически-активных соединений, в том числе нуклеиновых кислот, пептидов/белков, низкомолекулярных соединений.
Достичь заявленного технического эффекта позволяет совокупность факторов.
• Измерение напряжения в качестве сигнала биосенсора, позволяет снизить требования к аппаратной базе биосенсора и приводит к повышению достоверности анализа.
• Одновременное измерения сигнала от контрольных (референсных) и специфичных транзисторов приводит к повышению достоверности анализа.
• Автоматизация переключения измерений между транзисторными узлами позволяет проводить одновременное измерение со всех узлов, что приводит к увеличению скорости анализа и достоверности результатов
• Реализована возможность одновременного нанесения различных специфических зондовых молекул, что позволяет проводить многопараметрические исследования, в том числе молекул различной природы (нуклеиновые кислоты, белки).
• Уникальный подход конструирования специфических зондов на основе незаряженных производных нуклеиновых кислот, с учетом термодинамических параметров связывания их с аналитом, приводит к снижению фонового заряда вокруг транзистора и к повышению чувствительности и специфичности разработанного биосенсорного устройства. Существенным преимуществом разработанного сенсора с предложенной структурой специфических зондов является возможность проведения процедуры анализа нуклеиновых кислот в бессолевых условиях, что приводит к существенному повышению отношения сигнал/шум и, следовательно, повышает чувствительность анализа.
Предложенный способ позволяет получить экспоненциальную зависимость проводимости кремниевой нанопроволоки от электрического заряда на ее поверхности, таким образом, повысить соотношение сигнал/шум и получить чувствительность детекции биомолекулярных маркеров до 10"14 - 10"15 М.
Изобретение подробнее проиллюстрировано ниже следующими примерами конкретного выполнения, которые не ограничивают объем изобретения. Многочисленные варианты осуществления изобретения в объеме формулы изобретения, которые вытекают из примеров, должны быть очевидны специалистам в данной области техники на основе вышеприведенного описания и последующих примеров.
Пример 1.
Для демонстрации применения ФГ олигонуклеотидов как специфичных зондов при выявлении коротких (до 40 нуклеотидов) последовательностей нуклеиновых кислот (фиг. 2. структура и сравнение ФГ с ДНК и ПНК), поверхность КНИ-транзисторов функционализировали в двух вариантах функционализирующего покрытия, с использованием модифицированных силанов (фиг. 3) или бифункциональных реагентов (фиг. 4). Иммобилизацию ФГ-олигонуклеотидных зондов проводили в диапазоне концентраций 10-6 Μ - 10-9 Μ. Выявление короткого ДНК-аналита (до 40 нуклеотидов) проводили в диапазоне концентраций 10-6 Μ - 10-15 Μ в воде или низкосолевом 10 мМ фосфатном буферном растворе. Приведены стандартные кривые сток-затворных характеристик транзисторов до и после гибридизации с коротким ДНК-аналитом (фиг. 5). Продемонстрирована чувствительность на уровне 10-15 М.
Пример 2.
Для демонстрации применения ФГ олигонуклеотидов как специфичных зондов при выявлении протяженных (более 500 нуклеотидов) последовательностей нуклеиновых кислот, поверхность КНИ-транзисторов функционализировали в двух вариантах функционализирующего покрытия, с использованием модифицированных силанов (фиг. 3) или бифункциональных реагентов (фиг. 4). Иммобилизацию ФГ-олигонуклеотидных зондов проводили в диапазоне концентраций 10-6 Μ - 10-9 Μ. Выявление протяженного РНК-аналита (более 500 нуклеотидов) проводили в диапазоне концентраций 10-9 Μ - 10-19 Μ в воде или низкосолевом 10 мМ фосфатном буферном растворе. Приведены стандартные кривые сток-затворных характеристик транзисторов до и после гибридизации с коротким ДНК-аналитом и отклик транзисторов при напряжении 15 В (фиг. 6). Продемонстрирована чувствительность на уровне 10-19 М.
Пример 3.
Для демонстрации применения ФГ-олигонуклеотидов как специфичных зондов при специфичном выявлении однонуклеотидных несоответствий в последовательностях нуклеиновых кислот (рисунок 7, рисунок 8) с помощью транзисторного биосенсора, поверхность КНИ-транзисторов функционализировали в двух вариантах функционализирующего покрытия, с использованием модифицированных силанов (фиг. 3) или бифункциональных реагентов (фиг. 4). Иммобилизацию ФГ-олигонуклеотидных зондов проводили в диапазоне концентраций 10-6 Μ - 10-9 Μ. Использовали как полностью комплементарный ФГ-зонд (I), так и содержащий два нуклеотидных несоответствия (схема нанесения зондов на КНИ-транзисторы представлена на фиг. 7). Выявление специфического ДНК-аналита проводили в диапазоне концентраций 10-6 Μ - 10-15 Μ в воде или низкосолевом 10 мМ фосфатном буферном растворе. Приведены стандартные сток-затворные характеристики КНИ-биосенсора (3 мкм), функционализированного с использованием ФГ-олигонуклеотидов до (синяя кривая) и после (красная кривая) гибридизации с РНК-мишенью в зависимости от зоны. А - контрольная зона, не содержащая ФГ-зонда, Б - полностью комплементарный ФГ-зонд, В - зонд, содержащий два мисматча (фиг. 8). Продемонстрирована возможность высокоспецифического выявления нуклеиновых кислот.
Пример 4.
Для демонстрации применения разработанного КНИ-биосенсора для специфичного выявления белкового аналита в качестве биосенсорного покрытия использовали низкомолекулярный специфический к ряду белков лиганд биотин. Показано в двух вариантах функционализирующего покрытия, с использованием модифицированных силанов или бифункциональных реагентов. Взаимодействие с белковыми молекулами проводили в 10 мМ фосфатном буфере в диапазоне концентраций 10-6 Μ - 10-12 М. В качестве специфического белкового аналита использован белок авидин, в качестве контрольного неспецифического белка использовали близкий по массе и размеру белок бычий сывороточный альбумин (БСА). Приведены стандартные кривые сток-затворных характеристик транзисторов до и после связывания со специфическим белком авидином (специфическое связываение, А) и неспецифическим контрольным белком БСА (Б). В - отклик микропроволочного транзистора (3 мкм) с иммобилизованным функциональным слоем (биотином) после связывания со специфическим белком авидином (красный столбец) и неспецифическим контрольным белком БСА (синий столбец) (фиг. 9).
Показано, что максимальная чувствительность и отклик системы продемонстрирован для протяженных полианионных молекул нуклеиновых кислот, что соответствует структуре КНИ-биосенсору, чувствительной к изменению заряда в ближайшем окружении транзистора. Однако успешное выявление продемонстрировано для различных типов рассмотренных, включая короткие ДНК-аналиты и белковые молекулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ ранней диагностики онкологического заболевания | 2022 |
|
RU2790290C1 |
| Способ ранней диагностики глиомы | 2021 |
|
RU2772193C1 |
| Биосенсор для индикации биопатогенов | 2021 |
|
RU2774307C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ И РАКА ЯИЧНИКОВ | 2017 |
|
RU2696114C2 |
| ИНТЕГРАЛЬНАЯ СХЕМА С МАТРИЦЕЙ СЕНСОРНЫХ ТРАНЗИСТОРОВ, СЕНСОРНОЕ УСТРОЙСТВО И СПОСОБ ИЗМЕРЕНИЯ | 2013 |
|
RU2650087C2 |
| СПОСОБ КОНСЕРВАЦИИ ТВЕРДОТЕЛЬНОЙ ПОВЕРХНОСТИ И КОНСЕРВИРУЮЩЕЕ ТВЕРДОТЕЛЬНУЮ ПОВЕРХНОСТЬ ПОКРЫТИЕ | 2015 |
|
RU2601745C1 |
| СПОСОБ БЕЗМЕТОЧНОГО ОДНОМОЛЕКУЛЯРНОГО СЕКВЕНИРОВАНИЯ ДНК И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ НА ОСНОВЕ ЗАРЯДОЧУВСТВИТЕЛЬНОГО СЕНСОРА | 2021 |
|
RU2780050C1 |
| СПОСОБ СОЗДАНИЯ РЕГЕНЕРИРУЕМОГО БИОСЕНСОРА НА ОСНОВЕ КОМПЛЕКСА ФОТОННОГО КРИСТАЛЛА С АФФИННЫМИ МОЛЕКУЛАМИ | 2015 |
|
RU2618606C1 |
| ОБНАРУЖЕНИЕ МОЛЕКУЛЯРНЫХ КОЛОНИЙ ПОСРЕДСТВОМ ГИБРИДИЗАЦИИ НА МЕМБРАНАХ С ФЛУОРЕСЦЕНТНЫМИ ЗОНДАМИ | 2006 |
|
RU2338787C2 |
| УСТРОЙСТВО ДЛЯ ОБНАРУЖЕНИЯ И РАСПОЗНАВАНИЯ АНАЛИТОВ В МНОГОКОМПОНЕНТНОЙ СРЕДЕ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2019 |
|
RU2713099C1 |

Группа изобретений относится к области биотехнологии. Предложены устройство и способ автоматизации параллельной безметочной детекции биологического маркера. Устройство содержит первый и второй источники питания постоянного напряжения, сенсорный элемент, блок измерения, блок управления, блок анализа, блок управления переключением транзисторными узлами, блок преобразования тока в напряжение, измеритель постоянного напряжения, датчик температурного режима. Сенсорный элемент состоит из транзисторного блока, где транзисторный блок включает затвор и транзисторный узел с нанопроволочным транзистором с нанесенным функционализирующим и биосенсорным покрытиями. Способ включает формирование зоны с нанесенными покрытиями нанопроволочным транзистором и референсным транзисторным узлом без биосенсорного покрытия, генерирование управляющих сигналов, преобразование постоянного тока в напряжение, регистрирование разности напряжения между транзисторный узлом и референсным транзисторным узлом, регистрирование зависимости измеряемого напряжения от времени, определение температурного режима транзисторного блока, формирование сигнала для блока управления с возможностью проведения измерений исследуемого биологического маркера. Изобретения обеспечивают повышение достоверности, чувствительности и специфичности детекции, повышение быстродействия. 2 н. и 22 з.п. ф-лы., 4 пр., 9 ил.
1. Устройство для автоматизации параллельной безметочной детекции биологического маркера, содержащее корпус; первый источник питания постоянного напряжения; второй источник питания постоянного напряжения; сенсорный элемент, который состоит из транзисторного блока, который включает в себя затвор и хотя бы один транзисторный узел, каждый из которых состоит из хотя бы одного нанопроволочного транзистора, с нанесенными функционализирующим покрытием толщиной не более 100 нм и биосенсорным покрытием с возможностью селективного взаимодействия с исследуемым биологическим маркером, нанесенным на хотя бы один транзисторный узел; блок измерения; блок управления; блок анализа; блок управления переключением транзисторными узлами, отличающееся тем, что оно дополнительно оснащено блоком преобразования тока в напряжение, который выполнен преобразующим постоянный ток в напряжение, определяющим напряжение, зависимое от отклика транзисторного узла на исследуемый биологический маркер, и регистрирующим разность напряжения между хотя бы одним транзисторный узлом с нанесенным биосенсорным покрытием и хотя бы одним транзисторным узлом без нанесенного биосенсорного покрытия; измерителем постоянного напряжения, который выполнен регистрирующим напряжение, выдаваемое транзисторным узлом с нанесенным биосенсорным покрытием и без нанесенного биосенсорного покрытия, в зависимости от напряжения на затворе транзисторного узла и с возможностью изменения напряжения на затворе транзисторного узла во временном периоде; датчиком температурного режима выполненного определяющим температурный режим транзисторного блока и формирующим сигнал посредством блока анализа для блока управления с возможностью проведения измерений исследуемого биологического маркера и расположенным вблизи сенсорного элемента, а блок управления выполнен формирующим систему с зоной, содержащей хотя бы один нанопроволочный транзистор с нанесенным функционализирующим покрытием и биосенсорным покрытием и одного референсного транзисторного узла без нанесенного биосенсорного покрытия для контроля исследуемого биологического маркера и генерирующим управляющие сигналы первому источнику питания постоянного напряжения, второму источнику питания постоянного напряжения и блоку измерения для переключения между выбранным числом транзисторных узлов, с возможностью переключения между ними последовательно для получения зависимости напряжения, измеряемого блоком преобразования тока в напряжение от транзисторного узла с нанесенным биосенсорным покрытием и без нанесенного биосенсорного покрытия, от напряжения первого источника питания постоянного напряжения, второго источника питания постоянного напряжения и времени посредством блока управления переключением транзисторными узлами.
2. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что функционализирующее покрытие выполнено с нейтральным зарядом и толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов без использования модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм.
3. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что функционализация покрытием выполнено толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов с использованием модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм.
4. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что биосенсорное покрытие выполнено в виде нейтрально-заряженных аналогов нуклеиновых кислот.
5. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что биосенсорное покрытие выполнено в виде биополимера белковой природы.
6. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что биосенсорное покрытие выполнено в виде биополимера нуклеотидной природы.
7. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что биосенсорное покрытие выполнено в виде низкомолекулярного соединения белковой природы.
8. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что биосенсорное покрытие выполнено в виде низкомолекулярного соединение нуклеотидной природы.
9. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что что биосенсорное покрытие выполнено в виде низкомолекулярного соединения синтетического аналога нуклеотидной природы.
10. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что первый источник питания постоянного напряжения выполнен с возможностью подачи напряжения в диапазоне 0-100 В.
11. Устройство для автоматизации параллельной безметочной детекции биологического маркера по п.1, отличающееся тем, что второй источник питания постоянного напряжения выполнен с возможностью подачи напряжения в диапазоне 0-10 В.
12. Способ автоматизации параллельной безметочной детекции биологического маркера с использованием устройства по любому из пп.1-11, включающий подготовку сенсорного элемента посредством очистки и последовательной функционализации покрытием толщиной менее 100 нм и биосенсорным покрытием, с возможностью селективного взаимодействия с исследуемым биологическим маркером; подача постоянного напряжения, проведение измерений отклика транзисторного узла на наличие исследуемого биологического маркера, выявление биологического маркера, отличающийся тем, что дополнительно формируют систему с зоной, содержащей хотя бы один нанопроволочный транзистор с нанесенным функционализирующим покрытием и биосенсорным покрытием и одного референсного транзисторного узла без нанесенного биосенсорного покрытия для контроля с возможностью измерения одновременно нескольких транзисторных узлов, генерируют управляющие сигналы первому источнику питания постоянного напряжения, второму источнику питания постоянного напряжения и блоку измерения для переключения между выбранным числом транзисторных узлов и с возможностью переключения между ними последовательно, преобразовывают постоянный ток в напряжение посредством блока преобразования тока в напряжение и определяют напряжение, зависимое от отклика транзисторного узла на исследуемый биологический маркер, регистрируют разность напряжения между хотя бы одним транзисторный узлом с нанесенным биосенсорным покрытием и хотя бы одним референсным транзисторным узлом без нанесенного биосенсорного покрытия, регистрируют зависимость измеряемого напряжения транзисторного узла с нанесенным биосенсорным покрытием и без нанесенного биосенсорного покрытия от времени, определяют температурный режим транзисторного блока, передают в блок анализа, далее формируют сигнал для блока управления с возможностью проведения измерений исследуемого биологического маркера.
13. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что функционализирующее покрытие выполняют с нейтральным зарядом и толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов без использования модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм.
14. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что функционализирующее покрытие выполняют толщиной не более 100 нм последовательно стадией предварительной подготовки поверхности к функционализации, стадией нанесения функционализирующего покрытия, при этом стадию предварительной подготовки поверхности к функционализации осуществляют неповреждающей очисткой поверхности сенсорного элемента, приводящей к формированию на поверхности полярных групп, а нанесение функционализирующего покрытия на поверхность осуществляют с использованием бифункциональных реагентов с использованием модифицированных силанов в органическом растворителе, обеспечивая контакт функционализирующего реагента с поверхностью и формируя покрытие, содержащее, по крайней мере один остаток функционализирующего реагента, получаемый в результате реакции с полярными группами на поверхности сенсорного элемента с толщиной функционализирующего слоя не более 100 нм.
15. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что биосенсорное покрытие выполняют в виде нейтрально-заряженных аналогов нуклеиновых кислот.
16. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что биосенсорное покрытие выполняют в виде биополимера белковой природы.
17. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что биосенсорное покрытие выполняют в виде биополимера нуклеотидной природы.
18. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что биосенсорное покрытие выполняют в виде низкомолекулярноего соединения белковой природы.
19. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что биосенсорное покрытие представляет собой низкомолекулярное соединение нуклеотидной природы.
20. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что нейтрально-заряженное биосенсорное покрытие выполняют в виде низкомолекулярного соединения синтетических аналогов нуклеотидной природы.
21. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что первый источник питания постоянного напряжения выполняют с возможностью подачи напряжения в диапазоне 0-100 В.
22. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что второй источник питания постоянного напряжения выполняют с возможностью подачи напряжения в диапазоне 0-10 В.
23. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что выявление биологического маркера осуществляют в воде.
24. Способ автоматизации параллельной безметочной детекции биологического маркера по п.12, отличающийся тем, что выявление биологического маркера осуществляют в буферном растворе с концентрацией ионов от 0.1 до 100 мМ.
| Dmitrienko E.V | |||
| et al, Surface modification of SOI-FET sensors for label-free and specific detection of short RNA analyte // Nanomedicine (Lond) | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| 0 |
|
SU178180A1 | |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ПАССИВНОЙ РЕТРАНСЛЯЦИИ | 0 |
|
SU184943A1 |
| СПОСОБ ДИАГНОСТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ И РАКА ЯИЧНИКОВ | 2017 |
|
RU2696114C2 |
| Токарный резец | 1924 |
|
SU2016A1 |
Авторы
Даты
2021-12-20—Публикация
2020-08-20—Подача