Настоящее изобретение относится к композиции, которая содержит смесь, которая включает или, альтернативно, состоит из экстракта (а) плода по меньшей мере одного растения рода Vaccinium и по меньшей мере одного ингредиента (b), приемлемого для фармацевтического или пищевого применения, и к её использованию для профилактики и/или лечения дивертикулеза или патологии, возникающей из-за дивертикулеза или связанной с ним.
Кишечник представляет собой орган-мишень многочисленных воспалительных патологий, которые могут быть причиной серьезных расстройств и часто трудно поддаются лечению.
Среди них первостепенную роль играют:
- воспалительное заболевание кишечника (ВЗК);
- резервуарный илеит;
- дивертикулярная болезнь и дивертикулит.
Воспалительные заболевания кишечника (ВЗК) характеризуются наличием хронического воспаления слизистой оболочки кишечника, которое имеет прерывистое течение и может вызывать тяжелые осложнения. Они включают болезнь Крона (БК), язвенный ректоколит (ЯРК) и так называемый «недифференцированный колит» (НК).
Симптомы различаются для двух наиболее важных патологий группы, а именно, болезни Крона (БК) и язвенного ректоколита (ЯРК).
В случае БК наиболее частыми начальными симптомами являются диарея и боль в животе, локализованная прежде всего в правой подвздошной ямке (соответствует последней петле подвздошной кишки, наиболее частому участку заболевания).
ЯРК, с другой стороны, почти всегда проявляется кровавой диареей (содержащей ярко-красную кровь и слизь, смешанная со стулом), связанной с «тенезмом» (ощущением неполной эвакуации) и иногда анемией.
Оба заболевания могут иметь периоды латентности, чередующиеся с обострением воспаления. Когда кишечное воспаление снова становится острым, появляются конституциональные симптомы, такие как лихорадка, потеря массы тела, астения и потеря аппетита. Со временем БК может осложниться образованием стеноза (сужением просвета пораженного участка кишечника, что в конечном итоге может привести к непроходимости кишечника), свищей (связи между кишечником и кожей или между органами брюшной полости) или абсцессов.
Так называемый «недифференцированный колит» - НК, напротив, является относительно недавно описанным заболеванием, при котором воспаление ограничено толстой кишкой с такими гистологическими, клиническими, рентгенологическими и эндоскопическими характеристиками, которые исключают классификацию, поскольку они могут быть не приписывается ни к БК, ни к ЯРК; в 13-20% случаев они представляют собой начальные формы одного из двух заболеваний.
Так называемый «недифференцированный колит» - НК обычно характеризуется наличием сегментарных поражений, обширным изъязвлением, возможным поражением восходящей ободочной кишки - даже при том, что дистальная ободочная кишка (нисходящая ободочная кишка) более серьезно нарушена - и наличием воспаления, распространяющегося на более чем 50% поверхности слизистой, с возможным расширением толстой кишки, связанной с токсическим мегаколоном.
В подавляющем большинстве случаев (95%) симптомы первоначально характеризуются диарейными движениями кишечника в начале; в 72% случаев наблюдается кровавая диарея, в 74% - боли в животе. У меньшего процента пациентов наблюдается потеря массы тела (44%) и лихорадка (26%).
Резервуарный илеит представляет собой неспецифическое воспаление илеального резервуара или кармана, и является наиболее частым долговременным осложнением хирургического вмешательства, известного как подвздошно-резервуарно-анальная реконструкция.
Этиология до сих пор неизвестна и, скорее всего, является многофакторной. Были предложены различные патогенетические гипотезы, включая застой каловых масс и бактериальное разрастание, рецидив ЯРК и ишемию слизистой оболочки кармана.
Резервуарный илеит клинически характеризуется различными симптомами, которые включают увеличение числа эвакуаций и текучести фекалий, ректальное кровотечение, спастические боли в животе, императивные позывы и тенезмы, а иногда недержание мочи и лихорадку.
Дивертикулез толстой кишки является наиболее частым анатомическим изменением толстой кишки, часто выявляемым при колоноскопии. Он относится к наличию структурных модификаций стенки толстой кишки и, по-видимому, характеризуется наличием карманов, называемых «дивертикулами»; он отличается от воспалительного заболевания кишечника (ВЗК) и резервуарного илеита.
Дивертикулы представляют собой небольшие выступающие карманы, которые могут образовываться в слизистой оболочке толстой кишки в точках относительной слабости мышечного слоя стенки.
Состояние, при котором обнаруживаются дивертикулы, даже если нет симптомов, связанных с их наличием, называется «дивертикулез». С практической точки зрения, дивертикулез является медицинским состоянием, характеризующимся наличием выпячиваний слизистой и подслизистой оболочки, определяемых как дивертикулы, конкретно - вдоль стенки полых органов пищеварительной системы. Они обычно образуются в областях относительной слабости мышечного слоя («Locus minoris resistentiae») толстой кишки (прежде всего сигмовидной кишки и прямой кишки из-за более высоких давлений). Дивертикулез проявляется без симптомов; если он становится симптоматическим, таким как, например, в случае дивертикулита, говорят о дивертикулярной патологии или заболевании.
Дивертикулез наиболее распространен в странах Запада, с распространенностью 5% среди населения в возрасте от 30 до 39 лет и 60% среди населения старше 80 лет.
Дивертикулы чаще встречаются в нижней части задней кишки (или толстой кишки), называемой сигмовидной кишкой.
Считается, что развитие дивертикулов толстой кишки является результатом повышения внутрипросветного давления в толстой кишке. Чтобы было ясно, развитие дивертикула является феноменом, который полностью отличается от воспалительных и/или аутоиммунных явлений, таких как хроническое воспалительное заболевание кишечника (ВЗК), например, болезнь Крона и язвенный колит, и, основываясь на наших современных знаниях, такие патологии не имеют связи с дивертикулезом и расстройствами, связанными с ним.
Наличие дивертикула является постоянным анатомическим изменением структуры стенок толстой кишки, которое может оставаться бессимптомным или приводить к развитию симптомов. По оценкам, примерно у 20% пациентов развиваются симптомы, при наличии которых состояние определяется как «дивертикулярная болезнь» (ДБ).
Неосложненная дивертикулярная болезнь обычно не связана с конкретными симптомами. Дивертикулярная болезнь является частой причиной значительного кровотечения из толстой кишки.
Подтипом ДБ является СНДБ (симптоматическая неосложненная дивертикулярная болезнь), при которой постоянные абдоминальные симптомы, связанные с дивертикулами, отмечаются при отсутствии макроскопических проявлений колита или дивертикулита.
Другие симптомы обычно связаны с осложнениями дивертикулярной болезни, такими как «дивертикулит», который представляет собой макроскопическое острое воспаление дивертикула. Дивертикулит может быть простым или осложненным, в зависимости от того, наблюдаются ли на компьютерной томографии (КТ) такие признаки осложнений, как абсцессы, перитонит, обструкция, свищи или кровотечение.
Дивертикулит может вызвать боль в животе, дрожь, лихорадку и изменение функционирования кишечника. Наиболее интенсивные симптомы связаны с серьезными осложнениями, такими как перфорация (свободный разрыв в животе), абсцессы (накопление гноя) или образование свищей (аномального прохода, который создается между толстой кишкой и другим органом или кожей после перфорации дивертикула).
Основные патологические механизмы, которые вызывают образование дивертикулов ободочной кишки (дивертикулез), до сих пор остаются неясными. Не желая углубляться в теорию, такие образования, вероятно, являются результатом сложных взаимодействий между диетой, кишечной микробиотой, генетическими факторами, подвижностью толстой кишки и микроскопическим воспалением.
Хотя это не было доказано, в настоящее время преобладает теория, что диета с низким потреблением пищевых волокон является одной из причин дивертикулярной болезни. Заболевание было отмечено в первые годы XX века в Соединенных Штатах, в то время, когда определенные продукты были введены в американскую диету, значительно сокращая потребление пищевых волокон американским населением.
Дивертикулярная болезнь распространена в промышленно развитых странах и, в частности, в Соединенных Штатах, Англии и Австралии, где преобладают диеты с низким потреблением пищевых волокон. В отличие от этого, это редкое заболевание в Азии и Африке, где большинство людей потребляют большое количество пищевых волокон.
Пищевые волокна содержатся во фруктах, овощах и неочищенных (цельных) зернах, которые организм не в состоянии полностью переваривать. Некоторые волокна, называемые растворимыми волокнами, легко растворяются в воде, создавая мягкий желеобразный материал в кишечнике, тогда как нерастворимые волокна проходят через кишечник практически без изменений. Оба типа пищевых волокон помогают предотвратить запор благодаря мягкому стулу, который легко выводится.
Запор проявляется в необходимости значительных усилий для дефекации; усилие может вызвать увеличение давления в толстой кишке, и это, в свою очередь, может привести к выбуханию слизистой оболочки толстой кишки через слабые точки в стенке толстой кишки, что может привести к образованию мешочков, то есть дивертикулов.
Недостаток физических упражнений может увеличить риск формирования дивертикула, хотя этот аспект еще не считается определяющим.
В настоящее время голод, специфическая диета с низким содержанием пищевых волокон и антибиотики широкого спектра действия, часто связанные с антиспастическим препаратом, назначаются в качестве медицинской терапии при дивертикулярной болезни и/или дивертикулите. Использование нестероидных противовоспалительных средств (НПВС) и кортикостероидов не распространено, поскольку эти препараты могут способствовать перфорации вблизи дивертикула. В наиболее сложных случаях, таких как, например, перитонит, абсцессы и свищи, может потребоваться экстренная резекция с анастомозом или без анастомоза.
В настоящее время не существует доступного лечения, способного предотвратить образование дивертикула или вызвать его уменьшение, или эффективно предотвратить дивертикулит у лиц с дивертикулярной болезнью или дивертикулезом.
Для того чтобы ответить на вышеупомянутые ограничения предшествующего уровня техники, настоящее изобретение предлагает новую композицию для перорального применения, которая содержит экстракт, полученный из растений рода Vaccinium, с целью использования в профилактике или лечении дивертикулеза в толстой кишке, или в части сигмовидной кишки и прямой кишки, и патологий или заболеваний, связанных с наличием дивертикулов, таких как дивертикулярная болезнь, СНДБ (симптоматическая неосложненная дивертикулярная болезнь) и дивертикулит в толстой кишке, или в части сигмовидной кишки и прямой кишке.
Настоящее изобретение относится к композиции для перорального применения (CR), которая содержит или, альтернативно, состоит из:
(i) сердцевины, содержащей или, альтернативно, состоящей из экстракта (а) по меньшей мере одного растения рода Vaccinium и по меньшей мере одного ингредиента или вспомогательного вещества (b), приемлемого для фармацевтического или пищевого применения;
(ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), и полностью покрывающего указанную сердцевину (i), и который содержит по меньшей мере один ингредиент или вспомогательное вещество (с), приемлемое для фармацевтического или пищевого применения, где указанный гастрорезистентный слой (ii) способен обеспечить высвобождение экстракта (а) в слизистую оболочку кишечника; он предпочтительно способен обеспечить высвобождение экстракта (а) в толстой кишке.
Настоящее изобретение также относится к композиции для перорального применения (CR), которая содержит или, альтернативно, состоит из:
(i) сердцевины, содержащей или, альтернативно, состоящей из экстракта (а) по меньшей мере одного растения рода Vaccinium и по меньшей мере одного ингредиента или вспомогательного вещества (b), приемлемого для фармацевтического или пищевого применения;
(ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), и который полностью покрывает указанную сердцевину (i), и который содержит по меньшей мере один ингредиент или вспомогательное вещество (с), приемлемое для фармацевтического или пищевого применения, где указанный гастрорезистентный слой (ii) способен обеспечить высвобождение экстракта (а) в толстой кишке.
Настоящее изобретение далее относится к композиции для перорального применения (CR), которая содержит или, альтернативно, состоит из:
(i) сердцевины, содержащей или, альтернативно, состоящей из экстракта (а) по меньшей мере одного растения рода Vaccinium и по меньшей мере одного ингредиента или вспомогательного вещества (b), приемлемого для фармацевтического или пищевого применения;
(ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), который полностью покрывает указанную сердцевину (i) и который содержит по меньшей мере один ингредиент или вспомогательное вещество (с), приемлемое для фармацевтического или пищевого применения, где указанный гастрорезистентный слой (ii) способен обеспечить высвобождение экстракта (а) в толстой кишке; где указанная композиция предназначена для применения при профилактике и/или лечении дивертикулеза в толстой кишке или в части сигмовидной кишки и прямой кишки, а также патологий или заболеваний, связанных с наличием дивертикулов, таких как дивертикулярная болезнь, СНДБ (симптоматическая неосложненная дивертикулярная болезнь) и дивертикулит в толстой кишке или в области сигмовидной кишки и прямой кишки.
Композиция (CR) по настоящему изобретению является защищенной от действия желудочного сока и находится в твердой форме порошка, гранул, хлопьев, таблеток, пилюль или капсул; это предпочтительно защищенная от действия желудочного сока монолитная таблетка. В этом случае сердцевина (i) представлена и совпадает с монолитной таблеткой.
Настоящее изобретение относится к композиции (С), которая содержит или, альтернативно, состоит из:
- экстракта (а) плода по меньшей мере одного растения рода Vaccinium; и
- по меньшей мере одного ингредиента и/или вспомогательного вещества (b), приемлемого для фармацевтического или пищевого применения,
где указанная композиция предназначена для применения при профилактике и/или лечении дивертикулеза в толстой кишке или в части сигмовидной кишки и прямой кишки, а также патологий или заболеваний, связанных с наличием дивертикулов, таких как дивертикулярная болезнь, СНДБ (симптоматическая неосложненная дивертикулярная болезнь) и дивертикулит в толстой кишке или в части сигмовидной кишки и прямой кишке; предпочтительно, когда указанное применение включает пероральное введение (С).
Композиция (С) может также находиться в твердой форме, например, порошка, гранул, сфер или микрогранул или хлопьев, содержащейся внутри оболочки, например, капсулы или мягкого геля, из гастрорезистентного материала, способного к разрушению при рН выше 6, предпочтительно при рН от 6,5 до 8, например, рН 7,5. В этом случае композиция (С), содержащаяся в указанной капсуле или мягком геле, все еще может найти применение в профилактике и/или лечении дивертикулеза в толстой кишке или в части сигмовидной кишки и прямой кишки, а также патологий или заболеваний, связанных с наличием дивертикулов, таких как дивертикулярная болезнь, СНДБ (симптоматическая неосложненная дивертикулярная болезнь) и дивертикулит в толстой кишке или в части сигмовидной кишки и прямой кишки; предпочтительно, где указанное применение включает пероральное введение (С).
Предпочтительные варианты осуществления будут проиллюстрированы ниже без намерения каким-либо образом ограничить их объем и содержание.
Если не указано иное, содержание ингредиента в композиции относится к процентному содержанию по массе этого ингредиента по отношению к общей массе композиции.
Если не установлено иное, указание на то, что композиция «содержит» один или несколько компонентов, означает, что могут присутствовать другие компоненты в дополнение к одному или нескольким конкретно названным компонентам, а указание на то, что композиция «состоит» из данных компонентов, означает, что присутствие других компоненты исключено.
Композиция (C) может состоять из (a) и (b), или может включать другие ингредиенты или вспомогательные вещества в дополнение к (a) и (b).
В качестве неограничивающего примера указанные дополнительные ингредиенты, которые могут присутствовать в композициях (CR) и (C) настоящего изобретения, могут представлять собой другие активные ингредиенты, такие как:
- пищевые волокна (например, инулин, псиллиум);
- ферменты (например, галактозидаза и тому подобное);
- противовоспалительные средства (например, месалазин и его производные, беклометазон и аналогичные активные ингредиенты);
- антибиотики (например, рифаксимин и аналогичные активные ингредиенты);
- вещества с абсорбирующим действием на кишечном уровне и/или ветрогонным и/или пероральным противовспенивающим действием для уменьшения образования кишечного газа (например, мята перечная, симетикон и его производные, активированный уголь);
- антиоксиданты;
- вещества с иммуномодулирующим действием;
• короткоцепочечные жирные кислоты (КЦЖК, такие как бутират и его производные);
• омега-3 полиненасыщенные жирные кислоты;
• пробиотики или, альтернативно, микроорганизмы в форме лизата или экстракта (парапробиотики), метаболические биопродукты, вырабатываемые микроорганизмами (постбиотики), и/или любой другой продукт, полученный из них.
Неограничивающими примерами указанных микроорганизмов, которые могут присутствовать в композициях (CR) и (C) по настоящему изобретению, являются пробиотические бактерии, принадлежащие к родам Lactobacillus, Bifidobacterium и Enterococcus, и дрожжи, предпочтительно принадлежащие к роду Saccharomyces, взятые по отдельности или в разных комбинациях.
В предпочтительном варианте осуществления сердцевина (i), присутствующая в указанной композиции (CR) или (C), дополнительно содержит маннитол и/или по меньшей мере один активный ингредиент с противовоспалительным действием, выбранный из стероидного противовоспалительного лекарственного средства, нестероидного лекарственного средства, и вещества или смеси веществ природного происхождения.
Настоящее изобретение также будет ссылаться на следующие фигуры:
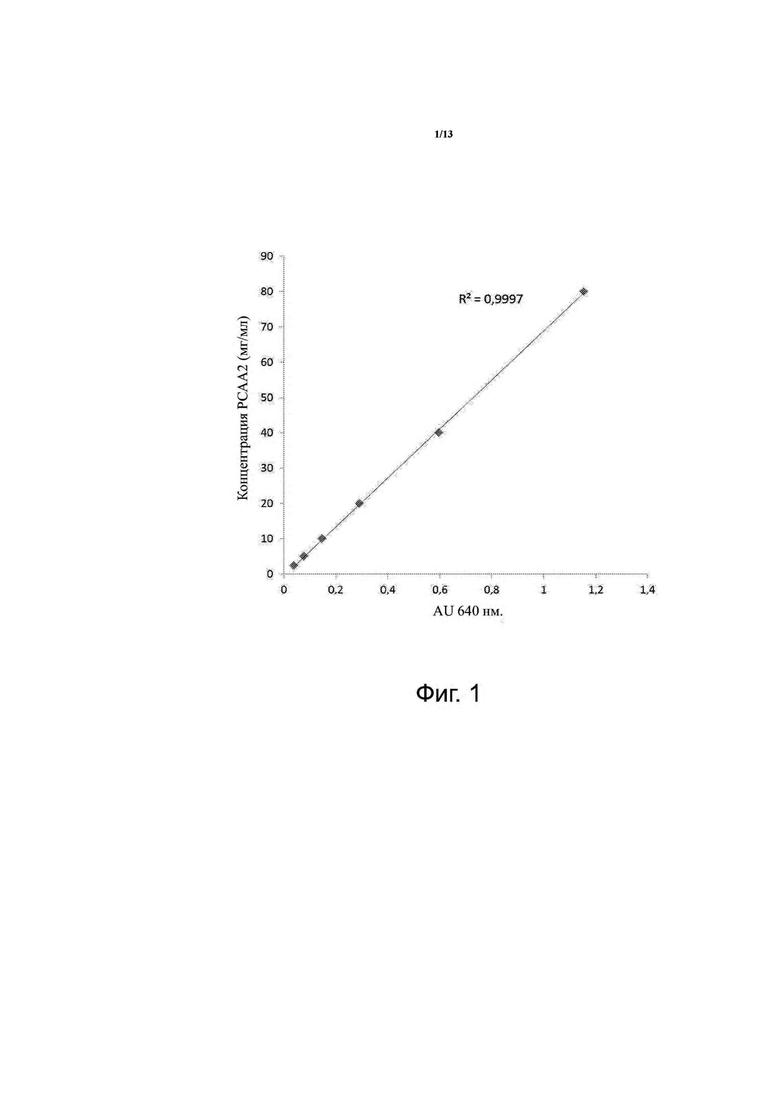
фигура 1 — калибровочная кривая для теста на растворение;
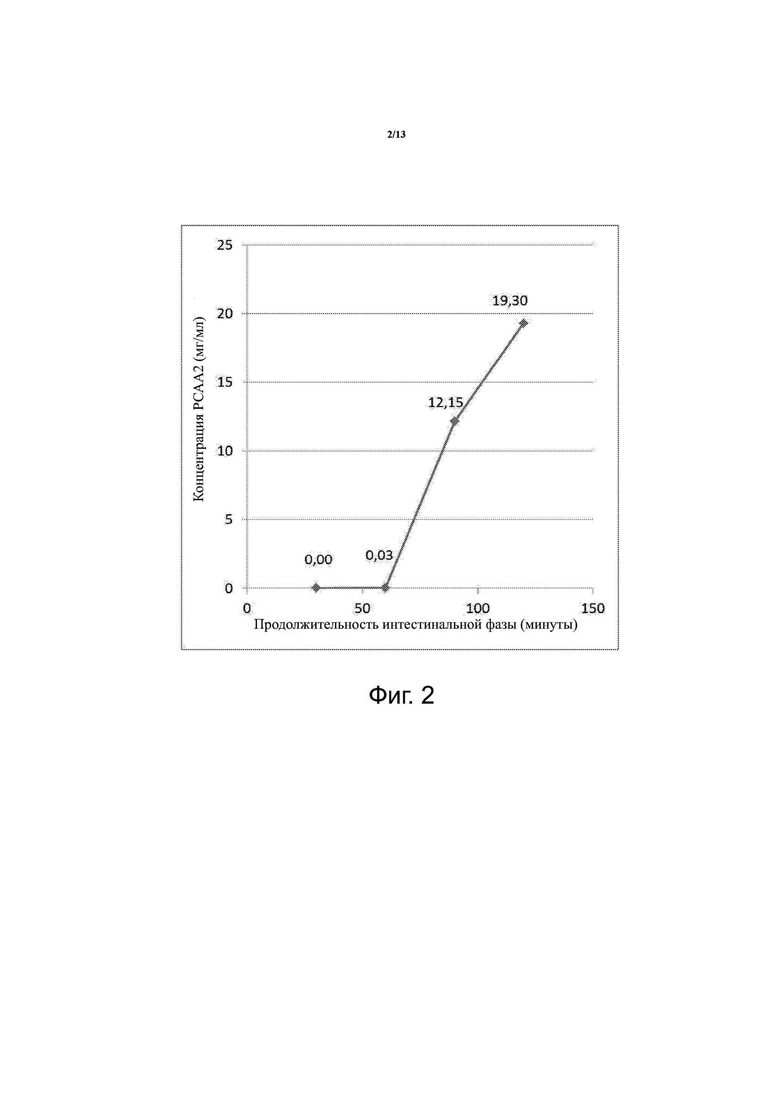
фигура 2 — результаты теста растворения на таблетке, защищенной от действия желудочного сока, согласно изобретению, в кишечной фазе;
фигуры 3-10 — результаты исследования по защитной эффективности в отношении слизистой оболочки кишечника (CacoGoblet): колонизация E.сoli;
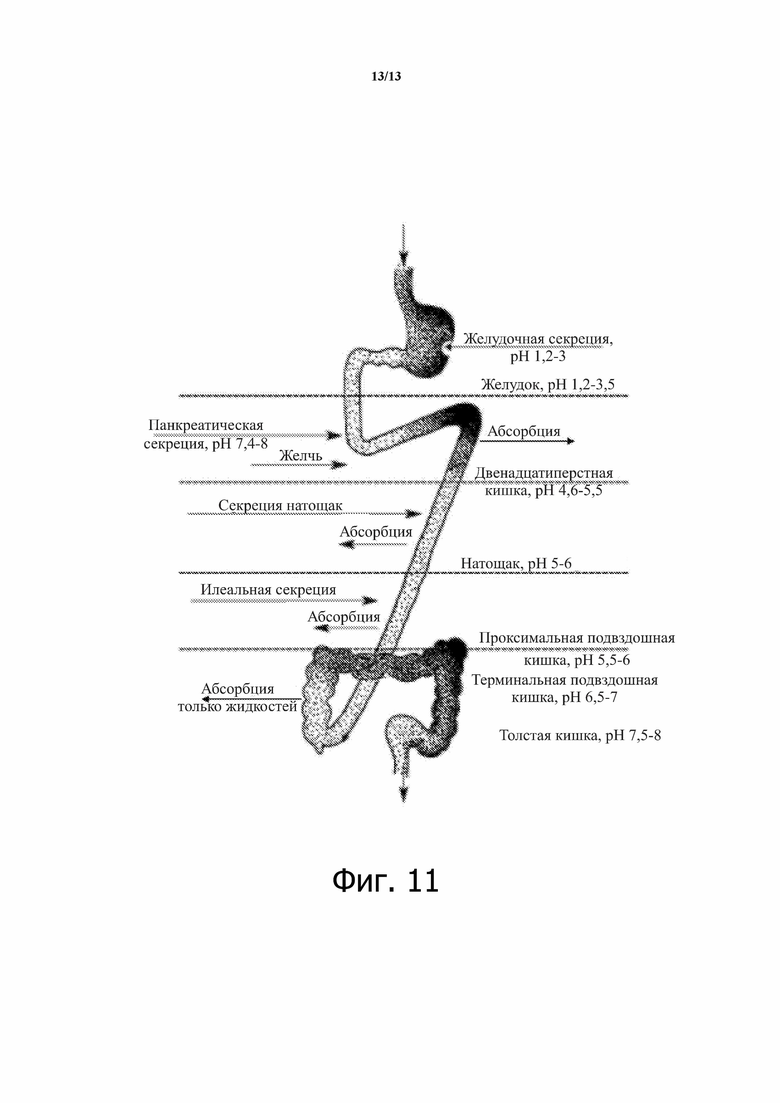
фигура 11 — иллюстрация желудочно-кишечного тракта.
В контексте настоящего изобретения термин «противовоспалительное лекарственное средство» используется в общем значении этого термина и указывает, как известно специалисту в данной области, любое вещество, способное уменьшать или устранять воспалительный процесс, в частности, повреждение кишечника человека, но не ограничиваясь им.
В композиции (CR), как определено выше, гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), содержит или, альтернативно, состоит по меньшей мере из одного вещества, выбранного из биотика Eudragard E1207, гастрорезистентного полимера, такого как поли(метилакрилат-со-метилметакрилат-со-метакриловая кислота) 7:3:1 или другой анионный метакриловый сополимер, триэтилцитрата E1505, талька, этилцеллюлозы, анионного метакрилатного сополимера и их смесей, лака, альгината натрия и их смесей, крахмала и модифицированных крахмалов, олеиновой кислоты, стеариновой кислоты и триглицеридов со средней длиной цепи.
Предпочтительные формы гастрорезистентного слоя (ii), наружного по отношению к сердцевине (i), включают или, альтернативно, состоят из:
- гастрорезистентного полимера, такого как поли(метилакрилат-со-метилметакрилат-со-метакриловая кислота) 7:3:1 или другого анионного метакрилатного сополимера: от 5 до 50 мг; от 10 до 35 мг; 18-25 мг;
- триэтилцитрата E1505: от 0,1 до 5 мг; от 0,3 до 3 мг; 0,5-2 мг;
- талька: от 1 до 30 мг; от 3 до 20 мг; 5-15 мг; или альтернативно:
- этилцеллюлозы: от 5 до 15 мг; от 8 до 12 мг; 9,97 мг;
- альгината натрия: от 5 до 15 мг; от 8 до 12 мг; 9,30 мг;
- гидроксида аммония: от 0,5 до 4 мг; от 1,5 до 3 мг; 2,34 мг;
- триглицеридов со средней длиной цепи: от 0,5 до 5 мг; от 1,5 до 3 мг; 2,12 мг;
- олеиновой кислоты: от 0,5 до 3 мг; от 1 до 2 мг; 1,17 мг;
- очищенной стеариновой кислоты: от 0,01 до 0,5 мг; от 0,05 до 0,3 мг; 0,1 мг; или альтернативно:
- этилцеллюлозы: от 5 до 50 мг; от 10 до 30 мг; 15-20 мг;
- диоксида титана: от 0,1 до 15 мг; от 0,5 до 10 мг; 1-5 мг;
- альгината натрия: от 0,1 до 5 мг; От 0,3 до 4 мг; 0,5-2 мг;
- олеиновой кислоты, стеариновой кислоты, триглицеридов со средней длиной цепи: каждый от 0,01 до 3 мг; от 0,05 до 1 мг.
Предпочтительные формы гастрорезистентного слоя (ii), наружного по отношению к сердцевине (i), включают или, альтернативно, состоят из:
- Eudragard ® биотика E1207 (Evonik): например, 20,4 мг;
- триэтилцитрата E1505: например, 1 мг;
- талька: например, 10,2 мг; или, альтернативно:
- этилцеллюлозы: например, 9,97 мг;
- альгината натрия: например, 9,30 мг;
- гидроксида аммония: например, 2,34 мг;
- триглицеридов со средней длиной цепи: например, 2,12 мг;
- олеиновой кислоты: например, 1,17 мг;
- очищенной стеариновой кислоты: например, 0,1 мг.
Указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), имеет характеристику разрушения и растворения в зависимости от значения рН и/или времени; преимущественно указанный слой (ii) составлен и приготовлен таким образом, чтобы он мог разрушаться и растворяться при значении рН примерно от 6,5 до 8, предпочтительно при рН примерно от 7 до 7,5 за время, составляющее от 30 минут до 120 минут, предпочтительно от 45 минут до 90 минут; например, при температуре от 30 до 40°С, предпочтительно от 34 до 37°С.
После продолжительных исследований и многочисленных экспериментальных попыток было обнаружено, что преимущественно использование одного или нескольких из указанных веществ для формирования внешнего гастрорезистентного слоя позволяет получить композицию (CR) для перорального применения, например таблетку, способную проходить неповрежденной через полость рта, пищевод и желудочный тракт и обеспечивать первоначальное разрушение указанного (ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), начиная с терминального отдела подвздошной кишки при pH около 6,5-7, с первоначальным растворением сердцевины (i) и выделением экстракта (а) или без него, и последующее разрушение указанного (ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), в толстой кишке, при рН около 7- 8 с растворением сердцевины (i) и выделением экстракта (а), главным образом в толстой кишке, при рН 7,5 (фиг.11).
Проведенные экспериментальные испытания показывают, что композиция (CR) по настоящему изобретению, например, в форме монолитной таблетки согласно примерам 1 и 2, остается неповрежденной в течение 2 часов при pH 1, тогда как при pH 6 она остается интактной в течение 1 часа. При pH 7,2 гастрорезистентное покрытие, наружное по отношению к сердцевине (i) из композиции (CR), начинает разрушаться примерно через 30 минут, тогда как указанное покрытие достаточно разрушается при pH 7,2 через 90 минут; пленка/ покрытие открывается, и внутри нее остаются небольшие участки сердцевины (i) или, в некоторых случаях, порошок, образующийся в результате полного разрушения сердцевины (i).
Что касается высвобождения указанного экстракта (а), присутствующего в указанной сердцевине (i), до подвздошной кишки высвобождение не происходит до рН 6,5. В терминальном отделе подвздошной кишки высвобождение составляет примерно от 5% до 20%, предпочтительно примерно от 10% до 15%. В толстой кишке при pH около 7,5, например, при pH около 7,2, высвобождение составляет примерно от 80% до 95%, предпочтительно примерно от 85% до 90%. Большая часть высвобождения указанного экстракта (а) происходит в толстой кишке, которая точно представляет место, где присутствуют дивертикулы и где проявляется патология или заболевание. Таким образом, экстракт (а), высвобождаемый в толстой кишке, способен действовать благодаря присутствию также ПАЦ (проантоцианидинов), которые способны оказывать противовоспалительное действие.
Композиция (CR) по изобретению находится в форме композиции для пищевой добавки или композиции для медицинского устройства, или композиции для питания для специальных медицинских целей, или фармацевтической композиции; все композиции находятся в фармацевтической форме для перорального применения.
В контексте настоящего изобретения термин «медицинское устройство» используется в значении согласно Итальянскому законодательному декрету № 46 от 24 февраля 1997 г., что соответствует определению, предоставленному Всемирной организацией здравоохранения и доступному по адресу http://www.who.int/medical_devices/full_deffinition/en/, т.е. оно указывает на вещество или другой продукт, используемый отдельно или в комбинации, предназначенной для использования производителем, отдельно или в комбинации, для людей в целях диагностики, профилактики, мониторинга, лечения или облегчения заболевания, причем это устройство не достигает своего основного предполагаемого действия фармакологическими, иммунологическими или метаболическими средствами внутри или на теле человека, но которому могут содействовать в его предназначенной функции такие средства.
В композиции (CR), как определено выше, экстракт (а) может быть представлен фруктами (более конкретно, ягодами), принадлежащими к роду Vaccinium и, при необходимости, также Sambucus, Lycium, Euterpe и их комбинациями. Экстракт (а) предпочтительно представляет собой сухой экстракт.
В композиции (CR), как определено выше, экстракт (а) предпочтительно получен из плодов по меньшей мере одного растения рода Vaccinium и подрода Oxycoccus, такого как Vaccinium macrocarpon (клюква крупноплодная), Vaccinium oxycoccos (клюква обыкновенная), или подрода Vaccinium, такого как Vaccinium arboreum (голубика обыкновенная), Vaccinium crassifolium (черника ползучая), Vaccinium boreale (северная черника), Vaccinium myrtillus (черника обыкновенная) или их смеси; предпочтительно, где экстракт (а) представляет собой плоды Vaccinium macrocarpon или Vaccinium oxycoccos или их смеси. Еще более предпочтительно, экстракт (а) содержит или состоит из плодов Vaccinium macrocarpon. Предпочтительно экстракт (а) представляет собой сухой экстракт; в одном варианте осуществления он представляет собой сухой экстракт клюквы, предпочтительно содержащий ПАЦ (проантоцианидины) в концентрации от 5 до 30% по массе или объему, например, 10%, или 15%, или 20%, или 25%.
Американская клюква (Vaccinium macrocarpon) представляет собой небольшой вечнозеленый кустарник, принадлежащий к семейству вересковых (Ericaceae), который растет в зонах с умеренно-холодным климатом средних широт, в частности, в Северной Америке и в некоторых северных регионах Европы и Азии, и производит красные плоды, похожие на ягоды, с плотной мякотью и обычно терпким вкусом.
В прошлом среди индейцев Северной Америки клюква считалась священным фруктом и использовалась как в качестве пищи, так и для лечения камней в почках и различных проблем мочевыводящих путей.
В настоящее время американская клюква используется во всем мире благодаря своим бесчисленным полезным свойствам, в основном благодаря высокому содержанию проантоцианидинов (ПАЦ), в частности, проантоцианидинов А-типа.
Экстракты американской клюквы используются прежде всего для профилактики и лечения заболеваний мочевыводящих путей, а также в качестве профилактики против адгезии Helicobacter pylori, бактерии, которая часто является причиной язвы желудка и двенадцатиперстной кишки, к стенкам желудка, или против адгезии бактерий, которые заселяют полость рта и ответственны за образование зубного налета, или против адгезии потенциально патогенных бактерий, таких как E.сoli, на кишечном уровне.
Европейский патент EP 2135616 B1 относится к применению клюквы для лечения ВЗК и язвенного колита, которые, как указано выше, являются патологиями, совершенно отличными от тех, к которым относится настоящее изобретение.
В контексте настоящего изобретения использование клюквы для лечения ВЗК и язвенного колита исключено и, таким образом, не предусматривается, так же как использование клюквы для предотвращения адгезии Helicobacter pylori к стенкам желудка не предусматривается. Кроме того, исключается использование клюквы для лечения инфекций мочевыводящих путей (ИМП), таких как цистит (воспаление мочевого пузыря) или бактериальный цистит или небактериальный цистит, такой как, например, цистит интерстициального типа, и, таким образом, не предусмотрено.
Автор изобретения обнаружил, что экстракт плодов рода Vaccinium, в частности, американской клюквы, полезен для профилактики и/или лечения, предпочтительно посредством перорального введения, дивертикулеза в толстой кишке или в части сигмовидной кишки и прямой кишки, и/или патологий или заболеваний, возникающих или связанных с наличием дивертикулов, таких как дивертикулярная болезнь, симптоматическая неосложненная дивертикулярная болезнь (СНДБ) и дивертикулит в толстой кишке или в части сигмовидной кишки и прямой кишки.
В композиции (CR) согласно настоящему изобретению экстракт (а) предпочтительно содержит по меньшей мере 10%, более предпочтительно по меньшей мере 15% или 20%, или 30% и/или не более 95%, или 60%, или 40% проантоцианидинов от общей массы указанного экстракта (а), более предпочтительно, проантоцианидинов А-типа, но не ограничиваясь ими. Проантоцианидины (ПАЦ) представляют собой олигомеры и полимеры флаван-3-олов, которые принадлежат к семейству флавоноидов и могут быть количественно определены, например, с помощью метода «BL-DMAC» из Prior, R.L. et al. J. Sci Food Agric 2010, 90 (9), 1473-8, или эквивалентными методами. Указанный экстракт (а) предпочтительно представляет собой сухой экстракт; еще более предпочтительно, это сухой экстракт клюквы.
Композиция (CR) или (C) согласно изобретению предпочтительно содержит по меньшей мере:
- указанный экстракт (а) от 150 до 600 мг, предпочтительно от 200 до 300 мг, более предпочтительно от 240 до 260 мг экстракта Vaccinium macrocarpon, содержащего по меньшей мере 10%, более предпочтительно по меньшей мере 15% проантоцианидинов (ПАЦ) по массе, от общей массы (а);
- по меньшей мере один ингредиент или вспомогательное вещество (b), приемлемые для фармацевтического или пищевого применения, при необходимости выбранные из целлюлозы, маннитола, стеарата магния, магниевых солей насыщенных и/или ненасыщенных жирных кислот, диоксида кремния, карбоксиметилцеллюлозы, карбоксиэтилцеллюлозы, сшитой карбоксиметилцеллюлозы натрия и их смесей. Указанный экстракт (а) предпочтительно представляет собой сухой экстракт; еще более предпочтительно, это сухой экстракт клюквы. Ингредиенты или вспомогательные вещества (b), приемлемые для фармацевтического или пищевого применения, предпочтительно выбраны из целлюлозы, маннитола, диоксида кремния, сшитой карбоксиметилцеллюлозы натрия и магниевых солей насыщенных и/или ненасыщенных жирных кислот.
Композиция (CR), как определено выше, особенно полезна для лечения и/или профилактики дивертикулярной болезни и связанных с ней патологий.
В одном варианте осуществления настоящее изобретение предлагает композицию (С), которая содержит или, альтернативно, состоит из:
- экстракта (а) плода по меньшей мере одного растения рода Vaccinium, и
- по меньшей мере, одного ингредиента (b), приемлемого для фармацевтического или пищевого применения,
причем указанная композиция предназначена для профилактики и/или лечения дивертикулярной болезни или патологии, вызванной дивертикулезом, предпочтительно, где указанное применение включает пероральное введение (С).
Применение может быть осуществлено любым путем. Предпочтительно композицию принимают перорально, более предпочтительно в форме пилюль, капсул, таблеток, гранулированного порошка, капсул с твердой оболочкой, растворяющихся в полости рта гранул, саше, пастилок или флаконов для питья.
Альтернативно, композицию по изобретению составляют в виде жидкости, например, в виде сиропа или напитка, или же ее добавляют в пищу, например, в йогурт, сыр или фруктовый сок.
Альтернативно, композиция по изобретению представлена в форме, способной оказывать действие местно, например, посредством клизмы.
Указанная композиция (С) предпочтительно предназначена для применения с целью лечения или профилактики по меньшей мере одного из дивертикулярной болезни, симптоматической неосложненной дивертикулярной болезни (СНДБ) и дивертикулита. Указанная композиция (С) предпочтительно предназначена для применения с целью лечения и/или профилактики дивертикулита.
В предпочтительном варианте осуществления композиция (C) для вышеописанного применения находится в форме перорального фармацевтического препарата, или пищевой добавки, или медицинского устройства, содержащего гастрорезистентное покрытие и способного обеспечить высвобождение экстракта (а) в толстой кишке.
В предпочтительном варианте осуществления в композиции (С) для применения, как указано выше, экстракт (а) получают из плодов по меньшей мере одного растения рода Vaccinium и подрода Oxycoccus, такого как Vaccinium macrocarpon, Vaccinium oxycoccos, или подрода Vaccinium, такого как Vaccinium arboreum, Vaccinium crassifolium, Vaccinium boreale, Vaccinium myrtillus (черника), или их смесей.
Более предпочтительно в композиции (С) для применения согласно настоящему изобретению экстракт (а) получают из плодов Vaccinium macrocarpon (американской клюквы) или Vaccinium oxycoccos или их смеси. Еще более предпочтительно, экстракт (а) содержит или состоит из плодов Vaccinium macrocarpon. Экстракт (а) предпочтительно представляет собой сухой экстракт.
В композиции (С) для применения согласно настоящему изобретению экстракт (а) предпочтительно содержит по меньшей мере 10%, более предпочтительно по меньшей мере 15% или 20% или 30%, и не более 95%, или 60%, или 40% проантоцианидинов от общей массы (а), предпочтительно проантоцианидинов А-типа, но не ограничиваясь ими. Предпочтительно экстракт (а) представляет собой сухой экстракт; в одном варианте осуществления он представляет собой сухой экстракт клюквы, предпочтительно содержащий ПАЦ (проантоцианидины) в концентрации от 5 до 30% по массе или объему, например, 10%, или 15%, или 20%, или 25%.
Проантоцианидины (ПАЦ) представляют собой олигомеры и полимеры флаван-3-олов, которые принадлежат к семейству флавоноидов и могут быть количественно определены, например, с помощью метода «BL-DMAC» из Prior, R.L. et al. J. Sci Food Agric 2010, 90 (9), 1473-8, или эквивалентными методами.
В контексте настоящего изобретения ингредиенты, приемлемые для фармацевтического или пищевого применения, включают все вспомогательные вещества, известные специалисту в данной области техники, для приготовления форм для перорального введения, такие как, в качестве неограничивающего примера, разбавители, абсорбенты, подсластители, ароматизаторы, красители, любриканты, антиадгезивные средства, глиданты, связующие вещества, дезинтегранты, сурфактанты, антимикробные средства, антиоксиданты, стабилизаторы, загустители, гелеобразующие агенты и вещества, способные изменять высвобождение активного ингредиента с течением времени, позволяя высвобождать его только при определенных физиологических условиях, например, в определенном интервале рН.
Композиция (С) для применения, как описано выше, предпочтительно содержит по меньшей мере:
- (а) от 150 до 600 мг, предпочтительно от 200 до 300, более предпочтительно от 240 до 260 мг экстракта Vaccinium macrocarpon, содержащего по меньшей мере 10%, более предпочтительно по меньшей мере 15%, проантоцианидинов по массе от общей массы (а);
- (b) по меньшей мере один фармацевтически приемлемый ингредиент, при необходимости выбранный из целлюлозы, маннитола, стеарата магния, диоксида кремния, карбоксиметилцеллюлозы и их смесей. Более предпочтительно, указанная композиция (C) дополнительно содержит покрытие, защищающее от воздействия желудочного сока, то есть такое, которое способно защищать смесь, содержащую по меньшей мере (a) и (b), от действия желудочного сока.
Следующие примеры обеспечивают практические варианты осуществления изобретения, при этом нет намерения ограничивать его объем и пределы.
Предпочтительные формы композиций (CR) по настоящему изобретению изложены ниже.
(i) Сердцевина, содержащая:
- экстракт клюквы, содержащий ПАЦ в концентрации (по массе) 10% или 15% или 30%: от 100 до 500 мг; от 150 до 400 мг; 240-300 мг;
- целлюлозу — от 100 до 400 мг; от 200 до 350 мг; 300-310 мг;
- маннитол — от 1 до 50 мг; от 5 до 30 мг; 10-18 мг;
- диоксид кремния — от 1 до 50 мг; от 3 до 30 мг; 5-8 мг;
- сшитую карбоксиметилцеллюлозу натрия — от 1 до 30 мг; от 3 до 20 мг; 5-12 мг;
- магниевые соли жирных кислот — от 1 до 30 мг; от 3 до 20 мг; 5-10 мг.
(ii) Первый тип покрытия (пленки) сердцевины (i), включающий следующие агенты:
- гастрорезистентный полимер, такой как поли(метилакрилат-со-метилметакрилат-со-метакриловая кислота) 7:3:1 или другой анионный метакрилатный сополимер: от 5 до 50 мг; от 10 до 35 мг; 18-25 мг;
- триэтилцитрат E1505 — от 0,1 до 5 мг; от 0,3 до 3 мг; 0,5-2 мг;
- тальк — от 1 до 30 мг; от 3 до 20 мг; 5-15 мг; или, в качестве альтернативы.
(ii) Второй тип покрытия (пленки) сердцевины (i), включающий следующие агенты:
- этилцеллюлозу — от 5 до 15 мг; от 8 до 12 мг; 9,97 мг;
- альгинат натрия — от 5 до 15 мг; от 8 до 12 мг; 9,30 мг;
- гидроксид аммония — от 0,5 до 4 мг; от 1,5 до 3 мг; 2,34 мг;
- триглицериды со средней длиной цепи — от 0,5 до 5 мг; от 1,5 до 3 мг; 2,12 мг;
- олеиновую кислоту — от 0,5 до 3 мг; от 1 до 2 мг; 1,17 мг;
- Очищенную стеариновую кислоту: от 0,01 до 0,5 мг; от 0,05 до 0,3 мг; 0,1 мг.
Предпочтительные формы композиций (CR) по настоящему изобретению изложены ниже.
(i) Сердцевина, содержащая:
- экстракт клюквы, содержащий ПАЦ в концентрации (по массе) 10% или 15% или 30%: от 100 до 500 мг; от 150 до 400 мг; 240-300 мг;
- микрокристаллическую целлюлозу — от 100 до 400 мг; от 200 до 350 мг; 320-335 мг;
- стеарат магния — от 1 до 30 мг; от 2 до 20 мг; 5-10 мг;
- диоксид кремния — от 1 до 50 мг; от 3 до 30 мг; 5-8 мг.
(ii) Первый тип покрытия (пленки) сердцевины (i), включающий следующие агенты:
- этилцеллюлозу — от 5 до 50 мг; от 10 до 30 мг; 15-20 мг;
- диоксид титана — от 0,1 до 15 мг; от 0,5 до 10 мг; 1-5 мг;
- альгинат натрия — от 0,1 до 5 мг; от 0,3 до 4 мг; 0,5-2 мг;
- олеиновую кислоту, стеариновую кислоту, триглицериды со средней длиной цепи: каждый от 0,01 до 3 мг; от 0,05 до 1 мг; или альтернативно.
(ii) Второй тип покрытия (пленки) сердцевины (i), включающий следующие агенты:
- этилцеллюлозу — от 5 до 15 мг; от 8 до 12 мг; 9,97 мг;
- альгинат натрия — от 5 до 15 мг; от 8 до 12 мг; 9,30 мг;
- гидроксид аммония — от 0,5 до 4 мг; от 1,5 до 3 мг; 2,34 мг;
- триглицериды со средней длиной цепи — от 0,5 до 5 мг; от 1,5 до 3 мг; 2,12 мг;
- олеиновую кислоту — от 0,5 до 3 мг; от 1 до 2 мг; 1,17 мг;
- очищенную стеариновую кислоту — от 0,01 до 0,5 мг; от 0,05 до 0,3 мг; 0,1 мг.
В качестве неограничивающего примера композиция (CR) по настоящему изобретению может содержать:
Пример 1
(i) Сердцевину, содержащую:
- экстракт клюквы, содержащий 15% ПАЦ (по массе): 240 мг;
- целлюлозу: 304,4 мг;
- маннитол: 15 мг;
- диоксид кремния: 5,8 мг;
- сшитую карбоксиметилцеллюлозу натрия: 9 мг;
- магниевые соли жирных кислот: 5,8 мг.
Общая сердцевина 580 мг. Диапазон массы — 575–585 мг
(ii) Покрытие (пленку) сердцевины (i), содержащую:
- биотик Eudragard® E1207 (Evonik) — 20,4 мг;
- триэтилцитрат E1505 — 1 мг;
- тальк — 10,2 мг.
Общее покрытие/ пленка 31,6 мг. Диапазон массы — 26,1 мг - 37,7 мг.
Общая покрытая/ защищенная оболочкой таблетка 612 мг. Диапазон массы: 607 мг - 617 мг.
Пример 2
(i) Сердцевина, содержащая:
- экстракт клюквы, содержащий 15% ПАЦ (по массе): 240 мг;
- целлюлозу — 270 мг;
- маннитол — 29 мг;
- диоксид кремния — 5,8 мг;
- сшитую карбоксиметилцеллюлозу натрия — 29 мг;
- магниевые соли жирных кислот — 5,8 мг.
Общая сердцевина 580 мг. Диапазон веса —575–585 мг
(ii) Покрытие (пленка) сердцевины (i), содержащее:
- этилцеллюлозу — 9,97 мг;
- альгинат натрия — 9,30 мг;
- гидроксид аммония — 2,34 мг;
- триглицериды со средней длиной цепи — 2,12 мг;
- олеиновую кислоту — 1,17 мг;
- очищенную стеариновую кислоту — 0,1 мг.
Общее покрытие/ пленка 25 мг. Диапазон массы — 20–30 мг.
Общая покрытая/ защищенная оболочкой таблетка 605 мг. Диапазон массы — 595 мг – 615 мг.
Анализ растворимости
Материалы
Были испытаны таблетки с гастрорезистентным покрытием в соответствии с изобретением, согласно примеру.
Реагенты
- Диметиламиноциннамальдегид (DMAC, Sigma, код D-4506).
- Процианидин А2 (PCAA2, Sigma, код 28660).
- Ферменты и реагенты для GID (Sigma).
Методы
- Анализ проантоцианидинов (РСА) в соответствии со спектрофотометрическим методом, предложенным Prior et al. (Multi-laboratory validation of a standard method for quantifying proanthocyanidins in cranberry powders. J. Sci. Food Agric. (2010), 9, 1473–1478. DOI 10.1002/jsfa.3966).
- Анализ гастроинтестинальной растворимости (GID) in vitro в соответствии с методом, предложенным Minekus et al. («A standardised static in vitro digestion method suitable for food - an international consensus» Food Funct. (2014), 6, 1113-1124. DOI 10.1039/C3FO60702J).
Результаты
Таблетки подвергали in vitro GID (в трех экземплярах), образцы отбирали через 120 минут желудочной фазы и через 30, 60, 90 и 120 минут кишечной фазы. Различные образцы анализировали на содержание PCAA2 (проантоцианидина А2-типа) в мг-эквивалентах, используя метод DMAC, и количественно определяли в соответствии с калибровочной кривой, показанной на фиг.1 (полученной тем же методом, что и для стандарта PCAA2 при 640 нм).
Профиль растворения таблеток согласно настоящему изобретению показан на фиг.2.
По существу эквивалентные результаты были получены для таблеток с гастрорезистентным покрытием из примеров 1 и 2.
Во время желудочной фазы in vitro GID не было аналитически подтвержденного высвобождения процианидина (РСА).
Кинетика высвобождения PCA (выраженная в виде эквивалентов PCAA2 на таблетку, среднее из трех повторностей) во время кишечной фазы in vitro показана на фиг.2. Высвобождение PCA было аналитически наблюдаемым во время кишечной фазы через 60 минут.
Содержание непереваренного PCAA2 в таблетке в эквивалентах мг определяли после механического разрушения самой таблетки и экстракции PCA гастроинтестинальными жидкостями и ферментами (холостая проба GID) или экстракционным растворителем (ацетон/вода/уксусная кислота, 75:24,5:0,5 объемные отношения), как предложено Prior et al. (2010). Полученные результаты были соответственно равны 19,39 и 19,81 мг-эквивалентов PCAA2 на таблетку.
Оценка эффективности
С целью оценки эффективности настоящего изобретения, в частности, в отношении эффективности защиты слизистой оболочки кишечника, было проведено несколько испытаний in vitro для определения:
- активности конкуренции против адгезии штаммов Escherichia coli путем блокирования механизмов адгезии на основе анализа специфических белков;
- противовоспалительной активности за счет снижения активации моноцитов в макрофаги, основанной на исследовании кишечной проницаемости, оцениваемой, как описано ниже:
o Измерение ТЭЭС (трансэпителиального электрического сопротивления)
Трансэпителиальное электрическое сопротивление (ТЭЭС) является прямой мерой функциональности барьера эпителиальных тканей: оно отражает глобальное сопротивление ткани, обусловленное как толщиной, так и структурой, и представляет показатель уровня целостности монослоя и, следовательно, образования плотных соединений между клетками. Трансэпителиальное электрическое сопротивление (выраженное в Ωсм2) измеряли с помощью вольтметра (ERS Millicell).
o Анализ с Люцифером желтым в присутствии вещества, подлежащего оценке.
Люцифер желтый (LY) является флуоресцентным маркером, не проникающим через клеточную мембрану, который позволяет проверить целостность клеточных соединений (в процентах). Его использовали для изучения проницаемости вещества на параклеточном уровне в моноклеточных слоях бокаловидных клеток Caco-2/Caco. Транспорт LY оценивали, как проход в базолатеральный компартмент после определенного периода инкубации. Показания флуоресцентного вещества определяли с помощью спектрофлуориметра с возбуждением 428 нм и испусканием 525 нм.
В частности, будет проведена оценка эффективности настоящего изобретения в защите слизистой оболочки кишечника после стресса, вызванного кишечной палочкой, с использованием экспериментальной модели Caco2-goblet®, которая состоит не только из кишечных клеток, но также и из клеток, секретирующих слизь, HT29, в совместной культуре, которая является гораздо более реалистичной системой.
Было проведено исследование защитной эффективности слизистой оболочки кишечника (CacoGoblet): колонизация E.сoli.
1. Введение и цель исследования
Биологическая значимость модели Caco-2 хорошо известна, поскольку она является эталонной моделью in vitro, используемой для воспроизведения функций слизистой оболочки кишечника.
CacoGoblet представляет собой модель секретирующих слизь клеток, состоящую из проницаемых засеянных подложек на микропористых поликарбонатных фильтрах с человеческими секретирующими слизь бокаловидными клетками и дифференцированными и поляризованными клетками Caco-2.
Экспериментальную модель, основанную на модели CacoGoblet, применяли для оценки эффективности экстракта клюквы от имени Sofar S.p.A.
Нецитотоксическую концентрацию тестировали на предварительной стадии с помощью анализа МТТ, чтобы исключить потенциальную внутреннюю токсичность продукта.
Были использованы два протокола:
1) противовоспалительные свойства экстракта клюквы в системе совместной культуры (клетки THP-1 и клетки кишечного эпителия);
2) способность клюквы предотвращать адгезию E.coli к слизистой оболочке.
2. Дизайн эксперимента
1) Противовоспалительные свойства экстракта клюквы в системе совместной культуры in vitro (клетки THP-1 и клетки кишечного эпителия).
Клетки CacoGoblet предварительно обрабатывали 10 нг/мл ИЛ-1-бета в течение ночи. После удаления ИЛ-1-бета кишечную модель обрабатывали клюквой в нецитотоксической концентрации в течение 24 часов. Параллельную обработку проводили с эталонным веществом этакортиленом (дексаметазона натрия фосфатом) в концентрации 0,15% для изучения преодоления воспалительного состояния слизистой оболочки.
Затем продукты удаляли, и маркированные клетки THP-1 (помеченные клеточным маркером 5-хлорметил-флуоресцеин-диацетатом) добавляли к клеткам CacoGoblet в апикальном компартменте и инкубировали в течение 1 часа при 37°C.
После удаления неприлипающих клеток остаточную поверхностную флуоресценцию клеток THP-1 оценивали под микроскопом.
Противовоспалительную активность различных соединений на кишечном уровне оценивали в статическом анализе, используя снижение клеточной адгезии THP-1 на CacoGoblet в качестве параметра конечной точки.
2) Способность клюквы предотвращать адгезию E.coli к слизистой оболочке.
Клетки CacoGoblet, предварительно обработанные клюквой в течение 4 часов, колонизировали с 50 мкл Escherichia сoli (ATCC 8739) при 37°C в течение 2 часов. В конце колонизации избыток бактерий удаляли и оценивали следующие параметры:
- трансэпителиальное электрическое сопротивление (ТЭЭС) и параклеточное прохождение Люцифера желтого;
- иммунофлюоресценцию альфа-актинина: альфа-актинин взаимодействует с Tir, белком E.сoli, с образованием адгезивной бляшки, известной как пьедестал, и является маркером инфекции E.сoli;
- ультраструктурный анализ E.сoli с помощью сканирующего электронного микроскопа (СЭМ) с целью оценки плотности бактерий и адгезии к поверхности CacoGoblet.
3. Материалы
3.1. Экспериментальная система
CacoGobletTM представляет собой готовый набор для секреции слизи для оценки интестинальной абсорбции in vitro. Набор состоит из проницаемых подложек с 24 лунками, засеянными бокаловидными продуцирующими слизь клетками человека и клетками Caco-2, дифференцированными и поляризованными в чашках Transwell HTS, с добавлением эксклюзивной запатентованной транспортной среды, стабильной при комнатной температуре.
Клеточную линию CacoGoblet получали на 20-й день дифференцировки и использовали в течение 5 последовательных дней, изменяя полную среду и измеряя ТЭЭС на основе внутренней процедуры. Техническое описание CacoGobletTM приведено в Приложении I.
DMEM (серия RNBF5082), содержащую 10% ЭТС, 1% глутамина 200 мМ и 1% заменимых аминокислот, использовали в качестве среды, как показано в таблице 1.
Таблица 1
3.1.1. Условия культивирования и использования экспериментальной системы
Получив продукт CacoGoblet, извлекали пакеты с застежками-молниями, в которых находятся пластины. Открывали застежку и оставляли сумку в темноте при комнатной температуре до пятницы на той же неделе. В пятницу инкубировали чашки при 37°C, с 5% CO2, при насыщенной влажности, в течение 4 часов. Заменяли среду и начинали эксперимент в следующий понедельник.
3.2. Исследуемое вещество: идентификация и характеристика.
Спонсор несет ответственность за паспорт безопасности и характеристику исследуемых веществ (таблица 2).
Таблица 2
Sofar S.p.A.
3.3. Отрицательный и положительный контроль
Отрицательный контроль был средой как таковой.
Положительный контроль для протокола 1: интерлейкин 1-бета (SRP6169; серия 9E126460) (таблица 3).
Таблица 3
Дексаметазона натрия фосфат (SIFI, серия 160040)
Серия № 38/76
1,2*107 КОЕ
4. Методики
4.1. E.coli.
Штамм: E.coli ATCC 8739, номер серии.
Штамм инокулировали за неделю до эксперимента в питательном бульоне. Кроме того, его засевали на чашки с агаровой средой для проверки его нормальной морфологии. Затем следовала инкубация при 37°С в течение 16-24 часов.
4.1.1. Приготовление суспензии Escherichia coli и процедура колонизации
В день колонизации проверяли оптическую плотность (OП) при 600 нм раствора E.coli и использовали для приготовления колонизационных суспензий на основе внутренних процедур (PM 18).
Подсчет бактерий проводили для проверки каждого инокулята в питательной агаровой среде путем посева соответствующих 10-кратных разведений на чашки (от неразбавленной версии до 10-7-кратного разведения суспензии каждого компартмента). Количество жизнеспособных бактерий, применяемое к CacoGoblet, соответствует 1,2*107 КОЕ.
4.2. Тест трансэпителиального сопротивления (ТЭЭС)
4.2.1. Принцип метода
Трансэпителиальное электрическое сопротивление (ТЭЭС) является прямой мерой барьерной функции кожи: оно отражает общее сопротивление ткани, как по структуре, так и по толщине, и измеряет целостность барьера с точки зрения плотных контактов.
Значение ТЭЭС для монослоя дифференцированных клеток Caco-2 указывает на степень целостности самого монослоя и, соответственно, образование плотных контактов между энтероцитами. Измерение ТЭЭС (в Ω*см2) производили с помощью вольтметра (Millicell ERS) (диапазон 200-2000 Ω).
4.2.2. Процедура
ТЭЭС оценивали на монослое хорошо дифференцированных клеток CacoGoblet после 21 дня культивирования, выполняя измерение путем введения с использованием правильного электрода и расположения короткого конца электрода внутри вставки в апикальных положениях (в 0,3 мл среды). Длинный конец электрода погружали в лунку в базолатеральном положении (в 0,9 мл среды).
4.3. Тест с Люцифером желтым
4.3.1. Принцип метода
Люцифер желтый (LY) - флуоресцентный краситель, не проникающий через клеточную мембрану. Его используют для изучения параклеточной проницаемости вещества. Когда контакты не повреждены, у них отмечается для Люцифера желтого очень низкая проницаемость; с другой стороны, если контакты повреждены, поток Люцифера желтого увеличивается. Следовательно, этот тест позволяет проверить целостность клеточных контактов в присутствии исследуемого вещества.
4.3.2. Процедура
Люцифер желтый (LY) наносили в апикальном компартменте в концентрации 100 мкМ после воздействия исследуемого вещества, растворенного в физиологическом растворе (0,25 мл). 0,70 мл физиологического раствора добавляли в базолатеральный компартмент. Транспорт LY оценивали с точки зрения прохождения из апикального компартмента в базолатеральный компартмент после определенного периода инкубации, равного 1 часу при 37°С.
Считывание производили с помощью спектрофлуориметра (TECAN INFINITE M200) с возбуждением 428 нм и излучением 525 нм.
Процент проницаемости рассчитывали по следующей формуле:
Поток LY = (RFUBL / RFUAP исходный) x 100
В интактном монослое CacoGoblet поток LY должен составлять менее 1,4%.
4.4. Сканирующая электронная микроскопия (СЭМ)
Образцы, подлежащие исследованию с помощью СЭМ, фиксировали 2,5% раствором глутаральдегида в 0,1 М ФБР в течение 24 часов, промывали 0,1 М буфером какодилата натрия, рН 7,4 и экстрагировали в 1% тетроксиде осмия (OsO4) в том же образце (2 часа при комнатной температуре). Затем образцы дегидратировали в возрастающих концентрациях этанола при комнатной температуре, и в гексаметилдисилазане в течение ночи.
Образцы помещали на штыри с угольными наконечниками и покрывали слоем золота, используя устройство для нанесения металлических покрытий SEM E5100 от Polaron Equipment Limited, а затем переносили в электронный сканирующий микроскоп Zeiss Sigmoid для просмотра и фотографирования.
Таблица 4
Образец СЭМ, созданный при исследовании (таблица 4)
4.5. Иммунофлуоресценция: Альфа-актинин.
4.5.1. Принцип метода
Иммунофлуоресцентная маркировка является гистологическим методом обнаружения специфических структур или молекул в клеточных компартментах гистологических срезов. Методика основана на специфичности антитела, связывающего антиген, для обнаружения молекулы-мишени и системы обнаружения с помощью флуоресцентного микроскопа с использованием непрямого метода: первичного антитела, способного специфически распознавать мишень, и вторичного антитела, связанного с флуорофором, способного распознавать первичное антитело.
4.5.2. Процедура
После фиксации в холодном этаноле в течение 30 минут и в холодном ацетоне в течение 3 минут слизистую оболочку кишечника промывали ФБР, и неспецифические реакции блокировали 1% БСА в ФБР в течение 30 минут. Каждую вставку инкубировали в течение ночи при 4°C с антителом к альфа-актинину (моноклональное антитело мыши, ab18061, партия GR256204-1) в концентрации 1 мкг/мл в 1% БСА в ФБР. После промывания ткани инкубировали при комнатной температуре в течение 1 часа со вторичным антителом (козье антимышиное антитело Alexa Fluor 488, Invitrogen A10-680) 1:400 в 1% БСА в ФБР. После промывания ядра окрашивали DAPI и анализировали под флуоресцентным микроскопом Leica DM 2500.
4.6. Анализ адгезии моноцитов-эпителиальных клеток
4.6.1. Принцип
Клетки CacoGoblet обрабатывали в течение ночи ИЛ-1-бета, провоспалительным цитокином, перед анализом адгезии, чтобы создать воспаленную слизистую оболочку. Обработанные монослои затем обрабатывали продуктами в течение 24 часов. Меченные клетки THP-1 добавляли поверх CacoGoblet в каждую лунку. Клетки THP-1 маркировали флуоресцентным красителем, хлорметилфлуоресцеина диацетатом (CMFDA; Invitrogen). После инкубации монослой осторожно промывали для удаления неприлипающих клеток THP-1. Прилипшие клетки, меченные флуоресцентным красителем, анализировали под флуоресцентным микроскопом.
4.6.2. Процедура
После обработки маркированные клетки THP-1 наносили поверх CacoGoblet.
Клетки THP-1 маркировали флуоресцентным красителем, хлорметилфлуоресцеина диацетатом (CMFDA Exc. 492, Em 517; Invitrogen).
После 1 часа инкубации монослой осторожно промывали для удаления неприлипающих клеток THP-1. Прилипшие клетки, помеченные флуоресцентным красителем, просматривали под флуоресцентным микроскопом.
5. Результаты
5.1. Жизнеспособность клеток при определении посредством MTT анализа
Результаты теста МТТ представлены на фигуре 3. На фигуре 3 показана жизнеспособность клеток после 24 часов обработки клюквой в концентрации 10-100-1000 мкг/мл.
Отрицательному контролю (среда без добавок) была присвоена жизнеспособность 100%.
При всех протестированных концентрациях продукты не снижали жизнеспособность по сравнению с отрицательным контролем.
Нецитотоксическая концентрация, выбранная для исследования эффективности, составляла 1000 мкг/мл. При этой концентрации влияние вещества, исследуемого с помощью теста МТТ, составило 32%.
Противовоспалительные свойства экстракта клюквы в системе совместной культуры in vitro (клетки THP-1 и клетки кишечного эпителия).
5.2. Анализ адгезии моноцитов-эпителиальных клеток
После обработки маркированные клетки THP-1 наносили поверх CacoGoblet. После 1 часа инкубации монослой осторожно промывали для удаления неприлипающих клеток THP-1. Прилипшие клетки, меченные флуоресцентным красителем, анализировали под флуоресцентным микроскопом; результаты представлены на фигуре 4.
На фиг.4 показана адгезия моноцитов-эпителиальных клеток в необработанных воспаленных CacoGoblet.
- Как и ожидалось, после обработки ИЛ-1-бета наблюдалось увеличение адгезии клеток THP-1.
- Как и ожидалось, очень небольшое количество клеток THP-1 оказалось прикрепленным к эпителию CacoGoblet (отрицательный контроль, NT).
- Клюква как таковая, на здоровой слизистой оболочке, снижает адгезию клеток THP-1.
- Значительное снижение адгезии клеток ТНР-1 наблюдалось после нанесения этакортилена на воспаленную слизистую оболочку.
- Значительное снижение адгезии клеток THP-1 наблюдалось после нанесения клюквы на воспаленную слизистую оболочку, немного меньше, чем после обработки этакортиленом.
Способность клюквы к предотвращению адгезии E.coli к слизистой оболочке
5.3. Анализ ТЭЭС
На фиг.5 показаны результаты анализа трансэпителиального электрического сопротивления (ТЭЭС), выраженные в Ом*см2, на базовом уровне (0 часов), после 4 часов обработки продуктами и после 2 часов колонизации E.coli (6 часов обработки в целом).
Значения ТЭЭС перед обработкой (T = 0 часов) указывают на общее сопротивление барьера, коррелирующее с целостностью структуры плотных соединений.
ТЭЭС, физический параметр целостности барьера слизистой оболочки, был использован для характеристики влияния продукта на параклеточный поток ионов на уровне эпителия слизистой оболочки.
На фиг.5 показано трансэпителиальное электрическое сопротивление (ТЭЭС), выраженное в Ом*см2 на базовом уровне (0 часов), после 4 часов обработки клюквой 1000 мкг/мл как таковой или после 2 часов колонизации E.сoli. Общее время культивирования для отрицательного контроля составило 6 часов.
Как показано на фигуре 5, колонизация E.coli вызвала снижение ТЭЭС с 274,67 Ом*см2 до 218,68 Ом*см2 после 2 часов обработки (-21%).
4-часовая предварительная обработка клюквой привела к увеличению ТЭЭС с 315 Ом*см2 до 325,82 Ом*см2 и препятствовала адгезии E.coli (восстановление ТЭЭС на 3%).
После 4 часов обработки клюква как таковая вызывала увеличение значений ТЭЭС на 43% (с 299,86 Ом*см2 до 430,54 Ом*см2): эти результаты указывают на действительные свойства пленкообразования и положительную эффективность экстракта клюквы на эпителиальный барьер как при наличии, так и при отсутствии E.coli.
5.4. Испытание с Люцифером желтым: параклеточная проницаемость.
Параклеточный поток Люцифера желтого (LY) оценивали в конце периода обработки; результаты измерения флуоресценции показаны на фигуре 6.
На фигуре 6 показан процент потока LY по сравнению с LY в нулевой момент времени в апикальном отделе. На фиг.6 показан поток LY после 6 часов обработки (4 часа с клюквой и 2 часа с колонизацией E.coli).
Отрицательный контроль (НК) имел проницаемость 0,52% для LY.
E.coli вызывала большую проницаемость для LY (0,91%), чем отрицательный контроль (увеличение прохождения LY по сравнению с NC) на 74%.
Не выявлено существенных различий между отрицательным контролем и тестируемым продуктом: предварительная обработка клюквой восстановила кишечный эпителий и предотвратила адгезию E.coli.
Клюква как таковая обладает защитной эффективностью: наблюдалось снижение прохождения LY на 29% по сравнению с отрицательным контролем.
5.5. Иммунофлуоресцентное окрашивание альфа-актинина
На серии изображений ниже показаны образцы, проанализированные под флуоресцентным микроскопом. Зеленый цвет представляет белок альфа-актинин, расположенный на уровне мембраны. Альфа-актинин взаимодействует с Tir, белком E.сoli, с образованием адгезивной бляшки, известной как пьедестал, и является маркером инфекции E.сoli.
На фигуре 7 показана иммунофлуоресценция альфа-актинина в образцах, колонизированных Escherichia сoli и обработанных или не обработанных клюквой.
Увеличение флуоресцентного цвета на уровне мембраны очевидно после колонизации E.coli по сравнению с отрицательным контролем.
Клюква индуцировала небольшое снижение альфа-актинина, когда его применяли самостоятельно или в качестве предварительной обработки перед колонизацией E.coli (несущественная разница по сравнению с колонизацией E.сoli).
5.6. Сканирующая электронная микроскопия
На фигуре 8 показаны ультраструктурные изображения микроворсинок клеток Caco-2, взятые из литературы. (BCD Cancer 2008 8: 227)
В необработанных клетках Caco-2 можно наблюдать большое количество микроворсинок. Поля ячейки не отображаются. Вставка: присутствуют длинные микроворсинки. (b) Клетки, обработанные ЭФР. Видны многочисленные пузырьки. Вставка: присутствует уменьшенное количество микроворсинок. (c-f): Обработанные клетки. Количество микроворсинок уменьшается, и они теряют свое прямое положение.
Исторические данные VitroScreen о колонизации клеток Caco-2 E.coli: видны пролиферация и адгезия E.coli к клеточному слою (красная стрелка).
На фигурах 9А и 9В показаны образцы, проанализированные под сканирующим электронным микроскопом.
Фигура 10А показывает отрицательный контроль: необработанные CacoGoblet через 6 часов.
Как и ожидалось, отрицательный контроль не показал клеточного стресса или бактериального загрязнения. Ткань была трофической, с хорошо структурированными десмосомами (1000х). Микроворсинки, по-видимому, хорошо организованы по всей поверхности: можно наблюдать плотную щеткоподобную границу микроворсинок (5000x, красная рамка).
Фигура 10В показывает колонизацию ткани E.coli, 2 часа
Благодаря решению технических проблем, на поверхности CacoGoblet отсутствует распространение E.coli. Однако на монослое видны микроворсинки, поврежденные на поверхности; их меньше по количеству и они потеряли свое нормальное положение (10000x, красная рамка) по сравнению с отрицательным контролем, что указывает на то, что E.coli нанесли ущерб щеткообразной границе.
На фигуре 10C показана предварительная обработка клюквой в течение 4 часов до колонизации E.coli в течение 2 часов.
Монослой выглядит хорошо структурированным и показывает микроворсинки на поверхности (5000x). Видно мало клеток E.coli, и их морфология изменена (10000x, красная стрелка) с явными признаками лизиса. Кроме того, обильный бактериальный детрит (10000x, красная звезда) очевиден, что указывает на то, что обработка клюквой нанесла вред E.coli.
6. Выводы
Различные экспериментальные модели на основе кишечного эпителия CacoGoblet in vitro были применены для оценки эффективности экстракта клюквы по поручению Sofar S.p.A.
Нецитотоксическую концентрацию тестировали на предварительной стадии с помощью анализа МТТ, чтобы исключить потенциальную внутреннюю токсичность продукта.
Самая высокая нецитотоксическая концентрация, выбранная для исследования эффективности, составила 1000 мкг/мл.
Были использованы два протокола:
1) противовоспалительные свойства экстракта клюквы в системе совместной культуры (клетки THP-1 и клетки кишечного эпителия);
2) способность клюквы предотвращать адгезию кишечной палочки.
Следующие параметры были оценены, чтобы прийти к заключению относительно:
- адгезии моноцитов-эпителиальных клеток в CacoGoblet с воспалением, вызванным ИЛ-1-бета (противовоспалительной эффективности);
- трансэпителиального электрического сопротивления (ТЭЭС) и параклеточного потока LY (изменения эпителиального барьера);
- ультраструктурного анализа E.сoli с помощью сканирующего электронного микроскопа (СЭМ) (противодействия адгезии и размножению E.coli);
- расположения альфа-актинина иммунофлуоресценцией (противодействия адгезии E.coli).
В заключение, результаты показали, что:
1) Клюква, нанесенная на воспаленную слизистую оболочку кишечника, индуцировала значительное снижение адгезии к клеткам THP-1, что свидетельствует о значительном противовоспалительном действии.
2) Предварительная обработка клюквой в течение 4 часов слегка противодействовала повреждению барьера, вызванному адгезией E.coli; клюква сама по себе после 4 часов обработки вызывала увеличение значений ТЭЭС на 43%, что указывает на превосходную способность к пленкообразованию.
3) Клюква сама по себе выполняет защитное действие в отношении целостности барьера: наблюдалось снижение проникновения LY на 29% по сравнению с отрицательным контролем. Не было выявлено существенных различий по сравнению с отрицательным контролем: предварительная обработка клюквой восстановила кишечный эпителий и предотвратила адгезию E.coli.
4) Окрашивание альфа-актинином, который действует в качестве биомаркера адгезии E.coli, не было в значительной степени изменено при обработке клюквой в принятых экспериментальных условиях; однако наблюдалось небольшое снижение флуоресценции.
5) Анализ методом сканирующей электронной микроскопии выявил прямую активность клюквы в отношении адгезии, жизнеспособности и морфологии E.coli.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛУЧЕНИЕ КОМПОЗИЦИИ КЛЮКВЕННЫХ ГРАНУЛ С УСТОЙЧИВЫМ СОДЕРЖАНИЕМ ПРОАНТОЦИАНИДИНОВ | 2017 |
|
RU2766084C2 |
| КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ЭКСТРАКТ КЛЮКВЫ КРУПНОПЛОДНОЙ И ФОСФОЛИПИДЫ | 2019 |
|
RU2772433C1 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ МОЧЕВЫВОДЯЩИХ ПУТЕЙ | 2016 |
|
RU2637650C2 |
| СПОСОБ ОЦЕНКИ РЕГЕНЕРАЦИИ ТОЛСТОЙ КИШКИ ПРИ ДИВЕРТИКУЛЕЗЕ | 2010 |
|
RU2452396C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ДИВЕРТИКУЛЯРНОЙ БОЛЕЗНИ ОБОДОЧНОЙ КИШКИ | 2009 |
|
RU2391667C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ДИВЕРТИКУЛЕЗА | 2010 |
|
RU2445712C1 |
| Способ лечения перфоративного дивертикула сигмовидного отдела толстой кишки | 2016 |
|
RU2621168C1 |
| КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, СОДЕРЖАЩАЯ ГЛИЦЕРИН И ТАНИН | 2013 |
|
RU2640020C2 |
| Бактериальный штамм, способный метаболизировать оксалаты | 2012 |
|
RU2624033C2 |
| Терапевтические системы с модифицированным высвобождением для перорального введения куркумина в лечении кишечных расстройств | 2014 |
|
RU2692473C1 |










Изобретение относится к фармацевтической промышленности, а именно к применению композиции на основе экстракта Vaccinium macrocarpon для перорального введения для профилактики и/или лечения дивертикулеза толстой кишки, патологий или заболеваний, связанных с наличием дивертикулов, выбранных из дивертикулярной болезни, симптоматической неосложненной дивертикулярной болезни (СНДБ) и дивертикулита толстой кишки. Предлагается применение композиции на основе экстракта Vaccinium macrocarpon для перорального введения для профилактики и/или лечения дивертикулеза толстой кишки, патологий или заболеваний, связанных с наличием дивертикулов, выбранных из дивертикулярной болезни, симптоматической неосложненной дивертикулярной болезни (СНДБ) и дивертикулита толстой кишки, где композиция содержит или состоит из: (i) сердцевины, содержащей или состоящей из по меньшей мере (а) экстракта Vaccinium macrocarpon в количестве, составляющем от 150 до 600 мг по отношению к общей массе (i), и содержащем от 5 до 30% проантоцианидинов (ПАЦ) в концентрации по массе или по объему, и по меньшей мере одного вспомогательного ингредиента и/или вспомогательного вещества (b), приемлемого для фармацевтического или пищевого применения; (ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), и полностью покрывающего (i) и содержащего по меньшей мере один вспомогательный ингредиент и/или вспомогательное вещество (с), приемлемые для фармацевтического или пищевого применения, причем указанный гастрорезистентный слой (ii) способен обеспечить высвобождение экстракта (а) в толстой кишке. Вышеописанное применение композиции эффективно для профилактики и/или лечения дивертикулеза толстой кишки, патологий или заболеваний, связанных с наличием дивертикулов, выбранных из дивертикулярной болезни, симптоматической неосложненной дивертикулярной болезни (СНДБ) и дивертикулита толстой кишки. 10 з.п. ф-лы, 11 ил., 4 табл., 2 пр.
1. Применение композиции на основе экстракта Vaccinium macrocarpon для перорального введения для профилактики и/или лечения дивертикулеза толстой кишки, патологий или заболеваний, связанных с наличием дивертикулов, выбранных из дивертикулярной болезни, симптоматической неосложненной дивертикулярной болезни (СНДБ) и дивертикулита толстой кишки, где композиция содержит или состоит из:
(i) сердцевины, содержащей или состоящей из по меньшей мере (а) экстракта Vaccinium macrocarpon в количестве, составляющем от 150 до 600 мг по отношению к общей массе (i), и содержащем от 5 до 30% проантоцианидинов (ПАЦ) в концентрации по массе или по объему, и по меньшей мере одного вспомогательного ингредиента и/или вспомогательного вещества (b), приемлемого для фармацевтического или пищевого применения;
(ii) гастрорезистентного слоя, наружного по отношению к сердцевине (i), и полностью покрывающего (i) и содержащего по меньшей мере один вспомогательный ингредиент и/или вспомогательное вещество (с), приемлемые для фармацевтического или пищевого применения, причем указанный гастрорезистентный слой (ii) способен обеспечить высвобождение экстракта (а) в толстой кишке.
2. Применение по п.1, в котором указанный экстракт (а) присутствует в количестве, составляющем от 200 до 300 мг по отношению к общей массе (i).
3. Применение по любому из предыдущих пунктов, в котором указанный экстракт (а) предпочтительно представляет собой сухой экстракт клюквы, предпочтительно содержащий ПАЦ в концентрации 10%, или 15%, или 20%, или 25% по массе или объему.
4. Применение по п.1, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), имеет характеристику разрушения и растворения в зависимости от значения рН и/или времени; предпочтительно указанный слой (ii) способен разрушаться и растворяться при значении рН примерно от 6,5 до 8.
5. Применение по п.4, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), способен разрушаться и растворяться при значении рН примерно от 7 до 7,5; предпочтительно в течение времени, составляющего от 30 до 120 мин; еще более предпочтительно от 45 до 90 мин.
6. Применение по пп.1, 4 или 5, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), содержит или состоит из по меньшей мере одного вспомогательного ингредиента и/или вспомогательного вещества, выбранного из биотика Eudragard® E1207, гастрорезистентного полимера, такого как поли(метилакрилат-со-метилметакрилат-со-метакриловая кислота) 7:3:1 или другой анионный метакриловый сополимер, триэтилцитрата E1505, талька, этилцеллюлозы, анионного метакрилатного сополимера и их смесей, шеллака, альгината натрия и их смесей, крахмала и модифицированных крахмалов, олеиновой кислоты, стеариновой кислоты и триглицеридов со средней длиной цепи.
7. Применение по любому из пп.1-6, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (1), содержит или состоит из:
- гастрорезистентного полимера, такого как поли(метилакрилат-со-метилметакрилат-со-метакриловая кислота) 7:3:1 или другой анионный метакрилатный сополимер: от 5 до 50 мг; от 10 до 35 мг; 18-25 мг;
- триэтилцитрата E1505: от 0,1 до 5 мг; от 0,3 до 3 мг; 0,5-2 мг;
- талька: от 1 до 30 мг; от 3 до 20 мг; 5-15 мг.
8. Применение по любому из пп.1-7, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), содержит или состоит из:
- этилцеллюлозы - от 5 до 15 мг; от 8 до 12 мг; 9,97 мг;
- альгината натрия - от 5 до 15 мг; от 8 до 12 мг; 9,30 мг;
- гидроксида аммония - от 0,5 до 4 мг; от 1,5 до 3 мг; 2,34 мг;
- триглицеридов со средней длиной цепи - от 0,5 до 5 мг; от 1,5 до 3 мг; 2,12 мг;
- олеиновой кислоты - от 0,5 до 3 мг; от 1 до 2 мг; 1,17 мг;
- очищенной стеариновой кислоты - от 0,01 до 0,5 мг; от 0,05 до 0,3 мг; 0,1 мг.
9. Применение по любому из пп.1-6, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), содержит или состоит из:
- этилцеллюлозы - от 5 до 50 мг; от 10 до 30 мг; 15-20 мг;
- диоксида титана - от 0,1 до 15 мг; от 0,5 до 10 мг; 1-5 мг;
- альгината натрия - от 0,1 до 5 мг; от 0,3 до 4 мг; 0,5-2 мг;
- олеиновой кислоты, стеариновой кислоты, триглицеридов со средней длиной цепи: каждый от 0,01 до 3 мг; от 0,05 до 1 мг.
10. Применение по любому из предыдущих пунктов, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), содержит или состоит из:
- биотика Eudragard® E1207 (Evonik) - 20,4 мг;
- триэтилцитрата E1505 - 1 мг;
- талька - 10,2 мг.
11. Применение по любому из предыдущих пунктов, в котором указанный гастрорезистентный слой (ii), наружный по отношению к сердцевине (i), содержит или состоит из:
- этилцеллюлозы - 9,97 мг;
- альгината натрия - 9,30 мг;
- гидроксида аммония - 2,34 мг;
- триглицеридов со средней длиной цепи - 2,12 мг;
- олеиновой кислоты - 1,17 мг;
- очищенной стеариновой кислоты - 0,1 мг.
| УСТРОЙСТВО для ОПРЕДЕЛЕНИЯ РАЗМЕРОВ СУЧЬЕВ И УЧЕТА ИХ КОЛИЧЕСТВА | 0 |
|
SU180870A1 |
| WO 2012123491 A1, 20.09.2012 | |||
| DE 2010008308 U1, 25.11.2010 | |||
| GB 23670002 A, 27.03.2002 | |||
| US 6248362 B1, 19.06.2001. | |||
Авторы
Даты
2022-05-26—Публикация
2017-12-01—Подача